32006D0437[1]
2006/437/EK: A Bizottság határozata ( 2006. augusztus 4. ) a 2005/94/EK tanácsi irányelvben előírt, a madárinfluenzára vonatkozó diagnosztikai kézikönyv elfogadásáról (az értesítés a C(2006) 3477. számú dokumentummal történt)
A BIZOTTSÁG HATÁROZATA
(2006. augusztus 4.)
a 2005/94/EK tanácsi irányelvben előírt, a madárinfluenzára vonatkozó diagnosztikai kézikönyv elfogadásáról
(az értesítés a C(2006) 3477. számú dokumentummal történt)
(EGT vonatkozású szöveg)
(2006/437/EK)
AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA,
tekintettel a madárinfluenza elleni védekezésre irányuló közösségi intézkedésekről és a 92/40/EGK irányelv hatályon kívül helyezéséről szóló, 2005. december 20-i 2005/94/EK tanácsi irányelvre (1) és különösen annak 50. cikke (1) bekezdésének második albekezdésére,
mivel:
(1) A 2005/94/EK irányelv a madárinfluenza megfigyelését és korai észlelését célzó bizonyos megelőző intézkedéseket, valamint a baromfi és más, fogságban tartott madarak körében előforduló madárinfluenza-járvány kitörése esetén alkalmazandó járványvédelmi minimumintézkedéseket állapít meg.
(2) A madárinfluenza-járvány kitörésének megállapítására szolgáló diagnosztikai eljárásokat, mintavételi módszereket és a laboratóriumi vizsgálati eredmények értékelési kritériumait közösségi szinten kell megállapítani.
(3) A 2005/94/EK irányelv VII. melléklete megállapítja a madárinfluenza közösségi referencialaboratóriumának szerepét és feladatait annak érdekében, hogy a Bizottsággal egyeztetve összehangolja a tagállamok által a betegség diagnosztizálására használt módszereket. E szerepek és feladatok közé tartozik a rendszeres összehasonlító vizsgálatok megszervezése és közösségi szinten a standard reagensek rendelkezésre bocsátása.
(4) A közelmúltban laboratóriumi vizsgálatokat fejlesztettek ki a madárinfluenza gyors diagnosztizálásának biztosítására.
(5) A madárinfluenza elleni védekezésben az utóbbi években nyert tapasztalatok eredményeként meghatározták azon mintavételi eljárásokat és a laboratóriumi vizsgálati eredmények azon értékelési szempontjait, amelyek a legalkalmasabbak a betegség különféle helyzetekben történő helyes diagnosztizálására.
(6) Az e határozatban előírt intézkedések összhangban vannak az Élelmiszerlánc- és Állategészségügyi Állandó Bizottság véleményével,
ELFOGADTA EZT A HATÁROZATOT:
1. cikk
A 2005/94/EK rendeletben előírt és e határozat mellékletében található diagnosztikai kézikönyvet jóváhagyták.
2. cikk
A tagállamok a következő időpontok közül a korábbitól kezdődően alkalmazzák a diagnosztikai kézikönyvet: a 2005/94/EK irányelv átültetése a nemzeti jogba, illetve 2007. július 1-je.
3. cikk
Ennek a határozatnak a tagállamok a címzettjei.
Kelt Brüsszelben, 2006. augusztus 4-én.
a Bizottság részéről
Markos KYPRIANOU
a Bizottság tagja
(1) HL L 10., 2006.1.14., 16. o.
MELLÉKLET
MADÁRINFLUENZA: DIAGNOSZTIKAI KÉZIKÖNYV
I. FEJEZET
Bevezetés, célok és meghatározások
1. Annak érdekében, hogy a Közösségben folytatott, a madárinfluenza diagnosztizálására szolgáló eljárások egységesek legyenek, e diagnosztikai kézikönyv meghatározza:
a) a diagnosztikai eljárásokra, a mintavételi módszerekre és a laboratóriumi vizsgálati eredmények értékelési szempontjaira vonatkozó iránymutatásokat és minimumkövetelményeket, a madárinfluenza helyes diagnosztizálása céljából;
b) a madárinfluenza diagnosztizálását célzó laboratóriumi vizsgálatokat és a madárinfluenza-vírus izolátumai genotípusának azonosítására alkalmazandó laboratóriumi technikákat;
c) a diagnosztikai laboratóriumok által, valamint a minták szállítása során betartandó minimális biológiai biztonsági követelményeket és minőségi előírásokat.
2. E diagnosztikai kézikönyv a madárinfluenza elleni védekezésért felelős hatóságok számára készült. Témája ezért főleg a laboratóriumi vizsgálati elvek és e vizsgálatok alkalmazása, a vizsgálati eredmények értékelése, valamint a laboratóriumi technikák.
3. E kézikönyv alkalmazásában a 2005/94/EK irányelv 2. cikkében említett meghatározásokon túlmenően a következő fogalommeghatározást is alkalmazni kell:
"diagnosztikai minta": diagnosztizálási vagy vizsgálati célból szállított bármilyen állati eredetű anyag, ideértve az egész állattetemet is, kivéve azonban a fertőzött élő állatot.
4. A madárinfluenza megállapításának baromfi és más, fogságban tartott madár esetében az e diagnosztikai kézikönyvben meghatározott eljárásoknak, mintavételi módszereknek és a laboratóriumi vizsgálati eredmények értékelési szempontjainak megfelelően kell történnie és az alábbi a), b) vagy c) pontban meghatározott kritériumokon kell alapulnia:
a) ragályos vírus, antigén vagy különleges genetikai anyag kimutatása a baromfi vagy más madár szöveteiből, szerveiből, véréből vagy ürülékéből vett mintákban;
b) a betegségre utaló klinikai tünetek és kórbonctani elváltozások kimutatása e madaraknál;
c) specifikus ellenanyag kimutatása a madarak vérmintájában.
5. Az alábbi a) vagy b) alpontban meghatározott kritériumokra kell alapozni annak megállapítását, hogy egy emlősállat olyan A-típusú influenzavírussal fertőzött-e, amely madaraktól származik, magas vagy alacsony patogenitású, illetve H5 vagy H7 altípusú:
a) ragályos madárinfluenza-vírus, antigén vagy különleges genetikai anyag kimutatása az emlős szöveteiből, szerveiből, véréből vagy ürülékéből vett mintákban;
b) a madárinfluenza-vírusra adott specifikus ellenanyagválasz kimutatása az emlős vérmintájában.
6. Az eljárásoknak, a mintavételi módszereknek és a laboratóriumi vizsgálati eredmények értékelési szempontjainak:
a) az e diagnosztikai kézikönyvben foglaltakkal megegyezőknek kell lenniük; vagy
b) az illetékes hatóság által engedélyezettnek kell lenniük, feltéve, hogy:
i. a madárinfluenza közösségi referencialaboratóriumában (a továbbiakban: közösségi referencialaboratórium) összehasonlító vizsgálattal kimutatták, hogy az engedélyezett laboratóriumi vizsgálat érzékenysége és specifikussága megfelelő; vagy
ii. amennyiben a közösségi referencialaboratórium nem végzett ilyen vizsgálatot egy bizonyos laboratóriumi vizsgálat tekintetében, az engedélyezett laboratóriumi vizsgálat érzékenységét és specifikusságát nemzeti referencialaboratórium validálta, mint a célnak megfelelő laboratóriumi vizsgálatot; a jóváhagyási vizsgálat eredményeit ellenőrzés céljából be kell nyújtani a közösségi referencialaboratóriumnak.
II. FEJEZET
A madárinfluenza leírása és a differenciáldiagnózis
1. Kóroktan és virulencia
A madárinfluenza egy igen ragályos vírusos fertőzés, amelyet az Orthomyxoviridae családba tartozó influenzavirus A típusú vírus okoz. Ismereteink szerint az A-típusú influenzavírus az egyetlen olyan orthomyxovírus, amely madarakat is megfertőz. Számos madárfajtáról kimutatták, hogy hajlamosak az A-típusú influenzavírusoktól megfertőződni; leginkább a vízimadarak a hordozói (rezervoárjai) e vírusoknak, a csirkékben és pulykákban (a betegség által érintett legfontosabb, gazdasági jelentőségű madarakban) található izolátumok túlnyomó többsége ugyanakkor alacsony patogenitású.
Az A-típusú influenzavírusok tartalmaznak antigén-tulajdonságokkal rendelkező nukleoproteineket és antigén-tulajdonságokkal rendelkező mátrixproteineket, de altípusokba történő besorolásuk a felszíni glikoproteinek - hemagglutinin (HA) és neuraminidáz (NA) - antigén-tulajdonságai szerint történik. Jelenleg 16 HA-altípust (H1-H16) és 9 NA-altípust (N1-N9) ismerünk. Valamennyi A-típusú influenzavírus egy HA-antigénnel és egy NA-antigénnel rendelkezik, egymással láthatóan tetszőleges kombinációban.
Az A-típusú influenzavírusok két csoportba oszthatók attól függően, hogy milyen mértékben képesek betegséget kiváltani az erre érzékeny baromfiban:
a) magas patogenitású madárinfluenza (HPAI - highly pathogenic avian influenza )-vírusok, amelyek a fertőzött baromfiállomány általános fertőzöttségével járó, rendkívül komoly betegséget okoznak, az állományban igen nagy arányú (akár 100 %-os) elhullást idézve elő; és
b) alacsony patogenitású madárinfluenza (LPAI - low pathogenic avian influenza )-vírusok, amelyek az enyhe, elsősorban légzőszervi baromfi-megbetegedésekért felelősek, hacsak nem súlyosbítják más fertőzések vagy tényezők.
Vírushordozóként (rezervoárként) rendkívül fontos szerepet játszanak a vadon élő madarak (különösen a vándor vízimadarak), amit az is mutat, hogy a vadon élő madarakból a HA altípus és NA altípus valamennyi lehetséges kombinációját izolálták. A vadon élő madaraknál többnyire csak az alacsony patogenitású madárinfluenza-vírust mutatták ki, kivéve, amikor fertőzött baromfitól származó magas patogenitású madárinfluenza is elterjedt közöttük.
A madárinfluenza-vírusok baromfitelepeken első ízben történő elterjedése valószínűleg a vadon élő madarakkal való közvetlen vagy közvetett kontaktus eredménye.
A házi baromfi esetében előfordulhat, hogy a vadon élő vírushordozókból származó alacsony patogenitású vírusok észrevétlenek maradnak, mivel a klinikai tünetek gyakran enyhék, illetve nem is jelentkeznek.
A baromfiban az alacsony patogenitású, H5 vagy H7 altípusú madárinfluenza-vírus törzsei mutáció útján magas patogenitású madárinfluenza-törzsekké alakulhatnak át. Eddig kizárólag a H5 és H7 altípusú vírusokról mutatták ki, hogy magas patogenitású madárinfluenzát okozhatnak.
Noha valószínűleg több mechanizmus tehető felelőssé az alacsony patogenitású madárinfluenzának magas patogenitású madárinfluenzává történő alakulásáért, az e mutációt létrehozó tényezők nem ismertek. Úgy tűnik, hogy bizonyos esetekben a mutáció a vadon élő madaraktól eredő fertőzés után gyorsan, még az elsődleges területen megtörtént, míg máskor az alacsony patogenitású madárinfluenza-vírus hónapokig lappangott a baromfiban, mielőtt mutációra került volna sor. Lehetetlen ezért előre megmondani, hogy történni fog-e mutáció, és ha igen, mikor. Ésszerűen kijelenthető azonban, hogy minél szélesebb körű az alacsony patogenitású madárinfluenza jelenléte a baromfiállományban, annál nagyobb az esély a magas patogenitású madárinfluenza-vírus kialakulására.
A lappangási időszak nehezen felbecsülhető, és valószínűleg a vírustörzstől és a vírusgazdától függ; általában 5-6 napot szoktak említeni, ugyanakkor a különböző madaraknál ez az időszak néhány órától körülbelül hét napig is terjedhet.
2. A magas patogenitású madárinfluenza-vírussal megfertőzött madarak klinikai tünetei
A klinikai tünetek igen különfélék és olyan tényezőktől függnek, mint a fertőző vírus virulenciája, a megfertőzött fajok, az életkor, a nem, a meglévő betegségek és a környezet.
A korai tünetek közé tartoznak: étvágytalanság, a folyadékfelvétel csökkenése és a viszonylag alacsony mortalitás. A betegség ugyanakkor hirtelen is kitörhet egy állományban, és több madár előzetes tünetek nélkül, vagy minimális tünetekkel (bágyadtság, étvágytalanság, borzolt tollazat, láz) is elpusztulhat. Általában minél hosszabb ideig él egy beteg madár, annál jelentősebbek a klinikai tünetek. A tünetek kialakulásának időpontja a vírustól, a vírusgazdától és a fertőzés kezdeti dózisától, illetve a baromfitenyésztési rendszertől függ. A broiler baromfihoz képest a vírus lassabban terjed a ketrecben tartott tojó tyúkok vagy a szabadon tartott madarak körében.
A magas patogenitású madárinfluenza-vírussal fertőzött tojók először lágyhéjú tojásokat tojnak, a tojástermelés azonban hamarosan megszűnik. A beteg madarak gyakran félig kómás állapotban ülnek vagy állnak, fejük a talajt érinti. A taréjt és a bőrfüggeléket a cianózis és a vizenyős duzzanat jellemzi, végükön bővérűség (petechialis) és véraláfutás is megfigyelhető. Gyakran jelentkezik bőséges, híg hasmenés, és a madarak rendkívül szomjasak. A légzés nehézkessé válhat és túlzott könnyezés jelentkezhet. A bőr tollakkal nem fedett részén vérzés fordulhat elő. Az állomány mortalitása 50-100 % között váltakozik.
A broiler szárnyas esetében a magas patogenitású madárinfluenza tünetei gyakran kevésbé szembeötlők, mint más baromfi esetében. E tünetek közé tartozik a súlyos bágyadtság és az étvágytalanság; az elsőként észlelt rendellenesség a mortalitás jelentős mértékű növekedése. Megfigyelhető ezenkívül a fej és a nyak vizenyős duzzanata, illetve idegrendszeri tünetek, mint például a nyakmerevség és az ataxia (végtagok mozgási zavara).
A pulykák esetében a magas patogenitású madárinfluenza hasonló ahhoz, ami a házi szárnyasoknál megfigyelhető, ugyanakkor a pulykáknál néhány magas patogenitású madárinfluenza-vírus virulensebbnek, míg más ilyen vírus kevésbé virulensnek bizonyul.
A magas patogenitású madárinfluenza-vírussal fertőzött ludak esetében a tojó tyúkéhoz hasonló tünetek figyelhetők meg (bágyadtság, étvágytalanság és hasmenés), viszont a szinuszok gyakran gyulladtak. A fiatalabb madaraknál idegrendszeri tünetek is jelentkezhetnek.
A kacsáknál előfordulhat, hogy a magas patogenitású madárinfluenza-vírusnak nincsenek klinikai tünetei, ugyanakkor a szakirodalom szerint néhány vírustörzs a ludakéhoz hasonló tüneteket okoz és bizonyos arányú mortalitást idéz elő.
A magas, illetve alacsony patogenitású madárinfluenza-fertőzések a struccoknál tünetmentesek lehetnek. A magas patogenitású madárinfluenza-járvány kitörései során (mint amilyen az 1999/2000-es olaszországi is volt) arról számoltak be, hogy a gyöngytyúk és a japán fürj is megfertőződhet; a tünetek és a mortalitás a beteg csirkééhez vagy pulykáéhoz hasonlított. Néhány kísérlet ugyanakkor azt mutatta, hogy a fürj néhány magas patogenitású madárinfluenza-törzzsel szemben ellenálló. Valamennyi madár esetében ugyanazon H altípussal szemben termelődött ellenanyagok jelenléte - amely lehet vakcina vagy természetes fertőzés eredménye - azt eredményezheti, hogy a magas patogenitású madárinfluenza-vírussal történő fertőzés nem jár szemmel látható klinikai tünetekkel.
3. A magas patogenitású madárinfluenza-vírussal megfertőzött madarak kórbonctani elváltozásai
A gyors lefolyású betegségben elhullott madarakon minimális makroszkopikus elváltozások figyelhetők meg, amelyek: a belső részekben és az izmokban jelentkező dehidratáció és vértolulás.
Hosszabb klinikai folyamat után elpusztult madarak testén (különösen a gégefőn, a légcsőn, a mirigyes gyomorban, az epicardium zsírszövetében és a szegycsonttal szomszédos savóshártyán) bővérűség (petechialis) és véraláfutás is megfigyelhető. A bőr alatt (különösen a fej és a lábszár körül) nagy kiterjedésű ödéma jelentkezik. A tetem esetleg dehidratált. Sárga vagy szürke gócpontok jelentkezhetnek a lépen, a májon, a vesén és a tüdőn. A légzsák váladékot tartalmazhat. A lép megnagyobbodhat és vérzések jelentkezhetnek rajta.
Szövettanilag a madárinfluenzát érrendszeri rendellenességek jellemzik: ödémát, vérzéseket és perivaszkuláris beszűrődést okozhatnak, különösen a szívizomban, a lépben, a tüdőben, az agyban, a hasnyálmirigyben és a bőrfüggeléken. Üszkös gócpontok lehetnek a tüdőben, a májban és a vesékben. Az agyban gliosis, érrendszeri proliferáció és az idegsejtek elváltozásai jelentkezhetnek.
4. Differenciáldiagnózis
A magas patogenitású madárinfluenza differenciáldiagnózisa során különösen a következő betegségeket kell megvizsgálni:
a) egyéb olyan betegségek, amelyek hirtelen magas mortalitást okoznak, mint például:
i. baromfipestis (Newcastle-betegség);
ii. fertőző gége- és légcsőhurut;
iii. kacsapestis;
iv. akut mérgezés;
b) egyéb olyan betegségek, amelyek a taréj és a bőrfüggelékek duzzanatát okozzák, mint például:
i. akut baromfikolera és egyéb vérmérgezéses betegségek;
ii. bakteriális cellulitis a taréjon és a bőrfüggeléken.
5. Az alacsony patogenitású madárinfluenza-vírussal megfertőzött madarak klinikai tünetei
Az alacsony patogenitású madárinfluenza-vírus okozta betegség súlyosságát nagy mértékben meghatározza:
a) a vírustörzs;
b) a vírusgazda fajtája és életkora;
c) a vírusgazda vírussal szembeni immunológiai állapota, és különösképpen más fertőző kórokozók jelenléte, mint például:
i. Pasteurella spp;
ii. baromfipestis-vírus (ideértve a vakcinatörzseket is);
iii. avian pneumovírus, a fertőző bronchitis vírusa;
iv. E. coli;
v. Mycoplasma spp;
d) immunhiányos állapot;
e) környezeti tényezők (mint például a túl sok ammónia és por, túl magas vagy túl alacsony hőmérséklet).
Előfordulhat, hogy a betegség klinikai tünetei nem, vagy csupán csekély mértékben látszanak, és kizárólag enyhe légzőszervi tünetekben vagy a tojó madaraknál tojástermelési problémákban nyilvánulnak meg. Az is megtörténhet azonban (különösen a pulykáknál), hogy az alacsony patogenitású madárinfluenza-vírussal történő fertőzés a betegség súlyos tüneteivel társul, amelyek általában: hörgés, köhögés, a szemgödör alatti üregek gyulladása, valamint étvágytalansággal és magas mortalitással járó lázas állapot.
Az alacsony patogenitású madárinfluenza összetéveszthető több, légzőszervi vagy belgyógyászati tüneteket mutató betegséggel, illetve az ilyen betegségek súlyosbíthatják azt. Madárinfluenzára kell gyanakodni minden egyes alkalommal, amikor a baromfiállományban olyan betegség jelenik meg, amely a más betegségek elleni megelőző és gyógyintézkedések ellenére sem múlik el.
6. A fogságban tartott madarak klinikai tünetei
A klinikai tünetek igen széles körűek lehetnek, és a baromfinál a láthatatlan tünetektől a magas mortalitást előidéző súlyos tünetekig terjedhetnek.
A fogságban tartott madaraknál a fertőzés általában lassabban terjed, ami a fogságban tartott fajok különféleségével magyarázható: fogékonyságuk és vírusátadási képességük különböző; a vírus viszonylag lassú terjedése a kis mértékű kontaktusnak és az állomány viszonylag alacsony sűrűségének köszönhető.
III. FEJEZET
Iránymutatások a madárinfluenza gyanújának fennállása esetén egy gazdaságban
A magas és az alacsony patogenitású madárinfluenza klinikai tüneteinek változatossága miatt nem lehet határozott iránymutatásokat adni járványkitörés gyanújára vonatkozóan. A baromfinál hirtelen jelentkező, magas mortalitást (a II. fejezetben ismertetett klinikai tünetek meglétével vagy anélkül) ki kell vizsgálni: a laboratóriumi vizsgálat céljából mintavételre van szükség. Magas mortalitás hiányában ugyanakkor nehezebb megállapítani, hogy madárinfluenzáról van-e szó vagy sem.
Mivel a H5 és a H7 altípus okozta magas, illetve alacsony patogenitású madárinfluenza gyors diagnosztizálása kiemelkedően fontos a betegség korai megfékezése és a betegség kiírtása szempontjából, a madárinfluenza gyanúját mindig meg kell vizsgálni a légzőszervi és a tojástermelési problémák, valamint a baromfi megnövekedett mortalitásának differenciáldiagnózisa során, és a megfelelő mintákat laboratóriumi vizsgálatra kell küldeni.
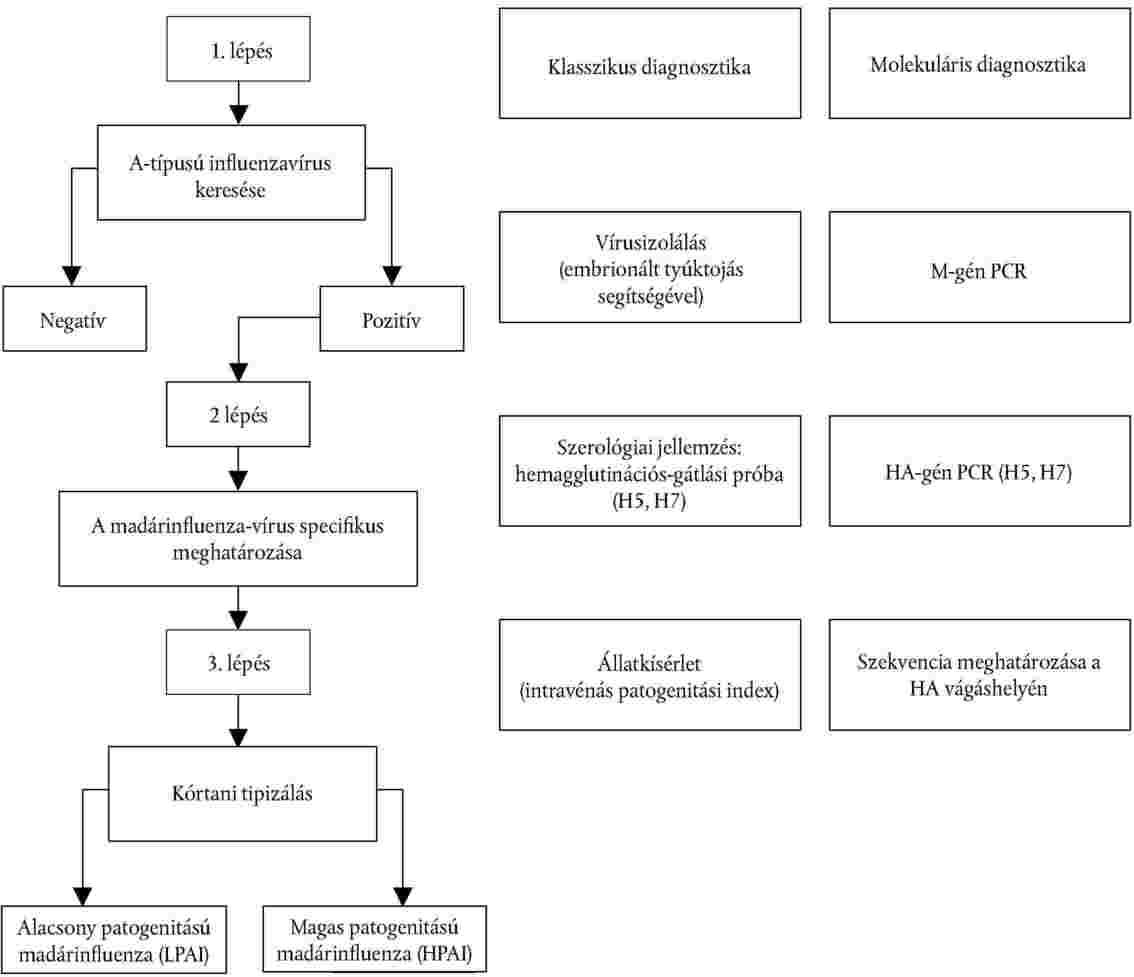
Ábra
A madárinfluenza megállapítására irányuló diagnosztikai lépések vázlatos áttekintése
IV. FEJEZET
A mintavétel és a minták szállításának általános eljárásai
1. A 2005/94/EK irányelv és a diagnosztikai kézikönyv
Ahol a 2005/94/EK irányelv a diagnosztikai kézikönyvre hivatkozik, a diagnosztikai kézikönyv e fejezetében meghatározott vizsgálatokat, mintavételi és megfigyelési (surveillance) eljárásokat kell elvégezni.
2. A madárinfluenza-járvány kitörésének gyanújakor követendő eljárások
Ha a hatósági állatorvos klinikai tünetek alapján madárinfluenza-járvány kitörésére gyanakszik, vagy ha az e betegségre vonatkozó laboratóriumi vizsgálat bármelyike nem negatív, az illetékes hatóságnak a betegség jelenlétének kizárása előtt biztosítania kell a diagnosztikai kézikönyv e fejezetében meghatározott vizsgálatnak a 2005/94/EK irányelv 7. cikke szerinti lefolytatását és kielégítő befejezését.
3. A virológiai vizsgálat értelmezése
Az illetékes hatóság akkor dönthet úgy, hogy a madárinfluenza-vírus jelenléte kizárható, ha e fejezettel összhangban megfelelő számú beteg vagy elhullott madarat vagy légcsőből/garatból vagy kloákából vett tamponminát vizsgáltatott meg a vírus vagy genomjának kimutatása céljából, és az V. vagy VI. fejezetben tárgyalt, vagy az illetékes hatóság által az I. fejezet (6)b) pontjával összhangban engedélyezett vírusfelismerési módszer egyikét használva, és a vizsgálat negatív eredménnyel zárult.
4. A virológiai vagy szerológiai vizsgálatra küldött szabványos mintacsomag
Olyan gazdaság vizsgálata céljából, ahol felmerült a madárinfluenzavírus-fertőzés gyanúja, virológiai vagy szerológiai vizsgálat céljából levett mintákból álló, az a) és b) alpontban bemutatott szabványos mintacsomagot (szabványos mintákat) kell közvetlenül virológiai vagy szerológiai vizsgálat alá vetni.
a) A virológiai vizsgálatra küldött szabványos mintacsomag a következőkből áll:
i. legalább öt beteg/elhullott madár (ha van); és/vagy
ii. legalább 20 darab légcsőből/garatból vett tamponminta és 20 darab kloákából vett tamponminta.
AA mintába nemrég elhullott madarak tetemét kell felvenni, illetve olyanokat, amelyek súlyosan betegek vagy haldoklók voltak, és amelyeket kíméletesen öltek le.
A tamponmintákat az a) alpontban meghatározott számú madárból, vagy pedig (ennél kisebb létszámú állomány esetén) a gazdaság valamennyi madarából kell venni. A mintákat a betegség klinikai tüneteit mutató madarakból kell venni.
A kloákából vett tamponmintákat bélsárral kell beborítani (optimális mennyiség = 1 g). Ha valamilyen oknál fogva nincs lehetőség élő madarak kloákájából tamponmintát venni, alternatív megoldásként gondosan összegyűjtött friss bélsárminta is szóba jöhet.
A légcsőből/garatból származó tamponmintákat gyakran a szájüregből a legpraktikusabb venni.
Miután a vírus szaporodási sajátosságait megállapították, az illetékes hatóság dönthet úgy, hogy kizárólag a légcsőből/garatból, vagy pedig kizárólag a kloákából vett tamponmintát gyűjti össze (nem pedig mindkettőt) attól függően, hogy a vírus a légzőszervekben vagy a gyomor-bél traktusban terjed-e jobban, illetve figyelembe véve az érintett fajokat.
b) A szerológiai vizsgálatra küldött szabványos mintacsomag minimum 20 darab vérmintából áll.
A mintákat a b) alpontban megadott számú madárból, vagy pedig (ennél kisebb létszámú állomány esetén) a gazdaság valamennyi madarából kell venni. A mintákat a láthatóan beteg, vagy felgyógyult madarakból kell venni.
Az illetékes hatóság dönthet úgy, hogy nem szükséges a szabványos minták teljes skáláját begyűjteni, hanem elegendő e minták egy része is.
5. A minták szállítása
A mintákat különleges figyelemmel kell tárolni, illetve a laboratóriumi vizsgálathoz szállítani.
A tamponmintákat jég vagy fagyasztott gél segítségével azonnal le kell hűteni és a lehető leghamarabb el kell őket juttatni a laboratóriumba. A mintákat csupán végszükséglet esetén szabad mélyhűteni. Ha a laboratóriumba történő szállítás 24 órán belül nem megoldható, a mintákat azonnal le kell fagyasztani, és szárazjégen kell tárolni, majd szállítani.
Ezenkívül - és nem ezt helyettesítendő - a tamponmintákat 4 °C-os antibiotikumos közegbe vagy különleges vírusszállító közegbe kell tenni oly módon, hogy az teljes mértékben lefedje a mintákat. Ilyen anyag hiányában a tamponmintákat vissza kell helyezni foglalatukba és száraz állapotban kell őket vizsgálat céljából a laboratóriumba küldeni.
A minták tárolását és szállítását több tényező is befolyásolhatja, ezért a kiválasztott szállítási módnak a célnak megfelelőnek kell lennie.
6. Antibiotikumos közeg
Az 5. pontban említett antibiotikumos közeg alapját 7,0-7,4 pH-jú foszfáttal pufferolt sóoldatnak kell képeznie (a pH-t az antibiotikum hozzáadása után ellenőrizni kell).
Proteinalapú közeg (mint például az agy-szív leves, vagy a tris-szel pufferolt triptóz) nagyobb stabilitást nyújthat a vírusnak, különösen a szállítás alatt. A felhasznált antibiotikumokat és ezek koncentrációját a helyi viszonyok és a hozzáférhetőség szerint módosítani lehet.
A bélsármintákhoz igen magas antibiotikum-szintre van szükség, amelynek megfelelő összeállítása: 10 000 NE/ml penicillin, 10 mg/ml sztreptomicin 0,25 mg/ml gentamicin és 5 000 NE/ml nisztatin. Ezek a mennyiségek ötödrészükre csökkenthetők a szövetek és a légcsőből vett tamponminták esetén.
A Chlamydiák gátlására 0,05-0,1 mg/ml oxitetraciklint kell adni a mintákhoz.
7. Agy-szív leves készítése
Porított agy-szív-leves alapanyagból 15 % súly/térfogatú oldatot készítünk desztillált vízben, majd 121 °C-on, 15 percig autoklávozással sterilizáljuk.
Sterilizálás után a következőket kell hozzáadni: 10 000 NE/ml penicillin G, 20 μg amfotericin B és 1 000 μg/ml gentamycin. A közeget 4 °C-on legfeljebb két hónapig lehet tárolni.
8. Alkalmazandó eljárások a 2005/94/EK irányelv megfelelő rendelkezései tekintetében
8. A. A járványkitörés gyanúja
8.1. 7. cikk (1) bekezdése - A járványkitörés gyanúja esetén az érintett gazdaságokban alkalmazandó intézkedések
Ha egy hatósági állatorvos olyan gazdaság ellenőrzését végzi, ahol járványkitörés gyanúja áll fenn, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és az egészségügyi nyilvántartásait (ha vannnak ilyenek). A hatósági állatorvosnak a vizsgálati jelentésbe be kell vezetnie a napi mortalitásra és a napi tojástermelésre vonatkozó adatokat, illetve az azon időtartamra vonatkozó folyadék- és/vagy táplálékfelvétel mennyiségét, amely a madárinfluenza klinikai tünetei megjelenése előtt egy héttel kezdődött és amely a hatósági állatorvos vizsgálatának napján ér véget.
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy a más, fogságban tartott madarakat (különösen a láthatóan beteg egyedeket) klinikai vizsgálat alá kell vetni.
c) Valamennyi termelési egységből szabványos mintát kell venni, kivéve, ha az illetékes hatóság meggyőződött arról, hogy a járványkitörés gyanúját az a) és b) alponttal összhangban végzett klinikai vizsgálat alapján ki lehet zárni.
d) A szabványos minták negatív vizsgálati eredményeitől függetlenül, és a helyi tényezők figyelembevételével valamennyi termelési egységben található baromfi klinikai vizsgálatát végre kell hajtani, mielőtt a hatósági megfigyelést feloldanák.
8.2. 10. cikk (3) bekezdése - A járványügyi vizsgálaton alapuló kiegészítő intézkedések
Valamennyi termelési egységben szabványos mintát kell venni a leölt baromfiból vagy más, fogságban tartott leölt madarakból.
8. B. Magas patogenitású madárinfluenza (HPAI)
8.3. 11. cikk (4) bekezdése - Olyan gazdaságokból begyűjtött tojásokból kikelt baromfi esetében alkalmazandó intézkedések, ahol a járvány jelenlétét már bebizonyították
Ha egy hatósági állatorvos olyan gazdaság ellenőrzését végzi, ahol magas patogenitású madárinfluenzával fertőzött gazdaságból a lappangási időszak alatt begyűjtött tojásokból kikelt baromfi van jelen, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait. A hivatalos állatorvosnak a gazdaságról szóló vizsgálati jelentésbe be kell vezetnie a napi mortalitásra vonatkozó adatokat, illetve az azon időtartamra vonatkozó táplálék- és/vagy folyadékfelvétel mennyiségét (amennyiben ez az adat rendelkezésre áll), amely a magas patogenitású madárinfluenza klinikai tüneteinek megjelenése előtt egy héttel kezdődött és amely a hatósági állatorvos vizsgálatának napján ér véget.
b) Valamennyi termelési egységet, illetve a baromfit (különösen azokat, amelyek betegnek tűnnek vagy amelyek nem a vártnak megfelelően fejlődnek) klinikai vizsgálat alá kell vetni.
c) A szabványos mintákat 2-3 hetes baromfiból kell venni.
d) A 21 napnál idősebb baromfin végzett klinikai vizsgálatot és a szabványos minták negatív vizsgálati eredményeit követően a hatósági megfigyelés feloldható.
8.4. 13. cikk (2) bekezdésének b) pontja - Egyes gazdaságokra vonatkozó eltérések
Ha egy hatósági állatorvos olyan gazdaság ellenőrzését végzi, amelynek eltérést engedélyeztek a 2005/94/EK irányelv 11. cikke (2) bekezdésének első albekezdésétől, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait (ha vannak ilyenek).
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy más, fogságban tartott madarakat (különösen a láthatóan beteg egyedeket) klinikai vizsgálat alá kell vetni.
c) Laboratóriumi vizsgálat céljából a szabványos minták helyett a következő mintákat kell venni valamennyi termelési egységből, 21 nappal a magas patogenitású madárinfluenza utolsó pozitív eredménye után és 21 napos időközönként:
i. a mintavétel idején jelen lévő bármely elhullott baromfiból vagy más, fogságban tartott madarakból származó minták;
ii. amennyiben gyakorlatilag lehetséges, legalább 60 baromfiból vagy más, fogságban tartott madárból légcső-, garat- és kloáka-tamponmina; ha 60-nál kevesebb baromfi vagy más, fogságban tartott madár van a gazdaságban, akkor mindegyikből mintát kell venni; vagy pedig ha a madár kis termetű, egzotikus és olyan, amelyhez nem szoktak kézzel hozzányúlni, illetve amelynek kézben tartása veszélyes lehet az emberre, friss bélsármintát kell gyűjteni.
A kockázatértékelési eredmények alapján az illetékes hatóság azonban eltérést engedélyezhet az i. és ii. alpontban említett mintamérettől.
d) A c) alpontban említett mintavételt és e minták laboratóriumi vizsgálatát addig kell megismételni, ameddig legalább két negatív laboratóriumi eredmény nem születik, egymástól 21 nap különbséggel.
8.5. 15. cikk (1) és (3) bekezdése - A kontaktgazdaságokban alkalmazandó intézkedések
Ha egy hatósági állatorvos kontaktgazdaság ellenőrzését végzi, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait (ha vannak ilyenek). A hatósági állatorvosnak a gazdaságról szóló vizsgálati jelentésbe be kell vezetnie a napi mortalitásra vonatkozó adatokat, illetve az azon időtartamra vonatkozó táplálék- és/vagy folyadékfelvétel mennyiségét (amennyiben ez az adat rendelkezésre áll), amely a madárinfluenza-gyanús állománnyal történő érintkezés időpontja előtt egy héttel kezdődött és amely a hatósági állatorvos vizsgálatának napján ér véget.
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy más, fogságban tartott madarakat (különösen a láthatóan beteg egyedeket) klinikai vizsgálat alá kell vetni.
c) Valamennyi termelési egységből azonnal szabványos mintát kell venni, ha a baromfinál vagy más, fogságban tartott madaraknál klinikai tünetek jelentkeznek, illetve ha a napi mortalitás megnövekszik (az állomány rendes napi elhullási arányának legalább háromszorosára), a napi tojástermelés csökken (több mint 5 %-kal), vagy a napi táplálék- és/vagy folyadékfelvétel csökken (több mint 5 %-kal).
d) Amennyiben a b) és c) alpontban említett tünetek hiányoznak, a szabványos mintákat a fertőzött gazdasággal való utolsó valószínűsíthető érintkezéstől, illetve a baromfi, vagy más, fogságban tartott madarak leölésétől számított 21 nap elteltével kell venni.
8.6. 18. cikk b) és c) pontja - A hatósági állatorvos általi számbavétel és ellenőrzések, valamint megfigyelés a védőkörzetben elhelyezkedő gazdaságokban
Ha egy hatósági állatorvos kereskedelmi célú gazdaság ellenőrzését végzi, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait. Valamennyi termelési egységből szabványos mintát kell venni, ha a napi mortalitás megnövekszik (az állomány rendes napi elhullási arányának legalább háromszorosára), a napi tojástermelés csökken (több mint 5 %-kal), vagy a napi táplálék- és/vagy folyadékfelvétel csökken (több mint 5 %-kal).
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit és más, fogságban tartott madarakat (különösen a láthatóan beteg egyedeket) klinikai vizsgálat alá kell vetni.
c) Ha a baromfifajtáktól vagy a más, fogságban tartott madaraktól nem várható, hogy világosan körülhatárolható klinikai tüneteket mutassanak, illetve ha vakcinázott madarakról van szó, az illetékes hatóság a kockázatértékelési eredmények alapján dönthet úgy, hogy valamennyi termelési egységből szabványos mintavételt ír elő.
d) A kockázatértékelési eredmények alapján az illetékes hatóságnak döntenie kell arról, hogy van-e szükség klinikai vizsgálat formájában történő további hatósági megfigyelésre és laboratóriumi vizsgálathoz vett mintákra az érintett gazdaságokban, egységekben vagy termelési típusokban.
8.7. 19. cikk f) pontja - A védőkörzetben elhelyezkedő gazdaságokban alkalmazandó intézkedések
Ha egy hatósági állatorvos olyan gazdaság ellenőrzését végzi, amelyből megnövekedett morbiditást, mortalitást vagy a termelési adatok megváltozását jelentették, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait. Valamennyi termelési egységből szabványos mintát kell venni, ha a napi mortalitás megnövekszik (az állomány rendes napi elhullási arányának több mint háromszorosára), a napi tojástermelés csökken (több mint 5 %-kal), vagy a napi táplálék- és/vagy folyadékfelvétel csökken (több mint 5 %-kal).
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy más, fogságban tartott madarakat (különösen a láthatóan beteg egyedeket) klinikai vizsgálat alá kell vetni.
8.8. 23. cikk b) pont - Eltérések az azonnali levágásra szánt baromfi közvetlen szállítására vonatkozóan
Ha egy hatósági állatorvos olyan gazdaság ellenőrzését végzi, amelynek eltérést engedélyeztek a 2005/94/EK irányelv 22. cikkétől, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait.
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. Az elszállítás időpontját megelőző 24 órán belül valamennyi baromfit klinikai vizsgálat alá kell vetni, különösen a láthatóan beteg egyedeket.
c) Az illetékes hatóság által végzett kockázatértékelés eredménye alapján és a szabványos minták helyett a baromfiból legalább 60 darab légcső-, garat- és/vagy 60 darab kloáka-tamponmintát kell venni valamennyi olyan termelési egységből, amelyből a baromfit levágásra szánják. A tamponmintákat a baromfi szállítását megelőző 48 órán belül kell venni.
8.9. 25. cikk b) pont - Eltérések a fiatal tojóbaromfi közvetlen szállítására vonatkozóan
Ha egy hatósági állatorvos olyan gazdaság ellenőrzését végzi, amelynek eltérést engedélyeztek a 2005/94/EK irányelv 22. cikkétől, a következő intézkedéseket kell végrehajtani a fiatal tojóbaromfi közvetlen szállítása előtt:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait.
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. Az elszállítás időpontját megelőző 24 órán belül valamennyi baromfit klinikai vizsgálat alá kell vetni, különösen a láthatóan beteg egyedeket.
c) Az illetékes hatóság által végzett kockázatértékelés eredményei alapján és a szabványos minták helyett legalább 60 baromfiból kell légcső-, garat- és/vagy kloáka-tamponmintát venni valamennyi olyan termelési egységből, amelyből a baromfit szállítani kívánják. A tamponmintákat a baromfi szállítását megelőző 48 órán belül kell venni.
8.10. 26. cikk (1) bekezdésének a) pontja - Eltérés a keltető- és étkezési tojás közvetlen szállítására vonatkozóan
Ha egy hatósági állatorvos olyan gazdaság ellenőrzését végzi, amely szülőállományból áll, és amelynek engedélyeztek a 22. cikktől való eltérést, a következő intézkedéseket kell végrehajtani a keltetőtojások közvetlen szállítása előtt:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait.
b) 15 naponként valamennyi termelési egységet klinikai vizsgálat alá kell vetni.
c) Valamennyi termelési egységből szabványos mintát kell venni.
8.11. 29. cikk (1) bekezdése - Az intézkedések időtartama
A védőkörzetben a 2005/94/EK irányelv IV. fejezetének 3. szakaszával összhangban alkalmazott intézkedések legkorábban a fertőzött gazdaságok előkészítő tisztítását és fertőtlenítését követő 21. nap után oldhatók fel, amennyiben:
a) A hatósági állatorvos a védőkörzetben elhelyezkedő valamennyi kereskedelmi célú gazdaságot megvizsgálta, és a 8.6. pont a), b) és c) alpontjában, illetve a 8.7. pontban meghatározott valamennyi ellenőrzés, klinikai és laboratóriumi vizsgálat negatív eredménnyel zárult.
b) A hatósági állatorvos a védőkörzetben elhelyezkedő valamennyi beazonosított nem kereskedelmi célú gazdaságot megvizsgálta, és sem a klinikai vizsgálat, sem pedig a laboratóriumi vizsgálatok eredményei nem utaltak a madárinfluenza-fertőzés gyanújára.
c) A 8.6. pont d) alpontja szerinti további hatósági vizsgálat negatív eredményekkel zárult.
8.12. 30. cikk g) pont - A megfigyelési körzetekben alkalmazandó intézkedések
Ha egy hatósági állatorvos olyan gazdaság ellenőrzését végzi, amelyből megnövekedett morbiditást, mortalitást vagy a termelési adatok megváltozását jelentették, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait.
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy más, fogságban tartott madarakat (különösen a láthatóan beteg egyedeket) klinikai vizsgálat alá kell vetni.
c) Valamennyi termelési egységből szabványos mintát kell venni.
8.13. 35. cikk - A magas patogenitású influenza vágóhidakon és szállítóeszközökön való jelenléte gyanújának kivizsgálása
Ha egy hatósági állatorvos olyan gazdaság ellenőrzését végzi, ahonnan vágóhidakra vagy szállítóeszközökre küldtek madarakat (származási gazdaság), a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait (ha vannak ilyenek).
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy a más, fogságban tartott madarakat klinikai vizsgálat alá kell vetni, figyelembe véve a vágóhíd hatósági állatorvosával történő konzultációt, aki részletekkel kell, hogy szolgáljon bármely korábbi fertőzéssel kapcsolatos adatokról és a vizsgálati, illetve kórbonctani eredményekről.
c) Valamennyi termelési egységből szabványos mintát kell venni, kivéve, ha az illetékes hatóság meggyőződött arról, hogy a magas patogenitású madárinfluenza jelenlétének gyanúját az a) és b) alponttal összhangban végzett állatorvosi vizsgálat alapján ki lehet zárni.
d) Laboratóriumi vizsgálatra a szabványos mintákon kívül mintát kell küldeni a vágóhídon lévő és kóros elváltozásokat mutató, legalább öt beteg, elpusztult vagy levágott madárból is.
8.14. 36. cikk (1) bekezdése - A vágóhidakon alkalmazandó intézkedések
A 8.13. pontban említett vizsgálatok befejezése után és feltéve, hogy a laboratóriumi vizsgálatok eredménye negatív, valamint a származási gazdaságban és a váróhídon a magas patogenitású madárinfluenza jelenlét nem támasztják alá klinikai eredmények, a hatósági felügyelet feloldható.
8.15. 37. cikk (1) és (2) bekezdése - Az állat-egészségügyi határállomásokon vagy szállítóeszközök esetén alkalmazandó intézkedések
8.15.1. Ha egy hatósági állatorvos a nagy patogenitású madárinfluenza gyanúja vagy megerősített jelenléte miatt állat-egészségügyi határállomásról vagy pedig szállítóeszközről származó, elszigetelt helyen (karanténban) tartott baromfit vagy más, fogságban tartott madarat vizsgál, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a megfelelő dokumentációkat és nyilvántartásokat (ha vannak ilyenek).
b) Klinikai vizsgálat alá kell vetni ezen elszigetelt helyre vitt baromfit vagy más, fogságban tartott madarakat, illetve a láthatóan beteg többi baromfit vagy más, fogságban tartott madarakat.
c) Szabványos mintát kell venni különböző, szállításra használt ketrecben vagy kalitkában lévő baromfiból vagy a más, fogságban tartott madárból.
8.15.2. Ha egy hatósági állatorvos olyan beazonosított származási gazdaság ellenőrzését végzi, ahol olyan baromfit vagy a más, fogságban tartott madarakat tartottak, amelyeket levágtak, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait (ha vannak ilyenek).
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy a más, fogságban tartott madarakat klinikai vizsgálat alá kell vetni, figyelembe véve a vágóhíd hatósági állatorvosával történő konzultációt, aki részletekkel kell, hogy szolgáljon bármely korábbi fertőzéssel kapcsolatos adatokról és a vizsgálati, illetve kórbonctani eredményekről.
c) Valamennyi termelési egységből szabványos mintát kell venni, kivéve, ha az illetékes hatóság meggyőződött arról, hogy a magas patogenitású madárinfluenza jelenlétének gyanúját az a) és b) alponttal összhangban végzett állatorvosi vizsgálat alapján ki lehet zárni.
d) A c) alpontban említett szabványos mintákon kívül a vágóhídon jelen lévő és kóros elváltozásokat mutató legalább öt beteg, elpusztult vagy levágott madárból vett mintákat laboratóriumi vizsgálatra kell küldeni.
e) Feltéve, hogy a c) és d) alpontban említett minták laboratóriumi vizsgálata negatív, és hogy a származási gazdaságban valamint a váróhídon a magas patogenitású madárinfluenza jelenlétét nem támasztják alá klinikai eredmények, a hatósági felügyelet feloldható.
8. C. Alacsony patogenitású madárinfluenza (LPAI)
8.16. 39. cikk (6) bekezdésének b) és h) pontja - Alacsony patogenitású madárinfluenza-járvány megerősített kitörése esetén az érintett gazdaságokban alkalmazandó intézkedések
Ha egy hatósági állatorvos egy gazdaság ellenőrzését végzi mielőtt a baromfit a vágóhídra szállítják, illetve ha egy állatorvos olyan gazdaság ellenőrzését végzi, ahol lappangási időszak alatt begyűjtött tojásokból kikelt baromfi található, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait.
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy a más, fogságban tartott madarakat klinikai vizsgálat alá kell vetni.
c) Valamennyi termelési egység levágásra szánt madaraiból szabványos mintát kell venni, a baromfi elszállítását megelőző 48 órán belül.
d) Valamennyi termelési egységben a lappangási időszak alatt begyűjtött tojásokból kikelt baromfiból szabványos mintát kell venni
8.17. 40. cikk (2) bekezdésének b) pontja - Egyes gazdaságoknak engedélyezett, a járványkitörés esetén alkalmazandó intézkedésekre vonatkozó eltérések
Ha egy hatósági állatorvos olyan gazdaság ellenőrzését végzi, amelynek eltérést engedélyeztek a 2005/94/EK irányelv 39. cikkének (2) bekezdésétől és 39. cikke (5) bekezdésének b) pontjától, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait (ha vannak ilyenek).
b) Rendszeres időközönként valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy más, fogságban tartott madarakat (különösen a láthatóan beteg egyedeket) klinikai vizsgálat alá kell vetni.
c) A laboratóriumi vizsgálat számára a szabványos minták helyett a következő mintákat kell venni valamennyi termelési egységből, 21 nappal az alacsony patogenitású madárinfluenza utolsó pozitív eredménye után és 21 napos időközönként:
i. a mintavétel idején jelen lévő bármely elhullott baromfiból vagy más, fogságban tartott madárból származó minták;
ii. 60 baromfiból vagy más, fogságban tartott madárból vett légcső-, garat- és kloáka-tamponminta; ha a gazdaságban 60-nál kevesebb baromfi vagy más, fogságban tartott madár van, akkor mindegyikből mintát kell venni; friss bélsármintát kell gyűjteni olyan kis termetű, egzotikus baromfi vagy más, fogságban tartott madarak esetén, amelyekhez nem szoktak kézzel hozzányúlni, illetve amelyek kézben tartása veszélyes lehet az emberre.
A kockázatértékelési eredmények alapján az illetékes hatóság ugyanakkor felmentést adhat az i. és ii. alpontban említett mintaméret alól.
d) A c) alpontban említett mintavételt és e minták laboratóriumi vizsgálatát addig kell megismételni, ameddig legalább két negatív laboratóriumi eredmény nem születik, egymástól 21 nap különbséggel.
8.18. 42. cikk (1) és (3) bekezdése - A kontaktgazdaságokban alkalmazandó intézkedések
Ha egy hatósági állatorvos kontaktgazdaság ellenőrzését végzi, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a kontaktgazdaság termelési és egészségügyi nyilvántartásait (ha vannak ilyenek).
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy a más, fogságban tartott madarakat (különösen a láthatóan beteg egyedeket) klinikai vizsgálat alá kell vetni.
c) Valamennyi termelési egységből, vagy pedig a baromfi, illetve más, fogságban tartott madár leölésekor szabványos mintát kell venni.
8.19. 44. cikk (1) bekezdésének b) pontja - Korlátozás alatt álló körzetben alkalmazandó intézkedések
Ha egy hatósági állatorvos korlátozás alatt álló körzetben található kereskedelmi célú gazdaság ellenőrzését végzi, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait.
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy más, fogságban tartott madarakat (különösen a láthatóan beteg egyedeket) klinikai vizsgálat alá kell vetni.
c) Valamennyi termelési egységből szabványos mintát kell venni.
d) A kockázatértékelési eredmények alapján az illetékes hatóságnak döntenie kell arról, hogy van-e szükség klinikai vizsgálat formájában történő további hatósági megfigyelésre és laboratóriumi vizsgálathoz vett mintákra az érintett gazdaságokban, egységekben vagy termelési típusokban.
8.20. 45. cikk a) és b) pontja - Az intézkedések időtartama
A korlátozás alatt álló körzetben a 2005/94/EK irányelv V. fejezetének 3. szakaszával összhangban alkalmazott intézkedéseket legkorábban a fertőzött gazdaságoknak a kiürítés utáni előkészítő tisztítását és fertőtlenítését követő 21. nap után, vagy pedig legkorábban az alacsony patogenitású madárinfluenza megállapítását követő 42. nap után lehet feloldani, feltéve, hogy:
a) a hatósági állatorvos a korlátozás alatt álló körzetben található valamennyi kereskedelmi célú gazdaságot megvizsgálta és a 8.13. pont c) és d) alpontjában említett minták valamennyi laboratóriumi vizsgálata megtörtént és eredményeik rendelkezésre állnak;
b) valamennyi további klinikai és laboratóriumi vizsgálat eredménye rendelkezésre áll (e vizsgálatok irányulhatnak nem kereskedelmi célú gazdaságokra is, az alacsony patogenitású madárinfluenza veszélyének megállapítása céljából);
c) az illetékes hatóság a járványügyi helyzetet figyelembe vevő kockázatértékelés, illetve az a) és b) alpontban említett laboratóriumi vizsgálat eredményei alapján meggyőződött arról, hogy az alacsony patogenitású madárinfluenza elterjedésének veszélye elhanyagolható; ezen értékelés megállapíthatja, hogy amennyiben a szerológiai eredmények pozitívak és a virológiai eredmények negatívak, a megszorításokat fel lehet oldani.
8. D. A madaraktól származó influenzavírusok más fajokra történő átterjedésének elkerülését szolgáló intézkedések
8.21. 47. cikk (1) és (6) bekezdése - Sertéseket és más fajokat érintő laboratóriumi vizsgálatok és egyéb intézkedések
Ha egy hatósági állatorvos olyan gazdaság ellenőrzését végzi, ahol sertéseket tartanak, a madárinfluenza megállapítását követően a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait (ha vannak ilyenek).
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A sertéseket (különösen a láthatóan beteg egyedeket) klinikai vizsgálat alá kell vetni.
c) Valamennyi termelési egységben legalább 60 sertésből orr-, és garat-tamponmintát kell venni, ha a termelési egységben 60-nál kevesebb sertés van, akkor mindegyikből mintát kell venni; a mintavételt a fertőzött baromfi vagy más, fogságban tartott madár leölése napján, vagy az azt megelőző napon kell elvégezni. Legalább 60 darab vérmintát kell venni a sertésekből, a leölés időpontját követő 2-4 héten belül. A mintákat úgy kell venni, hogy legalább egy minta az egymással közvetlen kapcsolatban álló sertések csoportjából származzon.
d) A sertések más gazdaságokba történő szállítása akkor engedélyezhető, ha valamennyi termelési egységben a legalább 60 sertésből a madárinfluenza jelenléte pozitív megerősítésének időpontját követő 14. nap után vett orr- és garat-tamponminta, valamint a 60 vérminta negatív eredményeket adott.
A sertések vágóhídra történő szállítása akkor engedélyezhető, ha valamennyi termelési egységben a legalább 60 sertésből a madárinfluenza jelenlétének megállapítása után 14 nappal vett orr- és garat-tamponminta negatív eredményeket adott.
Nem meggyőző vagy pozitív laboratóriumi eredmények esetén további vizsgálatokat kell elvégezni abból a célból, hogy a fertőzést, illetve a madárinfluenzának a sertések körében történő elterjedését kizárják.
e) Laboratóriumi vizsgálat céljából mintavételre van szükség, ha a hatósági állatorvos arra gyanakszik, hogy a gazdaság más háziasított emlősei (különösen azok, amelyekről ismert, hogy fogékonyak a H5 és H7 altípusú madárinfluenza-vírussal történő fertőzésre) érintkezésbe kerülhettek a fertőzött baromfival vagy a más, fogságban tartott madarakkal.
8. E. Újratelepítés
8.22. 49. cikk (2) bekezdése b) és c) pontja - A gazdaságok újratelepítése
Ha egy hatósági állatorvos újratelepített, kereskedelmi célú gazdaság ellenőrzését végzi, a következő intézkedéseket kell végrehajtani:
a) Meg kell vizsgálni a gazdaság termelési és egészségügyi nyilvántartásait.
b) Valamennyi termelési egységet klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy más, fogságban tartott madarakat (különösen a láthatóan beteg egyedeket) klinikai vizsgálat alá kell vetni.
c) A szabványos minták helyett a következő mintavételekre kell sort keríteni :
i. legalább 20 darab vérmintát az újra betelepített baromfiból (rögtön a betelepítés után), kivéve a naposcsibéket; amennyiben ez megfelelőnek tűnik, az ilyen mintavételt a származási gazdaság baromfiján is el lehet végezni, mielőtt azokat újratelepítés céljából a gazdaságba szállítják;
ii. hetente legfeljebb 10 elhullott madárból vett minták vagy tetemükből vett tamponminták, az újratelepítés időpontjától számított 21 napon keresztül.
d) Ha a gazdaság korábban magas patogenitású madárinfluenzával volt fertőzött, valamennyi termelési egység vízimadaraiból (kacsákból/ludakból) 20 darab légcső-/garat- és 20 darab kloáka-tamponmintát kell venni, az újratelepítés időpontjától számított 21 napos időszak utolsó hetében.
e) Ha a gazdaság korábban alacsony patogenitású madárinfluenzával volt fertőzött, valamennyi termelési egységből 20 darab légcső-/garat- és 20 darab kloáka-tamponmintát, valamint 20 darab vérmintát kell venni.
8. F. Vakcinázás
8.23. 56. cikk (2) bekezdésének i) pontja - Baromfi vagy más, fogságban tartott madarak megelőző vakcinázása
Amennyiben a vadvírus ismert, a beoltott baromfit vagy más, fogságban tartott madarakat a jóváhagyott DIVA-próbák alkalmazásával a 2005/94/EK irányelv IX. fejezetében meghatározott laboratóriumi vizsgálat alá kell vetni.
Ha jelzőmadarak használatára kerül sor, akkor valamennyi beoltott állományban kell, hogy legyenek ilyen madarak; klinikai vizsgálat alá kell őket vetni és hemagglutináció-gátlási próbát (HI) kell rajtuk elvégezni. E célból valamennyi beoltott gazdaságban a be nem oltott jelzőmadarakból legalább 60 naponként 20 darab vérmintát kell venni.
8.24. IX. melléklet - A sürgősségi vakcinázással kapcsolatban a baromfi vagy más, fogságban tartott madarak, valamint a baromfitermékek mozgatására vonatkozó követelmények
Az élő baromfi és más, fogságban tartott madarak, valamint ezek tojásainak mozgatására szigorú ellenőrző intézkedéseket kell alkalmazni annak érdekében, hogy a magas patogenitású madárinfluenza-fertőzés továbbterjedésének veszélye minimálisra csökkenjen.
E célból a sürgősségi vakcinázási kampány elején ugyanezeket az ellenőrző intézkedéseket kell alkalmazni az élő baromfi és más, fogságban tartott madarak, valamint ezek tojásainak mozgatására vonatkozóan annak érdekében, hogy a magas patogenitású madárinfluenza-fertőzés továbbterjedésének veszélye minimálisra csökkenjen a vakcinázási területen belül és kívül.
a) A hatósági állatorvosnak legalább 30 naponként a következő intézkedéseket kell végrehajtania a keltető- és étkezési tojásoknak a vakcinázási területen belül, és onnan kívülre történő első mozgatása előtt:
i. Valamennyi termelési egység be nem oltott szülőállományát vagy tojó baromfiját klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit (különösen a láthatóan beteg egyedeket) klinikai vizsgálat alá kell vetni; valamennyi termelési egység baromfijából szabványos mintákat kell venni; vagy
ii. valamennyi termelési egység beoltott szülőállományát vagy tojó baromfiját klinikai vizsgálat alá kell vetni, ideértve a termelési egység klinikai múltjának ellenőrzését is. Az ezen állományokban található jelzőmadarakat klinikai vizsgálat alá kell vetni; e jelzőmadarakból szabványos mintákat kell venni.
b) A hatósági állatorvosnak a következő intézkedéseket kell végrehajtania a beoltott élő baromfi vagy más beoltott, fogságban tartott madarak egyéb gazdaságokba történő mozgatása, vagy a beoltott élő baromfi vakcinázási területen belül, és onnan kívülre történő mozgatása során:
i. meg kell vizsgálnia a gazdaság termelési és egészségügyi nyilvántartásait;
ii. valamennyi termelési egységet klinikai vizsgálat alá kell vetnie, ideértve a termelési egység klinikai múltjának ellenőrzését is. A baromfit vagy más, fogságban tartott madarakat (különös figyelemmel a jelzőmadarakra) az indulás előtti 72 órán belül klinikai vizsgálat alá kell vetni;
iii. szabványos mintákat kell vennie a jelzőmadarakból, ha az i. és ii. alpontban említett ellenőrzés és klinikai vizsgálatok eredményei nem kielégítőek; amennyiben azonban az eredmények kielégítőek, a következő mintákat kell venni:
- a beoltott baromfiból vagy más, beoltott fogságban tartott madarakból: legalább 20 darab légcsőből/garatból vett tamponminta és 20 darab kloákából vett tamponminta, valamint 20 darab vérminta, az indulás előtti 72 órán belül a megfelelő DIVA-próba elvégzése érdekében, és
- jelzőmadarakból: 20 darab légcsőből/garatból vett tamponminta és 20 darab kloákából vett tamponminta, valamint 20 darab vérminta, a hemagglutináció-gátlási próbával (HI) végzett szerológiai vizsgálat indulás előtti elvégzése érdekében.
V. FEJEZET
Diagnosztikai virológiai vizsgálatok és az eredmények értékelése
1. A molekuláris alapú vizsgálatok megjelenéséig és kifejlesztéséig az embrionált tyúktojás oltásával történő vírusizolálás számított a madárinfluenza legérzékenyebb diagnosztikai vizsgálatának, illetve a fertőző vírus azt követő azonosításához és jellemzéséhez vezető elkerülhetetlen lépésének. A főbb lépéseket e fejezet határozza meg.
2. A minták feldolgozása
A száraz tamponnal vett mintákat olyan mennyiségű antibiotikumos közegbe kell helyezni, hogy az ellepje őket. A mintákat ötösével össze lehet vonni, amennyiben ugyanazon fajra, időpontra és járványügyi egységre vonatkoznak.
A laboratóriumba beküldött tetemeket kórbonctani vizsgálatnak kell alávetni és a következő szervekből kell mintákat venni: bélsár vagy béltartalom, agyszövet, légcső, tüdő, máj, lép és más, nyilvánvalóan érintett szervek. E szervek és szövetek összevonhatók, de a bélsár elkülönített kezelése alapvető fontosságú.
A bélsármintákat és a szerveket antibiotikumos közegben homogenizálni kell (zárt keverőt, mozsarat vagy dörzscsészét, valamint steril homokot használva), és 10-20 % tömegkoncentrációjú szuszpenziót kell létrehozni.
Az antibiotikumos közegbe helyezett tamponokat és a szuszpenziót körülbelül két órán át szobahőmérsékleten állni hagyjuk (vagy 4 °C-on hosszabb ideig), majd centrifugálással feltisztítjuk (pl. 800-1 000 x g 10 percig).
3. Vírusizolálás embrionált tyúktojásban
A tisztított felülúszó folyadékot 0,1-0,2 ml mennyiségben minimum négy darab, 9-11 napig keltetett embrionált tyúktojás allantoisüregébe fecskendezik. E tojásoknak ideális esetben specifikuskórokozó-mentes állományból (SPF) kell származniuk, de ha ez nem lehetséges, olyan állományból származó tojások is használhatók, amelyek mentesek a madárinfluenzával szemben termelődött ellenanyagtól (szeronegatív).
A beoltott tojásokat 37 °C-on kell tartani, és naponta kell lámpázni. Az elpusztult vagy pusztuló embriójú tojásokat, valamint az oltást követő hatodik nap után megmaradt tojásokat 4 °C-ra le kell hűteni, és az allantois-/amnion-folyadékokban vizsgálni kell a hemagglutinációs aktivitást. Ha nem mutatható ki hemagglutináció, az eljárást meg kell ismételni, inokulumként hígítatlan allantois-/amnion-folyadékot használva. Ha a hemagglutináció kimutatható, a baktériumok jelenléte a vírusfolyadékokban kizárandó. Ha a minta baktériumokkal kontaminált, a folyadékokat egy 450 nm-es membránfilteren át lehet szűrni, további antibiotikumokat lehet hozzáadni, majd a fenti eljárás szerint embrionált tojásokba oltható.
A diagnózis meggyorsítása céljából néhány laboratórium két 3 napos passzázst vagy egy 2 napos és egy 4 napos passzázst végzett és a két 6 naposhoz hasonló eredményekről számolt be, de ezt még nem bizonyították teljes mértékben.
Ellenőrizni kell, hogy a pozitív folyadékok ne tartalmazzanak baktériumokat. Amennyiben baktériumok találhatók benne, azok eltávolítása érdekében a folyadékokat egy 450 nm-es membránfilteren át lehet szűrni, vagy centrifugálni lehet és még több antibiotikum hozzáadása után a tojásokba újra befecskendezhető.
4. Differenciáldiagnózis
a) Előzetes differenciálás
Fontos, hogy a madárinfluenza-vírus terjedését megakadályozó védekező intézkedéseket a lehető leghamarabb hajtsák végre. A hemagglutináló vírust izoláló valamennyi nemzeti referencialaboratóriumnak meg kell tudnia határozni, hogy (H5 vagy H7 altípusú) A-típusú influenzavírusról, vagy baromfipestis-vírusról van-e szó. A hemagglutináció-gátlási próbákban hemagglutináló folyadékokat kell használni, a IX. fejezetben leírtaknak megfelelően. Az ideiglenes védekező intézkedések bevezetését lehetővé tévő előzetes azonosításra a pozitív gátlás szolgálhat (ami legfeljebb 2-3 log2-vel maradhat el a pozitív kontroll titerétől), az A-típusú és H5 vagy H7 altípusú influenzára jellemző poliklonális antiszérummal.
b) Megerősítő azonosítás
Mivel az influenzavírusoknak 16 hemagglutinin altípusa, és 9 neuraminidáz altípusa létezik, és ezeknek a kombinációi is előfordulnak, nem megvalósítható és nem is költséghatékony, hogy minden nemzeti referencialaboratórium az influenzavírus-izolátumok teljes altípusjellemzését lehetővé tevő antiszérumokat tartson. Valamennyi nemzeti referencialaboratóriumnak azonban legalább a következőket végre kell hajtania:
i. az antigéncsoportokat kimutató kettős immundiffúziós próbával meg kell erősítenie, hogy az izolátum valóban A-típusú influenza;
ii. meg kell határoznia, hogy az izolátum H5 vagy H7 altípusú-e. Pozitív eredmény esetén védekező intézkedések végrehajtására van szükség a H5 és H7 altípusú, alacsony patogenitású madárinfluenzával szemben;
iii. valamennyi magas patogenitású madárinfluenzát és valamennyi H5 és H7 izolátumot haladéktalanul a közösségi referencialaboratórium rendelkezésére kell bocsátania megerősítés és teljes mértékű jellemzés céljából. E követelményre vonatkozóan a d) pontnak megfelelően eltérést engedélyezhetnek.
A megfelelő eszközökkel rendelkező laboratóriumok számára ezenkívül kívánatos lenne:
iv. a VII. fejezetben ismertetett, hathetes csirkéken végzett intravénás patogenitási index vizsgálatot végrehajtania. Az 1,2-nél nagyobb intravénás patogenitási index azt jelzi, hogy a vírus jelenléte megkívánja a védekező intézkedések teljes mértékű végrehajtását a magas patogenitású madárinfluenzával szemben.
A nemzeti referencialaboratóriumoknak meg kell fontolniuk olyan szakértői vizsgálat bevezetését és olyan felszerelések felállítását, amelyek segítségével meghatározható a hemagglutinin-gén nukleotidszekvenciája annak megállapítására, hogy a H5 vagy H7 altípusú, alacsony patogenitású madárinfluenza-vírusban a bázikus aminosavak feldúsultak-e vagy sem a hemagglutin prekurzor fehérje vágáshelyénél. Noha a közösségi referencialaboratórium a 2005/94/EK irányelv VII. melléklete (2) bekezdésének b) pontjában említett feladatok részeként elsődleges prioritásai közé sorolja majd a patogenitás meghatározását, az ilyen vírusjellemzés nemzeti szinten nagy mértékben csökkenti a diagnosztizálásra, illetve pozitív eredmény esetén a magas patogenitású madárinfluenzával szembeni védekező intézkedések teljes körű végrehajtására rendelkezésre álló időt.
c) Az izolátumok további tipizálása és jellemzése
A nemzeti referencialaboratóriumoknak valamennyi hemagglutináló vírust el kell küldeniük a közösségi referencialaboratóriumba, hogy további antigén és genetikai vizsgálatok elvégzésére kerülhessen sor a betegség(ek) Közösségen belüli járványtanának jobb megértése érdekében, a közösségi referencialaboratóriumnak a 2005/94/EK irányelv VII. mellékletében meghatározott szerepével és feladataival összhangban .
E szerepen és feladatokon kívül a közösségi referencialaboratóriumnak minden átvett influenzavírus teljes antigén-tipizálását el kell végeznie. Az 1,2-nél nem nagyobb intravénás patogenitási indexszel ellátott H5 és H7 vírusnál is haladéktalanul el kell végezni a hemagglutinin-gén nukleotidszekvenciáját annak megállapítása érdekében, hogy a hemagglutin prekurzor fehérje vágáshelyénél a bázikus aminosavak feldúsultak-e vagy sem; a nemzeti referencialaboratóriumot és a származási ország illetékes hatóságát az eredmények megszületése után azonnal értesíteni kell, hogy teljes mértékben végre tudják hajtani a magas patogenitású madárinfluenzával szembeni védekező intézkedéseket.
d) A magas, illetve alacsony patogenitású madárinfluenzára vonatkozó változó járványügyi helyzetre való tekintettel egy, a Bizottság és a közösségi referencialaboratórium között létrejött megegyezés egyrészt eltérést engedélyezhet a vírus gyors jellemzésére képes laboratóriumoknak, hogy az adatok vizsgálatát követően e vírusok egy részét küldjék el; másrészt a közösségi referencialaboratóriumnak megfelelő válogatás létrehozására. Ezen eltérések csak akkor engedélyezhetők, ha a nemzeti referencialaboratórium gyors adatszolgáltatást tud biztosítani, és ha azokat haladéktalanul a közösségi referencialaboratórium rendelkezésére tudja bocsátani.
VI. FEJEZET
Molekuláris vizsgálatok és az eredmények értékelése
A magas patogenitású madárinfluenza jelenlegi meghatározása lehetővé teszi a virulenciatényezők molekuláris azonosítását és megerősíti a molekuláris technikák alkalmazását a madárinfluenza diagnosztizálásánál. Az utóbbi években a madárinfluenza-vírusnak a fertőzött madarakból vett klinikai minták segítségével történő kimutatása és jellemzése terén a molekuláris technikák alkalmazása fejlődésnek indult. A klinikai minták esetében alkalmazott hagyományos RT-PCR technikák (ha a primereket megfelelően meghatározták) hamar kimutatják a vírust, azonosítják az altípust (legalábbis a H5-öt és a H7-et) és a nukleotidszekventálására felhasználható amplifikált PCR-végterméket eredményeznek; az RT-PCR technikák alkalmazása bizonyítottan fontos lépés az elkövetkezendő járványok azonosításában, miután az elsődlegesen fertőzött helyek azonosítása és a vírus jellemzése megtörtént. Az egy lépésből álló, valós idejű RT-PCR, amely primer/fluoreszcenciás próbarendszereket használ (rRT-PCR), még gyorsabb és érzékenyebb diagnózist képes felállítani, amely klinikai mintákon történő madárinfluenzavírus-kimutatásból és a H5 vagy H7 altípus meghatározásából áll.
Az RT-PCR és az rRT-PCR rendszer problémája, hogy különböző laboratóriumok eddig különböző rendszereket dolgoztak ki, amelyeket - noha teljes mértékben szabályszerűek - még nem validáltak vagy ellenőriztek nagy számú mintákon és különböző laboratóriumokban. A közösségi referencialaboratórium és bizonyos nemzeti referencialaboratóriumok egy közösségi finanszírozású projekt (EU AVIFLU) keretében felvetették e problémát, és a hagyományos RT-PDR és rRT-PCR technikák olyan megerősített jegyzőkönyvezését javasolták, amelyeket egyéb nemzeti referencialaboratóriumok is elfogadhatnának. Amennyiben a próba paraméterei (mint például a ciklus és a hőmérséklet-emelkedés, a ramp mértéke) különböznek a jegyzőkönyvekben javasoltakétól, a próba alkalmazása előtt e diagnosztikai kézikönyv I. fejezetének 6. bekezdésével összhangban bizonyítani kell, hogy azok a célnak megfelelnek.
A molekuláris vizsgálatokhoz és értékelésükhöz a közösségi referencialaboratóriumban alkalmazott szabványos jegyzőkönyvek a következő weboldalon találhatók:
http://www.defra.gov.uk/corporate/vla/science/science-viral-ai-reflab.htm
VII. FEJEZET
In vivo patogenitási vizsgálat és az eredmények értékelése
A madarakból izolált A-típusú influenzavírusok virulenciáját csirkékben az intravénás patogenitási index vizsgálattal kell felmérni; a vizsgálatot a következőképpen kell elvégezni:
a) Friss allantoisfolyadékot (legalacsonyabb passzázsból, lehetőleg a kezdeti izolálásból származó, válogatás nélküli folyadékot, amely HA-keverési aránya >1/16 [reciprok értékben kifejezve: >24 vagy >log2 4]) 1/10-hez arányban steril izotóniás sóoldatban el kell keverni.
b) A hígított vírusból 0,1 ml-t intravénásan be kell adni mind a 10 hathetes szeronegatív vagy specifikus patogénmentes csirkébe.
c) Tíz napon át 24 óránként vizsgáljuk a madarakat. Valamennyi vizsgálat során a következő pontozási rendszert kell alkalmazni valamennyi madárra: 0 = egészséges, 1 = beteg, 2 = súlyos beteg, 3 = elpusztult. A "beteg" és "súlyos beteg" megállapítás szubjektív klinikai értékelés eredménye.
A "beteg" madarak rendesen a következő tünetek egyikét mutatják, míg a "súlyos beteg" madarak egynél több tünetet produkálnak: légzési panaszok, bágyadtság, hasmenés, a szabadon lévő bőr vagy bőrfüggelékek cianózisa, az arc és/vagy a fej ödémás elváltozása, idegrendszeri tünetek. Az elpusztult madarak az elpusztulásuk után naponta elvégzett valamennyi fennmaradó vizsgálatban a 3-as pontot kapják.
Állatvédelmi okokból az iváshoz és evéshez már túl beteg madarakat kíméletesen le kell ölni, és a következő vizsgálat során "elpusztult"-nak kell nyilvánítani, mivel beavatkozás nélkül 24 órán belül elpusztultak volna. Az akkreditációs hatóságok számára ezen eljárás elfogadható.
d) Az intravénás patogenitási index a madaranként és vizsgálatonként 10 napon keresztül adott pontok átlagának felel meg. A 3-as index azt mutatja, hogy 24 órán belül valamennyi madár elpusztult, míg a 0-s index azt jelzi, hogy a 10 napos megfigyelési időszak alatt egyetlen madáron sem mutatkoztak klinikai tünetek.
Az eredmények feljegyzésének és az indexek kiszámításának egyik egyszerű módját a következő táblázat példázza:
| Klinikai tünetek | Az oltástól számított nap | A pontok összesítése | |||||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | ||
| egészséges | 10 | 2 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 12 x 0 = 0 |
| beteg | 0 | 4 | 2 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 6 x 1 = 6 |
| súlyos beteg | 0 | 2 | 2 | 2 | 0 | 0 | 0 | 0 | 0 | 0 | 6 x 2 = 12 |
| elpusztult | 0 | 2 | 6 | 8 | 10 | 10 | 10 | 10 | 10 | 10 | 76 x 3 = 228 |
| Összesen = 246 | |||||||||||
Megjegyzések:
10 napon keresztül megfigyelt 10 madár = 100 megfigyelés
Index = átlag/madár/megfigyelés = 246/100 = 2,46
Az 1,2-nél nagyobb intravénás patogenitási index azt jelzi, hogy az adott A-típusú influenzavírust (tekintet nélkül az altípusra) magas patogenitású madárinfluenza-vírusnak kell tekinteni.
VIII. FEJEZET
Szerológiai vizsgálatok és az eredmények értékelése
A legjobb módszer az A-típusú influenzavírus jelenlétének kimutatására a valamennyi A-típusú influenzavírusban megtalálható nukleprotein vagy mátrixantigén-tartalom kimutatása.
Ezt általában kettős immundiffúziós próbával mutatják ki, amelyben vagy koncentrált víruskészítményeket, vagy a fertőzött chorioallantois hártyák kivonatát használják.
A madárinfluenza-vírusokkal szemben termelődött ellenanyagok kimutatására szolgáló szerológiai vizsgálatok kedvelt módszere a hemagglutinációs próba (HA) és a hemagglutináció-gátlási próba (Hl).
A Nemzetközi Állatjárványügyi Hivatal (OIE) szárazföldi állatok egészségügyi kódexének és a szárazföldi állatok diagnosztikai vizsgálatainak és a vakcinák szabványainak kézikönyvének 2.7.12. fejezete részletes információkat tartalmaz a laboratóriumi technikákkal és az eredmények értékelésével kapcsolatban.
A szerológiai vizsgálatok és azok eredményei értékelésének a közösségi referencialaboratóriumban alkalmazott szabványos jegyzőkönyvei a következő weboldalon találhatók:
http://www.defra.gov.uk/corporate/vla/science/science-viral-ai-reflab.htm
IX. FEJEZET
Vakcinázással kapcsolatos ellenőrző rendszerek
1. A 2005/94/EK irányelv és a diagnosztikai kézikönyv
A 2005/94/EK irányelv IX. fejezetének 2. és 3. szakasza bizonyos feltételek mellett engedélyezi a sürgősségi és megelőző vakcinázás alkalmazását. Az egyik ilyen feltétel, hogy a fertőzött állatoknak a beoltottaktól történő megkülönböztetése stratégiáját (DIVA-stratégia, Differentiating Infected from Vaccinated Animals) alkalmazzák.
A vakcinázást abból a célból kell elvégezni, hogy megelőzzék a fertőzést és a vírus későbbi terjedését az állományok között. Vitán felül álló bizonyítékok léteznek arra vonatkozóan, hogy a vakcinázás növeli a madarak megfertőzéséhez szükséges vírus mennyiségét és csökkenti a kiválasztódott vírusok mennyiségét. Annak ellenére azonban, hogy a beoltott madarakon nem jelentkeznek klinikai tünetek, a vírust ezek a madarak - ha fertőzöttek - még mindig képesek terjeszteni. Ezért a H5 vagy H7 altípusú, magas patogenitású madárinfluenza-vírusok bizonyos ideig észrevétlenül terjedhetnek olyan állományban, amelynek immunszintje nem optimális, ugyanúgy, mint ahogy az alacsony patogenitású madárinfluenza-vírusok terjedhetnek egy be nem oltott állományban. Ezért tudni kell azonosítani a vadvírus által fertőzött, víruspozitív beoltott állományokat annak érdekében, hogy más védekező intézkedések (mint például az állományok felszámolása) végrehajthatók legyenek.
2. Jelzőmadarak használata a fertőzés ellenőrzése céljából
Az állomány szintjén megvalósítható egyszerű módszer az, ha rendszeresen ellenőrizzük a valamennyi beoltott állományban jelen lévő, be nem oltott jelzőmadarakat, ugyanakkor e megközelítés néhány szervezési problémával jár, a jelzőmadarak azonosítása különösen a nagy állományokban például nehézségekbe ütközhet. Biztosítani kell, hogy a jelzőmadarak és a beoltott madarak érintkezzenek egymással.
3. DIVA laboratóriumi vizsgálat a fertőzés ellenőrzése céljából
E módszer alternatívájaként vagy kiegészítéseként a DIVA laboratóriumi vizsgálatok segítségével meg lehet állapítani, hogy a beoltott madarak vadvírus-expozíciónak vannak-e kitéve. Az elmúlt években több olyan vizsgálati rendszert fejlesztettek ki, amelyek kimutatják a beoltott madarak vadvírus-fertőzöttségét is. Az egyik ilyen használhatónak bizonyuló módszer az olyan vakcina alkalmazása, amely az adott vadvírussal megegyező hemagglutinin (H) altípusból, de attól különböző neuraminidázból (N) álló vírust tartalmaz. A vadvírusban jelen lévő neuraminidáz ellen termelt ellenanyagok a fertőzés természetes jelzői.
Ezt a módszert alkalmazták Olaszországban az alacsony patogenitású, H7N1 altípusú madárinfluenza-vírus újbóli felbukkanását követően. A közvetlen védekező intézkedések kiegészítéseként DIVA-stratégiát alkalmaztak, amely során H7N3 altípusú vírust tartalmazó vakcinát használtak a H7N1 vadvírus-fertőzés leküzdésére. A beoltott és a vadvírusnak kitett madarak megkülönböztetése szerológiai vizsgálattal történt, amely kimutatta a specifikus anti-N1 ellenanyagokat. Ugyanezt a módszert használták a H7N3 vírus okozta alacsony patogenitású madárinfluenza megfékezésére Olaszországban 2002/2003-ban; ebben az esetben H7N1 vakcinát és az N3-mal szemben termelődött ellenanyagokat kimutató szerológiai vizsgálatot alkalmaztak. A vakcinázás és az állományoknak a DIVA-stratégián alapuló felszámolása segítségével a vadvírust sikerült kiírtani.
E rendszer akkor okoz problémát, ha olyan vadvírus jelenik meg, amely ugyanolyan N antigénnel rendelkezik, mint a már meglévő vadvírus, de a H5-től vagy H7-től eltérő altípusú, illetve ha ugyanolyan N antigénnel rendelkező vírusaltípusok már jelen vannak az állományban. Különösen a kacsákról ismert, hogy egynél több altípus hordozói. Szükség volt olyan megfelelő vizsgálat kifejlesztésére is, amely lehetővé teszi az állományban az anti-neuraminidáz ellenanyagok rutinszerű ellenőrzését. Olaszországban kifejlesztettek és használtak egy indirekt fluoreszcens antitest-próbán alapuló "ad hoc" szerológiai vizsgálatot, amelyhez antigénként rekombináns bakulovírusok által exprimált N fehérjéket alkalmaztak. E vizsgálatok alkalmazása szélesebb körű és könnyebb lehet, amennyiben ELISA-vizsgálatot is végeznek.
A kizárólag HA-t tartalmazó vakcinák (mint például a rekombináns vektor vakcinák) alkalmazása lehetővé teszi a hagyományos AGID vagy ELISA vizsgálatot, amely a beoltott madarak fertőzöttségét a nukleoprotein, a nem strukturális fehérjék vagy a mátrix fehérjék alapján állapítja meg.
Az inaktivált vakcinák vonatkozásában olyan vizsgálatot fejlesztettek ki, amely kimutatja a nem strukturális vírusfehérjékkel szemben termelődött olyan ellenanyagokat, amelyek kizárólag a természetes fertőzés során keletkeznek. Ezt a rendszert a gyakorlatban még validálni kell, de korlátai ott jelentkeznek, hogy egy állománynak bármely influenzavírussal történő természetes fertőzése (függetlenül a vírus altípusától) a nem strukturális fehérjék ellen irányuló ellenanyagok termelését eredményezi.
A gyors, érzékeny és különösen az automatizálható víruskimutató módszerek (mint például a valós idejű RT-PCR) kifejlesztése azt jelentené, hogy ezeket a beoltott madarak egyszerű, széles körű és rendszeres vizsgálatára lehetne használni, a vadvírus kimutatása céljából. Az adott kórokozó kimutatása ugyanakkor egy rövid ablakperiódusra korlátozódik a fertőzés akut szakaszában, és segítségével nem állapítható meg, hogy az állomány ki volt-e téve a vírusnak egy régebbi időpontban. E megközelítés leginkább a beoltott madarak elszállítás előtti vizsgálatára alkalmas, annak megállapítása érdekében, hogy nem aktívan fertőzöttek-e.
A választott rendszerrel vizsgálandó minták számának a madárinfluenzavírus-fertőzés egy állományban történő előfordulásának több, mint 15 %-át kell 95 %-os megbízhatósági szinten kizárnia.
X. FEJEZET
A madárinfluenza diagnosztizálásának stratégiái
A 2005/94/EK irányelv IV. mellékletében leírtaknak megfelelően az arra irányuló döntések, hogy különleges területeken vagy kontaktgazdaságokban intézkedések meghozatalára kerüljön sor, illetve ezen intézkedések súlyossága, nagy mértékben függhet a kockázat mértékétől. Hasonlóképpen, a betegség diagnózisának kötelező megerősítését is az uralkodó helyzet, a veszély nagysága és a kockázat mértéke befolyásolja. Az állatorvosi hatóságoknak a diagnosztikai bizonyítékokra támaszkodva olyan döntéseket kell hozniuk, amelyek a rossz diagnózis lehetséges hatásával szemben a betegség gyors megfékezését és felszámolását eredményezik. E döntéseket számos, egy időben jelentkező tényező figyelembevételével kell meghozni, ugyanakkor néhány helyzet előre látható.
| Járványügyi helyzet | Lehetséges problémák | Diagnosztikai kritériumok |
| Nincsenek különleges tünetek, hivatalosan nem merül fel gyanú | Elszigetelt gazdaság | Gyors kimutatást kell végezni M génen alapuló RT-PCR vizsgálattal. Adott esetben differenciáldiagnózist kell végezni. |
| Elsődleges járványkitörés gyanúja | Elszigetelt gazdaság | Teljes diagnosztikai vizsgálatot, vírusizolálást és -jellemzést kell végezni. |
| Elsődleges járványkitörés gyanúja | Nagy baromfisűrűségű területen található gazdaság | Teljes diagnosztikai vizsgálatot, vírusizolálást és -jellemzést kell végezni; előnyben kell részesíteni a gyors kimutatást, valamint különösen az RT-PCR vizsgálatra és a szekvenciaazonosításra épülő jellemzési módszereket (1). |
| Másodlagos és azt követő járványkitörés gyanúja | Járványügyileg elsődleges járványkitörés-gyanús területhez kapcsolódó elszigetelt gazdaság | Előnyben kell részesíteni a gyors kimutatást, valamint különösen az RT-PCR vizsgálatra és a szekvenciaazonosításra épülő jellemzési módszereket (1). |
| Másodlagos és azt követő járványkitörés gyanúja | Nagy baromfisűrűségű vagy járványügyileg jelentősen érintett területen található gazdaság | A bármely madárinfluenza-vírus jelenlétét a legkorábban kimutató gyors detektálási módszerekhez kell folyamodni. |
| Több járványkitörés gyanúja vagy a betegség gyors terjedése, ideértve a megfigyelést | Gyors beavatkozás nélkül a terjedés szabályozhatatlanná válik | A bármely madárinfluenza-vírus jelenlétét a legkorábban kimutató gyors módszerekhez vagy a klinikai tünetek értékeléséhez kell folyamodni. |
XI. FEJEZET
Madárinfluenza-vírusok okozta fertőzés diagnosztizálása sertésekben és más emlősökben
1. Madárinfluenzával fertőzött sertések
A madárinfluenza-vírusok könnyen képesek megfertőzni a sertéseket és bár a vírus replikációja a legtöbb esetben viszonylag korlátozott, a fertőzött sertések átadhatják a betegséget a baromfinak és más, érzékeny állatoknak. Jelenlegi ismereteink szerint nincs konkrét bizonyíték arra nézve, hogy a fertőzött sertések átadják a H5 vagy H7 altípusú madárinfluenza-vírust.
A 2003-as hollandiai járvány során kiderült, hogy a H7N7 altípusú vírussal fertőzött sertések nem mutatnak a H7N7-fertőzésnek tulajdonítható klinikai tüneteket. Úgy tűnik továbbá, hogy az Ázsiában és máshol jelentkező H5N1-járvány során nem jelentettek be fertőzött sertést.
Ezért nem szabad a klinikai tünetekre hagyatkozni annak megállapításakor, hogy a sertések fertőzöttek-e, noha a sertésekben más madár-influenzavírusok okozta fertőzéskor - a vírusnak a gazdához való adaptációja után - klinikai jelek alakulhatnak ki. A sertések madárinfluenza-vírussal történő fertőzésének diagnózisa lényegében hasonló a madárfajok diagnózisához: a vírusizolálást, a molekuláris vizsgálatokat és a hemagglutináció-gátlási próbával történő specifikus ellenanyagok kimutatását foglalja magában. Léteznek azonban bizonyos különbségek és a sertéseknek a madárinfluenza-vírus okozta fertőzésének bizonyítására egyik vizsgálat sem teljes mértékben jóváhagyott.
2. Minták a vírusizoláláshoz
A sertések madárinfluenza-vírus okozta fertőzései rendszerint a légzőtraktusra korlátozódnak, így a mintákat a légzőtraktus szöveteiből kell venni. Adott esetben garat- vagy orr-tamponmintát kell venni, lehetőség szerint a betegség tüneteit mutató sertésekből. E minták és tamponok a fentebb már ismertetett, madarakból történő mintavételre vonatkozó technikákkal dolgozhatók fel, vírusizolálás és a vírus molekuláris vizsgálattal történő kimutatása céljából. A PCR-technikák alkalmazása során azonban megfelelő módon ellenőrizni kell, hogy az amplifikációt ne gátolják a sertésből vett mintákban található anyagok.
3. Tojások beoltása és inkubálása
Az emlősök influenzavírusainak izolálása 9-11 napos embrionált tyúktojásban rendszerint úgy történik, hogy valamennyi tojás esetében az allantoisüregen keresztül az amnionüregbe fecskendezünk. A madárinfluenza-vírusokkal érintkezett sertések vizsgálatakor azonban - amennyiben a vírusnak kevés lehetősége volt adaptálódni - valószínűleg az allantoisüreg befecskendezése elégséges lehet.
Hasonlóképpen, az A típusú emlős-influenzavírusok izolálásának javasolt inkubációs hőmérséklete rendszerint 35 °C, de a sertésekhez rosszul adaptálódott vírusok izolálásának a 37 °C-os hőmérséklet sem ártalmas.
4. Különleges ellenanyagok kimutatása a hemagglutinációs-gátlási próbákban
A sertések madárinfluenza-vírusos fertőzése kimutatásának legérzékenyebb módja a vírusizolálás vagy a molekuláris vizsgálattal történő kimutatás. Szerológiai válaszokat is kimutattak azonban a sertésekben anélkül, hogy vírust izoláltak vagy kimutattak volna. A sertésből származó szérumokat használó hemagglutinációs-gátlási próbákat a VIII. fejezetben meghatározott, madárból származó szérumokat felhasználó vizsgálathoz képest néhány módosítással kell elvégezni.
A sertésekből származó szérum a hemagglutinációs-gátlási próbákban mutatott nem specifikus gátlásáról ismert és ezért ezt megelőzendő, valamennyi szérummintát a receptormegsemmisítő enzimmel (RDE) kell kezelni. A következő módszert kell használni:
a) 100 μl sertésantiszérumhoz 400 μl receptormegsemmisítő enzimet (előzetes hígítás) kell adni és alaposan össze kell őket keverni.
b) Egy órán keresztül 37 °C-on kell inkubálni.
c) Ezután 30 perc 56 °C-on történő inkubáció következik.
d) A mintákat 4 °C-on 15 percig hűteni kell.
e) 10 μl 30 %-os csirkevörösvérsejtet (térfogat/térfogat koaguláló sejtek, v/v packed cells) kell hozzáadni és erőteljesen elkeverni.
f) Egész éjjel 4 °C-on kell inkubálni. Amennyiben a mintákat még aznap fel kívánjuk használni, alternatív megoldásként 37 °C-on inkubáljuk egy órán keresztül és öt percig tisztítsuk fel 300 x g-on.
A kezelt szérumot ezután a [...] bekezdésben meghatározott, a madárszérumokkal megegyező módszerrel használjuk a hemagglutinációs-gátlási próbához. Madárinfluenzával szemben elismerten szeronegatív státuszú sertésszérum-együttessel meg kell állapítani a felhasználandó vírustörzsre vonatkozó hemagglutinációs-gátlási próba specifikusságát (lásd a szerológiai vizsgálatra használt, járványból eredő vírustörzsek felhasználását; VIII. fejezet). A 2003-as hollandiai járvány során a járványtól függetlenül gyűjtött sertésszérumokat alkalmazó hemagglutinációs-gátlási próbában kimutatott nem specifikus reakciók aránya 2,6 %-ig terjedt.
5. Mintavétel sertésekből
A sertéseknél fennáll az a veszély, hogy a baromfival vagy baromfitermékekkel történő érintkezés útján közvetlenül vagy közvetetten madárinfluenza-vírussal fertőződnek meg, különösen az olyan gazdaságokban, amelyek sertést és baromfit egyaránt tartanak (azonos vagy különböző ólakban). E fertőzés kizárása érdekében garat- vagy orr-tamponmintát és vérmintát kell venni, a IV. fejezet 8.21. pontjában ismertetett eljárásokkal összhangban. Mintákat a betegség klinikai tüneteit mutató sertésekből kell venni. Klinikai tünetek hiányában azonban a minták a gazdaság bármely részén véletlenszerűen kiválasztott sertésekből vehetők. A tamponmintákat gyors molekuláris vizsgálat vagy vírusizolálás alá kell vetni, amennyiben erre lehetőség van a laboratóriumban. Az RT-PCR-t megfelelő módon validálni kell és érzékenységének legalább az A-típusú influenzavírusoknak tojásokban történő vírusizolálálásával megfelelőnek kell lennie.
2-4 nappal a madárinfluenzával fertőzött baromfi leölése után legalább 60 vérmintát kell a sertésekből venni olyan módon, hogy legalább néhány minta az egymással közvetlen érintkezésben lévő sertések csoportjából származzon. A mintákat a baromfijárványból származó vírust felhasználó hemagglutinációs-gátlási próbának kell alávetni. Az akut és a konvaleszcens fázisból vett mintákat egyaránt ugyanabban a próbában kell vizsgálni. A pozitív mintákat vítusneutralizációval és/vagy Western-Blot analízissel lehet megerősíteni.
Amennyiben a minták valamelyike pozitív, járványügyi vizsgálatot kell folytatni a védőkörzetben található valamennyi sertéstartó gazdaságban, függetlenül attól, hogy vegyes gazdaságokról van-e szó.
6. Madárinfluenza-vírusok a sertésektől eltérő emlősökben
Meg kell vizsgálni a sertésektől eltérő, a madárinfluenzára hajlamos emlősöket, ideértve a macskát. Különös tekintettel a H5N1 altípusú magas patogenitású madárinfluenza kimutatására, a macskák vizsgálatára a következők vonatkoznak:
Mivel nagy mértékű, vírusreplikációval kísért patológiai elváltozások figyelhetők meg a tüdőn és a májon, a virológiai vizsgálathoz szükséges mintákat lehetőleg az elpusztult állat ezen szerveiből kell venni. A vírus kimutatásához az élő állatból lehetőleg légcső-/garat- tamponmintát kell venni. Ezenkívül bélsárminta is vehető, amelyet elkülönítve kell kezelni.
A hemagglutinációs-próbákkal vizsgálandó vérmintákat 30 percig 56 °C-ra fel kell melegíteni; a receptormegsemmisítő enzimes kezelés elhagyható.
XII. FEJEZET
A minták szállítása során alkalmazandó biztonsági minimumkövetelmények
1. A patogén kórokozókat bizonyítottan vagy valószínűsíthetően tartalmazó minták szállítására szigorú nemzeti és nemzetközi szabályok vonatkoznak, amelyeket mindig be kell tartani. A vírusizolátumokat nem diagnosztikai mintákként sorolják be, azonban a nemzetközi szabványoknak megfelelően kell őket csomagolni.
Az e fejezetben meghatározott előírások a légi szállításra vonatkoznak, de hasonló csomagolási szabályok érvényesek a minták szárazföldi vagy tengeri szállítására.
2. Diagnosztikai minták szállítási célú csomagolása
Az IATA-rendeletekkel összhangban szállított diagnosztikai minták az esetnek megfelelően az UN 2814, 2900 vagy 3373 jelzés valamelyikét kapják.
A szállításért a feladó, nem pedig a szállítást végző vállalat felelős, amíg a csomag a címzetthez nem ér.
3. Elsődleges csomagolás
a) Az elsődleges edénynek/edényeknek vízállónak kell lennie/lenniük, a csavaros kupakot például szigetelőszalaggal vagy celluxszal le kell ragasztani, vagy hasonló védekező intézkedéseket kell tenni.
b) Az egyes elsődleges edényeket egyenként be kell csomagolni, hogy el ne törjenek.
c) A szállítandó diagnosztikai minták mennyiségének meghatározásakor figyelembe kell venni a vírusszállító közeget.
d) Az elsődleges edénynek/edényeknek legfeljebb 500 ml vagy 500 g anyagot szabad tartalmaznia/tartalmazniuk.
Az elsődleges edény teljes tartalma a diagnosztikai minta.
4. Másodlagos csomagolás
a) A másodlagos tartályba elegendő abszorbens anyagot kell tenni, hogy szivárgás vagy sérülés esetén fel tudja szívni az elsődleges edények teljes tartalmát.
b) A másodlagos csomagolásnak meg kell felelnie a diagnosztikai mintákra vonatkozó IATA-követelményeknek, amelyek tartalmazzák az 1,2 méterről (3,9 láb) történő ejtési próbát. Mivel a fertőző anyag csomagolása (602-es IATA Csomagolási Előírás) túlmutat a diagnosztikai minta csomagolására vonatkozó követelményeken, így ezen előírás alkalmazható.
c) A fertőző anyag csomagolásán fel kell tüntetni az előírt jelzéseket (az "UN" betűket be kell karikázni): például
"UN 4G/CLASS 6.2/99/GB/2450"
d) A másodlagos csomagolásnak vízállónak kell lennie. Be kell tartani a másodlagos csomagoláshoz mellékelt, a csomagolást gyártó vagy egyéb felhatalmazott fél csomagolási utasításait.
e) A másodlagos csomagolás legkisebb külső szélességének legalább 100 mm-nek (4 hüvelyk) kell lennie.
f) A másodlagos csomagolásnak elég nagynak kell lennie ahhoz, hogy tartalmazza a szállítási okmányokat (például a légi fuvarlevelet).
5. Külső csomagolás
a) A külső csomagolás nem tartalmazhat 4 l-nél vagy 4 kg-nál súlyosabb tárgyat.
b) Adott esetben a másodlagos csomagolást szárazjéggel vagy nedves jéggel körül lehet venni. Szárazjég használatakor a csomagolásnak a szén-dioxid-gáz távozását lehetővé kell tennie. A nyomásnak nem szabad felhalmozódnia benne, mert az a csomagolás szakadásához vezetne. Nedves jég használatakor a csomagolásnak szivárgásmentesnek kell lennie.
Valamennyi csomagolásnak és a légi fuvarlevélnek a következő szöveget szó szerint kell tartalmaznia:
"UN 3373 DIAGNOSTIC SPECIMEN
PACKED IN COMPLIANCE WITH
IATA PACKING INSTRUCTION 650"
c) A másodlagos és a külső csomagolás között részletes listát kell mellékelni a csomag tartalmáról.
d) A külső csomagolást lezárt műanyag zacskóba kell helyezni, ami megvédi a nedvességtől.
e) A feladónak nem kell "veszélyes áru" nyilatkozatot mellékelnie.
XIII. FEJEZET
Vírusok és minták közösségi referencialaboratóriumnak történő küldése
1. A közösségi referencialaboratóriumba küldendő mintáknak meg kell felelniük a veszélyes patogén anyagok Közösségen belüli szállítására vonatkozó ajánlásoknak, illetve az Egyesült Királyságban hatályban lévő előírásoknak és jogszabályoknak.
Követni kell az e fejezetben meghatározott előírásokat.
2. Vírusok és egyéb anyagok közösségi referencialaboratóriumnak történő küldése
a) Valamennyi anyagot az e fejezetben meghatározott előírásoknak megfelelően kell csomagolni.
b) A külső csomagolásra a következőket kell írni:
"ANIMAL PATHOGEN - PACKAGE ONLY TO BE OPENED AT THE AVIAN VIROLOGY SECTION, VLA, WEYBRIDGE. IMPORTATION AUTHORISED BY LICENCE NUMBER ...*...ISSUED UNDER THE IMPORTATION OF ANIMAL PATHOGENS ORDER."
c) A következő engedélyszámok egyikét kell beilleszteni:
| SZÖVEG HIÁNYZIK |
Mivel ezen engedélyszámok időnként változnak, a mintákat küldő laboratóriumoknak a csomagok feladása előtt meg kell bizonyosodniuk, hogy az éppen aktuális engedélyszámokat használják-e.
d) A csomagot a következő címre kell küldeni:
Avian Virology
VLA Weybridge,
New Haw, Addlestone,
Surrey KT15 3NB
United Kingdom
e) A csomagot levélnek kell kísérnie, amelyben a lehető legtöbb információt megadják az izolátumokról (pl. faj és kor, az izolálás területe/országa, klinikai múlt).
f) A csomagokat légi postával vagy légi áruszállítással kell szállítani.
A légi áruszállítással küldött csomagok esetében az anyagok érkezése előtt a légi fuvarlevél számát faxon, telefonon vagy e-mailben el kell küldeni a közösségi referencialaboratóriumnak.
A gyors repülőtéri kezelés érdekében a légi áruszállítással küldött csomagokra a következőt kell írni:
"CARE OF TRANSGLOBAL".
A közösségi referencialaboratórium kapcsolattartó személyei:
Ian H. Brown, a referencialaboratórium igazgatója
Közvetlen telefon: (44-1932) 35 73 39;
Közvetlen fax: (44-1932) 35 72 39;
E-mail: i.h.brown@vla.defra.gsi.gov.uk
Ruth Manvell, a referencialaboratórium ügyvezetője
Közvetlen telefon: (44-1932) 35 77 36 vagy (44-1932) 35 77 08
Közvetlen fax: (44-1932) 35 78 56
E-mail: r.manvell@vla.defra.gsi.gov.uk
XIV. FEJEZET
A madárinfluenza diagnosztizálását végző laboratóriumra vonatkozó biztonsági minimumkövetelmények
1. A madárinfluenza-vírusokkal dolgozó diagnosztikai laboratóriumok biztonsági követelményeinek az állategészségügyre veszélyt jelentő vírusok elszigetelésére és a laboratóriumban (és külső helyszínen) dolgozó személyeknek a járványveszélytől való védelmére egyaránt ki kell terjednie.
A Közösségben a laboratóriumokra vonatkozó biztonsági minimumkövetelményeket több irányelv határozza meg. A működésre vonatkozó szempontokat továbbá az alapul szolgáló Európai Normákban (EN) mutatták be és határozták meg. A diagnosztikai céllal felállított laboratóriumok működését további rendeletek (EN), illetve a bevált laboratóriumi gyakorlatok szabályozzák.
2. Laboratóriumokra vonatkozó közösségi irányelvek
A Tanács1989. június 12-i89/391/EGK irányelve a munkavállalók munkahelyi biztonságának és egészségvédelmének javítását ösztönző intézkedések bevezetéséről (HL L 183., 1989.6.29., 1. o.).
A Tanács1990. november 26-i90/679/EGK irányelve a munkájuk során biológiai anyagokkal kapcsolatos kockázatoknak kitett munkavállalók védelméről (hetedik önálló irányelv a 89/391/EGK irányelv 16. cikkének (1) bekezdése értelmében) (HL L 374., 1990.12.31., 1. o.).
E két irányelv mellett a következő irányelv és Európai Normák (EN) alkalmazandók, amennyiben polimeráz láncreakcióval (PCR) történő diagnózis felállítására és a PCR-termékek bakteriális plazmidba történő tenyésztése céljából klónozásra került sor.
A Tanács1990. április 23-i90/219/EGK irányelve a géntechnológiával módosított mikroorganizmusok zárt rendszerben történő felhasználásáról (HL L 117., 1990.5.8., 1. o.).
3. A közösségi irányelveken kívül figyelembe kell venni az Európai Normákat (EN):
EN 12128 Biotechnológia. Kutató-, fejlesztő- és elemzőlaboratóriumok. A mikrobiológiai laboratóriumok elszigetelési szintjei, veszélyterületek, helyszínek és fizikai biztonsági követelmények
EN 12738 Biotechnológia. Kutató-, fejlesztő- és elemzőlaboratóriumok. Útmutató a kísérletek során mikroorganizmusokkal beoltott állatok elszigeteléséhez.
EN 12740 Biotechnológia. Kutató-, fejlesztő- és elemzőlaboratóriumok. Útmutató a hulladék kezelésére, ártalmatlanítására és vizsgálatára.
EN 12741 Biotechnológia. Kutató-, fejlesztő- és elemzőlaboratóriumok. Útmutató a biotechnológiai laboratóriumi tevékenységekhez.
A laboratórium működésére/irányítására a következő feltételek alkalmazandók:
4. A laboratóriumokra vonatkozó követelmények (1-4-ig terjedő elszigetelési szint)
A munkájuk során biológiai anyagokkal kapcsolatos kockázatoknak kitett munkavállalók védelméről szóló (hetedik önálló irányelv a 89/391/EGK irányelv 16. cikkének (1) bekezdése értelmében), 2000. szeptember 18-i2000/54/EK európai parlamenti és tanácsi irányelvvel (HL L 262., 2000.10.17., 21. o.) összhangban a 90/219/EGK irányelv és az európai normák: EN 12128; EN 12740; EN 12741.
| Elszigetelési intézkedések | Elszigetelési szint | |||
| 1 | 2 | 3 | 4 | |
| A laboratórium elszigetelése | nem | igen | igen | igen |
| A laboratóriumokat ajtókkal választják el | nem | igen | igen | igen |
| A jelen lévők megfigyelését lehetővé tévő megfigyelőablak vagy hasonló berendezés | fakultatív | fakultatív | fakultatív | igen |
| Kézmosásra alkalmas berendezések a személyzet számára | igen | igen | igen | igen |
| A (kéz-) fertőtlenítésre alkalmas berendezések | fakultatív | igen | igen | igen |
| Korlátozott belépés | nem | igen | igen | igen |
| Az aeroszol ellenőrzését célzó különleges intézkedések | nem | Igen minimálisra csökkenti | Igen megelőzi | Igen megelőzi |
| Biológiai veszélyt jelző tábla az ajtón | nem | igen | igen | igen |
| Zuhany | nem | nem | fakultatív | igen |
| Szemöblítés | igen | igen | igen | igen |
| A gőzt hermetikusan elzáró laboratórium | nem | nem | igen | igen |
| Víznek, savnak, lúgnak, oldószernek, fertőtlenítőszernek, dekontamináló anyagnak ellenálló, könnyen tisztítható felületek | Igen (munkapad) | Igen (munkapad) | Igen (munkapad, padló) | Igen (munkapad, padló) |
| Zsilip (a laboratóriumba történő belépéshez) | nem | nem | fakultatív | igen |
| A közvetlen környezet nyomásához képest kisebb nyomás | nem | nem | fakultatív | igen |
| A laboratóriumba be-, valamint onnan kimenő levegő HEPA-szűrőn történő átengedése | nem | nem | igen (kimenő levegő) | igen |
| Autokláv | a helyszínen | az épületben | a laboratóriumban | laboratóriumban, kettős végű |
| Védőöltözet | Megfelelő védőöltözet | Megfelelő védőöltözet | Megfelelő védőöltözet (cipő fakultatív) | Teljes ruhaváltás |
| Kesztyűk | nem | fakultatív | igen | igen |
| A kórokozó-hordozók elleni hatékony védekezés (pl. rágcsálók, rovarok) | fakultatív | igen | igen | igen |
| A biológiai anyag biztonságos tárolása | igen | igen | igen | igen |
| A laboratóriumnak saját felszerelése van | nem | nem | ajánlott | igen |
A laboratóriumok működését/irányítását további Európai Normák tárgyalják.
Egyéb nemzeti és nemzetközi rendeleteket és ajánlásokat is követni kell. A WHO a következő weboldalon közzétette a Laboratóriumok biológiai biztonsága című kézikönyvének 3. kiadását:
http://www.who.int/csr/resources/publications/biosafety/WHO_CDS_CSR_LYO_2004_11/en/
5. Az állategészségügyre vonatkozó elszigetelés
A tagállamok állatorvosi hatóságainak létre kell hozniuk a madárinfluenza (különösen a magas patogenitású madárinfluenza, de ideértve valamennyi H5 és H7 altípusú madárinfluenza) vírusainak elszigetelésére vonatkozó szabályokat. Az Állat-egészségügyi Világszervezet (OIE) a Szárazföldi állatok 2005. évi egészségügyi kódexének 1.4.5 fejezete néhány útmutatóval szolgál ehhez; a magas patogenitású madárinfluenzát elszigetelés szempontjából az OIE a 4-es számú patogenitási csoportba sorolja.
A madárinfluenza-vírusok kezelésére vonatkozó szabályokat a tagállam állatorvosi hatóságai alakítják ki.
A közösségi referencialaboratórium által alkalmazott biztonsági minimumkövetelmények (amelyek egyben az Egyesült Királyság nemzeti szabályai is) a következő weboldalon találhatók:
http://www.defra.gov.uk/corporate/vla/science/science-viral-ai-reflab.htm
6. Az emberi egészségre vonatkozó elszigetelés
A madárinfluenza-vírusokkal dolgozó laboratóriumoknak folyamatosan figyelembe kell venniük azt a tényt, hogy e vírusok - legalábbis potenciálisan - veszélyesek az emberre; tevékenységeik során el kell kerülni, hogy a személyzet megfertőződjön, és hogy a vírus a laboratóriumon kívülre kerüljön.
Az Egészségügyi Világszervezet (WHO) weboldalán az A-típusú madárinfluenza-vírusokkal valószínűsíthetően fertőzött minták kezelésére vonatkozó útmutatók olvashatók:
http://www.who.int/csr/disease/avian_influenza/guidelines/handlingspecimens/en/
(1) Ennek érdekében teljes mintavételre van szükség, és a mintákat későbbi vizsgálat céljából meg kell őrizni.
Lábjegyzetek:
[1] A dokumentum eredetije megtekinthető CELEX: 32006D0437 - https://eur-lex.europa.eu/legal-content/HU/ALL/?uri=CELEX:32006D0437&locale=hu


