15/2016. (VII. 15.) EMMI rendelet
a törzskönyvezett gyógyszerek és a különleges táplálkozási igényt kielégítő tápszerek társadalombiztosítási támogatásba való befogadásának szempontjairól és a befogadás vagy a támogatás megváltoztatásáról szóló 32/2004. (IV. 26.) ESZCSM rendelet és a finanszírozási eljárásrendekről szóló 31/2010. (V. 13.) EüM rendelet módosításáról
A kötelező egészségbiztosítás ellátásairól szóló 1997. évi LXXXIII. törvény 83. § (3) bekezdés c) pontjában kapott felhatalmazás alapján, a Kormány tagjainak feladat- és hatásköréről szóló 152/2014. (VI. 6.) Korm. rendelet 48. § 2. pontjában meghatározott feladatkörömben eljárva - a Kormány tagjainak feladat- és hatásköréről szóló 152/2014. (VI. 6.) Korm. rendelet 90. § 2. pontjában meghatározott feladatkörében eljáró nemzetgazdasági miniszterrel egyetértésben -,
a 2. alcím és a 6-18. melléklet tekintetében a kötelező egészségbiztosítás ellátásairól szóló 1997. évi LXXXIII. törvény 83. § (6) bekezdés a) pontjában kapott felhatalmazás alapján, a Kormány tagjainak feladat- és hatásköréről szóló 152/2014. (VI. 6.) Korm. rendelet 48. § 2. pontjában meghatározott feladatkörömben eljárva
a következőket rendelem el:
1. A törzskönyvezett gyógyszerek és a különleges táplálkozási igényt kielégítő tápszerek társadalombiztosítási támogatásba való befogadásának szempontjairól és a befogadás vagy a támogatás megváltoztatásáról szóló 32/2004. (IV. 26.) ESZCSM rendelet módosítása
1. § A törzskönyvezett gyógyszerek és a különleges táplálkozási igényt kielégítő tápszerek társadalombiztosítási
támogatásba való befogadásának szempontjairól és a befogadás vagy a támogatás megváltoztatásáról szóló 32/2004. (IV. 26.) ESZCSM rendelet (a továbbiakban: 32/2004. ESZCSM rendelet) a következő 26. §-sal egészül ki:
"26. § (1) A 3. számú mellékletnek a törzskönyvezett gyógyszerek és a különleges táplálkozási igényt kielégítő tápszerek társadalombiztosítási támogatásba való befogadásának szempontjairól és a befogadás vagy a támogatás megváltoztatásáról szóló 32/2004. (IV. 26.) ESZCSM rendelet és a finanszírozási eljárásrendekről szóló 31/2010. (V. 13.) EüM rendelet módosításáról szóló 15/2016. (VII. 15.) EMMI rendelet (a továbbiakban: MódR.2.) 3. mellékletével hatályon kívül helyezett EÜ90 3/a1., EÜ90 3/a2., EÜ90 3/a3., EÜ90 3/b1., EÜ90 3/b2., EÜ90 3/b3. pontja alapján felírt vények 2016. október 31-éig válthatóak ki és számolhatóak el.
(2) A 3. számú mellékletnek a MódR.2. 3. mellékletével hatályon kívül helyezett EÜ90 3/a1., EÜ90 3/a2., EÜ90 3/a3. pontjára vonatkozó szakorvosi javaslatok érvényesek a 3. számú mellékletnek a MódR.2. 3. mellékletével megállapított EÜ90 3/a. pontjára.
(3) A 3. számú mellékletnek a MódR.2. 3. mellékletével hatályon kívül helyezett EÜ90 3/b1., EÜ90 3/b2., EÜ90 3/b3. pontjára vonatkozó szakorvosi javaslatok érvényesek a 3. számú mellékletnek a MódR.2. 3. mellékletével megállapított EÜ90 3/b. pontjára."
2. § (1) A 32/2004. ESZCSM rendelet 1. számú melléklete az 1. melléklet szerint módosul.
(2) A 32/2004. ESZCSM rendelet 2. számú melléklete a 2. melléklet szerint módosul.
(3) A 32/2004. ESZCSM rendelet 3. számú melléklete a 3. melléklet szerint módosul.
(4) A 32/2004. ESZCSM rendelet 4. számú melléklete a 4. melléklet szerint módosul.
(5) A 32/2004. ESZCSM rendelet 7/b. számú melléklete az 5. melléklet szerint módosul.
3. § Hatályát veszti a 32/2004. ESZCSM rendelet
a) 8. § (4) bekezdésében a "(+/-20%)",
b) 6/a., 6/b. és 7/b. számú mellékletében a "Beadás dátuma: (OEP tölti ki)" és
c) 7/a. számú mellékletében a "Beadás dátuma: (Országos Egészségbiztosítási Pénztár tölti ki)"
szövegrész.
2. A finanszírozási eljárásrendekről szóló 31/2010. (V. 13.) EüM rendelet módosítása
4. § (1) A finanszírozási eljárásrendekről szóló 31/2010. (V. 13.) EüM rendelet (a továbbiakban: 31/2010. EüM rendelet) 6. melléklete a 6. melléklet szerint módosul.
(2) A 31/2010. EüM rendelet 15. melléklete a 7. melléklet szerint módosul.
(3) A 31/2010. EüM rendelet 16. melléklete a 8. melléklet szerint módosul.
(4) A 31/2010. EüM rendelet 20. melléklete a 9. melléklet szerint módosul.
(5) A 31/2010. EüM rendelet 21. melléklete a 10. melléklet szerint módosul.
(6) A 31/2010. EüM rendelet 23. melléklete a 11. melléklet szerint módosul.
(7) A 31/2010. EüM rendelet 24. melléklete a 12. melléklet szerint módosul.
(8) A 31/2010. EüM rendelet 28. melléklete a 13. melléklet szerint módosul.
(9) A 31/2010. EüM rendelet 30. melléklete a 14. melléklet szerint módosul.
(10) A 31/2010. EüM rendelet 32. melléklete a 15. melléklet szerint módosul.
(11) A 31/2010. EüM rendelet 33. melléklete a 16. melléklet szerint módosul.
(12) A 31/2010. EüM rendelet 36. melléklete a 17. melléklet szerint módosul.
(13) A 31/2010. EüM rendelet 41. melléklete a 18. melléklet szerint módosul.
5. § Hatályát veszti a 31/2010. EüM rendelet 5. § (16) bekezdése és 34. melléklete.
3. Záró rendelkezések
6. § Ez a rendelet 2016. augusztus 1-jén lép hatályba.
Balog Zoltán s. k.,
emberi erőforrások minisztere
1. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
1. A 32/2004. ESZCSM rendelet 1. számú mellékletében foglalt táblázat J01CA megjelölésű sora helyébe a következő rendelkezés lép:
| (ATC | ATC MEGNEVEZÉS | TÁMOGATÁSI KATEGÓRIÁK | ||||||
| NORMATÍV | EMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KIEMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KÜLÖN- KERET) | |||||
| 0% | 25% | 55% | 80% | |||||
| ÉRTÉK NÉLKÜL | ÁTLA- GON ALULI | ÁTLA- GOS | ÁTLA- GON FELÜLI | |||||
| " | ||||||||
| J01CA | széles spektrumú penicillinek | X | X | X | ||||
| " | ||||||||
2. A 32/2004. ESZCSM rendelet 1. számú mellékletében foglalt táblázat J01CE megjelölésű sora helyébe a következő rendelkezés lép:
| (ATC | ATC MEGNEVEZÉS | TÁMOGATÁSI KATEGÓRIÁK | ||||||
| NORMATÍV | EMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KIEMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KÜLÖN- KERET) | |||||
| 0% | 25% | 55% | 80% | |||||
| ÉRTÉK NÉLKÜL | ÁTLA- GON ALULI | ÁTLA- GOS | ÁTLA- GON FELÜLI | |||||
| " | ||||||||
| J01CE | béta-laktamáz érzékeny penicillinek | X | X | X | ||||
| " | ||||||||
3. A 32/2004. ESZCSM rendelet 1. számú mellékletében foglalt táblázat J01CR megjelölésű sora helyébe a következő rendelkezés lép:
| (ATC | ATC MEGNEVEZÉS | TÁMOGATÁSI KATEGÓRIÁK | ||||||
| NORMATÍV | EMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KIEMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KÜLÖN- KERET) | |||||
| 0% | 25% | 55% | 80% | |||||
| ÉRTÉK NÉLKÜL | ÁTLA- GON ALULI | ÁTLA- GOS | ÁTLA- GON FELÜLI | |||||
| " | ||||||||
| J01CR | penicillinek kombinációi, beleértve a béta-laktamáz gátlókat | X | X | X | ||||
| " | ||||||||
4. A 32/2004. ESZCSM rendelet 1. számú mellékletében foglalt táblázat J01DC megjelölésű sora helyébe a következő rendelkezés lép:
| (ATC | ATC MEGNEVEZÉS | TÁMOGATÁSI KATEGÓRIÁK | ||||||
| NORMATÍV | EMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KIEMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KÜLÖN- KERET) | |||||
| 0% | 25% | 55% | 80% | |||||
| ÉRTÉK NÉLKÜL | ÁTLA- GON ALULI | ÁTLA- GOS | ÁTLA- GON FELÜLI | |||||
| " | ||||||||
| J01DC | második generációs cephalosporinok | X | X | X | ||||
| " | ||||||||
5. A 32/2004. ESZCSM rendelet 1. számú mellékletében foglalt táblázat J01DD megjelölésű sora helyébe a következő rendelkezés lép:
| (ATC | ATC MEGNEVEZÉS | TÁMOGATÁSI KATEGÓRIÁK | ||||||
| NORMATÍV | EMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KIEMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KÜLÖN- KERET) | |||||
| 0% | 25% | 55% | 80% | |||||
| ÉRTÉK NÉLKÜL | ÁTLA- GON ALULI | ÁTLA- GOS | ÁTLA- GON FELÜLI | |||||
| " | ||||||||
| J01DD | harmadik generációs cephalosporinok | X | X | X | ||||
| " | ||||||||
6. A 32/2004. ESZCSM rendelet 1. számú mellékletében foglalt táblázat J01EE megjelölésű sora helyébe a következő rendelkezés lép:
| (ATC | ATC MEGNEVEZÉS | TÁMOGATÁSI KATEGÓRIÁK | ||||||
| NORMATÍV | EMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KIEMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KÜLÖN- KERET) | |||||
| 0% | 25% | 55% | 80% | |||||
| ÉRTÉK NÉLKÜL | ÁTLA- GON ALULI | ÁTLA- GOS | ÁTLA- GON FELÜLI | |||||
| " | ||||||||
| J01EE | Szulfonamidok és trimethropim kombinációi | X | X | X | ||||
| " | ||||||||
7. A 32/2004. ESZCSM rendelet 1. számú mellékletében foglalt táblázat J01FA megjelölésű sora helyébe a következő rendelkezés lép:
| (ATC | ATC MEGNEVEZÉS | TÁMOGATÁSI KATEGÓRIÁK | ||||||
| NORMATÍV | EMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KIEMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KÜLÖN- KERET) | |||||
| 0% | 25% | 55% | 80% | |||||
| ÉRTÉK NÉLKÜL | ÁTLA- GON ALULI | ÁTLA- GOS | ÁTLA- GON FELÜLI | |||||
| " | ||||||||
| J01FA | makrolidok | X | X | X | X | |||
| " | ||||||||
8. A 32/2004. ESZCSM rendelet 1. számú mellékletében foglalt táblázat L04AC megjelölésű sora helyébe a következő rendelkezés lép:
| (ATC | ATC MEGNEVEZÉS | TÁMOGATÁSI KATEGÓRIÁK | ||||||
| NORMATÍV | EMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KIEMELT INDI- KÁCIÓ- HOZ KÖTÖTT | KÜLÖN- KERET) | |||||
| 0% | 25% | 55% | 80% | |||||
| ÉRTÉK NÉLKÜL | ÁTLA- GON ALULI | ÁTLA- GOS | ÁTLA- GON FELÜLI | |||||
| " | ||||||||
| L04AC | Interleukin-gátlók | X | X | |||||
| " | ||||||||
2. melléklet a 15/2016. (VII. 15.)EMMI rendelethez
1. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 8/l1. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
- Hólyagtumor alacsony és közepes kockázatú eseteiben az intravesicalis instilláció céljára a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján"
2. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 8/l2. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
- Hólyagtumor magas kockázatú eseteiben intravesicalis instilláció céljára és in situ carcinomában a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján"
3. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 10/a1. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
- Schizophrenia esetén a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján
- Schizotypiás és paranoid (delusiv) rendellenességek esetén"
4. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 10/a2. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
- Schizophrenia esetén a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján
- Schizotypiás és paranoid (delusiv) rendellenességek esetén"
5. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 28. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
Súlyos asthma bronchiale kiegészítő kezelése céljából - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrendek (felnőttkori asthma bronchiale és gyermekkori asthma bronchiale) alapján - a következő feltételek teljesülése esetén:
- IgE-szint > 76 NE/ml és az IgE-szint nem haladja meg az alkalmazási előírás szerinti maximális értéket,
- perenniális inhalatív allergénnel szembeni pozitív bőrpróba vagy specifikus IgE kimutatása a szérumban,
- szisztémás szteroid tartós (legfeljebb 4 hétig történő) alkalmazása ellenére az asthma nem kontrollált vagy nagy dózisú ICS+LABA alkalmazása ellenére gyakoriak a szisztémás szteroidot igénylő exacerbációk (≥ 4/év),
- FEV1 < ref. 80%-a.
Az anti-IgE-kezelés megkezdését követően évente értékelni kell a kezelés hatását és az anti-IgE-kezelés kizárólag akkor folytatható, ha az utolsó egy év során szisztémás szteroidot igénylő exacerbáció legfeljebb 2 alkalommal fordult elő."
6. A 32/2004. ESZCSM rendelet 2. számú melléklete a következő EÜ100 34. ponttal egészül ki:
"EÜ100 34.
TÁMOGATOTT INDIKÁCIÓK:
- Sclerosis multiplex esetén a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján
A JAVASLATOT KIÁLLÍTÓ ÉS A GYÓGYSZERT RENDELŐ ORVOS MUNKAHELYÉRE ÉS SZAKKÉPESÍTÉSÉRE VONATKOZÓ ELŐÍRÁSOK:
| MUNKAHELY: | SZAKKÉPESÍTÉS: | JOGOSULTSÁG: |
| Kijelölt intézmény | Neurológia | írhat |
ELFOGADHATÓ BNO KÓDOK: (beleértve az összes azonosan kezdődő kódot)
G35
Kijelölt intézmények:
| Város | Intézmény neve |
| Budapest | Egyesített Szent István és Szent László Kórház-Rendelőintézet |
| Budapest | Péterfy Sándor Utcai Kórház-Rendelőintézet és Baleseti Központ |
| Budapest | Semmelweis Egyetem Neurológiai Klinika |
| Budapest | Bajcsy-Zsilinszky Kórház és Rendelőintézet |
| Budapest | Szent Imre Kórház |
| Budapest | Szent János Kórház és Észak-budai Egyesített Kórházak |
| Budapest | Semmelweis Egyetem Kútvölgyi Neurológiai Klinikai Csoport |
| Budapest | Magyar Honvédség Egészségügyi Központ |
| Budapest | Uzsoki Utcai Kórház |
| Budapest | JahnFerenc Dél-Pesti Kórház és Rendelőintézet |
| Budapest | Országos Klinikai és Idegtudományi Intézet |
| Budapest | Országos Reumatológiai és Fizioterápiás Intézet |
| Debrecen | Debreceni Egyetem Klinikai Köpont, Neurológiai Klinika Neuroimmunológia |
| Debrecen | Kenézy Gyula Kórház és Rendelőintézet |
| Eger | Markhot Ferenc Kórház Kft. |
| Esztergom | Vaszary Kolos Kórház |
| Győr | Petz Aladár Megyei Oktató Kórház |
| Gyula | Békés Megyei Központi Kórház |
| Kaposvár | Somogy Megyei Kaposi Mór Oktató Kórház |
| Kecskemét | Bács-Kiskun Megyei Kórház a Szegedi Tudományegyetem Általános Orvostudományi Kar Oktató Kórháza |
| Kistarcsa | Pest Megyei Flór Ferenc Kórház |
| Miskolc | Borsod-Abaúj-Zemplén Megyei Kórház és Egyetemi Oktató Kórház |
| Nyíregyháza | Szabolcs-Szatmár-Bereg Megyei Kórházak és Egyetemi Oktatókórház |
| Pécs | Pécsi Tudományegyetem Klinikai Központ, Neurológiai Klinika |
| Salgótarján | Szent Lázár Megyei Kórház |
| Szeged | Szegedi Tudományegyetem Szent-Györgyi Albert Klinikai Központ, Neurológiai Klinika |
| Székesfehérvár | Fejér Megyei Szent György Egyetemi Oktató Kórház |
| Szekszárd | Tolna Megyei Balassa János Kórház |
| Szolnok | Jász-Nagykun-Szolnok Megyei Hetényi Géza Kórház-Rendelőintézet |
| Szombathely | Markusovszky Egyetemi Oktatókórház |
| Veszprém | Csolnoky Ferenc Kórház |
| Zalaegerszeg | Zala Megyei Kórház |
"
7. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 35. pontjában foglalt "Kijelölt intézmények:" táblázat helyébe a következő rendelkezés lép:
"Kijelölt intézmények:
| Város | Intézmény neve |
| Budapest | Heim Pál Gyermekkórház |
| Budapest | Szent János Kórház és Észak-budai Egyesített Kórházak |
| Budapest | Semmelweis Egyetem I. és II. sz. Gyermekgyógyászati Klinika |
| Budapest | Semmelweis Egyetem I. és II. sz. Belgyógyászati Klinika - Endokrinológia |
| Budapest | Magyar Honvédség Egészségügyi Központ |
| Debrecen | Debreceni Egyetem Klinikai Központ Gyermekklinika, I. sz. Belgyógyászati Klinika Endokrinológiai Tanszék |
| Eger | Markhot Ferenc Kórház Kft. |
| Győr | Petz Aladár Megyei Oktató Kórház |
| Hódmezővásárhely | Erzsébet Kórház-Rendelőintézet |
| Miskolc | Borsod-Abaúj-Zemplén Megyei Kórház és Egyetemi Oktató Kórház |
| Pécs | Pécsi Tudományegyetem Klinikai Központ Gyermekgyógyászati Klinika |
| Pécs | Pécsi Tudományegyetem Klinikai Központ I. sz. Belgyógyászati Klinika Endokrinológia |
| Salgótarján | Szent Lázár Megyei Kórház |
| Szeged | Szegedi Tudományegyetem Szent-Györgyi Albert Klinikai Központ Endokrinológia |
| Szeged | Szegedi Tudományegyetem Szent-Györgyi Albert Klinikai Központ Gyermekgyógyászati Klinika |
| Szolnok | Jász-Nagykun-Szolnok Megyei Hetényi Géza Kórház-Rendelőintézet |
| Szombathely | Markusovszky Egyetemi Oktatókórház |
| Veszprém | Csolnoky Ferenc Kórház |
"
8. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 36/b. pontjában foglalt "Kijelölt intézmények:" táblázat helyébe a következő rendelkezés lép:
"Kijelölt intézmények:
| Város | Intézmény neve |
| Budapest | Egyesített Szent István és Szent László Kórház-Rendelőintézet |
| Budapest | Magyar Honvédség Egészségügyi Központ, I. Belgyógyászati Osztály |
| Budapest | Semmelweis Egyetem I., II., III. sz. Belgyógyászati Klinika |
| Debrecen | Debreceni Egyetem Klinikai Központ II. sz. Belgyógyászati Klinika |
| Győr | Petz Aladár Megyei Oktató Kórház |
| Gyula | Békés Megyei Központi Kórház |
| Kaposvár | Somogy Megyei Kaposi Mór Oktató Kórház |
| Kecskemét | Bács-Kiskun Megyei Kórház a Szegedi Tudományegyetem Általános Orvostudományi Kar Oktató Kórháza |
| Miskolc | Miskolci Semmelweis Kórház és Egyetemi Oktatókórház |
| Mosonmagyaróvár | Karolina Kórház |
| Nyíregyháza | Szabolcs-Szatmár-Bereg Megyei Kórházak és Egyetemi Oktatókórház |
| Pécs | Pécsi Tudományegyetem Klinikai Központ I. sz. Belgyógyászati Klinika |
| Sopron | Országos Vérellátó Szolgálat |
| Szeged | Szegedi Tudományegyetem Szent-Györgyi Albert Klinikai Központ II. sz. Belgyógyászati Klinika |
| Szekszárd | Tolna Megyei Balassa János Kórház |
| Szombathely | Markusovszky Egyetemi Oktatókórház |
| Tatabánya | Szent Borbála Kórház, Belgyógyászat Onko-Hematológia részlege |
| Veszprém | Csolnoky Ferenc Kórház |
"
9. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 37/b. pontjában foglalt "Kijelölt intézmények:" táblázat helyébe a következő rendelkezés lép:
"Kijelölt intézmények:
| Város | Intézmény neve |
| Budapest | Bajcsy-Zsilinszky Kórház és Rendelőintézet |
| Budapest | Országos Onkológiai Intézet |
| Budapest | Egyesített Szent István és Szent László Kórház-Rendelőintézet |
| Budapest | Semmelweis Egyetem I. sz. Belgyógyászati Klinika, Urológiai Klinika |
| Budapest | Szent Margit Kórház |
| Budapest | Magyar Honvédség Egészségügyi Központ |
| Budapest | Uzsoki Utcai Kórház |
| Debrecen | Debreceni Egyetem Klinikai Központ, Onkológiai Tanszék |
| Gyula | Békés Megyei Központi Kórház |
| Kaposvár | Somogy Megyei Kaposi Mór Oktató Kórház |
| Kecskemét | Bács-Kiskun Megyei Kórház a Szegedi Tudományegyetem Általános Orvostudományi Kar Oktató Kórháza |
| Miskolc | Borsod-Abaúj-Zemplén Megyei Kórház és Egyetemi Oktató Kórház |
| Pécs | Pécsi Tudományegyetem Klinikai Központ, Onkoterápiás Klinika |
| Szeged | Szegedi Tudományegyetem Szent-Györgyi Albert Klinikai Központ, Onkoterápiás Klinika |
| Szombathely | Markusovszky Egyetemi Oktatókórház |
| Veszprém | Csolnoky Ferenc Kórház |
| Zalaegerszeg | Zala Megyei Kórház |
"
10. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 37/c. pontjában foglalt "Kijelölt intézmények:" táblázat helyébe a következő rendelkezés lép:
"Kijelölt intézmények:
| Város | Intézmény neve |
| Budapest | Bajcsy-Zsilinszky Kórház és Rendelőintézet |
| Budapest | Országos Onkológiai Intézet |
| Budapest | Egyesített Szent István és Szent László Kórház-Rendelőintézet |
| Budapest | Semmelweis Egyetem I. sz. Belgyógyászati Klinika, Urológiai Klinika |
| Budapest | Szent Margit Kórház |
| Budapest | Magyar Honvédség Egészségügyi Központ |
| Budapest | Uzsoki Utcai Kórház |
| Debrecen | Debreceni Egyetem Klinikai Központ, Onkológiai Tanszék |
| Gyula | Békés Megyei Központi Kórház |
| Kaposvár | Somogy Megyei Kaposi Mór Oktató Kórház |
| Kecskemét | Bács-Kiskun Megyei Kórház a Szegedi Tudományegyetem Általános Orvostudományi Kar Oktató Kórháza |
| Miskolc | Borsod-Abaúj-Zemplén Megyei Kórház és Egyetemi Oktató Kórház |
| Pécs | Pécsi Tudományegyetem Klinikai Központ, Onkoterápiás Klinika |
| Szeged | Szegedi Tudományegyetem Szent-Györgyi Albert Klinikai Központ, Onkoterápiás Klinika |
| Szombathely | Markusovszky Egyetemi Oktatókórház |
| Veszprém | Csolnoky Ferenc Kórház |
| Zalaegerszeg | Zala Megyei Kórház |
"
11. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 38/b. pontjában foglalt "Kijelölt intézmények:" táblázat helyébe a következő rendelkezés lép:
"Kijelölt intézmények:
| Város | Intézmény neve |
| Budapest | Egyesített Szent István és Szent László Kórház-Rendelőintézet |
| Budapest | Magyar Honvédség Egészségügyi Központ, I. Belgyógyászati Osztály |
| Budapest | Semmelweis Egyetem I. sz. Belgyógyászati Klinika |
| Budapest | Semmelweis Egyetem II. sz. Belgyógyászati Klinika |
| Budapest | Semmelweis Egyetem III. sz. Belgyógyászati Klinika |
| Budapest | Semmelweis Egyetem I. sz. Gyermekgyógyászati Klinika |
| Budapest | Semmelweis Egyetem II. sz. Gyermekgyógyászati Klinika |
| Debrecen | Debreceni Egyetem Klinikai Központ, II. Belgyógyászati Klinika |
| Debrecen | Debreceni Egyetem Klinikai Központ, Gyermekklinika |
| Gyula | Békés Megyei Központi Kórház |
| Kaposvár | Somogy Megyei Kaposi Mór Oktató Kórház |
| Kecskemét | Bács-Kiskun Megyei Kórház a Szegedi Tudományegyetem Általános Orvostudományi Kar Oktató Kórháza |
| Miskolc | Miskolci Semmelweis Kórház és Egyetemi Oktatókórház |
| Mosonmagyaróvár | Karolina Kórház |
| Nyíregyháza | Szabolcs-Szatmár-Bereg Megyei Kórházak és Egyetemi Oktatókórház |
| Pécs | Pécsi Tudományegyetem Klinikai Központ, Gyermekgyógyászati Klinika |
| Pécs | Pécsi Tudományegyetem Klinikai Központ I. sz. Belgyógyászati Klinika |
| Sopron | Országos Vérellátó Szolgálat |
| Szeged | Szegedi Tudományegyetem Szent-Györgyi Albert Klinikai Központ, Belgyógyászati Klinika Haematológiai Osztály |
| Szeged | Szegedi Tudományegyetem Szent-Györgyi Albert Klinikai Központ, Gyermekgyógyászati Klinika |
| Szekszárd | Tolna Megyei Balassa János Kórház |
| Szombathely | Markusovszky Egyetemi Oktatókórház, Haematológiai és Haemostaseológiai Osztály |
| Tatabánya | Szent Borbála Kórház, Belgyógyászat Onko-Hematológia részlege |
| Veszprém | Csolnoky Ferenc Kórház |
"
12. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 56. pontjában foglalt "Kijelölt intézmények:" táblázat helyébe a következő rendelkezés lép:
"Kijelölt intézmények:
| Város | Intézmény neve |
| Budapest | Magyar Honvédség Egészségügyi Központ, I. Belgyógyászati Osztály |
| Budapest | Egyesített Szent István és Szent László Kórház-Rendelőintézet Haematológiai és Csontvelőtranszplantációs Osztály, I. Belgyógyászat |
| Budapest | Semmelweis Egyetem I. sz. Belgyógyászati Klinika |
| Budapest | Semmelweis Egyetem II. sz. Belgyógyászati Klinika |
| Budapest | Semmelweis Egyetem III. sz. Belgyógyászati Klinika |
| Debrecen | Debreceni Egyetem Klinikai Központ Belgyógyászati Intézet |
| Győr | Petz Aladár Megyei Oktató Kórház II. sz. Belgyógyászat-Haematológiai Osztály |
| Gyula | Békés Megyei Központi Kórház |
| Kaposvár | Somogy Megyei Kaposi Mór Oktató Kórház |
| Kecskemét | Bács-Kiskun Megyei Kórház a Szegedi Tudományegyetem Általános Orvostudományi Kar Oktató Kórháza |
| Miskolc | Miskolci Semmelweis Kórház és Egyetemi Oktatókórház |
| Nyíregyháza | Szabolcs-Szatmár-Bereg Megyei Kórházak és Egyetemi Oktatókórház |
| Pécs | Pécsi Tudományegyetem Klinikai Központ I. sz. Belgyógyászati Klinika |
| Sopron | Országos Vérellátó Szolgálat |
| Szeged | Szegedi Tudományegyetem Szent-Györgyi Albert Klinikai Központ II. sz. Belgyógyászati Klinika |
| Szekszárd | Tolna Megyei Balassa János Kórház |
| Szombathely | Markusovszky Egyetemi Oktatókórház |
| Tatabánya | Szent Borbála Kórház, Belgyógyászat Onko-Haematológiai részlege |
| Veszprém | Csolnoky Ferenc Kórház |
"
13. A 32/2004. ESZCSM rendelet 2. számú melléklete a következő EÜ100 60. ponttal egészül ki:
"EÜ100 60.
TÁMOGATOTT INDIKÁCIÓK:
Teljes vagy részleges hasnyálmirigy-eltávolítás esetén
A JAVASLATOT KIÁLLÍTÓ ÉS A GYÓGYSZERT RENDELŐ ORVOS MUNKAHELYÉRE ÉS SZAKKÉPESÍTÉSÉRE VONATKOZÓ ELŐÍRÁSOK:
| MUNKAHELY: | SZAKKÉPESÍTÉS: | JOGOSULTSÁG: |
| Járóbeteg szakrendelés / | Gastroenterológia | javasolhat és írhat |
| Fekvőbeteg gyógyintézet | ||
| Járóbeteg szakrendelés / | Klinikai onkológia | javasolhat és írhat |
| Fekvőbeteg gyógyintézet | ||
| Járóbeteg szakrendelés / | Sebészet | javasolhat és írhat |
| Fekvőbeteg gyógyintézet | ||
| Járóbeteg szakrendelés / | Sugártherápia | javasolhat és írhat |
| Fekvőbeteg gyógyintézet | ||
| Háziorvos | Megkötés nélkül | javaslatra írhat |
| SZAKORVOSI JAVASLAT ÉRVÉNYESSÉGI IDEJE: 12 hónap | ||
ELFOGADHATÓ BNO KÓDOK: (beleértve az összes azonosan kezdődő kódot)
C 25"
14. A 32/2004. ESZCSM rendelet 2. számú melléklet
a) EÜ100 7/a., EÜ100 7/b., EÜ100 8/t., EÜ100 9/b., EÜ100 23/a., EÜ100 24., EÜ100 30/a., EÜ100 31/a., EÜ100 31/b., EÜ100 31/c., EÜ100 31/d., EÜ100 36/a., EÜ100 36/c., EÜ100 37/a., EÜ100 39/a., EÜ100 39/b., EÜ100 41., EÜ100 42., EÜ100 43., EÜ100 51., EÜ100 52. és EÜ100 59. pontjában a "Debreceni Egyetem Orvos- és Egészségtudományi Centrum" szövegrész helyébe a "Debreceni Egyetem Klinikai Központ" szöveg,
b) EÜ100 28. pontjában a "Debreceni Egyetem Orvos- és Egészségtudományi Centrum" szövegrészek helyébe a "Debreceni Egyetem Klinikai Központ" szöveg
lép.
15. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 8/t., EÜ100 23/a., EÜ100 36/a., EÜ100 37/a. és EÜ100 51. pontjában a "Békés Megyei Pándy Kálmán Kórház" szövegrész helyébe a "Békés Megyei Központi Kórház" szöveg lép.
16. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 23/a. és EÜ100 36/a. pontjában a "Réthy Pál Kórház-Rendelőintézet" szövegrész helyébe a "Békés Megyei Központi Kórház" szöveg lép.
17. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 42. pontjában a "Réthy Pál Kórház" szövegrész helyébe a "Békés Megyei Központi Kórház" szöveg lép.
18. A 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 23/a., EÜ100 29., EÜ100 36/a., EÜ100 36/b., EÜ100 37/b. és EÜ100 37/c. pontjában a "protokoll" szövegrész helyébe az "eljárásrend" szöveg lép.
19. Hatályát veszti a 32/2004. ESZCSM rendelet 2. számú melléklet EÜ100 10/a3., EÜ100 10/a4., EÜ100 10/a5., EÜ100 34/a., EÜ100 34/b., EÜ100 53/a. és EÜ100 53/b. pontja.
3. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
1. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ50 9/a1. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
Az asthma bronchiale ICS+LABA kombinációjával nem kontrollált formájában a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján"
2. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ50 10. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
- Coronariascleroticus stabil angina pectoris, komplex antianginás kezelés mellett ismétlődő anginiform panaszok fennállása esetén a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján"
3. A 32/2004. ESZCSM rendelet 3. számú melléklete a következő EÜ50 11. ponttal egészül ki:
"EÜ50 11.
TÁMOGATOTT INDIKÁCIÓK:
Az 5 év alatti gyermekek antibiotikummal történő kezelésére
A JAVASLATOT KIÁLLÍTÓ ÉS A GYÓGYSZERT RENDELŐ ORVOS MUNKAHELYÉRE ÉS SZAKKÉPESÍTÉSÉRE VONATKOZÓ ELŐÍRÁSOK:
| MUNKAHELY: | SZAKKÉPESÍTÉS: | JOGOSULTSÁG: |
| Járóbeteg szakrendelés / | Csecsemő- és gyermekgyógyászat | írhat |
| Fekvőbeteg gyógyintézet | ||
| Háziorvos | Megkötés nélkül | írhat |
ELFOGADHATÓ BNO KÓDOK: (beleértve az összes azonosan kezdődő kódot)
Y40-Y41"
4. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 2/a1. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
- Lezajlott tranziens ischemias attack (TIA), illetve stroke után halmozott atherothrombotikus rizikó esetén secunder stroke prevenció céljából a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján"
5. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 2/a3. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
- Akut koronária szindróma (instabil angina, NSTEMI, STEMI) perkután endovasculáris intervencióját követően egy évig ASA-val kombinálva
- ST-eleváció nélküli akut coronaria szindrómában (instabil angina vagy NSTEMI/non-Q myocardialis infarctus) egy évig ASA-val kombinálva
- STEMI-ben thrombolitikus kezelést követően ASA-val kombinálva maximum négy hétig
- Ischaemiás eredetű cerebrovascularis betegségek, instabil angina, non-QMI, NSTEMI, AMI, perifériás artériás obstrukció angiográfiával, vagy egyéb képalkotó vizsgálattal igazolt eseteiben, szekunder prevenció céljára, dokumentált ASA-allergia, ASA rezisztencia, műszeresen igazolt ASA-non-responsió, valamint ASA adása mellett kialakult endoscoppal, vagy Weber-vizsgálattal igazolt gastrointestinalis vérzés, ASA-indukálta asthmaroham esetén a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján"
6. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 9/a1. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
Kalcium- és D-vitaminbevitel kiegészítő pótlására, ha a dokumentáltan gondozott posztmenopauzás nő vagy 55 év feletti férfi beteg oszteoporózisa igazolódott (BMD érték -2,5 SD T-score alatti), vagy a fokozott töréskockázati tényezőkből legalább három egyidejűleg bizonyítottan fennáll, vagy a FRAX alapján számított 10 éves törési kockázata magas (általános > 20%, illetve csípő > 3%), vagy típusos oszteoporotikus törést szenvedett el - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján. A szükséges kalcium- és D-vitaminbevitel (amennyiben nem kontraindikált), továbbá a megfelelő életvitel kialakítása az oszteoporózis terápiájának folyamatos követelménye."
7. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 9/a2. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
Orális biszfoszfonát oszteoporotikus csonttörések primer prevenciója céljából, azoknak az igazolt oszteoporózissal élő (BMD érték -2,5 SD T-score alatti), de oszteoporotikus csonttörést nem szenvedett posztmenopauzás nő vagy 55 év feletti férfi betegeknek, akiknek a FRAX alapján számított 10 éves törési kockázata magas (általános > 20%, illetve csípő > 3%) - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján. A terápiát megfelelő kalcium- és D-vitaminbevitel (amennyiben nem kontraindikált) biztosításával, továbbá a megfelelő életvezetésre is kiterjedő gondozás mellett kell folytatni."
8. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 9/a3. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
Parenterális biszfoszfonát oszteoporotikus csonttörések primer prevenciója céljából, azoknak az igazolt oszteoporózissal élő (BMD érték -2,5 SD T-score alatti), de oszteoporotikus csonttörést nem szenvedett posztmenopauzás nő vagy 55 év feletti férfi betegeknek, akiknek a FRAX alapján számított 10 éves törési kockázata magas (általános > 20%, illetve csípő > 3%), de az EÜ70 9a/2. pontban meghatározott kezelés ellenjavallt, vagy dokumentált intolerancia vagy a kezelést hátrányosan befolyásoló egyéb tényező miatt nem folytatható - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján. A terápiát megfelelő kalcium- és D-vitaminbevitel (amennyiben nem kontraindikált) biztosításával, továbbá a megfelelő életvezetésre is kiterjedő gondozás mellett kell folytatni."
9. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 9/a4. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
Az oszteoporotikus csonttörés primer prevenciójának alternatív lehetőségeként alkalmazható, azoknál a posztmenopauzás nő vagy 55 év feletti férfi betegeknél, akiknek az oszteoporózisa igazolt (BMD értéke -2,5 SD T-score alatti), és a FRAX alapján számított 10 éves törési kockázata magas (általános > 20%, illetve csípő > 3%), amennyiben az EÜ70 9a/2. vagy az EÜ70 9a/3. pontjában meghatározott kezelés ellenjavallt, vagy azzal szemben dokumentált intolerancia lép fel, vagy a készítmény legalább 12 hónapon át történő alkalmazása nem volt eredményes (a BMD értéke a kiindulási értékhez képest legkevesebb 5%-kal csökkent, illetve oszteoporotikus csonttörés történt), a megfelelő gyógyszeres kalcium- és D-vitaminbevitel (amennyiben nem kontraindikált) biztosításával együtt - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján."
10. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 9/b1. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
Orális biszfoszfonát oszteoporotikus csonttörések szekunder prevenciója céljából, annak a posztmenopauzás nő vagy 55 év feletti férfi betegnek, aki típusos oszteoporotikus törést szenvedett el, és a FRAX alapján számított 10 éves törési kockázata magas (általános > 20%, csípő > 3%) vagy az oszteoporózisa csontsűrűség vizsgálattal igazolt (BMD érték -2,5 SD T-score alatti) - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján. A terápiát megfelelő kalcium- és D-vitaminbevitel (amennyiben nem kontraindikált) biztosításával, továbbá a megfelelő életvezetésre is kiterjedő gondozás mellett kell folytatni."
11. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 9/b2. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
Parenterális biszfoszfonát oszteoporotikus csonttörések szekunder prevenciója céljából, annak a posztmenopauzás nő vagy 55 év feletti férfi betegnek, aki típusos oszteoporotikus törést szenvedett el, és a FRAX alapján számított 10 éves törési kockázata magas (általános > 20%, csípő > 3%), vagy az oszteoporózisa csontsűrűség vizsgálattal igazolt (BMD érték -2,5 SD T-score alatti), de az EÜ70 9b/1. pontban meghatározott kezelés ellenjavallt, vagy dokumentált intolerancia vagy a kezelést hátrányosan befolyásoló egyéb tényező miatt nem folytatható - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján. A terápiát megfelelő kalcium- és D-vitaminbevitel (amennyiben nem kontraindikált) biztosításával, továbbá a megfelelő életvezetésre is kiterjedő gondozás mellett kell folytatni."
12. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 9/b3. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
Az oszteoporotikus csonttörés szekunder prevenciójának alternatív lehetőségeként alkalmazható annál a posztmenopauzás nő vagy 55 év feletti férfi betegnél, aki típusos oszteoporotikus törést szenvedett el, és a FRAX alapján számított 10 éves törési kockázata magas (általános > 20%, csípő > 3%), vagy az oszteoporózisa csontsűrűség vizsgálattal igazolt (BMD érték -2,5 SD T-score alatti), amennyiben az EÜ70 9b/1. vagy az EÜ70 9b/2. pontban meghatározott kezelés ellenjavallt, vagy azzal szemben dokumentált intolerancia lép fel, vagy a készítmény legalább 12 hónapon át történő alkalmazása nem volt eredményes (a BMD értéke a kiindulási értékhez képest legkevesebb 5%-kal csökkent, illetve újabb oszteoprotikus törés történt), a megfelelő gyógyszeres kalcium- és D-vitaminbevitel (amennyiben nem kontraindikált) biztosításával együtt - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján."
13. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 26. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
Stroke és szisztémás embolizáció megelőzésére nem billentyű eredetű pitvarfibrillációban szenvedő felnőtt betegeknél,
- K-vitamin antagonista (acenocumarol és/vagy warfarin) alkalmazásának ellenjavallata esetén, vagy
- K-vitamin antagonista kezelés ellenére elszenvedett stroke vagy szisztémás embolizáció esetén, vagy amennyiben 6 hónapot meghaladó K-vitamin antagonista kezelés során a mért INR értékek kevesebb mint 60%-a esik terápiás tartományba (INR 2 és 3 közé), a következő kockázati tényezők közül legalább kettő fennállása esetén:
- bal kamrai ejekciós frakció < 40%,
- tünetekkel járó szívelégtelenség New York Heart Association (NYHA) II. stádium,
- életkor >= 75 év,
- életkor >= 65 év, a következők valamelyikével: diabetes mellitus, koszorúér-betegség vagy hypertonia."
14. A 32/2004. ESZCSM rendelet 3. számú melléklete az EÜ90 2/b. pontot követően a következő EÜ90 3/a. ponttal egészül ki:
"EÜ90 3/a.
TÁMOGATOTT INDIKÁCIÓK:
- Asthma bronchiale kezelésére a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrendek alapján.
A JAVASLATOT KIÁLLÍTÓ ÉS A GYÓGYSZERT RENDELŐ ORVOS MUNKAHELYÉRE ÉS SZAKKÉPESÍTÉSÉRE VONATKOZÓ ELŐÍRÁSOK:
| MUNKAHELY: | SZAKKÉPESÍTÉS: | JOGOSULTSÁG: |
| Járóbeteg szakrendelés / | Allergológia és klinikai immunológia | javasolhat és írhat |
| Fekvőbeteg gyógyintézet | ||
| Járóbeteg szakrendelés / | Csecsemő-gyermekgyógyászat | javasolhat és írhat |
| Fekvőbeteg gyógyintézet | ||
| Járóbeteg szakrendelés / | Gyermektüdőgyógyászat | javasolhat és írhat |
| Fekvőbeteg gyógyintézet | ||
| Járóbeteg szakrendelés / | Tüdőgyógyászat | javasolhat és írhat |
| Fekvőbeteg gyógyintézet | ||
| Háziorvos | Megkötés nélkül | javaslatra írhat |
| Megkötés nélkül | Allergológia és klinikai immunológia | írhat |
| Megkötés nélkül | Csecsemő-gyermekgyógyászat | írhat |
| Megkötés nélkül | Gyermektüdőgyógyászat | írhat |
| Megkötés nélkül | Tüdőgyógyászat | írhat |
| SZAKORVOSI JAVASLAT ÉRVÉNYESSÉGI IDEJE: 12 hónap | ||
ELFOGADHATÓ BNO KÓDOK: (beleértve az összes azonosan kezdődő kódot)
J45"
15. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ90 3/a4. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
- Gyermekkori asthma bronchiale kezelésére (14 éves korig, az életkorra vonatkozó rendelési előírások szigorú figyelembevételével) a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján"
16. A 32/2004. ESZCSM rendelet 3. számú melléklete a következő EÜ90 3/b. ponttal egészül ki:
"EÜ90 3/b.
TÁMOGATOTT INDIKÁCIÓK:
- Krónikus obstruktív tüdőbetegség (COPD) esetén a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján
A JAVASLATOT KIÁLLÍTÓ ÉS A GYÓGYSZERT RENDELŐ ORVOS MUNKAHELYÉRE ÉS SZAKKÉPESÍTÉSÉRE VONATKOZÓ ELŐÍRÁSOK:
| MUNKAHELY: | SZAKKÉPESÍTÉS: | JOGOSULTSÁG: |
| Járóbeteg szakrendelés / | Gyermektüdőgyógyászat | javasolhat és írhat |
| Fekvőbeteg gyógyintézet | ||
| Járóbeteg szakrendelés / | Tüdőgyógyászat | javasolhat és írhat |
| Fekvőbeteg gyógyintézet | ||
| Háziorvos | Megkötés nélkül | javaslatra írhat |
| Megkötés nélkül | Gyermektüdőgyógyászat | írhat |
| Megkötés nélkül | Tüdőgyógyászat | írhat |
| SZAKORVOSI JAVASLAT ÉRVÉNYESSÉGI IDEJE: 12 hónap | ||
ELFOGADHATÓ BNO KÓDOK: (beleértve az összes azonosan kezdődő kódot)
J44"
17. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ90 14/a. pont "ELFOGADHATÓ BNO KÓDOK:" része helyébe a következő rendelkezés lép:
"ELFOGADHATÓ BNO KÓDOK: (beleértve az összes azonosan kezdődő kódot)
H441, L209, L4050, L409, M059, M0690, M0800, M352"
18. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ90 29. pont "TÁMOGATOTT INDIKÁCIÓK:" része helyébe a következő rendelkezés lép:
"TÁMOGATOTT INDIKÁCIÓK:
- Oszteoporotikus törések szekunder prevenciójára választható annál a posztmenopauzás nő vagy 55 év feletti férfi betegnél, aki típusos oszteoporotikus törést szenvedett el, és a törzscsontok ásványianyag tartalmának fotonabszorpciós meghatározással igazolt BMD értéke -4,0 SD T-score alatti, a megfelelő gyógyszeres kalcium- és D-vitaminbevitel (amennyiben nem kontraindikált) biztosításával együtt - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján. A beteg legfeljebb 18 havi kezelést, legfeljebb 24 hónap alatt vehet igénybe. A kezelés nem ismételhető.
- Oszteoporotikus törések szekunder prevenciójára választható annál a posztmenopauzás nő vagy 55 év feletti férfi betegnél, aki egynél több típusos oszteoporotikus törési eseményt szenvedett el, és a törzscsontok ásványianyag tartalmának fotonabszorpciós meghatározással igazolt BMD értéke -3,0 SD T-score alatti, a megfelelő gyógyszeres kalcium- és D-vitaminbevitel (amennyiben nem kontraindikált) biztosításával együtt - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján. A beteg legfeljebb 18 havi kezelést, legfeljebb 24 hónap alatt vehet igénybe. A kezelés nem ismételhető.
- Az oszteoporotikus csonttörés szekunder prevenciójában kezelési alternatívaként alkalmazható annál a posztmenopauzás nő vagy 55 év feletti férfi betegnél, aki típusos oszteoporotikus törést szenvedett el, és a törzscsontok ásványianyag tartalmának fotonabszorpciós meghatározással igazolt BMD értéke -3,0 SD T-score alatti, amennyiben az EÜ70 9b/1., az EÜ70 9b/2. és az EÜ70 9b/3. pontban meghatározott készítményekkel megelőző, legalább 12 hónapon át tartó kezelés hatástalan (a BMD értéke a kiindulási értékhez képest legkevesebb 5%-kal csökkent, illetve újabb oszteoprotikus törés történt), vagy azzal szemben intolerancia lép fel, vagy a kezelés ellenjavallt, a megfelelő gyógyszeres kalcium- és D-vitaminbevitel (amennyiben nem kontraindikált) biztosításával együtt - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott finanszírozási eljárásrend alapján. A beteg legfeljebb 18 havi kezelést, legfeljebb 24 hónap alatt vehet igénybe. A kezelés nem ismételhető."
19. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 18. pontjában a "Debreceni Egyetem Orvos- és Egészségtudományi Centrum" szövegrész helyébe a "Debreceni Egyetem Klinikai Központ" szöveg lép.
20. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 24. pontjában a "Debreceni Egyetem, Orvos- és Egészségtudományi Centrum" szövegrész helyébe a "Debreceni Egyetem Klinikai Központ" szöveg lép.
21. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 24. pontjában a "Békés Megyei Pándy Kálmán Kórház" szövegrész helyébe a "Békés Megyei Központi Kórház" szöveg lép.
22. A 32/2004. ESZCSM rendelet 3. számú melléklet EÜ90 6/a., EÜ90 6/b., EÜ90 6/c. pontjában a "protokoll" szövegrész helyébe az "eljárásrend" szöveg lép.
23. Hatályát veszti a 32/2004. ESZCSM rendelet 3. számú melléklet EÜ70 9/c1., EÜ90 3/a1., EÜ90 3/a2., EÜ90 3/a3., EÜ90 3/b1., EÜ90 3/b2., EÜ90 3/b3. pontja.
4. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
1. A 32/2004. ESZCSM rendelet 4. számú melléklet 1. pont t) alpontjában a "B-domain-depletált" szövegrész helyébe a "B-domain rövidített" szöveg lép.
2. A 32/2004. ESZCSM rendelet 4. számú melléklet 1. pontja a következő u) alponttal egészül ki:
(A veleszületett vérzékenység kezelésére:)
"u) recombináns technológiával humán sejtvonalon előállított 3. generációs B-domain-rövidített VIII. faktor koncentrátum."
3. A 32/2004. ESZCSM rendelet 4. számú melléklet 2. pontjában a "protokoll" szövegrész helyébe az "eljárásrend" szöveg lép.
5. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
A 32/2004. ESZCSM rendelet 7/b. számú melléklet II. pontja helyébe a következő rendelkezés lép:
"II. A Gyftv. 29. § (4) bekezdése szerinti bejelentés indoka:
| A megfelelő rész jelölendő! | |
| - már támogatott tápszer kiadhatóságának változása | □ |
| - már támogatott tápszer névváltozása | □ |
| - már támogatott tápszer törlése | □ |
| - már támogatott tápszer árcsökkentése | □ |
| - nyilvántartási szám változása | □ |
| - támogatás megszüntetése [Gyftv. 29. § (4) bekezdés b) pontja] | □ |
"
6. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
A 31/2010. EüM rendelet 6. melléklet 4. pontjában foglalt ábra helyébe a következő ábra lép:
"
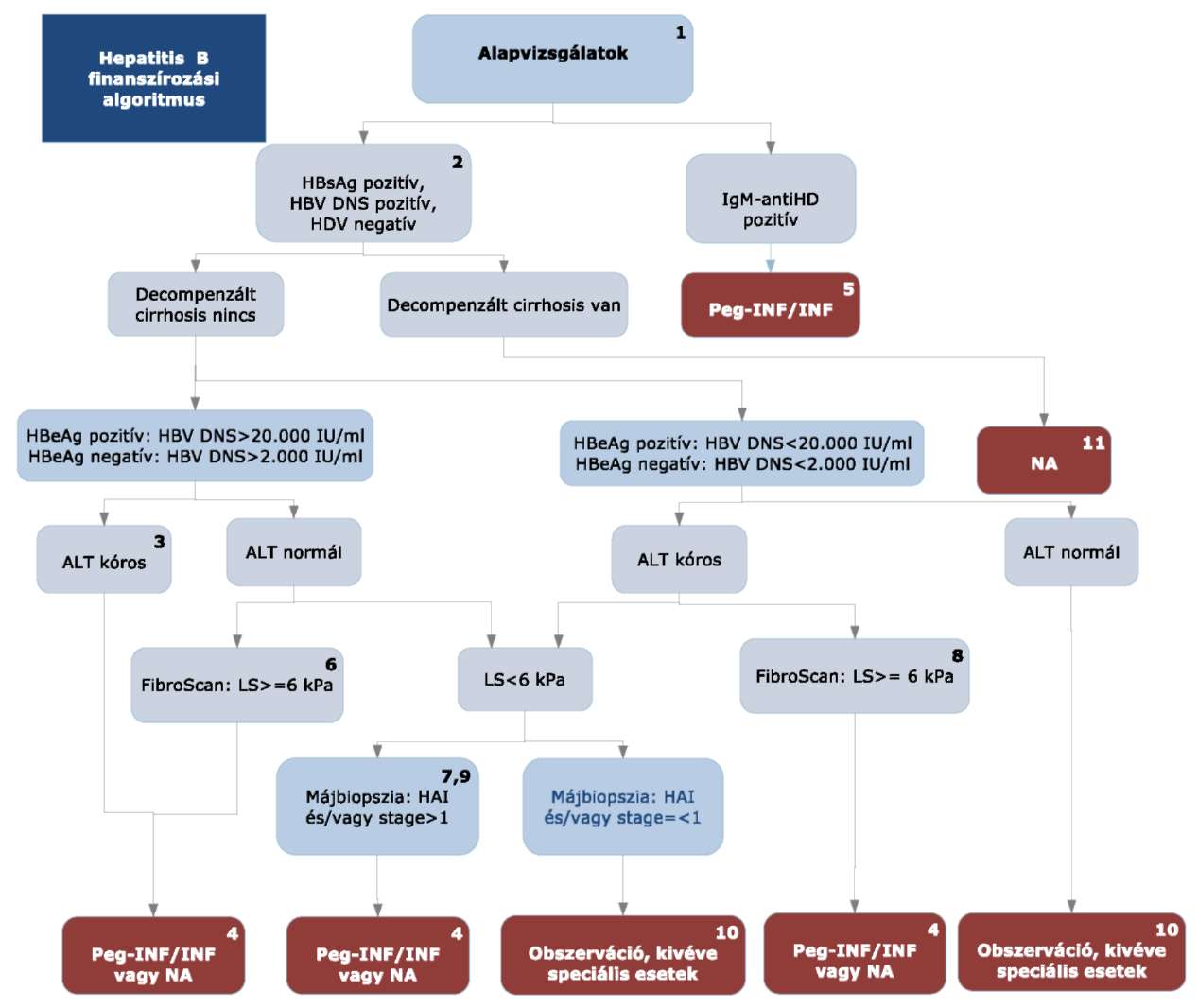
"
7. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
1. A 31/2010. EüM rendelet 15. melléklet 4.4. alpontja helyébe a következő rendelkezés lép:
"4.4. A denoszumab, raloxifen és teriparatid oszteoporotikus csonttörés primer prevenciójában való alkalmazását a társadalombiztosítás nem támogatja."
2. A 31/2010. EüM rendelet 15. melléklet 5.1. alpontja helyébe a következő rendelkezés lép:
"5.1. Az algoritmus posztmenopauzás nők és 55 év feletti férfiak oszteoporotikus csonttörését megelőző kezelésének sémáját mutatja be.
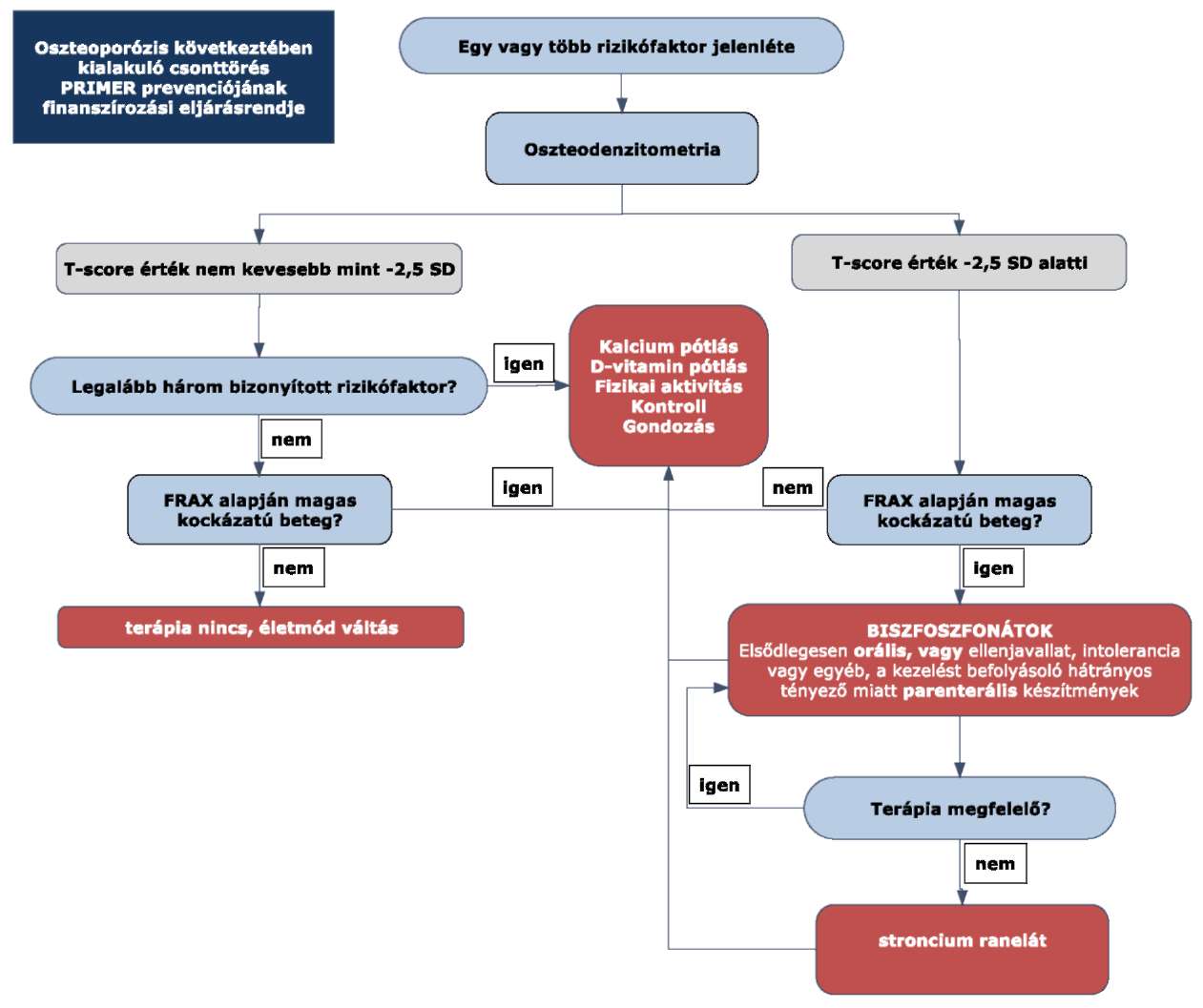
"
3. Hatályát veszti a 31/2010. EüM rendelet 15. melléklet 7.3. alpontjában foglalt táblázat 15. sora.
8. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
A 31/2010. EüM rendelet 16. melléklet 4.5.2. alpontjában az "a posztmenopauzás nő vagy 55 év feletti férfi betegnél" szövegrész helyébe az "a posztmenopauzás nő betegnél" szöveg lép.
9. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
A 31/2010. EüM rendelet 20. melléklet 2.8.4. alpontja helyébe a következő rendelkezés lép:
"2.8.4. Emelt, indikációhoz kötött társadalombiztosítási támogatással adható új típusú oralis antikoaguláns készítmények
Stroke és szisztémás embolizáció megelőzésére nem billentyű eredetű pitvarfibrillációban szenvedő felnőtt betegeknél,
- K-vitamin antagonista (acenocumarol és/vagy warfarin) alkalmazásának ellenjavallata esetén, vagy
- K-vitamin antagonista kezelés ellenére elszenvedett stroke vagy szisztémás embolizáció esetén, vagy amennyiben 6 hónapot meghaladó K-vitamin antagonista kezelés során a mért INR értékek kevesebb mint 60%-a esik terápiás tartományba (INR 2 és 3 közé), a következő kockázati tényezők közül legalább kettő fennállása esetén:
- bal kamrai ejekciós frakció < 40%,
- tünetekkel járó szívelégtelenség New York Heart Association (NYHA) II. stádium,
- életkor >= 75 év,
- életkor >= 65 év, a következők valamelyikével: diabetes mellitus, koszorúér-betegség vagy hypertonia dabigatran etexilate, rivaroxaban, apixaban (Eü70 26.)."
10. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
A 31/2010. EüM rendelet 21. melléklet 2.3.3.4. alpontja helyébe a következő rendelkezés lép:
"2.3.3.4. Pitvarfibrilláció
A pitvarfibrilláció a stroke erős, független rizikófaktora. TIA-t vagy ischemiás stroke-ot szenvedett betegeket antikoagulálni kell.
Pitvarfibrillációban emelt társadalombiztosítási támogatással adható új típusú oralis antikoaguláns készítmények a vonatkozó Eü70 26. indikációs pont szerint:
Stroke és szisztémás embolizáció megelőzésére nem billentyű eredetű pitvarfibrillációban szenvedő felnőtt betegeknél,
- K-vitamin antagonista (acenocumarol és/vagy warfarin) alkalmazásának ellenjavallata esetén, vagy
- K-vitamin antagonista kezelés ellenére elszenvedett stroke vagy szisztémás embolizáció esetén, vagy amennyiben 6 hónapot meghaladó K-vitamin antagonista kezelés során a mért INR értékek kevesebb mint 60%-a esik terápiás tartományba (INR 2 és 3 közé), a következő kockázati tényezők közül legalább kettő fennállása esetén:
- bal kamrai ejekciós frakció < 40%,
- tünetekkel járó szívelégtelenség New York Heart Association (NYHA) II. stádium,
- életkor >= 75 év,
- életkor >= 65 év, a következők valamelyikével: diabetes mellitus, koszorúér-betegség vagy hypertonia
Vonatkozó hatóanyagok: dabigatran etexilate, rivaroxaban, apixaban (Eü70, 26).
Néhány kiemelt betegcsoport:"
11. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
A 31/2010. EüM rendelet 23. melléklet 3.2-3.4. alpontja helyébe a következő rendelkezések lépnek:
"3.2. A gyomordaganat ellátása - Stádium 0-IA
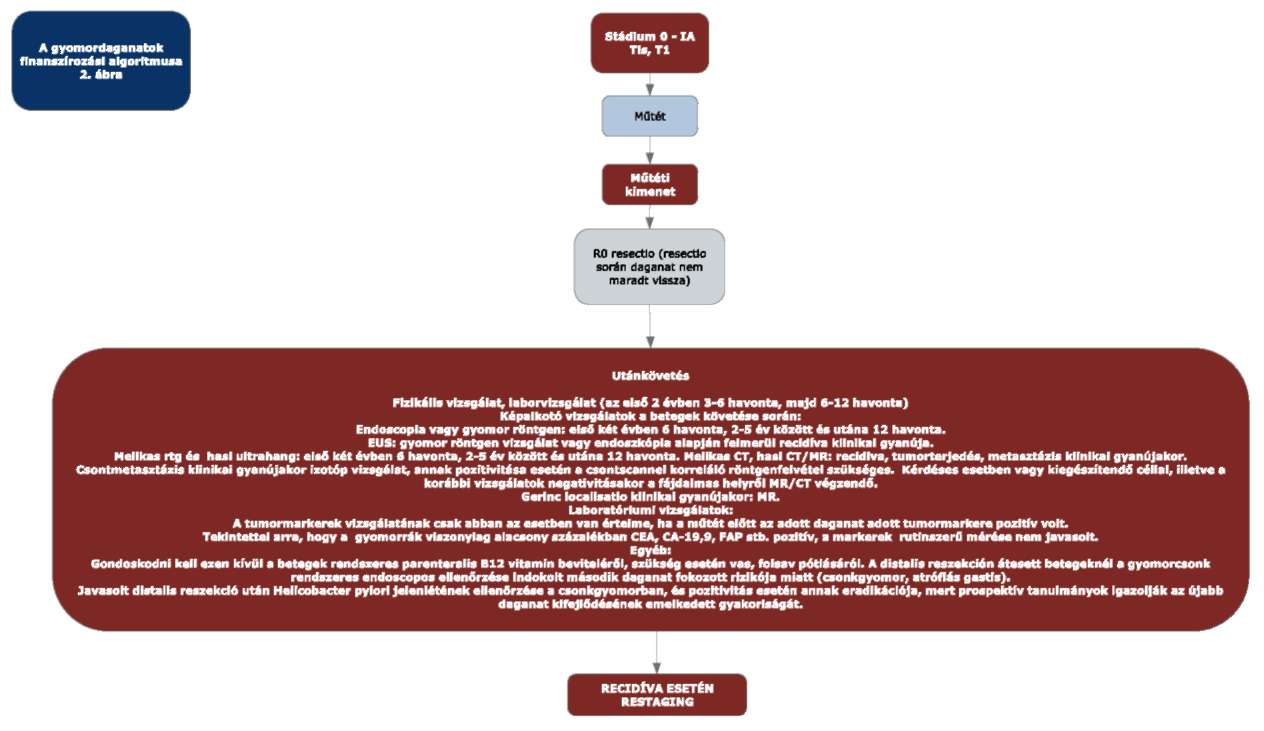
3.3. A gyomordaganat ellátása - Stádium IB-II-III
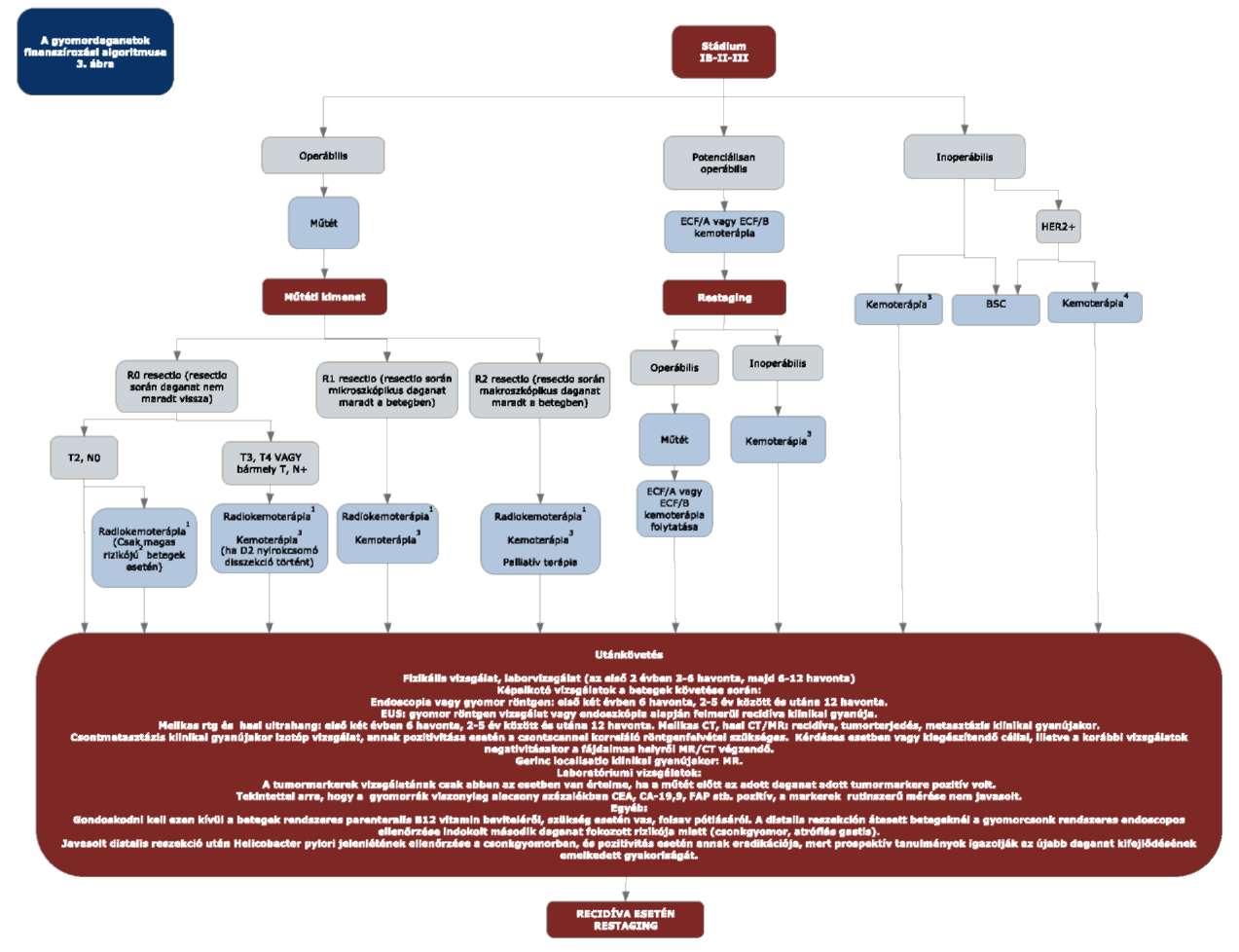
3.4. A gyomordaganat ellátása - Stádium IV
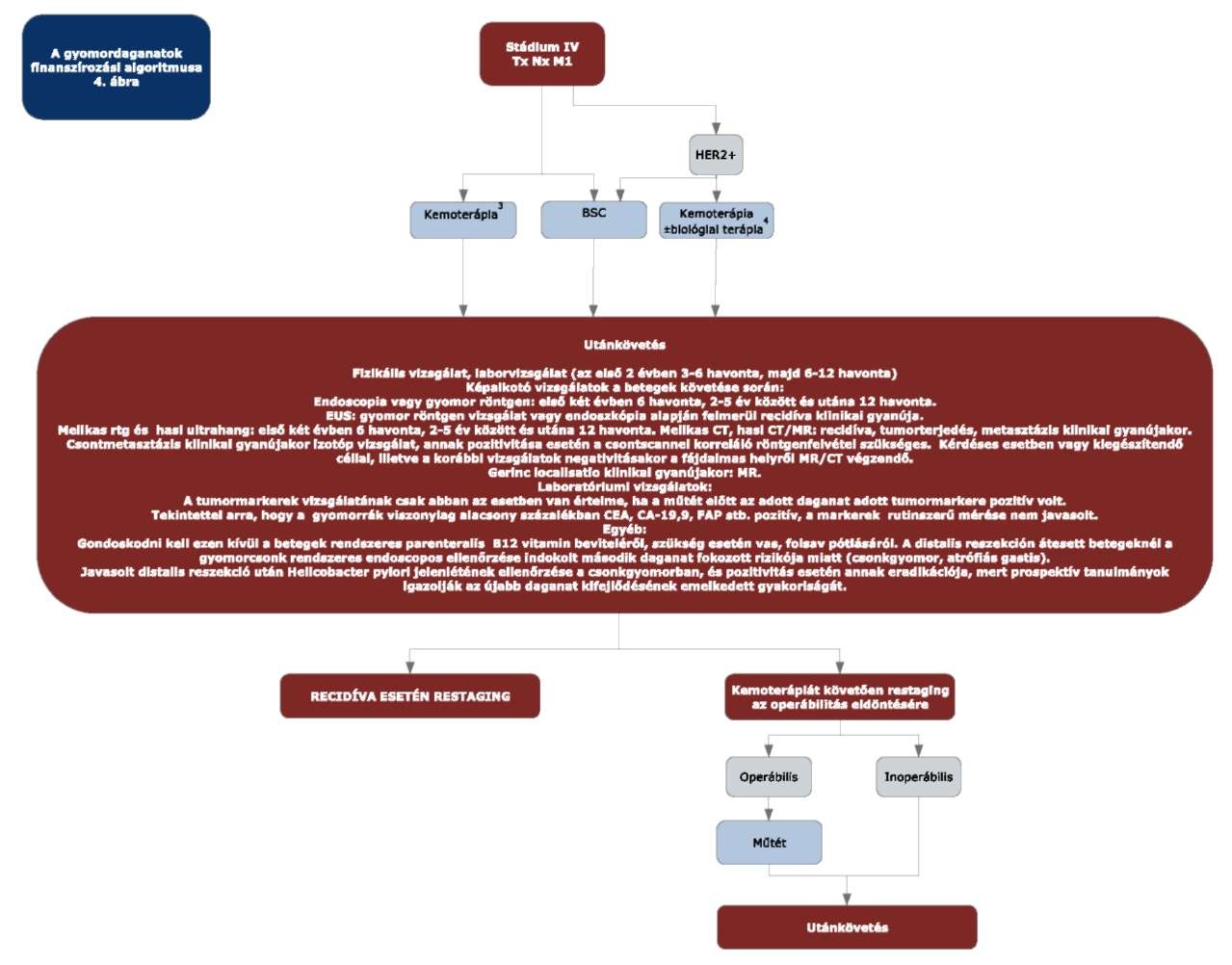
"
12. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
A 31/2010. EüM rendelet 24. melléklet 3. pontjában foglalt ábra helyébe a következő ábra lép:
"
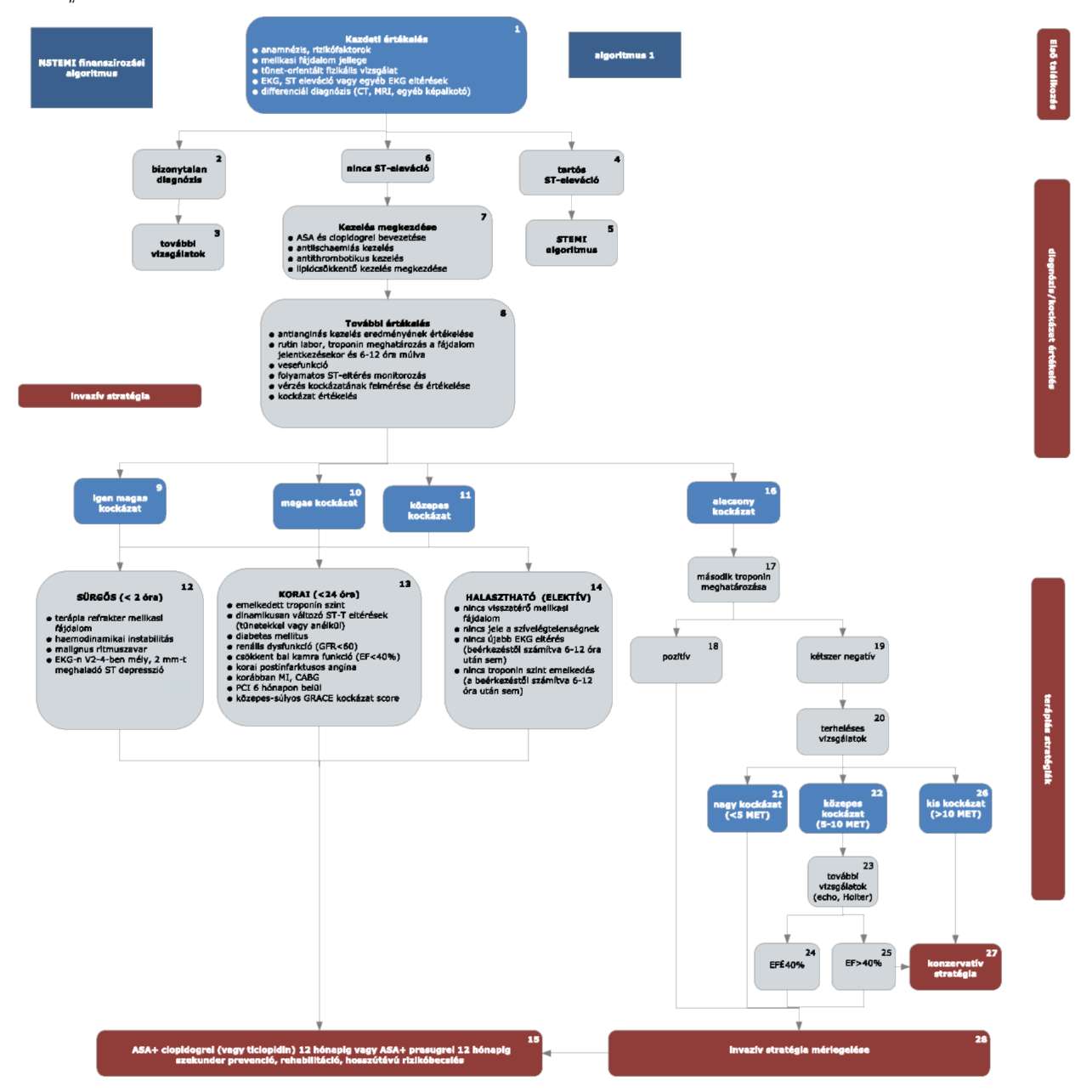
"
13. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
A 31/2010. EüM rendelet 28. melléklet 3.2. alpontja helyébe a következő rendelkezés lép:
"3.2. A nem invazív tumorok finanszírozási algoritmusa
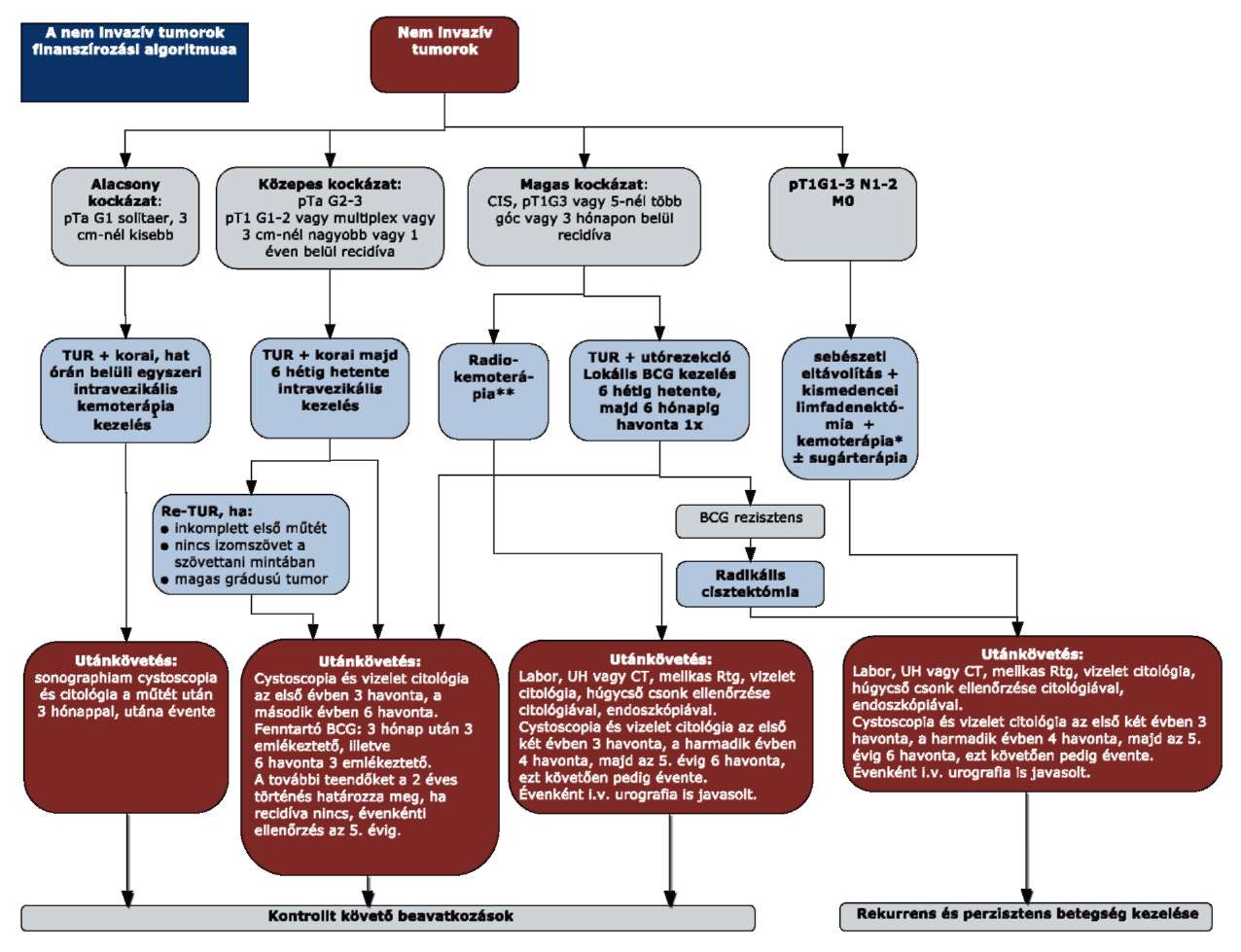
"
14. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
A 31/2010. EüM rendelet 30. melléklet 3.1. alpontjában foglalt ábra helyébe a következő ábra lép:
"
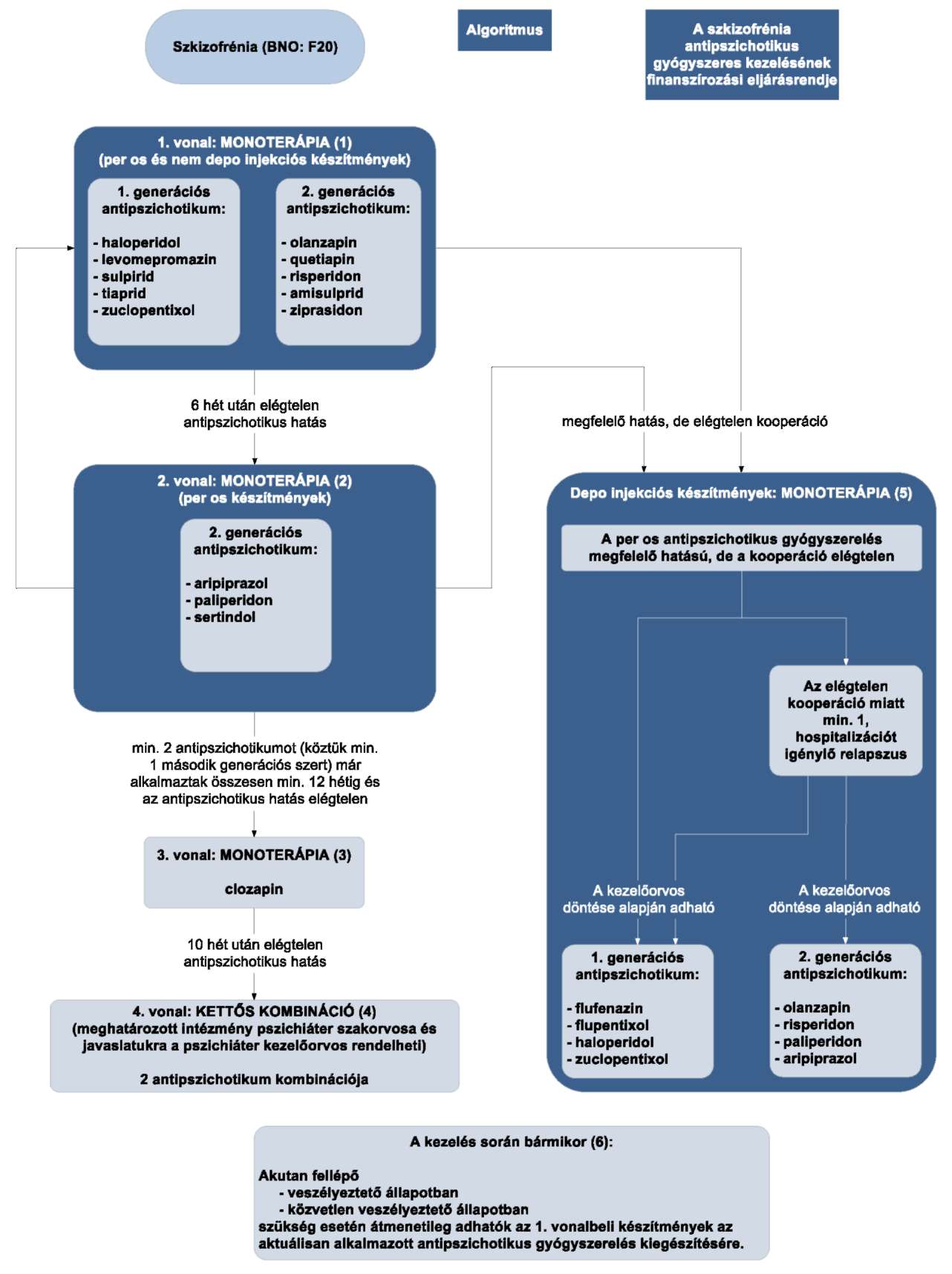
"
15. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
1. A 31/2010. EüM rendelet 32. melléklet 3. pontjában foglalt "2. ábra" helyébe a következő ábra lép:
"
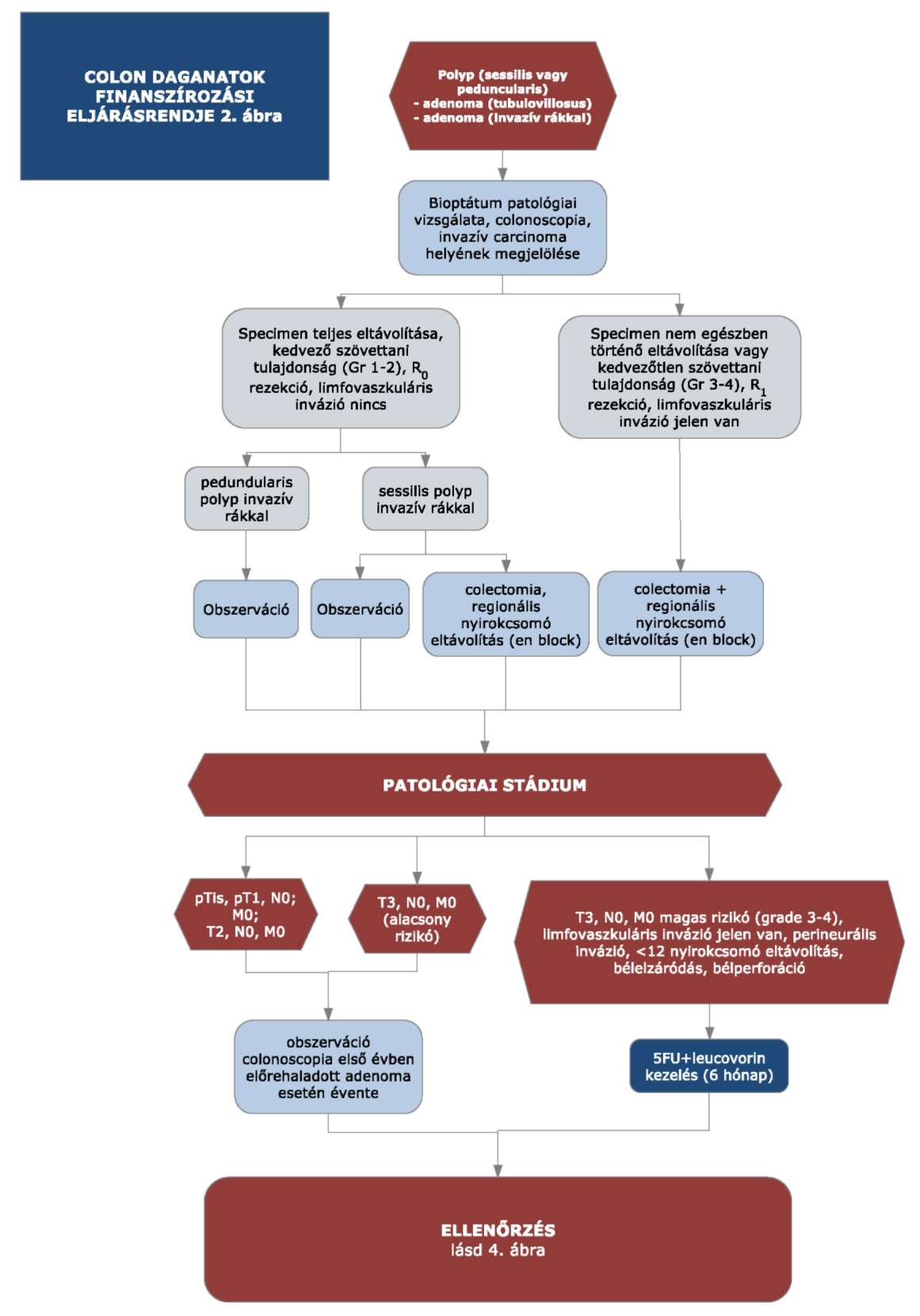
"
2. A 31/2010. EüM rendelet 32. melléklet 3. pontjában foglalt "4. ábra" helyébe a következő ábra lép:
"
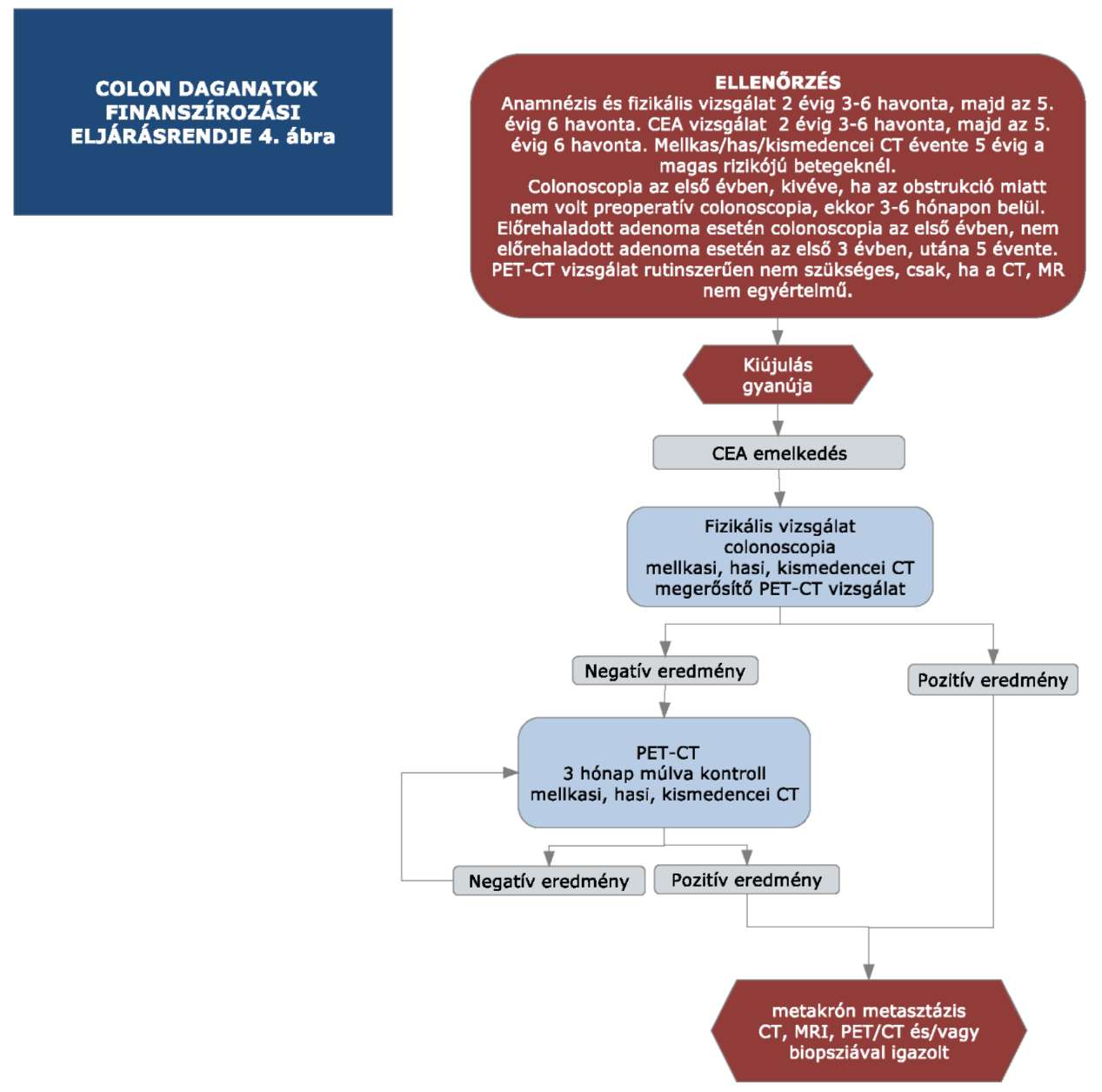
"
3. A 31/2010. EüM rendelet 32. melléklet 3. pontjában foglalt "6. ábra" helyébe a következő ábra lép:
"
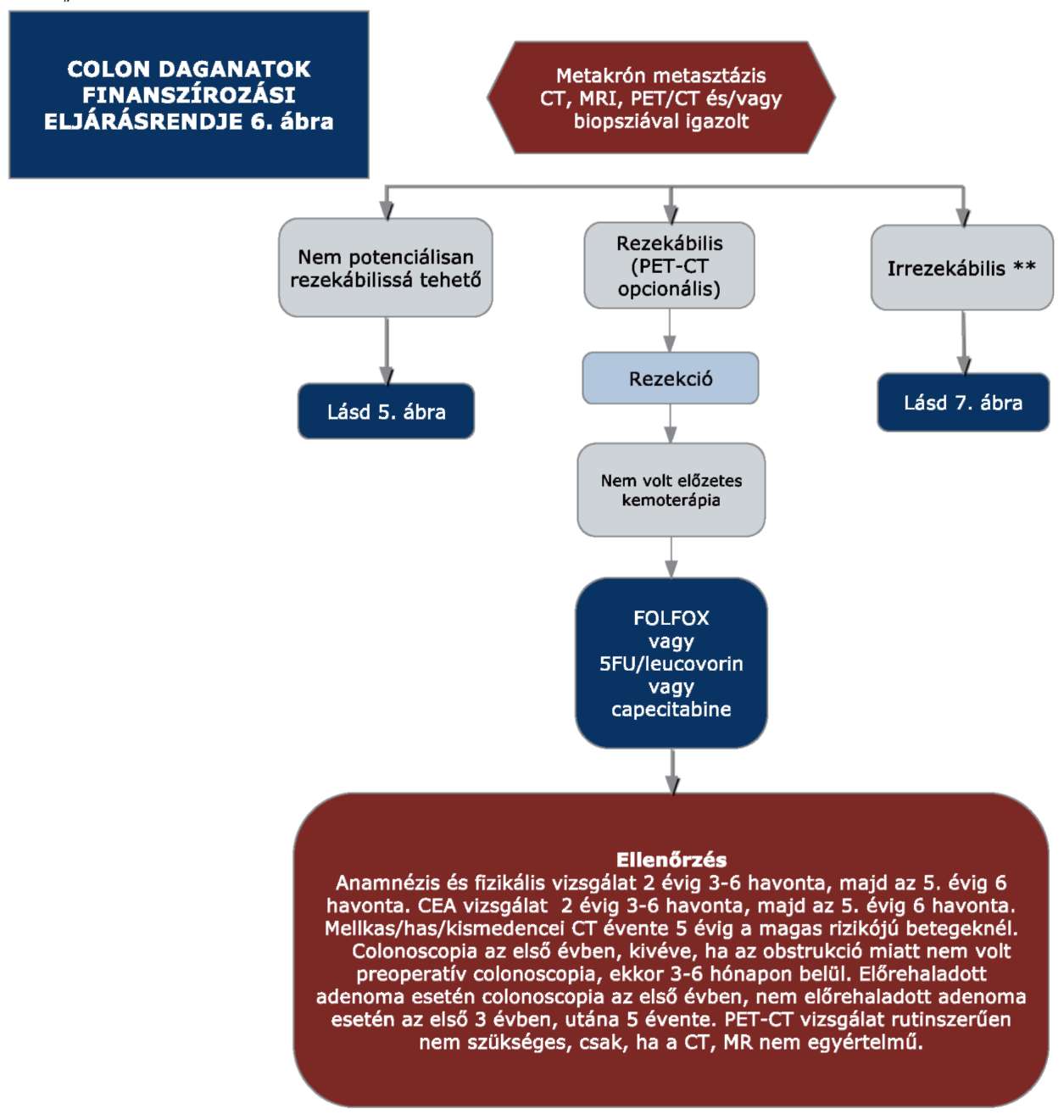
"
4. A 31/2010. EüM rendelet 32. melléklet 3. pontjában foglalt "7. ábra" helyébe a következő ábra lép:
"
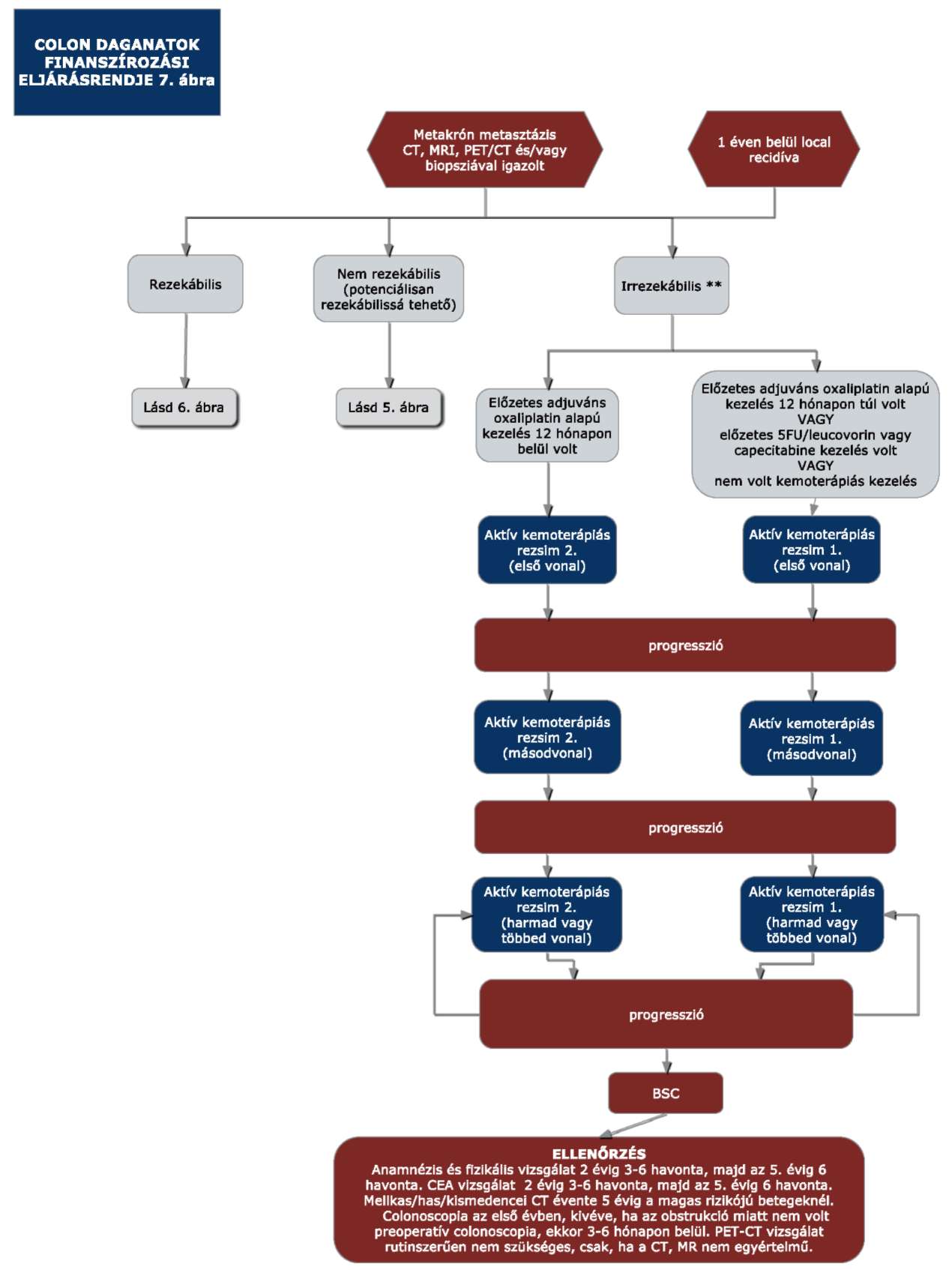
"
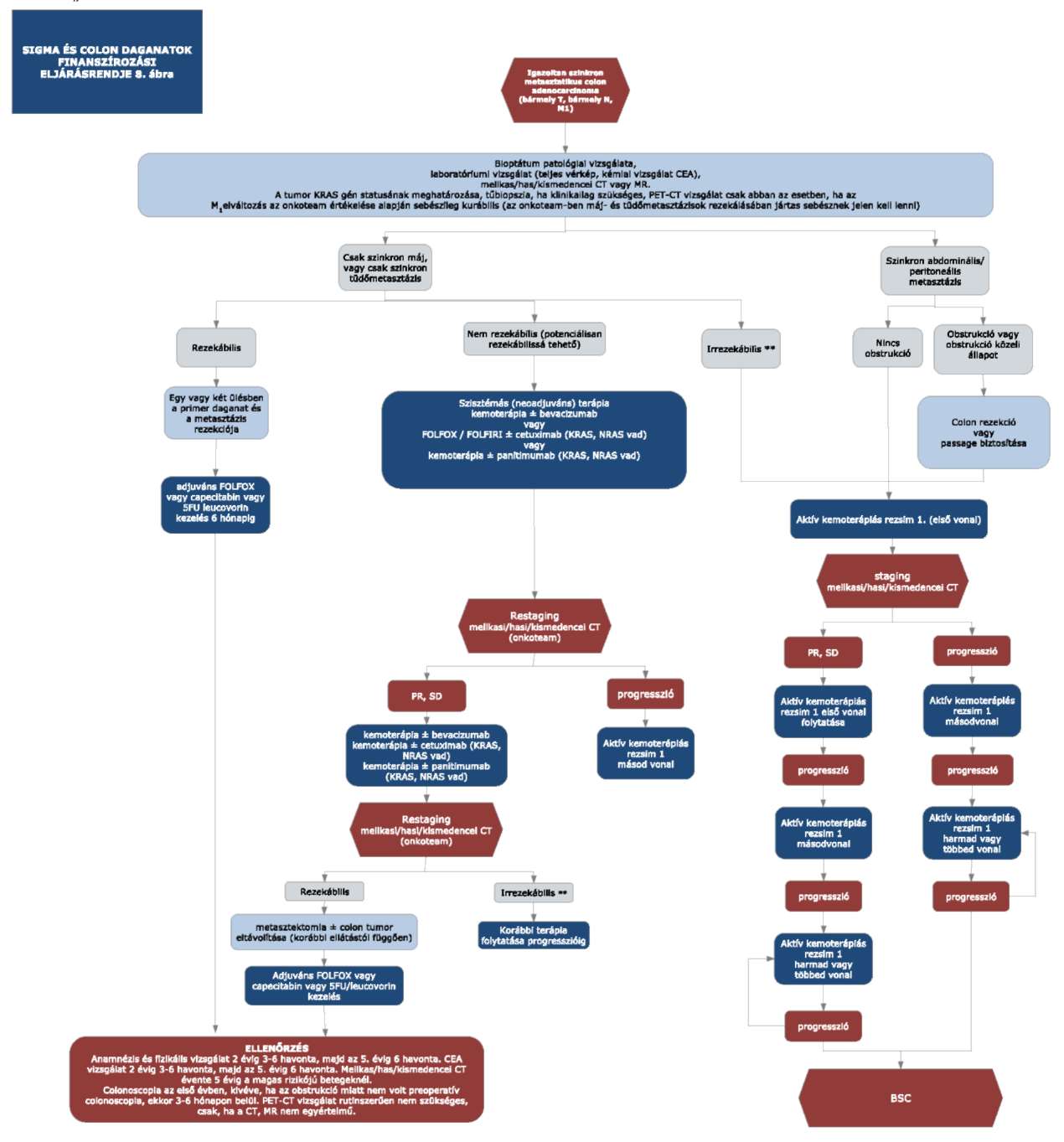
5. A 31/2010. EüM rendelet 32. melléklet 3. pontjában foglalt "8. ábra" helyébe a következő ábra lép:
"
"
6. A 31/2010. EüM rendelet 32. melléklet 3. pontjában foglalt "9. ábra" helyébe a következő ábra lép:
"

"
16. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
1. A 31/2010. EüM rendelet 33. melléklet 3. pontjában foglalt "1. ábra" helyébe a következő ábra lép:
"
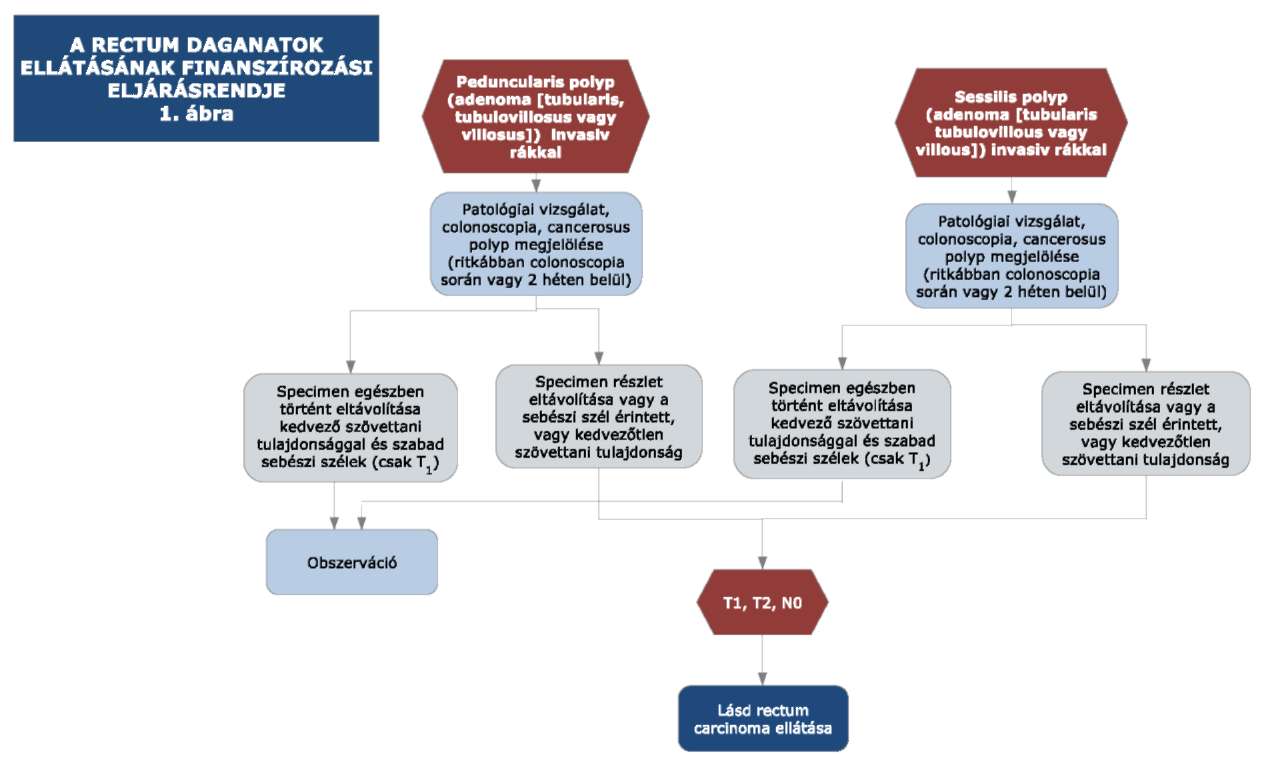
"
2. A 31/2010. EüM rendelet 33. melléklet 3. pontjában foglalt "7. ábra" helyébe a következő ábra lép:
"

"
17. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
1. A 31/2010. EüM rendelet 36. melléklet 4.1. alpontja helyébe a következő rendelkezés lép:
"4.1. A stabil COPD kezelésében választható hatóanyagcsoportok a beteg csoportja szerint

"
2. A 31/2010. EüM rendelet 36. melléklet 4.6. és 4.7. alpontja helyébe a következő rendelkezések lépnek:
"4.6. "A" csoport:
- Szükség szerint alkalmazhatók:
- SABA,
- SAMA,
- SABA+SAMA.
4.7. "B"csoport:
- Első választandó kezelés:
- LABA (kivéve: indacaterol és olodaterol),
- LAMA. A LAMA akkor választható, ha a LABA kontraindikált vagy vele szemben intolerancia lép fel vagy a légzésfunkciós vizsgálat alapján a beteg a GOLD 2 osztályba tartozik.
- Alternatív kezelés:
- LABA
- LABA+LAMA. A LABA+LAMA akkor választható, ha a gyógyszerbeállítást megelőző 6 hónapban a beteg a "B" csoport első választandó gyógyszeréből legalább 3 havi adagot kiváltott, és ennek ellenére a tünetek továbbra is jelentősek (mMRC>2 vagy CAT>10).
- Szükség szerint alkalmazhatók:
- SABA,
- SAMA,
- SABA+SAMA."
18. melléklet a 15/2016. (VII. 15.) EMMI rendelethez
A 31/2010. EüM rendelet 41. melléklet 3.2. alpontja helyébe a következő rendelkezés lép:
"3.2. A kiterjedt kissejtes tüdődaganat ellátása
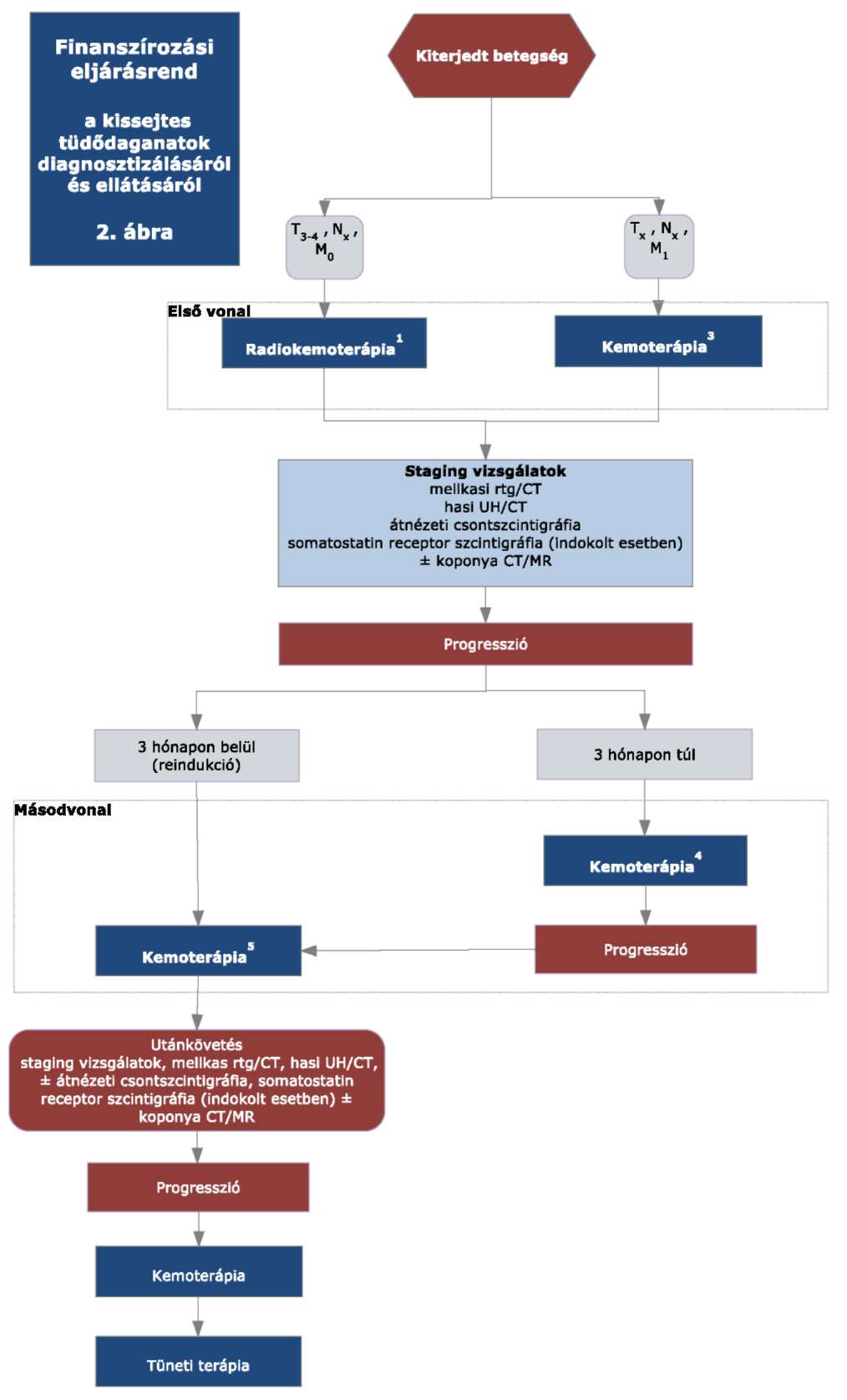
"


