22/2006. (V. 17.) EüM-FVM-KvVM együttes rendelet
a biocid termékek előállításának és forgalomba hozatalának feltételeiről szóló 38/2003. (VII. 7.) ESZCSM-FVM-KvVM együttes rendelet módosításáról
A kémiai biztonságról szóló 2000. évi XXV. törvény 34. §-a (4) bekezdésének h) pontjában kapott felhatalmazás alapján a következőket rendeljük el:
1. §
A biocid termékek előállításának és forgalomba hozatalának feltételeiről szóló 38/2003. (VII. 7.) ESZCSM-FVM-KvVM együttes rendelet (a továbbiakban: R.) 2. §-ának h) pontja helyébe a következő rendelkezés lép:
[2. § E rendelet alkalmazásában]
"h) forgalomba hozatal: biocid termék térítés ellenében vagy ingyenesen történő rendelkezésre bocsátása, illetőleg ezt követő raktározása, kivéve, ha a raktározást az Európai Gazdasági Térség vámterületéről való kiszállítás vagy ártalmatlanítás követi. Biocid terméknek az Európai Gazdasági Térség vámterületére történő behozatala e rendelet alkalmazásában forgalomba hozatalnak tekintendő;"
2. §
Az R. 9. §-ának (3) bekezdése helyébe a következő rendelkezés lép:
"(3) Az (1) bekezdéstől eltérően
a) az 1048/2005/EK bizottsági rendelettel módosított, a biocid termékek forgalomba hozataláról szóló 98/8/EK európai parlamenti és tanácsi irányelv 16. cikkének (2) bekezdésében említett tízéves munkaprogram második szakaszáról szóló, 2003. november 4-i 2032/2003/EK bizottsági rendelet (a továbbiakban: közösségi rendelet) 4. cikkének (3) bekezdése szerint az Európai Unióban 2000. május 14-én forgalomban levőnek minősülő, illetve
b) a forgalmazni kívánt biocid termék hatóanyagaként 2004. május 1. előtt bejelentett,
a közösségi jegyzékben nem szereplő hatóanyag is forgalomba hozható a közösségi jegyzékbe történő felvételéig, illetve annak elutasításáig, legkésőbb a 30. § (8) (10) bekezdése szerinti időpontig. E rendelkezés alkalmazásában a közösségi jegyzékbe történő felvétel elutasításának minősül az is, ha a hatóanyag a 98/8/EK irányelv 16. cikkének 2. bekezdése szerinti munkaprogram (a továbbiakban: felülvizsgálati program) keretében nem kerül értékelésre."
3. §
(1) Az R. 30. §-ának (2)-(3) bekezdése helyébe a következő rendelkezések lépnek:
"(2) A gyártó vagy importáló a 11. számú melléklet szerint - bejelenti az OKK-OKBI-nek a biocid termékben felhasznált, korábban a Magyar Köztársaságban be nem jelentett, de a közösségi rendelet szerint az adott terméktípusban forgalomba hozható hatóanyagot. A bejelentést legalább 15 nappal a forgalomba hozatalt megelőzően kell megtenni.
(3) A (2) bekezdés szerint bejelentett, önállóan vagy biocid termékben forgalomban lévő hatóanyagokat tartalmazó jegyzéket az országos tisztifőorvos a gyártók, illetve importálók új bejelentései alapján rendszeresen módosítja, és a jegyzéket internetes honlapján közzéteszi."
(2) Az R. 30. §-ának (8) bekezdése helyébe a következő rendelkezés lép:
"(8) Az a bejelentett biocid termék, amelynek hatóanyaga(i) nem kerül(nek) fel az 1. vagy 1/a) számú melléklet szerinti közösségi jegyzékre - a (9) bekezdésben foglaltakra is figyelemmel -, 2010. május 14-ig forgalmazható. Ettől eltérően egyes hatóanyagokat - ideértve a felülvizsgálati program keretében értékelésre nem kerülő hatóanyagokat is - tartalmazó biocid termék a közösségi rendelet szerinti, illetve az annak alapján megállapított határidők figyelembevételével forgalmazható."
(3) Az R. 30. §-a a következő (9) (10) bekezdéssel egészül ki:
"(9) A 2004. május 1. előtt bejelentett, de a közösségi rendelet szerint 2000. május 14-én forgalomban lévőnek nem minősülő hatóanyagot tartalmazó biocid termék - a hatóanyag közösségi jegyzékbe történő felvétele nélkül is - 2010. május 14-ig a Magyar Köztársaság területén forgalomba hozható. Az ilyen hatóanyagot tartalmazó biocid termék forgalmazására az OTH 2010. május 14-nél rövidebb határidőt is megállapíthat.
(10) A nem helyettesíthető hatóanyagok forgalmazásának a közösségi rendelet 4a. cikke szerinti meghosszabbítása kezdeményezésére a gyártó, az importáló, a forgalmazó, a felhasználó vagy más hatóság javaslatot tehet az OTH-nak. A javaslatot különösen a következőkre kiterjedő részletes indokolással kell ellátni:
a) az adott hatóanyag forgalmazásának meghosszabbítása a közösségi rendelet 4a. cikkének (1) bekezdésében említett mely okból szükséges,
b) annak bemutatása, hogy nem állnak rendelkezésre technológiailag és gazdaságilag megvalósítható más lehetőségek vagy környezetvédelmi és egészségügyi szempontból elfogadható helyettesítő hatóanyagok,
c) a tervezett felhasználás emberi egészségre, állatokra és környezetre gyakorolt hatása,
d) a lehetséges kockázatcsökkentő intézkedések.
Az OTH a javaslat alapján vagy saját hatáskörben kezdeményezheti a felhasználás meghosszabbítását az Európai Bizottságnál. A forgalomba hozatal részletes feltételrendszerét - az Európai Bizottság határozatában foglaltakra is tekintettel - az OTH állapítja meg."
4. §
Az R. 31. §-a a következő (4) bekezdéssel egészül ki:
"(4) Az állategészségügyről szóló 2005. évi CLXXVI. törvény szerinti állat-egészségügyi biocid termék forgalomba hozatalára - annak valamennyi hatóanyaga közösségi jegyzékbe történő felvételéig - a külön jogszabály rendelkezéseit kell alkalmazni."
5. §
Az R. 32. §-ának (3) bekezdése helyébe a következő rendelkezés lép:
"(3) Ez a rendelet - a kémiai biztonságról szóló 2000. évi XXV. törvénnyel együtt - a biocid termékek forgalomba hozataláról szóló, 1998. február 16-i 98/8/EK európai parlamenti és tanácsi irányelvnek való megfelelést szolgálja.
(4) Ez a rendelet az 1048/2005/EK bizottsági rendelettel módosított, a biocid termékek forgalomba hozataláról szóló 98/8/EK európai parlamenti és tanácsi irányelv 16. cikkének (2) bekezdésében említett tízéves munkaprogram második szakaszáról, valamint az 1896/2000/EK rendelet módosításáról szóló, 2003. november 4-i 2032/2003/EK bizottsági rendelet 4. cikke (1)-(3) bekezdése, 4a. cikke végrehajtásához szükséges rendelkezéseket állapítja meg."
6. §
(1) Az R. 7. számú melléklete helyébe e rendelet melléklete lép.
(2) Az R. 8. számú melléklete 6. pontjának 22. d) alpontja a következő mondattal egészül ki:
[22. Egyes irtószer-kijuttatási eljárásokra vonatkozó különleges előírások:]
"d) szabadban melegköd képzéssel/hidegköd képzéssel/ULV-eljárással/permetezéssel történő rovarirtás esetén, a méhek védelme érdekében 400 m2 feletti terület kezelésekor, legkésőbb a kezelés megkezdését megelőző munkanapon 9 óráig bejelentést kell tenni. Ebben közölni kell a kezelendő terület helyét és nagyságát, a rovarirtás kezdetének és befejezésének időpontját, az alkalmazásra kerülő irtószert, továbbá a kijuttatás módját."
A bejelentést a növényvédelemről szóló 2000. évi XXXV. törvény 45. § (3) bekezdésében foglaltakkal megegyezően a kezelendő terület helye szerint illetékes települési önkormányzat jegyzőjének kell írásban megtenni.
"A méhesek tulajdonosait (kezelőit) a bejelentésköteles rovarirtási tevékenységről a jegyző az Nvt. 57. §-ának d) pontjában foglaltakkal megegyezően értesíti."
7. §
(1) Ez a rendelet a kihirdetését követő 8. napon lép hatályba, ezzel egyidejűleg hatályát veszti
a) az R. 30. §-ának (1) bekezdése;
b) az R. 12. számú melléklete.
(2) E rendelet hatálybalépésével egyidejűleg
a) az R. 3. §-ának (1) bekezdésében az "a földművelésügyi és vidékfejlesztési miniszter által kijelölt szerv" szövegrész helyébe "az Állatgyógyászati Oltóanyag-, Gyógyszer- és Takarmány-ellenőrző Intézet" szövegrész,
b) az R. 3. §-ának (2) bekezdésében az "Európai Unió" szövegrész helyébe az "Európai Gazdasági Térség" szövegrész,
c) az R. 8. §-ának (9) bekezdésében az "a 8004/2000. (EüK. 22.) EüM tájékoztató" szövegrész helyébe "az Európai Unióban osztályozott veszélyes anyagok jegyzékéről szóló külön jogszabály," szövegrész,
d) az R. 8. számú melléklete 6. pontjának 22. d) alpontjában a "2000. évi XXXV. törvény" szövegrész helyébe a "2000. évi XXXV. törvény (a továbbiakban: Nvt.) " szövegrész lép.
(3) E rendelet 1-2. §-a és 3. §-ának (2)-(3) bekezdése a biocid termékek forgalomba hozataláról szóló, 1998. február 16-i 98/8/EK európai parlamenti és tanácsi irányelv 2. cikk (1) bekezdése h) pontjának és 16. cikke (1) bekezdésének való megfelelést szolgálja.
(4) Ez a rendelet a következő uniós jogi aktusok végrehajtásához szükséges rendelkezéseket állapítja meg:
a) a Bizottság 2032/2003/EK rendelete (2003. november 4.) a biocid termékek forgalomba hozataláról szóló 98/8/EK európai parlamenti és tanácsi irányelv 16. cikkének (2) bekezdésében említett tízéves munkaprogram második szakaszáról, valamint az 1896/2000/EK rendelet módosításáról, 4. és 4a. cikk;
b) a Bizottság 1048/2005/EK rendelete (2005. június 13.) a biocid termékek forgalomba hozataláról szóló 98/8/EK európai parlamenti és tanácsi irányelv 16. cikkének (2) bekezdésében említett tízéves munkaprogram második szakaszáról szóló 2032/2003/EK rendelet módosításáról, 1. cikk 3-4. pont.
Budapest, 2006. május 15.
Dr. Rácz Jenő s. k.,
egészségügyi miniszter
Gráf József s. k.,
földművelésügyi és vidékfejlesztési
miniszter
Dr. Persányi Miklós s. k.,
környezetvédelmi és vízügyi miniszter
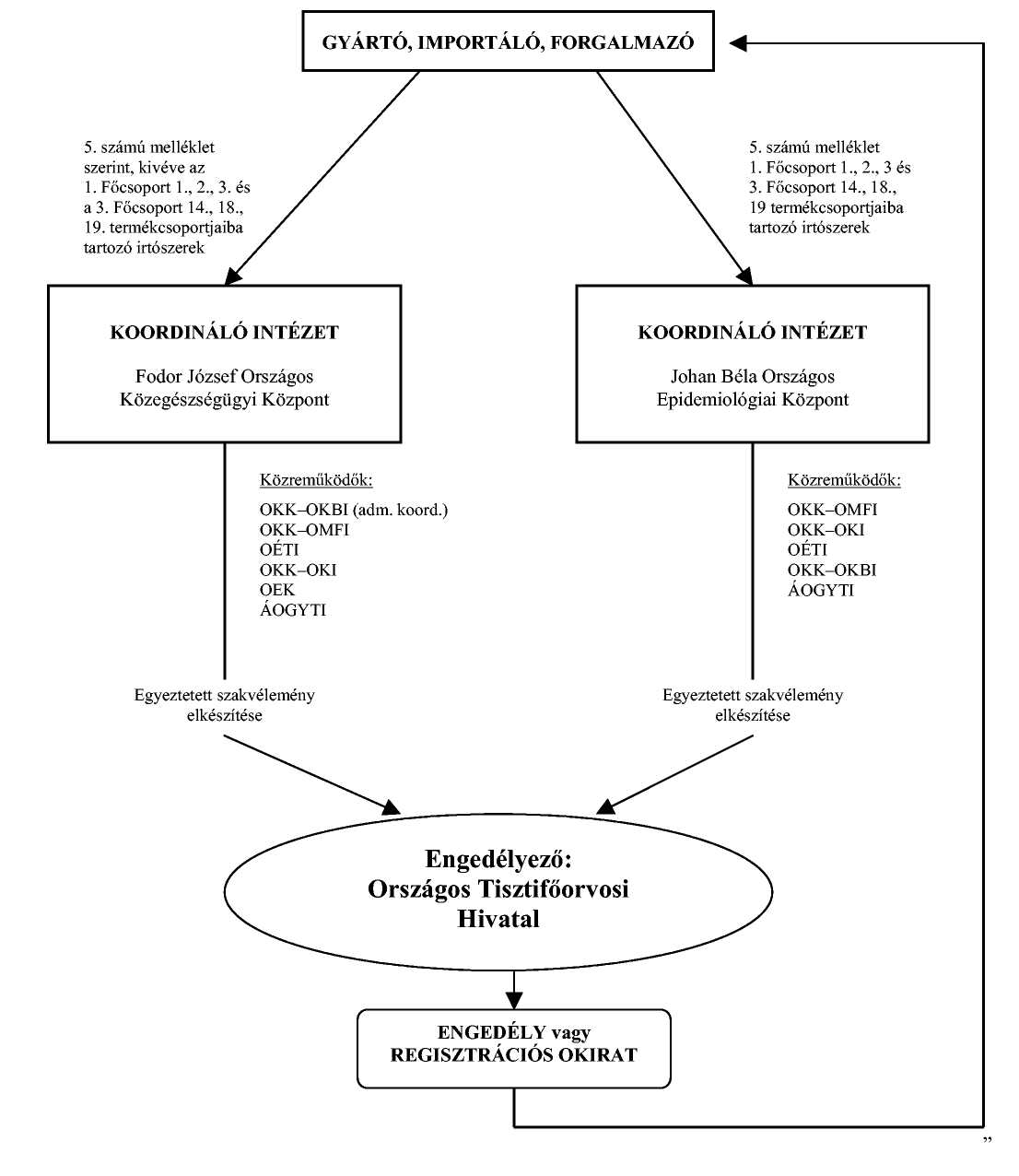
Melléklet a 22/2006. (V. 17.) EüM-FVM-KvVM együttes rendelethez
" 7. számú melléklet a 38/2003. (VII. 7.) ESZCSM-FVM-KvVM együttes rendelethez
Biocid termék engedélyeztetési eljárása