EüM közlemény (HÉ 2009/53.)
az Egészségügyi Minisztérium szakmai irányelvéről, szakmai protokolljáról, módszertani leveléről[1]
Tartalomjegyzék
| ÁPOLÁS | ||
| A szondatáplálásról | P | |
| BELGYÓGYÁSZAT | ||
| A diabetes mellitus kórismézéséről, a cukorbetegek kezeléséről és gondozásáról a felnőttkorban | IE | 1. módosítás |
| Krónikus kritikus végtag ischaemiáról | P | |
| CSECSEMŐ- ÉS GYERMEKGYÓGYÁSZAT | ||
| A cerebralis paresisről (CP) | P | |
| A scoliosis rehabilitációjáról | P | |
| A krónikus gyulladásos bélbetegségekről (IBD) | P | 1. módosítás |
| Az epilepsziáról | P | 1. módosítás |
| Az egészséges csecsemő táplálásáról | P | 1. módosítás |
| A 0-18 éves életkorú gyermekek látásfejlődésének követése, a kancsalság és a fénytörési hibák felismeréséről | IE | |
| A 0-18 éves életkorú gyermekek teljeskörű, életkorhoz kötött hallásszűréséről | IE | |
| FOG- ÉS SZÁJBETEGSÉGEK | ||
| Az állcsontok, a periosteum és a lágyrészek fogeredetű gennyes gyulladásainak kezeléséről | P | |
| FOGLAKOZÁS ORVOSTAN | ||
| A foglalkozási asthmáról | P | 1. módosítás |
| GYERMEKSEBÉSZET | ||
| A gyermekkori lágyéksérv kezeléséről | P | 1. módosítás |
| INFEKTOLÓGIA | ||
| A varicella kezeléséről és megelőzéséről | P | 1. módosítás |
| Az oltások és műtétek egybeesése esetén szükséges teendőkről | IE | |
| A neutropéniás beteg fertőzéseinek megelőzéséről és kezeléséről | P | 1. módosítás |
| KLINIKAI GENETIKA | ||
| A praeimplantatios genetikai diagnosztikáról | IE | |
| MEGELŐZŐ ORVOSTAN | ||
| A nozokomiális pneumónia megelőzéséről | IE | |
| A dohányzás leszokás támogatásáról | IE | |
| NEUROLÓGIA | ||
| A Sclerosis multiplex kezelésről | IE | 1. módosítás |
| A Parkinson kór és a parkinsonismus gyógyszeres kezelésésről | IE | 1. módosítás |
| A botulin toxin-A alkalmazásáról neurológiai kórképekben | IE | 1. módosítás |
| ORTOPÉDIA | ||
| A glenohumeralis izület instabilitásáról | P | 1. módosítás |
| A Carpal tunnel szindrómáról | P | 1. módosítás |
| A csontok áttétes tumorairól | P | 1. módosítás |
| A Dupuytren contracturáról | P | 1. módosítás |
| Felnőttkori aszeptikus combfejnekrózisról | P | 1. módosítás |
| Habituális patella ficamról | P | 1. módosítás |
| Infantilis cerebralis paresisről (ICP) | P | 1. módosítás |
| A kézízületi synovitisekről és tenosyvitisekről | P | 1. módosítás |
| Meniscus sérülés ellátásáról | P | 1. módosítás |
| Perthes kórról | P | 1. módosítás |
| Epiphyseolysis capitis femoris juvenilis ellátásáról (Serdülőkori femurfejelcsúszás) | P | 1. módosítás |
| Subacromialis impingement ellátásáról | P | 1. módosítás |
| Térdarthrosis elllátásáról | P | 1. módosítás |
| A csípőficamról | P | 1. módosítás |
| Veleszületett dongaláb ellátásáról | P | 1. módosítás |
| Primer csonttumorokról és tumorszerű elváltozásokról | P | 1. módosítás |
| Lábtő betegségek ellátásáról | P | |
| A lúdtalp (pes planus) ellátásáról | P | |
| Hanyagtartásról | P | |
| Előláb betegségek ellátásáról | P | |
| A könyök betegségeiről | P | |
| Gerincdeformitásokról | P | |
| ORVOSI LABORATÓRIUMI DIAGNOSZTIKA | ||
| A számított GFR (eGFR) bevezetésvel kapcsolatos ismeretekről útmutató laboratóriumi szakemberek számára | IE | |
| A számított GFR (eGFR) bevezetésvel kapcsolatos ismeretekről útmutató háziorvosok és szakrendelések számára | IE | |
| ORVOSI MIKROBIOLÓGIA | ||
| A tuberkolózis mikrobiológiai diagnosztikájáról | IE | |
| A felsőlégúti infekciók bakteriológiai diagnosztikájáról | IE | |
| PATHOLÓGIA | ||
| A tápcsatornából vett diagnosztikus szövetminták kórszövettani feldolgozásáról | ML | 1. módosítás |
| A haematológiai minták feldolgozásáról és patológiai diagnosztikájáról | ML | |
| Az aspiratios cytológiai vizsgálatok gyakorlatáról | ML | |
| Húgyhólyag, vesemedence és ureter daganatok diagnosztikájáról, a biopsziás, illetve a műtéti anyagainak pathológiai feldolgozásáról | P |
| RADIOLÓGIA | ||
| Szabványos negatív leletről | IE | |
| REHABILITÁCIÓ | ||
| A traumás gerincvelősérültek orvosi rehabilitációjáról | P | 1. módosítás |
| A stroke rehabilitációs ellátásáról (felnőtt) | IE | 1. módosítás |
| REUMATOLÓGI AÉS FOZIOTERÁPIA | ||
| A gyógyszeres fájdalomcsillapításról és gyulladásgátlásról a reumatológiai betegségekben | P | 1. módosítás |
| SEBÉSZET | ||
| A jó- és rosszindulatú strummák sebészeti kezeléséről | P | 1. módosítás |
| Légyéktáji és hasfali sérvek ellátásáról felnőttkorban | IE | 1. módosítás |
| SZEMÉSZET | ||
| A szemészeti szövődmények terápiájáról diabetes mellitusban | P | 1. módosítás |
| A felnőttkori szürkehályog diagnosztikájáról és kezeléséről | IE | 1. módosítás |
| A kontaktlencse rendelésről | P | |
| SZÜLÉSZET-NŐGYÓGYÁSZAT | ||
| A méhnyakrák szűrésének szempontjai | IE | |
| TÜDŐGYÓGYÁSZAT | ||
| Interstitialis tüdőbetegségekről | P | |
| A krónikus obstruktiv légúti betegség (chronic obstructive pulmonary disease - COPD) diagnosztikájáról és kezeléséről | IE | 1. módosítás |
| VÉDŐNŐI | ||
| Az egészséges csecsemő (0-12 hónap) táplálásáról | P |
P - protokoll
IE - irányelv
ML - módszertani levél
Az Egészségügyi Minisztérium
szakmai protokollja
A szondatáplálásról
Készítette: az Ápolási Szakmai Kollégium
I. Alapvető megfontolások
- A táplálkozás alapvető fiziológiai szükséglet, amelyet ha nem elégítenek ki, az egyén halálához vezet.
- A malnutrició minden esetben a beteg állapotát jelentősen súlyosbító (komorbid) tényező.
- A mesterséges táplálás a terápia részeként kezelendő, a specifikus kezelési terv része.
- Az enterális szondatáplálás az orális táplálás kiegészítésére vagy teljes helyettesítésére alkalmazható, minden esetben orvosi indikáció alapján.
1. A protokoll alkalmazási / érvényességi területe
- Alapellátás.
- Otthoni szakápolás.
- Fekvőbeteg-ellátás.
- Szociális ellátás.
2. A protokoll bevezetésének alapfeltétele
- Ez a protokoll az ápolási szakmai eljárási leírásokkal kiegészítve alkalmazandó.
- A tápláltsági állapot szűrése, az anamnézis felvétele, a fizikális vizsgálat, a diagnózis felállítása, a beavatkozások, a terápiás terv kivitelezése, az elért eredményekértékelése, valamint a terápiás terv korrigálása team munka eredménye, a feladatok kompetencia szerinti tagozódása és egymásra épülése alapvető az eredmények eléréséhez.
- Ajánlott a Táplálási team (TT) szervezett működése.
3. Definiciók Malnutrició
Olyan tápláltsági állapot, melyben az energia, fehérje, vagy egyéb tápanyagok hiánya vagy többlete (vagy azok egyensúlyának hiánya) mérhető, káros hatással jár a szövet/test formájára/megjelenésére, funkciójára és a klinikai eredményekre nézve. Enterális szondatáplálás
A gyomor-bélrendszer működőképessége bizonyított, így a tápanyagokat tartalmazó oldatokat rendszerint különböző hosszúságú és vastagságú szondák útján juttatják az emésztőcsatorna megfelelő szakaszába. Speciális tápszer
Különleges táplálkozási igényt kielégítő olyan élelmiszer, amely különleges eljárással, beteg emberekdiétás ellátására készül és orvosi felügyelet mellett használható. Olyan betegek kizárólagos vagy részleges táplálására szolgál, akiknél a természetes eredetű tápanyagok vagy azok metabolitjainak felvétele, emésztése, felszívódása, feldolgozása vagy kiválasztása korlátozott, csökken vagy zavart szenved, valamint más orvosilag meghatározott tápanyagszükséglet áll fenn és az nem biztosítható hagyományos étrend megváltoztatásával, más különleges táplálkozási igényt kielégítő élelmiszerrel vagy e kettő kombinációjával. Energiaszükséglet
Az a táplálékkal felveendő energiamennyiség, amely az egyén állandó testtömege és változatlan testtömeg összetétele mellett, hosszú távon, jó egészségi állapotban fedezi az energiafelhasználást úgy, hogy lehetővé teszi a gazdaságilag hasznos és szociálisan szükséges fizikai aktivitást.
3.1. Kiváltó tényezők
- Az alapbetegség.
- A táplálék felvételének, emésztésének és felszívódásának zavarai. (mechanikus akadályok, malignus elváltozások, gyulladásos bélbetegségek, az emésztőrendszer fekélyei, sipolyok, emésztőrendszer egyéb betegségei)
- A tápcsatornán át történő táplálkozás tilalma.
- A nagymértékben csökkent étvágy.
- Az idült hasmenés és/vagy befolyásolhatatlan hányás.
- A táplálkozási képtelenség vagy negativizmus.
- A felgyorsult anyagcserével (hypermetabolizmus) és / vagy a fehérjék fokozott lebontásával (hyperkatabolizmus) járó állapotok, pl. tartós láz, súlyosabb sérülés, elsősorban politrauma, égésbetegség, szepszis, hyperthyreozis stb.
3.2 Kockázati tényezők
- Csökkent tápanyagbevitel.
- Idegen környezet.
- A nem megszokott és nem időben tálalt, gyakran ízetlen, hideg étel.
- Különböző betegségek esetén alkalmazott terápiák hatása (gyógyszeres, sugár stb.).
- Az egészségügyi ellátó személyzet helytelen szemlélete, elméleti és gyakorlati ismeretek hiánya (iatrogén ártalom).
- Fokozott, kóros tápanyagvesztés (hányás, vérzés, hasmenés).
- Ismerethiány.
- Szegénység.
4. Panaszok/Tünetek/Általános jellemzők Panaszok
- Gyengeség érzet.
- A test alaki változásának panasza (soványság).
- Testtömegvesztés.
- Emésztési panaszok (puffadás).
- Étvágytalanság.
- Hányás.
- Hányinger.
- Székletürítéssel kapcsolatos panaszok (hasmenés, székrekedés).
- Láb duzzanata.
- Hasi fájdalom.
- Nyelési nehezítettség.
Tünetek
- Soványság alaki jelei (lesoványodott test, beesett arc).
- A bőr turgorának csökkenése.
- A vázizomzat tömegének csökkenése (izomatrófia).
- Csökkent mozgás és állóképesség.
- Fénytelen haj, repedezett köröm.
- Hányinger, hányás.
- Hasmenés.
- Késleltetett sebgyógyulás.
- Apátia, depresszió, magatartásban bekövetkező zavarok.
- Oedémák megjelenése. Általános jellemzők
- Izomfehérjék mennyisége csökkent.
- Zsigeri fehérjék csökkentek.
- Zsírraktárak kiürültek.
- Immunvédekezési reakciókanergiáig csökkentek.
- A szervezet megnövekedett tápanyagigénye.
5. A betegség leírása
- A malnutrició olyan kóros állapotnak tekinthető, amely egy vagy több lényeges tápanyag relatív vagy abszolút hiányának, esetleg iatrogén feleslegének következtében alakul ki.
- A malnutrició fogalomkörébe tartozik az abszolút alultápláltság, továbbá azok a relatív hiányállapotok vagy aránytalanságok is, amelyek egyes specifikus tápanyagok hiánya vagy ellenkezőleg, aránytalan felhalmozása következtében jönnek létre.
5.1. Érintett szervrendszerek
A malnutrició következtében-az agy kivételével-a szervezet valamennyi szervének tömege megfogyatkozik:
- A vesében a tubulusok atrophizálnak és a kéregállomány megduzzad, ami a glomerolus filtráció és a tubuláris resorpció csökkenését idézi elő. Az átmeneti poliuria gyakori kísérője ezeknek az elváltozásoknak. Emellett nem ritkán észlelhető metabolikus acidózis.
- Haemodinamikai következményként bradikardia és vérnyomáscsökkenés figyelhető meg. A szívinnotropiája romlik és ezzel párhuzamosan a perctérfogat, valamint a centrális vénásnyomás is csökken. Mindezeknek a keringési változásoknak hatására a szervezet oxigénellátása zavart szenved.
- A légzési funkcióban csökken a belégzési erő, a vitálkapacitás, valamint a funkcionális reziduális kapacitás és végeredményként romlik a gázcsere.
- A bélfal a fokozott fehérjebontás és az " utánpótlás "- elsősorban a feltételes esszenciális aminosav, a glutamin -hiánya miatt elvékonyodik és a mucosa réteg atrophizál. Csökken a bélfal motilitása, a táplálék emésztése és felszívódása is zavart szenved. A bél élettani baktérium - flórája is megváltozik és kórós kolonizációk alakulnak ki. A bélfal átjárhatósága fokozódik és elkezdődik a translokáció: a mikroorganizmusok és termékeik kilépése a bél lumenéből, ahonnan - a nyirokcsomók és a máj makrofágjai által kialakult védekező-rendszer áttörése után -a szisztémás keringésbe kerül.
- A vázizmok tömegének megfogyatkozása lassúbb folyamat, amely ősi alkalmazkodási reakció következménye. (Magyarázat: tartós éhezés során a szervezet a mozgatórendszer viszonylag hosszú időtartamú épsége következtében nagyobb eséllyel képes az éhezést kiváltó vészhelyzetből elmenekülni vagy a tápanyagszerzéshez szükséges mozgási tevékenységet kivitelezni).
A váz izomfehérjéinek bontását megelőzi a szervezet egyéb adaptációs folyamata.
- Pszichés elváltozásként csökken az intellektuális teljesítőképesség, depresszió, kezdeményezés hiánya, érdektelenség, önzés, agresszivitás, személyiségváltozás, majd zavartság és teljes apátia, végül kóma alakul ki.
5.3. Morbiditás Magyarországon
A betegségekhez társuló malnutricióban szenvedő betegek száma csupán becslésen alapszik, mert felmérés a valós állapotokról, a betegellátás teljes egészét lefedő vizsgálat nem áll rendelkezésünkre. Számos hazai szerző kimutatása alapján úgy becsülhető, hogy a klinikai ellátásban részesülők 45%-a már az ellátás megkezdésekor közepes fokú malnutricióban szenved, súlyos malnutrició kb.30%-ra tehető. Az ellátás közben kialakult malnutritív állapot arányát még becslés alapján sem tudjuk a hazai ellátás területén megítélni.
A Magyar Dietetikusok Országos Szövetsége 2004.-ben végzett vizsgálata alapján az alapellátásból kórházba került 1266 beteg tápláltsági állapot szűrésekor 41% volt közepesen ill. súlyosan veszélyeztetett a malnutrició szempontjából.
5.4 Jellemző életkor
- Minden korosztály érintett, azonban a csecsemők, gyermekek valamint az idősebb korosztály veszélyeztetettsége a kiszolgáltatottság, az alapvető szükségletek nagyobb fokú kielégítése iránti igény miatt sokkal nagyobb.
II. Diagnózis
- Malnutrició (mint diagnózis felállítása orvosi kompetencia).
- Malnutrició kockázata (mint ápolási diagnózis szakdolgozói kompetencia is).
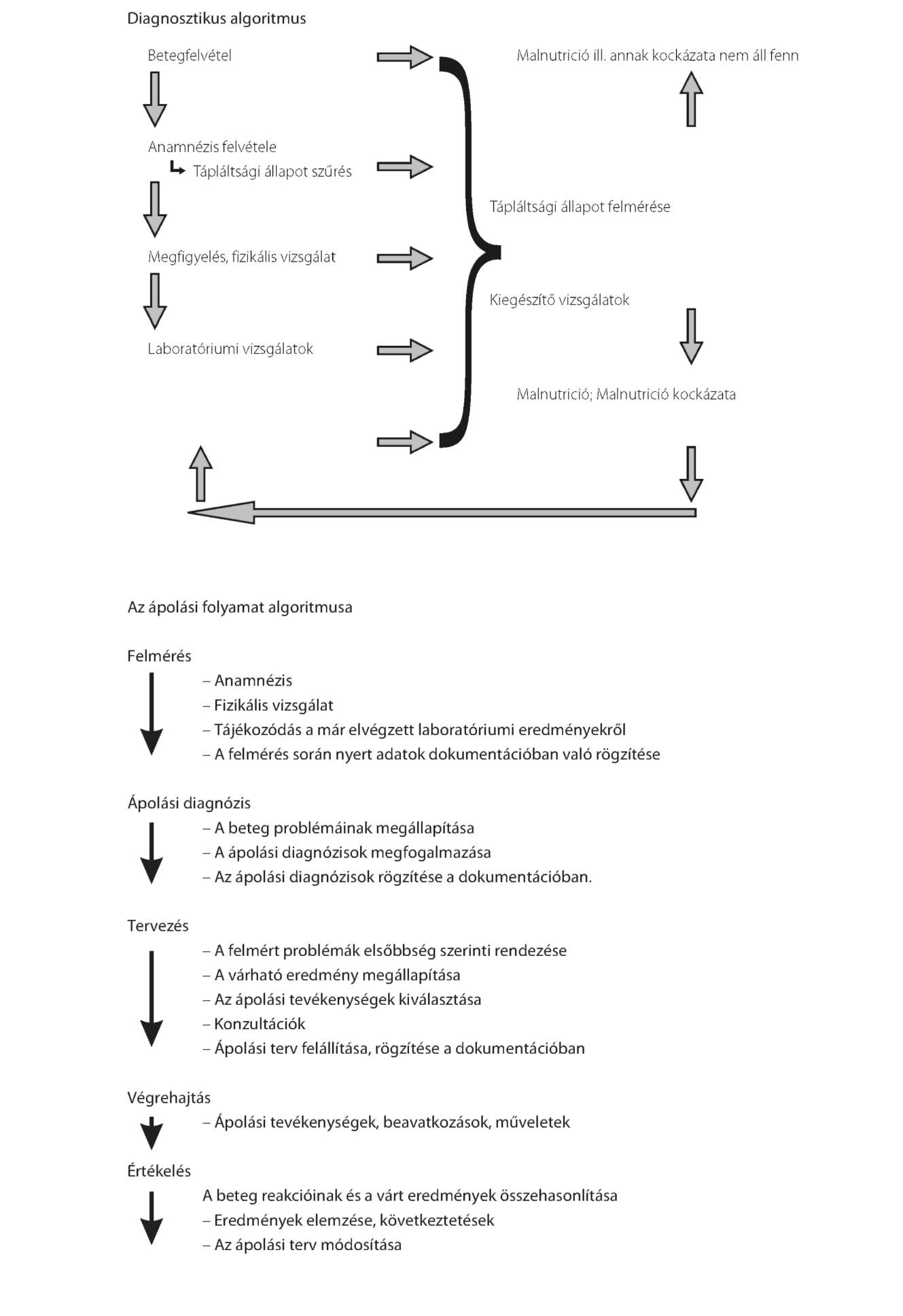
1. Anamnézis
A tápláltsági állapot vizsgálatakor a malnutrició tünetei keresendők. A tápláltsági állapotra vonatkozó ápoló által végzett anamnézis és a táplálkozási adatfelvétel során felderített fontos információk segítenek eldönteni szükséges-e részletes tápláltsági állapotfelmérést, illetve mélyreható táplálkozási felmérést javasolnia az ápolónak.
1.1. Ápoló által végzett anamnézis felvétel
A tápláltsági állapotra vonatkozó ápolói anamnézis felvételének első lépése a tápláltsági állapot szűrés, amely egyszerű módszer, minimális adat felhasználásával tájékoztató jellegű információt szolgáltat a táplálkozás szempontjából magasabb kockázatú betegek köréről.
A kapott értékek a kockázat szintjeit határozzák meg, -e mellett az ápoló további teendőit is megjelöli.
FONTOS, HOGY A TESTTÖMEG ÉS A TESTMAGASSÁG MEG LEGYEN MÉRVE!
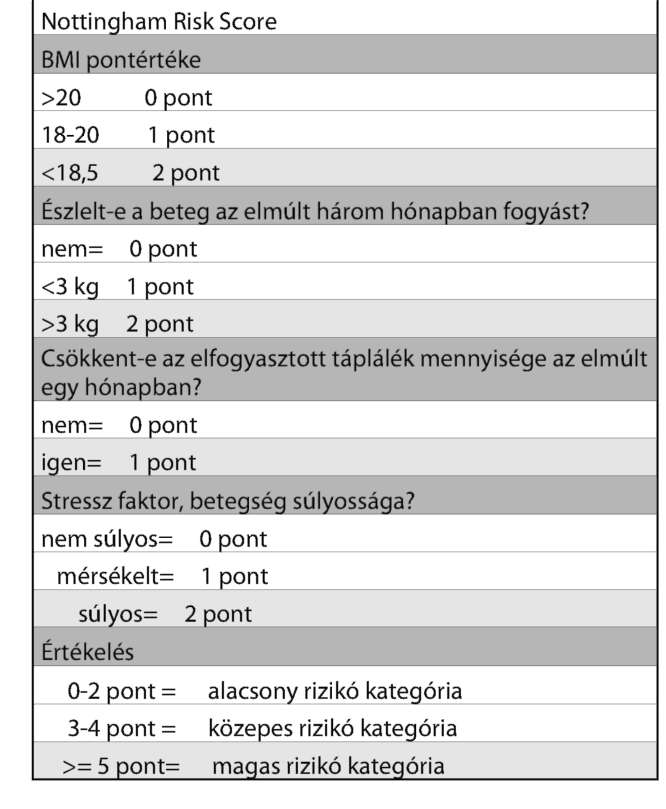
További szűrő módszerek:
MNA - Mini Nutritional Assessment Idős betegek ellátására fejlesztették ki
NRS - Nutritional Risk Screening Fekvőbeteg ellátásban külföldön gyakran használt módszer
MUST - Malnutritio Universal Screening Tool Főleg az alapellátásban alkalmazzák
Ápolói teendő a szűrési módszer eredményének értékelése után:
Alacsony rizikó kategória
Teendő:
- Speciális ellátás a táplálkozás szempontjából jelenleg nem indokolt. Közepes ill. magas rizikó kategória
Teendő: A tápláltsági állapot és az elfogyasztott táplálék folyamatos követése
- A beteg kezelőorvosát a szűrés eredményéről tájékoztatni kell.
- Az ápoló jelölje műszakonként piktogrammon az ápolási dokumentációba tapasztalatát a beteg által elfogyasztott ételek napi mennyiségéről, legalább négy egymást követő napon keresztül.

- A szűrést követő negyedik napon mérje meg újra a beteg testtömegét.
- Amennyiben a beteg testtömegében indokolatlan csökkenés észlelhető és a négy nap alatt elfogyasztott táplálék mennyisége átlagban kevesebb, mint a felét teszi ki a tálalt ételnek, az ápoló tegyen javaslatot a beteg kezelőorvosa és a dietetikus felé részletes tápláltsági és táplálkozási állapot felmérésére.
További kérdések az ápoló által végzett anamnézis felvételéhez
- Étvágyban következett-e be változás az elmúlt egy hónapban?
- Az elmúlt egy hónapban voltak-e nyelési problémák?
- Az étel megrágása okozott -e gondot az elmúlt hetekben?
- Van-e olyan étel, amelynek fogyasztását kerüli?
- Napi átlagos folyadékfogyasztás (ml) ?
- Táplálékkal összefüggő beteg által tudott érzékenység / allergia?
- Emésztési problémák, hányinger, hányás, puffadás, hasmenés, székrekedés?
- Fájdalom; jellege, időtartama, erőssége?
- Hozzájut-e a beteg rendszeresen táplálékhoz?
- Rendszeresen étkezik-e?
- Mikor evett utoljára?
- Ki végzi a bevásárlást, illetve az ételek előkészítését? - Tart-e speciális diétát illetve használ-e étrend kiegészítőket?
- Fogyaszt-e (mennyit és milyen rendszerességgel) alkoholt, kábítószert, kávét, dohány árut, gyógyszert ? A táplálékfelvételt, a tápanyagok felhasználását vagy szükségletét befolyásoló betegség fenn áll-e?
1.2. Fizioterápiás anamnézia
- Decubitus, tromboembóliás szövődmények által veszélyeztetett csoportok feltárása:
- Csökkent mobilitás, immobilitás.
- Keringési zavarok érbetegségek, varicositás.
- Idegsérülés.
- Érzés kiesés.
- Idős kor. -Tudatállapot.
- Súlyos krónikus betegség.
1.3. Dietetikus által végzendő anamnézis felvétel
A dietetikus a tápláltsággal és a táplálkozással kapcsolatos részletes anamnézis felvétele előtt tájékozódjon a beteg dokumentációjában addig rögzített adatokról. A már felvett adatok figyelembevételével egészítse ki a tápláltságra ill. táplálkozásra vonatkozó anamnézist.
Kiegészítő kérdések a dietetikus által végzett tápláltsági anamnézis felvételéhez
- Testtömeg változás üteme?
- Napi étkezések száma változott-e a szokásoshoz képest?
- Átlagosan elfogyasztott napi táplálék mennyisége, minősége, aránya, energia értéke? (FFQ = Food Freqvency Questionare, FAQ= Food Amount Questionare, tápanyag számító szoftware-kalkalmazása ajánlott )
2. Fizikális vizsgálatok
Az elégtelen táplálkozás a teljes szervezetet érinti. A rosszul tápláltságra utaló jelek megfigyelhetők a beteg fizikális vizsgálata során.
2.1. Ápoló által végzett fizikális állapot felmérése

2.2. Gyógytornász által végzendő mozgásállapot felmérése
- Megtekintés
- Bőr gyakori és rendszeres megtekintése veszélyeztetett helyeken izomatrófiák feltérképezése.
- Ágyban való mobilitás vizsgálata.
- Képes-e a beteg önállóan oldalra, hasra fordulni, ágyszélére kiülni.
- Mozgás korlátozottság okának vizsgálata.
- Ízületi mozgásterjedelem vizsgálat.
- Izomerő-vizsgálat.
- Motoros és szenzoros idegi funkciók vizsgálata.
- Motiváció.
- Segédeszközök használata befolyásolja-e a beteg mozgásállapotát.
- FIM-skála.
- Alapbetegségre specifikus skálák, objektív mérőszámok használata.
2.3. Dietetikus által végzendő tápláltsági állapot felmérése

3. Diagnosztikai vizsgálatok
Ápolói kompetencia
- Testtömegmérés
(Hitelesített orvosi mérlegen 0,1 kg pontossággal, cipő és felsőruházat nélkül mért érték.)
- Testmagasságmérés
(Hitelesített eszközzel, 0,1 cm pontossággal mért érték. Mérendő személy cipő nélkül, összezárt sarokkal a mérőrúddal
háttal áll, állcsúcs-állkapocs közti képzelt egyenes merőleges a gerincre.)
- BMI.
- Tápláltsági állapot szűrés.
Orvosi-dietetikusi kompetencia
- Tápláltságiállapot-felmérés.
- Antropometriai felmérés.
- Bioelektromos impedancia.
- Direkt kalorimetria.
4. A felmérés keretében talált bizonyítékok, azonosított problémák felismerése Az ápolási folyamat helyzetfelmérését követő lépés az ápolási diagnózis felállítása.
A klinikai véleményalkotás a tényleges vagy lehetséges problémákra adott egyéni /családi /közösségi reakciókról legyen pontos és szabatos. A megfogalmazott ápolási diagnózisok szabják meg a tervezés irányát és az ápolási beavatkozások megválasztását.
A következő szabályok betartásával kell az ápolási diagnózisokat felállítani: Aktuális diagnózis:
A feltárt alapvető adatok tartalmazzák a diagnózis jeleinek és tüneteinek vagy meghatározó jellegzetességeinek fennállása mellet szóló bizonyítékokat. Kockázati diagnózis:
A feltárt alapvető adatok tartalmazzák a diagnózis kapcsolódó (kockázati) tényezőinek fennállása mellett szóló bizonyítékokat. ( A meghatározó jellegzetességek fennállta mellett szóló bizonyítékok azonban értelemszerűen hiányoznak.)
Ápolási diagnózis felállításának algoritmusa
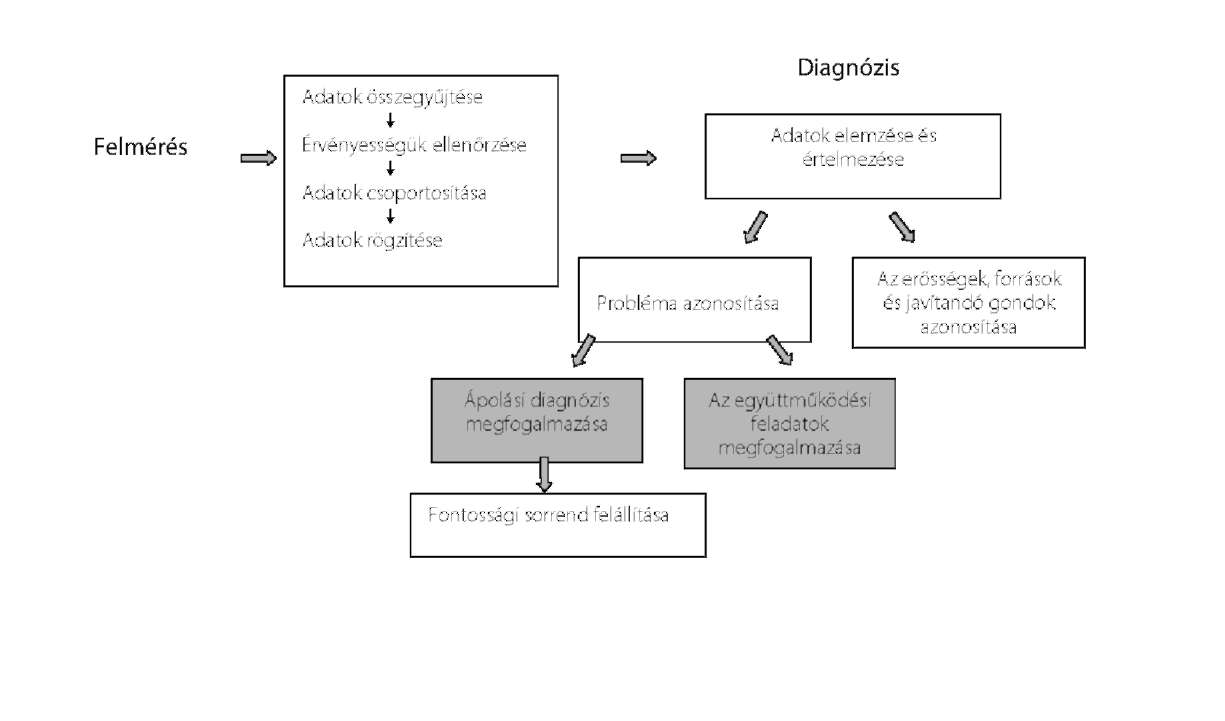
4.1. Leggyakoribb ápolási diagnózisok

Ajánlott ápolási diagnózisok az ápolás folyamata során
- Tápanyagbevitel akut csökkenése.
- Nem megfelelő energia és tápanyagbevitel.
- Étkezésben tapasztalt nehézségek.
- Fáradtság, gyengeség.
- Csökkent testmozgás.
- Csökkent mozgásképesség és állóképesség.
- Fertőzés kockázata.
- Késleltetett sebgyógyulás.
- Gyógyulás elhúzódása.
- Zavartság.
- Rossz koordináció.
- Felfekvés és trombózis kialakulásának kockázata.
Ezek a diagnózisok a beteg ellátása során is felmerülhetnek, megjelenésük jelezheti a beteg tápláltsági állapotának romló tendenciáját.
4.2. Funkcionális diagnózisok
- Mozgásképesség csökkenése.
- Izomgyengeség.
- Fizikai teherbírás csökkenése.
- Helyzetváltoztatási képtelenség.
- Immobilitás.
- Izomatrófia.
5. Az ellátás tervezése
A betegek ellátásának tervezése az "ápolási terv"ben fogalmazódik meg.
A dietetikus által elkészített táplálási tervet figyelembe kell venni az ápolási terv elkészítésénél.
Az ápolási terv fő elemei:
- A diagnózisok vagy problémák elsőbbségek megjelölésével való megfogalmazása.
- Elvárható eredmények (kimenetel, cél) megjelölése.
- Az ápolási utasítások (beavatkozások, eljárások) megfogalmazása.
5.1. Ápolási terv felépítésének logikai menete
| Ápolási diagnózis | Elvárható eredmény | Ápolói beavatkozások |
| Táplálkozási hiba a szervezet szükségleteihez képest csökkent táplálék felvétel a nyelés képtelensége miatt | A szervezet táplálékkal való ellátása | A beteg előkészítése nasojejunális szonda lehelyezésére |
| A szervezet szükségletének megfelelő tápanyag bevitel | A táplálási terv szerinti szonda-táplálás kivitelezése | |
| A mesterséges táplálás szövődménymentes | A beteg általános állapotának folyamatos kontrollálása | |
| Testtömeg csökkenés megáll | A beteg tápláltsági állapotának követése | |
| Szorongás a szonda-táplálással kapcsolatos ismeretek hiánya miatt | Szorongás csökkentése | A beteg igényeinek megfelelő ismeretek átadása |
| Félelem a beavatkozástól, a vele járó fájdalmaktól | A beteg biztonságba érezze magát | Megnyugtató, gondos kommunikálás |
| Folyadékhiány nagyfokú kockázata...... |
5.2. Gyógytorna - fizioterápia kezelési terv
- Gyengült izmok erősítése funkcionális helyzetben az önálló fordulás tanítása.
- Nyomásnak kitett helyek feltérképezése.
- További nyomás megelőzése megfelelő pozicionálással.
- Keringésjavítás.
- Mobilizálás.
- Mellkasi fizioterápia, expectorácós technikák alkalmazása.
- Vénás torna, keringési szövődmények megelőzése.
- Az alapbetegségnek megfelelő speciális fizioterápiás kezelés.
5.3. Táplálásterápiás terv Alapja:
- A dietetikus által készített táplálási terv alapja a beteg tápláltsági és táplálkozási problémáinak, állapotának pontos ismerete, ezért minden enterális szonda- táplálásban részt vevő betegnél ezeket fel kell mérni.
- Az orvos által meghatározott táplálási módszer ismerete.
- Táplálási team tagjainak megfelelő kommunikációja.
Tartalmi elemei:
- A táplálkozási anamnézis részletes felvétele.
- Részletes tápláltsági állapot felmérése.
- Egyénre szabott napi energia és tápanyagszükséglet meghatározása.

(A napi alap-kalóriaszükséglet becslésének még elfogadott módszere: 30 kcal / ttkg )
- Enterális táplálás módja.
- A tápszeradagolás eszközeinek meghatározása.
- Alkalmazandó tápszer.
- megnevezése.
- hígítási aránya (ha a hígítás szükséges).
- A táplálás folyamatos követése, szükség esetén a táplálásterápia módosítása.
- A beteg tápláltsági állapotának kontrollálása.
- A táplálás szövődményeinek kontrollálása.
- Táplálásterápia értékelése, időszakok megjelölésével.
- Betegtájékoztatás, diétás tanácsadás, betegoktatás.
- Dokumentáció.
III. Terápia
Enterális táplálás terápia
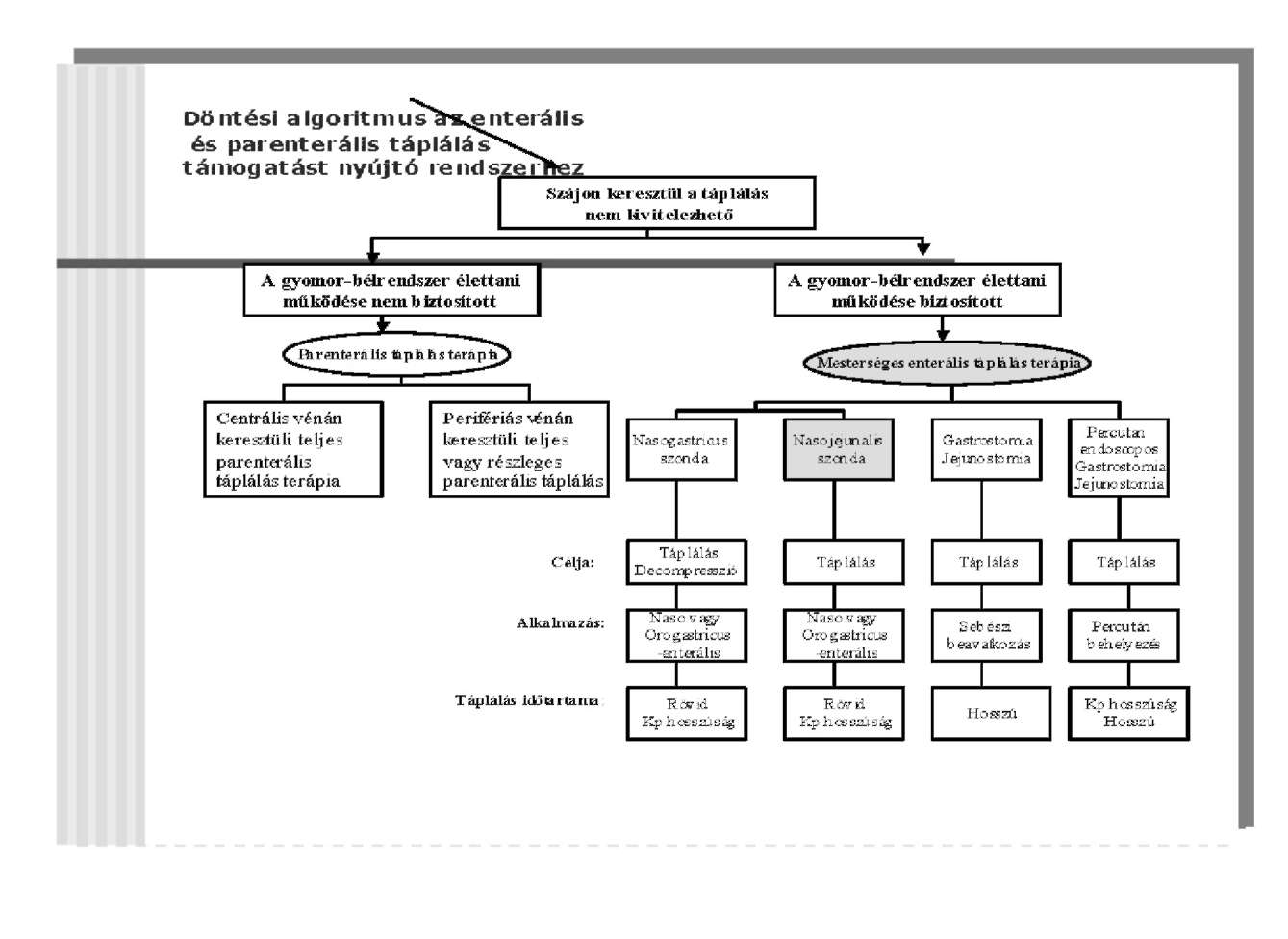
Az enterális táplálás módját orvos határozza meg a beteg alapbetegsége, az anyagcseréjénekstabilitása, a táplálkozási képtelenség időtartamának hossza, a gyomor-bélrendszer funkciója, általános állapota, tápláltsági állapota alapján. Terápiás beavatkozásnak számít a táplálásra alkalmas eszközök behelyezése, amely a megválasztott táplálási mód szerint lehet orvosi elrendelésre az ápoló függő funkciója (nasogastrikus szonda lehelyezése esetén), míg a nasojejunális szonda, PEG, PEJ behelyezése orvosi funkció.
Az enterális táplálás módjának meghatározása, amely orvosi kompetencia egyben meghatározza a táplálási stratégiát,
az alkalmazott táplálási eljárások alkalmazását valamint módosítja az ápolási tervet.
A dietetikus által készített egyénre szabott táplálási tervet be kell építeni az ápolási tervbe.
Alkalmazható enterális táplálási módok:
- Nazogasztrikus szondán keresztül bolusban vagy szakaszosan (intermittáló) történő, rövid ideig tartó
- néhány naptól-néhány héten keresztül, acut betegség esetén, standardként ajánlható táplálás,
- az aspiráció lehetőségét növeli, ezért ez a módszer kizárólag tiszta tudatú és ép reflexkörű betegek, valamint zavartalan emésztés és felszívódás esetén ajánlatos.
- Duodenális / jejunális szondán keresztül történő, 24 órán keresztül, folyamatos, de időtartamát tekintve rövid ideig tartó táplálás.
- néhány naptól-néhány héten keresztül, elsősorban acut betegség esetén
- aspiráció szempontjából veszélyeztetett, átmeneti táplálkozási tilalom eseteiben
- Entero -sztómákalkalmazásával történő táplálás, hosszú távú táplálás. -több hónap, év, főleg krónikus betegségek esetén.
- Perkután endoszkópiás gaszrosztóma (PEG) ill. PEG-Button.
- Perkután endoszkópos jejunosztóma (PEJ).
- Finomtű-katéter-jejunosztóma.
Táplálkozást támogató rendszer -Súlyos keringési elégtelenség, shock.
- A víz-elektrolit és sav-bázis háztartás fennálló súlyos zavarai.
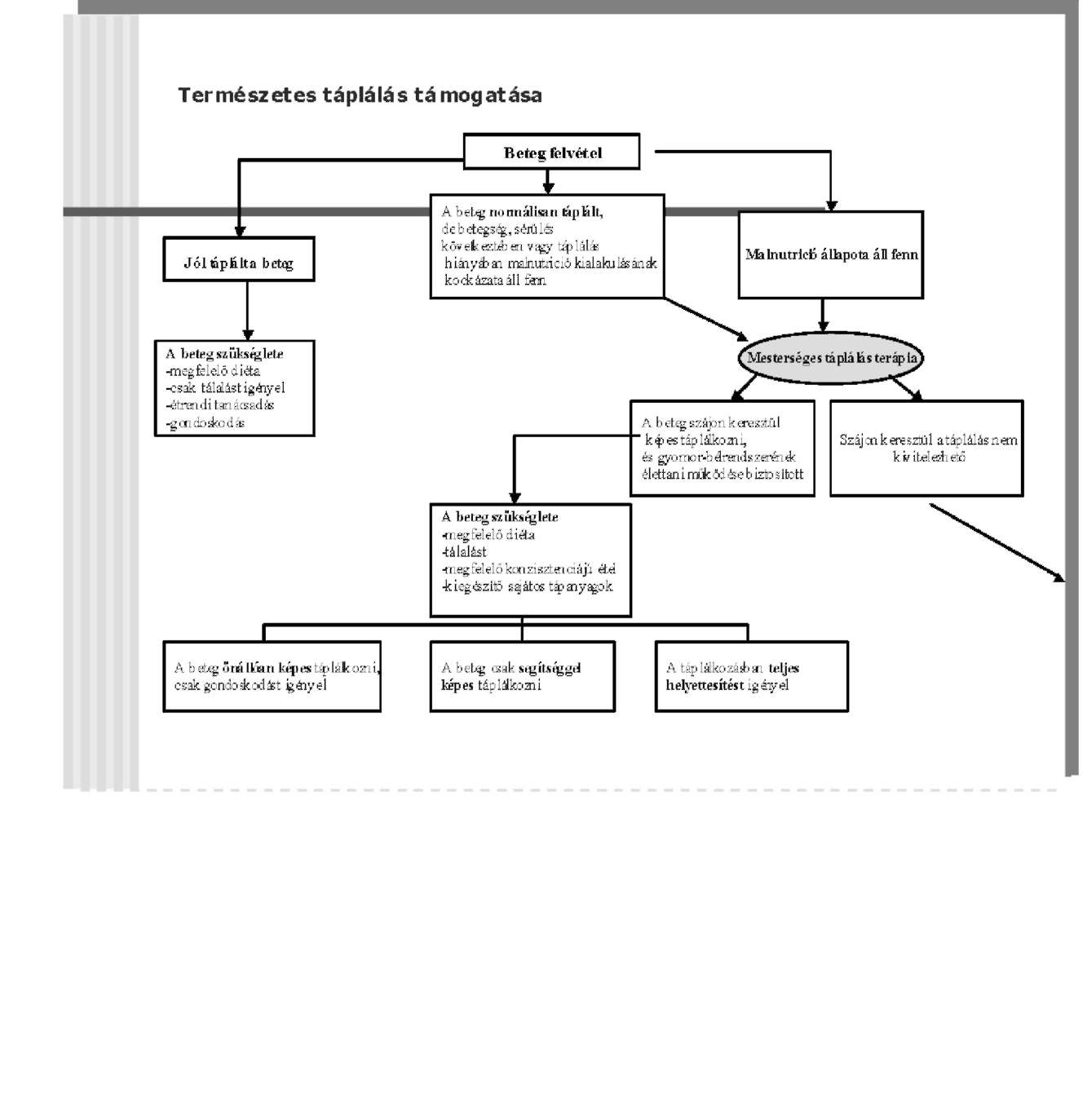
Ellenjavallatok:
- Paralitikus ileussal járó diffúz peritonitis.
- Bélelzáródás (mechanikus ileus).
- Nem befolyásolható paralitikus ileus.
- Befolyásolhatatlan hányás, hasmenés.
- Nem csillapítható vérzés az emésztőcsatornából.
- " Rövidbél" szindróma ( 30 cm-nél rövidebb bélrészlet). Relatív ellenjavallatok
- Gastro-intestinális ischémia.
- Súlyos pancreatitis ( A tudomány mai állása szerint vitatott relatív ellenjavallat).
- Magas bélsipolyok.
- Marószermérgezés.
1. Szakdolgozói tevékenységek
1.1 Általános ápolói intézkedések a tápláló eszköz le ill. behelyezésé előtt
- A beteg tájékoztatása a beavatkozás menetéről.
- Beteg előkészítése a beavatkozáshoz.
- Pszichés vezetés.
- Beteg együttműködésének megnyerése.
- Beavatkozás előtt ellenőrizni kell a beteg felvételekor készült tápláltsági állapot szűrés eredményét, a beteg általános állapotát, vitális paramétereit.
Speciális ápolási teendők a tápláló eszköz le ill. behelyezése után
- Gondoskodni kell arról, hogy beavatkozás után a beteg pár órát ágynyugalomba tölthessen.
- Kontrollálni kell a beteg általános állapotát, vitális paramétereit.
- A behelyezett tápláló eszköz megfelelő helyzetét ellenőrizni kell.
- Részvétel a táplálási terv elkészítésénél, az ápolási tervet ennek megfelelően módosítani kel.l - A táplálási terv végrehajtása.
- A beteg együttműködő képességének felmérése.
- A beteg bevonása a táplálás folyamatába.
- A táplálásnak megfelelő testhelyzetek biztosítása.
Ápolási tevékenység, beavatkozások, műveletek
- Nasogasztrikus / nasoduodenális szonda lehelyezése, táplálás céljából (szakmai eljárási leírás).
- Nasogasztrikus / nasoduodenális szondán keresztüli táplálás, szonda gondozása (szakmai eljárási leírás).
- Nasogasztrikus / nasoduodenális szonda eltávolítása (szakmai eljárási leírás).
- PEG /PEJ keresztüli táplálás, eszköz gondozása, cseréje (szakmai eljárási leírás).
- Nasojejunális szondán keresztüli táplálás, szonda gondozása (szakmai eljárási leírás).
1.2 Gyógytorna -fizioterápia
- Keringésjavítás. Vénás torna a vénás visszaáramlás segítése.
- Az artériás vérkeringés fokozása fizikai gyakorlatokkal.
- A vérkeringés fokozása svéd masszázzsal.
- Mellkasi fizioterápia: váladék mobilizálási technikák, posturális drainage, expectoratiós technikák alkalmazása.
- Légzőtorna.
- ElektrostimulációTENS-kezelés.
- Mozgásterjedelem növelés a mobilitás biztosítása érdekében.
- Manuálterápiás módszerek és lágyrész mobilizációs technikák alkalmazása.
- Célzott izomerősítés az alapbetegség függvényében.
- PNF-módszer alkalmazása a fordulás segítésére és tanítására, funkcionális izomerősítésre, stabilitás és mobilitás kialakítása az újhelyzetben.
- Progresszív ellenállásos gyakorlatok.
- Az alapbetegségnek megfelelő speciális fizioterápiás kezelés.
1.3. Táplálásterápia
Az enterális szondatáplálás általános elvei.
A tápszerek kiválasztásának szempontjai:
- A beteg táplálkozási képessége.
- Malnutrició súlyossága.
- A beteg energiaszükséglete.
- A gyomor-bélrendszer működésének esetleges zavarai.
- A táplálék felszívódás zavarainak súlyossága.
- A belek motilitási zavarai.
- A szerveket érintő funkciózavarok fennállása.
- Mióta nem táplálkozott a beteg kielégítően.
- A választott táplálási mód (gyomorba, vékonybélbe).
A tápszerek típusai:
A tápszerek a különleges /speciális szükségletet kielégítő élelmiszerek csoportjába tartoznak. Az enterális táplálásterápiában kizárólag gyárilag előállított, meghatározott tápanyag és energiatartalmú steril tápszer használható táplálásra. A szondán keresztül történő táplálást segítő korszerű eszközök alkalmazása szükséges az adekvát terápiához. Választandó tápszerek:
- Komplett, polimer ( nagymolekulájú) tápszerek.
- Szemielementális, előemésztett, kémiailag meghatározott, alkotóelemeire bontott tápszerek.
- Betegségspecifikus tápszerek.
- légzési-keringési elégtelenség eseteiben alkalmazható,
- máj működési zavarokban alkalmazható,
- veseelégtelenség eseteiben alkalmazható,
- sajátos tápanyagokkal kiegészített tápszerek.
- Egyéb tápszerek.
Tápszerek hígítása:
- Normál esetekben nem javasolt a tápszereket hígítani, hanem a megfelelő kalóriájú és osmolaritású tápszerek közül kell választani és változtatni a beteg toleranciájának megfelelően.
- Amennyiben szóba jön a tápszer hígítása a következő oldatok használata ajánlott:
- Steril Izotóniás NaCl-oldat.
- Tiszta ivóvíz - Otthoni ellátás keretein belül, gyomorba való táplálás esetén.
- Forralt, majd lehűtött tiszta ivóvíz - Otthoni ellátás keretein belül vékonybélbe való táplálás esetén.
Tápszer adagolásának módjai:
- Folyamatos adagolás.
- 24 órán keresztüli adagolás gravitációs szereléken keresztül vagy táplálópumpával.
- Szakaszos adagolás (intermittáló)
- a nap egy-egy adott időszakában folyamatos adagolás gravitációs szereléken keresztül vagy táplálópumpával
- Nagyobb adagokban (bolusokban),
- a nap folyamán több alkalommal, fecskendővel beadott tápszer.
Tápszeradagolás eszközei:
- Különböző átmérőjű, alapanyagú, hosszúságú, kiképzésű, funkciójú tápláló szondák.
- Gastrotubus.
- PEG.
- Button szonda.
- Jejunokath.
- Táplálópumpa.
- Szerelék
- táplálópumpához
- gravitációs adagoláshoz.
Folyadék és elektrolit egyensúly kontrollálása
- A napi folyadék igényt a beteg állapotához kell igazítani.
- A tápszer folyadék mennyiségét valamint az öblítő folyadék mennyiségét figyelembe kell venni a napi folyadék és elektrolit igény meghatározásánál.
- A beteg szervezetének folyadékellátottságát naponta kell ellenőrizni. (testtömeg, oedema, turgor, nyelv állapota, bevitt és ürített folyadék mennyisége).
Táplálás higiénés elvei:
- A táplálás minden tevékenységénél a higiénés szabályokat a fertőzés elkerülésének érdekében be kell tartani.
- tiszta munkaterület,
- higiénés kézmosás,
- a szerelék tiszta folyóvízzel való átmosása,
- a szonda steril fiziológiás sóoldattal való átmosása,
- bontatlan tápszerek tárolása,
- bontott, de azonnal nem felhasznált tápszerek tárolása,
- a betegbe helyezett eszköz és az azzal érintkező bőrterület folyamatos tisztántartása,
- a beteg testi higiéniájának biztosítása.
Szövődmények kontrollálása:
- A táplálás szövődményeinek kontrollálása a táplálás alatt folyamatosan történik.
- A fellépő szövődményekről a beteg kezelőorvosát haladéktalanul értesíteni kell, a táplálás felfüggesztése után. A szövődménymentes táplálás tényét műszakonként az ápolási dokumentációba fel kell jegyezni.
Táplálószondával-eszközzel kapcsolatos szövődmények
- elsődleges málpozíció (szonda eltéved a légutakban),
- különböző perforációk a levezetés alatt,
- másodlagos málpozíció (elmozdulás, kicsúszás),
- a szonda "csomósodása",
- nem szándékos eltávolítás (a beteg részéről),
- szonda elzáródása ("eltömeszelődés"),
- szonda megtöretése és áteresztése,
- a bevezetés útjainak sérülése, fertőzése, vérzése,
- a bőr és/vagy nyálkahártyák eróziója, kifekélyesedése, nekrózisa,
- sinusitis, otitis, meningitis,
- bélelzáródás (mechanikus ileus),
- vérzés.
PEG, PEJ-l kapcsolatos szövődmények
- a sztóma környékéről vérzés,
- tápszerszivárgás a sztómán keresztül,
- aspiráció,
- a sztóma környéki bőr károsodása,
- a mikroorganizmusok elszaporodása a PEG környékén,
- a szonda megtöretése,
- a szonda elzáródása.
A táplálás szövődményei
- Hasmenés.
Oka:
- a vékonybél csökkent felszívási képessége,
- a tápoldat ozmolaritása >450-500 mosm/l,
- a tápoldat túl gyors és rendszertelen adagolása,
- laktázenzim hiánya,
- a zsír emésztésének és felszívódásának zavarai,
- a tápoldat helytelenül megválasztott hőmérséklete,
- bakteriális fertőzés,
- hipoalbuminaemia,
- alkalmazott gyógyszerek mellékhatásai,
- a bél motilitásainak zavarai sugárkezelés, kemoterápia.
- Székrekedés
Oka:
- paralitikus, mechanikus ileus,
- dehidráció,
- nem megfelelő tápszer választás.
- Hányinger, reflux, hányás, aspiráció
Oka:
- tápszer túl gyors bevitele,
- a tápoldat ozmolaritása >500 mosm/l,
- fekvő illetve lejtőztetett pozició.
- Has puffadása, teltségérzet
Oka:
- laktáz enzim hiánya,
- a tápoldat túl gyors és rendszertelen adagolása.
- Akut has
Oka:
- dumping szindróma,
- pneumatosis intestinális,
- enterocolitis necrotisans,
- vékonybél-infarktus,
- egyéb szövődmények (perforációk, peritonitis). Gyógyszerek adagolása táplálószondán-eszközön keresztül:
- A tápszerrel együtt gyógyszert nem szabad beadni, ezt a táplálás előtt vagy után lehet elvégezni, a szondát gyógyszeradagolás után át kell öblíteni.
- Csak az orvos utasítására lehet gyógyszert a tápláló eszközökön keresztül bejuttatni.
- A szilárd gyógyszerformák hatása a feloldás, elegyítés után megváltozhat, ezt figyelembe kell venni. (pl. retard készítmények)
A táplálás felépítésének általános szempontjai:
- A táplálás felépítését befolyásoló tényezők ismerete
(pl. mióta nem táplálkozott/táplálták a beteget enterálisan?)
- A természetes táplálkozás megszakítás nélkül folytatható szonda-táplálással
- Az alultápláltság mértékének figyelembevétele.
(Súlyos alultápláltság esetén a jelen testtömeg az energiaszükséglet meghatározásának alapja.)
- Folyamatosan kontrollálni kell a napi energia szükségletet, ehhez mérten kell a napi tápanyag bevitelt növelni a szükséges határig, figyelembe kell venni minden esetben a beteg egyéni toleranciáját valamint a szakmai ajánlásokat.
Dokumentáció:
Célszerű az egészségügyi dokumentáció részeként egy táplálásterápiás lapot minden esetben kitölteni, a beteg személyi adatain, az ellátó hely adatain, kezelőorvos nevén kívül tartalmaznia kell a következőket:
- Felvételkor készült tápláltsági szűrés eredményét.
- A tápláltsági és táplálkozási állapot vizsgálatának eredményét.
- Napi energiaszükségletet.
- Aktuálisan és napi összesítésben a beadott tápszer mennyiségét.
- A napi folyadék és energia egyensúlyt.
- A táplálás módját.
- A tápszer adagolás módját.
- A táplálás folyamatának feljegyzéseit.
- Szövődmények ill. a szövődménymentes táplálásának tényét.
- A beteg táplálás terápiában való részvételét.
- A beteg oktatását.
1.3.1 Enterális szondatáplálás speciális elvei
Gyomorba történő táplálás nasogasztrikus szondán vagy sztóma eszközökön keresztül Táplálás felépítése:
- Egyéni toleranciának megfelelően kell emelni a tápszer adagokat.
- A táplálást fokozatosan kell felépíteni, akár bolus, akár szakaszos táplálás kerül alkalmazásra.
- A táplálási tervben meghatározott napi maximálisan bevihető, kívánatos kalóriamennyiségnek megfelelő tápszermennyiséget 24 órás napszakra, a táplálási szünetek figyelembevételével kell egyenletesen elosztani.
A táplálás fokozatos felépítésének javaslata
| Gyomorba történő táplálás felépítése | |||||
| 1.nap | 2.nap | 3.nap | 4.nap | 5.nap | |
| Gravitációs szerelékkel, pumpával | 1000 ml | 1000 ml | 1500 ml | 2000 ml | 2000ml |
| 65 ml/óra | 65 ml/óra | 70-85 ml/óra | 100-125 ml/óra | 100-125 ml/óra | |
| 21 csepp/perc | 21 csepp/perc | 23-27 csepp/perc | 32-40 csepp/perc | 32-40 csepp/perc | |
| Bolusban | 1000 ml | 1000 ml | 1500 ml | 2000 ml | 2000ml |
| 5-7x100-200 ml | 5-6x100-200 ml | 5x150-300 ml | 6 x 250-350 ml | 6 x 300-350 ml | |
- Akár szakaszosan, akár bolusban történik a táplálás, minden újabb adag beadása előtt a gyomor retenciót, ill. refluxot ellenőrizni kell.
- A tápszer beadása előtt és után a szondát át kell mosni 30-50 ml mosó folyadékkal. Szövődmények megelőzése:
- Nasogasztrikus szondán keresztül történő táplálás esetén, különös gondot kell fordítani a beteg testhelyzetére az esetleges szövődmények elkerülése miatt.
- Naponta egyszer meg kell győződni arról, hogy a sztóma nyílásban a behelyezett eszköz szabadon mozgatható.
- A behelyezett eszközt mindig tisztán, szárazon, tápszer és váladékmentesen kell tartani.
- A tápláláshoz szükséges szereléket naponként cserélni kell.
Táplálási szünetek szakaszos táplálás esetén:
- Stabil állapotú beteg esetén legalább napi 2 alkalommal >1 óra szünetet kell tartani, a gyomor megfelelően savas vegyhatásának kialakulása céljából.
- Intenzív ellátást igénylő betegek esetén 4-6 alkalommal 0,5-1 órás szünet ajánlott. Ezeket a szüneteket célszerű összhangba hoznia a betegnél elvégzendő ápolási feladatokkal (mosdatás, forgatás, mobilizálás)
1.3.2. Enterális szonda-táplálás speciális elvei
Vékonybélbe való táplálás nasoduodenális /nasojejunális szondán vagyegyéb eszközökön keresztül. Táplálás felépítése:
- Egyéni toleranciának megfelelően kell emelni a tápszer adagokat, a táplálást fokozatosan kell felépíteni. Táplálás fokozatos felépítésének javaslata
| Vékonybélbe történő táplálás felépítése | |||||
| 1.nap | 2.nap | 3.nap | 4.nap | 5.nap | |
| Gravitációs | 0,5 kcal/ml | 0,5 kcal / ml | 0,75 kcal/ml | 1 kcal / ml | 1 kcal / ml |
| szerelékkel, | 500 ml | 1000 ml | 1500 ml | 2000 ml | 2000ml |
| 8 csepp/perc | 16 csepp/perc | 24 csepp/perc | 25-32 csepp/perc | 25-32 csepp/perc | |
| Pumpával | 500 ml | 1000 ml | 1500 ml | 2000 ml | 2000ml |
| 25 ml/óra | 50 ml/óra | 75 ml/óra | 80-100 ml/óra | 100 ml/óra | |
A tápszer napi összmennyisége ne haladja meg a 2000-2500 ml-t.
- A vékonybélbe történő táplálásnál többnyire folyamatos táplálást alkalmaznak. Azonban ebben az esetben is van mód, hogy naponta két-három alkalommal igen rövid táplálási szünetet iktassanak be. Ezek a szünetek azonban egy alkalommal 5-10 percnél hosszabbra ne nyúljanak. Célszerű négy óránként átmosni a szondát. (A szünet igénye többnyire az önmagát ellátni tudó betegek esetén merül fel).
- A tápszer beadása előtt és után a szondát át kell mosni 30-50 ml mosó folyadékkal.
- A tápláláshoz szükséges szereléket naponként cserélni kell.
2. Fizikai aktivitás
2.1. Ápolói teendők a táplálás időszaka alatt a beteg fizikai aktivitásának támogatására
- Izomerő fenntartása a beteg állapotának a figyelembevételével.
- Izomerő fenntartása a beteg napi ellátásába való bevonással. (felülés, forgás, felállás, járás)
- Naponta több alkalommal, rövid séták (2-3 perctől-akár 15 percig) beiktatása.
- A családtagok bevonása a mozgás megtartásában
- A gyógytornász által előírt mozgások gyakoroltatása, elvégzésének elvárása.
- Lelki támogatás, a beszélgetés a beteg lelki erejének fokozására.
2.2. Gyógytorna, fizioterápia
- Keringésjavítás. Vénás torna a vénás visszaáramlás segítése.
- Az artériás vérkeringés fokozása fizikai gyakorlatokkal.
- A vérkeringés fokozása svéd masszázzsal.
- Mellkasi fizioterápia: váladék mobilizálási technikák, posturális drainage, expectoratiós technikák alkalmazása
- Légzőtorna.
- ElektrostimulációTENS kezelés.
- Mozgásterjedelem növelése a mobilitás biztosítása érdekében.
- Manuál terápiás módszerekés lágyrész mobilizációs technikák alkalmazása.
- Célzott izomerősítés az alapbetegség függvényében.
- PNF-módszer alkalmazása a fordulás segítésére és tanítására, funkcionális izomerősítésre, stabilitás és mobilitás kialakítása az újhelyzetben.
- Progresszív ellenállásos gyakorlatok.
- Az alapbetegségnek megfelelő speciális fizioterápiás kezelés.
3. Betegoktatás
3.1. Ápolói feladatok a betegoktatás területén
- A beteg önellátó képességének helyreállításában nagy szerepet játszik, ha képes megtanulni a tápszer adagolását, a szonda átmosását ill. a szerelék tisztántartását. Ezért minden beteg esetén fel kell mérni az együttműködési készségét, hajlandóságát a táplálásban való részvétel érdekében. Amennyiben biztonsággal megtanítható néhány folyamatra a beteg, az oktatását az ápoló vagy a dietetikus végezze el. Ebben az esetben az ápoló vagy a dietetikus külön feladata a beteg által elvégzett tevékenységek folyamatos ellenőrzése.
- A beteg otthoni ellátásra csak a megfelelő oktatás után bocsátható.
- Amennyiben a beteg várhatóan nem képes önmagát a táplálás területén ellátni, családtagot kell bevonni és oktatni erre.
- A beteg oktatás tényét mindig rögzíteni kell a beteg dokumentációjába.
- Az ápolási zárójelentés pontosan tartalmazza a beteg ill. a családtag otthon végzendő táplálással kapcsolatos feladatait, amelyet az oktatás keretén belül már megismertek.
3.2. Diétás tanácsadás
Sok esetben a szondán keresztül történő táplálás mellett a beteg fogyaszthat szájon keresztül is táplálékot. Minden esetben a kezelőorvos és a dietetikus határozza meg a fogyasztható táplálék körét, összetételét, mennyiségét, amelyet a dietetikus tanácsadás keretén belül személyesen beszél meg a beteggel / hozzátartozóval. A diétás tanácsadás tényét a beteg dokumentációjában jelölni kell.
IV. Rehabilitáció
V. Gondozás
1.1. Otthoni szakápolás
- Az otthoni mesterséges táplálás a terápia részeként kezelendő, a specifikus kezelési terv része.
- Minden esetben orvosi indikáció alapján végezhető szakfeladat, amelyet a háziorvos és a kezelőorvos szakmai irányítása alapján, dietetikus segítségével, megfelelően képzett szakápoló végezhet.
- Az ellátás feltétele, hogy a gondozást végző otthonápolási szolgálatnak a protokollban szereplő tevékenységek szakmai eljárási leírásaival rendelkeznie kell.
- A táplálást a beteg szükségleteinek pontos meghatározásával és annak megfelelően, a szakma szabályainak betartásával kell végezni.
- A táplálás felépítése a protokoll leírásai szerint, a háziorvossal, dietetikussal történt konzultáció alapján történjen.
A megfelelő színvonalú és biztonságos otthoni szonda-táplálás alapvető feltételei
- A beteg és környezetének megfelelő oktatása, betanítása, illetve ellenőrzött megbízható tudása.
- Folyamatos tápoldat- és szerelékellátás.
- Folyamatos szakmai kontroll és a különböző szakterületek biztosított információcseréje.
- A beteg számára bármikor elérhető szakmai segítség.
- Szabályozott finanszírozás. -Jogi szabályozás.
Ápolási folyamat Ápolási anamnézis
- Az ápolási anamnézist a hatályos otthoni szakápolásról szóló rendeletben szereplő dokumentáció alapján kell felvenni, kiegészítve az alábbiakkal: (ápolási és orvosi zárójelentés alapján)
- a tápláló szonda típusa, helye,
- a táplálás módja,
- a táplálás felépítésének módja,
- a kórházban elfogyasztott tápszer neve, mennyisége,
- az esetleges táplálási szövődmények.
A tápláltsági állapot felmérése
- Az ápoló a táplálás megkezdése előtt mérje fel a beteg tápláltsági állapotát
- testtömegmérés,
- testmagasságmérés,
- BMI-számítás,
- A dietetikus a táplálás megkezdése előtt végezzen részletes tápláltsági állapot felmérést
- testtömeg vesztés mértéke, jellege
- a jelenlegi testtömeg, optimális testtömegtől való eltérésének mértéke, ha a beteg ágyban fekvő és a testtömeg mérés lehetetlen:
- felkarkörfogat-mérés,
- bőr alatti zsírszövet mérése,
- izomerő mérése.
Az ellátás tervezése és dokumentáció:
- A beteg problémáinak azonosítása és a szükségletek felmérése után meg kell határozni az ápolási diagnózist/diagnózisokat, ki kell tűzni az ápolási célokat és egyéni ápolási tervet kell készíteni.
- Minden vizit alkalmával fel kell mérni a beteg állapotát és aktuális szükségleteit, és ha szükséges, új ápolási célokat kell kitűznünk
Minden vizit alkalmával rögzíteni kell az ápolási dokumentációban
- a beteg tápláltsági állapotát,
- az elvégzett tevékenységek részletes leírását,
- a beteg hogyan viselte a beavatkozást,
- a beteg és hozzátartozó tudásának mértékét,
- az egyes célok teljesülésének mértékét,
- a kezelőorvos utasításait.
Ápolói tevékenységek, beavatkozások, műveletek
Általános ápolói intézkedések
- Pszichés vezetés.
- Beteg és a család együttműködésének megnyerése.
- A szonda és a szondatáplálás elfogadásának segítése.
- A táplálásnak megfelelő testhelyzet biztosítása.
Ápolói beavatkozások, műveletek
- Nazogasztricus szonda levezetése.
- Nazogasztricus szonda eltávolítása.
- Sztómaeszköz cseréje.
- Szondatáplálás felépítése.
Gondozáshoz kapcsolódó szakápolói tevékenységek
- Nazogasztricus vagy nasojejunális szonda napi gondozása.
- PEG napi gondozása.
- Szondatáplálás bolusban.
- Szondatáplálás táplálópumpa segítségével.
- Szondatáplálás gravitációs szerelékkel.
- Gyógyszer beadása szondán keresztül.
- Szájápolás végzése.
Betegoktatáshoz kapcsolódó szakápolói tevékenységek:
- Higiénés szabályok betartatásának oktatása.
- Szonda napi gondozásának oktatása.
- Gyógyszeradás oktatása.
- Szájápolás oktatása.
- PEG-gondozás oktatása.
- Az orvos által javasolt táplálási mód oktatása.
Lehetséges szövődmények megelőzése és kezelése
- Hasmenés kezelése szondatáplált betegnél.
- Hányás kezelése szondatáplált betegnél.
- Szonda átjárhatóságának biztosítása elzáródott szonda esetén.
- A tápszerek helyes tárolása.
Eredmények értékelése
A tápláltsági állapotot az enterális szonda-táplálás elkezdése előtt, majd a táplálás folyamata alatt ( kéthetente) és a táplálás befejezésekor is el kell végezni. A kapott eredmények birtokában kell megítélni, hogy a beteg táplálása szükségleteinek megfelelő mértékben teljesült-e.
1.2 Gyógytorna fizioterápia
- Mozgás állapot felmérése.
- Egyénre szabott fizioterápiás terv készítése (adatok rögzítése).
- Fiziotherápiás beavatkozások.
- Elért eredmények értékelése.
2. Az ellátás/ápolás megfelelőségének indikátorai
Javasolt módszer a szakmai munka eredményességének értékeléséhez a táplálási folyamat meghatározott kritériumok szerinti mérése. A táplálási folyamatot átlagszámítással kapott értékkel lehet jelölni, a neve táplálási-folyamat-index.
Enterális szondatáplálás ápolás szakmai értékelése
| Enterális szonda-táplálás ápolás szakmai értékelése | |||||
| Értékelt szempontok | Értékelési szintek | ||||
| a | Az ápolási diagnózis specifikus a beteg problémáira | 3=igen | 2=részben | 0=nem | |
| b | Tápláltsági állapot felmérés megtörtént az enterális szonda - táplálás kezdetén és a végén | 3=igen | 2=részben | 0=nem | |
| c | A beteg általános állapotának nyomon követése folyamatos, dokumentált a táplálás alatt | 3=igen | 2=részben | 0=nem | |
| d | A szonda-táplálás terv szerint és kontrolláltan zajlik | 3=igen | 2=részben | 0=nem | |
| e | A táplálás kiegyensúlyozott és egyenletes ritmusú | 3=igen | 2=részben | 1=nem mérhető | 0=nem |
| f | A táplálás szövődményeinek kontrollálása folyamatosan megtörtént | 3=igen | 0=nem | ||
| g | A táplálás körülményei megfelelnek a higiénés előírásoknak | 3=igen | 0=nem | ||
| h | A beteg oktatása megtörtént a táplálásban való részvételéről | 3=igen | 1=nem mérhető | 0=nem | |
| i | A dokumentáció részletes, az információ átadásra alkalmas | 3=igen | 2=részben | 0=nem | |
Az értékelés kritériumai
3 pont=maximális megfelelés az előírásoknak
2 pont=az előírások teljesülése csak részben valósult meg
1 pont=az előírások teljesítésére a feltétel fennállt, de egyéb kizáró ok miatt az nem volt megvalósítható 0 pont=Az előírás teljesülése nem valósult meg
Az átlagszámítással kapott táplálási folyamat-index értékelése 0 = nem minősíthető a táplálás folyamata 1,5 = elfogadható minőségi szintű a táplálás folyamata 3 = megfelelő a táplálás folyamata
A táplálási-folyamat index értéke összehasonlítható a betegség kimenetelével, a szövődmények gyakoriságával, az átlagos ápolási és tápszondás napokkal, a betegek tápláltsági állapotában bekövetkező változással.
VI. Irodalomjegyzék Felhasznált irodalom
1. Csomós Ákosl dr., Ökrös Ilona dr: .,Betegséghez kapcsolódó malnutrició A terápia bizonyítékokon alapuló megközelítése Összegző dokumentum, Nutricia, 2002
2. R. Meier (Svájc), C. Beglinger (Svájc), P.Layer (Németo.), L. Gullo (Olaszo.)V. Keim (Németo.), R. Laugier (Franciao.), H Friess (Németo.), M. Schweitzer (Németo.) J. Macfie (Nagy Brittannia) Clinical Nutrition (2002)21(2) 173-8 A mesterséges táplálás helyzetének összehasonlító elemzés Nutricia, 2003;II.2-3:12-16
3. Espen vezérfonal az akut pancreatitises betegek táplálásához (konszenzus nyilatkozat)
4. Harsányi László dr.,Csapó Zsolt dr. A tápláltsági állapot felmérésének módszerei Metabolizmus 2003,1(2) 108-112
5. Mesterséges táplálás hazai helyzete. Állásfoglalás és módszertani ajánlás Orvosi Hetilap, 1977;138:2013-2016
6. Pap Ákos dr., A mesterséges táplálás a gastroenterológiai gyakorlatban In:VarróV.: Gastroenterológia Medicina Budapest, 1997p.245.
7. Télessy István dr., Vezérfonal a mesterséges enterális tápláláshoz Praxis, 1994(3)3;15-19
8. Patricia A. Potter, Anne Griffin Perry Az ápolás elméleti és gyakorlati alapja Medicina Budapest,1999
9. Varga Péter dr., Korszerű folyadékterápia és mesterséges táplálás. Medicina RT, Budapest, 1992
10. Varga Péter dr., A klinikai táplálás elmélete és gyakorlata Melania Kiadó Kft.Budapest
11. Lonovics János dr., Tulassy Zsolt dr., Varró Vince dr., Klinikai Gastroenterologia Medicina Könyvkiadó Rt. Budapest, 2003
12. Barna Mária Táplálkozás-Diéta Medicina Könyvkiadó Rt. Budapest, 1999
13. Fonyó Attila Az orvosi élettan tankönyve Medicina Könyvkiadó RT. Budapest, 2004
14. Szollár Lajos Kórélettan Semmelweis Kiadó Budapest, 2005
15. Ormai Sándor Dr Élettan-kórélettan Semmelweis Kiadó Budapest, 1993
16. Rosalinda Alfaro-LeFevre Az ápolási folyamat alkalmazása Medicina Könyvkiadó RT. Budapest, 2001
17. P. Quillin Ph.D. RD Proven and Easy-To-Follow Strategiesto Dramatically Improve quality and quantity (http://www.healthy.net/scr/Article.asphttp://www.healthy.com)
18. Európa Tanács Miniszteri Értekezletének határozata 2003 a kórházi élelmezési és táplálási ellátásról http://wcom.coe.int/rsi/CM/index.jsp
19. 117/1998. évi (VI.16.) Kormány Rendelet egyes egészségügyi ellátások visszautasításának részletes szabályairól.
20. J.Kondrup,S.P. Allison, M.Plauth Espen Guidelines for Nutrition Screening 2002. Clinical Nutrition (2003) 22/4;415-421
21. 24/2003. (V. 9.) EszCsM rendelet a speciális gyógyászati célra szánt tápszerekről
22. 1949. évi XX. Törvény az Alkotmányról
23. 1997. évi CLIV. Törvény az egészségügyről
24. Lelovics Zs., Henter I. Tápláltsági állapot minitorozása alapellátásból kórházba került betegek körében ÚjDiéta (2005) 2.24.
25. Tanulmány a gasztroenterológusok enterális táplálási szokásairól 2002. MMTT.MGT. Henter, I.Egy felmérés tanulságai ÚjDiéta, 2003/2., 14. o. és 2003/3., 14.15. o.
(A kérdőív letölthető: URL: http://www.worlductx.com/must/; magyarul: URL: http://www.nutricia.hu/asp/show_ subject.asp? id=16399&bgcl=%23f0fcc6.)
26. Butterworth, C. E. The sceleton in the hospitals closet. Nutrition, 1994,10(5), 435.441. o.
27. Beck, A. M., Balknas, U. N., Furst, P. et al. Food and nutritional care in hospitals: how to prevent undernutrition . report and guidelines from the Council of Europe. Clin Nutr., 2001,20(5), 455.460. o.
28. Beck, A. M., Balknas, U. N., Camilo, M. E. et al.: Practices in relation to nutritional care and support . report from the Council of Europe. Clin Nutr., 2002, 21(4), 351.354. o.
29. Food and nutritional care in hospitals: how to prevent undernutrition, 2002.
30. Szakmai konszenzus a betegségekhez társuló alultápláltság szűrése, felmérése és terápiája mindennapi gyakorlati kérdéseinek témakörében. Tatabánya, 2004. március 26. (URL: http:// www.diet.hu/portal/downloads /tbanya_konsz_ENG_2004.doc).
31. Kondrup,J., Allison, S. P., Elia,M.et al. Educational and Clinical Practice Committee, European Society of Parenteral And Enteral Nutrition (ESPEN): ESPEN guidelines for nutrition screening, 2002. Clin Nutr., 2003, 22(4), 415.421. o.
A szakmai protokoll érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai irányelve
A diabetes mellitus kórismézéséről, a cukorbetegek kezeléséről és gondozásáról a felnőttkorban
(1. módosított változat)
Készítette: a Belgyógyászati Szakmai Kollégium és a Magyar Diabetes Társaság
"Az irányelv-az adott klinikai állapotellátására vonatkozó,-a kiadás időpontjában rendelkezésre álló tudományos és szakmai szempontok körültekintő mérlegelésén alapuló ajánlásokat tartalmaz, melyeket az orvos/egészségügyi szolgáltató az egyedi beteg ellátásakor saját belátása szerint használhat."
Tartalomjegyzék
1. Bevezetés, alapvető megfontolások
1.1. A szakmai irányelv megújításának indoka, előzmények
1.2. A szakmai irányelv érvényességi területe
1.3. A diabetes mellitus definíciója
1.4. A diabetes mellitus hazai előfordulása
2. A diabetes mellitus diagnózisa és klasszifikációja
2.1. A diabetes mellitus diagnózisa
2.2. A diabetes mellitus klasszifikációja
3. A diabetes mellitus kezelése
3.1. Nem gyógyszeres kezelés
3.1.1. Orvosi táplálkozási terápia
3.1.2. Fizikai aktivitás
3.2. Gyógyszeres kezelés
3.2.1. Az 1-es típusú cukorbetegek kezelése
3.2.2. A 2-es típusú cukorbetegek kezelése
3.3. Pancreas- és Langerhans-sziget-transzplantáció
3.4. Vércukor-önellenőrzés
3.5. Kezelési célértékek, az ellátás megfelelőségénekindikátorai, a szakmai munka eredményességének mutatói
4. Diabeteszes krízisállapotok kezelése
4.1. Hypoglykaemiás coma
4.2. Diabeteszes ketoacidosis
4.3. Nem ketoacidoticus, hyperosmolaris coma
4.4. Lactatacidoticus coma
5. Diabeteszes micro- és macroangiopathiás szövődmények és kezelésük
5.1. Retinopathia diabetica
5.2. Nephropathia diabetica
5.3. Neuropathia diabetica
5.4. Macroangiopathia diabetica - cardiovascularis szövődmények diabetes mellitusban
6. Diabeteshez társuló kóros állapotok/kísérő betegségek kezelése
6.1. Dyslipidaemia
6.2. Hypertonia diabetes mellitusban
6.3. Thrombocytaaggregáció-gátló kezelés
7. Diabetes és terhesség
8. Diabetes és műtét
9. Gondozás, betegoktatás, rehabilitáció
10. A diabetes megelőzésének lehetőségei A szakmai irányelv érvényessége Irodalom (összegző munkák) Melléklet
Érintett társszakmákkal való konszenzus
I. Alapvető megfontolások 1. Bevezetés
1.1. A szakmai irányelv megújításának indoka, előzmények
A diabetes mellitus a XXI. század elejének egyik legjelentősebb népegészségügyi problémájává vált és előkelő helyet foglal el a nem fertőző ún. "civilizációs" betegségek sorában. Mérvadó becslés szerint a 2000-ben 171 millióra tartott cukorbetegszám (20 éven felüliek körében) 2030-ra várhatóan 366 millióra fog növekedni. A cukorbetegségnek elsősorban az esetek 90%-át kitevő, a felnőtt korban manifesztálódó, 2-es típusú változata - a jelenlegi prevalencia-adatok és a várható incidencia-növekedés, ill. a társuló cardiovascularis szövődmények folytán -világméretű gondokat okoz.
A cukorbetegség kezelése terén az inzulin felfedezése a XX. század egyik legjelentősebb orvostudományi áttörése volt: a korábban halálos kimenetelű, mai nevezéktan szerint 1-es típusú cukorbetegségben szenvedő egyének élete megmenthetővé vált. Az elmúlt nyolc és fél évtizedben az inzulinkutatás hatalmas ívet futott be, a harmincas években megjelent az NPH-inzulin, az 50-es években pedig a Lente-inzulin. A 80-as éveket a nagyfokban tisztított, monokomponens (MC) sertés inzulinok elterjedése jellemezte, míg a 90-es évek elején a humán inzulin (HM) teljes térhódítása következett be. Néhány éve rendelkezésre állnak az inzulinanalógok különböző képviselői (gyors hatású, hosszú hatású, ill. bifázisos készítmények).
A cukorbetegek oralis antidiabetikus kezelési lehetőségei az elmúlt években új hatástani csoportokkal bővültek, s a jelenlegi kutatási eredmények alapján valószínűsíthető, hogy ez a terápiás paletta az elkövetkezendő években még tovább fog bővülni.
A cukorbetegek kezelési lehetőségei nemcsak a szorosan vett, s egyre korszerűbb antidiabetikus gyógyszerek elérhetőségével, hanem a technikai újdonságok bevezetésével a gyógyászati segédeszközök és a műtéti eljárások terén is rohamosan fejlődött.
A diabetes mellitus kórlefolyásának jelentős megváltozása folytán napjainkban a klinikai gondok előterében a késői szövődmények állnak. Így a micro- és macroangiopathiás szövődmények megelőzése és kezelése a mindennapos klinikai cukorbeteg-gondozás egyik igen hangsúlyos területét képezik.
A diabetológia terén a fejlődés rendkívül intenzív és szerteágazó. A kutatás újeredményei a klinikai tevékenységünket napról-napra megújítják. Nemcsak a szorosan vett diabetológiai ténykedésünk között találhatók új terápiás lehetőségek (mind a gyógyszereket, mind a kezelési módszereket tekintve), hanem a diabetes szövődményeivel összefüggésben a határterületi tudományok újeredményei is bevonulnak a mindennapi cukorbeteg-gondozásba.
Indokolt ezért, hogy a 2005-ben írt, 2006-ban publikált korábbi szakmai irányelvet megújítva ismét összegezzük a klinikai diabetológia legújabb eredményeit. A korábbi (2005) és a jelenlegi szakmai irányelv írói azonosak. Fontos körülmény, hogy a szerzők nagyban támaszkodtak a Magyar Diabetes Társaság 2003-ban és 2004-ben megtartott, ún. konszenzus-értekezleteinek ajánlásaira, melyeket a Diabetologia Hungarica hasábjain korábban szisztematikusan közöltünk. Napjaink tényeken alapuló orvostudományának szelleme megköveteli, hogy az ajánlások mögött kellő szintű evidenciák húzódjanak meg. A szerzők ezt az elvet igyekeztek követni, s számos helyen megadják a terápiás ajánlás "A"-tól "D"-ig terjedő erősségi szintjét.
A jelenlegi szakmai irányelv a Magyar Diabetes Társaság vezetőségének jóváhagyásával, a vezetőségi tagok javaslatainak figyelembevételével készültel. A szakmai irányelveta Belgyógyászati Szakmai Kollégium jóváhagyta.
1.2. A szakmai irányelv érvényességi területe
A jelenlegi szakmai irányelv a felnőttkori cukorbeteg-ellátás szakmai kérdéseivel foglalkozik. Bár számos területen azonosság mutatkozika gyermekkori és felnőttkori cukorbetegség között, a gyermekkorban kezdődő és zajló diabetes több olyan speciális problémát vet fel, amely a gyermekgyógyászat kompetenciájába tartozik. Erre való tekintettel a jelenlegi szakmai irányelv nem érinti a gyermekkori diabetes kérdéskörét.
1.3. A diabetes mellitus definíciója
A diabetes mellitus (cukorbetegség, cukorbaj) olyan anyagcsere-betegség, amelynek központjában a szénhidrát-anyagcsere zavara áll, de a kórfolyamat következményesen érinti a zsír- és a fehérje-anyagcserét is. A cukorbetegség alapvető oka az inzulin viszonylagos vagy teljes hiánya, ill. az inzulinhatás elmaradása. Bizonyos körülmények között mindkét eltérés együttesen fordulhat elő. A cukorbaj okozta patofiziológiai eltérések számos szerv működését károsíthatják. A cukorbetegségnek ismeretesek heveny és idült (micro- és macroangiopathiás) szövődményei. A diabetes és szövődményeinek kezelése nagy terhet jelent a betegnekés a társadalomnakegyaránt.
A diabetes mellitus elnevezés - mely szószerinti fordításban édes (mellitus), bő vizelést (diabinein = túlcsordulás) jelent - arra a tünetre utal, hogy a vizeletben cukor jelenhet meg. A diabetes mellitus diagnózisának kritériumait 1999-ben tette közzé az Egészségügyi Világszervezet (WHO), Magyarországon is ezt az ajánlást követjük. A cukorbetegség csak látszólag egységes kórkép, a számos típus besorolása, rendszerezése, azaz a diabetes mellitus szindróma felosztása ugyanebben az ajánlásban található meg. A cukorbetegség klinikai tünetei nagyban függenek attól, hogy milyen típusú diabetesről van szó.
1.4. A diabetes mellitus hazai előfordulása
Hazánkban a felnőttkorban előforduló cukorbetegség gyakoriságáról - központi regiszter hiányában - megbízható adatokkal alig rendelkezünk. A térségünk külföldi adatait, a világméretű trendet tekintve hazánkban az ismert cukorbetegség gyakorisága 5,0 - 5,5%-ra becsülhető, azaz kb. fél millió magyar állampolgár szenved cukorbetegségben. E betegek döntő (90%-ot meghaladó arányú) többségének felnőttkori, 2-es típusú diabetese van. A legújabb hazai, reprezentatív szűrővizsgálat eredményei alapján a 20-69 év közötti populációban a diabetes előfordulása 8,65% volt, ami a teljes 20-69 éves populációra vetítve 7,47%-os súlyozott gyakoriságot jelent.
A 2-es típusú diabetes előfordulása az életkorral együtt növekszik, a magasabb életkorú lakosság körében az előfordulási gyakoriság elérheti a 15-20%-ot is. Napjaink jellegzetes gondja, hogy a 2-es típusú diabetes manifesztációja egyre fiatalabb életkor felé tolódik el. Ezzel összefüggésben új, korábban nem észlelt diabetes-típus, a gyermek- és ifjúkori 2-es típusú cukorbetegség észlelése már hazánkban sem számít ritkaságnak. A rossz irányú változások hátterében az elhízás és a metabolikus szindróma világméretű, látszólag feltartóztathatatlan terjedése áll.
A 2-es típusú diabetest megelőző glukózintolerancia-stádiumok (IGT: csökkent glukóztolerancia, IFG: emelkedett éhomi vércukor) gyakoriságáról hazánkban kevés adattal rendelkezünk. A hazai reprezentatív szűrés eredményei alapján a 20-69 éves populációban az IFG gyakorisága 4,88%-nak adódott (a vizsgálat éhomi vércukorérték meghatározásán alapult, így az IGT előfordulásáról adat nem volt nyerhető). Európában az IGT prevalenciája néhány országot tekintve 2,2% és 8,6% közöttinek adódott. Világviszonylatban 10% felettire tehető a diabetes és a csökkent glukóztolerancia együttes előfordulása. Ezek alapján valószínű, hogy hazánkban az IGT-ben szenvedők száma eléri az ismert diabetesben szenvedőkét. Szűrővizsgálatok általános tapasztalata szerint minden ismert cukorbetegre egy fel nem ismert diabetesben szenvedő egyén esik. Ha ezeket az adatokat tekintjük, akkor hazánkban kb. egy-másfél millió ember szenved ismert vagy ismeretlen módon diabetesben, ill. a glukózintolerancia valamely korábbi stádiumában.
A nemzetközi irodalom az IGT-t és az IFG-t együttesen prediabetesként említi, utalva arra, hogy a glukózintolerancia e stádiumai a manifeszt 2-es típusú diabetest megelőző állapotoknak tekinthetők (az állapot jelölésére használják az intermediate hyperglycemia [köztes hyperglykaemia] fogalmát is). A metabolikus szindróma nevezéktanilag nem tartozik a prediabetes közé, de jól ismert módon ez az állapot is a diabetes kórfejlődésének korai stádiumát jelenti. A metabolikus szindróma hazai előfordulásáról reprezentatív szűrővizsgálat eredményei tudósítanak: 20-69 éves populációban nők körében a gyakoriság 24,1%, férfiak körében pedig 26,0% volt (ATP III kritérium alapján).
Az 1-es típusú diabetes incidenciája napjainkban világméretekben növekszik, bár a 2-es típusú diabeteshez viszonyítva a növekedés üteme szerényebb, mert az 1-es típusú diabetes incidencia-emelkedése átlagosan csak évi 3%-ra tehető. A Magyar Gyermekdiabetes Regiszter közel 30 éves adatokkal rendelkezik, adatai a 0-14 éves populációban előforduló, 18 megyére kiterjedő 1-es típusú diabetesre vonatkoznak. E regiszter adatai szerint az 1-es típusú diabetes incidencia-növekedése hazánkban 1978-2002 között átlagosan évi 5,1% volt.
Napjaink újabb felismerése, hogy 2-es típusú diabetes klinikai képében megjelenhet a lassú kialakulású felnőttkori autoimmun diabetes (LADA) is, amelyet a diagnosztikus lehetőségek bővülésével egyre gyakrabban kórisméznek. A LADA prevalenciája a 2-es típusnak kórismézetteken belül a UKPDS adatai alapján 10-15%-ra tehető, egyes felmérések alapján a hazai gyakoriság a 2-es típusúnak tartott cukorbetegek körében hasonló nagyságrendű.
Irodalom
1. Zimmet P, Alberti KGMM, Shaw J: Global andsocietal implications of diabetes epidemic. Nature414: 782-787,2001.
2. Wild S, RoglicG,Green A, Sicree R, King H: Global prevalenceof diabetes. Estimatefortheyear 2000 and projectionsfor 2030. Diabetes Care 27:1047-1053, 2004.
3. Kerényi Zs: A diabetes mellitus epidemiológiája. In: Diabetes mellitus. Elmélet és klinikum (szerk: Halmos T, Jermendy Gy). Medicina Kiadó, Budapest, 2002. pp. 55-71.
4. Alberti G, Zimmet P, ShawJ, BloomgardenZ, Kaufman F, SilinkM:Type 2 diabetes in theyoung: theevolving epidemic: the International Diabetes Federation consensus workshop. Diabetes Care 27: 1798-1811, 2004.
5. Körner A,Madácsy L: Rising tideof type 2 diabetes mellitus and impairedglucose toleranceamong Hungarian children and adolescents. Diabetologia Hungarica 10 Suppl 2: 22-27, 2002.
6. Gyűrűs É, Soltész Gy: Az 1-es típusú diabetes mellitus incidenciája Európában, a EURODIAB adatai alapján. LAM 14: 399-404,2004.
7. Pánczél P, Külkey O, Luczay A, Bornemisza B, Illyés Gy, Halmos T, Baranyi É, Blatniczky L, Mészáros J, Kerényi Zs,Gerő L, Tamás Gy, Hosszúfalusi N, Horváth L, Madácsy L, Romics L: Hasnyálmirigy-szigetsejt elleni antitestek vizsgálata a klinikai gyakorlatban. Orv Hetil 140: 2695-2701,1999.
8. Szigethy E, Széles Gy, Vikó Z, Horváth A, Hidvégi T, Jermendy Gy, Paragh Gy, Blaskó Gy, Ádány R: A metabolikus szindróma epidemiológiája felnőtt magyar lakosság körében. Diabetologia Hungarica 16 Suppl 1: 127, 2008.
9. Jermendy Gy, Nádas J, Szigethy E, Széles Gy, Hidvégi T, Paragh Gy, Ádány R: A cukorbetegség és az emelkedett éhomi vércukor prevalenciája a hazai felnőtt korú (20-69 éves) lakosság körében: reprezentatív keresztmetszeti szűrővizsgálat eredményei. Magyar Belorv Arch 61: 203-207,2008.
II. Diagnózis
2. A diabetes mellitus diagnózisa és klasszifikációja
2.1. A diabetes mellitus diagnózisa
A diabetes mellitus kórisméjét általában a klinikai tünetekkeltette gyanú alapján, máskorszűrővizsgálat keretén belül végzett vércukor-meghatározás eredménye biztosítja.
A cukorbetegség klasszikus klinikai tünete a polyuria (a vizelet mennyiségének megnövekedése), a polydipsia (fokozott folyadékfelvétel az állandó szomjúságérzés miatt) és az egyéb okkal nem magyarázható fogyás. A fogyás kialakulhat átlagos, fokozott (polyphagia), vagy rossz étvágy mellett. Fentieken kívül a beteg panaszkodhat fáradtságra, az étvágytalanság mellett hányingerre, hányásra; ez utóbbiak már a ketosis tünetei lehetnek. Időnként homályos látás lép fel, amelyet a szemlencsének a hyperosmolaris csarnokvíz miatt megváltozott fénytörése okoz. Nőkön gyakran pruritus vulvae, férfiakon ritkán balanitis alakulhat ki. Visszatérő, nehezen gyógyuló infekciók is felhívhatják a figyelmet a cukorbajra. Olykor lábikragörcs, vagy a kézujjakon zsibbadás jelentkezik. Súlyos esetben a kialakuló hyperglykaemiás ketoacidosis vagy a nem-ketotikus hyperosmolaris állapot tudatzavarhoz, eszméletvesztéshez vezethet, és kezelés nélkül halált okozhat. Elsősorban a 2-es típusú diabetes azonban gyakran lehet tünetszegény, ilyenkor a diagnózis egy már elszenvedett szövődmény - myocardialis infarctus, stroke- kapcsán derülhet ki.
2.1.1. Vércukor-meghatározás indokolt
- Diabetesre utaló tünetek (polyuria, polydipsia, más okkal nem megmagyarázható fogyás, pruritus vulvae, balanitis) fennállása, ill. súlyos tudatzavar, vagy coma esetén.
Ez esetekben egyetlen vércukor-meghatározás eredménye diagnosztikus lehet, ugyanis ilyen esetekben a vércukor magas, s a vizeletben is cukor mutatható ki.
- Veszélyeztetett egyének (45 év feletti korúak, pozitív családi anamnézissel rendelkezők, elhízottak, hyperlipidaemiások, hypertoniások, nagy magzatot szülő nők, anamnézisben gesztációs diabetes, kórelőzményben cardiovascularis megbetegedés) esetében.
Tünetmentes egyénekesetén a diabetes kórisméjét sohasem szabad egyetlen kóros vércukorértékalapján kimondani. Követelmény, hogy ilyen esetben legalább egy további, más alkalommal történő, ismételt vizsgálat eredménye is kóros legyen.
Epidemiológiai vizsgálatok céljára azéhomi vércukor-meghatározás önmagában megfelelő lehet; ha szervezési, vagy financiális lehetőségek lehetővé teszik, az OGTT elvégzése ajánlott. Egyedi esetekben mindig OGTT végzendő, melynek kapcsán az éhomi és a terhelés után 2 órával vett vérmintából határozandó meg a vércukor értéke.
2.1.2. Diabetes mellitus állapítható meg
- Ha klasszikus tünetek figyelhető meg, és
- az éhomi (az utolsó energia-felvételt követően minimum 10 óra múlva mért) vércukorszint kóros, azaz értéke vénás plazmában, enzimatikus módszerrel meghatározva eléri, vagy meghaladja a 7,0 mmol/l értéket, vagy
- étkezés után bármely időpontban mért (random) vércukorszint eléri, vagy meghaladja a 11,1 mmol/l értéket.
- Ha klasszikus tünetek hiányában az éhomi vércukorszint értéke ismételten mérve eléri, vagy meghaladja a 7,0 mmol/l értéket.
A diagnózis megállapításához professzionális szintű laboratóriumi meghatározás szükséges. A kisméretű, hordozható, a cukorbetegek ellenőrzésére vagy önellenőrzésre használt vércukormérők mérési eredménye alapján a cukorbetegség kórisméjét megállapítani nem lehet.
2.1.3. A glukóz-intolerancia stádiumai
A szénhidrátanyagcsere-zavar stádiumait az éhomi vércukorszint és az OGTT 2 órás értéke alapján állapíthatjuk meg (1. táblázat).
2.1.3.1. Diabetes mellitus
A diabetes mellitus, tekintet nélkül a háttérben álló ok(ok)ra, három szakaszra osztható:
1. "inzulin szükséges az életben maradáshoz" (ez megfelel a korábbi inzulindependens diabetes [IDDM] csoportnak,
2. "inzulin szükséges a megfelelő anyagcsere-egyensúlyhoz - de nem a túléléshez" (ez olyan állapot, amelyben valamilyen mértékű endogén inzulintermelés még fennáll, de exogén inzulin alkalmazása nélkül nem biztosítható a megfelelő anyagcsere-állapot), és 3. "inzulinra nem szoruló periódus" (ez esetben az anyagcsere nem-farmakológiai módszerekkel, vagy orális antidiabetikus kezeléssel egyensúlyban tartható). Az utóbbi két betegség-szakasz megfelel a korábbi nem-inzulindependens [NIDDM] kategóriának.
2.1.3.2. Károsodott glukózreguláció: emelkedett éhomi vércukor (IFG) és csökkent glukóztolerancia (IGT)
A diabetes mellitus diagnosztikus kritériumát el nem érő, de a fiziológiás értékektől eltérő vércukorszintek a szénhidrát-anyagcsere enyhébb zavarára utalhatnak. Az emelkedett éhomi vércukorszint (impairedfasting glycaemia, IFG) és a csökkent glukóztolerancia (impairedglucose tolerance, IGT) a cukoranyagcsere átmeneti állapotai a normális glukóztolerancia és a diabetes mellitus között. Az IFG és az IGT egymással nem helyettesíthető fogalom. Az IFG az éhomi, az IGT pedig a postprandialis állapotnak az élettanitól való eltérését jelenti. Az IFG-t és IGT-t együttesen károsodott glukózreguláció (impaired glucose regulation) névvel jelölik. Az irodalomban az IFG és IGT együttes elnevezésére azonban a prediabetes, ill. legújabban a köztes hyperglykaemia (intermediate hyperglycemia) elnevezés is használatos.
IFG (emelkedett éhomi vércukor) állapítható meg, ha az éhomi plazma glukóz értéke 6,1 mmol/l vagy nagyobb, de kisebb, mint 7,0 mmol/l (teljes vérből történő mérés esetén e számértékek 5,6 mmol/l, ill. 6,1 mmol/l). Egyedi esetekben minden emelkedett éhomi vércukor (IFG) esetén indokolt az OGTT elvégzése. Ennek elvégzésekor a 2 órás érték alapján az adott egyén lehet IGT-s, vagy diabeteszes is, de ez utóbbi két kategóriát csak az OGTT eredménye alapján lehet kimondani. Ha a 2 órás vércukorérték normális, IFG állapítható meg, s az egyén követése ajánlott.
Meg kell jegyezni, hogy 2003 második felében az Amerikai Diabetes Társaság (ADA) az éhomi vércukor normális-kóros határát 5,5 mmol/l-re (vénás plazma érték) javasolta leszállítani, következésképpen az IFG kritériuma ezek szerint az 5,6-6,9 mmol/l közötti tartomány lenne. Az új határérték helyességét a szakirodalom erősen vitatja, s az egyelőre Európában nem terjedt el, s azt a WHO sem fogadta el. A metabolikus szindróma legújabb, 2005-ben közétett diagnosztikai kritériumrendszere azonban már tekintettel volt erre a módosító javaslatra.
IGT (csökkent glukóztolerancia) csak OGTT-vel ismerhető fel. IGT akkor állapítható meg, ha az éhomi vércukorszint < 6,0 mmol/l és az OGTT 2 órás értéke > 7,8 mmol/l,de <11,1 mmol/l (egyszerűbben kifejezve 7,8-11,0 mmol/l közötti, beleértve természetesen a két szélső értéket). Abban az esetben, ha a 2 órás érték megfelel az IGT-nek és az éhomi vércukorérték 6,1 - 6,9 mmol/l közé esik, akkor IGT + IFG együttes fennállása állapítható meg.
Az OGTT helyes kivitelezésének kritériumai
- A vizsgálatot reggel, éhomra kell végezni, előzetes (minimum 10 órán keresztüli) koplalást követően.
- A terhelést megelőző 3 napon keresztül korlátozás nélküli, de legalább 150 gramm szénhidrátot tartalmazó étrend tartása szükséges.
- A vizsgálatot megelőző napokban a terhelendő személynek átlagos fizikai tevékenységet kell végeznie.
- A vizsgálatot nyugalmi körülmények között, dohányzás és fizikai aktivitás mellőzésével kell lebonyolítani.
- A vizsgálat eredményét és értékelését esetleg befolyásoló tényezők (infekciók, gyógyszerhatások, stb.) fennállását figyelembe kell venni - egyes esetekben indokolt lehet a terheléses vizsgálat halasztása is.
- A teszt elvégzéséhez szükséges 75 gramm glukózt 250-300 ml vízben feloldva, 5 perc alatt kell elfogyasztani (gyermekek számára 1,75 gramm/testtömeg kg, de maximum 75 gramm tesztdózis ajánlott).
- A szénhidrát-anyagcsere kategorizálásához elégséges a terheléses vizsgálat 0. és 120. percében mért értéket figyelembe venni. Egyéb klinikai és experimentális célok további időpontokban történő vizsgálatot is indokolttá tehetnek.
2.1.3.3. Normoglykaemia
Élettani körülmények között az éhomi vércukorszint <6,0 mmol/és az OGTT 2 órás értéke <7,8 mmol/l.
2.1.4. A metabolikus szindróma diagnosztikai kritériumrendszere
A metabolikus szindróma és a 2-es típusú diabetes között szoros patogenetikai összefüggés van, ezért érdemes e helyen a metabolikus szindróma diagnosztikai kritériumrendszerét is megadni. Noha a metabolikus szindróma és a 2-es típusú diabetes patogenézise számos vonatkozásban közös, nevezéktanilag a két betegség nem azonos, hanem azokegy időben elnyúló kórfejlődés kezdeti (metabolikus szindróma) és végállapotát (manifeszt 2-es típusú diabetes) jelzik. A metabolikus szindróma elmélete napjainkban vitatottá vált, gyakorlati haszna azonban nem kérdőjeleződött meg. Újabban a metabolikus szindróma helyett inkább a globális kardiometabolikus kockázat elnevezés terjed el.
A metabolikus szindróma diagnosztikai kritériumrendszere az elmúlt években sokat változott, a legutóbbi (2005-ben publikált), az IDF (International Diabetes Federation) konszenzusértekezletén jóváhagyott változatot a 2. táblázat tünteti fel.
2.1.5. Teendők a diabetes mellitus kórisméjének megállapítását követően
- El kell kezdeni a diétás oktatást és - sürgősségi állapotoktól eltekintve - bizonyos időtartamú megfigyelési idő eltelte után - ha szükséges - a gyógyszeres kezelést.
- El kell kezdeni a betegnevelést.
- Célokat kell kitűzni az anyagcsere-beállításra vonatkozóan.
- Törekedni kell a diabetes mellitus korrekt klasszifikációjára.
1. táblázat. A normális glukóztolerancia és a szénhidrátanyagcsere-zavarok diagnosztikai kritériumai
| A szénhidrát-anyagcsere állapota | Glukózkoncentráció, mmol/l (vénás plazma, laboratóriumi mérés) |
| Normális glukóztolerancia: Éhomi vércukorszint OGTT 2 órás érték | < 6,0 < 7,8 |
| Emelkedett éhomi vércukor (IFG) Éhomi vércukorszint OGTT 2 órás érték | > 6,1 de < 7,0 (azaz: 6,1-6,9) < 7,8 |
| Csökkent glukóztolerancia (IGT)* Éhomi vércukorszint OGTT 2 órás érték | < 6,0 > 7,8 de < 11,1 (azaz: 7,8-11,0) |
| Diabetes mellitus Éhomi vércukorszint OGTT 2 órás érték | > 7,0 > 11,1 |
OGTT: orális glukóztolerancia teszt (kivitelezésének módja: ld. a szöveget)
* Abban az esetben, ha a 2 órás érték megfelel az IGT-nekés az éhomi vércukorérték 6,1 - 6,9 mmol/l közé esik, akkor IGT + IFG együttes fennállása állapítható meg.
2. táblázat. A metabolikus szindróma diagnosztikai kritériuma az IDF (International Diabetes Federation) ajánlása (2005) szerint
A metabolikus szindróma diagnózisának megállapításához a következő összetevők jelenléte szükséges:
Centrális obesitas (definíció szerint >94 cm-es derékkörfogat europid férfiak és >80 cm europid nők esetében, más etnikai csoportok számára a rájuk jellemző értékekkel)
mellett a következő négy faktor közül bármelyik kettő jelenléte:
- emelkedett triglycerid koncentráció: >1,7 mmol/l (150 mg/dl), vagy e kóros lipidparaméter miatt folytatott specifikus kezelés
- alacsony HDL-cholesterin koncentráció: <1,03 mmol/l (40 mg/dl) férfiak és <1,29 mmol/l (50 mg/dl) nők esetében vagy e kóros lipidparaméter miatt folytatott specifikus kezelés
- emelkedett vérnyomás: systolés érték>130 Hgmm vagy diastolés érték ?85 Hgmm vagy korábban diagnosztizált hypertonia miatt folytatott kezelés
- emelkedett éhomi vércukor koncentráció: >5,6 mmol/l (100 mg/dl) vagy korábban diagnosztizált 2-es típusú diabetes mellitus
Oralis glukóztolerancia teszt (OGTT) elvégzése kifejezetten javasolt 5,6 mmol/l (100 mg/dl) feletti éhomi vércukorértéknél, de nem szükséges a szindróma diagnosztizálásához.
2.2. A diabetes mellitus klasszifikációja
Az új klasszifikáció aetiológiai csoportosításra törekszik (3. táblázat). A diabetes klasszifikációja átlagos esetben nem okoz nehézséget. Mindig vannak azonban olyan esetek, ahol a klasszifikáció nehéz, de ebben az esetben sem szabad késlekedni a kezelés megkezdésével.
2.2.1. 1-es típusú diabetes
A béta-sejtek károsodása olyan diabetes mellitus létrejöttét eredményezik, ahol az érintett egyén életben maradásához inzulin alkalmazása szükséges. Inzulin nélkül ketoacidoticus coma, végül halál következik be. A kórkép általában klasszikus klinikai tünetekkel, zömében 35 év előtt manifesztálódik (korábbi nomenklatura: IDDM), de az életkor alapján önmagában nem lehet a diabetes típusát megállapítani. Az 1-es típusú diabetest a korai stádiumban autoimmun folyamat fennálltát jelző autoantitestek (szigetsejt-, anti-GAD-, tirozinfoszfatáz-, vagy inzulin-ellenes antitestek) kimutathatósága jellemzi. Az 1-es típusú diabetesre gyermekek és serdülők esetén a klinikai kép gyors pogresszója jellemző, bára betegségre vezető autoimmun folyamat lényegesen korábban elkezdődik. Felnőttkorban ismeretesek lassan kialakuló formák is, amelyeket latens autoimmun formaként (latent autoimmune diabetes in adults, LADA) írtak le. A genetikai sajátosságok, az autoantitest-profil és az inzulin- (C-peptid-) szekréció vizsgálata alapján a LADA nem önálló kórkép, hanem az 1-es típusú diabetes mellitus lassú progressziójú formája és ezért kórismézésekor inzulinkezelése indokolt. Klinikailag a 2-es típustól az elkülönítése nehéz lehet, dignózisában az autoantitest (GADA, ICA) kimutatása a döntő. Az 1-es típusú diabetesben szenvedők egy részénél más autoimmun betegségek (Basedow-Graves-betegség, Hashimoto-thyreoditis, Addison-kór,gluténszenzitíventeropathia) társulása is kimutatható.
Az 1-es típusú diabetesnek vannak olyan formái is, ahol a kóreredet nem ismert és nem mutatható ki autoimmun folyamat jelenléte sem. Ezeket az eseteket "idiopathiás 1-es típusú diabetes" formaként jelölik. Ez a forma gyakrabban észlelhető ázsiai, ill. afrikai származású egyénekben.
2.2.2. 2-es típusú diabetes
A diabetes leggyakoribb formája, amelyet az inzulinelválasztás és az inzulinhatás károsodása jellemez, ezek közül valamelyik kórtani folyamat az adott esetben meghatározó lehet. Típusos esetben klasszikus tünetek nélkül, elhízáshoz társulóan, 35 év felett jelenik meg (korábbi nomenklatura: NIDDM).
2.2.3 Egyéb speciális diabetes-formák
E csoportban a béta-sejt-működés genetikai zavarai (MODY, MIDD), az inzulinhatás genetikai zavarai, a pancreas exocrin állományának megbetegedéseihez társuló formák, endocrinopathiákhoz csatlakozó, gyógyszerek és kémiai anyagok kiváltotta, infekciókhoz társuló formák, ill. az immungenézisű diabetes szokatlan formái, és más, esetenként diabetesszel társuló genetikai szindrómák találhatók. A részletes felsorolás megtalálható: Diabetologia Hungarica 8 Suppl 2:1-28,2000. Egy - egy MODY (glukokináz gén mutáció) és MIDD (mitochondrialis A3243G mutáció) családot már Magyarországon is leírtak, a mutációt molekuláris genetikai módszerrel igazolták.
2.2.4 Gesztációs diabetes
A gesztációs diabetes olyan, különböző súlyosságú hyperglykaemiát okozó szénhidrátanyagcsere-zavar, amely első ízben a terhesség során kezdődik, vagy kerül felismerésre. Fogalma nem zárja ki annak a lehetőségét, hogy a glukóz-intolerancia mára terhesség előtt is fennállt, csak korábban nem került kórismézésre. A meghatározás nem tesz különbséget aszerint, hogy az állapot igényel-e inzulinkezelést, vagy sem, ill. hogy fennáll-e a terhességet követően is, vagy sem.
A terhesek általános diabetes-szűrését a terhesség 24-28. hetében indokolt elvégezni. A szűrést a 75 gramm glukózzal történő, standard oralis terhelés (OGTT) formájában kell lebonyolítani. Gesztációsdiabeteszesnek kell tekinteni azokat a terheseket, akik a WHO-feltételek alapján diabeteszesnek, vagy IGT-s állapotúnak minősülnek.
Szülés után leghamarabb 6 héttel, általános esetben ennél később, újabb OGTT végzendő, a reklasszifikáció céljából. A reklasszifikációt elősegítő OGTT eredménye lehet normális, de a terhelés utáni 2 órás értékalapján IGT,vagy diabetes is megállapítható.
A gesztációs diabetesben szenvedő terhes egy később manifesztálódó diabetes szempontjából fokozott kockázatú egyénnek tekintendő akkor is, ha a reklasszifikáció során normális glukóztolerancia állapítható meg.
3. táblázat. A szénhidrátanyagcsere-zavarok aetiológiai klasszifikációja (WHO, 1999)
| - 1-es típusú diabetes mellitus (béta-sejt károsodás következtében általában abszolút inzulinhiány áll elő) - autoimmun mechanizmusú - idiopathiás |
| - 2-es típusú diabetes (a diabetes széles tartományát átfogja, a dominálóan inzulinrezisztencián alapuló, relatív inzulinhiánnyal társuló formáktól, az elsődlegesen szekréciós zavarra visszavezethető, inzulinrezisztenciával társuló vagy anélkül megjelenő formákig) |
| - Egyéb speciális típusok |
| - a béta-sejt működés genetikai zavarai - az inzulinhatás genetikai zavarai - a pancreas exocrin részének megbetegedéseihez társuló formák |
| - endocrinopathiák |
| - gyógyszerekés kémiai anyagok kiváltotta típusok |
| - infekciókhoz társuló |
| - az immungenezisű diabetes szokatlan formái |
| - más, esetenként diabétesszel társuló genetikai szindrómák |
| - Gesztációs diabetes |
Irodalom
1. WHO: Definition,diagnosis and classification of diabetes mellitus and its complications. Report of a WHO consultation. Part 1: Diagnosis and classification of diabetes mellitus. Geneva, 1999. Magyar nyelvű szöveghű fordítása: Diabetologia Hungarica 8 Suppl 2:1-29,2000.
2. Magyar Diabetes Társaság Metabolikus Munkacsoportja (Halmos T, Hidvégi T, Jermendy Gy, Káplár M, Korányi L, Pados Gy, Paragh Gy, Zajkás G): A metabolikus szindróma definíciója, diagnosztikai kritériumrendszere és szűrése. Orv Hetil 143:785-788, 2002.
3. International Diabetes Federation IGT/IFG Consensus Statement. Impaired glucose tolerance and impaired fasting glycaemia: the current status on definition and intervention. Diabetic Med 19: 708-723, 2002.
4. Alberti G: IDF Consensus on the metabolic syndrome: Definition and treatment, presented atz 1st International Congress on Prediabetes and the Metabolic Snydorme, Berlin, 14 April 2005, available on-line: http://www.idf.org/webcast
5. Magyar nyelvű szöveghű fordítása: Diabetologia Hungarica 13: 107-112, 2005.
6. The Epxert Committee on the Diagnosis and Classification of Diabetes Mellitus: Follow-up
7. report on the diagnosis of diabetes mellitus. Diabetes Care 26:3160-3167,2003.
8. Hosszúfalusi N,Vatay Á, Rajczy K, ProhászkaZ, Pozsonyi É, Horváth L,Grósz A,Gerő L, Madácsy L, Romics L, Karádi I, Füst G, Pánczél P: Similar genetic features and different autoantibody pattern of latent autoimmune diabetes in adults (LADA) compared with adult onset type 1 diabetes with rapid progression. Diabetes Care 26: 452-457, 2003.
9. Gaál Zs, Kántor I, Somogyi A, Farkas K, Jermendy Gy, Dicső F, Valenta B: A MODY klinikai és genetikai heterogenitása. Diabetologia Hungarica 11: 261-263, 2003.
10. Pánczél P, Hosszúfalusi N, Vatay Á, Horváth L, Karczagi V, Horváth R, Bende I, Palik É, Várkonyi J, Karádi I, Romics L: Mitochondrialis génmutációhoz társuló diabetes mellitus: az első magyarországi család leírása. Diabetologia Hungarica 12:199-206, 2004.
11. Halmos T, Kautzky L, Suba I: Metabolicus syndroma. Medicina Kiadó, Budapest, 2005.
12. Després JP, Lemieux I: Abdominal obesity and metabolic syndrome. Nature 444:881-887,2006.
13. World Health Organization: Definition and diagnosis of diabetes mellitus and intermediate hyperglycemia. Report of a WHO consultation. Geneva, 2006.
14. Després JP,Cartier A, Cőté M, Arsenault BJ: The concept of cardiometabolic risk: Bridging the fields of diabetology and cardiology. Ann Med 40: 514-523, 2008.
III. Kezelés
3. A diabetes mellitus kezelése
A kezelési lehetőségek nem-gyógyszeres és gyógyszeres formákra oszthatók, válogatott esetekben kezelési lehetőségként pancreas- vagy Langerhans-sziget-transzplantáció is szóba jön.
3. 1. Nem gyógyszeres kezelés
A diabetes kezelésének három alappillére a megfelelő étrend, a napi rendszerességű fizikai aktivitás és az ezekhez adaptált gyógyszeres kezelés, ideértve az inzulinadást is. Az étrendi és a fizikai aktivitásra ("exercise") vonatkozó előírásokegyüttese az ún. "életmódkezelés". Diéta helyett ma orvosi táplálkozási terápiáról (medical nutrition therapy)
beszélünk, ami magába foglalja a makro- és mikrotápanyagok, élelmi rostok, élvezeti szerek, cukorpótszerek és helyettesítők alkalmazásával kapcsolatos megfontolások és irányelvek összességét.
3. 1. 1. Orvosi táplálkozási terápia
3. 1. 1. 1. A "diéta" szükségességének elméleti háttere
Az étrendi előírások célja az optimális anyagcsere-állapot elérése és fenntartása, a vércukorszint ideális esetben normális, de legalább biztonságos értékhatárok között tartása, a kezelés más elemei vércukorcsökkentő hatásának erősítése. 1-es típusú diabetesben -a teljes remisszió többnyire rövid szakaszától eltekintve- inzulinkezeléssel együtt, 2-es típusú diabetesben az esetek egy részében önmagában, gyógyszeres kezelés nélkül is biztosítja a kívánt glykaemiás kontrollt. Ez utóbbi diabetes-formában csupán az "életmódkezelés" önmagában nem kielégítő volta esetén szükséges a terápiát oralis antidiabeticummal és/vagyinzulin adásával kiegészíteni.
Az inzulininjekció nélkül kezelt cukorbeteg szervezetének alapproblémája egyrészt, hogy az étkezések során a vércukor szintentartásához szükséges inzulin elválasztása késve indul meg -késik a prandialis szekréció korai fázisa-, másrészt, hogy a keringésbe került inzulin az inzulinrezisztenciából adódóan nem képes hatását teljes értékűen kifejteni. Az inzulinválasz késéséből adódóan elégtelen vagy elmarad a hepatikus glukózkibocsátás gátlása is, ami tovább emeli az étkezést követő vércukorszintet. Ezért:
- kerülni célszerű a gyors vércukor emelkedést okozó ételeket,
- a napi szénhidrát- és energia-felvételt több alkalomra, inzulin nélkül kezelteken - az esetlegesen alkalmazott antidiabeticus kezelés függvényében- általában háromszori-ötszöri, inzulinnal kezelteken a készítmény típusától függően három-hatszori alkalomra javasolt elosztani,
- háromnál többszöri étkezés esetén az egyes étkezések szénhidráttartalmát fő- és köztes étkezésekre javasolt elosztani. ("B").
Inzulinkezelés alatt álló cukorbetegnek azért kell "diétáznia", mert az alkalmazott inzulinkészítmények hatásgörbéje enélkül nem fedi le a táplálékból felszívódó szénhidrátok okozta vércukor-emelkedést, mert
- az étkezést követő vércukorszint-emelkedés maximuma általában egy óra múlva alakul ki, s három órán belül rendszerint lecseng. A különböző inzulinok hatásgörbéje ettől eltérő, s a vércukorszint alakulását az étkezési (prandialis) és bázisinzulinként alkalmazott készítmények esetleges interferenciája is befolyásol(hat)ja. Humán inzulinnal (gyors hatású reguláris és közepes hatású NPH inzulinnal) történő kezelés mellett általában 6-7-szeri étkezés javasolt a táplálékfelszívódás és az inzulinok hatásdinamikájának eltéréséből adódó vércukoresések kiküszöbölésére;
- még az ún. intenzív inzulinkezelés keretei között sem védhető ki a vércukor túlzott megemelkedése nagyobb mennyiségű - 80-90 grammot meghaladó - szénhidrát egyszerre történő bevitelét követően, mert a szubkután beadott reguláris, gyorshatású inzulin nem képes olyan gyors ütemben felszívódni és olyan magas vérszintet létrehozni, mint az az egészséges szervezet esetében megfigyelhető. Bár gyorshatású inzulinanalóggal folytatott intenzív konzervatív inzulinkezelés során az alkalmanként nagyobb mennyiségű szénhidrát vércukoremelkedést okozó hatása is jobban ellensúlyozható, a nagy egyszeri szénhidrátbevitel inkább kerülendő.
- gyorshatású inzulinanalóggal (Humalog®, NovoRapid®, Apidra®) történő kezelés során -étkezési vércukorszint-szabályozó típusú (prandialis glukóz regulátor, korábban "glinideknek" nevezett) orális készítményekkel (Starlix®, NovoNorm®) kezeltekhez hasonlóan- elégséges lehet az étkezés három alkalomra történő korlátozása, feltéve, hogy összhangba hozzákaz egyes étkezések kapcsán alkalmazott adagot az elfogyasztani kívánt szénhidrát mennyiségével. Háromszori étkezés általában elegendő napi 2-3 alkalommal bifázisos analóg készítményeket kapók esetében is (ún. prandialis premix /PPT/, más elnevezéssel intenzív keverék terápia /IMT/), ritkábban azonban kis köztes étkezés beiktatása, elsősorban délelőtt, ilyenkor is szükséges lehet.
3. 1. 1. 2. Az étrend főbb szempontjai
3. 1. 1. 2. 1. Energiatartalom
Normális testsúlyú cukorbetegnek naponta annyi energiához kell juttatnia szervezetét, amennyit az - életkor, testmagasság, az anyagcsere jellemzői, a végzett napi tevékenység jellege, tartama, intenzitása függvényében -megkíván (általában 7600-10 500 kJ-t, azaz 1800-2500 kcal-t).
Súlyfelesleggel rendelkező cukorbetegekesetében az étrendnek kevesebb energiát kell tartalmaznia, mint amennyit a szervezet a testsúly állandóság érdekében megkívánna (általában 4200-6300 kJ-t, illetve 1000-1400 kcal-t).
Inzulinrezisztencia fennállása esetén már a mérsékelt fogyás is javít(hat)ja az inzulinhatást -és következményesen a glykaemiát. Az energiatartalom megszorítása a kívánt súlyleadás és/vagy a glykaemia eléréséhez önmagában rendszerint nem eredményes, csak a napi rendszerességű fizikai tevékenység-növeléssel együtt. Komplex kezelés (csökkentett energia-bevitel - <30 energia% zsír -, rendszeres fizikai tevékenység, rendszeres kapcsolattartás az érintett személlyel és környezetével, részletes életmódtanácsokra is kiterjedő edukáció) 5-7%-os testtömeg csökkenéshez vezet. 2-es típusú diabetes túlsúllyal társult eseteiben az anyagcsere akut kisiklásától eltekintve minden esetben az energia-bevitel korlátozását is magába foglaló életmódkezelés az első terápiás lépés. Idősek energiaszükséglete alacsonyabb, mint a középkorúaké.
3. 1. 1. 2. 2. Az étrend összetétele
Az egyes tápanyag összetevők optimális étrendi arányára vonatkozó előírások időről-időre változtak a korábbiakban. Ma a zsírban és fehérjében szegény, szénhidrátokban gazdag étrend ajánlott a cukorbetegség mindkét fő típusában. Ennek megfelelően 50-55% komplex, magas rosttartalmú (>30 g élelmi rost/nap) szénhidrát, 15-20% fehérje (testtömeg kilogrammonként 0,8-0,9 g), a fennmaradó hányadban zsír bevitele javasolt. Ez utóbbi tekintetében az a kívánatos, hogy a telített zsírsavak (SFA) bevitele % (de LDL >2,5mmol/l esetén <7%), a többszörösen telítetlen zsírsavaké (PUFA) ~10%, az egyszeresen telítetlen zsírsavaké (MUFA) -10-12°% (a szénhidrátok és a MUFA együttes aránya 60-70%) legyen ("A").
Az étrendi javaslat megadásánál minden esetben célszerű meghatározni a napi táplálék szénhidrát- és energiatartalmát. Egyensúlyban lévő 2-es típusú cukorbetegség esetén a fogyasztott fehérje nem növeli a vércukorszintet ("B").
Bár az alacsony glykaemiás indexű (GI) ételek étrendi hatása kedvező - a fogyasztásukat követő glykaemiás válasz alacsonyabba magas GI-ű táplálékokéval szemben -, e fogalom nehézkes használata, értékének számos tényezőtől (a készétel összetétele, konyhatechnikai feldolgozás, stb.) függő volta folytán napjaink betegoktatásában a korábbinál kisebb hangsúlyt kap.
3. 1. 1. 2. 3. Az étkezések gyakorisága
Általában gyakori - a választott antidiabeticus kezeléstől függően -, ötszöri-hatszori étkezés javasolt, de rövid hatású orális inzulinszekretagog készítményt (étkezési vércukorszint szabályozót: nateglinid -Starlix®, repaglinid -NovoNorm®), illetve gyors hatású inzulinanalógot (lizpro-inzulin -Humalog®, aszpart-inzulin -NovoRapid®, glulizin (Apidra®) kapó betegeken a napi háromszori étkezés is elég lehet.
3. 1. 1. 2. 4. Az egyes étkezések szénhidráttartalma
Általános szabály, hogy minden étkezésnek megfelelő mennyiségű szénhidrátot kell tartalmaznia. Ennek oka inzulinnal kezelt betegek esetében az, hogy ha a folyamatos inzulinhatást többször ismétlődő szénhidrátbevitellel nem ellensúlyozzák, vércukorszint-esés, hypoglykaemia következhet be. Inzulin nélkül kezelt betegeknél a gyakori szénhidrátbevitel egyrészt az inzulin-elválasztást biztosítja, másrészt, inzulin-elválasztást serkentő orális antidiabeticumot szedőkön kivédi a gyógyszer adására bekövetkező inzulinválasz esetleges vércukoresést eredményező hatását.
3.1.1. 2. 5. A vércukrot gyorsan emelő élelmiszer, ital fogyasztása
Általában javasolható, hogy a cukorbeteg cukrot, cukorral készült ételt, italt ne fogyasszon, s ez különösen érvényes a vércukrot igen gyorsan emelő cukortartalmú (üdítő) italokra. Nád-, illetve répacukrot tartalmazó ételek/italok fogyasztása vércukoresés korrekciójaként jöhet elsősorban szóba.
Bár igaz, hogy az étkezés során fogyasztott szénhidrát mennyisége fontosabb, mint annak forrása, illetve típusa, valamint, hogy a cukor és az izokalorikus keményítő utáni glykaemiás válasz diabetesben azonos a nem-cukorbetegeken észlelttel, törekedni kell a cukor más szénhidrátforrással történő helyettesítésére. Előnyben részesítendőka magas rosttartalmú zöldségek, teljes őrlésű gabonafélék, a magas korpatartalmú kenyerekés pékáruk, gyümölcsök, a sovány tejés tejtermékek ("A").
3. 1. 1. 2. 6. A "diétás" élelmiszerek
A cukorbetegeknek elsősorban nem "diétás" élelmiszereket kell fogyasztaniuk, hanem étrendjüket a mindenki számára ajánlott élelmiszerekből kell összeállítaniuk
Az édesítőszerek két nagy csoportra oszthatók: mesterséges édesítőszerekre és cukorhelyettesítő anyagokra.
Mesterséges édesítőszerek (szacharin, ciklamát, aceszulfám-K, aszpartám) és a velük készült energiamentes italok fogyasztása megengedett. Időről-időre megjelennek egyes származékok (korábban a ciklamát és a szacharin, legutóbb az aszpartám) kevéssé biztonságos voltáról szóló tudósítások, ezeket azonban adatok kellően nem támasztják alá. Nemzetközi szakértő testületek állásfoglalása alapján e készítmények szokásos napi adagú használata egészségkockázatot nem jelent.
A mesterséges édesítőszerek különböznek egymástól édesítőerejükben, esetleges mellékízt okozó hatásukban, valamint hőstabil- (ízhatását melegítést követően is megtartó), illetve-labilis természetükben. Gyakorlati jelentősége ez utóbbinak van. Hőstabil tulajdonságú a ciklamát és az aceszulfám-K, hőlabilis a szacharin és az aszpartám. Az aszpartám fényérzékeny is, s a lejárati időn túl elbomlik (a felhasználásával készült termékekédes ízüket elveszítik). Ez utóbbi vegyület fenilalanin származék, fenilketonuriában szenvedők ezért nem használhatják. A forgalomban lévő mesterséges édesítőszerek kisebb része egykomponensű, többségük azonban kombináció, amelyek élvezeti, hasznosíthatósági sajátosságai az összetevők függvényében változnak.
A cukorhelyettesítő anyagok (fruktóz, illetve cukoralkoholok: szorbit, ritkábban xylit, maltit, isomalt) és a velük készült sütő- és édesipari termékek fogyasztása - tekintettel a cukorral azonos energiatartalmukra - lehetőleg kerülendő. Ha fogyasztásukra mégis sor kerül, a napi szénhidrátmennyiségbe beszámítandó. Fruktózból a napi mennyiség ne haladja meg a 25 grammot. A szorbit >30 gramm/nap adagban hasmenést okoz ("A").
3.1.1.2.7. Élvezeti szerek fogyasztása
Kávé, tea: 1-3 -babkávéból készült- eszpresszó kávé, illetve 2-4 csésze tea naponta fogyasztható. A coffein, thein nem emeli a vércukor szintjét.
Alkoholos italok: fogyasztásukkal kapcsolatban két szempont, alkohol- és cukortartalmuk igényel mérlegelést. Az alkoholtartalom tekintetében cukorbetegekre és egészséges anyagcseréjűekre azonos irányelvek érvényesek: Nők számára naponta legfeljebb 1, férfiak részére 2 egység fogyasztása jöhet szóba. (Egy egység = 1-1,5 dl bor; 3 dl sör; 2-3 cent töményital, azaz ~ 15 gramm tiszta alkohol.). Cukorbeteg alkohoholfogyasztása csak étkezéshez kapcsoltan tanácsolható ("B"). A mérsékelt alkoholfogyasztás (napi 1-2 dl száraz -vörös- bor) a szív- és érrendszeri megbetegedések megelőzésében kockázatcsökkentő tulajdonságú ("D").
3. 1. 1. 2. 8. Mikrotápanyagok
Vitamin-, ill. ásványisó-készítmények kedvező hatása nem igazolt. Antioxidánsok rutinszerű adása nem ajánlott -szövődmények megelőzésére/késleltetésére gyakorolt hatásuk eddig nem igazolódott -, megadózisok tartós adása ártalmas.
3. 1. 2. Fizikai aktivitás
A teherbíró képességhez és az edzettségi állapothoz igazodó fizikai tevékenység az "életmódkezelés" része kell, hogy legyen. A fizikai tevékenység mértékét, intenzitását, időtartamát, formáját és gyakoriságát egyénre szabottan kell meghatározni ("A").
A mozgásprogram megkezdése előtt teljes körű kivizsgálás végzése javasolt ("D"), amelynek egyaránt ki kell terjednie az általános állapot, különös tekintettel a cardiopulmonalis terhelhetőség felmérésére, valamint a diabetes-specifikus szempontokra (esetleges szövődmények feltérképezése, különös tekintettel a mozgásszervek állapotára, neuro-, retino-, osteoarthropathia fennállására).
Általánosságban javasolható a fokozatosan növelt, kezdetben legalább heti háromszori, közepes intenzitású, alkalmanként 15-20 percig - vagy kiizzadásig - tartó tevékenység, ami fokozatosan heti 5-7 alkalommal folytatott 25-40 perces mozgásprogrammá fejleszthető. Helyes, ha e mozgásprogram 70-80%-ban dinamikus - az izomrostok hosszúságának változását eredményező, relatíve kis intramuscularis erőkifejtéssel járó -, és 20-30%-ban statikus -változatlan izomrost hosszúság, és nagy intramuscularis erőkifejtés mellett megvalósuló-, izometriás gyakorlatokból áll
A mozgásprogram alatti/utáni anyagcsere monitorozást igényel, az antidiabeticus gyógyszeres kezelés és/vagy inzulin adagjának a mozgáshoz igazodó meghatározása, vércukoresés elkerülése érdekében ("A").
A terhelés alatti munkapulzust a szubmaximális pulzusszám 50-80%-ában adjuk meg. Általánosságban elmondható, hogy a biztonságos munkapulzus 100-120/min között mozog. A 40 év feletti férfiaknál, ill. 45 év feletti nőknél intenzív mozgásprogram megkezdése előtt terheléses EKG végzése javasolt, hogy a program egyénre szabott, hatékony és biztonságos lehessen.
A fizikai aktivitás fokozása a 2-es típusú diabetes mellitus prevenciójában, a cukorbetegség mindkét fő típusa kezelésében egyaránt hasznos ("A").
3. 2. Gyógyszeres kezelés
3.2.1. Az 1-es típusú cukorbetegek kezelése
3.2.1.1. Az inzulinkezelés céljai 1-es típusú diabetes mellitusban
3.2.1.1.1. Rövid távú, minimális célkitűzés
A betegség akut tüneteinek és szövődményeinek megszüntetése és a beteg közérzetének javítása.
3.2.1.1.2. Hosszú távú célkitűzés
Lehetőség szerint a betegség felfedezésétől kezdődően (biokémiai) normo- vagy euglykaemia, az egészséges egyének vércukorszintjét leginkább megközelítő beállítás elérése és fenntartása. Ez az anyagcserehelyzet - 1-es típusú diabetesben ma már bizonyítottan - alkalmas a cukorbetegség késői szövődményeinek késleltetésére, kivédésére, egyes, már kialakult szövődmények progressziójának lassítására, sőt megállítására.
3.2.1.1.3. A közel-normoglykaemia
Bár a kockázati szinteket illetően az inzulinnal kezelt diabetesre is érvényeseka 6. táblázatban szereplő paraméterek, az inzulinkezeléssel többnyire törvényszerűen együtt járó anyagcsere-labilitásra tekintettel csupán a vércukor céltartományokon belül tartására törekedhetünk: ez éhgyomorra ideális esetben 4,0 és 6,6 mmol/l közötti, étkezés után 60-90 perccel pedig 6,0 és 8,0 mmol/l közötti értékeket jelent. Amennyiben a mért esetek legalább 70%-ában a vércukor a fenti céltartományokon belül mozog, és a HbA1c szintje sem haladja meg a 7%-ot, elfogadhatónak tekinthető az anyagcsereállapot. Még elfogadható a 7,8 mmol/l alatti éhomi és 10,0 mmol/l alatti étkezést követő vércukorszint. Az éjszakai hypoglykaemia elkerülése céljából a lefekvés előtti vércukorértéket kívánatos magasabban, 6,0-7,5 mmol/l között tartani.
3.2.1.2. Az inzulin adásának abszolút indikációi
Az 1-es típusú diabetes kórisméjének felállításakor az inzulinkezelés abszolút indikált. Ugyanígy abszolút indikált az inzulin adagolása a bármely okból létrejövő diabeteses ketoacidosisban és nem-ketotikus hyperosmolaris állapotban. A hazánkban elérhető inzulinkészítményeket a 4. táblázat sorolja fel.
4. táblázat. A betegek számára hazánkban 2008 végén elérhető inzulinkészítmények
| Készítmény | Kiszerelési forma | Előállító | Hatáskezdet | Hatástartam |
| GYORS HATÁSÚ HUMÁN REGULÁRIS INZULINOK | ||||
| Actrapid HM | penfill 3,0 ml NovoLet 3,0 ml* | Novo Nordisk | 30-45 perc | 5-6 óra |
| Humulin R | ampulla 100 E/ml patron 3,0 ml | Lilly | 30-45 perc | 5-6 óra |
| KÖZEPES HATÁSTARTAMÚ, HUMÁN, NPH-TÍPUSÚ KÉSZÍTMÉNYEK | ||||
| Insulatard HM | penfill 3,0 ml NovoLet 3,0 ml* | Novo Nordisk | 1,5 óra | 14-16 óra |
| Humulin N | ampulla100 E/ml patron 3,0 ml | Lilly | 1,5 óra | 14-16 óra |
| GYORS HATÁSÚ INZULINANALÓGOK | ||||
| Humalog | patron 3,0 | Lilly | 5-10 perc | 2,5-3,0 óra |
| NovoRapid | penfill 3,0 ml | Novo Nordisk | 5-10 perc | 2,5-3,0 óra |
| Apidra | penfill 3,0 ml | Sanofi-Aventis | 5-10 perc | 2,5-3,0 óra |
| HOSSZÚ HATÁSÚ INZULINANALÓGOK | ||||
| Lantus Lantus SoloStar** | patron 3,0 ml | Sanofi-Aventis | 20,5-23,2 óra | |
| Levemir | penfill 3,0 ml | Novo Nordisk | 14-20 óra | |
| ELŐKEVERT (BIFÁZISOS) HUMÁN INZULINKÉSZÍTMÉNYEK | ||||
| Gyors hatású rész és aránya | NPH rész és aránya | |||
| Mixtard 30 | NovoLet 3,0 ml* | Novo Nordisk | Actrapid HM 30% | Insulatard HM 70% |
| Humulin M3 | ampulla 100 E/ml patron 3,0 ml | Lilly | Humulin R 30% | Humulin N 70% |
| ELŐKEVERT (BIFÁZISOS) INZULINANALÓGOK | ||||
| Gyors hatású rész és aránya | NPH rész és aránya | |||
| NovoMix30 | penfill | Novo Nordisk | aszpart-inzulin 30% | protaminizált aszpart-inzulin 70% |
| Humalog Mix 25 | penfill | Lilly | lizpro-inzulin 25% | NPL-inzulin (protaminizált lizpro-inzulin) 75% |
| Humalog Mix 50 | penfill | Lilly | lizpro-inzulin 50% | NPL-inzulin (protaminizált lizpro-inzulin) 50% |
*A NovoLet előtöltött, használat után eldobandó adagoló toll.
** A Lantus SoloStar előtöltött, használat után eldobandó adagoló toll.
3.2.1.3 Intenzívkonzervatívinzulinterápia: ICT
Ajánlott kezelési forma a közel normoglykaemia fenntartására 1-es típusú cukorbetegségben a napjában többször adagolt inzulinnal végzett intenzív kezelés. Ily módon érhető el, hogy az inzulin aktuális vérszintje legjobban hasonlítson az egészséges hasnyálmirigy inzulin-elválasztási dinamikájához, minimálisra csökkentve a hypoglykaemia veszélyét.
3.2.1.3.1. Az intenzív inzulinkezelés fogalma
Az intenzív inzulinkezelés olyan többkomponensű kezelési rendszer, amelynek célja az egyes étkezések, valamint az étkezés-mentes napszakok ideális inzulinszükségletének biztosítása, napjában többször adott inzulin segítségével. Végrehajtásában egyaránt részt vesz a beteg és az őt irányító egészségügyi csapat. A rendszer elengedhetetlen része a rendszeres vércukor-önellenőrzés, valamint azon ismeretek megtanítása és elsajátítása, amelyek lehetővé teszik egy előzetesen beállított alaprendszer életstílusnak és élethelyzeteknek megfelelő, rugalmas alkalmazását. A betegnek tudnia kell inzulinját tervezett mozgásának, étkezési rendjének megfelelően előre szabályoznia. Ismernie kell teendőit különböző élethelyzetekben. Az intenzív inzulinkezelés ennek megfelelően javítja az életminőséget, biztosítja az egészséges életmódot folytató nem cukorbeteg egyén szokásaihoz hasonló napi ritmus követését.
3.2.1.3.2. Az intenzív inzulinkezelés alkalmazásának feltételei
- Személyi feltételek:
- a kezelést irányító team: a diabetológus orvos, az oktatónővér, a dietetikus, a pszichológus,
- megfelelő ismeretek az ICT alapjairól, alkalmazásáról,
- a beteg motiválása,
- oktatás csapatmunkában, a beteg (és családja) pszichés támogatása mellett, probléma esetén a team valamelyik tagja - legalább telefonon - mindig elérhető legyen a csapat egyenrangú tagjaként kezelt beteg számára.
- Tárgyi feltételek:
- a vércukor-ellenőrzés eszközei,
- a beteg motivációját és flexibilis életvitelét segítő inzulint adagoló eszközök,
- a megfelelő inzulinkészítmények.
3.2.1.3.3. Az ICT alkalmazásának korlátai
- Meggondolandó az ICT alkalmazása olyan betegeknél, akik alkalmatlanok a szükséges tudásanyag megtanulására, alkalmazására, nem hajlandók vagy nem képesek rendszeres vércukor-önellenőrzésre.
- Kérdéses a használata azon esetekben is, ahol az egyén azonos rend szerint él, vércukor- és HbA1c-értékei elfogadhatók és így az intenzív kezeléstől sokoldalú előny nem várható.
3.2.1.3.4. Az intenzív inzulinkezelésben alkalmazott inzulinadási rendszerek
- Napjában egyszeri humán, intermedier, NPH-típusú inzulin lefekvés előtt, az étkezésekelőtt gyors hatású reguláris inzulinnal kombinálva. Ilyenkora főétkezéseket megelőzően beadott gyors hatású reguláris inzulin biztosítja az adott
- 5-7 órás - napszak bazális inzulin szükségletét is (reggel általában 8-14 NE, délben 6-12 NE, késő délután 8-14 NE gyors hatású inzulin, lefekvéskor adott 8-14 NE intermedier inzulinnal kiegészítve).
- Napjában kétszer - reggel és lefekvés előtt - egyaránt sor kerülhet intermedier humán inzulinkészítmény alkalmazására. Ilyenkor az étkezésekelőtt kevesebb gyors hatású reguláris inzulin adására szorul a beteg (reggel 6-10, délben 4-6, késő délután 8-12 NE, reggel 10-16, illetve lefekvés előtt 8-14 NE intermedier humán inzulin adagolása mellett). Ez utóbbi rendszer főként a kisebb postprandialis vércukorválasszal reagáló betegekesetében alkalmazható sikeresen. Külön előnye, hogy a-főként déli-étkezés időpontja viszonylag tág határok között változtatható. Az esetek kisebb hányadában harmadik (ebéd előtt alkalmazott) intermedier humán inzulin is szükségessé válhat a vacsora előtti vércukor-emelkedések kivédésére. Ilyenkora reggeli intermedier humán inzulin adagja csökkentendő és reggel 6-12, délben 2-6, lefekvés előtt 8-14 NE intermedier humán inzulin adagolható.
3.2.1.3.5. Az inzulinanalógok alkalmazása ICT során
3.2.1.3.5.1. Gyors hatású inzulinanalógok
A jelenleg Magyarországon is forgalomban levő, gyors hatású inzulinanalógok, a lizpro- inzulin (Humalog®), az aszpart-inzulin (NovoRapid®), ill. a glulizin (Apidra®) reguláris gyors hatású inzulin helyett történő alkalmazása az alábbi esetekben javasolható ICT rendszerekben:
- Amennyiben a korábban alkalmazott ICT során humán inzulin adása mellett nem volt biztosítható megfelelő anyagcserehelyzet (HbA1c<7,0%), ill. a postprandialis vércukorérték ismételten meghaladta a 10,0 mmol/l értéket; vagy dokumentáltan gyakori, tünetekkel járó hypoglykaemia jelentkezett;
- A betegség remissziós fázisa esetén a főétkezésekelőtt adva, lefekvéskor adott bázis inzulinnal kombinálva;
- Jelentős, egyéb módszerekkel nem befolyásolható postprandialis vércukor-emelkedés esetén, napjában kétszer (háromszor) adott, NPH-típusú bázis inzulin mellett.
- Mivel ezen inzulinok adása esetén közti étkezés nem szükséges, így az étkezések számának csökkentése -testsúlycsökkentési célzattal vagy rendszertelenebb életmód miatt - relatív indikációt képez.
- Bázisinzulinként hosszú hatású inzulinanalógot alkalmazó betegekben a főétkezésekelőtt adva.
3.2.1.3.5.2. Hosszú hatástartamú inzulinanalógok
Amennyiben az ICT részeként hosszú hatástartamú inzulinanalógot (glargin [Lantus®] ill. levemir [Detemir®]) alkalmazunk, a 3.2.1.3.4. pont első bekezdésében leírt arányok változnak: az általában ugyancsak este, lefekvés előtt adott hosszú hatású inzulinanalóg optimális esetben az alkalmazott teljes inzulinmennyiség 50-55%-át teszi ki, a napközben adott gyors hatású inzulinok egymáshoz viszonyított arányai nem változnak. Hosszú hatástartamú inzulinanalóg mellé prandialis inzulinként bármelyik gyors hatású inzulinanalóg adható. Jelenleg glargin (Lantus®) ill detemir (Levemir®) az alábbi esetekben alkalmazható:
- Amennyiben a korábban alkalmazott ICT során humán inzulin adása mellett nem volt biztosítható megfelelő anyagcserehelyzet (HbA1c<7,0%), vagy dokumentáltan gyakori, tünetekkel járó hypoglykaemia jelentkezett.
3.2.1.4. Egyéb inzulinkezelési formák
3.2.1.4.1. Konvencionális inzulinkezelés, előkevert inzulinok alkalmazása
A konvencionális inzulinkezelés-amelyen ma a napi kétszeri inzulinadást értjük-az 1-es típusú diabetes kezelésében teljesen háttérbe szorul, minthogy a jellemzően nagy napi vércukor-ingadozások kiküszöbölésére, a kívánt normoglykaemia biztosítására kivételes esetektől eltekintve nem alkalmas. Kielégítő eredménnyel csak a vércukor rendszeres mérésével bizonyítottan stabil anyagcsere-helyzetű, rendszeres életmódot folytató, korábban így kezelt betegekben alkalmazható. Ezen kivételes esetekben reggel és este alkalmazott gyors és intermedier hatástartamú készítmények keveréke - a beteg által kombinált, vagy gyárilag "előkevert", ún. premix készítmény - jelenti a legelterjedtebb konvencionális kezelést. A reggeli és esti inzulinadagok aránya 2:1, vagy 3:2, az alkalmazott keverék leggyakrabban 20-30% gyors, és 70-80% közepes hatástartamú inzulin. Gyárilag előkevert humán inzulinként jelenleg a Humulin® M3 (30% gyors, 70% intermedier hatástartamú inzulin) áll rendelkezésre.
3.2.1.4.2. Inzulinanalógot tartalmazó előkevert inzulin adása
Hazánkban a NovoMix® 30 Penfill, a Humalog Mix25® és a Humalog Mix50® inzulinkészítmények vannak forgalomban. A Novomix® 30 gyors hatású analóg komponense az aszpart-inzulin, elhúzódó komponense pedig az aszpart-inzulin protaminizált változata. A Humalog Mix25® és Humalog Mix50® esetében a gyors hatású analóg komponens a lizpro-inzulin (25%, illetve 50%), míg a bázis komponens az NPL (lizpro-inzulin protamin szuszpenzió) (75%, illetve 50%). Fő alkalmazási területük a 2-es típusú diabetes, 1-es típusú cukorbetegségben használatukra inkább csak kivételként kerülhet sor.
3.2.1.5. Inzulinpumpa-kezelés
Világszerte elfogadott, speciális, intenzív kezelési mód az inzulinadagoló készülék (pumpa) használata. Hazánkban közel 1300 beteg alkalmazza.
Az inzulinpumpa-kezelés az inzulinterápia korszerű módszerét jelenti. Az inzulinpumpa elemmel működő elektromechanikus szerkezet, amely tartállyal rendelkezik az inzulinpatron számára, és folyamatosan adagol gyors hatású inzulinanalógot a bőr alatti szövete. Rendkívül fontos leszögezni azt, hogy a nagyon hatékony technikai összetevők mellett az inzulinpumpa nem automatizált eszköz. Mind a bazális, mind a bólus inzulin beadásának mennyiségét a páciens döntésétől függően, az önellenőrzés eredményei alapján kell meghatározni. A kanült 2-4 naponta cserélni kell.
Az inzulinpumpa-kezelés előnyei:
- kevesebb és kevésbé súlyos hypoglykaemia fordul elő
- a vércukorértékek variabilitása csökken
- a terhesség korai szakában a vércukorértékek és a szénhidrát-anyagcsere könnyebben kezelhető (pl. hyperemesis estén)
- az inzulinhatás reprodukálása könnyebb
- az inzulin-hatásprofil 24 órás változásának élettanihoz közelítő megvalósítása lehetséges
- életminőséggel kapcsolatos előnyök
- flexibilisebb életmód (a napi aktivitások megszervezése, nem várt események pl. fizikai aktivitás, több étkezés)
- kevesebb inzulin-injekció
- burn-out szindróma esetén a beteg számára segítség jelent Az inzulinpumpa-kezelés indikációja:
1-es típusú diabetesben szenvedő (a diabetes típusa az egyértelmű klinikai kép, ill. annak hiányában az éhomi C-peptid érték <0,5 ng/ml] alapján állapítandó meg) cukorbeteg számára, akinek diabetes-tartama 18 év feletti kezdet esetén minimum 3 év, 18 év alatti kezdet esetén minimum 1 év), ha más, korszerű inzulinnal, eszközzel, napi többszöri inzulininjekcióval,jól végzett intenzív inzulinkezeléssel (ICT) az optimális edukáció, a diéta korrekt betartása ellenére
- a HbA1c-érték ismételten >7,0% (prekoncepcionális gondozás során >6,5%) és
- a napi vércukor-ingadozás jelentős (a minimális és maximális érték közötti különbség >10,0 mmol/l), vagy
- hajnali jelenség igazolható (reggeli éhomi vércukor ismételten >8,0 mmol/l), vagy
- gyakran (havonta legalább 3 alkalommal) észlelhető klinikai tünetekkel járó hypoglykaemia, vagy
- a hypoglykaemia-érzet csökkenése-elvesztése dokumentálható (beharangozó tünetek nélküli súlyos hypoglykaemia [vércukor <3,0 mmol/l] legalább 1 ízben 6 hónap alatt)
Életkortól és diabetes-tartamtól függetlenül az inzulinra való érzékenység olyan kirívó esetében (elsősorban csecsemő- és kisgyermekkorban), ahol a hagyományos eszközökkel történő legkisebb adag inzulin (0,5 E), vagy az ennyivel történő adagváltoztatás túlzott hatást eredményez.
Inzulinpumpa-kezelés nem ajánlott:
- súlyos fogyatékosság fennállásakor (érzészavar, alapvető kézügyesség hiánya, a véralvadás-zavarai, stb.),
- pszichés ellenállás esetén: a diabetes tényének elutasítása, az önellenőrzés képtelensége, vagy elutasítása,
- ha rossz, vagy nem elegendő az együttműködés a gondozó csoport és a páciens között,
- társuló súlyos pszichiátriai kórképek esetén,
- a szociális támogatás (család, barátok) bizonytalansága; analfabétizmus esetén.
Napjainkban pumpainzulinként gyors hatású inzulinanalógok használatosak. Az inzulinpumpa hazánkban pumpaközpontokban áll a betegek rendelkezésére, egyedi igény alapján a készülék beszerzése társadalombiztosítási támogatásban részesül.
3.2.1.6. Vércukor-önellenőrzés, mint az inzulinkezelés előfeltétele
A vércukor-önellenőrzés során mindig tendenciákat, vércukorpárok egymáshoz viszonyított viselkedését vizsgáljuk, legalább 2-3 napon, szerencsésebb módon 4-5 napon keresztül. Ha az egyes inzulinbeadási időpontokban mért vércukorértékek az adott inzulin hatásának végén emelkedő tendenciát jeleznek, a megfelelő időtartam kivárása után az adagot 1, maximum 2 NE-gel emelni lehet, az alaprendszer felépítését célozva. Ha a trend ismételten csökkenő, vagy a beadások között hypoglykaemiás epizódok jelentkeznek, az adott inzulin mennyisége a kívánatosnál több, ezért azt csökkenteni kell.
Az alaprendszer beállítását nemcsak az inzulinok adásakor mért vércukorérték-párok (algoritmusok), hanem a vércukor étkezést követő emelkedését (főétkezések előtt, valamint egy-másfél órával utána mért értékek) vizsgáló algoritmikus szabályozók, vagy a lehetséges hypoglykaemia kizárására szolgáló hajnali meghatározások is befolyásolják. Stabilan felépített rendszer mellett is elengedhetetlen a vércukor rendszeres mérése.
A vércukor-önellenőrzéssel a 3.4 fejezet külön foglalkozik.
3.2.1.7. Az inzulinkezelést befolyásoló tényezők
Az inzulinkezelés, különösen az ICT beállítása és alkalmazása során ismernünk kell azokat a - részben a betegtől független, részben a beteg szokásain, viselkedésén alapuló - tényezőket, amelyek a kezelést befolyásolhatják. Ilyen -betegtől független - kezelést befolyásoló esemény pl. a meteorológiai fronttevékenység. A kettős fronthatás, vagy a labilis melegfront hypoglykaemiához, egyes hidegfrontok hyperglykaemiához vezethetnek. Ismerni kell a menstruációs ciklus inzulinigényt módosító hatását (a premenstruumban az inzulinigény jelentősen növekszik, a peteérés idején csökken), a hajnali jelenség (dawn phenomenon), vagy a szezonális inzulinigény-változások hatását az adott betegben.
- A hajnali jelenség kezelésében a Semilente MC® inzulin piacról történt kivonását követően hosszú hatástartamú inzulinanalóg adása javasolt.
- Somogyi-hatás: hypoglykaemiás vagy ahhoz közeli - esetenként meg nem érzett - vércukorértékek mintegy 6 óra múlva és 12-72 órán keresztül tartó ellenregulációt válthatnak ki a szervezetben, jelentős hyperglykaemiás értékeket eredményezve. Ha nem ismerjük fel e magas vércukorértékek okát, vagy nem megfelelően (túl)korrigáljuk azokat, az inzulincsökkentés elmaradása, vagy az inzulinemelés jelentős labilitáshoz vezet.
A kezelés eredményességének ellenőrzésére rendszeres minőség-ellenőrzést (HbA1c, vérzsírok, vesefunkciók, albuminürítés, a szem, a láb vizsgálata, az autonóm és perifériás idegrendszeri funkciók, vérnyomás, pulzus vizsgálata) kell végezni.
3.2.1.8. Speciális diabetesformák, helyzetek, állapotok kezelése
A rendkívül labilis pancreas-diabetesben, valamint veseelégtelenség inzulinkezelése során, a két bázison alapuló rendszer használata - interferencia és így nagyobb hypoglykaemia veszély miatt - nem javasolt.
3.2.1.8.1. A pancreas-diabetes kezelése
Pancreas-diabetes esetén az első kezelési lépés az adekvát diéta - amennyiben alkoholos eredetű, teljes absztinenciát javasolva. Figyelembe véve a béta-sejtek fennálló és várható lézióját, a diéta elégtelensége esetén orális terápia helyett idejekorán inzulinkezelést kell kezdeni. Mivel a táplálék felszívódása kiszámíthatatlan, az állapot labilis, így a főétkezések előtt adott gyors hatású inzulin - lefekvéskor adagolt bázis inzulin rendszer a választandó, rendszeres önellenőrzés mellett. Terápiástörekvéseinketa hasnyálmirigy-enzimek megfelelő szubsztitúciójával kell kiegészíteni.
3.2.1.8.2. Veseelégtelenség
E betegekesetében az inzulin elhúzódó kiválasztása miatt kezdetben a főétkezésekelőtt adagolt gyors hatású inzulin, lefekvés előtt adott intermedier inzulinnal megfelelő anyagcsere-egyensúlyt biztosíthat. Szem előtt kell tartani az inzulinigény nagyarányú csökkenését. A későbbiekben - a veseelégtelenség előrehaladásával - napjában többszöri gyors hatású inzulint adagolva, többnyire bázis inzulin nélküli kezelési rendszert kell alkalmazni. Értelemszerűen a dialízisre szoruló cukorbeteg kezelése csupán a nephrológus szakorvossal együttes csapatmunkában képzelhető el.
3.2.1.8.3. A frissen felfedezett 1-es típusú diabetes kezelése
Frissen felfedezett diabetes esetén már a kezdet kezdetén is célszerű az ICT bevezetése, hiszen ez a periódus az intenzív motiváció és edukáció időszaka. A remissziós fázis is kezelhető ICT-vel, az adagokat fokozatosan csökkentve, esetenként egyes, a normoglykaemia fenntartásához átmenetileg szükségtelen inzulinadásokat kihagyva.
3.2.1.9. Orális antidiabetikumok az 1-es típusú diabetes kezelésében
Az orális antidiabetikumok az 1-es típusú diabetes kezelésében alárendelt jelentőségűek és csak az inzulinkezelés kiegészítéseként alkalmazhatók. Szulfanilureák, glinidek, tiazolidindionok (glitazonok) és inkretinhatáson alapuló készítmények adása egyáltalán nem javasolt. Amennyiben a klinikai adatok inzulinrezisztencia fennállására utalnak -ami hazai adatok szerint is gyakori az 1-es típusú diabetesben szenvedőkben - metformin adása indokolt lehet. A postprandialis vércukor-emelkedés mérséklésére az akarbóz 1-es típusú betegekben is alkalmas, noha napjainkban ilyen esetben egyre inkább gyors hatású inzulinanalógot választunk.
3.2.1.10. 1-es típusú diabetes kezelése: evidenciák, ajánlások összefoglalása
- A tartósan jó anyagcsere-helyzetre való törekvés (alacsonyabb HbA1c-érték biztosítása)
- számottevően csökkenti a microangiopathiás szövődmények kialakulásának és progressziójának kockázatát,
- rövid távon szerény mértékben, hosszabb távon azonban értékelhetően csökkenti a macroangiopathiás szövődmények kialakulásának és progressziójának kockázatát, ezért e betegekben intenzív konzervatív inzulinkezeléssel / pumpakezeléssel tartósan közel-normoglykaemia biztosítására kell törekedni ("A").
- A jobb anyagcserehelyzetnek a micro- és macroangiopathiás szövődmények progresszióját előnyösen befolyásoló hatása az intervenció után évekkel is kimutatható ("A").
- Az inzulinkezelés kockázatát a hypoglykaemia és a testsúlygyarapodás jelenti. Lokális szövődmény (allergia, infekció) jelentkezése igen ritka. Intenzív inzulinkezelés mellett a hypoglykaemia kockázata 3x nagyobb, mint konvencionális inzulinkezelés mellett. Az intenzív inzulinkezeléssel elért HbA1c-érték inverz összefüggést mutat a hypoglykaemia kockázatával.
- Gyors hatású inzulinanalógok adása mellett az étkezést követő vércukor-emelkedés jóval kisebb mértékű, a hypoglykaemiák száma csökken ("A").
- A gyors hatású inzulinanalógokat tartalmazó rendszerek bármely diabetes-típusban és bármely életkorban előnyösen alkalmazhatók, arra alkalmas betegek esetében, a rendszereket megfelelően alkalmazva ("A"). Terhesség esetén az egyes készítmények alkalmazási előirata követendő.
- Pumpainzulinként a gyors hatású inzulinanalógok hatásosnak bizonyultak ("A").
- A diabetes remissziós fázisa kivételével gyors hatású inzulinanalógot csak megfelelő bázisinzulinnal (1-es típusú diabetes esetén régebben olykor 3-4-szer adott NPH-típusú inzulinnal, újabban napjában egyszer adott glarginnal (Lantus®), ill. egyszer vagy kétszer adott levemirrel [Detemir®]) együtt lehet hatásosan alkalmazni ("A"). -Optimalizált kezelési algoritmusokat alkalmazva ilyen rendszerek mellett a humán inzulint tartalmazó rendszerekhez viszonyítva hasonló javulás érhető el, flexibilisebb életvitel mellett ("A").
- Az új, hosszú hatású, napjában egyszer (glargin [Lantus®]), ill egyszer vagy kétszer detemir [Levemir®]) adott inzulinanalóg + napjában többször adott gyors hatású inzulinanalóg adása jobb beállítást eredményezhet, mint a hagyományos, humán bázis-bólus kezelési rendszer.
- A hypoglykaemia kockázatát az inzulinanalógok (humán inzulinhoz viszonyítva) csökkentik ("A").
- A testsúlygyarapodás detemir (Levemir®) mellett a legkevésbé kifejezett, egyes esetekben szerény testsúlycsökkenés is remélhető ("A").
3. 2. 2. A 2-es típusú cukorbetegek kezelése
3. 2. 2. 1. Orális antidiabeticumok
A 2-es típusú diabetesben szenvedők oralis antidiabeticus kezelését akkor indokolt elkezdeni, ha az étrendi és életmódbeli tanácsok (orvosi táplálkozási terápia és a fizikai aktivitás, közös, újkeletű névvel: életmódkezelés) következetes megvalósítása önmagában nem vezet eredményre. A jelenleg legelfogadottabb, az Amerikai (ADA) és az Európai Diabetes Társaság (EASD) közös, legutóbb 2008. végén megújított nemzetközi ajánlása akut anyagcserekisiklás (éhomi vércukor >13,9 mmol/l, random vércukor ismételten >16,7 mmol/l, HbA^ >10,0%, ketonuria és/vagy cukorbetegségre jellemző karakterisztikus tünetek fennállása) kivételével intenzív életmódkezelés és metformin egyidejű alkalmazását javasolja. Egyéni mérlegelés alapján megengedhető azonban előbb életmódkezelés alkalmazása és metformin kiegészítő adásának másodikként történő bevezetése akkor, ha az intenzív életmódkezelés önmagában 6-8 hét elteltével sem biztosítja a kívánt glykaemiás kontrollt. Akut anyagcserekisiklás esetén inzulin alkalmazandó, s az anyagcserehelyzet rendezése után lehet mérlegelni más kezelés esetleges alkalmazását.
A ma klinikai használatban álló gyógyszerek két nagy csoportba sorolhatók:
- vércukorcsökkentő hatásukat az inzulinhatás javítása útján biztosítók (ún. antihyperglykaemiás, monoterápiában nem hypoglykaemizáló szerek):
- a szénhidrátok felszívódásának csökkentése útján hatók (akarbóz /Glucobay®/);
- metformin (Adimet®, Gluformin®, Meforal®, Meglucon®, Merckformin®, Merck-formin XR®, Metfogamma®, Stadamet®, valamint a hatóanyagot kombinációkban tartalmazó készítmények: ld. később). Az ugyancsake csoportba, a biguanidok közé tartozó buformin (dibutylbiguanid, Adebit®) bár még forgalomban van, mára túlhaladottnak tekinthető, újkezelésként való alkalmazása nem javasolt;
- tiazolidindionok - szoros értelemben vett inzulinérzékenyítők (insulin sensitisers)-(rosiglitazon /Avandia®/, pioglitazon /Actos®/, valamint a hatóanyagokat kombinációkban tartalmazó készítmények: ld. később).
- az inzulinelválasztást serkentő (inzulinszekretagog típusú) szerek:
- étkezésivércukor-szabályozók-prandialisglukózregulátorok-(nateglinid/Starlix®/, repaglinid /NovoNorm®/); -szulfanilureák(gliclazid /Diaprel MR®,Gliclada®/,glimepirid /Amagen®,Amaryl®, Dialosa®, Diamitus®,Glempid®,
Glibezid®, Glimepirid®, Glimewin®, Glindia®, Gliprex®, Limeral®, Melyd®, Sintecal®, valamint a hatóanyagot kombinációban tartalmazó készítmények: ld. később/, gliquidon /Glurenorm®/, glipizid /Minidiab®/, glibenclamid /Gilemal®, Gilemal micro®, Glucobene®, Maninil®/).
Az előző két csoportot együtt, megkülönböztetendő a következő csoportba sorolt készítményektől, újabb keletű elnevezéssel hagyományos inzulinszekretagog vegyületekként is említik.
- inkretin hatásmechanizmusú - új típusú inzulinszekretagog - vegyületek: inkretinhatás-fokozók (dipeptidilpeptidáz /DPP/-4 gátlók): sitagliptin (Januvia®), vildagliptin (Galvus®), valamint az összetevőket kombinációban tartalmazó készítmények. Az inkretinhatás-fokozók másik csoportja, az ún. inkretinmimetikumok képviselői - ez idő szerint törzskönyvezett származékukaz exenatid (Byetta®) - nem szerepelneka felsorolásban, lévén nem orálisan, hanem parenteralisan alkalmazandó készítmények.
A készítményválasztást több mérlegelési szempont együttes értékelése (a vércukorszint-emelkedés típusa /étkezés utáni - postprandialis -, illetve éhomi és postprandialis/, az érintett személy tápláltsági állapota, életkora, társbetegségei, stb.) segíti.
A 2008. végén hazánkban forgalmazott gyári antidiabeticum-kombinációkat az 5. táblázat foglalja össze.
5. táblázat. A hazai forgalmazásban 2008. végén hozzáférhető fix összetételű orális antidiabeticum-kombinációk
tiazolidindion (rosiglitazon) + metformin
Avandamet® 2 mg/500 mg, 2 mg/1000 mg, 4 mg/1000 mg tiazolidindion (rosiglitazon) + szulfanilurea (glimepirid)
Avaglim® 4 mg/4 mg, 8 mg/4 mg inkretinhatás-fokozó (vildagliptin) + metformin
Eucreas® 50 mg/850 mg, 50 mg/1000 mg
3. 2. 2.1.1. Az első kezelés megválasztása
Első választandó kezelésként az akut anyagcserekisiklással nem járó esetekben intenzív életmódkezelés és -ellenjavallat vagy intolerancia hiányában, tápláltsági állapottól függetlenül- metformin alkalmazása javasolt ("A"). Célértékként minden kezelési fázisban a <7,0% HbA^-érték szerepel, terápiaváltás szükséges, ha az alkalmazott kezelés a kívánt glykaemiás kontrollt 3 hónap elteltével sem biztosítja ("A").
Metformin-ellenjavallat,vagy-intolerancia esetén tiazolidindion típusú szer (pioglitazon),vagy szulfanilurea csoportú készítmény lehet a megfelelő első választás.
3.2.2.1.2. Antidiabeticum-kombináció bevezetése
Ha életmódkezelés és metformin-monoterápia 3 hónap elteltével sem biztosítja a terápiás célt (HbA1c <7,0%), kombinált antidiabeticus kezelés bevezetése szükséges. Metformin mellé kombinációként kellően validált eljárások tekintetében bázis inzulin -tapasztalatok szerint a leghatékonyabb-, vagy hagyományos inzulinszekretagog hatású szer-szulfanilurea választása esetén a legköltséghatékonyabb-adása jöhet szóba. Kevésbé validált kezelési eljárásként tiazolidindion (pioglitazon [Actos®]), vagy inkretinmimetikus hatású szer (exenatid [Byetta®]) kiegészítő adása is választható. Pioglitazon, vagy exenatid alternatívájaként inkretinhatás-fokozó (DPP-4 gátló) csoportú szer (sitagliptin [Januvia®], vildagliptin [Galvus®] választása is szóbajön. A választásnál mérlegelhető szempontokat készítményenként tekintjük át:
- metformin: adása ellenjavallt veseelégtelenségben (ha a szérum kreatinin férfiben >130, nőben >110 umol/l, vagy a mért, ill. számított /estimated/ GFR [eGFR] <60 ml/min/1,73m2), kifejezett májkárosodásban, hypoxiával járó állapotokban, interkurrens megbetegedések esetén, általános érzéstelenítést igénylő műtétek perioperatív szakában, myocardialis infarctus akut szakában, terhesség és szoptatás alatt. Óvatosság ajánlott és inkább kerülendő recurráló pancreatitis, valamint rendszeres alkoholfogyasztás esetén is. Az alkalmazásával kapcsolatos biztonsági előírások betartása esetén legsúlyosabb potenciális mellékhatása, a tejsavacidózis fellépése ritka, 0,01-0,084/1000 betegév. Egyéb mellékhatásai között gastrointestinalis diszkomfort-panaszok, lágyabb széklet, hasmenés, igen ritkán B12-vitaminhiány fordulhatnak elő. A hasi panaszok kis kezdőadag (500 mg) alkalmazásával, s fokozatos dózisemeléssel nagyrészt elkerülhetők. Önmagában adva -az ún. antihyperglykaemiás szerek más képviselőivel egyezően- hypoglykaemiát nem okoz. Maximális napi adagja 3000 mg, de 2000 mg napi adag felett a dózis-hatás görbe ellapul. Ajánlási szint: "A". A 2-es típusú diabetesben szenvedők kezelése során bármely terápiás rezsim választása esetén (kombinált orális vagy inzulinterápia esetén is) indokolt a metformin megtartása - amennyiben adásának nincs ellenjavallata ("D"). A gastrointestinalis mellékhatások ritkábban jelentkeznek az újabban forgalomba került, elhúzódó kioldódású (extended release) készítményváltozat (Merckformin® XR) alkalmazásakor.
- tiazolidindionok: míg a metformin döntően a máj glukózkibocsátását csökkenti, e készítményekegy magreceptor, a PPAR-y serkentésén keresztül elsősorban a zsír- és izomszövet glukózfelvételét javítják, de kis mértékben mérséklik a hepatikus glukóztermelést is. Adásuk ellenjavallt súlyos (eGFR <30 ml/min/1,73 m2) vese-, illetve a hepatoparenchymás enzimek kétszeresnél nagyobb emelkedésével járó májműködési zavarban, NYHAI-IV. stádiumú keringési elégtelenség fennállásakor. A jelenleg forgalmazott készítmények közül a pioglitazon (Actos®) zsíranyagcsere-hatásai kedvezőbbek, mint a rosiglitazoné (Avandia®) és egyes adatok szerint előnyösebb a cardiovascularis kimenetelt befolyásoló tulajdonsága is. Erre való tekintettel tiazolidindion típusú szerként elsősorban pioglitazon (Actos®) választandó. Mindkét származék mellékhatásaként folyadékretenció, a zsírkompartmentek közötti eloszlás előnyös változásával kísért súlygyarapodás, dilutiós anaemia, macula oedema fordulhat elő, s fokozódhat az atípusos helyeken előforduló csonttörési gyakoriság is. A rosiglitazon (Avandia®) napi adagja 1-2x4-1 x 8 mg, a pioglitazoné (Actos®) 1 x 30-45 mg. Adhatók monoterápiában -metformin-intolerancia vagy -ellenjavallat esetén-, valamint metforminnal és/vagy szulfanilureával kombináltan is. Inzulinnal történő együttadásuk csak kivételesen indokolt esetben, gondos mérlegelés alapján tanácsolható. Ajánlási szint: "B".
- étkezésivércukor-szabályozók (prandialis glukózregulátorok, korábban glinideknek, vagy meglitinideknek nevezett vegyületcsoport): az étkezésre bekövetkező inzulinelválasztás korai - első - fázisát serkentik, helyreállítva a 2-es típusú diabetes egyik legkorábbi patogenetikai vonását, e szekréciós fázis kiesését vagy késését, a bázis inzulinszekréció befolyásolása nélkül. Hatásuk gyorsan kialakul és rövid tartamú - a hypoglykaemia fellépésének kockázata kicsi-, inzulinszekretagog természetük azonban elmarad a szulfanilureákétól. Az éhomi vércukorszintet alig befolyásolják. Adásuk - metformin kiegészítéseként - akkor jöhet szóba, ha a beteg - elhúzódóbb és erélyesebb szekretagog természetű - szulfanilureát még nem kapott, valamint az éhomi vércukorszint csak mérsékelten emelkedett. Főétkezések előtt adandók, a szükséglethez igazodóan napi 1-3 alkalommal. Együttadásuk szulfanilureákkal kerülendő, mivel azonos effektor rendszeren keresztül, a káliumcsatorna zárása útján hatnak, így nem erősítik, hanem inkább kompetitorként gátolják egymás hatását. Ajánlási szint: "D".
- szulfanilureák: az étkezésre bekövetkező inzulinelválasztás egyik vagy mindkét fázisát serkentik, de fokozzák a bázis inzulin termelődését is. E tulajdonságuk eredményezi a vércukorszint csökkenését, de potenciális mellékhatásukat, a vércukor esését (hypoglykaemiát) is. A szulfanilurea-receptorhoz való kötődésük alapján megkülönböztetünk pancreas-szelektív (gliclazid) és nem-szelektív - más szövetek, elsősorban a cardiovascularis rendszer szulfanilurea-receptoraihoz (káliumcsatornáihoz) is kötődő-vegyületeket (az összes többi készítmény). Ez utóbbiaka glimepirid kivételével gátolják az ischaemiás prekondícionálás mechanizmusát. E hatástani sajátosságok ajánlási következménnyel ez idő szerint nem járnak.
Hatástartam szerint korábban különbséget tettünk rövid (glipizid,gliquidon), közepes (gliclazid) és hosszú (glimepirid, glibenclamid) hatástartamú származékok között. A tabletta-formuláció módosításaival e különbségtétel mára túlhaladottá vált: pl. a gliclazid jelenleg hozzáférhető, "módosított felszabadulású" (modified release, MR) változata a hosszú hatásúak közé sorolható. A glibenclamid micronizált változata ugyanakkor az alapmolekulához képest valamivel gyorsabb hatáskezdetet és rövidebb hatástartamot eredményezett. A gliquidon 95%-ban a májon át eliminálódik, ezért mérsékelten beszűkült veseműködés mellett is adható, de 200 umol/l fölötti szérum kreatininszint és/vagy <60 ml/min GFR-érték esetén célszerűbb inzulinkezelésre áttérni.
Fentiek alapján a szulfanilureák adásával kapcsolatban az alábbi mérlegelési szempontok jönnek szóba: idősebb korban (>65 év) kerülendő az elhúzódó hypoglykaemizáló hatású, az ischaemiás prekondícionálást potenciálisan gátló származék (glibenclamid) adása; a gliclazid pancreas-szelektív természete révén nem gátolja az ischaemiás prekondícionálást, a készítménycsoporton belül alacsony a hypoglykaemia kockázata, s kedvező egyedi haemovascularis sajátossága; a glimepirid ugyancsak nem gátolja az ischaemiás prekondícionálást, emellett erélyes első fázisú szekréciófokozódást eredményez. Ajánlási szint: "D". A gliquidon a fentiek szerinti megfontolásokkal beszűkült veseműködés mellett is adható. Ajánlási szint: "D". Az egyes származékok napi adagja változó, a glipizid és a gliquidon kivételével -amelyek napi 1-3-szori adagolása szükséges- napi egy dózisban adhatók. Maximális dózisú alkalmazásra csak ritkán van szükség. A dózis emelésével a béta-sejt terhelése nő és fokozódik a mellékhatások potenciális kockázata is.
- Inkretin hatásmechanizmusú szerek: mind az orálisan adható DPP-4 gátlók, mind a már törzskönyvezett, de hazai forgalomba még nem került, parenteralisan alkalmazandó inkretinmimeticum (exenatid, Byetta®) vércukorcsökkentő tulajdonsága az inkretinek, elsősorban a glukagonszerű-peptid (GLP)-1 hatástani sajátosságain alapul.
- Bár a DPP-4 gátlók monoterápiában is eredményesnek bizonyultak, adásuk jelenleg metformin (ellenjavallat vagy intolerancia esetén szulfanilurea) mellé második, esetleg metformin és szulfanilurea mellé harmadik antidiabeticumként jöhet szóba (a hármas kombináció helyett azonban inkább az inzulinterápia megkezdése preferálandó). Klinikai vizsgálatokban eredményesen adták tiazolidindion típusú szerrel is, ez az alkalmazás azonban hazai gyakorlatunkban egyelőre nem támogatott. A sitagliptin (Januvia®) dózisa 1 x 100 mg, a vildagliptiné (Galvus®) metformin mellett adva 1-2 x 50 mg,szulfanilureával kombinálva 1 x 50 mg (a két származék hatástartama eltérő, ez a magyarázata a sitagliptin napi egy, a vildagliptin egy vagy két dózisban történő adagolásának). Mellékhatásspektrumuk kedvező, az esetek kis részében nasopharyngitis, felső légúti catarrhalis tünetek jelentkezhetnek. A testsúlyt nem növelik, nem csökkentik. Szulfanilureával együttadva a hypoglykaemia kockázat fokozódhat, ezért javasolják az egyidejűleg alkalmazott szulfanilurea adagjának csökkentését.
- Az exenatid (Byetta®) dózistitrálás nélkül, sc. injekció formájában alkalmazandó. Az esetek egy részét kezdetben hányinger, hányás kísérheti, adását ezért kis kezdőadag, napi 1 x 5 μg választása kívánatos. A dózis 7-10 nap elteltével emelhető 2x5& #956;g, majd további kb. 2 hét múlva 2x10 μg-ra. Alkalmazása során a testsúly csökken.
- Alfa-glukozidáz-gátlók (hazai képviselőjük az akarbóz): elsősorban az étkezés utáni vércukorszintet csökkentik, bár tartós alkalmazás mellett mérséklődik az éhomi vércukorérték is. Az akarbóz gastrointestinalis mellékhatásokat, haspuffadást, fokozott bélgázképződést okozhat, ami az adag fokozatos bevezetésével enyhíthető. Szűk sérvkapujú hasi sérvvel rendelkezőkön adása fokozott óvatosságot igényel. Ajánlási szint: "A". Máj- és vesekárosodás fennállása esetén adása óvatosságot igényel, mert bár csak 3-4%-a szívódik föl a bélből, a felszívódott rész teljes egészében a májban metabolizálódik,a metabolitok pedig részben a vesén át ürülnek. Néhány esetben megfigyelték-reverzibilis-májenzim-emelkedést okozó hatását. Ajánlási szint: "D". Egy nagy klinikai tanulmányban kedvezőnek bizonyult a cardiovascularis szövődmények visszaszorítása terén ("A"), az adatok azonban még megerősítést igényelnek. Átlagos anyagcserejavító hatása elmarad a metforminétől és a szulfanilureákétól, monoterápiában adva a HbA1c-értéket 0,5-0,8%-kal csökkentheti. Kezdőadagként este 25 mg javasolt, ami 2-3 naponkénti emeléssel fokozatosan 3 x 100 mg-ig emelhető.
- A (bázis) inzulinadást az inzulinkezelés tárgyalása kapcsán tekintjük át.
Ha a választott antidiabeticum-kombináció - helyesen alkalmazott életmódkezelés mellett - az adott esetben optimális (maximális) dózisban három hónap elteltével sem biztosítja a kívánt glykaemiás kontrollt (HbAu <7,0%), a kombináció módosítása, vagy kiegészítése szükséges. Ha addig nem került rá sor, (bázis)inzulin bevezetése mindenkor megfelelő megoldás lehet, természetesen, a fent összefoglaltak figyelembevételével ilyenkor minden esetben felülvizsgálandó és szükség szerint módosítandó az addigi antidiabeticus kezelés is. Három oralis antidiabeticum megfelelő javallattal történő együttes alkalmazása elvben nem kifogásolható, ilyen esetekben azonban helyette inkább inzulin bevezetése és az orális kezelés módosítása szükséges. Ha metformin és bázisinzulin együttes adása nem biztosítja a kívánt glykaemiás kontrollt, az inzulinkezelés intenzifikálása javasolt.
3. 2. 2. 1. 3. Az orális antidiabeticus kezelés gyakorlata:
Monoterápia esetén a választott gyógyszer dózisa a maximális megengedett, ill. az adott beteg esetében maximálisan tolerált értékig növelhető. Ha kellő hatás nem mutatkozik, az elsőként választott gyógyszer adagjának megtartása vagy csökkentése mellett kombinált kezelésre kell áttérni. Az oralis antidiabeticumok-bizonyos korlátozások mellett-egymással kombinálhatók. A kombinált kezelés elméleti alapját az képezi, hogy egy adott betegben az inzulinrezisztencia és az inzulintermelési zavar - esetenként változó mértékű- jelenlétével számolhatunk. Így a két patogenetikai tényező, vagy az inzulinrezisztencia különböző komponensei egyidejű befolyásolásával eredményesebb vércukorcsökkentő hatás remélhető. Nem adhatók együtt azonos hatású szerek különböző képviselői, így különböző szulfanilurea-, vagy biguanid-készítmények, illetve szulfanilurea és étkezésivércukor-szabályozó szerek. A pioglitazon és akarbóz, illetve pioglitazon és étkezésivércukor-szabályozók kombinációjával ez idő szerint nem áll elegendő tapasztalat rendelkezésre. Ajánlási szint: "B".
Preferált kombinációk:
- metformin + bázis inzulin
- metformin + szulfanilurea
- metformin + étkezésivércukor-szabályozó
Megengedett további kombinációk:
- metformin + tiazolidindion
- metformin + DPP-4 gátló
- metformin + exenatid
- metformin + akarbóz metformin-intolerancia esetén:
- szulfanilurea + tiazolidindion
- szulfanilurea + DPP-4-gátló
- szulfanilurea + exenatid
- szulfanilurea + akarbóz
3.2.2.2. Inzulinkezelés 2-es típusú diabetesben
Minden olyan esetben, amikor életmódkezelés + orális antidiabeticum helyes javallattal és adagban történő alkalmazása három hónap elteltével sem biztosítja a kívánt glykaemiás kontrollt (HbA^ <7,0%), felmerül az inzulin bevezetésének szükségessége. Korábban általában két, vagy három különböző csoportú orális szer hatástalansága esetén került sor az inzulin alkalmazására, az újirányelvek, az inzulin korai bevezetésének bétasejt-kímélő és a rövid időn belül biztosítható jó anyagcsereállapot szövődmény-megelőző hatását szem előtt tartva ezt már a kezelés korai fázisában, akár a metformin-monoterápia sikertelensége esetén -bázisinzulin formájában- alternatív választási lehetőségként tekintik. Inzulin adásának mind a túlsúlyos, mind a normális tápláltsági állapotú személyek esetében több formája lehetséges (a megfelelő étrend + fokozott fizikai aktivitás fenntartása mellett).
3.2.2.2.1. Orális antidiabeticum + bázis inzulin kombinációja
A bázisinzulin-hatás biztosítására korábban csak közepes (intermedier) hatástartamú, többségében NPH-típusú humán inzulinkészítmények (Humulin N®, Insulatard HMge®) álltak rendelkezésre, amelyeket a kívánt éhomi vércukorszint elérése érdekében lefekvéskor (magyarban is meghonosodott angol kifejezéssel "bedtime") adagoltunk. A hosszú hatású inzulinanalógok (glargin /Lantus®/, detemir /Levemir®/) forgalomba kerülése lehetővé tette a beadás akár korábbi időpontra helyezését is, alkalmazásuk emellett nemcsak az éhomi, hanem az étkezések előtti (preprandialis) vércukorszintek kedvezőbb alakulását is elősegít(het)ik. Az analóg bázisinzulin és orális kezelés kombinációját a szakirodalom újkeletű kifejezéssel BOT (basal insulin and oral treatment) kezelésként jelöli.
Ha a lefekvés előtt NPH-típusú inzulint alkalmazunk, akkor ennek kezdő adagja 8-12 NE lehet, amely a szükséglethez igazodóan fokozatosan emelhető. A 40 NE meghaladása, a hajnali hypoglykaemia-kockázat fokozódása miatt nem célszerű. Ha glargin (Lantus®) adagolását választjuk, ennek beadása a készítmény közel 24 órás hatásából adódóan bármely napszakban történhet, de fontos, hogy az mindig közel azonos időpontban történjen. Orális antidiabeticus kezeléssel kombinált alkalmazása esetén kezdő adagja általában 10 NE, ami a reggeli vércukorértékek függvényében fokozatosan emelhető. Bevált egyszerű titrálási rendszer szerint amennyiben három egymást követő nap éhomi vércukorértékeinek átlaga >6,0 mmol/l és éjszaka nem fordult elő megélt vércukoresés vagy <4 mmol/l alatti mért vércukorszint, az adag 2 E-gel növelhető. Ez a séma folytatandó a fenti célérték (éhomi vércukorszint <6,0 mmol/l) eléréséig. Ha az érték ennél alacsonyabb és/vagy éjkszakai hypoglykaemia fordult elő, az adag 2 E-kénti csökkentése szükséges. A detemir (Levemir®) hatástartama valamelyest rövidebb a glarginénál, 2-es típusú diabetesben azonban orális antidiabeticus kezelés kiegészítéseként az esetek túlnyomó többségében napi egyszeri adása elegendő lehet. Adagolása történhet vacsorakor, vagy lefekvés előtt. Ez utóbbi akkor jöhet szóba, ha a korábbi beadás a kívánt éhomi vércukorszintet nem biztosítja. Kezdő adagja és dózistitrálási mechanizmusa lényegében a glargin esetében leírtakkal egyező.
A kombinált kezelés (orális antidiabeticum + inzulin) annál eredményesebb, minél kedvezőbb anyagcserehelyzetben kerül sor bevezetésére. Amennyiben a fenti inzulinadagokkal sem sikerül biztosítani a reggeli normoglykaemiát, és/vagy napközben a vércukorszint meghaladja a 10 mmol/l-t, célszerű leállítani az orális (elsősorban a szulfanilurea) készítmények adagolását és átállni a napjában kétszeri vagy többszöri inzulin adagolására. Megjegyzendő, hogy 10% feletti kiindulási HbA1c esetén célszerű azonnal inzulinkezelést alkalmazni napi többszöri inzulinadás formájában, mert ezen esetekben a kombinált (orális antidiabeticum + bázis inzulin) kezeléstől hosszú távú jó eredmény kevéssé várható.
3.2.2.2.2. Orális antidiabeticum + prandialis (humán reguláris, gyors hatású /kristályos/) inzulin kombinációja
Bár az esetek többségében orális antidiabeticus kezelés inzulinnal történő kiegészítésekor az inzulin adása a bázisinzulin-pótlást szolgálja, kifejezett étkezés(ek) utáni vércukor-emelkedéssel járó esetekben sor kerülhet a metformin + prandialis inzulin kombináció alkalmazására is. Ez a kombináció olyan esetekben választható, amikor az inzulin-elválasztást serkentő antidiabeticum adása valamilyen okból nem jöhet szóba, vagy metformin és inzulinszekretagog hatású szer együttadása a kívánt postprandialis vércukorcsökkenést nem biztosítja, de az éhomi vércukorszint a beállított kezelés mellett elfogadható tartományú. Ajánlási szint: "D"
Fenti meggondolásból metformin és étkezések előtt (prandialisan) alkalmazott gyorshatású inzulinanalóg kombinációja is előfordulhat azon ritka esetekben, amikor a metformin a kívánt mértékű bázisinzulin-hatást biztosítja, de a postprandialis vércukor-emelkedés kifejezett és más módon biztonságosan nem csökkenthető.
3.2.2.2.3. Konvencionális inzulinkezelés 2-es típusú diabetes mellitusban
A 2-es típusú diabetesben szenvedő, idősebb betegek jelentős része jól kezelhető konvencionális inzulinterápiával, ami általában napjában kétszer adott, előkevert (premix, gyors és intermedier hatástartamú komponenst 30/70 arányban tartalmazó) humán inzulin adását jelenti. Ilyen esetekben a reggeli és esti inzulinadagokaránya 2:1,vagy 3:2 szokott lenni. E betegek életmódja, étrendje ugyanis eléggé stabil, a konvencionális kezelés viszonylag könnyen kivitelezhető, s az esetek többségében az elért eredmény is megfelelő.
3.2.2.2.4. Bifázisos inzulinanalógok adása
Inzulinanalógot tartalmazó előkevert inzulin (Humalog Mix® 25, Humalog Mix® 50, NovoMix® 30) igen jól alkalmazható 2-es típusú diabeteszesek kezelésére. Bár adhatók napjában kétszer, reggel, illetve az esti főétkezéselőtt, terjed a napi háromszori alkalmazásuk gyakorlata is, minden főétkezéshez, a beállított étrend szerint szükséges keverékarányú változatot adagolva. E kezelésformát újabb keletű elnevezéssel intenzív keverékterápiaként (intensive mixture therapy: IMT), vagy újabban prandialis premix kezelésként (prandial premix therapy: PPT) említik. A magas gyorskomponens-arányú változat adása akkor javasolt -általában reggel, az esetek egy részében ebéd előtt is-, ha az érintett személy nagyobb szénhidráttartalmú ételeket fogyaszt.
3.2.2.2.5. Szemi-intenzív inzulinkezelés 2-es típusú diabetes mellitusban
A betegekegy részében ún. szemi-intenzív kezelési formát lehet választani, főleg akkor, ha az étkezések között inkább a vacsora a hangsúlyos. Ilyenkor reggeli előtt humán premix inzulin, délután öt óra körül gyors hatású és lefekvéskor intermedier típusú humán inzulint választunk, amivel a vacsoratáji vércukor-emelkedés jól kivédhető, s a másnap reggeli, éhomi vércukorértéksem magas. Előfordulhat az is, hogy az ebéd utáni-vacsora előtti vércukorszint magasabb a kívántnál, ilyenkora reggel és vacsora előtt adott premix humán inzulinokat ebéd előtt adagolt gyorshatású (humán reguláris) inzulin adagolásával lehet kiegészíteni.
3.2.2.2.6. Intenzív konzervatív inzulinkezelés 2-es típusú diabetes mellitusban
A 2-es típusú diabetesben szenvedők esetében is helye van - az 1-es típusú diabetesben történő alkalmazáshoz hasonlóan - az intenzív konzervatív inzulinkezelésnek (ICT), főleg akkor, ha az adott beteg fiatalabb életkora, foglalkozása, életmódja ezt indokolttá teszi (ekkor érdemes rögtön ezzel a kezelési formával indítani), vagy ha a betegeknél a korábbi inzulinkezelés (konvencionális, szemi-intenzív vagy IMT) nem hozta meg a remélt eredményt.
3.2.2.2.7. Inzulinkezelés 2-es típusú diabetesben: evidenciák, ajánlások összefoglalása
- A tartósan jó anyagcsere-helyzetre való törekvés (alacsonyabb HbA1c-érték biztosítása)
- számottevően csökkenti a microangiopathiás szövődmények kialakulásának és progressziójának kockázatát,
- a microangiopathiás károsodásokéhez képest szerényebb mértékben, de hosszabb távon értékelhetően csökkenti a macroangiopathiás szövődmények kialakulásánakés progressziójának kockázatát, ezért e betegekben az adott helyzethez igazodó, várhatóan legeredményesebb antidiabeticus kezeléssel minél jobb anyagcsere-helyzet biztosítására kell törekedni ("A").
- Az inzulinkezelés kockázatát a hypoglykaemia és a testsúlygyarapodás jelenti. Lokális szövődmény (allergia, infekció) jelentkezése igen ritka. Az inzulinkezeléssel elért HbA1c-érték inverz összefüggést mutat a hypoglykaemia kockázatával. Inzulinanalóg alkalmazása mellett a hypoglykaemia kockázata (a humán inzulinhoz viszonyítva) csökken, a testsúlygyarapodás detemir (Levemir®) mellett a legkevésbé kifejezett ("A").
3.3. Pancreas- és Langerhans-sziget-transzplantáció
Tökéletes normoglykaemia sikeres pancreas- vagy Langerhans-sziget-transzplantációval érhető el.
3.3.1. Pancreas-transzplantáció
A szimultán vese + pancreas-átültetés eredményei felülmúlják a "csak" pancreas-beültetés eredményeit, mind a graft-túlélés, mind az immunológiai "graft-failure" szempontjából. Sikeres kombinált vese + pancreas-transzplantáció esetén megszűnik az uraemiás toxicosis és a szénhidrát-anyagcsere zavara, elhagyható az inzulin, a diéta, a menetrendszerű életmód, azaz a beteg életminősége jelentősen javul. A microangiopathiás szövődmények közül a nephropathia és a neuropathia javulása remélhető, ez a retinopathia vonatkozásában nem bizonyított ("D"). A macrovascularis szövődmények az esetekegy részében romolhatnak ("D"). Transzplantációt követően a beteg tartós -olykor mellékhatásokkal járó - immunszupresszív kezelésre szorul. A műtéti beavatkozás perioperatív mortalitása 4-5%.
Kombinált vese + pancreas-transzplantáció indokolt minden olyan 1-es típusú cukorbeteg esetében, aki a végstádiumú veseelégtelenség állapotába került és vesetranszplantációra vár.
Szoliter pancreas-transzplantáció csak kellően szelektált beteganyagon, megfelelő indikáció alapján végezhető. Ilyen indikációk az alábbiak lehetnek: a hypoglykaemia tüneteinek meg-nem-érzése ("unawareness syndrome") gyakori eszméletvesztéssel, igazi "brittle" diabetes, gyorsan progrediáló retinopathia, súlyos diabeteszes gastroparesis.
3.3.2. Langerhans-sziget-transzplantáció
A Langerhans-sziget-transzplantáció során az intervenciós radiológus képernyő alatt katétert vezet a portális vénába és lassú infúzióban bejuttatja az izolált szigeteket tartalmazó tápoldatot. A szövődmények elhanyagolhatóak, a beavatkozás szükség szerint ismételhető. A transzplantációt követően tartós immunszupresszív kezelés szükséges, napjainkban az ún. Edmonton-protokoll szerint végzik a transzplantációt és az utókezelést. Az inzulinadás szükségessége csak a betegek egy hányadában válik tartósan elkerülhetővé.
Langerhans-sziget-transzplantáció indikálásakor gondosan mérlegelni kell a várható előnyt és az elkerülhetetlen (döntően a tartós immunszupresszív kezeléssel összefüggő) kockázatot.
Langerhans-sziget-transzplantáció indokolt azoknál a labilis anyagcseréjű, 1-es típusú cukorbetegeknél, akik már egyéb szervtranszplantációban (pl. vesetranszplantációban) részesültek és immunszupresszív kezelés alatt állnak
Nem-immunszupprimált beteg esetében a Langerhans-sziget-transzplantáció ugyanazokkal az indikációkkal jön szóba, mint a szoliter pancreas-transzplantáció. A kétféle beavatkozás közül a Langerhans-sziget-transzplantáció előnyben részesítendő akkor, ha a beteg általános állapota miatt a nagy hasi műtét túl kockázatosnak látszik.
3. 4. Vércukor-önellenőrzés
A vércukor-önellenőrzés célja a beteg vércukorszintjének rendszeres ellenőrzése, így az a cukorbetegség kezelésének, követésének hasznos eszköze. Megfelelő edukáció/edukáltsági szint nélkül a vércukor-önellenőrzés célja nem teljesül. A vércukor-önellenőrzésre használt (ágy melletti) gyors, reflektometriás vércukor-meghatározás a szénhidrátanyagcsere-zavarok kórismézésére nem alkalmas, e célra nem használható.
A vércukor-önellenőrzés szerepe diabetesben:
- hypoglykaemia felismerése és elkerülése,
- hyperglykaemiás anyagcsere-kisiklás megelőzése, ill. korrigálása,
- a kezelés életvezetéshez, aktuális élethelyzethez történő igazítása,
- optimális anyagcsere-kontroll elérése és fenntartása,
- a felsoroltak révén a betegség megismerésének, a kezelés bizonyos határok közötti önmenedzselésének, a beteg-edukációnak hatékony eszköze ("D").
Vércukor-önellenőrzés javasolt minden cukorbeteg számára a diabetes-gondozás keretén belül, miután az
- az aktuális vércukorértékéről tájékoztat késedelem nélkül,
- lehetővé teszi az éhomi (étkezés előtti) és postprandialis vércukor meghatározását,
- növeli a kezelés biztonságát a hypoglykaemia felismerése révén,
- mind az orvos, mind a beteg számára segítséget jelent az antidiabeticus kezelés szükség szerinti módosításának eldöntésében, ill. annak elfogadásában ("A").
A rendszeres vércukor-önellenőrzés hozzájárul az anyagcserehelyzet javulásához és a késői szövődmények mérsékléséhez
- 1-es típusú diabetesben és inzulinnal kezelt 2-es típusú cukorbetegségben ("A"),
- életmódkezelés, ill. életmódkezelés + orális antidiabeticumok alkalmazása esetén 2-es típusú cukorbetegségben
("D").
A rendszeres véruckor-önellenőrzés hozzájárul az anyagcsere-helyzet javulásához, ill. az anyai és magzati szövődmények csökkentéséhez a diabeteszes terhesség minden formájában ("A").
A vércukor-önellenőrzés gyakorisága és időpontja függ
- az alkalmazott antidiabeticus kezelés módjától,
- az általános anyagcsere-helyzettől,
- a hypoglykaemia-kockázat mértékétől,
- a kezelés rövid-, közép- és hosszútávú céljától
- speciális körülményektől (terhesség, interkurrens betegség, perioperatív állapot) ("A")
A vércukor-önellenőrzés történhet
- alkalmi mérésekkel,
- vércukorpárok (étkezés előtti/utáni) mérésével,
- napi 5-8-szori - étkezések előtti, étkezések utáni, ill. lefekvéskor, éjfélkor és hajnalban mért - meghatározást magában foglaló "profil" készítésével,
- lépcsőzetes mérési módszerrel (naponta más-más időpontban történő vércukormérésekkel.
A gyors vércukor-meghatározás krízisállapotokban is nagy jelentőségú, de - méréstechnikai okokból eredően -laboratóriumi vércukorméréssel történő folyamatos megerősítése szükséges ("B").
3. 5. Kezelési célértékek, az ellátás megfelelőségének indikátorai, a szakmai munka eredményességének mutatói 3.5.1. Kezelési célértékek
A cukorbetegség hosszú távú prognózisát a kis- és nagyér-szövődmények (micro-és macroangiopathiás károsodások) határozzák meg. Míg a microangiopathiás szövődmények nem atherogen genezisűek és elsősorban a glykaemiás kontroll függvényei, a macroangiopathiás károsodásoknak ez csak egyik összetevője. Minthogy a szénhidrát-anyagcsere alkalmi (étkezés utáni vércukorszint emelkedések = postprandialis glukóz spike-ok) és tartós károsodása (jelzői a különböző glikált fehérjék, így a HbAic, illetve a szérum fruktózamin emelkedett értéke), a magas vérnyomás, valamint a vérzsír-eltérések ugyanazon célszervre, az endothelre fejtik ki kedvezőtlen, atherogenesist indukáló hatásukat, az alacsony kockázati határt jelző értéktől való kisebb eltérésük is jelentős kockázatfokozódást eredményez. Ez a magyarázata, hogy a korábbi ajánlásokban szereplő a nagyér (más néven: artériás) kockázat határértékei alacsonyabbak voltak, mint a microangiopathiás károsodások fokozott kockázatára utalók. A vérnyomásérték esetében nincs különbség a macro- és microangiopathiás kockázat tekintetében.
A 2-es típusú cukorbetegség, valamint a micro- vagy macroangiopathiával társuló 1-es típusú diabetes a nagy keringési kockázatú állapotokhoz tartozik, s ide sorolódik a metabolikus szindróma is. A fehérjeürítés nagyobb kockázatot jelző voltának az a magyarázata, hogy az nemcsak a vese károsodását jelzi, hanem az endothelkárosodásnak, azaz az atherosclerotikus eredetű szövődményeknek is markere. Nemzetközi ajánlások, és ehhez igazodva a legutóbbi, III. Magyar Kardiovaszkuláris Konszenzus Konferencia (2007) a nagy kockázatú állapotokon túl egy igen nagy kockázatú kategóriát is megkülönböztet. A cukorbetegség esetében azon formák tartoznak ide, ahol a kórelőzményben már manifeszt keringési betegség (infarctus, stroke, alsóvégtagi obliterativ érszűkület, vagy rekonstrukciós műtét) jelenléte is szerepel.
A glykaemiás célértékek tekintetében nincs különbség a különböző keringési kockázatú csoportok között (6. táblázat). Igazolást nyert ugyanis, hogy a határértéket meghaladó minden vércukortartomány fokozza a kis- és a nagyér-szövődmények kockázatát. A követendő értékek tekintetében az 1-es és 2-es típusú cukorbetegség esetében sincs különbség azzal a kivétellel, hogy a HbAic célértéke 1-es típusú diabetesben <6,5%, 2-es típusú diabetesben <7,0%. Ajánlási szint: "A".
6. táblázat. A szénhidrát-anyagcsere kezelési célértékei nem-terhes állapotban, felnőttkori cukorbetegségben
| kezelési célérték | |
| HbAic (DCCT-re standardizálva) (%)* | < 6,5 |
| Éhomi / preprandialis plazmaglukóz (mmol/l) | |
| Laboratóriumban mérve | < 6,0 |
| Önkontrollosan mérve** | < 5,5 |
| Postprandialis plazmaglukóz (mmol/l) | |
| Laboratóriumban mérve | < 7,5 |
| Önkontrollosan mérve** | < 7,5 |
*1-es típusú diabetesben <6,5%, 2-es típusú diabetesben <7,0%;
**a hazánkban forgalmazott ágy melletti vércukormérők (glucometerek) jelenleg capillaris vérre kalibráltak, nemzetközi állásfoglalások azonban a készülékek plazmára történő kalibrálását szorgalmazzák. Amennyiben az átállításra nálunk is sor kerül, az önkontrollosan mért célérték módosulni fog. Inzulinnal kezelt cukorbetegek esetében lefekvéskor 6,0-7,5 mmol/l közötti vércukor érték követése kívánatos, az éjszakai vércukoresések elkerülése érdekében, ez a mutató azonban hivatalos ajánlásokban nem szerepel.
A lipidértékek tekintetében az a kezelési cél, hogy fokozott keringési veszélyeztetettséget jelző állapotokban (2-es típusú diabetes, micro- vagy macroalbuminuriával szövődött 1-es típusú cukorbetegség, metabolikus szindróma) szintjük ne haladja meg a korábban nagy keringési kockázatot jelző határértéket. 1-es típusú diabetes keringési betegségektől, vagy keringési kockázati tényezők társulásától mentes, fehérjeürítéssel nem szövődött formáiban,
fiatal betegeken elfogadhatók valamivel magasabb határértékek is. Ugyanakkor, fokozott keringési veszélyeztetettség esetén (a fokozott kockázatúként említett formák több keringési kockázati tényező egyidejű társulásával, vagy manifeszt keeringési betegséggel) szigorúbb határértékek követendők (7. táblázat).
7. táblázat. Az antilipaemiás kezelés célértékei (a III. Magyar Kardiovaszkuláris Konszenzus Konferencia, 2007) ajánlása.

A vérnyomás célértéke tekintetében egységesen a <130/80 Hgmm elérése és hosszú távú fenntartása a cél (8. táblázat). Ajánlási szint: "A"
8. táblázat. Az antihypertensiv kezelés célértékei (a III. Magyar Kardiovaszkuláris Konszenzus Konferencia, 2007) ajánlása.

3.5.2. Az ellátás megfelelőségének indikátorai, a szakmai munka eredményességének mutatói
A végkimeneteli mutatók a diabetes micro- és macrovascularis szövődményeinek végállapotát jelentik (végstádiumú veseelégtelenség, vakság, alsó végtagi amputáció, szívinfarctus, stroke). Miután kialakulásuk általában több éves folyamat következménye, elemzésük csak hosszú távon célszerű.
A köztes kimeneteli mutatók a diabetes-specifikus végállapotokat megelőző patológiás elváltozásokat jelentik, ezek közé tartoznak a szemen észlelhető eltérések (retinopathia súlyossági foka), a lábon megjelenő elváltozások (pl. talpi fekély), ill. kóros neurológiai vizsgálati leletek, a micro- vagy macroalbuminuria és a szérum kreatininérték. Köztes kimeneteli mutatóként értékelik az anyagcsere-kontroll fokát (HbA1c-érték, vércukor), a hypoglykaemia és ketoacidosis előfordulási gyakoriságát, ill. a macrovascularis kockázati tényezők (szérum lipidek, vérnyomás, testtömegindex, haskörfogat, carotis-falvastagság) alakulását.
Irodalom
1. European Diabetes Policy Group: A desktop guide to type 1 diabetes. IDF European Region, Brussels, 1998.
2. European Diabetes Policy Group: A desktop guide to type 2 diabetes. Diabetic Medicine 16: 716-730,1999.
3. American Diabetes Association: Standards of medical care in diabetes. Diabetes Care 28 (Suppl. 1): S4-S36,2005.
4. MOTESZ I. Interdiszciplináris Fórum: A nagy kardiovaszkuláris kockázatú betegek általános kezelési irányelvei. Diabetologia Hungarica 11: 292-295, 2003.
5. Zajkás G: Táplálkozási irányelvek diabetesben. Diabetologia Hungarica 12 (Suppl. 2): 5-9, 2004.
6. Sidó Z: Diabetes és fizikai aktivitás. Diabetologia Hungarica 12 (Suppl. 2): 10-15,2004.
7. Barnett A.H.: A review of basal insulins. Diabetic Med 20:873-885, 2003.
8. Tamás Gy.: Inzulinkezelés (in: Halmos T., Jermendy Gy. /szerk./: Diabetes mellitus. Elmélet és klinikum. Medicina, Budapest, 2002.) pp. 305-336.
9. Gyimesi A: A konzervatív inzulinkezelés. Diabetologia Hungarica 12 Suppl 2: 28-32,2004.
10. Kautzky L: Az inzulinpumpa (CSII) a diabetes kezelésének"gold standard"-ja. Diabetologia Hungarica 12 Suppl 2:42-48, 2004.
11. Kerényi Zs, Tamás Gy: Inzulinanalógok. Diabetologia Hungarica 12 (Suppl 2): 28-32, 2004.
12. Jermendy Gy: Tényeken alapuló inzulinterápia. Orv Hetil 146: 341-352, 2005.
13. Scherbaum, WA, Landgraf, R /szerk./: Evidenzbasierte Leitlinien - Antihyperglykámische Therapie des Diabetes mellitus Typ 2. Deutsche Diabetes Gesellschaft, 2001.
14. Winkler G: Az antihyperglykaemisáló oralis antidiabeticumok helye, alkalmazási javallatai a bizonyítékok tükrében. Diabetologia Hungarica 12 (Suppl.2): 16-21,2004.
15. Winkler G, Cseh K: A differenciált sulfanylurea-kezelés elméleti alapjai és gyakorlati lehetőségei. Diabetologia Hungarica 10: 249-257, 2002.
16. Winkler G: Az étkezési inzulinszükségletet biztosító (prandialis glükózregulátor) csoport helye az orális antidiabetikumok differenciálterápiájában. Metabolizmus 2: 81-85, 2004.
17. Pogátsa G: Az inzulin-elválasztást serkentő antidiabeticumok helye a cukorbetegség kezelésének oralis lehetőségei között. Diabetologia Hungarica 12 (Suppl. 2): 22-27,2004.
18. Jermendy Gy: Tényeken alapuló oralis antidiabetikus kezelés. LAM 15:33-43,2005.
19. UK Prospective Diabetes Study (UKPDS) Group. Intensive blood glucose control with sulphonylureas or insulin compared with conventional treatment and riskof complications in patients with type 2 diabetes (UKPDS 33). Lancet 352:837-853,1998.
20. The Diabetes Control and Complications Trial Research Group: The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med 329: 977-986, 1993.
21. Gerő L: Pancreas- és Langerhans-sziget-transzplantáció az 1-es típusú diabetes gyógyításában. Diabetologia Hungarica 12 Suppl 2: 57-61,2004.
22. TabákGy Á, Kerényi Zs,Tamás Gy: Minőségbiztosítás, minőség-ellenőrzés diabetes mellitusbann. In: Diabetes mellitus - elmélet és klinikum (szerk: Halmos T, Jermendy Gy), Medicina Kiadó, Budapest, 2002, pp. 767-784.
23. Nathan, DM, Buse, JB, Davidson, MB, Heine, RJ, Holman, RR, Sherwin, R, Zinman, B: Management of hyperglycemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy. A consensus algorithm from the American Diabetes Association and the European Association for the Study of Diabetes. Diabetes Care 29:1963-1972, 2006. és Diabetologia 49:1711-1721, 2006. (párhuzamos közlés)
24. Nathan, DM, Buse, JB, Davidson, MB, Ferrannini, E, Holman, RR, Sherwin, R, Zinman, B: Management of hyperglycemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy. Update regarding thiazolidinediones:a consensus statement from the American Diabetes Association and the European Association fo the Study of Diabetes. Diabetes Care 31:173-176, 2008.
25. Winkler G: A 2-es típusú diabetes vércukorcsökkentő kezelése az Amerikai és az Európai Diabetes Társaság megújított állásfoglalása alapján. Magy Belorv Arch 61: 7S-82, 2008.
26. Winkler G: Inkretin hatáserősítők, inkretin mimetikumok - a terápiás alkalmazás kigondolásától a gyakorlati megvalósításig. Orv Hetil 148: S79-S87,2007.
27. Gerő L, Jermendy Gy: Inzulinanalógok. Medicina Kiadó, Budapest, 2006.
28. Winkler G, Barkai L, Jermendy Gy: A vércukor-önellenőrzés gyakorlati szempontjai. A Magyar Diabetes Társaság konszenzus-értekezletének állásfoglalásai. Diabetologia Hungarica 1S Suppl 2: 40-4B, 2007.
29. Jermendy Gy: A 2-es típusú diabetes kezelési stratégiája az újszakmai irányelvek tükrében. B0. Magyar Belorv Arch 60: 2B1-2B8,2007.
B1. III. Magyar Kardiovaszkuláris Konszenzus Konferencia a koszorúér-eredetű, agyi- és perifériás érbetegségek kockázatának becslésére, megelőzésére és kezelésére. Metabolizmus 6 Suppl A: B-94,2008.
B2. Jermendy Gy, Winkler G: A III. Magyar Kardiovaszkuláris Konszenzus Konferencia a koszorúér-eredetű, agyi és perifériás érbetegség kockázatának becslésére, megelőzésére és kezelésére. Diabetol Hung 16: 29-B4,2008. BB. Nathan DM, Buse JB, Davidson MB, Ferrannini E, Holman RR, Sherwin R, Zinman B: Medical management of hyperglycemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy. A consensus statement of the American Diabetes Association and the European Association fo the Study of Diabetes. Diabetes Care 2008. Oct 22. epub ehaed of print.
4. Diabeteszes krízisállapotok kezelése
Cukorbetegségben a vércukorértékek túl alacsony, ill. jelentősen emelkedett volta krízisállapotokhoz vezethet el.
4.1. Hypoglykaemia
Hypoglykaemiáról akkor beszélünk, ha a vér cukortartalma B mmol/l alá csökken, az állapotot általában jellegzetes klinikai tünetek kísérik. A definíció azonban nem köthető egy határozott számhoz, mert az élettani szabályozás alapján esetenként e vércukor-határérték felett is észlelhető hypoglykaemiás tünetegyüttes. Olykor azonban észlelünk B mmol/l alatti vércukorértéket tünetek nélkül is. Ez utóbbit biokémiai hypoglykaemiának nevezzük. Hypoglykaemia kialakulhat inzulinnal kezelt cukorbetegekben, de előfordulhat 2-es típusú cukorbetegek inzulinszekretagog tulajdonságú orális antidiabeticummal történő kezelése kapcsán is.
A hypoglykaemia súlyossága szerint megkülönböztetünk enyhébb, ill. súlyosabb állapotot. Az enyhébb állapotot hypoglykaemiás epizódnak szokás nevezni, utalva arra, hogy ebben az esetben a vércukoresést kísérő enyhébb tüneteket a beteg maga megérzi, s szénhidrátbevitellel az állapotot korrigálni képes. A súlyos hypoglykaemia kezelése külső segítséget igényel, ilyenkor joggal beszélhetünk hypoglykaemiás comáról. Hypoglykaemiás coma következtében - általában késői felismerés esetén - maradandó neurológiai deficit is kialakulhat, ill. a beteg halála is bekövetkezhet.
Az enyhe-középsúlyos hypoglykaemia elhárítását maga a beteg végzi. A cukorbetegség kórlefolyása során a beteg megtanulja a beharangozó tünetek felismerését, s az autonóm tünetek észlelésekor kb. 10-20 g gyorsan felszívódó szénhidrátot (gyümölcs, tej, cukrozott üdítőital, tea) fogyaszt. Fontos felhívni a figyelmet, hogy alfa-glukozidáz-gátló (akarbóz) kezelésben részesülő cukorbeteg ilyen esetben csak szőlőcukrot fogyasszon.
Súlyos hypoglykaemia észlelésekor a sürgősségi ellátás kapcsán B0-40 ml 40%-os glukózt kell intravénásan, lassan adni. A beteg eszméletre téréséhez bizonyos idő szükséges. A vércukorértékek alakulásáról ismételt kapilláris vércukor-meghatározással (glucometer) tájékozódhatunk. Inzulinnal kezelt cukorbeteg súlyos hypoglykaemiájának rendeződése után diabetológiai ellenőrzés, szükség esetén a korábbi terápia módosítása szükséges. Szulfanilurea okozta súlyos hypoglykaemia elsődleges ellátását követően a beteg kórházba utalandó, mert az ilyen körülmények között kialakult hypoglykaemia 48-72 órán belül ismételten jelentkezhet, s ennek megelőzése érdekében tartós, S-%-os glukózinfúzióra és rendszeres vércukor-ellenőrzésre van szükség. Természetesen, a korábbi oralis antidiabetikus kezelés is revideálandó. A súlyos hypoglykaemia ellátásában, inzulinnal kezelt cukorbetegek esetén jelentősége van a glucagonnak, melyet a beteg hozzátartozója subcutan, vagy intramuscularisan alkalmazhat a vércukor emelése érdekében, az orvosi segítség megérkezte előtt. A glucagon használata idős, 2-es típusú, szulfanilurea-kezelésben részesült cukorbeteg hypoglykaemiájánál kerülendő.
4.2. Diabeteszes ketoacidosis
Diabetesben abszolút, vagy relatív inzulinhiány következtében diabeteszes ketoacidosis alakulhat ki. A diabeteszes ketoacidosis tüneteiért (polyuria, polydipsia, exsiccosis jelei, a szem belnyomásánakcsökkenése,acetonszagú lehelet, hányás, Kussmaul-légzés) a hyperglykaemia, ill. a ketosis a felelős. Kezeletlen esetben tudatzavar, eszméletlenség következik be, kis arányban fatális kimenetellel is számolni lehet.
A diabeteszes ketoacidosisban szenvedő beteg minden esetben kórházba utalandó. A sürgősségi ellátás a perifériás véna biztosítását és izotóniás sóoldat infúziójának megkezdését jelenti. Kórházi körülmények között - lehetőség szerint a beteg intenzív monitorozását biztosító osztályon - a kezelés alapját az elektrolit- és vízháztartás rendezése, az inzulin pótlása, ill. szükség esetén a sav-bázis viszonyok korrekciója képezi. A beteg kiegészítő kezeléseként thrombosis-profilaxis, antibiotikum adása (infekció megalapozott gyanúja esetén), a pangó gyomorbennék leszívása, agy-oedemára utaló jelek esetén glicerin vagy mannit adása jön szóba.
4.3. Nem ketoacidoticus, hyperosmolaris szindróma
Az állapotot az extracelluláris térben kialakult excesszív hyperglykaemia és/vagy hypernatraemia jellemzi anélkül, hogy ketoacidosis érdemben jelen lenne. Elsősorban 2-es típusú cukorbetegekben, viszonylag ritkán fordul elő. A klinikai képet az extrém exsiccosis és a tudatzavar dominálja. Minden esetben kórházi kezelést igényel. A sürgősségi ellátás a perifériás véna biztosítását és izotóniás NaCl-oldal bekötését jelenti. Kórházi körülmények között a beteg intenzív ellátást igényel, a kezelés tengelyében a só- és vízháztartás rendezése (általában jelentős mennyiségű, iso-és/vagy hypotoniás sóoldat, hypernatraemiás esetekben olykor glukózoldat adása) és kisadagú inzulin ismételt adása áll. A szérum ionok ellenőrzése és szükség szerinti korrekciója szintén alapvető fontosságú. A mortalitás az intenzív terápia ellenére magas (10-70% közötti).
4.4 Lactatacidoticus coma
Diabetesben ritkán észlelhető, általában hypoxiára hajlamosító súlyos társuló betegségekben is szenvedő egyéneknél fordul elő. A biguanid-kezelés nemkívánatos, súlyos mellékhatása lehet, metformin mellett azonban ritkán, általában csak a gyógyszer kontraindikációjának figyelmen kívül hagyásakor fordul elő.
A diagnózist a metabolikus acidosis jelei, ill. az emelkedett szérum laktátszint biztosítja. A kezelés csak kórházi körülmények között valósítható meg, a terápia tengelyében a bikarbonát kellő mennyiségű infúziója áll. Hasznos lehet a dialíziskezelés is.
Irodalom
1. JermendyGy: Diabeteszes krízisállapotok kezelése. Orv Hetil 145:81-83,2004. 5. Diabeteszes micro- és macroangiopathiás szövődmények és kezelésük
A diabetes mellitus idült szövődményei között a microangiopathia (retino-, nephro- és neuropathia diabetica) diabetes-specifikusnak minősül, míg a macroangiopathiás szövődmények az atherosclerosis különböző klinikai formáinak kialakulását jelenti. A micro- és macroangiopathiás szövődmények egyaránt fenyegetik az 1-es és a 2-es típusú diabetesben szenvedőket, mégis a macroangiopathiás (cardiovascularis) szövődmények döntően a 2-es típusú cukorbetegségre jellemzőek. Mindazonáltal cardiovascularis megbetegedések kialakulhatnakaz 1-es típusú diabetes kórlefolyása során is, főleg micro-, vagy macroalbuminuriával kísért nephropathia diabetica esetén. Napjainkban az 1-es típusú diabetes mellitusban is a cardiovascularis betegségek állnaka haláloki statisztikák élén. Fontos körülmény, hogy a 2-es típusú diabetes manifesztálódását megelőzően, a csökkent glukóztolerancia (IGT) stádiumában is fokozott a cardiovascularis megbetegedések kialakulásának kockázata. Ez utóbbi tény magyarázata a metabolikus szindróma koncepciójában rejlik.
5.1. Retinopathia diabetica
A retinopathia diabetica a diabetes mellitus idült, microangiopathiás szövődménye, amely látásromlással, szerencsétlen esetben pedig teljes látásvesztéssel fenyegeti az érintett beteget. A szövődmény megelőzésének lehetősége elsősorban a cukorbetegeket gondozó orvosoknak (diabetológusnak, belgyógyásznak, háziorvosnak) a kezében van, a már kialakult szövődmény kezelésében a szemész szakorvosok és a diabetológusok együttműködése szükséges.
A retinopathia diabetica kialakulásában a diabetes-tartamnak és az anyagcsere-helyzetnek van döntő jelentősége. Noha a retinopathia gyakorisága az elmúlt egy-két évtizedben - feltehetően a jobb terápiás lehetőségek miatt -csökkenő tendenciát mutat, számos országban még ma is a retinopathia diabetica képezi az újonnan kialakuló vaksági esetek leggyakoribb okát. A proliferativ retinopathia incidenciája nagyobb az 1-es típusú, mint a 2-es típusú cukorbetegekben, ezzel szemben a macula oedema incidenciája nagyobb a 2-es típusú, mint az 1-es típusú cukorbetegekben.
A diabetes mellitus diagnózisakor retinopathia nem észlelhető az 1-es típusú betegekben. Általában 3-5 év után várható a retinopathia első jeleinek megjelenése. Ezzel ellentétben a 2-es típusú diabetesben szenvedőknél a cukorbetegség kórisméjének megállapításakor már jelen lehet a retinopathia enyhébb, vagy súlyosabb formája, aminek magyarázatát e diabetes-típus jól ismert, lappangó fejlődése adja. Egyöntetű a vélemény ezért, hogy a 2-es típusú cukorbetegségben szenvedőknél a diabetes diagnózisakor indokolt a szemészeti vizsgálat, s ellenőrzésre legalább évente egy alkalommal célszerű sort keríteni. A hazai gyakorlat nem tesz éles különbséget az ellenőrzés gyakoriságánakszükségességét illetően az 1-es és a 2-es típusú diabetes között, s ezért, ill. az egységes elv könnyebb követhetősége érdekében, az évenkénti legalább egy alkalommal történő szemészeti konzíliárusi vizsgálat indokolt minden cukorbeteg esetében. A diabetes már kialakult szemészeti szövődményei esetén az ellenőrzés gyakoriságát a szemész szakorvos állapítja meg.
A retinopathia diabetica kórlefolyásában négy stádium különíthető el (prae-retinopathia, nonproliferatív vagy háttér-retinopathia, prae-proliferatív retinopathia, proliferatív retinopathia). Az egyik stádiumból a következő stádiumba való átmenet folyamatos. Jellemző, hogy látási panasza kórfejlődés kezdetén szinte nincs, míg a kórlefolyás végén gyakorlatilag teljes látásvesztés alakulhat ki.
A retinopathia diabetica kórlefolyásában az alábbi tényezők szerepe bizonyított: tartós hyperglykaemia, hypertonia, szérum lipideltérések, terhesség.
Gyógyszeres kezelési lehetőségek a diabetológiai gondozás során
A retinopathia diabetica kialakulásának megelőzésében, ill. a progresszió kockázatának csökkentésében a minél tökéletesebb anyagcsere-egyensúlyra való törekvés, a közel normoglykaemia (ideális esetben a tényleges normoglykaemia) tartós biztosítása a döntő tényező. Meg kell említeni azonban, hogy az anyagcsere gyors rendezésére való törekvés a retinopathia átmeneti romlását okozhatja, ezért kellő türelemmel és óvatossággal kell a cukorbetegek anyagcsere-vezetését végezni.
Néhány nagy klinikai tanulmány igazolta, hogy a szorosabb vérnyomáskontroll csökkenti a retinopathia progresszióját, a lézer-kezelés szükségességét és a látásromlás mértékét. Egyes ACE-gátlók (lisinopril, ramipril) és ARB-k(candesartan) bizonyos fokú eredményességét külön tanulmányok dokumentálták.
A thrombocytaaggregáció-gátló szerek (aszpirin, dipyridamol,ticlopidin,clopidogrel) nem vonultak be a retinopathia diabetica gyógyszeres kezelési lehetőségei közé. Ha egy cukorbeteg esetében bármely okból (legtöbbször cardiovascularis prevenció céljából) indokolt az aszpirin adása, az esetleg jelen lévő retinopathia annak adását nem kontraindikálja. A retinopathia diabetica jelenléte nem képezi kontraindikációját a myocardialis infarctus acut ellátása kapcsán alkalmazott thrombolysisnek.
Az oxidatív stressz előnyös befolyásolását célzó, étkezési kiegészítésként alkalmazott antioxidáns komplex (C-vitamin, E-vitamin, béta-karotin) nincs hatással a retinopathia diabetica előfordulására, ill. progressziójára.
A hazánkban széles körben alkalmazott calcium-dobesilattal kapcsolatban néhány pozitív experimentális adat ismeretes, jelenleg azonban a calcium-dobesilattal kapcsolatban evidenciákkal alátámasztott ajánlás nem fogalmazható meg, miután nem állnak rendelkezésre kontrollált, randomizált, prospektív vizsgálatok eredményei.
Szemészeti kezelési lehetőségek
A retinopathia diabetica tényleges kezelési lehetősége a szemész szakorvos kollégák kezében van. Több tanulmány egyértelműen igazolta, hogy a lézer-terápia a retinopathia diabetica hatékony kezelési módját jelenti. Előrehaladott esetekben a vitrectomia jelenthet a betegek számára segítséget.
Retinopathia diabetica a diabetológiai gondozásban - evidenciák, ajánlások
A terhesség a retinopathia diabetica kórlefolyását előnytelenül befolyásolhatja, az aszpirinterápia nem fokozza a szemészeti vérzés gyakoriságát, ezért
- Ismert cukorbeteg tervezett terhessége előtt szemészeti szakvizsgálat szükséges ("A");
- Cukorbetegek más okból indokolt aszpirinterápiáját a retinopathia jelenléte nem kontraindikálja ("A").
A retinopathia diabetica kialakulása és kórlefolyása összefüggést mutat a hyperglykaemiával, a hypertoniával és a kóros szérum lipidértékekkel, ezért a retinopathia diabetica kialakulása és progressziója előnyös befolyásolása érdekében
- Cukorbetegekben minél tökéletesebb anyagcsere-egyensúlyra kell törekedni ("A");
- Cukorbetegekben korrekt antihypertensiv kezelést kell folytatni ("A");
- Cukorbetegek lipideltérései megfelelő módon kezelendők ("A").
A retinopathia diabetica átmeneti romlását okozhatja a gyors vércukor-korrekció, ezért
- A minél tökéletesebb anyagcsere-egyensúly elérését célzó terápia során a magasabb vércukorértékek fokozatos csökkentésére kell törekedni ("A").
5.2. Nephropathia diabetica
A nephropathia diabetica egy olyan klinikai entitás, amelyre a fokozatosan növekvő albuminuria, az emelkedő vérnyomás és a csökkenő glomeruláris filtrációs ráta a jellemző. Patomorfológiailag a háttérben a klasszikus adatok alapján a Kimmelstiel-Wilson-féle intercapilláris (nodularis) glomerulosclerosis áll, noha ma már tudjuk, hogy a diffúz glomerusclerosis gyakoribb, s ismert az is, hogy a kezdeti klinikai eltérések hátterében olykor csak elektronmikroszkópos vizsgálattal felismerhető elváltozások mutathatók ki.
Nephropathia diabetica kialakulására számíthatunk mind 1-es típusú, mind 2-es típusú diabetesben szenvedők esetén. A szövődmény előfordulási gyakorisága függ a diabetes típusától és a diagnosztikai kritériumtól. Nyilvánvaló, hogy más számértéket kapunk a prevalencia-adatok meghatározásakor, ha csak a klinikailag manifeszt (macroalbuminurával jellemzett) nephropathiát tekintjük, vagy ha figyelembe vesszük a korai vesekárosodás (microalbuminuriával jellemzett) stádiumát is. A micro- vagy macroalbuminuria 1-es típusú diabetesben igen nagy (kb. 95%-os) valószínűséggel nephropathia diabetica utal, 2-e típusú diabetesben azonban e kóros paraméter számottevően alacsonyabb specificitással jelzi a veseérintettség diabeteszes eredetét. Ez az adat arra utal, hogy 2-es típusú diabetesben szenvedő betegek albuminuriájának hátterében az esetek bizonyos hányadában nem nephropathia diabetica, hanem más, belgyógyászati jellegű idült vesebetegség áll.
A nephropathia diabetica kialakulásában több tényező szerepet kap. Noha genetikai tényezőknek és a dohányzásnak részoki jelentősége lehet a szövődmény kialakulásában, nem vitatott módon a tartós hyperglykaemiának és a megváltozott haemodinamikai viszonyoknak van döntő szerepe a kórfolyamat elindításában és fenntartásában. Az előnytelen metabolikus és haemodinamikai hatások renális következményei egymástól élesen nem különülnek el.
A nephropathia diabetica évekre-évtizedekre elhúzódó kórlefolyással, kezelés nélkül, vagy elégtelen kezelés mellett végstádiumú veseelégtelenség kialakulásába torkollik. A nephropathia diabetica kórfejlődése során öt jól körülhatárolható stádiumot lehet elkülöníteni, amely 1-es típusú diabetesben könnyen azonosítható, 2-es típusú diabetesben azonban - a diabetes lappangó kezdete és az albuminuria kevésbé specifikus volta miatt - a stádium-meghatározás nehézségekbe ütközhet, különösen a kórfejlődés kezdetén. A stádium-besoroláshoz jól használható a szérum kreatininértéke alapján becsült GFR-érték (estimated GFR: eGFR).
A nephropathia diabetica a cardiovascularis megbetegedések fokozott kockázatával jár együtt. A microalbuminuria nemcsak a macroalbuminuria (azaz a veseszövődmény progressziója) szempontjából, hanem a társuló cardiovascularis megbetegedéseket tekintve is prediktív tényezőnek minősül. Ez a tény mind 1-es, mind 2-es típusú diabetesben bizonyított. A microalbuminuria az általános vascularis (endothel) károsodás jeleként értékelhető.
5.2.1. A nephropathia diabeticában szenvedő cukorbetegek belgyógyászati (diabetológiai) gondozása
A tartós közel-normoglykaemia biztosításának jelentőségét mind 1-es, mind 2-es típusú diabetesben több, randomizált, kontrollált klinikai vizsgálat igazolta. Nephropathia diabetica előrehaladottabb stádiumában szenvedő cukorbetegeknél a kezelési vércukor- és HbA1c-célértéket általában csak inzulinkezeléssel lehet megvalósítani. Az emelkedő szérum kreatininérték (ill. a csökkenő GFR) határt szab az orális antidiabeticumok alkalmazhatóságának, mert ez a körülmény a legtöbb szer (a májon keresztül metabolizálódó gliquidon [Glurenorm®] kivételével) adásának kontraindikációját jelenti. Bármely okból veseműködési zavarban szenvedő cukorbeteg esetleges orális antidiabeticus kezelése esetén az adhatóságot, ill. a potenciális dózisredukciót az adott készítmény alkalmazási előirata alapján kell megállapítni. Általánosságban véve leszögezhető, hogy nephropathia diabetica esetén az inzulinkezelés preferálandó. Progresszió (szérum kreatinin emelkedése) esetén általában az inzulindózis fokozatos csökkentése válik szükségessé.
Az antihypertensiv kezelés kiemelt jelentőségét több randomizált, kontrollált klinikai vizsgálat igazolta, mind 1-es, mind 2-es típusú diabetesben. Az antihypertensiv kezelés célértéke diabetes mellitusban <130/80 Hgmm, nephropathia diabetica (fehérjeürítés >1g/die) esetén azonban <125/75 Hgmm elérésére kell törekedni (ha azt a beteg tolerálja). Ezt a célt antihypertensiv monoterápiával gyakorlatilag elérni nem lehet, így az esetek szinte mindegyikében kombinált antihypertensiv terápiát kell folytatni.
A statin-kezelés eredményességét idült veseelégtelenségben szenvedő betegekben igazolták. Helyes, ha a kezelés minél korábbi stádiumban történik, mert végstádium esetén e terápia előnye már kétséges. Fontos, hogy beszűkült vesefunkció esetén különös óvatosság szükséges a statin megválasztásakor, s dózisának meghatározásakor, a súlyos mellékhatások elkerülése érdekében.
Végstádiumú veseelégtelenségben szenvedők nephrologiai gondozásához az anaemia korrekciója hozzátartozik. Ez a korrekció előnyös a veseszövődmény kevésbé előrehaladott stádiumában is. A vérképben a Hb kezelési célértéke 11-12 g/dl, a kezelés megkezdése a 10-11 g/dl tartományban indokolt. Az anaemia korrekciója az életminőséget javítja, a cardiovascularis események alakulására azonban nincs befolyással, sőt a túlzott korrekció olykor kedvezőtlen is lehet.
Aszpirin adása indokolt a cukorbetegek cardiovascularis szövődményeinek szekunder prevenciója érdekében. Micro-vagy macroalbuminuria detektálása esetén aszpirin adandó a primer cardiovascularis prevenció érdekében.
A nephropathia diabetica belgyógyászati kezelésekor a betegeknek általában a napi <0,8 g/ideális testsúlykg fehérjebevitelt tanácsoljuk. A nephrologiai gondozás stádiumában a fehérjebevitel ezen általános előírása a kórlefolyás stádiumával összefüggésben módosulni szokott. A sóbevitel korlátozása (napi 6 g só) előnyös a kellő mértékű vérnyomáscsökkentés érdekében. A dohányzás abbahagyása indokolt.
5.2.2. A diabetológiai gondozás összefoglalása, evidenciák - ajánlások
A nephropathia diabetica belgyógyászati (diabetológiai) gondozása során az alábbi teendők válnak szükségessé a kialakulás kockázatának csökkentése, a progresszió lassítása, a társuló cardiovascularis szövődmények megelőzése, ill. az életminőség javítása érdekében:
- Optimális (közel-normoglykaemia [ideális esetben tényleges normoglykaemia] megvalósítását célzó) szénhidrát-anyagcserekontroll tartós biztosítása ("A").
- Optimális (<130/80 Hgmm, nephropathia [fehérjeürítés >1g/die] esetén <125/75 Hgmm elérését célzó) vérnyomáskontroll biztosítása ("A").
- Nephropathia diabetica (albuminuria) esetén mind ACE-gátlók, mind ARB-k használhatók. Az antihypertensiv szerek között a RAS-gátlást biztosító készítményeknek (ACE-gátlók vagy ARB-k) kiemelt helye van, mert alkalmazásukkal a nephropathia progressziója mérsékelhető ("A").
- Ha az egyik hatástani csoportba tartozó szer (ACE-gátló vagy ARB) a beteg számára nem hozzáférhető, vagy azt a beteg nem tolerálja, akkor a másik hatástani csoportba tartozó szert kell választani ("D").
- Diabetesben micro-, vagy macroalbuminuria esetén, hypertonia hiányában is indokolt ACE-gátlót adni ("B") -intolerancia esetén ARB jön szóba ("B").
- Nephropathia diabetica esetén a vérnyomás-célérték a legtöbb esetben csak kombinált antihypertensiv kezeléssel érhető el, ezért
- az antihypertensiv kezelés során az ACE-gátló vagy ARB mellett helye van a dihydropyridin-típusú calciumantagonistáknak("B"),a nem dihydropyridin-típusú calciumantagonistáknakés béta-blokkoló szereknek, ill. a diuretikumoknak is ("D").
- Statin-kezelés csökkenti a nephropathia diabetica progresszióját és mérsékli a társuló cardiovascularis betegségek kockázatát ("A").
- A diétás fehérje-megszorítás csökkenti a GFR romlását ("B"), a belgyógyászati kezelés során a 0,8 g /ideális testsúlykg fehérjebevitelt érdemes tartani ("B").
- A társuló hypertonia nem-farmakológiai kezelésében a sóbevitel megszorítása (6 g/die) ajánlott (A").
- A dohányzás előnytelenül befolyásolja a nephropathia diabetica kórlefolyását, ezért a
dohányzás mellőzendő ("A").
- Idült renális elégtelenségben az anaemia korrekciója előnyös az életminőség javítása érdekében ("A"). A vérképben a Hb kezelési célértéke 11-12 g/dl, a kezelés megkezdése a 10-11 g/dl tartományban indokolt. Az anaemia korrekciója a cardiovascularis események alakulására nincs befolyással, sőt a túlzott korrekció olykor kedvezőtlen is lehet ("A").
- Micro- vagy macroalbuminuriával kísért 1-es és 2-es típusú cukorbetegekben a cardiovascularis megbetegedés kockázata fokozott, ezért e betegeket mind primer, mind szekunder prevenciós célzattal (ha nincs kontraindikáció) aszpirinkezelésben kell részesíteni ("A").
A nephropathia diabetica előrehaladottabb stádiumában a betegek kezelésében a nephrológusok kapnak egyre nagyobb szerepet, a vesepótló kezelés lebonyolítása terén, ill. adott esetben a vese-transzplantációra való előkészítésben.
5.3. Neuropathia diabetica
Általánosan elfogadott becslés szerint - pontos prevalencia-adatok hiányában - az ismert cukorbetegek kb. 1/3-a szenved a neuropathia okozta valamely panasztól, leggyakrabban diabeteszes polyneuropathiától. Panaszokat okozó neuropathiás szövődménnyel 1-es típusú diabetesben a betegség felismerését követő első években nem találkozunk. Ettől eltérően, újonnan felismert 2-es típusú cukorbetegekben neuropathiára utaló vizsgálati eltérés, vagy neuropathiás panasz már jelen lehet a betegség felismerésekor. A neuropathiás szövődmény érintheti a somaticus (sensoros és/vagy motoros működést biztosító) innervatiot, de károsodások alakulhatnak ki az autonom (cardiovascularis, gastrointestinalis, sexualis) idegrendszeri funkciók működésében, ill. zavart szenvedhetnek bizonyos élettani folyamatok (vasomotor-, sudomotor funkciók, hypoglykaemia-érzet).
A neuropathiás szövődmények kialakulását döntően metabolikus tényezők és/vagy vascularis okok magyarázzák. Újabb epidemiológiai jellegű megfigyelések szerint jelentősége van a társuló cardiovascularis kockázati tényezőknek is. Csak szórványos adatok vannak arra nézve, hogy a neuropathia kialakulásában immunológiai folyamatoknak, vagy genetikai faktoroknak lenne szerepe.
5.3.1. A gondozás során igénybe vehető alapvető diagnosztikus eljárások
A perifériás, distalis típusú, sensoros vagy sensomotoros polyneuropathia diabetica a beteg panaszai alapján könnyen felismerhető, ezért a diagnózis az esetek nagy részében a beteg alapos kikérdezését követően már megalapozottan gyanítható. A kórisme megállapítását segíti a vibrációérzés csökkenésének azonosítása kalibrált hangvilla segítségével. A hazai gyakorlatban a 128 Hz-es Rydel-Seiffer féle hangvilla használatos, amellyel a vibrációérzés (mélyérzés [pallaesthesia]) zavara könnyen detektálható. A gondozási gyakorlatban további, egyszerű vizsgáló módszert jelent a 10 g súlyú Semmes-Weinstein monofilamentum használata, melynek segítségével a talpak területén a protektív érzés könnyen vizsgálható. Az autonom neuropathia jelenléte a cardiovascularis reflextesztekkel vizsgálható a legkönnyebben. Miután a polyneuropathia diabetica alapvető jelentőséggel bír a diabeteszes láb szindróma kialakulásában,a diabetes felismerésekor, ill. a beteg első megjelenésekora teljes körű fizikális vizsgálathoz hozzátartozik a láb vizsgálata (talp, deformitások, gombásodás, neuropathia ellenőrzése, perifériás artériák tapintása [bizonytalan esetben a Doppler index meghatározása]), amely a gondozás során legalább évente egy alkalommal megismétlendő ("D").
5.3.2. Terápiás lehetőségek
A neuropathia diabetica kezelésében jelenleg egyetlen olyan gyógyszer sem áll rendelkezésünkre, amelyről igazolták volna, hogy a háttérben álló patomorfológiai elváltozásokat (myelinhüvely pusztulása,axon-degeneráció) stabilizálná, vagy visszafordítaná.
A neuropathia kezelésének megkezdése előtt minden egyéb társuló kóroki tényezőt (pl. alkoholfogyasztás) ki kell iktatni. Indokolt a cardiovascularis kockázati tényezők megfelelő kezelése is.
Az oki terápiás lehetőségek tengelyében az anyagcsere megfelelő kontrollja (a közel-normoglykaemia tartós biztosítása) áll (A"). Oki terápiás lehetőségként szerepel az alfa-liponsavalkalmazása ("A"). A benfotiamin a legújabban felderített hatásmechanzimus alapján szintén oki terápiás lehetőségként tartható számon, a polyneuropathia diabetica egyes kóros vizsgálati paraméterei benfotiamint is tartalmazó B-vitamin kombinációval javíthatók ("C").
A tüneti kezelés lehetőségei sokfélék.
A gondozási gyakorlatban
- közönséges fájdalomcsillapítók (aszpirin, paracetamol) adását egyes esetekben nem lehet nélkülözni;
- triciklikus antidepresszánsok előnyösen befolyásolják a fájdalomküszöböt, s enyhítik a beteg panaszát;
-a carbamazepin (eredetileg antiepileptikum) régi szer, fájdalmas neuropathiában érdemes adásával kísérletet tenni;
- a gabapentin membránstabilizáló antiepileptikum, neuropathia diabeticában inkább a magasabb dózisok hatásosak, fájdalmas neuropathiában használatos;
- a pregabalin a gabapentin továbbfejlesztett változata, szintén fájdalmas neuropathiában használatos;
- a phenytoint elsősorban antiepileptikumként alkalmazzák, előnyét neuropathia diabeticában kontrollált vizsgálat igazolta;
- a nátrium valproát (antiepileptikum) hatékonyságát kisebb, kontrollált vizsgálatban igazolták;
- a duloxetin kettős re-uptake gátló, használatát fájdalommal járó neuropathia diabeticában regisztrálták;
- a mexiletin és a lidocain elsősorban a kardiológiában használatos antiarrhytmicumok, néhány tanulmány azonban arra hívta fel a figyelmet, hogy fájdalmas neuropathiában adásuk előnyös lehet, szoros ellenőrzés mellett, olykor parenteralis formában, kórházi körülmények között;
- a capsaicin kenőcs formájában, lokálisan alkalmazva a zsibbadásos, kellemetlen végtagpanaszokat enyhítheti;
- kisebb klinikai vizsgálatokban az alábbi gyógyszereket tesztelték még: nem steroid gyulladáscsökkentők, fluoxetin (SRRI típusú antidepresszáns), tramadol (opioid típusú fájdalomcsillapító), levodopa (antiparkinson szer) lisinopril, trandolapril, quinapril (ACE-gátlók), isosorbid-dinitrát spray lokálisan;
- válogatott esetekben a kezelésben helye lehet nem farmakológiai módszereknek (transzkután elektromos ingerlés, akupunktúra) is.
A fenti lehetőségeket áttekintve a hazai gyakorlatban (tekintettel az alkalmazási előiratban rögzített indikációkra is) tüneti szerként elsősorban az alábbi készítmények használatosak: pregabalin (Lyrica®), duluxetin (Cymbalta®), gabapentin (Gordius®, Gabagamma®).
Az oki és a tüneti kezelés lehetőségei a jobb terápiás eredmény elérése érdekében egymással kombinálhatók ("D").
5.3.3. Önálló klinikai kórformák terápiája
Orthostaticus hypotonia esetén fokozni kell a folyadék- és sóbevitelt, a diuretikumokat és az alfa-adrenerg blokkoló szereket kerülni kell, napközben célszerű a betegnek rugalmas harisnyát viselnie, s alváskor az ágy fejvégét megemelnie. A gyógyszerek közül a fludrocortison ajánlott elsősorban, hatását a plazmavolumen megnövelésével fejti ki. Történtek vizsgálatok pindollal (az intrinsic sympathomimeticus tulajdonságtól remélt hatás okán), indometacinnal, nem diabeteszes betegcsoportban erythropoetinnel, ill. az alfa-agonista tulajdonságú midodrinnel.
A gyomor- és bélrendszer csökkent motilitása esetén a kezelésben helye lehet metoclopramid, domperidon és erythromycin adásának is. A cizapridot a piacról visszavonták EKG-rendellenességet (QT-távolság megnyúlását) provokáló hatása miatt. Agastroparesis diabeticorum súlyosabb esetei feltétlen kórházi kezelést igényelnek, egyrészt az antidiabeticus kezelés optimális megválasztása, másrészt a parenteralis folyadék- és ionbevitel szükségessége miatt. Elkeseredett helyzetekben eletromos stimulálás, vagy műtéti megoldás mérlegelése is szóba jön ("D").
Az enteropathia diabetica (diabeteszes diarrhoea) a tüneti szereken kívül per os tetracyclin (egyes esetekben metronidazol) adásával enyhíthető, szerencsére a tünetek spontán remissziójára is számítani lehet. Nehezen befolyásolható esetekben kísérlet tehető clonidinnal, cholestyraminnal, metronidazollal, ill. somatostatin-analóggal (octreoid) ("D").
Azerectilis diszfunkció kezelésében ma a foszfodieszteráz-5-gátló szereknek (sildenafil [Viagra®], vardenafil [Levitra®], tadalafil [Cialis®]) van kiemelt jelentősége ("A").
5.3.4. A polyneuropathia diabetica terápiája - ajánlások
A hazánkban elérhető gyógyszereket, alkalmazási előirataikat és az általános gyakorlatot tekintve az alábbi ajánlások fogalmazhatók meg:
- A neuropathiás szövődmények kialakulásánakés progressziójának kockázata az anyagcsere-helyzet rendezésével, a tartós közel-normoglykaemia biztosításával mind 1-es, mind 2-es típusú diabetesben csökkenthető ("A").
-A neuropathia okozta panaszokés idegrendszeri deficittünetek alfa-liponsav(Thiogamma®) parenteralis vagy peros adásával csökkenthetők ("A").
-A polyneuropathia diabetica egyes kóros vizsgálati paraméterei benfotiamint is tartalmazó B-vitamin kombinációval (Milgamma N®, nagyobb napi dózissal és 3 hónapon keresztüli kezeléssel) javíthatók ("C").
- A panaszokat okozó perifériás polyneuropathia tüneti kezelésében helye van pregabalin (Lyrica®), duloxetin (Cymbalta®), vagy gabapentin (Gordius®) tabletta adásának, mert alkalmazásuk során a kellemetlen panaszok, elsősorban a fájdalom csökken ("A").
Az oki és tüneti kezelés gyógyszerei a jobb terápiás eredmény érdekében egymással kombinálhatók ("D").
5.4. Macroangiopathia diabetica - cardiovascularis szövődmények diabetes mellitusban
Cukorbetegségben a cardiovascularis megbetegedések kialakulásának kockázata - a nem-cukorbeteg populációhoz viszonyítva - fokozott. A cardiovascularis kockázat megítélésekor a kórelőzményben dokumentált diabetes mellitus súlya egyenértékű három más kockázati tényező, vagy egy célszerv-károsodás jelenlétével. Szélsőséges megfogalmazás szerint a 2-es típusú diabetes olyan cardiovascularis megbetegedés, amelyet hyperglykaemia jelenléte kísér.
A diabetesben kialakuló atherosclerosis klinikai kórformái között kiemelt jelentőségűek a coronariák érintettségén alapuló megbetegedések, a cerebrovascularis szövődmények és az alsó végtagi artériás keringési zavar következményei. Az atherosclerosis kórfejlődéséből adódóan az egyik érterületen mutatkozó kórképek észlelése esetén joggal feltételezhető, s ezért vizsgálandó a szervezet egyéb érterületeinek érintettsége is. A cardiovascularis kockázat már a diabetes előállapotaiban (IGT, IFG) is fokozott.
5.4.1. A koszorúér atherosclerosisának klinikai következményei diabetes mellitusban
A cukorbetegek szívműködési zavarának (ischaemiás szívbetegség, myocardialis infarctus) hátterében a legnagyobb jelentősége a coronariák atheroscleroticus elváltozásának van, noha a szívműködési zavar klinikumához hozzájárul a cukorbetegségben észlelhető szekunder szívizom-károsodás (cardiomyopathia diabetica), ill. a diabeteszes neuropathia részjelenségeként megmutatkozó cardiovascularis autonóm neuropathia is.
Myocardialis infarctusra gyanús tünetek észlelése esetén a betegek azonnali hospitalizációja indokolt. Az időfaktornak nagy jelentősége van, ezért acut esetben sürgősségi szállítással a beteget olyan kardiológiai centrumba kell irányítani, ahol az azonnali coronarographiára, s a lelet alapján szükségessé váló ténykedésekre (PCI: percutan intervenció) adottaka lehetőségek. Cukorbetegekben a myocardialis infarctus gyakran fájdalom nélkül, vagyatípusos panaszokkal alakulhat ki.
Cukorbetegekben a myocardialis infarctus acut szakában egyértelműen inzulinkezelés indítandó, s ezt a kezelésmódot a DIGAMI-tanulmány eredményei alapján tartósan folytatni kell ("A"). Noha a DIGAMI-2 vizsgálat eredményei nem erősítették meg a korábbi DIGAMI eredményeit, szakértői ajánlási szinten infarctust szenvedett cukorbeteg esetében az antidiabeticus terápia a későbbiekben is elsősorban inzulinkezelést jelent ("D").
Infarctust szenvedett cukorbetegek antidiabeticus kezelésével kapcsolatban az alábbi ajánlás fogalmazható meg:
- Heveny myocardialis infarctust szenvedett cukorbetegek inzulinkezelése indokolt, az inzulinkezelést az infarctus átvészelése után legalább három hónapig fenntartani célszerű ("A"). Az infarctus utáni inzulinkezelést helyesebb minél hosszabb ideig (véglegesen) folytatni, bár nem nehezményezhető az orális antidiabeticus kezelés folytatása akkor, ha az jó anyagcsere-helyzetet biztosít ("D").
5.4.2. Cerebrovascularis szövődmények diabetesben
A diabetes mellitus a cerebralis atherothromboticus szövődmények ismert kockázati tényezője. A cerebralis haemorrhágiás kórképekés a diabetes közötti kapcsolat nem bizonyított, utóbbi esetben a hypertonia patogenetikai szerepe a döntő.
Agyi érkatasztrófa észlelése esetén a beteg azonnali hospitalizációja indokolt, az ellátásra hazánkban stroke-centrumok szerveződtek. Az időfaktornak - a myocardialis infarctushoz viszonyítva - még nagyobb jelentősége van.
5.4.3. Alsó végtagi artériás keringési zavar diabetesben
Az alsó végtagi macroangiopathia diabetesben jellemző módon inkább distalis típusú, s sokszor szegmentális jellegű. A lábszár (sokszor a lábfej) artériáin occlusio nélkül is jelentős véráramlás-csökkenést okoz a gyakori-Mönckeberg-féle
- mediasclerosis. A klinikai képet gyakran színezi az egyidejűleg jelenlévő polyneuropathia diabetica. Az artériás keringési zavar megállapításában a perifériás erek tapintása, a Doppler-vizsgálat, a plethysmographia nyújthat segítséget. Tudományos igényű vizsgálatokban hasznosítják a laser-Doppler és a transcutan pO2-mérés lehetőségét. Invazív vizsgálatként az angiographia jön szóba.
Vascularis érintettség esetén a konzervatív terápia részeként kísérlet tehető a microcirculatiot befolyásoló gyógyszerek (pl. pentoxyphyllin), válogatott esetekben prostaglandin-készítmény adásával. Az angiographia lelete alapján angioplastica vagy helyreállító érműtét hozhat megnyugtató eredményt. A sympathectomia (sebészi vagy kémiai) hatásossága megkérdőjelezhető, ennek ellenére egyes esetekben ma is sor kerül alkalmazására. A terápiás lehetőségek kimerülésével - folyamatos progresszió esetén - csonkoló műtétre kényszerülünk.
5.4.4. Gondozói feladatok a macroangiopathiás szövődmények kezelése/megelőzése terén
A nem-farmakológiai intervenciónak (étrendi, életmódbeli tanácsok megfogadásának, a dohányzás kerülésének) igen nagy jelentősége van. Az anyagcsere-vezetés jelentőségét több nagy, randomziált, kontrollált klinikai vizsgálat analizálta. Az atherosclerosis kialakulásában és fenntartásában szerepet kapó hypertonia kezelésének, a lipid-eltérések korrigálásának, ill. a thrombocyta-aggregációt csökkentő terápiának a részletei a megfelelő fejezetekben lelhetők fel. A kezelést a globális cardiovascularis kockázat megállapításával kell kezdeni, s azt holisztikus szemlélettel, valamennyi kóros tényező egyidejű, kitartó, erélyes kezelésével kell folytatni.
A diabetológiai teendők az alábbiak szerint foglalhatók össze:
A diagnosztika terén évente legalább egy alkalommal
- EKG-vizsgálat végzése indokolt,
- a szérum lipideket (cholesterin, triglycerid, HDL-cholesterin) meg kell határozni,
- a lábak esedékes ellenőrzése kapcsán a perifériás ereket vizsgálni indokolt, ill. minden beteg-orvos találkozáskor
- a vérnyomást ellenőrizni szükséges (ajánlási szint: "D").
Az anyagcsere-egyensúlyelérése érdekében 1-es típusú diabetesben
- A tartósan jó anyagcsere-helyzetre való törekvés (alacsonyabb HbA1c-érték biztosítása)
- számottevően csökkenti a microangiopathiás szövődmények kialakulásának és progressziójának kockázatát,
- rövid távon szerény mértékben, hosszabb távon azonban értékelhetően csökkenti a macroangiopathiás szövődmények kialakulásának és progressziójának kockázatát, ezért e betegekben intenzív inzulinkezeléssel / pumpakezeléssel tartósan közel - normoglykaemia biztosítására kell törekedni ("A" szintű ajánlás)
2-es típusú diabetesben
- A tartósan jó anyagcsere-helyzetre való törekvés (alacsonyabb HbA1c-érték biztosítása)
- számottevően csökkenti a microangiopathiás szövődmények kialakulásának és progressziójának kockázatát,
- rövid távon szerény mértékben, hosszabb távon azonban értékelhetően csökkenti a macroangiopathiás szövődmények kialakulásának és progressziójának kockázatát, ezért e betegekben az adott helyzethez igazodó, várhatóan legeredményesebb antidiabetikus kezeléssel minél jobb anyagcsere-helyzet biztosítására kell törekedni ("A" szintű ajánlás).
A kezelési célértékeket a 3.5 fejezet részletezi.
Irodalom
1. Németh J: A szemészeti szövődmények terápiája diabetes mellitusban. Diabetologia Hungarica 12 Suppl 5: 22-28,
2005.
2. Jermendy Gy: A retinopathia diabetica prevenciója és kezelése a diabetológiai gondozás során. In: Jermendy Gy: Tényeken alapuló cukorbeteg-gondozás. Medicina Kiadó, Budapest, 2005, pp. 181-198.
3. Jermendy Gy: A nephropathia diabetica belgyógyászati (diabetológiai) terápiája. Diabetologia Hungarica 12 Suppl 5: 37-42, 2005.
4. Wittmann I, Szegedi J, Kalmár Nagy K, Nagy J: Beszűkült vesefunkciójú cukorbetegek antidiabetikus kezelése és előkészítése pancreas-vese transzplantációra. Diabetologia Hungarica 12 Suppl 5:43-51,2005.
5. Szegedi J: Vesepótló kezelés diabeteszes vesebetegekben. Diabetologia Hungarica 12 Suppl 5: 52-59, 2005.
6. Kempler P: A neuropathiák terápiája. Orv Hetil 145:1145-1147, 2004.
7. Jermendy Gy: A neuropathia diabetica diagnózisa és terápiája a gondozási gyakorlatban. In: Jermendy Gy: Tényeken alapuló cukorbeteg-gondozás. Medicina Kiadó, Budapest, 2005, pp. 199-227.
8. Tamás Gy, Kerényi Zs: Az erektilis diszfunkció terápiája diabetes mellitusban. Diabetologia Hungarica 12 Suppl 5: 11-21, 2005.
9. Kempler P: Cardiovascularis kockázatbecslés, kezelés célértékek, kezelési stratégia - a szemlélet és az ajánlások változása napjainkban. Diabetologia Hungarica 12 Suppl 4:12-19,2004.
10. Pécsvárady Zs: A perifériás érbetegségek kezelése diabetes mellitusban. Diabetologia Hungarica 12 Suppl 3: 5-14, 2004.
11. Jermendy Gy: Szív- és érrendszeri megbetegedések megelőzése diabetes mellitusban. 1. A primer prevenció gyógyszerei. Diabetologia Hungarica 11: 235-247, 2003.
12. Jermendy Gy: Szív- és érrendszeri megbetegedések megelőzése diabetes mellitusban. 2. A secunder prevenció gyógyszerei. Diabetologia Hungarica 12: 5-17, 2004.
13. Jermendy Gy: Hypertonia diabetológus szemmel. Melánia Kiadó, Budapest, 2007.
14. Kempler P, Várkonyi T: Neuropathia diabetica 2007 - fókuszban a fájdalommal járó
15. neuropathiák kezelése. Diabetologia Hungarica 15 (Suppl. 1): 29-40,2007.
16. Jermendy Gy: A szív-és érrendszeri megbetegedések kockázatát csökkentő terápia késői
17. hatásai. A kardiometabolikus terápiás memória hipotézise. LAM 18:459-466, 2008.
18. Jermendy Gy: Metabolikus memória diabetes mellitusban. Magyar Belorv Arch 61:361-367,2008.
6. Diabeteshez társuló kóros állapotok/kísérő betegségek kezelése 6.1. Dyslipidaemia
Az 1-es típusú diabetesben nincs sajátos lipideltérés, ill., ha van, az csupán másodlagos: a diabetes nem tökéletes kezelésének a következménye. Jól beállított 1-es típusú cukorbetegekben a lipidszintek lényegében normálisak (sőt: inzulinkezelés mellett a szérum triglyceridszint gyakran alacsonyabb és a HDL-cholesterin értéke magasabb, mint a korosztálynak megfelelő kontroll érték).
A 2-es típusú cukorbetegségben viszont gyakran figyelhetők meg jellegzetes lipideltérések. Ezek a kóros értékek eltérések már a diabetes manifesztációja előtt is kimutathatók, helyesebb tehát ezeket a metabolikus szindróma jellegzetes lipideltéréseiként tekinteni (a jellegzetes dyslipidaemia döntően az inzulinrezisztenciának a következménye). Ezekazeltérésekaz alábbiak: elhúzódó posztprandiális lipaemia, fokozott hepatikus VLDL-szekréció, magas szérum triglycerid- és alacsony HDL-cholesterinszint, ill.az LDL-cholesterin kvalitatív eltérése (a kicsiny, denz [small dens] LDL aránya növekedése).
6.1.1. A lipidcsökkentő kezelés célértékei
Az emelkedett lipidszintek szignifikánsan növelik - a diabetesben amúgy is fokozott - cardiovascularis kockázatot. Ezért a lipidszinteket olyan határértékalá kell csökkenteni, ahol a cardiovascularis kockázat már nem számottevő, és az artériafalban lévő plakk növekedése megáll, esetleg regresszió is kialakul.
Nemzetközi konszenzus szerint 2-es típusú diabetesben (és metabolikus szindrómában) a lipidszintek célértékei a következők: LDL-cholesterin <2,5 mmol/l, triglycerid <1,7 mmol/l, HDL-cholesterin férfiakban >1,1 mmol/l és nőkben >1,3 mmol/l. Igen nagy cardiovascularis kockázat esetén az LDL-cholesterin kezelési célértéke még alacsonyabb
(<1,8 mmol/l). Ilyen kiemelten nagy cardiovascularis kockázatot jelent a 2-es típusú diabetes, ill. a metabolikus szindróma akkor, ha hozzájuk igazolt cardiovascularis betegség, akut coronaria szindróma vagy jelentős cardiovascularis kockázati tényező (pl. erős dohányzás) társul.
6.1.2. Lipidcsökkentő kezelési módszerek és ajánlási szintek
A terápia elsődleges célja az LDL-cholesterinszint csökkentése. Fontossági sorrendben ezt követi a HDL-cholesterin növelése, majd a triglyceridszint csökkentése.
Mint minden anyagcserebetegségben, az első kezelést az életmód-terápia - orvosi táplálkozási terápia + rendszeres fizikai aktivitás - jelenti. Ennek alkalmazása természetesen már a diabetes miatt is kötelező. A dyslipidaemia diétás kezelésekor fontos szempont, hogy a napi kalória-bevitelnek max. 30%-át képezhetik a zsírféleségek, ezen belül max. 7% lehet a telített zsírok aránya. A transz-zsírsavak bevitelét a lehetséges minimumra kell csökkenteni. Súlyfelesleg esetén alapvető a testsúly csökkentése. A hatékony életmód-terápia csökkenti a testsúlyt, a triglyceridszintet és növeli a HDL-cholesterin értékét ("A").
Amennyiben életmód-terápiával nem sikerül a célértékeket elérnünk, gyógyszeres kezelést kell indítani. Az első kezelést a statinterápia jelenti, mert az LDL-cholesterinszintet ez a vegyület csökkenti a legerősebben. Ezen kívül a statinkezelés bizonyítottan csökkenti a cardiovascularis halálozást ("A") és az össz-halálozást ("A"), nagy dózisban adva megállítja a plakk növekedését ("A") és hatékony statinvegyület adása plakkregressziót is eredményezhet ("A").
Diabeteszes dyslipidaemiában a következő meggondolások alkalmazandók:
- ha az LDL-cholesterin szintje >3,4 mmol/l, akkor az életmód-terápiával együtt statinkezelést kell indítani;
- ha az LDL-cholesterinszint 2,5-3,4 mmol/l között van és nincs cardiovascularis szövődmény, akkor az életmód-terápiát kell alkalmazni, de ha néhány hónap alatt az LDL-cholesterin szint 2,5 mmol/l felett marad, statinkiegészítés szükséges;
- ha az LDL-cholesterin 2,5 mmol/l felett van és cardiovascularis szövődmény áll fenn, haladéktalanul statinkezelést kell indítani ("A"); az LDL-cholesterin további csökkentése (<1,8 mmol/l) növeli a vasculoprotectiv hatást ("B");
- statinterápia javasolt a lipidszintektől függetlenül is, ha igazolt cardiovascularis betegség áll fenn ("A"), vagy cardiovascularis betegség nélkül, ha a beteg elmúlt 40 éves, és egy vagy több cardiovascularis kockázati tényezővel rendelkezik ("A");
- mérlegelendő a statinterápia bevezetése 40 év alatt is, igazolt cardiovascularis betegség esetén, ill. cardiovascularis betegség nélkül is, ha egy vagy több cardiovascularis kockázati tényező van jelen és/vagy az LDL-cholesterin >2,5 mmol/l ("D");
- bár a fenti megállapítások a 2-es típusú diabetesre vonatkoznak, célszerű a statinkezelést elkezdeni 1-es típusú cukorbetegségben is, ha nephropathia alakult ki, vagy ha igazolt cardiovascularis betegség áll fenn és az LDL-cholesterin >2,5 mmol/l;
Ha a kívánt LDL-cholesterin-célértéket statin-monoterápiával nem sikerül elérni, akkor legalább a kiindulási érék 50%-os csökkentésére kell törekedni. Felmerül egyúttal a kombinációs kezelés (ezetimib [Ezetrol®]) bevezetésének lehetősége. A statinkészítményhez adott ezetimib (Ezetrol®) az LDL-cholesterin további 15-26%-os csökkenését eredményezi (de jelenleg még nincs bizonyítékarra nézve, hogy ez egyúttal a cardiovascularis események kialakulását is csökkentené, vagy azok kimenetelét javítaná).
Ezetimib (Ezetrol®) adható első kezelésként is, ha az egyébként indokolt statinterápia mellékhatások miatt nem alkalmazható.
Az alacsony HDL-cholesterinszint emelhető rendszeres testmozgással,a dohányzás elhagyásával. Ha a célértéket nem érjük el, fibrátterápia javasolt. HDL-szint emelő hatású a nikotinsav is, de hazánkban egyelőre nem áll rendelkezésre sem elhúzódó hatású, sem "flush-mentes" (prostaglandin-D2-receptor antagonistával kiegészített) nikotinsav-készítmény.
Igen magas (>4,5 mmol/l) triglyceridszint esetén statin-fibrát kombináció javasolt. Ilyenkor a mellékhatásokra (myositis, rhabdomyolysis) fokozottan figyelni kell (rendszeres CK- és ALAT-ellenőrzés szükséges). A kombinációs kezelésre fenofibrát(Lipidil®) ajánlott, mert kevésbé fokozza a statin-mellékhatásokat, mint a gemfibrozil (Innogem®).
Magas (>4,5 mmol/l) triglycerid-és céltartományban lévő LDL-cholesterinszint esetén fibrát lehet az első antilipaemiás gyógyszer. Fontos a szénhidrátháztartás rendezése és az egyéb triglycerid-emelő tényezők (dohányzás, alkohol, fruktóz-bevitel) elhagyása.
Irodalom
1. Gerő L: Lipidanyagcsere zavarok cukorbetegségben. I. A diabetesre jellemző lipideltérések és azok patomechanizmusa. Diabetologia Hungarica 6:66-76,1998.
2. Romics L, Szollár L, Karádi I, Pados Gy, Paragh Gy (Magyar Atherosclerosis Társaság Munkabizottsága): Összefoglalása hyperlipoproteinaemiák kezelési irányelveiről. Metabolizmus 1: 2-4, 2003.
3. Paragh Gy, Balogh Z: A kockázatbecslésen alapuló lipidszintcsökkentő terápia. LAM 14: 747-752, 2004.
4. Paragh Gy, Harangi M: Evidence based vizsgálatok a lipidológiában. Metabolizmus 2: 2-7, 2004.
5. Grundy SM,Cleeman JI, Merz CN, Brewer HB,Clark LT, Hunninghake DB, Pasternak RC, Smith SC, Stone NJ: Implications of recent clinical trials for the National Cholesterol Education Program Adult Treatment Panel III guidelines. Circulation 110:227-239, 2004.
6. Paragh Gy, Balogh Z: Diabeteses dyslipidaemia. Orvostovábbképző Szemle különszám, 2008.
7. Jermendy Gy, Winkler G: AIII. Magyar Kardiovaszkuláris Konszenzus Konferencia a koszorúér-eredetű, agyi és perifériás érbetegség kockázatának becslésére, megelőzésére és kezelésére. Diabetol Hung 16: 29-34,2008.
6.2. Hypertonia diabetes mellitusban
Cukorbetegségben gyakran észlelhető hypertonia. A hypertonia kialakulásának patomechanizmusa a diabetes két alapvető típusában egymástól eltér. Míg 1-es típusú diabetesben a hypertonia a diabeteszes nephropathia egyik jellemző tüneteként van jelen, addig 2-es típusú diabetesben a hypertonia kialakulását a metabolikus szindróma koncepciója alapján értelmezzük. Nephropathiához társuló hypertonia azonban kialakulhat 2-es típusú diabetesben is.
A hypertoniás cukorbetegek antihypertensiv kezelése nagy jelentőségű. Meggyőző klinikai tanulmányok igazolták, hogy diabetesben a korrekt antihypertensiv kezelés a macroangiopathiás szövődmények visszaszorítását eredményezi és ez a ténykedés előnyös a microangiopathiás szövődmények (nephropathia és retinopathia diabetica) kórlefolyását tekintve is.
A cukorbetegek hypertoniájának kezelési célértéke <130/80 Hgmm, renális károsodás (proteinuria >1g/die) esetén ennél alacsonyabb, <125/75 Hgmm elérésére kell törekedni (ha ezt az értéket tolerálja a beteg).
A nem-farmakológiai kezelésnek elsősorban a testsúlyfelesleggel rendelkező 2-es típusú cukorbetegek, vagy metabolikus szindrómában szenvedők esetén van nagy jelentősége. Az alapvető étrendi, életmódbeli előírások betartása (a túlsúly mérséklése, rendszeres fizikai terhelés beiktatása, sófogyasztás csökkentése, alkoholbevitel mérséklése, dohányzás abbahagyása) nemcsak a vércukor-, hanem a vérnyomásértékek alakulása szempontjából is előnyös. Általánosságban igaz, hogy minél kisebb a globális cardiovascularis kockázat, annál inkább előtérbe kerül az életmódbeli-étrendi előírás bevezetése (abban a reményben, hogy ez a ténykedés önmagában sikeres lesz), minél kifejezettebb a kockázat, annál inkább azonnali gyógyszeres antihypertensiv kezelést kell indítani (életmódbeli-étrendi tanácsok adása mellett).
Számos adat támasztja alá, hogy hypertoniában szenvedő cukorbetegek kezelési vérnyomás-célértékeit monoterápiával nem lehet elérni, ez az állítás különösen a metabolikus szindrómában vagy diabetesben jelentkező, ill. vesebetegségekhez társuló hypertonia II-III. stádiumára érvényes. Ez utóbbi esetekben a betegek jelentős hányadában kettős, olykor hármas, vagy többszörös kombináció alkalmazása válik szükségessé. A kombinált antihypertensiv kezelésnek ilyen esetekben az antihypertensiv terápia megkezdésekor is helye lehet.
Egyes antihypertensiv szerek (elsősorban ACE-gátlók és ARB-k) mellett megfigyelték az újonnan kialakuló diabetes kockázatának csökkenését, ami a cardiovascularis kockázat csökkentése szempontjából is előnyösnek minősül. A rendelkezésre álló adatok azonban nem teljesen egybehangzóak.
Microalbuminuria detektálása esetén a vérnyomásértéktől függetlenül indokolt a cukorbetegek antihypertensiv kezelése, ilyen esetekben az ACE-gátlók, vagy az ARB-k preferálandók a renin-angiotenzin-rendszer (RAS: renin angiotensin system) gátlása érdekében.
Napjainkban gyakorlatilag csak egyszeri adagolású, hosszú hatástartamú antihypertensiv szerek használatosak. A betegek időszakos ellenőrzése időnkénti ABPM-vizsgálatot is magába foglal.
Az antihypertensiv kezelés hatástani csoportjai:
- ACE-gátlók - diabeteszes nephropathia, társuló cardialis érintettség esetén választandók. A szérum kreatinin és kálium időszakos ellenőrzése kívánatos. Mellékhatásként improduktív köhögés jelentkezhet.
- Angiotenzin-II-receptor-blokkoló szerek (ARB-k) - diabeteszes nephropathia kezdeti vagy előrehaladottabb stádiumában egyes képviselői bizonyítottan előnyösek. Az ARB-k a legkevesebb mellékhatással rendelkező szerek, ACE-gátló okozta mellékhatás (köhögés) esetén is jól alkalmazhatók. Nincs adat arra nézve, hogy az ACE-gátlókhoz viszonyítva többlet-előnnyel rendelkeznének, kivéve a jobb mellékhatásprofilt. Az ARB-k és az ACE-gátlók egymással helyettesíthetők.
- Béta-blokkolók - nem nélkülözhetők a myocardialis infarctus szekunder prevenciójában, angina pectorisban, vagy szívelégtelenségben szenvedők kezelésében. Első szerként nem választjuk, hypertonia kezelésére akkor alkalmazzuk, ha az előzőekben említett társbetegségek igazolhatók. Csak cardioselectiv szert célszerű választani. Az anyagcsere-paraméterek tekintetében az alfa1-receptorblokkoló hatással is rendelkező carvedilol előnyösebbnek tűnik. Béta-blokkoló szer kontraindikációja, vagy intoleranciája esetén helyette tartós hatású diltiazem, vagy coronariabetegekben verapamil alkalmazható. A béta-blokkolóktársuló perifériás verőérbetegség esetén kerülendők. Alkalmazásuksorán a lipidprofil ellenőrizendő. Erectilis dysfunctiót okozhatnak. A hypoglykaemia tüneteit elfedhetik.
- Kálcium-antagonista szerek - elsősorban kombinációs kezelés céljaira alkalmasak a hosszú hatástartamú dihidropiridin-származékok és a phenylalkilamin-szerek. Az időskori izolált szisztolés hypertoniát jól befolyásolják. Lábszár-oedemát, obstipatiót okozhatnak. A rövid hatású dihidropiridinek nem alkalmazhatók tartós kezelés céljaira.
- Diuretikumok- az alacsony dózisú, tiazid-típusú diuretikumok elsősorban kombinációban hasznosíthatók. Idősebb korban, izolált szisztolés hypertonia, ill. társuló cardialis elégtelenség esetén választandók. Anyagcsere-hatásuk hosszabb távon kedvezőtlen is lehet. A közel-neutrális anyagcserehatása miatt az indapamid előnyben részesítendő. Szexuálisan aktív férfiaknál kerülendők. A kacs-diuretikumok előrehaladott veseszövődmény kezelésében használatosak.
-Alfa-1-adrenerg-blokkoló szerek- metabolikus szindróma talaján fejlődő hypertonia kezelésében jól hasznosíthatók. Előnyös lehet társuló prostata-hypertrophia esetén. Orthostaticus hypotoniát okozó diabeteszes autonóm neuropathiában kerülendő.
-Imidazolin-II-receptor-agonista szerek- metabolikus szindrómában, sympathicus túlsúly esetén jól alkalmazhatók.
- Centrális alfa-2-receptor-agonisták (alfa-metildopa) - terhességben választandó.
A diabeteshez társuló hypertonia kezelése terén az alábbi ajánlások fogalmazhatók meg:
- Általában csak többszörös gyógyszer-kombinációval érhető el a cukorbetegekben megkívánt vérnyomás-célérték (<130/80 Hgmm) ("B").
-Kezdeti terápiaként azokból a hatástani csoportokból kell választani, amelyekesetében bizonyított a cardiovascularis eseményeket csökkentő hatás (ACE-gátlók, ARB-k, kalciumcsatorna-blokkolók, diuretikumok) ("A"). Béta-blokkoló csak társ-indikáció (myocardialis infarctus szekunder prevenciója, angina pectoris, szívelégtelenség) esetén alkalmazandó ("A").
- Diabeteshez társuló hypertonia esetén a gyógyszer-kombináció tagjaként vagy valamelyik ACE-gátló, vagy valamelyik ARB szer mindenképpen szerepeljen, a két hatástani csoport egymással helyettesíthető. A megkívánt vérnyomás-célérték elérése érdekében kis dózisú, tiazid-típusú diuretikum kombinálása kívánatos ("D"). A közel-neutrális anyagcserehatása miatt az indapamid előnyben részesítendő. Szükség esetén (azaz ha a vérnyomás kettős kombinációval nem csökkenthető 130/80 Hgmm alá) a kezelést ki kell egészíteni kálcium-antagonistával (a nem-dihidropiridin típusúak [tartós hatású verapamil] proteinuriát csökkentő hatása előnyösebbnek tűnik, mint a dihidropiridineké), vagy speciális indikáció (ISZB, myocardialis infarctus utáni állapot, szívelégtelenség) esetén béta-blokkolóval is, az anyagcserehatás (lipidek) tekintetében az alfa1-receptorblokkoló hatással is rendelkező carvedilol előnyösebbnek tűnik. Béta-blokkoló szer kontraindikációja, vagy intoleranciája esetén helyette tartós hatású diltiazem, vagy coronariabetegekben verapamil alkalmazható. A terápiás kombináció részeként az inzulinrezisztenciára gyakorolt kedvező hatása miatt az imidazolin-Ii-receptor agonista (moxonidin, rilmenidin), ill. az alfa1-adrenoceptor blokkoló (doxazosin) szerek alkalmazása is logikusnak tűnik, különösen a fokozott szimpatikus tónusú, ill. a benignus prostata hyperplasiában szenvedő betegekben ("D").
Irodalom
1. JermendyGy: A cukorbetegségben kialakuló hypertonia klinikai spektruma. Diabetologia Hungarica 12 Suppl 4:32-41, 2004.
2. Magyar Diabetes Társaság vezetősége: Hypertonia diabetes mellitusban (szerk: JermendyGy). Diabetologia Hungarica 11: 67-77, 2003.
3. Jermendy Gy: A renin-angiotenzin rendszer gátlásának jelentősége a diabeteshez társuló hypertonia kezelésében. Metabolizmus 1:212-219, 2003.
4. Winkler G, Jermendy Gy, Matos L: Az angiotensin II receptor-gátlás alkalmazásának kardiológiai és diabetológiai aspektusai. Orv. Hetil. 144:1861-1867,2003.
5. Jermendy Gy, Farsang Cs: ACE-gátló és angiotenzin-receptorblokkoló (ARB) kezelés diabeteshez társuló hypertoniában. Diabetologia Hungarica 12 Suppl 4: 50-58, 2004.
6. Jermendy Gy: Milyen körülményekre kell tekintettel lenni az antihypertensiv terápia megkezdésekor diabetes mellitusban? Orv Hetil 145: 949-956, 2004.
7. Jermendy Gy: Hypertonia diabetológus szemmel. Melánia Kiadó, Budapest, 2007. 6.3. Thrombocytaaggregáció-gátló kezelés
6.3.1. Aszpirin kezelés
A thrombocytaaggregáció-gátló kezelésként a leggyakrabban aszpirint alkalmazunk, melynek javasolt napi dózisa 75-162 mg, a gyakorlatban 100 mg. Előnyben részesítendő a bélben oldódó kiszerelési forma.
6.3.1.1. Aszpirin kezelés - szekunder prevenció
Szekunder prevencióként aszpirin adása mind 1-es, mind 2-es típusú diabetesben macroangiopathia fennállása esetén javasolt. Az idetartozó kórképek az alábbiak: kórelőzményben szereplő myocardialis infarctus, bypass műtét utáni állapot, stroke, TIA, perifériás érbetegség, claudicatio és angina pectoris (A").
6.3.1.2. Aszpirin kezelés - primer prevenció 1-es típusú diabetesben
Aszpirin adása javasolt primer prevencióként 1-es típusú diabetesesekben az alábbi cardiovascularis rizikófaktorok fennállása esetén (a rizikófaktorok kezelése mellett): 40 év feletti életkor, cardiovascularis betegség előfordulása a családban, dohányzás, hypertonia, dyslipidaemia, albuminuria ("C").
6.3.1.3. Aszpirin kezelés - primer prevenció 2-es típusú diabetesben
Aszpirin adása javasolt primer prevencióként 2-es típusú diabeteszesekben az alábbi cardiovascularis rizikófaktorok fennállása esetén (a rizikófaktorok kezelése mellett): 40 év feletti életkor, cardiovascularis betegség előfordulása a családban, dohányzás, hypertonia, dyslipidaemia, albuminuria ("A"). A gyakorlatban a 40 év feletti cukorbetegekben aszpirin kezelés indokolt, és alkalmazása javasolt metabolikus szindrómában szenvedő betegekben is ("D").
6.3.2. Egyéb antithrombocyta szerek (ticlopidin, clopidogrel) adása
Aszpirin-allergia,-intolerancia vagy-rezisztencia esetén ADP-receptorblokkoló készítmény, ticlopidin (Ticlid®, Ipaton®, 2x250 mg), vagy clopidogrel (Plavix®, 75 mg) adandó. Az eddigi klinikai adatok szerint a clopidogrel alkalmazása biztonságosabb. Aszpirin-rezisztencia véleményezése előtt a szokásosan alkalmazott 100 mg-os aszpirin dózist célszerű napi 300 mg-ra emelni.
6.3.3. Aszpirin és clopidogrel együttes adása
Akut coronaria szindrómában - függetlenül attól, hogy konzervatív vagy intervenciós kezelést végeztek - indokolt a kombinált aszpirin-clopidogrel kezelés és e terápiát legalább egy évig kell folytatni ("A"). Cukorbetegekre vonatkozóan ezen ajánlás evidencia szintje alacsonyabb ("D"), a követendő elv azonban azonos.
Ugyancsak indokolt aszpirin és clopidogrel együttes adása igen magas globális cardiovascularis kockázattal rendelkező betegekben ("D"). Általában érvényesnek tekinthető, hogy a különböző cardiológiai szakmai protokollokban megfogalmazott, az antithrombocyta kezelés alkalmazására vonatkozó irányelvek cukorbetegekben is érvényesek.
Irodalom
1. American Diabetes Association: Aspirin therapy in diabetes (Position Statement). Diabetes Care 27 (Suppl. 1): S72-S73, 2004.
2. Bernát SI, Pongrácz E, Gonda F: Az aszpirin dózisának változtatása és a thrombocytaaggregáció-gátlás mértéke a kardiovaszkuláris és iszkémiás cerebrovaszkuláris betegségek szekunder prevenciója során. Cardiologia Hungarica 33: 240-244,2003
3. Káplár M, Paragh Gy, Udvardy M: Diabetes mellitus, metabolikus szindróma és koaguláció, thrombocyta aggregáció-gátló kezelés. Diabetologia Hungarica 12: 173-184, 2004.
4. Kempler P: Thrombocyta-aggregációt gátló kezelés diabetes mellitusban. Diabetologia Hungarica 12: 93-102,2004.
5. Kempler P.: Thromboemboliás szövődmények kezelése diabetes mellitusban. Diabetologia Hungarica 12 (Suppl. 3): 15-21, 2004.
6. Ajjan R, Storey RF, Grant PJ: Aspirin resistance and diabetes mellitus. Diabetologia 51: 385-390, 2008. 7. Diabetes és terhesség
A diabetes mellitus a terhességhez társuló egyik leggyakoribb kóros állapot. Irodalmi adatok szerint a fogamzóképes korú nők 0,3%-a cukorbeteg. Az esetek egy részében a diabetes már a terhességet megelőzően is fennáll. Ez az ún. pregestatiós diabetes képezi az összes esetek mintegy 10%-át. Az érintettek döntő hányada -90%-a- gestatiós diabetesben szenved, azaz a cukorbetegség felismerésére a terhesség idején kerül sor. Ez utóbbi állapot a szülést követően reklasszifikációt igényel: az esetek egy részében a szénhidrát-anyagcsere normalizálódik, más részében csökkent glukóztolerancia (IGT), ritkábban manifeszt diabetes mellitus marad vissza. Tekintettel arra, hogy az aktuálisan rendezett anyagcserehelyzettel rendelkezők is egy következő terhesség szempontjából, illetve - ettől függetlenül - életük egész tartama során diabetesre fokozottan veszélyeztetettnek tekintendők, követésük és szénhidrát-anyagcseréjük időszakos ellenőrzése elengedhetetlen követelmény.
7.1. Pregestatiós diabetes
Gyermeket kívánó/tervező diabetica - tekintet nélkül diabetese típusára - prekoncepcionális gondozásba irányítandó. Gyermeket nem kívánó diabetica figyelmét fel kell hívnia biztonságos fogamzásgátlás szükségességére.
A prekoncepcionális gondozás célja a leendő anya és a születendő gyermek lehető legjobb egészségi állapotának biztosítása, a terhesség anyai és magzati szövődményeinek-elsősorban a fejlődési rendellenességek kialakulásánakmegelőzése. A beteg ezzel kapcsolatos felvilágosítása az őt először észlelő, vagy gondozó orvos feladata. Az érintett személlyel rendszeres kapcsolatot tartó orvos - háziorvos, gyermekorvos, belgyógyász - feladata a megfelelő gondozóhelyre történő irányítás is. A prekoncepcionális gondozást a kívánt terhességet megelőző fél-egy évvel korábban kell elkezdeni. A gondozást minden esetben e téren jártassággal és megfelelő interdiszciplináris szakmai háttérrel rendelkező centrumban kell végezni.
A prekoncepcionális gondozás során föl kell mérni a leendő anya aktuális egészségi állapotát, diabetese esetleges szövődményeit -azok aktuális stádiumát- és társbetegségeit, gondoskodni kell a tartósan normoglykaemiás anyagcsere állapot létrejöttéről. A szénhidrát-anyagcsere kezelésére -ha az "életmódkezelés" önmagában a kívánt cél elérését nem biztosítja- csak inzulinadás -az intenzív inzulinkezelés valamelyik formája-jön szóba. A kezelést úgy kell meghatározni, hogy a vércukorértékek (laboratóriumban, vénás plazmában mérve) 3,5 -7,0 mmol/l között, a glikált fehérjeértékek (HbAic, szérum fruktózamin) pedig az adott laboratóriumban mért normális tartományon belül legyenek (tekintetbe kell ugyanis venni, hogy az értékek a nem-terhes állapothoz képest egyébként is alacsonyabbak). Ajánlási szint: "A". A prekoncepcionális gondozás feladatait a 9. táblázatban foglaljuk össze.
Ha a kívánt terhesség bekövetkezett, a diabeteszes gravida belgyógyászati és szülészeti gondozását akkreditált terhes diabetológiai centrumban kell végezni. A terhesség vállalása bizonyos körülmények esetén nem tanácsos, ezeket a 10. táblázat összegzi.
A diabetes terhesség alatti súlyosságának megítélésére szolgáló módosított White-féle osztályozás, illetve a napszakos vércukor-, illetve más anyagcsere "célértékek" ismerete és terhesség alatti ellenőrzése a speciális terhes diabetológiai centrumok feladata, ezért e kérdésekre módszertani levelünkben nem térünk ki.
7. 2. Gestatiós diabetes
A felismeretlen gestatiós diabetes (GDM) mind a magzat, mind az anya egészségét potenciálisan veszélyeztető állapot, érinti az aktuális ("index") terhességet, s érintheti az anya későbbi terhességeit és egészségi állapotát is. Kezeletlen esetekben a macrosomia előfordulása 40%, fokozott az egyéb szövődmények -szülési trauma, operatív beavatkozás szükségessége, magzati hypocalcaemia, respiratiós distress syndroma, hypoglykaemia, hyperbilirubinaemia- előfordulása is.
A GDM távlati kockázatai tekintetében kiemelendő, hogy 5-15 éven belül 2-es típusú diabetes kialakulása 3-4-szeres a terhességük során normális szénhidrát-anyagcseréjű nőkéhez képest. A szülést követő anyagcsere-állapottól függetlenül egy következő terhesség idején fokozott a glukóztolerancia ismételt károsodásának valószínűsége. A GDM az esetek túlnyomó többségében a metabolikus szindróma korai manifesztációja, ennek megfelelően kialakulása fokozott keringési kockázatot jelent.
Megfelelő szűrési eljárásokkal idejében és biztonságosan kórismézhető. Csökkent glukóztolerancia (IGT) terhesség alatti megjelenése a GDM-mel minden tekintetben azonos elbírálásban részesül. Ajánlási szint: "A".
Bár az egyes országok gyakorlata eltér a szűrésbe vontak és a szűrési módszerek tekintetében, a szórvány vizsgálatokból ismert hazai GDM incidencia-értékek -6,4 - 7,9%- indokolják, hogy az Egészségügyi Világszervezet (WHO) ajánlásához igazodva teljes körű szűrés történjen. Ez azt jelenti, hogy terhessége 24-28. hete között valamennyi asszonyt szűrni kell. Ajánlási szint: "D".
A WHO állásfoglalása szerint a "terhességben kialakuló cukorbetegség" diagnózisát ugyanazon elvek (75 grammos terheléses cukorvizsgálat [oralis glukóztolerancia teszt, OGTT]) alkalmazásával kell felállítani, mint a nem-terhes felnőttek esetében. A jelen irányelvek szerint - a manifeszt diabetesre utaló értékek (éhomi vércukor >7,0, random vércukor vénás plasmában mérve >11,1 mmol/l) mellett- GDM-ként értékelendő terhes nőn a 75 grammos OGTT 120. percében mért >7,8 mmol/l mmol/l érték is.
GDM-re fokozott kockázatú személyeken - megelőző terhességekben fellépő szénhidrátanyagcsere-zavar, diabetes halmozott családi előfordulása, 30 kg/m2-nél nagyobb terhesség előtti súly, anamnézisben halvaszüléssel végződött korábbi terhesség(ek), ikerterhesség fennállta, az anya 40 év fölötti életkora - a terhesség első trimeszterében is javasolt random vércukorvizsgálat, kétes értéke esetén OGTT végzése. GDM-re fokozott kockázatú személyeken a 24-28. hét negatív vizsgálatai esetén a terhesség harmadik trimeszterében is javasolt a szénhidrát-anyagcsere fentiek szerinti ellenőrzése.
7. 2.1. AGDM kezelése
7. 2.1.1. Életmódkezelés
A GDM kezelésének két alappillére a megfelelő étrend és az annak kiegészítéseként szükséges antidiabetikus (inzulin) kezelés. Az étrend hatását erősíti a rendszeres fizikai tevékenység is.
Az étrendi kezelés célja az anya és magzat számára szükséges tápanyagok biztosítása, normoglykaemia fenntartása mellett. A ketonuria/ketonaemia elkerülése érdekében az első trimeszterben minimálisan napi 140 gramm szénhidrát, 1500 kcal (= 6300 kJ) energia bevitele szükséges. Bár a szokásos napi energia felvételt 22-35 kcal/testsúlykg között tartják optimálisnak, a GDM-es terhesek gyakori túlsúlyára tekintettel az esetek jelentős részében ennél kisebb energia-bevitel, a terhesség előtti testsúly függvényében akár 12 kcal/testsúlykg-ig terjedő megszorítás lehet szükséges. A második trimesztertől kezdve az energiaszükséglet napi 250-300 kcal-val (= 1050-1260 kJ) nő. Az étrend ajánlott összetétele nem különbözika nem-terhes cukorbetegek részére ajánlottól: 50-55% szénhidrát (főleg komplex szénhidrát, sok rost), 20% fehérje, 25-30% zsír. Ajánlási szint: "A".
A gyakori, alkalmanként kis szénhidráttartalmú étkezések az étkezés utáni (postprandialis) vércukorcsúcs mérséklését szolgálják. A reggeli és a tízórai szénhidrát elosztása a nem-terhesek számára ajánlottól eltér, itt reggelire valamivel kevesebb, tízóraira a reggelivel azonos mennyiségű, vagy valamivel több szénhidrát fogyasztása ajánlott. Cél, hogy a terhesség alatti testsúly növekedése ne legyen több 8 kg-nál.
A teherbíró-képességhez igazodó fizikai tevékenység GDM-ben is kifejezetten ajánlott. Javítja az anyagcsere-helyzetet, csökkenti a macrosomia előfordulását, de nem igazolták a császármetszések számát csökkentő hatását. Ajánlási szint: "A".
7. 2.1. 2. Inzulinkezelés GDM-ben
Ha az életmód (döntően: étrendi) kezelés a tartós euglykaemiát önmagában nem biztosítja, inzulin bevezetése szükséges. Inzulin adása indokolt, ha két hetes adekvát diéta ellenére az éhomi vércukorszint >5,3 és/vagy az 1 órás postprandialis vércukorszint >7,0 mmol/l laboratóriumban, vénás plazmából meghatározva (a 2 órás postprandialis értéknek <6,7 mmol/l alatt kell maradnia). Inzulinkezelésre a GDM-es esetek 20-25%-ában kerül sor. Ajánlási szint: "A".
Normális éhomi, emelkedett postprandialis vércukor értékek esetén elegendő lehet étkezések előtt alkalmazott gyorshatású inzulin alkalmazása. Az esetek kisebb részében előfordulhat, hogy csak reggel, máskor reggel és a vacsorához szorulunk inzulin adására. Amennyiben az éhomi vércukorszint is emelkedett, lefekvéskor történő intermedier ("bázis", a gyakorlatban NPH-típusú) inzulin bevezetése is szükséges. Ennek kezdő adagjaként 4-8 E adása javasolt. Két, reggel és lefekvéskor adott "bázis" inzulin adása az inzulinhatások potenciális interferenciája folytán nem ajánlott. A normoglykaemia eléréséhez szükséges inzulinadag napi 6-7 vércukorméréssel titrálható ki, ami még túlsúlyos gravidákon sem nagy, átlagosan 12-24 E. Ajánlási szint: "D".
Az antidiabetikus kezelés akkor megfelelő, ha a HbA^-érték 6%, a szérum fruktózamin umol/l. Inzulinnal kezelteken -éjszakai hypoglykaemiákelkerülése érdekében-a lefekvéskor mért vércukorszint 4,5-6,0 mmol/l értéke a követendő.
Inzulinpumpa-kezelés alkalmazását GDM-ben semmilyen megfontolás nem támogatja. Önmagában a terhesség nem indikáció a pumpakezelés megkezdésére pregesztációs cukorbetegségben sem, de inzulinpumpán lévő pregesztációs cukorbetegek pumpakezelése rendezett anyagcsereállapot esetén folytatható. Újabb vizsgálatok mind a lispro-inzulin (Humalog®), mind az aszpart-inzulin (NovoRapid®) adását terhességben is biztonságosnak találták, a harmadik gyors hatású inzulinanalóg, a glulizin (Apidra®) terhességben való biztonságos alkalmazhatósága tekintetében még nem áll elegendő adat rendelkezésre. Ajánlási szint: "D". Az aszpart-inzulin (NovoRapid®) a legújabb alkalmazási előirat szerint adható terhesség alatt is.
7. 2. 2. A GDM-ben szenvedők gondozása
A GDM-es gravida gondozása team-munkát igényel. A belgyógyászati gondozás a diabetes szakellátó hely -diabetológus orvos, diabetes szakápoló, dietetikus- és a családorvos közös feladata, míg a terhesgondozást e téren jártassággal rendelkező szülész-nőgyógyász szakorvosnak kell végeznie. Fontos az állapottal társuló keringési kockázat felmérése, a diabetes szövődményeinekés kísérőbetegségeinek feltárására irányuló vizsgálatok-szemészeti vizsgálat (fundus + vízus), microalbuminuria meghatározása, vérzsír-értékek vizsgálata, neuropathia esetleges fennállásának detektálása- teljes körű elvégeztetése. Diabetológiai ellenőrzés hetente szükséges, a vizsgálatoknak ki kell terjednie az éhomi és a postprandialis vércukorszint, a vizelettel ürített cukor (és aceton) meghatározására, vércukor-önellenőrzést folytató gravidák esetében a kezelési napló áttekintésére (a lefekvéskor, inzulinnal kezelteken alkalmanként a hajnali vércukorszint vizsgálatára), a szérum fruktózamin és a HbAic vizsgálat szükség szerinti elvégeztetésére. A kiegészítő laboratóriumi vizsgálatok közül fontos a szérum TSH, pajzsmirigy immunmarkerek vizsgálata (terhességi thyreoiditis, egyéb pajzsmirigy funkciózavar időben történő felismerése céljából). A diabetes típusának meghatározására csak ritkán kényszerülünk a terhesség idején, ennek módszerei (széerum C-peptid, ICA, GAD/A/ meghatározás) azonosak a nem-terhes állapotban történő meghatározásokkal. Ajánlási szint: "D".
Irodalom
1. Baranyi É, Tamás Gy, Egyed J: Terhesség és diabetes (in: Halmos T, Jermendy Gy: Diabetes mellitus. Elmélet és klinikum. Medicina, Budapest, 2002.) pp. 653-664.
2. Gyimesi A: Gestatiós diabetes - belgyógyászati kérdések. Diabetologia Hungarica 13 Suppl. 2: 39-45,2005.
3. WHO Study Group: Prevention of diabetes mellitus. WHO Technical Report Series No 844. WHO, Geneva, 1994.
4. Report of a WHO Consultation: Definition, diagnosis and classification of diabetes mellitus and its complications. Part 1: Diagnosis and classification. World Health Organization, Department of Noncommunicable Diseases Surveillance, Geneva, 1999.
5. Kerényi Zs, Tamás Gy: Gestatiós diabetes (in: Halmos T, Jermendy Gy. /szerk./: Diabetes mellitus. Elmélet és klinikum. Medicina, Budapest, 2002.) pp. 665-677.
6. Baranyi É, Winkler G: Terhesség és inzulinrezisztencia: elméleti és klinikai kérdések. LAM 18:97-102,2008.
7. Baranyi É, Winkler G: Inzulinanalóg- és inzulinpumpa-kezelés diabetesszel társult terhességben. Diabetol Hung 13 (Suppl. 3): 37-43, 2005.
8. Kitzmiller JL, Block JM, Brown FM, Catalano PM, Conway DL, Coustan DR, Gunderson EP, Herman WH, Hoffman LD, Inturrisi M: Managing preexisting diabetes for pregnancy. Summary of evidence and consensus recommendations for care. Diabetes Care 31: 1060-1079, 2008.
9. táblázat. Manifeszt cukorbeteg nők prekoncepcionális gondozásának irányelvei
Az alapellátás és gondozás során:
Minden generatív korban lévő diabetica esetében tisztázandó, hogy a közeljövőben kíván-e gyermeket:
- ha nem: felvilágosítás és hatékony anticonceptio
- ha igen: egyelőre anticonceptio és tervezett prekoncepcionális gondozási program elindítása Az intenzív, interdiszciplináris szakellátás és gondozás során:
- Részletes felvilágosítás és a beteg kooperációjának megnyerése
- Általános vizsgálatok
- anamnézis, fizikális vizsgálat
- "rutin" laboratóriumi vizsgálatok (vizelettenyésztés is)
- EKG, mellkas rtg
- nőgyógyászati vizsgálat
- Diabéteszes érszövődményekvizsgálata
- retinopathia
- fundusvizsgálat
- fundusfotó
- válogatott esetben: fluorescein angiographia
- nephropathia
- vesefunkciók
- microalbuminuria
- izotóp-renographia
- ultrahangvizsgálat, szükség esetén pyelographia
- Anyagcsere-állapot felmérése
- vércukorszint, vizelettel történő cukorürítés meghatározása
- vércukor-önellenőrzés eredményeinek áttekintése
- HbA1c és/vagy szérum fruktózamin meghatározás
- Pajzsmirigy működés vizsgálata
- Állandó edukáció és motiváció közben a kóros eltérések rendszeres ellenőrzése és kezelése
- A tervezett terhesség prognózisának megítélése:
- időpontjának optimalizálása ("startjel")
- esetleges ellenjavallatának megítélése
10. táblázat. Cukorbetegségben a terhesség az alábbi körülmények esetén nem tanácsos
- kezelésre nem reagáló, látást veszélyeztető proliferatív retinopathia
- a vesefunkció csökkenését eredményező előrehaladott nephropathia
- súlyos ischaemiás szívbetegség
- magas glikált hemoglobin szint a koraterhességben (HbAu >10%)
- diabeteszes ketoacidosis a koraterhességben
- 38 évesnél idősebb cukorbeteg nő, 2 gyermekkel
- tinédzser diabetica nem tervezett terhessége
8. Diabetes és műtét
Cukorbetegek esetében a műtéti beavatkozás fokozott kockázattal jár, mert a műtéti stressz-helyzet a szénhidrát-anyagcsere felborulását eredményezheti, ill. a rossz anyagcsere-helyzet növeli a különböző műtéti szövődmények kialakulásának veszélyét.
Diabetológiai gyakorlati szempontok alapján a sebészi beavatkozásokat kis- és nagyműtétekre lehet osztani.
Kisműtétről beszélünk akkor, amikor a műtét időtartama rövid (általában nem több, mint félóra), a beavatkozás helyi érzéstelenítésben történik és nagy testüreg megnyitására nem kerül sor. A beteg a műtét után már néhány órával étkezhet.
Nagyműtétről beszélünk akkor, amikor a műtét több óráig tart, általános anaesthesiában történik és valamelyik nagy testüreg (mell- vagy hasüreg) megnyitásával jár. A beavatkozás után a beteg egy bizonyos ideig csak parenterálisan táplálható.
Célszerű, ha a cukorbeteg műtétjére kora reggel (első műtétként) kerül sor. Laktát tartalmú infúziók kerülendők. Biguanid vegyületeket 48 órával a műtét előtt el kell hagyni. Ugyancsak fel kell függeszteni hosszú hatású hypoglykaemizáló szerek (szulfanilureák, "bázis" inzulinok) adását is.
Tervezett műtét előtt a szénhidrát-anyagcserét rendezni kell, szükség esetén akár hospitalizált körülmények között. Akut műtét esetén az anyagcsere lehetőség szerinti gyors rendezésére kell kísérletet tenni.
A perioperatív időszakban a betegek vércukorértékei rendszeresen ellenőrzendők.
8.1. Kisműtét, diétás vagy orális antidiabetikus kezelés mellett
Csak étrendi előírást tartó, rendezett anyagcseréjű cukorbeteg kis műtéte különösebb terápiás változtatás nélkül elvégezhető. Ugyanígy nincs szükség a terápia lényeges átalakítására akkor sem, ha a beteg nem-hypoglykaemizáló orális antidiabeticumot szed, s anyagcseréje rendezett. A műtét éhgyomorra történik, így a tabletták is az első megengedett étkezés előtt vehetők be. A metformin adása a műtét előtt 48 órával felfüggesztendő. Elhúzódó hatású hypoglykaemizáló szerek (pl. glibenclamid) adását 1-2 nappal a műtét előtt abba kell hagyni.
8.2. Kisműtét, inzulinkezelés
Korábban inzulinkezelésben részesülő cukorbeteget a kisműtét perioperatív időszakára célszerű naponta többszöri (általában napi 5-szöri) gyorshatású inzulinkészítményre állítani. Bizonyos esetekben ettől eltérő beállítás is megengedett.
8.3. Nagyműtét
Nagyműtét esetén a cukorbeteg antidiabetikus kezelése a műtétet megelőző minimum 2-3 napban naponta többször (általában 5 alkalommal) adott gyors hatású inzulinkészítménnyel történik.
A műtét napján az anyagcsere-vezetés az ún. GIK (glukóz-inzulin-kálium) sémát követi (glukóz és kálium tartalmú infúzió mellett a beteg gyors hatású inzulint kap, szintén infúzióban - a bejuttatott glukóz és inzulin mennyisége a gyakori vércukor-ellenőrzések eredményétől függően változik. Az alapinfúzió általában 500 ml 10%-os glukóz, amelyben 15 NE gyors hatású inzulin (Actrapid HM® vagy Humulin R®) és 10 mmol KCl van. Az infúzió ajánlott sebessége 100 ml/óra, azaz 1 óra alatt 10g glukózt, 3 NE inzulint és 2 mmol KCl-tjuttatunk a szervezetbe. A műtét során az aktuálisan mért vércukorszintek alapján az alapsémát módosíthatjuk, ill. bizonyos műtéti típusoknál eleve más, többnyire emelt dózisú inzulinbevitelt alkalmazhatunk.
A per os táplálás megkezdésekor az infúzió elhagyható, és a beteget ismét napi többszöri gyorshatású inzulinnal kell kezelni. A végleges antidiabeticu kezelés beállítása a beteg állapotának teljes stabilizálódását követően történik meg.
Akutan szükségessé váló nagyműtét esetén, ha az anyagcsere-helyzet kielégítő, a GIK-séma követendő, rossz anyagcsere-helyzet esetén a lehetőség szerinti gyors rendezésre való törekvés után szintén a GIK séma követendő.
Irodalom
1. Somogyi A, Iványi J: Diabetes és műtét. In: Diabetes mellitus. Elmélet és klinikum (szerk.: Halmos T, Jermendy Gy.), Medicina, Budapest, 2002, pp. 685-696.
2. Gerő L: Adiabeteses krízisállapotok tünettana és kezelése. In: A diabetes perioperatív vonatkozásai (szerk.:TekeresM.). Bibliomed, Med. Verlag GmbH, Melsungen, 2002, pp. 45-54.
3. Gerő L: Endokrin-anyagcsere betegségek perioperatív/aneszteziológiai vonatkozásai idős korban. In: Idős betegek ellátásának sajátosságai (szerk.: Tekeres M.), Bibliomed, Med. Verlag GmbH, Melsungen, 2003, pp. 71-78.
4. Baranyi É, Winkler G: Az anyagcserevezetés szempontjai a perioperatív időszakban. Diabetologia Hungarica 16: 251-258,2008.
IV-V. Gondozás, Rehabilitáció
9. Gondozás, betegoktatás, rehabilitáció
9.1. A cukorbetegek gondozása
A 2-es típusú cukorbetegségben szenvedők gondozása a komplex háziorvosi ellátás keretében valósulhat meg a legeredményesebben. Helyes, ha inzulinkezelésben részesülő, ill. szövődménnyel terhelt 2-es típusú cukorbetegek, valamint az 1-es típusú cukorbetegek diabetes-szakambulancián állnak gondozás alatt, szorosan együttműködve a háziorvossal. A sok időt és egyéni törődést igénylő feltételezi a jól képzett, önállóan (is) dolgozó diabetes-szakápoló, ill.
dietetikus jelenlétét a szakgondozást végző munkacsoportban. A cukorbeteg-gondozás keretében megvalósítandó feladatok attól függenek, hogy a beteget első alkalommal látjuk-e, vagy ismételten jelenik meg a szakrendelésen.
A diabetes felismerésekor, illetve a beteg első megjelenésekor tisztázandó körülmények, ill. elvégzendő feladatok:
- anamnézis (családi is, nőknél szülészeti események), táplálkozási és életmódi szokások, foglalkozás, fizikai aktivitás, iskolai végzettség, korábbi gyógyszeres kezelés tisztázása;
- teljes körű fizikális vizsgálat: testsúly, testmagasság, derékkörfogat, vérnyomás mérése, a láb vizsgálata, (talp, deformitások, gombásodás, perifériás artériák tapintása, neuropathia ellenőrzése hangvillával), EKG készítése;
- szemfenék (gyakorlott szemész általi) vizsgálata, tágított pupillák mellett;
- laboratóriumi vizsgálatok: vércukor éhomra és postprandiálisan, szérum össz-cholesterin, HDL-cholesterin, LDL-cholesterin (mérve vagy becsülve), triglycerid, kreatinin, becsült GFR, vizeletcukor és -aceton, üledék, szükség esetén vizelettenyésztés, kvantitatív albuminürítés (microalbuminuria), HbA^;
- a betegoktatás megkezdése;
- diétás tanácsadás;
- az orális antidiabeticumok helyes alkalmazásának elmagyarázása (ha aktuális);
- az inzulinterápia beállítása (ha szükséges), az ehhez szükséges injekciózási technika megtanítása.
- vércukor-önellenőrzés jelentőségének elmagyarázása (ha aktuális: megtanítása);
A beteg ellenőrzésének (gondozásának) gyakoriságát a betegség típusa, a kezelés módja, valamint az esetleges szövődmények jelenléte határozza meg. 1-es típusú betegek esetében általában évi 4-6, 2-es típusú (nem inzulinnal kezelt) beteg gondozása során évi 2-4 alkalommal javasolt az ellenőrzés.
Minden orvos-beteg találkozáskor elvégzendő:
- az oktatás folytatása,
- testsúly- és derékkörfogat mérése,
- vérnyomásmérés,
- éhomi és postprandiális vércukormérés, önellenőrzést végző betegnél a kezelési napló alapján az anyagcsere-vezetés megbeszélése.
Évente legalább egy alkalommal elvégzendő:
- teljes körű vizsgálat (mint első alkalommal), különös tekintettel a láb vizsgálatára,
- a szemfenék ellenőrzése,
- teljes körű laboratóriumi vizsgálat (mint első alkalommal),
- a kezelés áttekintése,
- az önellenőrzési technika ellenőrzése.
A HbA1c meghatározása 1-es típusú és inzulinnal kezelt 2-es típusú betegeknél évi legalább 4 alkalommal, egyéb esetekben évi legalább 2 alkalommal javasolt. Speciális esetekben (gyermekek, terhesség, idős kor), a HbAu célértéket egyénileg kell a beteg számára meghatározni. A szérum lipidek vizsgálata általában évente egy alkalommal javasolt. Kóros vérzsírszintű és/vagy antilipaemiás kezelésben részesülő egyének esetében ennél gyakoribb vizsgálat válhat szükségessé.
9.2 Betegoktatás, rehabilitáció
Az oktatás a diabetes megelőzésénekés kezelésénekalapvető eleme, mindez egyaránt vonatkozika cukorbetegekre, a kezelést végző személyzetre, sőt a lakosság egészére is. Megfelelő tudásanyag nélkül a beteg és családtagjai képtelenek megbirkózni a betegséggel együtt járó terhekkel és az életmód megkívánta változásokkal. A cukorbeteg joga és kötelessége, hogy megtanulja a betegségével kapcsolatos alapvető ismereteket. A páciensedukációval együtt járó "hozzáadott érték", a terápiás betegoktatás az alábbiakat jelenti:
- Az egészségügyi ellátás integráns részeként megvalósuló folyamatos oktatás és tanulás eredményeképpen a beteg képes lesz saját életét optimálisan menedzselni;
- A betegközpontú oktatás magába foglalja a cukorbetegekszervezett felkutatását, megfelelő információ biztosítását, az önellenőrzés elsajátítását, a betegséggel kapcsolatos pszichoszociális támogatást, az orvosi kezelés előírásait, kórházi és ambuláns ellátás megszervezését, szervezési információkat, egészség- és betegség-magatartással kapcsolatos tájékoztatást, szükség esetén a rehabilitációs lehetőségek körvonalazását.
A betegoktatás az alapellátástól a szakorvosi ellátás szintjéig team-munka keretén belül valósulhat meg sikeresen. A betegeket jól oktatni, sikeresen gondozni csak akkor lehetséges, ha az ellátást végzők folyamatos ön- és továbbképzésben részesülnek.
Irodalom
1. International Diabetes Federation: International Standards for Diabetes Education 2003.
2. Lacroix A, Assal JP: Therapeutic patient education. Ed. Maloine, Paris, 2003, pp. 57-79.
3. International Diabetes Federation Position Statement: Diabetes education: A right for all 2004.
4. Structured Patient Education in Diabetes. Report from the Patient Education Working Group Department of Health UK.January 2005.
5. Standards of Medical Care in Diabetes - 2008. Diabetes Care 31 Suppl 1: S12-45,2008. 10. A diabetes megelőzésének lehetőségei
10.1. Az 1-es típusú diabetes megelőzése
Noha a családi anamnézisben szereplő 1-es típusú diabetes, az autoantitest (ICA, GADA, IA-2) pozitivitása és az intravénás glukózra bekövetkező első, gyorsfázisú inzulinválasz kiesése előrejelzik az 1-es típusú diabetes kialakulását, jelenleg az orvostudomány nem ismer olyan megelőzési módszert, amely hatékonyan, biztonságosan és mellékhatástól mentesen biztosítaná az 1-es típusú diabetes megelőzését. Napjainkban - bár ismereteink egyre bővülnek - az 1-es típusú diabetes megelőzése nem megoldott, azaz a klinikai gyakorlatban az 1-es típusú diabetes prevenciója jelenleg nem tekinthető realitásnak.
10.2. A 2-es típusú diabetes megelőzése
A diabetes megelőzésének leghatékonyabb eszköze az életmód-terápia: megfelelő táplálkozással a kívánatos testsúly elérése és/vagy megtartása, valamint a rendszeres fizikai aktivitás ("A"). A prevenciós tevékenység a cukorbetegség kialakulása vonatkozásában nagy kockázattal rendelkező személyek felkutatására és kezelésére irányul. A nagy kockázattal rendelkező személyek felkutatása:
Költséghatékonysága és egyszerűsége miatt első lépésként kérdőívvel történő szűrés ajánlott, amely jól megválasztott kérdések esetében 71-84%-os találati valószínűséggel használható a háziorvosi gyakorlatban, gyógyszertárakban, az alapellátás szintjén. Az alábbi kérdésekre adott válaszok alapján a veszélyeztetett egyén azonosítható. -Obesitas (A centrális obesitas könnyen mérhető a haskörfogat meghatározásával. Az európai népességben férfiaknál >94cm, nőknél >84 cm minősül kórosnak)
- Családi kórelőzmény (Cukorbetegség előfordulása a közeli, vagy távolabbi rokonok között.)
- Életkor (>45 év az európai, míg >35 az egyéb népességben nagyobb kockázatot jelent)
- Hypertonia, vagy szív- és érrendszeri betegség a kórelőzményben
- Mozgásszegény életmód
- Gestatiós diabetes, vagy 4000g feletti magzat szülése a kórelőzményben
- Bizonyos gyógyszerek szedése (glucocorticoidok, tiazid-típusú diureticumok, antipsychoticumok, interferon-alfa, stb.)
A kérdőív alapján nagy kockázattal rendelkező személyek esetében a háziorvosi gondozás keretében laboratóriumi meghatározással először éhomi vércukorvizsgálatot kell végezni. Amennyiben a kórisme egyértelműen nem bizonyítható, a diagnosztikai fejezetben részletezettek alapján kell eljárni. Cardiovascularis betegség esetén a szénhidrát-anyagcsere, cukorbetegségben a szív- és érrendszer állapota a szükséges vizsgálatok elvégzésével tisztázandó. A testtömeg-index meghatározása mellett a haskörfogat mérése, a vérnyomás, a lipidértékek ellenőrzésével együtt fontos a dohányzás, táplálkozási szokások és életmódi tényezők regisztrálása.
Prediabetes
A diabetes mellitus diagnosztikus kritériumát el nem érő, de a fiziológiás értékektől eltérő vércukorszintek a szénhidrát-anyagcsere enyhébb zavarára utalnak. Az emelkedett éhomi vércukorszint (impaired fasting glycaemia, IFG) és a csökkent glukóztolerancia (impairedglucose tolerance, IGT) a cukoranyagcsere átmeneti állapotai a normális glukóztolerancia és a diabetes mellitus között. Az IFG az éhomi, az IGT pedig a postprandialis állapotnakaz élettanitól való eltérését jelenti. Az IFG-t és IGT-t együttesen károsodott glukózreguláció (impaired glucose regulation) névvel jelölik. Az Amerikai Diabetes Társaság az IFG-t és az IGT-t együtt véve prediabetes névvel illeti. Újabban használatos a köztes hyperglykaemia (intermediate hyperglycemia) elnevezés is. Az elnevezésben uralkodó bizonytalanság ellenére nyilvánvaló, hogy ez az állapot a diabetes előállapotát jelenti.
Kellően kivitelezett klinikai tanulmányok eredménye alapján megállapítható, hogy
- Csökkent glukóztolerancia (IGT) stádiumában lévő (testsúlyfelesleggel rendelkező) egyének esetén a 2-es típusú diabetes kialakulásának kockázata diétával és fokozott fizikai aktivitással, valamint metformin, akarbóz, orlistat, rosiglitazon adásával csökkenthető.
- Nem cukorbeteg egyének antihypertensiv (ACE-gátló-, ARB-, calciumantagonista) terápiája, lipidszintcsökkentő (pravastatin) kezelése, ill. postmenopausalis hormonpótló terápiája esetén az újonnan kialakuló 2-es típusú diabetes kockázata csökkenhet.
A 2-es típusú diabetes prevencióját célzó indikációval hazánkban 2008-ban egyetlen gyógyszer sincs regisztrálva. Irodalom
1. Jermendy Gy: A 2-es típusú diabetes megelőzésének lehetőségei. Diabetologia Hungarica 12 Suppl. 3: 22-29,2004.
2. Jermendy Gy: Tényeken alapuló cukorbeteg-gondozás. Medicina Kiadó, Budapest, 2005, pp. 349-386.
3. International Diabetes Federation: a consensus on Type 2 diabetes prevention. Diabetic Med 24:451-463,2007.
4. The Task Force on Diabetes and Cardiovascular Diseases of the European Society of Cardiology (ESC) and of the European Association for the Study of Diabetes (EASD): Guidelines on diabetes, pre-diabetes, and cardiovascular diseases: executive summary. Eur Heart J 28: 88-136, 2007.
VI. Irodalomjgyzék
Irodalom (összegző munkák)
1. A diabetes mellitus kórismézése, a cukorbetegek kezelése és gondozása felnőttkorban. A Magyar Diabetes Társaság szakmai irányelve, 2005. (szerk: Jermendy Gy, írta: Gerő L, Hidvégi T, Jermendy Gy, Kempler P, Winkler G). Diabetologia Hungarica 14 Suppl 1:1-48, 2006.
2. Alberti G,Zimmet P, ShawJ, BloomgardenZ, Kaufman F, SilinkM:Type 2 diabetes in the young: the evolving epidemic: the International Diabetes Federation consensus workshop. Diabetes Care 27:1798-1811,2004.
3. American Diabetes Association (ADA): Clinical Practice Recommendations 2008. Diabetes Care 51 Suppl 1: S1-S107, 2008.
4. Cameron AJ, Shaw JE, Zimmet PZ: The metabolic syndrome: prevalence in worldwide population. Endocrinol Metab Clin North Am 33: 351-375, 2004.
5. Gerő L, Jermendy Gy: Inzulinanalógok, Medicina Kiadó, Budapest, 2006.
6. Halmos T, Jermendy Gy. (szerk): Diabetes mellitus. Elmélet és klinikum. Medicina Kiadó, Budapest, 2002.
7. Halmos T, Kautzky L, Suba I: Metabolicus syndroma. Medicina Kiadó, Budapest, 2005.
8. IDF Clinical Guidelines Task Force: Global guideline for type 2 diabetes. Brussels, International Diabetes Federation, 2005.
9. International Diabetes Federation IGT/IFG Consensus Statement. Impaired glucose tolerance and impaired fasting glycaemia: the current status on definition and intervention. Diabetic Med 19: 708-723, 2002.
10. Jermendy Gy (szerk): Hypertonia diabetológus-szemmel. Melánia Kiadó, Budapest, 2007.
11. Jermendy Gy, Winkler G: 100 kérdés 100 felelet a klinikai diabetológiából. Tudomány Kiadó, Budapest, 2005.
12. Jermendy Gy: Tényeken alapuló cukorbeteg-gondozás. Medicina Kiadó, Budapest, 2005.
13. Jermendy Gy: A 2-es típusú diabetes világméretű terjedésének okai és következményei. LAM 16:105-113,2006.
14. Kempler P. (szerk): Neuropathiák - pathomechanizmus, klinikum, diagnosztika, terápia. Springer Tudományos Kiadó Kft., Budapest, 2002.
15. King H, Aubert RE, Herman WH: Global burden of diabetes, 1995-2025: Prevalence, numerical estimates, and projections. Diabetes Care 21:1414-1431,1998.
16. Magyar Diabetes Társaság Metabolikus Munkacsoportja (Gerő L, Jermendy Gy, Káplár M, Kautzky L, Pados Gy, Paragh Gy,Zajkás G.): A metabolikus szindróma terápiája. Orv Hetil 144:1145-1152,2003.
17. Magyar Diabetes Társaság Metabolikus Munkacsoportja (Halmos T, Hidvégi T, Jermendy Gy, Káplár M, Korányi L, Pados Gy, Paragh Gy, Zajkás G): A metabolikus szindróma definíciója, diagnosztikai kritériumrendszere és szűrése. Orv Hetil 143:785-788, 2002.
18. Magyar Diabetes Társaság vezetősége: Hypertonia diabetes mellitusban (szerk: Jermendy Gy).
19. Diabetologia Hungarica 11: 67-77, 2003.
20. III. Magyar Kardiovaszkuláris Konszenzus Konferencia a koszorúér-eredetű, agyi- és perifériás érbetegségek kockázatának becslésére, megelőzésére és kezelésére. Metabolizmus 6 Suppl A: 3-94,2008.
21. The Expert Committee on the Diagnosis and Classification of Diabetes Mellitus: Follow-up report on the diagnosis of diabetes mellitus. Diabetes Care 26: 3160-3167,2003.
22. WHO: Definition,diagnosis and classification of diabetes mellitus and its complications. Report of a WHO consultation. Part 1: Diagnosis and classification of diabetes mellitus. Geneva, 1999. Magyar nyelvű szöveghű fordítása: Diabetologia Hungarica 8 Suppl 2:1-28,2000.
23. Wild S, RoglicG, Green A, Sicree R, King H: Global prevalence of diabetes. Estimate for the year 2000 and projections for 2030. Diabetes Care 27:1047-1053, 2004.
24. Winkler G, Jermendy Gy: Újabb 121 kérdés és felelet a klinikai diabetológiából. Tudomány Kiadó, Budapest, 2006.
25. Winkler G, Baranyi É: Gyakorlati diabetológia (szerk). Melania Kiadó, Budapest, 2008.
26. Zimmet P, Alberti KGMM, Shaw J: Global and societal implications of diabetes epidemic. Nature 414: 782-787,2001.
27. Zimmet P, Shaw J, Alberti KG: Preventing type 2 diabetes and the dysmetabolic syndrome in the real world: a realistic view. Diabet Med 20: 693-702, 2003.
A szakmai irányelv érvényessége: 2010. szeptember 30.
Érintett társszakmákkal való konszenzus
A Magyar Diabetes Társaság 2004/2005-ben több konszenzusértékezletet tartott, amelyen a diabetes mellitus kezelésével kapcsolatos irányelvek kidolgozásában az alábbi társszakmák tudományos társaságának képviselői vettek részt:
Magyar Atherosclerosis Társaság
Magyar Angiológiai és Érsebészeti Társaság
Magyar Belgyógyász Társaság
Magyar Dermatológiai Társaság
Magyar Elhízástudományi Társaság
Magyar Hypertonia Társaság
Magyar Kardiológusok Társasága
Magyar Nephrológiai Társaság
Magyar Nőgyógyász Társaság
Magyar Sportorvos Társaság
Magyar Stroke Társaság
Magyar Szemész Társaság
Magyar Táplálkozástudományi Társaság
Az Egészségügyi Minisztérium
szakmai protokollja
Krónikus kritikus végtag ischaemiáról
Készítette: a Belgyógyászati Szakmai Kollégium
I. Alapvető megfontolások
1. A protokoll alkalmazási / érvényességi területe Belgyógyászat, érsebészet, angiológia.
2. A protokoll bevezetésének alapfeltétele
A belgyógyászati angiológiai ellátás minimumfeltétele.
3. Definíció
Krónikus kritikus végtagischaemiáról beszélünk diabeteses és nem diabeteses betegen, ha a következő 3 ismérvből valamelyik fennáll:
- Több, mint 2 hete fennálló, tartósan visszatérő rendszeres fájdalomcsillapítást igénylő nyugalmi fájdalom.
- A bokán mért szisztolés vérnyomás kisebb, mint 50 Hgmm, az öregujjon mért vérnyomás kisebb, mint 30 Hgmm.
- A lábujjakon fekély, vagy gangraena van.
3.1. Kiváltó és kockázati tényezők Atherosclerosis obliterans:
A verőerek atherosclerosisa következtében kialakuló diffúz, degeneratív folyamat, mely a verőerek lumenének szűkületéhez, illetve elzáródásához vezet. Ennek következtében a keringés nem képes a szöveti oxigénigényt biztosítani. Ez enyhébb esetben claudicatio intermittenshez (Fontaine II stádium) vagy súlyosabb esetben szöveti károsodáshoz, kritikus végtagischaemiához vezet (Fontaine III, IV stádium). Alsó és felső végtagokon is előfordulhat, az alsó végtagokon sokkal nagyobb gyakorisággal.
A leggyakoribb az obliteráló érbetegség.
Kockázati tényezők:
dohányzás
diabetes mellitus
kor
atherogen dyslipidaemia hyperhomocysteinaemia emelkedett CRP hypertonia nem (férfiak)
emelkedett plazma fibrinogen szint emelkedett plazma- és vérviszkozitás
Thromboangiitis obliterans (TAO):
A kis- és közepes méretű artériák és vénák ismeretlen etiológiájú, szegmentális gyulladásos megbetegedése, mely elsősorban az alsó és felső végtagon jelentkezik, és gyakran kíséri Raynaud jelenség, illetve az esetek egy részében migráló phlebitis. Szövettani jellemzője az erősen gyulladásos, sejtes elemekben gazdag thrombus okozta érelzáródás, ugyanakkor az erekre terjedő másodlagos gyulladásos folyamat az erek strukturális károsodását jellemzően nem eredményezi, a lamina elastica interna érintetlen marad. Ez a tény és a szisztémás gyulladás és immunreakció hiánya adja a nekrotizáló vaszkulitiszektől, illetve az atheroscleroticus érkárosodástól való elkülönítés alapját. A perifériás érbetegek 0,5-5 %-a szenved TAO-ban (Európa).
Kockázati tényezők:
dohányzás
nem (férfiak)
Angiopathia diabetica:
Makroangiopátia: általában nem különbözikaz atheroscleroticus eredetű nagyérkárosodástól,de gyakrabban érinti a cruralis artériákat. Speciális formája a Mönckeberg féle mediasclerosis, mely az érfal diffúz elmeszesedésével jár, következményként az ér összenyomhatatlanná válik, mely diagnosztikus nehézséget okozhat (lásd Doppler vizsgálat). Mikroangiopátia: Jellemzője a kapillárisok basalmembránjánakdiffúz megvastagodása és mikroaneurizma képződés. Leggyakoribb klinikai megnyilvánulási formái a diabéteszes retinopátia, nefropátia, kardiopátia, illetve a diabéteszes láb szindroma. Ez utóbbi kialakulásában a mikroangiopátia mellett a neuropátia játssza a fő szerepet. Kockázati tényezők: 2-es típusú diabetes nem megfelelő glikaemiás kontroll
4. Panaszok/Tünetek/Általános jellemzők
Fontaine III. stádium: az érintett végtag nyugalmi fájdalma, mely előszőr éjszaka, majd állandóan jelentkezik Fontaine IV. stádium: trophicus zavar, gangraena, ulcus a végtagokon.
II. Diagnózis
1. Anamnézis
1.1. Családi kórtörténet: A családban atherosclerosis obliterans, thromboangiitis obliterans, diabetes mellitus, hypertonia, ISZB, ischaemias cerebralis laesio, dyslipidaemia előfordulása.
1.2. Előző betegségek: A kockázati tényezők tisztázása. Hypertonia, diabetes mellitus, ISZB, carotis atherosclerosis, stroke, dyslipidaemia előfordulása, azok stádiuma, tünetei, kórlefolyás.
1.3. Jelen panaszok: dysbasias panaszok, a dysbasiás távolság mértéke, nyugalmi panaszok, gangraena, Raynaud fenomen, ritkán migráló phlebitis.
2. Fizikális vizsgálatok:
Inspekcióval a végtag sápadtsága, lividsége, valamint a trophicus zavar konstatálható. Palpációval a végtagok hűvössége, a perifériás artériák pulzációja vagy annak hiánya, a nagy erek felett surranás észlelhető.
Auscultációval a nagy kaliberű artériák feletti systoles ejectios típusú zörej detektálható.
3. Kötelező diagnosztikai vizsgálatok
3.1. Laboratóriumi vizsgálatok vércukor, vese-, májfunkciós vizsgálatok, vérlipidek/összchol., HDL-chol., LDL-chol, triglycerid / vérkép haemostasis (vérzési idő, alvadási idő, PTI, prothrombin) vércsoport
3.2. CW (folyamatos hullámú) Doppler ultrahang vizsgálat
Adott érszakaszon a szisztolés vérnyomás meghatározható. Az értékekből a Boka/Kar index (az adott végtag bokánál mért magasabb szisztolés nyomás/a felkaron mért magasabb szisztolés nyomással) kiszámítható. A szisztolés nyomás mérésének protokollja a vizsgálandó érszakaszokon:
A vizsgálat előtt 5 percig a betegnek feküdni kell.
Doppler áramlásmérővel mérjünk.
Mindkét karon a szokásos helyen mérjünk, a magasabbal számoljunk.
Mindkét oldalt mérjük az ADP és ATP szisztolés nyomását, a mandzsettát közvetlenül a boka felett felhelyezve, a magasabbal számoljunk.
A felkar és boka mandzsetta azonos méretű.
A mérőfejet 60°- os szögben kell tartani.
Mindig a leeresztésnél mérjünk, soha a felpumpálásnál.
Lassan kell leereszteni a mandzsettát. (2 Hgmm/sec)
A Boka/Kar index normál érték: >0,9. Amennyiben 0,9-0,7 enyhe fokú, 0,69-0,4 kp. súlyos, <0,4 súlyos fokú érszűkületről beszélünk.
1,3 feletti értékazt jelzi, hogy az ér nem komprimálható. Ez gyakran fordul elődiabeteses mediasclerosis(Mönckeberg) és végállapotú veseelégtelenség esetén, ilyenkora hagyományos módon végzett Boka/Kar index meghatározás nem értékelhető. Ilyenkor egyszerű módszerrel, az ún. oszlop teszttel ("pole test") határozhatjuk meg a pedális erekben uralkodó nyomást: az alsó végtag emelésével párhuzamosan monitorozva a pedális pulzusnál meghatározzuk azt a magasságot, amikor a pulzus eltűnik. Ekkor a kalibrált tesztoszlopon leolvasható az aktuális nyomásérték. Nem komprimálható cruralis artériák esetén ajánlott azöregujjszisztolés nyomásának mérése (a distalis erek kalcifikációja ritkább).
Az öregujjszisztolés nyomásmérésének a módja:
CW Doppler, fotopletizmograf, ill. laser Doppler alkalmas a méréshez: Mandzsetta szélessége 2,5 cm, hossza: 10 cm. A vizsgálat előtt 5 perc pihenés.
Szobahőmérséklet 22 C° (a beteg soha ne érezzen hideget). A hallux hőmérséklete legalább 25 C° legyen.
4. Kiegészítő diagnosztikai vizsgálatok
4.1. Laboratóriumi vizsgálatoka kórképjellegétől függően:
Lp(a)
plazma fibrinogen
plazma- és vérviszkozitás, vvs-deformabilitás
thromboangiitis obliterans esetén immunológiai vizsgálatok (immunkomplexek,
antinukleáris antitest aktivitás, kollagén ellenes antitestek, stb.)
diabetes mellitus esetén Hgb A1C
thrombocyta funkcióra utaló vizsgálatok
CRP
4.2. Duplex ultrahang vizsgáló eljárással a verőerek fala, lumenük átjárhatósága, a véráramlási sebesség, a szűkület mértéke és a plakk morfológiájának a meghatározása lehetséges.
4.3. A mikrocirkuláció vizsgáló eljárásai
4.3.1. Transzkután oxigénnyomás mérése: A szöveti oxigénszint meghatározása kémiai elektróddal. A nyugalmi érték a claudicatio intermittens-szel jellemezhető időszakban a normálistól lényegesen nem tér el, azonban terhelést követően a normál szint elérése több időt igényel, mint kielégítő keringésű végtag esetén. Kritikus végtagi ischaemiában,ahol a mikrocirkulációis károsodott, a nyugalmi transzkután oxigénnyomás is kórosan alacsony értéket mutat ( 30 Hgmm alatt ), az ischaemiás régióban mértéke prognosztikus jelentőségű.
4.3.2. Laser Doppler áramlásmérés: Semiquantitatív módon méri a bőr mikrocirkulációját, a mért értékekből vérátáramlást számít. A nyugalmi áramlás vizsgálata mellett provokációs tesztek végzése is javasolt.
4.3.3. Kapillármikroszkópia: Statikus formájában a kapillárisok alakja, sűrűsége, tágassága, a bennük lévő áramlás és az interkapilláris tér eltérései figyelhetők meg. A dinamikus vizsgálat funkcionális tesztek végzésére is alkalmas.
4.4. CT-angiographia: Az érrendszer vizsgálatára alkalmas non-invazív eljárás. Nagy felbontást tesz lehetővé, de a sugárterhelése a beteg számára jelentősen magasabb a hagyományos röntgenfelvételekhez képest. Beszűkült vesefunkció, vagy kontrasztanyagérzékenység esetén alkalmazása kerülendő.
4.5. MR-angiographia: Non-invazív módon részletgazdag leírást ad az arteriák falának összetételéről, kisebb erek vizsgálatára is alkalmas. Kontrasztanyag-érzékenység esetén is alkalmazható. A betegtől a CT-nél nagyobb együttműködést igényel és fémimplantatum esetén nem alkalmazható.
4.6. Invazívvizsgálatok
4.6.1. Katéteres angiographia: Abban az esetben végezzük, ha az anatómiai viszonyok tisztázására ez a módszer áll rendelkezésre ill., ha intervenciós radiológiai beavatkozás szükségessége és elvégezhetősége felmerül.
III. Kezelés
A beteg megfelelő fekvőbeteg intézeti elhelyezése szükséges.
Nem gyógyszeres kezelés dohányzás elhagyása diétás tanácsadás
IN/2. Gyógyszeres kezelés
2.1. Atherosclerosis obliterans kezelése
2.1.1. A általános therápiája:
kockázati tényezők eliminálása (dyslipidaemia, hypertonia kezelése)
thrombocyta aggregáció gátló kezelés
a vér rheologiai viszonyait kedvezően befolyásoló kezelés
lipidszinttől függetlenül antilipidaemias kezelés fájdalom csillapítása
kísérő betegségek kezelése (szénhidrát anyagcsere, szívelégtelenség (pumpafunkció
javítása), anaemia rendezése (oxigénszállító kapacitás javítása)).
Megjegyzés: A hypertonia jelentős, hirtelen csökkentése kerülendő: emlkedettebb tenzió a végtag keringés biztosítása céljából átmenetileg elfogadható.
A végtag alacsonyabb pozicióba helyezése ugyancsakjavítja a perfúziót, lehetőleg anélkül, hogy oedemát okoznánk. Antibiotikum rutinszerű alkalmazása nem javasolt, azonban gangraenát kísérő gyulladásos reakció esetén szisztémás alkalmazása indokolt (Anaerob fertőzés veszélye !).
Kiemelt figyelmet érdemel a diabeteses betegekben kialakult seb kezelése. A gyakori infectio esetén antibiotikum alkalmazása, a seb szárazon tartása, felülfertöződéstől védése szükséges. A következményes osteomyelitis felismerése és kezelése alapvető a végtag sorsa szempontjából.
A gangraenas, purulens területeket el kell távolítani, a sebfelületeket lehetőség szerint szárazon kell tartani. Helyi kezelésként fertőtlenítő oldatok javasoltak, kerülendő az antibiotikum lokális alkalmazása. Az alapfolyamat progressziójánakgátlása, valamint az inmobilitás okozta fokozott thromboemboliás veszélyeztetettség miatt heparin profilaxis javasolt.
2.1.2. A krónikus kritikus végtagi ischaemia célzott kezelési lehetőségei: Intervenciós radiológiai beavatkozások (percutan translumináris angioplastika, stent implantáció, stb.)
Fibrinolysis ( lokális, szisztémás )
Érsebészeti beavatkozás. Amennyiben ez nem lehetséges, úgy hyperemizáló eljárás jöhet szóba.
2.1.3. Célzott konzervatív kezelés: Haemodilutio
Haemorheologiai kezelés (vazoaktív szerek, defibrinognáció)
Prostanoid kezelés
Heparin,
Hyperbaricus oxigénkezelés
Ezen therápiák invazív beavatkozások előkészítésére, illetve utókezelésre is javasoltak. Amputáció csak abban az esetben végzendő, ha angiológiai centrum (angiológus, érsebész, radiológus) véleménye szerint egyéb lehetőség nincs. Amputáció előtt képalkotó vizsgálat végzése kötelező az anatómiai viszonyok tisztázása céljából.
III/3. Az ellátás megfelelőségének indikátorai
Intervenciós radiológiai beavatkozások aránya.
Érsebészeti beavatkozások aránya.
Éves amputációk száma.
Amputált végtagok száma.
Mortalitás.
IV. Rehabilitáció
Lásd az "Angiológiai betegek rehabilitációja" protokollt
V. Gondozás
1. Rendszeres ellenőrzés: háziorvosnál havonta, angiológia szakrendelésen 1 hónap múlva, majd 3 havonta.
2. Megelőzés: nikotin absztinencia, rendszeres fizikai tréning, egészséges táplálkozás, rizikó állapotok rendszeres szűrése.
3. Kezelés várható időtartama/Prognózis
A kezelés folyamatos, a halálozás 1 év alatt 20%.
VI. Irodalomjegyzék
1. Blaskó György (szerk.): Az atherothrombosis. A patofiziológiai alapoktól a prevencióig. PharmaPress Kft. Budapest, 2003
2. Farsang Cs. (szerk). Hypertonia kézikönyve, 2. kiadás, Medintel Könyvkiadó, Budapest, 2002.
3. Hiatt et. al. (Eds).: Peripheral arterial disease, CRC Press, 2001.
4. Libby, P. Prevention and treatment of atherosclerosis. Harrison's Principles of Internal Medicine, 16th edition, Chap. 225,1430-1433,2005, The McGraw-Hill Companies, Inc.
5. Meskó Éva (szerk.): Vascularis medicina, Therápia kiadó, Budapest, 2004.
6. Meskó É-Farsang Cs-Pécsvárady Zs. (szerk.): Belgyógyászati angiológia, Medintel Könyvkiadó, Budapest, 1999.
7. Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II) Eur J Vasc Endovasc Surg 33, S1eS70 (2007)
8. European guidelines on cardiovascular disease prevention in clinical practice. Third Joint Task Force of European and other Societies on Cardiovascular Disease Prevention in Clinical Practice. European Heart Journal 2003; 24:1601-1610.
9. Third Report of the National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III) final report. Circulation.
2002;106(25):3143-421
10. Magyar Atherosclerosis Társaság: Összefoglalás a hyperlipoproteinaemiák kezelési irányelveiről. Összeállította a Társaság Munkabizottsága: Romics L., Szollár L., Karádi I., Pados Gy., Paragh Gy. Metabolizmus 2003;1:2-4.
A szakmai protokoll érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai protokollja
A cerebralis paresisről (CP)
Készítette: a Csecsemő- és Gyermekgyógyászati Szakmai Kollégium és a Rehabilitációs Szakmai Kollégium
Szinonima: spasztikus agyi bénulás
I. Alapvető megfontolások
1. A protokoll alkalmazási területe
Gyermek rehabilitációs ellátórendszer minden szintje, gyermekgyógyászat, gyermekneurológia, ortopédia
2. A protokoll kidolgozásának indoklása és körülményei
A cerebralis paresis (CP) gyermekkorban a leggyakoribb komplex rehabilitációt szükségessé tevő állapot, amelyben összehangolt multidiszciplináris tevékenységgel lehet eredményesen javulást elérni. Az elmúlt évek során számos olyan jelentős változás történt mind hazai mind nemzetközi téren a kórforma kezelésével és rehabilitációjával kapcsolatosan, ami indokolja, hogy új szakmai protokoll készüljön a CP ellátásáról. 2008. december 31-ig vannak érvényben az Ortopédiai Szakmai Kollégium, valamint a Neurológiai Szakmai Kollégium Gyermekneurológiai Szakcsoportja által készített szakmai protokollok, amelyekben a rehabilitáció szempontjai csak említés szintjén szerepelnek (1,2-C). Készítésük óta jelent meg 2005 áprilisában egy neves nemzetközi munkacsoport által készített ajánlás: Proposed definition and classification of cerebral palsy, April 2005" (3-B). A fogyatékosságok fogalomrendszerének 2001-ben elfogadott általános újnómenklatúrája,az International Classification of Funtioning, Disability and Health (ICF) 2004-ben magyar nyelven kiadásra került és 2004 óta a rehabilitációs fekvőbeteg intézményekben használata kötelező (4,5-C). Az FNO gyermekváltozata is elkészült, de még nem áll rendelkezésre magyar nyelven (6-B). 2005. ősztől 2008. december végéig terjedő időszakra a magyar kormány jóváhagyta a "Közös kincsünk a gyermek" Nemzeti Csecsemő és Gyermekegészségügyi Programot, amelynek VIII. Céljában a gyermek rehabilitáció hazai rendszerének kiépítése van kitűzve. A program részét képezi az ellátó rendszer fejlesztésén és a gyermek rehabilitációs szakemberek képzésének szorgalmazásán túl a szakmai protokollok és irányelvek továbbfejlesztése, így jelenleg négy szakmai protokoll van kidolgozás alatt beleértve a jelen protokollt (7-D). Az utóbbi öt évben több olyan nemzetközi szakmai ajánlás, irodalmi áttekintés, metaanalízis és kontrollált klinikai vizsgálat jelent meg, amelyek a CP ellátásában alapvető fontosságú megállapításokat tartalmaznak szakmai és költséghatékonysági szempontból egyaránt (8,9,10,11,12-B). Végezetül 2007. januárban kiadásra került az újWhite book on physical and rehabilitation Medicine", ami a Union Européenne des Médicins Spécialites (UEMS) fizikális és rehabilitációs orvoslási szekciójának európai tanácsa, a L'Academie Européenne de Médicine de Réadaptation és a The European Society of Physical and Rehabilitation Medicine (ESPRM) közös munkájaként született rehabilitációs elveket foglalja össze (13-B).
3. A protokoll bevezetésének feltétele
Megfelelő tájékozottság a fent említett szakmákban. Ennek érdekében a szakemberek képzésének szorgalmazása szükséges nemcsak a már említett szakorvosképzésben, de a rehabilitációban szükséges további team tagok képzésében is (14-C; 7-D).
4. A bizonyítékok forrásai a következők
A: nagyszámú randomizált, ellenőrzött klinikai prospektív vizsgálaton vagy metaanalízisen alapuló eredmények, vagy randomizált, ellenőrzött tanulmányban és legalább három nemzeti vagy nemzetközi szakmai irányelvben szereplő megállapítások
B: előbbinél kisebb betegszámon alapuló randomizált és ellenőrzött vizsgálatok vagy szisztematikus áttekintések
(review), vagy legalább három nemzeti vagy nemzetközi szakmai irányelvben szereplő megállapítások
C: nemzeti vagy nemzetközi szakmai irányelvben szereplő megállapítások, nem randomizált, de szisztematikus értékű klinikai vizsgálaton alapuló eredmények
D: szakértői testület egyeztetett véleménye
B-C: Tankönyvek, monográfiák esetében a bizonyítékokra együttesen hivatkozunk
5. Definíció
A CP a tartás és a mozgás zavarainak nem-progresszív szindróma-csoportját jelenti, amely a tevékenységek korlátozásával jár, és amelyet a fejlődőben lévő (magzati élet, csecsemő ill. kisdedkor) központi idegrendszert ért károsodásokokoznak. A motoros rendszer zavarát gyakorta kísérik az érzékelés, a kognitívkészségek,a kommunikáció, a percepció és / vagy a viselkedés zavarai ill. epilepsiával járó állapotok. CP-ben gyakran alakulnak ki ortopédiai komplikációk (3-B). A CP minden formájának ellátása: diagnosztikája, kezelése és rehabilitációja multidiszciplináris megközelítést tesz szükségessé.
5.1. Klasszifikáció
Nemzetközi munkacsoport tekintette át azokat a szempontokat, amelyeknek érvényesülni kell az osztályozásban ahhoz, hogy standardizált beosztási rendszert kapjunk (3-B). Ezek a következők:
(1) leíró jelleg: pontos leírás az adott személy mozgászavarának természetéről és súlyosságáról;
(2) jósló jelleg: olyan információk, amelyek a jelenlegi és a később várható szolgáltatásokkal kapcsolatos szükségleteket tartalmazzák;
(3) összehasonlító jelleg: a különböző helyeken elvégzett beosztások egymással megbízhatóan összevethetők legyenek;
(4) a változások követésére alkalmas jelleg: ugyanazon személy jellemzésére az időben változó állapot ellenére is alkalmas legyen.
Besorolás:
- Típus szerint (spasztikus, dyskinetikus, ataxias)
- Eloszlás szerint (egy vagy kétoldali ill. alsó végtagi vagy felső végtagi túlsúlyú: hemi-, és di- és tetraparesis vagy
-plegia))
- Súlyosság szerint (Gross Motor Function Classification System - GMFCS I-V szint)
- Ko-morbiditás szerint (epilepszia, kognitív zavarok, érzékelési, érzékszervi zavarok)
5.2. Érintett szervrendszerek
Elsősorban a központi idegrendszer érintettsége jellemző, felső motoneuron szindróma képében. A nagyagy különböző részei:acortex,a corticospinális pályarendszer, az agyalapi szürke magvak, az agytörzs, a nyúltagy, a kisagy és a corpus callosum egyaránt érintve lehet (15,16-C). A perifériás manifesztációka test izomzatát (törzs és a végtagok, arc) továbbá az érzékszerveket és egyes belszervi funkciókat érintik. Az agykárosodás lokalizációjától függően a kognitív képességek, a beszéd, a viselkedés zavarai is létrejöhetnek (17,18-A; 19-20-C; 1-C). A másodlagos változások, amelyek a CP természetes lefolyása következtében alakulnak ki, a fejlődés kapcsán változhatnak, kóros ízületi és végtagállás alakulhat ki (21-C). A hasznos mozgás, a járás, a fogás jelentős mértékben károsodhat.
5.3. Kiváltó tényezők
ACP szindrómát az éretlen agyat ért különféle noxákaz intrauterin életben, szülés alatt vagy az első három életévben okozhatnak CP-t (18-A; 22-B; 19,20-C). A genetikai ártalmak és a méhen belüli infekciók gyakorta szerepelnek kóroki tényezőként (23-B; 24-C). Az első és második trimeszterben elsősorban agyi fejlődési zavarok, a harmadik trimeszter korai szakában PVL és agyvérzés, míg a terhesség késői szakában corticalis vagy subcorticalis és mély agyi szürkeállomány léziók okozzák. Hátterükben többnyire agyi hypoxia és/vagy ischemia áll (26-B; 20,25-C).
5.4. Kockázati tényezők
Éretlenség, elhúzódó vagy gyors, nehéz szülés, anyai EPH gestosis, köldökzsinór vagy lepény rendellenességek, perinatalis hypoxia, infekció, korai burokrepedés, tartós mechanikus lélegeztetés, ikerterhesség (28-B; 27,29-C). 1000 g-nál kisebb születési súlyú újszülöttekben 17% a CP előfordulási gyakorisága, míg az átlagos populációban ez az arány 2-4 %o (22,26-B; 25-C).
5.5. Genetikai háttér
Genetikai okot egyre gyakrabban tudnak kimutatni. Ez lehet a cerebrovascularis kórképekre hajlamosító genetikai konstelláció vagy öröklött agyi fejlődési zavar vagy egyéb neurogenetikai rendellenesség (15,30,31-C).
5.6. Incidencia/Prevalencia/Morbiditás/Mortalitás
Prevalenciája 2-4 / 1000 gyermek a 3-10 éves korosztályban. Az extrém kis súllyal születettek között az elmúlt évtizedekben csökkent a CP gyakorisága (28,30-B). A súlyos esetekben a mortalitás meghaladja az átlagos populációét (36-B; 15,25,27,32,33,34,35-C; 37-C).
5.7. Jellemző életkor
A teljes tünet együttes rendszerint 12-18 hónapos korra bontakozik ki, ezt követően a nagyon enyhe esetek kivételével a teljes élettartam alatt fennállnak a tünetek. Általában a 4-5 éves életkort tekinti az irodalom mérvadónak a CP végső kialakulására (3,38-B; 18,20,21-C; 37-C).
5.8. Jellemző nem
Mindkét nemben egyforma gyakorisággal fordul elő (10-B; 18-C). 2. A rehabilitáció célja
A rehabilitáción a CP-s gyermek és később felnőtt élethossziglan tartó, életszakaszonként változó szükségletű ellátási rendszerét értjük, amelyet cél-orientált módon valósítunk meg, és amelynek időről időre eredményesnek kell lenni. A CP tünetei változatos kombinációban és súlyosságban jelentkeznek minden egyes gyermekben (21,39-C). Az individuális jellemzők rehabilitációs szempontból probléma-csoportokra oszthatók, amelyek jól definiálható rehabilitációs célokat jelölnek. Az alábbiakban a rehabilitációs célokat a fogyatékosságokjellemzői alapján soroljukfel.
2.1. Mozgásfogyatékosság: lehetnek nagymotoros, finom mozgásokat érintő, egyensúlyi, tartási, vizuo-motoros és oromotoros funkciózavarok ill. ezek kombinációi.
A rehabilitáció célja: a lehető legnagyobb önállóság elérése a motoros funkciókban, így önálló járás, stabil állás, önálló vagy támasztott, de statikailag helyes ülés, önálló hely- és helyzetváltoztatás, fogás, mindennapi élettevékenység (ivás, evés, öltözés, gombolás, stb.) során önálló kézhasználat, írás, rajzolás és egyéb kézügyesség, továbbá az önálló evés, az étel megrágása, a beszédhez szükséges oromotoros funkciók elsajátítása, továbbá a CP-s gyermek és családja életminőségének javítása (18-A; 40-B).
A mozgásfogyatékosságot a CP-s gyermekek 80%-ában a spaszticitás okozza (18-A; 9-B). A spaszticitás mérséklésének speciális céljai:
- Motoros funkciókjavítása (nagymozgások, finom motorika, koordináció, egyensúly, tartás)
- Kontraktúrák kialakulásának lassítása / megakadályozása / kialakult kontraktúrák oldása
- Ápolhatóság biztosítása
- Fájdalom elkerülése / kezelése
2.2. Beszédfogyatékosság és a kommunikáció zavarai
A rehabilitáció célja: a lehető legnagyobb önállóság elérése a kommunikációban verbális vagy egyéb kommunikációs csatornák segítségével (17-A).
2.3. Értelmi fejlődés zavarai (pszichomotoros fejlődési zavar, értelmi fogyatékosság, tanulási zavar)
A rehabilitáció célja: a lehető legnagyobb önállóság elérése a kognitív képességekben, ezzel a lehetséges legkorábban beilleszkedés az óvodai ill. az iskolai oktatásba, optimális esetben a többségi oktatási rendszerben (41-C; 42-B-D).
2.4. Érzékszervi fogyatékosságok: a látás és a hallás zavarai
A rehabilitáció célja: a lehető legnagyobb önállóság elérése az életvezetésben a látási és hallási funkciók javításával (43-B-C; 44-C).
2.5. Epilepszia: az egyik leggyakoribb és az életminőséget leginkább rontó idegrendszeri tünet.
Amennyiben a CP értelmi fogyatékossággal is együtt jár előfordulási gyakorisága 90 % is lehet. A különböző CP formákban - értelmi fogyatékosság nélkül - az előfordulási gyakoriság kisebb, spaszticus hemiparesisben 50 %, spasztikus diplegiaban 40%, míg spasztikus tetraparesisben 70 % is lehet. A rehabilitáció célja: a lehető legnagyobb önállóság elérése az életvezetésben (43-B-C)
2.6. Egyéb fogyatékosságok: magatartási, viselkedési zavarok
A rehabilitáció célja: a lehető legnagyobb önállóság elérése, közösségi élet akadályainak mérséklése (43-B-C; 37-C).
2.7. Az önállóság (önkiszolgálás, önálló közösségi élet) zavarai
A rehabilitáció célja: a lehető legnagyobb önállóság elérése, közösségi élet akadályainak mérséklése. Felnőtt életre felkészülés, a későbbiekben munka világába történő beilleszkedés elősegítése. A testi, a kognitív és a pszichés fogyatékosságok együttese ill. összessége határozza meg az elérhető maximális önállóságot. Ennek fenntartása a felnőtt korra átívelően szükséges (45-C).
A CP-s gyermekek ill. felnőttekellátásában az alábbi team tagok vehetnek részt: rehabilitációs szakorvos (mozgásszervi rehabilitációs és gyermekgyógyász vagy orvosi rehabilitáció gyermekgyógyászat ill. gyermek rehabilitáció területén szakvizsgával), gyermekgyógyász, belgyógyász, neurológus, gyermekneurológus, idegsebész, ortopéd szakorvos, szemész, audiológus, szakasszisztens, ápoló, logopédus, gyógytornász-fizioterapeuta, pszichológus, szociális munkatárs, konduktor, ergoterapeuta, szomatopedagógus, fejlesztő pedagógus, tanár, kreatív terapeuta (zene, képzőművészet), hippoterápiás oktató, gyógyúszás oktató, gyógytestnevelő, ortopéd műszerész, rehabilitációs szakmérnök és egyes esetekben más szakemberek is.
A rehabilitáció során funkciózavarok komplex ellátására törekszünk. A team munkában végzett tevékenység összehangoltan, cél-orientáltan zajlik.
3. A rehabilitálhatóság feltételei
A rehabilitációs alkalmasság megállapításának menete
3.1. Gyanút keltő tünet(ek) felismerése különböző ellátókban történhet (szakorvosi ill. fokozottan veszélyeztetettek gondozói rendszerében vagy a háziorvosnál), de előfordul, hogy az első gyanújeleket a szülők vagy laikusok veszik észre.
3.2. Szakintézeti diagnosztikai vizsgálat (speciális gyermek ambulancia, gyermekneurológiai, gyermek-rehabilitációs vagy gyermekortopédiai vizsgálat) a gyanút megerősíti.
3.3. Kivizsgálás: okkeresés, társuló rendellenességek feltárása (specializált gyermekkórház vagy klinika és egyéb speciális ellátók: gyermekneurológiai, genetikai, szemészeti, audiológiai, gyermekpszichiátriai), képalkotó és funkcionális elektromos vizsgálatok elvégzése.
3.4. Funkcionális kivizsgálás: rehabilitációs team (gyermek rehabilitációs szakorvos, pszichológus, gyógytornász-fizioterapeuta, pedagógus, logopédus): funkcionális besorolás, egyéni rehabilitációs terv készítése.
3.5. Gyógypedagógiai Rehabilitációs Szakértői Bizottsági vizsgálat amennyiben a sajátos nevelési szükséglet felmerül: integrált / speciális fejlesztés vagy óvodai / iskolai nevelés elrendelése.
II. Diagnózis
4. A rehabilitációs program elemei 4.1. Anamnézis
A CP kialakulásával összefüggést mutató anamnesztikus tényezők számosak. Kiemelten fontos a többedik terhesség, ikerterhesség, chorioamnionitis, anyai infekció, antepartum vaginális vérzés, elhúzódó, rohamos szülés, késői Apgar érték, élesztés, lélegeztetés, elégtelenül kezelt hyperbilirubinaemia, magzati anoxiás epizódok, magzati infekciók (elsősorban meningitis, ventriculitis) és a periventrikuláris leukomalácia (PVL). Az immaturitás az egyik legfontosabb hajlamosító tényező (22,26-B; 19,25-C).
Az anamnézis gondos felvétele során az alábbi korai, aspecifikus tünetekfelderítése szükséges (42,43,46-B-C;47-C; 1-C):
a. Tartási rendellenességek(ökölképzés, elhúzódó flexiós tartás, aszimmetrikus tartás, a fejlógatása ülésbe húzáskor ill. lebegtetett ülésben)
b. Perzisztáló újszülött reflexek (Moro, markolás, talpi fogóreflex, szimmetrikus és aszimmetrikus tónusos nyaki reflex)
c. Izomtónusbeli eltérések (csökkent vagy fokozott tónus)
d. Késve mutatkozó beállítódási és vesztibuláris reakciók (ejtőernyő reakció, támaszreakció, fej beállítódási reakciók)
e. Lassult és/vagy minőségileg eltérő nagymotoros, finom motorikai,vizuomotoros fejlődés, amit gyakorta kísérneka mentális és érzékszervi fejlődés zavarainak korai jelei vagy/és epilepsia
f. Táplálással kapcsolatos nehézségek (a szopás ritmusának, minőségének eltérései, gyarapodás zavara, félrenyelés, a levegővétel és a szopás ritmusának zavara)
g. Nyugtalanság, fokozott irritabilitás, amelyet gyakori sírás vagy / és az alvás és ébrenlét ritmusának zavara kísér
4.2. Panaszok, tünetek
A klinikai tünetek a központi idegrendszert ért károsodás kiterjedésétől, lokalizációjától és súlyosságától függenek (18-A; 43-B-C). A CP gyűjtőfogalom, egyes formáiban a tünetek nem azonos időben és sorrendben mutatkoznak (21-C; 42-B-C).
A CP-s gyermekek döntő többségének vannak a mozgászavar mellett egyéb fogyatékosságai is, amelyek a szülő számára komoly gondot jelenthetnek. Gyarapodási képtelenség, alvás-ébrenlét ritmusának zavara, székrekedés, vizelet-inkontinencia, fokozott nyálcsorgás, fájdalmak, ápolhatóság nehézségei (hajlatok tisztántartása), etetési nehézségek, szokatlan sírás, beszédképtelenség, beszédzavar, figyelmi problémák. Az életkor előre haladtával egyre szembetűnőbbek a magatartási, tanulási és szocializációs zavarok (17,18-A; 22-B; 45,47-C). Az alábbiakban rendszerezve kerülnek felsorolásra a jellemző tünetek.
Diagnosztikus tünetek szakasza 9-18 hónapos kor után
Többlet (pozitív/plusz) motoros tünetek) (42,46-B-C; 47,48-C; 1-C)
a. Izomtónusbeli eltérések: fokozott izomtónus, hipertónia - elsősorban az érintett végtagokban és csökkent tónus, hipotónia - leggyakrabban az axiális izmokban
b. Felső motoneuron lézióra jellemző dinamikus spaszticitás (nyújtási sebességtől függő tónusfokozódás) ill. akaratlan szinkinézisek, kóros szinergizmusok (izolált mozgáselemek kiépülésének késése vagy zavara)
c. Fokozott saját reflexek
d. Kóros reflexek (perzisztáló archaikus reflexekés hosszúpálya tünetek)
e. Patológiás reflexek és patológiás vagy megkésett poszturális reflexek
f. Kóros testtartások, kényszertartások, aszimmetriák
g. Fokozott nyálcsorgás
Hiányzó (negatív/mínusz) motoros tünetek) (17-A;42,46- B-C; 47,48-C; 1-C)
a. Ügyetlenség (koordináció, nagy és finom mozgások terén)
b. Gyengeség, csökkent izomerő, fokozott fáradékonyság
c. Megkésett vagy hibás mozgásfejlődés, amelyet gyakorta kísérnek alternáló mozgások helyett együttmozgások és tükörmozgások
d. Hiányzó vagy zavart testvázlat, a statikus és dinamikus testkép, a motoros minta hiánya
e. Testséma zavarok
f. Rágás nehezítettsége vagy képtelensége
g. Beszédfejlődés késése, fonációs, artikulációs zavarok
Másodlagos vagy "természetes lefolyás" során mutatkozó motoros tünetek (42,46-B-C; 48,50-C; 1-C)
a. Kontraktúrákjelennekmeg (a csontok növekedése meghaladja az izom-ín-kötőszöveti egység nyúlási és növekedési képességét)
b. A dinamikus spaszticitást rigiditás válthatja fel, amely gyakorta fájdalmas
c. Megnő a mozgások energiaszükséglete
d. A testen viselt ortéziseket egyre nehezebb tolerálni
e. Járásképes CP-sekben jellegzetes kóros járásmódok jönnek létre: "jump gait", "crouch gait", "stiff gait", "recurvatum gait", "intoeing-outtoeing gait" - mindegyik jellegzetes kinematikai és kinetikai profillal bír járásanalízis során
Egyéb fogyatékosságokkal és a kísérő betegségekkel összefüggő funkcionális zavarok és tünetek (17,18-A; 22-B; 45,49-C).
a. Kognitív képességek zavara (30%) (18-A; 42-B-C)
b. Beszédértés és beszédprodukció zavarai (17-A)
c. Neurológiai problémák (42,43-B-C; 41-C) Epilepszia (CP típusonként változó gyakorisággal) a felső végtagok érzékelési zavarai (97%) hydrocephalus (9%)
d. Vizuális percepciós zavarok (20-40%) (44-C)
e. Hallászavarok (42,43-B-C)
f. Autonóm diszfunkciók (vizelet és széklet inkontinencia, táplálkozási nehézségek) (42,43-B-C; 49-C)
g. Tanulási nehézségek (44,45-C; 52-D)
h. A hemiplegiásokra különösen jellemző (51-C) abnormális stereogosis (97%)
csökkent két-pont-diszkrimináció (90%) csökkent propriocepció (46%).
i. Iskolai teljesítmény zavarokelsősorban a tetraplegiás értelmileg is érintett gyermekekben fordul elő (42-B-C;45,52-C)
4.3. Funkcionális vizsgálatok
4.3.1. A fogyatékosság és a részvétel értékelése
Számos nemzetközileg ismert teszt szolgál az aktivitás és a részvétel (szociális beilleszkedés) meghatározására. Az FNO az idősebb gyermekekben és a felnőttekben alkalmas az aktivitás és a részvétel leírására, az akadályozó és a segítő környezeti tényezők értékelésére (4,5-C). Az FNO gyermekváltozata, az ICF-YC tartalmazza a gyermekre vonatkozó speciális szempontokat, ennek a magyarnyelvű fordítása azonban még nem áll rendelkezésre (6-D). Hasonló a helyzet a FIM skálával, amelynek szintén van gyermekváltozata: a WeFIM skála, amely nemzetközileg széles körben használt, azonban nincs hivatalos magyar fordítása (53-C; 54-B; 55-C). Az életminőség mérésre kifejlesztett kérdőívek közül nemzetközileg elterjedt a PedsQL, de használnak betegség-specifikus életminőség vizsgáló eszközt is (56,57,58-B). A magyarországi alkalmazás szórványos jelenleg.
4.3.2. A funkcionális aktivitás értékelése
- Motoros aktivitás értékelésére szolgál gyermekkorban a Gross Motor Function Measure (GMFM) teszt, amelyet célirányosan CP-s gyermekek nagymotoros funkcióképességének vizsgálatára fejlesztettek ki (60-B; 59-C). A Bruininks-Ozereczky és a Peabody mozgásteszt nem ennyire CP-specifikus, de hasonlóan elterjedt (61,62-C). Utóbbiakban a finom mozgások értékelésére is van lehetőség. A felső végtagok funkcionális vizsgálatának legismertebb módszere a Quality of Upper Extremity Skills Test (QUEST) és a Manual Ability Classification System (MACS) (63,64-B). A tesztek magyarországi elterjedése még várat magára.
- A kognitív funkciók értékelésére IQ tesztekkel történik, ezek alkalmazása az életkori normák szerint történik (56-B; 42,65-B-C).
4.3.3. A testi funkciók és a károsodások vizsgálata
- A funkcionális vizsgálatok típusa is változik a gyermek életkorával. Csecsemő és kisdedkorban a fejlődésneurológiai (Katona-féle, Vojta, Prechtl, Dubowitz,stb.) (43,65-B-C) és a fejlődéspszichológiai (Bayley II, Brunet-Lezine, Griffith, stb.) tesztvizsgálatok eredményére lehet támaszkodni (42,65,66-B-C; 67-C).
- Későbbi életkorban és a felnőtté válást követően specifikus mozgásvizsgáló és egyéb tesztek alkalmazhatók: az izületi mozgástartomány mérése goniometriával, az izomerő dinamométerrel történhet (68-B; 42,65-B-C). A spaszticitás megítélésére az Ashworth skála, a Tardieau index, a dystonia megítélésére a Barry-Albright dystonia skála szolgál (69-B; 42,65-B-C). A károsodás objektívebb megítélését szolgálja a 6 perces járásteszt a terhelhetőség megítélésére, az energia felhasználás mérése, az egyensúly értékelése és a járás megfigyelése ill. computeres analízise (40-B; 70,71,72-C). A károsodás mértékének globális megítélésére szolgál a GMFCS besorolás, ami 5 súlyossági kategóriát ír le a mobilitási szintek alapján (73,74-C). A terápiás válaszok megítélésében alkalmazható az un. célskála (goal attainment scale- GAS) és a vizuális analóg skála (VAS) is (75-B; 76-C).
- Az egyéb funkciók károsodásánakértékelése a beszéd-, a látás-, a hallászavarok kimutatásában a szokásos teszteket és vizsgálatokat alkalmazzuk (56-B; 65,66-B-C).
4.4. Diagnosztikai vizsgálatok
A központi idegrendszer károsodása miatt a diagnosztikai szakaszban együttműködő team tagjai: gyermekneurológus, gyermekgyógyászati neuro-radiológiában jártas szakember, gyermekgyógyász, szemész, gyermek rehabilitációs szakorvos, gyermek orthopéd szakorvos, pszichológus, gyógytornász, EEG szakasszisztens, gyógypedagógus és szükség esetén további szakemberek.
4.4.1. Klinikai vizsgálatok leírása a 2. pontban.
4.4.2. Képalkotó vizsgálatok: koponya sonográfia (nyitott nagykutacs szükséges). A CP etiológiájának, ill. pathogenesisének meghatározásában a koponya MRI vizsgálat alapvető jelentősége van (77-A; 78,79-B). Az USA-ban 2004-ben készített ajánlásban a pontos oki diagnózis ismeretének hiánya agyi képalkotó vizsgálat elvégzését tartja szükségesnek.
Amennyiben rendelkezésre áll, az MRI van első helyen a CT-vel szemben (77-A).
4.4.3. Metabólikus és genetikai vizsgálat CP-ben rutinszerűen nem szükséges. Amennyiben a képalkotó vizsgálattal, az anamnézis alapján vagyatípusos megjelenés miatt gyanú merül fel, ezen vizsgálatok elvégzendők (77-A).
4.4.4. Funkcionális elektromos vizsgálatok: EEG (elsősorban görcstevékenység megállapítására), kiváltott potenciál vizsgálatok (BERA, VEP) (1-C).
4.5. Differenciál diagnosztika
Differenciáldiagnosztikai szempontjából felmerülhetnek neuromuscularis és neurometabóliás kórképek, így spinalis izomatrophia, herediter sensomotoros betegségek, idiopathias v. familiaris lábujjhegyen járás, familiaris spasztikus paraplegia, egyéb genetikai vagy szerzett neurológiai betegségek (39,79-C).
III. Kezelés
5. Intervenciós stratégiák: terápia és rehabilitáció
CP-ben a terápiás és a rehabilitációs tevékenység gyakorta egymást fedve, párhuzamosan vagy egymást váltva történik (18-A; 80-C). Egyes beavatkozások tekinthetők terápiának is és rehabilitációs ténykedésnek is. Ugyanazt az eljárást team munkában alkalmazva a rehabilitáció folyamatába illesztve nagyobb hatásossággal, költséghatékonyabban és eredményesebben lehet alkalmazni, mint izolált terápiaként (9,10-B). Erre jó példa a Botulinum toxin A kezelés. Hatásosságát B szintű evidenciák sora bizonyítja, költség-hatékonysága és eredményessége azonban kombinációban (dinamikus boka ortézissel, célzott gyógytornával és elektroterápiával) alkalmazva lényegesen felülmúlja az izolált alkalmazást. Éppen ezért a kezelés relatív kontraindikációi közé sorolják ma már azt, ha nem állnak az adjuváns terápiák rendelkezésre (B-11; 81-C).
5.1. Nem gyógyszeres megközelítések
5.1.1. Mozgásterápia
Célok: az izületi mozgástartományok megőrzése és javítása, a spaszticitás mérséklése, a gyengébb antagonista izomzat erősítése, izomerő növelése, ügyesség fokozása, a motoros, a beszéd, az értelmi és a szociális fejlődés elősegítése (82-C).
Technikák:
Fizioterápia
- Reflexgátló, spaszticitást csökkentő gyógytorna
A gyógytorna tekinthető a CP bázis terápiájának. Az un. "Neuro-Developmental Training - NDT - gyermek Bobath" a világon a legelterjedtebb eljárás, ez a nemzetközi etalon (9,10,11, 83,84,85-B). Egyéb fizioterápiás módszerek hatásosságát is ehhez viszonyítják. Általános tapasztalat, hogy az egyes kezelési eljárások között messze nincs olyan különbség az eredményességben, mint ami a gyógytornával kezelt és terápiában nem részesített gyermekek között mutatkozik (Vojta, Delacato, Kabat) (85-B; 86-C). Ez a megállapítás részben annak tudható be, hogy nagyon kevés B szintű evidencia áll rendelkezésre e téren. Hasonló a helyzet a terápiás program tartamának, hetenkénti gyakoriságának kérdésében. A terápia mennyiségének növelése nem feltétlenül jelenti az eredményesség javulását (11-B). A szakaszolt (2-4 hetes), igen intenzíven adagolt terápiák tartós hatásában sincs lényeges különbség a szokványos rendszerben végzett kezelésekéhez képest (87,88-B; 89-C).
- Izomerősítő módszerek
Az izomzat erősítését szolgáló módszerekkel az alsó végtagokban elsősorban az extensor izomcsoportok (gluteus maximus, quadriceps, tibialis anterior) gyengesége miatt szükséges alkalmazni. Egyrészt gyógytorna, másrészt elektroterápia alkalmas erre a célra.
- Gyógytorna: elsősorban célzottan végzett izokinetikus gyakorlatok, továbbá nagyobb gyermekekben a célzott izomerő fejlesztés és a kardio-vascularis állóképesség megőrzésére végzett gyakorlatok alkalmazhatók (8,90,91-B)
- Elektroterápia: Funkcionális elektromos stimuláció: a gyenge antagonista izomzat erősítésére szolgáló funkcionális elektrostimulációról készült eddigi felmérésekalapján a hatásosság biztonsággal nem állítható, bár több adat szól mellette, mint ellene (93-B; 94-C)
- Kényszerítéssel indukáló terápia (Constraint Induced Movement Therapy - CIMT)
Speciális rehabilitációs megközelítést alkalmaz ez a terápia az egyik oldali végtagokat érintő folyamatokban (hemiparesis). Kifejlesztése a 70-es években kezdődött, eleinte felnőttekben, majd kiterjesztették alkalmazását gyermekekre (95-C; 96-B). Lényege, hogy az époldali felső végtag használatát korlátozzák (könnyű ortézises "lekötéssel") naponta legalább 6 órára néhány héten át, ezzel kényszerítve a paretikus kéz használatára (96-B). A kezelés ismételhető, ami fokozza hatását (97-C).
- Egyensúlyt javító terápiás megközelítések
Futószalagon végezhető tréning alkalmazható a járásképes (ill. támasztással segített módon járásképes) CP-s gyermekek esetében az egyensúly és a testsúly áthelyezés gyakoroltatására (98-B; 99-C). A Hydroterápiás Rehabilitációs Gimnasztika (HRG) is elsősorban a mozgáskoordinációt javító tréningprogram. Hazánkban kifejlesztett módszer, amelynek egyes elemei alkalmazhatók tornatermi körülmények között is. Hazai módszer a Dévény-féle speciális manuális technika is, amely a kötőszöveti ín-izom-pólya kapcsolódások letapadásainak oldásával javítja a mozgástartományt, és ezzel az egyensúlyt. A művészi torna és a gimnasztika tradicionális elemeinek adaptálásával hozzájárulhat az egyensúly javításához (1,100-D).
- Újabb megközelítések
Kéz-kar bimanuális intenzív terápia (hand-arm bimanual intensive therapy - HABIT) a hemiparetikus gyermekek kezelésében kezd újabban tért hódítani és ígéretesek az első eredmények (101-B). A "virtual reality" (VR) kezelésmóddal is a féloldali bénulásban a contralateralis agykéreg működésének serkentését végzik indirekt módszerrel (102-C).
- Komplementer eljárások
Hydroterápia, hideg és meleg kezelések, hippoterápia, gyógyúszás, akupunktúra/akupresszúra. Ezek hatásosságára jelenleg változó erősségű bizonyítékok állnak rendelkezésre, amelyek nem vetik el, de nem is bizonyítják ezen eljárások eredményességét (103,104,105,106-C).
5.1.2. Konduktív pedagógiai nevelés (Pető módszer)
Speciális nevelési jellegű pedagógiai megközelítés, amelyet elsősorban csoportos formában lehet eredményesen alkalmazni. Az óvodai és iskolarendszerű napirendnek megfelelően, napi több órás foglalkoztatás keretében tanítja az önellátást, e mellett a konduktori rávezetés mozgásvezérlést eredményezhet, miközben az akaraterőt is fejleszti (107,108,109-B; 110-D). A konduktív pedagógiai megközelítést a hazai gyakorlatban más terápiákkal kombináltan alkalmazzuk.
5.1.3. Beszédterápia és kommunikáció fejlesztés
A beszédfejlesztés ill. a non-verbális kommunikációs képességek kialakítása a CPs gyermekek rehabilitációjának a mozgásfogyatékosság okozta nehézségek leküzdése mellett a másik kiemelt területe. Az önállóság fokát meghatározó mozgás- és beszédképességben egyaránt keverednek a motoros, a szenzoros és a kognitív funkciók zavarából adódó fogyatékosságok. A beszéd és más kommunikációs jelek megértése elsősorban a mentális képességeképségéhez, míg a verbális és non-verbális expresszív kommunikáció inkább a szenzoros és a motoros funkciók képességszintjéhez kapcsolható (111-C).
A rehabilitáció során a tevékenység irányulhat közvetlenül a gyermekre - direkt fejlesztés formájában és a környezetében élőkre - kommunikációs lehetőségek tanítására. A beszédfejlesztő és egyéb alternatív ill. augmentatív kommunikációs eljárások hatásosságára nézve megdönthetetlen erejű bizonyíték nincs, azonban a vizsgálatok többségéből pozitív tapasztalatok származnak (17-A). A szülők / gondozók kommunikációs ismereteinek gyarapításából származó előnyökre nézve kevesebb adat áll rendelkezésre, ami ezek hatékonyságára nézve nem ad elegendő információt (17-A)
5.1.4. Rehabilitációs foglalkoztató terápia (ergoterápia)
Az ergoterápia a CP-s gyermekek rehabilitációjának harmadik pillére. A nemzetközi gyakorlatban elterjedten használatos, azonban eddig mindössze 5 tanulmány jelent meg értékeléséről, amelyek közül kettő tekinthető szisztematikus áttekintő tanulmánynak. Jelenleg folyamatban van egy Cochrane szisztematikus áttekintés készítése (112-B). Hazánkban a konduktív pedagógiai rendszerben (5.1.2.) és a gyógypedagógiai fejlesztés során történik az önállóságra nevelés. A foglalkoztató terápiának gyermekkorban nincs elegendő hagyománya, így a nemzetközi tapasztalatokra támaszkodhatunk. Ennek alapján az ergoterápia szükségessége a CP-s gyermekek rehabilitációjában nem kétséges (112-B).
5.2. Gyógyszeres kezelések Spaszticitás gyógyszeres kezelése
A CP-s gyermekek ellátásában azért kap különös hangsúlyt, mert a CP-s gyermekek 80%-ában jelentkezik spaszticitás (18-B). Az antispasztikus gyógyszeres kezeléseket (indikáció, életkor, alkalmazás tartama) alább részletezzük. Egyéb gyógyszeres beavatkozások részben a kísérő betegségek, mint epilepsia, gastro-oesophagealis reflux (GOR), viselkedési problémák, nyugtalanság kezelésére szolgálnak, részben általános gyermekgyógyászati problémákat érintenek (anémia, infekciók). A fájdalom kezelése része a rehabilitáció folyamatának a CP-s gyermek ellátása során, ebben a tekintetben a fájdalomkezelésre vonatkozó általános alapelvek érvényesek, amelyeket nem részletezünk. A probléma az egyes kezelési eljárások fájdalmassága tekintetében is felmerül (113-C). Másrészt a spaszticitás hatásos kezelésével egyben fájdalomcsillapító hatás is elérhető (114-B), amire a spaszticitás gyógyszeres kezelése során külön nem térünk ki.
5.2.1. Szisztémás antispasztikus gyógyszeres kezelés
5.2.1.1. Oralisan alkalmazott gyógyszerek
A szisztémás oralis gyógyszeres kezelést minden olyan esetben alkalmazni szükséges, ha a CP a gyermekben sok izomra, a test jelentős részére kiterjed és a spaszticitásból származó funkcionális hátrányok (pl. mozgásbeszűkülés, kontraktúra, fájdalom, ápolási szükséglet) ezt indokolják. A diagnosztizált CP-ben a spaszticitás kifejlődését követően alkalmazható első választandó szerként az alábbi gyógyszerek egyike, amennyiben a jelzett indikációk fennállnak. Két szert alkalmaznak igen elterjedten: diazepam és baclofen.
- A diazepam a GABA repectorokra hat gerincvelői szinten. Járulékos központi idegrendszeri hatása (az agytörzs formáció reticularis területére fejti ki) miatt nyugtató effektust és észlelünk.
- A baclofen GABA b agonista, és elsősorban a gerincvelőben fejti ki hatását, de van kevés centrális hatása is.
Az oralisan alkalmazott szisztémás antispasztikus gyógyszerek hatásáról eddig átfogó tanulmány nem készült. Egy Cochrane review van előkészítés alatt (115-B). A rendelkezésre álló bizonyítékok alapján a kezelésnek van létjogosultsága, bár az egyéni érzékenység és reakciókészségben nagy különbségek mutatkoznak (mellékhatások és a hatás tekintetében egyaránt), ami a kezelés irányításában gyakorlatot feltételez, és óvatosságra int (116-B, 117,118,119,120,121-C).
5.2.1.2. Intrathecalis gyógyszeres kezelés
Az intrathecalis gyógyszeres kezelés koncepciója több mint száz éves. 1901-ből ismert az első publikált gyógyszer beadás az intrathecalis térbe. Lehet reverzibilis hatású gyógyszert adni és lehet neurolyticus irreverzibilis hatású szert adni. CP-ben csaknem kizárólag baclofent alkalmaznak. Az intrathecalis adagolás legfőbb előnye a szájon át történő kezeléssel szemben, hogy a kellemetlen szisztémás mellékhatások (bágyadtság, egyensúlyi zavarok) nem mutatkoznak (122,124-B; 121,123-C).
A baclofen szelektíven hat a gerincvelő substantiagelatinosa II. és III. szürkeállomány rétegében és az agyban található receptorokra azáltal, hogy gátolja a preszinaptikus transzmitterek felszabadulását, amit részben a preszinaptikus terminálba történő calcium beáramlás gátlásával (115-B), a posztszinaptikus terminálon pedig a kálium felvétel csökkentésével és redukált neuronális aktivitással ér el. Egyaránt csökkenti az alfa-motoneuron-rendszer ingerelhetőségét, és impulzusfrekvenciáját, valamint a gamma-rendszer aktivitását. Kisebb mértékben gátolja a gerincvelői vegetatív reflexeket, a zsigeri reflexeket, a myoclonusos és a rigoros jelenségeket. Spazmusoldó hatása másodlagosan fájdalomcsillapító hatással is járhat.
Intrathecalis kezelésre biztonsággal csak implantálható gyógyszeradagoló rendszerek alkalmasak. Ma már 40 és 20ml-es telemetrikusan programozható pumpák léteznek. A gyógyszer dózis fokozatosan titrálható a pumpa telemetrikus programozása révén a megfelelő terápiás szintre.
A kezelés indikációját spasztikus CP-s gyermekekesetében sok izom érintettségen és megfelelő izomerőn túl a várható funkcionális javulás (pl. önálló járás elérése, nagyobb függetlenség az evésben, ülésben, öltözésben) képezi. A másik indikációs kört a súlyosan spasztikus és generalizált dystoniás gyermekek jelentik, akiknek az ápolhatósága és napi életritmusa (fájdalom, torz tartás) másként nem javítható. Az eljárás Magyarországon szakértői munkacsoport vizsgálata és engedélye után hozzáférhető. Az eljáráshoz gyakorlott ellátó team szükséges idegsebész, rehabilitációs szakorvos, neurológus és kezelést ismerő szakasszisztens részvételével (125-C).
5.2.2. Lokális gyógyszeres kezelés
Helyileg, a spasztikus izmot vagy a spasztikus izmot beidegző perifériás ideget lehet blokáddal bénítani. Utóbbi beavatkozás tartósabb, de nagyon fájdalmas. Alkohollal és fenollal vannak próbálkozások, de gyermekekben nem alkalmazzák. A spasztikus izom lokális infiltrációja botulinum toxin A (BoNT-A) vagy más derivát segítségével a leginkább elterjedt eljárás.
Botulinum toxin: A BoNT hatásmechanizmusa a neuromuscularis junctioban (NMJ) az achethylcholin (Ach) felszabadulás gátlása, amivel az ingerületátvitel blokkolása érhető el átmenti (mintegy 2-3 hónap) időtartamra (12-B). Az axon nyúlványa ugyanis újraképződik: már 2-3 héttel a blokádot követően elkezdődika "sprouting" jelensége - az elhalt NMJ környékén számos axon nyúlvány kezdemény jelenik meg, de a végleges NMJ csak mintegy 3 hónappal a blokád után válik ismét működőképessé (18-A; 12,126-B).
A BoNT molekulát a Clostridium botulinum baktérium termeli: 150 kilodalton nagyságú dimer, amelynek a könnyű lánca aktív. A molekulának 7 szerológiailag eltérő altípusa van, az altípusok között a hatásosság tekintetében lényeges különbségek vannak. A legelterjedtebben a botulinum toxin A szerotípust (BoNT-A) használják (12-B).
A BoNT-A kezelés hatásosságát számos randomizált, kontrollált klinikai tanulmány bizonyítja: csökkenti a spaszticitást a kezelt izmokban, ezzel lehetővé válik a motoros tanulás, könnyebben kimozgathatóvá válnak az izületek, a kontraktúrák kialakulása meggátolható vagy legalább időben eltolható (18-A; 12,126,127,128,129-B; 130,131-C). Ez utóbbi segítségével a műtétes beavatkozások részben elkerülhetővé válnak ill. későbbre tolódnak. Nagyon fontos szempont, hogy a kezelés veszélyei minimálisak (12,132,133-B). A BoNT kezelés 2 éves kor után alkalmazható, a felső életkori korlátot a rögzült kontraktúrák megjelenése adja (általában 7-9 éves kor után jelennek meg az alsó végtagokban és jóval később a felső végtagokban). A kezelés ismételhető, számos tanulmány foglalkozik a sorozat kezelésekkel (12,134-B). Az utóbbi időben leírtak szórványos esetekben szisztémás mellékhatást nagydózisú kezelések szövődményeként, azonban a szokványos dózisban alkalmazott kezelések jelentéktelen melléhatással járnak (néhány napos borzongás, átmeneti gyengeség a szomszédos izmokban és bőrpír fordulhat elő 2%-nál kisebb gyakorisággal (12,128,129,135,136-B; 130,131-C).
5.3. Műtéti kezelés
5.3.1. Idegsebészeti beavatkozások
Általános szempontok: cél a spaszticitás okozta panaszok mérséklése. Az elmúlt két évtizedben az irreverzibilis eljárások felől a reverzibilis megoldások irányába történt eltolódás, vagyis a funkcionális neuromodulációs eljárások kerültek előtérbe.
a./ Szelektív dorzális rizotómia. Indikáció: jó intellektuális funkciók, tiszta spaszticitás, diplégia, fixalt kontraktúrák hiánya, jó izomerő és poszturális stabilitás. Nem indikált: athetosis, ataxia, rigiditás, dystonia, izomgyengeség, túlnyújtott inak és súlyos fixált izületi kontraktúrák esetén (137-B). A műtét utáni megfordíthatatlan állapot különös óvatosságra int. Az ideális életkort 5-8 éves korra teszik. Hazánkban az eljárást még nem végzik. b./gyógyszeradagoló pumpa beültetésére elsősorban a spaszticitás kezelése érdekében kerül sor, általában 8-10 éves kor után (ld. Intrathecalis baclofen terápia) (121-B).
c./ mély agyi elektromos stimuláció módszerét már alkalmazzák hazánkban is, de CP esetében még nem került erre az eljárásra sor. Dystonias CP esetében alkalmazása lehetséges (138,139,140-C).
5.3.2. Ortopédiai műtétek
Általános szempontok: A CP ortopédiai kezelésében az utóbbi évtizedben paradigmaváltás történt (50-B; 141,142-C; 2-C). A csípő másodlagos deformitásainak komplex konzervatív kezelésének eredménytelensége esetén korai (2-5 éves korban végzett) lágyrész műtéti eljárást javasolnak. Minden más esetben a műtétek időpontja a lehető legkésőbbre tolódik ki a hatásos nem-műtétes, ebből adódóan reverzibilis eljárások kiterjedt alkalmazásának köszönhetően (lehetőleg 7-9 éves kornál későbbre). A biomechanikai szempontokelőtérbe kerülése, különösen, ahol lehetőség van komputeres mozgásanalízisre, a műtéti megoldások finomodását, többféleségét és az egy ülésben végzett teljes rekonstrukciót, az un. "multilevel surgery" technikát hozta előtérbe a frakcionáltan végzett "single level" beavatkozások helyett (143-B; 144,145-C). A botulinum toxin A kezelés eredményessége és a kvantitatív járás analitikai adatok elemzése együttesen a járóképes vagy azzá tehető spasztikus CP-s gyermekek esetében alapvetően megváltoztatta a műtéti beavatkozások szükségességét és idejét (146-B).
Célok: a kontraktúrák oldása, izületre ható erők kiegyensúlyozása, az izomerő átcsoportosítása, instabil izületek fúzióval történő stabilizálása, csontos deformitások korrekciója, amellyel a biomechanikai terhelési viszonyok javulnak, az izületi diszlokáció és (sub)luxatio csökkentése, a spaszticitás okozta fájdalom csökkentése, a gerinc stabilitásának megőrzése vagy javítása.
Technikák: neurectomia, tenotomia, arthrodesis, osteotomia, ín-átültetés, ín-hosszabbítás, myotendinosus egység frakcionált hosszabbítása, multiszegmentális csigolya fúzió és a felsoroltak kombinációi
Indikációk: a deformitások romlása, azokfájdalmassága vagy funkciózavart okozó mértéke: rögzült kontraktúra, izületi subluxatio vagy instabilitás, előrehaladott gerinc deformitás; olyan deformitások, amelyek az ápolást lehetetlenné teszik vagy nagyon megnehezítik.
Típusok
Gerincstabilizáló műtétek
Ezek egyrészt a szagittális irányú görbületek (hyperlordosis, hyperkyphosis) korrekcióját, másrészt a strukturális scoliosisok korrekcióját szolgálják (2-C).
Instabil csípő és csípőficam műtéti ellátása
Konzekvens korai konzervatív kezeléssel sem lehet gyakorta megakadályozni az általában aszimmetrikusan romló másodlagos csípőficam kialakulását. A szekunder prevenció eszköze lágyrész műtét, a kialakult subluxatio műtéti kezelése csontos beavatkozást is szükségessé tesz (143-B; 145,147,148-C).
Végtagi műtétek
A végtagi műtétek többsége az alsó végtagon a járás elérése vagy a járásfunkció javítása érdekében történik: kontraktúrák korrekciója, spaszticitás következményének mérséklése, a végtag erőkarjainak megtartása ill. a forgatónyomaték eltérések korrekciója érdekében. A felső végtagokon főként a kéz funkcióinak javítása, a csukló, a könyök és a váll kóros tartásából fakadó önellátási funkciózavarok korrekciója a cél (50,142,144,145-C).
5.4. Egyéb terápiák
5.4.1. Gyakori társ-betegségek ellátása
A CP-s gyermekekgyakorta többféle betegséggel és funkciózavarral élnekegyütt, ami indokolja a komplex ellátásukat. Az alábbi problémák részletes taglalása a jelen protokoll kereteit meghaladja, azonban a problémákat felsorolás szintjén jelezzük:
- Evési és gyarapodási zavarok ellátása (149-B; 150-C; 151-B-D;52-D)
- Inkontinencia ellátás (152-B-C; 52-D)
- Inaktivitással összefüggő problémák ellátása: osteopenia, osteoporosis (153-B; 154-C; 52-D)
- Gastro-esophagealis reflux kezelése (155-B; 151-B-C; 52-D)
- Székrekedés (151,152-B-C; 52-D)
- Gyermek neurológiai problémák:
- Epilepsia (9-B; 66-B-C; 52-D)
- Hydrocephalus (9-B; 66-B-C; 52-D)
- Fokozott nyálzás (156-B; 157-C; 52-D)
- Viselkedési zavarok: hyperaktivitás-figyelemzavar szindróma, tanulási zavar (52-D)
- Érzékszervi problémák: látási problémák, hallászavar (52-D)
5.4.2. Újutak keresése terápiában
- Hyperbaricus oxigén: Nincs egyértelmű bizonyíték arra vonatkozóan, hogy a nagy nyomású 100% (hyperbaricus) oxigén belélegeztetése kedvező hatású lenne CP-ben (158-A; 159-B; 160-C).
- Őssejt terápia: Az embrionális, a köldökzsinór vérből, vagy az idegrendszerből származó őssejtekkel folytatott vizsgálatok nagyon ígéretesnek tűnnek, jelenleg azonban még kísérleti stádiumban vannak. Őssejt terápia az általánosan elfogadott orvosi etikai elvek alapján ma még nem ajánlható a CP kezelésére (161,162-C).
- Transcraniális mágneses stimuláció: újabban direkt kortikális ingerléssel is próbálkoznak, az első eredmények bíztatóak (163-C).
5.5. Technológiai segítés: gyógyászati segédeszközök
Magyarországon a gyógyászati segédeszközök rendelése és ellenőrzése szakorvosi feladat. A rehabilitációs team tagjai közül a gyógytornász-fizioterapeuta, a rehabilitációs foglalkoztató terapeuta (ergoterapeuta), egyes szakasszisztensek (audiológiai, légzésfunkciós, optometrikus), továbbá ortopéd műszerészek és a rehabilitációs szakmérnökök vesznek részt az adekvát gyógyászati segédeszközzel történő ellátásban. A speciális eszközök rendelésénél a kipróbálás lehetőségét biztosítani szükséges. Ez olyan centrumokban lehetséges, ahol speciális gyakorló helyiségek állnak rendelkezésre. Az alábbiakban a CP-s gyermekek kezelése során alkalmazott gyógyászati segédeszközök főbb csoportjaira utalunk a legfontosabb terápiás cél megjelölésével (82,164-C).
Típusok és célok
5.5.1. Pozícionáló eszközök
- Gerincpozícionálók: a törzs helyzetének stabilizálására szolgálnak (165,166,167-C)
- Végtag pozícionálók:
- sorozat-gipszelés: az ín-izom egység nyújtása érdekében - ellentmondó
- sínezés: izomhossz megtartása és az izületek stabilitásának növelése érdekében használják, a funkcionális értéke mérhető hatású (170,171-C)
- Egész-test pozícionálók:
- Álló helyzet: állító modulok / állító és felállító készülékek alkalmazására a függőleges testhelyzet önálló megtartásának képtelensége esetén, amennyiben láb-térd-csípő-törzs támasztással a testtömeg megtartására képes a gyermek
- Ülő helyzet: ülőkorzett, ültető modul és moduláris ülés különböző típusai alkalmazandók az ülő pozíció önálló megtartásának léptelensége ill. a torz törzs-tartás korrekciójának szükségessége esetén, amelyekfunkcionális javulást tesznek lehetővé (172,173-C)
- Fekvő helyzet: pozícionálásra fekvő helyzetben korrigálható deformitások esetén van szükség.
5.5.2. Funkcionális ortézisek: az izületi mozgástartomány megtartása, kontraktúra kialakulási esélyének csökkentése, tehermentesítés és funkciók javítása a cél.
- felsővégtagi ortézis alkalmazásának célja: izom-ín egység hosszának megtartása, a kemodenerváció ill. műtét eredményének megtartása (131-B; 82-C)
- alsóvégtagi ortézis alkalmazásánakcélja: funkcionális javulás elérése az izület helyzeténekstabilizálása révén állás ill. járás során és a felsővégtagnál leírtak (174-B; 175,176-C). Speciális dinamikus csípő ortézisként alkalmazható készülék a botulinum toxin A lokális gyógyszeres infiltrációjával együtt jó funkcionális javulást biztosíthat, azonban a csípőficam progressziójának megakadályozására nem elegendő (177,178-B).
- gerinc ortézisek alkalmazásának célja: scoliosis, kyphosis vagy lordosis korrekciója. Alkalmazásuk korlátozottabb és hatásuk csekélyebb, mint idiopathiás scoliosisban. A puha ortézisek előtérben vannak a kemény anyagból készültekkel szemben (179,180-C).
5.5.3. Egyéb tónusredukáló testközeli eszközök
- kinezio-taping: bőrbarát ragasztó szalagok alkalmasak izmok tehermentesítésére, az izületi mozgástartomány befolyásolására.
- Adeli ruházat, Lycra ruházat: elsősorban az izomzat feszességének mérséklésére alkalmazzák
5.5.4. Mobilitást segítő eszközök
- Járást segítők: az egyszerű támbotoktól a fix és gurulós járókereteken, könyökés hónaljtámasztásos mankókon át a törzsnek is támaszt és stabilitást nyújtó járást segítő ill. gyakoroltató és tanító eszközökig állnak rendelkezésre technikai megoldások (181-C).
- Kerekesszékes mobilitás eszközei: a hagyományos "toló" és ápoló székektől (minimális aktivitás esetén), a standard kerekesszékeken (átlagos aktivitás, önhajtási képességgel) át az un. aktív (nagy aktivitás) és sportolásra alkalmas aktív kerekesszékekig terjed a mechanikus székek csoportja. A speciális indikációval használjuk az elektromos kerekesszékeket (182,183-C).
5.5.5. Egyéb segédeszközök (felsorolás)
- Kommunikációs eszközök (kommunikációs táblák, komputerizált eszközök, speciális nyelvi segítő eszközök)
(184-B-C)
- Evési eszközök (étkezést segítő tárgyak, evéshez szükséges mozgást segítő eszközök) (151-B-C)
- Higiéniai és ápolási eszközök (decubitus védelem eszközei, vizelet és széklet inkontinencia eszközei, fürdés, mosdás, WC használat eszközei, öltözködést segítő eszközök) (42,46-B-C; 164-C,)
- Látást és hallást segítő eszközök (szemüveg, nagyító, speciális olvasó, hallókészülék) (42,46-B-C; 164-C)
5.6. Terápiás kombinációk
A CP hatékony terápiájában az eddig felsorolt eljárások különböző kombinációit alkalmazzuk. Különösen gyakori a funkcionális ortézisek és a gyógyszeres kezelések, az elektromos kezelés és a gyógyszeres kezelések ill. ezek egyéb kombinációinak alkalmazása (177,178,185,186-B;81-C)
5.7. Fejlesztő foglalkozások
A gyógypedagógiai fejlesztés, logopédiai foglalkozás és terápia, és a pszichológiai megsegítés együttesen szolgáljáka gyermekek integrációjának elősegítését (17-A, 187-B; 188,189-C).
5.8. Közösségi integrációt segítő ténykedések
A CP-s gyermekek gondozásában a családokkal való foglalkozásnak, a gyermekek közösségi integrációját elősegítő intézkedéseknek kell szerepelni. A szülők akkor képesek tartósan és jól együttműködni a gyermekeket segítő programokban a szakemberekkel, ha a közösségben lehetőséget kapnak a terápiákra, a korai fejlesztésre, a lelki megsegítésre és a közösségi integrációra. Hazánkban még nem beszélhetünk az inklúzív (teljesen befogadó) társadalmi modellről (190-A; 10-B; 191,192-C). A 8 évnél idősebb CP-s gyermekek körében végzett életminőség vizsgálatok azonos korú átlagos gyermekekhez viszonyítva hat Európai országra terjedő tanulmányban azt mutatták, hogy a nagyfokú mobilitási és beszéd nehezítettség, valamint intellektuális zavarok esetén mutatkoztak alacsonyabb értékek a CP-s gyermekek körében a fizikai ill. az emócionális skálán. A CP-s gyermekek az átlag gyermekekhez viszonyítva hasonló életminőség profilt mutattak az iskolai lehetőségek és a fizikai állapot kivételével. Ez rámutat annak szükségességére, hogy a szociális és oktatatási rendszerek tervezésekor a CP-s gyermekek teljes társadalmi részvételét szükséges biztosítani (193-A).
IV.-V. Rehabilitáció-Gondozás
6. Megelőzés
6.1. A primer prevenció
Legfontosabb eszközei: megfelelő terhes gondozás; az anyai krónikus betegségek (epilepszia, endokrin betegségek, magas-v. alacsony vérnyomás) kezelése; az állapotnak megfelelő szülés vezetés megválasztása a magzat érettségének megfelelő centrumban; a koraszülés prevenciója; a prenatális steroid kezelés; az intrauterin szállítás megszervezése centrumokba fenyegető koraszülés esetén; a perinatális ellátás minőségének javítása (18-A; 30-B).
6.2. Szekunder prevenció
6.2.1. Korai neuroterápia
Felkészült neonatológiai és neonatológiai-intenzívellátás, megfelelően felszerelt centrumokban, ahol mind a tárgyimind a személyi feltételek folyamatosan (24 órában) rendelkezésre állnak. Az újszülött vegetatív statusának stabilizálódását követően végzett fejlődésneurológiai diagnózison alapuló, megfelelően strukturált és folyamatosan ellenőrzött Katona-féle komplex neuroterápia hatására a CP kialakulásának kockázata csökkenthető (43-B-C).
6.2.2. Korai fizioterápia veszélyeztetett csecsemők számára
Korai fizioterápia a diagnózis megállapítását megelőzően nem változtat a CP kialakulásának menetén és a tünetek súlyosságán (194-C). Ugyanakkor a korai intervenció jótékony hatású a kognitív fejlődésre, ami 2 éves korig szignifikáns, iskolás korra azonban bizonytalan hatású (190-A).
6.2.3. Korai fejlesztés családközpontú szemlélettel
A szociokulturális hátrányos helyzetű családokban nagyobb eséllyel fordul elő koraszülés, ami a CP kialakulása szempontjából többszörösen veszélyezteti ezt a populációt. A szülők bevonása és támogatása számos vizsgálatban bizonyult jótékony hatásúnak a gyermekek fejlődésére (17,18,190-A; 10-B; 188,189,192,195-C; 196-D)
7. Prognózis
A CP-s gyermek állapota felnőtté válást követően a "természetes lefolyás" újabb szakaszába lép. Életen átívelő ill. hosszmetszeti nyomon követő tanulmányok bizonyítják, hogy az évek előre haladtával különböző funkciók vesztése zajlik. Ezért a CP-ben szenvedők rehabilitációs ellátása élethossziglan szükséges. Leggyakrabban az étkezésben válnak kiszolgáltatottabbá vagy a járás képessége szűkül be (45-C). A beltérben önállóan vagy segédeszközzel járóképes CP-s gyermek terápiás járóvá válását vagy a járás képességének teljes elvesztését intenzív járástréning segítségével késleltetni lehet (197-C). A serdülőkor számos változást indukál, elsősorban a lelki állapotban, a problémákkal való megküzdésben (198-B). A depresszió felnőtt korra válik egyre gyakoribbá (45-C). Az elmagányosodás és az élettér beszűkülése tovább rontja ezt a helyzetet (199-C). Az egészségügyi szolgáltatások igénybe vétele is jelentősen meghaladja minden életkorban a nem fogyatékos kortársakét, ami az idősebbek körében nagyobb arányú (200,201-C).
8. Az ellátás indikátorai
1) Korai ellátás: a diagnózis megállapítását követően 1 hónapon belül elkezdve. A CP gyanújeleinek észlelése esetén haladéktalanul törekedni kell az alapbetegség tisztázására. Egyes esetekben a diagnosztikus eljárások hetekig-hónapokig is tarthatnak, ilyenkor a korai intervenció megkezdése javasolt (6.2.3.)
2) Gyermek rehabilitációs szakorvosi konzílium / szakvizsgálat minimálisan évente egy alkalommal
3) Gyógyászati segédeszköz rendelése gyermek rehabilitációs szakorvos által történik. Speciális eszközök / egyedi méltányosságot igénylő eszközök esetében gyermek rehabilitációs centrumban, vagy team tagok közreműködésével kipróbálást követően történik
4) Ellátás tervezése és értékelése team munkában történik
5) Műtéti döntés előtt rehabilitációs szakorvosi és team vizsgálat történik
6) Korai fejlesztés / speciális oktatás vagy képzés elrendelése a jogszabályok adta kereten belül megtörténik
VI. Irodalomjegyzék
1. A cerebralis paresissel élő gyermekek ellátása. Egészségügyi Minisztérium Szakmai Protokollja. Készítette: A Neurológiai Szakmai Kollégium Gyermekneurológiai Szakcsoportja. Érvényes: 2008. dec.31.
2. Infantilis cerebralis paresis (ICP): Az Egészségügyi Minisztérium szakmai protokollja. Készítette: Ortopédiai Kollégium. Érvényes: 2008. dec.31.
3. BaxM, Goldstein M, Rosembaum P, Levinton A, Paneth N: Proposed definition and classification of cerebral palsy. April 2005. Dev Med Child Neurol 2005;47:571-6.
4. International Classification of Functioning, Disability and Health. WHO 2001.
5. A funkcióképesség, fogyatékosság és egészség nemzetközi osztályozása (FNO) WHO:ESZCSM:OEP, Budapest, 2004.
6. International Classification of Functioning, Disability and Health - Children and Youth Version. ICF-CY WHO 2007.
7. Elemző tanulmány a "Közös kincsünk a gyermek" csecsemő és gyermekegészségügyi program VIII. céljához. "Régiónként komplex gyermek-rehabilitációs ellátás kialakítása, feltételeinek megteremtése" 2006. www.eum.hu, www.ogyei.hu, www.rehab.dote.hu
8. Dodd KJ, Taylor NF, Damiano DL: A systematic review of the effectiveness of strength-training programs for people with cerebral palsy. Arch Phys Med Rehabil 2002;83:1157-64.
9. Stanger M, Oresic S: Rehabilitation approaches for children with cerebral palsy: Overview. J Child Neurol 2003;18:S79-88.
10. Krigger KW: Cerebral palsy: An overview. Am Family Physician 2006;73:91-100.
11. Weindling AM, Cunningham CC, Glenn SM, Edwards RT, Reeves DJ: Additional therapy foryoung children with spastic cerebral palsy: a randomized controlled trial. Health Techn Assessment 2007;11:(16).
12. Heinen F, Molenaers G, Fairhust C, et al: European consensus table 2006 on botulinum toxin or children with cerebral patsy. Eur J Paediatr Neurol 2006;10:215-225.
13. Gutenbrunner C, Ward AB, Chamberlain MA (eds): White book on physical and rehabilitation Medicine in Europe. J Rehab Med 2007;Suppl 45.
14. Kullmann L, Vekerdy Zs: A képzés és a szakember ellátottság jelentősége a rehabilitációban. Kórház. 2006;9:89-91.
15. Pharoah PO: Prevalence and pathogenesis of congenital anomalies in cerebral palsy. Arch Dis Child (Fetal Neonat Ed) 2007;92:F489-93.
16. Anderson NG, Laurent I, Woodward LJ, Inder TE: Detection of impaired growth of the corpus callosum in premature infants. Pediatrics 2006;118:951-60.
17. Pennington L, Goldbart J, Marschall J: Speech and language therapy to improve the communication skills of children with cerebral palsy. Cochrane Database for Systematic Reviews 2003, Issue 3. Art No.: CD003466.
18. Koman LA, Smith BP, Shilt JS. Cerebral palsy. Lancet 2000;363:1619-31
19. Nelson KB, GretherJK: Causes of cerebral palsy. CurrOpin Pediatr 1999;11:487-91
20. Stanley FJ, Blair EM, Alberman E: Cerebral palsies: epidemiology and causal pathways. London MacKeith Press. 2000.
21. Beckung E, Carlsson G, Carlsdotter S, Uvebrant P: The natural history of gross motor development in children with cerebral palsy aged 1 to 15 years. Dev Med Child Neurol 2007;49:751-6.
22. Cans C. Surveillance of cerebral palsy in Europe: a collaboration of cerebral palsy surveys and registers. Dev Med Child Neurol 2000;42:816-24.
23. Willoughby RE, Nelson KB: Chorioamnionitis and brain injury. Clin Perinatol 2002;29:603-21.
24. Bax M, Tydeman C, FlodmarkO: Clinical and MRI correlates of cerebral palsy: the European Cerebral Palsy Study. JAMA 2006;296:1602-8.
25. Resch B, Vollaard E, Maurer U, Haas J, Rosegger H, Müller W: Risk factors and determinants of neurodevelopmental outcome in cystic periventricular leucomalacia. Eur J Ped 2000;159:663-70.
26. Vohr B, Wrightt LL, Poole WK, McDonald SA: Neurodevelopmental outcomes of extremely low birthweight infants weeks' gestation between 1993 and 1998. Pediatrics 2005;116:635-43.
27. Drougia A, Giapros V, Krallis N, Theocharis P, Nikaki A, Tzoufi M, Andronikou S: Incidence and risk factors for cerebral palsy in infants with perinatal problems: a 15-year review. Early Hum Dev 2007;83:541-7.
28. Wilson-Costello D, Friedman H, Minich N, Siner B, Taylor G, Schluchter M, Hach M: Improved neurodevelopmetal outcomes for extremely low birth weight infants in 2000-2002. Pediatrics 2007;119:37-45.
29. Himmelmann K, Hagberg G, Wiklund LM, Eek MN, Uvebrant P: Dyskinetic cerebral palsy: a population-based study of children born between 1991 and 1998. Dev Med Child Neurol 2007;49:246-51.
30. Croen LA, GretherJK, Curry CJ, Nelson KB: Congenital anomalies among children with cerebral palsy: More evidence for prenatal antecedents. J Pediatr 2001;138:791-2.
31. Fink JK: Hereditary spastic paraplegia. Neurol Clin 2002;20:711-26.
32. Rumeau-Rouquette C, Grandjean H,Cans C, du MC, Verrier A: Prevalence and time trends of disabilities in school-age children. Int J Epidemiol 1997;26:137-45.
33. Nelson KB: The epidemiology of cerebral palsy in term infants. Ment Retard Dev Disabil Res Rev 2002;8:146-50.
34. Strauss D, Shavelle R: Life expectancy of adults with cerebral palsy. Dev Med Child Neurol 1998;40:369-75.
35. Hutton JL, Pharoah PO: Effects of cognitive, motor, and sensory disabilities on survival in cerebral palsy. Arch Dis Child 2002;86:84-9.
36. O'Shea TM, Preisser JS, Klinepeter KL, Dillard RG: Trends in mortality and cerebral palsy in a geographically based cohort of very low birth weight neonates born between 1982 to 1994. Pediatrics 1998;101:642-47.
37. Hollódi K: Spasticus cerbralis paresis és perinatális intenzív ellátás. PhD Értekezés. PTE 1998.23.
38. Evans P, Elliott M, Alberman E, Evans S: Prevalence and disabilities in 4 to 8 year olds with cerebral palsy. Arch Dis Child 1985;60:940-45.
39. Ketelaar M, Vermeer A, Helders PJ: Functional motor abilities of children with cerebral palsy: a systematic literature review of assessment measures. Clin Rehabil 1998;12:369-80.
41. Beckung E, Hagberg G: Neuroimpairments, activity limitations, and participation restrictions in children with cerebral palsy. Dev Med Child Neurol 2002;44:309-16.
42. Molnar GE, Alexander MA: Pediatic Rehabilitation 3rd ed., Hanley & Belfus, Inc. 1999.
43. Katona F: Klinikai fejlődésneurológia. Medicina, Budapest, 2000.
44. Stiers P, Vanderkelen R,VannesteG,Coene S, De Rammelaere M,Vandenbussche E: Visual-perceptual impairments in a random sample of children with cerebral palsy. Dev Med Child Neurol 2002;44: 370-82.
45. Krakovsky G, Huth MM, Lin L, Levin RS: Functional changes in children, adolescents, and young adults with cerebral palsy. Res Dev Disabil 2007;28:331-40.
46. Campbell SK, Vander Linden DW, Palisano RJ: Physical Therapy for Children, 2nd ed. Saunders, 2000.
47. Boyce W, Gowland C, Hardy S, Rosenbaum P, Lane M, Plews N, Goldsmith C, Russel D: Development of a quality of movement measure for children with cerebral palsy. Phys Ther 1991;71:820-32.
48. Green LB, Hurwitz EA: Cerebral Palsy. Phys Med North Am 2007;18:859-82.
49. Roijen LE, Postema K, Limbeek VJ, Kuppevelt VH: Development of bladder control in children and adolescents with cerebral palsy. Dev Med Child Neurol 2001;43:103-07.
50. NovacekTF, Gage JR: Orthopedic management of spasticity in cerebral palsy. Childs Nerv Syst 2007;23:1015-31.
51. Van Heest AE, House J, Putnam M,: Sensibility differences in the hands of children with spastic hemiplegia. J Hand Surg (Am) 1993;18:278-81.
52. Recommendations for minimum standards of healthcare in children with cerebral palsy. HemiHelp Bredford House 1999.
53. Dénes Z: Tesztek használata a mozgásszervi rehabilitációban. Rehabilitáció 2000;10/4/97-100
54. Msall ME, DiGaudio K, Rogers BT et al: The Functional Independence Measure for Children (WeeFIM): conceptual basis and pilot use in children with developmental disabilities. Clin Pediatr 1994;33:421-30.
55. WeeFIM System Clinical Guide, Version 5.01. Buffalo, NY, University of Buffalo, 1998.
56. Ottenbacher KJ, Msall ME, Lyon N, Duffy LC, Granger CV, Braun S: Measuring developmental and functional status in children with disabilities. Dev Med Child Neurol 1999;41:186-94.
57. Varni JW, Seid M, Kurtin PS: PedsQL 4:0: reliability and validity of the Pediatric Quality of Life Inventory version 4.0 generic score scales in healthy and patient population. Mes Care 2001;39:800-12.
58. Arnaud C, White-Koning M, Michelsen SI, Parkers J, Parkinson K, Thyen U, Becklung E, Dickinson HO, Fauconnier J, Marcelli M, McManus V, Colver A: Parent-reported quality of life of children with cerebral palsy in Europe. Pediatrics 2008;121:54-64.
59. Russell DJ, Rosenbaum PL, Growland C. et.al: Gross Motor Function Manual, 2nd ed. Hamilton, ON, McMaster University, 1992.
60. Russel DJ, Avery LM, Rosenbaum PL, Raina RS, Walter SD, Palisano RJ: Improved scaling of the gross motor function measure for children with cerebral palsy: evidence of reliability and validity. Phys Ther 2000;80:873-85.
61. Folio MR, Fewell RR: Peabody Developmental Motor Scales, 2nd ed. Examiner's Manual Austin, TX, Pro-Ed, 2000.
62. BruininskRH: Bruininks-OseretskyTest of Motor Performance: Examiner's Manual Circle Pines, MI, American Guidence Services, 1978.
63. Eliasson AC, Krumlinde-Sundholm L, Rösblad B, Beckung E, Arner M, Öhrvall AM, Rosenbaum P: The Manual Ability Classification System (MACS) for children with cerebral palsy: scale development and evidence of validity and reliability. Dev Med Child Neurol 2006;48:549-54.
64. Haga N, van der Heiden-Maessen HC, van Hoorn JF, Boonstra AM, Hadders-Algra M: Test-retest and Inter- and Intrareliability of the Quality of the Upper-Extremity Skills Test in Preschool Children With Cerebral Palsy. Arch Phys Med Rehabil 2007;88:1686-89.
65. Kendall FP, McCreary EK: Testing and Function. Baltimore, Williams and Wilkins, 1993.
66. Kálmánchey R: Gyermekneurológia, Medicina, Budapest, 2000.
67. Vekerdy Zs., Ittzésné Nagy B., Gallai M,et al: A Bayley N-csecsemőteszt magyarországi bevezetése. Gyermekgyógyászat 1998;49:466-78.
68. McDowell BC, Hewitt W, Nurse A, Weston T, Baker R: The variability of goniometric measurements in ambulantory children with spastic cerebral palsy. Gait Posture 2000;12:114-21.
69. Barry MJ,VanSwearingen MJ, Albright AL: Reliability and responsiveness of the Barry-Albright Dystonia Scale. Dev Med Child Neurol 1999;41:404-11.
70. Mackey AH, Lobb GL, Walt SE, Stott NS: Reliability and validity of the Observational Gait Scale in children with spastic diplegia. Dev Med Child Neurol 2003;45:4-11.
71. Mulder T, Nienhuis B, Pauweis J: Clinical gait analysis in a rehabilitation context: some controversial issues. Clin Rehabil
1998;12:99-106.
72. Walters R, Mulroy S: The energy expenditure of normal and pathologic gate. Gait Posture 1999;9:207-31.
73. Palisano R, Rosenbaum P, Walter S, Russel D, Wood E, Galuppi B: Development and reliability of a system to classify gross motor function in children with cerebral palsy. Dev Med Child Neurol 1997;39:214-223.
74. Palisano RJ, Hanna SE, Rosenbaum PL et al: Validation of a model of gross motor function for children with cerebral palsy. Phys Ther 2000; 80:974-85.
75. Steenbeek D: Goal attainment scaling in pediatric rehabilitation: a critical review of the literature. Dev Med Child Neurol 2007;49:550-6.
76. Vles GF, de Louw, Speth LA. Et al: Visual Analogue Scale to score the effects of Botulinum Toxin A treatment in children with cerebral palsy in daily clinical practice. Eur Paed Neurol 2007; in press. Online available 22.Oct.2007.
77. Ashwal S, Russman BS, Blasco PA, Miller G, Sandler A, Shevell M, Stevenson R; Quality Standards Subcommittee of the American Academy of Neurology; Practice Committee of the Child Neurology Society. Dev Med Child Neurol 2007;49:948-53.
78. Krägeloh-Mann I, Horber V: The role of magnetic resonance imaging in furthering understanding of the pathogenesis of cerebral palsy. Dev Med Child Neurol 2007;49:799-800.
79. Bodensteiner JB, Johnsen SD: Magnetic resonance imaging (MRI) findings in children surviving extremely premature delivery and extremely low birthweight with cerebral palsy. Child Neurol 2006;21:743-7.
80. Sanger TD, Delgado MR, Gaebler-Spira D, Hallett M, Mink JW: Classification and definition of disorders causing hypertonia in childhood. Pediatrics 2003;111:e89-97.
81. Kang BS, Bang MS, Jung SH: Effects of botulinum toxin A therapy with electrical stimulation on spastic calf muscles in children with cerebral palsy. Am J Phys Med Rehabil 2007;86:901-6.
82. Ketelaar M, Vermeer A, Hart H, van Petegem-van Beck E, Helders PJ: Effects of a functional therapy program on motor abilities of children with cerebral palsy. Phys Ther 2001;81:1534-45.
83. Goldstein EM: Spasticity management: an overview. J Child Neurol 2001;16:16-23.
84. Palmer FB, Shapiro BK, Wachtel RC, Allen MC, Hiller JE, Harryman SE, et al: The effects of physical therapy on cerebral palsy: a controlled trial in infants with spastic diplegia. N Engl J Med 1988;318:803-8.
85. Brown GT, Burns SA: Efficacy of neurodevelopmental treatments in children: a systematic review. Br J Occup Ther 2001;64:235-244.
86. D'Avignon MD, Noren L, Arman T: Early physiotherapy modum Vojta or Bobath in infants with suspected motor disturbances. Neuropediatrics 1981;12:232-41.
87. Bower E, Mitchell D, Burnett M, Cambell MJ, McLellan DL: Randomized controlled trial of physiotherapy in 56 children with cerebral palsy followed for 18 months. Dev Med Child Neurol 2001;43:4-15.
88. Butler C, Darrach J: Effects of neurodevelopmental treatment (NDT) for cerebral palsy: An AACPDM evidence report. Dev Med Child Neurol 2001;43:778-90.
89. Tsorlakis N, Evaggelinou C, Grouios G, Tsorbatzoudis C: Effect of intensive neurofdevelopmental treatment in gross motor function of children with cerebral palsy. Dev Med Child Neurol 2005;47:287-91.
90. Patikas D, Wolf SI, Mund K, Ambrust P, Schuster W, Döderlein L: Effects of postoperative strength-training program on the walking ability of children with cerebral palsy: a randomized controlled trial. Arch Phys Med Rehabil 2006;87:619-26.
91. Verschuren O, Ketelaar M, Takken T, Helders PJM, Gorter JW: Exercise programs for children with cerebral palsy: A Systematic Review of the Literature. Am J Phys Med Rehabil 2007;86: available online
92. Stackhouse SK, Binder-Macleold SA, Stackhouse CH, McCarthy JJ, Prosser LA, Lee SC: Neuromuscular electrical stimulation versus volitional isometric strength training in children with spastic diplegic cerebral palsy: a preliminary study. Neurorehabil Neural Rapair 2007;21:475-85.
93. Glinsky J, Harvey L: Efficacy of electrical stimulation to increase muscle strength in people with neurological conditions: a systematic review. Physiother Res Int 2007;12:174-94.
94. Kerr C, McDowell B, McDonough S: Electrical stimulation in cerebral palsy: a review of effects on strength and motor function. Dev Med Child Neurol 2004;46:205-213.
95. Taub E, Ramey SL, DeLuca S, Echols K: Efficacy of constraint-induced movement therapy for children with cerebral palsy with asymmetric motor impairment. Pediatrics 2004;113:305-12.
96. Hoare BJ, Wasiak J, Imms C, Carey L: Contraint-induced movement therapy in the treatment of the upper limb in children with hemiplegic cerebral palsy. Cochrane Database of Systematic Reviews 2007 Issue 4. (first published online: in issue 2,2007).
97. Charles JR, Gordon AM: A repeated course of constraint-.induced movement therapy results in further improvement. Dev Med Child Neurol 2007;49:770-3.
98. Richards CL, Malouin F, Dumas F et al: Early and intensive treadmill locomotor training foryoung children with cerebral palsy: A feasibility study. Pediatr Phys Ther 1997;9:158-65.
99. Schindl MR, Forstner C, Kern H, et el: Treadmill training with partial body weight support in nonambulantory patients with cerebral palsy. Arch Phys Med Rehabil 2000;81:301-6.
100. Dévény A: DSGM. Dévény speciális manuális technika - gimnasztika módszer. Dévény A Alapítvány, Budapest, 1995.
101. Gordon AM, Schneider JA, Chinnan A, Charles JR: Efficacy of a hand-arm bimanual intensive therapy (HABIT) in children with hemiplegic cerebral palsy: a randimzed control trial. Dev Med Child Neurol 2007;49:830-8.
102. You SH, Jang SH, Kim YH, Kwon YH, Barrow I, Hallett M: Cortical reorganization induced by virtual reality therapy in a child with hemiparetic cerebral palsy. Dev Med Child Neurol 2005;47:628-35.
103. Sterba JA, Rogers BR, France AP, et al: Horseback riding in children with cerebral palsy: Effect on gross motor function. Dev Med Child Neurol Suppl 2002;44:301-8.
104. Hurwitz EA, Leonard C, Ayyangar R, Nelson VS: Complementary and alternative medicine use in families of children with cerebral palsy. Dev Med Child Neurol 2003;45:364-70.
105. Duncan B, Barton L, Edmonds D, Blashill BM: Parental perceptions of the therapeutic efficacy of osteopathic manipulation or acupuncture in children with spastic cerebral palsy. Clin Pediatr 2004;43:859-68.
106. Huang M, Fan HF, Lei SE: Scalp-acupuncture plus body-acupuncture for treatment of spastic cerebral palsy and its effects on bone density and trace elements in diseased children. Chinese Acupunct Mixibust 2007;27:395-7.
107. Reddihough DS, King J, Coleman G, Catanese T: Efficacy of programmes based on conductive education for young children with cerebral palsy. Dev Med Child Neurol 1998;40:763-70.
108. Darrach J, Watkins B,Chen L, Bonin C: Conductive education intervention for children with cerebral palsy: An AACPDM evidence report. Dev Med Child Neurol 2004;46:187-203.
109. Ödman PE, Öberg BE: Effectiveness and expectations of intensive training: A comparison between child and youth rehabilitation and conductive education. Disab Rehabil 2006;28:561-70.
110. Hári M, Horváth J, Kozma I, Kőkúti M: A konduktív pedagógiai rendszer hatékony működésénekalapelvei és gyakorlata. Nemzetközi Pető Intézet, Budapest, 1991.
111. Pirila S, van der Meere J, Pentikainen T, Ruusu-Niemi P, Korpela R, Kilpinen J, Nieminen P: Language and motor skills in children with cerebral palsy. Communic Disord 2007;40:116-28.
112. Steultjens EMJ, DekkerJ, Bouter LM? Van de Nes JCM, Lambregts BLM,van den Ende CHM: Occupational therapy for children with cerebral palsy, (Protocol) Cochrane Database for Systematic Reviews 2003, Issue 4. Art No.: CD004490.
113. Hadden KL, Baeyer CL: Global and specific measures of pain in children with cerebral palsy. Clin Pain 2005;21:140-6.
114. Barwood S, Baillieau C, Boyd R, et al: Analgesy effect of botulinum toxin A: a randomized, placebo-controlled clinical trial. Dev Med Child Neurol 2000;42-116-21.
115. Howard DC: Anti spastic medication for spasticity in cerebral palsy. (Protocol) Cochrane Database of Systematic Reviews 2000, Issue 2. Art.No.: CD002260.
116. Montané E, Vallano A, Laporte JR: Oral antispastic drugs in nonprogressive neurologic diseases. A systematic review. Neurology 2004;63:1357-1363.
117. Flett PJ: Rehabilitation of spasticity and related problems in childhood cerebral palsy. Paediatr Child Health 2003;39:6-14.
118. Kita M, Goodkin DE: Drugs used to treat spasticity. Drugs 2000;59:487-495.
119. Tilton AH: Therapeutic interventions for tone abnormalities in cerebral palsy. NeuroRx 2006;3.217-224.
120. Verotti A, Greco R, Spalice A, et al: Pharmacotherapy of spasticity in children with cerebral palsy. Pediatr Neurol 2006;34:1-6.
121. Krach LE: Pharmacotherapy of pasticity: Oral medications and intrathecal baclofen. J Child Neurol 2001;16:31-36.
122. Rice JE, O'Donell ME: Intrathecal baclofen for treating spasticity in children with cerebral palsy. Cochrane Database of Systematic Reviews Protocol. 2007 Issue 4. (first published online: in issue 1,2004)
123. de Lissovoy G, Matza LS, Green H, et al: Cost-effectiveness of intrathecal baclofen therapy for the treatment of severe spasticity associated with cerebral palsy. J Child Neurol 2007;22:49-59.
124. Hoving MA, van RaakEP, SpincemailleGH, Palmans LJ,Sleypen FA,Vles JS: Intrathecal baclofen in children with spastic cerebral palsy: a double-blind, randomized, placebo-controlled, dose-finding study. Dev Med Child Neuol 007;49:654-9.
125. Bábel B. T, Kertész Gy, Fehér M, Dénes Z, Komoly S, Benoist Gy, Klauber A: Az intrathecalis Baclofen kezelés módszertana; Rehabilitáció 2003;13:18-21.
126. Uhbi T, Bhakta BB, Ivea HL, AllgarV, Roussounis SH: Randomized, double-blind placebo-controlled trial of the effect of botulinum toxin on walking in cerebal palsy. Arch Dis Child 2000;83:481-7.
127. Koman LA, MooneyJF, Smith BP, Walker F, Leon JM: Botulinum toxin type A neuromuscular blockade int he treatment of lower extremity sapsticity in cerebral palsy: a randomized, double-blind, placebo-controlled trial. BOTOX Study Group. J Pediatr Orthop 2000;20:108-15.
128. Corry IS, Cosgrove AP, Walsh EG, McClean D, Graham HK: Botulinum toxin A in the hemiplegic upper limb: a double-blind trial. Dev Med Child Neurol 1997;39:185-93.
129. Love SC, Valentine JP, Blair EM, et el: The effect of botulinum toxin type A on the functional ability of the child with spastic hemiplegia a randomized controlled trial. Eur J Neurol 2001;8 (suppl 5):50-8.
130. Wasiak J, Hoare B, Wallen M: Botulinum toxin A as an adjunct to treatment in the management of the upper limb in children with spastic cerebral palsy. Cochrane Database of Systematic Reviews 2007 Issue 4. (first published online: in issue 4,2004)
131. Vekerdy Zs, Lente Gy, Fazekas K, Mező R, Bodea T: A botulinumtoxin A- típusával való kezelés helye az infantilis cerebralis paresis rehabilitációjában. Gyermekgyógyászat 2005;56:461-73.
132. Bjornson K, Hays R, Graubert C, et al: Botulinum toxin for spasticity in children with cerebral palsy: A comprehensive evaluation. Pediatrics 2007;120:49-58.
133. Ade-Hall RA, Moore AP: Botulinum toxin type A in the treatment of lower limb spasticity in cerebral palsy. Cochrane Database of Systematic Reviews 2007 Issue 4. (first published online: in issue 1,2000)
134. Lowe K, Novak I. Cusick A: Repeat injection of botulinum toxin A is safe and effective for upper limb movement and function in children with cerebral palsy. Dev Med Child Neurol 2007;49:823-9.
135. Scholtes VA, Dallmeijer AJ, Knol DL, et al: Effect of multilevel botulinum toxin A and comprehensive rehabilitation on gait in cerebral palsy. Pediatr Neurol 2007;36:30-39.
136. Willis AW, Crowner B, Brunstrom JE, et al: High dose botulinum toxin A for The treatment of lower extremity hypertonicity in children with cerebral palsy. Dev Med Child Neurol 2007;49:818-822.
137. Steinbock P: Selective dorsal rhizotomy for spastic cerebral palsy: a review. Childs Nerv Syst 2007;23:981-90.
138. Davis R: Cerebellar stimulation for cerebral palsy spasticity, function and seizures. Arch Med Res 2000;31:290-9.
139. Eltahawy HA, Saint-Cyr J, Giladi N, Lang AE, Lozano AM: primary dystonia is more responsive than secondary dystonia to pallidal interventions: outcome after pallidotomy or pallidal deep brain stimulation. Neurosurgery 2004;54:613-21.
140. Alterman RL, Tagliati M: Deep brain stimulation for torsion dystonia in children. Childs Nerv Syst 2007;23:1033-40.
141. deLuca PA, Davis RB,Öonpuu S, Rose S, Sirkin R: Aletrations in surgical decision makings in patients with cerebral palsy based on three-dimensional gait analysis. J Pediatr Orthop 1997;17:608-14.
142. Davids JR,Öunpuu S, DeLuca PA, Davis RB: Optimization of walking ability of children with cerebral palsy. J Bone Joint Surg 2003;85:224-34.
143. Soo B, Howard JJ, Boyd RN, Reid SM, Lanigan A, Reddihough D, Graham KH: Hip displacement in cerebral palsy. J Bone Joint Surg 2006;88:121-9.
144. Rodda J, Graham HK: Classification of gait patterns in spastic hemiplegia and spastic diplegia: a basis for management algorithm. Eur J Neurol 2001;8:98-108.
145. Nene AV, Evans GA, Patrick JH: Simultaneous multiple operations for spastic diplegia: outcome and functional assessment of walking in 18 patients. J. Bone Joint Surg. (Br.) 1993;75-B:488-494.
146. Molenaers G, Desloovere K, Fabry G, De Cock P: The effects of quantitative gait assessment and botulinum toxin A on musculosceletal surgery in children with cerebral palsy. J Bone Joint Surg 2006;88:161-70.
147. Ounpuu S, DeLuca P, Davis R, Romness M: Long-term effects of femoral derotation osteotomies: an evaluation using three-dimensional gait analysis. J. Pediatr. Orthop 2002;22:139-145.
148. Cooperman DR, Bartucci E, Dietrick E, Millar EA: Hip dislocation in spastic cerebral palsy: Long term consequences. J. Pediatr. Orthop 1987;7: 268-276.
149. Sleigh G, Sullivan PB, Thomas AG: Gastrostomy feeding versus oral feeding alone for children with cerebral palsy. Cochrane Database of Systematic Reviews 2007 Issue 4. (first published online: in issue 2,2004)
150. Gisel EG: Effect of oral sensorimotor treatment on measures of growth and efficiency of eating in the moderately eating-impaired child with cerebral palsy. Dysphagia 1996;11:48-58.
151. Vekerdy Zs., Oláh É.(szerk.): A táplálás és a gyarapodás zavarai. Sérült gyermekek ellátásának sajátosságai. PRRO Bt. Debrecen, 1999.
152. Behrman RE, Kliegman R, Jenson HB (eds): Nelson Textbook of Pediatrics. 17th ed. Saunders Co. 2003.
153. Henderson RC, Lark RK, Kecskemethy HH, Miller F, Farcke HT, Bachrach SJ: Bisphosphonates to treat osteopenia in children with quadriplegic cerebral palsy: a randomized, placebo-controlled clinical trial. J Pediatr 2002;141:644-51.
154. King W, Levin R, Schmidt R, Oestreich A, Heubi JE: Prevalence of recuced bone mass in children and adults with spastic quadriplegia. Dev Med Child Neurol 2003;45:12-6.
155. Vernon-Roberts A, Sullivan PB: Fundoplication versus post-operative medication for gastro-eoesophageal reflux in children with neurological impairment undergoing gastrostomy. Cochrane Database of Systematic Reviews 2007 Issue 1. Art. No.:CD006151.
156. Jongerius PH, van den Hoogen FJ, van LimbeekJ,Gabreels FJ,van Hulst K, Rotteveel J: Effect of botulinum toxin in the treatment of drooling: a controlled clinical trial. Pediatrics 2004;114:620-7.
157. Gerlinger I, Szalai G, Hollódy K, Németh A: Ultrasound-guided, intraglandular injection of botulinum toxin A in children suffering from excessive salivation. J Laryngol Otol 2007;121:947-51. Epub 2007 Mar 29
158. Collet JP, Vanasse M, Marois P, Amar M, Goldberg J, Lambert J, Lassonde M, Hardy P, Fortin J, Tremblay SD, Montgomery D, Lacroix J, Robinson A, Majnemer A, HBO-CP Research Group: Hyperbaric oxygen for children with cerebral palsy: a randomised multicentre trial. Lancet 2001;357:582-6.
159. McDonagh MS, Morgan D, Carson S, Russman BS: Systematic review of hyperbaric oxygen therapy for cerebral palsy: the state of the evidence. Dev Med Child Neurol 2007;49:942-7.
160. Essex C: Hyperbaric oxygen and cerebral palsy: No proven benefit and potentially harmful. Dev Med Child Neurol 2003; 45:213-15.
161. McGuckin C, Forraz N, Baradez MO, Basford C, Dickinson AM, Navran S, Hartgerink JD: Embryonic-like stem cells from umbilical cord blood and potential for neural modeling. Acta Neurobiol Exp 2006;66:321-9.
162. Kornblum HI: Introduction to neural stem cells. Stroke 2007,38[part 2]:810-6.
163. Valle AC, Dionisio K, Pitskel NB, Pascual-Leone A,Orsati F, Ferreira MJ, Boggio PS, Lima MC, Rigonatti SP, Fregni F: Low and high frequency repetitive transcranial magnetic stimulation for the treatment of spasticity. Dav Med Child Neurol 2007;49:534-8.
164. Ronan S, Gold JT: Nonoperative management of spasticity in children. Childs Nerv Syst 2007;23:943-56.
165. Crenshaw S, Herzog R, Castagno P, et al: The efficacy of tone-reducing features in orthotics on the gait of children with spastic diplegic cerebral palsy. J Pediatr Orthop 2000;20:210-16.
166. Renshaw TS, Green NE, Griffin PP, Root L: Cerebral palsy: orthopaedic management. J Bone Joint Surg 1995;77A:1590-606.
167. Vekerdy Zs: Management of seating posture in children with cerebral palsy by using thoraco-lumbar-sacral orthosis with non-rigid SIDO® frame. Disab Rehabil 2007;29:1434-41.
168. Preissner KS: The effects of serial casting on spasticity: A literature review. OccupTher Health Care 2001;14:99-106.
169. McNee AE, Will E, Lin JP, Eve LC,Gough M, Morrissey MC, Shortland AP: The effect of serial casting on gait in children with cerebral palsy: preliminary results from a crossover trial. Gait Posture 2007;25:463-8.
170. Bertoli DB: Effects of short-leg casting on ambulation in children with cerebral palsy. Phys Ther 1986;66:1522-9.
171. Burtner PA, Woollacott MH,Qualls C: Stance balance control with orthoses in a group of children with spastic cerebral palsy. Dev Med Child Neurol 1999;41:748-757.
172. Myhr U, von Wendt L: Improvement of functional sitting position for children with cerebral palsy. Dev Med Child Neurol Suppl 1993;35:870-80.
173. Vekerdy Zs: Vergleich von Sitzhilfen für die Positionierung von Kindern mit scgweren motorischen Störungen. [Comparison of seating devices for positioning of children with severe motor disorders]. Orthopädie-Technik 2007;10:760-8.
174. Morris C: A review of the efficacy of lower-limb orthoses used for cerebral palsy. Dev Med Child Neurol 2002;44:205-11.
175. Hylton NM: Postural and functional impact of dynamic AFOs and FOs in a pediatric population. J Prosthet Orthot 1989;2:40-53.
176. Buckon CE, Thomas SS, Jakobson-Huston S, Moor M, Sussman M, Aiona M: Comparison of three ankle-foot orthosis configuration for children with spastic hemiplegia. Dev Med Child Neurol 2001;43:371-78.
177. Graham HK, Boyd R,Carlin JB,Dobson F,Lowe K, NattrasG,Thomason P,Wolfe R, Reddihough D: Does Botulinumtoxin A combined with bracing prevent hip displacement in children with cerebral palsy and "hips at risk"? A randomized, controlled trial. J Bone Joint Surg 2008;90:23-33.
178. Boyd RN, Dobson F, Parrott J et al: The effect of Botulinum toxin A and a variable hip orthosis in gross motor function: a randomized controlled trial. Eur J Neurol 2001;8(suppl 5):109-19.
179. Miller A, Temple T, Miller F: Impact of orthoses on the rate of scoliosis progression in children with cerebral palsy. J Pediatr Orthop 1996;16:332-35.
180. Olafsson Y, Saraste H, Al Dabbagh Z: Brace treatment in neuromuscular spine deformity. J Pediatr Orthop 1999;19:376-79.
181. Vekerdy Zs, Mező R, Bösenbacher T, Karadin Cs: Járást segítő eszközök helye a cerebralis paresises gyermekek rehabilitációjában. Mozgásterápia, 2006;XV:28-34.
182. Kullmann L: Segédeszköz ellátás in: Huszár-Kullmann-Tringer (szerk): A rehabilitáció gyakorlata . Medicina, Budapest 2000.
183. Vekerdy Zs: A mobilitás eszközei gyermekkorban. Rehabilitáció 2006;6/2:37-44.
184. Kálmán Zs: Mással-hangzók... Az augmentatívés alternatív kommunikáció alapjai. Bliss Alapítvány, Budapest. 2006.
185. Corry IS, Cosgrove AP, Duffy CM, et al: Borulinum toxin A compared with stretching casts in the treatment of spastic equinus: a randomized prospective trial. J Pediatr Orthop 1998;18:304-11.
186. Desloovere K, Moleanaers G, Jonkers I ert al: A randomized study of combined botulinum toxin type A and casting in the ambulant child with cerebral palsy using objective outcome measures. Eur J Neurol 2001;8 (suppl 5):75-87.
187. Robinson M, Israel C, Parker D, Lawrence E, Smith J, Dolby S. et al: Randomized trial of parental support for families with very preterm children. Arch Dis Child 1998;79:F4-11.
188. Guralnik MJ: Effectiveness of early intervention for vulnerable children: a developmental perspective. Am J Ment Retard 1998;102:319-45.
189. Ramey CT, Cambell FA, Burchinal M, Skinner ML, Gardner DM, Ramey SL: Persistent effects of early intervention on high-risk children and their mothers. Appl Dev Sci 2000;4:2-14.
190. Spittle AJ, Orton J, Doyle LW, Boyd R: Early developmental intervention programs post hospital discharge to prevent motor and cognitive impairments in preterm infants. Cocrane Database of Systematic Reviews 2007, Issue 2. Art No.: CD005495.
191. LawlorK, MihaylovS, Welsh B,Javris S,Colver A: A qualitative study of the physical, social and attitudinal environments influencing the participation of children with cerebral palsy in northeast England. Ped Rehab 2006;9:219-28.
192. Manuel J, Naughton MJ, Balkrishnan R, Smith SP, Koman LA: Stress and adaptation in mothers of children with cerebral palsy. J Ped Psychol 2003;28:197-201.
193. Dickinson HO, Parkinson KN, Ravens-Sieberer U, Schirripa G,Thyen U, Arnaud C, Beckung E, Fauconnier J,McManus V, Michelsen SI, Parkes J, Colver AF: Self-reported quality of life of 8-12-year-old children with cerebral palsy: a cross-sectional European study. Lancet 2007;369:2171-7.
194. Harris SR: Early intervention: does developmental therapy make a difference?Top Early Child Spec Educ 1988;7:20-32.
195. Turnbull JD: Early intervention for children with or at risk of cerebral palsy. Am J Dis Child 1993;147:54-9.
196. Büky Gy, Gallai M, Paksy L: 2.sz. Módszertani Levél: A pszichomotoros fejlődés zavarainak felismerése és ellátása az alapellátási gyakorlatban. OGYI 2004.
197. Andersson C,Grooten W, Hellsten M, Kaping K, Mattsson E: Adults with cerebral palsy: walking ability after progressive strength training. Dev Med Child Neurol 2003;45:220-8.
198. Bjorson KF, Belza B, Kartin D, Logsdon RG, McLaughin J: Self-reported health status and quality of life in youth with cerebral palsy and typically developing youth. Arch Phys Med Rehabil 2008;89:121-7.
199. Ballin L, Balandin S: An exploration of lonelisűness: communication and the social networks of older people with cerebral palsy. Intel Development Disab 2007;32:315-26.
200. Young NL,Gilbert TK,McCormickA, Ayling-Campos A, Boydell K, Law M, Fehlings DL,MukherjeeS, Wedge JH, Williams JI: Youth and young adults with cerebral palsy: their use of physician and hospital services. Arch Phys Med Rehabil
2007;88:696-702.
201. ElrodCS, DeJong G: Determinants of physical rehabilitation services for persons with chronic and disabling conditions: an exploratory study. Arch Phys Med Rehabil 2008;89:114-20.
A szakmai protokoll érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai protokollja
A scoliosis rehabilitációjáról
Készítette: a Csecsemő- és Gyermekgyógyászati Szakmai Kollégium és a Rehabilitációs Szakmai Kollégium
Szinonimák: gerincferdülés, dorsopathia
I. Alapvető megfontolások
1. A protokoll alkalmazási területe Gyermek rehabilitáció
2. A protokoll kidolgozásának indoklása és körülményei
A scoliosis ellátására készült eddig két szakmai anyag: az Orthopédiai Kollégium protokollja és az Iskolás Gyermekek Testnevelési Kategóriába Sorolása című ajánlás, amelyben a gerincferdülésben szenvedő gyermekekre vonatkozó javaslatok is szerepelnek (1,2). Egyik összeállítás sem tartalmazza a rehabilitáció szempontjait kellő mélységben. A szakmai protokoll érvényessége 2006. december 31. volt. Tekintettel arra, hogy a scoliosis ellátása multidiszciplináris feladat, ami a gyermek rehabilitációs központokban történik az ország számos pontján, fontosnak tartottuk, hogy a rehabilitációhoz az elveket protokoll formájában is megfogalmazzuk.
3. A protokoll bevezetésének feltétele
Megfelelő tájékozottság a fent említett területen. Ennek érdekében a szakemberek továbbképzése szükséges nemcsak a team tagokkal együtt. Ez a protokoll nem vonatkozik a teljesen egyedi sajátosságokat mutató fejlődési rendellenességek, és a tumoros eredettel kialakuló scoliosisok ellátására.
4. A bizonyítékok forrásai a következők:
A: nagyszámú randomizált, ellenőrzött klinikai vizsgálat és ellenőrzött vizsgálatok vagy metaanalízisen alapuló eredmények
B: előbbinél kisebb betegszámon alapuló randomizált eredmények
C: nem randomizált, nem ellenőrzött klinikai vizsgálaton alapuló eredmények
D: szakértői testület egyeztetett véleménye
B-C: Tankönyvek, monográfiák esetében a bizonyítékokra együttesen hivatkozunk
5. Definíció
A scoliosis, mint tünet, sokféle okra visszavezethető eltérés. Lényege a gerinc kóros görbülete a frontális síkban, amelyhez bizonyos esetekben a tér szagittális és horizontális irányában is további deformitások társulhatnak. B-C szintű evidencia: 3
6. A rehabilitáció célja
Az orvosi, pedagógiai, szociális, foglalkozási területeken alkalmazott intézkedésekkel a lehető legjobb életminőség elérésével a társadalmi szerepekben legkevésbé akadályozó élet kialakítása.
A rehabilitáció akkor eredményes, ha a következő feltételek teljesülnek:
A konzervativ terápia mellett a progresszió lassul vagy megáll, a beteg panasza megszűnik, a tartása kompenzált lesz, a gerinc rugalmassága, a görbület mobilitása megmarad B-C szintű evidencia: 3
A görbület a fűzőben 10 Cobb foknál nagyobb csökkenést mutat a feladást követ 6-8 héttel készült kontroll rtg. felvételen B-C szintű evidencia: 3
7. A rehabilitálhatóság feltétele
Az etiológia lehetőség szerinti tisztázását követően a rehabilitációs team által nyújtott megfelelő tájékoztatás a gyermek és szülei részére, amelynek eredményeként terápiás egyezmény jöhet létre. A rehabilitálandó személy (kiskorú esetén a család is) vállalja az aktív részvételt, együttműködik az aktuális feladatok végrehajtásában. Az érintett populáció szűrése a fizikális vizsgáló módszerekben jártasságot szerzett orvos (házi/ gyermekorvos, iskolaorvos, védőnő) feladata. Gyanú esetén a szűrő orvos beutalásával ortoped szakorvosi vizsgálat kell, hogy kövessen. D szintű evidencia (1,2)
II. Diagnózis
8. A rehabilitációs program elemei
8.1. Anamnézis
A családi anamnézis a scoliosis besorolhatósága szempontjából fontos. Az etiologiai besorolás szerint a scoliosis lehet ismert okra visszavezethető, un. másodlagos (secunder), vagy napjainkban még ismeretlen tényezők, okozta idiopathiás (primer) típusú. B-C szintű evidencia (3)
Az ismeretlen etiológiájú scoliosisok háttere az intenzív kutatások ellenére sem magyarázható meg egyetlen, egyértelmű okkal a jelenlegi tudásunk alapján. Nem egyértelmű kutatási adatok szólnak a genetikai predispozició (poligénes öröklődés 6, 10, 12, 18, 13-as kromoszóma érintettségével) talaján ható hormonális (ösztrogén receptor polimorfizmus, melatonin), kötőszöveti és neuromuszkuláris tényezők mellett. C szintű evidencia (4) Az ismert okú lehet funkcionális- statikai, bénulásos, vagy antalgias tartást kísérő- vagy strukturális- congenitalis, neuromuszkuláris, mezenchimális, vagy egyéb, pl. traumás eredetű.
8.2. Életkor
A tünetek megjelenése alapján a scoliosisokosztályozásakor infantilis scoliosisról beszélünk, ha 3 éves kor előtt jelenik meg, juvenilisről, ha 3-10 éves kor közt, és adolescensről, ha a pubertas ideje körül jelentkezik, de a nemzetközi irodalomban mára korai kezdetű -early onset -5éves kor előtt, ill. késői kezdetű -late onset- csoportosítást használják. B-C szintű evidencia (3)
8.3. Gyakoriság
Az idiopathiás strukturális scoliosis előfordulási gyakorisága Magyarországon megegyezik az irodalmi gyakorisággal: 0,3-0,4%, a fiú-lány arány 1:6-8, ami a 20 Cobb fok feletti görbületekre vonatkozik. Ha az enyhébb görbületekkel is számolunk és minden 10 Cobb foknál nagyobb görbületre együttesen, adjuk meg a gyakoriságot, akkor 2-3 %-os incidenciávalés 1:2 fiú-lány aránnyal számolhatunk. Az ismert etiologiájú scoliosisokennél nagyságrenddel ritkábbak, de az alapbetegség súlyossága miatt rehabilitációs szempontból sokkal, nagyobb jelentőséggel bírnak. B-C szintű evidencia (3)
8. 4. Diagnosztikai vizsgálatok
Minden esetben - a statikai gerincferdülés kivételével - a gerincről röntgen vizsgálat szükséges (ap. és oldalirányú teljesgerinc), szükség szerint funkcionális felvételekkel kiegészítve. Bizonyos esetekben, ahol a támasztórendszeren és a mozgatóapparátuson kívül az idegrendszer is érintett lehet, speciális képalkotó eljárás (CT, MR) végzése is szükséges.
8.5. Funkcionális állapot felmérése 8.5.1. Szomatikus állapot felmérése
A secunder scoliosisok általában az alapbetegség tüneteivel jelentkeznek. Az idiopátiás (primer) esetben a háti típusoknál a mellkas torzulása, a bordapúp, míg lumbalis típusoknál a derékaszimmetria és az izompúp hívják fel a figyelmet, ritkán jelentkezik első tünetként fájdalom. A progresszió sebességétől és mértékétől függően a fiziológiás görbületek ellapulnak. A deformitás az érintett szakaszokon a csigolyák, a háti szakaszon a csigolyákkal összefüggő bordák szerkezeti változását eredményezi, mely a kapcsolódó izomzat eredési-tapadási pontjának megváltozását és az érintett izom jellegzetességétől függően funkcionális eltérést hoz létre. Az állapotfelmérés keretében az életkornak megfelelő percentilis táblázatok használatával a növekedés mértéke, annak üteme, a gyarapodás mértéke minden alkalommal rögzítendő.A jelenlegi gyakorlatban alkalmazott álló testmagasságmérés mellett kívánatos lenne az ülőmagasság mérése is. Mivel serdülő kor előtt az epifizis fúgák nyitottsága miatt a teljes testmagasság növekedés 2/3-a a végtagokra esik, így az ülőmagasság növekedésénekelmaradása jobban jelzi a scoliosis progresszióját A status felmérés kötelező része a végtaghosszúság mérése azokban az esetekben, ahol az abszolút, ill. relatív rövidülés mértéke a statikai scoliosisok kezelésének alapja. A tünetek és panaszok alapján az orvos és/vagy gyógytornász megvizsgálja a gerinc és a végtagi izületek mozgását, felméri az izomstatust (tónus, izomerő). B-C szintű evidencia (3)
8.5.2. Pszichés állapot felmérése
A strukturális eltéréssel járó esetekben a testkép megváltozása jellemző. Ez különösen serdülőkorban kóros szorongást okozhat, míg a gyors progressziót mutató és a súlyos alapbetegség részeként jelentkező ferdülések esetében emellett depressziós reakciókra is számítani lehet. A beteg és családja, valamint a kortárs közösség, a beteg szociális izolálódása ellen sokat tehet, a pszichológiai vizsgálatoknak erre ki kell térni.
8.5.3. Terhelhetőség mérése
A légzőapparátus állapotát légzésfunkciós vizsgálattal is rendszeresen ellenőrizni kell. Kerékpár ergometriás vizsgálat javasolt azokban az esetekben, ahol a súlyos mellkas deformitás miatt a kardiorespiratórikus rendszer jelentős károsodása észlelhető. A neuromuszkuláris betegnél a vizsgálat nehézségekbe ütközhet, a mozgatórendszer jelentős gyengülése miatt. A légzésfunkciós vizsgálat eredménye is befolyásolja a terhelhetőséget, ezért ezt, sz. sz. vérgáz méréssel kiegészítve, súlyos görbületű betegeknél szükséges elvégeztetni. B-C szintű evidencia (3)
A mindennapos mozgás során a pulzusszám ellenőrzése, a nyugalmi pulzusszám visszatérési idejének ismerete segít az erőnléti edzésterhelés ellenőrzésére.
III. Kezelés
8. 6. Kezelés
8.6.1. Az alapbetegség kezelésének folytatása
Ismert etiológiájú scoliosisok esetében az alapbetegség gyógyszeres terápiáját folytatni szükséges, amennyiben erre szükség és mód van (pl. Cystas Fibrosis). A neuromuszkuláris betegségekben, bizonyos esetekben adható szteroidok nem csak a betegség természetes lefolyását változtatják meg, de a scoliosis megjelenésének idejét is, ill. a terhelhetőséget is. Erre az alapbetegséget kezelő szakorvos döntése alapján kerül sor, azonban erről a scoliosis kezelését végző szakembereknek is tudnia kell.
8.6.2. A scoliosis kezelése és a szövődmények megelőzése
Gyógyszeres: Az idiopátiás scoliosisokban a jelen ismeretek szerint sem a D vitamin, sem a Ca, Mg, vagy fehérjebevitel forszírozása nem csökkenti a progressziót. B-C szintű evidencia (3)
A súlyos, torziós scoliosis a mellkasdeformitás miatt hozzájárulhat a légúti betegségek súlyosabb lefolyásához, ezért ilyen betegeknél fokozott figyelmet érdemel a légzőtorna felügyelete, akut betegség esetén a váladékoldás gyógyszeres kezelése és a váladék eltávolítás, fizioterápia segítségével történő biztosítása. Fájdalommal járó esetekben gyógyszeres csillapítás, ill. lazító TENS kezelés, masszázs egészítheti ki a terápiát. C szintű evidencia (4)
Mozgásterápia: Az erőnlét javításának legfontosabb eszköze a mozgás. A fizioterápia a betegség etiologiájától, a beteg életkorától és általános állapotától függően egyéni és csoportos formában érhető el. Alapja a gyógytorna, mely különböző módszerekkel segíti a mozgás során a gerinc élettani mozgástartományának megőrzését (túlmobilizálás a progressziót fokozza káros,kivéve a műtéti előkészítést), a deformitás csökkentését (pl. PNF, Schroth). A fizioterápia 20-40 Cobb fok közt fűzőkezeléssel kiegészítve, 40 fok felett műtéti előkészítésként és utókezelésként minden betegnek szükséges. A fizioterápia eredményét a betegség etiologiája mellett a beteg kooperációja és a terapeuta által választott módszerben való jártassága is befolyásolja. A gyógytorna rövidtávú előnye a javuló tüdőfunkció, csökkenő fájdalom, a progresszió csökkenése, esetleg megállása, javuló tartás, csoportos torna esetén pszichés támogatás a "sorstársak" részéről. A szintű evidencia (5, 6, 9) C szintű evidencia (7,8)
- Az erőnlétet javítja a szárazföldi foglalkozások mellett végezhető gyógyúszás is, erre külön képesítéssel rendelkező oktató vezetésével. Jelen szabályozás szerint scoliosis miatt 2x52 alkalom javasolható (írható fel receptre), melyet heti 2 alkalommal 45 perces foglakozások keretében lehet igénybevenni biztosítói támogatással 18 év alatt. Ezt követően már csak 15 alkalommal vehető igénybe fürdőkezelés részeként támogatott formában az úszás. Ez azonban nem helyettesítheti a scoliosis kezelését!
- Iskolai gyógytestnevelés: Az alapbetegség függvényében törekedni kell arra, hogy minél kevesebb korlátozással éljenek a betegek, így helytelen gyakorlat a scoliosis miatt testnevelés alóli felmentés, ha más ezt nem indokolja. Szükség lehet azonban könnyítésre a gerinc hosszirányú terhelésével járó gyakorlatok esetén, vagy gyógytestnevelés elbírálására. D szintű evidencia (2)
- Műtéti kezelés:40 Cobb fok felett általában a konzervativ kezelés nem elegendő, ezért gerincsebészeti konzilium javasolt A kezelés külön protokoll szerint szabályozott, mivel a gerinc görbületeit korrigáló műtéteknek számtalan változata létezik és speciális feltételrendszere van. A műtéti kockázat jelentősen csökkenthető a fejlett instrumentációs technikáknak, a műtét alatti gondos, műszeres megfigyelésnek, a magas szintű szakmai felkészültségnek köszönhetően, de a műtéti időpont gondos mérlegelése az operáló orvos feladata. Speciális szövődmény a plégia. A kezelő team a műtéti előkészítésben és az utókezelésben is eredményesen segítheti az operatőr munkáját.
C szintű evidencia (11,12)
- Sport: Súlyos deformitással járó esetekben a féloldalas sportok megfontolandók, ill. célszerű a kondicionálóterem használatánál megfelelő edző segítségének kikérése. Hobbi szinten a sportolás mindenképpen ajánlott a gerinctorna gyakorlatainak végzése mellett.
C szintű evidencia (13)
IV.-V. Rehabilitáció, Gondozás
8.6.3. Önellátás elérése
A mindennapi élettevékenységek terén a scoliosis általában nem okoz eltérést, de fűzőkezelés során az öltözés, ill. a toalett használat problémás lehet. A műtéti kezelés után az elmerevített gerincszakasz hosszától függően kiesik a gerinc mozgása, így a még mozgó szakaszok és a végtagi nagyizületek optimális ergonómiai kompenzácios mozgásának segítése a terapeuta feladata.
8.6.4. Mobilitás biztosítása
A scoliosis a mobilitást általában nem befolyásolja, azonban amennyiben az alapbetegség miatt kerekesszék használatra szorul a beteg, a súlyos deformitás nehezítheti a hajtást.
8.6.5. Állapot elfogadtatása (lelki vezetés) és az annak megfelelő életvitel elsajátítása
A scolosis kezelésében a rendszeres gyógytorna elfogadása, a fűző kezelés elviselése gondot jelenthet különösen az adolescens korosztályban, ezért az USA-ban a fizioterápia visszaszorulása mellett a műtéti kezelések kerültek előtérbe. A scoliosis miatt kezelt beteg nagy része ambuláns formában ellátható, ami segíti az együttműködést. Az állapot nyomon követése csak rendszeres gondozás mellett biztosítható, ami a növekedés befejeződésig 3-6 havonta végzett fizikális vizsgálatot és évente röntgen kontrollt jelent. A fűzőkezelést igénylő esetekben a fűző cseréje esetén is szükséges kontroll röntgen, a korrekció mértékének ellenőrzésére. B-C szintű evidencia (3)
Szervezett gyógytorna, legalább heti 2 alkalommal szükséges a kezelés teljes tartama alatt. A betanult gyakorlatokat azonban otthon, naponta végezni kell! Egyéni torna szükséges nagyon fiatal páciensek esetén a kialakulatlan izomérzet miatt a korrekció megtanítására és gyors növekedés esetén, fokozott progresszió mellett. Ez legalább 2-3 hétig, heti 5 alkalommal, gyógytornász segítésével végzett foglalkozást jelent. Amennyiben a beteg/család kooperációja nem megfelelő, a konzervatív terápia eredménytelensége esetén műtéti kezelés javíthat az állapoton, de itt is fontos a megfelelő konzervatív előkészítés és utókezelés, ilyenkor intézeti keretek közt. Mindkét esetben javasolt a rossz kooperáció okának pontos felderítése, az esetleges ismerethiány miatti kommunikációs probléma kezelése, a beteg és családjának képzése. C szintű evidencia (14)
8.6.6. Segédeszközök biztosítása
Fűzőkezelés
Strukturális scoliosisban 20 Cobb fok feletti görbület az esetek több mint felében a konzervatív kezelés elmaradása esetén progrediál. B-C szintű evidencia (3)
Idiopátiás scoliosis esetén a romlás mértéke és sebessége függ az alapbetegségtől (ismert aetiologiájú esetekben), a görbület formájától és nagyságától, a beteg életkorától, nemétől, a maturáltság fokától, a várható növekedés mértékétől, a menarche-tól eltelt idő hosszától, a kezelés kezdetének időpontjától, az alkalmazott kezeléstől. A szintű evidencia(5,6) A fűzők egyedi gipszminta után, magas hőfokon lágyuló műanyagból készülnek.
Az idiopátiás scoliosis fűző kezelésének szabályai:
- Jelentős progressziónál (fél év alatt több mint 5 Cobb fok), amint eléri a görbület a 20 Cobb fokot, el kell kezdeni a fűzőkezelést.
- A görbületnek megfelelő típusú fűző használata ajánlott.
- Viselési idő: 18- 20 óra / nap. Kezelőorvosi kontroll vizsgálat 3-4 havonta.
- Röntgenfelvételek készítése két irányból, álló helyzetben évente, de új fűző készítése előtt mindig, valamint az új fűző feladását követően 6-8 héttel.
- Állapotváltozáskor (magasság-, súlynövekedés, görbület nagyságának jelentős változása) fűzőcsere.
- Fűzőkezelés folytatása a csontérettség eléréséig szükséges
- 40 -50 Cobb foknál nagyobb görbületeket már ne kezeljünk fűzővel.
A progresszió lassítására a 40 fok alatti görbületek esetén a tanulmányok egy része szerint a fűzőkezelés alkalmas. A szintű evidencia (5,6,15) B szintű evidencia (19,20)B-C szintű evidencia (3)C szintű evidencia (4,17,18,21)
Fűző típusok strukturális scoliosis kezelésére:
Boston korzett- rövid műanyagfűző, kétféle formája van. Hátul nyitható formájában, elsősorban a thoracolumbalis és lumbalis gerinc frontális és sagittalis irányú strukturális görbületeinél alkalmazható, amikor a görbület csúcspontja a Th X. csigolya alatt helyezkedikel. A korzett, elől nyitható formája az ágyéki gerincszakasz rögzítésére szolgál.
Charlestone korzett - a gerinc egyívű, mobilis , a háti-ágyéki átmenetében elhelyezkedő strukturális, scoliotikus görbületének kezelésére alkalmas. A fűző a beteget túlkorrigált helyzetben tartja, ezért csakfekve, elsősorban éjszakai viseletre alkalmas, mobilis és relatíve kicsi, maximum 25 Cobb fokos görbületek esetén ajánlott.
Cheneau korzett - a leggyakrabban alkalmazott fűző, amely alkalmas, mind a frontális (scoliosis), mind a sagittális (kyphosis, lordosis) síkban elhelyezkedő strukturális gerincgörbületek korrekciójára. Álltartóval kiegészítve, nemcsaka háti és ágyéki, hanem a nyaki gerinc görbületeinek korrekcióját is lehetővé teszi.
Stagnara (lyoni) korzett-a törzs elülső és hátsó oldalán, a középvonalban futó 1 -1 fémsínből és a fémsínekhez rögzített korrekciós pelottákból áll. Alkalmas strukturális scoliosis kezelésére, napjainkban elsősorban műtétek utáni rögzítésre használják. Kiegészíthető nyakgyűrűvel. Némi módosítással nyílirányú strukturális gerincgörbületek (pl. Scheuermann féle betegség) korrekciójára is alkalmassá tehető.
Milwaukee korzett - bármilyen irányú és lokalizációjú görbület kezelésére alkalmazható. A fűző medencekosárból, nyakgyűrűből, összekötő sínekből és a görbületeknek megfelelően elhelyezett korrekciós párnákból áll. A nyakgyűrű, amely kilátszik a ruhából, súlyos lelki problémákat okozhat a serdülőknél. A nyakgyűrű használata csak a magas háti görbületeknél (csúcscsigolya a Th 5. csigolya felett) ill. a nyaki folyamatoknál kötelező. Hibája még a korzettnek, hogy a háti gerinc, idiopathias scoliosisnál jelentkező ellaposodását nem lehet vele megelőzni.
Merev fűzők előnyei
- A korszerű, korrekciós fűzők képesek 3D korrekcióra, a Milwaukee-t kivéve. Az elsődleges korrekció már a feladást követően azonnal jelentkezik, de a teljes korrekció, 6 hét múlva készült fűzős röntgenfelvétellel mutatható ki
Merev fűzők hátrányai
- Neuromuscularis eredetű scoliosisban a merev fűzők bár "kényszerítenek" a korrigált tartásra csak rövid ideig képesek a progressziót lassítani, ezért általában nem ajánlható a használatuk.
- Serdülőkorú pácienseknél a kortárs közösség elutasításától való félelem gátolhatja a nappali viselést. A szintű evidencia (5,6,15) B szintű evidencia (19,20) B-C szintű evidencia (3) C szintű evidencia (4,10,16,17,18,21)
Rugalmas fűzők
A merev műanyagfűzők mellett léteznek rugalmas, dinamikus fűzők is. Az ezzel kapcsolatos eredmények ellentmondóak. C szintű evidencia (22) Rugalmas fűzőkezelés előnyei
- A merev fűzőkkel szemben előnye, hogy gyakorlatilag láthatatlan, minden mozgás kivitelezhető benne, így a 20 órás viselés könnyebben megoldható, könnyebb a gerinc rugalmasságát megőrizni.
Rugalmas fűzőkezelés hátrányai
- Szűk az indikációs területe, a felhelyezést követően azonnal nem észlelhető a javulás, nem korrigál minden síkban, a napi felvétele nagyobb odafigyelést kíván (pántok, tépőzárak pontos elhelyezése, a medenceöv gondos beállítása) és a toalett használat bonyolult.
VI. Irodalomjegyzék
1. Gerincdeformitások, scoliosis, kyphosis. Az Ortopédiai Szakmai Kollégium Protokollja. Érv: 2006. december 31.
2. A testnevelés kategóriákba sorolás szempontjai. Az Országos Gyeremekegészségügyi Intézet szakmai irányelve 2007
3. Szendrői M. (szerk): Az Ortopédia Tankönyve, Semmelweis Kiadó, Budapest, 2005.
4. Orosz M: Az idiopathias scoliosis kezelése Gyermekgyógyászat 2005; 6: 649-655
5. Rowe DE, Bernstein SM, Riddick MF et al.: A meta-analysis of the efficacy of non-operative treatments for idiopathic scoliosis. J Bone Joint Surg Am 1997; 79: 664-74.
6. Lenssinck ML, Frijlink AC, Berger MY.: Effect of bracing and other conservative interventions in the treatment of idiopathic scoliosis in adolescents: a systematic review of clinical trials. Phys Ther 2005; 85:1329-39.
7. Nagy Sz.: Az idiopathias scoliosis korszerű, komplex mozgásterápiája Gyermekgyógyászat, 2005; 6: 657-665.
8. Rigo M, Reiter Ch, Weiss HR.: Effect of conservative management on the prevalence of surgery in patients with adolescent idiopathic scoliosis. Pediatr Rehabil 2003; 6: 209-14.
9. Maruyama T, Kitagawa T, Takeshita K.: Conservative treatment for adolescent idiopathic scoliosis: can it reduce the incidence of surgical treatment? Review. Pediatr Rehabil 2003; 6: 215-9.
10. O'Neill PJ, Karol LA, Shindle MK.: Decreased orthotic effectiveness in overweight patients with adolescent idiopathic scoliosis. J Bone Joint Surg Am 2005;87:1069-74.
11. Illés T.: A gerincdeformitások 3 dimenziós analízise és műtétti terápiája MTA Doktori disszertáció 2003
12. Jeszenszky D: A gerincdeformitások műtéti kezelése neuromuscularis betegségekben Gyermekgyógyászat, 2005; 5: 523-530.
13. Weiss HR, Weiss G, Schaar HJ.: Incidence of surgery in conservatively treated patients with scoliosis. Pediatr Rehabil 2003; 6: 111-8.
14. Reichel D, Schanz J: Developmental psychological aspects of scoliosis treatment. Pediatr Rehabil 2003; 6: 221-5.
15. Weiss HR, Negrini S, Hawes MC et al.: Physical exercises in the treatment of idiopathic scoliosis at riskof brace treatment
- SOSORT consensus paper 2005. Scoliosis 2006;1:1748-7161.
16. Karol LA.: Effectiveness of bracing in male patients with idiopathic scoliosis. Spine 2001; 26: 2001-5.
17. Weiss HR, Weiss GM.: Brace treatment during pubertal growth spurt in girls with idiopathic scoliosis (IS): a prospective trial comparing two different concepts. Scoliosis 2005; 8:199-206.
18. Howard A, Wright JG, Hedden D. :A comparative study of TLSO, Charleston, and Milwaukee braces for idiopathic scoliosis. Spine 1998;23:2404-11.
19. Nachemson AL, Peterson LE.: Effectiveness of treatment with a brace in girls who have adolescent idiopathic scoliosis. A prospective, controlled study based on data from the Brace Study of the Scoliosis Research Society. J Bone Joint Surg
Am 1995; 77: 815-22.
20. YrjonenT,YlikoskiM, SchlenzkaD. :Results of brace treatment of adolescent idiopathic scoliosis in boys compared with girls: a retrospective study of 102 patients treated with the Boston brace. Eur Spine J 2007; 16: 393-7. Epub 2006 Aug 15.
21. Janicki JA, Poe-Kochert C, Armstrong DG.: A Comparison of the Thoracolumbosacral Orthoses and Providence Orthosis in the Treatment of Adolescent Idiopathic Scoliosis: Results Using the New SRS Inclusion and Assessment Criteria for Bracing Studies. J Pediatr Orthop 2007; 27: 369-374.
22. Coillard C, Vachon V, Circo AB, Beauséjour M, Rivard CH: Effectiveness of the SpineCor brace based on the new standardized criteria proposed by the scoliosis research society for adolescent idiopathic scoliosis. J Pediatr Orthop.
2007; 27:375-9
A szakmai protokoll érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai protokollja
A krónikus gyulladásos bélbetegségekről (IBD)
(1. módosított változat)
Készítette: a Csecsemő- és Gyermekgyógyászati Szakmai Kollégium I. Alapvető megfontolások
1. A protokoll alkalmazási / érvényességi területe Csecsemő és gyermekgyógyászat, 0-18 éves kor között
2. A protokoll bevezetésének alapfeltétele
Az ebbe a betegségcsoportba tartozó két leggyakoribb kórkép, a Crohn-betegség és a colitis ulcerosa az utóbbi évtizedekben egyre gyakrabban lép fel már gyermekkorban is. Mindkét betegség igen változatos tünetekkel jelentkezhet, számtalan szövődmény kísérheti azokat. Ezek a korábban reménytelennek tűnő betegségek az utóbbi évtizedekben az újabb és korszerűbb gyógyszerek elterjedésével és a modern sebészi eljárások alkalmazásával egyre jobban kezelhetővé váltak. Jelen protokoll bevezetésének alapfeltétele, hogy az abban tárgyalt diagnosztikus és terápiás lehetőségek rendelkezésre álljanakés az adott intézmény rendelkezzen képzett gyermek-gasztroenterológus szakorvosokkal
3. Definíció
Acolitis ulcerosa a vastagbél és a rectum hyperaemiával, ulcerációval és oedemával járó krónikus gyulladása, ami csak a mucosára és a submucosára terjed, és a beteg bél folyamatos gyulladást mutat. Ritka esetben érintett lehet a terminális ileum is, de további bélszakaszokat a betegség nem involvál.
A Crohn-betegség a gastrointestinalis traktus krónikus, ismeretlen eredetű gyulladásos megbetegedése, ami szemben a colitis ulcerosával, a gyomor-bélrendszer bármelyik szakaszán felléphet. Megjelenése általában szegmentális és a bélfal minden rétegére kiterjedhet (transmuralis). Leggyakoribb lokalizációja az alsó vékonybélszakasz és/vagy a vastagbél. 3.1.) Kiváltó tényezők 3.2.) Kockázati tényezők
A kockázatot befolyásoló főbb környezeti tényezők:
Crohn betegségben a kockázatot emeli a dohányzás, a fogamzásgátlók rendszeres szedése,a stresszes életmód, míg a rendszeres fizikai aktivitás csökkenti a kockázatot. Colitis ulcerosában a kockázatot növeli a stresszes életmód, a rendszeres fizikai aktivitás pedig csökkenti. Mindkét betegségben a kockázat magasabb a jobb szociális helyzetű családokban
4. Panaszok/Tünetek/Általános jellemzők
A Crohn-betegség tünetei közé legtöbbször az alábbiak tartoznak:
- Hasi fájdalom, gyakran evést követően
- Növekedésbeli elmaradás
- Pubertás késése
- Véres széklet
- Fissurák, fistulák, perianalis fekélyek,
- Bőrfüggelék az anus körül
- Étvágytalanság
- Rossz közérzet, fogyás, láz
- Iridocyclitis
- Erythema nodosum
Típusos Crohn-betegségre a legjellemzőbb a hasi fájdalom és a fogyás, amit rossz közérzet kísér, gyakori a láz. Előfordulhat, a legtöbbször az ileocoecalis régiónak megfelelően tapintható hasi terime is, amit bélkonglomerátumok okoznak. Ilyen tünetegyüttes esetén többnyire a vékonybél, elsősorban a terminális ileum érintett. Gyermekkorban gyakrabban fordul elő, hogy a tünetek előterében kizárólag a malnutritio áll, amit az étvágytalanság és a rossz felszívódás okoz. Kiemelést érdemel, hogy sokszor csupán a növekedésbeli elmaradás és/vagy a pubertás tarda lehet a Crohn-betegség egyetlen manifesztációja, így ilyenkor erre a kórképre mindenképpen gondolni kell. A colitis ulcerosa jellemző tünetei az alábbiak:
- Hasmenés, gennyes, véres székletek
- Tenesmus
- Láz
- Hasi fájdalom (gyakran székelés előtt)
- Növekedési elmaradás (ritkább, mint Crohn-betegségben)
A véres, nyákos székletekés a tenesmus a colon gyulladását jelzik, de önmagukban természetesen nem bizonyítják a colitis ulcerosa fennállását. Hangsúlyozandó, hogy a Crohn-betegség is jelentkezhet colitis ulcerosára jellemző tünetekkel, abban az esetben, ha elsősorban a colont érinti a gyulladás. A colitises tünetegyüttes esetén a hasi fájdalom gyakran lehet diffúz, égő jellegű és jellemzően a székletürítéshez társul.
Bármilyen eredetű colitis súlyos szövődménye a toxicus megacolon, amire az alábbi tünetek a jellemzőek:
- Haspuffadás
- A bélhangok nem hallhatók
- Elektrolit eltérések mutathatók ki.
- Gram-negativsepsis és masszív vérzés is felléphet.
- Könnyen vezet colon perforációhoz.
A 1. táblázat segít a Crohn-betegség és a colitis ulcerosa elkülönítésében az intestinalis tünetek alapján
1. táblázat. A Crohn-betegség és a colitis ulcerosa intestinalis manifesztációinak összehasonlítása
| Intestinalis tünetek | CD | UC |
| Haematochezia | + | +++ |
| Diarrhea | + | +++ |
| Hasi fájdalom | +++ | + |
| Anorexia | +++ | + |
5. A betegség leírása
5.1.) Érintett szervrendszer(ek)
Az 2. táblázatban egymással összehasonlítva látható, hogy a Crohn-betegség és a colitis ulcerosa a gyomor-bél traktus mely részein fordul elő leginkább.
2. táblázat. A gastrointestinális traktus érintettsége Crohn-betegségben és colitis ulcerosában
| Lokalizáció | Crohn-betegség | Colitis ulcerosa |
| Nyelőcső, gyomor | + | - |
| Vékonybél proximalis és középső része | + | - |
| Distalis ileum | +++ | + |
| Colon | ++ | +++ |
| Rectum | ++ | +++ |
| Anus | +++ | - |
+++ igen gyakori, ++ gyakori, + ritka, - nem fordul elő
Vastagbél lokalizáció esetén a két betegség az esetek kb. 10 százalékában nem különíthető el egymástól, ilyenkor un. indeterminált colitisről beszélünk.
Extraintestinalis tünetek
A gyulladásos bélbetegségnek sokszor vannak extraintestinalis manifesztációi is, amelyek közül egyesek inkább colitis ulcerosa esetén, mások inkább Crohn-betegség esetén gyakoribbak (3. táblázat). Fontos tudni, hogy sokszor az extraintestinalis manifesztációk megelőzhetik az intestinális tünetek fellépését.
3. táblázat. A Crohn betegség és a colitis ulcerosa extraintestinalis manifesztációi
| Extraintesztinális megjelenés | Crohn-betegség | Colitis ulceros |
| Episcleritis, uveitis | + | + |
| Aphthák | +++ | + |
| Erythema nodosum | + | + |
| Pyoderma gangrenosum | + | + |
| Dobverőujj | ++ | + |
| Arthritis | ++ | ++ |
| lparSpondylitis ankylopoetica | + | + |
| Primer szklerotizáló cholangitis | + | + |
| Steatosis hepatis | + | + |
| Perianalis lézió | +++ | - |
| Növekedési elmaradás | +++ | + |
| Pancreatitis | + | + |
| Pericarditis | - | + |
| Láz | +++ | ++ |
+++ igen gyakori, ++ gyakori, + ritka, - nem fordul elő
5.2.) Genetikai háttér
A Crohn-betegek egyharmadában a 16-os kromoszómán elhelyezkedő CARD15 gén mutációja mutatható ki. Amennyiben mindkét allélen ezen gén mutációja észlelhető, akkor a Crohn-betegség kialakulásának a relatív kockázata: 30-40 % körül van. A genetikai meghatározottságra utal az is, hogy egypetéjű ikerpárokban a Crohn-betegség konkordanciája 36%, kétpetéjűekben pedig csupán 4%. Colitis ulcerosában a genetikai hajlam kevésbé kifejezett és még nem teljesen feltárt. Egypetéjű ikerpárokban a betegség konkordanciája 16%, kétpetéjűekben pedig 4% colitis ulcerosa esetén.
5.3.) Incidencia / Prevalecia /
Az utóbbi évtizedekben a gyulladásos bél betegségek gyakorisága jelentős mértékben növekedett gyermekkorban is. A 10-19 éves korcsoportban a colitis ulcerosa korspecifikus incidenciája 2-3/100000, míg a Crohn-betegségé 3-4/100000 között mozog.
A betegség gyakoribb a fejlett európai országokban és Észak-Amerikában. Ázsiai és afrikai populációban ritka, de érdekes módon közöttük is gyakoribb, amennyiben a magasan civilizált országokba vándorolnak, ami a környezeti tényezők szerepére utal. Igen gyakran fordul elő gyulladásos bélbetegség askenázi zsidókban
5.4.) Jellemző életkor
Hangsúlyozandó, hogy a Crohn-betegségben szenvedők 25-30%-ban, a colitis ulcerosásoknak pedig a 20%-ában kezdődik a betegség 20 éves kor alatt, vagyis mindkét kórképnek nagy a gyermekgyógyászati jelentősége.
II. Diagnózis
1. Diagnosztikai algoritmusok
3. Fizikális vizsgálatok
Igen fontos az anamnézis pontos felvétele, gyulladásos bélbetegség gyanúja esetén elsősorban azokra a jelekre kell figyelni, illetve rákérdezni, amelyeket a "Panaszok, tünetek, általános jellemzők" fejezetben tárgyaltunk. Fontos kitérni az esetleges extraintestinalis érintettségre utaló panaszokra is. Mindez vonatkozik a fizikális vizsgálatra is.
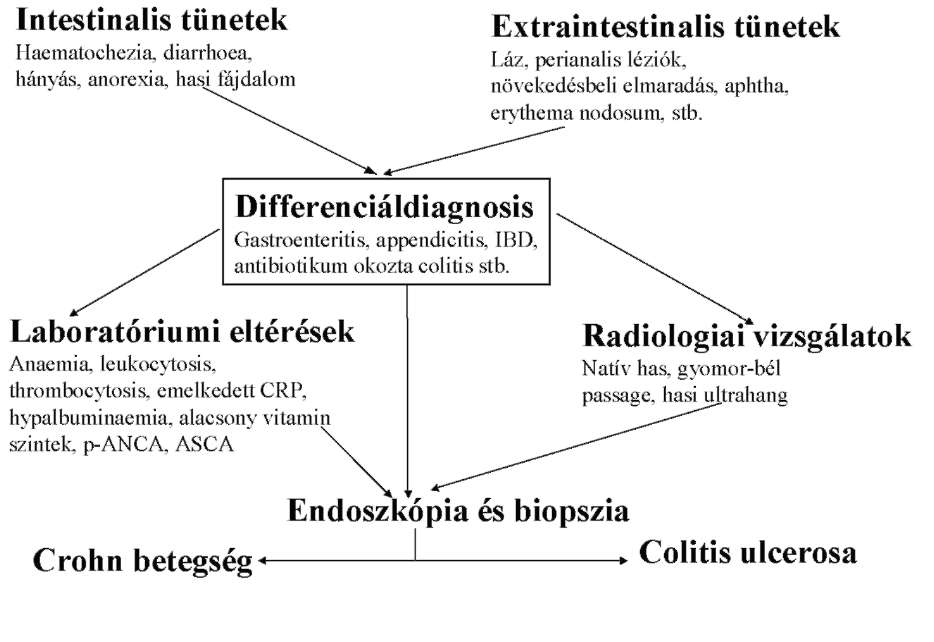
2. Anamnézis
4. Kötelező (minimálisan elvégzendő) diagnosztikai vizsgálatok (felhasznált bizonyítékok, azok szintjei) 4.1.) Laboratóriumi vizsgálatok
A jó anamnézis és fizikális vizsgálat természetesen már legtöbbször felveti a gyulladásos bélbetegség gyanúját,de annak bizonyításához laboratóriumi, endoszkópos és hisztológiai vizsgálatokelvégzésére van szükség. Egyetlen olyan eltérés sincs azonban, aminek alapján a Crohn-betegséget, vagy a colitis ulcerosát önmagában kórismézni lehetne. A diagnózis mindig a különböző vizsgálatok során nyert jellemző eltérések alapján, mozaikszerűen áll össze. Természetesen típusosnak tekinthető esetekben könnyű eljutni a diagnózishoz, de előfordul, hogy azt csak igen nehezen tudjuk felállítani. A diagnosztikus módszereket foglalja össze a 4. táblázat.
4. táblázat. A gyulladásos bélbetegségek kórismézésében alkalmazott módszerek
| Laboratóriumi vizsgálatok | Haemoglobin, haematokrit, vvt indexek, leukocyta, thrombocytaszám, Gyulladásos márkerek: CRP, süllyedés, fibrinogén Se vas, TVK, ferritin Se összfehérje, albumin, elfo, immunelfo pANCA, ASCA |
| Képalkotó vizsgálatok | Natív has Ultrahang Felső passzázs vizsgálat Irriogsocopia (ritkán) Szelektív enterográfia.... Izotóp vizsgálatok CT MR |
| Endoszkópia | Colonoscopia Felső endoszkópia |
| Hisztológiai vizsgálat | Bélnyálkahártya |
Vastag betűvel jelölve a kötelezően elvégzendő vizsgálatok
Alapvetően fontos a teljes vérkép és a süllyedés vizsgálat elvégzése. Bár az IBD-re nem tekinthető specifikusnak, mégis általában kimutatható a legtöbbször microcyter, hypochrom anaemia. Az anaemia leggyakrabban felszívódási zavar, vagy okkult vérzés miatti vashiány következtében jön létre, de kiválthatja folsav és/vagy B12-vitaminhiány, vagy egyéb malnutritiós ok is. A kialakuló anaemia másik patogenetikus oka lehet az IBD-ben felszabaduló gyulladásos cytokinek, így elsősorban az IL-1, a TNF-a és az interferon-g, melyek az erythropoetin gátlása révén csökkentheti az erythropoesist.
Igen gyakori az emelkedett thrombocytaszám és a magas süllyedés. Jellemző az alacsony szérum albumin szint, ami a kórkép okozta enterális fehérjevesztés következménye. A szérum kálium szint a profúz hasmenéssel járó formákban lehet alacsony. Dehidráció esetén a karbamid nitrogén szint egyes esetekben emelkedett lehet, általában azonban inkább alacsony a fokozott katabolizmushoz képest csökkent protein felvétel miatt. A thrombocytosis, a hypalbuminaemia és az akut fázis proteinek szintjének az emelkedése korrelációt mutat a szövettanilag látható gyulladásos jelek mértékével.
A colitis ulcerosa és a Crohn-betegség egymástól történő differenciálásában segítséget jelenthet a perinukleáris antineutrophil cytoplasmatikus antitest (pANCA) és a Saccharomyces cerevesiae (pékélesztő) elleni antitest titerek arányának meghatározása. Előbbinek a titere colitis ulcerosában, az utóbbié pedig inkább Crohn-betegségben emelkedik. Ezeknek a teszteknek a pozitivitása segít elkülöníteni az IBD-ben szenvedő betegeket a nem-gyulladásos bélbetegségben szenvedőktől.
4.2.) Képalkotó vizsgálatok
Crohn-betegség esetén a felső passzázs vizsgálatnak ma már csak ritkán van létjogosultsága a vékonybél eltérések megítélésére. A röntgenjelek közül a korai elváltozást jelzikaz ulcusokés a mucosa nodularis elváltozásai. Később már megfigyelhetőek lehetnek a jellemző utcakő rajzolat és a bélszűkület következtében kialakuló zsinór tünet. Fontos hangsúlyozni, hogy a felső passzás vizsgálat kevésbé invasiv, jobban tolerálható, kisebb sugárterheléssel jár, de kevésbé specifikus, mint a szelektív enterográfia. Az utóbbi alkalmazása csak ritkán javasolt gyermekkorban.
A vastagbél vizsgálatában a colonoscopia jelentős mértékben csökkentette az irriogoszkópia indikációját. A kettős kontrasztos irrigoszkópia csak akkor jön szóba, ha a colonoscopia elvégzése nem volt lehetséges technikai okokból a colon egész területén. Colitis esetén megfigyelhető a haustratio eltűnése és jellemző a fekélyképződés. Az irrigoscopia elvégzése abszolút kontraindikált toxicus megacolonra utaló tünetek fennállása esetén, ilyenkor natív hasi röntgen elvégzése indokolt, s azon jellemző a colon dilatációja, átmérője nagyobb mint 8 cm.
A hasi ultrahang vizsgálatnak elsősorban Crohn-betegségben van jelentősége, jellemzően kimutatható ilyenkor az érintett bélfal megvastagodásása és nyomon követhető annak változása a kezelés hatására. Az 5 mm-nél vastagabb bélfal kórosnaktekinthető. Ugyancsak kimutatható az ultrahang vizsgálattal a betegség következtében kialakult ileus, tályog, valamint a parenchymás szervek elváltozása és a retroperitoneum gyulladásos érintettsége. Szcintigráfiás vizsgálat során a beteg jelzett anyagot, ami a gyulladásos területen szelektíven dúsul. Alkalmazhatóak a beteg saját véréből in vitro 99-Technéciummal jelölt fehérvérsejtek, vagy in vivo jelölt granulocyta antitestek. Enneka módszernek elsősorban a betegség aktivitásának nyomonkövetésében van jelentősége. Ez az eljárás segíthet a részleges bél obstructio okának a tisztázásában. Izotóphalmozódás jelenléte arra utal, hogy a szűkület aktív gyulladás következménye, vagyis eredményt várhatunk a gyógyszeres kezeléstől, míg annak hiánya azt jelzi, hogy a strictura irreversibilis fibrosis következménye, tehát sebészi megoldás, stricturoplasztika elvégzése indokolt.. A CT és MR vizsgálat jól alkalmazható a Crohn-betegség következtében kialakuló tályogokés fistulák kimutatására. MR vizsgálattal ítélhetők meg legjobban a szükületek is.
4.3.) Egyéb vizsgálatok Endoszkópos vizsgálat
A gyulladásos bélbetegségek diagnosztikájában a legfontosabb eljárás. Elsősorban a colonoscopia informatív, de Crohn-betegség esetén felső endoszkópiára is szükség lehet, ha a tünetek a nyelőcső és a gyomor érintettségére is utalnak. A colonoscopiát gyermekkorban altatásban végezzük, a vizsgálat megfelelő előkészítést igényel. A vizsgálat előtti két napon a gyermek már csak folyékony, pépes ételt fogyaszt és a vizsgálat előtti napon X-Prep egyszeri adásával (l ml/kg) érjük el a vastagbél kiürülését. A colonoscopia előnye, hogy a vizsgálat során a nyálkahártya közvetlenül megtekinthető és biopsziás minták is vehetők. Legtöbbször az endoszkópos kép alapján nagy valószínűséggel elkülöníthető egymástól a colitis ulcerosa és a Crohn-betegség (5.táblázat).
5. táblázat. A colitis ulcerosráa és a Crohn-betegségre jellemző endoszkópiás lelet
| Vizsgált eltérés | Colitis ulcerosa | Crohn-betegség |
| Confluáló gyulladás | Gyakorlatilag mindig | Ritkán, jellemző az un. skip lèzio, ép részek a gyulladt területek között |
| Törékeny, sérülékenymucosa | Mindig | Ritkán |
| Granulált mucosa | Mindig | Ritkán |
| Fekélyek | Egymással konfluáló, felszínesesek | Éles szélű, mély, diszkrét, fissura-szerű, |
| Linearis fekélyek | Soha nem látható | Jellemző |
| Aphtoid elváltozások | Ritkán | Gyakori |
| Rectum érintettsége | Gyakorlatilag mindig, s kifejezettebb elváltozások, mint a colon többi részén | Nem jellemző |
5. Kiegészítő diagnosztikai vizsgálatok (felhasznált bizonyítékok, azok szintjei) Szövettani vizsgálat
Colitis ulcerosára jellemző az akut és a krónikus gyulladásos sejtinfiltratum a vastagbél és rectumnyálkahártya lamina propriájában. Az előbbit a neutrophil és eosinophil sejtek alkotják, míg az utóbbiakat a lymphocyták, plasmasejtek, monocytákés macrophágok képezik. Ezenkívül típusos esetben a cryptákban abscessusok láthatókés a kehelysejtek száma csökkent. A gyulladás a toxicus megacolon ritka eseteitől eltekintve, gyakorlatilag soha nem terjed a submucosara, a muscularis rétegre, vagy a serosára. Ezzel szemben Crohn- betegségben inkább krónikus gyulladásos sejtinfiltrátum figyelhető meg, ami a mucosán túlterjed és transmuralis jellegű. A betegségre jellemző lehet a granulomaképződés,deez nem mindig látható, tehát hiánya nem zárja ki a Crohn-betegség diagnózisát. Az eseteknek nagyjából 10%-ában a szövettani kép alapján nem lehetséges a colitis ulcerosa és Crohn- betegség közötti elkülönítés (indeterminált colitis).
Az IBD súlyosságának a megítélése
A 6. táblázat összefoglalja azokat a tüneti és laboratóriumi paramétereket, amelyek alapján a kórkép klinikailag könnyen besorolható enyhe, középsúlyos és súlyos formákba. A besorolásnak nagy jelentősége van a megfelelő terápia beállításában, és annak hatékonyságának objektív megítélésében.
6. táblázat. Az IBD különböző súlyossági formái
| Tünet, vagy laboratóriumi eltérés | Enyhe | Középsúlyos | Súlyos |
| Hasmenés | 0-6/nap | 6-10/nap | 10/napnál több |
| Véres széklet | Ritkán | Rendszeresen | Minden széklet |
| Hasi fájdalom | Enyhe | Középsúlyos | Súlyos |
| Súlyesés | Nincs | 1 kg-nál kisebb | 1 kg-nál több |
| Láz | Nincs | Nincs | >37,5 oC |
| Laboratóriumi leletek Süllyedés Haemoglobin Albumin | Normális Normális Normális | <30 mm/óra >100 g/l >30 g/l | >30 mm/óra <100 g/l <30 g/l |
6. Diferenciál diagnosztika (felhasznált bizonyítékok, azok szintjei)
A gyulladásos bélbetegség elkülönítő kórismézésében elsősorban azenteralis infekciókat fontos elkülöníteni, amiben a széklet bakteriológiai és parazitológiai vizsgálatok nyújtanak fontos segítséget. A szóbajövő kórokozók közül a legfontosabbak: E. Coli, Campylobacter jejuni, Salmonella, Shigella, Entamoeba histolytica, Giardia lamblia, Mycobacterium tuberculosis, és különösen antibiotikummal előkezelt betegekben, Clostridium difficile. Az akut hasi fájdalmakkal járó kórképek közül leggyakrabban az appendicitis, az adnexitis, az invaginatio és a lymphadenitis mesenteralis lehetőségére kell gondolni, elsősorban a Crohn-betegség diagnózisakor. A krónikus hasi fájdalommal járó betegségek közül differenciál diagnosztikai szempontból az irritabilis bél szindróma, az ételallergia, a coeliakia, a húgyúti fertőzésekés a visszatérő hasi fájdalom elkülönítése fontos. A táblázat betegségcsoportokszerint részletezi, hogy a Crohn-betegség és a colitis ulcerosa differenciál diagnosztikája során mely kórképek jönnek inkább szóba (7. táblázat)
7. táblázat. A Crohn-betegség és a colitis ulcerosa differenciáldiagnosztikája
| Elkülönítendő kórkép | Crohn-betegség | Colitis ulcerosa |
| Infekciós kórképek Appendicitis Lymphadenitis mesenterialis Enteritis | ++ ++ ++ | + +++ |
| Vascularis kórképek HUS, Henoch-Schönlein purpura, Behcet betegség, polyarteritis nodosa, SLE, dermatomyositis | + | +++ |
| Immunhiányos állapotok | + | + |
| latrogén (irradiáció, kemoterápia, graft versus host betegség) | + | + |
| Nőgyógyászati kórképek (extrauterin graviditas, ovárium cysta, daganatok, endometriosis) | + | + |
| Allergia (eosinophil gastroenteritis) | + | + |
| Neuromuscularis kórképek (Hirschsprung betegség, pseudo-obstructiós szindróma) | + | ++ |
| Egyéb (Meckel diverticulum, invaginatio, tumor) | + | ++ |
+ Az elkülönítő kórismézésben + előfordul ++ gyakori, +++ igen gyakori
III. Terápia
Az utóbbi évtizedekben jelentősen javultaka gyulladásos bélbetegségek kezelési lehetőségei. Az esetek többségében a gyógyszeres kezeléssel jó eredmény érhető el, de vannak helyzetek, amikor sebészi megoldásra van szükség. A kezeléssel többféle egymásra épülő célt szeretnénk elérni, ezek sorrendben az alábbiak:
- Klinikai javulás
- Remisszió
- Leválasztás a szteroidról, amennyiben adására szükség volt
- A remisszió fenntartása, relapszus megelőzése
- A szöveti gyógyulás elérése
- Gyógyulás
Emellett fontos figyelmet fordítani a helyes táplálásra, a szövődmények kezelésére, valamint a minél jobb életminőség biztosítására.
Nem gyógyszeres kezelés
A kezelésben igen fontos a megfelelő táplálékbevitel, hiszen a különösen Crohn-betegségben megfigyelt gyakori növekedésbeli elmaradás a csekély energia- és proteinbevitel következménye. Speciális colitises diéta nincs. Amíg a beteg szájon át táplálható, az akut szakban is lényegében bármit fogyaszthat. Súlyos esetekben célszerű magas energiatartalmú enteralis tápszerek alkalmazása. Speciális enterális tápláláshoz speciális formulák is alkalmazhatók, amelyek fehérjehidrolizátumokat tartalmaznak, a zsírtartalom jelentős részét pedig MCT fedezi. Újabb vizsgálatok szerint azonban nem bizonyítható az elemi diéta előnye a polimerrel szemben. Ha a megfelelő táplálékbevitel másképpen nem biztosítható, akkor nasogastricus szondatáplálás alkalmazása szükséges, ami pumpa segítségével éjszaka is végezhető. Célszerű, hogy az energiabevitel az átlagos életkori szükséglet 140%-a legyen. A fizikai aktivitást remisszióban nem szükséges korlátozni, sőt javasolt a sok mozgás és a nem versenyszerűen folytatott sportolás is.
III/2. Gyógyszeres kezelés (felhasznált bizonyítékok, azok szintjei)
A 8. táblázat a gyulladásos bélbetegségben rendszeresen használt gyógyszereket és terápiás adagjait mutatja be, míg a 9. táblázat a kezelésben igen elterjedt 5-ASA származékokat csoportosítja a hatáskifejtés módja szerint. Legelőször a sulfasalazint alkalmazták a colont érintő gyulladásos bélbetegségekben, hiszen ebből a vegyületből az aktív hatóanyag, az 5-ASA bakteriális bontás következtében a vastagbélben szabadul fel. A sulfasalazin gyulladásgátló hatásában nem csak az 5-ASA, hanem a sulfapyridin komponens is részt vesz, ami érthetővé teszi, hogy az 5-ASA tartalmú gyógyszereket relatíve magasabb dózisban kell alkalmazni ugyanolyan terápiás hatás eléréséhez, mint a sulfasalazint. Önmagában az 5-ASA már a vékonybél felső szakaszán felszívódna, s ezért nem fejtene ki terápiás hatást. Mára azonban már több olyan szabad 5-ASA tartalmú gyógyszert is kifejlesztettek, amelyekben az aktív hatóanyag speciális összetételű mikrokapszulákban helyezkedik el. Ezekkel az újabb gyógyszerekkel lehetővé vált annak a szabályozása, hogy az 5-ASA melyik bélszakaszon szabaduljon fel. Az 5-ASA származékok antifolátok, alkalmazásuk során a megfelelő folsavellátásról gondoskodni szükséges.
8. táblázat. A gyulladásos bélbetegség kezelésében használt fontosabb gyógyszerek hatóanyagai és dózisai
| Hatóanyag | Dózis |
| 5-ASA | 50-100 mg/kg/nap (maximum 4 g/nap) |
| prednisolon | 1-2 mg/kg/nap (maximum 60 mg) |
| budesonide | 9 mg/nap |
| metronidazol | 10-20 mg/kg/nap |
| azathioprin | 2-3 mg/kg/nap |
| 6-mercaptopurin | 1,5 mg/kg/nap |
| anti-TNFa (Remicade, infliximab) | 5 mg/kg egyszeri adag, amit kettő és újabb négy hét után ismételni kell. |
9. táblázat. Az 5-ASA származékok felosztása
| A hatáskifejtés módja | A hatás fő lokalizációja | Hatóanyagok |
| A diazo kötés bakteriális bontása | Colon | Sulfasalazin (5-ASA és sulfapiridin komponensek) Olsalazin (2 5-ASA diazo kötéssel) Balsalazin (5-ASA és 4-aminobenzo-b-alanin |
| Resinnel fedett szabad 5-ASA, aminek a bomlása pH függő | A vékonybél középső szakasza (pH>5,6) | mesalazin |
| A distalis ileum és a jobb colonfél | mesalazin | |
| Etilcellulóz tartalmú granulumokból a szabad 5-ASA fokozatosan szabadul fel | Az egész vékonybél és a colon | mesalazin |
A betegség aktív szakaszában a leggyorsabb javulás prednisolon adásával érhető el (1 2 mg/ttkg/nap, maximum 60 mg). Súlyos esetben a szteroid intravenásan is adható. Ügyelni kell a szteroid mellékhatásaira. Ulcus megelőzésére gyomorsav-secretiót gátló kezelés javasolt, elengedhetetlen a káliumpótlás is.
Újabban rendelkezésre állnak olyan szteroid származékok is, amelyek szisztémás hatása a rossz felszívódás következtében csekély (beclomethason, budesonid), viszont lokálisan jó hatásúak. Ezek a gyógyszerek colon érintettség esetén klizmában és kúpban is adhatók. Jól alkalmazható a terápiában egy újabb szteroid készítmény, a budesonid. Ennek a vegyületnek az a nagy előnye, hogy a gastrointestinalis tractusból nehezen szívódik fel, de a nyálkahártyára kifejti a hatását. Szteroid dependens esetekben megkísérelhető az azathioprin (2 mg/ttkg/nap) vagy a 6-mercaptopurin (1,5 mg/ttkg/nap) adása.
A 10. táblázat Crohn-betegség különböző lokalizációjában és súlyossági formáiban mutatják a javasolt gyógyszeres kezelést a diagnózis felállítása után.
10. táblázat. A Crohn-betegség gyógyszeres kezelése különböző lokalizációkés súlyosság esetén
| Lokalizácó | Enyhe | Középsúlyos | Súlyos |
| Ileum | 5-ASA per os | prednisolon és 5-ASA per os | prednisolon i.v. és 5-ASA, total parenterális táplálás szükséges lehet |
| (Ileo)colitis Rectosigmoideum is érintett | 5-ASA vagy sulfasalazin per os | prednsiolon és 5-ASA per os Steroid rezisztens, vagy dependens esetekben azathioprin | prednisolon i.v és 5-ASA, teljes parenteralis táplálás szükséges lehet steroid rezisztens, vagy dependens esetekben azathioprin,fistulázó esetben anti-TNF-a |
| Kiegészítés klizmával (budesonid, prednisolon és/vagy 5-ASA) | Kiegészítés klizmával (budesonid, prednisolon és/vagy 5-ASA) | Kiegészítés klizmával (budesonid, prednisolon és/vagy 5-ASA) |
Steroid dependens, vagy rezisztens esetekben azathioprin adása szükséges, fistula képződés és anális érintettség esetén a terápia kiegészítendő metronidazollal, egyéb esetekben is lehet jótékony adjuváns hatása. Gyermekekben is alkalmazható a fenti indikációkban a ciprofloxacin 20 mg/kg/nap dózisban, amit a betegek általában jól tolerálnak. Az anti-TNF-a (infliximab) alkalmazása egyéb terápiára rezisztens esetekben, vagy a Crohn-betegség súlyos fistulaképződéssel járó formáiban indokolt. Az infliximab dózisa 5 mg/kg intravénásan, ezt a dózist az indukciós kezelés során a 0,2. és 6. héten kell alkalmazni. Az infúziós kezelés után négyórás kórházi megfigyelés után bocsátható a beteg otthonába. Amennyiben ez az indukciós kezelés eredményes, akkor a fenntartó terápiát 8 hetes időközökben kell folytatni ugyancsak 5 mg/kg dózisban. Ha az indukciós kezelés eredménytelen, akkor további infliximab kezelés nem indokolt. (Evidencia szint: I, ajánlás erőssége: A) (2)
Az infliximab kezelés mellett többnyire szükséges a korábban bevezetett immunszuppressziós kezelést folytatni. Az infliximab terápiának bizonyos esetekben súlyos szövődményei is lehetnek, amelyeket a kezelés bevezetése előtt mindenképpen figyelembe kell venni. Már a kezelés előtt lehetőség van arra, hogy kiszűrjük azokat a betegeket, akikben az infliximab alkalmazása ellenjavallt, mert fokozott kockázatot jelent.
A kezelés legfontosabb ellenjavallatai az alábbiak:
- Tuberkulózis
- Súlyos egyéb fertőzések (szepszis, tályog és opportunista fertőzések)
- Súlyos passzázs-zavart okozó szűkület
- Malignitásra utaló tünet jelenléte
- Közepes, vagy súlyos fokú szívelégtelenség (New York Heart Association [NYHA] III/IV osztály
11. táblázat. A colitis ulcerosa gyógyszeres terápiás elvei
| Enyhe | Középsúlyos | Súlyos |
| Rectalis 5-ASA tartalmú kúp, vagy klizma Lehet adni per os is sulfasalazint, vagy 5-ASA-t | Rectalis prednisolon és 5-ASA kombinációja Sulfasalazin, vagy 5-ASA per os Fenti terápiára rezisztens esetekben: azathioprin, cyclosporin, antibiotikum | Rectalis prednisolon és 5-ASA kombinációja Sulfasalazin, vagy 5-ASA és prednisolon per os Fenti terápiára rezisztens esetekben: azathioprin, cyclosporin, antibiotikum |
11. táblázat. A colitis ulcerosa gyógyszeres kezelése különböző súlyosság esetén
| Crohn-betegség | Colitis ulcerosa |
| - Sikertelen gyógyszeres kezelés | - Szteroid dependencia és intolerancia az |
| - Vérzés | immunszuppresszív szerek iránt |
| - Fulmináns colitis | - Vérzés |
| - Perforáció | - Toxicus megacolon |
| - Obstructio | - Perforáció |
| - Fistulák | - Növekedésbeli elmaradás |
| - Növekedésbeli elmaradás | - Nagyfokú dysplasia, carcinoma |
| - Nagyfokú dysplasia |
Újabban probiotikumok adását is megkísérelték a gyulladásos bélbetegségek kezelésében. Az eddigi eredmények biztatóak, de még nem áll rendelkezésre elegendő kontrollált vizsgálati adat ahhoz, hogy rutinszerűen alkalmazzuk ezeket a készítményeket a gyulladásos bélbetegségek kezelésében.
Fenntartó kezelésre, recidiva megelőzésére gyermekkorban 1 mg/kg/nap azathioprin, illetve 50 mg/kg/nap 5-ASA adása indokolt.
IN/3. Műtét (felhasznált bizonyítékok, azok szintjei)
Ha a konzervatív kezelés nem vezet eredményre, akkor sebészi megoldás jön szóba. Crohn- betegség esetén azonban az a cél, hogy minél kisebb bélszakasz kerüljön eltávolításra. Sebészi beavatkozás szükséges stricturák, abscessusokés fistulák esetén. Ha a strictura csak kis szakaszokra terjed ki, akkor célszerű a stricturoplastica, amivel a resectio elkerülhető. Colitis ulcerosában a gyógyszeres kezelésre rezisztens formákban, illetve toxicus megacolon esetén indokolt a sebészi megoldás.. Ez általában teljes colectomiát jelent. Az utóbbi időben lehetőség van arra is, hogy a rectumnyálkahártya eltávolítása után a rectumcsonkhoz szájaztassák az ileumot (ileoanostomia), s így legtöbbször a continentia megtartható.
A sebészi indikációkat a 12. táblázat foglalja össze. 12. táblázat Sebészi indikációk
Crohn-betegség • Sikertelen gyógyszeres kezelés • Vérzés • Fulmináns colitis • Perforáció • Obstructio • Fistulák • Növekedésbeli elmaradás • Nagyfokú dysplasia Colitis ulcerosa • Szteroid dependencia és intolerancia az immunszuppresszív szerek iránt • Vérzés • Toxicus megacolon • Perforáció • Növekedésbeli elmaradás • Nagyfokú dysplasia, carcinoma
III/4. Egyéb terápia (pszichoterápia, gyógyfoglalkoztatás stb.)
IV. Rehabilitáció
V. Gondozás
Ebben a betegségben különösen fontos a jó kapcsolat az orvos, a beteg és a szülők között, hiszen ez az alapfeltétele annak, hogy a beteg állapota az elérhető legjobb legyen. A gyulladásos bélbetegség életre szólóan fennálló krónikus kórkép, amit a betegnek igen nehéz elfogadnia. Ezért szükséges a betegek jó pszichés vezetése, adott esetben pszichológus bevonása is indokolt a kezelésbe. A legfontosabb az optimális életminőség biztosítása. Ennek megfelelően kell beállítani a fentiekben tárgyalt módon a gyógyszeres kezelést, illetve adott esetben indikálni a sebészi beavatkozást. A betegség kezdetén a remisszióba kerülés után szoros, akár hetente történő ellenőrzésre van szükség, ami később ritkítható, tünetmentesség esetén elégséges lehet a 2-3 havonta történő kontroll vizsgálat. A helyes gondozással sokszor megelőzhetőek a relapszusok, illetve azokat korábbi stádiumban észlelve és kezelve, hamarabb érhető el remisszió
Dokumentáció, bizonylat
- Az első kivizsgáláskor, valamint súlyosabb relapsusokesetén a kórházi ápolás dokumentumai, zárójelentés, további diagnosztikus és terápiás tervvel
- Rendszeres további gondozás esetén ambulás lap vezetése az aktuális fizikális vizsgálat eredményeiről a vizsgálatokról és terápiáról
VI. Irodalomjegyzék
1. B. Kovács J., Füzesi K.: A krónikus gyulladásos bélbetegségek. In: Gyermek-gasztroenterológia (szerk. Arató A., Szőnyi L.), Medicina, Budapest, 2003. 327-344. old.
2. Hyams J, Crandall W, Kugathasan S, et al. Induction and maintenance infliximab therapy for the treatment of moderate-to-severe Crohn's disease in children. Gastroenterology 2007 132:863-873.
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Gyakori társbetegségek
A 3. táblázat tünteti fel azokat az extraintestinalis manifesztációkat, amelyek önállóan, tehát intestinális tünetek jelentkezése nélkül is jelentkezhetnek.
2. Érintett társszakmákkal való konszenzus
A protokollban ismertetett diagnosztikus és terápiás irányelvek harmonizálnak a belgyógyászok gyakorlatával
Az Egészségügyi Minisztérium
szakmai protokollja
Az epilepsziáról
(1. módosított változat)
Készítette: a Csecsemő- és Gyermekgyógyászati Szakmai Kollégium
I. Alapvető megfontolások Definíció
Epilepsziás roham alatt az idegrendszer rohamszerűen fellépő, átmeneti működészavarát értjük, mely nagytömegű neuron kóros kisülésén alapul.
Ha a jelenséget a rohamkészséget átmenetileg fokozó tényezők provokálják (láz, acut idegrendszeri betegség, mint gyulladás, trauma, görcsre hajlamosító anyagcsere- vagy elektroliteltérések), acut epilepsziás rohamról beszélünk. Epilepszia szindrómának tartjuk, ha az epilepsziás rohamok provokáció nélkül, ismétlődve lépnek fel. Elkülönítendők az epilepsziát utánzó paroxizmális történések (collapsus, affectiv apnoe stb.)
Panaszok, tünetek
Mivel epilepsziás roham az agy számos területéről kiindulhat, a hirtelen fellépő és megszűnő rohamtünetek igen változatosak. Megnyilvánulhatnak motoros, szenzoros, cognitiv, vegetatív és affectiv jelenségekben. A működészavarokfelléphetnek izoláltan, többnyire azonban együtt, vagy a roham alatt egymást követően észlelhetők.
Jelentkezhetnek kiesési tünetek formájában is (tónusvesztés, beszédképtelenség stb.) Az epilepsziás roham többnyire másodpercekig vagy percekig tart, járhat convulsioval vagy anélkül. Ha tartama elhúzódó, beszélünk status epilepticusról.
A rohamok osztályozása:
- Epilepsziás spasmus
- Myoclonus
- Tónusos roham
- Clonusos roham
- Tónusos-clonusos roham
- Atoniás, astaticus
- Absence
- Szenzoros, vegetatív vagy affectiv tünetekkel járó fokális roham
- Komplex parciális roham (tudatbeszűkülés, automatizmusok)
Ha a rohamtünetek jelzik, hogy melyik agyi régió működészavarából erednek, fokális vagy parciális rohamról beszélünk. Generalizált rohamok esetében a roham kezdettől bevonódik mindkét félteke. Gyermekkorban gyakori a szekunder generalizáció, mikor a fokálisan kezdődő epilepsziás roham generalizálódik.
Az epilepszia oka és epidemiológiai jellemzői
Az epilepszia lehet genetikai eredetű és agykárosodás következménye. A genetikai hátterű epilepszia szindrómákat ma az idiopátiás csoportba sorolják, míg az agykárosodból eredő epilepsziákat tünetinek nevezik. A kettő nem különül el minden esetben élesen. Kimutatott, hogy agysérülés után gyakrabban lép fel epilepszia azoknál, akik családjában előfordul ez a betegség, tehát genetikai hajlammal bírnak.
A genetikai háttér felderítése napjainkban folyik. Több mint 20 gén szerepét tételezik fel, vagy bizonyították. Ezek elsősorban az ioncsatornák működését kódolják, illetve a neurotransmittereket szabályozzák. Bár felismertek olyan tünetcsoportokat, melyek monogénes károsodással magyaráznak (például a benignus familiáris neonatalisconvulsiok a feszültség függő K csatornákat kódoló gén mutációja miatt), legtöbb esetben azonban azonos szindróma mögött többféle génkárosodást lehet kimutatni, és az azonos génmutációk heterogén fenotípussal járhatnak. Az agykárosodást követően az epilepszia hosszabb-rövidebb idővel jelentkezik. Az ez idő alatt zajló folyamatot nevezik epileptogenesisnek. Ma azt tételezzük fel, hogy ennek mechanizmusa kóros szinapszisok kialakulása a sérülést követő regeneráció kapcsán.
A gyermekek 1%-a szenved epilepsziában. Az incidencia a csecsemőkortól a serdülőkorig csökken. A két nem egyformán érintett. A kórképjelentőségét emeli, hogy elkülönítendő paroxizmális történések viszont a gyermekek 4,5-5%-ában fordulnak elő.
A kórkép mortalitása gyermekkorban elenyésző. A kiszámíthatatlanul jelentkező, balesetveszélyes és egyes szindrómákban elbutuláshoz vezető rohamok azonban nagymértékben rontják az életminőséget. Mivel ez az életkor az ismeretek megszerzésének, a készségek kifejlesztésénekvalamint a szocializációnakdöntő fontosságú periódusa, a sikeres kezelés, a beteg rohammentesítése és meggyógyítása mentesítheti az egyént és a társadalmat az egész életre kiható rokkantságtól.
Kiváltó és kockázati tényezők (evidencia szint I a)
- Genetikai hajlam
- Perinatális agysérülés (hypoxia, vérzés stb.)
- Az idegrendszer infekciói (intrauterin és postnatális fertőzések)
- Agyi traumák
- Neurometaboliás betegségek
- Bizonyos kromoszóma rendellenességek és szindrómák
- Agydaganatok Rohamprovokáló faktorok
Bár az epilepsziát úgy határozzuk meg, hogy provokálatlan, ismétlődő rohamok jellemzik, az epilepsziás betegeknél kb. 40 rohamprovokáló tényezőt ismerünk. Ezek közül legfontosabb az alvásmegvonás, az alkoholfogyasztás, a rendszertelen gyógyszerszedés, a stressz, a láz.
II. Diagnózis (evidencia szint Ia ill. Ib) Lépései:
- 1. Eldöntendő, hogy epilepszia vagy alkalmi roham
- 2. Ha epilepsziát állapítunk meg, besorolás a megfelelő szindrómába
- 3. A háttérben álló ok meghatározása Eszközei:
1. Anamnézis
Heteroanamnesis felvétele a szülőtől és a roham szemtanúitól. Nagyobb gyermektől autoanamnesis (auratünetek, tudatszint a roham alatt). Kívánatos a rohamtünetek részletes elemzése. Mivel az orvos ezt a legfontosabb tünetet ritkán észleli, hasznos segítség a rohamról otthon készített videofelvétel.
Kikérdezendő: familiaritás, korábbi, agyi sérülést okozó betegségek, manifesztációs kor, a roham fellépésének körülményei, esetleges kiváltó tényezők, kezdeti tünetek, rohamlefolyás, postictális tünetek. Ha többféle roham jelentkezik, valamennyi részletes elemzése szükséges.
2. Fizikális vizsgálat
Belgyógyászati és ideggyógyászati vizsgálat egyéb betegségek kizárására illetve az agykárosodás egyéb jeleinek felismerésére
3. Kötelező diagnosztikai vizsgálatok (Evidencia szint Ia)
a) Laboratóriumi vizsgálatok
Vércukor, elektrolitok a szérumban, az anamnézis függvényében vesefunkciók, szérum ammonia, laktát, piroszőlősav, speciális vizsgálatok neurometaboliás betegség irányában, genetikai (kromoszóma és DNS) vizsgálatok. Gyulladásos idegrendszeri betegség gyanújakor liquorvizsgálat.
b) Képalkotó vizsgálatok (Ib ill. IIa)
A vizsgálatok célja az epileptogén károsodás (góc) kimutatása, adat a csoportbeosztáshoz, a prognózishoz, öröklődő formákban a genetikai tanácsadáshoz. Műtét előtt a megoldás tervezéséhez nélkülözhetetlen. CT csak akut neurológiai kórkép esetén javasolt sürgős kivitelezhetősége miatt, egyébként minden betegnél
MR végzendő. Kivételt csak az idiopátiás generalizált epilepsziák (pl. absence) típusos esetei képeznek, ahol a képalkotó vizsgálatoktól eltekinthetünk. Az epileptogén laesio kimutatására speciális MR-protokollok szükségesek, a rutineljárás sokszor elégtelen.
Csecsemőkorban sürgős vizsgálatként a koponya UH is gyakran informatív.
c) EEG (evidencia szint la)
Rutin EEG 20 perces tartammal, melyben 3 perces hyperventilláció és ritmusos fényinger provokációként kötelező. Ha ennek lelete normális, epilepszia gyanújakor spontán alvásban, ill. alvásmegvonás után ismételjük a vizsgálatot. Törekszünk alvás alatti regisztrálásra, mivel egyes típusokban az alvás alatti tevékenység kórjelző. Normális skalp-EEG nem zárja ki az epilepsziát, és klinikai tünetek nélkül kóros EEG alapján nem diagnosztizálható epilepszia. Ha speciális szempontok merülnek fel, tartós (long-term) regisztrálás, egyidejű roham- és EEG-videoregisztrálás, ictalis, postictalis vizsgálat, poligráfia, speciális elektródák használata lehet szükséges. Műtét előtt szóba jöhet intracranialis elektródák behelyezésével.történő regisztrálás is a rohamkiindulás pontos lokalizációja végett. Az EEG-vizsgálat indikációi:
- epilepszia megállapítása az első roham után;
- típusba soroláskor;
- kezelt betegen rohamszám emelkedésekorvagy típusváltáskor;
- kezelteknél a mentális állapot romlásakor (szubklinikus elektromos rohamok!);
- gyógyszerkihagyás előtt és közben;
- gyógyuláskor állapotrögzítésre.
4. Kiegészítő diagnosztikai vizsgálatok (evidencia szint lla; lib, ill. Ill.) Funkcionális képalkotók
SPECT elvégzése a gyógyszerrezisztens, műtétre váró betegeknél indokolt. lnterictalisan hipoperfúzió, ictalisan hiperperfúzió látható a kóros kérgi területen. Csak az ictális SPECT lokalizációs értékű. Az interictalis PET ugyanezen régióban a glükózanyagcsere csökkenését mutatja. PET-nél az interictális felvétel is informatív. Angiográfia
Az MR-angiográfia sokszor csak tájékozódó jellegű, azaz érmalformáció gyanúja esetén ki kell egészíteni DSA-val. Funkcionális MR: műtét előtt egyes funkciók, elsősorban a beszéd lokalizációjának meghatározását segíti. MR spectographia: Neurometaboliás betegségek gyanújakorés gócmeghatározásra indokolt Neuropszichológiai vizsgálat
Műtét előtt a kivizsgálás fontos eleme. Memória- és lebenyfunkciók mérésére szolgál. Alkalmas a memória, illetve a beszéd oldallokalizációjának megállapítására.
Pszichológiai és gyógypedagógiai vizsgálat (evidencia szint lll.)
Memóriazavar, depresszió, mentális retardáció, személyiségtorzulás az epilepsziásoknál gyakoribb. Ezek felmérése, szükség szerint, a gyermek megfelelő fejlesztése és a család gondozása, a prognózis javítása szempontjából nélkülözhetetlen.
5. Differenciális diagnosztika (evidencia szint la) Eldöntendő, hogy epilepszia vagy alkalmi roham Figyelembe vesszük:
- a roham keletkezésének körülményeit;
- lefolyását;
- a kiváltó tényezőket;
- a családi anamnézist (genetikus formák!);
- a postictalis tüneteket;
- van-e agykárosodásra utaló egyéb jel (pl. cerebralparesis);
- az EEG-leletet;
- a laboratóriumi értékeket.
6. Diagnosztikai algoritmusok
Az első roham után kötelező: (evidencia szint Ia)
- Részletes családi és a perinatalis/postnatalis betegségekre kiterjedő anamnézis.
- A rohammal kapcsolatos adatok pontos kikérdezése lehetőleg szemtanútól.
- Gondos bel- és ideggyógyászati vizsgálat.
- Laboratóriumi vizsgálatok
- Rutin EEG-vizsgálat
Epilepszia diagnózisakor besorolás a megfelelő szindrómába (evidencia szint IIa)
Jelenleg az 1989-es ILEA-klasszifikáció érvényes, amely részben az etiologiát veszi figyelembe (idiopátiás és tüneti formák), részben pedig azt, hogy a roham indulásába az egész agy (generalizált), vagy annak csak egy régiója vonódik be (fokális vagy parciális epilepsziák). A klasszifikáció ma már sok pontban vitatható. A betegek 20-30%-a nem osztható be a típusokba. Generalizált epilepsziák
1. Idiopátiás formák életkorfüggő kezdettel
1.1. Neonatalis idiopátiás konvulziók
1.1.2. Benignus familiáris újszülöttkori rohamok
1.1.3. Ötödik napos rohamok
1.2. Csecsemőkori benignus myoclonus epilepszia
1.3. Kisgyermekkori absence epilepszia
1.4. Serdülőkori absence epilepszia
1.5. Juvenilis benignus myoclonus epilepszia
1.6. Ébredési grand mal epilepszia
1.7. Egyéb, generalizált tónusos-clonusos rohammal járó epilepsziák
2. Tüneti vagy kriptogén generalizált epilepsziák 2.1 West-szindróma
2.2. Lennox-Gastaut-szindróma
2.3. Epilepszia myoclonusos asztatikus rohamokkal
2.4. Epilepszia myoclonusos absence-okkal
2.5. Korai myoclonusos encephalopathia
2.6. Korai csecsemőkori encephalopathia (Ohtahara-szindróma) Parciális vagy fokális epilepsziák
1. Idiopátiás parciális epilepsziák
1.1. Benignus gyermekkori epilepszia centrotemporalis tüskékkel
1.2. Benignus gyermekkori occipitalis epilepszia
1.3. Egyéb benignus gyermekkori fokális epilepsziák
2. Tüneti parciális epilepsziák
Frontális, parietalis, occipitalis, temporalis lebenyepilepsziák
Epilepsziák, melyekről nem lehet meghatározni, hogy generalizáltak vagy fokálisak
1. Súlyos csecsemőkori myoclonus epilepszia
2. Epilepszia folyamatos tüskehullám-mintával alvás alatt (ESES)
3. Szerzett epilepsziás afázia (Landau-Kleffner-szindróma)
4. Tüneti epilepsziák generalizált rohamokkal Speciális epilepsziaszindrómák Szituációhoz kötött görcsök
Stimulus szenzitív epilepsziák
(Az egyes típusok diagnosztikai kritériumait illetően a szakirodalomra utalunk.) A típusba sorolásnál figyelembe vesszük
- Anamnézis: rohamtípus (-ok), manifesztációs kor, egyéb társuló tünet, etiológia
- EEG kép
III. Kezelés
Cél: a rohamok megszüntetése, az epilepszia progressziójának kivédése, az életminőség javítása
A) NEM GYÓGYSZERES KEZELÉS (evidencia szint III és IV, ajánlás B,CésD)
1. A megfelelő egészségügyi ellátás szintje
A diagnózis felállítása, a gyógyszeres kezelés és az életvezetés gyermekideggyógyász feladata, meghaladja a gyermekorvos kompetenciáját. A betegek jelentős részében a diagnózis felállítása illetve a kezelés ambulanter is elvégezhető. Acut (azaz más betegséghez csatlakozó) epilepsziás rohamok, valamint gyakori rohamok és status epilepticus esetében, illetve mütét előtti kivizsgáláskor az intézeti bentfekvés nélkülözhetetlen.
2. Általános intézkedések
A szociálisan hátrányos helyzetű, gyógyszer rezisztens vagy halmozottan sérült epilepsziás gyermek szülei a meglévő rendelkezések értelmében emelt családi pótlékra , GYES meghosszabbításra jogosultak
3. Fizikai aktivitás (ajánlás D)
Epilepsziában nem ártalmas, testnevelés alóli felmentés ritkán indokolt. Tiltandó viszont a vízben a felügyelet nélküli tevékenység.
4. Diéta (ajánlás B, C)
Gyógyszer rezisztens betegek mind nagyobb hányadánál jön szóba add-on terápiaként a ketogén diéta alkalmazása, különös tekintettel a csecsemő és kisgyermekkorra. Egyébként gyermekkori epilepszia esetében a diétás megszorítás nem indokolt.
5. neuromodulációs eljárások
Gyógyszer rezisztens és műtéti kezelésre nem alkalmas betegek esetében gyermekkorban is eredményes lehet a vagus ideg stimulációs eljárás (VNS - terápia) alkalmazása.
6. Betegoktatás
Nagyjelentőségű és nélkülözhetetlen, hiszen a betegség tartósan (akár élethossziglan) fennáll, és életmódi korlátokat eredményez. Így a copping stratégia, azaz a betegséggel együttélés szabályainak kialakítása nélkülözhetetlen. Ez megköveteli a pontos ismereteket a kórképről.
B) GYÓGYSZERES KEZELÉS (evidencia szint Ia; Ib)
1. Ajánlott gyógyszeres kezelés és terápiás algoritmus (ajánlás A)
Beállítás: az 1. roham után antiepileptikum beállítása nem kötelező. Kezdjük el azonban a kezelést, ha epilepszia mellett szól az EEG-ben megfigyelhető paroxizmális tevékenység, továbbá ha az epilepszia klasszifikációja egyértelmű, és ha a roham hosszú tartamú volt. Ha nem alkalmazunk gyógyszert, ellátjuk a szülőt rectalis diazepammal, hogy a roham ismétlődése esetén elsősegélyt tudjon nyújtani. Megbeszéljük vele a fokozott megfigyelést és az életmód korlátjait (vízben felügyelet nélkül nem tartózkodhat a gyermek!). Epilepszia esetén a rohamok többnyire egy éven belül kiújulnak. Ha gyógyszerbeállítás mellett döntünk, alapelv a célzott monoterápia. Tehát egy gyógyszert válasszunk, azt ami a tapasztalat szerint az epilepszia meghatározott típusában a leghatásosabb. Generalizált epilepsziáknál a valproat az első választandó szer, fokális epilepsziák esetében a carbamazepin. Kivétel a Lennox-Gastaut-szindróma, ahol a társuló több rohamtípus mindig gyógyszer-kombinációt tesz szükségessé, ezért többnyire valproattal és lamotriginnel indulunk. West szindrómánál az első választandó szer a gamma-vinil-GABA. A gyógyszerbeállítás a mellékhatások elkerülése végett fokozatosan emelkedő dózisban történik. A gyógyszerdózis napi osztása a szer felezési idejétől függ. A valproat- és a retardált felszívódású carbamazepin készítmények naponta egyszer is adhatók, azonban ezeket is többnyire naponta kétszer javasoljuk osztani (az elfelejtés veszélye kisebb!). Vannak szerek (lamotrigin,abapentin), melyek rövid felezési idejűek. A dózist a testsúly szerint á biztosítja-e az adag a hatásos szérumszintet.
2. Teendők a rohamok ismétlődése esetén (ajánlás A)
- Vérszintet ellenőrzünk, így kiszűrhető a compliance hiánya, vagy az elégtelen gyógyszeradag.
- Ha a szint alacsony, dózist emelünk.
- Újragondoljuk a típusba sorolást, esetleg tévedtünk, és rossz gyógyszert választottunk. Emiatt EEG-t végzünk.
- Ha az előzők nem oldják meg a problémát, gyógyszert váltunk. A váltás csak fokozatosan hajtható végre.
- Eredménytelenség esetén kombináljuk a gyógyszereket. Figyelembe vesszük a racionális politerápia szabályait: additív hatású, de eltérő mellékhatású szereket kombinálunk. Figyelembe vesszük a gyógyszerinterakciókat is. - Legtöbbször két szer alkalmazása hatásos, háromnál több általában már nem javítja a hatást.
- Egyes katasztrofális formákban aspecifikus szerek is kipróbálandók (ACTH vagy szteroid, illetve IVIG West- és Lennox-Gastaut-szindrómában).
Az antiepileptikum-szérumszint meghatározásának indikációi (ajánlás B)
- Bázisérték meghatározása a gyógyszerbeállítás után (ajánlott, de nem feltétlenül szükséges).
- Rohamok kiújulása.
- Dózisfüggő mellékhatás gyanúja.
- Biológiai változáskor (máj-, vesegyulladás, terhesség stb.).
- Politerápiában az interakciók miatt.
A vérvétel ideje a gyógyszertől függ. Retard készítménynél gyakorlatilag egész nap azonos a szint, egyébként völgyszintet nézünk a reggeli gyógyszerbevétel előtt, és csúcsszintet 2 vagy 3 óra múlva. Fontos tudni, hogy a hatásos sávot statisztikai úton állapították meg, individuálisan ennél alacsonyabb vagy magasabb szint is hatásos lehet egyes betegeknél.
A gyógyszeres kezelés tartama (evidencia szint IIa; IIb, ajánlás B ill C)
Individuálisan döntendő el. Legrövidebb a 2 rohammentes év, többnyire azonban 3 évet tartunk kívánatosnak. Egyes szindrómákban nem megengedett a gyógyszerszedés leállítása. A gyógyszerkihagyás fokozatosan, lassan (hónapok alatt) és folyamatos ellenőrzés mellett történik.
a) Kontraindikációk (ajánlás B)
Bizonyos betegségekés biológiai állapotokesetén egyes antiepileptikumok kerülendők. (terhesség alatt valproat stb.)
b) Lehetséges jelentős interakciók (ajánlás C)
Az antiepileptikumok jelentős része enziminduktor. Ezért csecsemőkorban mellettük magasabb D vitamin adag szükséges. Az antibiotikumok közül főleg a makrolidekkel interaktívak. Kombinált antiepileptikus kezelésnél mindig figyelembe kell venni az antiepileptikumok interakcióját is.
C) SEBÉSZETI KEZELÉS (evidencia szint IIa; IIb, ill. III.)
A betegek 15-20%-a rezisztens a gyógyszeres kezelésre. Ezek egynegyedében szóba jön a műtéti megoldás. Elsősorban a temporalis és frontális lebenyből kiinduló, valamint a "katasztrofális" gyermekkori epilepsziák esetében kell műtétre gondolni. Minden kezelésbe vett, a fenti csoportba sorolható betegnél mérlegelni kell ezt a lehetőséget már a terápia első 2-4 évében, West-szindrómánál még előbb. Az MR által kimutatott laesio esetén elektrofiziológiai eszközökkel is igazolni kell, hogy ez a terület az epilepszia forrása
1. Műtéti indikáció (ajánlás A, illetve B)
- Gyógyszer-rezisztencia (kipróbálva minimálisan kettő adekvát gyógyszeres terápiás opciót)
- A beteg életminősége rossz.
- Az epileptogén zóna meghatározható.
- A műtét várhatóan nem okoz neurológiai deficittüneteket.
2. Műtéti előkészítés (ajánlás A)
A helyes lokalizáció nélkülözhetetlen feltétele az eredményes beavatkozásnak, ezért a műtét előtti kivizsgáláskor minden szükséges diagnosztikai eszköz igénybevétele indokolt. (MR, funkcionális képalkotók, rohamelemzés videoEEG-vel, neuropszichiátria stb.)
3. Műtéti érzéstelenítés (ajánlás B) Szokásos anaesthesia
4. Műtét (ajánlás B)
Célja az epileptogén zóna eltávolítása, vagy összeköttetéseinek megszakítása. Ha az epileptogén laesio kiterjedt, de fél oldalra lokalizálódik, funkcionális hemispherotomia végzendő.
5. Posztoperatív teendők
Abeteg további epileptológiai gondozása,a rohammentesség elérésekor azantiepileptikumokfokozatoskihagyása,a beteg rehabilitációja, az esetleges (többnyire cognitiv vagy pszichés, esetleg motoros) szövődmények kezelése
IV. Rehabilitáció
1. Rehabilitáció (ajánlás D)
Az epilepsziás gyermekek egy része az agyi károsodás egyéb tüneteiben is szenved (cerebrális paresis, mentális retardáció, tanulási nehézségek, magatartási zavarok). Ezek felismerése, felmérése és kezelése is kívánatos és szükséges a roham mentesítés mellett. Különösen fontos ez a katasztrófális gyermekkori epilepsziás encephalopathiákban, melyek a rohamok mellett elbutulással is járnak.
V. Gondozás (evidencia szint IIb, ill. III., IV)
1. Rendszeres ellenőrzés (ajánlás C)
Mint minden krónikus betegségnél, az epilepszia esetében is nélkülözhetetlen, hogy a gyógyulásig a beteg folyamatos orvosi felügyelet alatt álljon. Célszerű, ha az időszakos ellenőrzést ugyanaz az orvos végzi. Kívánatos, hogy az ellenőrzés jól lévő beteg esetében is negyedévenként megtörténjen.
2. A gondozás célja: (ajánlás C) Az optimális gyógyszerbeállítás
Szerencsés esetben a beteg már az első beállított gyógyszerrel panaszmentes, sokszor szükséges azonban a dózis vagy a gyógyszer módosítása.
a. A beteg életvezetésének irányítása
Az epilepszia diagnózisa kezdetben még a jó prognózisú esetekben is súlyos pszichés teher a szülő, illetve a betegséget már érzékelni tudó gyermek számára. Számtalan kérdés merül fel a helyes életvezetés, a prognózis, a kiváltó ok, az öröklődés stb. szempontjából. Ezek megválaszolása javítja a compliance-t, ellene hat a "túlvédésnek" vagy a betegség alábecsülésének, ezzel javítja a szociális prognózist. Ha magatartászavar vagy értelmi probléma is társul, a gondozó orvos ezek lehetséges megoldásáért is felelős.
b. Szakértés
Továbbtanulás, pályaválasztás, vezetői jogosítvány stb. ügyében reális véleményt az az orvos tud adni, aki a gyermek betegségét folyamatosan végigkísérte.
c. A gyógyszermellékhatások figyelése
A gyógyszermellékhatások lehetnek idioszinkráziásak, azaz kiszámíthatatlanok (pl. Reye-like-szindróma a valproat esetében), allergiásak (bőrkiütés Lamictalra, Diphedanra) teratogének (velőcső-záródási rendellenességek) és toxikusak. Utóbbiak sokszor dózisfüggőek, így vérszint-meghatározást indikálnak. Lehetnek akut toxikus tünetek (szédülés, aluszékonyság), vagya károsodások krónikus szedés után alakulnak ki (polycystás ovárium valproat szedésekor stb.). Érinthetik a központi idegrendszert, a csontvelőt, a májat, az immun-, az endokrin-, a csontrendszert stb. A beteget kezelő orvosnak ezeket figyelnie és laboratóriumi vizsgálatokkal ellenőriznie kell.
d. Gyógyszerkihagyás
A beteget folyamatosan követő gondozó orvos hivatott annakeldöntésére, mikor és milyen ütemben hajtható végre az antiepileptikum kihagyása.
3. Feladatok az ellátás különböző szintjein (ajánlás B)
Körzeti gyermekorvos
- Roham esetén elsősegélynyújtás.
- Küldje gyermekideggyógyászhoz a beteget
- A diagnózis birtokában segítse a compliance kialakulását (felvilágosítás, gyógyszerfelírás)
- Együttműködjön a gondozó orvossal (védőoltások, beiskolázás, pályaválasztás, sport stb.).
- Védje a betegét a társadalmi diszkriminációtól! Szakrendelés, ambuláns ellátás
Ideális az állandó gondozó orvos, aki gyermekideggyógyász legyen. Végezze el a diagnosztika, gyógyszeres kezelés és a gondozás korábban ismertetett feladatait Kórházi ellátás
Krízisállapotok megoldása (halmozott rohamok, status epilepticus) csak intézetben történhet. Kórházi kivizsgálást igényel minden katasztrófális gyermekkori epilepszia. Mivel a betegek jó részét roham esetén mentővel intézetbe szállítják, az első kivizsgálás is többnyire ott történik. Speciális centrumok
A gyógyszerrezisztens betegek gyógyszerbeállítása, a műtétre alkalmasak kiválasztása és a műtét előtti kivizsgálás olyan intézetben javasolt, ahol annak személyi és tárgyi feltételei adottak.
4. Megelőzés (evidencia szint IV.)
Ma az epileptogenesist gátló gyógyszerrel még nem rendelkezünk. Ismereteink a genetikus formákban nem elégségesek a prenatális diagnosztikára sem, ami egyébként csak a ritka, súlyos formákban lenne indokolt. Tehát a megfelelő kezeléssel csak a gyakori rohamok illetve az epilepsziás encephalopathia okozta szekunder károsodások megelőzésére törekedhetünk. Az életvezetéssel el kell érnünk, hogy azok a gyermekek, akik várhatóan meggyógyulnak, a diszkrimináció vagy helytelen szülői attitüd miatt ne kerüljenek képességeik kibontását gátló hátrányos helyzetbe.
5. Lehetséges szövődmények
5.1. Status epilepticus (ajánlás B)
Convulsiv formája ma is életveszélyes állapot, a nonconvulsiv forma tartós fentállása pedig elbutuláshoz vezet. Kezelése intézetben történjen. Az induló státusban diazepámot alkalmazunk rectálisan vagy vénásan. Újabban a buccalis midazolam is elterjedőben van. Prolongált státusban fontos a supportív kezelés. Második szerként a phenytoint javasolják iv. Rezisztens státusban általános anaesthesiát alkalmazunk.
5.2. Epilepsziás encephalopathia (ajánlás C, illetve D)
Bizonyos, katasztrófális gyermekkori epilepsziák velejárója jellegzetes EEG mintával. Ha 3 hónap alatt nem sikerül megszüntetni, tartós mentális károsodást okoz. Kezelésére ACTH-t, steroidot, iv. gammaglobulint ill. ketogén diétát alkalmazunk.
6. A kezelés időtartama, prognózis (ajánlás B)
Ma a gyermekek 75-80%-a a tartós (2-5 éves) gyógyszerszedés után meggyógyul, és még kb. 5%-uk ezen felül is rohammentessé tehető, de a gyógyszerek szedése náluk nem hagyható abba.
7. Az ellátás megfelelőségének indikátorai (ajánlás B ill. C) Gyógyulási ráta, rohammentesség, rohamszám csökkenés Szociális beilleszkedés (iskolázottság, munkavállalás, családalapítás)
8. Gyakori társbetegségek
Cerebrális paresis, mentális károsodottság, érzékszervi fogyatékosság, magatartási zavar, tanulási nehézségek
9. Érintett társszakmák
Gyermekgyógyászat, gyermekpszichiatria, neurológia, neuroradiologia, genetika
10. Korfüggő tényezők
a) Gyermekkor-ban gyakoribb, jobb prognózisú, de egyes típusokban tanulási nehézségek, a képzettség akadályozottsága miatt az egész életre kiható hátrány, a katasztrófális formákban súlyos elbutulás
b) Időskor : Gyakoribb
c) Egyéb
Terhesség. Az antiepileptikumok teratogén hatásával számolni kell. Az újszülött kapjon K vitamint. Szophat.
11. Kapcsolódó internetes oldalak
Minden keresőprogram bőségesen tartalmaz a témához kapcsolódó cikkeket
VI. Irodalomjegyzék
1. Kálmánchey R (szerk) Gyermekideggyógyászat, Medicina, Bp. 2000.
2. György llona: A gyermekkori epilepszia diagnosztikus és terápiás kérdései Orvosi Hetilap. 2005. megjelenés alatt
3. György llona: A gyermekkori epilepszia gyógyszeres kezelése Gyermekgyógyászati Továbbképzés 2004
4. Engel J: A proposed diagnostic scheme for people with epileptic seizures and with epilepsy: report of the lLAE task force on classification and terminology. Epilepsia 2004,42:796-803.
5. Rosenow F, Lüders H.: Presurgical evaluation of epilepsy. Brain 2001,124:1683-1700.
6. Hahn A, Pistoh J, Neubauer BA, Stephani U.: Atypical "benign" partial epilepsy or Pseudo-Lennox syndrome. Part l. Symptomatology and long-term prognosis. Neuropeadiatrics 2001,32:1-8.
7. Doose H, Neubauer BA, Petersen B: The concept of hereditary impairment of brain maturation. Epileptic Disorders 200 2(Suppl. 1): 45-49.
8. Haverkamp F, Hanisch C, Mayer H, Noeker M: Evidence of a specific vulnerability for deficient sequential cognitive information processing in epilepsy. J Child Neurol 2001.16: 901-905.
9. Rating D,Schneble H.: Statement of the Königsteiner working group on epileptologyon the new antiepileptic drugs .Z. Epileptol 2004; 17:215-230.
10. Korinthenberg R.: Epilepsies with primary generalized tonic-clonic seizures in adolescents and adults. ls valproic acid or lamotrigin the drug of first choice? Z Epileptol 2005; 18:7-14.
11. Bourgeois BF: Chronic management of seizures in the syndromes of idiopathic generalized epilepsy. Epilepsia 2003, 44(Suppl 2) S27-32.
12. Gil-Nagel A: Review of new antiepileptic drugs as initial therapy. Epilepsia 2003,44(Suppl 4) 3-10.
13. Kwan P, Brodie MJ: Early identification of refractory epilepsy N. Engl J Med 2000 342:314-319.
14. Schmidt D: The clinical impact of new antiepileptic drugs after a decade of use in epilepsy. Epilepsy Res 2002,50:21-32.
15. Kloss S, PieperT, Pannek H., Holthausen H, Tuxhorn l.: Epilepsy surgery in children with focal cortical dysplasia (FCD): results of long-term seizure outcome. Neuropediatrics 2002,33:21-26.
16. Neal GE, Chaffe H, Schwartz RH, et al.: The ketogenic diet for the treatment ofr childhood epilepsy: a randomised controlled trial. Lancet Neurol 2008;7:500-506
A szakmai protokoll érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai protokollja
Az egészséges csecsemő táplálásáról
(1. módosított változat)
Készítette: a Csecsemő- és Gyermekgyógyászati Szakmai Kollégium és a Szoptatást Támogató Nemzeti Bizottság
Tartalomjegyzék
A protokoll átdolgozásának célja Bevezetés
Csecsemőkés kisdedek táplálása - standard ajánlásokaz Európai Unio számára (kivonat)
A csecsemőtáplálás definíciói
Az anyatej összetétele és kalóriatartalma
A szoptatás/anyatejes táplálás jótékony hatásai
A csecsemő fejlődése
A szopás mennyisége
Szoptatás és sárgaság
Szoptatás és vitamin szupplementáció
A szoptató anya étrendje
A szoptatás - anyai betegségek és állapotok
A szoptatás kontraindikációi
Táplálás 0-6 hónapos korban
Szoptatás kiegészítő táplálással
Mesterséges/vegyes táplálás
- Hozzátáplálás/Kiegészítő táplálás/ Elválasztás
- Szolidok/szemiszolidok bevezetése
A tápszerek felosztása
- Anyatej-helyettesítő tápszerek
- Anyatej-kiegészítő (követő, elválasztási) tápszerek
- Speciális tápszerek
Mellékletek
1. A Sikeres Szoptatáshoz vezető 10 lépés
2. A Szoptatás gyakorlata
3. Szoptatás és gyógyszerek
Irodalom
A protokoll átdolgozásának célja: a témával kapcsolatos újismeretek alapján szükséges módosítások, valamint a szoptatással kapcsolatos kérdések bővebb ismertetése a gyermekgyógyászok és a védőnők egységes gondolkodásának segítése érdekében.
Bevezetés
A protokoll az érett, egészséges csecsemő táplálásával foglalkozik. A koraszülött táplálék igénye lényegesen különbözik az időre született, egészséges újszülöttétől - ezért erre nem térünk ki.
A megfelelő táplálás alapvető fontosságú a gyorsan növekvő és fejlődő szervezet számára.
Az egészséges csecsemőnek az első 6 hónapban a kizárólagos szoptatás/anyatejes táplálás, azt követően legalább 12 hónapos korig a 6 hónapos kor körül elkezdett megfelelő kiegészítő táplálás mellett folytatott szoptatás az ideális táplálási mód és a biológiai norma. A legtöbb nemzetközi szakmai szervezet javasolja, hogy a szoptatást folytassák, amíg azt az anya és a gyermek kívánja (1-5).
Az anyák 98%-a képes lenne szoptatni gyermekét, ha megfelelő ismeretekkel, önbizalommal rendelkezne, továbbá, ha megkapná a szükséges segítséget és támogatást az egészségügyi rendszeren belül és kívül egyaránt.
A WHO/UNICEF és nemzetközi szakmai grémiumok arra szólítanak fel, hogy az egészségügyi dolgozók segítsék elő, támogassák és védjék a szoptatást, amit az indokol, hogy a mesterséges táplálással való összehasonlításban a csecsemő fejlődése, az anya és a csecsemő betegségek elleni védelme és az anya-gyermek párosnál észlelt pozitiv hatása bizonyított (2,4).
A 6 hónapos korig folytatott kizárólagos szoptatás a referencia, melyhez valamennyi ettől eltérő táplálási módok mérendők a növekedésre, egészségre, fejlődésre és egyéb rövid és hosszútávú hatásokra vonatkozóan (4). A gyermekgyógyászok és a védőnők szoptatás-támogatásban betöltött szerepe lényegbevágó a csecsemők és gyermekek optimális egészsége, növekedése és fejlődése szempontjából. Hatékony támogatásukhoz azonban elengedhetetlenek az elméleti és gyakorlati ismeretek (4).
A szoptatás sikerében a szakma pozitív tevékenységén túl nagy szerepe van a család, a társadalom támogatásánakés a szoptatást támogató jogalkotásnak.
Csecsemőkés kisdedek táplálása - standard ajánlásokaz Európai Unió számára (2) (kivonat)
- A szoptatáshoz való jogot tisztelni és védelmezni kell és ebben segíteni a családokat, azonban az anya nem köteles szoptatni, és ha a kellő információ birtokában úgy dönt, hogy nem kíván szoptatni ill.nem kívánja folytatni a szoptatást, ugyanannyira helytelen túlzott nyomást gyakorolni rá a szoptatás érdekében, mint a tápszeres táplálás vonatkozásában.
- A várandós nőt és leendő apát el kell látni bizonyítékokon alapuló objektív (kereskedelmi érdekektől független) ismeretekkel a csecsemő táplálására vonatkozóan, hogy döntésüket a megfelelő tudás birtokában hozzák meg.
- Mindazon anyákat, akik szoptatni kívánnak, támogatni kell, hogy elkezdjék a szoptatást, 6 hónapos korig kizárólag szoptassanak, majd a megfelelő kiegészítő táplálás mellett folytassák a szoptatást 2 éves korig és azon túl, vagy ameddig ezt az anya és gyermek kívánják.
- Az optimális táplálás érdekében speciális támogatásban kell részesíteni a hátrányos helyzetű egyéneket, csoportokat és közösségeket.
- Mivel nincs bizonyíték arra, hogy a tápszer magasabb vagy egyenlő értékű az anyatejjel, az egészségügyi dolgozók ne ajánlják ezt a szoptatás helyett ill. kiegészítésére, hacsak ennek nincs orvosi javallata.
- Valamennyi várandós nővel ismertetni kell az optimális táplálás módját szülésfelkészítő tanfolyamon, a várandós ambulancián és a szülés után.
- Támogatni kell a dolgozó anyákat, hogy folytathassák a szoptatást.
- Mielőtt a csecsemő eléri a 6 hónapos kort, valamennyi szülő kapjon felvilágosítást és tanácsot arra vonatkozóan, hogy mi a megfelelő kiegészítő táplálék és mikor és hogyan kell ezeket bevezetni a csecsemő étrendjébe.
- 6 hónapos kor körül valamennyi szülőnek tanácsot kell adni, hogy vezesse be a kiegészítő táplálékot és fokozatosan növelje gyakoriságát és változatosságát, kerülve a cukros és alacsony tápértékü italok adását.
- Valamennyi kórház, szülészeti intézmény és területi ellátó egység adaptálja és valósítsa meg a hatékony szoptatás-támogató stratégiákat, melyek a "Bababarát Kórház Kezdeményezés"-ben foglaltak.
- Valamennyi egészségügyi és egyéb, anyákkal, csecsemőkkel és kisdedekkel foglalkozó dolgozó kapjon megfelelő képzést az irányelvek alkalmazására.
- Valamennyi egészségügy és egyéb, anyákkal, csecsemőkkel és kisdedekkel foglalkozó dolgozó kövesse a Nemzetközi Kódex előírásait.
- Legyen együttműködés az egészségügyi dolgozók, szoptatási tanácsadók, egyéb, az ellátásban résztvevők és a támogató csoportok között
- A média úgy mutassa be a szoptatást és megfelelő kiegészítő táplálást, mint a csecsemő és kisded normális, természetes és optimális táplálási módját
- Történjen széleskörű és pontos adatgyüjtés a szoptatási mutatókról, standard definíciók és módszerek alkalmazásával.
Csecsemőtáplálás definíciói (3,6)
A WHO definíció a csecsemőtáplálás módját a szoptatás /anyatejes táplálás szempontjából határozza meg.
Kizárólagos szoptatás (exclusive breastfeeding): a csecsemő anyatejet- beleértve a saját anya lefejt tejét és idegen női tejet- kap. Ez a definíció megengedi a vitaminok, ásványi anyagok, és gyógyszerek csepp és szirup formában történő adását, de ezen kívül semmi mást.
Túlnyomó szoptatás (predominant breastfeeding): a kizárólagos szoptatás definiciótól abban különbözik, hogy a vitaminok, ásványi anyagokés gyógyszerekcsepp és szirup formában történő adásán túl folyadék (víz, víz-alapú italok, gyümölcslé, orális rehidráló folyadék) adását is megengedi, de ezen kívül semmi egyebet (nem-humán tejek, tápszer, étel alapú folyadékok).
Ez a definíció fedi a "szoptatás folyadék kiegészítéssel" fogalmát.
Szoptatás kiegészítő táplálással (breastfeeding with complementary foods): anyatejmellett minden egyéb: szolidok (az anyatejen és tápszeren kívüli ételek) vagy nem-humán tejés tápszer adása. Ez a definició nem tesz különbséget olyan táplálási módok között, amikor az anyatejen kívül csak tápszert, csak nem-humán tejet, csak szilárd és pépes ételeket vagy ezeket különböző kombinációban vagy arányban alkalmazzák. Ugyancsak nem veszi figyelembe, hogy a 24 órás táplálékban milyen az anyatej aránya. Ez a definíció fedi a kevert táplálás fogalmát.
Nem-szoptatás (non-breastfeeding/bottle-feeding): bármely étel vagy folyadék- beleértve a nem-humán tejet és
tápszert - anyatej ill. idegen női tej nélkül.
Ez a definíció fedi a mesterséges táplálás fogalmát.
Teljes szoptatás (full breastfeeding): ez a fogalom magába foglalja a kizárólagos és túlnyomó szoptatást.
Az ESPGHAN a Kiegészítő táplálás (hozzátáplálás, complementary feeding) szempontjából definiál. Ebből az aspektusból a "kiegészítő táplálás" magában foglal valamennyi szolid és folyékony táplálékot, ami nem anyatej, tápszer vagy követő tápszer.
Az anyatej összetétele és kalóriatartalma (7,8)
Az anyatejnemcsak összetételében, hanem kalória tartalmában is biztosítja az optimális fejlődést. Az anyatejolyan összetevők elegye, melyek biztosítják az energia és tápanyag (zsírok, laktóz, fehérjék) bevitelt, tartalmaznak a fejlődésben (pl.LCPUFA, növekedési faktorok, citokinek,oligoszacharidok, enzimek) és a védelemben (szekretoros IgA, lizozim, laktoferrin stb) szerepet játszó faktorokat. A tej több komponense multifunkcionális, egyidejűleg nutritívés protektív (pl. alfa-laktalbumin, kazein és laktoferrin).
Összetételében változik; a laktáció stádiumától, a napszaktól (zsírtartalma az esti órákban magasabb), az előző szopás óta eltelt időtől, az előző szopás alkalmával elfogyasztott mennyiségtől függően és ugyanazon szoptatáson belül is.
Colostrum-átmeneti tej-érett női tej
A colostrum (előtej) az emlőmirigyek által a várandósság idején és a születés utáni első élethéten termelt sárgás, sűrű alkalikus folyadék. Nagy mennyiségű immunglobulint, az érett anyatejnél több fehérjét, zsírban oldódó vitamint és ásványi anyagot, valamint kevesebb zsírt és szénhidrátot tartalmaz. Jelentős szerepe van a bélcsatorna születés utáni adaptációjában és véd az infekciókkal szemben. Mellette sem folyadék, sem tápszer kiegészítésre nincs szükség. Az átmeneti teja szülés után 7-10 naptól a 2. élethétig termelődik, átmenetet képezve a colostrum és az érett anyatej között. Az átmeneti tej immunglobulin, fehérje és zsírban oldódó vitamin tartalma kisebb, míg a zsír-, laktóz-, vízben oldódó vitamin koncentrációja, valamint energiatartalma nagyobb, mint a colostrumé. Az érett anyateja női tej végső formája, rendszerint a szülés utáni 15.naptól termelődik.
Az anyatej összetevői
1. Fehérjék és non-protein nitrogén
Az anyatejfehérjetartalma összesen 0.9g/100 ml, a laktáció előrehaladtával valamelyest csökken. Savófehérjék
Az anyatej főként savófehérjéket tartalmaz. A savófehérjék a savas precipitálódást követően is oldatban maradnak, könnyebben emésztődnek, elősegítik a gyorsabb gyomorürülést. A savófehérjék fenilalanin-, tirozin és metionintartalma kisebb, taurintartalma nagyobb, mint a tejkazeineké.
Az anyatejfő savófehérjéje, az alfa-laktalbumin fontos nutrícionális fehérje a csecsemő számára.
Az anyatejben lévő laktoferrin, lizozim és szekretoros immunglobulin-A (sIgA) az immunvédelemben fontos savófehérjék.
Ez utóbbi három funkcionális fehérje csak nyomokban ill. igen kis mennyiségben található meg a tehéntejben. A tehéntejfő savófehérjéje a béta-laktoglobulin csak nyomokban van jelen az anyatejben.
Kazein
A női tejR és K-kazeint tartalmaz. Elsősorban nutritív funkciója van, esszenciális ásványi anyagokat és aminosavakat biztosítva a csecsemő számára. Ezen túlmenően a kazeinből származó különböző peptidek, melyek a calciumfoszfát felszívódását segítő funkción túl antimikrobiális, antihipertenzív, antithrombotikus, opioid és immunmoduláló funkciókkal rendelkeznek.
A tehéntejfehérjetartalma dominálóan kazein tej, a savófehérje/kazein arány 0.25. Non-protein nitrogén (NPN)
Az anyatej teljes nitrogén tartalmának 18-30%-a, 0.35-0.53g/100ml. Koncentrációja változik a laktáció folyamán (carnitin koncentráció nő) és az anyai étrendtől függően (szabad aminosav koncentráció).
A NPN alkotóelemei: Amino-cukrok (legnagyobb mennyiségben
N-acetylglucosamin), peptidek (pl. epidermalis növekedési faktor, IGF, insulin, alvás-indukáló peptid), szabad aminósavak (legnagyobb koncentrációban taurin és glutaminsav), carnitin, cholin, nukleinsavak, nukleotidok, poliaminok.
Jelentőségük elsősorban funkcionális (növekedés, intestinális colonizáció, bélnyálkahártya érés, immunológiai funkciók stb).
2. Zsír
A kalóriabevitel 45-55%-át adja.
Az anyatej össz-zsírtartalma 30-50g/L között változik, a leginkább változó összetevő. A női tej össz-zsírtartalmának 98-99%-át a triacylglycerinek (három zsírsavmolekula kötődikegy glycerin molekulához) képezik. A további 1-2% di-és monoacylglycerinek, nem-észterifikált zsírsavak, phospholipidek, cholesterin és cholesterin-észterek. Az anyatej több mint 200 különböző zsírsavat tartalmaz.
Esszenciális zsírsavtartalma (linolsavés linolénsav) lényegesen nagyobb a tehéntejénél. Az anyatej egyedülálló ellátást biztosít a hosszú szénláncú, többszörösen telítetlen zsírsavakból (LCPUFA) is, melyeknekjelentős szerepe van az agy és a retina funkcionális érésében.
A zsírsavösszetételt az individuális különbségek mellett befolyásolja a laktáció szakasza, a gesztációs kor, a paritás és az anya táplálkozása.
3. Szénhidrát
A női tej szénhidráttartalma a kalória 40%-át adja.
Nutrícionálisan a legfontosabb a laktóztartalom (7 g/l). Az oligoszacharidok mennyisége 1 g/l körül van, több mint 130 különböző szénhidrát-polimer és glikoprotein alkotja ezt a csoportot.
Ezeknek a vegyületeknek prebiotikus aktivitása és antiinfektív hatása van, képesek a különböző specifikus bakteriális antigének megkötése révén megakadályozni a baktériumok nyálkahártyához való tapadását, s így fontos szerepet töltenek be a mucosalis immunvédelemben. Ezen túlmenően szerepük van a központi idegrendszer szürke állományában levő gangliozidok felépítésében.
4. Vitaminok - nyomelemek
Az anyatej savófehérjéi optimális szállítói a vitaminoknak, a nyomelemeknek és így az anyatejes csecsemők csak ritkán szorulnak vas vagy vitamin kiegészítésre.
Ez utóbbiak közül kivételt képez a D- és K-vitamin.(lsd. Szoptatás és vitamin szupplementáció). Azanyatejvastartalma a tehéntejével azonosan alacsony (0,05-0,13 mg/100 ml). A vas azonban a női tejből több mint 50%-ban, míg a tehéntejből mindössze 10%-ban, a vassal dúsított tápszerekből pedig csupán 5%-ban szívódik fel. Az anyatejben lévő vas jó felszívódásában valószínűleg jelentős szerepe van az anyatej egyrészt magas laktoferrin- és C-vitamin-, másrészt alacsony foszfát-, kalcium- és fehérjetartalmának. Ezért a kizárólag szoptatott csecsemőnek 4-6 hónapos koráig nincs szüksége vaspótlásra, ha az anya nem súlyosan vashiányos és a csecsemő vasraktárai is elegendőek. Az első élethónapokban a csecsemő nagy mennyiségű vasat használ fel a gyors vérvolumen-növekedéshez, ezáltal a raktárak 4 hónapos életkorra a felére csökkennek.
Az első életévben az egészséges csecsemő bélrendszeréből mintegy 0,8 mg/nap táplálékvasnak kell felszívódnia. Ebből a csecsemő szervezete 0,6 mg/nap-ot a növekedésre, 0,2 mg-ot pedig a vizelettel, a széklettel és a bőrön keresztül bekövetkező folyamatos vesztés pótlására fordít.
A kizárólagosan szoptatott csecsemők esetében, ha nem rendelkeztek születéskor kielégítő vasraktárakkal, 4-6 hónapos korban szükség lehet vaspótlásra.
5. Ásványi sók
relatíve alacsony nátrium és sóterhelés, relatíve alacsony calcium tartalom (kiváló biohasznosulás)
6. Enzimek
amiláz, lipáz, proteázok stb
7. Hormonok
thyroxin, trijódthyronin, cortisol, progesteron, pregnandiol, prolaktin, oxytocin stb.
8. Sejtes elemek
Macrophagok, polymorphonucleáris leukocyták, Tés B lymphocyták.
9. Egyéb anyagok
Prostaglandin, erythropoietin, citokinek, interleukinek stb.... A női tej átlagos kalóriatartalma 70 Kcal/100 ml (293 kJ/100 ml).
A szoptatás/anyatejes táplálás jótékony hatásai (9,10)
1. A csecsemő számára
Fajspecifikus táplálék, nutritív előnyökkel.
A szoptatott (minimum 3-6 hónapig folytatott szoptatás) és tápszerrel táplált csecsemőket összehasonlítva a fejlett országokban végzett vizsgálatok metaanalízise alapján bizonyított:
Infekciókkal szembeni védelem-ritkább a heveny középfülgyulladás, a gastroenteritis, az alsó légúti infekció
Immunológiai védelem-ritkáb az akut lymphoid és myeloid leukaemia, az 1-es és 2-es tipusú diabetes, a gyermekkori lymphoma.
Allergia prophylaxis-Ritkább az atopiás eczema (pozitív családi anamnézis esetén), asthma. Egyéb pozitív hatások-ritkább a hirtelen csecsemőhalál, elhízás a későbbi életkorban.
2. Anya számára
Segít a szülés utáni felépülésben Pszichológiai előnyök (szoros kötődés, önbizalom) Ritkább a mellrák és petefészekrák Ritkább az elhízás
Ritkább a 2-es típusú diabetes (csak azokra érvényes, akiknek nem volt gestatios diabetesük) A csecsemő fejlődése (7-8,10-14)
A legnagyobb ütemű fejlődés a csecsemőkorban zajlik. A fejlődés üteme egyéni variációkat mutat, függ a táplálás módjától is. A szoptatott csecsemők súlyfejlődése nem egyenletes, gyorsabb az első két hónapban és lassúbb a 3-12 hónapban és időszakonként növkedési ugrások (growth spurts) figyelhetőek meg, Általában véve a csecsemők a születési súlyukat féléves korukra megduplázzák és egy éves korukra megháromszorozzák. A szoptatott csecsemők testsúlya az első évvégére kb. 650g-mal alacsonyabb, mint tápszerrel táplált kortársaiké.
A csecsemők testhossza az első 3 hónapban gyorsabban, majd a következőkben kissé lassúb,egy éves korra kb. eléri a 75 cm-t. Az adott csecsemő fejlődésének megítélésében a növekedés ütemén kívül számos tényezőt figyelembe kell venni. Fontos, hogy a tápanyagok kielégítsék a gyors testi növekedés és fejlődés igényeit, valamint az optimális pszichoszociális fejlődést is.
Korábban a csecsemők kalóriaigényét a szükségesnél jelentősen magasabbnak ítélték meg. Ennek az volt a magyarázata, hogy nem álltak rendelkezésre olyan módszerek, amelyekkel objektíven meghatározható lett volna ebben az életkorban az energiafelhasználás mértéke, másrészt optimálisnakaz ad libitum tápszerrel táplált csecsemők energia-felvételét tekintették. Befolyásolta a helyzetet az is, hogy a nemzetközileg használt csecsemő súly- és hosszfejlődési referencia grafikonokat és táblázatokat is tápszerrel, illetve vegyesen táplált csecsemők adatai alapján állapították meg. Ezekhez viszonyítva a kizárólagosan szoptatott csecsemőksúly- és hosszfejlődési értékei általában az alacsonyabb percentilis értékeken helyezkednek el. Mivel az anyatejjel történő táplálást tekintjük fiziológiásnak, az újszülöttek és csecsemők optimális napi kalóriaigénye a kizárólag szoptatott csecsemők adatai alapján állapítható meg.
Az életkor növekedésével a csecsemő, illetve a kisded az energiabevitel egyre kisebb hányadát használja fel növekedésre. Négy hónapos korban ez az arány 30%, míg 1 éves korban már csak 5%, 3 éves korban pedig 2%-ra csökken. Ez a magyarázata annak, hogy az első hat hónapban a legkritikusabb az elégtelen táplálékbevitel a növekedés szempontjából és már kismértékű, de folyamatos energiahiány kumulatív súly- és hossznövekedésbeli elmaradást okoz. Az agy növekedésének és differenciálódásának üteme a várandósság utolsó harmadában és az első két életévben a legnagyobb.
A szopás mennyisége
Az első szoptatáskor, mely a születést követő 60 percen belül történik, az újszülött néhány ml colostrumot vesz magához, az egész nap elfogyasztott mennyiség kicsi (7-125 ml), de ez rendszerint fedezi a szükségletét. A születést követő első 24 órában általában 3-8x szopik, megközelítőleg 30 ml mennyiséget fogyaszt az első étkezésekkor, ami fokozatosan, néhány nap alatt 60-90 ml-re emelkedik.
A 2-6. napon átlagosan 5-10 alkalommal szopnakés a tejbevitel gyorsan nő, elérve a 4. naptól testsúlya egytized részét (250-300 ml-t), majd 6-7. naptól testsúlykilogrammonként a 150 ml mennyiséget. A táplálás sikerességére utal, ha az újszülött nem veszít a súlyából már az 5-7. életnapon, és a 12-14. életnapra a gyarapodása megfelelően megindul. Egy hónapos korra az átlagos anyatej tejbevitel 750-800 ml (8) körül mozog, de az egyéni eltérések nagyok lehetnek. 450 - 1150g anyatejfogyasztása mellett a csecsemők egészségesen fejlődhetnek. Mivel az egyes szopások mennyisége változhat az elhanyagolhatóan kis mennyiség és 240 ml között, továbbá az anyatej összetétele folyamatosan változik, az egy adott alkalommal szopott anyatejmennyiség nem ad felvilágosítást a csecsemő tápláltságáról (13).
Jól megy a szoptatás, ha a csecsemő (14)
- legalább nyolcszor szopik 24 óra alatt
- a hatékony tejbevitel jelei észlelhetők a csecsemőnél és az anyánál (l. Szoptatás Gyakorlata c. mellékletben)
- a harmadik naptól naponta általában három székletet ürít, amely a negyedik nap után már aranysárga, un. anyatejes széklet.
- az ötödik naptól vizelete víztiszta vagy halványsárga és legalább 5-6 kellően nedves pelenkája van,
- iniciális súlyesése a 7%-ot nem haladja meg
- súlya a harmadik nap után nem csökken
- súlya az ötödik nap után gyarapodásnak indul
- a tizedik (legkésőbb 14.) napra visszanyeri születési súlyát
- az első két élethónapban naponta kb. 20-35g-ot gyarapszik
- az 5-6. élethónapra megduplázza a súlyát
Szoptatás és sárgaság (15,16)
A szoptatással/ anyatejes táplálással összefüggő sárgaságnak két formája van.
1. U.n. "nem elegendő tej okozta sárgaság" (not enough breastmilk jaundice, breastfeeding jaundice).
Elégtelen kalóriabevitellel függ össze, a 2-5. napon kezdődő korai, fiziológiás mértéket meghaladó sárgaság az egyébként egészséges szoptatott csecsemőnél (a hyperbilirubinaemia egyéb okainak kizárása után). Megelőzése a korai mellretétel és a napi 8-12x történő igény szerinti szoptatás, nem pedig a cukros víz/tea itatása.
2. U.n. "anyatejes sárgaság"(breastmilkjaundice).
Később, a második élethéten kezdődik, elhúzódhat egy hónapos koron túl is. Ennek hátterében nem az elégtelen anyatejbevitel, hanem egy, az anyatejben lévő faktor által előidézett fokozott enterohepatikus shunt áll. A csecsemő jól szopik és megfelelően gyarapszik. A szoptatás folytatható, ritkán átmeneti, egy napra történő felfüggesztése szóbajöhet.
Szoptatás és vitamin szupplementáció
A legutóbbi hazai módszertani ajánlás szerint D-vitaminból a szoptatott csecsemők 2 hetes kortól napi 400 lU-t (10 microgram) kapjanak 1 éves korukig. Akik az 1 éves kort késő ősszel töltik be, a profilaxis további fél évig folytatandó(17).
A legutóbbi hazai módszertani ajánlás szerint minden érett újszülött kapjon 2mg K-vitamint peros, majd 1 hét múlva 2mg-ot. A kizárólagosan szoptatott csecsemők további havi 2mg-ot per os kapjanak(21). A K-vitamin pótlására a kizárólagos szoptatás idején a bélflóra még elégtelen K-vitamin-termelő képessége miatt van szükség.
A szoptató anya étrendje
Egészséges táplálkozás esetén nincs szükség jelentős étrendi változtatásokra csak azért, mert az anya szoptat. Az étrend legyen változatos, tartalmazzon megfelelő mennyiségű fehérjét, vitaminokat és nyomelemeket. A napi teljes folyadékbevitel a szomjúságnak megfelelően történjen, de érje el a napi 2 liter mennyiséget. Ebből a tejaz 5 dl-t ne haladja meg.
Amennyiben a kizárólag szoptatott csecsemő allergia tüneteit mutatja, célszerű az allergizáló anyag megkeresése. Leggyakrabban indokolt a tej, tejtermék valamint a tojás átmeneti kiiktatása, majd ezek egyenkénti emelkedő mennyiségben - a tünetmentesség megtartásáig a visszaadása. Hiba a nevezett ételek fogyasztásának teljes és tartós tilalma, tünetet okozó hatásuk bizonyítása nélkül. Erősen puffasztó ételek, olajos magvak kerülése célszerű a szoptatás idején.
A szigorú vegetáriánus diétát tartó anyák teje elégtelen mennyiségben tartalmaz B2- és B12-vitamint, valamint vasat, kálciumot és cinket. Ezen kívül ilyen esetekben az anyatej mennyiségi és minőségi fehérje összetétele sem megfelelő, ezért a gyermekben egyes esszenciális aminosavakból (pl. lizin és metionin) hiány alakulhat ki. Amennyiben az édesanya ragaszkodik a szigorú vegetáriánus diétához, akkor a gyermekorvos feladata, hogy ezek pótlásáról gondoskodjon. Egyes esetekben ilyenkor szükséges lehet az anyatejes táplálás helyett mesterséges táplálásra áttérni.
A szoptatás - anyai betegségek és állapotok (19)
- Szilikon mell implantátum: nincs bizonyíték, hogy a szoptatás kontraindikált lenne
- Környezetszennyező anyagok: jelenlétük ellenére is a szoptatás javasolt.
- "Utazók hasmenése" esetén a szoptatás folytatható-az anya kezelésére a bizmut-subsalicylát nem javasolt, szükség esetén elsősorban kaolin-pektin, esetleg loperamid adható.
- Hepatitis B infekció esetén a szoptatás nem ellenjavallt és közvetlenül a születés után megkezdhető. A HBsAg pozítiv anyák újszülöttjeit hepatitis B immunglobulin és a hepatitis B vakcina sorozat első oltásában kell részesíteni, lehetőleg 12 órán belül. A második oltást 1 hónapos, a harmadikat 6 hónapos korban kell beadni. A szoptató anya fokozottan figyeljen a bimbó berepedésének és vérzésének elkerülésére. (20)
- Hepatitis C fertőzött anya esetén nem kontraindikált a szoptatás, mert a vírus anyatejjel történő átvitelére nincs bizonyíték. Mivel HCV a fertőzött vérrel vihető át, ezért az anya mellén lévő berepedés, vérzés esetén a szoptatást átmenetileg fel kell függeszteni és a mell gyógyulásáig a lefejt tejsem használható fel.
- Hepatitis A infekció esetén folytatható a szoptatás, szükséges a passzív védelem (gammaglobulin) és a higiéne betartása.
- CMV, EBV, enterovírusok és parvovírus infekció esetén folytatható a szoptatás
- Varicella-zoster vírus infekció: a szoptatás folytatható. VZIG profilaxis mindenképpen szükséges, ha az anyai megbetegedés a szülés előtt 5 napon belül ill. azt követően 2 napon belül jelentkezik(21) Később fellépő anyai fertőzés esetén VZIG adása mérlegelendő.
- HSV-1, HSV-2 esetén folytatható a szoptatás, azonban ha a lézió a mellen van az érintett mellből a teljes gyógyulásig a szoptatást fel kell függeszteni és az onnan lefejt tejsem használható fel.
- HIV pozitivitás és AIDS: a szoptatást kontraindikálja
- Tuberkulózis: aktív kezeletlen megbetegedés esetén a szoptatás kontraindikált és a csecsemőt el kell különíteni az anyjától.
- Syphilis esetén a szoptatás folytatható, ha a megfelelő kezelés az anyánál és a csecsemőnél már legalább 24 óráig tartott.
- Mastitis esetén a szoptatás folytatása javasolt
- Melltályog esetén az érintett mellből való szoptatás az antibiotikus kezelés megkezdése és/vagy a sebészeti drainage után az első 24 órában nem javasolt. Eközben a másik mellből a szoptatás folytatható.
- Anyai addikció: dohányzás, alkohol és drog fogyasztás esetén legtöbb esetben a szoptatás megengedett, intravénás drog használat esetén kontraindikált. Az esetleges alkoholfogyasztást követően 2 órás szünet után a szoptatás folytatható.
A szoptatás kontraindikációi
1. A galactosaemia és egyes ritka anyagcsere betegségek a csecsemőnél
2. Az anyának diagnosztikus vagy terápiás célból adott radioaktív izotop vagy egyéb radioaktív expozíció-amíg a radioaktivitás jelen van.
3. Antimetabolitok, vagy kemoterápiás szerekkel történő kezelés.
4. Egyes drogok és kis számú gyógyszerek (3. melléklet)
5. Anyai mellen lévő herpeses lézió
6. Anyai aktív, kezeletlen tuberkulózis
7. HIV pozitivitás és AIDS
Szoptatás és gyógyszerek (3. melléklet) Táplálás 0-6 hónapos korban A. Kizárólagos szoptatás
Az élet első hat hónapjában a csecsemő igényeit optimálisan a kizárólagos szoptatás/anyatej elégíti ki (22). Az anyatej mennyiségi és minőségi összetételében a csecsemő legmegfelelőbb tápláléka. Ezen túlmenően az első 6 hónapban aktívan és passzívan támogatja a csecsemő emésztőrendszerének emésztő, felszívó és védő funkcióját (8 ) A csecsemő kizárólagos szoptatása/ anyatejes táplálása a csecsemő 6 hónapos (26 hetes) koráig javasolt. Ezt az alapelvet javasolják az európai és az amerikai szakmai grémiumok (1-5).
B. Szoptatás folyadék/ táplálék kiegészítéssel - Mesterséges táplálás
Az első 6 élethónapban azokban a ritkán előforduló esetekben, amikor az anyánál vagy a csecsemőnél fennálló orvosi indikáció miatt a szoptatás nem lehetséges, a szoptatás átmeneti felfüggesztése vagy orvosi indikáció alapján tápszerrel történő kiegészítése válik szükségessé, vagy a megfelelő felvilágosítás megadása után az anya úgy dönt, hogy nem kíván szoptatni ill. a szoptatást nem kívánja tovább folytatni, mesterséges táplálás bevezetése szükséges. Az anyát a megfelelő információ megadása után hozott döntésében támogatni kell, és a megfelelő mesterséges táplálásra vonatkozó tanácsokkal el kell látni.
Részletesen lásd az anyatej-helyettesítő tápszerekről szóló fejezetben. Szoptatás kiegészítő táplálással (6-12 hónapos kor)
A második félévben az anyatej már nem elégíti ki önmagában a fejlődő csecsemő tápanyagszükségletét, de kb. egyéves korig a csecsemő fő tápláléka marad. Az anyatejtovábbra is jelentősen hozzájárul a csecsemő tápanyag- és energiaigényének kielégítéséhez csakúgy, mint immunológiai védelméhez. A szoptatás lelki-érzelmi jelentősége a világot egyre inkább felfedező, az anyától rövidebb-hosszabb időre eltávolodó csecsemő számára szintén igen nagy. Az újételek bevezetése nem a szoptatás helyettesítése vagy befejezése miatt történik, hanem annak kiegészítésére. Ezért helyesebb kiegészítő és nem "elválasztó" (weaning) táplálékról beszélni a 6 hónapos koron túl szoptatott csecsemő esetében. Az elválasztás ui. a szoptatás abbahagyását jelenti, holott a cél az, hogy a kiegészitő táplálék kiegészítse és ne helyettesítse a szoptatást (3) és legalább egy éves korig folytatódjon. A WHO és Amerikai gyermekgyógyász Akadémia (1,4) javasolja a 2 éves korig és azon túl is folytatott szoptatást, amennyiben azt az anya és a gyermek is igy kívánják. Mivel a csecsemő fő tápláléka továbbra is az anyatej, fontos, hogy mennyisége ne csökkenjen a második félévben sem. Ennek biztosítására a kiegészítő táplálékokat mindig szoptatás után kínálja az édesanya, miközben a szoptatás gyakorisága a korábbiakhoz képest nem csökken.
A kiegészítés a szoptatás kiegészítésére, a csecsemő plusz tápanyag-és energiaigényének kielégítésére szolgál, nem a szoptatás helyettesítésére. A csecsemők többsége 6 hónapos kor után válik alkalmassá az anyatejen kívül egyéb táplálék fogyasztására. Ennek látható jelei, hogy megfogja az ételt, szájába teszi, rágja, a nyelvével nem löki ki (23). Az új ételek adásának sorrendjében nincs szigorú kötöttség, de arra ügyelni kell, hogy egyenként kerüljenek bevezetésre és közöttük legalább 3-5 nap teljen el. Kezdetben pépes, majd darabos étel adható. Az egyes ételek adásának sorrendjét és időpontját a "Szolidok (az anyatejen és tápszeren kívüli ételek) bevezetése" című fejezet tárgyalja.
Ahogy fejlődik a csecsemő, a kiegészítő táplálék egyre változatosabbá válik, mennyisége is emelkedik. Az anyatej összes előnye továbbra is érvényesül. A tápláló funkciót fokozatosan a megnyugtatás, a kötődés, az un. komfort szoptatás válthatja fel.
Vegyes vagy mesterséges táplálás
Az anyatej teljes hiánya, vagy elégtelen mennyisége esetén tápszerek adása válhat szükségessé. A tápszerek emberi fogyasztásra szolgáló, szigorúan meghatározott minőségi és higiénés követelményeknek megfelelő, különleges gyártási eljárásokkal, iparilag előállított, állandó összetételű, élelmezésre használt anyagkeverékek vagy készítmények. Az EU országaiban a tápszerekre vonatkozó előírás több mint 50 alkotórész esetében határozza meg a minimum értékeket és közel 30 esetben a maximális mennyiséget is előírja.
A tápszerek általában szilárd por, granulátum, perlórum vagy folyékony kiszerelésben kerülnek forgalomba. A szilárd tápszereket kb. 5 percig forralt és 50 °C-ra lehűtött ivóvízben kell oldani, az eredeti, mérőkanállal kimért, lesimított (nem púpozott!) adagban, a csomagoláson feltüntetett arányban. A kész oldatot hűtőszekrényben tárolva maximum 24 óráig lehet felhasználni, fogyasztás előtt testhőmérsékletűre felmelegítve (lehetőség szerint meleg vízben tartott hőálló üvegben); ismételt felmelegítése nem megengedett! Bontott csomagolás esetén a folyékony tápszerek felhasználhatósága 24 óra, a bontott szilárd tápszerek esetén 10-21 nap.
Mesterséges táplálás esetén négy-hat hónapos korban megkezdhető a kiegészítő táplálás, a szoptatott csecsemőknél leírtaknak megfelelően.
Hozzátáplálás (Kiegészítő táplálás) /Elválasztás
Hat hónapos kor után már indokolt elkezdeni a hozzátáplálást. Az idegen fehérje tartalmú ételeket fokozatosan vezetjük be a csecsemő étrendjébe. A hozzátápláláskor (elválasztáskor) sem szabad áttérni tejhígításra, vagy színtej adására, mivel annak összetétele nem fedezi a csecsemő igényeit és egyéb káros következményei is lehetnek. Magas fehérje tartalma bélvérzést okozhat, fokozott ásványi anyagtartalma pedig növeli a vesék ozmotikus terhelését. Vastartalma viszont igen alacsony, ami vashiányos anaemia kialakulásához vezet. Egy éves kor alatt natív tehéntejet semmiképpen ne adjunk ivóléként.
Elválasztás/elválasztódás
Az elválasztást vagy az anya kezdeményezi ( túl fárasztónak tűnik a szoptatás, vissza kell mennie dolgozni vagy a családja nem támogatja gyermeke szoptatásában), vagy ritkábban egészségi okokállnaka háttérben. Az elválasztódás azt jelenti, hogy a szoptatás abbahagyását a gyermek kezdeményezi.
Amennyiben az anya el kívánja választani gyermekét, a fokozatos elválasztás kívánatos. Általában l -3 hét alatt célszerű egy szoptatást teljesen helyettesíteni. Legutoljára a reggeli, illetve az esti szoptatást hagyjuk el. Az elválasztást fokozatosan kell végrehajtani, ezesetben a kiegészítő táplálást a szoptatás előtt adjuk. Az új táplálék adásának bevezetése a délelőtti, vagy déli szoptatás előtt kis mennyiséggel (10-20 g) történjen, az adag a következő napokban a csecsemő igénye szerint növelhető.
Szolidok (az anyatejen és tápszeren kívüli ételek) bevezetése
A nemzetközi irodalom "szolid" néven foglalja össze az anyatejen és a tápszeren kívüli egyéb ételeket. Bevezetésük a folyékony-pépestől a szilárd ételekig folyamatosan történik, mind típus, mind állag szempontjából. Nagy jelentőséggel bír a szolidok bevezetésének időpontja, amelyet a csecsemő fizikai fejlettsége és állapota (a gyomor-bél rendszer érettsége, a fogfejlődés, betegségek, örökletes hajlam) mellett pszichés tényezők is befolyásolnak. Ez a rendkívül érzékeny korai időszaka későbbi problémák (allergiák, hiányállapotok, rossz étkezési szokások, obesitas stb.) kialakulása szempontjából is meghatározó.
Bevezetésükre általában 6 hónapos kor körül kerül sor, de az anyatejes táplálás hiánya esetén 4 hónapos korban állíthatók be legkorábban
Az első szolidok lehetnek gyümölcsök, gluténmentes (pl. rizs) vagy glutén-tartalmú (búza, árpa, rozs, zab) cereáliákés főzelékfélék.
Gluten tartalmú szolidokat 4 hó előtt semmiképp nem, 7 hó előtt azonban mindenképp fokozatosan be kell vezetni, lehetőség szerint amíga csecsemő szopik (a legújabb ismeretekszerint ez csökkenti a coeliakia, a diabetes mellitus és a búzaallergia kockázatát).
A szolidok bevezetésének sorrendje nem szigorúan kötött, de minden területen a fokozatosságra kell törekedni azért, hogy a fentebb említett problémákelkerülhetőklegyenekés az anya-gyermek kapcsolat se szenvedjen kárt. Egyszerre csak egy ételt, kis mennyiségben (10-20 g) adjunk és fokozatosan emeljuk az adagot. Ha az elválasztás a cél, az a célszerű, hogy 2-4 hét alatt váltsunk ki egy szopást. Az újételek3-5 nap különbséggel kövessékegymást, de abban az esetben, ha valamely új ételt a csecsemő nem fogyaszt szívesen, vagy problémát észlel a szülő, figyelmeztessük, hogy semmiképpen ne erőltesse annak folytatását.
Ha a gyümölcsöt választjuk, akkor az alma és az őszibarack után óvatosan idénygyümölcsként: a sárgadinnye, a meggy, a cseresznye, a jó minőségű, hámozott szilva, majd a toleranciának és érzékenységnek megfelelően körte, déligyümölcsök (narancs, banán stb.) következnek. A gyümölcsöt lé, majd pép formájában adjuk.
Csecsemőnél kerüljük az apró magvas (hashajtó hatású), nehezen tisztítható, hisztamin felszabadulást kiváltó (eper, málna) gyümölcsöket. Ne cukrozzuk, ne adjunk hozzá kekszet, babapiskótát. Friss hiányában mélyhűtött gyümölcs is adható.
A főzelékfélék bevezetését burgonyával kezdjük, és a csecsemőkor idején leginkább ezzel történjen a sűrítés is. Ezen kívül a rántás helyett használhatunk rizs, illetve kukoricapelyhet is. Texturáltság szempontjából a csecsemő kora és a zöldség fajtája szerint döntünk passzírozás vagy turmixolás mellett (zöldborsó héját csak passzírozással lehet eltávolítani). Darabosan csak akkor adjuk, ha már zápfogai is vannak, amelyekkel meg tudja őrölni a főzelékrészeket. A rágásra szoktatást általában 8-10 hónapos kor körül kezdjük úgy, hogy egy-egy nagyobb de egészen puha darabot hagyunk a főzelékben, amit az ínyével összenyomhat. A főzelék kezdetben mézsűrűségű, később a csecsemő ízléséhez igazodik. A burgonya után a sárgarépa, a cékla, a saláta, a sütőtök, a szelőtök, a gesztenye, a brokkoli, a kelbimbó, a spenót, a zöldborsó, a zöldbab és a spárga következzék. Magas, nehezebben emészthető rosttartalmuk miatt a kelkáposztát, karalábét, karfiolt csak8 hónapos kor után próbáljuk meg. Főzelékekhez bio-termesztésű zöldség lenne az ideális, de ennek hiányában mindenképpen törekedjünk arra, hogy ellenőrzött beszerzési helyről (élelmezés-egészségügyi várakozási idő betartása) vásárolt alapanyagot használjunk, és ha az alapanyag magas nitrát tartalma nem zárható ki, illetve az előbb részletezett probléma fennáll, akkor inkább kész bébiételt válasszunk. (A nitrát tartalmú élelmiszereknél még az elkészítés és a fogyasztás közötti időtartamnak is jelentősége van!). Spenótot, sóskát magas oxalát tartalma miatt csak hetente egy alkalommal adjunk. A száraz hüvelyesekfelhasználása csecsemőkorban leginkább a vegetáriánus módon étkezőknél bír jelentőséggel. Csecsemők nem táplálhatók vegetarianus diétával. Ha mégis akkor legalább 500 ml anyatejet, vagy tápszert kell kapniuk! (6) Gyorsfagyasztott alapanyagot használhatunk, de a csecsemő ne kapjon tartósítószert, festékanyagot, mesterséges édesítőt tartalmazó élelmiszert.
A főzelék komplettálás és a vashiány megelőzése céljából 6-7 hónapos kortól adjunk húst is. (Fiatal állattól, zsírtalanított, elsősorban baromfi és sertés.) Húskészítményt, felvágottat ne használjunk. A hal (szálkamentes édesvízi) adása táplálkozás-élettani szempontból hasznos lenne, de fokozott figyelmet igényel a túlérzékenység gyakorisága szempontjából. (A csirkemáj adása előnyei mellett méregtelenítő-szerv szerepe miatt meggondolandó és legfeljebb hetente egyszer fiatal állaté adható.) Állati fehérje komplettálásra a tojás is hasznos, de allergizáló tulajdonsága miatt csak 8 hónapos kortól ajánlott a főtt tojásnak a szétválasztott sárgája, majd 1 év felett a fehérje.
Tehéntejet 12 hónapos kor alatt ne, de tejterméket (sajt, túró, joghurt) már (a családi anamnézistől függően), kis mennyiségben a főzelék komplettálására adhatunk legkorábban 7-9 hónapos kortól. Kávé, kakaó szintén 12 hónapos kor után.
A kecsketej önmagában táplálkozás-élettani szempontból nem megfelelő, mivel egyes vitaminokban (B6, B12, C, D, folsav) szegény, ásványi-anyag tartalma pedig magas. Adása azonban kiegészítő táplálékként egészséges csecsemőknek egy éves kor körül nem kontraindikált, amennyiben hatóságilag ellenőrzött és allergiás reakciót nem vált ki.
A főzelékbe 6-7 hónapos kortól növényi olaj adása is ajánlott (1 dl-hez 1 kávéskanál). Az ételt lehetőleg ne sózzunk és cukrozzunk. Nagyobb csecsemőnél alkalmazhatunk enyhe fűszerezést (só pótló) pl. zöldpetrezselyem, kapor, fehérrépa, paradicsom stb.
Az egyéb szolidok közül kiemelendő az, hogy 1 éves kor alatt a méz és a gyógyteák esetleges pollentartalmuk miatt nem javasolhatók. Az olajos magvak sem adhatók az allergizálódás veszélye miatt.
A szükséglet szempontjából kiemelendő még, hogy az elfogyasztott táplálék mennyisége 1 éves korig nem haladja meg az 1000 g-ot. Az étkezések száma 6 hónap fölött 5 (4) és az egyszeri adag 200 (250 ml) legyen.
A 8-9-ik hónaptól be lehet vezetni a "rágcsálnivalókat" is. Amikor már a szem - száj - kéz mozgása összerendezett, felügyelet mellett, puha zöldségdarab, sárgadinnye, banán, kiflivég stb. adható a csecsemő kezébe. Ilyenkor fel kell hívni a figyelmet a veszélyes ételekre is, ezek félrenyelve fulladást okozhatnak, ezért ne jusson hozzájuk a csecsemő (cukorka, cseresznye, kukorica, dió, kemény, nyers gyümölcs vagy zöldségdarab stb.).
Világszerte terjed az alternatív táplálkozás (vegetáriánus irányzatok), ezért a csecsemőtápszereknél felsoroltakon kívül a szolidok szempontjából is nagyon fontos alapelv, hogy az esetleges energia, aminosav (L-carnitin, taurin, calcium), vas, B12-vitamin, D-vitamin elégtelen bevitelét megakadályozzuk. Ilyen esetben fokozott odafigyelést, szakember segítségét igényli az étrend összeállítása (speciális nyersanyagok, technikákstb.) és a gyermek megfigyelése esetleges hiányok irányában.
A tápszerek felosztása
Az anyatej elégtelen mennyisége, vagy teljes hiánya esetén, illetve elválasztáskor, vagy különböző kóros állapotokban tápszerek (formulák) adására szorulunk. Ennek megfelelően a tápszereket anyatej-helyettesítő, anyatej-kiegészítő (követő) és speciális tápszerekre oszthatjuk fel.
Váltások azonos tápszercsoporton belül értelmetlenek, más csoportbeli tápszerre való áttérés szakmailag magalapozott kell, hogy legyen.
A tápszerek részletesebb tárgyalása nem feladata jelen ajánlásnak, mivel önálló kiadványok foglalkoznak a témával.
Anyatej-helyettesítő tápszerek alkalmazása
Abban az esetben, ha az anyatejes táplálásra semmiképpen nincs mód, akkor a csecsemőknek hat hónapos korukig speciális tápszerekre van szükségük, amely mennyiségi és minőségi összetételében egyaránt az anyatej összetételét próbálja megközelíteni. Természetesen a legjobb minőségű tápszer sem vetekedhet az anyatej előnyeivel. Ezeknek a tápszereknek az összetételét az Európai Gyermek-Gasztroenterológiai, Hepatológiai és Táplálkozási Társaság irányításával nemrégiben egy nemzetközi grémium határozta meg, az egyes összetevők minimum és maximum értékeit az 1. táblázat mutatja. A táblázatban említetteken kívül ez az ajánlás szabályozza az opcionális összetevők, így pl. a nukleotidok és többszörösen telítetlen hosszú szénláncú zsírsavak minimum és maximum értékeit is. Fontos hangsúlyozni, hogy a WHO az anyatejpótló tápszerekforgalmazását szigorúan szabályozza, hogy azokkal csakvalóban azokat a csecsemőket táplálják, akiknél az anyatejes táplálás nem biztosított.
1. TÁBLÁZAT Az ESPGHAN vezette nemzetközi szakértői csoport ajánlása a csecsemőtápszerek egyes összetevőinek minimum és maximum értékeire (100 kcal tápszerre)
| Minimum | Maximum | |
| Energia (kcal/100 ml) | 60 | 70 |
| Makronutriensek | ||
| Fehérje (g) | 1,8 | 3 |
| Zsír (g) ebből linolsav (g) ebből linolénsav (mg) | 4,4 0,3 50 | 6,0 1,2 NM |
| Szénhidrát (g) | 9,0 | 14,0 |
| Mikronutriensek | ||
| Ásványi anyagok, nyomelemek | ||
| Nátrium (mg) | 20 | 60 |
| Kálium (mg) | 50 | 160 |
| Klorid (mg) | 50 | 160 |
| Kálcium (mg) | 50 | 140 |
| Foszfor (mg) | 25 | 90 |
| Kálcium/foszfor arány (mg/mg) | 1:1 | 2,1 |
| Magnézium (mg) | 5 | 15 |
| Vas (mg) | 0,3 | 1,3 |
| Cink (mg) | 0,5 | 1,5 |
| Réz (ug) | 35 | 80 |
| Jód (ug) | 10 | 50 |
| Szelén (ug) | 1 | 9 |
| Fluor | NM | 60 |
| Mangán (ug) | 1 | 50 |
| Vitaminok | ||
| A-vitamin (ug RE) | 60 | 180 |
| D3-vitamin (ug) | 1 | 2,5 |
| E-vitamin (mq a-TE) | 0,7 | 0,5 |
| K-vitamin (ug) | 4 | 25 |
| C-vitamin (mg) | 10 | 30 |
| Thiamin (ug) | 60 | 300 |
| Riboflavin (ug) | 80 | 400 |
| Niacin(ug) | 30 | 1500 |
| B6-vitamin (ug) | 35 | 175 |
| Pantoténsav (ug) | 400 | 2000 |
| Folsav (ug) | 10 | 50 |
| B12-vitamin (ug) | 0,1 | 0,1 |
| Biotin (ug) | 1,5 | 7,5 |
| Egyéb összetevők | ||
| Cholin (mg) | 7 | 50 |
| Inositol (mg) | 4 | 40 |
| L-carnitin (mg) | 1,2 | NM |
RE: Retinol ekvivalens Img = 3,33 IU
Img a-TE (a-tocopherol ekvivalens) = 1mgd-a-tocopherol
NM = nem meghatározott
Anyatej-kiegészítő (követő, elválasztási, follow on, follow up 2-es, 3-as) tápszerek
Hat hónapos kor után a csecsemőknek un. követő tápszereket helyes adni, amelyek módosított összetételű tehéntejfehérje alapú tápszerek. Az összetételükre vonatkozó nemzetközi rendelkezéseket a 2 táblázat foglalja össze (25). A 2-es tápszerek 6 hónapos kortól, míg az ún. babatejek (3-as jelűek) 9 hónapos kortól javasolhatók. Ezekben a tápszerekben a tehéntejhez képest csökkentett a fehérje tartalom és magasabb a szénhidrát koncentráció. Ugyancsak a csecsemő igényeinek megfelelő a vitamin és ásványi anyag tartalma is. Mindegyik követő tápszert olyan mértékben dúsítják vassal, hogy abból a csecsemő szükségletének megfelelő vasfelszívódás biztosítva legyen. Optimális, ha a csecsemő életének második fél évében hozzávetőleg 500 ml követő tápszert kap naponta. Ezt a tápszert fel lehet használni tejhelyett a főzelékekelkészítéséhez is. A napi fél liternyi mennyiség nagyjából biztosítja a csecsemő vitamin és vas igényét is. A színtejre történő áttérés csak egy éves kor körül javasolt, alacsony zsírtartalmú tej adása azonban akkor sem ajánlott.
2. TÁBLÁZAT ESPGHAN ajánlás a követő (follow-on) tápszerek összetételére (per 100 kcal)
| ESPGAN | |
| Enerqia (kcal/100 ml) | 60-80 |
| Fehérje (q) | 3-4,5 |
| Zsír (q) | 4-6 |
| ebből linolsav (q) | 0,3 |
| Szénhidrát (q) | 8-12 |
| Vas (mq) | 1-1,7 |
| Cink(mq) | 0,5 |
| Jód (mikroqram) | 5 |
| A-vitamin (IU) | 200-600 |
| D-vitamin (IU) | 40-120 |
| E-vitamin (IU/q linolensav) | 0,5 |
A táblázatban meg nem adott ásványi anyagokat a tehéntej alapú követő tápszerekben olyan arányban kell csökkenteni, amilyen arányban csökkentik a tehéntejfehérje koncentrációját.
Az utóbbi években elterjedtek a prebiotikumot vagy probiotikumot tartalmazó tápszerek. A prebiotikum olyan nem emészthető élelmiszer-összetevő, amely elősegíti a kedvező hatású, az anyatejes csecsemőkéhez hasonló bélflóra kialakulását, mivel szelektíven stimulálja a bifidobaktériumok és a Lactobacillusok növekedését. A prebiotikumok leggyakrabban a rövid láncú, kis molekulasúlyú galakto-oligoszacharidok(GOS) és a hosszú láncú, nagy molekulasúlyú frukto-oligoszacharidok (FOS) keverékei.
A probiotikumok olyan nem-patogén mikroorganizmusok, amelyek a természetes környezetben is előfordulnak, részei a humán intestinalis mikroflórának, a szervezetre egészségvédő, jótékony hatást fejtenek ki azzal, hogy javítják az intestinalis mikrobiális egyensúlyt.
A pre- és probiotikumok előnyösen befolyásolják a bélflórát, a székelési szokásokat, a széklet konzisztenciáját, lerövidítik az infektív gastroenteritis (különösen rotavírus esetén) lefolyásának idejét. Az allergiás megbetegedések, kontrollált klinikai vizsgálatok az atopiás dermatitis gyors javulását igazolták alkalmazásuk esetén. Ezeknek a hatásoknak azért is nagy jelentősége van, mert az egészséges, heterogén mikroflóra kóros irányba való változásai számos betegséggel ok-okozati összefüggésbe hozhatók (pl. m. Crohn, pseudomembranosus, irradiációs colitis, obstipatio, NEC, szepsis stb.).
Speciális tápszerek alkalmazása
Fehérje hidrolizátumok
A hat hónapig tartó kizárólagos anyatejes táplálás jelentősen csökkenti a későbbi allergiás manifesztációkat. Abban az esetben, ha az anyatejes táplálás nem biztosítható és a családban atopiás betegség a szülőkben vagy a testvérekben előfordult, akkor szükséges prevenció céljából speciális tápszerek adása. Ezek az un. fehérje hidrolizátumok, amelyek tehéntejfehérjéből (casein vagy savófehérje), szarvasmarha vagy sertéskollagénből és szójafehérjéből. A protein hidrolízis mértéke szerint ezeket a készítményeket extenzíven, vagy részlegesen (parciálisan) hidrolizált készítményekre oszthatjuk fel. Az extenzíven hidrolizált készítmények túlnyomó részben 1500 Daltonnál kisebb polipeptideket tartalmaznak, a részlegesen hidrolizáltak pedig főként ennél jelentősen nagyobbakat, többnyire 1500 és 5000 Dalton molekulasúlyú polipeptideket. Tehéntejfehérje allergia esetén terápiás célból kizárólag csak az extenzíven hidrolizált készítmények alkalmazhatóak. Ebben az esetben csak azok a tápszerek megfelelőek, amelyeknek alkalmazása esetén a tejallergiás csecsemők legalább 90 %-a tünetmentes marad. Azoknak a tejallergiás csecsemőknek, akik az extenzíven hidrolizált tápszereket sem tolerálják, aminosav hidrolizátumokat tartalmazó készítmények adása indokolt (26). Allergia prevenciójára extenzíven és parciálisan hidrolizált termékek egyaránt adhatók, mivel egyértelmű különbség nincs preventív hatásuk között. Megjegyzendő azonban, hogy a kérdés végleges eldöntéséhez további nagyobb beteganyagon végzett összehasonlító vizsgálatokra van szükség (27).
Szója tápszerek
A korszerű szója alapú tápszerek szójafehérje izolátumot tartalmaznak, laktóz és így galaktózmentesek. A szója tápszerek összetételére speciális kritériumok vonatkoznak, amit a 3. táblázat mutat (28).
3. TÁBLÁZAT A szójatápszerek összetételének speciális kritériumai 100 kcal-ra vonatkoztatva
| Anyatejhelyettesít ő szójatápszerek | Követő szójatápszerek | |||
| Minimum | Maximum | Minimum | Maximum | |
| Fehérje (g) | 2,25 | 3,0 | 2,25 | 4,5 |
| Metionin (mg) | 29 | - | 29 | - |
| L-karnitin (umol) | 7,5 | - | - | - |
| Laktóz (g) | 3,5 | - | 1,8 | - |
| Vas (mg) | 1 | 2 | 1 | 2 |
| Cink (mg) | 0,75 | 2,4 | 0,75 | - |
| Foszfor (mg) | 30 | 100 | 30 | 100 |
A szója fehérjék biológiai értéke alacsonyabb, mint a tehéntejfehérjéje, ezért metionin szupplementációra is szükség van. Habára megfelelő kiegészítés után a szójatápszerek alkalmazásával kielégítő fejlődés érhető el a csecsemőkben, mégis használatukfitoösztrogén tartalmuk miatt nem indokolt széles körben. Napjainkban ezekneka tápszereknek az indikációs köre beszűkült. Alkalmazásuk feltétlenül indokolt galactosaemiában, amikor a laktóz nyomnyi mennyiségben is károsító hatású. Javasolt adásuk a hazánkban igen ritkán előforduló congenitalis primer alactasia esetén is. Végül fontos indikációs területe a szójatápszereknek, ha a szülők a vegetáriánus diétához ragaszkodnak. Tehéntejfehérje allergiában elsősorban az extenzív fehérje hidrolizátumot, vagy aminosav keveréket tartalmazó tápszerek alkalmazása indokolt a gyakran előforduló szója allergia miatt. Különösen gyakori a szója allergia tehéntejfehérje okozta enteropathiában és enterocolitisben. Szójatápszerek adása csupán IgE-mediált tejallergiában jöhet szóba, de csak hat hónapos kor után. Ilyen esetekben is elengedhetetlen a szójatápszer bevezetése előtt a szójaterhelés elvégzése. Szójatápszerek alkalmazása nem indokolt allergia prevenció céljából. A szójatápszerek adása nem javasolt koraszülöttekben sem (28,29).
irodalomjegyzék
1. WHO/UNICEF: Global Strategy on Infant and Young Child Feeding. Geneva Switzerland:World Health Organization 2003
2. Infant and Young Child Feeding: Standard Recommendations for the European Union, 2006 http://www.burlo.trieste.it/old_site/Burlo%20English%20version/Activities/research_develop.htm
3. Protection, promotion and support of breastfeeding in Europe: a blueprint for action (revised 2008) EU Project Contract N.SPC 2002359 http://ec.europa.eu/health/ph_projects/2004/action3/action3_2004_18_en.print.htm
4. Gartner LM, Morton J, Lawrence RA, Naylor AJ, O'Hare D, Schanler RJ, et al. American Academy of Pediatrics Section on Breastfeeding. Policy Statement (This policy is a revision of the policy posted on December 1,1997) Breastfeeding and the Use of Human Milk, Pediatrics. 2005;115:496-506. [PMID: 15687461] [Abstract/Free Full Text]
5. Leawood, KS: Breastfeeding (Position Paper), American Academy of Family Physicians. http://www.aafp.org/online /en/home/policy/policies/b/breastfeedingpositionpaper.html 2007
6. Agostini C, DecsiT, Fewtrell M et al. Complementary Feeding: Medical Position Paper, A Commentary by the ESPGHAN Committee on Nutrition Journal of Pediatric Gastroenterology and Nutrition, 2008;46:99-110
7. Lawrence RA Breastfeeding: a quide for the medical profession.6th ed. 2005.Mosby Inc
8. Hale & Hartmann: Textbook of Human Lactation 1st ed. 2007 Hale Publishing, AmarilloTx
9. Ip S, Chung M, Raman G, Chew P, Magula N, DeVine D,et al. Breastfeeding and Maternal and Infant Health Outcomes in Developed Countries. Evidence Report/Technology Assessment no. 153. (Prepared by Tufts-New England Medical Center Evidence-based Practice Center, under contract no. 290-02-0022.) AHRQ Publication no. 07-E007. Rockville, MD: Agency for Healthcare Research and Quality; 2007.www.ahrq.gov/downloads/pub/evidence/
10. Breastfeeding-Best For Baby. Best For Mom. Washington, DC: Department of Health and Human Services; 2007. Accessed at http://www.4women.gov/breastfeeding on 3 Sept. 2008
11. DeweyKG,Heinig MJ, Nommsen LA, Peerson JM, Lonnerdal B.: Growth of breast-fed and formula-fed infants from 0-18 months:the Darling study. Pediatrics 1992;89:1035-41 http://pediatrics.aappublications.org/cgi/content/abstract /89/6/1035
12. WHO Multicentre Growth reference Study Group. WHO Child Growth Standards based on length/height, weight and age. Acta Paediatr. 2006,76-85.
13. Kent JC: How breastfeeding works. J. Midwifery Womens Health 2007;52:564-570 http://www.breastbabyproducts.com /pdf/10_how_breastfeeding_works.pdf
14. Hill,PD, Johnson TS: Assessment of Breastfeeding and Infant Growth. J. Midwifery Womens Health 2007;52:571-578 http://www.medscape.com/viewarticle/565624
15. Gartner LM: Breastfeeding and jaundice. J Perinatol. 2001 Dec;21 Suppl 1:S25-9; discussion S35-9 http://www.nature.com /jp/journal/v21/n1s/pdf/7210629a.pdf
16. Management of Hyperbilirubinemia in the Newborn Infant 35 or More Weeks of Gestation Pediatrics 2004,114; 297-31
17. Szabó András: D-vitamin profilaxis, Módszertani levél, megjelenés alatt
18. Gyermekgyógyászati Útmutató 2008 Klinikai Irányelvek Kézikönyve. K-vitamin Profilaxis 186-188
19. Department of Health and HumanServices,CDC;http://www.cdc.gov/breastfeeding/index.htm
20. AzOEKMódszerteni Levele a 2007. évi Védőoltásokról Epinfo 14 évfolyam, 1. különszám, 2007. január 25.www.oek.hu
21. Gyermekgyógyászati Útmutató, Klinikai Irányelvek Kézikönyve. Mediton Budapest.
22. WHO:The optimal duration of exclusive breastfeeding. Report of an Expert Consultation. Geneva World Health Organization. 2001
23. Naylor AJ, ed. And Morrow A co-ed. 2001 Developmental Readiness of Normal Full Term Infants to Progress from Exclusive Breastfeeding to the Introduction of Complementary Foods: Reviews of the Relevant Literature Concerning Infant Immunologic, Gastrointestinal, Oral Motor and Maternal Reproductive and Lactational Development, Wellstart International and the LINKAGES Project/Academy for Educational Development, Washington
24. Koletzko B, Baker S, Cleghor G. et al. Global standard for the composition of infant formula: recommendation of and ESPGHAN coordinated international expert group. 2005,41,584-599.
25. Aggett PJ, Haschke F, Heine W. et al. Comment on the composition of cow's milk based follow-up formulas. ESPGAN Committee on Nutrition. Acta Paediatr Scand.1990,79,250-4.
26. VandenplasY, Brueton M, Dupont Cet al. Guidelines for the diagnosis and management of cow's milk protein allergy in infants. Arch Dis Child 2007, 92, 902-908.
27. Host A, Halken S, Muraro A. et al. Dietary prevention of allergic diseases in infants and small childen. Pediatr Allergy Immunol 2008,19,1-4.
28. Medical position paper. Soy protein infant formulae and follow-on formulae: A commentary by the ESPGHAN Committee on Nutrtion. J Pediatr Gastroenterol Nutr 2006,42,352-361.
29. Bhatia J, Greer F, Committee on Nutrition of American Academy of Pediatrics. Use of soy protein-based formulas in infant feeding. Pediatrics 2008,121,1062-1068.
30. Kent J: Breastfeeding patterns-the wide range of "normal". 3rd International Breastfeediung and Lactation Symposium, 4thNov. 2008, Manchester, UK
31. The Changing Concept of Sudden Infant Death Syndrome: Diagnostic Coding Shifts, Controversies Regarding the Sleeping Environment, and New Variables to Consider in Reducing Risk. AAP Policy Statement, Pediatrics 2005; 116:1245-1255)
32. Academy of Breastfeeding Medicine Protocol No6: Guideline on Co-sleeping and Breastfeeding, revised March 2008, http://www.bfmed.org/ace-images/Protocol6.pdf
33. Evidence for the ten steps to successful breastfeeding WHO, Divison of Child Health and Development 1998 http://www.who.int/nutrition/publications/evidence_ten_step_eng.pdf (A kiadvány magyar nyelvű kivonata: Bizonyítékok "A sikeres szoptatáshoz vezető tíz lépés"-hez, Egészségügyi Szakképző és Továbbképző Intézet, 2006)
34. The Breastfeeding Couple: Pacifiers and Breastfeeding http://www.breastfeedingbasics.org/cgi-bin/deliver. cgi/content /Normal/pacifiers.html
35. Academy of Breastfeeding Medicine Protocol No8: Human Milk Storage Information for home use for healthy full-term newborns, http://www.bfmed.org/ace-files/protocol/milkstorage_ABM.pdf
36. Proper Handling and Storage of Human Milk -Division of Nutrition and Physical Activity. National Center for Chronic Disease Prevention and Health Promotion (updated: May 2007), http://www.cdc.gov/breastfeeding/ recommendations/handling_breastmilk.htm
37. American Academy of Pediatrics AAP Policy Statement(This policy is a revision of the policy posted on January 1,1994. Committee on Drugs: The Transfer of Drugs and other Chemicals into Human Milk. Pediatrics 2001,108; 776-789
38. Breastfeeding and Maternal Medication WHO/UNICEF Recommendations for Drugs in the Eleventh WHO Model List of Essential Drugs 2002 p.1-43 http://whqlib.doc.who.int/hq/2002/55732.pdf
39. LACTMed National Library of Medicine, Database on Drugs and Lactation toxnet.nlm. nih.gov/cgi-bin/sis/htmlgen?LACT
A szakmai protokoll érvényessége: 2010. szeptember 30.
Mellékletek
A sikeres szoptatáshoz vezető 10 lépés (WHO/UNICEF)
A WHO és az UNICEF 1991-ben indította el a Bababarát Kórház Kezdeményezést. Az erre a címre pályázó szülészeti ellátást biztosító egészségügyi intézményeknek tíz pontnak kell eleget tenniük, be kell tartaniuk az anyatejhelyettesítők marketingjére vonatkozó Nemzetközi Kódex előírásait(30). A 2005-ben megjelent hazai Nemzeti Csecsemő-és Gyermekegészségügyi Program I./9 céljaként a Bababarát Kórház kezdeményezés szerepel.
1. LÉPÉS: A kórház rendelkezzen írásos szoptatási irányelvekkel, amelyeket rendszeresen ismertessenek az egészségügyi dolgozókkal.
2. LÉPÉS: Minden egészségügyi dolgozó kapjon megfelelő felkészítést az irányelvek alkalmazásához.
3. LÉPÉS: Tájékoztassanak valamennyi várandós nőt a szoptatás előnyeiről és gyakorlatáról.
4. LÉPÉS: Segítsék az anyákat, hogy az újszülöttet már a születést követő első félórában a mellükre tehessék.
Ez úgy értendő, hogy közvetlenül a megszületése után helyezzékaz újszülöttet bőrkontaktusba az anyjával, tartsák ott legalább egy óra hosszat és bátorítsák az anyát, hogy felismerje, mikor áll készen az újszülött a szopásra és ajánljanak fel segítséget, ha szükséges.
5. LÉPÉS: Mutassák meg az anyáknak, hogyan kell szoptatni és a tejelválasztást fenntartani, még akkor is, ha valamilyen okból el vannak különítve az újszülöttjüktől.
6. LÉPÉS: A csecsemő ne kapjon az anyatejen kívül más ételt vagy italt, amennyiben az orvosi szempontból nem indokolt.
7. LÉPÉS: Legyen általános gyakorlat az anya és az újszülött együttes elhelyezése (rooming-in) a nap 24 órájában.
8. LÉPÉS: Ösztönözzék az igény szerinti szoptatást.
9. LÉPÉS: A szoptatott csecsemőnek ne adjanak cumit.
10. LÉPÉS: Támogassák a szoptatást segítő anyacsoportok létrehozását és az egészségügyi intézményekből távozó anyákat irányítsák ezekhez.
Az utóbbi években elindult a "Bababarát Terület program., ami a bababarát területi ellátást célozza.
A szoptatás gyakorlata Bevezető
A szoptatás tanult készség, szemben a tej produkcióval, ami "természetes". Ezért rendkívül fontos, hogy az anya a várandósság alatt felkészüljön a szoptatásra, és tisztában legyen a szoptatás helyes gyakorlatával. A szoptatás pótolhatatlan előnyei indokolttá teszik, hogy a társadalom és ezen belül az egészségügy tegyen meg mindent a szoptatás védelme, elősegítése és támogatása érdekében. A szülők (a család) kapják meg a szükséges elméleti és gyakorlati ismereteket, továbbá támogatást, hogy önbizalmukés kompetenciájuk növekedjen a csecsemő táplálásában, gondozásában és nevelésében.
Ehhez elengedhetetlen az egységes szoptatási irányelvek oktatása és megvalósítása az egészségügyi rendszerben. Szükséges biztosítani a szakemberek ezirányú képzését és rendszeres továbbképzését, hogy a tudomány állásának megfelelő, bizonyítékokon alapuló ismeretekkel rendelkezzenek.
Helyes lenne minden anya-gyermek páros számára lehetővé tenni a szülés után az azonnali bőrkontaktust, annak segítését, hogy az első életórában az újszülött mellre helyezését, a csecsemővel való 24 órás együttes elhelyezést (rooming-in rendszert), szoptatás-támogató csoportok létrehozását ill a hazaadott anyák számára biztosítani a szoptatással kapcsolatos tanácsadás lehetőségét.
Felkészülés a szoptatásra
A leendő szülőkkel, általában a magzatmozgás észlelését követően, meg kell beszélni, hogy milyen módon kívánják majd gyermeküket táplálni (8). Ezirányú döntésük meghozatalában joguk van a megfelelő információhoz. A sikeres szoptatást bizonyítottan elősegíti, ha az anya a várandósság során megfelelő tájékoztatást kap a szoptatás előnyeiről és gyakorlatáról (l.Bababarát Kórház Kezdeményezés 3. Lépés).
A szoptatásra való felkészítésre írásos tájékoztató anyagok kiosztása önmagában nem elég hatékony módszer, erre a legalkalmasabbak a szoptatás mellett elkötelezett szülésre felkészítő tanfolyamok. A szülés előtti felkészítésnek komplex információkat kell tartalmaznia. A várandós nőnek segítséget jelent, ha részt vehet moderált csoportos beszélgetéseken, vagy ha egy laikus támogató csoporthoz irányítják őket a szülés előtt (2)
Az emlő várandósság alatti vizsgálata kiváló alkalmat ad a szoptatás megbeszélésére. Az anyát biztosítani kell arról, hogy a nők mindenféle alakú és méretű mellből és bimbóval képesek sikeresen szoptatni..
Az emlőbimbó bármiféle módszerrel való felkészítése nem segíti elő a szoptatás sikerét, viszont elbizonytalaníthatja az anyát és az érzékeny szövetek sérülését okozhatja.
Korábban lapos vagy befelé fordult mellbimbó esetén javasolt eljárások, mint az utolsó trimeszterben melltartóban viselt bimbókiemelő vagy a Hoffmann gyakorlat ( a bimbó alapjának nyomása és kihúzása) az újabb kutatások tanúsága szerint nem járulnak hozzá a szoptatás sikeréhez és koraszülés hajlam esetén a bimbó manipulálása méhösszehúzódásokat válthat ki, ezért nem javasoltak. (7)
Lapos vagy befelé fordult emlőbimbó esetén megnyugtathatjuk az anyát, hogy a csecsemő nem a bimbót, hanem a mellet szopja, azonban különös figyelmet kell fordítni arra, hogy a mellretapadás során az areola alatti területből megfelelő mennyiségű mellszövet kerüljön a csecsemő szájába. A szülés után a szoptatások előtt a lapos vagy befelé fordult emlőbimbót legtöbbször gyengéd szívásra állított mellszívóval sikeresen ki lehet húzni. Figyeljünk arra, hogy nincs-e az anya emlőin valamilyen anatómiai rendellenesség vagy sebészi beavatkozás jele. Ha a várandós korábban mellműtéten esett át vagy olyan betegségben szenved, ami befolyásolhatja a szoptatási képességét, hasznos lehet már a szülés előtt konzultálni orvossal vagy laktációs szaktanácsadóval, és kidolgozni egy olyan tervezetet, amelynek megvalósítását a szüléskor el lehet kezdeni
Az emlőbimbó korábbi időkben alkalmazott "edzése" nem javasolt. A kutatások azt igazolják, hogy a bimbósérülés elsődleges oka a helytelen pozíció és mellre helyezés.
A várandósság alatt termelődött colostrum kipréselése nincs hatással a későbbi tejelválasztásra, azonban a fejés okozta stimuláció megindíthatja a vajúdást, ezért nem ajánlott.
Az emlő ápolása a szoptatás alatt
A megfelelő napi tisztálkodás, illetve szükség esetén melegvizes lemosás elegendő, tekintettel arra, hogy a bimbóudvar területén található Mongomery mirigyek terméke védelmet nyújt. Szoptatás után a bimbó-bimbóudvar területének egy kevés lefejt tejjel történő bemasszírozása javasolt és lehetőleg a mellet addig hagyjuk szabadon,amíg a tej rá nem száradt.
A fertőtlenítő oldatok és szappan túlzott használata a bimbósérülés előfordulását fokozhatja. A krémek, olajok, ecsetelők alkalmazása is hatástalannak bizonyulnak a bimbósérülések megelőzésében, kezelésében.
A helyes mellrehelyezésre és mellretapadásra kell fokozottan odafigyelni, ugyanis a helyes szoptatási technikával a szoptatás során fellépő szövődmények (emlőbimbó kisebesedés, tejvezeték elzáródás, mastitis stb) nagyrészt kivédhetőek.
A szoptatás módja
Alapvető fontosságú, hogy a szoptatások nyugalomban teljenek és kellemes élményt nyújtsanak az anya és a gyermeke számára. Az anyát meg kell tanítani a helyes szoptatási technikára, hogy szorongásmentesen, kellő önbizalommal tudjon szoptatni.
1. Az anya és csecsemő elhelyezkedése a szoptatáshoz
Az anya és csecsemő ruházata legyen kényelmes, nem korlátozó.
Szoptatni legkényelmesebb ülve vagy fekve. Ülő helyzetben többféle módon tehetjük mellre a csecsemőt; bölcső-, kereszt-, hónalj-tartásban, nagyobb csecsemőket lovagló-tartásban.
Az anyának legyen támasztéka, ne dőljön hátra, vagy ne hajoljon előre. A csecsemő legyen megfelelően alátámasztva, feje ne a könyökhajlaton, hanem az alkaron nyugodjon.
Az anya tartsa a csecsemőt testközelben, mellmagasságban maga felé fordítva, úgy, hogy a csecsemő szája legyen egy magasságban a mellbimbóval, és lehetőség legyen a szemkontaktusra. A csecsemő füle, válla, csípője legyen egyvonalban.
2. Helyes mellrehelyezés
A helyes mellrehelyezés elengedhetetlen ahhoz, hogy a csecsemő hatékonyan szopjon, és hogy a bimbósérüléseket megelőzzük. A mell megtámasztásánál ügyelni kell arra, hogy az "C" alakban történjen (hüvelykujja bimbóudvar felett, a többi ujjaz emlő alatt) és nem a nálunk hagyományos "olló" tartásban. Így biztosítható a megfelelő mellre tapadás. Megérintve a gyermek ajkát a mellbimbóval, meg kell várni, míg nagyra nyitja a száját (mintha ásítana), majd az anya határozott mozdulattal húzza magához a csecsemőt az alsó ajkat a bimbóudvar alsó széle felé irányítva.
3. Helyes mellretapadás jelei
- a bimbó körüli területből legalább 2,5 cm-t a szájába vesz, a bimbóudvarból több látszik a felső ajak felett
- száját szélesre tátja (a szájzug 100o-nál nagyobb szöget zár be)
- ajkai kifelé fordulnak
- nyelve a mell alatt van, és félkörben simul a mellhez
- fejét enyhén hátrahajtja, állával nekitámaszkodik a mellnek, orrhegye érinti az emlőt, az orrnyílások szabadok.
4. A hatékony szopás jelei A csecsemőnél
- ritmikusan szopik (présel, szív, nyel), az állkapocs izmainak mozgása kiterjed a fülekig, olykor a fülcimpa is mozog
- az orcák kitöltöttek; nem horpadnak be
- hallhatóan/láthatóan nyel, nem nehezített a légzése
- fenti jelek legalább 5-10 percig észlelhetőek
- nem szorítja ököllbe a kezét, ellazult testtartást vesz fel
- nedves a szája (tejcsöppek)
- a csecsemő magától engedi el a mellet, szoptatás után elégedett
Az anyánál
- az oxytocin reflex jelei észlelhetőek, szomjúságérzet, ellazult érzés, álmosság, méhösszehúzódások, az első 3-5 napban bőséges lochia ürül a szopás közben és után
- tejcsepegés a másik mellből
- az anya kényelmesen érzi magát, nem érez fájdalmat a mellében
- ellazult érzés, álmosság
- csökken a mell telítettségérzete
- szoptatás után a mellbimbó kicsit megnyúlik, de nem deformált, nem sebes
A helyes szoptatási technikával nagyrészt kivédhetőek a szoptatás során fellépő szövődmények (emlőbimbó kisebesedés, tejvezeték elzáródás, mastitis stb).
5. Igény szerinti szoptatás
Az első 6 élethónapban kívánatos kizárólagos szoptatás eléréséhez elengedhetetlen, ugyanis a tejtermelést a kereslet-kínálat elve szabja meg.
Az igény szerinti szoptatás azt jelenti, hogy az édesanya mindig mellre teszi csecsemőjét, amikor az jelzi, hogy szopni szeretne és nem korlátozzuk sem a szoptatások gyakoriságát sem az időtartamát. Az édesanyát meg kell tanítani a korai éhségjelek felismerésére. Ezek a következők:
- gyors szemmozgások láthatók a szemhéja alatt
- éberség vagy fokozott aktivitás
- a csecsemő szopó mozgásokat végez
- cuppog
- lágy gügyögő hangokat hallat vagy sóhajtozik
- kezét szájához viszi
- nyugtalanná válik
A sírás késői jel, ezért biztassuk az anyát, hogy ne várja meg, amíg a csecsemő sírni kezd, mert olyankor sokkal nehezebb mellre tenni.
A szopásoknakcsak egy része szolgálja a táplálkozást (nutritív szopás), a többi a csecsemő megnyugtatására szolgál (non-nutritív szopás, komfort szopás). A csecsemő sírás a kommunikáció egy módja, tudni kell, hogy a sírást nemcsak az éhség, hanem fájdalom, diszkomfort, frusztráció is kiválthatja.
A jól szopó csecsemő 24 óra alatt legalább 8x, átlagosan 11 x szopik. A szopások időtartama kezdetben hosszú, a csecsemő korának előrehaladtával csökken, 4-6 hónapos korban akár 5 percre is redukálódhat.
Nemcsak a szopások hossza, hanem a szopások között eltelt idő is változó. A csecsemők döntő többsége délelőtt alszik egy hosszabbat, a késő délutáni-esti órákban pedig rendkívül gyakran, akár félóránként szopni akar. Bátorítsuk az anyát, hogy ez normális, csakúgy, mint az anyatejmennyiségének és zsírtartalmának napszakos változása.
Az újszülöttek döntő többsége igényli az éjszakai szopást és még a hatodik élethónapban is a csecsemők több mint fele szopik éjszaka (30).
Jelentős részük nem nappal, hanem éjjel veszi magához az anyatejnagy részét. 3-4 hónapos kortól kezdve az a csecsemő is gyakrabban ébredhet és kéredzkedhet mellre, aki korábban átaludta az éjszakát. Ez életkori sajátosság, ami a csecsemő fejlődésével van összefüggésben és nem jelenti az anyatejmennyiségének elégtelenségét. Az éjszakai szoptatások szükségessége miatt célszerű a csecsemőt az anya szobájában elhelyezni. Az együttalvás definíciójából következik (olyan szoros közelségben aludni a csecsemővel, hogy lehetőség legyen szenzoros jeladását észlelni és arra reagálni), hogy az egy ágyban alvás az együttalvás egy lehetséges, de nem egyedüli módja.
Az együttalvásnak az a formája, amikor a csecsemő fekhelye az anyával egy szobában, az anya közelében, lehetőleg tőle karnyujtásnyira van, több szempontból is pozitív hatású; a gyakori éjszakai szoptatás kevésbé fárasztó az anya számára továbbá az anya és a csecsemő egymás közelében alvása csökkenti a bölcsőhalál kockázatát (31). Az egy ágyban alvással kapcsolatban az utóbbi években számos ellentmondás merült fel, azonban egyre inkább körvonalazódnak azok a feltételek, amelyek betartásával az egy ágyban alvás biztonságosnak látszik (32).
6. A szoptatás és a nyugtató cumi (4,33, 34)
A szoptatás sikeréhez az is szükséges, hogy a csecsemő legalább az első élethónapban ne kapjon nyugtató cumit. (Bababarát Kórház Kezdeményezés 9.lépés).
Összefüggés van a cumi használat és az otitis media, a későbbi fogproblémák (malocclusio) megnövekedett kockázata továbbá a szoptatás rövidebb tartama között. A cumi használatnak a szoptatás időtartamát csökkentő hatása dózisfüggő. A négy hetes kor után kezdett nyugtató cumi használat a vizsgálatokalapján úgy tűnik, hogy nem befolyásolja a szoptatás időtartamát (34), azonban semmi esetre sem szabad a csecsemőre erőltetni a cumi használatát.
A cumi használat bármely életkorban felveti a szoptatási probléma lehetőségét, de a vizsgálatok alapján úgy tűnik, hogy ezek különösen gyakoriak és súlyosak lehetnek akkor, ha a cumi bevezetésére már az első élethónapban sor kerül. Ezért a cumit használó anyának külön támogatásra és tanácsadásra van szüksége.
7. Az emlő fejése (7)
Ha az anya igény szerint szoptat, fejésre csak bizonyos esetekben lehet szüksége, amelyek a következők:
1. Anyatejgyűjtése
- ha a csecsemő beteg vagy koraszülött
- ha nincs együtt az anya és a csecsemő
- ha az anya visszatér a munkahelyére
- tárolás céljából
- donor anyatej leadása céljából
2. A szoptatás kezdetén, hogy meginduljon a tej áramlása
3. A mell teltségénekcsökkentésére túltelítődés, tejcsatorna elzáródás és mastitis esetén
4. A tejképződés fokozása céljából, ha a csecsemőnek szopási nehézsége van
5. A tej eltávolítása céljából, ha specifikus gyógyszer szedése miatt a csecsemő nem zoptatható.
A kézi fejés módját minden szoptató anyának meg kell tanulnia.
( A sikeres szoptatáshoz vezető Bababarát Kórház Kezdeményezés 5.lépése).
A kézi mellszívók és elemmel működtetett, vagy elektromos fejőgépek széles választéka kapható, azonban legtöbbjüknek vannak hátrányai az ideális mellszívóval támasztott elvárások tükrében. Az ideális mellszívó képes a mellet kiüríteni és a tejtermelést stimulálni, tiszta, nem kontaminált, könnyű a használata, nem drága és atraumatikus. A mellszívókat és fejőgépeket használat előtt fertőtleníteni kell.
8. A lefejt anyatejtárolása
Frissen lefejt anyatejtárolása az egészséges érett csecsemő számára otthoni használatra (35, 36)
| Hol? | Hőmérséklet | A felhasználhatóság tartama | Megjegyzés |
| Asztalra helyezve | Szobahőmérsékleten Max 25 C° | 6-8 óra | A tárolóedényt le kell fedni és a lehető legalacsonyabb hőmérsékleten tartani |
| Hűtőtáska | 4-15C° | 24 óra | A hűtőelemet tartsuk közvetlenül a tej mellett és kerüljük a táska nyitását |
| Hűtőszekrény | 4C° | 5 nap | Tároljuk a tejet a hűtőszekrény hátsó részén |
| Fagyasztó | |||
| Fagyasztó tér a hűtőszekrényen belül | -15 C° | 2 hét | Tároljuk a tejet a fagyasztó hátsó részén, ahol a legstabilabb a hőmérséklet. Az így tárolt tej biztonságos, de egyes lipidek degradálódnak és gyengébb minőségűek |
| Fagyasztó tér a hűtőszekrényen belül külön ajtóval | -18 C° | 3-6 hónap* | |
| Mélyhűtőláda vkülönálló mélyhűtő szekrény (manuális leolvasztású) | -20 C° | 6-12 hónap | |
*3 hónap automatikusan leolvasztó mélyhűtő esetén
A fenti ajánlások nem vonatkoznak a koraszülött, beteg csecsemők számára vagy donor anyatej céljára gyüjtött tej kezelésére és tárolására.
9. Donor női tej
Magyarországon a donor anyatejgyüjtését és elosztását Anyatejgyűjtő Állomások végzik. Amennyiben a szoptatás és lefejt anyatej adása nem lehetséges, meghatározott feltételek teljesülése esetén a jelenleg érvényben levő 47/1997. (XII. 17.) NM rendelet térítés mentes anyatej ellátására ad lehetőséget
(1.§a koraszülött, kis súlyú újszülött továbbá az érett újszülött és csecsemő, ha súlyos táplálkozási allergiában, felszívódási zavarban, hasműtéttel járó fejlődési rendellenességben szenved és az anya saját tejével táplálni nem tudja.,
2§ ha az anya fizikailag alkalmatlan az anyatejjel történő táplálásra, olyan fertőző betegségben vagy mérgezésben szenved, amely a csecsemő egészségét veszélyezteti, olyan gyógyszert szed, amely szedése a szoptatás időszakában ellenjavallt, súlyos, gyakori tudatvesztéssel járó állapotban van, pszichés állapota a szoptatást lehetetlenné teszi)
3. MELLÉKLET
Szoptatás és gyógyszerek Bevezetés (7,8,37)
A szoptatás felfüggesztésének gyakori oka az anya gyógyszerszedése, mert ezt tanácsolja a gyógyszert felíró orvos. A legtöbb esetben ez a tanács nem indokolt. Az alábbiakban közölt adatok és irodalmi hivatkozások azt célozzák, hogy ellássák az orvosokat a gyógyszer anyatejbe történő kiválasztásával kapcsolatos ismeretekkel. A legtöbb, szoptatott anyánakfelírt gyógyszernek nincs hatása a csecsemő egészségi állapotára és a tejtermelésre. Ez az információ nemcsak azt szolgálja, hogy a csecsemőt védje az esetleges nem-kívánatos gyógyszerhatásoktól, hanem hogy lehetővé tegye a szoptató anya hatékony gyógyszeres kezelését.
Az anyai gyógyszerek a csecsemőre gyakorolt lehetséges hatásuk mellett befolyásolhatják a tejtermelést, csökkentve vagy növelve azt.
Ahhoz, hogy a gyógyszer megjelenjen az anyatejben, el kell érnie az anyai keringést, majd pedig ki kell választódnia a tejbe. Ehhez át kell haladnia számos lipoprotein membránon. Ez, ritka kivételektől eltekintve, passzív diffúzióval történik. A teljes gyógyszermennyiségnek csak a plazmafehérjékhez nem kötődő, és nem ionizált szabad hányada diffundál az anyatejbe. A transzfer a legnagyobb, ha a gyógyszernek alacsony a kötődése az anyai plazma fehérjékhez ill magas a zsíroldékonysága. Az anyatejbe való átjutást a gyógyszerek egyéb fizikokémiai tuljadonságai - mint pl. a molekulaméret vagy az ionizáltság foka a plazmában- is befolyásolják. Mivel a tej enyhén savasabb a plazmánál, a gyengén alkalikus vegyületek könnyebben jutnak be az anyatejbe. Minthogy a tej összetétele az egyes etetések során ill. etetésenként változik, ez is befolyásolhatja a gyógyszer transzfert (a zsírdúsabb "hátsó" tejben magasabb a zsírtartalom és igy abban koncentrálódhatnak a zsíroldékony gyógyszerek). Általánosságban elmondható, hogy azok a gyógyszerek, melyeknek magas a fehérjekötődése, nagy molekulasúlyúak és alacsony a zsíroldékonyságuk, nem mennek át klinikailag jelentős mmennyiségben a tejbe. Lehetséges a gyógyszer retrográd diffúziója az anyatejből az anyai plazmába, akkor is ha az anya nem ürítette ki a mellét.
A gyógyszer transzfert az anyatejbe leggyakrabban a tej/plazma aránnyal (M/P= milk/ plazma ratio) jellemzik.
A legtöbb anya által szedett gyógyszer átmegy az anyatejbe, rendszerint az anyai dózis kevesebb, mint 5%-a, azonban legtöbb esetben a csecsemő által igy fogyasztott kis dózis klinikailag nem szignifikáns.
Alapvetően azt, hogy a szoptatott csecsemő milyen gyógyszerhatásnak van kitéve, a gyógyszer koncentrációja a tejben és a csecsemő által elfogyasztott tejmennyiség határozza meg. A gyógyszer farmakológiai aktivitása pedig függ attól, hogy milyen a gyógyszer felszívódása, metabolizmusa és disztribúciója a csecsemőben.
Például, ha csökken a csecsemő metabolizmusa csökkent májenzim működés miatt vagy csökkent a vesén át történő kiválasztás az alacsonyabb glomerularis filtrációs ráta miatt, ez a gyógyszer felhalmozódásához vezethet.
A jelenleg rendelkezésre álló információ nagy része egyedi esetleírásokból származik. Gyakran úgy végeznek tanulmányokat, hogy egyetlen adagot adnak be, ami nem a valós helyzetet tükrözi.
Kevés olyan gyógyszer van, ami a szoptatás abszolút ellenjavallatát képezi (1. Táblázat).
Szerencsére legtöbb esetben az anyai gyógyszer fogyasztása mellett folytatható a szoptatás.
A szoptató anya gyógyszerszedésével kapcsolatos általános elvek
- ne használják a gyógyszer elhúzódó hatású formáját,
- olyan gyógyszer kiválasztása az azonos hatású gyógyszerek közül, ami legkisebb mennyiségben választódik ki a tejbe,
- a gyógyszer adása a legkisebb hatásos adagban történjen,
- az anya a gyógyszert közvetlenül a szoptatás után vegye be,
- a csecsemő megfigyelése; vannak-e gyógyszer mellékhatásra utaló szokatlan jelek vagy tünetek.
A szoptatással kapcsolatos gyógyszer osztályozás többféle módon történhet:
- Aszerint, hogy a gyógyszer átmegy-e a tejbe
- Aszerint, hogy a szoptatás mellett a gyógyszer ellenjavallt, felfüggesztendő, aggályos, óvatosan adható, kompatibilis (Amerikai Gyermekgyógyász Akadémia)
- Kórállapotok szerint értékelik a gyógyszerek biztonságát a szoptatás mellett, pl WHO Osztályozás (38)
Az egyes gyógyszerek és egyéb vegyi anyagok kiválasztása az anyatejbe. Alkalmazásuk szoptatós anyáknál.
Az Amerikai Gyermekgyógyászati Akadémia hangsúlyozza, hogy amennyiben valamely gyógyszer nem található meg a táblázatban, az nem jelenti azt, hogy nem megy át az anyatejbe és nincs hatása a csecsemőre, csupán azt, hogy ezekkel kapcsolatban nem volt fellelhető irodalmi hivatkozás.
A National Medical Library hozzáférhető szolgáltatatása, a LACTMED, melynek weboldalán az egyes gyógyszerek kereshetők (39)
1. TÁBLÁZAT Gyógyszerek, amelyek hatást gyakorolhatnak szoptató csecsemő sejtanyagcseréjére, szedésük esetén a szoptatás ellenjavallt
| Gyóqyszer | Az aggodalom oka, a csecsemőnél kiváltott tünetek vagy a laktációra gyakorolt hatás | |||
| Cyclophosphamid | Potenciális immunszuppresszív hatás; nem ismert a hatása a növekedésre és összefüggése a carcinogenezissel; neutropenia. | |||
| Cyclosporin | Potenciális immunszuppresszív hatás; nem ismert a hatása a növekedésre és összefüggése a carcinogenezissel; | |||
| Doxorubicin* | Potenciális immunszuppresszív hatás; nem ismert a hatása a növekedésre és összefüggése a carcinogenezissel; | |||
| Methotrexat | Potenciális immunszuppresszív hatás; nem ismert a hatása a növekedésre és összefüggése a carcinogenezissel; neutropenia. | |||
| *A gyógyszer az anyatejben koncentrálódik | ||||
| 2. TÁBLÁZAT Drog abususok | ||||
| Drog | Hatás a csecsemőben | |||
| Amphetamin | Irritabilitas, alvászavar | |||
| Kokain | Kokain intoxikáció: irritábilitás, hányás, hasmenés, tremor, görcsök | |||
| Heroin | Tremor, nyugtalanság, hányás, rossz étvágy | |||
| Marihuana | Hatása nem ismert, egyes komponensek felezési ideje hosszú | |||
| Phencyclidin | Potens hallucinogen | |||
Az AAP Gyógyszerbizottságának szilárd meggyőződése, hogy a szoptató anya ne használjon drogokat, mert azok veszélyeztetik a szoptatott csecsemőt és az anya egészségét
A dohányzás nem ellenjavallata a szoptatásnak, de az egészségügyi dolgozók tanácsoljáka dohányzó anyáknak, hogy kerüljék a dohányzást a lakásban és tegyenek meg mindent azért, hogy a lehető leggyorsabban szokjanak le a dohányzásról.
Szoptató anyák kerüljék az alkoholfogyasztást, mivel az alkohol koncentrálódik az anyatejben és gátolhatja a tejtermelést. Ritka ünnepi alkalmakkor egyetlen kis mennyiségű alkoholos ital fogyasztása elfogadható, de az anya az ital fogyasztása utáni két órában ne szoptasson (4)
3. TÁBLÁZAT Rádióaktív vegyületek, melyek a szoptatás átmeneti felfüggesztését teszik szükségessé
| Radioaktív vegyület | Az anyatejes táplálás felfüggesztésének ajánlott időtartama (az anyatejben észlelhető radioaktivitás időtartama alapján) |
| Réz 64 | 50 óra |
| Gallium 67 | 2 hét |
| Indium 111 | 24 óra |
| Jód 123 | 36 óra |
| Jód 125 | 12 nap |
| Jód 131 | 2- 14 nap (különböző tanulmányok szerint) |
| Radioaktív nátrium | 96 óra |
| Technetium- 99m, (99m Tc) 99mTc macroaggregatum, 99mTcO4 | 15 -72 óra hosszat mutathatók ki a tejben |
A vizsgálat előtt helyes konzultálni a radiológussal, hogy olyan izotópot használjon, aminek az anyatejbe történő kiválasztása a legalacsonyabb. Érdemes lefejt tejet félretenni arra az időszakra, amíg az anyatejes táplálás nem lehetséges. A szoptatás felfüggesztése alatt helyes, ha az anya a tejét lefeji, hogy így biztosítsa a tejtermelés fenntartását, ezen időszakban lefejt tejet ki kell önteni. A szoptatás megkezdése előtt szóbajön a tej radioaktivitásának ellenőrzése.
4. TÁBLÁZAT Gyógyszerek, amelyeknek a hatása a szoptatott csecsemőkre nem ismert
| Gyógyszer | Közölt, vagy lehetséges mellékhatások |
| Anxiolitikumok | |
| Alprazolam | Nem ismert |
| Diazepam | Nem ismert |
| Lorazepam | Nem ismert |
| Midazolam | Nem ismert |
| Perphenazin | Nem ismert |
| Prazepam** | Nem ismert |
| Quazepam | Nem ismert |
| Temazepam | Nem ismert |
| Antidepresszánsok | |
| Amitriptylin | Nem ismert |
| Amoxapin | Nem ismert |
| Bupropion | Nem ismert |
| Clomipramin | Nem ismert |
| Desipramin | Nem ismert |
| Dothiepin | Nem ismert |
| Doxepin | Nem ismert |
| Fluoxetin | Kólika, irritabilitás, evés és alvászavar, lassú súlyfejlődés |
| Fluvoxamin | Nem ismert |
| Imipramin | Nem ismert |
| Nortriptylin | Nem ismert |
| Trazodon | Nem ismert |
| Paroxetin | Nem ismert |
| Sertralin** | Nem ismert |
| Trazadon | Nem ismert |
| Antipsychoticumok | |
| Chlorpromazin | Galactorrhea az anyában, kábultság és lethargia a csecsemőben, a fejlődési mutatók rosszabbak |
| Chlorprothixen | Nem ismert |
| Clozapin** | Nem ismert |
| Haloperidol | A fejlődési mutatók rosszabbak |
| Mesoridazin | Nem ismert |
| Trifluoperazin | Nem ismert |
| EGYÉB GYÓGYSZEREK | |
| Amiodaron | Hypothyroidismust okozhat |
| Chloramphenicol | Csontvelő szuppressziót okozhat |
| Metoclopramid** | Nem írtak le káros mellékhatást, dopaminerg blokkoló hatás |
| Metronidazol | In vitro mutagén, amennyiben az anyának egyszeri adása szükséges, célszerű a szoptatást 12-24 órára felfüggeszteni |
| Tinidazol | Ld. metronidazol |
A psychotrop gyógyszerek, melyek az anxiolytkum, antidepresszáns és antipszichotikus gyógyszer felsorolásban szerepelnek, különösen akkor adnak okot aggodalomra, ha a szoptató anyának hosszú ideig adják. Bár nagyon kevés esetismertetésben számolnak be káros mellékhatásokról a szoptatott csecsemőben, mivel ezek a gyógyszerek megjelennek az anyatejben, rövid és hosszútávú hatásuk lehet a központi idegrendszerre. A ** -gal jelölt gyógyszereknek az anyai plazmaszinthez viszonyítva magas a koncentrációja az anyatejben
5. TÁBLÁZAT Gyógyszerek, amelyeknek szignifikáns hatása lehet a szoptatott csecsemőkre, s ezért csak elővigyázatossággal adhatók a szoptató anyáknak
| Gyógyszer | Leírt hatás |
| Acebutolol | Hypotensio, bradycardia, tachypnoe |
| 5-Aminosalicyl sav | Hasmenés (1 esetleírás) |
| Atenolol | Cianózis, bradycardia |
| Aspirin (szalicilátok) | Metabolikus acidosis (1 esetleírás) |
| Clemastin | Aluszékonyság, irritabilitás, étvágytalanság, éles sírás, tarkókötöttség (1 esetleírás) |
| Ergotamin | Hányás, hasmenés, convulsio (migrén esetén használatos dózisnál) |
| Lithium | Potenciális lithium toxicitás (a csecsemőbe a terápiás dózis egyharmada-fele mehet át) |
| Phenindion | Anticoaguláns, megnövekedett prothrombin és partialis thromboplastin időt irtak le egy csecsemőben, |
| Phenobarbital | Aluszékonyság, elválasztás után colica jelentkezhet, methemoglobinemia (1 esetleírás) |
| Primidon | Aluszékonyság, etetési problémák |
| Sulfasalazin (salicylazosulfapyridine) | Véres hasmenés (1 esetleírás) |
6. TÁBLÁZAT Anyai gyógyszerek, melyek általában kompatibilisek a szoptatással +
| Gyógyszer, vagy gyógyszercsoport | Tünetek, amit leírtak a csecsemőkben, hatásuk a laktációra |
| Acetaminophen | Nincs |
| Acetazolamide | Nincs |
| Acitretin | - |
| Acyclovir | Nincs |
| Alcohol (ethanol) | Nagy mennyiség aluszékonyságot, mély alvást, gyengeséget okoz, csökkenti a növekedést és a súlyfejlődést; 1 g/kg/nap-nál több fogyasztása csökkenti a tej leadó reflexet |
| Allopurinol | - |
| Amoxicillin | Nincs |
| Antimon | - |
| Atropin | Nincs |
| Azapropazon (apazon) | - |
| Aztreonam | Nincs |
| B1 (thiamin) | Nincs |
| B 12 | Mincs |
| Baclofen | Nincs |
| Barbiturátok | ld. 5. táblázat |
| Bendroflumethiazid | Csökkenti a tejtermelést |
| Bromid | Kiütés, gyengeség és a sírás hiánya, ha az anya többet szed napi 5.4 g-nál |
| Butorphanol | Nincs |
| Koffein | Irritabilitás, álmatlanság, lassan vélasztódik ki, nincs hatása mérsékelt koffeinfogyasztás (2-3 csésze/nap) esetén |
| Captopril | Nincs |
| Carbamazepin | Nincs |
| Carbetocin | Nincs |
| Carbimazol | Strúma |
| Cascara | Nincs |
| Cefadroxil | Nincs |
| Cefazolin | Nincs |
| Cefotaxim | Nincs |
| Cefoxitin | Nincs |
| Cefprozil | - |
| Ceftazidim | Nincs |
| Ceftriaxon | Nincs |
| Chloral hydrat | Aluszékonyság |
| Chloroform | Nincs |
| Chloroquine | Nincs |
| Chlorothiazid | Nincs |
| Chlorthalidon | Lassan ürül ki |
| Cimetidin* | Nincs |
| Cisaprid | Nincs |
| Cisplatin | Az anyatejben nem mutatható ki |
| Clindamycin | Nincs |
| Cloqeston | Nincs |
| Codein | Nincs |
| Colchicin | - |
| Contraceptív tabletta (esroqen/proqesteron) | Ritkán mellmegnagyobodás, csökkenti a tejtermelést és a tejfehérjetartalmát (számos tanulmány nem erősítette meg ezt a hatást) |
| Cycloserin | Nincs |
| D-vitamin | Nincs (ellenőrizzük a csecsemő szerum calcium szintjét, ha az anya farmakológiai dózist kap) |
| Danthron | Fokozott bél motilitás |
| Dapson | Nincs (szulfonamid mutatható ki a csecsemő vizeletében) |
| Dexbrompheniramin maleat d-isoephedrinnel | Sírás, irritabilitás, rossz alvás |
| Diatrizoat | Nincs |
| Diqoxin | Nincs |
| Diltiazem | Nincs |
| Dipyron | Nincs |
| Disopyramid | Nincs |
| Domperidon | Nincs |
| Dyphylline * | - |
| Enalapril | Nincs |
| Erythromycin* | Nincs |
| Estradiol | Megvonásakor vaginális vérzés |
| Ethambutol | Nincs |
| Ethanol (ld alcohol) | ld. alcohol |
| Ethosuximid | Nincs, a gyógyszer kimutatható a csecsemő szérumában |
| Dicumarol | Nincs |
| Fentanyl | - |
| Fexofenadin | Nincs |
| Flecainid | - |
| Flufenamic acid | Nincs |
| Fluorescein | - |
| Folic acid | Nincs |
| Gadopentetic(Gadolinium) | Nincs |
| Gold salts (Arany sók) | Nincs |
| 6. Táblázat Folytatása | |
| Halothan | Nincs |
| Hydralazin | Nincs |
| Hydrochlorothiazid | - |
| Hydroxychloroquin | Nincs |
| Ibuprofen | Nincs |
| Indomethacin | Egyesetben leírtakconvulsiót |
| Jodid | Befolyásolhatja a pajzsmirigy működését, l. jód |
| Jód | Strúma. |
| Iodin (povidon-iodin pl. hüvelyöblítés) | Emelkedett iodine szint az anyatejben, iodine szaga érezhető a csecsemő bőrén |
| Iohexol | Nincs |
| Gyógyszer, vaqy qyóqyszercsoport | Tünetek, amit leírtak a csecsemőkben, hatásuk a laktációra |
| Iopanoic sav | Nincs |
| Isoniazid | Nincs ( acetil metabolitok, melyek hepatotoxikusak, kiválasztódnak az anyatejbe, de nem írtak le hepatotoxicitást a csecsemőben) |
| Interferon-alfa | - |
| Ivermectin | Nincs |
| K1 (vitamin) | Nincs |
| Kanamycin | Nincs |
| Ketoconazol | Nincs |
| Ketorolac | - |
| Labetalol | Nincs |
| Levonorgestrel | - |
| Levothyroxin | Nincs |
| Lidocain | - |
| Loperamid | Nincs |
| Loratadin | Nincs |
| Magnesium sulfat | Nincs |
| Medroxyprogesteron | Nincs |
| Mefenamic acid | Nincs |
| Meperidin | Nincs |
| Methadon | Nincs |
| Methimazol (carbamizol aktív metabolitja) | Nincs |
| Methohexital | Nincs |
| Methyldopa | Nincs |
| Methyprylon | Kábultsáq |
| Metoprolol* | Nincs |
| Metrizamid | Nincs |
| Metrizoat | Nincs |
| Mexiletin | Nincs |
| Minoxidil | Nincs |
| Morphin | Nincs, |
| Moxalactam | Nincs |
| Nadolol* | Nincs |
| Nalidixic sav | Haemolysis qlukóz-6-foszfát dehidroqenáz deficiens csecsemőkben |
| Naproxen | - |
| Nefopam | Nincs |
| Nifedipine | - |
| Nitrofurantoin | Haemolysis qlukóz-6-foszfát dehidroqenáz deficiens csecsemőkben |
| Gyógyszer, vagy gyógyszercsalád | Tünetek, amit leírtak a csecsemőkben, hatásuk a laktációra |
| Norethynodrel | Nincs |
| Norsteroidok | Nincs |
| Noscapin | Nincs |
| Ofloxacin | Nincs |
| Oxprenolol | Nincs |
| Phenytoin | Methemoqlobinaemia (1 esetleírás) |
| Piroxicam | Nincs |
| Prednisolon | Nincs |
| Prednison | Nincs |
| Procainamid | Nincs |
| Progesteron | Nincs |
| Propoxyphen | Nincs |
| Propranolol | Nincs |
| Propylthiouracil | Nincs |
| arPseudoephedrinet* | Nincs |
| Pyridostigmin | Nincs |
| Pyrimethamin | Nincs |
| Quinidin | Nincs |
| Quinin | Nincs |
| Riboflavin | Nincs |
| Rifampin | Nincs |
| Scopolamin | - |
| Secobarbital | Nincs |
| Senna | Nincs |
| Sotalol | - |
| Spironolactone | Nincs |
| Streptomycin | Nincs |
| Sulbactam | Nincs |
| Sulfapyridin | Használata óvatosságot igényel olyan csecsemőkesetében, akiknek sárgasága, G-6PD deficienciája van betegek vagy koraszülöttek |
| Sulfisoxazol | Használata óvatosságot igényel olyan csecsemőkesetében, akiknek sárgasága, G-6PD deficienciája van betegek vagy koraszülöttek |
| Sumatriptan | Nincs |
| Suprofen | Nincs |
| Terbutalin | Nincs |
| Terfenadin | Nincs |
| Tetracyclin | Nincs, elhanyagolható mennyiség szívódik fel a csecsemőbe |
| Theophyllin | Irritabilitás |
| Gyógyszer, vagy gyógyszercsalád | Tünetek, amit leírtak a csecsemőkben, hatásuk a laktációra |
| Thiopental | Nincs |
| Thiouracil | Nincs |
| Ticarcillin | Nincs |
| Timolol | Nincs |
| Tolbutamid | Sárgaság lehetséges |
| Tolmetin | Nincs |
| Trimethoprim/sulfamethoxazol | Nincs |
| Triprolidin | Nincs |
| Valproic acid | Nincs |
| Verapamil | Nincs |
| Warfarin | Nincs |
| Zolpidem | Nincs |
+A fent felsorolt gyógyszerekről megjelent irodalmi adatok szerint vagy a feltüntetett tüneteket vagy semmilyen tünetet nem észleltek a szoptatott csecsemőben. A "nincs" azt jelenti, hogy nem volt megfigyelhető változás a szoptatott csecsemőben, mialatt az anya a gyógyszert szedte. A szaggatott vonal azt jelenti, hogy nem említettek klinikai hatást a csecsemőre. Hangsúlyozzuk, hogy az irodalmi adatok általában egyedi esetek vagy kisszámú csecsemőt vizsgáltak.
7. TÁBLÁZAT Ételekés egyéb környezeti faktorok hatása
| Hatóanyag | Tünetek, amit expozíció esetént leírtak a csecsemőkben, hatásuk a laktációra |
| Aflatoxin | Nincs |
| Aspartam | Óvatossáqot iqényel, ha az anya, vaqv a csecsemő fenilketonuriás |
| Bromid (fotólaboratórium) | Lehet, hoqv a bromid felszívódik és bejut a tejbe (ld. 6. táblázat) |
| Cadmium | Nem számoltak be |
| Chlordan | Nem számoltak be |
| DDT(dichlorodiphenyltri- chloroethane), benzene hexachloridok, dieldrin, aldrin, heptachlorepoxide | Nincs |
| Fava bab | Haemolvsis G6PD-deficienciás csecsemőkben |
| Fluorid | Nincs |
| Hexachlorobenzen | Kiütés, hasmenés, hányás, sötét vizelet, neurotoxiciutás, halál |
| Hexachlorophen | Nincs, a tej lehetséqes contaminációja, ha a mell lemosására használják |
| Higany | Kórosan befolyásolja az ideqrendszer érését |
| Mononátrium glutamat | Nincs |
| Ólom | Toxikus ideqrendszeri hatás |
| Polychlorinált bifenilek | Hypotonia, kifejezéstelen arc |
| Tetrachloroethylen (tisztító folyadékban) | Obstructiv icterus, sötét vizelet |
| Theobromin (csokoládéban) | Irritabilitás vagy fokozott bélműködés, ha excessziv mennyiséget foqyaszt az anya(>500q csokoládé/nap) |
| Vegetáriánus diéta | B12 vitamin hiány tünetei |
Az Egészségügyi Minisztérium
szakmai irányelve
A 0-18 éves életkorú gyermekek látásfejlődésének követése, a kancsalság és a fénytörési hibák felismeréséről Szűrővizsgálati irányelvek védőnők és gyermekorvosok számára
Készítette: az Országos Gyermekegészségügyi Intézet
a Szemészeti Szakmai Kollégiummal,a Gyermekszemészekés StrabológusokTársasággal,
a Csecsemő és Gyermekgyógyászati Szakmai Kollégiummal, és a Védőnői Szakmai Kollégiummal egyeztetve
1. Az irányelvek érvényességi területe
Az útmutató érvényességi területe egész Magyarország: a kórházak újszülött-, újszülött-intenzív (NICU) osztályai, a gyermekegészségügyi alapellátás és az iskolaegészségügyi ellátás.
2. Az útmutató témaválasztásának indoklása
A 0-18 éves életkorú gyermekek szemészeti szűrésére vonatkozóan 1996-ben készült módszertani levél (Országos Csecsemő- és Gyermekegészségügyi Intézet 51. számú Módszertani levele: A kancsalság és a fénytörési hibák felismerése és kezelése, a tompalátás megelőzése) nem hozzáférhető,és nem felel meg az Egészségügyi Minisztérium 23/2006 (V.18.) EÜ. M rendeletében foglaltaknak. (A vizsgálati és terápiás eljárásrend kidolgozásának, szerkezeténekés szakmai egyeztetése lefolytatásának eljárásrendjéről)
Az Útmutató fejlesztésének szükségességét a következő jogszabályok és nemzeti programban foglalt feladatok, valamint az ellátás követelményei indokolják:
51/1997. (XII. 18.) NM rendelet, illetve módosítása: 67/2005. (XII. 27.) EüM rendelet A kötelező egészségbiztosítás keretében igénybe vehető, betegségek megelőzését és korai felismerését szolgáló egészségügyi szolgáltatásokról és a szűrővizsgálatok igazolásáról. A rendelet 1. számú melléklete foglalja magában a gyermekkorban, meghatározott életkorban elvégzendő szűrővizsgálatokat.
49/2004. (V. 21.) ESzCsM rendelet a területi védőnői ellátásról (3 § dd)
1092/2007. (XI. 29) Kormányhatározatának kiemelt fejlesztési területekhez kapcsolódó intézkedési terve, melynek I.A) 2.) alapján: "Ki kell dolgozni a 0-7 éves korú gyermekek fejlődésének komplex (szomatikus, pszichomotoros, érzékszervi, kognitív stb.) méréséhez és követéséhez szükséges állapotfelmérő adatlapok standardjait és eljárási protokolljait annak érdekében, hogy a fejlődésben való megakadás és a fejlődést hátráltató problémák időben felismerhetők és kezelhetők legyenek."
A "Közös Kincsünk a Gyermek" Nemzeti Csecsemő- és Gyermekegészségügyi Program I. célkitűzésének 13. pontja: az újszülöttkori hallás- és látásszűrések egységes módszertanának biztosítása.
A hazai gyermekegészségügyi ellátás
Magyarországon a 0-18 éves gyermekek egészségügyi alapellátásához a betegellátás mellett szervesen hozzátartozik a gyermekek szomatikus, pszichomotoros fejlődésének követése, a fejlődést akadályozó tényezők, köztük az érzékszervi zavarok időben történő felismerése, és az ezekre irányuló szűrővizsgálatok elvégzése. Az alapellátásban, amely magában foglalja az iskola-egészségügyi ellátást is, a fejlődés követése és a szűrővizsgálatok elvégzése a háziorvos, a házi gyermekorvos, az iskolaorvos,a területi és az iskolavédőnőkfeladata. Ezen belül a védőnőkfeladata és kompetenciája a szűrésben jól meghatározott.
3. Az útmutató célkitűzései
Korszerű elméleti és gyakorlati ismeretek nyújtása az alapellátás számára annak érdekében, hogy a szemészeti eltéréseket (látásélességbeliés térlátászavar, kancsalság, színtévesztés stb.) időben felismerhessükés korrigálhassuk, a tompalátás ne alakuljon ki.
4. Az útmutató célcsoportjai
Ellátandók: minden 0-18 éves gyermek Ellátók:
Orvosok: újszülött- és neonatalis-intenzív osztályokon, háziorvosok, házi gyermekorvosok, iskolaorvosok. Területi és iskolavédőnők
5. A látás fejlődésének vázlatos ismertetése
A látás fejlődésének ismerete azért fontos, mert ennekalapján kell az alapellátás orvosának és védőnőjének megítélni, illetve viselkedése alapján felmérni a gyermek látásának fejlődését.
A 30. gest. hétre születetteknél: a pupillareflex fényre általában már kiváltható, de előfordul, hogy az újszülöttek szűk pupillája miatt nehezen értékelhető. A szemhéj fényre záródik.
Időre születetteknél: az újszülöttek a fényt érzékelik, de nagyfokú távollátással születnek, ezért csak homályosan látnak. Az optokineticus nystagmus kiváltható. Az újszülött szemének átmérője a felnőtt szem 66%-a /50/. 2.-3. hét: tárgyat közelítve a szemhez a szemhéjak záródnak.
A kb. hathetes, normálisan fejlődő csecsemőnek képesnek kell lennie arra, hogy emberekkel szemkontaktust vegyen fel, ezt fenn is tartsa, és arckifejezéssel reagáljon rá /50/.
A 2-3 hónapos csecsemő már érdeklődik az élénk színű tárgyak iránt. A koraszülöttek-érettségüknek megfelelően -később érik el ezt a fejlettséget. A kezdetben összerendezetlen szemmozgásoknak négy hónapos korra meg kell szűnniük, vagyis a szaruhártya fényreflexei szimmetrikusak.
6. hó: a térlátás tanulása megkezdődik, kialakul a szivárványhártya színe.
2. év: a látásélesség azonos a felnőttekével.
3. év: a szemgolyó mérete lényegében eléri a felnőttkorit.
7. év: a térlátás hasonló a felnőttéhez.
10.-12. év: a binokuláris látás fejlődése befejeződött.
6. A legfontosabb gyermekszemészeti betegségek rövid ismertetése, epidemiológiája, típusos megjelenési ideje, nemi arányai
1. Táblázat. Gyermekkori szemészeti betegségek és a nemzetközi felmérésekben talált gyakoriságuk
| Szemészeti betegség | Gyakoriság (prevalencia vagy incidencia) |
| Veleszületett szürke hályog | 0,06% (prevalencia) /12/ |
| Retinopathia prematurorum (ROP) | 52% incidencia <750 g születési súly esetén /13/ 32% incidencia 750-199 g születési súly esetén /13/ 15% incidencia 1000-1250 g születési súly esetén /13/ |
| Veleszületett zöld hályog | 0,01% (prevalencia) /14/ |
| Retinoblastoma | 0,005% incidencia 15 éves kor alatt /15/ |
| Kancsalság | 4% (prevalencia) /16,17/ |
| Amblyopia | 2-3% (prevalencia) /7,18-22/ |
| Fénytörési hibák myopia hypermetropia astigmia | 9% prevalencia 5 és 17 éves kor között /23/ 13% prevalencia 5 és 17 éves kor között /23/ 28% prevalencia 5 és 17 éves kor között /23/ |
| Színlátászavar | Nőkben ritkább, mint a férfiakban Férfiak 5-8%-a /52-53/ |
Újszülött- és csecsemőkorban a legfontosabb, kezelést igénylő kórképek közé a veleszületett szürke és zöld hályog, a retinopathia prematurorum (ROP), valamint a retinoblastoma tartozik. Idejében való felismerésük és kezelésük a megfelelő vizuális fejlődés szempontjából nélkülözhetetlen.
Kancsalság: egyenes szemállás esetén a nézővonalak a nézett pontban metszik egymást, kancsalság esetén azonban ez a feltétel nem teljesül. A kancsalság szöge egyénenként változó, lehet egészen kicsi, amely a felismerését nehezíti.
-A 4-6 hónapos csecsemőnél észlelt kancsalság már kóros. Ekkor veleszületett kancsalságról beszélünk.
-2-4 éves kor körül jelenik meg általában a közepes fokú távollátás okozta összetérő kancsalság, és előfordulhat, hogy
sokáig csak fáradtság, betegség esetén jelentkezik.
- Hatéves kor előtt a gyermekek kb. 4%-ánál fordul elő kancsalság, ennek kezelése nélkül 30-35%-ban alakul ki kisebb-nagyobb mértékű tompalátás /50/. A gyermekkori kancsalság polietiológiájú, a háttérben túlnyomórészt valamilyen fénytörési hiba mutatható ki. Nagyobb százalékban alakulhat ki kancsalság örökletes tényezők, koraszülés, komplikált szülés kapcsán. Látóidegkárosodás, retinoblastoma, súlyos szemgyulladás (uveitis) első tünete lehet a kancsalság.
Fénytörési hibák: becslések szerint az iskolás kor előtt a gyermekek 5-7%-nak van a látásfejlődés szempontjából fontos fénytörési hibája (nagyfokú hypermetropia, közepes és súlyos fokú myopia, közepes fokú astigmia, anisometropia) /24/. A 6 és 18 év közötti korosztály negyedének lenne szüksége korrekció viselésére /25/. A korrigálatlan fénytörési hiba jelentősen befolyásolhatja a gyermek iskolai teljesítményét.
Tompalátás (Amblyopia): Az esetek megközelítőleg felében kancsalság (főként esotropia) következtében alakul ki, míg a többi betegnél nagyfokú fénytörési hiba, anisometropia vagy strukturális rendellenesség következménye /4-7/. A fejlődésben megkésett gyermekeknél az amblyopia előfordulása hatszor gyakoribb az egészségesekhez képest/9,10/. A tompalátás a WHO szerint olyan komoly egészségügyi probléma, mely megfelelő vizsgálatokkal korán diagnosztizálható, illetve van hatékony kezelési módszere, így a célirányos szűrésétől mindenképpen várhatók népegészségügyi előnyök /28, 29, 30-37/. Ha az amblyopia nem derül ki időben, vagy elégtelen a kezelése, az életre szóló látáscsökkenéshez vezet. A gyermekkori szemészeti eltéréseket - főként az amblyopiát és az ehhez vezető kórképeket - a lehető legkorábban fel kell ismerni. Így a kezelés sikeresebb, nagyobb arányú gyógyulást eredményez /30, 42, 43/. Az amblyopia kezelési tanulmánya (Amblyopia Treatment Study) a hétévesnél fiatalabb tompalátó gyermekek 75%-ánál talált jelentős (0,6 v. annál jobb visust elérő) javulást a terápiát követően /31, 45, 46, 51/. A tompalátás kezelése kb. 12 éves korig lehetséges, azt követően a látópálya funkcionális plaszticitása nagymértékben csökken /3, 47/.
Mivel a tompalátás és a kancsalság jelentős részét nem ismerik fel és nem kezelik időben /38, 39/, ezért rendkívül fontos, hogy minden gyermek rendszeresen kerüljön szemészeti szűrővizsgálatra /1,40,41/.
7. A gyermekszemészeti betegségek kockázati tényezői, genetikai háttere
"Ha az első fokú rokonok anamnézisében veleszületett szürke vagy zöld hályog, retinoblastoma, vagy szemészeti betegségeket okozó, szemészeti betegségekkel társuló anyagcserezavar, genetikai rendellenesség szerepel, a gyermekvállalás előtt genetikai tanácsadásra van szükség, a kockázat mértékének megbecsülése, a lehetséges praenatalis vizsgálatokelvégzése céljából. Az újszülöttnél ilyen esetben teljes körű szemészeti szakvizsgálat szükséges (A III)".
Ha a családi anamnézisben tompalátás, kancsalság, fénytörési hiba szerepel, akkor a teljes körű gyermekszemészeti vizsgálatot legkésőbb 12 és 24 hónapos kor között kell elvégezni /11/.
A 2. táblázatban találhatók a kóros látásfejlődés szempontjából nagyobb kockázatot jelentő faktorok, amelyek fokozott figyelmet, gondozást, szakorvosi vizsgálatot igényelnek.
2. Táblázat. A kóros látásfejlődés rizikótényezői
| Ha a gyermek anamnézisében szerepel: (a szülő kikérdezése, zárójelentésekalapján) |
| koraszülöttség (<1500g, <30 gesztációs hét) |
| - ROP |
| - intrauterin növekedési elmaradás |
| - perinatalis komplikáció |
| - neurológiai rendellenesség |
| - juvenilis idiopathiás arthritis |
| - pajzsmirigybetegség |
| - szájpadhasadék vagy más craniofacialis abnormalitás |
| - diabetes mellitus |
| - Tartós gyógyszeres kezelés (pl. szteroid ) |
| Ha a családtagok anamnézisben szerepel: (zárójelentések alapján) |
| - retinoblastoma |
| - veleszületett szürke hályog |
| - veleszületett zöld hályog |
| - retinadisztrófia |
| - kancsalság |
| - tompalátás |
| - gyermekkori szemüvegviselés |
| - sarlósejtes anaemia |
| - szemészeti eltéréssel járó szindrómák |
| - gyermekkori vakság (amit nem trauma okozott) |
8. Az ellátási folyamat algoritmusa. A látásfejlődés követése, a látásélességre, kancsalságra, tér- és színlátásra vonatkozó szűrővizsgálatok módszertani leírása
8.1 A szemészeti szűrővizsgálatok célja a kancsalság, fénytörési hibák, színtévesztés gyanújának időben történő felismerése; a gyanú alapján a gyermekszemészeti szakellátásra irányítása.
A kancsalságra, fénytörési hibákra és színtévesztésre vonatkozó vizsgálatok megfelelnek a szűrésre vonatkozó kritériumoknak1.
- A látószervek megtekintése a mindennapi (rutin) orvosi vizsgálat szerves része.
- Az első vizsgálatnak már az újszülött osztályon meg kell történnie, ez az újszülött- osztályt ellátó orvos feladata.
- A látás fejlődésének követése (a látással kapcsolatos viselkedés megfigyelése) az alapellátás orvosainak és védőnőinek feladata (A II.).
- A hatályos jogszabály alapján a területi és iskolavédőnők feladata a látásélesség, a kancsalság, a sztereó- és a színlátás szűrése. Rendszeres időközönkénti szűrésre azért van szükség, mert az évek során újabb és újabb szemészeti eltérések jelentkezhetnek (A III.).
- A szűrések alapján felmerült gyanút a védőnő jelzi a gyermek ellátásáért felelős orvosnak, aki gondoskodik a szemészeti szakellátásra irányításról.
- A gyanú megerősítése, a diagnózis felállítása és a kezelés a szemészeti szakellátás feladata (A III.).
- Ha egy gyermeknél egy hónapon belül két egymást követő alkalommal nem sikerül elvégezni kielégítő eredménnyel a szűrést az alapellátásban, akkor az mindenképpen szakorvosi beutalás abszolút indikációját jelenti. Irodalmi adatok alapján ugyanis -a szűrővizsgálaton megfelelően teljesítő gyermekekkel összehasonlítva - ilyenkor jóval nagyobb arányban fordul elő kóros szemészeti eltérés (BII) /2/.
- Az elvégzett szűrővizsgálatok eredményét és a szemszakorvosi leletet végül a védőnőnek és a gyermekorvosnak dokumentálni kell, mert ez a feltétele az eredményes kezelésnek, a követésnek és az értékelésnek.
1 A szűrés: Rejtett, tünetet még nem okozó, korábban még nem diagnosztizált betegség valószínűsíthető felismerése gyorsan kivitelezhető tesztekkel, vizsgálatokkal és egyéb eljárásokkal. Vagyis ily módon az egészségesnek tűnő személyek közül kiválaszthatók a valószínűleg betegek. A szűrés nem a diagnózis, hanem a különválasztás eszköze, a pozitív vagy bizonytalan szűrési eredményű betegek további kivizsgálása szükséges.
8.2. A látószervek vizsgálata, a kancsalságra, fénytörési hibákra, színtévesztésre vonatkozó szűrővizsgálatok rendje 0-18 éves kor között
0-5. hó: A családi és a perinatalis anamnézis felvétele; a csecsemőt gondozó(k) kikérdezése az esetleges észrevételekről; a szem és védőszerveinek megtekintése, a pupillareakciók,a vörös visszfény vizsgálata, a szemmozgás és a szemállás vizsgálata.
Életkornak megfelelő állapot: a szemhéjak épek; a szemrésben nem áll a könny; a szaruhártya átmérője kb. 10 mm; a pupillák közepesen tágak, alakjuk normális, fényre jól reagálnak; jó a vörös visszfény mindkét szemben (ld. alább!); a szemmozgások az életkornak megfelelőek; 4 hónapos kortól a szemek párhuzamosan állnak.
6. hó: A csecsemőt gondozó (k) kikérdezése az esetleges panaszokról; a csecsemő szemének megtekintése; látásának játékos módon való megítélése (pl. apró - 2-3 cm-es - színes tárgyakat felmutatva a gyermek nyúl-e a tárgyak után); takarási próbák (ld. alább!); a cornealis fényreflex szimmetriájának vizsgálata; a szemmozgások, a szemállás vizsgálata. Életkornak megfelelő állapot: a csecsemő nem kerüli a fényt, nem hunyorog; a szaruhártya fényreflexe szimmetrikus, a szemmozgások szabadok; nincs beigazító mozdulat; a szemek váltott takarásakor a gyermek a játékért nyúl, vagy mindkét szem takarása ellen egyaránt tiltakozik; jó vörös visszfény van; a fejtartás egyenes.
12-14. hó: A feladatok és az elvárható szemészeti állapot az előző korcsoportéval azonos.
Életkornak megfelelő állapot: a gyermek a korának megfelelően mozog, tájékozódik, az apró képeket felismeri, egyszerű képekre mutogat.
2,5-3. év: A feladatok és az elvárható szemészeti állapot az előző korcsoportéval azonos. A védőnő kikérdezi a szülőket az esetleges észrevételeiről, a gyermek panaszairól. A közellátás vizsgálata 40 cm-ről a kártyasorozat képeivel. Ebben az életkorban a mélységérzékelés már vizsgálható.
Életkornak megfelelő állapot: a gyermek ügyesen mozog, normális olvasótávolságban (30-40cm) rajzol, nem hunyorog, nem pislog feltűnően gyakran; sztereóteszten az ábrákat megnevezi (ha legalább rámutat azokra, az már jó kétszemes együttlátásra utal); nincs beigazító mozdulat; a szemmozgások szabadok; a látásélesség 5 méterről vizsgálva mindkét szemen 1,0.
4-5. év: A feladatok és az elvárható szemészeti állapot az előző korcsoportéval azonos. Ötéves kortól vizsgálható tesztekkel (ld. később) a gyermek a színlátása
Életkornak megfelelő állapot: ha a gyermek játékokban ügyes, színezésnél nem téveszt, jó a sztereólátása, 1,0 a látásélessége Ammon-villákkal, 5 méterről; jól konvergál; nincs beigazító mozdulat; a szemmozgások szabadok. 6-18. év (2-évente): A szülő, a tanító, a gyermek kikérdezése az esetleges panaszokról, megtekintés, visusvizsgálat. Életkornak megfelelő állapot: a látásélesség mindkét szemen 1,0; a színlátás jó; ha egyszerű megtekintésre nincs semmi feltűnő.
8.3. A látószervek vizsgálatának módszertani leírása és sorrendje Anamnézisfelvétel: a fenti táblázatban foglalt összes rizikótényezőre kérdezzünk rá! Először a szem védőszerveit, majd a szemeket külsőleg tekintsük meg!
A szemmozgások vizsgálata
4-5 hónapos kortól vizsgálható, amikor a tárgykövetés már kialakult. Óvatosan rögzítve a csecsemő állát, egy színes (de hangot nem adó) tárgyat mozgatunk minden irányba, és figyeljük a szemgolyók mozgását. Bénulásos kancsalság esetén az egyik szem adott irányú mozgása akkor is elmarad, amikor a gyermek fejét a várható szemmozgással ellentétes irányba próbáljuk fordítani (babafej manőver). Ha a gyermek orra felé egy kisebb tárgyat közelítünk, akkor normális esetben a szemek szimmetrikusan konvergálnak.
A mélységérzékelés (sztereólátás) vizsgálata
A mélységérzékelés vizsgálata kifejezetten alkalmas a két szem együttműködésének vizsgálatára (anisometropia, astigmia, kancsalság esetén a képek felismerése bizonytalanná válik, vagy egyáltalán nem sikerül. Kétéves kortól már általában elvégezhető. A gyermek feladata az, hogy a tesztábrák figuráit felismerje és megnevezze. Miután azonban jó teljesítmény érhető el vele akkor is, amikor az egyik szem látása gyengébb, ténylegesen csak a visusvizsgálattal együtt ad a kétszemes együttlátásra vonatkozó értékes információt.
Ha a gyermek nem nevez meg egyetlen figurát sem (ha pl. a gyermek a Lang-II-teszten a csillagot igen, de a többi figurát nem ismeri fel), felvetődik a gyanú, hogy az egyik szem nem lát jól. Ez a szem lehet kancsal vagy tompalátó, tehát mindenképpen szakorvosi vizsgálat indokolt.
A cornealis fényreflex vizsgálata
A gyermek arcát kb. 1 m-ről, pl. pupillalámpával megvilágítjuk, és figyeljük a fényforrás tükörképét a szaruhártyán. Ha az a két szemen nem szimmetrikusan helyezkedik el, valószínű a kancsalság. Bizonytalan esetben segítséget jelentenek a gyermekről készült fényképek. Gyanú esetén szakorvosi vizsgálat indokolt.
Takarásos teszt
A kisgyermeknek kb. fél méterről olyan kis tárgyat mutatunk, amely felkelti az érdeklődését. A vizsgáló egy "takaró lapáttal" eltakarja a gyermek egyikszemét (monokuláris takarás), de közben a másikszemesetleges mozdulatát figyeli. Ha ez a szem megtartja az eredeti állását, akkor ezen a szemen nincs kancsalság. Ha viszont nem, az kancsalságra utal. Ezt a tesztet mindkét szemen elvégezzük. Egymás utáni, váltott takarással (alternáló takarás) a heterophoriát deríthetjük ki. Ha a szem beigazító mozdulatát mindkét szemen felváltva észleljük, az heterophoriára utal. Ez azonban többnyire csak társuló panaszok és/vagy egyéb pozitív tesztek esetén jelent kóros állapotot.
A vörös visszfény vizsgálata
Kb. fél méter távolságról közvetlenül világítsuk meg a szemeket. Legkönnyebben szemtükörrel, vagy fényforrásból egyszerű síktükörrel vetíthetjük be a fényt a pupilla területére. Azt vizsgáljuk, hogy mindkét szemből nyerhető-e vörös visszfény, illetve hogy ez azonos színű és intenzitású-e a két oldalon. Azonnali szakorvosi vizsgálatot igénylő rendellenességre van gyanú, ha a vörös visszfény sötétebb vörös, világos és/vagy eltér a két szemen, fehér vagy egyáltalán nincs (A).
A látásélesség vizsgálata
A látásélességet "szabályosan" öt méter távolságból végezzük. Arra mindig gondosan kell ügyelni, hogy az éppen nem vizsgált szem megfelelően legyen takarva.
Már kétéves korú gyermeknél tegyünk kísérletet ennek elvégzésére: kérjük meg a gyermeket arra, hogy a távolból felmutatott ábrákat ( ld. 10.1 /1/) nevezze meg. Először a legnagyobb, majd az egyre kisebb méretűeket mutatjuk fel neki. Az ilyen korú kisgyermek látásélessége akkor megfelelő, ha 5 méter távolságról a két cm-es méretű ábrát felismeri. Ha ez nem sikerül, valószínűsíthető, hogy a gyermek nem lát elég élesen, és szemész szakorvosi vizsgálat indokolt.
Ha a gyermek nem beszél, a teszt elvégzésére ekkor is kísérletet tehetünk. Ehhez használni kell az "összesítő lapot" (ld. 10.1 /2/) ! A gyermek feladata az, hogy az öt méterről felismert figurát azonosítsa (mutasson rá) az ölében elhelyezett összesítő lapon lévővel.
Négyéves kornál idősebb, de iskolába még nem járó gyermek látásélesség vizsgálatára a többféle irányban elforgatott Ammon-villát vagy Landolt-gyűrűt tartalmazó kártyát használjuk. Ilyenkor a gyermek az ujjával azt az irányt (föl, le, jobbra vagy balra) jelzi, amellyel a villa "szúr" vagy mondjuk egy "autó kereke" kipukkadt. Az ilyen korú gyermek akkor lát jól (visusa: 1.0), ha a 0,7 cm-es jelet felismeri.
Ha a gyermek visusa egyik vagy mindkét szemen csak 0,7 gyermekszemész vizsgálata szükséges.
Csoportos szűréseknél gondoskodni kell arról, hogy a sorban következő gyerekek egyike se hallja meg a választ
A színlátás vizsgálata
Már 5 éves kortól vizsgálható táblákkal, azonban felismerésének a pályaválasztást megelőző időszakban van jelentősége.
Beszélni nem tudó gyermek próbálja meg az ábra vonalán végighúzni az ujját.
Csoportos szűréseknél gondoskodni kell arról, hogy a sorban következő gyerekek egyike se hallja meg a választ
9. Az ellátási folyamat megfelelőségének kritériuma
Teljes körűnek tekinthető a szülést közvetlenül követő szűrés, ha az érintettek (intézetben vagy azon kívül születettek) 100 %-a átesik szűrővizsgálaton (az előzőek még a hazabocsátás előtt, utóbbiak egy hónapon belül). A szűrővizsgálatokat szabályozó rendelet szerint (jelenleg a 51/1997. (XII. 18.) NM rendelet I. számú melléklete) az adott életkorú csecsemők és gyermekek 100%-ánál meg kell történnie a fenti algoritmus szerinti vizsgálatoknak.
A szűrővizsgálatok elvégzésére a gyermekegészségügyi ellátás szakembereit továbbképzés keretében fel kell készíteni.
10. Az irányelv bevezetésének feltételei 10.1. Tárgyi feltételek
Az éleslátás vizsgálatához:
1. Kártyasorozat kisgyermekek számára. A képek "bölcsődei jeleket", sematikus figurákat ábrázolnak, és négyféle (0,1, 0,3, 0,6 és 1,0) visusnak felelnek meg (ld. a módszertani leírást!)
2. 1 db összesítő lap kártyasorozathoz.
3. Landolt-gyűrűt és Ammon-jelet tartalmazó kártyasorozat. Elegendő a 0,6-0,7-0,8-0,9-1,0 visusnak megfelelő méret. Ha ezt a gyermek nem látja, a "bölcsődei jeleket" ábrázoló, nagyobb képekkel kiegészíthető a vizsgálat.
4. Kettesy-féle visustábla 5 m-es vizsgálati távolsághoz
5. Szemtakaráshoz egyszer használatos, kettéhajtott papírlap vagy álarc
6. Betanításhoz "Szurtos Peti keze"
7. Sakktábla-mintás, nyeles tábla csecsemők látásának megítéléséhez
8. mínusz fél dioptriás (-0,5D) lencse (ld. 10.1 /6/) A színlátás vizsgálatához:
Egy-egy figurát és számokat tartalmazó pseudoisochromaticus tábla. Mélységérzékelés (mélységélesség, sztereóélesség) vizsgálatához:
A legkorszerűbbek [48] a véletlenszerű pontokból szerkesztett tesztábrák (pl. a Lang-tesztek). A Lang II. előnyösebb, mert a csillag ábrát az az egyén is látja, akinek nincs térlátása. Ezzel elkerülhető, hogy a gyermek kudarcként élje meg, ha nem ismeri fel az egyébként térben érzékelhető többi figurát.
A vörös visszfény és pupillareflex vizsgálatához: egyszerű nyeles síktükör, közepén lyukkal és egy kis asztali olvasólámpa opál izzóval; pupillalámpa, (újszülött osztályokon elvárható a szemtükör);
A takarási teszthez a legalkalmasabb a vizsgáló keze.
A fixálás és a konvergencia vizsgálatához a gyerekre veszélyt nem jelentő apró tárgyakra van szükség. (pálca végére erősíthető apró figura, rajz, közeli fixációs léc, játék).
Hasznosak lehetnek a közeli látásvizsgáló olvasó táblák (Csapodi-féle olvasó táblák, Landolt-gyűrűs "autós" tábla).
A szűrés helyszíne a gyermekorvosi rendelő, az iskolaorvosi rendelő, a védőnői tanácsadó helyiség, a bölcsőde, az óvoda vagy a gyermek otthona lehet.
10.2 Személyi feltételek
A csecsemő és gyermekkori látásproblémák korai felismeréséhez és ellátásához szoros és szabályozott együttműködésre van szükség mind a helyi, mind az országos szintű szakmai intézmények, mind az alapellátásban dolgozó orvosok, védőnők és a szemészeti szakellátásban dolgozók között. A civil szervezetek hasznos támogatást nyújthatnak a szülők és gondozók információkkal való ellátásában. Nagy hangsúlyt kell fektetni a megfelelő kommunikációra az érintett szülők, a különböző érdekvédelmi szervezetek képviselői, és a programban érintett résztvevők között.
10.3 Oktatás, továbbképzés
A útmutató alapján elvégzendő vizsgálatokra a védőnőket, a háziorvosokat, a házi gyermekorvosokat, az iskolaorvosokat és az iskolavédőnőket célirányú továbbképzésekkel kell felkészíteni, melyet szemész, gyermekszemész szakorvosok végeznek.
10.4 Szervezési feltételek
Biztosítani kell, hogy a szűrővizsgálatokon látászavar szempontjából gyanúsnak talált csecsemők és gyermekek a progresszív betegellátás megfelelő szintű intézményébe kerüljenek, és ezek hollétéről és hozzáférhetőségéről mind a szűrővizsgálatokat végzők, mind a hozzátartozók kellőképpen tájékozódjanak.
10.5 Az irányelv érvényben tartásának feltételei
A szűrővizsgálatok egyre korszerűbb eszközeinek igénybevételéhez elengedhetetlen, hogy hazai viszonyok között is készüljön olyan átfogó hatástanulmány (ráfordítás-előny, "megtérülés"), mely adatokat szolgáltat a szűrővizsgálat gyakorlatának megbízhatóságáról (szenzitivitás, specifitás).
11. Szakorvosi konzíliumot igénylő panaszok és tünetek
- A nystagmus, a kancsalság megjelenése, a tágabb, fehérebb pupilla, a tartós fényfixálás, a vizuális érdeklődés teljes hiánya a gyengén látás első jele lehet.
- A gyermek mozgásának változása, mozgásfejlődésének lemaradása, ügyetlenség, az iskolai eredmény romlása, hunyorgás, olvasási nehézség utalhat rosszabb látásra vagy a két szem együttműködési zavarára.
- Rendellenes fejtartás (torticollis) szemizom eredetű bénulásos kancsalságra hívhatja fel a figyelmet. A rendellenes fejtartás a kettős látást kompenzálja, a fejtartás "kiigazítása" provokálhatja a kettős látást, és észrevehetővé teheti a kancsalságot.
- Kettős látás. Ha agyermekerre panaszkodik, az mindig komoly figyelmeztető tünet, 4 évesnél nagyobb gyermeknél friss bénulásos kancsalságot jelezhet.
- Nagyobb terhelésre, többnyire délutánra jelentkező fejfájás (számítógép használata, tanulás) a szem kifáradására utal. A visszatérő panaszok elsősorban rejtett fénytörési hibára, rejtett kancsalságra hívhatják fel a figyelmet. Az alkalmazkodási zavar olvasási nehézséget okozhat.
- A szem kifáradásához vezethet a számítógép hosszantartó használata. Oka az alkalmazkodó képesség túlzott igénybevétele. A monitor tartós figyelése során kevesebbet pislogunk, továbbá a tágabb szemrés miatt szemszáradásos tünetek jelennek meg /49/. Az észlelt szemészeti panaszok pihenéssel, megfelelő korrekció viselésével, műkönnycseppel kezelhetők.
- Gyakori pislogás esetén gondolni kell fénytörési hibára, allergiára. Tic, könnyezés, szemhéjszéli gyulladás, olvasási problémák, az olvasási kedv csökkenése szintén fénytörési hibára utal
A szakorvos feladata (IV.)
Ahhoz, hogy a szakorvos által javasolt kezelést az alapellátásban dolgozók (gyermekorvosok, védőnők) hatékonyan ellenőrizni tudják, illetve a szülő által feltett kérdésekre könnyebben tudjanak válaszolni, az alábbi ismeretekfontosak. A fénytörési hiba korrigálása 18 éves korig minden esetben szakorvosi feladat. Az első szemüveg felírása előtt, főként ha kancsalság miatt történik a fénytörési hiba meghatározása, objektív módon, ú.n. skiaszkópiával állapítható meg a szemek fénytörése. Ehhez az alkalmazkodó képességet átmenetileg fel kell függeszteni. Ez egyúttal a pupilla tágulásával jár. A szemorvos dönti el, hogy ehhez rövid vagy hosszabb ideig ható cseppet vesz-e igénybe. (az Atropin csepp az akkomodációt 10 napra, a cyclopentolat 1-2 napra, a tropicamid egy órára függeszti fel). A pupillatágítás a binokuláris látást is befolyásolja, ezért a szemészeti (pl. konzíliumi) vizsgálat előtt nem szabad a pupillát kitágítani. Az objektív módon meghatározott fénytörési hibát szemüveggel korrigálja a szakorvos, és ő dönti el, hogy a szemüveget mikor kell viselni. Gyermekkorban a szemüveget többnyire állandó viselésre rendeli a szemorvos. Ha a látásélesség az egyik szemen nem éri el az elvárható értéket, a jobban látó szem bizonyos arányú takarása szükséges (szemtakaróval vagy egyéb módon).
Bizonyos esetben a kancsalság megnehezíti a kétszemes együttlátást és ezért, vagy kozmetikai okok miatt kancsalság ellenes műtétre lehet szükség. Ennek időpontját a szakorvos javasolja.
A műtét feladata a párhuzamos szemállás elérése, de elvégzése után a szemüveget többnyire továbbra is viselni kell, hiszen a fénytörési hiba a műtét után változatlanul fennáll.
Kisebb dioptriájú lencsék viselésekor problémát okozhat az, hogy az alkalmazkodás igénybevételével szemüveg nélkül is elérhető az éleslátás. Ekkor azonban a szemek fokozott igénybevétele asthenopiás panaszokhoz vezethet, tehát csak a szemüveg folyamatos viselésétől várható, hogy a panaszok megszűnjenek. A komoly panaszokkal járó heterophoria (a rendszeres fejfájáshoz, szemfájdalomhoz, olvasási nehézséghez vezető, ú.n. dekompenzált heterophoria) esetén prizmás szemüveget rendel a szakorvos. Indokolt esetben alkalmanként kontaktlencse is viselhető.
Az elsődleges cél a jó binokuláris látás elérése. Kancsalság esetén előfordul, hogy ez az ideális állapot nem érhető el. Felnőtt korban ennek az állapotnak az elérése már nem lehetséges, ezért van szükség a korai szűrésekre. Tanulási nehézség, diszlexia esetén a szemész feladata az, hogy a háttérben esetleg meghúzódó szemészeti problémát zárja ki, ezeket kezelje, mert e nélkül tovább nehezedik a diszlexia alapvetően logopédiai kezelése.
12. Mellékletek
Az útmutatóban használt definíciók és rövidítések
Amblyopia: tompalátás. A látásélesség a fénytörési hiba korrekciója ellenére sem éri el az 1,0-t. Anisometropia: különbség van a két szem fénytörése között Asthenopia: fáradásos tünetek, melyek elsősorban olvasáskor lépnek fel
Astigmia: a törőközegek görbületi egyenetlensége miatt a szemfenéken nem képződik éles kép
Binokuláris látás: kétszemes együttlátás
Fénytörési hibák: a szem optikai eltérései, mely miatt nyugalmi állapotban nem keletkezik éles kép az ideghártyán (myopia: rövidlátás; hypermetropia: túllátás; astigmia: ld. ott)
Gyengén látás: a két szem együttes látásélessége 0,3 vagy ennél gyengébb
Heterophoria: rejtett kancsalság; van binokuláris látás, nyugalmi helyzetben azonban van szemállásbeli eltérés Hypermetropia: távollátás, túllátás (=a szembe vetülő sugarak az ideghártya mögött fókuszálódnak) Konvergencia: a két szem összetérő, a fixált tárgyra irányuló mozgása Myopia: rövidlátás (a szembe vetülő sugarak az ideghártya előtt fókuszálódnak)
Nystagmus: a szemek akaratlan, többnyire veleszületett rezgő mozgása, esetenként gyenge látásélesség következménye
Strabismus (Heterotropia): kancsalság: a szem rendellenes állása következtében nincs kétszemes együttlátás, azaz nincs binokuláris látás Sztereólátás: mélységérzékelés
Visus: látásélesség
Rövidítések D dioptria
gest. gesztációs hét, terhességi hét
ROP (Retinopathy of Prematurity) retinopathia prematurorum, koraszülött-retinopathia
SIGN Scottish Intercollegiate Guidelines Network
WHO (World Health Organization) Egészségügyi Világszervezet
13. Az irányelv fejlesztésének folyamata, módszerei
Az útmutató az Országos Gyermekegészségügyi Intézet, és a Magyar Gyermekszemészeti k és Strabológusok Társaságának együttműködése eredményeképpen jött létre.
A munkacsoportban gyermekgyógyászok, gyermekszemészek, logopédus és védőnők dolgoztak együtt. Az irányelv fejlesztését az Országos Gyermekegészségügyi Intézet kezdeményezte.
14. Irodalomkeresés, az idézett irodalom kiválasztása
Szisztematikus irodalomkeresést végeztünk a fellelhető nemzetközi irányelv- adatbázisokban. A keresés az elmúlt 5 évben (2002-2007) született irányelvekre irányult. Az irodalomkutatást a Medline-adatbázisban végzett, a gyermekkori szemészeti szűrésekkel kapcsolatos rendszerezett irodalmi áttekintésekre, metaanalízisekre vagy randomizált vizsgálatokra vonatkozó keresés egészítette ki. A fellelt szakirodalomból csak azokat az anyagokat választottuk ki, melyek klinikailag lényegesek, és magas rangú bizonyíték támasztja alá az ajánlást.
15. A felhasznált nemzetközi útmutatók alkalmassá tétele hazai viszonyokra
A fentiek alapján leginkább az American Academy of Ophthalmology által 2007-ben kiadott Pediatric Eye Evaluations bizonyítékon alapuló irányelve 11 felelt meg a módszertani és szakmai kritériumoknak. Ezek adaptálása során áttekintettük és felhasználtuk a gyermekkori szemészeti betegségekkel foglalkozó hazai szakirodalmat is.
16. A bizonyítékok szintjének megadása
A kiválasztott irányelveket a bennük foglalt evidencia alapján soroltuk különböző erősségű kategóriákba. Az egyes ajánlásokat alátámasztó bizonyítékokat rangsoroltuk, és ezek erősségét a Scottish Intercollegiate Guidelines Network (SIGN) módszerei segítségével az alábbi skálán helyeztük el. Amikor nem találtunk az ajánlást alátámasztó bizonyítékot, az irányelvfejlesztő csoport konszenzusos véleményeit tüntettük fel. A megkülönböztető jel nélküli, egyszerű szöveges ajánlások konszenzuson alapulnak.
| kategória | Ajánlási szint | kategória | |
| Jól tervezett, randomizált, kontrollált klinikai tanulmányok. Randomizált tanulmányok metaanalízise. | I | Nagyon fontos ajánlás. | A |
| Jól tervezett, kontrollált, de nem randomizált tanulmány. Jól tervezett esetkontroll tanulmány, lehetőleg több centrumból. | II | Közepesen fontos ajánlás. | B |
| Esettanulmányok. Leíró tanulmányok. Szakértői vélemények | III | Releváns, de nem A bizonyítékok erősségefontos ajánlás. | C |
| Konszenzuson alapuló | IV |
17. Társszakmákkal történő véleményeztetés
Az útmutatót a Csecsemő és Gyermekgyógyászati Szakmai Kollégium észrevételek nélkül elfogadta. A Védőnői Szakmai Kollégium több észrevételt tett, amelyek elsősorban az útmutató által javasolt szűrési algoritmus és a jelenlegi jogszabály nem teljes egyezőségére vonatkoznak. Valamint javaslatot fogalmazott meg az orvosi és védőnői kompetencia világosabb megfogalmazására. Ez utóbbi javaslat alapján a védőnő és az orvos szűrővizsgálatokkal kapcsolatos feladatait pontosítottuk.
Nyilatkozatok
Az ajánlás kialakítása során a szerzők külső támogatást, az elkészítésnél szponzori támogatást nem vettek igénybe, magukat függetlennek és elfogulatlannak tekintik.
A szakmai irányelvet elfogadta:
- Szemészeti Szakmai Kollégium, Gyermekszemészekés StrabológusokTársasága
- Csecsemő és Gyermekgyógyászati Szakmai Kollégium
- Védőnői Szakmai Kollégium
A szakmai kollégiumok észrevételeit, módosítási javaslatait a szerzők figyelembe vették. irodalomjegyzék
1. Eye examination in infants, children, and young adults by pediatricians. Pediatrics 2003;111:902-7.
2. Maguire MG. Children unable to perform screening tests in vision in preschoolers study: proportion with ocular conditions and impact on measures of test accuracy. Invest Ophthalmol Vis Sci 2007;48:83-7.
3. Pediatric Eye Disease Investigator Group. Randomized trial of treatment of amblyopia in children aged 7 to 17 years. Arch Ophthalmol 2005;123:437-47.
4. Pediatric Eye Disease Investigator Group. The clinical profile of moderate amblyopia in children younger than 7 years. Arch Ophthalmol 2002;120:281-7.
5. Birch EE, Stager DR. Monocularacuityandstereopsisin infantile esotropia. Invest Ophthalmol Vis Sci 1985;26:1624-30.
6. Dickey CF, Metz HS, Stewart SA, Scott WE. The diagnosis of amblyopia in cross-fixation. J Pediatr Ophthalmol Strabismus 1991;28:171-5.
7. Thompson JR, Woodruff G, Hiscox FA, et al.The incidence and prevalence of amblyopia detected in childhood. Public Health 1991;105:455-62.
8. Donahue SP. Clinical practice. Pediatric strabismus. N Engl J Med 2007;356:1040-7.
9. Pike MG, Holmstrom G, de Vries LS, et al. Patterns of visual impairment associated with lesions of the preterm infant brain. Dev Med Child Neurol 1994;36:849-62.
10. van Hof-Van Duin J, Evenhuis-van Leunen A, Mohn G, et al. Effects of very low birth weight (VLBW) on visual development during the first year after term. Early Hum Dev 1989;20:255-66.
11. American Academy of ophthalmology: Pediatric Eye Evaluations. 2007. Avaible at: http://www.aao.org/ppp.
12. American Academy of Ophthalmology Basic and Clinical Science Course Subcommittee. Basic and Clinical Science Course. Pediatric Ophthalmology and Strabismus: Section 6, 2007-2008. San Francisco, CA: American Academy of Ophthalmology; 2007:Chapter 22.
13. Good WV, Hardy RJ, Dobson V, et al. The incidence and course of retinopathy of prematurity: findings from the early treatment for retinopathy of prematurity study. Pediatrics 2005;116:15-23.
14. American Academy of Ophthalmology Basic and Clinical Science Course Subcommittee. Basic and Clinical Science Course. Glaucoma: Section 10,2007-2008. San Francisco, CA: American Academy of Ophthalmology; 2007:Chapter 6.
15. Pendergrass TW, Davis S. Incidence of retinoblastoma in the United States. Arch Ophthalmol 1980;98:1204-10.
16. Donnelly UM, Stewart NM, Hollinger M. Prevalence and outcomes of childhood visual disorders. Ophthalmic Epidemiol 2005;12:243-50.
17. National Advisory Eye Council. Vision Research: A National Plan. Report of the Strabismus, Amblyopia, and Visual Processing Panel, Vol 2, Part 5. Bethesda: US DHHS, NIH Publ No. 83-2475, 2001.
18. Williams C, Harrad RA, Harvey I, Sparrow JM. Screening for amblyopia in preschool children: results of a population-based, randomised controlled trial. ALSPAC Study Team. Avon Longitudinal Study of Pregnancy and Childhood. Ophthalmic Epidemiol 2001;8:279-95.
19. Attebo K, Mitchell P, Cumming R, et al. Prevalence and causes of amblyopia in an adult population. Ophthalmology 1998;105:154-9.
20. Brown SA, Weih LM, Fu CL, et al. Prevalence of amblyopia and associated refractive errors in an adult population in Victoria, Australia. Ophthalmic Epidemiol 2000;7:249-58.
21. Newman DK, East MM. Prevalence of amblyopia among defaulters of preschool vision screening. Ophthalmic Epidemiol 2000;7:67-71.
22. Robaei D, Rose KA, Ojaimi E, et al. Causes and associations of amblyopia in a population-based sample of 6-year-old Australian children. Arch Ophthalmol 2006;124:878-84.
23. Kleinstein RN, Jones LA, Hullett S, et al. Refractive error and ethnicity in children. Arch Ophthalmol 2003;121:1141-7.
24. Agency for Healthcare Research and Quality. 2004 systematic evidence review number 27: Screening for visual impairment in children younger than age 5 years: a systematic evidence review for the U.S. Preventive Services Task Force. Available at: http://www.ahrq.gov/downloads/pub/prevent/pdfser/visualser.pdf. Accessed August 20,2007.
25. Kemper AR, Bruckman D, Freed GL. Prevalence and distribution of corrective lenses among school-age children. Optom Vis Sci 2004;81:7-10.
26. Repka MX. Ophthalmological problems of the premature infant. Ment Retard DevDisabil Res Rev 2002;8:249-57.
27. Rudanko SL, Fellman V, Laatikainen L. Visual impairment in children born prematurely from 1972 through 1989. Ophthalmology 2003;110:1639-45.
28. Wilson J, JungnerG. Principles and Practice of Screening for Disease. Geneva, Switzerland: World Health Organization; 1968. Public Health Papers No. 34. Available at: http://whqlibdoc.who.int/php/WHO_PHP_34.pdf. Accessed June 27, 2007.
29. Simons K. Preschool vision screening: rationale, methodology and outcome. Surv Ophthalmol 1996;41:3-30.
30. Kvarnstrom G, Jakobsson P, Lennerstrand G. Visual screening of Swedish children: an ophthalmological evaluation. Acta Ophthalmol Scand 2001;79:240-4.
31. Donahue SP, Arnold RW, Ruben JB. Preschool vision screening: what should we be detecting and how should we report it? Uniform guidelines for reporting results of preschool vision screening studies. J AAPOS 2003;7:314-6.
32. Arnold RW, Armitage MD, Gionet EG, et al.The cost and yield of photoscreening: impact of photoscreening on overall pediatric ophthalmic costs. J Pediatr Ophthalmol Strabismus 2005;42:103-11.
33. Kerr NC, Arnold RW. Vision screening for children: current trends, technology, and legislative issues. Curr Opin Ophthalmol 2004;15:454-9.
34. Arnold RW, Donahue SP. Compared value of amblyopia detection. Binocul Vis Strabismus Q 2006;21:78.
35. Kvarnstrom G, Jakobsson P, Lennerstrand G, Dahlgaard J. Preventable vision loss in children: a public health concern? Am Orthopt J 2006;56:3-6.
36. Joish VN, Malone DC, Miller JM. A cost-benefit analysis of vision screening methods for preschoolers and school-age children. J AAPOS 2003;7:283-90.
37. Kvarnstrom G, Jakobsson P, Lennerstrand G. Screening for visual and ocular disorders in children, evaluation of the system in Sweden. Acta Paediatr 1998;87:1173-9.
38. Ehrlich MI, Reinecke RD, Simons K. Preschool vision screening for amblyopia and strabismus. Programs, methods, guidelines, 1983. Surv Ophthalmol 1983;28:145-63.
39. Reinecke RD. Current concepts in ophthalmology. Strabismus. N Engl J Med 1979;300:1139-41.
40. American Association for Pediatric Ophthalmology and Strabismus and American Academy of Ophthalmology. Joint Policy Statement. Vision Screening for Infants and Children. San Francisco, CA: American Academy of Ophthalmology; 2007. Available at: http://www.aao.org/education/statements/.
41. U.S. Preventive Services Task Force. Screening for Visual Impairment in Children Younger than Age 5 Years: Recommendation Statement. May 2004. Agency for Healthcare Research and Quality, Rockville, MD. Available at: http://www.ahrq.gov/clinic/3rduspstf/visionscr/vischrs.htm. Accessed August 20, 2007.
42. Eibschitz-Tsimhoni M, Friedman T, NaorJ,etal. Early screening foramblyogenic risk factors lowers the prevalence and severity of amblyopia. J AAPOS 2000;4:194-9.
43. U.S. Preventive Services Task Force. Screening for visual impairment in children younger than age 5 years: recommendation statement. Ann Fam Med 2004;2:263-6.
44. Lithander J, Sjostrand J. Anisometropic and strabismic amblyopia in the age group 2 years and above: a prospective study of the results of treatment. Br J Ophthalmol 1991;75:111-6.
45. American Academy of Ophthalmology Pediatric Ophthalmology/Strabismus Panel. Preferred Practice Pattern® Guidelines. Amblyopia. San Francisco, CA: American Academy of Ophthalmology; 2007. Available at: http://www.aao.org/ppp.
46. Pediatric Eye Disease Investigator Group. A randomized trial of atropine vs. patching for treatment of moderate amblyopia in children. Arch Ophthalmol 2002;120:268-78.
47. Rahi JS, Logan S, Borja MC, et al. Prediction of improved vision in the amblyopic eye after visual loss in the non-amblyopic eye. Lancet 2002;360:621-2.
48. Gunter K. von Noorden, Emilio Campos. Binocular Vision and Ocular Motility. Theory and Management of Strabismus (6th edition)
49. Sényi Katalin: Útmutató Gyermekorvosok számára. 2004.
50. Gyermekszemészet és Strabismus. A Magyar Gyermekszemészekés StrabológusokTársaságának 2005-ös kiadványa. Fordítás. Felelős szerkesztő: Soproni Anna.
Az eredeti kiadvány címe: Pediatric Ophthalmology and Strabismus. Section 6. Basic and Clinical Science Course of American Academy of Ophthalmology, 2002-2003.)
51. PokoryJ.,Smith VC, Pinkers Ajet al Classification of complete and incomplete autosomal recessive achromatopsia Graefes Arc Clin. Exp. Ophthalmology,2002-2003.
52. Tanabasi PN,Anochie IC.Nkanginieme, K E.O. Pedro-Egbe C N Screening for congenital color vision deficiency in primary children in Port Harcourt City. Teachers' knowledge and performace MEDLINE 19048761
53. Chia,A. Gazzard G.Tong L. Zhang X. Sim EL. Fong A. Mei Saw S. Red-Green colour blindness in Singaporean children. MEDLINE 18942220
A szakmai irányelv érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai irányelve
A 0-18 éves gyermekek teljeskörű, életkorhoz kötött hallásszűréséről
Készítette: az Országos Gyermekegészségügyi Intézet
a Fül-Orr-Gégészeti Szakmai Kollégiummal,a Csecsemő és Gyermekgyógyászati Szakmai Kollégiummal, és a Védőnői Szakmai Kollégiummal egyeztetve
Az irányelvben használt evidencia szintek, definíciók, rövidítések részletes leírása a függelékben található.
Tartalomjegyzék
1. Bevezetés
2. Az Irányelv célkitűzése
3. Az Irányelvcélcsoportjai
4. Az Irányelvalkalmazási /érvényességi területe
5. Az Irányelvtémaválasztásának indoklása
6. Jogszabályi háttér
7. A gyermekkori tartós halláscsökkenés epidemiológiája
8. A gyermekkori tartós halláscsökkenés patológiája
9. A teljeskörű újszülöttkori hallásszűrés (UNHS)
10. Az újszülöttkori hallásvizsgálatok algoritmusa, módszertana és feltételei
11. Csecsemő és gyermekkori hallásvizsgálatok szűrési és diagnosztikus algoritmusa
12. A kiszűrt, nagyotthalló gyermekek ellátása, gondozása
13. Irodalomjegyzék
A szakmai irányelv érvényessége
Függelék
Nyilatkozatok
1. Bevezetés
A zavartalan beszéd- és nyelvfejlődés szempontjából az ún. kritikus életszakaszok idején elengedhetetlenül fontos, hogy a hallópályákon keresztül a hallóközpontokba állandó ingerület érkezzen, történjék az akár az élettani hanginger-átalakítás, akár az implantátumon keresztül érkező elektromos ingerek által (1). Az egyes nyelvi funkciók megjelenése a beszédfejlődés során az idegi elemek strukturálódásának bizonyos szakaszaihoz kötött. Moore neuroanatómiai vizsgálatai alapján a hallókéreg érése során három fejlődési szakaszt ír le, melyek mindegyikét más axonális rendszer kiépülése jellemzi. Vizsgálatai alapján 12 éves korra lezajlik azoknak a kommunikáló idegrost-kötegeknek a kiépülése, amelyek a hallókéreg egyes részei között teremtenek kapcsolatot (2). Sharma corticalis potenciálok P1 hullámának latenciáját vizsgálva süket és ép hallású gyermekeknél megállapítja, hogy 3 és fél éves kortól az agyi plaszticitás fokozatosan csökken, majd 7 éves korra igen nagymértékben beszűkül (3,4IA). Amennyiben a hallás károsodottságát nem fedezik fel elég korán, a korai beszédfejlődési periódus kritikus lezáródásáig, akkor az érintett gyermekszámára később már igen bonyolult, vagy éppen lehetetlen elsajátítani a nyelv alapelemeit. Kommunikációs sérültté válik. Általánosságban elmondható, hogy azoknál a gyermekeknél akiknek halláscsökkenése van, késik a szókincs kifejlődése, a nyelvtan elsajátítása, a beszélgetés és az olvasás (5 II-2, B;6 II-2, B; 7-12).
Ez a hátrány már 3 éves kor előtt is mérhető, (13 II-2, B) és egy egész életre kiható következményei lehetnek. A gyermeknek késik a szociális és kognitív fejlődése, melyek alapjául szolgálnak a későbbi beiskolázásnak és a társadalomban való boldogulásnak. Mindez igen nagy terheket ró mind a közvetlen, mind a tágabb környezetre. Számos vizsgálat igazolta, a halláscsökkenés korai felismerésének és a korán megkezdett rehabilitációnak a beszédfejlődésre kifejtett pozitív hatását (13 II-2, B; 14 II-2,C; 15 II-2, B; 16II-2, B, 17II-2 B; 18II-2, B, 19II-2, B; 20,21,22). A későbbi életkorban manifesztálódó vagy később kialakuló halláskárosodás is visszaveti a gyermek nyelvi fejlődését, ezáltal iskolai teljesítményét. Romlanak a kapcsolatteremés lehetőségei, ami pszichés-mentális defektusokban nyilvánulhat meg. Csökken illetve beszűkül a továbbtanulás és a pályaválasztás lehetősége. A hallászavar jelentősen rontja az életminőséget.
Újszülött-, és csecsemőkorban a halláscsökkenést nem könnyű észrevenni. Általános tapasztalat, hogy szűrés nélkül a súlyos, veleszületett nagyothallást csak 2-3 éves korban diagnosztizálják, és kezdik meg kezelni, amikor már jelentősen csökkennek a rehabilitáció esélyei.
Óvodás-iskolás korban az enyhe-közepes nagyothallást nehéz időben észlelni. Ilyenkor a gyakori visszakérdezés, a figyelmetlenség, a televízió, rádió stb. hangos hallgatása hívhatja fel erre a figyelmet. Ebben az életkorban igen gyakori a savóképződéssel járó középfül gyulladás (otitis media catarrhalis acuta et chronica serosa), és mivel nem jár fülfájással, könnyen elnézhető.
Meghatározott életkorban végzett teljes körű szűrővizsgálatokkal a nagyothallások időben diagnosztizálhatók és kezelhetők illetve rehabilitálhatók.
Az Irányelv az életkorhoz kötött szűrések módszertanát, kivitelezését írja le.
2. Az Irányelv célkitűzése
Korszerű elméleti és gyakorlati ismeretek nyújtása a gyermekkori hallásszűrést végző szakemberek számára annak érdekében, hogy a hallászavarok időben felismerésre és kezelésre kerüljenek.
3. Az Irányelv célcsoportjai
Ellátandók: minden 0-18 éves gyermek Ellátók:
- Orvosok: újszülött- és neonatalis-intenzív osztályokon, háziorvosok, házi gyermekorvosok, fül-orr-gégész szakorvosok, audiológus szakorvosok
- Szakdolgozók: kórházi-, területi- és iskolavédőnők, neonatológiai szakápolók, audiológus-, elektrofiziológiai szakasszisztensek, akusztikusok
- Szurdopedagógusok
4. Az Irányelv alkalmazási /érvényességi területe
Az Irányelv érvényességi területe Magyarország. A kórházak újszülött, újszülött intenzív (NICU), gyermekgyógyászati és fül-orr-gégészeti osztályai, fül-orr-gégészeti rendelők, audiológiai állomások. Gyermekegészségügyi alapellátás és iskolaegészségügyi ellátás.
5. Az Irányelv témaválasztásának indoklása
A gyermekek hallásszűréséről nincs érvényes irányelv, a hallásszűrésről utoljára 1983-ban adtak ki irányelvet: 7006/1983 (Eü. K.12.) "A 0-18 évesek audiológiai szűrővizsgálatáról" címmel, amely ma már korszerűtlen és nem hozzáférhető.
6. Jogszabályi háttér
Az Útmutató fejlesztésének szükségességét a következő jogszabályok és nemzeti programban foglalt feladatok indokolják:
51/1997. (XII. 18.) NM rendelet, illetve módosítása: 67/2005. (XII. 27.) EüM rendelet A kötelező egészségbiztosítás keretében igénybe vehető, betegségek megelőzését és korai felismerését szolgáló egészségügyi szolgáltatásokról és a szűrővizsgálatok igazolásáról. A rendelet 1. számú melléklete foglalja magában a gyermekkorban, meghatározott életkorban elvégzendő szűrővizsgálatokat.
49/2004. (V. 21.) ESzCsM rendelet a területi védőnői ellátásról (3 § dd)
1092/2007. (XI. 29) Kormányhatározatának kiemelt fejlesztési területekhez kapcsolódó intézkedési terve, melynek I.A) 2.) alapján: "Ki kell dolgozni a 0-7 éves korú gyermekek fejlődésének komplex (szomatikus, pszichomotoros, érzékszervi, kognitív stb.) méréséhez és követéséhez szükséges állapotfelmérő adatlapok standardjait és eljárási protokolljait annak érdekében, hogy a fejlődésben való megakadás és a fejlődést hátráltató problémák időben felismerhetők és kezelhetők legyenek."
A "Közös Kincsünk a Gyermek" Nemzeti Csecsemő- és Gyermekegészségügyi Program I. célkitűzésének 13. pontja: az újszülöttkori hallás- és látásszűrések egységes módszertanának biztosítása.
A vizsgálati és terápiás eljárásrend kidolgozásának, szerkezetének és szakmai egyeztetése lefolytatásának eljárásrendjéről a 23/2006 (V.18.) EÜ. M rendelet rendelkezik.
7. A gyermekkori tartós halláscsökkenés epidemiológiája
A veleszületett, súlyos, a beszéd megtanulását segítség nélkül lehetetlenné tevő bilaterális percepciós hypacusis gyakorisága a normál populációban 1-3 ezrelék (23-30).
Ez a leggyakoribb születéskori érzékszervi defektus, a születéskor szűrt metabolikus betegségekkel összehasonlítva az
USA-ban a kongenitális sensorineuralis halláscsökkenés ötvenszer gyakoribb, mint a phenylketonuria, háromszor gyakoribb, mint a Down kór, hatszor gyakoribb, mint a spina bifida (31 III, D; 32 III, D; 33 III, D).
Az intenzív újszülött osztályon kezelt újszülöttek körében ez egy nagyságrenddel gyakoribb, 4-5 % (34). Az USA-ban évente 4000 újszülött születik súlyos-nagyfokú kétoldali sensorineuralis halláscsökkenéssel (35, 36, 37), és 8000 fő egyoldali súlyos- nagyfokú vagy kétoldali enyhe-közepes fokú sensorineuralis halláscsökkenéssel (38).
Ez azt jelenti, hogy 1000 újszülöttből legalább 1 kétoldali, legalább 40dB-es sensorineuralis hallácsökkenéssel születik (23-30).
Ezek az adatok megegyeznek az univerzális hallásszűrést objektív módszerrel végző egyéb fejlett országok eredményeivel, amelyek 1000 vizsgáltból 2-4 sensorineuralis halláscsökkenésben szenvedő újszülöttet találtak (39-40, 41 II-2, B; 42,43 B; 44- 46,47 II-2, C).
Hazánkban már az 1990-es évek elején számos vizsgálat számolt be az újszülöttek OAE módszerrel végzett hallásszűréséről, de ezek csak célzott és időszakos vizsgálatok voltak (48). Az első valóban teljeskörűnek nevezhető UNHS-programokról 1998-ban számoltak be bajai és pécsi munkacsoportok. Eredményeik a nemzetközi epidemiológiai adatoknál kissé magasabb, 3,6 ezrelék előfordulási gyakoriságot mutattak (49-53).
2001-ben már 8,2005-ben már 27 helyen folyt objektív, teljeskörűséget célzó szűrés. 2006 májusában a Lions Klubok Magyarországi Szövetsége jóvoltából további 12 intézet kapott újszülöttek hallásszűréshez mérőeszközt. Egy 2006 februárjában készült - önkéntes adatszolgáltatáson alapuló - felmérés szerint a 2005-ben Magyarországon született 97.500 gyermekből 31.294-et (32%) szűrtek meg ezen metódus szerint (52).
Csecsemőkorban és a kisdedkorban a hypacusist okozó savós középfülgyulladás nagyon gyakori. 0-2 éves korig előfordulási gyakorisága meghaladja a 80 %-ot (54 II-3, C; 55 II-2, B). Egy, a témával foglalkozó irodalmi áttekintés szerint a savós középfülgyulladás prevalenciája a születéstől kezdve fokozatosan nő, maximumát kb. 2 éves korban éri el. Ezután egy egyenletes csökkenés következik, majd ismét a prevalencia emelkedése figyelhető meg 5 éves korban. Ez az emelkedés valamivel alacsonyabb az előzőnél (56 II-3, C).
Hazánkban egy BAZ megyei szűrési adatokat (0-iskolás korig) feldolgozó tanulmány 68651 gyerekből 14,1% -nál középfül folyamatot (fülkürt zavart, vagy savós középfülgyulladást) igazolt (57).
A savós középfülgyulladás legtöbbször átmeneti hallászavart jelent, de az esetek mintegy 10-20 %-ában kezelést igényel. A nem kezelt, elhanyagolt esetekben tartós nyelvi-beszédfejlődési hátrány alakul ki (8,9,12,1,58 II-2, B).
Az iskoláskorú gyermekeknél diagnosztizált halláscsökkenések egy része valószínűleg enyhe fokú veleszületett progresszív halláscsökkenés, mely nem elég nagyfokú ahhoz, hogy kisgyermekkorban diagnosztizálják. A 3-6 kHz-re korlátozódó küszöb emelkedés esetén zajártalom valószínűsíthető, ennek gyakorisága 6-7 éves korban nemzetközi adatok alapján 6-8% (59,60), 19 éves korra már 12,5% (61,62).
A tartós enyhe fokú halláscsökkenés, különösen ha csak néhány frekvenciát érint szintén felderítetlen maradhat iskoláskorig. Enyhe fokú halláscsökkenés (beleértve az egyoldali halláscsökkenést is), amely az iskoláskorú gyermekek 10-15%-át érinti, negatív hatással van az iskolai teljesítményre és szociális kihatásai is vannak.(63 II-2, C).
8. A gyermekkori tartós halláscsökkenés patológiája
Az újszülöttkori nagyothallások legtöbbször sensorineuralis (percepciós) típusúak. Újszülött korban (a koraszülöttek kivételével) az otitis media különböző formái ritkák.
A veleszületett, percepciós hypacusisok mintegy 50 %-ban genetikai eredetűek. A legtöbb esetben mindkét szülő normál hallású, tehát recesszívöröklődésű nem szindrómás sensorineuralis halláscsökkenésről van szó (az összes eset 75-80%-ában). A genetikai eredetű halláscsökkenések 20%-a autoszomális domináns öröklődésű, 2-5%-a X kromoszómához kötött, 1% mitochondrialiseredetű.(35) Az esetek kb. felében a GJB2 gén pontmutációjáról (35delG-Connexin 26 fehérje kódonja) van szó (64).
Az autoszomális domináns, nem szindrómás halláscsökkenéseket általában iskoláskorban rutin szűrés során diagnosztizálták. A szindrómás senzorineuralis halláscsökkenésekegy része is ekkor kerül felismerésre, pl. a Pendred és Usher szindróma, mely autoszomális recessziv öröklődésű betegség, így a családi anamnézis negatívitása nem jelzi a rizikófaktort.
A veleszületett nem genetikai, környezeti okok adják a percepciós hypacusisok másik felét. Sok nőt érhet a terhesség alatt fertőzés, a kórokozók közül csak néhány képes károsítani a placentát és a magzatot. Ezek a kórokozók nem csak hallásromlást, de látás-, magatartás- és neurológiai funkció zavart is okozhatnak pl. cytomegalovírus, toxoplasma, rubeola, mumps vírus (1. táblázat). A gyermekkori halláscsökkenés rizikófaktorait a 2. táblázat foglalja össze (65,66).
A fertőzésen kívül további környezeti rizikó faktorok: az intenzív újszülött osztályon való kezelés, craniofacialis anomáliák. Önmagában az intenzív osztályon való kezelés növeli a kétoldali sensorineuralis és kevert típusú halláscsökkenés valószínűségét (67).
A sensorineuralis halláscsökkenés környezeti és genetikai okait az 1. számú ábra szemlélteti (35).
A csecsemőkorban a fülkürt anatómiája és a gyermeket érő infekciók magyarázzák a gyakori savós középfül gyulladás okozta vezetéses nagyothallást (68). A halláscsökkenés mértéke általában nem haladja meg a 30 dB-t a beszédfrekvenciákon, fájdalommal nem jár, ugyanakkor a beszéd megtanulását nehezítheti, ha tartósan fennáll (55 II-2 B; 58II-2 B).
A csecsemő és kisdedkori fülkürt működés zavarát, középfül-gyulladásokat elősegítő tényezőket a 3. számú táblázat szemlélteti (68).
Iskoláskorú gyermekeknél a 3-6 kHz-re korlátozódó küszöb emelkedés esetén zajártalom valószínűsíthető, melynek kiváltásában hangot kibocsájtó játékok (némelyik akár 150 dB erősségűt) később a hangos zene hallgatása (fülhallgatón keresztül gyakran 100dB hangerővel) játszhat szerepet (69-72).
9. A teljeskörű újszülöttkori hallásszűrés (UNHS)
A halláscsökkenés korai kimutatásásnak és korai rehabilitációjának jelentősége
Kutatások szerint, a kiterjedt szőrsejtdegeneráció a ganglionsejtek és hallóidegrostok, valamint a nucleus cochlearis sejtek retrográd elfajulását, illetve a nucleus cochlearis sejtjeinektökéletlen érését okozza. A felsőbb hallópályákteljes kifejlődése is postnatalisan zajlik, melyhez szükségesek a hangingerek. (73).
Amennyiben akár az enyhe vagy csupán egyoldali halláscsökkenés is felderítetlen marad, már az is komoly következményekkel járhat (74-77 II-2 B; 78 II-3 C; 79 II-2 B; 80 B; 81 B; 82 B; 83 II-2 C). Bizonyított, hogy az egyoldali hallássérült gyermekeknek tízszer nagyobb az esélye arra, hogy normál hallású társaiknál legalább egy osztályzattal gyengébb iskolai teljesítményt, érjenek el. További kutatások hasonlították össze a hat hónapos koruk előtt kimutatott és megfelelő ellátásban részesült gyermekek teljesítményét, a hat hónapon túl ellátottakéval (37 B;84 B). Az első osztály befejezésekor, a korán kezelt gyermekek nyelvi, kognitív és szociális fejlettsége egy-két évvel előrébb járt, mint társaiké, akiknél később kezdtéka rehabilitációt. Egy másiktanulmányban a szókincset, a szóértést és a kifejezőkészséget vizsgálva, szintén szignifikáns különbséget találtak a korábban ellátott gyermekek javára (15 II-2 B; 85).
Az UNHS alkalmazásával lehetőség van a korai diagnózis felállitására, és a korai rehabilitáció megkezdésére (86 B). Az adekvát terápia időben megtörténő alkalmazása bizonyítottan képes csökkenteni vagy akár megszüntetni a későbbi életkorban jelentkező különbségeta hallóként és a nagyothallóként vagy akár a süketen született gyermekek fejlődése, nyelvi készsége között. A praelingualis süket gyermekek (akik a hallásukat a beszéd kialakulása előtt vesztették el) számára a korai cochlearis implantátummal történő ellátás, majd az adekvát hallásrehabilitáció a csecsemőkortól 12 éves korig, az agyi plaszticitást kihasználva teremti meg a lehetőséget a hallópályák kiépítésére. Ezzel a kezelés esélyt biztosít az audioverbális kommunikáció elsajátítására, így a gyermekek később a normál hallók között folytathatják tanulmányaikat. Lehetővé válik számukra a társadalomba való beilleszkedés (4 I A; 73, 87 I A; 88 I
A;).
A régebben használatos szubjektív módszerek, az úgynevezett acustico-emocionális - a hang hatására bekövetkező viselkedésváltozásokon alapuló - tesztekről mára kiderült, hogy alkalmazhatóságuk az újszülöttkori halláscsökkenések kimutatásában a súlyos fokúra korlátozottan, a közepes fokúra alig, a kisfokúra, egyoldalira pedig egyáltalán nem alkalmasak, igen nagy a tévesztési arányuk.
A teljes körű újszülöttkori hallásszűrés (UNHS) minőségi indikátorai
A teljes körű újszülöttkori hallásszűrésnek 100 %-ban szenzitívnek, és nagyfokban specifikusnak kell lennie, azaz minden nagyothallót ki kell szűrjön a módszer, lehetőleg minél kevesebb tévesen pozitív eredménnyel (utóbbiak diagnózisa a verifikálás során tisztázható).
A "teljes körűség": az intézetben születettekés a hazabocsátásig - vagy otthon szülés ill.a kórházi szűrésből bármilyen ok folytán kimaradtak esetén 1 hónapos korig -, megszűrtek százalékos arányának 96% vagy e felett kell lennie, mert egyébként hatástalanná válika szűrés. A halláscsökkentek mintegy felénél van csak kimutatható rizikó faktor (41 II-2 B), vagyis ha csupán azokat az újszülötteket szűrnénk akiknél rizikó faktor van jelen, akkor a hallássérültek másik fele csak megkésve kerülne diagnosztizálásra (89 II-3 C; 90 II-2 B; 91 II-3 C; 92 II-2 B; 93 II-3 C; 94 II-2 B). Ez is azt igazolja, hogy a szűrésnek teljes körűnek kell lennie (43 B;47 II-2 C; 90 II-2 B).
A "visszarendelési ráta": a megszűrtek és a hazabocsátáskor nem megfeleltek százalékos aránya 4-6%-nál nem lehet magasabb, mert a túl nagy számban visszarendelt fals pozitív esetek jelentősen megnövelik a költségeket, nem beszélve a szülőkben feleslegesen keltett aggodalomról.
A "kontrollt teljesítők aránya": míg a szűrésnél potenciálisan ép hallókat vizsgálunk, addig a visszarendeltek a vélt nagyothallók. Ebből következően ennek az értéknek a 100%-ot kell közelítenie. A kontroll teljesítésének monitorizálásában nagy szerepe van az alapellátás házi (gyermek) orvosainak s védőnőinek.
A kiszűrtekellátásának biztosítása: a szűrés megkezdésekor előre biztosítani kell a majdani kiszűrtekés a diagnosztizált hallássérültek progresszív ellátásának továbbküldési útjait, szurdopedagógiai fejlesztésük lehetőségét-amennyiben ezek közül bármelyik az adott intézményben nem megoldható.
A "szakmai irányelv" útmutatásán alapuló helyi protokollokat, vezérfonalakat, szakmai és civil tájékoztatókat, képzési és kontrollálási sémákat kell biztosítani az érintettek részére, melyeket a világhálón szabadon elérhetővé kell tenni.
Szükséges egy rendszeresen frissülő országos adatbázis, kötelezően, egységes szempontok szerint működtetve. A gyermekkori halláscsökkenés korai kimutatása és ellátása köré szerveződött program korrekt végrehajtásához szoros és szabályozott együttműködés szükséges mind a helyi, mind az országos szakmai szervezetek, az állami apparátusok és a civil szervezetek között. A szervezésben neonatológusok, gyermekgyógyászok, védőnők, audiológusok, fül-orr-gégészek, szurdopedagógusok, egészségügyi-népjóléti hatóságok képviselőinek kell együttműködő team-et alkotni. Nagy hangsúlyt kell fektetni a megfelelő kommunikációra mind az érintett szülők, a nagyothallók különböző érdekvédelmi szervezeteinek képviselői, mind a programban érintett résztvevők között.
Az életkorhoz kötött hallásszűrések közül a legnagyobb jelentősége az újszülöttkori szűrésnek van. A korai diagnosztika és ellátás itt eredményezi a leglátványosabb hatást, mivel az élet első néhány hónapja az egész későbbi életre kiható imprintinget jelent. Ezért fontos a teljeskörű, objektív módszeren alapuló hallásszűrés.
10. Az újszülöttkori hallásvizsgálatok algoritmusa, módszertana és feltételei
Újszülöttkori hallásvizsgálat, szűrési és diagnosztikus algoritmus
Szűrési fázis
Újszülöttkorban teljeskörűen, lehetőleg a kórházból történő hazabocsátás előtt OAE-val vagy szűrőBERA-val.
Az UNHS tárgyi minimumfeltétele normál újszülött részlegen szűrő üzemmódú OAE, intenzív újszülött részlegen szűrő BERA (AABR) (lásd még a szakmai minimumfeltételeknél).
Amennyiben a szűrés a kórházi hazabocsátás előtt nem valósul meg (korai hazaadás, otthonszületés, technikai hiba), úgy az adott ellátási területen gondoskodni kell az újszülöttek járóbeteg ellátásában történő teljeskörű szűrővizsgálatáról legkésőbb 1 hónapos korig.
Negatív mérési eredmény (ha mindkét fülén jó eredményt kaptak, minősítésre:"MEGFELELŐ") esetén a gyermekkel további teendő aktuálisan nincs, az eredményt a zárójelentésben rögzíteni kell.
Pozitív mérési eredmény (ha egy vagy egyik fülén sem kaptak megfelelő eredményt, minősítésre:"VISSZARENDELT") esetén a mérés ismétlése, akár többször is még a hazabocsátás előtt. További pozitivitás esetén visszarendelés (zárójelentésben ezt rögziteni kell).
A házi (gyermek) orvos az eredményt feltünteti a kisded dokumentációjában, és az eredménytől - illetve az esetlegesen meglévő rizikófaktoroktól (2. táblázat) - függően menedzseli a további kontrollokat.
Egy hónapos korban a visszarendeltek, illetve a kórházi szűrésből kimaradtak (technikai ok, otthonszülés, stb.) kontrollja vagy a korábbi szürést végző osztályon, vagy a területen szűrést végző audiológiai rendelésen. Negatív mérési eredmény esetén (minősítése: "MEGFELELT") a gyermek igazolást kap az eredményről, amit a területi védőnő és a gyermek házi (gyermek)orvosa rögzít a gyermek dokumentációjában.
Pozitív mérési eredmény esetén (minősítése: "VISSZARENDELT") a gyermeket további vizsgálatra az un. "diagnosztikai fázisra" a területileg illetékes, gyermekek objektív hallásvizsgálatára felkészült speciális audiológiai szakambulanciára kell irányítani.
Diagnosztikai fázis_
Három hónapos korig a végső diagnózis felállítása: fül-orr-gégészeti vizsgálat (mikroszkóppal!), tympanometria, klinikai BERA, MLR esetleg ASSR, kiegészítve szubjektív vizsgálatokkal, lehetőség szerint genetikai vizsgálat. Negatív mérési eredmény esetén (minősítésre: "MEGFELELT"), a gyermek igazolást kap az eredményről, amit a védőnő, a gyermek házi(gyermek)orvosa rögzít a gyermek dokumentációjában.
Pozitív mérési eredmény, azaz diagnosztizált halláscsökkenés esetén a gyermeket az ellátási és rehabiliciós szintre irányítják.
Az ún. rizikó újszülötteket (2. táblázat) - még negatív újszülöttkori OAE vagy szűrőBERA UNHS eredmény ellenére is vissza kell rendelni a diagnosztikai fázisra, majd hathavonta három éves korig.
A 2. ábra algoritmusa összefoglalja az UNHS, a diagnózis, az ellátás és az "utánkövetés" ismereteit.
A teljeskörű újszülöttkori hallásszűrés (UNHS) módszertana
| | Javaslatok a szűrés technikai kivitelezésére |
| - Az első 24 órában semmiképpen ne szűrjünk. A hallójáratban még lehet olyan váladék, ami később felszívódik. A legtöbb szerző csak 48 óra után ajánlja a mérés első ideális időpontját. Ha lehet, az etetés utáni alvást használjuk ki. Meg kell találni az újszülött részleg "csendes időpontjait", ne zavarjuk mindennapi rutinjait. Ebből a szempontból mindenképpen a legelőnyösebb, ha az újszülött osztály nővérei, vagy a kórházi védőnő szűr, akár több szakaszban, akár az éjjeli műszak nyugodtabb periódusában is. Az aktív időszakok (pl.: vizit idején, etetés előtt, fürdetés környékén, látogatáskor, egyéb szűrések alatt stb.) biztosan alkalmatlanoka hallásszűrésre. - Van ahol nem az újszülött részleg dolgozói szűrnek, hanem az audiológiai asszisztensek. Az újszülöttet azonban tilos indokolatlanul szállítani! Ha lehet, akkor az újszülött részlegen külön helyiséget kell biztosítani, ha nem, akkor egy csendes részre kell kérni a babákat. Lehet szűrni a "bölcsőknél" sőt a "rooming in"-ben is, de nehezebb. Átjáráskor minden bonyolultabb: időpont, hely, "otthoniak" segítőkészsége, stb. - Ne takarítsuk a baba fülét, maximum egy óvatos törlés megengedett a hallójárat bemenetében. - A cuppogó, szopizó, váladékos orrú, hurutos újszülött belső zajai zavaróbbak lehetnek a külvilági zajoknál. - OAE mérésénél a fülkagylót hátra-lefelé húzva, enyhe csavaró mozdulattal dugjuk be a szondát a hallójáratba, míg az illeszték pereméig be nem csúszik a hegye. A végén a zsinór a baba fejtetője felé álljon, hogy minél kevesebb súrlódásra legyen lehetőség a baba légzőmozgásainál. - AABR-nél a legfontosabb az elektródák jó rögzítése, és ezek stabil helyzetének megtartása végig a mérés folyamán. - A fölösleges aggodalomkeltés elkerülésére ne használjuk az "átment/nem ment át" minősítéseket, helyettük a "MEGFELELT/VISSZARENDELT" ajánlott. - A szűrési technika betanítása-elsősorban az illeszték behelyezése OAE-nél, elektródok felhelyezése AABR-nél - időszakos ellenőrzése, mindenképpen audiológusi feladat. A mérések szakmai felügyelete is audiológus szakorvosi kompetencia, közös együttműködésben a részleg működéséért felelős neonatológussal. |
| Összehasonlítás: Az objektív hallásvizsgálati módszerek alkalmazhatósága a szűrésben |
| - Az OAE előnye, hogy egyszerűen kivitelezhető, olcsóbb. Hátránya, hogy a hazabocsátásig a babák mintegy 30%-át minimum kétszer kell mérni a fals pozitív visszarendelések számának optimális lecsökkentéséhez (ez a második mérés után 4-6%-ra javul). Hátránya továbbá, hogy nem észleli a centrális léziókat (pl.: auditoros neuropátia/ disszinkrónia), de ezek száma a normál populációban olyan elenyésző, hogy a nemzetközileg elfogadott hibaszázalék alatt marad. (Ezen esetek egyébként is a rizikó újszülöttek közül kerülnek ki, akiket megfelelt minősítéssel zárult első mérés esetén is (akár OAE, akár szűrőBERA) vissza kell rendelni későbbi BERA kontrollra). - A szűrő BERA (AABR) előnye a kisebb visszarendelési ráta (2%), és a retrocholearis eltérésekre való érzékenysége. Hátránya, hogy csak a 2-3 kHz frekvenciatartományban érzékeny, a jelentősen nagyobb költség, a vizsgálat kissé bonyolultabb kivitelezhetősége, hosszabb volta. - A két metódus elterjedtsége a világban régiónként változó, de talán tendenciózusabban normál újszülött részlegeken OAE-val, NICU-ban AABR-rel szűrnek. Leggyakoribb a két szakaszos módszer (OAE ismételve, vagy OAE majd ABR vagy ABR ismételve ennek az eljárásnak a szenzitivitása 100%, specificitása 99% (87. I, A, 88. I, A, 95 II-3, C) |
Időpontja:
- kórházi szűrés: 3-5. életnap.
- ambuláns szűrés (technikai ok, otthonszülés, stb. ok miatt kimaradt): 1 hónapos korig.
- NICU-ban: leghamarabb, amikor az egyéb általános feltételek lehetővé teszik, de legkésőbb az intézeti hazabocsátás előttig, illetve a normál gesztációs időhöz kalkulált plusz 1 hónapos korig.
A teljeskörű újszülöttkori hallásszűrés (UNHS) szakmai feltételei Tárgyi minimum feltétel
Normál újszülött részlegen: szűrő üzemmódú, OAE (TEOAE v. DPOAE) mérésére alkalmas, CE minősítéssel rendelkező készülék.
Intenzív újszülött osztályon (NICU): szűrő üzemmódú BERA (AABR), CE minősítéssel. A Függelék 5. pontjában került felsorolásra az UNHS kivitelezésénél használatos eszközök és gyártók jegyzéke.
Mindkét esetben szigorúan be kell tartani a gyártó, illetve a forgalmazó ajánlásait az időszakosan szükséges alkatrészcserék és kalibrálások tekintetében. Ezeket, az intézet ISO minősítésének megfelelő belső minőségügyi dokumentációjában is fel kell tüntetni, az elvégzett időszakos felülvizsgálatok (általában 1 év) igazolásával együtt.
Szakmai minimum feltétel
A szűréshez nem szükséges audiológiai végzettség, azt az eljárásra betanított személyzet is végezheti. A szűrésben részt vehetnek az újszülött részleg intézeti védőnői, neoantológiai szakápolói, szakorvosai és audiológus ill. elektrofiziológiai szakasszisztensei, akusztikusai, fül-orr-gégész, audiológus szakorvosai is. A szakmai felügyelet audiológus szakorvos feladata.
A szűrésben résztvevők jártassága
A szűrést végző személyek betanításának módja: A programok indulásakor, illetve új munkába lépőnél a betanítást audiológiai végzettségű személynek kell végeznie. Az oktatásnál ki kell térni, OAE esetén, a szonda, BERA esetén, az elektródák helyes és biztonságos használatára. Fontos tudni, hogy az újszülött fülkagylóját, óvatosan hátra-lefele húzva kell a hallójárat bemenetet "nyitni". A hallójáratba tilos beletörölni, maximum a bemenetben esetlegesen lévő cerumen, debris óvatos letörlése megengedett. A szűrő személy feladatait szabatosan leíró helyi protokoll készítése szükséges. Az eszközöket a gyártó utasításainak megfelelően kell használni, fertőtleníteni.
A szűrésben résztvevőknek időszakos képzéseken kell résztvenniük, erről jártassági (licensz) vizsgát kell tenniük. Ezt célszerű az ötéves kredit szerzési periódushoz kötni. El kell érni, hogy egy kezdeti türelmi idő, pl. a következő periódus leteltéig (2015) minden szűrésben érintett megszerezze akreditációját, melyet a következő ciklusokban újra kell validálni. Ezen tanfolyamokat évente, regionálisan, a szűrésben és ellátásban már tapasztalatot szerző munkacsoportok összefogásával kell elérhetővé tenni, egységesíteni. A képzés elméleti részében ki kell térni a szűréshez szükséges anatómiai, élettani, fizikai, patológiai alapismeretekre, a szűrés jogszabályi, szervezési részleteire. Agyakorlati részben el kellsajátítania technikai fogásokat. A jártasság igazolását a mindkét részből letett sikeres vizsga után szerezheti meg a résztvevő, mely a következő képzési ciklusban megújítandó. A szükséges felkészítés és tudás karbantartás a vonatkozó jogszabálynak megfelelően kell történjen.
Kötelező a korrekt dokumentáció és az eredmények időszakos jelentése. A szűrés eredményét ("MEGFELELT" ill. 'VISSZARENDELT") a személyi azonosításra alkalmas jelzéssel dokumentálni kell, azt a gyermek zárójelentésén fel kell tüntetni, visszarendelés esetén a kontroll helyével és idejével együtt. Az eredményeket negyedévente egy központi adatbázisba kell elküldeni.
11. Csecsemő- és gyermekkori hallásvizsgálatok szűrési és diagnosztikus algoritmusa 1 éves korban, az életkorhoz kötött státuszvizsgálat keretében történik.
A vizsgálatot a vizsgálatra felkészített területi védőnő végzi, módszere a BOEL teszt. Ennek lényege, hogy a gyermek figyelmét az egyik vizsgáló valamivel leköti, míg a másik vizsgáló (szülő) egy hangot produkál (kanál vagy kulcs csörgetése) a gyermek látóterén kívül, és a gyermek hang irányába való fordulását vagy pislogását stb. detektáljuk.
3 éves korban az életkorhoz kötött státuszvizsgálat keretében történik. A vizsgálatot a vizsgálatra felkészített területi védőnő végzi, módszere a Barr-féle játékaudiometria. Ennek kivitelezésekor a gyermek hangot hall, és a hang meghallásakor egy számára szórakoztató tevékenységet folytathat (pl. játékkockából tornyot épít, és akkor teheti a következő kockát, ha meghallotta a hangot). Így jó közelítéssel felvehető a hallásküszöb görbe. A vizsgálat eszköze a Magyarországon forgalomban lévő CE minősítéssel rendelkező szűrő audiométer.
5 éves korban, az életkorhoz kötött státuszvizsgálat keretében történik. Fontos, hogy a gyermek az iskolában jól halljon, értse a beszédet és maga is érthetően beszéljen. A hallásszűrést a vizsgálatra felkészített területi védőnő végzi, a szülő segítségével. A vizsgálat csendesített helyiségben, a védőnői tanácsadóban, a gyermekorvosi rendelőben történik. Eszköze a Magyarországon forgalomban lévő CE minősítéssel rendelkező szűrő audiométer, mellyel felvethető a tisztahang hallásküszöb. Kivitelezéséhez a gyermek aktív együttműködése kell, néha ismételt vizsgálat (tanulás, kondicionálás) után lehet elvégezni a vizsgálatot.
13-14 éves korban, az iskolában történő szűrővizsgálat (VII. évfolyam) részeként.
Célja a pályaválasztás segítése. A vizsgálatot az iskolavédőnő- illetve ahol ez területileg szervezett, audiológus szakasszisztens végzi. Helye: iskolaorvosi rendelő, audiológiai állomás. A kivitelezés eszköze a szűrő audiométer.
17-18 éves korban, az iskolában történő szűrővizsgálat (XI.évfolyam) részeként, illetve a szakmai képzést szolgáló oktatási intézményekben az Országos Képzési jegyzékben meghatározott, előírás szerinti időszakos és soron kívüli vizsgálatok részeként. Célja a továbbtanulási alkalmasság és a szakmai alkalmasság elbírálása. A vizsgálatot, az iskolavédőnő illetve ahol ez területileg szervezett, audiológus szakasszisztens végzi. Helye: iskolaorvosi rendelő, audiológiai állomás.
A kivitelezés eszköze a Magyarországon forgalomban lévőCE minősítéssel rendelkező szűrő audiométer. A gyártókés eszközök jegyzéke a Függelék 6. pontja alatt található. Az audiométerek hitelesítésére ill. annak gyakoriságára az ISO 8253:1, a kalibrálásra pedig az ISO 389 vonatkozik, mindig figyelembe véve a gyárrtó ajánlását is.
| A szűrő audiometriai vizsgálat kivitelezése |
| A vizsgálat négy frekvencián (500,1000,2000,4000 Hz) és négy intenzitás szinten (20, 30,40,60dB), lehetőleg csendes helységben, zajvédett fejhallgatóval történik. A vizsgálatot mindíg 40 vagy 60dB-es teszthang kibocsájtásával kezdjük, hogy a vizsgált személy észlelje, milyen hangot kell meghallania. A tényleges vizsgálatot 20dB, 1000Hz és jobb oldali beállítással kezdjük. Két teszthangot bocsátunk ki 3-5 másodpercnyi szünettel. Ha a vizsgált személy észleli ezeket, a vizsgálatokat a következő frekvencián folytatjuk. A vizsgált személynek minden egyes frekvencián kettőt kell észlelnie. Ha ez nem történik meg, ez halláscsökkenésre utal. Ilyen esetben a további hangnyomás szinteken (30, 40, és 60dB ) kell felfelé lépkedve a fent részletezett eljárást megismételni mindaddig, míg a vizsgált személy a három teszthangból már kettőt képes észlelni egy adott hangnyomásszinten. Ezt az eljárást 2000,4000 és 500 Hz-en is el kell végezni |
Diagnózis
A kiszűrt nagyothallók diagnózisának bizonyítása (verifikálás) az audiológiai állomások feladata, valamennyi korosztályban.
A csecsemő és kisdedkorban kiszűrtek verifikálása kiváltott potenciál mérésekkel, valamint a dobüregi folyadék gyülem kimutatására szolgáló tympanometriával történik, előzetes részletes fül-orr-gégészeti vizsgálat után. 5-6 éves kortól elvégezhető a hagyományos klinikai tisztahang audiometria, klinikai audiométerrel. Utóbbi kiegészítendő 5-6 éves kor felett a tympanometriával, a stapedius reflex vizsgálatával (utóbbi eszköze a klinikai tympanometer), esetenként kor szerint adaptált beszédaudiometriával.
12. A kiszűrt nagyothalló gyermekek ellátása, gondozása
A kiszűrt, verifikált nagyothallót mihamarabb, de legkésőbb a diagnózis felállításától számított két héten belül gondozásba kell venni. Az ellátás függ a halláscsökkenés típusától, mértékétől, a beteg életkorától, általános állapotától. Az ellátást, gondozást az audiológiai állomás fül-orr-gégész, audiológus szakorvosa, szakasszisztense végzi.
Az ellátás formái
A "vezetéses" halláscsökkenés rendezése sebészi módszerrel (paracentesis, váladékeltávolítás, ventillációs tubus, adenotomia) történik. Fejlődési rendellenesség esetén hallókészülék is szóba jön (esetleg kombináltan a sebészivel: BAHA).
Amennyiben az "idegi" halláscsökkenés a két fülön külön-külön, a beszédfrekvenciák (250-500-1000-2000 Hz) átlagában a 25 dB-t eléri vagy meghaladja, hallókészülékkel történő ellátást és gondozást tesz szükségessé. A hallókészüléket viselő beteg rendszeres ellenőrzését, a készülék beállítását, az elemek cseréjét az audiológiai állomás szakorvosa, szakasszisztense végzi.
A hallókészülékes ellátást meg kell kezdeni a diagnózistól számított két héten belül, kisdednél lehetőleg hat hónapos kor előtt. Amennyiben ez a halláscsökkenés mértéke miatt nem eredményes, akkor a cochlearis implantáció lehet szükséges, lehetőleg két éves korig. Ahhoz, hogy ezek a gyermekek minél hamarabb műtétre kerülhessenek, eredményes újszülöttkori hallásszűrésre és a kiszűrt gyermekek kellő időben konvencionális hallókészülékkel való ellátására, valamint cochlearis implantációs programba való felvételére van szükség Az implantációs életkor jelentős hatással van a későbbi funkcionális eredményekre. Fordított arányban állnakegymással: minél fiatalabb korban esikát a gyermek az implantátum beültetésén, annál gyorsabb a beszédértés kialakulása, az érthető beszéd megjelenése és az erre épülő nyelvi funkciók fejlődése (4 I, A).
Rehabilitáció, szurdopedagógiai ellátás: a korai beavatkozás fontos eleme a készülékes/implantációs ellátást követő szurdopedagógiai fejlesztés haladéktalan beindítása, a gondozásba vétel.
Team munka:
Fontos hangsúlyozni a gyermekkori tartós halláscsökkenés korai kimutatásában és korai ellátásában részt vevő interdiszciplináris csapatmunka jelentőségét, melynek összehangolása elengedhetetlen. Meg kell nevezni a helyi koordinátort. Leginkább célravezető, ha ezt a szerepet a helyi audiológus szakorvos tölti be.
13. Irodalomjegyzék
1. Ruben RJ. A time frame of critical/sensitive periods of language development. Acta Oto-Laryngol 1997;117:202-205.
2. Moore J. K. Maturation of human auditory cortex: implications for speech perception. Ann Otol Rhinol Laryngol Suppl. 2002; 189,111,5,7-10.
3. Sharma A, Dorman M.F, Spahr A.J. A sensitive period for the development of the central auditory system in children with cochlear implants: implications for age of implantation. Ear Hear 2002;23,532-539.
4. Rezes Sz, O'Donoghue, Sziklai I. Az életkor szerepe a praelingualis süket gyermek cochlearis implantáció utáni hallás rehabilitációjában. Fül-orr-gégeggyógyászat 2003; 49 (4):207-215.
5. Watkin P, McCann D, Law C, Mullee M, Petrou S, Stevenson J, Worsfold S, Yuen H M, Kennedy C. ?Language Ability in Children With Permanent Hearing Impairment: The Influence of Early Management and Family Participation Pediatrics 2007; 120: e694-e701.
6. KennedyC.R,McCann D.C.,Campbell M. J,LawC.M.,Mullee M., Petrou S., Watkin P.,Worsfold S.,Yuen H. M.,Stevenson J Language Ability after Early Detection of Permanent Childhood Hearing Impairment. N Engl J Med 2006; 354:2131-2141.
7. Ruben RJ. Effectiveness and efficacy of early detection of hearing impairment in children. Acta Otolaryngol.1991;482:127-131.
8. Rach GH, Zielhuis GA, van den Broek P. The influence of chronic persistent otitis media with effusion on language development of 2- to 4-year-olds. Int J Pediatr Otorhinolaryngol. 1988;15:253-261.
9. Zinkus PW, Gottlieb MI. Patterns of perceptual and academic deficits related to early chronic otitis media. Pediatrics. 1980;66:246-253.
10. Moeller MP, Osberger MJ, Eccarius M. Receptive Language Skills: Language and Learning Skills of Hearing-Impaired Children. Bethesda, Md: American Speech, Language and Hearing Association; 1986.Monographs of the American Speech, Language and Hearing Association, 23:41-53.
11. Carney AE, Moeller MP. Treatment efficacy: hearing loss in children. J Speech Lang Hear Res. 1998;41:S61-S84.
12. JL Paradise, CA Dollaghan, TF Campbell, HM FeldmanLanguage, Speech Sound Production, and Cognition in Three-Year-Old Children in Relation to Otitis Media in Their First Three Years of Life Pediatrics 2000; 105:1119-1130.
13. Yoshinaga-Itano C, Apuzzo ML. The development of deaf and hard of hearing children identified early through the high-risk registry. Am Ann Deaf 1998; 143(5):416-24.
14. Yoshinaga-Itano C, Coulter D, Thomson V. The Colorado Newborn Hearing Screening Project: effects on speech and language development for children with hearing loss. J Perinatol 2000; 20 (8 Pt 2):S 132-7.
15. Yoshinaga-Itano C, Sedey AL, Coulter DK, Mehl AL. Language of early- and later-identified children with hearing loss. Pediatrics 1998; 102 (5):1161-71.
16. Yoshinaga-Itano C, Apuzzo ML. Identification of hearing loss after age 18 months is not early enough. Am Ann Deaf 1998; 143 (5):380-7.
17. Apuzzo M-rL, Yoshinaga-Itano C. Early identification of infants with significant hearing loss and the Minnesota child development inventory. Semin Hear 1995;16 (2):124-39.
18. Moeller MP. Early intervention and language development in children who are deaf and hard of hearing. Pediatrics 2000; 106 (3): E 43.
19. Calderon R, Naidu S. Further support of the benefits of early identification and intervention with children with hearing loss. Volta Review 2000; 100(5), 53-84.
20. Kuhl PK, Williams KA, Lacerda F, Stephens KN, Lindbloom B. Linguistic experience alters phonetics perception in infants by six months of age. Science 1992; 255:606-08.
21. Gopnik A, Meltzoff AN, Kuhl PK. The scientist in the crib: Minds, brains, and how children learn. New York: William Morrow and Company; 1999.
22. Sininger YS, Doyle KJ, Moore JK. The case for early identification of hearing loss in children. Auditory system development, experimental auditory deprivation, and development of speech perception and hearing. Pediatr Clin North Am 1999;46(1):1-14.
23. Maki-Torkko EM, Lindholm PK, Vayrynen MRH, Leisti JT, Sorri MJ. Epidemiology of moderate to profound childhood hearing impairments in northern Finland: any changes in ten years? Scand Audiol. 1998;27:95-103.
24. Fortnum H, Davis A. Epidemiology of permanent childhood hearing impairment in Trent Region, 1985-1993. Br J Audiol. 1997;31:409-446.
25. Karikoski JO, Marttila TI. Prevalence of childhood hearing impairment in southern Finland. Scand Audiol. 1995;24:237-241.
26. Parving A, Jensen JH. Prevalence of permanent childhood hearing impairment: its role in audit of local paediatric hearing health services. J Audiol Med.1998; 7:100-108.
27. Boyle CA, Yeargin-Allsopp M, Doernberg NS, Holmgreen MS, Murphy CC, Schendel DE. Prevalence of selected developmental disabilities in children 3-10 years of age: the metropolitan Atlanta developmental disabilities surveillance program, 1991. Mor Mortal Wkly Rep CDC Surveill Summ. 1996;45:1-14.
28. Van Naarden K, Decoufle P, Caldwell K. Prevalence and characteristics of children with serious hearing impairment in metropolitan Atlanta, 1991-1993. Pediatrics. 1999;103:570-575.
29. Stein LK. Factors influencing the efficacy of universal newborn hearing screening. Pediatr Clin North Am. 1999;46:95-105.
30. Fortnum H,SummerfieldQ, Marshall D, Davis A, Bamford J. Prevalence of permanent childhood hearing impairment in the United Kingdom and implications for universal neonatal hearing screening: questionnaire based ascertainment study. BMJ. 2001; 323:536.
31. Leonard DR, Shen T, Howe HL, Egler T, eds. Trends in the prevalence of birth defects in Illinois and Chicago 1989 to 1997.Epidemiologic report series 99:4. Springfield, IL: Illinois Department of Public Health, 1999.
32. Stierman L. Birth defects in California: 1983-1990. The California Birth Defects Monitoring Program, California Department of Health Services, 1994.
33. White KR. The current status of EHDI programs in the United States. Ment Retard Dev Disabil Res Rev 2003; 9: 79-88.
34. White KR, Vohr BR, Behrens TR. Universal newborn hearing screening using transient evoked otoacoustic emissions: results of the Rhode Island haring Assessment Project. Semin Hear 1993;14(1):18-29.
35. Smith RJH, Bale JFJr, WhiteKR: Sensorineural hearing loss in children. Lancet 2005; 365: 879-90.
36. Mohr PE, Feldman JJ, Dunbar JL, et al. The societal costs of severe to profound hearing loss in the United States. Int J Technol Assess Health Care 2000; 16:1120-35.
37. Thompson DC,McPhillips H, Davis RL, Lieu TL, Homer CJ,Helfand M. Universal newborn hearing screening: summary of evidence. JAMA 2001; 286: 2000-10.
38. White KR. Early hearing detection and intervention programs: opportunities for genetic services. Am J Med Genet A 2004; 130: 29-36
39. Parving A. The need for universal neonatal hearing screening: some aspects of epidemiology and identification. Acta Paediatr Suppl 1999; 432: 69-72.
40. Mason JA, Herrmann KR. Universal infant hearing screening by automated auditory brainstem response measurement. Pediatrics 1998;101:221-28.
41. Mehl AL, Thomson V. Newborn hearing screening: the great omission. Pediatrics 1998; 101: 1-6.
42. Maxon AB, White KR, Vohr BR, Behrens TR. Using transient evoked otoacoustic emissions for neonatal hearing screening. Br J Audiol 1993; 27:149-53.
43. Wessex Universal Neonatal Hearing Screening Trial Group. Controlled trial of universal neonatal screening for early identification of permanent childhood hearing impairment. Lancet 1998; 352:1957-64.
44. Barsky-Firkser L, Sun S. Universal newborn hearing screenings: a three-year experience. Pediatrics 1997; 99: E4.
45. .Johnson JL, Kuntz NL, Sia CC, White KR, Johnson RL. Newborn hearing screening in Hawaii. Hawaii Med J 1997; 56: 352-55.
46. White KR. Screening programmes for hearing impairment. In: Griffin A,ed. Atextbookof audiological medicine: clinical aspects of hearing and balance. London: Martin Dunitz Publishers, 2002:339-48.
47. Prieve BA, Stevens F. The New York state universal newborn hearing screening demonstration project: introduction and overview. Ear Hear 2000; 21: 85-91.
48. Katona G, Büki B, Ribári O. Otoakusztikus emisszió vizsgálata újszülötteken és koraszülötteken. Fül-orr-gégegyógyászat 1992; 38:143-147.
49. Pytel J: Univerzális újszülöttkori hallásszűrés. Fül-orr-gégegyógyászat. 1998 44; 66-76.
50. Vincze O, Pytel J, Eklics J, Erti T. Univerzális újszülöttkori hallásszűrés kezdeti tapasztalatai Fül-orr-gégegyógyászat 1998; 44 (2): 77-84.
51. Beke Zs, Deutsch O, Turi K, et al. Teljeskörű objektív újszülöttkori hallásszűrés megvalósítása Baján. Fül-orr-gégegyógyászat 1998; 44:86-91.
52. Beke Zs: Az újszülöttkori hallásszűrés céljai, lehetőségei, eredményei és a szűrőhálózat kialakulásánakeddigi alakulása hazánkban Gyermekorvos Továbbképzés 2006; 5: 264-269.
53. Pytel J. Univerzális újszülöttkori hallásszűrés. Magyar Orvos 2007; 15:22-25.
54. Engel J, Anteunis L,Volovocs A, Hendrisk J, Marres E. Prevalance rates of otitis media with effusion from 0-2 years of age: healthy-born versus high-risk-born infants Int J of Pediatric Otolaryngology 1999; 47: 243-251.
55. Zielhuis GA, Gerold H, Rach G, Van Denbroek P. The occurrence of otitis media with effusion in Dutch pre-school children Clinical Otolaryngology 1990; 15:2,147-153.
56. Zielhuis GA, Rach GH, Bosch A, Broek P.The prevalence of otitis media with effusion: a critical review of the literature.Clin. Otolaryngol 1990; 15:283-288.
57. Balog Cs, Szabó Zs, Szakács L, Turi B, Szakács G. Gyermekek komplex audiológia szűrésének eredményei Borsod-Abaúj-Zemplén megyében Gyermekgyógyászat 2008; 59. (4):62-66.
58. Ruben RJ, Wallace IF, Gravel J. Long term communication deficiencies in children with otitis medis during their first years of life. Acta Oto-Laryngol 1997;117:206-207.
59. Kruppa B, Dieroff HG, Ising H. Sensorineurale Gehörschaden bei Schulanfangern. HNO 1995; 43: 31-4.
60. HaapaniemiJ. The 6kHz acoustic dip in school-aged children in Finland. Eur Arch Otorhinolaryngol 1995;252:391-94.
61. Niskar AS, KiesakSM, Holmes AE, Esteban E, Rubin C, Brody DJ. Estimate prevalence of noise-induced hearing threshold shifts among children 6 to 19 years of age: the Third National Health and Nutrition Examination Survey, 1988-1994, United States. Pediatrics 2001; 108: 40-43.
62. Niskar AS, KiesakSM, Holmes AE, Esteban E, Rubin C, Brody DJ. Prevalence of hearing loss among children 6 to 19 years of age: the Third National Health and Nutrition Examination Survey. JAMA1998; 279:1071-75.84.
63. Bess FH, Dodd-MurphyJ, Parker RA: Children with minimal sensorineural hearing loss: prevalence, educational performance, and functional status. EarHear. 1998;19(5): 339-53.
64. Pandya A, Arnos KS,XiaXJ etal. Frequency and distribution of GJB2 (connexin 26) and GJB6(connexin 30) mutations in a large North American repository of deaf probands. Genet Med 2003; 5:295-303.
65. Joint Committee on Infant Hearing. Year 2007 Position Statement: Principles and Guidelines for Early Hearing Defection and Intervention Programs. Pediatrics 2007; 120; 898-921.
66. Cunningham M,CoxEO;theCommiteeon Practice and Ambulatory Medicine; and the Section on Otolaryngology and Bronchoesophagology. Hearing Assessment in Infants and Children: Recommendations Beyond Neonatal Screening Pediatrics 2003; 111;436-440.
67. Davis A, Wood S. The epidemiology of childhood hearing impairment: factors relevant to planning of services. Br J Audiol1992;26: 77-90.
68. Kenna M.A., Latz A. D.: Otitis media with effusion. In Head & Neck Surgery-Otolaryngology. 1265-1275. 4.Edition. Ed.:Bailey JB & Johnson JT. LippincottW&W Philadelphia 2006
69. OrchikDJ,WarkDJ. Hearing hazard of toy cellular telephones and walkie talkies. Clin Pediatr 1995; 34: 278-80.
70. Hetu R, Fortin M. Potential risk of hearing damage associated with exposure to highly amplified music. J Am Acad Audiol 1995;6:378-86.
71. Lees RE, Roberts JH, Wald Z. Noise induced hearing loss and leisure activities of young people: a pilot study. Can J Public Health 1985; 76:171-73.
72. Mostafapour SP, Lahargoue K, Gates GA. Noise-induced hearing loss in young adults: the role of personal listening devices and other sources of leisure noise. Laryngoscope 1998; 108:1832-39.
73. Küstel M, Répássy G. Cochlearis implantáció, a süketség gyógyításának újmódszere.Háziorvosi Továbbképző Szemle:.2006; 11.(8) 789-793.
74. Bess FH,Tharpe AM, Gibler AM. Auditory performance of children with unilateral sensorineural hearing loss. Ear Hear. 1986;7(1): 20-6.
75. BovoR, Martini A, Agnoletto M, Beghi A, CarmignotoD, Milani M,etal. Auditory and academic performance of children with unilateral hearing loss. Scand Audiol Suppl. 1988;30:71-4.
76. Culbertson JL, Gilbert LE. Children with unilateral sensorineural hearing loss: cognitive, academic, and social development. Ear Hear. 1986;7(1):3 8-42.
77. Bess FH,Tharpe AM. Unilateral hearing impairment in children. Pediatrics. 1984;74(2): 206-16.
78. Bess F, Tharpe A. Case history data on unilaterally hearing-impaired children. Ear Hear. 1986; 7(1):14-9.
79. Blair J, Peterson M, Viehwed S. The effects of mild sensorineural hearing loss on academic performance of young school-age children. The Volta Review. 1985;87: 87-93.
80. Halliday LF, Bishop DV: Frequency discrimination and literacy skills in children with mild to moderate sensorineural hearing loss. J Speech Lang Hear Res. 2005; 48:1187-1203.
81. Hansson K, Sahlén B, Mäki-Torkko M. Can a "single hit" cause limitations in language development? A comparative study of Swedish children with hearing impairment and children with specific language impairment. Int J Lang Comm Disord. 2007;42(3): 307-323.
82. Teasdale TW, Sorensen, MH: Hearing loss in relation to educational attainment and cognitive abilities; A population study. Int J Audiology. 2007; 46:172-175.
83. Wake M, PoulakisZ: Slight and mild hearing loss in primary school children. J Paediatr Child Health. 2004;40:11-13.
84. U.S. Preventive Services Task Force. Recommendations and rationale: newborn hearing screening. Accessed January 3,2007 at:http://ww Orlando M, w.ahrq.gov/clinic/uspstf/uspsnbhr.htm
85. Yoshinaga-Itano C: Early intervention after universal newborn hearing screening: impact on outcomes. Ment Retard Dev Disabil Res Rev. 2003;9:252-266.
86. Kennedy C, McCann D, Campbell MJ, Kimm L, Thornton R. Universal newborn screening for permanent childhood hearing impairment: an 8-year follow-up of a controlled trial. Lancet.2005; 366 (9486):660 -662.
87. Helfand M,Thompson C.D, Davis R, McPhillips H, Homer J.C, Lieu L.T. Newborn Hearing ScreeningSystematic Evidence Review Number 5 AHRQ Publication No. 02-S001 October 2001
88. Nelson D.H, Bougatsos C, Nygren P. Universal Newborn Hearing Screening: Systematic Review to Update the 2001 US Preventive Services Task Force Recommendation Pediatrics Vol. 122 No. 1 July 2008, e266-e276
(doi:10.1542/peds.2007-1422)
89. White KR, Vohr BR, Maxon AB Behrens TR, McPherson MG, Mauk GW: Screening all newborns for hearing loss using transient evoked otoacoustic emissions. Int J Pediatr Otorhinolaryngol1994; 29:203-217.
90. Vohr BR, Carty LM, Moore PE, Letourneau K:The Rhode Island Hearing Asessment Program: experience with statewide hearing screening (1992-1996). J Pediatr. 1998;133:353- 357.
91. Nagapoornima P, Ramesh A, Srilakshm, Rao S, Patricia PL, Gore M, Dominic M, Swarnarekha: Universal Hearing Screening. Indian J Pediatr. 2007;74:545-9.
92. Léveque M, Schmidt P, Leroux B, Danvin JB, LangagneT, Labrousse M, Chays A: Universal newborn hearing screening: a 27- month experience in the French region of Champagne- Ardenne. Acta Paediatr. 2007;96:1150-4.
93. Flynn M, Austin N, Flynn TS, Ford R, and Buckland L: Universal Newborn Hearing Screening introduced to NICU infants in Canterbury Province, New Zealand. The New Zealand Medical Journal. 2004:117(1206).
94. Dalzell L, Orlando M, MacDonald M, Berg A, Bradley M, Cacace A, Campbell D, DeCristofaro Gravel J, J Greenberg E, Gross S, Pinheiro J, Regan J, Spivak L, Stevens F, Prieve B. The New York State universal newborn hearing screening demonstration project: ages of hearing loss identification, hearing aid fitting, and enrollment in early intervention. Ear Hear. 2000,21:118-130.
95. Vohr B: The Rhode Island Hearing Assessment Program. Rhode Island Medicine. 1995;78:11-13.
Magyar nyelven segédanyagok, tájékoztatók, a magyarországi UNHS adatai a fejlesztés alatt álló www.unhs.hu illetve www.hallasszures.hu címeken lesznek elérhetőek.
A szakmai irányelv érvényessége: 2010. szeptember 30.
Függelék
1. Az irányelvben használt evidencia szintek
A bizonyítékok hatékonyságának amerikai rangsora (az U.S. Preventive Services alapján) I. szint: Randomizált kontrollált vizsgálatok (RCT), szisztematikus referátumok
szint: Jól tervezett nem randomizált kontrollált vizsgálatok II-2 szint: Jól tervezett kohorsz vagy esettanulmányok (lehetőleg több centrumból, vagy kutató helyről) II-3 szint: Esetsorozatok. Nem kontrollált vizsgálatnál jeletkezett nagy horderejű eredmény is tartozhat ebbe a csoportba
III szint: Elismert szakértők klinikai vizsgálatokon alapuló véleménye. Objektív leírást adó tanulmányok, vagy jelentések.
A bizonyítékok hatékonyságának európai beosztása (The UK National Health Service alapján)
| A | I. szint (Randomizált kontrollált vizsgálatok metaanalízise, szisztematikus referátumok, Randomizált kontrollált vizsgálatok) határozott következtetéssel |
| B | és II.-2 szintű tanulmányok (Nem randomizált kontroll vizsgálatok, Kohort és esettanulmányok), vagy az I. tanulmányokból extrapolált bizonyítékok |
| C | II.-3 szintű tanulmány (Eset sorozat és esettanulmányok), vagy a és II.-2 szintű tanulmányból levont következtetés |
| D | III. szintű evidencia, nem meggyőző vagy következetlen tanulmányok (Szakértői vélemények) bármilyen szinten, vagy bármilyen olyan tanulmány, amelynek magas az elfogultsági rizikója |
2. Az evidencia szinteknél használt kifejezések definiciói
Bizonyítékok szintje: A bizonyíték szintjét az alkalmazott vizsgálati elrendezés típusa (rendszerezett irodalmi áttekintés, meta-analízis, randomizált kontrollált "kettős vak" vizsgálatok - RCT-k -, kohorsz vagy eset-kontroll vizsgálat, stb.) és a vizsgálat eredményeiből származó bizonyíték minősége határozza meg. A klinikai kérdés jellege határozza meg, hogy mely vizsgálati elrendezés képviseli a legkisebb torzító hatással rendelkező, legmagasabb szintű bizonyítékot (pl. egy terápiás eljárás hatásosságának megítélésére a legmagasabb szintű bizonyítékot jól kivitelezett RCT-k, vagy több RCT eredményét összefoglaló meta-analízis képviselik; ugyanakkor egy diagnosztikai eljárás klinikai hatékonyságának vizsgálatára prospektív kohorsz vizsgálatok szogálnak legjobb tudományos bizonyítékul). Randomizált kontrollált vizsgálat (randomized controlled trial RCT): olyan kísérleti vizsgálat, amelyben egy egészségügyi beavatkozás biztonságosságának és/vagy hatásosságának vizsgálata során véletlenszerűen két vagy több csoportba, a kísérleti és a kontroll csoportba sorolják a résztvevőket, és összehasonlítják a két csoportban elért eredményeket. A véletlenszerű soroláshoz számos módszert használhatnak, mint pl. számítógép által generált random számok. Azok a csoport-kiválasztási módszerek, melyek a naptári napokat, a betegek társadalombiztosítási számát, vagy a kórlap sorszámát használják, az úgy nevezett kvázi-randomizációk, nem annyira megbízhatóak, mint a számítógépes random számtáblák.
Szisztematikus (rendszerezett) irodalmi áttekintés ("systematic review"): azok a rendszerezett irodalmi összefoglalók, melyek előre meghatározott, igényes tudományos módszertannal dolgozzák fel az összes elérhető szakirodalmat, hogy elkerüljék az irodalmi összefoglalók ("review"-k) leggyakoribb hibáit (pl. a publikációs hibából adódó közlési elfogultságot - ld. fent). A módszeres irodalmazást követően a tudományos közleményeket előre meghatározott feltételek alapján minőségi elemzésnek vetik alá, és a megfelelő vizsgálatok eredményeit kvalitatív, vagy kvantitatív (meta-analízis) módszerrel összesítik. Ilyen rendszerezett irodalmi áttekintésektalálhatóka Cochrane Könyvtárban is. Meta - analízis: a rendszerezett irodalmi áttekintések során alkalmazott statisztikai módszer. Segítségével kvantitatívan összesítik a különböző tanulmányok végeredményét. A statisztikai összesítés során az egyes tanulmányok eltérő súllyal szerepelnek. A meta-analízis valójában a különböző vizsgálatok adatait és eredményeit statisztikailag is összesítő és értékelő szisztematikus irodalmi áttekintés (ld. alább)."Kettős vak" vizsgálat: kettős vak vizsgálatról akkor beszélünk, ha sem a vizsgálati személy (beteg) sem a vizsgáló (kezelő orvos) nem tudja, hogy milyen gyógyító-megelőző eljárást (esetleg placébót) kap a vizsgálati személy. A célja az un. "performance" és "detection bias" lehetőségének a minimalizálása.
Kohorsz vagy követéses vizsgálat: olyan ok-okozati összefüggést kereső (prospektív vagy retrospektív) vizsgálat, amely során egy bizonyos hatásnak (expozíciónak) kitett csoportot hasonlítanak össze egy expozíciónak ki nem tett csoporttal. A két csoportban összehasonlítják, hogy a követési idő során milyen gyakorisággal lépett fel betegség, majd ebből próbálnak következtetni az expozíció és a betegség közötti összefüggésre.
Eset-kontroll vizsgálat: egy olyan ok-okozati összefüggést kereső (retrospektív) vizsgálat, amely során egy már betegségben szenvedő csoportot ("eset") hasonlítanak össze egy jól összevethető referencia ("kontroll") csoporttal. Megvizsgálják, hogy a két csoport milyen mértékben volt kitéve egy bizonyos hatásnak (expozíciónak), és ebből következtetnek az expozíció és a betegség között fennálló kapcsolatra
Eset sorozat: kontrollcsoport nélküli megfigyeléses vizsgálat, ahol egy gyógyító-megelőző eljárás hatásosságát, mellékhatását, eredményét több eset összegyűjtésével állapítják meg. Hasznos lehet ritka betegségek okának vizsgálatára.
Szűrővizsgálat: rejtett, tünetet még nem okozó, korábban még nem diagnosztizált betegség valószínűsíthető felismerése gyorsan kivitelezhető tesztekkel, vizsgálatokkal és egyéb eljárásokkal. Vagyis ily módon az egészségesnek tűnő személyek közül kiválaszthatók a valószínűleg betegek. A szűrés nem a diagnózis, hanem a különválasztás eszköze, a pozitív vagy bizonytalan szűrési eredményű betegek további kivizsgálása szükséges.
3. Az irányelvben használt röviditések, fogalmak magyarázatai
| Rövidítések, fogalmak - Magyarázat | ||
| NICU - Neonatal Intensive Care Unit.- | - | Újszülött Intenzív Osztály |
| GyTH - Gyermekkori tartós halláscsökkenés | Míg a halláscsökkenéseket általánosan idegi (szenzorineurális), vezetéses (konduktív) és kevert csoportokba osztjuk, addig kisgyermekeknél ezeket összeolvasztva, csak a fennállás (min. 3 hónap) idejére koncentrálva is definiálhatjuk, hiszen az eredet a beszédfejlődés gátoltsága szempontjából közömbös. A terápia meghatározásához természetesen pontos diagnózis szükséges. (A magyar audiológiai szaknyelvben széleskörben még nem terjedt el.) | |
| UNHS - Universal newborn hearing screening, magyarítva is használható: univerzális neonatális hallásszűrés. | Az adott intézetben született összes újszülött (min. 96%) hallásszűrése objektív hallásvizsgáló módszerekkel a hazabocsátásig. (Néhány helyen - pl. Hollandia - a nagyszámú otthonszülés, illetve a rövid intézeti tartózkodás miatt "kiszálló szűrő szolgálat" működik -ilyen esetben az "intézetben" helyett régió, illetve a "hazabocsátásig" helyett 1 hónapos korig értendő.) | |
| JCIH - Joint Committee on Infant Hearing | "Közös bizottság az újszülöttek hallásáért" - tagszervezetei: Amerikai Audiológus Társaság, Amerikai Gyermekgyógyász Társaság, Amerikai Beszéd-Nyelv-Hallás Szövetség, Siket-oktatás Tanácsa, Állami Egészségügyi és Jóléti Ügynökség Beszéd és Hallás Programjainak Igazgatói | |
| Objektív hallásvizsgáló módszerek | A szervezet azon fiziológiai válaszait figyelik, melyek a hang hatására jöttek létre. Nem szükséges a páciens aktív visszajelzése, a készülék automatikusan mér, majd a legtöbb ki is értékel, ezzel kikapcsolva a vizsgáló szubjektívumát is. Használatuk gyors, egyszerű, alvásban is kivitelezhető, ezért igen alkalmas újszülöttek hallásvizsgálatára. (Pl.: OAE, BERA, ASSR, stb.) | |
| OAE (TEOAE, DPOAE) -otoacusticus emisszió | Otoakusztikus emisszió mérésénél egy olyan szondát helyezünk a fülbe, amelyben egy vagy két miniatűr hangszóró és egy mikrofon van beépítve. A belsőfülbejutó hang hatására, a Corti-szerv külső szőrsejtjei aktív, ritmikus összehúzódásokkal élesítik ki a tovahaladó hullámzás legnagyobb kitérésének csúcsát, lehetővé téve ezzel a cochlea nagyon finom frekvencia-specifikusságát, illetve mintegy 120 dB-es hangerősség átfogó képességét. A külső szőrsejtek ezen aktív "rárezgése" visszavezetődik a cohlea alapmembránja-belsőfül folyadéktere-hallócsontok-dobhártya rendszeren, és ez a rezgés a hallójáratba helyezett mikrofonnal detektálható, a hozzákapcsolt számítógéppel az egyéb zajokból kiátlagolható. Röviden: miközben a jól halló belsőfül "dolgozik", halk hangot bocsát ki, ez az otoakusztikus emisszió (OAE), halláscsökkenésnél ez nem mérhető. A szűrésben elterjedt típusai: tranziensen kiváltott OAE (TEOAE) és a disztorziós szorzat OAE (DPOAE). | |
| BERA vagy ABR (szűrőBERA v. AABR) - Brainstem Electric Response Audiometry | Az agytörzsi kiváltott potenciálok mérésekor szintén hangot juttatunk a fülbe, de a mért fiziológiai jelenség, a hallóideg elektromos potenciálváltozása, melyet a fejre helyezett elektródákkal vezetünk el, és szintén számítógéppel átlagolunk ki, itt az agy egyéb - a hangingerrel nem összefüggő - elektromos tevékenységei közül. Típusai közül a szűrésben az agytörzsi potenciálok automatizált vizsgálata (AABR) terjedt el. A diagnosztikai lépcsőben a klinikai formája (ABR v. BERA) használatos. A 2-3 kHz körüli hallástartományról ad választ. | |
| MLR - Middle Late Responses | - | A BERA kiegészítésére alkalmazzák, az 500 Hz körüli hallástartomány megbecsülésére. |
| blASSR - Auditory Steady State Responses | Az agytörzsi potenciálok vizsgálatának jelenleg legmodernebb, frekvencia specifikus formája, a magyar WHO lista még nem tartalmazza. A BERA és az MLR által együttesen szolgáltatott "2 pontos" audiogramnál részletesebb, pontosabb objektív hallásküszöb feltérképezésére ad lehetőséget. | |
| BAHA- bone anchored hearing aid | Csonthoz horgonyzott hallókészülék - ha a hangvezető rendszer (hallójárat-dobhártya-hallócsontok) nem alkalmas a hallókészülék hangjának bevezetésére, akkor csontvezetéses készülék szükséges, ennek modern formája, a rezonátornak a koponya csontba horgonyzása műtéttel | |
| Auditoros neuropátia /disszinkrónia | Az idegi halláscsökkenések azon csoportja, amikor jó külső szőrsejt funkció (jó OAE mérhető) mellett a BERA rossz eredményt mutat. Oka lehet belső szőrsejt-, hallóideg károsodás, de sokszor a még éretlen idegrendszer diszfunkciója. |
4. Az irodalmi evidenciák összefoglaló táblázata
| IRODALOM | EVIDENCIA SZINT |
| 4. Rezes Sz, O'Donoghue, Sziklai I. Az életkor szerepe a praelingualis süket gyermek cochlearis implantáció utáni hallás rehabilitációjában. Fül-orr-gégeggyógyászat 2003; 49 (4):207-207-215 | IA |
| 5. Watkin P, McCann D, Law C, Mullee M, Petrou S, Stevenson J, Worsfold S, Yuen H M, Kennedy C. ?Language Ability in Children With Permanent Hearing Impairment: The Influence of Early Management and Family Participation Pediatrics 2007; 120: e694-e701 | II-2, B |
| 6. Kennedy C. R, McCann D. C., Campbell M. J, Law C. M., Mullee M., Petrou S., Watkin P., Worsfold S., Yuen H. M., Stevenson J Language Ability after Early Detection of Permanent Childhood Hearing Impairment. N Engl J Med 2006;354:2131-2141. | II-2, B |
| 13. Yoshinaga-Itano C, Apuzzo ML. The development of deaf and hard of hearing children identified early through the high-risk registry. Am Ann Deaf 1998; 143(5):416-24. | II-2, B |
| 14. Yoshinaga-Itano C, Coulter D, Thomson V. The Colorado Newborn Hearing Screening Project: effects on speech and language development for children with hearing loss. J Perinatol 2000; 20 (8 Pt 2):S 132-7. | II-2, C; |
| 15. Yoshinaga-Itano C, Sedey AL, Coulter DK, Mehl AL. Language of early- and later-identified children with hearing loss. Pediatrics 1998; 102 (5):1161-71. | II-2, B |
| 16. Yoshinaga-Itano C, Apuzzo ML. Identification of hearing loss after age 18 months is not early enough. Am Ann Deaf 1998; 143 (5):380-7. | II-2, B |
| 17. Apuzzo M-rL, Yoshinaga-Itano C. Early identification of infants with significant hearing loss and the Minnesota child development inventory. Semin Hear 1995;16 (2):124-39. | II-2 B |
| 18. Moeller MP. Early intervention and language development in children who are deaf and hard of hearing. Pediatrics 2000; 106 (3): E 43. | II-2, B |
| 19. Calderon R, Naidu S. Further support of the benefits of early identification and intervention with children with hearing loss. Volta Review 2000; 100(5), 53-84. | II-2, B |
| 31. Leonard DR, Shen T, Howe HL, EglerT, eds. Trends in the prevalence of birth defects in Illinois and Chicago 1989 to 1997.Epidemiologic report series 99:4. Springfield, IL: Illinois Department of Public Health, 1999. | III, D |
| 32. Stierman L. Birth defects in California: 1983-1990. The California Birth Defects Monitoring Program, California Department of Health Services, 1994. | III, D |
| 33. White KR. The current status of EHDI programs in the United States. Ment Retard Dev Disabil Res Rev 2003; 9: 79-88. | III, D |
| 41. Mehl AL, Thomson V. Newborn hearing screening: the great omission. Pediatrics 1998; 101:1-6. | II-2, B |
| 43. WessexUniversal Neonatal Hearing Screening Trial Group. Controlled trial ofuniversal neonatal screening for early identification of permanent childhood hearing impairment. Lancet 1998; 352: 1957-64 | II-1,B |
| 47. Prieve BA, Stevens F. The New York state universal newborn hearing screening demonstration project: introduction and overview. Ear Hear 2000; 21:85-91. | II-2, C |
| 54. Engel J, Anteunis L,Volovocs A, HendriskJ, Marres E. Prevalance rates of otitis media with effusion from 0-2 years of age: healthy-born versus high-risk-born infants Int J of Pediatric Otolaryngology 1999; 47: 243-251. | II-3, C |
| 55. Zielhuis GA, Gerold H, Rach G, Van Denbroek P. The occurrence of otitis media with effusion in Dutch pre-school children Clinical Otolaryngology 1990; 15:2,147-153. | II-2, B |
| 56. Zielhuis GA, Rach GH, Bosch A, Broek P.The prevalence of otitis media with effusion: a critical review of the literature.Clin. Otolaryngol 1990; 15:283-288. | II-3, C |
| 58. Ruben RJ, Wallace IF, Gravel J. Long term communication deficiencies in children with otitis medis during their first years of life. Acta Oto-Laryngol 1997;117:206-207. | II-2, B |
| 63. Bess FH, Dodd-MurphyJ, Parker RA: Children with minimal sensorineural hearing loss: prevalence, educational performance, and functional status. EarHear. 1998;19(5): 339-53. | II-2, C |
| 74. Bess FH, Tharpe AM, Gibler AM. Auditory performance of children with unilateral sensorineural hearing loss. Ear Hear. 1986;7(1): 20-6. | II-2 B |
| 75. Bovo R, Martini A, Agnoletto M, Beghi A, Carmignoto D, Milani M, et al. Auditory and academic performance of children with unilateral hearing loss. Scand Audiol Suppl. 1988; 30:71-4. | II-2 B |
| 76. Culbertson JL, Gilbert LE. Children with unilateral sensorineural hearing loss: cognitive, academic, and social development. Ear Hear. 1986;7(1):3 8-42. | II-2 B |
| 77. Bess FH, Tharpe AM. Unilateral hearing impairment in children. Pediatrics. 1984;74(2): 206-16. | II-2 B |
| 78. Bess F, Tharpe A. Case history data on unilaterally hearing-impaired children. Ear Hear. 1986; 7(1):14-9. | II-3 C |
| 79. Blair J, Peterson M, Viehwed S. The effects of mild sensorineural hearing loss on academic performance of young school-age children. The Volta Review. 1985;87:87-93. | II-2 B |
| 80. Halliday LF, Bishop DV: Frequency discrimination and literacy skills in children with mild to moderate sensorineural hearing loss. J Speech Lang Hear Res. 2005; 48: 1187-1203. | II-1,B |
| 81. Hansson K, Sahlén B, Mäki-Torkko M. Can a "single hit" cause limitations in language development? A comparative study of Swedish children with hearing impairment and children with specific language impairment. Int J Lang Comm Disord. 2007;42(3): 307-323. | II-1 B |
| 82. Teasdale TW, Sorensen, MH: Hearing loss in relation to educational attainment and cognitive abilities; A population study. Int J Audiology. 2007; 46:172-175. | II-1,B |
| yphpar083. Wake M, Poulakis Z: Slight and mild hearing loss in primary school children. J Paediatr Child Health. 2004;40:11-13. | II-2 C |
| 86. Kennedy C, McCann D, Campbell MJ, Kimm L, Thornton R. Universal newborn screening for permanent childhood hearing impairment: an 8-year follow-up of a controlled trial. Lancet.2005; 366 (9486):660 -662 | II-1 B |
| 87. Helfand M, Thompson C.D, Davis R, McPhillips H, Homer J.C, Lieu L.T. Newborn Hearing ScreeningSystematic Evidence Review Number 5 AHRQ Publication No. 02-S001 October 2001 | IA |
| 88. Nelson D.H, Bougatsos C, Nygren P. Universal Newborn Hearing Screening: Systematic Review to Update the 2001 US Preventive Services Task Force Recommendation Pediatrics Vol. 122 No. 1 July 2008, e266-e276 (doi:10.1542/peds.2007-1422) | IA |
| 89. White KR, Vohr BR, Maxon AB Behrens TR, McPherson MG, MaukGW: Screening all newborns for hearing loss using transient evoked otoacoustic emissions. Int J Pediatr Otorhinolaryngol1994; 29:203-217. | II-3 C |
| 90. Vohr BR, Carty LM, Moore PE, Letourneau K: The Rhode Island Hearing Asessment Program: experience with statewide hearing screening (1992-1996). J Pediatr. 1998;133:353- 357. | II-2 B |
| 91. Nagapoornima P, Ramesh A, Srilakshm, Rao S, Patricia PL, Gore M, Dominic M, Swarnarekha: Universal Hearing Screening. Indian J Pediatr. 2007;74:545-9. | II-3 C |
| 92. Leveque M, Schmidt P, Leroux B, Danvin JB, Langagne T, Labrousse M, Chays A: Universal newborn hearing screening: a 27- month experience in the French region of Champagne- Ardenne. Acta Paediatr. 2007;96:1150-4. | II-2 B |
| 93 Flynn M, Austin N, Flynn TS, Ford R, and Buckland L: Universal Newborn Hearing Screening introduced to NICU infants in Canterbury Province, New Zealand. The New Zealand Medical Journal. 2004:117(1206). | II-3 C |
| 94. Dalzell L, Orlando M, MacDonald M, Berg A, Bradley M, Cacace A, Campbell D, DeCristofaro Gravel J, J Greenberg E, Gross S, Pinheiro J, Regan J, Spivak L, Stevens F, Prieve B. The New York State universal newborn hearing screening demonstration project: ages of hearing loss identification, hearing aid fitting, and enrollment in early intervention. Ear Hear. 2000,21:118-130. | II-2 B |
| 95. Vohr B: The Rhode Island Hearing Assessment Program. Rhode Island Medicine. 1995;78:11-13. | II-3 C |
5. UNHS kivitelezéséhez használatos eszközök és gyártóik jegyzéke
| Gyártó | Eszköz neve | Technológia | ||
| ABR | DPOAE | TEOAE | ||
| Grason-Stadler Inc (GSI) | GSI 70 | X | ||
| Audioscreener | X | X | X | |
| Intelligent Hearing Systems | Smart Screener | X | ||
| Smart DPOAE | X | X | ||
| SmartTrOAE | X | X | ||
| Interacoustics | OtoRead | X | X | |
| Madsen Electronics | Accuscreen | X | X | X |
| Maico | Ero-Scan | X | X | |
| BERAphon MB11 | X | |||
| Natus Medical Inc | ALGO 5 | X | ||
| ALGO 3i | X | |||
| Echo-Screen® | X | X | X | |
| ABaer® | X | X | X | |
| AuDX® Pro, AuDX® Pro II, AuDX® Pro Plus, Scout Sport | X | X | ||
| Otodynamics Ltd | Otoport Lite | X | ||
| Otoport Screener | X | |||
| Otoport DP+TE | X | X | ||
| Otoport Advance | X | X | ||
| Echoport ILO288 USB I | X | |||
| Echoport ILO288 USB II | X | X | ||
| Echoport ILO282 USB | X | X | ||
| SLE | SABRe | X | ||
| Starkey Laboratories Inc | DP-2000 | X | X | |
6. Szűrő audiométerek és gyártóik jegyzéke
| Gyártó | Eszköz neve |
| Entomed AB | SA 50 |
| SA 201 | |
| SA 202 (GSI 66) | |
| Grason-Stadler Inc (GSI) | GSI 18 |
| Intelligent Hearing Systems | Smart Audiometer |
| Interacoustics | AS216 |
| AS 608 | |
| Madsen Electronics | Micromate 304 |
| Maico | MA 27 |
| MA 39 | |
| Mediroll | SA 5 |
1. számú ábra A sensoroneuralis halláscsökkenés környezeti és genetikai okai (35)
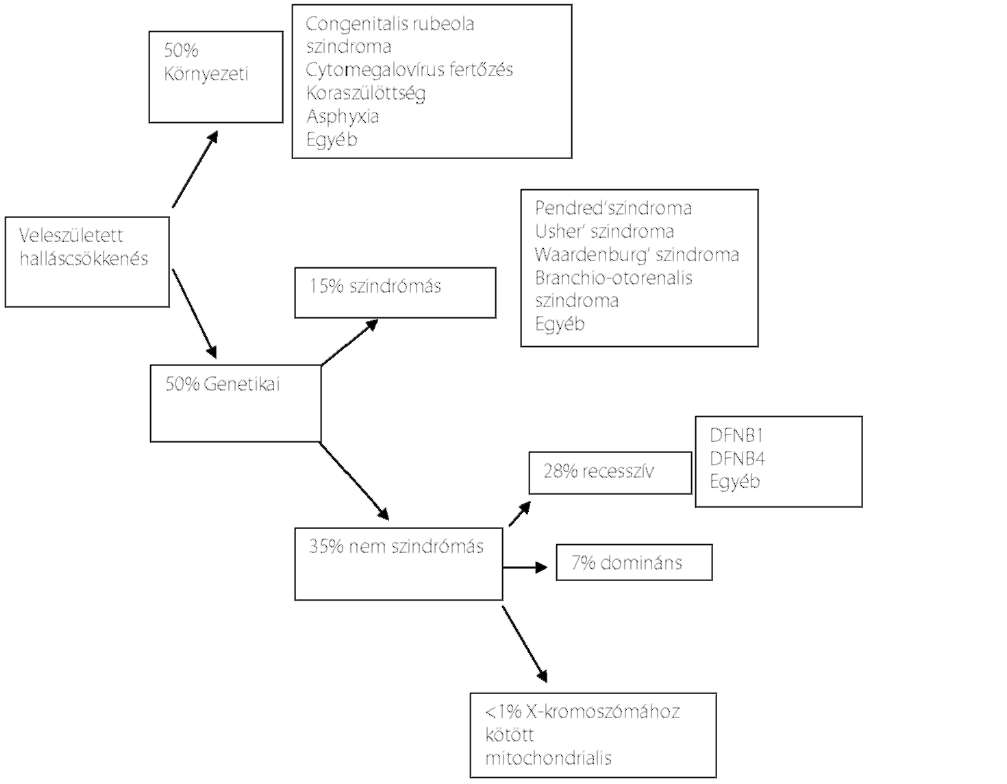
1. táblázat
| A gyermekkori halláscsökkenés rizikófaktorai* (újszülött kortól iskolakezdésig) | |
| I. Születéstől a 28. napig | |
| a) | Pozitív családi anamnézis gyermekkori tartós halláscsökkenéssel (GyTH) kapcsolatosan. |
| b) | GyTH-t okozó méhen belüli infekciók (pl. cytomegalovírus, herpes, rubeola, szifilisz és toxoplazmozis). |
| c) | Fül- és egyéb craniofaciális fejlődési rendellenességek. |
| d) | Transzfundálást igénylő hiperbilirubinémia. |
| e) | 1500 g-nál kisebb születési súly. |
| f) | Sensorineuralis halláscsökkenéssel járó postnatalis infekciók (pl. bakteriális meningitis). |
| g) | AlacsonyApgar értékek:0-3 5 perces és 0-6 10 perces. |
| h) | Respiratoricus distress szindróma (pl.: meconium aspiráció). |
| i) | Tartós (több mint 10 napig tartó) gépi lélegeztetés, pulmonáris hipertenzió, extrakorporeális membrán oxigenizációt igénylő állapotok. |
| j) | Ototoxicus gyógyszerelés (pl.:gentamicin, citosztatikum) több mint 5 napig, főleg kaccs-diureticummal kombinációban. |
| k) | Sensorineuralis vagykonduktív halláscsökkenéssel vagyEustach-kürt funkciózavarával társuló szindrómára utaló elváltozás vagy vizsgálati eredmény (pl.:Treacher-Collins szindróma, Down-kór, Waardenburg szindróma, stb.). |
| II. 29. naptól iskolakezdésig | |
| a) | Szülői vagy gondviselői gyanú a hallás, beszéd, a nyelv vagy a fejlődés késésével kapcsolatban. |
| b) | Az I. pontban felsorolt újszülöttkori rizikófaktorok bármelyike. |
| c) | Visszatérő vagyelhúzódóközépfülgyulladások (legalább 3 hónap). |
| d) | Az os temporale törésével járó fejsérülés. |
| e) | Sensorineuralis vagy konduktív halláscsökkenéssel járó gyermekkori fertőző betegségek (pl.: meningitis, mumpsz, kanyaró). |
| f) | Neurodegeneratív betegségek (pl.: Hunter-szindróma), sensorimotoros neuropátiák (pl.: Friedreich-ataxia és Charcot-Marie-Tooth szindróma). |
| g) | Progresszív halláscsökkenéssel járó szindrómák (pl.: neurofibromatózis, osteopetrózis és az Usher-szindróma) |
| Ezen indikátorok alapján fokozottan veszélyezettnek minősül az újszülött a progresszív vagy a késve-induló idegi és/vagyvezetéses halláscsökkenésekre. Ha a baba ezen rizikófaktorok bármelyikével rendelkezik,még ha "megfelelt" is az újszülöttkori szűrésen, akkor is audológiai kontrollja szükséges hathavonta 3 éves koráig. *JCIH 2000 Year Position Statement alapján, módosítva Weichobold és Cunningam (65) | |
2. számú táblázat (35)
Halláscsökkenést okozó kórokozók (terhesség és perinatalis időszak)
Veleszületett fertőzések Cytomegalovirus
Lymphocytás choriomeningitis virus Rubeola virus Toxoplasma gondii Treponema pallidum
Szerzett fertőzések
Borrelia burgdorferi Epstein-Barr virus Haemophilus influenzae Lassa virus Kanyaró virus Mumps virus Neisseria meningitidis Nem-polio enterovirusok Plasmodium falciparum Streptococcus pneumoniae Varicella zoster virus
3. számú táblázat.
A csecsemő és kisdedkori fülkürt működés zavarát, középfül gyulladásokat elősegitő tényezőket a 3. számú táblázat szemlélteti (67).
1) a fülkürt működését érintő craniofacialis anomáliák: szájpadhasadék, az arc középső részének, a koponya alap, az orr illetve a paranasalis sinusok deformitásai, Down kór, Apert szindróma, mucopoliszacharidosis
2) ismert, veleszületett immundeficienciával járó szindrómák pl: hypogammaglobulinaemia,
IgA hiány,
DiGeorge szindróma, HIV,
gyógyszer indukálta (citosztatikum, szteroid)
3) allergia
4) nasalis obstrukciót okozó betegségek: sinusitis,
adenoid hypertrophia, elhúzódó nasotrachealis intubáció, nasogastricus szonda behelyezés, orr és orrgarati tumorok,
5) egyéb okok: ciliáris dysfunkció, gastrooesophagealis reflux
Nyilatkozatok
Az ajánlás kialakítása során a szerzők külső támogatást, az elkészítésnél szponzori támogatást nem vettek igénybe, magukat függetlennek és elfogulatlannak tekintik.
A szakmai irányelvet elfogadta:
- Fül-Orr-Gégészeti Szakmai Kollégium
- Csecsemő és Gyermekgyógyászati Szakmai Kollégium
- Védőnői Szakmai Kollégium
A szakmai kollégiumok észrevételeit, módosítási javaslatait a szerzők figyelembe vették.
Az Egészségügyi Minisztérium
szakmai protokollja
Az állcsontok, a periosteum és a lágyrészek fogeredetű gennyes gyulladásainak kezeléséről
Készítette: a:Fog- és Szájbetegségek Szakmai Kollégiuma
I. Alapvető megfontolások
1. A protokoll alkalmazási / érvényességi területe
1.1. A protokoll témájának pontos meghatározása, a témaválasztás indoklása A fogeredetű gyulladások a leggyakoribb heveny kórképek közé tartoznak, ami miatt a betegek fogorvoshoz fordulnak. A protokoll a heveny fogeredetű gyulladás különféle formáival foglalkozik.
1.2. A protokoll célja: útmutatást nyújtani a heveny fogeredetű gyulladások diagnosztikájához, differenciál diagnosztikájához és kezeléséhez
1.3. A protokoll célcsoportja: az alapellátásban dolgozó fogorvosok, fogszakorvosok, háziorvosok, sürgősségi ellátó orvosok, valamint a szakellátásban dolgozó dento-alveolaris-, maxillofacialis-, szájsebész és fül-orr-gégész szakorvosok.
2. Definíciók
periodontitis apicalis acuta: a periapialis szövetek hevenygyulladása
pericoronitis acuta: az áttörésben lévő fogak koronája körül kialakult heveny gyulladás
cysta inflammata maxillae seu mandibulae: másodlagosan felülfertőződött állcsontciszta
subperiostealis infiltratum (periostitis (et ostitis) acuta serosa): a csont, a periosteum és a környező lágyrészek heveny gyulladása
submucosus abscessus (periostitis (et ostitis) acuta purulenta seu abscedens): a csont, a periosteum és a környező lágyrészek heveny gennyes gyulladása, mely a nyaki spatiumokba terjedhet osteomyelitis acuta: a csont és csontvelő heveny gyulladása phlegmone: a kötőszöveti rések lap szerint terjedő heveny gyulladása phlegmone colli: a nyak kötőszöveti réseiben lap szerint terjedő heveny gyulladás
angina Ludovici: mindkét oldali sublingualis és submandibularis régió kötőszöveti réseit érintő phlegmone phlegmone temporofacialis: az arc és halánték régió heveny gyulladása
phlegmone pterygocranialis: a koponyaalap irányába terjedő phlegmone, mely a sinus cavernosus thrombózisát, intracranialisan ascendáló heveny gyulladást okozhat
3. A betegség leírása
3.1. Oka dentalis eredetű bakterialis fertőzés, trauma, marginalis parodontitis, pericoronitis, megelőző szájsebészeti beavatkozás. Létrejötte leggyakrabban endodontális úton, caries és következményes megbetegedéseinek kialakulása útján történik. A kaszkád-szerű folyamat elemei: (caries, pulpitis, gangraena pulpae) acut v. chronicus periodontitis, ostitis, periostitis, osteomyelitis, phlegmone. Fő kockázati tényezők az elhanyagolt fogazati állapot, rossz szájhigiéné és általános szervezeti hajlamosító tényezők, hormonális és immunológiai háttér, immunszuppresszív vagy chemotherapiás kezelés, stb. [1]
3.2 Genetikai háttér: specifikus genetikai háttér nem ismert.
3.3 Incidencia / Prevalencia / Morbiditás Magyarországon: nincsenek elérhető adatok, de incidenciája várhatóan szorosan korrelál a cariesével.
3.4 Jellemző életkor és nem: nincs.
3.5. Panaszok/Tünetek/Álatlános jellemzők
3.5.1. Periodontitis apicalis acuta: a fog kopogtatásra érzékeny, a beteg "hosszabbnak" érzi az érintett fogat, az apexnek megfelelően a vestibulumban nyomási érzékenység lehet.
3.5.2. Pericoronitis acuta: az áttörésben részlegesen vagy teljesen visszamaradt fog (leggyakrabban bölcsességfog vagy szemfog) koronája körül a csontban és környező lágyrészben kialakuló gyulladás lokális ödémával, hyperaemiával, fájdalommal, izmokra terjedés miatt következményes szájnyitási korlátozottsággal
3.5.3. cysta inflammata maxillae seu mandibulae: a ciszta területének megfelelően lokális gyulladásos jelek, nagy kiterjedés esetén általános tünetek
3.5.4. Submucosus és subperiostealis infiltratio (periostitis (et ostitis) acuta serosa): a gyökércsúcs körüli csont, majd a periosteum és környező lágyrészek fájdalma, duzzanata, arcduzzanat, amely kemény tapintatú, fluktuáció nem észlelhető. A vestibulum kitöltött, a fog mozgatható lehet. Szájnyitási korlátozottság, nyelési, légzési nehezítettség lehet. Általános tünetek: subfebrilitás, láz, lymphadenomegalia, leukocytosis, balratolt vérkép, gyorsult süllyedés, CRP.
3.5.5. Submucosus és subperiostealis abscessus (periostitis (et ostitis) acuta purulenta seu abscedens): a gyökércsúcs körüli csont, majd a periosteum és környező lágyrészek fájdalma, duzzanata, arcduzzanat, mely kemény tapintatú, fluktuációt mutat. A mélyebb regiok, spatiumok felé terjedő gyulladás esetén a fluktuáció nem mindig tapintható! A vestibulum kitöltött, a fog mozgatható lehet. Szájnyitási korlátozottság, nyelési, légzési nehezítettség lehet. Intraoralisan vagy extraoralisan sipoly jelenhet meg. Általános tünetek: subfebrilitás, láz, lymphadenomegalia, leukocytosis, balratolt vérkép, gyorsult süllyedés, CRP, exsiccatio lehet.
3.5.6. osteomyelitis acuta: a betegséget okozó fog és a szomszédos, majd távolabbi fogak is mozgathatók, mérsékelt arcduzzanat, kifejezett lymphadenomegalia jellemző. Magas láz, elesettség, septikus lázmenet jelentkezik, balra tolt vérkép, gyorsult süllyedés, CRP is van. Rtg. jelek időben elmaradva követik a tüneteket (rötngen látencia)! Az odontogén osteomyelitis jóval gyakoribb a mandibulában mint a maxillában. Az állcsont osteomyelitisek kb. 10%-a nem odontogén: főként trauma, haematogén szórás következményeként (főleg gyermekkorban más regiok gyulladásaiból, tonsillitis, morbilli, scarlatina után), osteoradionecrosis, biszfoszfonát kezelést követően kialakuló csontnecrosis. [1,2,3]
3.5.7. phlegmone colli: a nyak duzzadt, lángvörös, tapintásra fájdalmas. Bár nagy kiterjedésű, beolvadásra nem hajlamos, de kisebb fluktuáló területek több helyen is tapinthatók lehetnek. A beteg elesett, lázas, lymphadenomegalia, leukocytosis, balratolt vérkép, gyorsult süllyedés, CRP jellemző, nyelési, légzési nehezítettség lehet. A gyulladás a nyaki kötőszövetes spatiumokba terjed. Speciális forma a Ludwig-féle angina, ami mindkét oldali sublingualis és submandibularis régió phlegmonéjét jelent. A nyaki phlegmonét korábban megkezdett antibiotikus kezelés "maszkírozhatja" jellegzetes tüneteit elfedheti, de a lap szerinti terjedés ekkor is jellemző marad. Phlegmone kialakulhat az arcon is (phlegmone temporofacialis): az érintett oldali arcfélen hasonló tünetek jelentkeznek, mint a nyaki phlegmonéban. A gyulladás az orbitát is érintheti. Előfordul ascendáló gyulladás (phlegmone pterygocranialis), ami a sinus cavernosus thrombosisát, intracranialis komplikációt okozhat.
3.6. Érintett szervrendszerek: a fej-nyak régió valamennyi szövete-szerve érintett lehet. Következményesen a mediastinum és az intracranialis tér is érintett lehet.
3.7. Gyakori társbetegség: diabetesben, immunsupprimált betegeknél súlyosabb formákban fordul elő. 4. Ellátási folyamat leírása, ellátási algoritmus
Az ellátás az alapellátó fogorvosnál vagy szájsebészeti, dentoalveolaris sebészeti szakrendelésen történjen. Hospitalizációra, maxillofacialis sebészeti osztályon történő kezelésre van szükség nyelési, légzési nehezítettséget okozó folyamat, phlegmone esetében mindig, illetve ha a beteg állapota vagy kísérőbetegsége azt igényli (pl. intravénás gyógyszeradagolás, folyadékpótlás szükséges). [1] Kiterjedt gyulladások (periostitis, osteomyelitis) ellátása dento-alveoláris szakrendelésen illetve maxillo-faciális sebészeti osztályon történjen.
II. Diagnosztikai eljárások
1. Anamnézis
1.1 Általános anamnézis - családi, szociális, magatartási, krónikus betegségek ( különös tekintettel endocrin, immunologiai, keringési betegségekre) terhesség, gyógyszerszedés, folyadékfogyasztás, akut gyulladásos jelek, láz, stb.
1.2 Fogászati-szá sebészeti anamnézis - A tünetek kezdete, megelőző kezelés, fá dalom ellege, változásai (ha a pus áttöri a periosteumot a fájdalom csökken).
2. Fizikális vizsgálatok
A fej-nyak régió részletes fizikális vizsgálata (tapintás is), a szájüreg és garat vizsgálata. Különösen fontos a garat vizsgálata a parapharyngealis illetve retropharyngealis terjedés lehetősége miatt. Keresni kell a folyamat lehetséges okát.
3. Kötelező diagnosztikai vizsgálatok
3.1. Laboratóriumi vizsgálatok: Rutin laboratóriumi vizsgálat (kvalitatív-kvantitatív vérkép, CRP vagy süllyedés, se Na, K, Ca, Cl, glükóz, vesefunkció, májfunkciós értékek, prothrombin) végzése hospitalizált betegnél feltétlenül szükséges, súlyosabb esetben ambulánsan is javasolt.
3.2. Képalkotó vizsgálatok
3.2.1. Röntgen diagnosztika: periodontitis esetén elegendő lehet a periapicalis felvétel. Ennél kiterjedtebb folyamat esetén kötelező az orthopantomogramm készítése. Szükség lehet más kiegészítő felvételekre is (ráharapásos felvétel, PA mandibula, PA sinus felvétel). CT vizsgálat is indikált lehet (parapharyngealis illetve retropharyngealis érintettség kizárására, mediastinum, orbita érintettségének megítélésére, intracranialis progressio esetén stb.)
3.2.2. Ultrahang vizsgálat: folyadékgyülem, beolvadás megítélésére javasolt, esetleg UH vezérelt punctio azabscessus lokalizálására.
3.3. Egyéb vizsgálatok: periostitisben javasolt, phlegmone, osteomyelitis esetén kötelező a mikrobiológiai diagnosztika.
4. Kiegészítő diagnosztikai vizsgálatok, differenciál diagnosztika: szükséges lehet elkülöníteni tumoroktól, specifikus, esetleg gombás eredetű gyulladástól, felszínes, bőr eredetű cellulitistől, fül-orr-gégészeti eredetű gyulladásoktól, illetve a terjedés irányának megfelelő további vizsgálatok lehetnekszükségesek. Ennek érdekében további, konzíliumi vizsgálatokra lehet szükség (fül-orr-gégészet, bőrgyógyászat, szemészet, mellkassebészet, idegsebészet, stb.).
5. Diagnosztikai algoritmus
III. Terápia (Kezelés)
Gyógyszeres kezelés: Az acut periodontitis általában nem igényel gyógyszeres kezelést. Pericoronitisben a helyi mechanikus kezelés (tasak megnyitás, gézcsík behelyezés) mellett helyi gyógyszeres kezelés alkalmazható (Betadine-os átmosás, dezinficiensek, Chlumsky oldat, különféle gyári készítmények). Periostitisben akkor indokolt az empirikus antibiotikus kezelés, ha a beteg általános állapota rossz, vagy a gyulladás progrediál. Javasolt rezisztencia profil alapján célzott antibakteriális kemoterápia alkalmazása. Acut osteomyelitis esetén az empirikusan megkezdett kezelést antibiogramm alapján kell módosítani. Lehetőleg a csontban nagy koncentrációban jelen lévő, hosszú távon tolerálható szert kell választani és 6-8 hétig adni. Phlegmone esetén intravénás empirikus kezelést kell kezdeni és a rezisztencia profil alapján módosítani.
Az első választandó szerek a penicillinek, de célszerű ezeket béta-laktamáz gátlóval kombinálni [4,5,6 Evidencia la, ajánlás A]. Az anaerobok ellen főként a metronidazol (Gramm-negatív) és a clindamycin adása javasolt [7,8,9 Evidencia la, ajánlás A], az utóbbi származék penicillin érzékenység esetén is alkalmazhatók. Penicillin-allergiában középsúlyos infekcióknál makrolid származékok alkalmazása is szóba jöhet. A clindamycin osteomyelitis empirikus kezelésére is javasolt. [7,8]
Fontos a szupportív terápia: láz- és fájdalomcsillapítás, bőséges folyadékpótlás.
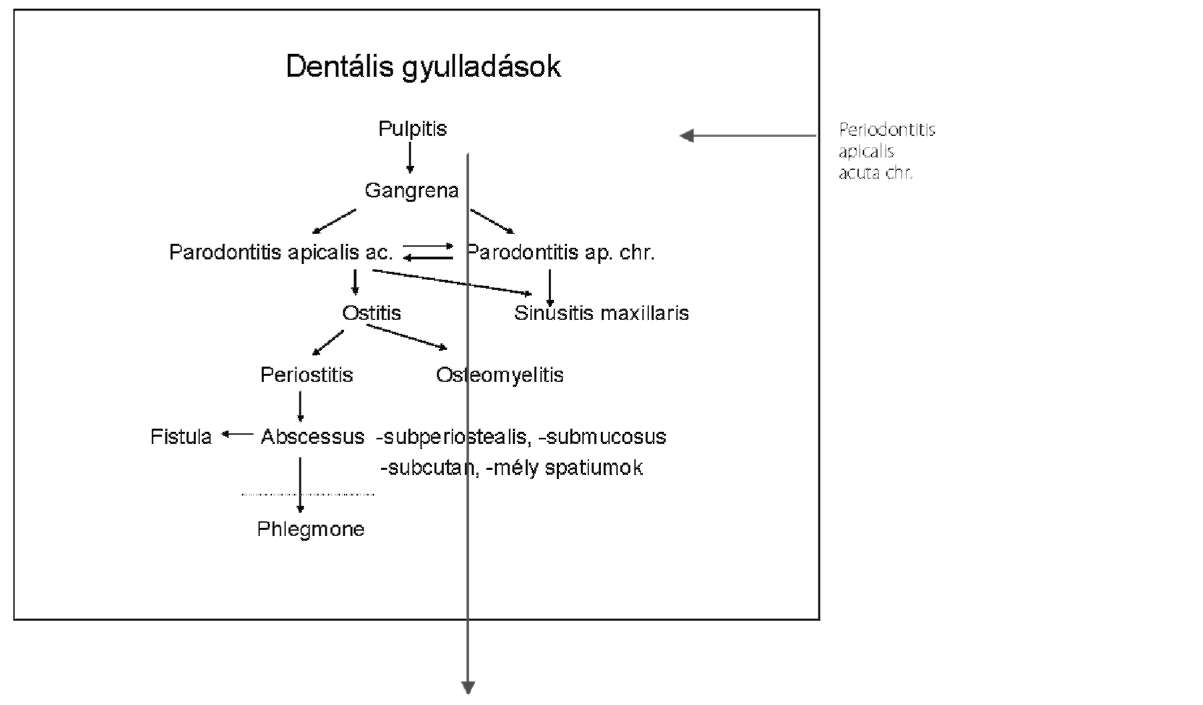
III/2 Sebészeti jellegű ellátás:
Az acut periodontitis ellátása endodonciai vagy esetleg extractio.
Pericoronitis esetén circumcisio végezhető hagyományos sebészi úton, elektromos, vagy laser eszközzel. Inflammált cysta esetén incisio, cystostomia végzendő.
Serosus stádiumban elsősorban az érintett területre helyezett párakötés, esetleg infralámpás kezelés, naponkénti kontroll javasolt antibiotikus kezeléssel kiegészítve (ld. III/1.). Abscessus esetén incisio elvégzése ill. drainage biztosítása javasolt esetleges antibiotikus kezeléssel kiegészítve. Fontos a gyulladást okozó fog mielőbbi ellátása (endodoncia vagy extractio).
Lehetőleg intraoralisan,a fluctuáló duzzanat punctum maximumán kell az incisiot végezni helyi érzéstelenítésben, és a subperiostealis teret is explorálni kell, retentio megelőzése céljából. Ha szükséges, extraoralis incisiot maxillofacialis sebészeti jártassággal rendelkező személy végezzen! Helyi vagy szükség szerint általános érzéstelenítésben bőrmetszés után tompán preparálva szélesen fel kell tárni a tályogüreget, kiüríteni és drainálni. Intraoralisan a drainage többnyire gézcsíkkal, extraoralisan gumicsíkkal vagy gumicsővel történik. Fontos a naponkénti vagy naponként többszöri kötéscsere, revízió. Az okozó fogat mielőbb el kell látni (endodoncia vagy extractio). [1,10] Acut osteomyelitisben elsődleges az okozó fog eltávolítása, szükség esetén a szomszédos, mozgatható fogak eltávolítása is. Egyebekben gyógyszeresen kezelendő betegség. Az elégtelen vagy későn kezdett kezelés subacut, chronicus osteomyelitis kialakulásához vezethet.
Phlegmonéban többnyire általános érzéstelenítésben több helyen, amennyiben szükséges extraorálisan széles feltárást, és drainage-t végzünk. Fontos a nyaki spatiumok feltárása. Naponkénti vagy naponként többszöri revízió, dezinficiens átöblítések, kötéscserék szükségesek. [1]
III/3 Egyéb beavatkozások: fokozott szájhigiéné, napi min. 2,5 l folyadékbevitel, diabetesesek esetén a serum glucose szint ellenőrzése, szükség esetén konzílium, belgyógyászati ellátás, hospitalizáció.
III/4 Egyéb terápia: Hasonló tünetekkel jelentkeznek a specifikus gyulladások is. Kezelésük is hasonló, de specifikus antibiotikus kezelést igényelnek.
IV. Rehabilitáció
Az aktív kezelés után az incisios seb gondozása szükséges a seb teljes záródásáig. Szükséges az acut gyulladás gyógyulása után a beteg teljes fogászati rehabilitációja, az esetleg felfedezett más kísérőbetegség kezelése. Megfelelő gyógyulási idő után hegkorrekcióra kerülhet sor.
V. Gondozás
1. Primer és szekunder prevenció: primer prevenció az általános fogászati prevenció. Szekunder prevenció: a kialakult carieses laesiok mielőbbi lege artis ellátása.
2. Prognózis: a betegségcsoport általában jó prognózisú. Legveszélyesebb a phlegmone, itt lethalis kimenetel is előfordul. Fokozottan veszélyeztetettek az immunsuppreszált betegek és a kezeletlen diabetesesek. A prognózist rontja az adekvát sebészi kezelés elmaradása. A hospitalizált esetek bennfekvési ideje átlag 5 nap, de a teljes kezelés 10-14 nap is lehet. [10]
Lehetséges szövődmények: progressio a mediastinum vagy az intracranialis tér felé, sepsis, távoli, "metastaticus" tályogok létrejötte.
Az ellátás megfelelőségének indikátora - Eredmények
Az ellátás akkor megfelelő, ha a heveny gyulladás annak összes tünetével együtt megszűnt, krónikus gyulladás jelei nem észlelhetők és a gyulladás okát is megszüntették.
Az eredmény indikátorai: a beteg láztalan, panaszmentes, az incisios seb váladékozása megszűnik, az záródott, retentiora utaló jel nincs, a gyulladásos tünetek regrediáltak.
A protokoll bevezetésének feltételei
1. Tárgyi feltételek
A minimumfeltételeknek megfelelő, működési engedéllyel rendelkező fogorvosi rendelő, szájsebészeti szakrendelő, maxillofacialis sebészeti fekvőbeteg osztály
2. Személyi feltételek
Fogorvos, fogszakorvos, szájsebész, dentoalveolaris sebész, maxillofacialis sebész szakorvos
3. Szakmai/képzési feltételek
Graduális és posztgraduális képzés, folyamatos továbbképzés különösen az antibiotikus szerek alkalmazása tekintetében.
4. Egyéb feltételek
- megfelelő betegirányítás az alapellátásból a szakellátás felé
- betegtájékoztató kiadványok terjesztése
- oktatáshoz, továbbképzéshez társuló terjesztés
- a minőségirányítási rendszer megköveteli a protokoll használatát
- gyógyszerészek továbbképzése a fájdalomcsillapítóért hozzájuk fordulók felvilágosításáról
VI. Irodalomjegyzék
1. Irodalom
1) Szabó Gy. (szerk.): Szájsebészet, maxillofacialis sebészet. Semmelweis Kiadó, Budapest, 2004.
2) Weitzman R, Sauter N, Eriksen EF,Tarassoff PG, Lacerna LV, Dias R, Altmeyer A, Csermak-Renner K, McGrath L, Lantwicki L, Hohneker JA.: Critical review: Updated recommendations for the prevention, diagnosis, and treatment of osteonecrosis of the jaw in cancer patients-May 2006. Crit Rev Oncol Hematol. 2007 Feb 28
3) Krueger CD, West PM, Sargent M, Lodolce AE, Pickard AS. Bisphosphonate-induced osteonecrosis of the jaw. Ann Pharmacother. 2007 Feb;41(2):276-84.
4) Kuriyama, T. Nakagawa, K. Karasawa, T. Saiki, Y. Yamamoto, E.: Past administration of beta-lactam antibiotics and increase in the emergence of beta-lactamase-producing bacteria in patients with orofacial odontogenic infections. Oral Surgery Oral Medicine Oral Pathology Oral Radiology & Endodontics. 89(2):186-92,2000 Feb.
5) Eckert AW. Hohne C. Schubert J.: Erregerspektrum und Resistenzsituation bei rein anaeroben odontogenen Infektionen. Mund-, Kiefer- und Gesichtschirurgie. 4(3):153-8,2000 May
6) Eick S. Pfister W. Korn-Stemme S. Magdefessel-Schmutzer U.: Erreger- und Resistenzspektrum bei intraoralen Infektionen des Kiefer-Gesichts-Bereichs unter besonderer Berucksichtigung der anaeroben Keimflora. Mund Kiefer Gesichtschir. 4(4):234-9,2000 Jul.
7) Mangundjaja S, Hardjawinata K.: Clindamycin alone compared with Clindamycin plus ibuprofen for odontogenic infections. Current Therapeutic Research Clinical and Experimental. 57(12):913-926,1996.
8) Flynn TR, Shanti RM, Levi MH, Adamo AK, Kraut RA, Trieger N.: Severe odontogenic infections, part 1: prospective report. J Oral Maxillofac Surg. 64(7):1093-103, 2006.
9) Flynn TR, Shanti RM, Hayes C.: Severe odontogenic infections, part 2: prospective outcomes study. J Oral Maxillofac Surg. 2006 Jul;64(7):1104-13.
10) Flynn, T R.: The swollen face. Severe odontogenic infections. Emerg Med Clin North Am. 18(3):481-519,2000 Aug.
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. A protokollfejlesztés módszerei
Az irodalomkeresés és kiválasztás módszerei
Elektronikus adatbázisok (Ovid, Embase, Medline) Irodalomkutatás elsősorban 2000-2006 között megjelent szakmai könyvek, cikkek, különös tekintettel a randomizált, kontrollált vizsgálatok, rendszerezett áttekintés angol publikációkra.
A felhasznált nemzetközi irányelvek adaptálási módszerei
Fogeredetű gyulladás témakörben adaptálható nemzetközi irányelvet nem találtunk. Érintett társszakmákkal való véleményezés és konszenzus
Egyeztetés javasolt a fül-orr-gégészeti és szemészeti, valamint a sürgősségi ellátás szakmai szervezeteivel. A bizonyíték és ajánlási szintek meghatározása, magyarázata A bizonyítékok szintjei:
Az Egészségügyi, Szociális és Családügyi Minisztérium szakmai irányelve a bizonyítékokon alapuló irányelvek fejlesztéséhez. Egészségügyi Közlöny 2004, 3, 753. 5. sz. táblázat.
2. Az ajánlások alkalmazását támogató segédanyagok, betegtájékoztatók - Betegtájékoztató a fogeredetű gyulladásokról
3. A protokollfejlesztést támogató szervezetek, szponzorok
Magyar Fogorvosok Egyesülete. Magyar Arc-, Állcsont-, Szájsebészeti Társaság. Szponzori támogatás nem volt.
BETEGTÁJÉKOZTATÓ
A fogeredetű gyulladások leggyakrabban elhalt fogak, foggyökerek körül alakulhatnak ki. Megelőzhetők rendszeres fogászati ellenőrzéssel, kezeléssel.
A kezeletlen fogeredetű gyulladás tovaterjedhet a mellüreg vagy az agykoponya irányába is, és így életet veszélyeztető következményekkel járhat, ezért fontos korai felismerése és kezelése.
Ha Ön fogain, állcsontjain, nyakán fájdalmat érez, vagy duzzanatot, esetleg nyelési vagy légzési nehezítettséget tapasztal, forduljon mielőbb fogorvoshoz. Fogeredetű gyulladás esetén a fogorvos röntgenfelvételt, felvételeket készíttet. Bizonyos esetekben más kiegészítő vizsgálatra is sor kerülhet (ultrahang, bakteriológiai mintavétel, vérvétel,
CT, stb.)
A fogeredetű gyulladások kezelése általában fogászati vagy sebészeti jellegű, szükség esetén gyógyszeres kezelést is igényelhet. Ha azonban az orvos gyógyszert rendel igen fontos annak pontos szedése! Az orvos által javasolt meleg borogatás, párakötés hatásos módszer. Szerepelhet a kezelésben gyökérkezelés, fogeltávolítás, tályogmegnyitás, ami történhet szájon belülről, vagy ha szükséges a bőr felől is, az arc vagy a nyak területén. A beavatkozásokat általában helyi érzéstelenítésben, ritkán altatásban végzik. Nagy kiterjedésű gyulladás esetén szükség lehet kórházi bennfekvésre, infúziós kezelésre is. Mind az ambuláns, mind pedig a kórházi kezelést követő időszakban mindenképpen be kell tartani az orvos által előírt visszarendelési időket, mert csak így előzhető meg a gyulladás kiújulása vagy idült betegséggé válása.
Különösen fontos, hogy állapotromlás esetén, vagy ha nyelése, légzése nehezítetté válna azonnal forduljon orvoshoz. Mint minden gyulladásos állapotban, itt is fontos a lázcsillapítás és a bőséges, napi 2-3 literes folyadékfogyasztás.
Az Egészségügyi Minisztérium
szakmai protokollja
A foglalkozási asthmáról
(1. módosított változat)
Készítette: a Foglalkozás-orvostani Szakmai Kollégium
I. Alapvető megfontolások
1. Bevezetés
A foglalkozási asthma azextrinsic asthma bronchialenakazt az alcsoportját képezi, melyeta munkahelyen felhasznált, előállított, illetve ott rendszeresen előforduló anyagok belégzése vált ki. E betegség a 27/1996. (VIII.28.) NM rendelet 2. számú mellékletében felsorolt bejelentendő foglalkozási betegség.
Kóroki tényezőként számos szerves és szervetlen por, gőz, gáz, aeroszol szerepelhet, amelyek vagy önmagukban rendelkeznek antigén sajátosságokkal, vagy hapténként fehérjéhez kötődve képeznek antigént. Már több mint 200 munkahelyi anyag asthmát okozó hatása bizonyított, s e szám állandóan növekszik. Ezzel egyidejűleg emelkedik a foglalkozási asthmás esetek száma, nemzetközi felmérések a felnőtt asthmások 3-20%-át véleményezik foglalkozási eredetűnek.
2. Diagnózis
A foglalkozási asthma diagnózisának alapvető kritériuma annak igazolása, hogy a munkahelyen jelenlevő anyagok
szerepet játszanaka bronchospazmus kiváltásában.
A betegvizsgálat menete a szokásos sorrendben történik (1. melléklet).
3. Alapkritériumok
A diagnózis első és legfontosabb része a gondosan, részletesen felvett és szakszerűen értékelt anamnézis. Minthogy a foglalkozási asthmáért munkahelyi anyag a felelős, döntő a munkaanamnézis pontos felvétele. Foglalkozási asthmában az esetek nagytöbbségében az asthmás roham a munkahelyen, munkavégzéskor, az allergén belégzését követően jelentkezik, az antigén jellegétől, s feltehetőleg az expozíció nagyságától is függően hetekig, hónapokig, gyakran hosszú évekig tartó tünetmentes szenzibilizálódás után. A szenzibilizálódás jelei közül a conjunctivitis és/vagy a rhinitis jelentkezése a dyspnoe kialakulását gyakran megelőzi. Az első időszakban az állapot spontán reverzibilis, a dolgozó munkája végeztével, hétvégeken, szabadsága alatt panasz- és tünetmentessé válik. A bronchospazmus azonban ebben az időszakban is kiváltható, mégpedig az allergén lényegesen kisebb mennyiségével, mint amilyen a szenzibilizációt létrehozta. Az expozíció folytatásával rosszabbodás léphet fel, súlyos esetekben irreverzibilis bronchiális obstrukció alakulhat ki.
Az allergénexpozíció és a panaszok, tünetek, időbeni összefüggésekor figyelemmel kell lenni arra, hogy az asthmás reakció lezajlása három típust követhet:
a. A "korai" vagy "azonnali" reakció esetén a bronchospazmus az expozíció után rövid idővel bekövetkezik, majd spontán oldódik.
b. "Késői" reakció esetén a bronchospazmus csak az expozíciót követően 4-8 órával lép fel, majd spontán oldódik. E típusnál tehát az asthmás roham látszólag a munkavégzéstől függetlenül léphet fel, mivel nem szükségszerűen a munkahelyen, hanem esetleg a munkavégzést követően, otthon jelentkezik.
c. A "kettős-reakció" lényegében egy korai és késői komponensből tevődik össze, azaz az expoziciót követően azonnal fellép egy spontán oldódó bronchospazmus, melyet 4-8 óra múlva újabb expozíció nélkül egy második követ.
II. Diagnózis
4. Vizsgálatok
4.1. A nyugalmi légzésfunkciós vizsgálatok segítségével elsősorban az obstruktív ventillációs zavar fennállását kell megállapítani.
4.2. A specifikus provokációs vizsgálat a tisztított antigén inhaláltatásával veszélyes, ezért nem javasolt.
4.3. Az esetek többségében a foglalkozási asthma megállapításához az u.n. munkahelyi feltételeket imitáló inhalatív provokációs vizsgálat elvégzése ajánlott. Ellenőrzött laboratóriumi körülmények között kell reprodukálni a munkahelyi tevékenységet. A provokáció előtt és azt követően legalább 8 órán keresztül kell regisztrálni azobstrukció detektálására kiválasztott légzésfunkciós paramétert (légúti áramlási ellenállást vagy FEV1-et, illetőleg ha egyik sem megvalósítható, a PEF-et). A vizsgálat akkor pozitív, ha a légúti áramlási ellenállás legalább 100%-kal emelkedik és meghaladja a 0,6 kPa/l/sec értéket, valamint mindez nem a légzési középállás (FRC) csökkenéséből adódik, illetve ha a FEV1 legalább 20%-kal csökken és a provokáció után mért értékek kóros tartományba esnek. (Amennyiben csak a PEF vizsgálatára van lehetőség, a 35%-ot meghaladó csökkenést tekintjük kórjelzőnek.)
5. Kiegészítő vizsgálatok
5.1. A nem specifikus hyperreaktivitás jellemző tünete az asthma bronchialénak. Fiziológiás mediátoranyagok, mint a hisztamin, az acetilkolin kisebb dózisban okoznak bronchospazmust asthmásokon, mint egészségeseken. A hyperreaktivitás nemcsak asthmásokra jellemző, hanem pl. krónikus bronchitisben, sőt néhány héten át izolált felső légúti infekció után is kimutatható. A vizsgálat a foglalkozási asztma diagnosztizálásában valamint a prognózis megítélésében is segítséget nyújt. A körültekintően végzett vizsgálat ellenére is számolni kell a gyors orvosi beavatkozást szükségessé tevő bronchospazmus felléptével, ezért az European Respiratory Society ajánlásainak megfelelelően, e vizsgálatokra csak jól felszerelt, kellőképpen felkészült szakintézetben kerülhet sor.
5.2. A bőrpróbák (Prick teszt, intracutan teszt) a kérdéses antigénnel szembeni ellenanyag termelés, illetve az atópiás alkat kimutatásával értékes információt adnak, de az adott antigén kóroki szerepét éppúgy nem bizonyítják, mint ahogy a negatív bőrpróba sem feltétlenül zárja ki azt. A foglalkozási allergének többségéből nem áll rendelkezésre tisztított antigén, ez korlátozza a vizsgálat e területen való alkalmazhatóságát.
5.3. Az in vitro vizsgálatok közül a munkahelyi allergénre specifikus IgE szint emelkedése a gyulladás allergiás pathomechanizmusára utal. Valószínűsíti az allergiás eredetet az expozíció során kialakuló eosinophylia, még inkább e sejtek megjelenése, felszaporodása a köpetben, orrváladékban.
5.4. A foglalkozási asthmát a csúcsáramlás (PEF) profilnakaz egyes munkafolyamatokkal való összefüggései alapján is lehet diagnosztizálni. A módszer azonban elsősorban a rehabilitáció és terápia eredményességének nyomon követésére javasolt.
5.5. A fizikális vizsgálat: foglalkozási asthma gyanúját veti fel, ha a munkavégzés során kialakuló nehézlégzést a bronchiális obstrukció jellegzetes tünetei - sípolás, búgás, megnyúlt kilégzés - kísérik.
5.6. A rhinológia vizsgálat a rhinitis allergica diagnózisának alátámasztására valamint egyéb gyulladásos megbetegedések kizárására javasolt.
Ha a bronchiális obstrukció nem teszi lehetővé az inhalaciós provokációs vizsgálatot, a foglalkozási betegség fennállásáról a rendelkezésre álló tapasztalatok, a jellegzetes anamnézis és az egyéb leletek alapján egyénileg kell dönteni.
6. Prognózis
A prognózist elsősorban az határozza meg, hogy a betegséget melyik stádiumban diagnosztizálják, mikor kerül sor az expozíció megszüntetésére. Korai diagnózis esetén, amikor a bronchiális obstrukció még spontán reverzibilis, az expozíció megszüntetésével többnyire megszűnnek az asthmás rohamok. Ha az expozíció megszüntetésére csak akkor kerül sor, amikor már a nem specifikus hyperreaktivitás igen kifejezett, csökkennek a teljes gyógyulás esélyei, s tartós, esetleg végleges munkaképesség csökkenés következhet be.
III. Terápia
7. Terápia
A beteg kiemelése az allergén expozícióból
Az allergén expozícióból való kiemelés javítja az asztmás tüneteket, és ezzel együtt a légzésfunkciós paramétereket. Korai kiemelés a gyógyulás esélyeit növeli. Az egyéni védőeszközök használata szintén csökkenti a légzési tünetek kialakulásának kockázatát. Gyógyszeres kezelés
A foglalkozási asztma kezelésére ugyanazok az antiasthmaticumok használandók, mint a nem foglalkozási asztmásoknál.
8. Bejelentési kötelezettség
A többször módosított 27/1996. (VIII. 28.) NM rendelet értelmében a foglalkozási asthma és rhinitis, valamint az extrinsic allergiás alveolitis bejelentendő foglalkozási megbetegedés. A bejelentést a diagnózist felállító orvosnak az erre rendszeresített nyomtatványon kell megtennie, az OMMF munkáltató székhelye szerinti illetékes intézetnek. Az Országos Munkahigiénés és Foglalkozás-egészségügyi Intézet (továbbiakban: OMFI) kivizsgálja az esetet, a kivizsgáláson jelen van a munkáltató képviselője, a munkavállaló és a foglalkozás-egészségügyi orvos is.
Tisztázatlan esetek kivizsgálását az OMFI Tüdőgyógyászati Szakrendelése végzi.
IV. Rehabilitáció
V. Gondozás
VI. Irodalomjegyzék
A szakmai protokoll érvényessége: 2010. szeptember 30.
Foglalkozási asthma kivizsgálási menete
1. Anamnézis - munkaanamnézis
2. Fizikális vizsgálat
3. Nyugalmi légzésfunkciós vizsgálat (minimum FVC, FEV1 meghatározás, lehetőség szerint áramlás-térfogat görbe felvétele és testpletizmográfiás mérés)
4. Bőrpróba (Prick teszt) általános inhalatív környezeti allergénekkel,- munkahelyi allergénekkel
5. Mellkas és orrmelléküreg rtg.
6. Fül-orr-gégészeti status
7. Laboratóriumi vizsgálatok: We, teljes vérkép, orrváladék kenet, esetleg allergén specifikus IgE
8. Bronchiális obstrukció esetén farmakodinámiás teszt
Csak Intézetben végezhető vizsgálatok:
9. Nem specifikus bronchiális hyperreaktivitás vizsgálata 10. Specifikus provokáció légzésfunkciós kontrollal
A European Respiratory Society ajánlásainak megfelelően végezve (Medicina Thoracalis XLVII. évfolyam 1994. Supplementum: Standardizált légzésfunkciós mérések.)
Provokációs tesztek ellenjavallatai
- légúti obstrukció (FEVi mint a kell érték 70 %-a, vagy 0,5 kPa/l/s vagy azt meghaladó légúti áramlási ellenállás)
- 3 hónapon belül lezajlott myocardialis infarctus
- 3 hónapon belül lezajlott agyi vascularis történés
- arteria aneurysma
A vizsgálat elvégzése megfontolandó:
- 2 héten belül lezajlott felső légúti hûléses megbetegedés
- asthma exacerbatio
- graviditas
- gyógyszeres kezelést igénylő epilepszia Az alkalmazott rövidítések magyarázata
| IgE | Immun globulin E |
| PEF | Csúcsáramlás |
| FEVi | Forszírozott kilégzési térfogat 1 s alatt |
| FRC | Funkcionális reziduális kapacitás |
| FVC | Forszírozott vitálkapacitás |
| We | Vérsejtsüllyedés |
Az Egészségügyi Minisztérium
szakmai protokollja
A gyermekkori lágyéksérv kezeléséről
(1. módosított változat)
Készítette: a Gyermeksebész Szakmai Kollégium
I. Alapvető megfontolások
1.1 A protokoll alkalmazási / érvényességi területe
Minden olyan fekvőbeteg intézet, ahol legalább I. szintű (gyermeksebészeti alapellátás) gyermeksebészeti tevékenység folyik Kívánatos, hogy minden 6 évesnél fiatalabb beteg legalább ilyen szintű háttér mellett kerüljön kivizsgálásra és műtétre.
1.2 A protokoll adott intézetben való bevezetésének feltétele
A gyermeksebészeti alapellátás működési feltételeinek (személyi és tárgyi) megvalósulása. Ezek hiányában 6 évnél fiatalabb beteg megfelelő szakintézménybe irányítandó.
1.3 Definíció
Lágyéksérv: a canalis inguinalison (lágyékcsatorna) a nyitott processus vaginalis peritonein (sérvtömlő) keresztül hasüregi szerv (bél, cseplesz, petefészek, méhkürt) előesésea lágyéki régióba, illetve fiúknál a herezacskóba, lányoknál a nagyajkakba.
Ha az előesett sérvtartalom nem kerül vissza a hasüregbe, szűk sérvkapu esetén sérvkizáródás jöhet létre, amely a kiszorult sérvtartalom leszorítása miatt bélelzáródáshoz illetve keringési zavar talaján nekrózishoz (sőt, a here vérellátási zavara miatt herekárosodáshoz is) vezethet, ezért sürgős sebészi beavatkozást (repozíció illetve szükség esetén műtét) igényel.
1.3.1 Klinikai felosztás
A sérvtömlő lefutását tekintve a gyermekkori lágyéksérvek (ritka kivételtől eltekintve) ferde (indirekt) sérvek. A sérvtömlő hosszát tekintve:
- komplett, scrotalis sérvről beszélünk, ha a scrotumba terjedő tömlő a here savós burkával (tunica vaginalis) közlekedik.
- inkomplett, inguinalis sérvről beszélünk a scrotumba nem terjedő és a hereburokkal nem közlekedő sérv esetén. A komplett és inkomplett sérvre szinonimaként használatos veleszületett és szerzett jelzők félreérthetők, mert a gyermekkori lágyéksérvekfejlődéstanilag 99%-ban veleszületettek, függetlenül azokscrotalis vagy inguinalis voltától.
1.3.2 Kockázati tényezők
- Koraszülöttség, intraventricularis vérzés
- Fokozott intra-abdominalis nyomással járó kórállapotok (cystás fibrosis, idült obstruktiv légúti betegségek, ascites, ventriculo-peritonealis shunt, tárolási betegségek)
- Kötőszöveti rendellenességek (Ehlers-Danlos syndroma, Hunter-Hurlersyndroma, mucopolysaccharidosis)
- Ikrek esetében a sérvek előfordulása gyakoribb
- Hasfali defektusok (pl. extrophia vesicae urinariae) rekonstrukcióját követően
1.3.3 Etiológia
A veleszületett lágyéksérvek genetikai eredete nem bizonyitott, de a familiáris halmozódás ismert tény. A processus vaginalis valamint a here leszállása szorosan összefügg a sérvek kialakulásával. Az intrauterin életben magasan retroperitonealisan fejlődő here a 4-5. hónapban kezdődő leszállása során a 8-9. hónapban áthalad a canalis inguinalison, és a hashártyát zsákszerű járatként (processus vaginalis) maga előtt türemitve süllyed a scrotumba. A járat here és hasüreg közötti része részben vagy teljesen elzáródik. Az obliteráció elmaradásával hernia ill. hydrocele változatos formái alakulnak ki, gyakran egymással kombinálódva. Ha az elzáródás a processus vaginalis teljes hosszában elmarad, scrotális sérv ill. kommunikáló vizsérv észlelhető fiúkban. Leányokban az utóbbi megfelelője a Nuck-cysta (hydrocele muliebris).
1.4 Panaszok/Tünetek
Vezető tünet a hol megjelenő, hol eltűnő, általában fájdalmatlan elődomborodás a lágyéki régióban ill. herezacskóban, leányokban a nagyajkak mentén. Az elődomborodás megjelenését hasprés, köhögés vagy sirás provokálhatja. A sérvtartalom többnyire könnyen reponálható, máskor nyugalomban, fektetésre (alváskor) spontán eltűnik.
A lágyéksérvekfő veszélye a kizáródás. Az összes sérvkizáródás 30 %-a az első három élethónapban és több mint fele az 1. életévben alakul ki. A csecsemőkori ileusok 71 %-áért a lágyéksérv kizáródása a felelős. A koraszülöttekben és intrauterin sorvadt újszülöttekben a bélelhalás veszélye 2-4-szer nagyobb, mint érett újszülöttekben. Csecsemőkorban mára rövid ideig tartó sérvkizáródás is a here vaszkuláris károsodásához vezethet, ez később a here atrophiáját okozhatja ("vanishing testis"). A sérvkizáródás klinikai tünetei életkoronként változnak. Kis csecsemőkben nyugtalanság, hányás, haspuffadás a korai jelek. A csecsemőkori esetek több mint 1/3-ában a sérvkizáródás lehet a lágyéksérv első klinikai jele.
Nagyobb gyermekek lágyéktáji vagy alhasi fájdalomra panaszkodnak, a feszesen domborodó sérvnek megfelelően. 6-8 órás sérvkizáródás esetén már a bélelhalás klinikai jelei dominálhatnak: ismétlődő hányások, véres széklet, hasi izomvédekezés. Ovariális kizáródást ritkán, szinte kizárólag csecsemőkorban látunk, ezek az esetek tünetszegényebbek.
1.5 A betegség gyakorisága
A gyermekkor leggyakoribb, sebészi kezelést igénylő állapota a congenitalis lágyéksérv, amellyel túlnyomórészt csecsemő és kisdedkorban találkozunk. Előfordulási gyakorisága a 14 év alatti gyermekpopulációban 1 - 3 %. Ezen
belül
- érett újszülötteknél:4-5%
- koraszülötteknél:5-7%
- fiúknál 8-9-szer gyakoribb, mint lányoknál
- a sérvek 60%-a jobboldali, 30%-a baloldali, 10% kétoldali (újszülöttkorban 30-40 % kétoldali!)
II. Diagnózis
A korai diagnózison alapuló kezelés alapvető fontosságú a szövődmények megelőzésében.
1.6 Diagnosztikus algoritmusok
- Anamnézis
- Fizikális vizsgálat
- Képalkotó vizsgálatok (UH, natív hasi röntgenfelvétel)
- Laboratóriumi vizsgálatok
- Egyéb diagnosztikus vizsgálatok
1.6.1 Anamnézis
Lásd panaszok, tünetek pontban.
1.6.2 Fizikális vizsgálat
A kórelőzmény adatai, a klinikai kép, valamint az esetek többségében észlelhető lágyéktáji (scrotális) elődomborodás, terime alapján a sérv ill. a hydrocele diagnózis felállítható. Ezek elkülönítése azért fontos, mert míg a fennálló lágyéksérv mindig sebészi kezelést igényel, addig újszülött-, és csecsemőkori vízsérvek esetén várakozás célszerű, tekintettel a jó eséllyel bekövetkező regresszióra. Egyszerű, de jó módszer a pupillalámpával történő átvilágítás: a hydrocele átvilágítható, a sérvtartalom nem.
Fizikális vizsgálatkor nem mindig észleljük a sérvet, de tömegesebb funiculus, a canalis inguinalisba vezetett ujjunk végén hasprésre (sírásra) "ütődés" gyakran észlelhető. Kis lágyéksérvek, különösen csecsemőkorban akár hosszú időre is "eltűnhetnek", azonban rendszerint előbb-utóbb újból megjelennek.
Újszülött-, csecsemőkori nyugtalanság, sírás, hányás, bukás esetén az inguinalis régiók (külső sérvkapu) mindig megvizsgálandók, mert kis lágyéksérvek - különösen jólfejlett vagy túltáplált babákon -könnyen elnézhetők.
1.6.3 Képalkotó vizsgálatok
Mivel a diagnózis rendszerint egyszerű fizikális vizsgálattal felállítható, végzésük nem kötelező. Differenciáldiagnosztikai nehézség vagy szövődmény esetén azonban segíthetnek a megítélésben.
1.6.3.1 Ultrahang vizsgálat Indokolt:
- Kizáródás gyanúja esetén a sérvtartalom megítélésére
- Sérv illetve hydrocele elkülönítésére
- Retineált here torsiojának elkülönítésére
1.6.3.2 Natív hasi rtg felvétel Indokolt:
- Sérvkizáródást kísérő ileus gyanújánál
- Kizárt sérv visszahelyezése után jelentkező, perforációra utaló tünetek esetén
1.6.4 Laboratóriumi vizsgálatok
- A diagnózis felállításában szerepük nincs.
- Szövődményes esetben (kizáródás, peritonitis, ileus) vagy egyéb kísérő betegség esetén az ezekhez kapcsolódó laboratóriumi vizsgálatok (hidratáció, só-, vízháztartás, vérveszteség, gyulladásos paraméterek) szükségesek, az aktuális állapottól illetve az anamnézistől függően.
- 6 hónapos kor alatt vérkép és az alvadási paraméterek (prothrombin, APTI) vizsgálata javasolt még egyébként egészségesnek ismert csecsemőknél is
1.6.5 Egyéb diagnosztikus vizsgálatok
Csak egyéb társuló alapbetegség ill. rendellenességek esetén szükségesek a műtéti kockázat ill. a speciális teendők megítéléséhez.
1.7 Differenciáldiagnosztika
Elkülönítés szempontjából az alábbi kórképek jönnek szóba:
- Lágyéki nyirokcsomó ill. annak gyulladása.
- Hydrocele testis ill. funiculi
- Retentio testis, testis retractilis
- Here (esetleg rejtett) torsioja
- Hernia femoralis
III. Terápia
A kezelés célja a sérv megszüntetése, lehetőleg a sérvkizáródás kialakulása előtt. Amennyiben a lágyéksérv diagnózisát felállítottuk és a sérv könnyen reponálható (háziorvos, gyermekgyógyász, sebész-, vagy gyermeksebész szakorvos által) a beteg választott időben olyan fekvőbeteg intézetbe utalandó, ahol a sebészi kezelés lehetősége biztosított. A műtétet tanácsos lehetőség szerint rövid időn belül elvégezni a kizáródás veszélye miatt. Sérvkizáródás esetén a beteg azonnal intézetbe utalandó.
1.8 Megfelelő egészségügyi ellátás szintje
Minden olyan fekvőbeteg intézet, ahol legalább I. szintű (gyermeksebészeti alapellátás) gyermeksebészeti tevékenység folyik. Ezen belül nem szövődményes lágyéksérv műtéti kezelése - az egynapos sebészeti ellátás általános feltételeinek teljesülése esetén - egynapos ellátásként is végezhető (3,4).
1.9 Indikáció
Minden lágyéki ill. scrotális sérv sebészi kezelést igényel. (1 éves kor felett a nagyságát változtató (hasüreggel közlekedő) hydrocele azonos megítélés alá esik)
- Elektív (tervezhető) műtét indikációja:
- Diagnosztizált sérv, de kizáródás nem áll fenn (a tömlőben lévő ovarium panaszmentesség esetén is relatív sürgősséget élvez - néhány napon belüli műtét)
- Kizáródott sérv manuális repozícióját követően, ha sem bélelzáródásra,sem bélkárosodásra utaló jelek nincsenek, a műtét 24- 48 órán belül végzendő.
- Baloldali sérv esetén kislányoknál ajánlható az ellenoldal együlésben történő explorációja is
- Sürgős műtéti indikáció:
- kizárt sérv sikertelen repositiója
- irreponábilis sérv akut hasi tünetekkel
- bélelzáródás vagy bélkárosodás tünetei esetén.
1.10 Általános intézkedések
Betegazonosítás, betegfelvétel, beleegyező nyilatkozatok beszerzése, aneszteziológiai konzílium (5,6,8).
1.11 Speciális ápolási teendők
Életkornak megfelelő szakápolás, testsúly- és testhőmérséklet mérés, vérvétel, vénás kapcsolat, kísérő betegségek terápiás beállítása.
1.12 Előkészítés és kiegészítő kezelés
1.12.1 Nem gyógyszeres kezelés
- Elektív műtét esetén: szájon át bevitel felfüggesztése 4 órával a műtét előtt. Az általános higiénés előkészítésen túlmenő speciális teendők egészséges gyermeknél nem szükségesek.
- Kizáródás esetén - szemben a felnőttkori kizáródással - manuális repozíció sikeresen megkísérelhető az alábbi feltételek megléte esetén:
- friss kizáródás lokális izgalmi jelenségek nélkül
- akut hasi tünetek nincsenek
- aneszteziológiai háttér biztosított
- gyakorlott gyermeksebész
- sebészeti osztályon történő megfigyelés azonnali műtéti lehetőséggel
- Amennyiben a repozíciós kísérlet kontraindikált, eredménytelen vagy utána akut hasi tünetek mutatkoznak: gyomorszonda levezetés és előkészítés sürgős műtéti beavatkozásra.
1.12.2 Gyógyszeres kezelés
- Szövődménymentes esetben, egyébként egészséges gyermeknél nem szükséges
- Kockázati tényezőt jelentő alapbetegség esetén annak kezelése ill. beállítása
- Sürgős műtéti indikáció esetén:
- infúziós terápia, elektrolit és sav-bázis állapot rendezése
- antibiotikus profilaxis/terápia előrehaladott kizáródás, perforáció, peritonitis esetén
1.13 Sebészeti (műtéti) kezelés
1.13.1 Terápiás cél
A terápiás cél minden esetben a sérvkizáródás lehetőségének (vagy magának a kizáródásnak) a megszüntetése.
- Elektív sérvműtét esetén elegendő a sérvtömlő felszámolása, esetenként a sérvkapu szűkítése.
- Sürgős műtét (sérvkizáródás) esetén a kizáródás megszüntetése, a sérvtartalom feltárása és életképességének megítélése, az esetleges szövődmények elhárítása, végül a sérvtömlő felszámolása, esetenként a sérvkapu szűkítése (a részleteket illetően az akut hasi kórképek ellátási szabályaira utalunk).
1.13.2 Műtéti érzéstelenítés
Gyermekkorban általános anaesthesia ajánlott, mely helyi vagy vezetéses (caudalis vagy spinalis) érzéstelenítéssel egészíthető ki (5,8).
1.13.3 Műtét
1.13.3.1 Feltárás megválasztása
- inguinalis redő- (ritkábban ferde) metszés: elektívsérvműtét esetén
- hernio-laparotomia: szövődményes kizáródás esetén
1.13.3.2 Műtét főbb szakaszai (2,6,11,13):
- bőrmetszés után a Scarpa-fascia behasítása
- a lágyékcsatorna teljes megnyitása 10 éves kor alatt általában szükségtelen, 2 éves kor felett a m.obliqus ext. fascia külső sérvkapuból történő 1 cm-es felhasítása rendszerint elegendő a belső sérvkapu magasságában történő sérvtömlő záráshoz.
- a funiculus spermaticus (lig. rotundum) kiemelése a külső sérvkapuból
- a funiculus spermaticus (ill. lig. rotundum) képleteinek kíméletes leválasztása a sérvtömlőről
- az esetleges sérvtartalom repozíciója a tömlő megnyitásával (opcionális) vagy anélkül
- a tömlő magas csonkolása aláöltést követően a peritonealis átmenetben
- a disztális tömlőrész rezekciója nem szükséges minden esetben.
- tágabb vagy felhasított sérvkapu esetén 1-2 szűkítő ültést helyezünk a sérvkapuba, vagy esetleg a csonkot a m.obliq.int-hoz "V" öltéssel felfüggesztve, rögzítjük azt, egyúttal a sérvkaput is szűkítjük.
- kizárt sérv műtéte esetén a várható következményekre tekintettel ajánlatos a here esetleges hypoxiás károsodásának véleményezése és dokumentálása
- újszülöttkorban testicularis retentióval társuló sérv műtétekora funiculus kíméletes mobilizálása és a testis scrotalis fixációja szükséges
- gondos vérzéscsillapítás, here scrotális helyzetének megítélése után réteges hasfalzárás.
- részletes műtéti leírás fentiek rögzítésével. Amennyiben a here a műtét során látótérbe került, célszerű nyilatkozni a here-mellékhere állapotáról és viszonyáról, tekintettel az esetleges fúziós zavarra, valamint a herezacskóba történt visszahelyezéséről.
- a gyermekkori laparoszkópos sérvműtét jelentősége és létjogosultsága (beleértve az ellenoldali nyitott sérvtömlő diagnosztikus értékelését is) az irodalomban vitatott, ezért ezen eljárást csak 6 éves kor felett tartjuk mérlegelésre érdemesnek (1,12,13)
1.14 Posztoperativ teendők
1.14.1 Posztoperativ megfigyelés
Elektív műtét esetén: teljes ébredésig megfigyelés, szükség szerinti fájdalomcsillapítás, óvatos itatás (általános posztoperatív megfigyelés). Zavartalan 4-8 órás szak után, ha az otthoni ápolás (és az egy napos sebészeti ellátás) feltételei adottak a beteg otthonába bocsátható.
Sürgős (sérvkizáródás miatt végzett) műtét esetén a beteg felügyelete az akut hasi esetek posztoperatív ellátási szabályait követi.
1.14.2 Diéta
- Elektív műtétet követő zavartalan közvetlen posztoperatív szak (ébredés) esetén: 1-2 óra múlva teáztatás, majd folyadékfelvétel szájon át. Panaszmentesség esetén (legkorábban 4-6 óra múlva) normál étrend.
- Sürgős műtét - kizáródás ill. annak szövődményei (ileus, bélelhalás) esetén, - az akut hasi műtétek utáni elvek szerint.
IV. Rehabilitáció - V. Gondozás
2 Rehabilitáció ill. gondozás
Szövődménymentes esetben rehabilitáció ill. rendszeres műtét utáni gondozás nem szükséges.
2.1 Ellenőrzés a műtét után
- Zavartalan posztoperatív szak és elsődleges sebgyógyulás esetén a beteg 7-10 nap múlva gyakorlatilag panaszmentes. Egyéntől függően3-4héttel a műtét után a teljes fizikai terhelés is megengedett.
- Herekárosodás lehetősége (több órás kizáródás, nehéz műtéti szituáció) esetén fél-egy éves távlatban érdemes az érintett oldali herét ellenőrizni.
2.2 Megelőzés
- lágyéksérv kialakulását megelőzni nem lehet, bár hajlamosító tényezők (lásd korábban leírtak) elősegítik annak kifejlődését ill. progresszióját.
- sérv diagnózisa esetén a kizáródás megelőzésére lehetőség szerint korai műtéti kezelés indokolt
3 Prognózis, kockázat és szövődmények
3.1 Prognózis, a kezelés várható időtartama
- a betegség prognózisa adekvát kezelés mellett jó, szövődménymentes esetekben teljes gyógyulás várható
- szövődménymentes esetben a sebészi gyógyulás 2 hétre tehető, a beteg 4-6 hét után sportolhat
- a beavatkozás egynapos sebészet keretében is végezhető
3.2 Kockázatok és szövődmények
Minden sebészeti beavatkozásnak (és narkózisnak) lehetnek szövődményei. Általában a műtéti kockázatnak az eredménytelenséget illetve az olyan szövődmények valószínűségét nevezzük, amelyek a szakmai szabályok betartása mellett is előfordulhatnak, bekövetkezésük előre nem látható és teljes biztonsággal nem védhető ki. Értelemszerűen ezért a sebészt (orvost ) nem terheli felelősség, ezt a (minimális) kockázatot betegnek (szülőnek) kell vállalni, amikor orvosi tájékoztatás után beleegyezik a műtétbe. Ilyen kockázati tényezők: a szokatlan anatómiai helyzet, más társuló betegség vagy kóros állapot, a szervezet szokatlan, előre nem látható reakciója a műtét során felhasznált anyagokra ill. magára a műtéti beavatkozásra, nem sterilitási hibából fakadó ún. endogén fertőzés, megfelelő tanúsítvány ellenére előforduló anyaghiba. Mindezek a mindennapi gyakorlatban vérzés, utóvérzés, véletlen sérülés, varratkilökődés, sebgennyedés vagy egyéb sebgyógyulási zavar, kóros hegesedés formájában jelentkezhetnek, de ezek statisztikai gyakorisága kicsi, veszélye messze kisebb, mint a műtét elmaradásának (a sérv kizáródásának) a veszélye. Ezen általános kockázati tényezők mellett elektíve végzett sérvműtéteknél a következő szövődmények léphetnek fel (9,10,11,13):
- másodlagos here retrakció: az ondózsinórt érintő hegesedés rövidülés miatt kiemelheti a herét a herezacskóból
- hereatrophia : hegesedés ill. a herét tápláló erek sérülése esetén
- sérvkiújulás (recidiva ): 5-10 %
- magasabb sérvkiújulási kockázatot jelentenek az 1.3.2 alatt felsorolt állapotok
3.3 Szövődmények kezelése
Korai posztoperativ szövődmények
- utóvérzés: rendszerint nem igényel kezelést. Ritkán műtéti haematoma evakuáció és vérzéscsillapítás, esetleg drainage is szükséges lehet
- sérvtömlőcsonk kinyílás: reoperáció szükséges.
- sebgennyedés: feltárás,drainage. Késői posztoperativ szövődmények:
- secunder testis retrakció: orchidopexia (l. rejtett here)
- here atrophia : pubertás után az afunkcionális here eltávolítása, here protézis implantáció
- sérv recidiva: reoperáció
3.4 Gyakori társbetegségek
- fokozott intraabdominalis nyomással járó betegségek, idült székrekedés, ascites, ventriculo-peritonealis shunt
- kötőszöveti gyengeség, mucopolysaccharidosis
4 Minőségbiztosítás
4.1 Az ellátás megfelelőségének indikátorai
(az EüK 2003.V. 19- számában megjelent indikátorok alapján
- halálozás adott dg-ra
- kórházi visszavétel aránya 6 héten belül azonos diagnózissal
- átlagos ápolási idő adott dg-ra
- egynapos sebészeti ellátásból többnapos ellátásba került betegek aránya
- kórházi sebfertőzések aránya
- reoperációk száma
4.2 Dokumentáció, bizonylat
- Ambuláns nyilvántartás, kórlap, lázlap, laboratóriumi leletek,(eseteleges) konzíliumi vélemények, műtéti beleegyező nyilatkozat, műtéti leírás, zárójelentés.
- Elszámolási Nyilatkozat (utóbbi kettő átvételekor szülői aláírásával)
4.3 Érintett társszakmákkal való konszenzus
- Gyermekgyógyász Szakmai Kollégium
- Sebész Szakmai Kollégium
VI. Irodalomjegyzék
1. Bende J. (szerk): Minimálisan invaziv sebészet. Medicina, Budapest, 2005
2. Donellan W.L. ed: Abdominal Surgery of Infancy and Childhood Hardwood Academic Pub. 1996
3. Gaál Cs.(szerk.): Ambuláns és egynapos sebészet. Medicina Könyvkiadó, 2008
4. Grosfeld JL, and al.: Pediatric Surgery. Mosby (Elsever), Philadelphia, 2006
5. Hirsch T., Tekulics P., Újhelyi E.: Gyermekaneszteziológia és gyermekintenziv-terápia. White Golden Book Budapest 2003
6. Keith W. Ashcraft, G. W. Holcomb III, J.Patrick Murphy: Pediatric Surgery.Elsevier Inc. 2005
7. Maródi L: Gyermekgyógyászat. Medicina Könyvkiadó RT Budapest, 2002
8. Oláh É.(szerk.): Gyermekgyógyászati kézikönyv. Medicina Könyvkiadó RT. Budapest 2004
9. O'Neil JA Jr at al.: Principles of Pediatric Surgery. Mosby, St. Louis. Missouri 2004
10. Pintér A.: Gyermeksebészeti vezérfonal Medicina 1996
11. Puri P, Höllwarth, M: Pediatric Surgery, Springer Verlag, Heidelberg 2006
12. Schier F: Laparoscopy in children. Springer Verlag, Heidelberg, 2002
13. Spitz L and Coran AG: Operative Pediatric Surgery. Hodder Arnold Publishers Ltd. London 2006 A szakmai protokoll érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai protokollja
A varicella kezeléséről és megelőzéséről
(1. módosított változat)
Készítette: az Infektológiai Szakmai Kollégium
I. Alapvető megfontolások
1. A protokoll érvényességi területe: minden ellátási szint.
2. A protokoll feltétel nélkül bevezethető.
3. Definíció. A bárányhimlő nagy kontagiozitású vírusfertőzés, amely a klinikai kép alapján csaknem minden esetben kórismézhető. Az átvészeltség szerokonverzióval jár és ép immunitás esetén életre szóló védettséget jelent. A gyermekkori megbetegedések általában enyhe lefolyásúak. Adoleszcens kortól lényegesen gyakoribbak a szövődmények. Immunkompromittált egyénben kezeletlenül halálos kimenetelű lehet.
4. Panaszokés tünettan. Heveny fertőzéses megbetegedés jellegzetes, viszkető hólyagos kiütéssel és többnyire lázzal.
5. A betegség leírása. A kórokozó a légutak nyálkahártyáját fertőzi meg, majd a nyirokrendszerbe kerülvén hét nappala fertőződés után primér virémiát okoz és a szövetekben replikálódik. Többnyire két héttel a fertőződés után, a szekunder virémia nyomán jelentkezneka betegség tünetei papulákkal, majd a jól ismert hólyagokkal. Újabb erupciók megjelenésére öt-hét napig lehet számítani. A bőr és a garatnyálkahártya után a leggyakrabban érintett szervek a tüdők, a belek, a mononukleáris-makrofág rendszer, ritkábban az agy, a retina és az izületek. A betegek többsége kisgyermek, ill. kisiskolás korú. 2007-ben hazánkban 48313 esetet jelentettek (incidencia: 480/100 ezer lakos). Ennél minden bizonnyal több eset fordult elő.
6. Kóreredet. Az alfa-herpeszvírusok alcsaládjába sorolt varicellovírus (korábbi elnevezése: varicella-zostervírus) okozza.
7. Epidemiológiai megfontolások.
7.1. Átvészeltséget jelent: az anamnesztikus bárányhimlő vagy a specifikus IgG osztályú antitest kimutathatósága
7.2. Szignifikáns expozició: fertőző egyén azonos háztartásban, szoros kontaktus legalább öt percig, azonos légtérben tartózkodás legalább egy órán keresztül. A fertőzés forrása lehet: bárányhimlős beteg, disszeminált övsömörben szenvedő beteg, fedetlen testtájon zostert hordozó beteg, immunkompromittált övsömörös beteg (virémia!).
7.3. Lappangási idő: 10-21-, az esetek döntő többségében 14-15 nap. Immun-szupprimált állapotban rövidebb, hiperimmunglobulin alkalmazása után hosszabb (28 nap) lehet.
7.4. A fertőzőképesség: a kiütés előtt két nappal kezdődik és a teljes pörkösödésig (általában 4-5 napig) tart (IV. szintű evidencia).
7.5. Elkülönités: a kiütés megjelenésétől legalább 5 napig, ill. az erupciók pörkösödéséig indokolt.
7.6. A szövődmények szempontjából magasabb kockázatú (nem immunszupprimált) populációk: felnőtt: terhes, erős dohányos, súlyos idült tüdőbeteg gyermek: súlyos idült tüdőbeteg, tartós salicylkezelésben részesülő, súlyos idült bőrbetegségben-, az intermedier anyagcsere zavarában szenvedő
II. Diagnózis (A klinikai kép ismeretén alapszik)
1. Az anamnézis az átvészeltség / szignifikáns expozíció megítélésével adhat segítséget a kórisme megállapításához.
2. A belszervi vizsgálat típusos kórkép esetében a kórisme megállapításához elegendő.
3. Egyéb vizsgálatok kezdeményezése csak szövődményes esetekben (ld. később) indokolt.
4. Differenciáldiagnózis. Kizárólag a kiütések morfológiája alapján olykor nehézséget okozhat az atypusos erupciók felismerése immunkompromittált betegben, továbbá egyéb infekciózus kórképektől (herpes simplex vírus, enterovírusok, Staphylococcus aureus okozta fertőzés), ill. nem fertőzéses, főleg allergiás patomechanizmusú betegségektől (gyógyszer-dermatózis, strofulus stb.) való elkülönítése. A klinikai kép alapján kétséges esetekben indokolt lehet a virológiai vizsgálat. A betegség első öt napján megkísérelhető a direkt víruskimutatás monoklonális fluoreszcens jelölésű monokolonális antitest segítségével a hólyagbennékből. A mintát torokváladék vételére alkalmas pálcával a hólyagalap széli részének erőteljes törlésével célszerű venni, hogy a morfológiai diagnózis megállapításához elegendő vírustartalmú sejt kerüljön a pálcára. Több, mint tíz napja zajló kórkép esetében a specifikus IgM kimutatása igazolja a kórismét.
III. Kezelés
A/ Nem gyógyszeres kezelés
1. Immunkompetens beteg típusos bárányhimlővel az alapellátás keretei között kezelendő.
2. A hospitalizáció javallatai:
- súlyosabb bőr-lágyrészfertőzés
- toxikus állapot
- mellkasi panasz/tünet
- idegrendszeri panasz /tünet
- atipusos kiütések
- vérzés
- hasi vagy mellkasi fájdalom
- elhúzódó / megújuló láz 6 nap után
- újabb erupciók jelentkezése 6 napon túl
- magas kockázatú egyén esetében megfontolandó
3. A betegség bejelentendő.
4. Betegápolás
A viszketést enyhítheti a bőrt hűsítő zuhanyozás, hintőporok alkalmazása. Gyermekkorban célszerű a körmöket rövidre vágni. Fontos a megfelelő folyadékbevitel biztosítása.
B/ Gyógyszeres kezelés
1. Oki terápia: acyclovir (ACV)
Posztexpozíciós állapotban megelőzésre, továbbá lokális alkalmazása nem javasolható. Nem bizonyított, hogy a szövődmények megelőzésére alkalmas. Az allergiától eltekintve az ACV kezelésnek ellenjavallata nincsen. Jelentős gyógyszerkölcsönhatással nem kell számolni. A vesefunkció beszűkülése esetén csökkentendő a dózis. Egyéb antivirális szer nem jön szóba a bárányhimlő kezelésében. Gyógyszer rezisztenciával csak AIDS betegnél kell számolni. (Terhesség alatti varicella antivirális kezelésre a 4. pontban van ajánlás.)
1.1. Az intravénás kezelés javallatai
- progresszív varicella /immunszupprimált egyén atipusos kiütéssel járó betegsége / generalizálódott zostere
- újszülött perinatális betegsége (ha az anyai varicella a születés előtt 5 napon belül, ill. azt követően 2 napon belül manifesztálódott) (Megjegyzés: a terhes anya övsömöre nem érinti a magzatot; III. szintű evidencia)
- vírus-mediálta szövődmények (pneumonitis, meningoencephalitis)
Adagolás: 3 hónaposnál fiatalabb csecsemőnek és felnőttnek 10(-15) mg/ttkg/dosi, 3 hónap és 12 év között 500 mg/m2/dosi 8 óránként infúzióban. A terápia tartama 5-10 nap (súlyos kórképben, ill. elhúzódó javulás esetén, pl. encephalitisben hosszabb).
1.2. Az orális kezelés javallatai
Az iniciális per os terápiának csak a kiütés megjelenését követően 24-36 órán belül elkezdve van értelme! Immunkompetens felnőtt szövődménymentes bárányhimlője esetén a kórlefolyást lerövidíti (Ib szintű evidencia).
- 13 évesnél idősebbek tipusos varicellája (opcionális; családban akvirált megbetegedés esetében indokolt)
- immunkompetens, de rizikócsoportba tartozó egyén típusos varicellája
- immunszupprimált betegek tipusos varicellája (folyamatos megfigyelés mellett)
- a parenteralisan megkezdett terápia folytatása
Adagolás:
- 13 év fölött 5 x 800 mg naponta öt-hét napig
- 3 hó-12év: 4x20 mg/ttkg naponta öt-hét napig (max. 800 mg/dosi) alternatíva: 3 hó - 2 év: 4 x 200 mg naponta öt-hét napig
2-5 év: 4 x 400 mg naponta öt-hét napig 6-12 év: 4 x 800 mg naponta öt-hét napig
Három hónaposnál fiatalabb csecsemő orális kezelésére vonatkozóan nincs elegendő tapasztalat. Immunkompromittált betegek kezelését a megfelelő ellenanyag szint kialakulásáig folytatni kell. Kétévesnél idősebb immunkompromittált gyermeknél a disszemináció megelőzésére a felnőtt adag alkalmazható.
2. Tüneti kezelés a szövődmények megelőzése érdekében.
Lázcsillapításra ne salicyltartalmú készítményt használjunk! A bőr öntisztulását akadályozó, arról nehezen eltávolítható rázókeverék (Susp. Zinci aquosa) kerülendő. Megkísérelhető antihistamin hatású szer szisztémás - nem lokális!- használata, bár erre vonatkozóan nincsenek az irodalomban evidencia szintek megállapításához klinikai vizsgálatok.
IV.-V. Rehabilitáció, Gondozás Szövődmények, prevenció és prophylaxis 1. Szövődmények; komplikált varicella
Komplikált bárányhimlős beteg ellátásához infektológiai konzílium szükséges.
- Bakteriális felülfertőzés
A 6. nap után, ill. újabb erupciók megjelenése nélkül észlelt láz avagy láztalan állapotot követő újabb láz esetén bakteriális szövődményt kell feltételezni. A bakterialis szuperinfekció többnyire az erupciók fertőződését jelenti (impetigo, cellulitis) és S. pyogenes, ill. S. aureus idézi elő. Invaziv Streptococcus betegség (véráram-fertőzés, toxicus shock syndroma) lehet a következménye. A mikrobiológiai diagnózishoz hemokultúra vizsgálat, ill. a felülfertőzés területéből vett minta (hólyagbennék, szövetnedv stb.) bakteriológiai vizsgálata szükséges. A felülfertőzést penicillinnel, S. aureus kóroki szerepe esetén antistaphylococcalis szerrel kell kezelni. A gyermekkori Streptococcalis Toxicus Shock Syndroma első kockázati tényezője a bárányhimlő.
- Pneumonitis
Egészséges adoleszcensekés felnőttek esetében leggyakoribb szövődmény a pneumonitis. A kiütések megjelenését 1-3 nappal követően légúti panaszok utalnak a tüdő érintettségére. A diagnózist mellkasröntgen felvétel igazolja.
- Neuroinfekció (cerebelláris ataxia, meningitis, meningoencephalitis)
- Hematológiai rendellenességek (thrombocytopenia, leukopenia)
A neurológiai és hematológiai komplikációk kórházi szakellátást igényelnek.
- Progresszív varicella
A folyamat a parenchymás szerveket is érinti és erre az erupciókatipusos volta utalhat. Kezeletlenül többnyire fatális.
- Reye syndroma
A salicylkészitmények és a Reye syndroma összefüggése miatt ezen szerek alkalmazása varicella esetében tilos. Csillapíthatatlan hányás - esetleg tudatzavarral társulva- föl kell vesse a betegség gyanúját.
2. Prevenció
A bárányhimlő megelőzősének hatékony eszköze az aktív immunizáció, élő, attenuált kórokozó tartalmú védőoltással. Az immunizáció globális járványügyi hatását, a bárányhimlő megbetegedés előfordulásának 85%-os csökkenését, igen magas 98-99%-os átoltottságnál észlelhetjük. Több mint 10 éves tapasztalat alapján az egyén leghatékonyabb védelmét - fertőzést hosszútávon kivédő humorális ellenanyagszintet, T sejtes immunválaszt és boosterelhető immunmemóriát -, minden életkorban 2 oltás után érhetjük el. Javallat:
- Fogékonyakalapimmunizálása: 2 oltás minimum 4-6 hét különbséggel *
- Korábban oltottak felzárkózó oltása**
*Alapimmunizálást javasolt 15 hónapos korban, az MMR oltással egy időben, és 18 hónaposan, az esedékes DPaT-IPV-HIB oltással egy időben elvégezni.
** Alapimmunizált egyént, - amennyiben oltás után áttöréses fertőzése nem volt - bármely időpontban (legkorábban 4-6 héttel az első oltás után), de legkésőbb egy újabb közösségbe kerülés előtt, második oltásban kell részesíteni.
Második oltás csökkenti az egyetlen adag után kialakuló elégtelen védettség előfordulását, és mind a humorális, mind a T sejtes immunválaszt a természetes immunválasznak megfelelő szintűre erősíti, ezáltal jelentően csökkenti az oltás után előforduló áttöréses fertőzés létrejöttét.
3. Posztexpoziciós profilaxis (fogékony egyén szignifikáns expozíciója esetén)
3/A Hyperimmunglobulin (Varicella-Zoster-Immunglobulin, VZIG) Javallat:
- immunszupprimált egyén
- terhes
- újszülött
- súlyos alapbetegségben szenvedő (opcionális)
Adagja: 0,2-1 (5-25 NE) ml/ttkg
A VZIG-et 72 órán belül célszerű beadni. Tiz napon belül alkalmazva is mérsékli a kórkép súlyosságát. Átvészeltség esetén, ill. a betegség jelentkezésekor a VZIG alkalmazása már fölösleges. 3/B Oltás (aktív immunizálás)
72 órán - legföljebb öt napon - belül ellenjavallat hiányában az élő, attenuált virust tartalmazó vakcinával védettség érhető el. Amennyiben az oltott személy egy oltás után a fertőzést nem aquirálta, 4-6 héttel az első dózis után, 2. oltás szükséges. Az immunizáció után 7-10 nappal (maximum 21 nappal) varicellára emlékeztető kiütés jelentkezhet, ez az oltási betegség tünete. Amennyiben ez immunszupprimált egyénben fordul elő, az illetőt antivirális kezelésben kell részesíteni. Az oltás után 1 héten belül észlelt kiütés "vad virus", azaz VZV fertőzés következménye.
4. Profilaxis és antivirális kezelés az egyes fogékony betegpopulációkban Immunkompetens, nem terhes egyén (egyhónaposnál idősebbek)*
- Posztexpoziciós prophylaxis: a VZIG alkalmazása fölösleges. Az egyévesnél idősebbek posztexpoziciós vakcinációja elfogadott.
- Terápia: 24-36 órán belül
- rizikócsoportba nem tartozó egyén: antivirális kezelést nem igényel
(11 év fölött opcionális-, családi kontaktus esetén javasolt az ACV terápia.)
- rizikócsoportba tartozó egyén: orális ACV kezelés 48 órán túl az orális terápia nem jön szóba.
Terhes*
A terhesség előrehaladtával nő a pneumonitis kockázata. A terhes bárányhimlője az első trimeszterben a fetalis varicella szindrómát okozhatja. Ez a varicellás terhes anyák magzatainak kevesebb, mint 2 %-ában fordul elő. A terhesség megszakítása az első trimeszterben varicella fertőzés miatt nem indokolt. A kórisme a magzat ultrahangvizsgálatával állapítható meg (III szintű evidencia). A magzatvíz vírus DNS irányú vizsgálata fölösleges. A magzati elhalás kockázatát a terhes varicellája nem növeli (IIb szintű evidencia).
- Posztexpoziciós profilaxis: VZIG a terhesség bármelyik szakaszában (III szintű evidencia). A foetalis varicella szindróma kialakulására vonatkozó effektusa nem ismert. Az aktív immunizáció tilos.
- Terápia
Az ACVembriopatogén hatására semmiféle adat nem utal. Azonban a 20. terhességi hét előtt csakaterhes megfelelő
tájékoztatását követően szabad alkalmazni (IV szintű evidencia). Erős dohányos terhesnek, továbbá annak, akin igen
sok (>100) kiütés jelentkezik, fokozottan javasolható.
A 20. terhességi hét után a/ 24-36 órán belül: per os ACV egy hétig
b/48órántúl:ACV iv.
Újszülött*
A. A születés előtt 5 napon belül, ill. azt követően 2 napon belül jelentkező anyai megbetegedés esetén nagy a kockázata az újszülött progresszív varicellájának (III szintű evidencia). Kielégítő anyai IgG szintre biztosan csak az anya betegségének ötödik napjától lehet számítani. A bárányhimlős gyermekágyas szoptatását nincs értelme megtiltani.
- magas kockázatú újszülött ("-5. - +2. nap"): VZIG profilaxis szükséges; megbetegedés esetén ACV iv.
- nem magas kockázatú újszülött: súlyosabb kórlefolyás esetén az ACV terápia egyedi elbírálást igényel
B. Egyhetes koráig minden fogékony anya (releváns kórelőzmény/pozitív szerostátusz hiányában) újszülöttje szignifikáns expozíció esetén VZIG profilaxisban kell részesüljön,.
C. Újszülött osztályon: a fogékony anyák újszülöttjei, továbbá minden éretlen újszülött (<30. terhességi hét és/vagy <1 kg születési súly) VZIG profilaxisban kell részesüljön szignifikáns expozíció esetén.
D. Súlyos alapbetegségben szenvedő, speciális ellátást igénylő csecsemők szignifikáns expozíció esetén specifikus ellenanyag hiányában VZIG profilaxisban kell részesüljenek.
Immunszupprimált egyén*
Ide tartoznak a veleszületett vagy szerzett immunhiány-betegségben szenvedők és az immunszuppressziv kezelés alatt álló betegek (Kivéve az izolált antitest hiány szindrómát, mely esetben a varicella normális lefolyású). Az egy hónapon belül alkalmazott szisztémás kortikoszteroid terápia (2 mg/ttkg-ot meghaladó adagban) immunkopromittált állapotot jelent varicella vonatkozásában. Nem jelent viszont veszélyt az inhalációs szteroidok használata és a másodnaponta alkalmazott steroidkezelés.
- Posztexpoziciós profilaxis:
kötelező; ilyen helyzetben a VZIG-nek nincs ellenjavallata. Celluláris immundefektus az oltást ellenjavallja. Humorális immundefektusban elfogadott az aktív immunizálás. A három hónapon belül alkalmazott citosztatikus kezelés és az egy hónapon belül naponta, fenti adagban adott steroidterápia esetén nem szabad aktíve immunizálni. Tünetmentes HIV fertőzött vagy fertőzésük CDC szerinti A1 vagy N1 stádiumában lévő gyermekek megkaphatják az oltást, ha CD4+ limfocita szubpopulációjuk száma a korcsoportuknak megfelelő érték 25 %-át eléri.
- Terápia:
atipusos erupciókkal járó / progresszív kórkép: ACV iv.
normális kórlefolyás: 24-36 órán belül kórházi megfigyelés mellett az orális ACV kezelés megkísérelhető Kórházban megbetegedett egyének (fogékony) kontaktjai* Alapbetegségüktől függően VZIG, ill. oltás egyaránt választható.
*Virus-mediálta szövődmény esetén intravénás ACV kezelés kötelező.
VI. Irodalomjegyzék
1. American Academy of Pediatrics. Committee on Infectious Diseases: Recommendations for the Use of Live Attenuated Varicella Vaccine. Pediatrics 1995;95; 791-796.
2. American Academy of Pediatrics. Committee on Infectious Diseases: Varicella Vaccine Update. Pediatrics Vol.105. No 1. January2000.
3. British National Formulary Vol49, March 2005. Published by the British Medical Association and the Royal Pharmaceutical Society of Great Britain.
4. HPA (2003) Guidelines on the management of communicable disease in schools and nurseries: chickenpox. Health Protection Agency. www.hpa.org.uk [Accessed: 27-9-2004].
5. HPA (2004a) Chickenpox - varicella zoster. Health Protection Agency. www.hpa.org.uk [Accessed: 27-9-2004].
6. HPA (2004b) Immunoglobulin handbook: indications and dosage for normal and specific immunoglobulin preparations issued by the HPA. Health Protection Agency. www.hpa.org.uk [Accessed: 27-9-2004].
7. Klassen, T.P., Belseck, E.M., Wiebe, N., and Hartling, L. (2004) Acyclovir for treating varicella in otherwise healthy children and adolescents (Cochrane Review). The Cochrane Library (Issue 2). Chichester, UK: John Wiley & Sons, Ltd.
8. K. L. Margo, A. F. Shaughnessy,: Antiviral Drugs in Healthy Children. Am Fam Phys Vol 57/No5 (March 1,1998)
9. Morgan-Capner, P. and Crowcroft, N. (2000) Guidance on the management of, and exposure to, rash illness in pregnancy (including consideration of relevant antibody screening programmes in pregnancy). Report of a PHLS Working Group. Health Prorection Agency. www.hpa.org.uk [Accessed: 27-9-2004].
10. Nathwani, D., Maclean, A., Conway, S., and Carrington, D. (1998) Varicella infections in pregnancy and the newborn: a review prepared for the UK Advisory Group on chickenpox on behalf of the British Society for the Study of Infection. Journal of Infection 36(Suppl 14), 59-71.
11. Nelson Textbook of Pediatrics. -17th ed. Edited by Behrman RE, Kliegman RM, Jenson HB. Saunders, Elsevier Science.
12. RCOG (2001) Chickenpox in pregnancy. Royal College of Obstetricians & Gynaecologists. www.rcog.org.uk [Accessed: 27-9-2004].
13. Varicella vaccination: Recommendation statement from the Canadian Task Force on Preventive Health Care. CMAJ 2001;164(13):1888-9.
14. PRODIGY Guidance - www.prodigy.nhs.uk/guidance.asp?gt=Chickenpox Cohen &Powderly: Infectious Diseases, 2nd ed., 2004 Mosby
15. Epidemiology and Prevention of Vaccine-Preventable Diseases. The Pink Book. Course Textbook. Updated 8th Edition 2nd Printing (January 2005 )
16. B. Watson .Humoral and Cell-Mediated Immune Responses in Children and Adults after 1 and 2 Doses of VaricellaVaccine. JID 2008:197 (Suppl 2) S143
17. B.Kuter,H.Matthews,H.Shinefield. Ten year follow-up of healthy children who received one or two injections of varicella vaccine. Pediatr Infect Dis J, 2004;23:132-37
18. S.S. Chaves, P.Gargiullo, J. X. Zhang, Loss of Vaccine-Induced Immunity to Varicella over Time N Engl J Med 356;11 www.nejm.org march 15,2007
19. A. Arvin, A. Gershon: Control of Varicella: Why Is a Two-Dose Schedule Necessary? Pediatr Infect Dis J. June2006Vol:25, No;6. 475-76.
20. A. Arvin: Humoral and Cellular Immunity to Varicella-Zoster Virus: An Overview JID 2008:197 (Suppl). S58-60
21. B. Kuter, F. Schodel F. Second varicella vaccine dose Pediatr Infect Dis J febr 2007. Vol:26,No;2.193-4.
22. B.Watson:Humoral and Cell-Mediated Immune Responses in Children and Adults after 1 and 2 Doses of Varicella Vaccine JID2008:197 (Suppl 2) S 143-146.
23. American Academy of Pediatrics .Committee on Infectious Diseases .Clinical report Guidance for the Clinician in Rendering Pediatric Care Prevention of Varicella: Recommendations for Use of Varicella Vaccines in Children, Including a Recommendation for a Routine Two-Dose Varicella Immunization Schedule www.aap.org/recommendations
24. Prevention of Varicella Recommendations of the Advisory Committee on Immunization Practices (ACIP) June 22,2007 /56(RR04);1-40
Az irányelvet összeállítók kinyilvánítják, hogy semmilyen szponzor nem támogatta az irányelv kialakítását, munkájukat külső támogatástól függetlenül végezték.
A szakmai irányelv érvényessége: 2010. szeptember 30.
1. Érintett társszakmák: elsősorban a gyermekgyógyászat, a belgyógyászat, a családorvoslás és a szülészet-nőgyógyászat.
2. Internetes oldalak: aafp.org; neli.org.uk; guideline.gov; aap.org; rcog.org.uk; cdc.gov; ctfphc.org; cd.gov/nip; dh.gov.uk; hpa.org.uk; prodigy.nhs.uk
Az Egészségügyi Minisztérium
szakmai irányelve
Az oltások és műtétek egybeesése esetén szükséges teendőkről
(ajánlás háziorvosoknak, házi gyermekorvosoknak, járó- és fekvőbeteg szakellátásban részt vevő egyéb képzettségű szakorvosoknak)
Készítette: az Infektológiai Szakmai Kollégium és
a Csecsemő- és Gyermekgyógyászati Szakmai Kollégium
Az irányelv célja
Útmutatás az életkor szerint kötelezően előírt védőoltások, továbbá a gyógyszertári forgalomban hozzáférhető, un. választható védőoltások és altatással, vagy anélkül végzett műtéti beavatkozások egybeesése esetén követendő eljárásra.
Az irányelv megalapozása, kiadásának indoklása
A vakcinológia látványos fejlődésének jeleként évről évre bővül a védőoltással megelőzhető betegségek száma. Jelenleg Magyarországon a minden gyermek számára életkor szerint előírt és ajánlott védőoltásokon túl minden, az Európai Unióban törzskönyvezett vakcinához is hozzá lehet jutni, ezért gyakran kerülhet sor védőoltás beadása és valamilyen beavatkozás időbeli egybeesésére.
A 2000-ben kiadott irányelv revíziójára azért van szükség, mert az eltelt 7 év alatt felgyűlt tapasztalatok arra utalnak, hogy az irányelv túlbiztosít, azaz túl hosszú várakozási időtartamokat jelöl meg az oltások és az altatással vagy anélkül végzendő beavatkozások között, ami jelenlegi tudásunk szerint akadálya lehet a beteg érdekében végzendő mindkét beavatkozásnak:
- hátrányt jelenthet védőoltások miatt szükséges beavatkozások halasztása
- ugyancsak hátrányt jelenthet, ha beavatkozás miatt nem kerül sor egyébként indokolt prevenciós lépésre - ezzel a megelőzhető fertőzés elkerülésének esélyére.
Az irányelvet felhasználók köre:
- háziorvosok, házi gyermekorvosok, azaz a mindennapi munkájuksorán leggyakrabban védőoltások beadását végző orvosok
- járó- és fekvőbeteg szakellátásban részt vevő egyéb képzettségű szakorvosok
Az irányelv kidolgozásában részt vett kollégiumok, társaságok, intézetek:
Infektológiai Szakmai Kollégium
Csecsemő- és Gyermekgyógyászati Szakmai Kollégium
Betegszervezetek véleményét - mivel ilyenek létezéséről ezzel a kérdéskörrel kapcsolatban, mely az egész lakosságot, és nem egyes betegcsoportokat érinti - nincs tudomásunk, nem kértük ki.
A szakmai irányelv érvényessége: 2010. szeptember 30.
Az irányelv kidolgozásához használt tudományos bizonyítékok és forrásmunkák köre:
A témakörrel meglepően keveset foglalkozik a szakirodalom. Az irányelv készítésekor vakcinológiával foglalkozó magyar és idegennyelvű kézikönyvek, tudományos publikációk mellett a Medline, a Cochrane adatbázisaiban fellelhető, 5 éven belüli közléseket vettük figyelembe. Az Egyesült Államokban érvényes ajánlásokat - Advisory Committee on Immunsation Practices (ACIP) és a német Standinge Impfkomission (STIKO, Robert Koch Institute) ajánlásait, továbbá az Országos Epidemiológiai Központ (OEK) Módszertani levél a 2008-as évi védőoltásokról ajánlásait egyeztetve dolgoztuk át a korábbi irányelvet.
Végezetül megjegyezzük, hogy saját, több, mint 10 éves védőoltási szaktanácsadóban végzett munkánk tapasztalatait is felhasználtuk.
Alapvető megfontolások
Teoretikus, vagyis elméleti feltevéseken, és nem gyakorlati tapasztalatokon alapul az a félelem, hogy a védőoltások beadását követően komplikációkra lehet számítani, ha altatás, és/vagy műtéti beavatkozás időben egybeesik. Ugyancsak teoretikus az aggodalom amiatt, hogy az altatás, mint beavatkozás befolyásolni lenne képes a védőoltások hatékonyságát. Egyik helyzetre vonatkozóan sem tartalmaz a szakirodalom összehasonlító vizsgálatokat, illetve nem határoz meg bizonyítékokon alapuló javallatokat, ellenjavallatokat.
Vannak azonban arra vonatkozóan közlések és állásfoglalások, hogy célszerű olyan helyzetekben, ahol ez orvosilag megengedhető, a védőoltások beadása után a várható oltási reakciók lezajlásáig valamilyen beavatkozást halasztani, hogy ezen reakciók ne nehezítsék meg a beavatkozást követő esetleges komplikációk megítélését.
A vakcinák fajtái és a várható oltási reakciók Élő és inaktivált vakcinák
Az aktív immunizációra használatos vakcinák abban különböznek egymástól, hogy a védettség kialakításra szolgáló antigént milyen formában tartalmazzák. Két nagy csoportra oszthatók:
- az élő - gyengített, azaz attenuált - kórokozót, illetve
- az elölt kórokozót, vagy annak valamilyen tisztított részét tartalmazó, ún. inaktivált vakcinákra.
A Magyarországon forgalomban lévő, törzskönyvezett vakcinák részletes ismertetése szerepel az OEKévente kiadott, a védőoltásokról szóló Módszertani levelében, mely az OEK honlapjáról - www.oek.hu - letölthető.
Oltási reakciók
A vakcinák beadását követően várható oltási reakciók két nagy csoportra oszthatók:
- helyi, vagy lokális reakciók - pl. a beadás helyén fájdalom, duzzanat, bőrpír, illetve
- általános, szisztémás reakciók - pl. láz, rossz közérzet, hányinger, stb.
Az egyes vakcina típusoknál eltérő időben lehet oltási reakciókra számítani:
- inaktivált vakcinák esetén átlagosan legfeljebb < 3 nap (STIKO, ACIP),
- élő vakcinák esetén átlagosan legfeljebb < 14 nap (STIKO, ACIP).
(Előfordulhatnak oltások beadása után nem várt események is - ezek azonban külön témakörhöz tartoznak és kivizsgálásukat, a követendő eljárásokat ugyancsak OEK ajánlás részletezi: Módszertani ajánlás az Oltásokat Követő Nem várt Eseményekről /OKNE/).
Javaslatok oltási intervallumokra műtétekés oltások egybeesése esetén:
- Vitális indikációval végzett beavatkozás az immunizáció idejétől függetlenül, bármikor elvégezhető és el is végzendő.
- Elektív műtét végzése védőoltás beadását követően
- Elölt kórokozót tartalmazó oltás esetén > 72 óra várakozás ajánlott,
- Élő kórokozót tartalmazó vakcina adása után > 14 nap várakozás ajánlott.
- Vitális indikációval adott oltások után (pl. rabies, tetanusz, HBV) azonnali műtéti beavatkozás is biztonsággal elvégezhető.
- Védőoltás beadása műtéti beavatkozás után
- Általában a posztoperatív rekonvaleszcencia időpontja egyben az olthatóság időpontja is, hacsak különös körülmény ezt nem sürgeti, általában a műtét típusától függően 1-2 hét (pl. sérvműtét, tonsillectomia, lépeltávolítás, stb.)
- Kiterjedt, roncsoló sérülések, polytrauma miatt végzett és/vagy szövődményes műtétek, illetve immunszuppresszióval is járó beavatkozások - pl. szervátültetések - külön, a védőoltási szaktanácsadók orvosaival konzultált, egyedi oltási tervet igényelnek.
Az irányelvet az Advance Course on Vaccinology (ADVAC) nemzetközi diplomával igazolt, képesített védőoltási szaktanácsadók állították össze, szponzori tevékenység vagy befolyás munkájukban nem játszott szerepet.
Irodalomjegyzék:
1. Advisory Committee on Immunsation Practices (ACIP): General recommendations on immunization. MMWR Recomm Rep. 2006 Dec 1;55(RR-15):1-48. Erratum in: MMWR Morb Mortal Wkly Rep. 2006 Dec 8;55(48):1303. MMWR Morb Mortal Wkly Rep. 2007 Mar 23;56(11):256. Pediatrics. 2007 May;119(5):1008.
2. Budai J, Velkey Gy: Teendők oltások és műtétek egybeesése esetén. Módszertani levél, 2000.
3. Burns, V,Caroll B: Antibody response to vaccination and psychosocial stress in humans: relationships and mechanisms. Vaccine, 2003;21:2523.
4. Robert Koch Insititute: Epidemiologisches Bulletin, No30,2004.
5. Immunsation against infectious diseases :The Green Book, NHS, 2006.
6. Short JA, van der Walt JH,Zoanetti DC: Immunisation and anesthesia - an international survey. Paediatr Anaesth. 2006
May;16(5):514-22.
Az Egészségügyi Minisztérium
szakmai protokollja
A neutropenias beteg fertőzéseinek megelőzéséről és kezeléséről (1. módosított változat)
Készítette: az Infektológiai Szakmai Kollégium és
a Transzfúziológiai és Hematológiai Szakmai Kollégium
ELŐZMÉNYEKÉS MÓDSZER
A neutropeniás betegek infekciónak kezelésével foglalkozó szakmai ajánlás korábban 2003-ban, majd átdolgozva 2005-ben jelent meg a Transzfúziológiai és Hematológiai Szakmai Kollégium valamint az Infektológiai Szakmai Kollégium közös protokolljaként.
A vezérfonal jelen frissítését a szöveg időszakos karbantartásán túl elsősorban új nemzeti és nemzetközi ajánlások megjelenése, az epidemiológiai környezetben bekövetkezett változások és a terápiás szemlélet hangsúlyváltozásai indokolják.
Az alábbiakban megfogalmazott megállapítások és ajánlások főként a súlyosan neutropeniás (elsősorban malignus alapbetegség miatt kemoterápiával kezelt) betegcsoportokra vonatkoznak. A gombák okozta megbetegedések tárgyalása során esetenként kitérnek a granulocytaszámtól függetlenül előforduló kórképekre, továbbá azokra az infekciókra, melyek jellemző módon a neutropeniát követő szakaszban alakulnak ki. A hemopoetikus őssejt átültetésben részesülők kezelése annak korai, neutropeniás időszakában, a leírtakhoz hasonló elvek szerint történik. Ugyanakkor e betegek ellátása során számos olyan speciális szempont (kockázati tényező, immunológiai szövődmény, gyógyszerkölcsönhatás) merül fel, melynek részletes ismertetése meghaladja a jelen dokumentum kereteit.
A szerzők felhívják a figyelmet arra, hogy a megfogalmazott ajánlások általános jellegűek, ezért konkrét klinikai helyzetben történő alkalmazásuk során körültekintően kell eljárni. Nem ismert ugyanis olyan kezelési séma, gyógyszer vagy gyógyszer kombináció, mely valamennyi neutropeniás beteg esetében - válogatás nélkül - azonos hatékonyságú volna. A betegek komplex ellátásába célszerű a témában járatos infektológust is bevonni. Az alábbiakban felsorolt antimikróbás szerek javallatait, ellenjavallatait, mellékhatásait, interakcióit illetően nem mellőzhető az alkalmazási előíratok és a vonatkozó szakirodalom gondos tanulmányozása.
EVIDENCIASZINTEK
Az ajánlás megalapozottsága
A A rendelkezésre álló adatok a módszer alkalmazását egyértelműen alátámasztják.
B A rendelkezésre álló adatok a módszer alkalmazását nagyrészt alátámasztják.
C A rendelkezésre álló adatoka módszer alkalmazását csak csekély mértékben támasztják alá.
D A rendelkezésre álló adatok nagyrészt a módszer alkalmazása ellen szólnak.
E A rendelkezésre álló adatok egyértelműen a módszer alkalmazása ellen szólnak.
Az evidencia forrása
I Egy vagy több, randomizált, kontrollált vizsgálat.
II Egy vagy több, megfelelően tervezett, nem randomizált vizsgálat.
III Szakértők, bizottságok véleménye, klinikai tapasztalat.
A LÁZAS NEUTROPENIA JELENTŐSÉGE
A neutrophil granulocyták számának jelentős csökkenésének hátterében különféle tényezők állhatnak: kezeletlen hematológiai betegség okozta csontvelői infiltráció vagy aplasia, nem várt gyógyszer mellékhatás (agranulocytosis), citosztatikus kezelés vagy irradiáció. Súlyos neutropenia kialakulásakor - azaz, ha a keringő neutrophilek abszolút száma 0,5 G/l alatti, vagy 1-0,5 G/l között van, és csökken - az infekciók gyakorisága és a következményes halálozás jelentősen növekszik. Adott beteg esetében súlyos/fatális infekció kialakulásának kockázata az alábbi tényezők függvénye: a neutropenia tartama, mélysége, a neutrophilek számának emelkedő vagy csökkenő tendenciája, az egyidejű barriersérülés (mucositis) mértéke, a kolonizáció és a nozokomiális környezet jellege, az esetleges malignus alapbetegség statusa, és az előforduló kísérő betegségek. Mindenképp fokozott kockázatúnak kell tekinteni a nagydózisú kemoterápiával kezelt acut myeloid leukaemiás betegeket, illetve a bármely kórkép miatt őssejt átültetésben részesülőket.
Gyakran az infekció egyetlen tünete a láz. A lázas, neutropeniás betegek mintegy felében kimutatható, vagy okkult infekció zajlik. Ha az abszolút neutrophilszám <0,1 G/l, a betegek ötödében bacteriaemia alakul ki. Hypothermia ritkán fordul elő, rossz prognózisra utal. A neutropeniás beteg lázának egyéb oka is lehet (vérkészítmény, gyógyszer), kérdéses esetben azonban fertőzést kell feltételezni.
KLINIKAI TÜNETEK
A gyulladás klasszikus jeleinek hiányában a neutropeniás betegek fertőzései tünetszegények. A bőr és a lágyrészek bakteriális fertőzéseiben hiányozhat az induratio, az erythaema és a suppuratio, pneumoniában a jellegzetes infiltrátum, meningitisben a liquor sejtszaporulata. A húgyúti infekciók - bár ritkák - pyuria nélkül is kialakulhatnak. Mindezek ellenére keresni kell az infekció bármily diszkrét jelét, különösen a leggyakrabban érintett testtájakon. Ezek: a szájüreg és a garat, az oesophagus alsó szakasza, a tüdő, a gáttájék, a szemfenék, a bőr (különösen a punkciók helyén), az intravascularis műanyag eszközök bemenete és a körömágy.
DIAGNOSZTIKA
Lázas neutropenia észlelésekor az 1. táblázat-ban ismertetett vizsgálatok elvégzése szükséges
KEZELES
KEZDETI ANTIBAKTERIÁLIS KEZELÉS
Mivel a neutropeniás betegek infekciói gyorsan progrediálhatnak, megfelelő ellátás nélkül halálozási arányuk magas, klinikai tünetek esetén pedig a fertőzés kizárására biztonságos módszer nem áll rendelkezésre, a neutropéniás láz felléptekor valamennyi beteget azonnal empirikus antibakteriális kezelésben kell részesíteni. A terápia a leggyakrabban előforduló, ezen belül a legnagyobb letalitást előidéző bakteriális kórokozók (P. aeruginosa, Klebsiella spp., E. coli, viridans streptococcusok, S. aureus) ellen irányul. Az antibiotikum választás során a baktériumok természetes rezisztenciáján kívül figyelembe kell venni a helyi epidemiológiai és rezisztencia viszonyokat, valamint a betegnél fennálló speciális korlátozó tényezőket (pl. veseelégtelenség, allergia). A perifériás és centralis vénás eszközök (kanülök) használatára, gondozására, esetleges infekcióik nyomon követésére és kezelésére a betegeket ellátó centrumok - a nemzetközi standardok figyelembe vétele mellett -helyi protokollokat dolgoznak ki
Parenterális terápia
A betegek parenterális antimikróbás kezelésére két lehetőség kínálkozik: a béta-laktám monoterápia, és a glikopeptidet tartalmazó kombináció. A hatóanyagok tekintetében részletesen ld. 1. ábrát és 2. táblázatot. A béta-laktám + aminoglikozid kombináció előnyeit az e tárgykörben végzett klinikai tanulmányok metaanalizise nem bizonyította,azaminoglikozidokokozta nephrotoxicitás pedig reálisveszélynekbizonyult. Ugyanakkor az utóbbi évek során egyes nozokomiális Gram-negatív baktériumok körében megnőtt a béta-laktám antibiotikumokra kevésbé érzékeny speciesekaránya. Ezt szem előtt tartva, súlyos szepszisben, szeptikus sokkban illetve rezisztens Gram-negatív baktérium okozta infekció gyanúja esetén a primer kombináció részeként aminoglikozidot is lehet alkalmazni (CIII). Orális terápia
Számos klinikai vizsgálat bizonyította, hogy megfelelő szempontokértékelésével a felnőtt, lázas neutropeniás betegek körében elkülöníthető egy olyan kis kockázatú csoport, amelyben a súlyos lefolyású vagy fatális kimenetelű infekció kialakulásának esélye elenyésző. Megfelelő feltételek teljesülése esetén ezek a betegek kizárólag orális antibiotikumokkal is eredményesen kezelhetőek (A-I). Szintén megfelelő feltételek mellett ellátásuk járóbetegként is történhet: kórházi megfigyelést követően a betegek rövid idő elteltével hazabocsáthatóak. A kockázat megítélésre több értékelési rendszert dolgoztak ki. A klinikai gyakorlatban is validált MASCC pontrendszert a 3. táblázat ismerteti. A felsorolt kritériumok mérlegelésén kívül a beteget az alábbi tényezők fennállása esetén is a nagy kockázatú csoportba kell sorolni: súlyos kísérőbetegség, nem kontrollált alapbetegség, máj-vagy veseelégtelenség, tüdőinfiltratum vagy az infekcióval összefüggésbe hozható egyéb lokalizált folyamat valamint a kórelőzményben szereplő alemtuzumab terápia. A kis kockázatú csoportban amoxicillin-klavulánsav plusz ciprofloxacin adható per os. Ez a terápiás lehetőség természetesen nem alkalmazható, ha a beteg profilaxisként fluorokinolont kapott.
FIGYELMEZTETÉS: A lázas, neutropeniás beteg hazabocsátása illetve ambuláns kezelése csak akkor engedhető meg, ha az alábbi feltételek maradéktalanul érvényesülnek:
1. A kockázat pontos értékelése a kérdésben járatos szakember(ek) által.
2. A beteg képes legyen orális gyógyszer szedésére. A súlyos mucositis, hányás vagy hasmenés az antibiotikumok bizonytalan felszívódása miatt az intézményen kívüli kezelést ellenjavallja.
3. A beteg és az otthoni környezet (család) megfelelő felvilágosítása és beleegyezése. A beteggel egy háztartásban éljen olyan felelős személy, aki állapotromlás esetén intézkedni képes.
4. A beteg megfelelő ítélőképessége.
5. Megfelelő telekommunikáció és szállítóeszköz háttér.
6. Megfelelő gyógyintézeti háttér, mely a nap 24 órájában a beteg rendelkezésére áll telefonon, ambuláns vizsgálattal és szükség szerint kórházi felvétellel.
AZ ANTIBAKTERIÁLIS KEZELES FOLYTATÁSA
A kezdeti antibiotikum kezelés hatékonyságának megítélésére neutropeniás beteg esetében rendszerint 3-5 (esetleg több) napra van szükség. Ha a beteg állapota romlik, az infekció tünetei súlyosbodnak, vagy újtünetek jelennek meg, szükség lehet az empirikus terápia korai módosítására. Ilyenkor új szer(ek) hozzáadásával, vagy az antibiotikum kicserélésével a spektrumot olyan irányba kell kiterjeszteni, hogy az azokat a specieseket is lefedje, melyekre a kezdeti terápia kevésbé hatásos (pl. glikopeptid hozzáadása). Releváns mikrobiológiai lelet birtokában a kórokozó antibiogramjának megfelelő, leghatékonyabb, célzott terápiára kell áttérni. Gram-negatív illetve Pseudomonas-ellenes hatékonysággal rendelkező vegyület adása még akkor is kötelező, ha a célzott kezelés dokumentált Gram-pozitív infekció ellen irányul. Az empirikus terápia első hetében a klinikai választ illetően az alábbiakat tapasztalhatjuk:
A beteg a terápia 3-5. napján láztalanná válik
(2. ábra)
Ha a kórokozó ismert, a célzott terápiát addig kell folytatni, amíg az infekció tünetei megszűnnek, a hemokultúrák sterillé válnak és az abszolút neutrophilszám meghaladja a 0,5 G/l-t. Ha az utóbbi feltétel nem teljesül, az antibiotikum csak a beteg szoros megfigyelése mellett hagyható el. A kezelés időtartama ne legyen 7 napnál rövidebb. Amennyiben a láz hátterében kórokozót identifikálni nem lehetett, szervi érintettségre utaló jelek (pl. pneumonia) hiányában a kis kockázati csoportba tartozó, legalább két napja láztalan beteg esetében mérlegelni lehet szekvenciális, orális terápia (amoxicillin-klavulánsav plusz ciprofloxacin) alkalmazását. Egyéb esetben a megkezdett parenterális terápia folytatása ajánlott.
A beteg a terápia 3-5. napján még lázas
(2. ábra)
Ha kórokozó baktériumot nem sikerült kimutatni, a perzisztáló láz hátterében az alábbi lehetőségek merülnekfel: 1. A fertőzés nem bakteriális eredetű. 2. A fertőzést a választott szerrel szemben rezisztens baktérium okozta. 3. Nem megfelelő az antibiotikum koncentráció az infekció helyén (okai: farmakokinetikai tényezők, nem vascularisált területen [kanül, abscessus] zajló infekció 4. Sejtfal-deficiens baktérium jelenléte valószínűsíthető. 5. A láz nem infekciós eredetű.
A tartósan lázas beteg megelőző és aktuális klinikai tüneteinek, mikrobiológiai és egyéb vizsgálati eredményeinek gondos újraértékelése után az alábbi terápiás döntéseket hozhatjuk:
1. Ha a beteg állapota nem változott (stabil), folytathatjuk a korábban megkezdett antibakteriális terápiát. Ha glikopeptid adásának indikációja nem áll fenn, és a beteg empirikus glikopeptid terápiában részesült, a szert el kell hagyni.
2. Ha az infekció progrediál, szükségessé válika kezdeti terápia módosítása vagy kiegészítése. A változtatás során szem előtt kell tartani az empirikusan adott szerek antibakteriális spektrumának hiányosságait, és a feltételezett kórokozó várható érzékenységét. Ha a beteg empirikusan nem kapott vancomycint vagy teicoplanint, és a glikopeptid adásának indikációja fennáll, kiegészítésként e szerek valamelyikét választhatjuk (C-III). A perzisztáló láz miatt, ha azt egyéb új tünet nem indokolja, glikopeptid vagy aminoglikozid empirikus adása nem javasolt (DI, CIII)
AZ ANTIBAKTERIÁLIS KEZELÉS IDŐTARTAMA
(3. ábra)
A lázas, neutropeniás beteg empirikus antibakteriális kezelése biztonságosan akkor függeszthető fel, ha az infekció jelei és tünetei elmúltak, és a neutropenia megszűnt (BII). Ha a beteg abszolút neutrophilszáma két alkalommal 0,5 G/l, és legalább két napja láztalan, a terápia abbahagyható. Láztalan, de tartósan neutropeniás beteg esetében a kezelést tovább kell folytatni, kivéve a kezdetben alacsony kockázati csoportba tartozó, klinikailag stabil betegeket, akiknél 5-7 nap után szekvenciális per os terápiára lehet áttérni. Nagyobb problémát jelent, ha a beteg láza 5-7 nap után sem szűnik meg. Ha időközben a neutrophilek száma 0,5 G/l fölé emelkedik, stabil állapotú betegben további 4-5 nap után az empirikus terápiát el lehet hagyni. A láz okának felderítésére (alapbetegség, nem bakteriális fertőzés, gyógyszer indukálta láz) azonban további diagnosztikus erőfeszítéseket kell tenni. A tartósan lázas és továbbra is neutropeniás beteg számára nem könnyű optimális terápiát javasolni. Kétheti kezelés után egyesek az empirikus antimikróbás terápia elhagyását ajánlják. A beteget ezt követően is szoros megfigyelés alatt kell tartani, és szükség esetén az antiinfektív kezelést haladéktalanul újra kell kezdeni. Az empirikus antibakteriális terápia folyamatát ld. 1. ábrán.
ANTIFUNGÁLIS TERÁPIA
Elhúzódó neutropeniában, különösen onkohematológiai és őssejt-transzplantált betegekesetében jelentősen megnő a gombainfekciók kialakulásának kockázata. Az invazív mycosisok döntő többségét (90%) Candida és Aspergillus speciesekokozzák, de nem elhanyagolható az u.n."emerging" gombákokozta fertőzések (fusariosis,trichosporonosis, scedosporiosis) jelentősége sem.
A gombák okozta szisztémás kórképek kezelésére növekvő számban állnak rendelkezésre antifungális gyógyszerek. Ezek hazánkban törzskönyvezett indikációit a 4. táblázatban összegezzük.
Candida infekciók
A candidákokozta fertőzésekdöntő többsége endogén eredetű, elsődleges forrásuka gyomor-béltraktus. Fluconazol profilaktikus vagy terápiás alkalmazása következtében ritkábban alakul ki véráram fertőzés, és ritkábbá váltak a C. albicansés C. tropicalis infekciók. A fluconazol kiterjedt használata ugyanakkor hozzájárul a fluconazol rezisztens vagy csökkent érzékenységű non-albicans Candida speciesek (C. krusei, C. glabrata, C. inconspicua, C. norvegensis, C. rugosa) gyakoribb izolálásához. Az intravascularis eszközök többnyire hematogén úton fertőződnek. A candidosis felismerése a klinikai jelek észlelésén, igazolása mikrobiológiai vizsgálatokon múlik. Az elváltozások etiológiáját tenyésztésre vett minta, biopsiás anyag feldolgozása tisztázhatja. Kulcsfontosságú a hemokultúra. A steril helyről kitenyészett sarjadzó gombákat a mikrobiológiai laboratórium köteles species szintig identifikálni. A species meghatározása alapján megjósolható az érzékenység, ami segítséget jelent a célzott antifungális kezelésben. Mindemellett az invazív folyamatokból izolált candidák esetében ajánlott in vitro érzékenységi vizsgálat, megfelelő, standardizált módszerekkel történő elvégzése is. Ennek előnye elsősorban az alábbi esetekben igazolható: 1. Ha az alkalmazott terápia mellett nem tapasztalható megfelelő klinikai vagy mikrobiológiai válasz (szepszis illetve infekció tüneteinek visszafejlődése, hemokultúrák sterillé válása) (A II). 2. A kiinduláskor alkalmazott terápia módosításának alátámasztására (B II). 3. Szekvenciális, orális azolterápiára való áttérés előtt (A II). Oropharyngealis candidosis, oesophagitis
Oropharyngealis candidosis rendszerint a neutropenia idején jelentkezik, de antifungális kezelésben nem részesülő betegekben az immunszupresszív kezelés következtében bármikor felléphet. Az oesophagitis rendszerint az oropharyngealis folyamat tovaterjedése, de jelentkezhet önmagában is.
Az oropharyngealis candidosis kezelésére lokálisan alkalmazott polién készítmény (amphotericin B orális szuszpenzió), vagy szisztémás hatással is rendelkező fluconazol (napi 100-200 mg) választható (B II, A I). Oesophagitis esetén nem elegendő lokális hatású szereket adni (B-II): elsősorban a 200-400 mg fluconazol i.v. vagy per os (A-I), refrakter esetben 0,3-0,7 mg/kg amphotericin B (B-II) adható infúzióban. A klinikai gyógyulást követően egy hétig illetve a neutropenia végéig kell folytatni a kezelést. Candidaemia, heveny disseminált candidosis
Candidaemia felléptével a neutropenia idején kell számolni. Az esetek egy részében a candidaemia következtében sokszervi elégtelenség tünetei jelentkeznek. Klinikai jelek alapján, instabil betegnél a candidaemia és a bacteriaemia nem különíthető el. A mikrobiológiai laboratórium jelzése az irányadó, a hemokultúrák50-90%-ban pozitívak. Heveny disseminált candidosisban érintett lehet a tüdő, kialakulhat központi idegrendszeri folyamat. Steril helyről származó mintából izolált sarjadzó gomba szintén disseminált candidosist bizonyíthat.
Az invazív candida fertőzések preemptív kezelésében az antifungális terápia kiválasztása során tekintettel kell lenni a lokális epidemiológiai viszonyokra, a szervezetet kolonizáló speciesekre, a korábban alkalmazott antifungális vegyületekre és a beteg általános állapotára.
Fluconazol csak klinikailag stabil és azol profilaxisban nem részesülő beteg esetében választható, dózisa első nap 800 mg (12 mg/kg) majd napi 400 mg (6 mg/kg) i.v. (A-I). Ha a beteg állapota stabilizálódott,a kezelés perosfluconazollalis folytatható. Egyéb esetekben az első választás caspofungin (első nap 70 mg, majd napi 50 mg i.v.) (A I) vagy amphotericin B (0,7-1 mg/kg/nap infúzióban) kell legyen. Ha az amphotericin B deoxikolát adása ellenjavallt, vagy alkalmazása során nem tolerálható mellékhatásokjelentkeznek, a szer lipidformulációira kell áttérni. Ha lehetséges, el kell távolítani az intravascularis kanülöket (B-III), különösen ha a kórokozó C. parapsilosis (A II). A vérből izolált Candida species szintű identifikálása és/vagy az in vitro érzékenység ismeretében kell dönteni a további kezelésről. A C.albicans,C. tropicalis és C. parapsilosis véráram fertőzésekegyaránt kezelhetőkamphotericin B deoxikoláttal (0.5-1 mg/kg/nap) vagy fluconazollal (12-6mg/kg/nap) (B III). C. glabrata fertőzésben csökkent amphotericin B érzékenységgel kell számolni. Azolokkal szemben e fajok szintén csökkent érzékenységűek vagy rezisztensek. A választandó terápia a fentiek értelmében caspofungin (első nap 70 mg, majd napi 50 mg i.v.) vagy 1 mg/kg amphotericin B infúzióban. Voriconazol (első nap 2x400 mg/2x6 mg/kg/, majd napi 2x200 mg /2x3 mg/kg/) i.v.
csak in vitro érzékenység meghatározás után jöhet számításba. AC. krusei fluconazol rezisztens, ezért izolálása esetén a javasolt terápia caspofungin (első nap 70 mg, majd napi 50 mg i.v.), vagy 1 mg/kg amphotericin B infúzióban. Ha az amphotericin B deoxikolát adása ellenjavallt, vagy alkalmazása során nem tolerálható mellékhatások jelentkeznek, a szer lipid formulációira kell áttérni. Az echinocandin csoport másik képviselője, az anidulafungin, jelenleg nem-neutropeniás betegek invazív candida infekcióiban törzskönyvezett szer. Bár neutropeniás betegek candidiasisában alkalmazásáról kevés adat áll rendelkezésre, regionális és nemzetközi ajánlásokban az echinocandin terápia egyik módozataként szerepel (A III - BII). Dózisa az első napon 200 mg, majd naponta 100 mg i.v. Ha a felsorolt szerekellenjavalltak, vagy nem hozzáférhetők, voriconazol (első nap 2x400 mg/2x6 mg/kg/, majd napi 2x200 mg /2x3 mg/kg/) i.v. is adható.
Amennyiben a beteg állapota megengedi és a terápia időtartama ezt szükségessé teszi, szekvenciálisan orális szer adására (fluconazol, voriconazol) át lehet térni. Erre azonban csak akkor kerülhet sor, ha az elvégzett in vitro rezisztencia vizsgálat eredménye ezt nem ellenjavallja.
A betegeta neutropenia és az infekcióra utaló tünetek megszűnése, illetve az utolsó pozitív hemokultúra után még két hétig kell kezelni (A-III).
Minden fungaemia esetén a kezelés befejezése előtt ki kell zárni endophtalmitis lehetőségét (A-II). A szemfenék vizsgálata neutropeniás betegek esetében a neutropenia elmúltával javasolt. Idült disseminált (hepato-splenicus) candidosis
A krónikus disseminált candidosis a neutropeniás időszakban fellépő fungaemia következménye. A klinikai kép a neutropenia elmúltával kerül felismerésre. Perzisztáló láz, jobb bordaívalatti fájdalom, a szérum alkalikus foszfatáz és gamma glutamilsav-transzpeptidáz szintjének emelkedettsége alapján merül fel a kórkép lehetősége. Képalkotó eljárások, CT és MRI erősíthetik meg a gyanút.
Az antifungális kezelésben figyelembe kell venni, ha rendelkezésre áll, a neutropenia alatt vérből izolált Candida spp. érzékenységét. A képalkotó eljárásokkal talált elváltozásokból végzett célzott biopsia ritkán tisztázza az etiológiát. Amphotericin Bdeoxikolát (0,5-0,7 mg/kg/nap), az amphotericin B lipid formulációi (3-5 mg/kg/nap) és a fluconazol (6 mg/kg/nap) (A-III) egyaránt adható. Súlyosabb állapotú betegek esetében megfelelő választás lehet 1-2 hétig alkalmazott caspofungin (első nap 70 mg, majd napi 50 mg i.v.), melyet per os 6 mg/kg/nap fluconazol tartós adása követ (B III).
A betegek állapota többnyire stabil. A chronicus disseminált candidosis tartós, gyakran több hónapos (egy éves) kezelést igényel. A folyamat gyógyulását az elváltozások eltűnése, vagy elmeszesedése jelzi. Ha a betegek ismételt kemoterápiára szorulnak, vagy őssejt transzplantációra kerülnek, az antifungális terápiát tovább kell folytatni a kezelés teljes időtartama alatt (A III).
Aspergillosis
Az acut invazív aspergillosis az alsó és felső légutakat érintő fonalasgomba infekció, mely főleg elhúzódóan neutropeniás, súlyos aplasticus anaemiás, allogén hemopoeticus őssejt átültetésen, solid szervtranszplantáción átesett, graft-versus-host betegségben szenvedő, corticosteroidokkal, a T-lymphocytákra ható immunszupresszív szerekkel, tumornecrosis faktor alfa antagonistákkal kezeltekben, továbbá idült tüdőbetegek valamint chronicus granulómás betegség (CGD) miatt csökkent immunitású személyek körében okoz súlyos megbetegedéseket. A hagyományos gombaellenes terápia alkalmazásával, illetve ha a háttérben álló immunhiány nem korrigálható, a következményes halálozás igen nagyarányú. Diagnózis és definíciók
A betegség fennállása kétséget kizáró módon (bizonyított invazív aspergillosis) csak invazív diagnosztika alkalmazásával, vagyis az érintett szervből, szövetből történő mintavétellel állapítható meg. A biopsia elvégzése azonban számos okból ellenjavallt lehet, vagy megvalósítását technikai korlátok hátráltathatják. Emiatt szükséges a valószínű, illetve lehetséges invazív gombabetegség (aspergillosis) fogalmának bevezetése. E kórképek definíció rendszerét 2002-ben nemzetközi munkacsoport állította össze, majd 2008-ban sor került a meghatározások átdolgozására. Ezek az információk elsősorban tudományos vizsgálatok, illetve klinikai tanulmányok céljait szolgálják, lényegük ismerete azonban elengedhetetlen az érintett betegek gyakorlati ellátásához. Adott beteg esetében mechanikus alkalmazásuk mindezek ellenére nem javasolt és nem pótolja az orvosi gondolkodást. Az alábbiakban a definíciók legfontosabb szempontjait emeljük ki:
1. Bizonyított invazív aspergillosis
a. A normálisan steril szövetből (tű)biopsiával nyert minta histológiai, cytologiai vagy direkt mikroszkópos vizsgálata során jellegzetes morfológiájú gombaelemek kimutatása a következményes szöveti károsodás jeleivel együtt. Megjegyzés: a módszer önmagában az invazivitást bizonyítja, a gomba pontos meghatározására azonban nem alkalmas. Morphologiai alapon az aspergillosis más fonalasgomba infekcióktól nem különíthető el. Ilyenkor célszerű a bizonyított invazív gombabetegség meghatározást használni (mely egyben valószínű invazív aspergillosis).
b. A fenti, normálisan steril anyagból Aspergillus spp tenyészik. Nem bizonyító erejű, ha a gomba bronchusmosó folyadékból (BAL), orrmelléküreg punctatumból vagy vizeletből nő ki. Megjegyzés: a tenyésztés önmagában a gomba jelenlétét bizonyítja, az invazivitást azonban nem.
2. Valószínű invazív aspergillosis (az alábbi kritériumok valamennyi csoportjából legalább egy -egy megléte esetén)
a. Hajlamosító tényezők
i. Neutropenia (<0,5 G/l, 10 napig) a betegséghez időben kapcsolódóan
ii. Allogén őssejt átültetés
iii. Tartós corticosteroid terápia (legalább 0,3 mg/kg/nap prednisonnal egyenértékű szer, > 3 hétig). iv.T-lymphocytákra ható immunszupresszív terápia (pl.: cyclosporin, tumornecrosis faktor alfa antagonista, specifikus monoclonalis antitestek [így pl. alemtuzumab] illetve nucleosid analóg kezelés az elmúlt 90 napban
v. Veleszületett immunhiány (CGD, súlyos kombinált immundefektus).
b. Klinikai tényezők
i. Alsólégúti betegségben az alábbi CT jelek közül legalább egy
1. Denz,jól körülírt elváltozás, halo jellel vagy anélkül
2. Légsarló jel.
3. Üregképződés
ii. Tracheobronchitisben
1. Bronchoscopiával exulceratio, nodulusok, álhártya, plakkvagy pörk a tracheában és a bronchusokban.
iii. Az orrmelléküregek érintettsége esetén: sinusitist igazoló képalkotó lelet és az alábbiak közül legalább egy
1. Lokalizált (szembe sugárzó) akut fájdalom
2. Orrnyálkahártyán fekete pörk
3. A csontos határokat áttörő folyamat
iv. Központi idegrendszeri infekcióban: az alábbiak közül legalább egy
1. Képalkotókkal igazolt fokális elváltozások
2. MR, CT: meningealis kontraszthalmozás
c. Mikológiai tényezők
i. Direkt vizsgálat (cytológia, direkt mikroszkópia vagy tenyésztés): fonalasgomba jelenléte a bronchusmosó folyadékban, bronchuskefével vett mintában, sinus aspirátumban melyet az alábbi leletek legalább egyike bizonyít
1. Gombaelemek kimutatása
2. Aspergillus spp. kitenyésztése
ii. Indirekt vizsgálatok (sejtfal alkotóelemek kimutatása)
1. Aspergillosis: galactomannan kimutatása plazmából, szérumból, BAL-ból, liquorból
2. Aspergillosis, vagy más invazív gombabetegség (kivéve cryptococcosis ill. zygomycosis): béta-D-glukán kimutatása szérumból.
3. Lehetséges invazív aspergillosis: csak a hajlamosító és a klinikai tényezők megléte állapítható meg, mikológiai bizonyíték nem áll rendelkezésre.
Az invazív aspergillosis terápiája
Bizonyított vagy valószínű invazív aspergillosis esetén a kezelés célja: lehető legkisebbre csökkenteni az infekció okozta halálozást, megelőzni a fenyegető szervkárosodásokat, javítani, illetve megőrizni az érintett beteg életének minőségét, és szükség esetén biztosítani a fennálló alapbetegség további kezelhetőségét. (5.táblázat). Toxicitás és nem megfelelő hatékonyság miatt nem javasolt az amphotericin B-deoxikolát, illetve az amphotericin B kolloid diszperzió (D-I).
A terápiára vonatkozó fontos megjegyzések:
- A gombaellenes vegyületek alkalmazása során különös figyelmet kell fordítani a mellékhatásokra, a gyógyszerkölcsönhatásokra és orális készítmény esetében a felszívódási viszonyokra. Ez utóbbi megítélésére, ha a feltételek adottak, szérum gyógyszerszint meghatározást lehet végeztetni (posaconazol, voriconazol).
- A kezelés hatékonyságát általában10-14 nap után kell megítélni. Amennyiben a neutrophil granulocyták megjelenésével párhuzamosan a tüdőinfiltrátumok radiológiai progressziója igazolódik, ez nem jelenti feltétlenül a kezelés ineffektivitását.
- A súlyos, a kezdeti terápiára nem megfelelően reagáló infekciókban az alkalmazott szer kicserélése vagy kiegészítése kínálhat megoldást. Az előbbi esetben elméletileg célszerűnek látszik olyan hatástani csoportra való áttérés, melyet a primer terápia nem tartalmazott. A gombaellenes szerek kombinációjával kapcsolatosan jó minőségű, randomizált vizsgálatokból származó evidenciák nem állnak rendelkezésre. Ugyanakkor klinikai megfigyelésekből gyűjtött adatok szólnak a módszer alkalmazhatósága mellett. Primer terápiában több antifungális szer együttes adása általában nem javasolt. Mentő kezelésként echinocandin + polién (pl. caspofungin + lipid formulációjú amphotericin B), illetve echinocandin + triazol (pl. caspofungin + voriconazol) jön számításba.
- A betegek jelentős része a kórházból való távozás után még fenntartó orális terápiát igényel. Stabil állapotú betegben, szekvenciális, fenntartó kezelés céljából per os voriconazol adható.
- Ahol erre lehetőség van, csökkenteni kell az immunszupresszív hatású szerek, különösen a corticosteroidok alkalmazását (A III).
- A kezelés ideális időtartamát pontosan nem lehet meghatározni. Általánosságban a kezelést addig kell folytatni, amíg klinikai és radiológiai regresszió következik be, a mikrobiológiai leletek (ha voltak ilyenek) negatívvá válnak, és a rizikótényezőket (ha azok befolyásolhatóak) lehetőség szerint kiküszöböltük. Ez rendszerint minimálisan 6-12 hetet vesz igénybe. Ha az immunszupresszió alkalmazására tartósan szükség van, a gombaellenes terápia folytatása a kockázatos időszak egésze során kedvezően befolyásolja a kimenetelt (A III). A kezelés során a galactomannan antigenaemia mértékének alakulásából következtetni lehet a folyamat gyógyhajlamára.
- Alsólégúti aspergillosisban tüdőműtét indikációját képezi: a/ a jelentős haemoptoe (10%-ban fordul elő), b/ a diagnosztikus mintavétel szükségessége, c/ relapsus megelőzése immunszupresszió/kemoterápia/transzplantáció előtt, d/ vérzés profilaxis, amennyiben a képalkotó vizsgálatok nagy érképlet érintettségét valószínűsítik. e/ a pericardiumra, mellkasfalra terjedő infekció vagyempyema.
- Az orrmelléküregek és a központi idegrendszer betegségeiben a műtét általában javasolt. Annak kockázatát, technikai elvégezhetőségét, a betegre vonatkozóan a kockázat (pl. vérzés) és hasznon arányát egyedileg kell mérlegelni.
Empirikus antifungális kezelés
Ha megfelelő antibakteriális kezelés ellenére a lázas neutropenia > 72-96 órája fennáll, számos centrumban empirikus amphotericin B deoxikolát terápiát alkalmaznak. Ez a gyakorlat az 1980-as években, kisszámú betegcsoporton végzett tanulmányok eredményére támaszkodik. Az azóta eltelt évtizedek tapasztalatai megmutatták, hogy a kezelés során a betegek jelentős része indokolatlanul kap amphotericin B. A vegyület mellékhatásai ugyanakkor kedvezőtlenül befolyásolják az életminőséget, a kezelés kimenetelét és a költségeket. A későbbiekben az ellentmondás feloldására az ún. preemptív gombaellenes terápia kínált megoldást. Ez a gyakorlatban az immunstatus és klinikai kép folyamatos követése mellett első sorban a szérum galactomannan rendszeres (hetente két alkalommal történő) meghatározását és nagy felbontóképességű mellkas CT vizsgálat elvégzését, a lelet pozitívvá válása esetén pedig haladéktalanul Aspergillus spp-szel szemben is hatékony terápiát jelent. A kérdést számottevően befolyásolták azok a klinikai vizsgálatok, melyekben kevésbé toxikus szerek hatékonyságát igazoltak az elhúzódó lázas neutropenia empirikus antifungális terápiájában. Főként a liposzómális amphotericin B és a caspofungin alkalmazhatósága nyert bizonyítást. Nemzetközi ajánlásokban az amphotericin B egyéb lipid formulációi és a voriconazol is megtalálhatóak. Mindezek értelmében jelenleg célszerű, ha a kockázati tényezők elemzése után, a kezelés nyújtotta előnyök és a lehetséges mellékhatások értékelése után az adott centrumok döntenek a preemptiv vagy az empirikus módszer előnyben részesítéséről. Általánosságban megfogalmazhatjuk, hogy a csökkent immunitású betegben a kifejlődőben lévő invazív mycosist ismételt képalkotó, mikrobiológiai és egyéb kiegészítő vizsgálatokkal rendszerint időben fel lehet ismerni. Empirikus antifungális kezelés - mindezek ellenére - indokolt lehet az alábbi esetekben: a/ kiemelkedő kockázatú betegcsoportokban (acut leukaemia indukciós kezelése, allogén őssejt átültetés, magas fokú GVHD, rezisztens vagy relabáló malignus betegség), b/ olyan centrumokban, ahol invazív aspergillosis időszakosan vagy rendszeresen nagygyakorisággal fordul elő.
Alkalmazható szerek: amphotericin B deoxikolát (B I, veseelégtelenség veszélye esetén azonban ellenjavallt : D I), caspofungin (A I), liposzómális amphotericinB(AI).
EGYÉB EMPIRIKUS INFEKCIÓELLENI KEZELÉS
Neutropenia önmagában, ép T-sejtes immunválasz esetén, nem jelent fokozott hajlamot vírusok és paraziták okozta fertőzések kialakulására. Lázas neutropeniában e kórokozó csoportokra ható terápia alkalmazása ezért csak megfelelő bizonyítékok birtokában indokolt.
A NEUTROPENIÁS INFEKCIÓK MEGELŐZÉSE
Általános profilaxis
A neutropeniás beteg számára, kórházi kezelése során, protektív környezetet kell biztosítani. A neutropenia időtartamára a beteget olyan (optimális esetben egyágyas) kórteremben kell elhelyezni, ahol az esetlegesen betegről betegre átvihető kórokozók terjedésének veszélye minimálisra csökkenthető. Számára, a megfelelő nemzetközi ajánlások figyelembe vétele mellett, standard neutropeniás étrendet kell előírni. A nagy kockázatú beteg spóraszegény levegőjű kórteremben való elhelyezése (HEPA filter alkalmazása) csökkentheti az invazív aspergillosis kialakulásának rizikóját. Amennyiben a gyógyintézményen belül, vagy annak közvetlen környezetében építkezésbe kezdenek, külön intézkedési terv keretében gondoskodni kell a betegek fokozott védelméről (szorosabb kórházi infekció kontroll, az épületrész izolálása, szükség esetén a centrum számára átmenetileg újműködési hely kijelölése). A kórházi infekciókat okozó baktérium és gomba speciesek körében egyre nagyobb gyakorisággal találkozhatunk az antimikróbás szerekkel szemben csökkent érzékenységű patogénekkel, Ugyanakkor a károsodott immunitású betegcsoportok ellátása során jelenleg elkerülhetetlennek látszik az antibiotikumok és gombaellenes szerek kiterjedt és tartós használata. A kockázatelemzés és a diagnosztika módszereinek alkalmazásával mindent meg kell tenni e szelekciós nyomás csökkentése érdekében. Mindezek mellett az epidemiológiai folyamatok monitorozásának és a probléma kórokozókáltal létrehozott infekciók megelőzésének leghatékonyabb eszköze az infekció kontroll rendszer, melynek minden neutropeniás betegek kezelésével foglalkozó intézményben folyamatosan, szervezetten és aktívan működnie kell.
Antimikróbás profilaxis
A neutropenia idején alkalmazott antibakteriális profilaxis ellentmondásos: alkalmazásával csökkenthető a Gram-negatív és részben a Gram-pozitív baktériumok okozta véráram infekciók gyakorisága, a lázas epizódok aránya, az empirikusan adott antibiotikumok felhasználása és a halálozás (A-I). Ugyanakkor rezisztens törzsek szelektálódásának veszélye fenyeget. Nagy kockázatú betegekben, különösen, ha a neutropenia várható időtartama meghaladja a 7 napot napi 2 x 500 mg ciprofloxacin p.o., vagy 1 x 500 mg levofloxacin p.o. profilaktikus alkalmazása javasolt. A profilaxist a neutropenia megszűnéséig, vagy az empirikus antimikróbás terápia megkezdéséig kell folytatni. A profilaxis hatékonyságát rendszeresen monitorozni kell. Ez a véráram infekciók gyakoriságának nyomon követését és azok következményeinek klinikai megfigyelését (lázas epizódok, halálozás, parenterális antibiotikum felhasználás) jelenti. Az izolált törzsek antibiotikum rezisztenciájának alakulását figyelemmel kell kísérni, nemcsak a fluorokinolon rezisztencia, hanem más multirezisztens (ESBL termelő Gram-negatívok, MRSA) kórokozókelőfordulása tekintetében is. A kitűzött célok elérése érdekében infekció kontroll rendszert kell működtetni. Főleg Gram-pozitív baktériumokra ható szerek (különösen vancomycin) profilaktikus adása nem ajánlott. Az antifungális profilaxis hatékonysága elsősorban a Candida fertőzések megelőzésében bizonyított. Acut leukaemia nagydózisú kemoterápiás kezelése (C-I), valamint őssejt átültetés során (A-I) napi 200-400 mg fluconazol csökkenti a felszínes és invazív candidosisok előfordulási gyakoriságát A fluconazol profilaxis kedvezőtlen következménye a fluconazol rezisztens non-albicans Candida speciesek megjelenése a surveillance kultúrákban, elsősorban a székletben. Az invazív aspergillosis incidenciájának növekedtével szükségessé vált az antifungális profilaxis spektrumának szélesítése. Randomizált klinikai tanulmányban igazolták, hogy a posaconazol 3x200 mg p.o.. napi adagolás mellett szignifikánsan csökkenti az invazív mycosisok és ezen belül az invazív aspergillosis incidenciáját a hagyományos azol profilaxishoz képest,acut myeloid leukaemiában illetve myelodysplasiában szenvedő betegekben. Mindezek értelmében fokozott kockázat esetén napi 200-400 mg fluconazolt i.v./p.o. javasolunk. Ha a centrumban magas az invazív aspergillosis előfordulási gyakorisága (~10%), ha környezeti faktorok növelik az infekció kialakulásának veszélyét (építkezés), illetve ha a betegnél allogén őssejt átültetés tervezett, mérlegelni kell posaconazol 3x200 mg p.o.. profilaktikus adásának lehetőségét.
Ha a beteg anamnézisében invazív gombainfekció, különösen aspergillosis szerepel, a tervezett újabb neutropeniát okozó terápia illetve immunszupresszív kezelés során másodlagos profilaxis alkalmazása ajánlatos. Az optimális gombaellenes szer kiválasztásához evidenciák nem állnak rendelkezésre. A hatásspektrum és a tolerálhatóság figyelembe vételével elsősorban voriconazol, posaconazol, alternatívaként caspofungin vagy lipid formulációjú amphotericin B jöhet számításba.
Neutropeniás betegek rutinszerű antivirális profilaxisát nem javasoljuk.
KIEGÉSZÍTŐ TERÁPIÁS LEHETŐSÉGEK A NEUTROPENIAS BETEGEK INFEKCIÓINAK KEZELÉSÉBEN ÉS MEGELŐZÉSÉBEN
Mind a megjelent nemzetközi ajánlásokban, mind a klinikai gyakorlatban eltérő megközelítésekkel találkozhatunk a myeloid növekedési faktorok, a granulocyta transzfúzió és az intravénás immunglobulin készítmények használatára vonatkozóan.
Myeloid hemopoeticus növekedési faktor (granulocyta kolóniastimuláló faktor [G-CSF, pegilált G-CSF]) kemoterápiás kezelést követő, profilaktikus adása indokolt lehet, ha az alkalmazott protokoll mellett a lázas neutropenia kialakulásának kockázata =20%. Mérlegelhető G-CSF alkalmazása 10-20% közötti rizikó esetén is, ha a neutropeniás infekció kialakulásának kockázatát egyéb tényezők (pl. idős kor, műtét utáni állapot, csökkent csontvelői tartalék) növelik. A már kialakult infekció intervenciós kezelésében G-CSF adásának előnyeit nem bizonyították. Alkalmazását ennek ellenére a granulocyták visszatérésének gyorsítása érdekében mérlegelni lehet, ha a neutropeniás betegben pneumonia, szepszis, invazív mycosis vagy egyéb súlyos, progresszív fertőzés alakult ki.
Granulocyta transzfúzió profilaktikus és terápiás adása - megfelelő evidencia híján - továbbra is experimentális kezelésnek tekinthető, ezért alkalmazásának módját és körét tekintve ajánlás nem fogalmazható meg. Intravénás immunglobulin rutinszerű adása neutropeniás infekciókban nem javasolt. Használata megfontolható jelentősen hypogammaglobulinaemiás betegek súlyos infekcióiban.
1. táblázat
Lázas neutropeniában szükséges vizsgálatok
| Vizsgálat | Feltétel |
| Fizikális vizsgálat | Minden esetben |
| Mennyiségi és minőségi vérkép | Minden esetben |
| Szérum kreatinin, karbamid nitrogén, transzaminázok | Minden esetben |
| Hemokultúra (kétszer, perifériás vénából +/- centrális vénás kanül valamennyi lumenéből) | Minden esetben |
| Kanülkörnyék leoltása + Gram festés | Kanülinfekció gyanúja esetén |
| Vizelettenyésztés | Klinikai tünetek esetén |
| Széklettenyésztés (enterális patogén baktériumok) | Területen szerzett hasmenés, kórházi járvány gyanúja esetén |
| Széklet Clostridium difficile toxin kimutatás | Klinikai gyanú esetén |
| Széklet protozoon | Egy hétnél hosszabb hasmenés esetén |
| Liquor vizsgálat | Klinikai tünetek esetén |
| Bőrléziók aspirációja/biopsziája | Klinikai tünetek esetén |
| Mellkas rtg. | Minden esetben |
| Mikrobiológiai mintavétel, biopszia egyéb anatómiai régióból | A területet érintő infekcióra utaló klinikai tünetek esetén |
| Nagy felbontóképességű mellkasi CT | > 5 napig tartó lázas neutropeniában ill. pulmonalis mycosis gyanújakor |
| Surveillance mikrobiológiai vizsgálatok (orrváladék, garatváladék, rectalis leoltás) | Infekció kontroll céljából (MRSA, VRE, rezisztens Gram-negatív törzs okozta kolonizáció) |
2. táblázat
Empirikus, parenterális antibiotikum terápia lázas neutropeniában
| Csoport | Vegyületek | Megjegyzés |
| Monoterápia | ceftazidim VAGY cefepim VAGY imipenem-cilasztatin VAGY meropenem VAGY piperacillin-tazobactam | A ceftazidim G+ törzsek elleni hatékonysága csekély. |
| Glikopeptid tartalmú kombináció | mint a monoterápiánál PLUSZ vancomycin VAGY teicoplanin | Indikációi: 1.Lágyrész- ill. kanül-infekció. 2.Kolonizáció rezisztens G+ baktériummal (pl. MRSA). 3.Hemokultúrában G+ baktérium, identifikálás folyamatban. 4.Hipotenzió. |
3.táblázat
Pontrendszer a felnőtt, lázas neutropeniás betegek kockázati tényezőinek jellemzésére (MASCC pontrendszer)
| Jellemzők | Pont | |
| Tünetek súlyossága (csak egy választható) | tünetmentes | 5 |
| enyhe tünetek | 5 | |
| súlyos tünetek | 3 | |
| Nincs hypotensio | 5 | |
| Nincs chronicus obstructiv tüdőbetegség | 4 | |
| Alapbetegség: szolid tumor. Hematologiai alapbetegség esetén: az előzményben nincs invazív gombainfekció | 4 | |
| Nincs dehidrált állapot | 3 | |
| A láz kezdetén a beteg nem fekszik kórházban | 3 | |
| Életkor < 60 év | 2 | |
Értékelés: > 21 pontszám esetén a beteg szövődmények tekintetében a kis kockázati csoportba tartozik. Megjegyzés: Ld. a szövegben a FIGYELMEZTETÉS-t.
4. táblázat
A Magyarországon forgalomban lévő, invazív mycosisokban adható gombaellenes szerek törzskönyvezett indikációi
| Vegyület | Indikáció |
| Fluconazol | Invazív candidiasis, candidaemia, (már gyanújelek alapján is adható). Invazív cryptococcosis. Gombainfekciók megelőzése (kemoterápia, radioterápia mellett). |
| Itraconazol * | Aspergillosis *. Candidiasis *. Cryptococcosis *. |
| Voriconazol | Invazív aspergillosis. Candidiaemia (csak nem-neutropeniás beteg). Scedosporium spp, Fusarium spp. okozta invazív mycosis. |
| Posaconazol | Invazív aspergillosis (amphotericin B-re vagy itraconazolra rezisztens vagy ezeket nem toleráló betegek, másodvonalbeli kezelés.) Fusarium spp. okozta invazív mycosis (amphotericin B-re rezisztens vagy azt nem toleráló betegek, másodvonalbeli kezelés.) Invazív gombainfekciók megelőzése (akut myeloid leukaemia, myelodysplasia, hemopoetikus őssejt átültetés esetén). |
| Amphotericin B (deoxikolát) | Invazív infekciók általában, ezen belül: aspergillosis, candidiasis, cryptococcosis, mucormycosis. Lázas neutropeniában empirikus gombaellenes kezelés céljából. |
| Amphotericin B (liposzómális) | Invazív infekciók általában, köztük candidiasis, cryptococcosis. mucormycosis (ha a deoxikolát formuláció adása kockázatos vagy nem tolerálható). Lázas neutropeniában empirikus gombaellenes kezelés céljából. |
| Amphotericin B (kolloid diszperzió) | Invazív infekciók általában, különösen: aspergillosis, candidiasis. Ha a beteg a deoxikolát formulációt nem tolerálja. Lázas neutropeniában empirikus gombaellenes kezelés céljából. |
| Amphotericin B (lipid komplex) | Első vonalban: invazív candidiasis. Második vonalban: invazív gombainfekciók, ha a deoxikolát formuláció nem elég hatékony, vagy toxicitás miatt ellenjavallt. Második vonalban: invazív aspergillosis, cryptococcosis. |
| Caspofungin | Invazív candidiasis. Második vonalban: invazív aspergillosis (ha a beteg amphotericin B formulációkra vagy itraconazolra nem reagál, vagy ezeket nem tolerálja). Lázas neutropeniában empirikus gombaellenes kezelés céljából. |
| Anidulafungin | Candidaemia (nem-neutropeniás betegek). |
*Az itraconazol kapszulás kiszerelésben, változó biohasznosulása miatt, akut invazív gombainfekciók kezelésére nem javasolt!
5.táblázat
Az invazív aspergillosis terápiája
| Kórkép | Terápia | Alternativa |
| Inavasiv pulmonalis aspergillosis (bizonyított illetve valószínű) | voriconazol (1. nap: 2x6 mg/kg i.v. majd 2x4 mg/kg/nap i.v./p.o.) (A I) | liposzómális amphotericin B, 3-5 mg/kg/nap, infúzióban (A I) |
| Inavasiv pulmonalis aspergillosis, ha a primer terápia hatástalan illetve azt a beteg nem tolerálja | caspofungin (1. nap 70 mg/nap majd 50 mg/nap), infúzióban (B-II), vagy posaconazol 4x200 mg p.o.. (B II), vagy amphotericin B lipid formuláció 3-5 mg/kg (B II) | antifungális kombináció (B II) |
| Heveny orrmelléküreg aspergillosis | Mint fent + műtét | Mint fent + műtét |
| Központi idegrendszeri aspergillosis | Mint fent + műtét | Mint fent + műtét |
Az egyes szerek alkalmazásának részleteit és korlátait ld. a szövegben ! 1.ábra.
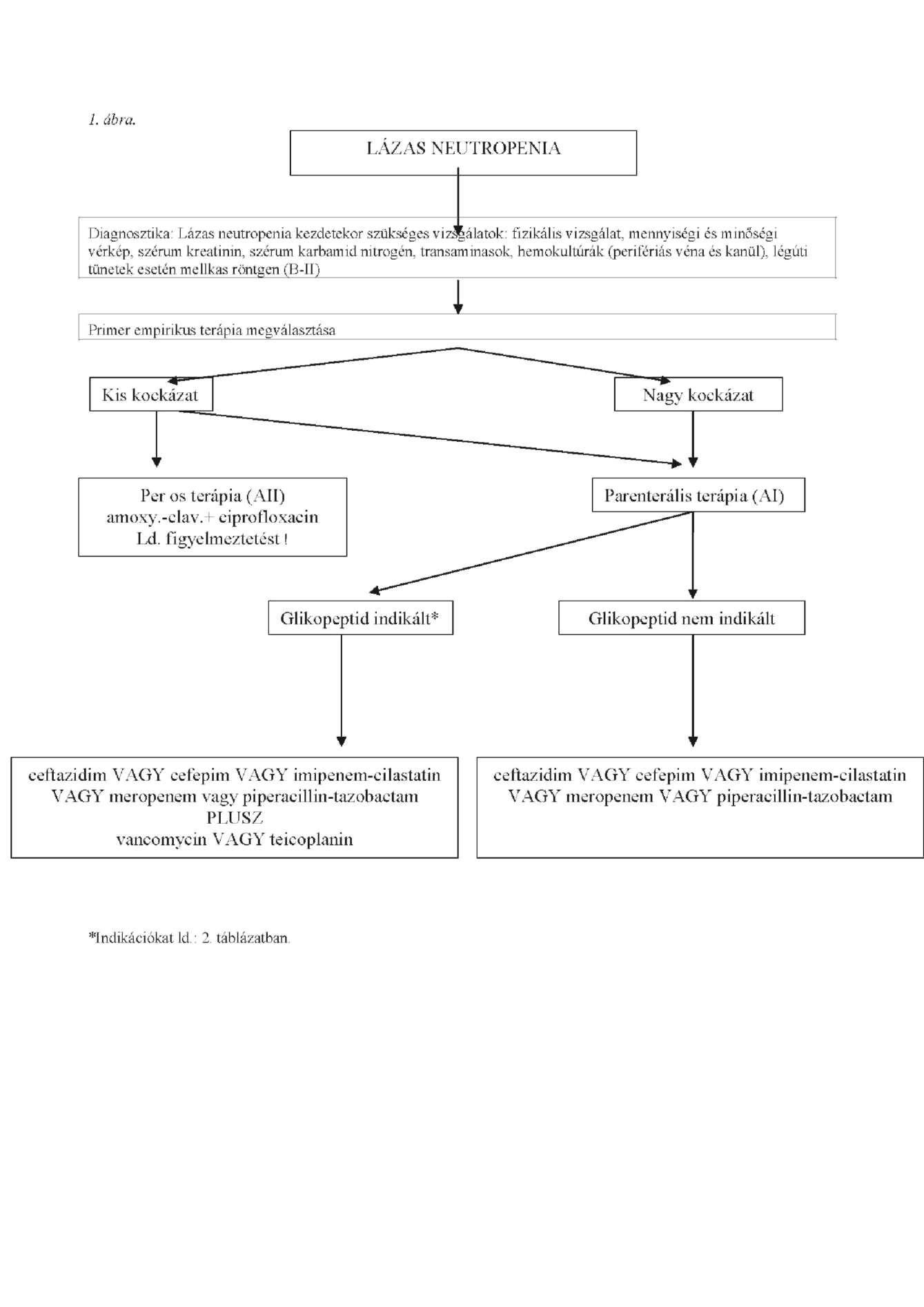

3. ábra
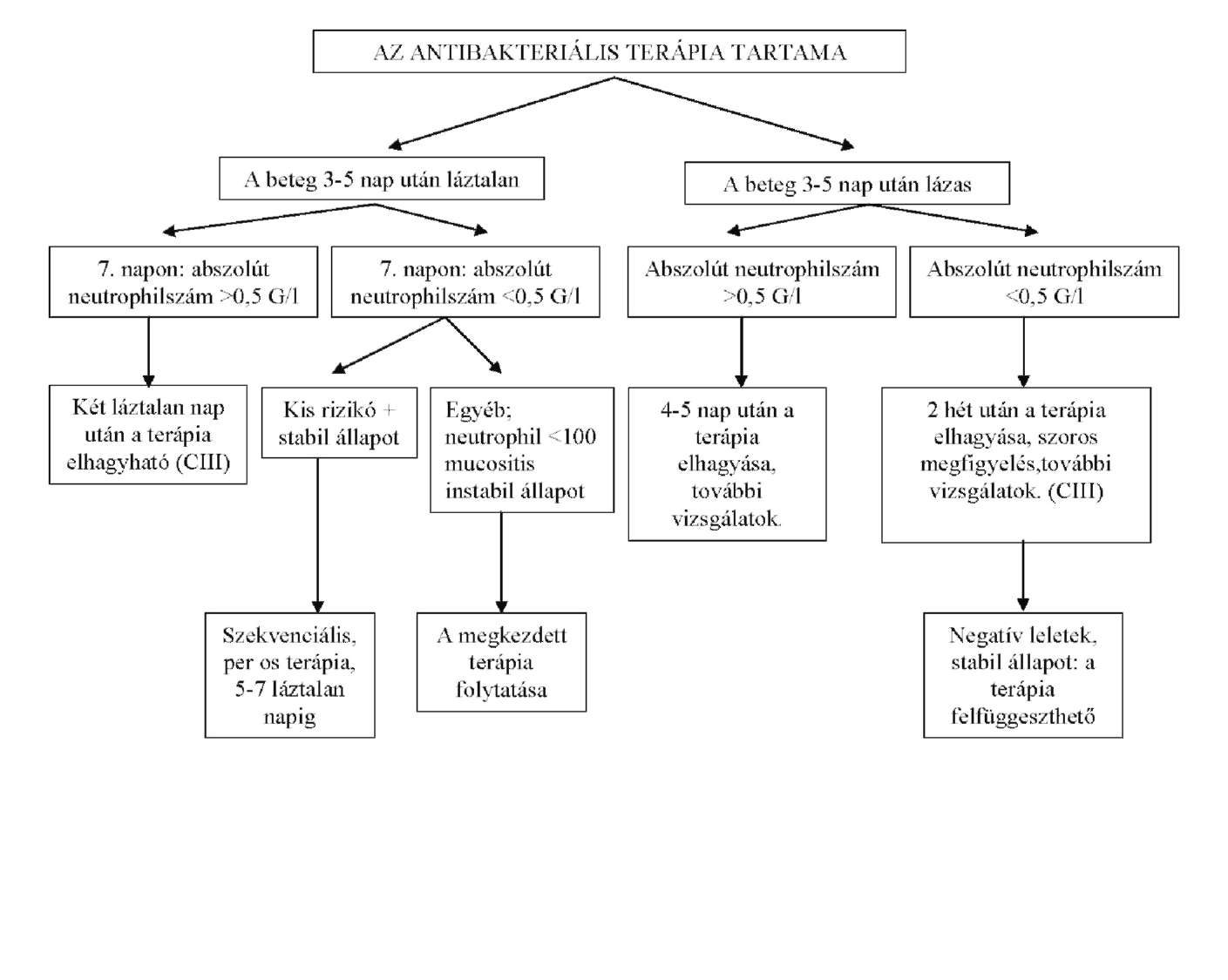
Irodalomjegyzék
1. Hughes WT, Armstrong D, Bodey GP et al: 2002 guidelines for the use of antimicrobial agents in neutropenic patients with cancer. Clin Infect Dis 2002;34:730-51.
2. Prevention and treatment of cancer-related infections. In: National Comprehensive Cancer Network ® NCCN Clinical Practice Guidelines in Oncology TM . (Co-chairs: Segal BH, Baden LR.) 2008.V.1, www.nccn.org.
3. Bucaneve G, Castagnole E, Viscoli C et al.: Quinolone prophylaxis for bacterial infections in afebrile high-risk neutropenic patients. Eur J Cancer 2007;Suppl.5:7-12.
4. Drgona L, Paul M, Bucaneve G et al.: The need for aminoglycosides in combination with betalactams for high-risk, febrile neutropaenic patients with leukaemia. Eur J Cancer 2007;Suppl.5:13-22.
5. Marchetti O, Cordonnier C, Calandra T: Empirical antifungal therapy in neutrpaenic cancer patients with persistent fever. Eur J Cancer 2007;Suppl.5:32-42.
6. Maertens JA, Frére P, Lass-Flörl C et al.: Primary antifungal prophylaxis in leukaemia patients. Eur J Cancer 2007;Suppl.5:43-48.
7. Herbrecht R, Flückinger U, Gachot B et al.: Treatment of invasive Candida and invasive Aspergillus infections in adult haematological patients. Eur J Cancer 2007;Suppl.5:49-59.
8. Cordonnier C, Pautas C, Maury S et al.: Empirical versu preemptive antifungal therapy for high-risk, febrile, neutropenic patients: a randomized, controlled trial. Clin Infect Dis 2009;48:1042-51.
9. Sinkó J, Ludwig E, Nikolova R, Masszi T, Prinz Gy, Rókusz L, Sréter L, Tímár L: A neutropenias beteg fertőzéseinek megelőzése és kezelése. Az Infektológiai Szakmai Kollégium és a Transzfúziológiai és Hematológiai Szakmai Kollégium közös szakmai protokollja. In: Útmutató, Klinikai Irányelvek Kézikönyve,Infektológia Medition Budapest,2007.nov:165-177.
10. Sinkó J, Ludwig E, Masszi T, Prinz Gy, Rókusz L, Sréter L, Tímár L: A neutropeniás beteg fertőzéseinek megelőzése és kezelése. Az Infektológiai Szakmai Kollégium és a Transzfúziológiai és Hematológiai Szakmai Kollégium közös szakmai protokollja. In: Hematológiai betegségek kezelésének módszertana. (Szerk: Lehoczky D) Documed, Budapest, 2004, 161-9.
11. De Pauw BE, Walsh TJ, Donnelly JP et al.: Revised definitions of invasive fungal disease from the European Organization for Research and Treatment of Cancer/Invasive Fungal Infections Cooperative Group and the National Institute of Allergy and Infectious Diseases Mycoses Study Group (EORTC/MSG) ConsensusGroup. Clin Infect Dis 2008;46:1813-21.
12. Ascioglu S, Rex JH, de Pauw BE et al: Defining opportunistic invazíve fungal infections in immunocompromised patients with cancer and hematopoietic stem cell transplants: an international consensus. Clin Infect Dis 2002;34:7-14.
13. Pappas PG, Kauffman CA" Andes D et al: Clinical practice guidelines for the management of candidiasis: 2009 update by the Infectious Diseases Society of America. Clin Infect Dis 2009;48:503-35.
14. Walsh TJ, Anaissie EJ, Denning DW et al:Tretment of Aspergillosis: clinical practice guidelines of the Infectious Diseases Society of America. Clin Infect Dis 2008;46:327-60.
A szakmai protokoll érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai irányelve
A praeimplantatiós genetikai diagnosztikól
Készítette: a Klinikai Genetikai Szakmai Kollégium és a Humán Reprodukciós Bizottság
I. A PGD meghatározása
A praenatalis diagnosztika alkalmazásával lehetővé vált, hogy azoknál a szülőknél, akiknél a gyermekvállalás során magas a genetikai kockázat, megelőzhető legyen a beteg utód születése. A praeimplantatiós genetikai diagnosztika (PGD) a praenatalis diagnosztika legkorábbi formája,a beágyazódás előtti preembrió (előébrény) genetikai vizsgálatát jelenti, amire a megtermékenyüléstől a blastocysta (hólyagcsíra) állapot eléréséig van lehetőség.
A módszer alkalmazása a jelenleg általánosan elfogadott álláspont szerint azon házaspárok esetében merül fel, akik utódainál monogénesen öröklődő betegség, illetve kiegyensúlyozatlan strukturális kromoszóma rendellenesség fokozott kockázata áll fenn, és akik spontán fogant terhesség esetében, praenatalis diagnosztikával igazolt beteg magzat esetén, a terhességmegszakítás gondolatát vallási, erkölcsi vagy egyéb ok miatt nem tudják elfogadni. Az eljárás során a szervezeten kívül megtermékenyítés útján a petesejtből, vagy az abból fejlődő preembrióból, mikromanipulátor segítségével az egyik, vagy mindkét sarkitestet, vagy a későbbi osztódás során néhány sejtet eltávolítunk úgy, hogy eközben a petesejt vagy a preembrió életképessége nem károsodik. Az eltávolított sarkitestekből vagy embrionális sejtekből molekuláris genetikai / molekuláris cytogenetikai vizsgálattal megállapítható, hogy mely előébrények érintettek egy adott genetikai betegségben. A vizsgálat eredménye alapján lehetőség nyílik arra, hogy a vizsgált tulajdonság szempontjából egészséges preembriót ültessük be az anya méhébe, a betegséget hordozó preembriók pedig megsemmisítésre kerülnek. A PGD megvalósulásához az in vitro fertilizáció területén alkalmazott mikromanipuláció, illetve a molekuláris genetikai vizsgálatok fejlődése teremtette meg a lehetőséget.
1. A beágyazódás előtti genetikai vizsgálatok csoportosítása azok javallata alapján
Az ivarsejteken és beágyazódás előtti preembriókon elvégezhető genetikai vizsgálatoknak számos formája létezik, amelyek között célszerű -azok indikációja alapján- az alábbiak szerint különbséget tenni:
1.1 Praeimplantatiós genetikai diagnosztika (PGD)
A PGD eljárás azon betegeknél kerülhet alkalmazásra, akiknél magas kockázat áll fenn arra, hogy születendő gyermeküknek olyan genetikai rendellenességet örökítsenek át, amely jelentősen csökkenti a születendő gyermek életkilátásait vagy életminőségét (=magas kockázatú PGD). A PGD javallatát képező betegség lehet génmutáció (autoszomális recesszív, autoszomális domináns vagy X kromoszómához kötött) vagy kiegyensúlyozott strukturális kromoszóma rendellenesség következménye.
1.2 Praeimplantatiós genetikai szűrés (PGS)
PGS eljárásról (=alacsony kockázatú PGD) akkor beszélünk, ha az eljárást kérő házaspárnál nem igazolható a PGD eljárásnál korábban említett, az életkilátást vagy életminőséget jelentősen csökkentő örökletes betegség előfordulásának magas kockázata. A vizsgálni (szűrni) kívánt rendellenesség előfordulásának valószínűsége alacsony, általában nem haladja meg az 1-2%-ot (pl. kromoszóma rendellenességek előfordulásának gyakorisága magas anyai életkor esetén). Javallata az egészségügy számos területén felmerülhet, jelenleg az alábbi esetekben számoltak be a módszer alkalmazásáról: Aneuploidia szűrés
A spontán fogant, illetve IVF módszerrel fogant preembriók jelentős hányada aneuploidiát mutat. Ezen preembriók beültetése az IVF-ET kezelések során a beágyazódás elmaradásához, illetve spontán vetéléshez vezethet. Kísérletek folynak bizonyos betegcsoportok esetében (pl. magas anyai életkor, többszöri sikertelen IVF-ET kezelés) az IVF eljárással létrehozott preembriók rutinszerű aneuploidia-szűrésének bevezetésére, melynek remélt célja az IVF eljárás eredményességének javítása. Ennek során azok a praembriók, amelyekben aneuploidia mutatható ki, nem kerülnek beültetésre. A módszer hatékonysága jelenleg vizsgálati stádiumban van, meggyőző bizonyítékok hiányában széleskörű alkalmazása egyelőre nem ajánlott. Prediktív genetikai tesztelés
Az alkalmazás speciális területe a poligénesen meghatározott genetikai hajlam vizsgálatára végzett prediktív genetikai tesztelés. Így pl. Alzheimer betegség kockázata miatt ApoE genotipizálást végeztek, amely után az E4 allélt hordozó preembriók nem kerültek beültetésre. Hasonlóképpen végeztek vizsgálatokat haemochromatosis és örökletes emlőrák (BRCA I, II; Brest cancer type I, II) génjeinek prediktív diagnosztikája céljából. A módszer etikai szempontból vitatható, ezért széleskörű alkalmazása nem javasolt.
1.3 HLA-tipizálás
Vitatott, de technikailag kivitelezhető alkalmazási terület a csontvelőátültetésre váró beteg gyermekszámára történő HLA-kompatibilis donor testvér biztosítása (HLA-tipizálás). Az eljárás során, a szervezeten kívül megtermékenyítés útján létrejött preembriók genetikai vizsgálatát követően azok kerülnek beültetésre, amelyek immunológiai
tulajdonságai hasonlítanak a beteg gyermekéhez, így a születendő gyermek donorként szolgálhat (elsősorban haemopoetikus őssejtek tekintetében) a beteg gyermekgyógyításához. A módszer hatékonysága jelenleg vizsgálati stádiumban van, meggyőző bizonyítékok hiányában, valamint alkalmazásával szemben felmerülő etikai kifogások miatt klinikai alkalmazása egyelőre nem ajánlott.
2. A PGD (PGS) eljárások során vizsgálható minta
A PGD (PGS) eljárások során ivarsejtekből, megtermékenyült petesejtből és beágyazódás előtti preembrióból származó genetikai minta vizsgálatára nyílik lehetőség az alábbi csoportosítás szerint:
2.1 Ivarsejtek genetikai vizsgálata (praeconceptionális genetikai diagnosztika)
A praenatális genetikai vizsgálatok legkorábbi formája, amely a megtermékenyítés előtti ivarsejtek genetikai vizsgálatát és a vizsgálati eredmény alapján történő szelekcióját jelenti. Hímivarsejtek genetikai vizsgálata
Kutatási eredmények alapján lehetőség van a hímivarsejtek genetikai vizsgálatára, valamint X és Y kromoszóma szerinti különválasztására. A módszer jelenleg kutatási stádiumban van. Klinikai gyakorlatban történő alkalmazása egyelőre nem ajánlott.. Petesejtek genetikai vizsgálata
A petesejtek megtermékenyítés előtti genetikai vizsgálatára az első sarki test eltávolításával és genetikai vizsgálatával nyílik lehetőség. Mivel az eljárást általában a PGD más formáival együtt alkalmazzák (második sarki test vagy blastomera vizsgálata), ezért ezt a PGD egyéb módszereivel együtt tárgyaljuk.
2.2 Beágyazódás előtti preembriók genetikai vizsgálata Sarki test biopszia
Megtermékenyült petesejt (zygota) első és második sarki testének vizsgálata. Az első sarkitest biopsziájára a petesejtnyerés napján, a megtermékenyítésig van lehetőség. A második sarkitest biopsziája a megtermékenyítést követő 18-22 óra között végezhető.
Ekkor az első és második sarkitest egyszerre is eltávolítható, azonban előfordulhat, hogy az első sarkitest ebben az időpontban már degenerálódott. A sarkitest biopszia eredményeiről csak korlátozottan állnak rendelkezésünkre adatok, a módszer alkalmazhatóságának azonban számos korlátja ismert, ezért rutinszerű alkalmazása nem javasolt. Blastomera biopszia
Az osztódó preembrió sejtjeinek a vizsgálata. A PGD eljárások során a leginkább ajánlott módszer, amely az osztódó, 4-10 sejtes állapotú preembrió 1 vagy 2 sejtjének eltávolítását jelenti a megtermékenyítést követő 2. vagy 3. napon. Trophectoderma biopszia
Hólyagcsíra (blastocysta) fejlődési állapotú preembrió trophectoderma sejtjeinek a vizsgálata . A megtermékenyítést követő 5. vagy 6. napon végezhető. A blasztociszta stádiumú preembrió trophectoderma sejtrétegéből történő mintavételt jelenti. A módszer előnye, hogy több sejt áll rendelkezésre a genetikai vizsgálathoz, azonban megbízhatóságáról csak korlátozottan állnak rendelkezésünkre adatok, ezért rutinszerű alkalmazása nem javasolt.
II. A PGD módszerei
1. Szervezeten kívüli megtermékenyítés
A vizsgálandó előébrények (preembriók) "létrehozása" hormonális petefészekstimulációt követően, ultrahang ellenőrzéssel végzett tüszőpunkcióval (petesejtnyeréssel) és szervezeten kívüli megtermékenyítéssel (in vitro fertilisatióval, IVF) történik.
2. A vizsgálandó minta gyűjtése:
A lehetséges mintavételi eljárások közül a PGD-vel foglalkozó laboratóriumokban leginkább a megtermékenyítést követő 2-3. napon végzett blastomera biopsia terjedt el, ezért a továbbiakban csak ennek az eljárásnak a módszereit ismertetjük. Az biopszia során a 4-10 sejtes előébrényből 1-2 sejtet (blastomerát) távolítunk el. Mivel a PGD során alkalmazott genetikai vizsgálati módszerek rendkívül érzékenyek, a vizsgálandó minta nem tartalmazhat semmilyen egyéb, nem az előébrényből származó sejtet (kontamináció), mert az megváltoztathatja a genetikai vizsgálat eredményét. Ezért a vizsgálatot megelőzően, főleg PCR módszer alkalmazása esetén, célszerű a petesejteket intracytoplasmaticus spermium injectioval (ICSI) megtermékenyíteni, így elkerülhető, hogy az esetleg a preembrióhoz tapadó hímivarsejtek bekerüljenek a genetikai vizsgálatra szánt mintába, meghamisítva ezzel annak eredményét. Gondot kell fordítani arra, hogy a megtermékenyítést megelőzően a petesejtet körülvevő cumulus sejteket maradéktalanul eltávolítsuk a zona pellucidáról.
A biopsziát mikromanipulátorral felszerelt mikroszkóp segítségével végezzük. A beavatkozás első lépéseként az előébrényt a mikromanipulátor tartókapillárisa segítségével rögzítjük. Ezt követi az előébrény külső burka, a zona pellucida megnyitása. Erre többféle technikai lehetőség van. A mechanikai úton végzett zona megnyitás a legkevésbé elterjedt módszer. Ekkora petesejt burkán egy vékony, hegyes üvegkapilláris segítségével ejtünk metszést úgy, hogy azon az előébrény egy-két sejtjét ki tudjuk emelni. A kémia úton végzett zona megnyitás során egy vékony üvegkapillárissal kis mennyiségű savas oldatot fecskendezünk az előébrény burkára, amely egy kis területen feloldja annak anyagát. Ezenkívül lézersugár segítségével is lehetőség van arra, hogy a blastomerák kiemeléséhez megfelelő méretű nyílást készítsünk az előébrény külső burkán.
Ezt követően a sejtek átmérőjénél valamivel kisebb biopszia pipettával a zona pellucidán készített nyíláson keresztül megközelítjük a kiválasztott blastomerát. Óvatosan, a sejthártya sérülését elkerülve, a pipettába szívjuk, majd kihúzzuk a zona pellucida nyílásán keresztül. A legalább 6 sejtet tartalmazó preembriókból ezt követően egy második blastomera kiemelését is elvégezhetjük.
A biopsziát követően a blastomerákat tiszta tápoldatban megmossuk, hogy elkerüljük a preembrióról esetleg átkerülő spermium vagy granulosa sejt továbbvitelét, amely kontaminációt okozva meghamisítaná a genetikai vizsgálat eredményét. A biopsziát követően a vizsgálandó mintát a genetikai vizsgálatnak megfelelő módon tároljuk, és a molekuláris genetikai laboratóriumba szállítjuk.
3. Genetikai vizsgálat
A molekuláris genetikai vizsgálat során a kivett sejt örökítő anyagát, a DNS-t vizsgáljuk és megállapítjuk, hogy a létrejött preembriók közül melyik hordozhatja a házaspárt érintő örökletes betegséget okozó genetikai hibát. A praeimplantációs diagnosztika során a preembriókból eltávolított blasztomérákat általában PCR (polymerase láncreakció), vagy FISH (fluorescens in situ hybridisatio) módszerrel vizsgálják. A FISH-módszer elsősorban nemmeghatározásra és aneuploidiák vizsgálatára alkalmazható, a PCR módszer monogénesen öröklődő betegségek kimutatására és a nem meghatározására alkalmazható. A későbbiekben várható a real-time PCR, a minisequencing, a microarray és a CGH (comparative genomic hybridisation) bevezetése és szélesebb körben történő elterjedése a PGD vizsgálatok területén.
4. Embrióbeültetés
Beültetésre csak a kérdéses genetikai rendellenességtől mentes előébrények kerülnek, míg a genetikai vizsgálat alapján rendellenesnek ítélt előébrények sorsáról a pár rendelkezik a beleegyező nyilatkozatban foglaltaknak megfelelően.
III. A PGD helyzete a világon
2004. év végéig világszerte mintegy 100 centrumban kb. 6000 vizsgálatot végeztek, amelyekből több mint 1000 gyermek született. Az embriótranszferre vonatkoztatott terhességi arány 20% körül van, a téves diagnózis aránya a nemzetközi adatok alapján 2-3%. Az eljárást a világ számos országában alkalmazzák, és a PGD végzésének körülményeit a legtöbb országban törvények szabályozzák. Egy, az IFFS (International Federation of Fertility Societies)
által összeállított nemzetközi felmérés1 részletes kimutatása alapján a világ 30 országában törvény, vagy etikai irányelv engedélyezi, 12 országban tiltja és további 12 országban pedig semmilyen törvény vagy etikai irányelv nem szabályozza a PGD végzését.
Magyarországon eddig nemhez kötötten öröklődő betegségekés cysticus fibrosis esetén történtek beavatkozások,és az első sikeres kezelésről és szülésről 2002-ben a Semmelweis Egyetem I. Sz. Szülészeti és Nőgyógyászati Klinikájáról számoltak be.2 Az elmúlt egy-két évben több IVF központ is érdeklődést mutatott a PGD gyakorlati alkalmazásával kapcsolatban.
Az alábbi táblázat összefoglalja azokat a legfontosabb genetikai kórképeket, amelyekben eddig sikeres praeimplantatiós genetikai vizsgálatot végeztek a világon.
| Autoszomális domináns öröklődésű beteqséqek(beteq utód kockázata 50%) |
| Marfan syndroma (kötőszöveti rendellenesség) |
| Huntington betegség (40 éves kor után jelentkező gyors szellemi és testi leépülés) |
| Dystrophia myotonica (korai gyermekkorban halálos izomgyengeség) |
| Familiáris adenomatosus colon polyposis (vastagbélrák) |
| Retinitis pigmentosa domináns változata (vakságot okozó retinadegeneráció) |
| Autoszomális recesszív öröklődésű betegségek (beteg utód kockázata 25%) |
| Cisztás fibrózis (elsősorban a tüdőt érintő gyakran fatális megbetegedés) |
| Tay-Sachs betegség (súlyos szellemi fogyatékossággal járó anyagcserebetegség) |
| á-thalassemia (a vérszegénység egyik súlyos formája) |
| Phenylketonuria (mentalis károsodással járó anyagcserebetegség) |
| Sarlósejtes vérszegénység (a vörösvérsejtek rendellenessége) |
| Spinalis muscularis atrophia (korai gyermekkorban halálos izomsorvadás) |
| á-1-antitripszin hiány (tüdő és májérintettséget okozó betegség) |
| Alport syndroma recesszív változata (veseelégtelenséget okozó betegség) |
| X-kromoszómához kötött rendellenességek (fiú utód kockázata 50%) |
| Valamennyi X-hez kötött recesszív öröklődésű betegségnél végezhető nemmeghatározás |
| HPRT-deffektus (hypoxantin-guanin foszforibozyltransferáz hiány) |
| Duchenne muscularis dystrophia (gyermekkorban halálos izomsorvadás) |
| Lesch-Nyhan syndroma (halálos kimenetelű anyagcserebetegség) |
| Haemophilia A és B (vérzékenység) |
| Congenitalis adrenalis hyperplasia ritka formája (leánymagzatokban intersexualitást okozó betegség) |
| Fragilis X syndroma (szellemi fogyatékosság) |
| Súlyos kombinált immunhiányos betegség (SCID) |
| Kromoszóma rendellenességek |
| Számbeli kromoszóma rendellenességek |
| Strukturális kromoszóma rendellenességek |
IV.EtikaikérdésekaPGD-velkapcsolatban
Az eljárás alkalmazása számos etikai kérdést is felvet. Ezek elsősorban a betegséget hordozó, és így beültetésre nem kerülő előébrények megsemmisítése miatt merülnek fel. Így a PGD alkalmazása feltételezi, hogy etikai szempontból különbséget teszünk a betegséget hordozó és méhen belül fejlődő, valamint az IVF kezelés útján létrehozott, a betegségben szintén érintett és ezért beültetésre nem kerülő előébrények megsemmisítése között. A másik etikai problémát az okozza, hogy praeimplantatiós genetikai vizsgálat nem csak a születendő gyermek életminőségét súlyosan befolyásoló örökletes betegségek esetén végezhető el, hanem, a módszer alkalmazásának nem megfelelő szabályozása és ellenőrzése esetén, alkalmas lehet arra is, hogy a szülők által preferált tulajdonságú gyermekek születéséhez segítsen hozzá (PGD nem orvosi javallatra történő alkalmazása.)
A PGS egyik speciális formája, a HLA-tipizálás esetében etikai problémaként merül fel az is, hogy a eljárás célja ebben az esetben nem egy egészséges gyermekszületése, hanem a születendő gyermekcsakeszköz egy másik, beteg gyermek meggyógyításához.
V. A PGD Magyarországon történő alkalmazásának minimumfeltételei
Összeállítva az ESHRE PGD consortium "Best Practice guidelines for Clinical Preimplantation Genetic Diagnosis (PGD) and Preimplantation Genetic Screening (PGS)" alapján.
1. PGD beavatkozások végzésének szervezeti feltételei
A PGD eljárások végzéséhez minden esetben olyan, a PGD eljárás végzése céljából létrejött interdiszciplináris együttműködés létrehozása szükséges mely az alábbi egységek munkáját fogja össze:
- klinikai genetikai egység (genetikai tanácsadás),
- asszisztált reprodukciós egység és
- a magyarországi populációban leggyakrabban előforduló betegségek esetében az egy sejt alapján történő genetikai vizsgálat elvégzésére képes genetikai diagnosztikai egység (genetikai laboratórium).
A kezelések végzésében közreműködő e három részleg között írásos megegyezés szükséges, amely részletesen tartalmazza a kivizsgálás, betegtájékoztatás és a kezelés protokollját valamint azt, hogy a három részleg közül melyik részleg a kezelés vezető szakmai felelőse. Biztosítani kell a fenti három egység közti megfelelő kommunikációt. A petesejtből illetve az embrióból a PGD céljából történő mintavétel kizárólag az asszisztált reprodukciós egységben történhet. Transzport PGD során az asszisztált reprodukciós egység és a genetikai laboratórium egymástól távol, más intézményben található, így a petesejtekből, embriókból származó, genetikai vizsgálat céljából vett mintát az embriólógiai laboratóriumból a genetikai laboratóriumba kell szállítani.
A PGD eljárások végzésében az alábbi feltételeknek megfelelő intézetek vehetnek részt:
a. Genetikai tanácsadás
A vizsgálat elvégzésének javallatát működési engedéllyel rendelkező genetikai tanácsadó központban humángenetikus, vagy klinikai genetikus szakorvos állítsa fel. A genetikai tanácsadás a Klinikai Genetikai Szakmai Kollégium által kidolgozott elvek alapján történik.
b. Asszisztált reprodukciós intézet
PGD eljárás részét képező, genetikai célú mintavétellel kiegészített in vitro fertilizációt és embriótranszfert olyan asszisztált reprodukciós intézet végezhet, amely megfelel "A reprodukciós eljárásra, illetve az ivarsejtek és a preembriók fagyasztva tárolására vonatkozó szakmai minimunfeltételek"-nek
c. Genetikai diagnosztikai laboratórium
A PGD eljárások során elvégzendő molekuláris genetikai vagy citogenetikai vizsgálatokat megfelelően felszerelt, megfelelő szakmai irányítás alatt álló egy sejt genetikai vizsgálatára felkészült laboratóriumban végezhető el. A genetikai diagnosztikai laboratóriumokra vonatkozó minimumfeltételeket a Klinikai Genetikai Szakmai Kollégium dolgozza ki.
2. Betegtájékoztatás, beleegyező nyilatkozatok
2.1. Általános irányelvek
A PGD eljárásban részt vevő párt megfelelő módon, szóban és írásban is tájékoztatni kell a kezelés valamennyi lépéséről, a genetikai adatok gyűjtésének illetve rögzítésének módjáról, az asszisztált reprodukciós és genetikai diagnosztikai eljárásokról.
A tájékoztatást az adott területen szakképesítéssel rendelkező szakorvos végezze.
A megfelelő tájékoztatást követően a PGD eljárás a pár férfi és nő tagja által is aláírt beleegyező nyilatkozat birtokában végezhető el.
2.2 Genetikai tanácsadással összefüggő tájékoztatás
A tanácsadást végző orvosnaka genetikai tanácsadás szakmai szabályainak megfelelően, részletesen tájékoztatnia kell a tanácskérő párt
- az őket érintő betegség továbbörökítésének az esélyéről,
- a betegség következményeiről,
- beteg gyermek születésének elkerülése érdekében alkalmazható egyéb módszerekről (prenatális diagnosztika)
- az adott betegség PGD keretében történő vizsgálhatóságának lehetőségéről
- Az IVF kezelés során létrejött embriókban a vizsgált betegség előfordulásának várható gyakoriságáról
2.3. A PGD eljárással összefüggő tájékoztatás
Az asszisztált reprodukciós beavatkozást végző orvosnak az egyéb, nem PGD céljából végzett IVF-ET kezelésekhez hasonlóan kell tájékoztatni a beteget a kezelés folyamatáról, várható eredményességéről, valamennyi kockázatáról, és esetleges következményeiről. A PGD eljárás kapcsán külön ki kell térni az alábbiakra:
- nem mindegyik embrió alkalmas a genetikai célú mintavételre
- a mintavétel során némelyik embrió megsemmisülhet
- előfordulhat, hogy némelyik embrió esetében nem ad megbízható eredményt a genetikai vizsgálat
- előfordulhat, hogy valamennyi embrió hordozza a vizsgált betegséget
- a kezelés eredményessége elmarad a PGD nélkül végzett IVF-ET kezelések eredményességétől
- fennáll a téves diagnózis lehetősége.
3. PGD eljárás genetikai javallatai
Egységes szakmai-etikai állásfoglalás szükséges a PGD útján vizsgálható betegségek köréről.
a. PGD eljárás alkalmazása
PGD eljárásban azon párok részesülhetnek:
- akiknél az egészségügyről szóló 1997. évi CLIV. törvény ide vonatkozó 167. §-a alapján asszisztált reprodukciós beavatkozás végezhető
- akiknél magas (>10%) genetikai kockázat áll fenn egy adott, az életminőséget jelentősen befolyásoló monogénes betegség továbbörökítésére, vagy
- a szülők valamelyikében igazolt kiegyensúlyozott szülői kromoszóma rendellenesség áll fenn,
- azon pároknál akiknél a vizsgálandó betegség biztosan nagy valószínűséggel igazolt és esetükben a vizsgálandó betegség kimutatására megbízható diagnosztikai módszer áll rendelkezésre
Az egy sejten történő molekuláris genetikai módszerek beállítása és ellenőrzése egy újabb betegség vizsgálatára hosszas előkészületeket tesz szükségessé, amely limitálja az egy laboratóriumban vizsgálható betegségek számát. Ajánlott a módszert olyan megbetegedésekben alkalmazni, amelyek viszonylag gyakran fordulnak elő a magyar populációban. Ilyen szempontból jelenleg elsősorban az alábbi betegségek vizsgálata jön szóba. (Az alábbiakban felsorolásra nem került, egyéb esetekben a három egység -genetikai tanácsadás, asszisztált reprodukciós egység, genetikai laboratórium- konszenzusa dönt.)
- Monogénesen öröklődő betegségek:
X kromoszómához kötötten öröklődő recesszív megbetegedések esetén nemmeghatározás
Duchenne muscularis dystrophia ismert deletioja
Cysticus fibrosis delta-F 508 mutatió
Spinalis muscularis atrophia
Dystrophia myotonica
Huntington chorea
- Kromoszóma rendellenességek
- kiegyensúlyozott transzlokáció vagy egyéb strukturális aberráció a pár valamelyikében
b. PGS eljárás alkalmazása
Alacsony kockázatú betegcsoportban végzett aneuploidia szűrés csak korlátozott javallattal (magas anyai életkor, többszöri eredménytelen IVF kezelés után) fogadható el, akiknél az egészségügyről szóló 1997. évi CLIV. törvény ide vonatkozó 167. §-a alapján asszisztált reprodukciós beavatkozás végezhető. Ugyanez vonakozik a poligénesen meghatározott hajlam prediktív genetikai tesztelésére is.
c. HLA-tipizálás alkalmazása
A módszer hatékonysága jelenleg vizsgálati stádiumban van, meggyőző bizonyítékok hiányában, valamint alkalmazásával szemben felmerülő etikai kifogások miatt, klinikai alkalmazása nem elfogadható.
d. Nem orvosi javallat alapján történő alkalmazás
A PGD kezelés nem végezhető genetikai javalat nélkül,a szülők kérésének megfelelő nemű, vagy egyéb kiválasztott tulajdonságú gyermek létrehozása céljából.
4. Asszisztált reprodukciós kezelés
PGD céljából végzett IVF-ET kezelések általános irányelvei megegyeznek az egyéb, meddőség kezelése céljából végzett IVF-ET kezelésekkel.
5. In vitro fertilizáció és embriótenyésztés
A genetikai mintavétel időpontjáig a PGD céljából végzett IVF kezelések általános irányelvei megegyeznek az egyéb, meddőség kezelése céljából végzett IVF kezelésekkel.
A biopsziát követően a petesejteket, embriókat egyedileg azonosítható módon, egymástól elkülönítve kell tartani és biztosítani, hogy a genetikai vizsgálat eredménye a megfelelő embrióhoz hozzárendelhető legyen.
6. Genetikai célú mintavétel
a. Genetikai célú mintavételre különböző fejlődési állapotokban
- Sarkitest biopszia (petesejten vagy zigótán végezhető)
- Blasztomera biopszia (a korai osztódás állapotában végezhető)
- Trophectoderma biopszia (blasztociszta állapotban végezhető)
b. A biopszia személyi feltételei
Genetikai célú mintavételt megfelelően felkészült embriológus végezhet, aki a folyamat valamennyi lépését kellően begyakorolta, és rutinszerűen el tudja végezni.
7. Genetikai vizsgálatok végzése
A PGD céljából egyetlen sejtből végzett molekuláris genetikai vagy citogenetikai vizsgálatokat végző laboratóriumok működésének minimumfeltételeit és az alkalmazható módszereket a Klinikai Genetikai Szakmai Kollégium állapítja meg. A vizsgálat minden lépéséről írásos protokollt kell készíteni.
8. Embrióbeültetés
A PGD eljárás során végzett embriótranszfer általános irányelvei megegyeznek a meddő betegek kezelése során alkalmazott IVF-ET módszerekkel. Az embrióbeültetést ajánlott a genetikai vizsgálat időigényétől függően a megtermékenyítést követő 3-6. napon elvégezni.
A beültethető embriókszámát illetően az egyéb, nem PGD céljából végzett IVF-ET kezelésekre vonatkozó szabályozást kell figyelembe venni.
A beültetésre kerülő embriók kiválasztása során elsődleges szempont a genetikai vizsgálat eredménye, és csak másodlagos szempont lehet az embriók morphológiai minősége. A vizsgált tulajdonságra nézve heterozigóta vagy kiegyensúlyozott kromoszóma rendellenességet hordozó embriók beültetése elfogadható, amennyiben a vizsgált betegség a hordozókban várhatóan nem manifesztálódik. A beültetésre alkalmas minőségű és a genetikai vizsgálat eredménye alapján beültethető, de beültetésre nem kerülő (számfeletti) és fagyasztásra alkalmas embriók kryokonzerválását a beteg kérésére el kell végezni.
9. PGD eljárás során fogant terhességek nyomonkövetése
A terhesgondozás során a PGD eljáráskor végzett genetikai vizsgálat eredményének megerősítésére ajánlott a prenatális genetikai diagnosztika valamely formáját elvégezni.
10. Dokumentáció
A PGD eljárás során részletes dokumentációt kell készíteni, amely kiterjed arra, hogy a PGD eljárásban résztvevő három egység (genetikai tanácsadás, asszisztált reprodukciós központ, molekuláris genetikai laboratórium) közül melyik a PGD eljárás végzésének szakmai felelőse, valamint az alábbiakra:
- a genetikai tanácsadás során végzett vizsgálatokra
- a reproduktív kórelőzményre a pár mindkét tagjánál
- a PGD eljárással kapcsolatos részletes betegtájékoztatóra és beleegyező nyilatkozatokra
- az IVF-ET kezelés körülményeinek dokumentálására
- a petesejtekből/embriókból történő mintavételre, a mintákegyedi jelölésére és a genetikai laboratóriumba történő eljuttatására
- a genetikai vizsgálatok körülményeire és eredményére
- a PGD eljárás eredményeként létrejött terhesség nyomonkövetésére.
A PGD eljárások javallatáról, az elvégzett vizsgálatokról, azok eredményéről és kimeteléről a hatályos adatvédelmi szabályok szerint a Humán Reprodukciós Bizottság felé jelentést kell tenni.
VI. Irodalomjegyzék
1. Jones H.W., Cohen J.: IFFS Surveillancs 04. Fertil Steril 2004;81(S4):S37-S38.
2. Papp Z., Fancsovits P., Bán Z., Tóthné G.Zs., Urbancsek J.: Előébrény diagnosztikát követően fogant sikeres terhesség első hazai esete. Orv Hetil 2002;143:1881-2883.
3. Papp Z., Fancsovits P., Bán Z., Tóthné G.Zs., Urbancsek J.: Előébrény diagnosztikát követően fogant sikeres terhesség első hazai esete. Orv Hetil 2002;143:1881-2883.
4. The ESHRE Ethics Task Force, Shenfield F., Pennings G., Devroy P., Sureau C., Tarlatzis B., Cohen J.: Taskforce 5: preimplantation genetic diagnosis. Hum Reprod 2003;18:649-651.
5. Thornhill A.R., deDie-Smulders C.E., Geraedts J.P., Harper J.C., Harton L.G., Lavery S.A., Moutou C., Robinson M.D., Schmutzler A.G., Scriven P.N., Sermon K.D., Wilton L.: ESHRE PGD consortium "Best practice guidelines for clinical preimplantation genetic diagnosis (PGD) and preimplantation genetic screening (PGS)". Hum Reprod 2005;20:35-48.
6. 21/1998. NM rendelet 9/A. számú melléklete (24/2000 EüM rendelet 2. § (2)
A szakmai irányelv érvényessége: 2012. június 30.
Az Egészségügyi Minisztérium
szakmai irányelve
A nozokomiális pneumonia megelőzéséről
Készítette: a Megelőző Orvostani és Népegészségügyi Szakmai Kollégium
I. Alapvető megfontolások Rövidítések
CDC - Centers for Diseases Control and Prevention, Atlanta
ATS - American Thoracic Society
NNSR- Nemzeti Nosocomiális Surveillance Rendszer
HAP - hospital acquired pneumonia (kórházban szerzett pneumonia)
VAP - ventilator associated pneumonia (gépi lélegeztetés kapcsán szerzett pneumonia)
HELICS - Hospitals in Europe Link for Infection Control Through Surveillance
SDD - szelektív digesztív dekontamináció
CFU - kolonia formáló egység
HICPAC - Healthcare Infection Control Practices Advisory Committee ESBL - kiterjedt spektrumú béta-laktamáz
ARDS - adult respiratory distress syndrome (felnőttkori respiratorikus distress szindróma) MRSA - methicillin rezisztens Staphylococcus aureus APACHE - Acute Physiology and Chronic Health Evaluation SAPS - Simplified Acute Physiology Score
1. Az irányelv célja
A nozokomiális pneumóniák kontrollja az Intenzív Osztályokon. A megelőzés lehetőségeinek feltárásával és az előfordulás gyakoriságának csökkentésével a multirezisztens kórokozók elterjedésének megakadályozása.
2. Az irányelvfejlesztéssel kapcsolatos információk
2.1. Előszó
Az elmúlt évtizedekben a súlyos betegek kezelése az intenzív osztályokra koncentrálódott. Az életmentő technikák fejlődése megnövelte a nozokomiális infekciók kockázatát. Intenzív osztályon ápolt betegekesetében a nozokomiális fertőzések aránya többszörösére nőtt a nem intenzív osztályon fekvőkéhez képest. Az egészségügyi intézményeknek jelentős költségterhet jelentenek a nozokomiális, ezen belül a multirezisztens kórokozók által okozott fertőzések. Az intenzív osztályokon leggyakrabban előforduló légúti fertőzések megelőzése, a multirezisztens kórokozók elterjedésének megakadályozása közérdek. Ennél fogva a nozokomiális pneumóniák megelőzésének irányelvét az intenzív osztályokon dolgozóknak, az összes műtétes szakmában tevékenykedő orvosnak és egészségügyi szakdolgozónak, valamint az egészségügyi intézményekvezetésénekegyaránt ajánljuk.
2.2. Irányelv fejlesztés módszerei fejlesztőcsoport:
2.2.1. Az irányelvfejlesztés folyamatában részt vettek:
2003-ban: A Magyar Kórházszövetség Infekciókontroll Szakbizottsága, a Kórházi Minőség Fórum Infekciókontroll Irányelv fejlesztő Csoportja 2007-ben a felülvizsgálatot végezte, a Megelőző Orvostan és Népegészségtan Szakmai Kollégium, Kórházhigiénés Munkabizottsága
2.2.2. Az irányelv fejlesztésében érintett klinikai szakterületek Aneszteziológia és Intenzív terápia
Infektológia
Mikrobiológia
Pulmonológia
2.2.3. Az aktualizált irányelv egyeztetésére került a Pulmonológiai, Infektológiai, Mikrobiológiai és Aneszteziológiai Szakmai Kollégiumokkal.
2.2.4. Az irányelv fejlesztés folyamatának leírása
Jelen szakmai irányelvnek a CDC és az ATS ajánlások képezik az alapját. A CDC irányelv 703 - a bizonyítékon alapuló orvoslás kritériumainak megfelelő - tanulmány alapján készült (7). Ezek között számos nagy randomizált kontrollált vizsgálat is szerepel. Az ATS irányelve ugyanakkor 294 tanulmányon alapszik (1).
Az irányelv magyarországi alkalmazhatóságát egyrészt, gyakorlati szakemberek részvétele, másrészt a hazai közleményekben és könyvekben fellelhető eredmények, beépítése biztosítja (3,4,6,22,27,28,30). A hazai adatokat a HELICS programból (16), az NNSR eredményeiből (2) és a kórházakban működő helyi surveillance tapasztalataiból vettük. A munkacsoport résztvevői a saját intézményükben alkalmazott surveillance technika eredményeit belső intézeti döntésekben használják fel. Így ez a szakmai irányelv a különböző típusú kórházi surveillance tevékenység egységesítését is szolgálja.
Értékelés és felülvizsgálat tervezett módszertana:
- Az infekciókontroll módszereivel történő szakmai ellenőrzés (surveilllance, antibiotikum politika, mikrobiológiai, szerológiai vizsgálatok, fertőtlenítés, sterilizálás, védőeszközök helyes használata (8) stb.)
- Patológiai surveillance végzése és intézményi rezisztencia-térkép meghatározása
2.3. Dokumentáció, jogi megfontolások:
Az irányelvben foglaltak betartása jogi védelmet nyújthat az intézetnek peres eljárások során.
Elősegíti az egészségügyi dolgozó elégedettségét az ismeretek bővítése által.
Hozzájárul az alkalmazó intézmény javuló társadalmi megítéléséhez. Növeli a betegelégedettséget.
2.3.1. A kiadás dátuma: 2009.
2.3.2. A szakmai irányelv felelős összeállítója: A Megelőző orvostan és Népegészségtan Szakmai Kollégium, illetve az általa kijelölt munkabizottság.
2.3.3. A szakmai irányelv érvényességi ideje: 2010. szeptember 30.
"Az irányelv - az adott klinikai állapot ellátására vonatkozó - a kiadás időpontjában rendelkezésre álló tudományos és szakmai szempontok körültekintő mérlegelésén alapuló ajánlásokat tartalmaz. Az irányelv ajánlásait az egészségügyi szolgáltató az egyedi beteg ellátásakor a rendelkezésre álló feltételek és lehetőségek körültekintő mérlegelésével, továbbá a beteg preferenciáinak és biztonságának figyelembevételével használhatja"
3. Az irányelv leírása
3.1. Összefoglalás
A nozokomiális pneumóniáka leggyakoribb kórházi fertőzések az intenzív osztályokon. Felismerésük nehéz a klinikai gyakorlatban, a korszerű diagnosztikai eljárások nem részei a hazai gyakorlatnak. A nozokomiális pneumóniák az intenzív osztályos ápolási napokat jelentősen megnövelik, kezelési költségük igen magas. A helyes infekciókontroll gyakorlat csökkenti a betegség morbiditását, mortalitását és költségeit.
3.2. Tartalom: Bevezetés
Legfontosabb megállapítások, ajánlások kategorizálása Részletes ajánlások
Az irányelv ajánlásai által elérhető eredmények
3.3. Bevezetés
3.3.1. A klinikai probléma háttere, klinikai relevanciája, magyarországi helyzetkép
A kórházi fertőzések fogalmát kiterjesztve a teljes egészségügyi ellátó rendszerre, nozokomiális helyett az utóbbi időben az "egészségügyi ellátással összefüggő" kifejezést használják.
Nozokomiálisnak definiáljuk azokat a pneumóniákat, amelyeket a beteg kórházi (egészségügyi) ellátás során akvirál, (HAP=hospital acquired pneumónia=kórházban szerzett) és annak tünetei a felvételt követő 48 óra után manifesztálódnak. A nozokomiális pneumóniák leginkább az intenzív osztály betegeit érintik, közülük is főként a lélegeztetésben részesülőket. Így az evidenciákon alapuló közlemények az intenzív osztályos betegpopuláció gyakorlatából származnak.
A széles spektrumú antibiotikumok ellenére a HAP mind a morbiditás, mind a mortalitás vezető tényezője, 1000 kórházi felvételből 5-10 esetben fordul elő. Az incidencia a gépi lélegeztettetek körében ennek 6-20 szorosa (10, 11, 13).
Lélegeztetéssel összefüggő pneumóniának nevezzük (VAP=ventilator-associate pneumonia), a nozokomiális pneumóniákazt a fajtáját, amely a lélegeztetés mellett 48-72 órát követően lépnekfel, amennyiben kizárható a felvétel idején inkubációs stádiumban lévő infekció.
Magyarországon a Nemzeti Nosocomiális Surveillance Rendszer (NNSR) keretében- 2006-ban az Intenzív Osztályokon végzett surveillance adatai szerint az eszközhasználattal összefüggő infekciók körében, a VAP fertőzési aránya a legmagasabb (13,1%). Ez az érték természetesen függ az Intenzív Osztály típusától is (2).
A nozokomiális pneumónia megelőzéséhez ismernünk kell a nozokomiális pneumónia kialakulásának rizikó tényezőit (21), kórokozóit, és a diagnosztikus lehetőségeit
(9, 12, 14, 15, 29, 31).
Patomechanizmus
Több tanulmány bizonyítja, hogy a nozokomiális pneumónia kialakulását kolonizáció előzi meg. Az alsólégutak felsőlégutakból történő kolonizációját elsősorban a Pseudomonas aeruginosa és más enterális Gram negatív kórokozó vonatkozásában bizonyították, azonban annak jelentősége a gasztrointesztinális traktus felől igen csekély (7). A lélegeztetéssel összefüggő pneumónia rizikófaktoraként szerepelnek még a kontaminált aeroszolok, és lélegeztetési eszközök, valamint a nem megfelelő kézhigiéne is.
Rizikófaktoroka multirezisztens kórokozók által kiváltott nozokomiális pneumóniákban (1):
- Antibiotikum terápia az előző 90 napban
- A jelenlegi kórházi kezelés 5 vagy ennél több napig fennáll
- Az antibiotikum rezisztens törzsek aránya magas az adott osztályon
- Immunszupresszív terápia vagy immunhiányos betegség
- A kórházi fertőzések kockázati tényezői fennállnak (2 napnál hosszabb kórházi ápolás, ápolási otthonból érkező beteg, otthoni infúziós kezelés, krónikus dialízis 30 napon belül, otthoni sebkezelés, multirezisztens kórokozót hordozó családtag a beteg környezetében).
Kórokozók (1,15):
A kórokozók spektruma széles. A leggyakrabban előforduló kórokozók az aerob Gram negatívak közül a Ps. aeruginosa, E. coli, Klebsiella pneumoniae, Acinetobacter- valamint a Gram pozitív S. aureus - különösen intenzív osztályon ápolt, diabeteszes, illetve fejsérülést elszenvedett betegeknél. Virális- és gomba pneumóniák immunkárosodott betegekben fordulnak elő.
Multirezisztens kórokozók a nozokomiális pneumónia vonatkozásában:
- Pseudomonas aeruginosa (carbapenem rezisztens, multidrug-rezisztens)
- Klebsiella spp, Enterobacter spp, Serratia spp (ESBL termelők)
- Acinetobacter spp, Stenotrophomonas maltophilia, Burkholderia cepacia
- MRSA
II. Diagnózis
Mikrobiológiai diagnosztikai lehetőségek:
Az ATS állásfoglalása szerint, kvantitatív mikrobiológiai vizsgálatot kell végezni mind az endotracheális aspirátumból, mind a bronchoszkóppal nyert mintákból. A trachea aspirátumszemikvantitatív tenyésztési eredménye nem alkalmas a pneumónia diagnózisánakalátámasztására és az antibiotikum terápia szükségességénekeldöntésére. Amennyiben bronchoszkópos mintavételre nincs lehetőség, az alsólégutakból nyert aspirátum kvantitatív mikrobiológiai vizsgálata megfelelő az antibiotikum terápiával kapcsolatos döntéshez. Segíthet a diagnózis felállításában a pozitív hemokultúra is, ezért a hemokultúra végzése minden esetben ajánlott.
Lélegeztetett betegen a bronchoszkópos mintavételi eljárás ajánlott. A védett kefe és a bronchoalveoláris lavage (9, 30, 33) révén nyert mintákat kvantitatív mikrobiológiai módszerrel kell vizsgálni (29). Az eredményeket CFU/ml vagy CFU/g-ban kell megadni, ami az 1 ml-re, vagy 1 g szövetre eső telepszámot jelenti.
Ma Magyarországon a megfelelően érzékeny és specifikus mintavételi lehetőségek és a légúti váladékok mikrobiológiai vizsgálatának lehetőségei korlátozottak a nozokomiális pneumonia felismerésében. A lélegeztetett betegen fellépő klinikai tünetek, mint a láz, a leukocitózis, CRP emelkedés, a RTG elváltozás és a purulens trahebronchiális váladék megjelenése alapján csak empirikus antibiotikum terápia indítható el. Az antibiotikum rezisztencia terjedése miatt azonban, feltétlenül szükséges lenne a gyors mikrobiológiai diagnózison alapuló célzott kezelés.
A nozokomiális pneumónia időbeli megjelenése szerint megkülönböztetünk korai és késői típusú pneumóniát. A korai és késői típusú nozokomiális pneumóniának eltérő a kórokozó spektruma.
- A felvételt követő első négy napban megjelenő pneumóniákat korai típusú pneumóniánaknevezzükés kórokozója leggyakrabban Haemophilus influenzae, Streptococcus pneumoniae, methicillin érzékeny Staphylococcus aureus.
- Az 5. napon, vagy azt követően megjelelő pneumóniát késői típusú nozokomiális pneumóniának hívjuk, leggyakoribb kórokozói az aerob Gram negatív baktériumok (Ps. aeruginosa, Enterobacteriaceae, Acinetobacter baumanni) és az MRSA (31).
- A még később -7 nap, vagy azon túli elhúzódó gépi lélegeztetés mellett-jelentkező VAP gyakori kórokozója még a fentieken kívül a Stenotrophomonas maltophilia is (3).
3.3.2. Az irányelv bevezetésével elérhető eredmények, várható egészség nyereség A nozokomiális pneumónia diagnosztikus kritériumainak megismerése.
Az intézetben előforduló lélegeztető gép használatával összefüggő nozokomiális pneumóniak gyakoriságának megismerése.
Az intézet Intenzív Osztályán lélegeztetett betegek száma, és a lélegeztetéssel összefüggő pneumóniák számának ismerete.
A gépi lélegeztetéssel összefüggő pneumóniák számának csökkenése.
A betegellátás költségeinek csökkenése.
Az egészségügyi ellátás minőségének javulása.
Az egészségügyi dolgozók szemléletének fejlődése.
3.3.3. Az irányelv céltcsoportjai
A felnőtt és gyermek Intenzív Osztályokon ellátásra kerülő betegek. 3.4 Legfontosabb megállapítások, ajánlások, algoritmusok
3.4.1 Az ajánlásokat két kategóriába,- ezen belül pedig három csoportba - rangsorolja, a tudományos evidencia mértéke, a racionalitás, az alkalmazhatóság és a gazdaságosság alapján (19).
I. Kategória
(IA) Szigorú előírás kategória, minden kórház számára kötelező, mert az ajánlásokat megfelelő jól tervezett és ellenőrzött kísérleti, klinikai és epidemiológiai vizsgálatok eredményei támasztják alá
(IB) Kifejezetten ajánlott kategória minden kórház számára a HICPAC által végzett multidiszciplináris konszenzus alapján, mert erős a racionalitásuk, kifejezetten evidenciákon alapulnak, de még nincs elegendő tudományos kísérleti bizonyíték.
II. Kategória
Javasolt a kórházak többsége számára, ezeket klinikai és epidemiológiai vizsgálatok támasztják alá, erős az elméleti racionalitásuk, és amelyeket az intézmények többsége is alkalmazhatónak tart.
III. Kezelés
3.5. Részletes irányelv
Ajánlások az egészségügyi ellátással összefüggő bakteriális pneumoniák megelőzésére
3.5.1. A munkatársak képzése: (IA)
- Az infekció kontroll szabályok ismerete
- A nozokomiális pneumónia CDC definíciójának ismerete (32)
- A megelőzés lehetőségeinek oktatása
- Fertőtlenítés, sterilizálás ismeretek oktatása (25,26)
-Az intenzív osztályra kerülő beteg rizikófaktorának becslése (18,19) (Ajánlott a SAPS-II. és APACHE-II. score-rendszer használata)
3.5.2. Surveillance: (IB)
- Az Intenzív Osztályokon szükséges célzott surveillance végzése, CDC definíciók alapján (32) különösen a nagy rizikójú betegcsoportokban (gépi lélegeztetett betegek és a műtéten átesettek).
- A kórokozók monitorozása és az antibiotikum rezisztencia adatainak folyamatos nyomon követése.
-Az adatok és az arányszámok elemzése (fertőződött betegek száma, 100 intenzív osztályos napra eső infekció szám, ezer lélegeztetett napra eső infekció szám), ami összehasonlítást tesz lehetővé kórházon belül és kórházak között.
3.5.3. Klinikai, epidemiológiai vagy infekciókontroll indok hiányában nem javasolt rutin bakteriológiai tenyésztés az alábbi mintákból: (II)
- a betegek váladékai, a lélegeztetéshez használt eszközök, a tüdőfunkció diagnosztikai eszközei, és az anesztézia eszközei.
3. 5. 4. A kórokozók átvitelének megakadályozása
3.5.4.1. Alapszabály: Valamennyi alkalmazott anyag, eszköz, gép folyamatos fertőtlenítése, sterilizálása, karbantartása: (IA)
- Sterilizálni kell minden olyan eszközt, műszert, ami a beteg nyílt test-szöveteivel, nyitott testüregével, nyálkahártyájával, testnyílásaival kerül kapcsolatba. (IA)
- A sterilizálás előtt az eszközök alapos megtisztítása, majd fertőtlenítése szükséges (25,26) (IA).
- Fertőtlenítés után alaposan öblíteni, szárítani, csomagolni kell az eszközöket a sterilizáláshoz.(IA)
- Az öblítéséhez desztillált vizet kell használni. (IB)
- Az egyszerhasználatos eszközöket nem szabad újra sterilizálni.(IC)
3.5.4.2. Lélegeztetés
- Lélegeztető gép belsejét nem kell rutinszerűen fertőtleníteni (II)
- A légző kör cseréje ugyanazon betegnél feltétlenül ajánlott, ha mechanikus funkciózavar lép fel vagy a légző kör láthatóan szennyezett (IA).
- A többször használatos légző köröket két beteg között mindig sterilizálni kell (26)(IB).
-A lélegeztető gép csövében képződött kondenzátumot rendszeresen le kell engedni, oly módon, hogy az sohasem a beteg felé történjen (IB)
- A folyadék leengedését kesztyűben kell végezni és utána higiénés kézfertőtlenítés szükséges (IB)
- Nincs egységes álláspont a filter használatára vagy csapda elhelyezésére a légző kör kilégző csövének disztális végénél a kondenzátum összegyűjtésére.
- A párásító tartályt steril desztillált vízzel közvetlenül használat előtt kell feltölteni.(II)
3.5.4.3. Porlasztók használata
- Steril desztillált vízzel kell feltölteni a porlasztót és aszeptikus körülmények között porlasztani (IA)
- Ugyanazon betegnél elegendő két kezelés között tisztítani, fertőtleníteni és steril desztillált vízzel leöblíteni. (IB)
- Két beteg között a gyógyszerporlasztó mobil tartozékait, - csutora, hullámcső - sterilizálni kell. (IB)
- Több dózist tartalmazó ampullák használatánál a felbontott ampulla kezelése, tárolása a gyógyszergyártó cég utasítása szerint kell, hogy történjen (IB)
3.5.4.4. Oxigén párásítók:
- Fali oxigén párásítók kezelését a gyártó cég ajánlása szerint kell végezni (IB)
- Két beteg között mindig cserélni kell a központi oxigénhez csatlakozó csöveket, az orr kanült, vagy a maszkot. (IB)
- Oxigén párásító tartályokat naponta fertőtleníteni és két beteg között sterilizálni kell (26) (IA).
- Az oxigén párásító tartály feltöltése csak steril desztillált vízzel történhet (IA).
3.5.4.5. Egyéb lélegeztetéshez kapcsolódó eszközök:
A hordozható respirátort és az oxigén szenzort és a lélegeztetéshez használt eszközöket fertőtleníteni vagy sterilizálni a gyártó cég utasítása szerint kell. (IB)
3.5.4.6. Az újraélesztő táska tartozékai
- Az intratrachealis tubust, maszkot, Mayo pipát, laringoszkópot mycobactericid szerrel kell fertőtleníteni, (AMBU Ballon)-t két beteg között sterilizálni kell (26) vagy esetenként egyszer használatosat kell alkalmazni. (IA)
- Nincs egységes álláspont a reszuszcitációs szetthez csatlakoztatható hidrofób filter cseréjének gyakoriságára vonatkozóan.
- A táskát is fertőtleníteni kell.
3.5.4.7. Az altatógépek légző köre és beteg köre
- Nem kell rutinszerűen fertőtleníteni az altató gépek belsejét. (IB)
- Tisztítani, fertőtleníteni, sterilizálni kell a gépkör és betegkör többször-használatos elemeit (25, 26) (trachea tubus, maszk, hullámcsövek, légző-zsákok, Y elágazás, stb. két beteg között a gyártó cég útmutatása szerint. (IB)
- A széndioxid abszorber, és a gázáramlást biztosító szelepek vonatkozásában a fertőtlenítés gyakoriságára nincs egységes álláspont.
- Rendszeresen le kell engedni a keletkezett kondenzátumot a betegkör csövéből, sohasem a beteg irányába (IB)
- A művelet kesztyűben végzendő és utána kezet kell fertőtleníteni (IB)
- A beteg és a gép-kör közé helyezett baktérium filter alkalmazásának szükségességéről nincs egységes álláspont.
- A gépkör és a betegkör egyéb tartozékainak karbantartására, tisztítására, fertőtlenítésére, sterilizálására vonatkozóan a gyártó által megadott ajánlások érvényesek. (IB)
3.5.5. A fertőzés átvitelének megakadályozása egyik személyről a másikra
- A lélegeztetett beteg ápolása, ellátása előtt és után a higiénés kézfertőtlenítés a kesztyű viselésétől függetlenül kötelező (IA)
- Egyszer használatos kesztyű viselése a légúti váladékok vagy légúti váladékkal kontaminált eszközök kezelésénél kötelező (IB)
-A beteggel való érintkezés után, ugyanazon beteg más testtájékának érintése után és a légúti beavatkozások között a kesztyűcsere és a kézfertőtlenítés kötelező.(IA)
- Ha légúti váladék fröccsenésére, szóródására lehet számítani védőköpenyt vagy kötényt, orr-szájmaszkot, védő szemüveget kell viselni. (IB)
- Tracheosztómia végzése műtéti sterilitás betartása mellett történjen (IB)
- Tubuscserénél aszepszis betartása és steril tubus használata kötelező (IB)
- A többször használatos tubust tisztítás, fertőtlenítés, öblítés, csomagolás után sterilizáljuk újra (IB) 3.5.5.1. Légutak leszívása:
- Nem szükséges steril kesztyű a légutak leszívásához.
- Ha nyílt leszívási rendszert használunk steril egyszer használatos katéter alkalmazása szükséges (II)
- A váladék katéterből történő eltávolításához steril oldatot használjon az ugyanazon időpontban végzett többszöri szívások között (II)
- Conicotomiás vagy intratracheális kanül kezelés:
- Hosszú ápolási idejű, lélegeztetett vagy tartós légúti eszközzel rendelkező személynél előnybe részesítjük a dupla ballonos légúti eszközök alkalmazását. A ballonok váltott használata a trachea falát kíméli. A váladék lecsorgás, szivárgás kivédése érdekében az endotracheális tubus nyomás 20 vízcm-en való tartása optimális.
- A légutak falának megóvása érdekében figyelembe kell venni: a, a váladék mennyiségét (száraz légutak leszívását kerüljük) ill. b, "falkímélő" leszívó katéterek alkalmazását helyezzük előtérbe
3.5.6. A beteg ellenálló képességének fokozása
Pneumococcus vakcináció általánosságban javasolt a rizikócsoportba tartozó betegeknél:
1). 5 év alatt: HIV fertőzés, leukémia, lymphoma, nephrozis szindróma, kemoterápia, transzplantáció, hosszan tartó kortikosteroid terápia esetén.
2). 5-64 éves kor között: kardiovaszkuláris betegségben, alkoholizmusban, valamint anatómiai és funkcionális aszpléniában és immunhiányos állapotokban
3). Diabeteszben, krónikus légzőszervi betegségben, krónikus májbetegségben, 4). 65 év felett
3.5.7. Az aspiráció megelőzése
Az aspiráció megelőzésére a beteg fél ülő helyzetben (30-45°) való tartása javasolt, különösen az enterális táplálás ideje alatt.(IA)
Amint a klinikai állapot engedi, szüntessük meg az intubációt, a traheosztomás nyílást zárjuk, a szondatáplálást szüntessük meg.(IB)
3.5.7.1. Endotrachealis intubációval összefüggő aspiráció megelőzése
- Ha nincs ellenjavallata, akkor a non-invazív pozitív nyomású lélegeztetést részesítjük előnyben arc és orr maszk alkalmazásával az endotracheális intubáció helyett (II)
- Amennyire lehet, kerüljük az ismételt endothracheális intubációt (II).
- Amennyiben nem kontraindikált az orotracheális intubációt alkalmazzuk a nasotracheális helyett (IB)
- Dorzális leszívó lumennel bíró tubus használata előnyösebb (II).
- Az endotrachealis tubus eltávolítása előtt a szubglottikus területet mindig le kell szívni (II)
3.5.7.2. Az enterális táplálással összefüggő aspiráció megelőzése:
- Lélegeztetett és gyomorszondával rendelkező betegeknél a felemelt testhelyzet előnyösebb a laposan fekvő helyzetnél (II)
- A tápszonda helyét rutinszerűen ellenőrizni kell.(IB)
- Minden etetés előtt ellenőrizni kell a kielégítő bélmotilitást, és a gyomor kiürülését. (IB)
- Nincs egységes álláspont a kis átmérőjű szondák használatára vonatkozóan.
-Nincs egységes álláspont arra vonatkozóan, hogy a folyamatos vagy az intermittáló táplálást kell előnybe részesíteni.
- Nem ajánlják a pylorus alá vezetett szonda használatát sem.
3.5.7.3.Az oropharingeális kolonizáció megelőzése:
- A szájhigiéne, (tisztítás antiszeptikumokkal való öblítés, áttörlés) ajánlott az egészségügyi intézményekben (II)
- 2% -os Chlorhexidines öblögetés ajánlott a perioperatív periódusban (II)
3.5.8. A posztoperatív pneumónia kialakulásának megelőzése
- Nagy rizikójú betegek oktatása a műtét előtt - köhögés, mély légvételek fontossága a tüdőgyulladás megelőzése szempontjából (IB)
-Amennyiben nincs kontraindikáció, műtét után a beteget mély légvételekre kell ösztönözni, és a korai mobiliziációra kell törekedni (IB)
- Nincs egységes álláspont a fizioterápia alkalmazására, minden posztoperatív betegnél.
- Nincs egységes álláspont a szisztémás antibiotikum profilaxisra vonatkozóan
- Nincs ajánlás a szelektív dekontaminációra (SDD), és a stress ulcus megelőzésére.
IV. Rehabilitáció
V. Gondozás
3.6. Az irányelv ajánlásai által elérhető eredmények
A kórházi infekció hazánkban is népegészségügyi probléma, mind gyakorisága, letalitása mind költségvonzata miatt. A kórházi fertőzéseken belül a nozokomiális pneumónia előfordulási gyakorisága, magas halálozási aránya és magas költségei miatt minden egészségügyi intézménynek, ahol gépi lélegeztetés folyik, törekednie kell a VAP megelőzésére (5, 6, 20). Mivel a nozokomiális pneumónia diagnosztikája igen nehéz, ezért már a diagnosztikus kritériumok elterjesztése is haszonnal jár.
Az infekciókontroll megvalósításának alapfeltétele a nővér-beteg arány közelítése a szakmai minimumfeltételekben előírtakhoz, valamint az izoláció lehetőségének biztosítása minden intenzív osztályon.
Az irányelv használata a minőségfejlesztés eszköze is lehet (24, 34), mert a nozokomiális pneumónia arány egy jól alkalmazható infekciókontroll-indikátor.
VI. Irodalomjegyzék:
1. American Thoracic Society Documents: Guidelines for the Management of Adults with Hospital-acquired, Ventilator-associated,and Healthcare-associated Pneumonia. Am J RespirCrit Care Med 171:388-416,2005.
2. A Nemzeti Nosocomiális Surveillance Rendszer eredményei Epinfo 14. évf. 28. szám 265-273, 2007.
3. Balikó Zoltán: A nosocomiális pneumóniák: diagnosztikus és terápiás megfontolások. Infekció és Infekciókontroll II. Évfolyam 1. szám, 39-45, 2005.
4. Bán Éva, Böszörményi Nagy György, Szalka András: Alsólégúti infekciók felnőtt korban Melánia Kiadó Kft. Budapest, 2002.
5. Bergogne-Bérézin E.: Treatment and prevention of nosocomial pneumonia Chest 108: 26S-34S, 1995.
6. Bogár Lajos: Az intenzív terápiában előforduló nosocomiális pneumoniák pathogenezise és diagnosztikája. Infektológia és Klinikai Mikrobiológia 2.évf. 4.sz. 129-133,1995.
7. CDC Guidelines for Health-Care Associated Pneumonia, 2003. MMWR 53 (RR03):1-36, 2004.
8. CDC Guideline for Isolation Precautions, 2007. www.cdc.gov
9. Chastre J.: Diagnosis and treatment of nosocomial pneumonia: brochial fiberoscopy, protected brushing and/or bronchial lavage is indispensable. Rev Pneumol Clin 57 (2): 113-123,2001.
10. Craven D.E.: Epidemiology of Ventilator-Associated Pneumonia Chest 117:186S-187S, 2000.
11. De Lassence A, Ricard JD, Pigne E, Dreyfuss D.: Prevention of nosocomial pneumonia in patients treated with invasive ventilation. Rev Pneumol Clin 57 (2): 79-89, 2001.
12. Duflo F et al: Alveolar and Serum Procalcitonin, Diagnostic and Prognostic Value in Ventilator-assosiated Pneumonia. Anesthesiology 96: 74-79, 2002.
13. Fagon JY.: Epidemiology and antibiotic therapy in nosocomial pneumonia. Rev Pneumol Clin 57(2): 132-138,2001.
14. Fiel S.: Guidelines and Critical Pathways for severe Hospital-Acquired Pneumonia. Chest 119:412S-418S, 2001.
15. Fluit AC, Scmitz F.J., Verhoef J.: Frequency of isolation of pathogens from bloodstream, nosocomial pneumonia, skin and soft tissue, and urinary tract infections occurring in European patients. Eur J Clin Microbiol Infect Dis 20 (3): 188-91, 2001.
16. Gulácsi László: Minőségfejlesztés az egészségügyben Medicina Könyvkiadó Kft.- Budapest, 2000.
17. Haley W.R. et al: The efficacy of infection surveillance and control programs in preventing nosocomial infections in US hospitals Am J Epidemiol 121:182-205,1985.
18. Knaus WAetal: APACHE II:A severity of diseases classification system. Crit Care Med 13:818-829,1985.
19. Le Gall JR et al: A new simplified acut physiology score (SAPS II) based on an Europien/North American multicenter study. JAMA 270: 2957-2963,1993.
20. Lentino JR.: Nosocomial pneumonia: More Than Just Ventilator-Associated. Curr Infect Dis Rep 3(3): 266-273,2001.
21. Lynch J.P.: Hospital-Acquired Pneumonia, Risk Factors, Microbiology, and Treatment Chest 119,2 Supplement: 373-384,2001.
22. Nemzetközi Információ - A nosocomiális pneumonia megelőzése. Országos Epidemiológiai Központ, Epinfo 9. évf. 26.szám 297-306, 2002.
23. Nemzetközi Információ - A CDC újirányelvei az egészségügyi ellátással összefüggő pneumónia megelőzésére. Országos Epidemiológiai Központ, Epinfo 11. évf. 36.szám 433-442, 2004.
24. Nathwani etal: Use of Indicators to Evaluate the Quality of Community-Acquired Pneumonia Management. Clin Inf Dis 34:318-323, 2002.
25. Pechó Zoltán, Milassin Márta: Tájékoztató a fertőtlenítésről, Országos Epidemiológiai Központ Budapest, 2000.
26. Pechó Zoltán, Milassin Márta: Tájékoztató a sterilizálásról, Országos Epidemiológiai Központ Budapest, 2006.
27.Pénzes I.: Légzési elégtelenséghez vezető fontosabb kórképek. A nosocomiális pneumoniák. Aneszteziológia és intenzív terápia. Medicina Könyvkiadó Rt. Budapest 692-694,1998.
28. Ribiczey Pál: A nosocomiális pneumoniák kezelése a Zala Megyei Kórházban Therápia Antimicrobialis 1. évf. 2. sz. 39-42, 2000.
29. San Pedro G.: Are Quantitattive Cultures Useful in the Diagnosis of Hospital-Acquired Pneumonia? Chest 119.2 Supplement: 385-390, 2001.
30. Strausz János: Mintavételi módszerek és indikációjuk alsó légúti fertőzésekben. Lege Artis Medicinae 9. évf. 9. sz. 647-651,1999.
31. Soto J.G.: Diagnostic strategies for nosocomial pneumonia. Curr opin Pulm Med 13: 186-191, 2007.
32. Tájékoztató a nosocomialis surveillance során alkalmazandó módszerekről. I. rész: A nosocomiális fertőzésekdefiníciói. Johan Béla Országos Epidemiológiai Központ, Epinfo 9.évf. 3. Különszám, 2002.
33. Timsit J.F., Cheval C., Gachot B., Bruneel F., Wolff M., Carlet J., Regnier B.: Usefulness of a strategy based on bronchoscopy with direct examination of bronchoalveolar lavage fluid in the initial antibiotic therapy of suspected ventilator-associated pneumonia. Intensive Care Med 27(4): 640-7,2001.
34. Weber J.D., Raasch R., Rutala W.A.: Nosocomial Infections int he ICU: The Growing Importance of Antibiotic-Resistant Pathogens Chest 115, 34-41,1999.
35. Woolf H S: Analytic Principles in Evaluating the Performance Characteristics of Diagnostic Tests for Ventilator-Associated Pneumonia. Chest 117:182S-185S, 2000.
36. Wunderink R.G.: Clinical Criteria in the Diagnosis of Ventilator-Associated Pneumonia. Chest 117:191S-194S, 2000.
Az Egészségügyi Minisztérium
szakmai irányelve
A dohányzás leszokás támogatásáról
Készítette: a Megelőző Orvostani és Népegészségtani Szakmai Kollégium
I. Alapvető megfontolások Bizonyítékok értékelése és meghatározása:
Az alább következő megállapítások és ajánlások különböző erejű bizonyítékokon alapulnak, amelyeket - a megállapítás, illetve ajánlás végén zárójelben - A, B, C, D betűkkel jelölünk.
A bizonyítékok meghatározásai (UK NHS alapján)
A magas esetszámú randomizált és ellenőrzött vizsgálatok
B az előbbinél kisebb esetszámon alapuló randomizált és ellenőrzött vizsgálatok (az adatok alcsoport elemzésen, vagy metaanalíziseken alapuló) eredményei C Szakértői testület egyeztetett véleménye
Célkitűzés:
A dohányzás leszokás támogatás szakmai irányelvének a célja, hogy az elérhető legmagasabb szintű bizonyítékokkal alátámasztott, szisztematikusan kifejlesztett klinikai döntési ajánlások sorozatával segítse a szakembereket a legmegfelelőbb ellátás kiválasztásában, javítsa a gyógyító-megelőző munka minőségét, hatékonyságát és költség-hatékonyságát.
A szakmai irányelvérvényességi területe:
A dohányzás leszokás támogatás szakmai irányelve mindazokhoz a szakemberekhez szól, akik ezt a tevékenységet kívánják folytatni. Ugyanakkor támpontot jelent az akkreditáló hatóság részére a megfelelő szakmai munka megítélésében.
Ajánlott, hogy a leszokás támogatást végezze minden háziorvos, szakorvos, a tevékenységére jellemző keretek között. Amennyiben a nikotin függőség fennállása esetén általában szükséges időigényesebb programszerű leszokás támogatást nem képes vállalni, akkor irányítsa páciensét megfelelő szakrendelésre.
Tartalom:
1. Bevezetés
2. Háttér, epidemiológia, morbiditás és mortalitás. Dohányzás okozta egészség károsodások. A leszokás kedvező hatásai.
3. A nikotinfüggőség. Pszichiátriai betegségekés a dohányzás összefüggései.
4. A leszokás
4.1. minimál intervenció
4.2. programszerű leszokás támogatás: gyógyszermentes módszerek
4.3. programszerű leszokás támogatás: farmakoterápiás módszerek
4.4. programszerű leszokás: magatartás orvoslási terápiával
5. A leszokás mellékhatásai, a megvonási tünetek menedzselése
6. Leszokás speciális esetekben (fiatalok, terhes nők, kórházban fekvő betegek)
1. Bevezetés:
Az egészségügyi Világszervezet (WHO) felmérése szerint Földünkön napjainkban mintegy másfél milliárd ember dohányzik rendszeresen. Évente legalább öt millióan vesztik életüket dohányzás következtében, ötven százalékuk 40-69 éves koruk között hal meg, átlagosan tíz évvel megrövidítve az életüket. 2025-ben prognosztizálhatóan tíz millióan halnak meg majd a dohányzásukkal összefüggő betegségek miatt [1], éppen ezért a dohányzás elleni küzdelem a WHO egyik legfontosabb feladata lett az utóbbi évtizedben. Célul tűzte ki a dohányzás visszaszorítását világszerte: a felnőtt lakosság körében 20 százalékalá kívánja szorítani a dohányzók arányát. Ennekelérése érdekében
megalkotta a "Dohányzás-ellenőrzési Keret Egyezményt (FWTC)", amelyet az országok döntő többsége elfogadott és jogrendjébe illesztett. Az Európai Unió tagállamai az európai egészségügyi biztos ajánlására a legszigorúbb intézkedéseket hozzák a dohányzás visszaszorítása érdekében.
Magyarországon a felnőtt lakosság harmada dohányzik rendszeresen. Ez mintegy két és fél millió embert jelent. Évente közel harmincezer honfitársunkat veszítjük el a dohányzással összefüggő megbetegedés miatt. A dohányosok magas aránya és a hiányos jogszabályi védelem következtében sokan szenvednek a hasonlóan ártalmas passzív dohányzás következtében is.
Az elmúlt évtized valamennyi Népegészségügyi Programja kiemelt célként kezelte a dohányzás visszaszorításának a feladatát. Ennekérdekében be kell építeni az alaptantervbe minden korosztályban a dohányzás ártalmasságáról szóló ismeretek oktatását, hogy kevesebben szokjanak rá. A dohányosoknál pedig el kell érni azt, hogy minél nagyobb arányban akarjanak leszokni. Ennekérdekében szigorú ár és adópolitika szükséges, a média segítségével fokozni kell a leszokás előnyeinek a népszerűsítését és az európai ajánlásnak megfelelően meg kell tiltani a zárt köztéri dohányzás minden formáját. A leszokni vágyó dohányosok számára megfelelő, evidenciákon alapuló leszokási programmal és szakemberekkel rendelkező akkreditált intézményi hátteret és a leszokást támogató készítményekhez megfelelő hozzáférést kell biztosítani. Biztosítani kell a leszokás támogatás minőség ellenőrzését oly módon, hogy a nemzetközi ajánlásoknak megfelelő módszerrel, szervezetten, akkreditált leszokás támogató rendeléseken történjék a tevékenység.
A dohányzás társadalmi méretekben történő visszaszorításához számos intervenciós módszer egyidejű (komprehenzív) alkalmazására van szükség (adópolitika, reklám szabályozás, a nemdohányzók védelme, képes figyelmeztetésekés a nikotin, illetve kátránytartalom feltüntetése a cigarettás dobozokon, tájékoztatás, prevenciós és leszokást segítő programok, intenzív magatartásorvoslási tanácsadás). A cigaretta elhagyásához nyújtott segítség, a leszokás támogatása egy jól meghatározható célcsoport felé - a leszokni akaró dohányosok felé - irányul. A leszokás támogatás orvosi, tágabb értelemben véve egészségügyi kompetenciába tartozik, mivel: a dohányzás-nemdohányzás kérdését az emberek az egészség-betegség problémakörébe sorolják; a dohányzás okozta panaszok, betegségek miatt a dohányosok többsége orvosi ellátást igényel; a dohányzás következtében kialakult idült egészség károsodásokaz egészségügyi ellátó hálózatot terhelik; a dohányosok többsége nikotin függőségben, vagyis egyfajta szenvedélybetegségben szenved. A bizonyítékokon alapuló orvoslás kritériumait kielégítő és a tartósan leszokottak arányát jelentősen (25-30%) növelni képes terápiás programok alapján megállapítható, hogy:
- a közvéleményt tájékoztatni kell a dohányzás következményeiről és arról, hogy a cigaretta elhagyásához hatásos segítséget kaphatnak
- az orvosok, gyógyszerészek és egészségügyi szakdolgozók graduális és posztgraduális képzése keretében ismertetni kell a dohányzással összefüggő egészség károsodásokat és oktatni kell a dohányzásról leszokást segítő módszereket.
- minden orvosnak a rutin betegellátás keretében foglalkoznia kell a páciensek dohányzásával. A dohányzás leszokás támogatás minimál intervenciójának módszerével támogatnia kell a leszokást.
- létre kell hozni és fenn kell tartani olyan, a dohányzásról leszokást segítő szakellátást, amely mindenki által hozzáférhető.
- biztosítani kell a leszokás támogatási tevékenység finanszírozottságát, az ehhez szükséges készítmények részleges támogatását a hatékonyság növelése érdekében.
A WHO Európai Regionális Irodája által kiadott állásfoglalás szerint a dohányzásról leszokást segítő rendelés működésének alapkövetelménye, hogy a tevékenységet végző szakember a feladatnak megfelelő kiképzésben részesüljön, ezért a tevékenységért díjazást kapjon és ez a tevékenység az intézmény egyéb tevékenységeitől időben elkülönítve történjék.
A dohányzásról való leszokást segítő módszerek és az ezt biztosító intézmény rendszer kétszintű. Az első szint az un. "minimál intervenció", vagyis a dohányosok motiválása és a tanácsadás a leszokás elhatározására. A második szint a szakellátás szintje, vagyis a "programszerű leszokás támogatás", amikor speciálisan képzett szakember segítségével hosszabb időn keresztül magatartásorvoslási terápiával kombináltan történik a leszokás.
2. Háttér, epidemiológia, morbiditás, mortalitás. Dohányzás okozta egészség károsodások. A leszokás kedvező hatásai. Magyarországon a 14 évesnél idősebb lakosság 34 százaléka dohányzik rendszeresen. (a nők 28 és a férfiak 40 százaléka). Ez az EU országai közül az ötödik legrosszabb arány. Különösen sok a dohányos a fiatalabb korosztályban, hiszen a húsz évesnél fiatalabbak több, mint 40 százaléka dohányzik rendszeresen. A dohányosok aránya összességében nem csökken, sőt a nők és a fiatalok körében folyamatosan növekszik. A mai 16 éves korosztály 72 százaléka már kipróbálta a cigarettát, 16 százalékuk már függőnek mondható. A dolgozó felnőttek 53 százaléka és a fiatalok nyolcvan százaléka passzív dohányosként kénytelen elviselni a környezeti dohányfüstöt.
A dohányzással összefüggő betegségek következtében évente mintegy ötmillió ember hal meg világszerte, s ebből harmincezer Magyarországon, ami minden ötödik hazai halálesetet jelenti.
A dohányzás egészségkárosító hatásai szerteágazóak. A dohányzás hatására jelentősen fokozódik a kardiovaszkuláris megbetegedések (hipertónia, érelmeszesedés, trombózis, angina, szívinfarktus, agyvérzés, agyi érelzáródás), egyes daganatok (tüdőrák, szájüregi daganatok, gégerák, nyelőcsőrák és hólyagrák) és az idült hörgőhurut-tüdőtágulás (COPD) kockázata. Szerepet játszik a dohányzás a csontritkulás, a szürkehályog, a macula degeneráció megjelenésében is. Jelentős szövődménye a dohányzásnak a fertilitás csökkenése és az impotencia. A terhes anyák dohányzása nem csak az anya, de a magzat egészségét, életkilátásait is rontja.
A dohányzás okozta betegségek megoszlása: kardiovaszkuláris megbetegedések (41%); tüdőrák (21%); COPD (13%); egyéb daganatok (13%); egyéb légzőszervi betegségek (6%); egyéb betegségek (7%).
A tüdőrák halálozásáttekintve Magyarország világelső, s ennek a betegségnek a 90 százaléka a dohányzás számlájára írandó. Az idült hörghurut és a tüdőtágulás (COPD) előfordulásának 80 százaléka függ össze a dohányzással. A szív és érrendszeri betegségek miatti halálesetek egynegyede is a dohányzás következményének tekinthető. A dohányzás nem csak számos betegség gyakoriságát növeli meg, de a lefolyásukat is súlyosbítja. Annak a valószínűsége, hogy egy dohányos szívinfarktusban meghaljon két-háromszoros a nemdohányzók kockázatához képest. A rendszeresen napi 20 szál cigarettát elszívók körében 15-ször gyakoribb a tüdőrák és 12-szer gyakoribb a COPD, mint a nemdohányzóknál. A kockázat értelemszerűen növekszika dohányzással töltött évek és a naponta elszívott cigaretták számával.
A leszokást követően változó mértékben és idő elteltével, de egyértelműen csökken az egyes egészségkárosodások kockázata. A dohányzás abbahagyását követően már 24 óra elteltével megkezdődik a hörgők regenerációja, 72 óra elteltével érezhetően könnyebbé válik a légzés, félév elteltével mérséklődik a köhögés és a nehézlégzés. A szívinfarktus kockázata már egy év elteltével feleződik és öt év elteltével közelíti a nemdohányzók kockázatát. A tüdőrák esetében a feleződés ideje öt év és tíz-tizenöt év alatt közelíti meg a soha nem dohányzók kockázatát.
3. A nikotinfüggőség. Pszichiátriai betegségekés a dohányzás.
3.1. A nikotinfüggőség
A dohányzás komoly függőséget (addikciót) alakít ki. Amíg a dohányosoknak csak 5-7 %-a számít könnyű, azaz nem függő dohányosnak(pl. maximum 5 szál cigarettát szível egy nap),addig a dohányosok túlnyomó többségére komoly függőség jellemző [2]. Az egyszeri használatból a függő státuszba való átmenet a dohányzás esetében a legmagasabb arányú a heroin, kokain és alkohol használatához viszonyítva [3].
A nikotinfüggőség kialakulásának hátterében elsősorban a nikotin megerősítő hatása áll, amelynek alapja a nikotin stimuláló hatására a mezolimbikus jutalmazó agyi területeken (különösen a nucleus accumbensben) kiáramló dopamin [4]. Az addikció kialakulásában fontos szerepet tölt be az, hogy a dohányos a nikotinszint csökkenésével (a nikotin átlagos felezési ideje 2 óra) fellépő megvonási tüneteket az újabb nikotin bevitellel gyorsan meg tudja szüntetni.
A nikotinfüggést érdemes krónikus betegségként kezelni, mivel jellegzetesek a relapszust és a remissziót tartalmazó ciklusok. A nikotinfüggőség kezelése éppen ezért folyamatos gondozást igényel [5]. A nikotin függőség kialakulására utalhat a Fagerström féle Nikotin Dependencia Teszt is [33].
A nikotinfüggés nagyon hasonlatos más pszichoaktívszerekkel kapcsolatos függésekhez, ezek kritériumait a DSM-IV-R alapján [6] az 1. táblázatban foglaltuk össze.
1. táblázat: A nikotinfüggés jellemzői
| A nikotinfüggés DSM IV-R kritériumai |
| l. Tolerancia, amelyet az alábbiak valamelyike jellemez: |
| (a) A szer jelentősen fokozott mennyiségének az igénye az intoxikáció vagy kívánt effektus elérése érdekében. |
| (b) A szer azonos adagjának folyamatos használata esetén jelentősen csökken a hatás. |
| 2. Megvonás, amit az alábbiak egyike jellemez: |
| (a) a szerrel kapcsolatban jellegzetes megvonási szindróma (ld. megvonás A. és B. kritériumait?3.táblázat) |
| b) ugyanolyan (vagy közel hasonló) szer bevitele a megvonásos tünetek csökkentésére vagy elkerülésére. |
| 4. Állandó szer-kívánalom vagy sikertelen kísérletek a szerhasználat abbahagyására vagy kontrollálására. |
| 5. Jelentős idő és aktivitás irányul a szer megszerzésére, használatára (pl. lánc-dohányzás) vagy a hatásaitól való megszabadulásra. |
| 6. Fontos szociális, foglalkozási vagy rekreációs tevékenységek feladása vagy csökkenése a szerhasználat miatt. |
| 7. A szerhasználat folytatása olyan állandóan meglévő vagy visszatérő fizikai vagy pszichológiai problémák megléte ellenére, amiről tudja, hogy valószínűleg a szerhasználat okozza vagy súlyosbítja. |
| A dohányzással kapcsolatos specifikumok |
| A nikotinbevitel okozta kellemetlen toxikus tünetekkel szemben gyorsan kialakul a tolerancia a rendszeres dohányzás során. |
| A nikotinnal kapcsolatos intoxikáció - a szokásos használat esetében - enyhe és rövid időtartamú, rendszerint a dohányzással kapcsolatos kísérletezés időszakára korlátozódik. |
| A legtöbb dohányos eléri a maximális adagját pár hónap vagy év alatt. |
| A rendszeres dohányos napi adagja kellemetlen tüneteket okozna a kezdő használónak. |
| A reggeli első cigaretták a legjobb megerősítők. A délelőtti cigaretták nagyobb megerősítő erővel bírnak, mint a nap második felében elszívottak. |
| A nikotin bevitelének megszakításakor, vagy a bevitt mennyiségének csökkentésekor fellépnek a megvonási tünetek. |
| A dohányzás abbahagyása vagy csökkentése nagyon hamar, akár 2 órán belül kiválthat megvonási tüneteket. |
| A rágyújtást követően mintegy 10 másodperc alatt csökkennek a megvonási tünetek. |
| Hazánkban a dohányosoknak kb. 45-50 % le akar szokni, akiknek 80 %-a már meg is próbált leszokni. |
| Jellemző a dohányosok életében a leszokás többszöri sikertelen kísérlete. |
| Mindössze a dohányosok 4 %-a éri el az egyéves absztinenciát saját maga kezdeményezésére segítség nélkül. |
| Egészségi állapot rosszabbodása vagy súlyos következmények ellenére is sokszor megtartott a dohányzás. |
3.2. Pszichiátriai betegségekés a dohányzás összefüggései
Régóta ismert tény, hogy a pszichiátriai betegek körében szignifikánsan magasabb - különböző vizsgálatok szerint átlagosan kétszeres - a dohányzók aránya az egészséges populációhoz képest [7]. A krónikus skizofrén betegek legalább 60 %-a [8], a bipoláris affektív betegek közül a mániások 71%-a, a major depressziósok49%-a dohányzott egy nagy amerikai epidemiológiai vizsgálat adatai szerint [7]. Az egyéb kémiai szerfüggőségben szenvedők (drog és alkoholbetegek), valamint a nem-kémiai szerhez kötődő, ún. viselkedés-addikcióban szenvedő (pl. kóros játékszenvedély) betegek több, mint 80%-a dohányzik. A különböző addikciók egymással gyakran kombinálódnak és ez a függőségre vonatkozó közös genetikai hajlammal magyarázható.
A skizofréniában szenvedő betegek jelentős hányada dohányzik, amelynekaránya a tartósan hospitalizált betegeknél tovább emelkedik (88%-ig). Ennek hátterében biológiai és pszichológiai/környezeti (pl. szorongás csökkentés, unaloműzés) tényezők állhatnak.
A hangulatzavarok (affektív kórképek) esetében az eddigi vizsgálatok szerint oki összefüggést nem lehet kimutatni a dohányzás és a mániás és/vagy depressziósállapot között (azaz nem a dohányzás okozza az affektív zavart, és nem az affektív zavar hatására kezdenek el a betegek dohányozni), inkább közös - részben genetikai, részben környezeti -rizikófaktorok vezethetnek a magasabb koincidenciához [9].
A legújabb epidemiológiai vizsgálatok a dohányzás és az öngyilkossággal kapcsolatos fantáziák, tervek, kísérletek között is szignifikáns összefüggést találtak [10]. Ennek elemzése és magyarázata további vizsgálatokat tesz szükségessé (pl. az öngyilkosságot megkísérlők, elkövetők jelentős része pszichiátriai beteg (depressziós, alkoholfüggő, skizofrén).
Annak ellenére, hogy a nikotin függőség jelentős probléma a pszichiátriai betegek körében, a dohányzásról történő leszokásnál óvatosság, szoros pszichiátriai kontroll szükséges, mivel:
1. Önmagában a nikotin elvonás is jelentős pszichés tünetekkel járhat (szorongás, inszomnia, stb..).
2. A dohányzás abbahagyása bármilyen módszerrel, a pszichiátriai betegeknél a betegség kiújulását, rosszabbodását idézheti elő.
3. A leszokást támogató szakembernek körültekintőnek kell lennie a leszokni kívánó páciens anamnézis felvételekor és leszokási vizitjein a látens pszichiátriai kórképek kiszűrése érdekében.
Összefoglalva a pszichiátriai betegek dohányzásról történő leszokása csak stabil pszichés állapotban kezdhető meg pszichiáter szakorvos bevonásával. Az egészségesekhez képest a mentális betegeknél a leszokás folyamata hosszadalmasabb és nehezebben kivitelezhető [11].
III. Terápia
4. A leszokás
A dohányzás súlyos egészségkárosító hatásainak az ismeretében a dohányzó pácienseknek ajánlani kell a leszokást. Ennek módját a leszokni kívánó dohányos közeli és távoli anamnézise alapján a pácienssel közösen szakembernek tanácsos meghatároznia. A dohányzás mértéke és időtartama, a nikotinfüggőség foka, az ismert, vagy feltételezett társbetegségek, különös tekintettel a pszichiátriai betegségekre, a páciens kora, állapota, esetleges terhessége mind megannyi tényező, amelyek befolyásolhatják a megfelelő leszokási módszer megválasztását, ajánlását. A leszokás támogatás folyamatát nemzetközileg az"5A" módszerrel határozhatjuk meg. Ezt illusztrálja a folyamatábra (1.ábra). Ask=kérdezzük; Advise=tanácsoljuk; Assess=Erősítsük; Assist=támogassuk; Arrange follow up=kövessük magyarul. Az ábrán a leszokás támogatás folyamata látható, magyarítva az egyes lépéseket [12]
A LESZOKÁS TÁMOGATÁS FOLYAMATA
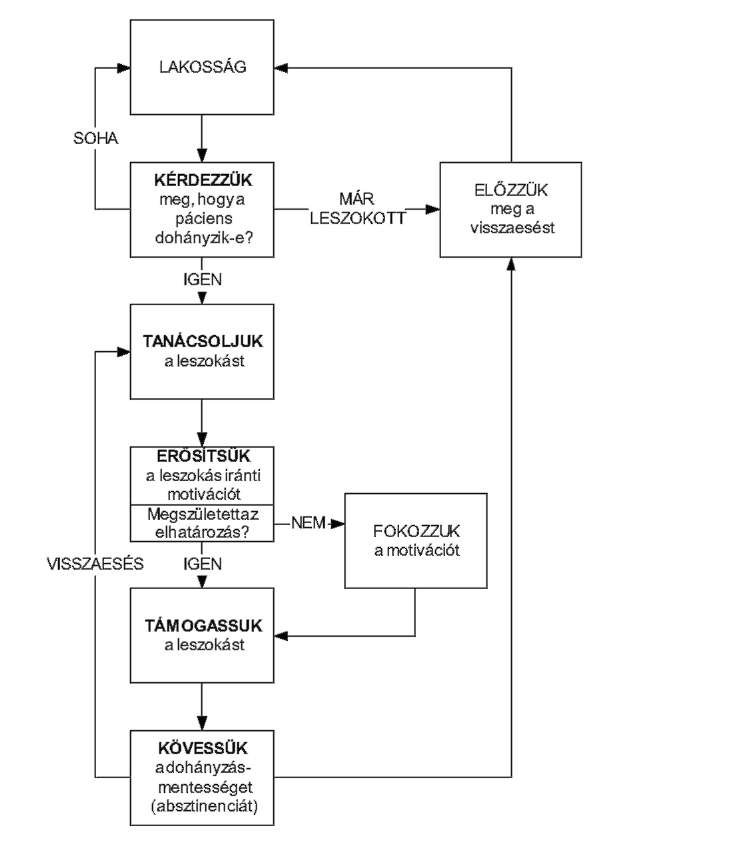
A fent meghatározott körülmények figyelembe vételével, különös tekintettel a nikotin függőség fokára a leszokás támogatásnak különböző módszerek lehetségesek. Ezek a minimál intervenció, illetve a programszerű leszokás támogatáson belül a gyógyszermentes és a farmakoterápiás módszerek.
4.1. Minimál intervenció
4.1.1. A minimál intervenció meghatározása
Valamennyi orvosnak kötelessége, hogy a páciensekkel történő találkozáskor rákérdezzen azokdohányzási szokásaira, ha dohányoznak, akkor tanácsolja a dohányzás abbahagyását (A típusú bizonyíték) [13]. Erősítse meg a leszokási szándékot, a motivációt. Ez a három tevékenység határozza meg alapvetően a "minimál intervenciót". Ez jelenti a leszokás támogatás első szintjét,
kevésbé időigényes, minta programszerű leszokás támogatás, az esetek egy részénél azonban megfelelő lehet, illetve bevezetheti a későbbi második szintű programszerű leszokás támogatást.
Az alapellátásban dolgozó orvosok, szakdolgozók, gyógyszerészek találkoznak leggyakrabban a betegekkel, egészséges páciensekkel. Nekik van leginkább lehetőségük arra, hogy felderítsék dohányzási szokásaikat, kezdeményezzék és elősegítsék a dohányzás abbahagyását. Bizonyíték van rá, hogy a minimál intervenció alkalmával rákérdezve a dohányzási szokásokra, ajánlva a leszokást, az erősíti a leszokás motivációját és ezen keresztül a leszokás sikerességét (A típusú bizonyíték) [14,15].
4.1.2. A minimál intervenció struktúrája
Ez a minimális vagy rövid intervenció meghatározott elemekből áll, amelyek alkalmazása időkímélő és maximalizálja az intervenció hatásosságát. A "rövid tanácsadás" magában foglalja az eseti tanácsadást, a dohányzásról történő beszélgetést, a leszokással kapcsolatos motiváció erősítését. A páciens-orvos találkozó, az intervenció időtartama (minimálisan 3 perc) hossza egyenesen arányos annak hatásosságával (A típusú bizonyíték) [13]. A minimál intervenció egyénre szabott kell, hogy legyen, így az adott helyzetben az adott dohányos részére nyújtott tanácsadást számtalan tényező befolyásolhatja: az egyén leszokás melletti elkötelezettsége, milyen mértékben fogadja el a tanácsadást, korábbi leszokási kísérletek során szerzett tapasztalatok. A "rövid tanácsadás" tartalmazza:
- a dohányzás abbahagyására történő tanácsot
- a dohányos leszokás melletti elkötelezettségének felmérését
- nyomtatott anyagok átadását
- a gyógyszeres terápia és/vagy pszichés támogatás felajánlását
- szükség esetén leszokási centrumba történő irányítást
Minden dohányosnak javasolni kell a leszokást (speciális élethelyzetekben lehetnek kivételek), dohányzási szokásait rögzíteni kell az egészségügyi dokumentációban. Azon dohányosokat, akik még nem készek a dohányzás abbahagyására, bíztatni kell a leszokás megfontolására. A dohányzással összefüggésbe hozható betegségben szenvedő, jelenleg is dohányzó betegekesetében a tanácsadás térjen ki a betegség és a dohányzás kapcsolatára [16]. A minimál intervenció célja az, hogy felderítsék a rendelésen megjelenő valamennyi páciens dohányzási helyzetét, azonosítsák a dohányzókat és közülük azokat, akik hajlandók a közeljövőben (pl. egy hónapon belül) abbahagyni a dohányzást. Az első lépésben ezekre a páciensekre érdemes figyelni. A nemdohányzók között célszerű azonosítani azokat, akik korábban dohányoztak, de már leszoktak (relapszus-prevenció). Az aktuálisan dohányzó, de jelenleg leszokni nem szándékozó pácienseknek is javasolni kell a dohányzás abbahagyását - jelezve számukra, hogy az orvosnak szándékában van később visszatérni a kérdésre. Ennek a "visszatérésnek" - azaz a páciens dohányzási helyzetével történő foglalkozásnak- a lehető leggyakrabban, de évente legalább egy alkalommal meg kell történnie. A fenti kategóriákat a dokumentációban jól felismerhető módon jelölni kell és a páciensek dohányzását a későbbiekben figyelemmel kell kísérni.
4.1.3. A minimál intervenció lépései
1. A dohányzási helyzet és a nikotinfüggőség mértékének meghatározása
2. Ha aktuálisan dohányzik a beteg, javaslat a dohányzás abbahagyására
3. A leszokási motiváltság felmérése - mennyire akarja abbahagyni a cigarettázást?
Társbetegségek, különös tekintettel a pszichiátriai betegségekre, feltérképezése és a páciens követése valamennyi leszokási tevékenység szerves része, így minimál intervenció esetében is indokoltak. Ennek során sor kerülhet a tartós absztinencia esetén a siker méltatására, kudarc esetén bátorításra, újabb leszokási kísérlet kezdeményezésére, az esetleges felmerülő kérdések megbeszélésére
4.1.4. A különböző szakemberek szerepe
4.1.4.1. Az orvos szerepe
Minden orvosnak, aki részt vesz a klinikai betegellátásban (alap-ellátás, járó- és fekvőbeteg szakellátás) alapfeladata, hogy foglalkozzon minden beteg dohányzási helyzetével és nyújtson segítséget számára a dohányzás abbahagyásához.. A járóbeteg szakellátás orvosa és a kórházi orvos rendszerint csak egy rövid időszakban van kapcsolatban a beteggel. Az általuk végzett intervenció sikeressége szempontjából előnyös egy esetleges súlyos akut történés (pl. koronária betegség), mert a legtöbb beteg ilyenkor fogékonyabb az életmód változtatásra és ezt a helyzetet ki kell használni a dohányzás abbahagyásának elérésére. A szakellátás orvosainak azonban kevésbé van lehetőségük a beteg tartós követésére. Ez alól kivétel krónikus betegség esetén (COPD, diabetes...) a beteg tényleges gondozását végző szakorvos.
A dohányzásról leszokást segítő intervenció szempontjából kitüntetett helyzetben vannak az alapellátás szereplői (háziorvos, fogorvos, védőnő, iskola egészségügyi szolgálat). Ők vannak folyamatos kapcsolatban a pácienssel, ismerik életkörülményeit, kórelőzményét, családi anamnézisét. Egy 25 országra kiterjedő EU tanulmány (PESCE)[47] megállapítása szerint a háziorvos által a dohányzó beteg számára nyújtott segítség a cigaretta elhagyásához a legjobb költség-hatékonyságú prevenciós tevékenység, jelentős egészségbeli és gazdasági előnyt eredményez össztársadalmi szinten.
4.1.4.2. A védőnő szerepe
Bizonyos élethelyzetekben (várandósság, kisgyermekes anyák) a védőnő kerül legközelebb a családokhoz és a gyermekérdekére hivatkozás nagyon hatásos motivációs tényező lehet a dohányzás abbahagyásában - elsősorban az anya, de a többi családtag esetében is. Célszerű ezért ha ő is képes a leszokást segítő rövid intervenció végrehajtására.
4.1.4.3. A szakdolgozó szerepe a rövid intervenció végrehajtásában
A mindennapos betegellátás körülményei között az orvosnak kevés ideje és lehetősége van arra, hogy a beteg dohányzásával, annak részleteivel hosszasan foglalkozzon. Bár bizonyítékok vannak arra, hogy az intervenció sikeressége egyenesen arányos annak időtartamával, de struktúrált program alkalmazásával és munkamegosztással már rövid idő (3-5 perc) alatt is eredményes intervenció végezhető. Az orvos és a nővér közötti munkamegosztással jelentős mértékben növelhető a tevékenység és hatékonysága [17]. A nővér feladata lehet
- A dohányosok kiszűrése
- a dohányzási helyzet meghatározása,
- a páciensek csoportosítása,
- a páciens esetleges kérdéseinek megválaszolása,
- leszokást segítő készítmények alkalmazásának részletes ismertetése,
- a dokumentáció kezelése.
Rendkívül fontos, hogy az intervenciót végző maga ne dohányozzon. Felmérésekszerint a dohányzó orvos, vagy nővér nem fektet elég hangsúlyt a dohányzás okozta egészségkárosodás hangsúlyozására és a beteg dohányzás leszokását segítő intervencióra.
4.2. Programszerű leszokás támogatás: gyógyszermentes módszerek
A páciens motivációja: A leszokás támogatásának gyógyszermentes módszerei alkalmazása során alapvető fontosságú a páciens motivációjának ismerete, mivel eltérő stratégiák alkalmazandók a leszokásra motivált és nem motivált dohányosoknál. Ugyanakkor az orvosi tanácsa és a minimál intervenció minden dohányosnál alkalmazandó.
4.2.1. A nem gyógyszeres támogatási formák a leszokásra motiváltak esetében
Az egészségügyben is alkalmazható nem gyógyszeres támogatás számos formája ismeretes, ezek csoportosíthatók a hatékonyságuk tekintetében rendelkezésünkre álló bizonyítékok mentén:
| A bizonyíték mértéke |
| Bizonyítottan hatékony módszerek - A szintű evidencia |
| Nincs elégséges bizonyíték a hatékonyságukról, további vizsgálatok szükségesek. Mindaddig azonban, amíg nem |
| állnak rendelkezésre bizonyítékok úgy kell állást foglalni, hogy hatástalanok. |
| Módszer[18] |
| - Orvosi tanács és minimál intervenció OR=1,3 [1,0-1,6](19) |
| - Önsegítő anyagok (OR=1,24 [1,07-1,45](19,20), 'testre szabott' önsegítő anyagok esetében OR=1,42 [1,26-1,61](20)) |
| - Intenzív egyéni tanácsadás (OR=1,7 [1,4-2,0](19) illetve OR=1.62 [1,35 - 1,94](21)) |
| - Intenzív csoportos tanácsadás (OR=1,3 [1,1 - 1,6](19) illetve OR=2,17 [1,37 - 3,45](22)) |
| - Proaktív telefonos tanácsadás (OR= 1,2 [1,1-1,4](19) illetve OR=1,41 [1,27-1,57](23)) |
| - Hipnoterápia(24) |
| - Akupunktúra és hozzá kapcsolódó újabb eljárások(25) |
| - Averzív kondicionálás (26) |
| - Biofeedback (a dohányzás negatív következményeinek műszeres visszajelzése, pl. CO mérés, spirometria)(27) |
| - Kiegészítő testedzésprogramok (28) |
| - Nicobrevin (29) |
A bizonyítottan hatékony gyógyszermentes intenzív módszerek egyaránt hatékonyak az addikció enyhébb és súlyosabb formáiban szenvedőknél, éppen ezért alkalmazásukat nem szabad kizárólag a súlyos esetekre korlátozni. A nem gyógyszeres módszerek kombinációjával a leszokás sikeressége növelhető, bár a kutatások erre vonatkozóan csakelvétve találhatók. Éppen ezért ajánlott az intenzív kezeléseket kombinációban alkalmazni. Az egyes kombinációk relatív hatásosságának vizsgálataira nincs külön-külön adat.
A nem gyógyszeres támogatás jellemzői a leszokásra motiváltak esetében
Egyéni, csoportos és telefonos tanácsadás egyaránt bizonyíthatóan növeli a leszokás esélyét, ugyanakkor a kezelés hatékonysága szorosan összefügg a kezelés tartalmával és intenzitásával. A kezelés intenzitásának indikátorai a találkozások száma, időtartama és tartalma:
- A találkozások száma: A kezelés során történő találkozások száma minimálisan 4 alkalom, optimálisan 8 alkalom, amit hosszú távú követés egészíthet ki. A 8 alkalomnál több találkozó nem növeli meg szignifikánsan a leszokás esélyét a 4-8 alkalomhoz képest.
- A találkozások időtartamának növelésével a leszokás esélye is növekszik. Az intenzív kezelések minimálisan 10 perc tanácsadási időt tételeznek fel.
- A tanácsadás során hatékonynak tartott komponensek a praktikus problémamegoldási készségek fejlesztése és a társas támogatás nyújtása a kezelés során. Ugyanakkora viselkedésterápia/magatartásorvoslás más elemei (relaxáció, ingerkontroll) részét képezhetik a problémamegoldás fejlesztésének. A problémamegoldás fejlesztése során ki kell térni a következőkre:
- A kihívást jelentő helyzetek felismerése
- A dohányzásra való késztetéssel való megküzdés készségeinek fejlesztése
- A stressz kezelésének fejlesztése
- A visszaesés megelőzése
4.2.2. Tanácsadás módja a leszokásra nem motivált dohányosoknál: A leszokásra motivált és a leszokásra nem motivált dohányosok eltérő kezelési megközelítést igényelnek. A minimál intervenció mellett a tanácsadás során a leszokásra nem motivált pácienseknél a páciensre orientált motivációs interjú módszereivel a leszokás motivációjának erősítésére van szükség. A motivációs interjú alapelemei [30,31]
- Az empátia kifejezése
- Az ellentmondásosság (diszkrepancia) felismertetése
- A vita kerülése
- Az ellenállás feldolgozása
- Az önbizalom támogatása és erősítése
A motivációs interjú ugyanakkor csak előkészíti, motiválja a pácienst a leszokásra, nem helyettesíti a leszokás intenzív támogatását. A leszokásra nem motivált dohányosokesetében tehát első lépés a motiváció kialakítása, majd a motivált dohányosok esetében használt kezelési/támogatási eljárások alkalmazása.
Amennyiben a tanácsadó nem képzett a motivációs interjú alkalmazásában, a leszokásra nem motivált dohányosokkal való foglalkozás során segíteni kell azonosítani és felismerni a következőket:
- a leszokás személyes fontossága a páciens számára.
- a dohányzás potenciális akut és hosszú távú veszélyei, valamint a dohányzás veszélyei a környezetében élőkre.
- a dohányzásról való leszokás potenciális nyereségei a páciens számára
- a leszokást akadályozó tényezők azonosítása és megoldási lehetősége.
4.2.3. A nem gyógyszeres és a gyógyszeres támogatás kombinációja
Az egyéni, csoportos és telefonos tanácsadás hatékonyságát növeli a gyógyszeres kezeléssel való kombinációja (A-típusú evidencia OR=1,7 [1,3-2,1](19) a csak tanácsadási helyzethez viszonyítva) és viszont a gyógyszeres kezelés hatékonyságát növeli a tanácsadás (A-típusú evidencia(19) OR=1,4 [1,2-1,6](19) a csak gyógyszeres kezeléshez viszonyítva). Éppen ezért a tanácsadásban résztvevőknek minden esetben - ha azt kizáró orvosi indokok nincsenek -fel kell ajánlani a gyógyszeres támogatást is. Amennyiben a tanácsadást nem orvos végzi, akkor - a kliens belegyezésével - a tanácsadónak konzultálnia kell a kliens kezelőorvosával. Ezzel párhuzamosan a gyógyszeres kezelés során, fel kell ajánlani az intenzív egyéni, csoportos és telefonos tanácsadás lehetőségét ott, ahol erre megfelelően képzett szakember valamint szakrendelés rendelkezésre áll. Gyógyszeres kezelés és az intenzív tanácsadás hatékonysága egyenes arányban nő a tanácsadási alkalmakszámával(19), éppen ezért - amikor csak lehet
- a gyógyszeres kezelést több intenzív tanácsadási alkalommal is ki kell egészíteni.
4.2.4. Kik végezzenek leszokást támogató tanácsadást
A dohányzásról való leszokás nem gyógyszeres támogatását egyaránt hatékonyan végezhetik orvosok, pszichológusok, nővérek [19,32]. A hatékonyságot növeli, ha több szakma képviselője vesz részt a leszokás támogatásában egymást kiegészítő kezeléseket nyújtva [19].
- Az egyéni, csoportos és telefonos tanácsadást végző szakembereknek (orvosok, nővérek, pszichológusok, más magatartásorvoslási szakembereknek) rendszeres képzésében ajánlott kitérni a következőkre:
- dohányzásról leszokást támogató bizonyítékon alapuló módszerek
- az egyéni, csoportos és telefonos tanácsadás alapelvei
- a nikotinfüggés, a leszokásra való motiváltság és a leszokás szempontjából lényeges kofaktorok (pl. depresszió) szűrésére használható eszközök, módszerek
- a dohányzásról való sikeres leszokásban szerepet játszó tényezők
- a dohányzással és leszokással esetenként együttjáró állapotok (pl. depresszió, negatív érzelmek) pszichológiai és gyógyszeres kezelésének módszerei
4.3. Programszerű leszokás támogatás: farmakoterápiás módszerek
A dohányzás abbahagyását a nikotin függőség, a dohányzás abbahagyását követően bekövetkező nikotin megvonási tünetek nehezítik meg. Azoknál a dohányosoknál, akiknél közepes, vagy erős nikotin függőség állapítható meg nagy valószínűséggel ki is alakulnakezek a tünetek. Emiatt ezekben az esetekben nem elég pusztán "akaraterejükre", vagy a gyógyszermentes módszerekre támaszkodni a leszokás során. Ilyenkor indokoltak a különböző farmakoterápiás módszerek.
A farmakoterápiás módszereknek két típusa ismert: a nikotinpótló terápia és a nikotin mentes készítmények használata. A szakembernek és a páciensnek közösen kell meghatároznia, több körülmény figyelembe vételével a megfelelő módszert.
4.3.1. Nikotinpótló terápia
Nikotin függőség esetén alkalmazandó készítmények. Általában 8-12 héten keresztül fokozatosan csökkenő dózisban juttathatunk többféle módon nikotint a szervezetbe. Ennek hatására csökkennek a nikotin megvonási tünetek (A típusú bizonyíték)[13,33,34]. Nikotinpótlásra használt készítmények a transzdermális tapasz (A típusú bizonyíték), a rágógumi (A típusú bizonyíték), a szopogató tabletta, az orrspray, az inhaláló (A típusú bizonyíték) és a nyelv alá helyezhető tabletta. Magyarországon jelenleg a tapasz, a rágógumi és a szopogató tabletta van forgalomban, amely vény nélkül megvásárolható (OTC készítmény). Vannak 16 és 24 órás tapaszok, de ezek effektusa között nincs szignifikáns különbség.
A nikotinpótló terápiák hatásossága placebo kontrollal szemben:
| Nikotinpótló terápiák összességében: | OR:1,73 (1,60-1,82). |
| Nikotinos rágógum | OR: 1,63 (1,49-1,79) |
| Nikotin tapasz | OR: 1,73 (1,56-1,93) |
| Nikotinos orrspray | OR: 2,27 (1,61-3,20) |
| Nikotinos inhaláló | OR: 2,08 (1,43-3,04) |
| Nyelv alá helyezhető tabletta | OR: 1,73 (1,07-2,80) |
| Nikotinos szopogató tabletta | OR: 2,10 (1,59-2,79) |
A nikotin pótló terápia kombinálható bupropionnal (A típusú bizonyíték) [35] Nikotin pótló tapasz+bupropion OR: 2,65 (1,58-4,40)
4.3.2. Nikotinmentes készítmények
4.3.2.1. Bupropion
A bupropiont eredetileg anti-depresszáns szerként alkalmazták, később figyelték meg azokat a hatásait, amelyek alapján effektívnek bizonyult a dohányzás leszokás támogatás terén (A típusú bizonyíték) [13]. A bupropion SR kettős hatásmechanizmusával emeli a dopamin és a noradrenalin szintjét, valamint lassítja ezek visszavételét a szinaptikus résekből. Így enyhíti a rágyújtásra késztetést, a sóvárgást. Csökkenti a megvonási tüneteket. Bupropion hatásfoka placebo kontrollhoz képest: Bupropion OR: 1,94 (1,72-2,19)
A bupropion jelenleg Magyarországon nincs törzskönyvezve dohányzás leszokás támogatásra.
4.3.2.2. Vareniklin
A vareniklin parciális agonista és antagonista hatása révén csökkenti a nikotin éhséget, csökkenti a megvonási tüneteket. Jelenleg ez a leghatékonyabbnak tekinthető leszokás támogató készítmény (A típusú bizonyíték)[36]. Hatásfoka meghaladja a placebot és a bupropiont egyaránt. Parciális agonista hatása részleges dopamin felszaporodást eredményez, ami csökkenti a megvonási tüneteket, antagonista hatásával pedig kompetitive gátolja a nikotin receprorokat. A dohányos hiába szívja el a cigarettát, a nikotin nem képes kötődni a receptorhoz. Ez azt eredményezi, hogy a "jutalmazási" érzés kevésbé lesz intenzív, vagy el is maradhat.
12 hetes terápia javasolt, de ez meghosszabbítható, ami javítja az effektivitást. Biztonságos és effektív módszer. Vareniklin hatásfoka a placebo kontrollhoz képest:
Vareniklin OR: 3,22 (2,43-4,27)
A 2. táblázatban [37] az egyes farmakoterápiás készítmények jellemzői láthatók.
| Farmakoterápiás készítmény | Kontraindikáció | Mellékhatás | Dózis | Kezelés időtartama | Elérhetőség | Monoterápia effektivitása (becsült absztinencia az elhagyást követően) | Kombinációs lehetőség | |
| 6 hónap | 12 hónap | |||||||
| Nikotin tapasz | 14 év alatt | lokális bőr irritáció insomnia | 21 mg/24 óra 14 mg/24 óra 7 mg/24 óra 15 mg/16 óra 10 mg/16 óra 5 mg/16 óra | 4 hét 2-4 hét 2-4 hét (dózisok szerint) teljes kezelés: 8-12 hét | OTC (recept nélkül) | 23.4-26.5 | 20.3 | nikotin rágógumi bupropion |
| Nikotin rágógumi | 14 év alatt | dyspepsia szájnyálkahártya irritáció | 1 -24 cigaretta/nap esetén: 2 mg (max 24 db/die) =25 cigaretta/nap esetén: 4 mg (max 24 db/die) | 8-12 hét | OTC (recept nélkül) | 19.0-26.1 | 8.2-11.2 | nikotin tapasz |
| Bupropion SR (Magyarországon jelenleg nem törzskönyvezett dohányzás leszokás indikációban) | epilepszia táplálkozási rendellenesség | insomnia szájszárazság görcs | 3 napig 150 mg reggel, majd 2x150 mg (kezelést 1-2 héttel a cigaretta letétel előtt érdemes kezdeni) | 8-12 hét mely 6 hónapig kiterjeszthető | vényköteles | 24.2 | 16.1 | nikotin tapasz |
| Vareniklin | veseelégtelenség dialízis | nausea alvási rendellenesség (vivid/furcsa álmok) | 0.5 mg 3 napig, 2x0.5 mg 4 napig, majd 2x1 mg (kezelést a 1 héttel a cigaretta letétel előtt érdemes kezdeni) | 12 hét mely 6 hónapig kiterjeszthető | vényköteles | 33.2 | 26.1 | |
4.4. Programszerű leszokás támogatás, magatartásorvoslási terápiával
A leghatékonyabb az, ha a hatékony készítményeket programszerű leszokás támogatás keretében magatartásorvoslási terápiával kombináltan alkalmazzuk. A program általában három hónapig tart. Ennek keretében több alkalommal találkozik a páciens a leszokást vezető szakemberrel. Leszokási vizitekre és követési vizitekre kerül sor. A kilélegzett levegő szénmonoxid szintjének a mérése kontrollálja a nikotin absztinenciát.
4.4.1. Dohányzási anamnézis felvétele
Az első találkozáskor kerül sor a dohányzási anamnézis felvételére, a nikotin függőség meghatározására, a társbetegségek feltérképezésére. Különös gondossággal kell eljárni az esetleges neurológiai és pszichiátriai betegségek megállapításának a terén. A pszichiátriai megbetegedések fennállásának még a gyanúja esetén is pszichiáter szakvéleményét kell kérni a cigaretta letevése, a nikotin megvonása előtt. Elvégzendőek a fizikális vizsgálatok, testsúlymérés, amihez majd viszonyítani lehet a jövőben a tényleges testsúlygyarapodást. EKG-t kell készíteni, vérnyomást kell mérni. Ezen a megbeszélésen a pácienssel közösen kell meghatározni a számára vélhetően leghatékonyabb leszokási módszert és az un. "stop napot", vagyis azt a napot, amikor leteszi a cigarettát.
4.4.2. Leszokási vizitek
A rendelések egységes módszereket (nikotin dependencia teszt, egyéni foglalkozás, csoportos foglalkozás, gyakorlati tanácsadás, nikotin függőség és megvonási tünetek kezelése) és dokumentációt alkalmaznak. A program időtartama általában három hónap, de erős függőség esetében - különösen a vareniklin esetében - ez hat hónapra meghosszabbítható. Ez idő alatt rendszeresen kerül sor követési vizitekre (szakember-páciens találkozások 1-3 hetente). Ezek időtartama minimálisan öt-tíz perc. A teendő a dohányzás/nem dohányzás tényének megállapítása, testsúlymérés, kilélegzett levegő szénmonoxid mérése, az időközben felmerült nehézségek megbeszélése, a meghatározott készítmény felírása. A program szoros követéssel történik. Ha nem jelenik meg a páciens, akkor az orvos, vagy az asszisztense telefonon kapcsolatba lép vele.
4.4.3. Követés
A program megkezdésétől számított 4, 6 és 12 hónap elteltével interjúra hívják a pácienst. A követési viziteken a dohányzás/nem dohányzás tisztázása mellett a kilélegzett levegő szénmonoxid mérésére, testsúlymérésre kerül sor. A program kiértékelésére 12 hónap elteltével kerül sor. Leszokott dohányosnak azt tekinthetjük, aki 12 hónap elteltével sem gyújt rá. Ha visszaesett időközben a páciens ismét felajánljuk neki a segítségünket, a programba történő bekapcsolódást [49].
5. A leszokás mellékhatásai, a megvonási tünetek menedzselése 5.1. A nikotin megvonási tünetek
A dohányzásról való leszokást kísérő megvonási tünetek komoly akadályai lehetnek a sikeres leszokásnak és fő okozói a relapszusnak, a visszaesésnek. Kiemelt figyelmet érdemelnek, mivel sokszor az ezektől való aggodalom tartja vissza a dohányost a leszokástól. A dohányzás abbahagyását követően 24-48 óra között a legerősebbekés néhány naptól akár több hetes időtartamig is eltarthatnak. A megvonási tünetek diagnosztikus kritériumait a DSM-IV-R alapján a 2. táblázat mutatja be [6]. További megvonási tünetek lehetnek még az erős sóvárgás a cigaretta után, gasztrointesztinális diszkomfort érzés, obstipáció. A tünetek előfordulási gyakoriságát és fennállásának várható időtartamát a 3. táblázat mutatja be.
3. táblázat: Pszichoaktív szer (nikotin) megvonás DSM-IV kritériumai
| A. A szer-specifikus szindróma kialakulása valamely szer prolongált vagy nagyfokú használatának a megszakadása vagy redukálása következtében jött létre. B. A szer-specifikus szindróma klinikailag jelentős zavart vagy károsodást okoz a szociális, foglalkozási vagy egyéb fontos működésekben. C. A tünetek nem felelnek meg valamely általános betegségi állapot kritériumainak és nem magyarázhatók meg jobban más mentális zavarral. A nikotinmegvonásos tünetei, tünetegyüttese a DSM-IV rendszerben 1. diszfóriás vagy depressziós hangulat |
| 2. inszomnia 3. irratibilitás, frusztráció, düh 4. szorongás 5. koncentrációs nehézségek 6. nyugtalanság 7. szívritmus csökkenése 8. fokozott étvágy vagy súlygyarapodás |
5.1.1. A nikotinmegvonás tünetei, és előfordulási gyakorisága [46]
| Tünet | Időtartam | Gyakoriság |
| Irritábilitás, ingerlékenység | <4 hét | 50% |
| Deprimált, lehangolt hangulat | <4 hét | 60% |
| Pszichomotoros nyugtalanság | <4 hét | 60% |
| A koncentráció zavara | < 2 hét | 60% |
| Az étvágy fokozódása | > 10 hét | 70% |
| Alvászavar | < 1 hét | 25% |
| Sóvárgás | > 2hét | 70% |
| Bradikardia | > 10 hét | > 80% |
| Obstipáció | > 4 hét | 17% |
5.1.2. A nikotin megvonás tüneteinek kezelése
A megvonási tünetek kezelése során elsősorban a támogató jellegű pszichoterápiás instrukciók mellett készségfejlesztést alkalmazható. A nikotinmegvonás tüneteinek átértelmezését érdemes javasolni a pácienseknek, miszerint a megvonási tünetek viszonylag rövid ideig tartanak, átmenetiekés elsősorban azt tükrözik, hogy a szervezet és az idegrendszer "gyógyulási" folyamatát képezik.
Amennyiben a tünetek intenzitása szükségessé teszi, akkor szorongás, irritábilitás, deprimált hangulat és/vagy alvászavar esetén nagypotenciálú benzodiazepin (alprazolam, clonazepam) beállítás indokolt, de orvosi kontroll mellett és limitált időtartamban (max. 6 hétig, és utána pszichiáter szakorvossal történő konzultáció alapján folytatható - szükség esetén). Az alvászavar (éjszakai felébredések) kezelésére korszerű elaltató és/vagy átaltató hipnotikumok alkalmazhatók szintén limitált időhatárokon belül.
5.2. A testsúly növekedése
A megvonási tünetek között a testsúlygyarapodásra kiemelt figyelmet kell fordítani, mivel a páciensek többségében a testsúly növekedése vagy az attól való félelem a leszokással szemben lényeges visszatartó erő és a relapszushoz vezető egyik legfontosabb tényező a férfiaknál és nőknél egyaránt [38].
Egyéves folyamatos absztinencia esetén a dohányzásról való leszokással magyarázható súlygyarapodás 4,8-5,9 kg [39] között van. A testsúlygyarapodás a leszokást követő 2 éven belül éri el a maximumát, majd ezt követően visszatér az alapszintre, azaz nem különbözik a nemdohányozók súlygyarapodásához viszonyítva [40], továbbá hosszú távon a testtömeg index növekedése elhanyagolható [41]. A testsúlygyarapodás egészségi veszélyei messze elhanyagolhatók a leszokással nyerhető egészségi előnyökhöz viszonyítva. A testsúlygyarapodás hátterében számos mechanizmus tételezhető fel, különösen az alapanyagcsere szint csökkenésének és az étvágy növekedésének lehet központi szerepe. Bár általános az egyetértés abban, hogy a testsúlygyarapodás mérsékelhető, nincs A-típusú bizonyíték a testsúlygyarapodás megelőzésére. B típusú bizonyítékok vannak arra, hogy nikotinpótló terápia és a bupropion csupán késlelteti a testsúlygyarapodást [5]. Általánosan az energia egyensúllyal kapcsolatos tanácsadás a táplálkozás megváltoztatására, az alkoholfogyasztás mérséklésére és a fizikai aktivitás növelésére kell irányulnia.
6. Leszokás speciális esetekben
(Speciális, magas rizikójú paciens csoportok dohányzása és leszokása)
A dohányzás abbahagyása minden dohányos érdeke. Vannak azonban olyan csoportok, akiknél egyrészt koruknál (pl. a serdülők, vagy fiatal felnőttek), vagy állapotuknál (pl. a terhes nők) a dohányzás leszokás támogatás, a megfelelő módszer kiválasztása a szokásosnál is fokozottabb körültekintést kíván. Külön szakaszban (3.2.) foglalkozunk a pszichiátriai betegek, illetve a fel nem ismert un. látens pszichiátriai betegek leszokásának a kérdésével.
6.1. Nők
Ugyanaz a dohányzás leszokás támogatási stratégia hatékony nők és férfiak esetében egyaránt. Ezért, a terhes nők kivételével nőkben ugyanazon eljárás követendő, mint férfiakban (B szintű evidencia).
Fiatal korban több nő dohányzik, mint férfi, felnőttkorban pedig gyakran az elhízástól való félelem miatt a nőksokszor kevésbé hajlandóak leszokni mint a férfiak Így a serdülő korukban már cigarettázó lányokból dohányos nők válnak. A dohányzás megváltoztatja az ösztrogén metabolizmusát praemenopauzában és menopauzában is. A csökkent ösztrogén szint következtében megnövekszik a szív és érrendszeri megbetegedés kockázata. A középkorú dohányos asszonyoknál atherogen lipid profilt és gyakoribb koszorúér megbetegedést és annak klinikai megjelenési formáit lehet kimutatni. Az erős dohányos nők kardiovaszkuláris veszélyeztetettsége többszöröse a nemdohányzókénak (A típusú evidencia)[42]. A menopauza korú nőkszívpanaszai különbözneka férfiakétól és sokszor kevésbé jellegzetesek, emiatt mind a konzervatív mind az invazív kezelési módokban kevésbé részesülnek mint a hasonló korú férfiak. Mikor a betegség felfedezésre kerül az állapot már gyakran előrehaladott, a szövődmények súlyosabbak. Az egyébként egészséges nőkben az aorta meszesedése korrelál az elszívott cigaretták számával. A dohányzás abbahagyásával az aorta kalcifikáció csökken.
Az adatok szerint a nőkgyakrabban kérnekés fogadnak el segítségeta leszokásban kinyilvánított küzdelemhez minta férfiak. Mivel a nők hajlamosabbak az elhízásra, a depresszióra és a hormonális ciklus is jobban meghatározza a kedélyállapotukat fontos figyelembe venni ezeket a tulajdonságokat is a leszokási metodika kiválasztásánál. A nők számára természetesen ugyanolyan fontos a dohányzás abbahagyása, mint a férfiaknak és életkilátásaik ugyanúgy javulni fognak. (A tipusú evidencia)
6.2. Terhes és szoptató nők
A dohányzásnak a terhes nőkre és magzatra gyakorolt káros hatása miatt, a terhes nőknek a leszokás támogatással kapcsolatos minimális intervenciót meghaladó mértékben kell pszichoszociális leszokás támogatást nyújtani (A szintű evidencia).
Bár a dohányzás abbahagyásának legnagyobb haszna akkor van, ha ez még a terhesség előtt, de legalább is a legelején történik meg, a cigaretta letétele bármely időpontban fontos és hasznos mind az anya, mind a magzat szempontjából, így a terhesség előtt és alatta végig a leszokási segítséget folyamatosan biztosítani kell személyes tanácsadás és konzultáció formájában (B szintű evidencia).
Ha a terhes, vagy szoptató nő képtelen farmakoterápia nélkül leszokni, azt lehet kezdeményezni, ha a dohányzás abbahagyásának valószínűsége és az így elérhető egészségnyereség nagyobb a farmakoterápia és az anélkül valószínűleg továbbra is fennálló dohányzás káros hatásainál (C szintű evidencia).
A terhesség alatti dohányzás károsítja a magzatot. A lepényi keringés károsodása következtében gyakrabban kell spontán vetéléssel, magzati halálozással számolni. A dohányzó terhesek újszülöttei kis súlyúak, gyakran 2500 gramm alattiakés ehhez gyakrabban társulnaka legkülönbözőbb kórállapotok. A fejlődésbeli lemaradást nehezen hozzák be ezek az újszülöttek. A terhességük alatt dohányzó anyák gyermekein még tízéves korukban is mutatkozhat értelmi, érzelmi fejlettségbeli lemaradás és ezekből eredő viselkedésbeli probléma (A tipusú evidencia). A terhesség alatti dohányzás némely rosszindulatú daganat előfordulásának a kockázatát is megnöveli.
Sok nő visszaszokik a szülés után. Érdemes ennek megelőzésére ismételni a leszokás támogatást szülés után. Az újszülöttbe az anyatejjel nikotin jut, ha a szoptató anya dohányzik. A tájékoztató füzetek, az ismételt leszokási próbálkozás hasznosnak bizonyultak ebben a csoportban.
6.3. Dohányzó gyermekek, serdülők
Az orvosoknak meg kell kérdezniük gyermekkorú (14 év alatti) és serdűlő korú (14-16 éves) pácienseiket és a szülőket a dohányzással kapcsolatban és határozottan állást kell foglalni a teljes dohányfüst mentesség mellett (C szintű evidencia). A felnőtteknél használt tanácsadás és magatartás alapú kezelés ajánlott ebben a csoportban. A beavatkozás tartalmát, az esetleges leszokási módszert azonban az életkori sajátosságok figyelembevételével módosítani kell (C szintű evidencia). Serdűlők kezelésekor, nikotinfüggőség esetén farmakoterápia is alkalmazható (C szintű evidencia). Gyermekorvosoknak tanácsolniuk kell a dohányzás abbahagyását, hogy a gyermekek dohányfüst expozícióját csökkenteni/megszűntetni lehessen (B szintű evidencia) [44,45].
A dohányosok kb. 90%-a 21 éves kora előtt kezd dohányozni. A dohányzó tinédzserek száma Magyarországon is gyorsan növekszik. A szülői, testvéri és kortárs minta, valamint a saját tapasztalatszerzés képezi a legfontosabb rizikótényezőket. A legfontosabb népegészségügyi törekvésnek a dohányzás primer prevenciójának kell lenni, az iskolai tantervbe történő beépítéssel. Eddigi néhány tapasztalat szerint az iskolákban működő multimodális megközelítésű programok mellett csökkenthető a dohányzó fiatalok aránya. Fiatalokesetében a dohány dependencia kezelése nehéz, általában a felnőtteknél hatékonynak talált pszicho-szociális intervenciót alkalmaztak, melynek eredményessége nem bizonyított ebben a korcsoportban és a tartalmát az életkornak megfelelően adaptálni szükséges. Mindössze két vizsgálatban alkalmaztak farmakoterápiát (nikotinpótló kezelés és bupropion), így ennek eredményessége nem ítélhető meg. Mindezek miatt a prevenciónak kulcsszerepe van (ideértve az ismételt pozitív megerősítést az absztinenciával kapcsolatban).
A dohányzás káros egészségügyi hatásait ismerő gyermekek fontos szerepet játszanak a dohányzó szülők leszokásának motiválásában. Tájékoztatni kell ezt a csoportot a dohányfüst expozíció (passzív dohányzás) káros hatásairól is [48].
6.4. Kórházi betegek
Kórházba kerülő betegek esetében a megbetegedés, a dohányzás korlátozása jó lehetőséget teremt a dohányzás elhagyására. Fekvőbeteg intézmény betegei esetében is fel kell mérni a beteg dohányzási szokásait, motiváltságát a leszokásra, tájékoztatni a dohányzás okozta kockázatokról, valamint a dohányzás elhagyásával járó előnyökről. A kezelőorvosnak fel kell készülnie az esetleg jelentkező megvonási tünetek ellátására. Kórházi körülmények között szervezett tájékoztató program, melybe a szakdolgozók és a klinikai pszichológus is bekapcsolódik, adhat alapot a kezelőorvosaka nikotin dependencia kezelés elindításához. Legalább négy alkalommal 10-10 perces ülésekjavasoltak, lehetőleg erre speciálisan kiképzett szakemberrel. Individuális és csoportterápia is alkalmas forma, melynek fő részét gyakorlati tanácsok, és ezek alkalmazása alkotja. Csak azon programok esetében igazoltak magasabb absztinencia rátát, ahol a betegek legalább 1 hónapos utánkövetésben részesültek. Megfontolandó a kezelés farmakoterápiával történő kombinálása, bár ennek hatékonysága még nem kellőképpen bizonyított [43].
IV. Rehabilitáció
V. Gondozás
VI. Irodalomjegyzék
[1] Mackay J., Eriksen M. et Shafey O.: The Tobacco Atlas (2nd ed.) Ed: American Cancer Society by Myriad Ed. Ltd. 2006
[2] Jarvik, M.E. (1995). The scientific case that nicotine is addictive. Psychopharmacology, 117,18-20.
[3]. Perkins, K.A. (1999). Nicotine self-administration. Nicotine and Tobacco Research, 1 (Suppl. 2), S133-S138.
[4] Watkins, S. S., Koob, G. F.; Markou, A. (2000). Neural mechanisms underlying nicotine addiction: acute positive reinforcement and withdrawal. Nicotine and Tobacco Research, 2 (1), 1,19-37.
[5] Fiore MC, Jaén CR, Baker TB, et al. (2008). Treating Tobacco Use and Dependence:
2008 Update. Clinical Practice Guideline. Rockville, MD: U.S. Department of Health and Human Services. Public Health Service.
[6] American Psychiatric Association (2000) Diagnostic and Statistical Manual of Mental Disorders, (4th ed., text revision). Washington DC: American Psychiatric Association.
[7] Hughes JR, Hatsukami DK, Mitchell JEet al.: Prevalence of smoking among psychiatric outpatients. Am J Psychiatry 1986;143:993-7 [Abstract/Free Full Text]
[8] De Leon J, Abraham G, Nair C. et al.: Nicotine addiction in chronic schizophrenic inpatients. Biol Psychiatry
1995;37:593-683 [Medline]
[9] Rihmer Z.: Dohányzás és depresszió. In: Addikciók (szerk:: Németh A., Gerevich J.) Medicina, Budapest,
2000.158-166.
[10] Kessler RC, Borges G, Sampson N. et al.: The association between smoking and subsequent suicide-related outcomes int he National Comorbidity Survey panel simple. Mol Psychiatry. 2008 Jul 22. [Epub ahead of print]
[11] William JM, Foulds J.: Successful tobacco dependence treatment in schizophrenia. Am J Psychiatry
2007;164:222-227
[12] Kovács G, Manchin R. (szerk): Dohányzás, vagy egészség? Medicina, Budapest. 2006.
[13] Treating Tobacco Use and Dependence, U.S. Departement of Health and Human Services, Public Health Service, June 2000
[14] West R, et al. Smoking cessation guidelines. Thorax 2000; 53:140-4. (4/3)
[15] A Clinical Practice Guideline for Treating Tobacco Use and Dependence, JAMA, 283:2000, No.24.3244-54. (4/4)
[16] Brief interventions and referral for smoking cessation in primary care and other settings, Quick reference guide, 2006. National Institute for Health and Clinical Excellence (4/7)
[17] Rice VH, Stead LF. Nursing interventions for smoking cessation. Cochrane Database of Systematic Reviews 2008, Issue 1. Art.No.:CD001188. DOI: 10.1002/14651858. CD001188.pub3.) (4/6)
[18] Stead LF. Bergson G. Lancaster T. Physician advice for smoking cessation.[update of Cochrane Database Syst Rev. 2004;(4):CD000165; PMID: 15494989]. Cochrane Database of Systematic Reviews. (2):CD000165, 2008.
[19] Fiore MC, Jaén CR, Baker TB, et al. Treating Tobacco Use and Dependence:
2008 Update. Clinical Practice Guideline. Rockville, MD: U.S. Department of Health and Human Services. Public Health Service. May 2008.
[20] Lancaster T. Stead LF. Self-help interventions for smoking cessation.[seecomment][update of Cochrane Database Syst Rev. 2002;(3):CD001118; PMID: 12137618]. Cochrane Database of Systematic Reviews. (3):CD001118, 2005.
[21] Lancaster T. Stead LF. Individual behavioural counselling for smoking cessation.[update in Cochrane Database Syst Rev. 2005;(2):CD001292; PMID: 15846616][update of Cochrane Database Syst Rev. 2000;(2):CD001292; PMID: 10796638]. Cochrane Database of Systematic Reviews. (3):CD001292,2002.
[22] Stead LF. Lancaster T. Group behaviour therapy programmes for smoking cessation.[update of Cochrane Database Syst Rev. 2002;(3):CD001007; PMID: 12137615]. Cochrane Database of Systematic Reviews. (2):CD001007, 2005.
[23] Stead LF. Perera R. Lancaster T.Telephone counselling for smoking cessation.[update of Cochrane Database Syst Rev. 2003;(1):CD002850; PMID: 12535442 Cochrane Database of Systematic Reviews. 3:CD002850, 2006.
[24] Abbot NC. Stead LF. White AR. Barnes J. Ernst E. Hypnotherapy for smoking cessation. Cochrane Database of Systematic Reviews. (2):CD001008,2000.
[25] White AR. Rampes H. Campbell JL. Acupuncture and related interventions for smoking cessation.[update of Cochrane Database Syst Rev. 2002;(2):CD000009; PMID: 12076375]. Cochrane Database of Systematic Reviews. (1):CD000009, 2006.
[26] Hajek P. Stead LF. Aversive smoking for smoking cessation.[update of Cochrane Database Syst Rev. 2000;(2):CD000546; PMID: 10796558]. Cochrane Database of Systematic Reviews. (3):CD000546, 2004.
[27] Bize R. Burnand B. Mueller Y.Cornuz J. Effectiveness of biomedical riskassessmentasan aid for smoking cessation: a systematic review. Tobacco Control. 16(3):151-6,2007 Jun.
[28] Ussher MH. West R. Taylor AH. McEwen A. Exercise interventions for smoking cessation.[update in Cochrane Database Syst Rev. 2005;(1):CD002295; PMID: 15674895]. Cochrane Database of Systematic Reviews. (3):CD002295, 2000.
[29] Stead LF. Lancaster T. Nicobrevin for smoking cessation. Cochrane Database of Systematic Reviews. (2):CD005990,
2006.
[30] Miller, W.R. and Rollnick, S. (1991). Motivational interviewing: Preparing people to change addictive behavior. New York: The Guilford Press.
[31] Rollnick, S., Miller, WR. And Butler, C.C. (2008). Motivational interviewing in health care, Helping patients change behavior. London: The Guilford Press.
[32] Mojica, W. A., Suttorp, M. J., Sherman, S. E., Morton, S. C., Roth, E. A., Maglione, M. A., Rhodes, S. L., & Shekelle, P. G. (2004): Smoking-cessation interventions by type of provider: a meta-analysis. American Journal of Preventive Medicine, 26(5), 391-401.0
[33] Fagerstrom, K.O.: Clinical Treatment of Tobacco Dependence: The Endurance of Pharmacologic Efficacy. J Clin Psychiatry Monograph 2003;18(1):35-40
[34] Haustein K.O.: Tobacco or Health. Springer (ed) 2001
[35] Lancaster T, Stead L et al for the Tobacco Addiction rewiev Group. Effectiveness of interventions to help people stop smoking: findings from the Cochrane Library; BMJ,5 August 2000, Vol 321,355-8.
[36] Gonzales D, Rennard SI, Nides M, et al. 2006. Varenicline,an a4a2 nicotinic acethylcoline receptor partial agonist, vs sustained-release bupropion and placebo for smoking cessation. A randomized controlled trial. JAMA, 296:47-55
[37] A Clinical Practice Guideline forTreating Tobacco Use and Dependence: 2008 Update, A U.S. Public Health Service Report. Am J Prev Med 2008;35(2):158-176
[38] Borrelli B. Spring B. Niaura R. Hitsman B. Papandonatos G. (2001). Influences of gender and weight gain on short-term relapse to smoking in a cessation trial. Journal of Consulting & Clinical Psychology. 69(3):511-5.
[39] Klesges RC, Winders SE, Meyers AW, et al. (1997). How much weight gain occurs following smoking cessation? A comparison of weight gain using both continuous and point prevalence abstinence. Journal of Consulting and Clinical Psychology, 65:286-91.
[40] Froom P, Melamed S, Benbassat J (1998). Smoking cessation and weight gain. Journal of Family Practice 46: 460-464.
[41] John U. Meyer C. Rumpf HJ. Schumann A. Dilling H. Hapke U. (2005). No considerable long-term weight gain after smoking cessation: evidence from a prospective study. European Journal of Cancer Prevention. 14(3):289-95.
[42] Evidence-based guidelines for cardiovascular disease prevention in women. 2007 /AHA guidelines/ Circulation 2007:115
[43] Rigotti NA, Munafo MR, Stead LF. Interventions forsmoking cessation in hospitalised patients. Cochrane Database Syst Rev. 2007 Jul 8;(3):CD001837.
[44] Thomas R, Perera R. School-based programmes for preventing smoking. Cochrane Database Syst Rev. 2006 Jul 19;3:CD001293.
[45] Grimshaw GM, Stanton A. Tobacco cessation interventions for young people. Cochrane Database Syst Rev. 2006 Oct 18;(4):CD003289.
[46] McRobbie, H (2005). Current insights and new opportunities forsmoking cessation, British Journal of Cardiology, 12, 37-44.
[47] www.tabac-liberte.com (PESCE)
[48] Müller V, Tamási L. A dohányzás megelőzése és a dependencia kezelése. Magyar családorvosok lapja 2008;2:2-6.
[49] Vadászi, Beke M, Huzián lés mtsai. Dohányzásról leszokást segítő országos program-öt év tapasztalatai. Medicina Thoracalis 2000;53:140-144.
A szakmai irányelv érvényessége: 2010. szeptember 30.
Az irányelv multidiszciplináris szakmai irányelv, elkészítésében az alábbi szakmai szervezetek vettek részt:
Tüdőgyógyászati Szakmai Kollégium
Kardiológiai Szakmai Kollégium
Pszichiátriai Szakmai Kollégium
Klinikai Pszichológiai Szakmai Kollégium
Megelőző Orvostani és Népegészségügyi Szakmai Kollégium
Semmelweis Egyetem Családorvosi Tanszéke
Országos Alapellátási Intézet
Az Egészségügyi Minisztérium
szakmai irányelve
A Sclerosis multiplex kezeléséről
(1. módosított változat)
Készítette: a Neurológiai Szakmai Kollégium
TARTALOMJEGYZÉK
I. ALAPVETŐ MEGFONTOLÁSOK
1.1 A protokoll alkalmazási területe
1.2 Az irányelvet összeállítók és a véleményezők
1.3 Az irányelv érvényessége
1.4 A kezeléssel kapcsolatos ismeretek (bizonyítékok) áttekintésének módszere
1.5 Az irányelvben a bizonyítékok szintjére és az ajánlások erejére alkalmazott jelölések
1.6 A sclerosis multiplex definíciója
1.7 Panaszok, tünetek, általános jellemzők
1.8 A betegség leírása, epidemiológia
II. DIAGNÓZIS
2.1 Anamnézis
2.2 Fizikális vizsgálatok
2.3 Kötelező diagnosztikai vizsgálatok
2.4 Kiegészítő diagnosztikai vizsgálatok
2.5 Differenciális diagnosztikai szempontból szükséges vizsgálatok
2.6 Elkülönítendő kórképek
2.7 Diagnosztikai algoritmusok, kritériumok
III. TERÁPIA
3.1 Nem gyógyszeres kezelés
3.2 Gyógyszeres kezelés
3.2.1 Relapszusok kezelése
3.2.2 A betegség aktivitásának és/vagy progressziójának csökkentése
3.2.3 A Neurológiai Szakmai Kollégium ajánlásai SM kialakulás, aktivitás és progresszió csökkentésére (ajánlás: A, bizonyítékok szintje: I.)
3.3. Tüneti kezelés
3.3.1 Spaszticitás
3.3.2 Kóros fáradékonyság
3.3.3 Fájdalom
3.3.4 Hólyag dysfunkció
3.3.5 Tremorok
3.3.6 Szexuális dysfunkció
3.3.7 Depresszió
3.3.8 Erőltetett patológiás sírás és emocionális instabilitás
3.3.9 Epilepsziás roham 3.4 Műtét
IV. REHABILITÁCIÓ
V. GONDOZÁS
5.1. Az SM centrum személyi feltételei 5.2 Az SM centrum tárgyi feltételei
VI. IRODALOMJEGYZÉK
I. Alapvető megfontolások
1.1 A protokoll alkalmazási területe
A sclerosis multiplexet (SM) részben a betegség kórlefolyását módosító SM-re specifikus, törzskönyvezett készítményekkel, másrészt más betegségben regisztrált tüneti szerek alkalmazási területének megfelelő készítményekkel kezeljük. Az irányelvek célja, hogy az Egészségügyi Minisztérium kezdeményezésére, összefoglalja a betegség kezelésének indikációit, a kezelés alkalmazásának szakmai és szervezeti feltételeit. Célcsoportok:
- SM centrumok
- neurológusok
- szemészek
- rehabilitációs szakemberek
- OEP és egyéb egészségügyi biztosítók
- Egészségügyi Minisztérium
Az irányelvet összeállító bizottság felhívja a figyelmet arra, hogy az irányelvben szereplő gyógyszerek alkalmazása tekintetében minden orvos köteles ismerni a hatályos OGYI törzskönyvi előírásokat és az indikáción kívüli alkalmazás jogszabályi feltételeit (32/2008.) (X.18)EüMim rendelete
1.2 Az irányelvet összeállító bizottság tagjai és a véleményezők
A dokumentumot összeállították: Nemzeti Sclerosis Multiplex Orvosi Tanácsadó Testület és ECTRIMS /European Committee for Treatment and Research in Multiple Sclerosis/, SOTE Neurológiai Klinika, (SCLEROSIS MULTIPLEXES BETEGEK ORSZÁGOS EGYESÜLETE Orvosi Tanácsadó Testület, ECTRIMS, SCLEROSIS MULTIPLEXES BETEGEK ORSZÁGOS EGYESÜLETE (Orvosi Tanácsadó Testület), PTE Neurológiai Klinika, Neurológiai Szakmai Kollégium. Az irányelv véleményezése: Az irányelvet a Neurológiai Szakmai Kollégium miden tagja, és az Országos Neurológus Szakfőorvos megkapta véleményezésre. Az irányelv gyakorlati alkalmazhatóságát formálisan nem teszteltük, az alkalmazás első 2 éve során nyert tapasztalatok alapján tartjuk indokoltnak a jelenlegi dokumentum felülvizsgálatát.
1.3 Az irányelvérvényessége
A szakmai irányelv érvényessége: 2010. szeptember 30.
1.4 A kezeléssel kapcsolatos ismeretek (bizonyítékok) áttekintésének módszere
A bizottság az ajánlások összeállításához áttekintette a rendelkezésre álló szakirodalmi adatokat. A szakirodalom áttekintése során figyelembevette a hozzáférhető nemzetközi irányelveket - National Institute for Clinical Excellence, American Academy of Neurology és az MS Council for Clinical Practice Guidelines, a Német Neurológiai Társaság neurológiai iránymutatásai (AWMF online), European Federation of Neurological Society (EFNS) -, valamint a Cochrane Könyvtárban és a MEDLINE adatbázisban az SM kezeléssel kapcsolatosan talált szisztematikus leírásokat. Az irányelv összeállításakor a bizottság nem értékelte újból egyenként a klinikai vizsgálatokat, hanem a talált szisztematikus összefoglalók elemzésére támaszkodott.
1.5 Az irányelvben a bizonyítékok szintjére és az ajánlások erejére alkalmazott jelölések
A jelenlegi klinikai irányelv a klinikai kutatás rendelkezésre álló legjobb bizonyítékai alapján tesz javaslatot az SM kezelésére. A bizonyítékok szintjét és az ajánlások erejét a European Federation of Neurological Societies (EFNS) által javasolt rendszer (Brainin és mtsai, 2004) szerint adjuk meg. A bizonyítékok szintjei és az ajánlás ereje a következő:
I. szintű bizonyíték: Megfelelő számú esetet magába foglaló, randomizált kontrollált klinikai vizsgálat, melyben az alkalmazott módszerek (megfelelő módon történő randomizálás, előre rögzített végpontok, egyértelműen definiált bevételi és kizárási kritériumok, a vizsgálatból kiesők megfelelő elemzése, stb.) miatt kicsi a szisztematikus hiba (az ún. torzítás) lehetősége. I. szintű bizonyító ereje van az ilyen, kiváló módszertannal végzett vizsgálatok szisztematikus összefoglalóinak is.
II. szintű bizonyíték: Az eredmények jó minőségű kohorsz vagy eset-kontroll vizsgálatok szisztematikus irodalmi áttekintéséből, vagy olyan jó minőségű kohorsz vagy eset-kontroll vizsgálatokból származnak, melyekben nagyon alacsony a szisztematikus hiba és a zavaró hatások esélye, vagy olyan randomizált, kontrollált vizsgálat, mely nem minden szempontból kifogástalan módszertannal készült.
III. szintű bizonyíték: Minden egyéb kontrollált vizsgálat (ideértve például az ún. "történelmi kontroll" csoport alkalmazását, vagy az önkontrollos vizsgálatokat is)
IV. szintű bizonyíték: Kontroll nélküli vizsgálatok, esetsorozatok, esetismertetések, szakértői vélemények. A fentiek alapján az ajánlások ereje a következőképp határozható meg:
A): Az adott beavatkozás hatásossága egyértelműen bizonyított (azaz: legalább egy I. szintű vagy legalább két II. szintű vizsgálat egybehangzó eredménye támasztja alá)
B): Az adott beavatkozás hatásossága valószínű (azaz: legalább egy II. szintű vagy legalább három III. szintű vizsgálat egybehangzó eredménye támasztja alá)
C): Az adott beavatkozás hatásossága lehetséges (legalább két III. szintű vizsgálat meggyőző és egybehangzó eredménye támasztja alá)
1.6 A sclerosis multiplex definíciója
A sclerosis multiplex (SM) a központi idegrendszer különböző fokú demyelinisatióval és axonális károsodással járó krónikus gyulladásos megbetegedése. A leggyakoribb fiatal felnőttkorban kezdődő ideggyógyászati megbetegedés, mely az esetek közel kétharmadában 10-15 év kórlefolyás után maradandó rokkantsághoz és idő előtti nyugdíjazáshoz vezet.
Klinikailag két alapvető formája definiálható:
- a visszaeső javuló forma (amely az esetek jelentős részében másodlagos progrediáló formába megy át)
- és a primer progresszív forma.
A legutóbbi évek neuropatológiai kutatásai arra utalnak, hogy az említett klinikai formák hátterében négy elkülöníthető szövettani patomechanizmus állhat. A sclerosis multiplex egyik formájának sem tisztázott jelenleg még az etiológiája.
1.7 Panaszok, tünetek, általános jellemzők
A betegséget multifokális, a látóideg, az agytörzs, a kisagy ill. a gerincvelő károsodására jellemző panaszok, tünetek jellemzik. 30-40%-ban spinális tünetek dominálnak. Leggyakoribb az aszimmetrikus spasticus paraparesis. A betegség bármilyen központi idegrendszeri tünettel kezdődhet, ami lehet homályos látás (neuritis retrobulbaris), zsibbadás, izomgyengeség, szédülés, kettőslátás. A kórlefolyás szerint alcsoportok különíthetők el. Az SM első szakaszára a betegek 60-85%-ában jellemző a hullámzás: rosszabbodások és javulások követik egymást. Az újabb és újabb rosszabbodások (klinikai epizódok, relapszusok, shubok) után általában már maradványtünetek keletkeznek. Ez a relapszusokkal és remissziókkal jellemezhető periódus néhány évtől akár 10-20 éven keresztül is tart. Kezelés nélkül a betegek kb. 40%-a 10 év után már másodlagos, krónikus progresszív stádiumba kerül, amikor a további kórlefolyás már shubok nélküli és a betegség a klinikai tünetek lassú fokozódásával súlyosbodik. A betegek 10-15%-ában a betegség tünetei nem shubokkal, hanem kezdettől fogva alattomosan, egyenletesen, maradandóan súlyosbodnak, melyet primer, krónikus progresszív kórlefolyásként különítünk el. A progresszív-relapszáló forma (5-10%) szintén egyenletes rosszabbodással indul, de alkalmanként shubok is felismerhetők. A betegek 20 - 30%-ában az SM enyhén zajlik, 10 - 20%-ban malignus a betegség, a beteg az első tünettől számítva két éven belül tolószékhez vagy ágyhoz kötötté válik. A fennmaradó esetekben a betegek 10-15 év után mozgáskorlátozottá válnak, járásukhoz segédeszközt kell használniuk. Gyakori shubok, poli-szimptomás kezdet, a tartós funkciókiesés szignifikánsan gyakrabban jelent prognosztikusan kedvezőtlen kórlefolyást.
Shub definíciója: Hirtelen állapotrosszabbodásról (shub, relapszus) akkor beszélünk, ha legalább 30 napja stabil, vagy javuló állapotú sclerosis multiplexes betegnek már meglévő (régi) tünetei súlyosbodnak vagy újtünet(ek) jelennek meg legalább 24 órán keresztül. Paroxysmalis tünetek (mint pl. tónusos görcsök) vagy meglévő tünetek fokozódása testhőmérséklet emelkedés, vagy infekció következtében nem tekinthetők shubnak (pseudoattack).
1.8 A betegség leírása, epidemiológia
Az SM prevalenciája változó, 25-224/100 000 lakos között van. Szegeden, illetve Csongrád megyében végzett, lektorált nemzetközi folyóiratban közölt epidemiológiai felmérés szerint 62-65/100 000. Ennek alapján Magyarországon az SM-ben szenvedő beteg száma 6-8000-re becsülhető, évente kb. 3-5/100 000, azaz országosan 3-500 újesetet diagnosztizálnak. Az SM kétszer gyakrabban fordul elő nőkben, mint férfiakban.
Leggyakrabban 20 és 40 év között jelentkezik, megjelenése ritka 15 éves kor alatt, illetve 50 év felett. Multifaktoriális betegség. A betegség mechanizmusában genetikai és környezeti tényezők együttes kóroki szerepe feltételezhető. A teljes genom vizsgálatok csak a 6. kromoszóma MHC II lókuszával jeleztek kifejezett asszociációt.
II. Diagnózis
2.1 Anamnézis
Az SM diagnózis a kórtörténet és a klinikai tünetek alapján felállítható. A részletes anamnézis felvételnél figyelembe kell venni a különböző funkciókat (hólyag-, bél-, szexuális funkció, fáradékonyság, kognitív hanyatlás). Kideríthető, melyek voltak az első tünetek, mikor jelentkeztek és hogyan alakultak. Ebből következtetni lehet a betegség kórformájára és a betegség prognózisára is. Az SM potenciális diagnózisáról tájékoztatni kell a beteget (C).
2.2 Fizikális vizsgálatok
SM-gyanús tünetek esetén alapos klinikai neurológiai vizsgálatot kell végezni, beleértve a visusvizsgálatot is, továbbá fizikális belgyógyászati vizsgálatot is.
2.3 Kötelező diagnosztikai vizsgálatok Koponya MRI vizsgálat.
2.4 Kiegészítő diagnosztikai vizsgálatok
Gerinc és nervus opticus MRI vizsgálat, kontrasztanyag adása, liquor immunológiai vizsgálat (oligoclonali gammopátia jelenlétének vizsgálata izoelektromos fókuszálással). A szubklinikai disszemináció kimutatása a kiváltott válaszok -visuális kiváltott válasz (VEP) - regisztrálásával, szemészeti vizsgálattal (látótér vizsgálat) történik.
2.5 Differenciális diagnosztikai szempontból szükséges vizsgálatok
Amennyiben az előző pontokban felsoroltak alapján a diagnózis nem egyértelmű, genetikai vizsgálatok, részletes elektrofiziológiai vizsgálat (SSEP, BAEP, ENG, EMG, EEG, transcranialis mágneses ingerlés), vírus szerológiai vizsgálatok szérumból, liquorból, speciális laboratóriumi vizsgálatok autoimmun-betegségek, leukodystrophiák irányába, intracranialis angiographia (MRA), n. suralis-, esetleg izom biopszia végzése indokolt lehet.
2.6 Elkülönítendő kórképek
- Neuromyelitis optica (Devic betegség)
- SM variánsok: opticus neuritis, izolált agytörzsi szindrómák, myelitis transversa, acut disseminalt encephalomyelitis (ADEM), acut necrotizáló haemorrhagias encephalomyelitis.
- Ritka SM variánsok: acut malignus SM (Marburg), Baló-féle koncentrikus sclerosis.
- Autoimmun kórképek: antifoszfolipid antitest szindróma, szisztémás lupus erythematosus, primer Sjögren-szindróma, Behcet kór, polyarteriitis nodosa.
- Fertőző betegségek: Lyme kór, meningovascularis syphilis, HIV myelopathia, HTLV-1 myelopathia.
- Granulomatosus betegségek: sarcoidosis, Wegener féle granulomatosis.
- Gerincvelői szindrómák: gerincvelő kompresszió, cervicalis myelopathia, B 12-vitamin hiány.
- Genetikai betegségek: adrenoleukodystrophia, adrenomyeloneuropathia, mitokondriális encephalopathia, Leber féle opticus atrophia
- Vascularis betegségek: kardiális eredetű agyi embolizáció, CADASIL, érmalformációk, központi idegrendszeri vasculitis
- Neoplasiák: cerebralis, craniospinalis, gerincvelő tumor, központi idegrendszeri lymphoma.
- Egyéb: Arnold-Chiari malformáció, olivopontocerebelláris atrophia, platybasia, basalis impressio.
2.7 Diagnosztikai algoritmusok, kritériumok
A diagnózis az anamnesis és a klinikai tünetek gondos elemzésén alapszik. Bizonyítani kell a betegség időbeli és térbeli (központi idegrendszeren, fehérállományon belüli) terjedését klinikai vagy képalkotó (MRI) vizsgálattal. Ha a relapszus ismétlődött és a neurológiai fizikális vizsgálat legalább két funkcionális rendszer objektív károsodására utaló eltérést igazol, az SM klinikailag határozott diagnózisa felállítható. Primer progresszív forma esetében a klinikai tüneteket folyamatos, lassú progressziónak kell jellemezni legalább egy éven át. A klinikai, laboratóriumi (liquor), radiológiai (MRI) vagy elektrofiziológiai (visuális kiváltott válasz) vizsgálattal kimutatható, sclerosis multiplexre jellemző eltérések alapján a diagnózis már a korai időszakban is felállítható (l.táblázat, Módosított McDonald kritériumok). Az első SM-re utaló demyelinisatiós tünet (klinikailag izolált szindróma /CIS/, opticus neuritis, inkomplett myelitis transversa, agytörzsi vagy cerebellaris góc) után a klinikailag definitív SM kifejlődésének valószínűsége egyénenként változik. Természetes kórlefolyást tanulmányozó vizsgálatok szerint a klinikailag izolált szindrómával (CIS) jelentkező betegek közül azok, akiknek MRI vizsgálata demyelinisatioval összeegyeztethető gócokat mutat és jelzi a térbeli disszeminációt, magas rizikójú betegeknek tekinthetők klinikailag határozott formájú SM kialakulása szempontjából. A betegség aktivitásának megítélése céljából három hónap különbséggel az MRI vizsgálatot ismételni kell.
Az SM diagnózishoz javasolt liquor alapvizsgálat magában foglalja:
- sejtszám meghatározás (< 50sejt/u.l, liquor citológia: lymphocyták, esetleg plasmasejtek)
- összfehérje (jellemzően < 0,6 g/L),
- hányados séma alapján történő albumin- és IgG meghatározás - a vér-liquor gát permeabilitás és a növekedett központi idegrendszeri lokális IgG szintézis mennyiségi kimutatásának értékelése,
- oligoclonalis IgG sávok (OGP) kimutatása.
1. Táblázat. SM diagnózis módosított McDonald kritériumok szerint
| Klinikai epizód (relapszus) | Objektív klinikai tüneteken alapuló lézió(k) | Szükséges vizsgálatok a diagnózishoz | |
| Relapszusokkal és remissziókkal jellemezhető kórforma | |||
| 2 vagy több | 2 vagy több | Nem szükséges | |
| 2 vagy több | 1 | Térbeli terjedés igazolása MRI-vela vagy Pozitív liquorb és 2 vagy több SM-re jellemző góc MRI-vel vagy Újabb klinikai epizód más funkcionális pálya károsodásával | |
| 1 | 2 vagy több | Időbeli terjedés igazolása MRI-velc vagy Második klinikai epizód | |
| 1 monoszimptómás (Klinikailag izolált szindróma -CIS) | 1 | Térbeli terjedés igazolása MRI-vela vagy Pozitív liquorb és 2 vagy több SM-re jellemző góc MRI-vel és Időbeli terjedés igazolása MRI-velc vagy Második klinikai epizód | |
| Primer progresszív kórforma | |||
| 0 (kezdettől progresszió) | SM-re gyanús neurológiai tünetek | Egy éve tartó folyamatos klinikai progresszió és Kettő feltétel a következőkből: a., pozitív koponya MRI (Térbeli terjedés igazolása:: MRI-vel 9 vagy több T2 agyi góc vagy 4 vagy több T 2 agyi gerincvelői góc pozitív VEPd-pel b., pozitív gerincvelői MRI (2 T2 góc) c., pozitívliquorb | |
| a | a térbeli disszemináció bizonyításának teljesítenie kell a Barkhof (1997) és Tintoré szerinti (2000) kritériumokat | ||
| b | pozitív liquorlelet oligoclonalis csíkokkal, ill. emelkedett liquor-IgG-index-szel | ||
| c | MRI kritériumok időbeli terjedéséhez: kontrasztanyagot halmozó góc vagy T2-hyperintenzivgóc> 3 hónappal a klinikai shub után más lokalizációban, mint a megelőző shubnál vagy új kontrasztanyag-felvevő vagy T2-hyperintenziv góc egy második MRI-nél > 3 hónap elteltével | ||
| d | patológiás visuális kiváltott válaszok, amelyek az SM-re jellemzőek (P100 latenciamegnyúlás jó konfiguráció esetén) | ||
III. Terápia
3.1 Nem gyógyszeres kezelés Életmódra vonatkozó ajánlás
- A testhőmérséklet emelkedése az idegekben csökkenti az ingerületvezetési sebességét. Minden olyan hatás, ami az SM-es beteg maghőmérsékletét 37 "Celsius fölé emeli, a meglevő tüneteket kifejezettebbé teheti, vagy fiziológiás testhőmérsékleten nem észlelhető tünetek megjelenéséhez vezethet. A testhőmérséklet-emelkedés állapotrosszabbodást okozó hatása az esetek döntő többségében átmeneti, a testhőmérséklet rendeződése után elmúlik. A jelenséget "pseudoshub"-nak, vagy a jelenség leírója után "Uchthofffenoménnek" nevezik. Kerülendő ezért a forró fürdő, szauna, stb. Lázas betegség esetén fokozottan kell figyelni a lázcsillapításra. Ha a lázas állapotban megjelent újtünet a testhőmérséklet normalizálódása után megszűnik, azt nem szabad relapszusként értékelni.
- A betegség egyik gyakori tünete a kóros fáradékonyság. Tanácsos a fizikai kímélet, illetőleg gyógytorna, egyéb fizikoterápia során a teljesítőképesség maximum 80%-os igénybevétele,a terhelés mennyiségénekés minőségéneka beteg aktuális állapotához történő igazítása. Munkaképes betegnek sem ajánlott nehéz fizikai terheléssel járó, vagy éjszakai, illetve váltóműszakos munka.
- A pszichés stressz negatív hatású lehet.
- Diétaként a növényi olajokban gazdag, telített zsírsavakban szegény, rostdús, de könnyű, ún. mediterrán típusú étrend az emésztésre kifejtett hatása miatt kedvezőbb. A linolénsav, 17-23 g/nap dózisban csökkentheti a rokkantság progresszióját (A), a relapszus súlyosságát, tartamát. Linolénsavban gazdag: a halolaj, napraforgómag, kukorica, szója olaj; Ligetszépe olaj. Az immunstimuláló hatással rendelkező szerek csökkenthetik az immunmoduláló szerek immunszuppresszív hatását, ezért szedésük nagy dózisban nem ajánlott (Ginseng, Coenzyme Q10 - interferonok
hepatotoxikus hatását fokozhatja, fokhagyma, Noni juice, Propolis, Selenium >60 mcg, B6 vitamin, E vitamin, C-vitamin - közepes dózisnál 90-120 mg/nap ne legyen több, Zn >10-15 mg/nap ne legyen több).
- Az infekciók relapszust triggerelhetnek. Az SM betegnek az influenza elleni védőoltást fel kell ajánlani (C). Az influenza védőoltással végzett vizsgálatok nem igazoltak relapszust kiváltó hatást.
- Nincs bizonyíték arra, hogy a terhesség hosszú távon negatívan befolyásolná az SM lefolyását. A terhesség előtt álló SM beteget fel kell világosítani, hogy a terhesség alatt csökken, a szoptatás alatti periódusban átmenetileg megnő a relapszus rizikója (C). Szülés során az SM betegnél olyan, a fizikális és szülészeti körülményeknek megfelelő szülésvezetés és analgesia alkalmazandó, mely nem okoz félelmet a beteg számára (C).
- Műtéti beavatkozások kapcsán a stressz relatív rizikót jelent a műtéthez képest, ezért fontos a beteg megfelelő pszichés támogatása. A műtéti beavatkozásnak megfelelő anaesthesia választható. A felvilágosítás tartalmazza, hogy a relapszus rizikójának növekedése nem ismert (B).
- A fizioterápia célja a mozgás javítása, ajánlott mindenjáróképes (segédeszközzel vagy anélkül) SM betegnek (A) akár otthonában, akár ambulanter (A).
- Rosszul mozgó, ülőkocsihoz kötött betegek esélye decubitus kialakulására fokozott. Megelőzésére megfelelő ágy és ülőmatracok javasoltak (A).
- Tájékoztatni kell a betegeket (A), hogy van néhány adat olyan eljárások kedvező hatásáról SM-ben, melyet időnként alkalmaznak, de ezek alkalmazását nem támasztja alá elegendő bizonyíték (pl. mágneses kezelés, test masszázs, thai chi kiegészítő kezelés) .
3.2 Gyógyszeres kezelés
3.2.1 Relapszusok kezelése
Glucocorticoid kezelésre a tünetek gyorsabban javulnak akut rosszabbodás esetén sclerosis multiplexben (I. szint). A nagy dózisú corticosteroid kezelés kedvező hatása hosszú távon nem bizonyított (II. szint). Nincs különbség a methylprednisolon, ACTH és dexamethason; az intravénásan vagy orálisan alkalmazott nagy dózisú methylprednisolon; 5 illetve 15 napig tartó methylprednisolon kezelés hatásában akut relapszusban (I. szint). A mellékhatások (arc-, boka-oedema, hangulatváltozás) gyakoribbak az ACTH kezelt csoportban. A rosszabbodás kezelése intravénás immunglobulinnal egy éves követés során nem hatásosabba placebonál, viszont a mellékhatások gyakoribbak (I. szint). Egyetlen vizsgálat (I. szint) szerint a súlyos tünetekkel járó, szteroid kezelésre nem javuló relapszus kezelésében a plasmapheresis valószínűleg kedvező hatású.
Relapszus esetén, ha aktív kezelés mellett döntünk, javasolt a methylprednisolon kezelést minél hamarabb elkezdeni (A). Opticus neuritis-szel járó relapszust is nagy dózisú methylprednisolonnal javasolt kezelni, 500 mg - 1 g / nap dózisban intravénásan vagy per os, 3 vagy 5 egymást követő napon (A). A fokozatos leépítés kérdésében nincs konszenzus,a nagy dózisú kezelés az ötödikegy grammos adag után hirtelen is abbahagyható. A gyakori (éventetöbb mint 3 alkalom) vagy elhúzódó (3 hétnél hosszabb) kezelést kerülni kell (C). A relapszus nagydózisú corticosteroid kezelésének megkezdése előtt mérlegelni kell a hatás-mellékhatások relatív kockázatát, és figyelembe kell venni, hogy a relapszus során kialakult neurológiai kórjele(k) spontán is remisszióba kerülhet(nek). Az akut relapszus kezelésben más szernek rutinszerű használata nem ajánlott (C).
3.2.2 A betegség aktivitásának és/vagy progressziójának csökkentése
A betegség klinikai lefolyása változatos. A betegség első éveiben a relapszáló-remittáló betegekelőre kiszámíthatatlan időközökben gyorsan kialakuló neurológiai tünetekkel járó epizódokat szenvednekel, amelyeket remissziók követnek. Átlagosan egy beteg 3 évenként 2 exacerbációt szenved el, a betegség kezdetekor gyakrabban, évenként 2 relapszus is lehet. Az idő előre-haladtával egyre kevésbé teljes a relapszusokból a felépülés és rokkantság kezd kialakulni. A sclerosis multiplexben (SM) szenvedő betegek idegrendszeri károsodásának, a rokkantság követésére a Kurtzke nevéhez fűződő Kiterjesztett Rokkantsági Skálát (Expanded Disability Status Scale, EDSS) használjuk. A neurológus által végzett fizikális vizsgálat során nyolc funkcionális rendszert értékelve (motoros rendszer, kisagyi, agytörzsi működés, sensoros, hólyag és sphincter működés, látórendszer, psychés működés, spasticitas), a tünetek a súlyosság alapján pontozhatók. Egy nem lineáris tízes skálán szám jelzi a rokkantság súlyosságát 0-tól (normális neurológiai állapot) 10-ig (halál), félpontonként emelkedve.
Az SM súlyosságát nem csak a funkcionális értékelő skálák segítségével mérhetjük, hanem az exacerbációk előfordulásának gyakoriságával (exacerbációs ráta: egy betegcsoport egy év alatt jelentkező exacerbációjából számított, egy betegre eső átlagszám) és súlyosságával is.
Az interferonok, a glatiramer acetát és a natalizumab csökkentik a relapszusok kialakulását, a központi idegrendszeri gyulladást, a natalizumab és az interferon béta-1a lassítja a rokkantság kialakulását is (A).
Számos I. szintű vizsgálat szerint a cyclophosphamidnak (B) és plasmapheresisnek nincs (A), a methotrexatnak és cyclosporinnak valószínűleg van (C) progressziót lassító hatása progresszív SM-ben. A cyclosporin kezelés azonban nephrotoxicitása miatt nem elfogadott (B). Az azathioprin és intravénás immunglobulin valószínűleg (C) csökkenti a relapszusok számát relapszáló SM-ben (C), a progresszióra kifejtett hatása nem bizonyított (C).
3.2.2.1 Interferonok
Relapszusokkal-remissziókkal járó definitív sclerosis multiplexes betegeken az interferonok csökkentik a relapszusok éves gyakoriságát (I. szint), az exacerbációksúlyosságát. Az interferon béta-1a mérsékli a progressziót (I. szint). Ajánlott a kezelés járóképes (EDSS <5,5) betegeken, a kezelést megelőző 2 évben (interferon béta 1a s.c. és interferon béta 1b) ill. 3 évben (interferon béta 1a i.m.) legalább 2 shubbal jellemezhető aktivitás esetén (I. szint). A kezelés optimális időtartamát a jelenlegi evidenciák alapján meghatározni nem lehet. Kontrollált vizsgálatok szerint 5 éves, nyílt vizsgálatok szerint 10-16 éves kezelés alatt is észlelhető az interferonok relapszus csökkentő hatása. Az interferonok adásának módja, frekvenciája különbözik. A hatás részben dózisfüggő, interferon béta-1b 8 millió NEsubcutan másod naponta, interferon béta-1a 6 millió NE illetve 12 millió NE subcutan hetente háromszor adva hatásos. Az interferon béta-1a hatása nem fokozódik a hetente egyszer intramuscularisan alkalmazott 6 millió NE felett (I. szint). Az interferon béta készítmények (CHAMPS, BENEFIT, ETOMS vizsgálatok) csökkentik a klinikailag határozott SM kialakulásának valószínűségét magas rizikójú betegcsoportban, ezért ebben a betegcsoportban már az első tünet jelentkezésekor javasolt a kezelés (I. szint).
Relapszusokkal járó szekunder progresszív SM-ben az interferonok csökkentik a relapszusok számát, az interferon-béta-lb a betegség progresszióját lassítja (ESP vizsgálat) (I. szint). Ajánlott a kezelés: ha a beteg képes 10 métert menni segédeszközzel vagy anélkül, legalább 2 relapszusa volt az elmúlt 2 évben, vagy a neurológiai tünetek minimális, de folyamatos progressziója észlelhető az utóbbi 2 évben. Relapszus mentes szekunder progresszív SM-ben az interferonok hatása nem bizonyított (NASP vizsgálat) (I. szint).
Az interferon kezelést abba kell hagyni sclerosis multiplexben: ha az interferonok által okozott mellékhatások nem tolerálhatók, terhesség tervezett vagy létrejött, a kezelés ellenére 12 hónap alatt 2 vagy több relapszus jelentkezett és jelentős maradványtünetekkel gyógyult, szekunder progresszívforma alakult ki és a folyamatos progresszió 6 hónapja fennáll, a beteg járásképtelenné vált (EDSS >7,0) és ez az állapot 6 hónapnál hosszabb ideje észlelhető. Mellékhatások: Többségük az immunmoduláns hatás következménye. Hőemelkedés, esetleg láz, izomfájdalom, gyengeség érzés, fáradtság, hidegrázás, izzadás, fejfájás, hányinger a kezelés kezdetén az injekció beadásakor jelentkeznek és további injekciók adásakor is megismétlődhetnek. Az influenza-szerű tünetek a kezelés kezdetén alkalmazott dózisredukcióval és/vagy paracetamol,ibuprofen adásával jól kezelhetők. Esetleges társuló szívbetegség esetén az influenza-szerű tünetek további megterhelést jelentenek a szívműködés szempontjából. Alkalmazásuk kezdetén lymphopenia, leukopenia, granulocytopenia és májenzimek (transaminasok) átmeneti emelkedése észlelhető. A mellékhatásokelőfordulási gyakorisága és súlyossága a kezelés alatt csökken. Interferonok mellett teljes vérkép, májfunkciók időszakos ellenőrzése ajánlott.
Az interferon béta-1b alkalmazásakor a depresszió mélyülése gyakoribb volt. Az interferonok alkalmazásakor álmatlanság, metrorrhagia, menorrhagia, mérsékelt alopecia előfordulhat. Nem tudni, hogy a kezelés alatt ritkán előforduló epilepsziás rohamot az SM, vagy a kezelés mellékhatásként okozza-e, ezért epilepsziás előzményben alkalmazása óvatosságot igényel.
A lokális injekciós reakció, lokális fájdalom, erythema, gyulladás, bőrnekrózis gyakoribb az interferonok subcutan adásakor (INF beta-1b, IFN beta 1a), mint intramuscularis alkalmazáskor (IFN béta-1a). Az injekciók autoinjectorral történő adása a subcutan injekciók lokális szövődményét jelentősen csökkenti.
Tolerancia, toxicitás: Az interferon beta készítmények fehérje természetű anyagok, ezért a szervezet ellenanyagokat termelhet ellenük. II. és III. szintű vizsgálatok szerint az interferon béta kezelés társul neutralizáló antitest termeléssel (A). A neutralizáló antitestek (NA) általában a kezelés megkezdése után 6-24 hónap között jelennek meg a vérsavóban és idővel az antitestek szintje csökken. Az antitest pozitivitás gyengíti a kezelés visszaesésekre gyakorolt hatását. Incidenciájuk különbözik, gyakoribb subcutan alkalmazás során (B), (38-47% interferon béta-1b, 12-24% subcutan interferon béta-1a, 5-22% intramuscularis interferon béta-1a kezelés esetében). Az intramuscularis interferon béta-1a
kevésbé immunogén a többi interferon béta készítményhez képest (A). A betegekegy részében folyamatos kezelés mellett a NA eltűnnek, ennek a különbségnek a folyamatosságát nehéz meghatározni (B). Bár a folyamatosan magas titerben (>100 to 200 NU/mL) mérhető NA-hez a radiológiai és klinikai paraméterekben mérhető hatás csökkenés valószínűleg kapcsolható (B), az American Academy of Neurology szerint mégsincs elegendő információ arra vonatkozólag, hogy mikor kell NA meghatározást végezni, hogy milyen tesztet és hány alkalommal végezzünk, ill. milyen titer szint köthető a hatásosság csökkenéshez (C). Az európai ajánlás szerint (EFNS ajánlása) szerint a kezelés megkezdése után 12 és 24 hónappal NA szűrővizsgálatot kell végezni és pozitív esetben speciális tesztekkel kell a NA szintet mérni (A). Amennyiben a NA pozitivitás 3 és 6 hónap különbséggel ismételt vizsgálattal folyamatosan fennáll,a kezelést meg kell szakítani (A).
Gyógyszerinterakciók: az interferonok és más gyógyszerek kölcsönhatásai nem tisztázottak. Kis számú betegcsoporton végzett vizsgálatok szerint biztonsággal kombinálhatók glatiramer acetáttal, azathioprinnal, cyclophosphamiddal, methotrexattal, mitoxantronnal. Nem befolyásolják az orális fogamzásgátlók hatékonyságát. Fokozott óvatosság szükséges az olyan készítményekkel, melyek kiürülése nagymértékben függ a májcytochrom P450 rendszerétől (pl. antiepileptikumok).
Ellenjavallatok részletes felsorolása az OGYI törzskönyvben található. Szakmai szempontok alapján a kezelés nem javasolt azoknál a betegeknél, akiknek az elmúlt három év (i.m. interferon béta-1a) ill. két év folyamán kettőnél kevesebb shubjuk volt. Ha a beteg nem reagál megfelelően a kezelésre (ha a mozgáskorlátozottság 6 hónapon keresztül folyamatosan progrediál). Primer progresszív SM-ben, relapsus nélkül zajló szekunder progresszív SM-ben az interferonok nem hatásosak. Annakellenére, hogy nincs adat arról, hogy milyen mellékhatást gyakorol az interferon béta a magzatra, adása terhességben nem javasolt. Súlyos depresszió, öngyilkossági gondolatokkal foglalkozó betegek esetében az interferonok alkalmazása nem biztonságos.
3.2.2.2. Glatiramer acetát
Relapszusokkal-remissziókkal járó definitív sclerosis multiplexes betegekben a glatiramer acetát (copolymer-A) az interferonokhoz hasonló mértékben csökkenti a fellépő relapszusok gyakoriságát (A), MRI vizsgálatok alapján lehetséges, hogy lassítja a progressziót (C). Nyílt vizsgálatok szerint hatását éveken át kifejti (C). A kezelés megfontolására relapszáló-remittáló SM beteg alkalmas (A). Szekunder progresszív SM-ben nem bizonyított a hatása. Ajánlottjáróképes(EDSS<5,0; azaz 100 métert, vagy annál hosszabb távolságot segítség nélkül megtesz) betegeknek" a kezelést megelőző 2 évben legalább 2 shubbal jellemezhető aktivitás esetén naponta 20 mg dózisban, subcutan adott formában (I. szint). A relapszus csökkentő kedvező hatás hosszú távon, 6 éves kezelés során is fennáll (III. szint). A kezelés megszakítása javasolt: ha a glatiramer acetate okozta mellékhatások nem tolerálhatók, terhesség tervezett, 12 hónap alatt 2 relapszus jelentkezik és jelentős maradvány tünetekkel gyógyul, szekunder progresszív forma alakul ki, a beteg járásképtelenné (EDSS <7,0) válik és ez az állapot 6 hónapnál hosszabb ideje már fennáll. Mellékhatás: Lokális injekciós reakciók, erythema, beszűrődés, hosszú távon lipoatrophia fordul elő. A szisztémás reakciók előfordulása közvetlenül az injekció beadását követően jelentkezhet: kipirulás, mellkasi szorító fájdalom, dyspnoe, palpitatio és szorongás, mely spontán szűnik, 30 másodperctől 30 percig tarthat, az injekció ismételt adásakor ismét jelentkezhet.
Tolerancia: ritkán a szisztémás reakciók nem tolerálhatók.
Gyógyszerinterakciók: a glatiramer acetate és más gyógyszerek kölcsönhatásai nem tisztázottak. Kis számú betegcsoporton végzett vizsgálatok szerint biztonsággal kombinálható interferon bétával, intravénás immunglobulinnal.
Ellenjavallat: részletes felsorolása az OGYI törzskönyvben található. Szakmai szempontok alapján kiemeljük, hogy annak ellenére, hogy nincs adat arról, hogy milyen mellékhatást gyakorol a glatiramer acetate a magzatra, adása terhességben nem javasolt.
3.2.2.3. Natalizumab
Relapszusokkal-remissziókkal járó definitív sclerosis multiplexes betegeken a natalizumab csökkenti a betegség aktivitását (I. szint A), markánsan csökkenti a relapszusok éves gyakoriságát (I. szint A), mérsékli a progressziót, a betegség súlyosságát (I. szint A). Más immunmoduláns készítményekkel összehasonlítva a natalizumab relatíve hatásossága pontosan nem meghatározható (C). Szekunder progresszív sclerosis multiplexben hatékonyságát nem ismerjük (C). Bár az intramuscularis nterferon béta 1a terápiában részesülő betegek kiegészítése natalizumabbal, mint kombinációs kezelés hatásosságfokozódást eredményezett (I. szint, B), nincs elegendő információ az együttadás hasznáról, ha a natalizumab kezelést egészítjük ki interferon béta készítménnyel (C). A natalizumab felelős lehet a
progresszív multifokális leukoencephalopathia (PML) rizikó növekedéséért (lásd alább), ezért a relapszáló-remittáló SM betegek szelektív csopotjában javasolt.
A natalizumab, mint önálló kezelés olyan betegeknek javasolt akik más, elsőnek választott - IFN-béta vagy glatiramer acetát - immunmoduláns kezelésre nem megfelelően reagálnak(a natalizumab kezelést megelőző 1 évben legalább 1 shubbal,MRI felvételen 9 T2 vagy 1-nél többGd halmozó lézió meglétével jellemezhető a betegség aktivitása), vagy a kezelést nem tolerálják, vagy a betegség kezdettől gyors és súlyos lefolyású (2 funkciókárosodással járó relapszus egy év alatt és MRI felvételen 1-nél több Gd halmozó lézió vagy megnövekedett T2 góctérfogat). Állapotukat tekintve olyan betegeknek ajánlott, akik shub-közötti periódusban, illetve a jelenlegi shub előtt járóképesek (EDSS <5,0; azaz 100 métert, vagy annál hosszabb távolságot segítség nélkül meg tudnak tenni. Adagolása havonta 300 mg, intravénásan (A betegek közvetlenül átállíthatók az INF-béta és glatiramer-acetát terápiáról natalizumab kezelésre, amennyiben nincs a korábbi kezeléshez kapcsolható laboratóriumi eltérés pl. neutropénia, májfunkció károsodásra illetve infekcióra utaló eltérés. A terápia megkezdése előtt friss MRI vizsgálat végzése szükséges. A betegek rendszeres ellenőrzése speciális centrumban nagyon fontos, hogy az esetleges PML-re gyanús jeleket időben felfedezzék és a szükséges kiegészítő vizsgálatokat (MRI és liquor vizsgálat) elvégezzék. A kezelést fel kell függeszteni, ha PML-re utaló tünetek jelennek meg, amíg annak kockázatát ki nem zárják (1. ábra Függelékbe). A potenciális haszon és kockázat újrabecslése fontos. A kezelés megszakítása javasolt: ha natalizumab okozta túlérzékenység lép fel, terhesség tervezett.
Mellékhatás: enyhe lefolyásúak, pl. fejfájás, fáradékonyság, húgyuti fertőzés, ízületi fájdalom. Alacsony a hiperszenzitivitási reakciók előfordulása (1.1%) és alacsony kockázatú a depresszió és más rosszindulatú betegségek előfordulása. Natalizumab kezelt betegekben a PML kialakulásának rizikója megnő, kombinációs kezelésben (A), monoterápiában (C). A PML rizikója I. szintű vizsgálatok szerint 1eset/1000 kezelt betegre becsülhető átlagosan 18 hónap kezelés után. Eddig összesen 6 PML eset kialakulását diagnosztizálták több, mint 37000 natalizumab kezelt esetből. I. szintű vizsgálatban három natalizumabbal kezelt betegnél alakult ki PML, melyből kettő volt SM beteg: mindkettő i.m. interferon beta 1a-val kombinációs kezelésben részesült, és egy volt Chron beteg, aki korábban immunszupressziv kezelést kapott. A kezelés más oppurtunista fertőzések rizikóját is emelheti (C). Tolerancia, toxicitás: natalizumab elleni antitestek a betegek 9%-ánál jelennek meg és 6% -uknál tartósan megmarad (I. szint). Az állandósult antitest pozitivitás csökkenti a hatékonyságot és az infúzióhoz kapcsolódó mellékhatások valamint túlérzékenységi reakciókfokozott előfordulását okozhatja. Az antitest pozitívitás a terápia első 3 hónapjában alakul ki. Hiperszenzitivitást a kezelt betegek 4%-ában figyeltek meg (I. szint). Az összes eset 1,3%-a súlyos, 0.8%-a anaphylactoid reakció.
Gyógyszerinterakciók: natalizumab és és más gyógyszerek kölcsönhatásai nem tisztázottak.
Ellenjavallat: részletes felsorolása az OGYI törzskönyvben található: Interferon béta vagy glatiramer acetát készítménnyel nem alkalmazható kombinációs kezelésben. Natalizumabbal vagy bármely vivőanyaggal szembeni túlérzékenység (4 %), akiknél nagyobb a kockázat opportunista fertőzésekre, immunszuppresszív kezelésből következően immunhiányos állapotúak (mitoxantron, ciklofoszfamid), PML vagy oppurtunista fertőzés alakult ki; ismert, aktív rosszindulatú daganatos betegségben szenvedőkben, kivéve azok, akiknek basaliomájuk van; túlérzékenységi reakció, perzisztáló natalizumab-ellenes antitestekjelenléte, terhesség, jelentős májkárosodás esetén nem javasolt.
Függelékbe 1. ábra Algoritmus natalizumab kezelés során újneurológiai tünetek jelentkezésekor

3.2.2.4 Mitoxantron
Sclerosis multiplexben végzett vizsgálatok szerint (II. és III. szint) csökkenti a relapszusok számát (B), lassíthatja a rokkantság fokozódását progresszív relapszáló és szekunder progresszív SM-ben (B) (MIMS vizsgálat), 3 havonta 12 mg/m2 dózisban, intravénás rövid infúzióban 18-55 éves korban, progrediáló tünetek (18 hónap alatt legalább 1,0 pont EDSS növekedés), közepes fokú mozgáskorlátozottság esetén (EDSS: 3,0-6,0). A kisebb dózisnak- 5 mg/m2 - nincs hatása a relapszusra, azonban a progressziót mérséklő hatás érvényesül. A betegség korai szakaszában potenciális toxicitása alkalmazását korlátozza. Cardiológiai monitorozás 100 mg/m2 kumulatív dózis elérésekor kötelező. A gyakori shubbal és progresszióval zajló esetekben választható, korlátozott ideig adható. Immunmoduláns (interferon, glatiramer acetate, natalizumab) kezelésre nem reagáló betegek kezelésében megfontolandó. Mellékhatás: Mellékhatásai között a hányinger, a hajhullás, felső légúti infekciók, menstruációs zavar, amenorrhoea, leukopenia, emelkedett gamma-glutamiltranszpeptidáz (GTP) szerepel.
Tolerancia: Súlyos leukopénia esetén stimulációs faktor adására lehet szükség.
Toxicitás: hosszútávon kardiotoxikus, kumulatív dózisa nem lehet nagyobb, mint 120-140 mg/m2. Két-három évig alkalmazható biztonsággal echocardiographiai kontroll mellett. Valószínűlg a malignitás kockázata növekszik, elsősorban akut myeloid leukémia alakulhat ki évek múlva a kezelést követően.
Ellenjavallat: részletes felsorolása az OGYI törzskönyvben található. Szakmai szempontok alapján a következőket emeljük ki: mitoxantronnal szembeni túlérzékenység, súlyos myelon-szuppresszió, súlyos szívelégtelenség. Terhesség idején történő biztonságos alkalmazása nem bizonyított. Jelentős koncentrációban választódik ki az anyatejjel a kezelést követően 28 napig, ezért a kezelés megkezdése előtt fel kell függeszteni a szoptatást.
3.2.3 A Neurológiai Szakmai Kollégium ajánlásai SM kialakulás, aktivitás és progresszió csökkentésére (ajánlás: A, bizonyítékok szintje: I.)
Az első vonalbeli immunmoduláns szerek ajánlott adagjai:
- Béta interferon 1a: 30 mg, 6 millió NE intramuscularisan, hetente egyszer
- Béta interferon 1b: 250 ug, 8 millió NE subcutan, másnaponta
- Glatiramer acetát: 20 mg subcutan, naponta
- Béta interferon 1a: 44 mg, 12 millió NE subcutan, hetente háromszor
Béta interferon ajánlott:
- SM kialakulására magas rizikójú betegcsoportnál az első demyelinisatiós eseményt követően
- Relapszáló-remittáló aktív SM (INF-R 1a i.m.: legalább 2 relapszusa volt az elmúlt 3 évben, INF-R 1b, INF-R 1a s.c.: legalább 2 relapszusa volt az elmúlt 2 évben)
- EDSS: <5,5
- INF-R 1b indikált: olyan szekunder progresszív SM-ben, ha a beteg képes 10 métert menni segédeszközzel vagy anélkül, legalább 2 relapszusa volt az elmúlt 2 évben, a neurológiai tünetek minimális, de folyamatos progressziója észlelhető az utóbbi 2 évben
Glatiramer acetát (GA) ajánlott:
- Relapszáló-remittáló aktív SM (legalább 2 relapszusa volt az elmúlt 2 évben)
- EDSS: <5,5
Meg kell szakítani a béta interferon kezelést:
- Ha terhesség tervezett, vagy kialakult, továbbá laktáció esetén
- Ha az interferonok által okozott mellékhatások nem tolerálhatók,
- 12 hónap alatt 2 vagy több relapszus jelentkezik és jelentős maradvány tünetekkel gyógyul,
- szekunder progresszív forma alakul ki és a folyamatos progresszió 6 hónapja fennáll,
- a beteg járásképtelenné (EDSS >7,0) válik és ez az állapot 6 hónapnál hosszabb ideje észlelhető
Meg kell szakítani a GA terápiát:
- Tervezett, vagy létrejött terhesség esetén.
- A glatiramer acetát okozta mellékhatások nem tolerálhatók,
- 12 hónap alatt 2 vagy több relapszus jelentkezik és jelentős maradványtünetekkel gyógyul,
- szekunder progresszív forma alakul ki
- a beteg járásképtelenné (EDD >7,0) válik és ez az állapot 6 hónapnál hosszabb ideje már fennáll
- ha gyorsan progrediáló funkciórosszabbodás lép fel
Mérlegelendő a kezelés megszakítása, vagy módosítása (általános szempontok)
- Amennyiben ugyanannyi, vagy több shub jelentkezik időarányosan az első 2 éves kezelési periódus alatt, mint az immunmoduláló kezelés megkezdése előtt, vagy egy év alatt egy súlyos relapszus jelentkezik, a felépülés részleges, vagy MRI felvételen Gd halmozó vagy szaporodó T2 gócok vannak (ilyen esetekben individuális megítélés alapján más kémiai szerkezetű immunmoduláló szerre váltás indokolt)
- Amennyiben a suboptimális terápiás válasz interferon kezelés mellett emelkedett neutralizáló antitest titerrel társul a szérumban (más kémiai szerkezetű immunmoduláló szerre váltás indokolt).
- Amennyiben egy adott immunmoduláló szerrel történő kezelés során a beadás módjához kapcsolható mellékhatás jelentkezik - de egyébként a kezelés hatásos -, indokolt lehet másik immunmoduláló szerre váltani.
- Amennyiben egyéb, nem tolerálható mellékhatás miatt kényszerülnek az adott béta interferon terápia megszakítására, másik béta interferon készítmény adása nem indokolt. Ilyen esetekben glatiramer acetat adása mérlegelhető. Glatiramer acetát mellékhatás esetén interferonokra történő átállás jöhet szóba.
2. Táblázat. Bizonyítottan hatékony kezelések a relapszusok csökkentésére és a funkciókárosodás késleltetésére Sclerosis multiplexben
| Kezelés | Indikáció (SM kórforma) | Alkalmazásmód | Gyakoriság | Ajánlott tesztek |
| Immunmoduláló kezelés | ||||
| Interferon beta-1b | Relapszus-remisszió, Szekunder progresszív forma még relapszussal Klinikailag izolált szindróma ismételt MRI-vel igazolt progresszióval | 250 µg sc. | Másnaponta 1x | Májfunkció, rutin haematológia |
| Interferon beta-1a | Relapszus-remisszió Klinikailag izolált szindróma ismételt MRI-vel igazolt progresszióval | 30 µg im. | Hetente 1x | Májfunkció, rutin haematológia |
| Interferon beta-1a | Relapszus-remisszió Klinikailag izolált szindróma ismételt MRI-vel igazolt progresszióval | 44 µg sc. 22 µg sc. | Hetente 3x1 | Májfunkció, rutin haematológia |
| Glatiramer acetate | Relapszus-remisszió Klinikailag izolált szindróma ismételt MRI-vel igazolt progresszióval | 20 mg sc. | Naponta 1x | Májfunkció, rutin haematológia |
| Natalizumab | Relapszus-remisszió, Rapidan progrediáló relapszus-remisszió kórforma Interferon bétára vagy glatiramer acetátra nem megfelelően reagálók Csak monoterápiában alkalmazható | 300 mg iv. | Négyhetente 1x | Kontrasztos agyi MRI a kezelés megkezdése előtt PML-re utaló tünetek esetén kontroll MRI, liquor vizsgálat JC vírus tesztre |
| Immunszuppresszív kezelés | ||||
| Mitoxantrone | Progrediáló relapszus-remisszió, relapszus-progresszív, szekunder progresszív | 12 mg/m2/iv Kumulatív dózis az élet során 140 mg/m2 | Három havonta | A terápia megkezdése előtt balkamra funkció ejekciós frakció vizsgálata, EF < 50%, terápia kontraindikált. Ejekciós frakció és rutin haematológiai paraméterek vizsgálata minden kezelés előtt. |
3.3. Tüneti kezelés
Az alábbiakban az egyes tünetek kezelésére leggyakrabban használt gyógyszereket tüntettük fel. A betegek állapota szerint lehet választani a lehetőségek közül.
3.3.1 Spaszticitás
A spasmus oldását baclofennel (p.o. 30-60 mg/nap max: 120 mg/nap, intrathecalis pumpában 300-800 μg/nap), tizanidinnel (maximális 25-36 mg/nap) javasolt kezdeni (A), esetenként benzodiazepin,dantrolen is hatásos lehet (C). Lokálisan a kiválasztott izomcsoport bénítására botulinus toxin (1500 U) adása megfontolható (B), amennyiben a gyógyszeres kezelés nem eredményes. A botulinus toxin kezelés rutinszerű használata nem indokolt.
Egyéb lehetőségek:
- Tolperison (C)
- Igen súlyos esetekben fenol injekció (C), vagy sebészeti beavatkozás - adductorok átmetszése, rhizotomia.
- Azokat a betegeket, akiknek gyógyszeres kezelés mellett legalább hetente 1x incontinentia jelentkezik, tanácsos a kérdéssel foglalkozó specialistához küldeni (C). Medence torna (A), a medencefenék izmainak elektromos stimulációja (B) jöhet kiegészítésként szóba.
3.3.2 Kóros fáradékonyság
- Amantadin naponta 200 mg dózisban mérsékelten hatásos a kóros fáradékonyság csökkentésére (A)
- Antidepresszívumok depresszió társulásakor (C) ajánlottak
3.3.3 Fájdalom
- A neuropathiás fájdalom carbamazepinnel, gabapentinnel, amitriptylinnel, pregabalinnal kezelhető (A). Egyéb típusú fájdalomcsillapításra evidenciák nincsenek, változó esetszámú betegcsoporton kedvező hatásról számoltak be:
- Az SM-mel összefüggő akut fájdalom esetén Carbamazepin
Benzodiazepinek
Baclofen, tizanidine, tolperison
- Az SM-mel összefüggő krónikus fájdalom Antidepresszívumok
Carbamazepin
Baclofen
Gabapentin
Fizikoterápia (TENS)
Esetleg sebészi beavatkozások
- Musculosceletalis fájdalom, amennyiben csökkent mozgás, kóros tartás miatt, másodlagosan alakul ki TENS (A)
Antidepresszánsok (A)
Rutinszerűen alkalmazott ultrahang kezelés, lézer kezelés, anticonvulsív gyógyszerek nem ajánlottak (A) Intakt kognitív funkciók esetén psychoterápia (A) Nem-szteroid gyulladáscsökkentők (NSAID) (C)
- A paroxysmalis tünetek (pl. dystonia) következtében kialakuló fájdalom Carbamazepin
Baclofen
Phenitoin
Valproát
Barbiturát
Acetazolamid
- A spaszticitás következtében kialakuló fájdalom (lásd a spaszticitás kezelésénél)
3.3.4 Hólyag dysfunkció
- Vizelettárolási zavarban az incontinentiát oxybutyninnal (3x5 mg/nap), amennyiben éjszaka is jelentkezik desmopressinnel (oralisan 100-400 μg, intranasalisan 10-40 μg dózisban, naponta csak egyszer alkalmazható) kezelik (A), egyéb szerek hatása nem bizonyított.
- Antikolinerg szerek: Oxybutynin (A) Tolterodin Emepron Imipramin Desmopressin (A)
- Vizeletürítési zavarokban Alfa blokkolók: Doxazosin
Alfuzosin
Prazosin
Terazosin
Fenoxibenzamin
Izomrelaxánsok:
Baclofen
Tizanidin
Diazepam
Dantrolen
Kolineszteráz bénítok:
Charbacol
Pyridostigmine
Neostigmine
Betachol
Tiszta intermittáló önkatéterezés (C)
- Gyógyászati segédeszközök
3.3.5 Tremorok
- Gyógyszeres lehetőségek kis számú esetismertetések alapján Carbamazepin
Clonazepam
Primidone
Propranolol
Clozapin
Gabapentin
- Sebészi
sztereotaxiás műtét: thalamotomia
- Fizikális
súly alkalmazása (500 g-os "fittness mandzsetta")
3.3.6 Szexuális dysfunkció
- Sildenafil az erectilis dysfunkciót 25-100 mg dózisban férfiaknál javítja (A).
- Apomorphin
- Alprostadilum - intracorporális injekció
- Papaverin - intracorporális injekció
- Prosztaglandin E
- Síkosítók
- Eszközök
- Psychoterápia
3.3.7 Depresszió
- Kognitív, viselkedésterápia (A)
- Antidepresszívumok
3.3.8 Erőltetett patológiás sírás és emocionális instabilitás
- Tricyclikus (B) és szelektív szerotonin reuptake gátló antidepresszívumok (C)
3.3.9 Epilepsziás roham
- Anticonvulsivumok
3.4 Műtét
Az alapbetegség műtéttel nem kezelhető.
IV. Rehabilitáció
V. Gondozás
- A betegség krónikus jellegénél fogva elengedhetetlen a beteg pszichés támogatása (A). Ez magában foglalja a betegségből eredő funkcióromláshoz való alkalmazkodás személyre szabott, együttes kidolgozását, a beteg coping stratégiáinak fejlesztését. A szupportív kezelés javítja az SM-es beteg életminőségét, csökkentheti a kórházi kezelések számát és időtartamát, valamint kedvezően befolyásolja a beteg kezelések iránti compliance-ét. A feladat multidiszciplináris team-et igényel, melynek hatékonyságát növelheti, ha a szakemberekés a betegek civil szervezetei között harmonikus együttműködés alakul ki.
- Az SM kezelésének komplexitása indokolja, hogy az SM-ben szenvedő betegek ellátása speciális centrumban történjék. SM gyanúja esetén is a beteget minél hamarabb (6 héten belül) speciális centrumba kell küldeni.
5.1. Az SM centrum személyi feltételei
- A rendelést legalább két, a rendelés vezetésére tartós megbízással rendelkező neurológus szakorvos lássa el, hogy a helyettesítés, a folyamatos munka megoldható legyen. (Ahol csak egy szakorvos van, ott szükség esetén helyettesítő centrum elérhetőségét kell biztosítani .)
- Állandó személyzet tagja az orvosok mellett az SM ellátásban gyakorlattal rendelkező szakápoló.
- Biztosítani kell, hogy a kezelésbe rendszeresen bevonható legyen gyógytornász, rehabilitációs szakember, pszichológus, valamint a beteg állapotától és szociális helyzetétől függően szociális munkás.
Munkájukat a Neurológiai Szakmai Kollégium által jóváhagyott klinikai irányelvek alapján végzik.
5.2 Az SM centrum tárgyi feltételei
- Minimális rendelési idő (általános neurológiai rendeléstől elválasztottan) heti 6 óra.
- Az illetékes egészségügyi intézmény az Országos Egészségbiztosítási Pénztárral megállapodik az SM szakrendelés működtetéséről és annak rendelési idejéről.
- A rendelés szakszerű dokumentációt vezet.
- Rendelkezik neurológiai osztályos háttérrel.
VI. Irodalomjegyzék
1. ABN guidelines for treatment of multiple sclerosis with p-interferon and glatiramer acetate (2007)
2. American Academy of Neurology (2000). The Role of Corticosteroids in the Management of Acute Monosymptomatic Optic Neuritis. URL: http://www.aan.com
3. American Academy of Neurology (2000). The Usefulness of Evoked Potentials in Identifying Clinically Silent Lesions in Patients with Suspected Multiple Sclerosis URL: http://www.aan.com
4. American Academy of Neurology (2002). Disease Modifying Therapies in Multiple Sclerosis. URL: http://www.aan.com
5. American Academy of Neurology (2002). Immunization and Multiple Sclerosis: A Summary of Published Evidence and Recommendations. Utility of MRI in Suspected MS. URL: http://www.aan.com
6. American Academy of Neurology (2003). The use of mitoxantrone (Novantrone) for the treatment of multiple sclerosis. URL: http://www.aan.com
7. American Academy of Neurology (2003). Utility of MRI in Suspected MS. URL: http:// www.aan.com
8. Andersson M, Alvarez Cermeno J, BernadiG, (1994) Cerebrospinal fluid in the diagnosis of multiple sclerosis: a consensus riport. J Neurol Neurosurg Psychiatry; 57: 897-902.
9. Barkhof F, Polman CH, Radue EWetal (2007) Magnetic resonance imaging effects of interferon beta-lbin the BENEFIT study: integrated 2-year results. Arch Neurol. 64:1292-1298.
10. BeckRW, Cleary PA, Anderson Jr MM, et al (1992) A randomised controlled trial of corticosteroids in the treatment of acute optic neuritis: the Optic Neuritis Study Group. N. Engl. J. Med. 326: 581-588.
11. Bencsik K, Rajda C, Füvesi J et al. (2001) The prevalance of multiple sclerosis, distribution of clinical forms of the disease and functional status of patients in Csongrad county, Hungary. Eur Neurol 46: 206-209
12. Bencsik K, Rajda C, Klivényi P, et. al. (1998) The prevalence of multiple sclerosis in the Hungarian city of Szeged, Acta Neurologica Scandinavica, 97:315-319.
13. Boster A, Edan G, Frohman E et al (2008) Intense immunosuppression in patients with rapidly worsening multiple sclerosis: treatment guidelines for the clinician. Lancet Neurol. 7:173-183.
14. Boz C, Oger J, Gibbs E, Grossberg SE; Neurologists of the UBC MS Clinic (2007) Reduced effectiveness of long-term interferon-beta treatment on relapses in neutralizing antibody-positive multiple sclerosis patients: a Canadian multiple sclerosis clinic-based study. Mult Scler. 13:1127-1137.
15. Brainin M, Barnes M, Baron JC, Gilhus NE, Hughes R, SelmajK, Waldemar G; Guideline Standards Subcommittee of the EFNS Scientific Committee (2004). Guidance for the preparation of neurological management guidelines by EFNS scientific task forces-revised recommendations. Eur J Neurol. 2004;11:577-581.
16. Bowling AC, Stewart TM. Dietary supplements and multiple sclerosis. A health professional's guide. Demos Medical Publishing kiadó New York 2004.
17. Comi G, Filippi M, Barkhof F, et al. (2001) Effect of early interferon Treatment On conversion to definite Multiple sclerosis (ETOMS): a randomized study. Lancet 357:1576-1582.
18. Coyle PK. Switching algorithms: from one immunomodulatory agent to another (2008) J Neurol. 255 Suppl 1:44-50.
19. Csépány T. Sclerosis multiplex. In: Bánki MC, Bereczki D. Hatóanyagok- készítmények- terápia. Fókuszban a neurológia ésa pszichiátria. Melinda Kiadó, Budapest, 2006;41-56.
20. Csépány T, Bereczki D (2004): Immunmoduláns kezelés sclerosis multiplexben. Ideggyógyászati Szemle57:401-416.
21. Csépány T, Illés Zs: Sclerosis multiplex. In: Csépány T, Illés Zs. Klinikai neuroimmunológia. Matyus-BENTEN kiadó.
2005;51-142.
22. Devonshire V, Duquette P, Dwosh E, et al. (2003) The Immune system and hormones: review and relevance to pregnancy and contraception in women with MS. International MS Journal 10:45-50
23. Dwosh E,Guimond C, Duquette P, et al. (2003) The interaction of MS and pregnancy: a critical review. International MS Journal 10: 39-42
24. European Study Group on interferon ß-1b in secondary progressive MS. (1998) Placebo-controlled multicenter randomized trial of interferon ß-1b in treatment of secondary progressive multiple sclerosis Lancet 352:1490-1497.
25. Filippini G, Brusaferri F, Sibley WA, Citterio A, Ciucci G, Midgard R, Corticosteroids or ACTH for acute exacerbations in multiple sclerosis Cochrane Database Syst Rev 2000;(4):CD001331
26. Goodin DS, Cohen BA, O'Connor P et al (2008) Assessment: the use of natalizumab (Tysabri) for the treatment of multiple sclerosis (an evidence-based review): report of the Therapeutics and Technology Assessment Subcommittee of the American Academy of Neurology. Neurology 71:766-773.
27. Goodin DS, Frohman EM, Garmany GP et al (2002) Disease modifying therapies in multiple sclerosis. Report of the Therapeutics and Technology Assessment Subcommittee of the American Academy of Neurology and the MS council for clinical practice guidelines. Neurology 58:169-178.
28. Goodin DS, Frohman EM, Hurwitz B et al (2007) Neutralizing antibodies to interferon beta: assessment of their clinical and radiographic impact: an evidence report: report of the Therapeutics and Technology Assessment Subcommittee of the American Academy of Neurology. Neurology 68:977-984.
29. Hartung HP, Gonsette R, König N, et al. and the Mitoxantrone in Multiple Sclerosis Study Group (MIMS) (2002). Mitoxantrone in progressive multiple sclerosis: a placebo-controlled, double-blind, randomized, multicenter trial. Lancet 360:2018-2025.
30. http://www.aan.com/professionals/practice/index.cfm
31. http://www.medical-tribune.hu
32. http://www.nationalmssociety.org/sourcebook-early.asp
33. http://www.update-software.com/publications/cochrane/
34. IFNB Multiple sclerosis study group, University of British Columbia MS/MRI analysis group. (1995) Interferon beta-1b in the treatment of multiple sclerosis: final outcome of the randomized controlled trial. Neurology 45:1277-1285.
35. IFNB Multiple sclerosis study group. (1993) Interferon beta-1b is effective in relapsing-remitting multiple sclerosis. I. Clinical results of a multicenter, randomized, double-blind, placebo-controlled trial. Neurology 43:655-661.
36. Illés Zs. Az immunmodulációs terápiák. In: Illés Zs. Sclerosis multiplex és autoimmunitás az ezredfordulón. PTE Neurológiai Klinika kiadó 2003:205-268.
37. Jacobs LD, Beck RW, Simon JG, et al. (2000) Intramuscular interferon beta-1a therapy initiated during a first demyelinating event in multiple sclerosis. CHAMPS Study Group. N Engl J Med 343:898-904.
38. Jacobs LD, Cookfair DL, Rudick RA, et al. (1996) Intramuscular interferon beta-1a for disease progression in relapsing multiple sclerosis. The Multiple Sclerosis Collaborative Research Group (MSCRG). Intramuscular interferon beta-1a for disease progression in relapsing-remitting multiple sclerosis. Ann Neurol 39:285-294.
39. Johnson KP, Brooks BR, Cohen JA, et al. (1995) Copolymer 1 reduces relapse rate and improves disability in relapsing-remitting multiple sclerosis: results of a phase III. multicenter, double-blind placebo-controlled trial. The Copolymer 1 Multiple Sclerosis Study Group. Neurology 45:1268-1276.
40. Johnson KP, Brooks BR, Ford CC, et al. and the Copolymer 1 Multiple Sclerosis Study Group. (2000) Sustained clinical benefits of glatiramer acetate in relapsing multiple sclerosis patients observed for 6 years. Mult Scler 6:255-266.
41. Kappos L, Freedman MS, Polman CH et al BENEFIT Study Group (2007) Effect of early versus delayed interferon beta-1b treatment on disability after a first clinical event suggestive of multiple sclerosis: a 3-year follow-up analysis of the BENEFIT study. Lancet 370:389-397.
42. Kappos L, Polman C, Freedman MS et al on behalf of the BENEFIT Srudy Group (2005). Betaferon in Newly Emerging Multiple Sclerosis for Initial Treatment (BENEFIT) clinical results. Mult Scler 11:Suppl1:S10.
43. Kleinschmidt-DeMasters BK, Tyler KL (2005) Progressive Multifocal Leukoencephalopathy Complicating Treatment with Natalizumab and Interferon Beta-1a for Multiple Sclerosis N Engl J Med 353:369-374.
44. Kurtzke JF. (1983) Rating neurologic impairment in multiple sclerosis: an expanded disability status scale (EDSS). Neurology 33:1444-1452
45. La Mantia L, Milanese C, Mascoli N, D'Amico R, Weinstock-Guttman B. Cyclophosphamide for multiple sclerosis (Cochrane Review). In: The Cochrane Library, Issue 3,2004. Chichester, UK: John Wiley & Sons, Ltd.
46. Langer-Gould A, Atlas S (2005) Progressive Multifocal Leukoencephalopathy in a Patient Treated with Natalizumab N Engl J Med 353:375-381.
47. Lovas G, Szilágyi N, Majtényi Ket al. (2000) Axonal changes in chronic demyelinated cervical spinal cord plaques. Brain
123: 308-317
48. Lublin FD, Reingold SC, for the National Multiple Sclerosis Society (USA) (1996) Advisory Committee on Clinical Trials of New Agents in Multiple Sclerosis. Defining the clinical course of multiple sclerosis: results of an international survey. Neurology 46:907-911.
49. Lucchinetti CF, Bruck W, Rodriquez M et al. (1996) Distinct patterns of multiple sclerosis pathology indicates heterogeneity in pathogenesis. Brain Pathology 6: 259-274.
50. McDonald WI, Compston A, Edan G et al. (2001) Recommended diagnostic criteria for multiple sclerosis: Guidelines from the International Panel on the Diagnosis of Multiple Sclerosis. Ann Neurol 50:121-127.
51. Multiple Sclerosis Therapy Consensus Group (2004) Escalating immunotherapy of multiple sclerosis-new aspects and practical application. J Neurol. 251:1329-39. Review.
52. Munari L, Lovati R, Boiko A. Therapy with glatiramer acetate for multiple sclerosis (Cochrane Review). In: The Cochrane Library, Issue 3,2004. Chichester, UK: John Wiley & Sons, Ltd.
53. National Institute for clinical excellence (NHS): Multiple sclerosis. Management of multiple sclerosis in primary and secondary care. Clinical guideline 8. November 2003.
54. National Multiple Sclerosis Society. Disease Management Consensus statement.
55. Pálffy G. (1983) A sclerosis multiplex prevalenciája Pécsett. Ideggyógyászati Szemle 36:12-17.
56. Paty DW, Li DK, the UBC MS/MRI Study Group and the INFB Multiple Sclerosis Study Group. (1993) Interferon beta-1b is effective in relapsing-remitting multiple sclerosis. II. MRI analysis results of a multicenter, randomized, double-blind, placebo-controlled trial. Neurology 43:662-667.
57. Polman CH, O'Connor PW, Havrdova E, et al (2006) AFFIRM Investigators. A randomized, placebo-controlled trial of natalizumab for relapsing multiple sclerosis.N Engl J Med 354:899-910.
58. Polman CH, Reingold SC, Edan G et al (2005) Diagnostic criteria for muntiple sclerosis: 2005 revision to the "McDonald criteria." Ann Neurol 58:840-846.
59. PRIMS (Prevention of Relapses and Disability by Interferon ß-1a Subcutaneously in Multiple Sclerosis) Study Group. (1998) Randomized, double-blind placebo-controlled study of interferon ß-1a in relapsing-remitting multiple sclerosis. Lancet 352:1498-1504.
60. Rajda C, Bencsik K, Vécsei L; Magyarországi Sclerosis Multiplex Centrumok Orvosi Tanácsadó Testület tagjai (2008) A natalizumab alkalmazása sclerosis multiplexben. Ideggyogy Sz. 61:204-208.
61. Rice G PA, Incorvaia B, Munari L, Ebers G, Polman C, D'Amico R, Filippini G. Interferon in relapsing-remitting multiple sclerosis (Cochrane Review). In: The Cochrane Library, Issue 3,2004. Chichester, UK: John Wiley & Sons, Ltd.
62. Rudick RA, Stuart WH, Calabresi PA et al (2006) SENTINEL Investigators. Natalizumab plus interferon beta-1a for relapsing multiple sclerosis. N Engl J Med 354:911-923.
63. Shakespeare DT, Boggild M, Young C. Anti-spasticity agents for multiple sclerosis (Cochrane Review). In: The Cochrane Library, Issue 3,2004. Chichester, UK: John Wiley & Sons, Ltd.
64. Soerensen PS, Deisenhammer F, Duda P, et al (2005) For the EFNS Task Force on Anti-IFN-ß Antibodies in Multiple Sclerosis: Guidelines on use of anti-IFN-ß antibody measurements in multiple sclerosis: report of an EFNS Task Force on Anti-IFN-ß Antibodies in Multiple Sclerosis. Eur J Neurology 12:817-827.
65. Taus C, Solari A, D'Amico R, Branäs P, Hyde C, Giuliani G, Pucci E. Amantadine for fatigue in multiple sclerosis (Cochrane Review). In: The Cochrane Library, Issue 3,2004. Chichester, UK: John Wiley & Sons, Ltd.
66. The PRISMS (Prevention of Relapses and Disability by Interferon ß-la Subcutaneously in Multiple Sclerosis) Study Group and the University of British Columbia MS/MRI Analysis Group. (2001) PRIMS-4: Long-term efficacy of interferon ß-la in relapsing MS. Neurology 56:1628-1636.
67. Thompson AJ, Montalban X, Barkhof F et al (2000) Diagnostic criteria for primary progressive multiple sclerosis: a position paper Ann Neurol 47 :831-835.
68. Van Assche G, Van Ranst M, Sciot R et al (2005) Progressive Multifocal Leukoencephalopathy after Natalizumab Therapy for Crohn's Disease N Engl J Med 353:362-368.
69. Vécsei L, Komoly S (szerk.): Sclerosis multiplex. Therapia kiadó 2003.
70. Yousry TA, Major EO, Ryschkewitsch C et al (2006) Evaluation for progressive multifocal leukoencephalopathy in patients treated with natalizumab. N Engl J Med 355:924-933.
Az Egészségügyi Minisztérium
szakmai irányelve
A Parkinson kór és parkinsonismus gyógyszeres kezeléséről
(1. módosított változat)
Készítette: a Neurológiai Szakmai Kollégium
TARTALOMJEGYZÉK
1. A Parkinson kórról általában
2. Az irányelv célja
3. Célcsoportok
4. Az irányelvet összeállító bizottság tagjai és a véleményezők
5. Összeférhetetlenségi nyilatkozat
6. Az irányelv gyakorlati kipróbálása
7. Az irányelv érvényessége
8. Az ismeretek (bizonyítékok) áttekintésének módszere
9. A parkinson kór kezeléssel kapcsolatos tudományos eredmények összefoglalása az egyes kórképekben: parkinson kór
10. A Parkinson kór kezelésével kapcsolatos eddigi irányelvek
11. A neurológiai szakmai kollégium ajánlásai
12. Irodalomjegyzék
1. A Parkinson kórról általában
A Parkinson kór progresszív lefolyású, degeneratív központi idegrendszeri betegség. Nagyrészt sporadikus előfordulású, kialakulásában komplex poligénes hatás és környezeti faktorok, toxinok együttes oki szerepét feltételezik. A monogénesen öröklődő formák ritkák.
A betegség prevalenciája 100-200/100 000 fő. Az előfordulás gyakorisága az életkor előrehaladtával növekszik.
A Parkinson kór biztos diagnózisa patológiai: a substantia nigra pars compactjának sejtpusztulása és Lewy testek (intraneuronalis hyalin zárványtestek) megléte jellemző. A klinikai diagnózis felállításához a három motoros alaptünet (hypokinesis/bradykinesis, rigor, nyugalmi tremor) közül legalább kettő fennállása szükséges. Idiopátiás Parkinson kórban a tünetek mindig féloldali indulásúak. A tünetek később a másik oldali végtagokat (testfelet) is érintik, de a tüneti aszimmetria a betegség teljes lefolyása alatt észlehető, a levodopa terápia jellemzően kedvező hatású. A betegség kezdeti fázisára a tartási instabilitás nem jellemző, de késői fázisában általában tartási instabilitás alakul ki. A motoros tünetek mellett pszichiátriai tünetek (depresszió, kognitív zavar, késői fázisban demencia) és autonóm zavarok (szintén késői fázisban) jelentkezhetnek. A betegség diagnózisánakin vivo felállítása a klinikai tünetekalapján lehetséges, azonban differenciáldiagnosztikai szempontok indokolhatják koponya MRI vizsgálat, válogatott esetekbenagyi SPECTvagy PET, Doppler vizsgálat és pszichológiai tesztekalkalmazását is. (Jelen irányelvnek nem célja részletes diagnosztikus algoritmus kidolgozása.)
Post mortem vizsgálatok szerint a klinikai diagnózis és a patológiai diagnózis gyakorlott klinikus esetén is csak kb. 80-85%-ban egyezik. A fő differenciáldiagnosztikai problémát egyéb, a Parkinson kórhoz hasonló klinikai tünetekkel járó degeneratív központi idegrendszeri kórképek: ún. "Parkinson plus szindrómák", illetve más, ismert etiológia (pl. vascularis, toxicus stb.) következtében kialakuló "másodlagos Parkinson szindrómák" jelentik.
2. Az irányelv célja
A jelenlegi klinikai irányelvet az Egészségügyi Minisztérium kezdeményezésére a Neurológiai Szakmai Kollégium által felkért bizottság állította össze. Az irányelv célja, hogy összefoglalja a Parkinson kór és a rokon szindrómák kezelésének szakmai és szervezeti feltételeit.
3. Célcsoportok
neurológusok; családorvosok; rehabilitációs szakemberek; Országos Egészségbiztosítási Pénztár; Egészségügyi Minisztérium.
4. Az irányelvet összeállító bizottság tagjai és a véleményezők
A dokumentumot összeállították: PTE OEC Neurológiai Klinika, SZTE ÁOK Neurológiai Klinika.
Az irányelvet véleményezték: a Magyar Tudományos Parkinson Társaság elnöke, a Neurológiai Szakmai Kollégium
minden tagja és az országos neurológiai szakfőorvos.
Az irányelvet összeállító bizottság felhívja a figyelmet arra, hogy az irányelvben szereplő gyógyszerek alkalmazása tekintetében minden orvos köteles ismerni a hatályos OGYI törzskönyvi előírásokat és az indikáción kívüli alkalmazás jogszabályi feltételeit (32/2008. (X.18) EüM rendelete
5. Összeférhetetlenségi nyilatkozat
Az irányelvet összeállítók nem rendelkeznek tulajdonrésszel vagy részvénnyel egyik érdekelt cégben sem, ill. egyikük sem kapott anyagi vagy egyéb támogatást ezen cégektől az irányelv összeállításához.
6. Az irányelvgyakorlati kipróbálása
Az irányelvet formális gyakorlati próbának nem vetették alá, azonban az irányelvben foglaltak tükrözik a Parkinson kór kezelésével kapcsolatos jelenlegi hazai és nemzetközi gyakorlatot.
7. A szakmai irányelv érvényessége: 2010. szeptember 30.
8. Az ismeretek (bizonyítékok) áttekintésének módszere
A bizottság az ajánlások összeállításához áttekintette a rendelkezésre álló szakirodalmi adatokat. A szakirodalom áttekintése során figyelembe vette a hozzáférhető nemzetközi irányelveket, valamint a Cochrane Könyvtárban és a MEDLINE adatbázisban talált szisztematikus áttekintéseket. Az irányelv összeállításakor a bizottság nem értékelte újból egyenként a klinikai vizsgálatokat, hanem a talált szisztematikus összefoglalók elemzésére támaszkodott.
A jelenlegi klinikai irányelva rendelkezésre álló legjobb bizonyítékokalapján tesz javaslatot a kezelésre. A bizonyítékok szintjei és az ajánlás ereje az Európai Neurológiai Társaságok Szövetsége javaslata (Brainin és mtsai, 2004) szerint szerepel. Ez rövidített formában a következő:
I. szintű bizonyíték: Megfelelő számú esetet magába foglaló, randomizált kontrollált klinikai vizsgálat, melyben az alkalmazott módszerek (megfelelő módon történő randomizálás, előre rögzített végpontok, egyértelműen definiált bevételi és kizárási kritériumok, a vizsgálatból kiesők megfelelő elemzése, stb.) miatt kicsi a szisztematikus hiba (az ún. torzítás) lehetősége. I. szintű bizonyító ereje van az ilyen, kiváló módszertannal végzett vizsgálatok szisztematikus összefoglalóinak is.
II. szintű bizonyíték: Az eredmények jó minőségű kohorsz vagy eset-kontroll vizsgálatok szisztematikus irodalmi áttekintéséből, vagy olyan jó minőségű kohorsz vagy esetkontroll vizsgálatokból származnak, melyekben nagyon alacsony a szisztematikus hiba és a zavaró hatások esélye, vagy olyan randomizált, kontrollált vizsgálatból, mely nem minden szempontból kifogástalan módszertannal készült.
III. szintű bizonyíték: Minden egyéb kontrollált vizsgálat (ideértve például az ún. "történelmi kontroll" csoport alkalmazását, vagy az önkontrollos vizsgálatokat is).
IV. szintű bizonyíték: Kontroll nélküli vizsgálatok, esetsorozatok, esetismertetések, szakértői vélemények. A fentiek alapján az ajánlások ereje a következőképp határozható meg:
A) Az adott beavatkozás hatásossága egyértelműen bizonyított (továbbiakban "hatásos"). Azaz: legalább egy I. szintű vagy legalább két II. szintű vizsgálat egybehangzó eredménye támasztja alá.
B) Az adott beavatkozás hatásossága valószínű. Azaz: legalább egy II. szintű vagy legalább három III. szintű vizsgálat egybehangzó eredménye támasztja alá.
C) Az adott beavatkozás hatásossága lehetséges. Azaz: legalább két III. szintű vizsgálat meggyőző és egybehangzó eredménye támasztja alá
9. A Parkinson kór kezeléssel kapcsolatos tudományos eredmények összefoglalása az egyes kórképekben: Parkinson kór
Általános bevezetés:
Parkinson kórban a terápiás törekvések a tünetek javítása mellett a betegség progressziójának lassítására, illetve a levodopa kezelés késői mellékhatásainak (motoros fluktuáció és diszkinéziák) megelőzésére és enyhítésére irányulnak.
1. MAO-B inhibitorok Általános bevezetés
A selegiline és rasagiline a dopamin metabolizálásában részt vevő MAO-B (monoamin-oxidáz-B) enzim szelektív, irreverzíbilis bénítói.
1.1. Rasagiline Hatásosság
1. szintű bizonyíték van a rasagiline betegség lefolyást módosító hatására. A rasagiline monoterápiában hatásos a betegség kezdeti szakaszában.
A rasagiline hatásos késői kombinációban fluktuáló betegekesetén.
Nincs elégséges adat arra, hogy a rasagiline a motoros szövődmények megelőzésében hatékony. Biztonságosság
A vizsgálatokalapján a rasagiline használata biztonságos, a mellékhatások rizikója elfogadható. Speciális monitorozást nem igényel.
1.2. Selegiline Hatásosság
Jelenleg nincs elégséges adat arra vonatkozóan, hogy a selegiline neuroprotektív hatású volna.
A selegiline hatásos monoterápiában is a betegség kezdeti szakaszában. Nincs elégséges adat arra vonatkozóan, hogy
a selegiline hatásos lenne levodopa kombinációban.
A selegiline nem hatásos a levodopa okozta diszkinéziák rizikójának csökkentésére, nincs elégséges adat arra, hogy motoros fluktuációk megelőzésében hatékony lenne.
Nincs elégséges adat arra, hogy a selegiline motoros komplikációk kezelésében hatékony. Biztonságosság
A vizsgálatokalapján a selegiline használata biztonságos, a mellékhatások rizikója elfogadható. Speciális monitorozást nem igényel.
2. Amantadin Általános bevezetés
Az antivirális szerként is használt amantadin hatásmechanizmusa nem pontosan ismert.
Fokozza a preszinaptikus terminálokon a dopamin felszabadulást, posztszinaptikusan gátolja a dopamin visszavételt. Emellett enyhe anticholinerg hatást is tulajdonítanak neki, illetve NMDA glutamát receptor blokkoló.
Hatásosság
Jelenleg nincs elégséges adat arra vonatkozóan, hogy az amantadin a betegség progresszióját lassítaná. Az amantadin monoterápiában valószínűleg hatásos a betegség kezdeti szakaszában. Az amantadin valószínűleg hatásos levodopával kombinálva.
Nincs elegendő adat arra, hogy az amantadin hatékony a motoros komplikációk rizikójának csökkentésére.
Az amantadin hatékony levodopa indukálta diszkinéziák kezelésében, nincs elégséges adat arra, hogy a motoros
fluktuációk kezelésére hatékony volna.
Biztonságosság
A vizsgálatok alapján az amantadin használata biztonságos, a mellékhatások rizikója elfogadható. Speciális monitorozást nem igényel.
3. Anticholinerg szerek Általános bevezetés
Indikációs területük nem demens, tremor domináns Parkinson kóros betegekre korlátozódik. Kedvező hatásúak antipszichotikumok szedése mellett létrejött Parkinson szindrómában. Az anticholinerg szerek alkalmazhatóságának korlátja a gyógyszerek mellékhatás profilja: centrális és perifériás anticholinerg hatások (kognitív teljesítmény romlása, konfúzió, hallucinózis, szájszárazság, obstipáció stb.).
Biperiden, Procyclidine
Hatásosság
Jelenleg nincs elégséges adat arra vonatkozóan, hogy az anticholinerg szerek lassítanák a betegség progresszióját. Az anticholinerg szerek valószínűleg hatékonyak monoterápiában és levodopával kombinálva. Jelenleg nincs elegendő adat arra vonatkozólag, hogy az anticholinerg szerek a motoros komplikációk rizikójának csökkentésében és kezelésében hatékonyak volnának.
Biztonságosság
A vizsgálatok alapján az anticholinerg szerek használata biztonságos, a mellékhatások rizikója elfogadható. Speciális monitorozást nem igényelnek.
4. Dopamin agonisták Általános bevezetés
A dopamin agonisták a posztszinaptikus dopamin receptorok közvetlen stimulálásával fejtik ki hatásukat. A levodopával ellentétben nem kell átalakulniuk aktív vegyületté, ill. nem függnek a túlélő (dopaminerg) sejtektől. Hátrányuk a levodopával szemben a kisebb tüneti hatás, valamint a nem eléggé szelektív receptor affinitás.
4.1. Bromocriptin Hatásosság
Jelenleg nincs rá megfelelő klinikai evidencia, hogy a bromocriptin neuroprotektív hatású volna.
Nincs megfelelő I. szintű placebo-kontrollált vizsgálat bromocriptin monoterápiában történő alkalmazásával, de az adatok alapján a gyógyszer valószínűleg hatásos monoterápiában is a betegség kezdeti szakaszában.
Jelenleg nincs rá megfelelő klinikai evidencia, hogy a bromocriptin hatásos lenne korai kombinációban stabil, nem fluktuáló betegeken.
Azonban hatásos késői kombinációban fluktuáló betegek esetén.
A bromocriptin valószínűleg hatásos a levodopa okozta motoros komplikációk rizikójának csökkentésére. A bromocriptin valószínűleg hatásos motoros komplikációk kezelésére.
Biztonságosság
A vizsgálatok alapján a bromocriptin használata biztonságos, a mellékhatások rizikója elfogadható. Speciális monitorozást nem igényel.
4.2. Ropirinol Hatásosság
Jelenleg nincs rá megfelelő klinikai evidencia, hogy a ropirinol neuroprotektív hatású volna.
A ropirinol monoterápiában hatásos a betegség kezdeti szakaszában.
A ropirinol hatásos levodopa kombinációban előrehaladott stádiumú betegekben.
A ropirinol hatásos a levodopa okozta motoros komplikációk rizikójának csökkentésére.
A ropirinol hatásos motoros komplikációk kezelésére.
Biztonságosság
A vizsgálatok alapján a ropirinol használata biztonságos, a mellékhatások rizikója elfogadható. Speciális monitorozást nem igényel.
Elhúzódó, 24 órás felszívódású ropinirol Hatásosság
Jelenleg nincs rá megfelelő klinikai evidencia, hogy az elhúzódó 24 órás felszívódású ropirinol neuroprotektív hatású volna.
Az rendelkezésre álló klinikai vizsgálatok alapján az elhúzódó felszívódású ropinirol ugyanolyan hatásos monoterápiában a Parkinson kór motoros tüneteinek kezelésére, mint az azonnali felszívódású forma. Az elhúzódó felszívódású ropinirol ugyanolyan hatásos kombinációs terápiában a Parkinson kór motoros tüneteinek kezelésére, mint az azonnali felszívódású forma.
A motoros tüneteken kívül ez a gyógyszerforma szignifikánsan javította a betegek életminőségét 5 kategóriában a levodopával nem megfelelően kontrollált betegcsoporthoz képest.
Biztonságosság
A vizsgálatok alapján az elhúzódó 24 órás felszívódású ropirinol használata biztonságos, a mellékhatások rizikója elfogadható. Speciális monitorozást nem igényel.
4.3. Pramipexole Hatásosság
Jelenleg nincs rá megfelelő klinikai evidencia, hogy a pramipexole progressziólassító hatású volna.
A pramipexole monoterápiában hatásos a betegség kezdeti szakaszában.
A pramipexole hatásos levodopa kombinációban előrehaladott stádiumban is.
A pramipexole hatásos a levodopa okozta motoros komplikációk rizikójának csökkentésére.
A pramipexole hatásos motoros komplikációk kezelésére.
Biztonságosság
A vizsgálatok alapján a pramipexole használata biztonságos, a mellékhatások rizikója elfogadható. Speciális monitorozást nem igényel.
4.4. Transdermális felszívódású rotigotine Hatásosság
A transzdermális rotigotine hatásos a Parkinson kórban szenvedő betegek motoros tüneteinek enyhítésére monoterápiában.
A transzdermális rotigotine hatásos a Parkinson kórban szenvedő betegek motoros tüneteinek enyhítésére kombinációs terápiában.
Biztonságosság
A vizsgálatok alapján a transzdermális rotigotine használata biztonságos, a mellékhatások rizikója elfogadható. Speciális monitorozást nem igényel.
Jelenleg nincs megfelelő evidencia arra, hogy relatív sorrendet lehessen felállítani a dopamin agonisták között.
5. Levodopa
Általános bevezetés
A bélből felszívódó levodopa gyorsan az agyba jut, ahol átalakul dopaminná a neuronokban, ili. a glia sejtekben. A gyógyszer adagolásából fakadóan a szintetizálódott dopamin koncentrációja ingadozást fog mutatni, amely a posztszinaptikus sejtek pulzatilis stimulációjához fog vezetni. Feltehetően ez a megváltozott tüzelési mintázat tehető felelőssé a motoros fluktuációk, ill. a diszkinéziák kialakulásáért.
Hatásosság
Nincs I. szintű placebo-kontrollált vizsgálat levodopa alkalmazásával, de a gyógyszer hatásossága egyértelműen megállapítható.
Jelenleg nincs rá megfelelő klinikai evidencia, hogy a levodopa kezelés befolyásolná a betegség progresszióját.
A levodopa monoterápia valószínűleg hatásosabb, mint az amantadin, ill. az anticholinerg szerek monoterápiában,
bár a vizsgálatok módszertana kifogásolható.
Monoterápiában egyértelműen hatásosabbnak tartható azonban a pramipexole és a ropirinol monoterápiánál. A levodopa szedése egyértelműen összefüggésbe hozható a motoros komplikációkés a diszkinéziák kialakulásával. Jelenleg nincs rá megfelelő klinikai evidencia, hogy a különböző levodopa készítmények alkalmazásával befolyásolni lehetne a motoros komplikációk kialakulását.
Biztonságosság
A vizsgálatokalapján a levodopa készítmények használata biztonságos, a mellékhatások rizikója elfogadható. Speciális monitorozást nem igényel.
Jelenleg Magyarországon elérhető levodopa tartalmú készítmények:
Madopar 250mg Madopar Dispersible Madopar HBS Sinemet CR Duellin 250mg Duellin 100mg
Duodopa (Jejunális levodopa infúzió)
Mindegyik levodopa készítmény egyértelműen hatásos. Nincs rá evidencia, hogy valamelyik készítmény hatásosabb volna, az észlelt különbségek az eltérő farmakokinetikai tulajdonságokból származik.
Jelenleg nincs rá megfelelő klinikai evidencia, hogy bármelyik levodopa készítmények alkalmazásával befolyásolni lehetne a motoros komplikációk kialakulását, kivéve a Duodopát, amely valószínűleg képes csökkenteni a motoros komplikációk súlyosságát. Azonban az invazivitása miatt használata korlátozott.
6. COMT inhibitorok
Általános bevezetés
A catechol-O-methyltransferas (COMT) enzim katalizálja a levodopa átalakulását az inaktív 3-O-metil-dopává. Így az enzim gátlása egyenletesebbé teszi a levodopa szintet a vérben, és ezáltal folyamatosabb dopaminerg stimulációt fog eredményezni. Jelenleg két COMT inhibitor van forgalomban: entacapone, tolcapone.
6.1. Tolcapone
Hatásosság
Jelenleg nincs rá megfelelő klinikai evidencia, hogy a tolcapone kezelés befolyásolná a betegség progresszióját.
A tolcapone hatásos motoros fluktuációkat mutató betegek kezelésében a tünetek javítására.
Jelenleg nincs rá megfelelő klinikai evidencia, hogy a tolcapone kezelés megelőzné a motoros komplikációk
kialakulását.
Biztonságosság
A vizsgálatok alapján azoknál a betegeknél, akik más szerekkel hatásosan kezelhetők, a tolcapone használata nem megengedhető rizikót jelent. Azoknál, akiknél a megfelelő kezelés más szerekkel nem oldható meg, a tolcapone alkalmazása megengedhető, de speciális labormonitorozást igényel.
6.2. Entacapone Hatásosság
Jelenleg nincs rá megfelelő klinikai evidencia, hogy az entacapone kezelés befolyásolná a betegség progresszióját.
Az entacapone hatásos motoros fluktuációkat mutató betegek kezelésében a tünetek javítására.
Jelenleg nincs rá megfelelő klinikai evidencia, hogy az entacapone kezelés megelőzné a motoros komplikációk kialakulását.
Biztonságosság
A vizsgálatok alapján az entacapone biztonságos, a mellékhatások rizikója elfogadható. Speciális monitorozást nem igényel.
6.3. Levodopa, carbidopa és entacapone kombinációja Hatásosság
A rendelkezésre álló klinikai vizsgálatok alapján ez a kombináció hatásos a motoros komplikációk enyhítésére, már levodopával kezelt betegekben.
Jelenleg nincs megfelelő szintű evidencia, hogy a kombináció csökkentené, vagy megelőzné a motoros komplikációk kialakulását.
Biztonságosság
A vizsgálatok alapján a hármas kombináció biztonságos, a mellékhatások rizikója elfogadható. Speciális monitorozást nem igényel.
10. A Parkinson kór kezelésével kapcsolatos eddigi irányelvek
A Parkinson kór kezelésével kapcsolatosan számos irányelvet azonosítottunk. Ezek közül több nem hozzáférhető magyarul.
A kezeléssel kapcsolatos több irányelv, így a legutóbbi amerikai útmutató (Olanow, 2001) is, jelen összeállításban felhasználásra került. Magyar kezelési javaslat a Magyar Tudományos Parkinson Társaság gondozásában 2000-ben készült.
11. A Neurológiai Szakmai Kollégium ajánlásai
A fentiek áttekintése után a Neurológiai Szakmai Kollégium a Parkinson kór kezelésére az alábbi ajánlásokat fogalmazza meg:
11.1. Indikáció Idiopathiás Parkinson kór
Egyéb, gyógyszer-indukálta másodlagos parkinsonismus Más külső tényezők okozta másodlagos parkinsonismus Agyvelőgyulladás utáni parkinsonismus Egyéb másodlagos parkinsonismus Másodlagos parkinsonismus k. m. n. Parkinsonismus máshová osztályozott betegségekben Hallervorden-Spatz betegség Progresszív supranuclearis ophthalmoplegia Striatonigralis elfajulás
A törzsdúcok egyéb, meghatározott elfajulásos megbetegedései A törzsdúcok nem meghatározott elfajulásos betegsége
11.2. Kontraindikáció: részletesen l. az OGYI előírásokban. Relatív kontraindikációk: cardiális decompenzáció; pszichomotoros nyugtalanság, agitáció, delírium, pszichózis Monoterápiában hatásos (A szintű): selegiline, rasagiline, pramipexole, ropirinol, rotigotine, levodopa készítmények, valamint a levodopa/ carbidopa/entacapone kombináció.
Kombinációs terápiában hatásos (A szintű): rasagiline, bromocriptin, pramipexole, ropirinol, rotigotine, levodopa készítmények, entacapone (tolcapone), valamint a levodopa/carbidopa/entacapone kombináció.
11.3. A kezelendő betegek várható száma
Magyarországon nincs átfogó epidemiológiai vizsgálat. A környező országok adatait figyelembe véve a prevalencia 200/100 000 lehet. Így Magyarországon Parkinson kór és rokon szindrómák esetén a betegszám 20 000 körül várható. Jelenleg kb. a betegek 50-70%-a kezelt. Az évi incidencia kb. 8/100 000 lehet, így az újbetegek száma 800 beteg/év körül alakulhat.
11.4. A kezelés gyakorisága
A készítmények használata a klinikai képtől és a mellékhatásoktól függően évekig/élethosszig tarthat.
11.5. Költséghatékonysági elemzés
Az irányelvhez jelenleg nem csatlakozik költséghatékonysági elemzés.
Appendix: A protokoll benyújtásakor még érvényben lévő jogszabály - a 44/2004. (IV. 28.) ESZCSM-rendelet -fogalmazta meg először, s a 2005. évi XCV. törvény 25. § (1) bekezdése megismételte, amely szerint "gyógyszert rendelni csak a forgalomba hozatali engedélyében jóváhagyott alkalmazási előírásban szereplő - Vényminták Gyűjteményében szereplő készítmény esetén az ott közölt - javallatban jogosult minden orvos és fogorvos" figyelembevétele mellett sem tartható etikusnak, ha nem tájékoztatjuk teljes körűen kollégáinkat "evidence based" kezelési lehetőségekről.
Clozapine
Magas impakt faktorral rendelkező vezető neurológiai szaklapokban közölt dupla vak multicentrális vizsgálatok bizonyították, hogy a clozapine hatásosan mérsékli a parkinsonos tünetek mérséklésére alkalmazott gyógyszerek által indukált pszichosist, diszkinéziákat és tremort.
12. Irodalomjegyzék
1. Brainin M, Barnes M, Baron JC, Gilhus NE, Hughes R, SelmajK, Waldemar G; Guideline Standards Subcommittee of the EFNS Scientific Committee. Guidance for the preparation of neurological management guidelines by EFNS scientific task forces-revised recommendations 2004. Eur J Neurol. 2004;11:577-581.
2. Clarke C E, Speller J M, Clarke J A. Pramipexole versus bromocriptine for levodopainduced complications in Parkinson's disease. Cochrane Database Syst Rev. 2000;(3):CD002259.
3.Clarke CE, Deane KH. Ropinirole versus bromocriptine for levodopa-induced complications in Parkinson's disease. Cochrane Database Syst Rev. 2001;(1):CD001517.
4. CW Olanow, O. Rascol: Ann Neurol 2008,64 (Suppl 12): S68
5. CW. Olanow, O. Rascol: 6th International Congress on Mental Dysfunction and Other Non-Motor Features in Parkinsons Disease, Dresden, Germany, October 16-19,2008
6. CW Olanow et al: A randomized, double-blind, placebo-controlled, delayed start study to assess rasagiliner as a disease-modifying therapy in Parkinsons disease (the ADAGIO study):Rationael, design, and baseline characteristics. Movemenrt Disorders 2008. E-published 19 Oct 2008.
7. Durif F, Debilly B, Galitzky M, Morand D, Viallet F, Borg M, Thobois S, Broussolle E, Rascol O. Clozapine improves dyskinesias in Parkinson disease: a double-blind, placebo-controlled study. Neurology. 2004 Feb 10;62(3):381-8.
8. Goetz CG, Koller WC, Poewe W, Rascol O, Sampaio C. Amantadine and Other Antiglutamate Agents. Mov Disord. 2002;17(Suppl.4):S13-S22.
9. Goetz CG, Koller WC, Poewe W, Rascol O, Sampaio C. AnticholinergicTherapies is the Treatment of Parkinson's Disease. Mov Disord. 2002;17(Suppl.4):S7-S12.
10. Goetz CG, Koller WC, Poewe W, Rascol O, Sampaio C. COMT inhibitors. Mov Disord. 2002;17(Suppl. 4):S45-S51.
11. Goetz CG, Koller WC, Poewe W, Rascol O, Sampaio C. DA Agonists - Ergot Derivaties: Bromocriptine. Mov Disord.
2002;17(Suppl. 4):S53-S67.
12. Goetz CG, Koller WC, Poewe W, Rascol O, Sampaio C. DA agonists - Non-Ergot derivaties: Pramipexole Mov Disord.
2002;17(Suppl. 4):S93-S97.
13. Goetz CG, Koller WC, Poewe W, Rascol O, Sampaio C. DA agonists - Non-Ergot derivaties: Ropinirole Mov Disord. 2002;17(Suppl.4):S98-S102.
14. Goetz CG, Koller WC, Poewe W, Rascol O, Sampaio C. Evidence based medical review update: pharmacological and surgical treatments of Parkinson's disease: 2001 to 2004. Mov Disord. 2005 May;20(5):523-39.
15. Goetz CG, Koller WC, Poewe W, Rascol O, Sampaio C. Levodopa Mov Disord. 2002 17(Suppl.4):S23-S37.
16. Goetz CG, Koller WC, Poewe W, Rascol O, Sampaio C. MAO-B Inhibitors for the Treatment of Parkinson's Disease: Mov Disord. 2002;17(Suppl. 4):S38-S44.
17. Goetz CG, Poewe W, Rascol O, Sampaio C. Evidence-based medical review update: pharmacological and surgical treatments of Parkinson's disease: 2001 to 2004. Mov Disord. 2005 May;20(5):523-39.
18. Jankovic J, Watts RL, Martin W, Boroojerdi B. Transdermal rotigotine: Double-blind, placebo-controlled trial in Parkinson disease. Arch Neurol.2007;64:676-682.
19. LeWitt PA, Lyons KE, Pahwa R, for the SP 650 Study Group. Advanced Parkinson disease treated with rotigotine transdermal system: PREFER study. Neurology. 2007;68:1262-1267.
20. Myllylä V, Haapaniemi T, Kaakkola S, Kinnunen E, Hartikainen P, Nuutinen J, Rissanen A, Kuopio AM, JolmaT, Satomaa O, Heikkinen H.Patient satisfaction with switching to Stalevo: an open-label evaluation in PD patients experiencing wearing-off (Simcom Study).Acta Neurol Scand. 2006;114(3):181-6.
21. Olanow CW, Watts RL, Koller WC. An algorithm (decision tree) for the management of Parkinson's disease (2001): treatment guidelines. Neurology. 2001 Jun;56(11 Suppl 5):S1-S88.
22. Parkinson Study Group. A randomized placebo-controlled trial of rasagiline in levodopa-treated patients with Parkinson disease and motor fluctuations: the PRESTO study. Arch Neurol. 2005 Feb;62(2):241-8.
23. Poewe WH, Rascol O, Quinn N,et al, for the SP 515 Investigators. Efficacy of pramipexole and transdermal rotigotine in advanced Parkinson's disease: A double-blind, double-dummy, randomised controlled trial. Lancet Neurol. 2007;6:513-520.
24. Pollak P, Tison F, Rascol O, Destee A, Pere JJ, Senard JM, Durif F, Bourdeix I. Clozapine in drug induced psychosis in Parkinson's disease: a randomised, placebo controlled study with open follow up. J Neurol Neurosurg Psychiatry. 2004 May;75(5):689-95.
25. Ramaker C, Hilten JJ. Bromocriptine/levodopa combined versus levodopa alone for early Parkinson's disease. Cochrane Database Syst Rev. 2002;(2):CD003634.
26. Ramaker C, van Hilten JJ. Bromocriptine versus levodopa in early Parkinson's disease. Cochrane Database Syst Rev. 2000;(3):CD002258.
27.Rascol O, Brooks DJ, Melamed E, Oertel W, Poewe W, Tolosa E: Rasagilin as an adjunct to levodopa in patients with Parkinson's disease and motor fluctuations (LARGO, Lasting effect in Adjunct therapy with Rasagiline Given Once daily, study): a randomised, double-blind, parallel-group trial. Lancet. 2005 Mar 12-18;365(9463):9146.
28. O.Rascol, CW Olanow, ADAGIO: a Prosppective, double-blind, delayed-start study to examine the disease-modifying effect of rasagiline in early Parkinsons disease (PD) Europ J Neurol 2008,15 (suppl 3): 413
29. R. Pahwa, MD; M.A. Stacy, MD; S.A. Factor, DO; K.E. Lyons, PhD; F. Stocchi,MD, PhD; B.P. Hersh,MD; L.W. Elmer,MD, PhD; D.D. Truong, MD; and N.L. Earl, MD; on behalf of the EASE-PD Adjunct Study Investigators. Ropinirole 24-hour prolonged release. Randomized, controlled study in advanced Parkinson disease. Neurology 2007;68:1108-1115
30. The Parkinson Study Group. A controlled trial of rotigotine monotherapy in early Parkinson's disease. Arch Neurol. 2003;60:1721-1728.
Az Egészségügyi Minisztérium
szakmai irányelve
A botulinum toxin-A alkalmazásáról neurológiai kórképekben
(1. módosított változat)
Készítette: a Neurológiai Szakmai Kollégium
TARTALOMJEGYZÉK
1. A botulinum toxin-a hatásmechanizmusa
2. A botulinum toxin-a magyarországon törzskönyvezett alkalmazási területei
3. Az irányelv célja
4. Célcsoportok
5. Az irányelvet szakemberekből álló bizottság állította össze.
6. Összeférhetetlenségi nyilatkozat
7. Az irányelv gyakorlati kipróbálása
8. A szakmai irányelv érvényessége.
9. A btx-a kezeléssel kapcsolatos ismeretek (bizonyítékok) áttekintésének módszere
10. A btx-a kezeléssel kapcsolatos tudományos eredmények összefoglalása az egyes kórképekben: 10.1. Blepharospasmus:
10. 2. Hemifacialis spasmus: 10.3. Torticollis spastica
10. 4. Egyéb dystoniák
10.5. Spasticus cerebralis paresis gyermekkorban (Little-kór)
10.6. Botulinum toxin alkalmazása felnőttkori spasticitásban
11. A btx-a kezeléssel kapcsolatos eddigi irányelvek
12. A neurológiai szakmai kollégium ajánlásai
12.1. Indikáció
12.2. Kontraindikáció
12.3. A kezelendő betegek várható száma
12.4. Alkalmazható készítmények
12.5. A kezelés gyakorisága
12.6. Költséghatékonysági elemzés
13. Irodalomjegyzék
14. Mellékletek
14.1. A módosított asworth skála
14.2. Javasolt adagolás
14.3. A központok minimum feltételei
1. A botulinum toxin-A hatásmechanizmusa
A botulinim toxin olyan neurotoxin, mely a neuromuscularis junctiónál az acetilkolin felszabadulásának gátlásával blokkolja a kolinerg ingerületátvitelt, ezért egy adott izomba injektálvalokális paresis hozható létre. Megfelelően alkalmazva, úgy csökkenti a kezelt izmok túlzott aktivitását, hogy közben nem befolyásolja más izmok erejét. A neurológiai gyakorlatban dystoniákban és spasticitassal járó kórképekben alkalmazzák a készítményt.
2. A botulinum toxin-A Magyarországon törzskönyvezett alkalmazási területei
Magyarországon a botulinum toxin A (BTX-A) blepharospasmus, hemifacialis spasmus és társuló focalis dystoniák, idiopathiás cervicalis dystoniák, gyermekkori spasticus cerebralis paresis, valamint stroke utáni kéz és csukló spasticitas kezelésére van törzskönyvezve. A regisztrált alkalmazási területek között szerepel még a hónaljárok súlyos, primer, helyi kezelésre nem reagáló hyperhydrosisa.
3. Az irányelv célja
A jelenlegi klinikai irányelvet 2005-ben az Egészségügyi Minisztérium kezdeményezésére, a Neurológiai Szakmai Kollégium által kijelölt bizottság állította össze, 2008-ban ennek frissítésére kerül sor. Az irányelv célja, hogy összefoglalja a BTX-A kezelés indikációit, és a kezelés alkalmazásának szakmai és szervezeti feltételeit.
4. Célcsoportok
- A BTX-A kezelést alkalmazó intézmények
- Neurológusok
- Gyermekneurológusok
- Szemészek
- Rehabilitációs szakemberek
- OEP és egyéb egészségügyi biztosítók
- Egészségügyi Minisztérium
5. Az irányelvet szakemberekből álló bizottság állította össze.
6. Összeférhetetlenségi nyilatkozat
Az irányelvet összeállítók nem rendelkeznek tulajdonrésszel vagy részvénnyel a BTX-A-t előállító egyik cégnél sem. Egyikük sem kapott sem anyagi, sem egyéb támogatást a BTX-A-t előállító cégektől.
7. Az irányelv gyakorlati kipróbálása
Az irányelvben foglaltak tükrözik a BTX-A alkalmazásával kapcsolatos több, mint 22 éves általános gyakorlatot.
8. A szakmai irányelv érvényessége: 2010. szeptember 30.
9. A BTX-A kezeléssel kapcsolatos ismeretek (bizonyítékok) áttekintésének módszere
A bizottság az ajánlások összeállításához áttekintette a rendelkezésre álló szakirodalmi adatokat. A szakirodalom áttekintése során figyelembe vette a hozzáférhető nemzetközi irányelveket, valamint a Cochrane Könyvtárban és a MEDLINE adatbázisban a BTX-A kezeléssel kapcsolatosan talált szisztematikus áttekintéseket. A keresés a Cochrane Könyvtárban a "botulin*" kulcsszó keresésével, a MEDLINE-ban a "botulin* AND guideline" szókapcsolat keresésével történt. Az irányelv összeállításakor a bizottság nem értékelte újból egyenként a klinikai vizsgálatokat, hanem a talált szisztematikus összefoglalók elemzésére támaszkodott.
A jelenlegi klinikai irányelv a klinikai kutatás rendelkezésre álló legjobb bizonyítékai alapján tesz javaslatot a BTX-A alkalmazására neurológiai kórképekben. A bizonyítékok szintjei és az ajánlás ereje az Európai Neurológiai Társaságok Szövetsége javaslata (Brainin és mtsai, 2004) szerint szerepel. Ez rövidített formában a következő: I. szintű bizonyíték: Megfelelő számú esetet magába foglaló, randomizált, kontrollált klinikai vizsgálat, melyben az alkalmazott módszerek (megfelelő módon történő randomizálás, előre rögzített végpontok, egyértelműen definiált bevételi és kizárási kritériumok, a vizsgálatból kiesők megfelelő elemzése, stb) miatt kicsi a szisztematikus hiba (az ún. torzítás) lehetősége. I. szintű bizonyító ereje van az ilyen, kiváló módszertannal végzett vizsgálatok szisztematikus összefoglalóinak is.
II. szintű bizonyíték: Az eredmények jó minőségű kohorsz vagy eset-kontroll vizsgálatok szisztematikus irodalmi áttekintéséből, vagy olyan jó minőségű kohorsz vagy eset-kontroll vizsgálatokból származnak, melyekben nagyon alacsony a szisztematikus hiba és a zavaró hatások esélye, vagy olyan randomizált, kontrollált vizsgálat, mely nem minden szempontból kifogástalan módszertannal készült.
III. szintű bizonyíték: Minden egyéb kontrollált vizsgálat (ide értve például az ún. "történelmi kontroll" csoport alkalmazását, vagy az önkontrollos vizsgálatokat is)
IV. szintű bizonyíték: Kontroll nélküli vizsgálatok, esetsorozatok, esetismertetések, szakértői vélemények. A fentiek alapján az ajánlások ereje a következőképp határozható meg:
A: Az adott beavatkozás hatásossága egyértelműen bizonyított (azaz: legalább egy I. szintű vagy legalább két II. szintű vizsgálat egybehangzó eredménye támasztja alá)
B: Az adott beavatkozás hatásossága valószínű (azaz: legalább egy II. szintű vagy legalább három III. szintű vizsgálat egybehangzó eredménye támasztja alá)
C: Az adott beavatkozás hatásossága lehetséges (legalább két III. szintű vizsgálat meggyőző és egybehangzó eredménye támasztja alá)
10. A BTX-A kezeléssel kapcsolatos tudományos eredmények összefoglalása az egyes kórképekben: 10.1. Blepharospasmus:
Három kettős vak és egy szimpla vak vizsgálat eredménye szerint a blepharospasmus eredményesen kezelhető 2-3 hónapig BTX-A-val. Bár a vizsgálatok jó része kevés beteget vont be, és rövid ideig tartott, a hatás mértéke alapján (kezelt a betegek 90%-a javult) továbbra sem valószínű, hogy a jövőben placebo-kontrollált nagy randomizált vizsgálatot terveznének (Costa és mtsai, 2004).
10. 2. Hemifacialis spasmus:
Nagy, nyílt eset-kontroll vizsgálatok, valamint egy kis, placebo kontrollált randomizált vizsgálat a kezelést a betegek 76-100%-ában találta hatásosnak. Bár nincs nagy létszámú, kontrollált, kiváló minőségű vizsgálat, az eddigi eredmények alapján nagy, placebo kontrollált vizsgálatok nem várhatók, mivel az eddigi adatok alapján a BTX-A kezelés hatásos és biztonságos (Costa és mtsai, 2005a).
10.3. Torticollis spastica
Tizenhárom, kiváló minőségű, randomizált, placebo-kontrollált vizsgálat szisztematikus összefoglalása alapján a beavatkozás statisztikailag és klinikailag is szignifikáns javulást eredményez. Mellékhatásként a nyakizmok gyengeségét, dysphagiát, szájszárazságot, torokfájdalmat és rekedtséget írtak le. Mind a hatások, mind a mellékhatások tekintetében egyértelmű volt a dózis-hatás összefüggés. A két forgalomban lévő készítmény (a Botox és a Dysport) között nem volt különbség sem a hatás, sem a mellékhatások vonatkozásában közvetett (Costa és mtsai, 2005b) és direkt összehasonlításban sem (Balash és Giladi, 2004). A kórképben korábban használt antikolinerg szerekhez képest a BTX-A hatásosabb, és jobban tolerálható (Costa és mtsai, 2005c)
10. 4. Egyéb dystoniák
A BTX-A-t próbálták oromandibularis dystoniában (egyetlen placebo-kontrollált, kettős vak vizsgálat). Laryngealis dystoniákban nagy betegszámot felölelő nyílt vizsgálatokban egyértelmű, jelentős klinikai javulást dokumentálnak (Gibbs 2000), de csak egy randomizált vizsgálat történt (Watts és mtsai, 2004). Az írás görcsben (writer's cramp) két placebo kontrollált vizsgálat történt. A kevés beteget felölelő vizsgálatok alapján a BTX-A ebben a kórképben is hatásos, de a kellő számú beteget felölelő randomizált kontrollált vizsgálatok kis száma miatt itt C erősségű ajánlás tehető.
10.5. spasticus cerebralis paresis gyermekkorban (Little-kór)
Gyermekkori spasticus cerebralis paresisben alsó végtagi spasticitás BTX-A kezelésére vonatkozó első szisztematikus összefoglaló (Ade-Hall és Moore, 2000) 3 randomizált, kontrollált vizsgálatot említ. A 3 vizsgálatból kettő javulást tapasztalt, de a kis elemszám miatt határozott ajánlás nem tehető. Egy későbbi szisztematikus összefoglaló (Boyd és Hays, 2001) már 10 randomizált vizsgálatot talált. Az elemzés közepes mértékű, és dózisfüggő hatást talált.
A felső végtagi tünetek kezeléséről is készült szisztematikus összefoglaló (Wasiak és mtsai, 2004). A két, kis számú beteget elemző randomizált vizsgálat alapján határozott ajánlást nem lehetett tenni. A felső végtagi dysfunctio kezeléséről egy másikszisztematikus összefoglaló is készült (Boyd és mtsai, 2001). Elsöprő hatásról ez sem számolt be, a BTX-A hatása leginkább az injekciót követő 3-4 hétig tart, további randomizált vizsgálatokat tartanak szükségesnek. Hasonló következtetésre jutott Hoare és Imms (2004) összefoglalója is.
Gyermekkori spasticus cerebralis paresis BTX-A kezelésére 2000-ben jelent meg kis részben kontrollált vizsgálatokra, nagyobbrészt konszenzusra alapuló klinikai irányelv, mely részletesen kitér a fizikális vizsgálatra, a kezelendő izmok kiválasztásának módjára, az adagolásra, a kezelésre alkalmas betegek kiválasztásának módjára, a kezelés időzítésére, és a kezelést végzők képzésére (Graham és mtsai, 2000).
10.6. Botulinum toxin alkalmazása felnőttkori spasticitásban
Tíz placebo kontrollált tanulmány igazolta a BTX hatásosságát és biztonságosságát a felső végtag spasticitásban. Az ismételt kezelések során is megmarad a toxin hatékonyság. Más nem kontrollált tanulmányok is hasonló eredményeket közölnek. Egy meta-analízis szintén alátámasztja a spasticitás csökkenését és a kar funkcionális javulását.
11. A BTX-A kezeléssel kapcsolatos eddigi irányelvek
A BTX-A kezeléssel kapcsolatosan a következő irányelveket vettük figyelembe: A 2005. évi magyar klinikai irányelvet.
Az Amerikai Neurológiai Akadémia (American Academy of Neurology) 2008. évi irányelvét, mely szerint a botulin toxin kezelés felnőttkori spaszticitásban A erejű az izomtónus csökkentésében és B erejű az aktív működés javításában.
Spanyol neurológiai társaság 2007 decemberében kiadott irányelvét.
12. A Neurológiai Szakmai Kollégium ajánlásai
A fentiekáttekintése utána Neurológiai Szakmai Kollégiuma BTX-A alkalmazására a következőajánlásokatfogalmazza meg:
12.1. Indikáció
1. Blepharospasmus (ajánlás: A; bizonyítékok szintje: I-II)
2. Hemifacialis spasmus(ajánlás:A; bizonyítékok szintje: I-III)
3. Spasticus torticollis (ajánlás: A; bizonyítékok szintje: I-II)
4. Laryngealis dystoniákban(ajánlás C; bizonyítékok szintje II-III)
5. Felsővégtagi spasticitás(ajánlás: A; bizonyítékokszintje:I-II)
amennyiben a módosított Asworth Skála1 pontszáma 3, 4, szisztémás gyógyszeres kezeléssel, fizikoterápiával nem javítható, ill. a mellékhatás(ok) miatt a gyógyszeres kezelés nem alkalmazható.
6. Cerebralis paresisek spasticus formái gyermekekben: (ajánlás: B; bizonyítékok szintje: II)
spasticus agyi bénulás spasticus kétoldali bénulás spasticus féloldali bénulás dystoniás bénulás spasticus hemiplegia spasticus paraplegia spasticus tetraplegia
A gyermekek kiválogatásának speciális szempontjai azoknál a betegeknél alkalmazható, akiknél
1. a fenti kórképekben az izom hyperaktivitás olyan mértékű, mely a mozgásukat jelentősen rontja, ágyhoz, ill. tolókocsihoz köti a betegeket;
2. a korábban alkalmazott gyógyszeres kezelés eredménytelen;
3. olyan "dinamikus deformitasok" vannak, melyek más gyógyszeres kezeléssel nem oldhatók;
4. az állapotjavulása csak egy későbbi műtéttől várható.
12.2. Kontraindikáció
1. Myasthenia gravis vagy Eaton Lambert szindróma
2. A készítmény bármely ismert összetevője iránt ismert túlérzékenység
3. Felsővégtagi spasticitásnál és cerebralis bénulásnál speciális kizárási szempont:
- a célízület fix kontraktúrája,
- korábbi sebészi kezelés.
12.3. A kezelendő betegek várható száma
1. Blepharospasmus, hemifacialis spasmus, spasticus torticollis: 700/beteg/év + évi 10% növekedéssel kell számolni (a megkezdett kezelést 2-4 havonta a beteg élete végéig kell folytatni)
2. Felsővégtagi spasticitás: Kezdetben központonként (hét központ aktív) 15 beteg kezelésének finanszírozását kellene biztosítani (legyen lehetőség a központok között átcsoportosításra).
3. Cerebralis paresis spasticus formái (gyermekekben): a jelenleg finanszírozott betegszám 150 - 160 + évi 15 % növekedés.
12.4. Alkalmazható készítmények hatóanyaga botulinum toxin-A
12.5. A kezelés gyakorisága
A klinikumtól függően2-4 havonta.
12.6. Költséghatékonysági elemzés
Az irányelvhez jelenleg nem csatlakozik költséghatékonysági elemzés. 13. Irodalomjegyzék
1. Ade-Hall RA, Moore AP. Botulinum toxin type A in the treatment of lower limb spasticity in cerebral palsy. The Cochrane Database of Systematic Reviews 2000, Issue 1. Art. No.: CD001408. DOI: 10.1002/14651858.CD001408.
2. Assessment: Botulinum neurotoxin for the treatment of spasticity (an evidence-based review) Report of the Therapeutics and Technology Assessment of the American Academy of Neurology. Neurology 2008;70:1691-1698
3. Balash Y, Giladi N. Efficacy of pharmacological treatment of dystonia: evidence-based review including meta-analysis of the effect of botulinum toxin and other cure options. Eur J Neurol. 2004;11:361-370.
4. Brashear A et al: Intramuscular injection of Botulin Toxin for the treatment of wrist and finger spasticity after a steoke. The New England Journal of Medicine 2003;348(3): 2585. Bihari K. Safety, effectiveness, and duration of effect of BOTOX after switching from Dysport for blepharospasm,
cervical dystonia, and hemifacial spasm. Current Medical Research and Opinions 2005 :21:433-438
6. Boyd RN, Hays RM. Current evidence for the use of botulinum toxin type A in the management of children with cerebral palsy: a systematic review. Eur J Neurol. 2001;8(Suppl 5):1-20.
7. Boyd RN, Morris ME, Graham HK. Management of upper limb dysfunction in children with cerebral palsy: a systematic review. Eur J Neurol. 2001;8(Suppl 5):150-166.
8. Brainin M, Barnes M, Baron JC, Gilhus NE, Hughes R, SelmajK, Waldemar G; Guideline Standards Subcommittee of the EFNS Scientific Committee. Guidance for the preparation of neurological management guidelines by EFNS scientific taskforces-revised recommendations 2004. Eur J Neurol. 2004;11:577-581.
9. Brin MF. Dosing, administration, and a treatment algorithm for use of botulinum toxin A for adult-onset spasticity. Spasticity Study Group. Muscle Nerve Suppl. 1997;6:S208-20.
10. Costa J, Espírito-Santo C, Borges A, Ferreira JJ, Coelho M, Moore P, Sampaio C. Botulinum toxin type A therapy for blepharospasm. The Cochrane Database of Systematic Reviews 2004, Issue 2. Art. No.: CD004900. DOI: 10.1002/14651858.CD004900.pub2.
11. Costa J, Espírito-Santo C, Borges A, Ferreira JJ, Coelho M, Moore P, Sampaio C. Botulinum toxin type A therapy for hemifacial spasm. The Cochrane Database of Systematic Reviews 2005a, Issue 1. Art. No.: CD004899. DOI: 10.1002/14651858.CD004899.pub2.
12. Costa J, Espírito-Santo C, Borges A, Ferreira JJ, Coelho M, Moore P, Sampaio C. Botulinum toxin type A therapy for cervical dystonia. The Cochrane Database of Systematic Reviews 2005b, Issue 1. Art. No.: CD003633. DOI:
10.1002/14651858.CD003633.pub2.
13. Costa J, Espírito-Santo C, Borges A, Ferreira JJ, Coelho M, Sampaio C. Botulinum toxin type A versus anticholinergics for cervical dystonia. The Cochrane Database of Systematic Reviews 2005c, Issue 1. Art. No.: CD004312. DOI: 10.1002/14651858.CD004312.pub2.
14. New Guidelines from AAN on Botulinum Neurotoxin . Neurology 2008; 70:1691-1698,1699-1706,1707-1714
15. Fármacos locales. Toxina botulinica tipo A en distonias focales. Neurol. Suppl 2007 ;3 (6): 34-40
16. Francis HP, Wade DT, Turner-Stokes L, Kingswell RS, Dott CS, Coxon EA. Does reducing spasticity translate into functional benefit? An exploratory meta-analysis. J Neurol Neurosurg Psychiatry 2004;75:1547-1551.
17. Hoare BJ, Imms C. Upper-limb injections of botulinum toxin-A in children with cerebral palsy: A critical review of the literature and clinical implications for occupational therapists. Am J Ocuup Ther 2004;58:389-397
18. Graham HK, Aoki KR, Autti-Ra I, Boyd RB, Delgado MR, Gaebler-Spira DJ, Gormley ME, Guyer BM, Heinen F, Holton AF, Matthews D,MolenaersG, Motta F,Garcy'a Ruiz PJ, Wissel J. Recommendations for the use of botulinum toxin type A in the management of cerebral palsy. Gait and Posture 2000; 11:67-79
19. Gibbs SR, Blitzer A.Botulinum toxin for the treatment of spasmodic dysphonia. Otolaryngol Clin North Am 2000;33:879-94.
20. Royal College of Physicians. Guidelines for the use of botulinum toxin (BTX) in the management os spasticity in adults. Royal College of Physicians, London, 2002
21. Turner-Stokes L, Ward A. Botulinum toxin in the management of spasticity in adults. Clin Med. 2002;2:128-130.
22. Ward AB, Wissel J, Molteni F, Yakovleff A, Gedin S, Aguilar M, Kanovsky P, Zegers de Beyl D. European consensus statement on the use of botulinum toxin type A in the management of adult spasticity. Acta Neurol Belg.2003;103:39.
23. Wasiak J, Hoare B, Wallen M. Botulinum toxin A as an adjunct to treatment in the management of the upper limb in children with spastic cerebral palsy. The Cochrane Database of Systematic Reviews 2004, Issue 4. Art. No.: CD003469. DOI: 10.1002/14651858.CD003469.pub3.
24. Watts CCW, Whurr R, Nye C. Botulinum toxin injections for the treatment of spasmodic dysphonia. The Cochrane Database of Systematic Reviews 2004, Issue 3. Art. No.: CD004327. DOI: 10.1002/14651858.CD004327.pub2.
14. MELLÉKLETEK
14.1. A módosított Asworth Skála
0 Nincs tónusfokozódás
1 Enyhe tónusfokozódás, megakadásban és ellazulásban nyilvánul meg, vagy minimális rezisztencia érezhető a mozgás végén, a végtag flexiós-extensiós, ill. abductiós-adductiós mozgatása során.
1+ Enyhe tónusfokozódás, megakadásban nyilvánul meg, amit minimális ellenállás követ a mozgás hátralévő (a mozgás tartomány kevesebb mint fele) részében.
2 Kifejezettebb izomtónus fokozódás, ami a mozgástartomány nagyobb részében érezhető, de az érintett végtag könnyen mozgatható.
3 Kifejezett izomtónus fokozódás, a passzív mozgás nehéz
4 Az érintett végtag flexioban vagy etensióban (abductióban vagy adductióban) rigid.
14.2. Javasolt adagolás (BOTOX-ra vonatkoztatva)
1. Blepharospasmus szemenkéntlO -30 E
2. Hemifacialis spasmus 10-30 E
3. Spasticus torticollis 50-300 E
| Nyaki dystonia típusa | Kezelendő izom |
| Rotatoros | contralateralis sternocleidomastoideus ipsilateralis splenius capitis |
| Retrocollis | bal splenius capitis jobb splenius capitis |
| Laterocollis | ipsilateralis sternocleidomastoideus ipsilateralis splenius capitis ipsilateralis trapezius |
| Dystonias fejtremor | bal splenius capitis jobb splenius capitis |
4. Felsővégtag spasticitás: 50 - 250 E az izom méretétől és a spasticitas fokától függően
5. Gyermekkori adagolás
5.1. Az izom méretétől és a spasticitas fokától függően, de kezdő adagként 1,25-2,5 E/tskg,
5.2. Testméretektől, súlytól függő individualis adagolás is elképzelhető,
5.3. Egy alkalommal min. 50, max. 300 E adható (testsúlyra meghatározva a maximális dózis 12 E/tskg). Equivalens dózisok: 1 E Botox = - 4-5E Dysport
14.3. A központok minimum feltételei
Tárgyi: toxin biztonságos tárolása, hűtőszekrény, elérhető EMG készülék*,
ajánlott speciális - infiltrációra alkalmas - EMG tű Személyi: kezelésben, izmok infiltrálásában és/vagy EMG-ben jártas orvos kisegítő szakszemélyzet.
*Elektromyographia (EMG): a célizom speciális tűelektródával történő vizsgálata, melynek során lehetséges a Botox beadása is.
A központok kaphatnak részleges akkreditációt is:
1. Blepharospasmus, hemifacialis spasmus kezelésénél az EMG készülék nem szükséges;
2. Torticollis kezelésénél ajánlott az EMG, de nem kötelező;
3. Felsővégtagi spasticitásban és cerebralis bénulásban az EMG kötelező feltétel.
Az Egészségügyi Minisztérium
szakmai protokollja
A glenohumeralis ízület instabilitásáról
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
Szinonimák: vállízületi instabilitás
I. Alapvető megfontolások
1. A protokoll alkalmazási, érvényességi területe
- Ortopédia, traumatológia, rheumatológia
- Családorvos - kompetencia szintnek megfelelően
2. A protokoll bevezetésének alapfeltétele
- Ortopéd Szakmai Kollégium legitimációja
- Ortopéd szakmai minimum feltételeknek megfelelő ellátás szerint
3. Definíció
A humerus fejének a cavitas glenoidalishoz képest történő, panaszt okozó, kóros mértékű elmozdulását nevezzük glenohumeralis instabilitásnak.
3.1. Kiváltó tényezők
- A humerusfejelülső ficama típusosan extenziós kirotációs mozdulatra jön létre míg a hátsó ficama flexiós berotációs mozdulatra.
- Többirányú instabilitás esetén patológia hátterében a vállízület szalagrendszerének túlzott lazasága, nagyon gyakran generalizált izületi lazaság, továbbá a scapulothoracalis és gelnohumeralis izomzat működési zavara áll.
- Akaratlagos ficam hátterében keresni kell az iskolai, családi vagy egyéb magánéleti konfliktust.
3.2. Kockázati tényezők
- Fiatal életkor
- Sportolás
- Fizikai munka
- Általános ízületi lazaság
- Idős korban a masszív rotátorköpeny szakadás
4. Panaszok, tünetek, általános jellemzők
A vállízületi ficam a váll rugalmas kötöttségével, fájdalommal jár. Bizonyos esetekben a felső végtagon zsibbadás, érzészavar is észlelhető.
5. A betegség leírása
- A vállízület posttraumás visszatérő elülső vagy hátsó instabilitásáról akkor beszélünk, ha először megfelelő traumás behatásra ficamodik a humerusfeje a vállízületben, majd a ficama későbbiekben akár kis erőbehatásra is ismétlődhet. A ficam illetve instabilitás iránya mindig ugyanaz (elülső vagy hátsó). A traumás vállficam jellemzője az elülső alsó capsulo-labralis komplexum glenoidalis peremről való leválása az ún. Bankart-laesio, valamint a humerusfej hátsó felső részén keletkező impressios törés az ún. Hill-Sachs-laesio.
- A vállízület multidirekcionális instabilitásáról akkor beszélünk, ha a humerus feje váltakozó jelleggel akár több irányban is képes elhagyni a vápát és az erőbehatás rendszerint mérsékelt vagy minimális. Csak ritkán észlelhető Bankart-laesio vagy Hill-Sachs-laesio.
- Akaratlagos vállficam esetén a beteg saját maga képes ficamot előidézni.
5.1. Érintett szervrendszerek
- Humerusfej, cavitas glenoidalis
- Rotátorköpeny izmai és inai
- Gnohumeralis ízület tokja
- Labrum glenoidalis
- Nervus axillaris
- Plexus brachialis
- Egész vállövi izomzat
5.2. Genetikai háttér
Genetikai érintettség egyedül a multidirectionalis instabilitás esetén fordul elő, mint általános ízületi lazaság.
5.3. Incidencia / Prevalencia / Morbiditás / Mortalitás Magyarországon A vállízületi ficam a leggyakoribb ízületi ficam.
5.4. Jellemző életkor
- A ficam külső erőbehatásra bármely életkorban előfordulhat. Jellemző, hogy minél fiatalabb a beteg az első ficam idején, annál nagyobb a valószínűsége a ficam ismétlődésének.
- Minél idősebb a beteg annál nagyobb a valószínűsége a rotátorköpeny járulékos szakadásának, továbbá a humerus proximális vég vagy a glenoidalis perem törése.
- Többirányú instabilitás esetén a panaszok elsősorban a kamaszkorban vagy fiatal felnőttkorban jelentkeznek és az évek előrehaladásával fokozatosan enyhülnek vagy spontán megszűnnek.
5.5. Jellemző nem
- Az egyirányú posttraumás visszatérő ficam férfiaknál gyakoribb.
- A multidirectionalis instabilitás nőknél gyakoribb.
II. Diagnózis
1. Diagnosztikus algoritmusok
A vállízületi instabilitás diagnózisa pontos anamnesis felvétellel és gondos fizikális vizsgálattal az esetek többségében biztonsággal felállítható. A vizsgálatokat a következő sorrendben, az alábbiak figyelembe vételével kell végezni.
2. Anamnesis
Vizsgálni kell az első, majd az ismétlődő ficamok, vagy ficamra utaló sérülések körülményeit, az erőbehatás jellegét vagy éppen hiányát, a feltételezett ficam irányát, a vele járó járulékos tüneteket (zsibbadás, gyengeség érzés, fájdalom), a repozíció körülményeit, az esetleges orvosi ellátással kapcsolatos dokumentumokat.
3. Fizikális vizsgálat
Az alábbi vizsgálatokat mindkét vállízületen el kell végezni. A két oldalon észlelt tünetek és vizsgálati lelet összehasonlításából következtethetünk a kóros elváltozásokra.
A vizsgálat megtekintéssel kezdődik, mely során megfigyeljük az esetleges nyugalmi alaki eltéréseket, izomsorvadást, tartási rendellenességeket. Ugyanezt megfigyeljük az aktív mozgások során. Az aktív mozgásterjedelmet ezután összehasonlítjuk a passzív mozgásterjedelemmel, közben figyeljük a mozgás kiváltotta esetleges fájdalmat és egyéb kóros eltéréseket (pl. intraarticularis roppanás, subluxatio, ficam).
Ezt követik az instabilitási tesztek úgymint elülső és hátsó apprehenziós próba, elülső és hátsó asztalfiók tünet, sulcus tünet. Vizsgáljuk a lapockamozgató, a rotátorköpeny és a m. deloideus erejét és a válltájék egyes pontjainak nyomásérzékenységét. A vizsgálat része egy tájékozódó felső végtagi neurológiai vizsgálat is.
4. Kötelező diagnosztikai vizsgálatok
Anamnezis értékelése, fizikális vizsgálat, képalkotó diagnosztika, szükség esetén kiegészítve laboratóriumi vizsgálattal.
4.1. Laboratóriumi vizsgálatok Nem feltétlenül szükségesek.
4.2. Képalkotó eljárások
Minimális követelmény az érintett váll 2 irányú, felvétele, ami lehetőség szerint a glenohumeralis ízület antero-posterior és axillaris felvétele.
Szükség esetén kiegészíthető scapula lateralis felvétellel vagy egyéb speciális ferde felvételekkel. Kétes esetben elvégzendő az ép oldal összehasonlító röntgen vizsgálata. (B típusú evidencia).
5. Kiegészítő diganosztikus vizsgálatok (B típusú evidencia).
Kétes diagnózis esetén, vagy a társsérülések tisztázása miatt lehet rá szükség
- Vállöv ultrahang vizsgálata a rotátorköpeny és labrum állapotáról ad információt
- MRI vizsgálat a rotátorköpeny és labrum állapotáról, valamint a csontok állapotáról ad információt
- CT és CT arthrogramm a labrum és a csontos anatómiáról (Hill-Sachs-laesio, csontos Bankart-laesio, glenoidalis dysplasia) ad információt
- Arthroscopos vizsgálatra ritkán szükség lehet, ez már a műtéti kezelés részét képezi.
6. Differenciál diagnosztika (B típusú evidencia)
- Rotátorköpeny szakadás
- Cervico-brachialis szindróma
- Thoracic outlet szindróma
- Glenohumeralis arthorsis
- Acromio-clavicularis arthrosis
- Rheumatoid arthritis
- Humerusfej necrosis
- Adhesivcapsulitis (befagyott váll)
- Bármely válltáji fájdalommal járó kórkép.
III. Terápia
Nem gyógyszeres kezelés
1. A megfelelő egészségügyi ellátás szintje ÁNTSz minimumfeltételek alapján
2. Általános intézkedések (B típusú evidencia)
A lapocka stabilizáló izmok és a rotátorköpeny erősítő tornája a multidirectionalis instabilitás elsődleges kezelési módszere, de unidirectionalis instabilitásban is hatékony lehet.
Akaratlagos ficam esetén a beteg és környezetének felvilágosítása, szükség esetén kezelése pszichológus vagy pszichiáter bevonásával.
3. Speciális ápolási teendők
Mozgássérült állapotának súlyosságától függően szóba jöhet speciális vállízületi rögzítő alkalmazása.
4. Fizikai aktivitás (B típusú evidencia)
A panaszokat kiváltó sport vagy munkatevékenység körülményeinek felülvizsgálata, módosítása, szükség esetén szüneteltetése.
5. Diéta
Nincs szerepe a kezelésben.
6. Betegoktatás (B típusú evidencia)
Általános betegtájékoztató, felvilágosítás, tanácsadás, életmód-terápia.
IN/2. Gyógyszeres kezelés
Nincs szerepe a kórkép kezelésében.
MI/3. Műtét
1. A megfelelő egészségügyi ellátás szintje Járóbeteg ellátás: ÁNTSz működési engedély alapján.
Fekvőbeteg ellátás / műtéti tevékenység: ÁNTSz működési engedély alapján.
2. Általános intézkedések 2.1.A műtét tárgyi feltételei
- Kiemelt sterilitást biztosító műtő, az ÁNTSz minimumfeltételeknek megfelelően felszerelve.
- A műtét biztonságos kivitelezését biztosító általános műszerkészlet. 2.2. A műtét személyi feltételei
- Minősített műtéti eljárás, amelynek végzésére olyan (szak)orvos vállalkozhat, aki az műtétek kivitelezésében alapos tapasztalatot szerzett. Képes a műtét biztonságos kivitelezésére és a műtét során adódó szövődmények, komplikációk ellátására.
- Egy vagy több műtéti asszisztens.
- Anaesthesiológus orvos.
- További szakemberek: gyakorlott műtősnő, műtőssegéd.
3. Speciális ápolási teendők
A műtétet követően, a beteg általános belgyógyászati statusában felmerülő állapot-változások korrekciójának biztosítása.
4. Sebészeti kezelés (B típusú evidencia)
4.1. Műtéti indikáció
Ismétlődő posttraumás vállficam esetén mindig ajánlott a műtéti kezelés.
Multidirekcionális instabilitás esetén minimum 6 hónap eredménytelen konzervatív kezelés (értsd alatta intenzív rotátorköpeny és lapocka stabilizáló izomzat erősítő tornája) esetén jön szóba műtét.
4.2. Műtéti kontraindikáció
- A vállízület lágyrészeinekés/vagy csontjainak gyulladásos megbetegedése
- Pustula, pyoderma a beteg bőrén bárhol
- A beteg rossz általános állapota (cardiális decompensatio, sepsis, thombosis gyanuja)
- Rossz kooperációs készség
- Akaratlagos vállficam
4.3. Műtéti előkészítés
Általános belgyógyászati kivizsgálás, szükség szerinti szakorvosi konzíliumokkal kiegészítve. Anaesthesiologiai protokoll szerinti előkészítés.
4.4. Műtéti érzéstelenítés:
A műtét végezhető általános érzéstelenítésben (altatás bármely formájában) valamint vezetéses érzéstelenítésben (interscalenicus blokád) az anaesthesiologiai protokoll leírása szerint
4.5. Műtét
Beavatkozás neve: A vállízületet stabilizáló műtét, melynek számos változata ismert.
A diagnózis és technikai lehetőségek függvényében lehet arthroscopos vagy nyitott stabilizációs műtét
Arthroscopos műtét:
Eszközigény: hidegfényoptikás videorendszer, speciális kézi műszer készlet, shaver, műtői tartozékok, folyadékpumpa, vízmentes izolálás
Az arthroscopos stabilizációt az irodalmi hivatkozásban listázott műtéttani könyvekben leírt műtéti technikát követve végezzük.
Nyitott stabilizációs műtétek (B típusú evidencia)
Számos nyitott stabilizációs műtét létezik, melyek közül az észlelt pathológiai elváltozás és a műtétet végző sebész gyakorlata alapján választhatunk. Az indikációs szempontokat és a műtéttechnikai leírást az irodalmi hivatkozásban szereplő szakkönyvek tartalmazzák. Leggyakoribb lágyrész műtétek:
- Bankart műtét
- Neer szerinti tokplasztika
- Putti-Platt műtét
- Egyéb tokplasztikák Leggyakoribb csontos műtétek:
- Bristow-Latrajet műtét
- Eden-Hybinette műtét
- Csontblokk beültetés
Eszközigény: vállsebészeti feltáró alaptálca, speciális kézi műszer készlet, vízmentes izolálás, műtői alapfelszereltség, diatermiás eszköz
4.6. Posztoperációs teendők
- A műtét menetének részletes leírása, a műtéti leírás csatolása kórlaphoz, archiváláshoz.
- A közvetlen postoperatív szakban fokozott felügyelet szükséges: szívódrainen keresztül ürült mennyiség regisztrálása, folyadékháztartás (só-elektrolit, sz.sz. vérpótlás) rendezése, fájdalomcsillapítás, a beteg ált. belgy. statusának ellenőrzése érdekében.
- A postoperatív szakban a műtött végtagot levehető kartartóval, Dessault- kötéssel vagy Gilchrist-kötéssel immobilizáljuk. Speciális esetben szükség lehet törzs-kar gipsz vagy egyéb orthesis alkalmazására.
- Kórházi ápolás 2-5 nap.
- Amennyiben alkalmaztunk draint, azt a műtét után 24 órával, a varratokat 10-12 nap elteltével kell eltávolítani.
- A műtét után thrombosis profilaxis rutinszerű alkalmazása nem szükséges. A thrombosis szempontjából rizikó csoportba tartozó betegekesetén a profilaktikusantithrombotikus kezelést egyéni elbírálás alapján kell alkalmazni. (A típusú evidencia)
5. Fizikai aktivitás
A műtéti típustól függően, a szakkönyvek iránymutatása alapján a rögzítési idő 1-6 hét lehet, mely időtartam alatt bizonyos előírt mozgások megengedettek. A rögzítés megszűntetése után a szakkönyvek útmutatása alapján, a műtéti típustól függően kell utókezelést végezni.
6. Diéta
Általános, vagy belgyógyászati indikációnak megfelően, dietetikai előírások szerint.
7. Betegoktatás
Általános betegtájékoztató szerint. III/4. Egyéb terápia
A beteg életkorához és fizikai aktivitási szintjéhez (munka, sport) szükséges tevékenység betanítása. Az életkörülmények, munka és sporttevékenység szükség szerinti módosítása.
IV. Rehabilitáció
A kórházi tartózkodás alatt
A beteg önálló járóképességének és önellátásának elérése fekvőbeteg osztályon, rehabilitációs részlegen, vagy házi ápolás keretében. Késői rehabilitáció
A beteg állapotának folyamatos ellenőrzése, utánkövetése, s amennyiben szükséges utókezelésre, gyógytorna kezelésre juttatása, otthoni ápolás elősegítése, sz.e. gyógyszeres kiegészítő kezelés. Végső cél a munkába való visszaállítás illetve a szokásos napi tevékenységi szint elérése.
V. Gondozás
1. Rendszeres ellenőrzés
Szövődménymentes esetben kontroll 4 alkalommal szükséges. Az első kontroll ideje a varratszedés időpontja, majd 6 hét, 12 hét és 6 hónap múlva.
A kontrollvizsgálatok során elegendő a fizikális vizsgálat. Radiológiai, laboratóriumi, vagy egyéb vizsgálatra csak szövődmények gyanúja esetén van szükség.
Társsérüléssel (rotátorköpeny laesio, törés, idegi sérülés) járó esetekben a postoperatív kezelés, a munkába, sportba való visszaállás időpontja a társsérüléstől függően a fenti protokolltól eltér.
2. Megelőzés
A betegséghez vezető kiváltó okok megszűntetése.
Az utókezelés során betanított gyógytorna otthoni rendszeres folytatása.
3. Lehetséges szövődmények
- Korai szövődmények:
- Infekció (valószínűsége 1% hagyományos műtőben)
- Haematoma
- Sebgyógyulási zavar
- Késői szövődmények:
- Ficam ismétlődése
- Arthrosis kialakulása
- Mozgásbeszűkülés
3.1. Szövődmények kezelése (B típusú evidencia)
Fontos a postoperatív localis szövődmények korai ellátása. Infectio gyanúja esetén korai feltárás, alapos debridement és átmosás majd szívódrainek behelyezése javasolt. Steril haematomát a műtőben steril körülmények között kell kiüríteni. Sebgyógyulási zavar, illetve bőrnecrosis esetén annak kiterjedésétől függően felületes hámosító kezelés vagy a defectus sebészi zárása szükséges (szükség esetén igénybe véve plasztikai sebész segítségét.) A késői szövődmények ellátását az adott betegségre vonatkozó szakmai szabályok szerint kell végezni.
4. Kezelés várható időtartama / Prognózis
A betegek az átlagos fizikai megterhelést igénylő munkát a műtétet követő 4-6 héten, a nehéz fizikai munkát, a sportolást a 3-6. postoperatív hónapban kezdhetik el.
5. Ellátás megfelelőségének indikátorai
A kezelés eredményességét a ficam ismétlődésének elmaradása, az egyéb panaszok megszűnése (zsibbadás, gyengeség, fájdalom, ficamtól való félelem stb.) valamint a korábbi fizikai aktivitáshoz (munka, sport) való visszatérés jelentik.
VI. Irodalomjegyzék
1. Vízkelety: Az orthopaedia tankönyve Semmelweis Kiadó, 2002.
2. Campbells: Operative orthopaedics
3. Traumatológia tankönyv (szerk.: dr. Renner Antal) Medicina 2003.
4. Bulstrode et al.: Oxford Textbookof Orhopaedics and Trauma. Oxford University Press 2002.
5. Rockwood-Matsen: The Shoulder, Saunders 1990
6. Hawkins: Atlas of shouldersurgery, Mosby 1996
7. A Magyar Thrombosis és Haemostasis Társaság Konszenzus nyilatkozata a thromboemboliák megelőzése és kezeléséről 2001.
Kapcsolódó internetes oldalak Kapcsolodó internetes oldalak www.ortopedtarsasag.hu www.gyogytorna.lap.hu www.egeszseg.lap.hu
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Gyakori társbetegségek Tankönyvi adatoknak megfelelően
2. Érintett társszakmák
Traumatológia, Reumatológia, Fizioterápia, Gyógytorna, Radiológia
3. Evidencia besorolás
A bizonyítékok szintjei
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
A Carpal tunnel szindrómáról
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
I. Alapvető megfontolások
1. A protokoll alkalmazási, érvényességi területe ortopédia és kézsebészet
radiológia, elektrofiziológia
2. A protokoll bevezetésének alapfeltétele Ortopéd Szakmai Kollégiumi legitimációja
Szakmai minimum feltételeknek megfelelő Ortopédiai Osztály
3. Definíció
A Carpal tunnel syndroma a n .medianus kompressiója a carpalis alagútban.
3.1. Kiváltó tényezők (B típusú evidencia - 5) Esetek felében ismeretlen .
Másik felében kb. 60 féle ok deríthető ki, melyek közül a legfontosabbak a következők:
csontos ok: exostosis, törés utáni állapot,stb.
daganatok: ganglion, lipoma, stb.
ér eredetű okok: trhombosis, aneurysma
vérzéses ok: haematoma
szisztémás betegség: RA, psoriasis, köszvény, diabetes, tbc, stb.
oedema készség: antikoncipiens szedése, hypothyreosis, tartós művese kezelés, stb.
inakra visszavezethető ok: tenosynovitis
3.2. Kockázati tényezők
A 3.1. pontban leírt, ismert tényezők.
4. Panaszok, tünetek, általános jellemzők
A hüvelykujjtól a IV. ujj radialis oldaláig, valamint a radialis tenyérfélre terjedő zsibbadásról, illetve hypaesthesiáról számol be a beteg a csuklótáji fájdalom mellett, mely tünetek tipikusan éjszaka dominálnak, emellett a thenar izomzat gyengeségét is említi.
5. A betegség leírása
5.1. Érintett szervrendszer
csukló-, kéztáji idegrendszer, izomrendszer (B tipusú evidencia - 7)
5.2. Genetikai háttér nem ismert
5.3.. Jellemző életkor és nem
elsősorban nőkön, főleg menopausa táján fordul elő.
incidencia:O,1-10 % (az életkor előrehaladtával nő), a leggyakoribb idegkompressziós szindróma (B típusú evidencia - 1,8)
II. Diagnózis
1. Anamnézis
A hüvelykujjtól a IV. ujj radialis oldaláig, valamint a radialis tenyérfélre terjedő zsibbadásról,illetve hypaesthesiáról számol be a beteg a csuklótáji fájdalom mellett, mely tünetek tipikusan éjszaka dominálnak, emellett a thenar izomzat gyengeségét is említi. A kockázati tényezőknél leírtak színezhetik a klinikai képet.
2. Fizikális vizsgálatok (B tipusú evidencia - 4)
A fenti területen hypaesthesia észlelhető, enyhe esetekben tapintásra a thenar konzisztenciája lágyabb, súlyosabb esetekben a thenar izomzat láthatóan hypotrophias, Diagnosztikus jelek (B tipusú evidencia - 11)
- csökkent hüvelykujjopposició (I-es és az V-ös ujjbegy nem ér össze)
- Provokációs tesztek:
- Tinel-jel
- Phalen-teszt
3. Kötelező diagnosztikai vizsgálatok
3.1. Laboratóriumi vizsgálatok specifikus vizsgálat nincs, az ismert okok némelyike az alapbetegség miatt kóros laboreredményeket eredményezhet.
3.2. Képalkotó vizsgálatok:
Osteografiás felvételek
- csontos elváltozások kimutatására
UH és MRI vizsgálat (B tipusú evidencia - 9,10,l2)
- lágyrész elváltozások (térszűkítő folyamatok) kimutatására
EMG, idegvezetési sebesség vizsgálata:
- idegvezetési sebesség lecsökkenését bizonyíthatja a carpalis alagútban (B típusú evidencia - 6)
4. Differenciáldiagnosztika
A fent részletezett okokon kívül, nem egyértelmű tünetek esetén mindig szóba jön a nyaki gerinc eredet, a TOS szindróma, illetve demyelinisatios neurológiai elváltozások, pronator teres alagút szindróma. (B típusú evidencia - 10 )
5. Diagnosztikus algoritmus
A biztos diagnózis felállításához az anamnézis, a fizikális vizsgálat és az osteografiás felvételek (beleértve a carpalis alagút betekintő felvételt is) általában nem elégségesek, az ok tisztázására esetenként UH, illetve MRI vizsgálat is szükséges lehet, az EMG és idegvezetési sebesség vizsgálata viszont elengethetetlenül fontos.
III. Terápia
Nem gyógyszeres kezelés Korrekt terápia nélkül a betegség nem gyógyul.
III./2. Gyógyszeres kezelés
1. Ajánlott gyógyszeres kezelés
enyhébb esetekben (ahol nincs motoros kiesés) NSAID, vízhajtók adásával, fizioterápiás kezelésekkel meg kell próbálkozni, esetlegesen localisan adott steriod injectio, illetve éjszakai gipszsin alkalmazása is szóba jöhet.
III./3. Műtét
1. Műtéti indikáció
- akut carpal tunnel szindróma progresszíóval
- krónikus carpal tunnel szindróma eredménytelen konzervatív kezelés után
- motoros érintettség
- térszűkítő folyamat
- pozitív EMG és idegvezetési sebesség csökkenés hiánya esetén is, ha a klinikai kép egyértelmű
2. Műtéti kontraindikáció
Az alkar, csukló, kéz területére lokalizálódó gyulladásos megbetegedés.
Aktív gyulladásos bőrfolyamat.
A beteg rossz általános állapota, kooperáció hiánya.
Ha a beteg a műtétet felvilágosítás ellenére sem akarja.
3. Műtéti előkészítés
A kézsebészeti műtéti előkészítés általános szabályainak betartása mellett speciális előkészítést nem igényel.
4. Műtéti érzéstelenítés Általános, vagy axilláris anesztézia.
5. Műtét (WHO: 50432, B tipusú evidencia - 2, 3, 7.)
Végezhető nyílt feltárással, vagy endoszkóppal fedetten, kipólyázásos vértelenségben.
A műtét lényege a ligamentum carpi transversum teljes átvágása (ellenkező esetben "recidiva" alakulhat ki), ha van lokális kiváltó ok, azt együlésben megoldjuk. A műtét során ügyelni kell a n. medianus mozgató ágára, mely radialisan helyezkedik el, ezért célszerű a ligamentumot a n. medianus ulnaris oldalán átmetszeni. Vérzéscsillapítás után csak a bőrt zárjuk, drain visszahagyásával. Gipszrögzítés nem szükséges.
6. Posztoperációs teendők
- eleváció,10 napig komforkötés, vagy gipszrögzítés
- 2. posztoperatív naptól fokozatos teljes kéztorna végezhető, ha az inak épek
- thenarfunkciók kiesése esetén szükséges a szelektív ingeráram kezelés
IV.-V. Rehabilitáció, Gondozás
1. Rehabilitáció és rendszeres ellenőrzés
Szövődménymentes esetekben 1-2 kontroll vizsgálat szükséges, ezen esetekben gondozás, rehabilitáció nem szükséges.
Krónikus esetekben neurorehabilitációs kezelés jöhet szóba.
2. Megelőzés
Az ismert kiváltó tényezők feltárása esetén, azok kezelésével a súlyos állapot megelőzhető.
3. Lehetséges szövödmények idegsérülés,
infekció, sebgyógyulási zavar
4. Szövődmények kezelése
fenti szövődmények korai felismerése, azok műtéti korrekciója (idegsérülés), illetve sebgyógyulási zavarnál vagy konzervatív kezelése (antibiotikum, locális sebkezelés), vagy/és adott esetben műtéti feltárás.
5. Kezelés várható időtartama / Prognózis
A végeredmény a kórkép fennállásának idejével fordítottan arányos, azaz minél hosszabb az anamnézis, annál szerényebb eredmény várható.
6. Az ellátás megfelelőségének indikátorai
A műtött beteg speciális mozgásszervi státuszának a rögzítése biztosítja az állapotváltozás prospektív nyomonkövetését.(fájdalom mértékének változása, mentessége, mozgástartomány változása, érzészavar, motoros funkció változása)
VI. Irodalomjegyzék
1. Dr.Kómár József:Alagút szindrómák. Medicina Könyvkiadó, 1985.
2. Udvarhelyi Iván (szerk.) Fejezetek a felnőttkori ortopédia gyakorlatából. Medicina Könyvkiadó Rt.. 1998.
Kapcsolódó internetes oldal www.ortopedtarsasag.hu
Evidencia meghatározásnál felhasznált irodalom
1. Petterson JD, Simmons BP.: Outcomes assessment in carpal tunnel syndrome. Hand Clin. 2002 May,18 (2) :359-63
2. Higgins JP, Graham TJ.: Carpal tunnel release via limited palmar incision. Hand Clin. 2002. May, 18 (2) :299-306
3. Steinberg DR.: Surgical release of the carpal tunnel. Hand Clin. 2002 May, 18 (2):291-8.
4. Palumbo CF, Szabo RM.: Examination of patients for carpal tunnel syndrome sensibility, provocative, and motor testing. Hand Clin. 2002 May, 18 (2):269-77.
5. Michelsen H, Posner MA.: Medical history of carpal tunnel syndrome. Hand Clin. 2002 May, 18 (2 ):257-68.
6. Kilmer DD, Davis BA.: Electrodiagnosis in carpal tunnel syndrome. Hand Clin. 2002 May, 18 (2): 243-55.
7. Rotman MB, Donovan JP.: Practical anatomy of the carpal tunnel. Hand Clin. 2002 May, 18 (2): 219-30.
8. Porter P, Venkateswaren B, Stephenson H, Wray CC.: The influence of age on outcome after operation for the carpal tunnel syndrome. A prospective study. J Bone Joint Surg Br. 2002 Jul, 84 (5) :688-91.
9. El-Karabaty H, Hetzel A,GallaTJ, Horch RE, Lucking CH,Glocker FX.:The effect of carpal tunnel release on median nerve flattening and nerve conduction. Elektromyogr Clin Neurophysiol.2005 Jun, 45 (4):223-7
10. Jillapalli D, ShefnerJM.: Elektrodiagnosisin common mononeuropathiesand plexopathies.Semin Neurol. 2005 Jun,25 (2):196-203.
11. Wainner RS, Fritz Jm, Irrgang JJ, Delitto A, Allison S, Boninger ML..Development of a clinical prediction rule for the diagnosis of carpal tunnel syndrome. Arch Phys Med Rehabil. 2005 Apr, 86 (4):609-18.
12. Kotevoglu N,Gulbahce.Saglam S.:Ultrasound imaging in the diagnosis of carpal tunnel syndrome and its relevance to clinical evaluation. Joint Bone Spine. 2005 mar, 72 (2):142-5.
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Gyakori társbetegségek
Az ismert kiváltó tényezőknél felsoroltak.
2. Érintett társszakmák
Kézsebészet, Radiológia, Idegsebészet, Fizioterápia, Gyógytorna.
Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
A csontok áttétes tumorairól
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
I. Alapvető megfontolások 1. Általános elvek
Rosszindulatú daganatok, az úgynevezett primer szűrők, a tüdő és a máj után harmadik helyen leggyakrabban a csontrendszerbeadnakáttéteket. Sarcomák25%-ban, míg carcinomák 19%-ban adnakcsontmetastasist (6D, 9A,12D).
A csontáttétek 65-75%-át az emlő-, tüdő-, vese-, és prostata rák adja. Csontmetastasisok hozzávetőlegesen 40-60-szor gyakrabban fordulnak elő, mint a primer rosszindulatú csont tumorok. A leggyakrabban érintett csontok csökkenő sorrendben: ágyéki-, mellkasi-, nyaki csigolyák, a femur proximalis harmada, bordák, koponyacsontok, medence, sternum és humerus. Igen ritka a kéz és láb rövid csöves csontjaiban. (2B, 8C, 9A)
Csontáttétek első és leggyakoribb tünete a fájdalom, de kb. 8-29%-ban patológiás törés az első történés. Ennek hátterében 50%-ban emlő, 10-10%-ban vese és tüdőrák, 5%-ban pajzsmirigy rák osteolyticus metastasisa szerepel. Ritkán törnek és jó gyógyhajlammal bírnak a prostata rák osteoplasticus metastasisai. A patológiás törések lokalizációját tekintve elsősorban a hosszú csöves csontok proximalis része érintett (50%-ban a femur, 15%-ban a nem teherviselő humerus). (9A, 12D)
Az elmúlt évtizedben a palliatív kezelések kiszélesedésével és fejlődésévek, modern kemo-, radio- és hormonterápia bevezetésével a csont metastasisos betegek jelentős százaléka a statisztikai adatok szerint évekig betegségével együtt túlélhet. Ez jelentős szemléletváltozást hozott a sebészi stratégia kialakításában is. (13D)
II. Diagnózis
2. Diagnosztikai teendők (6D, 13D)

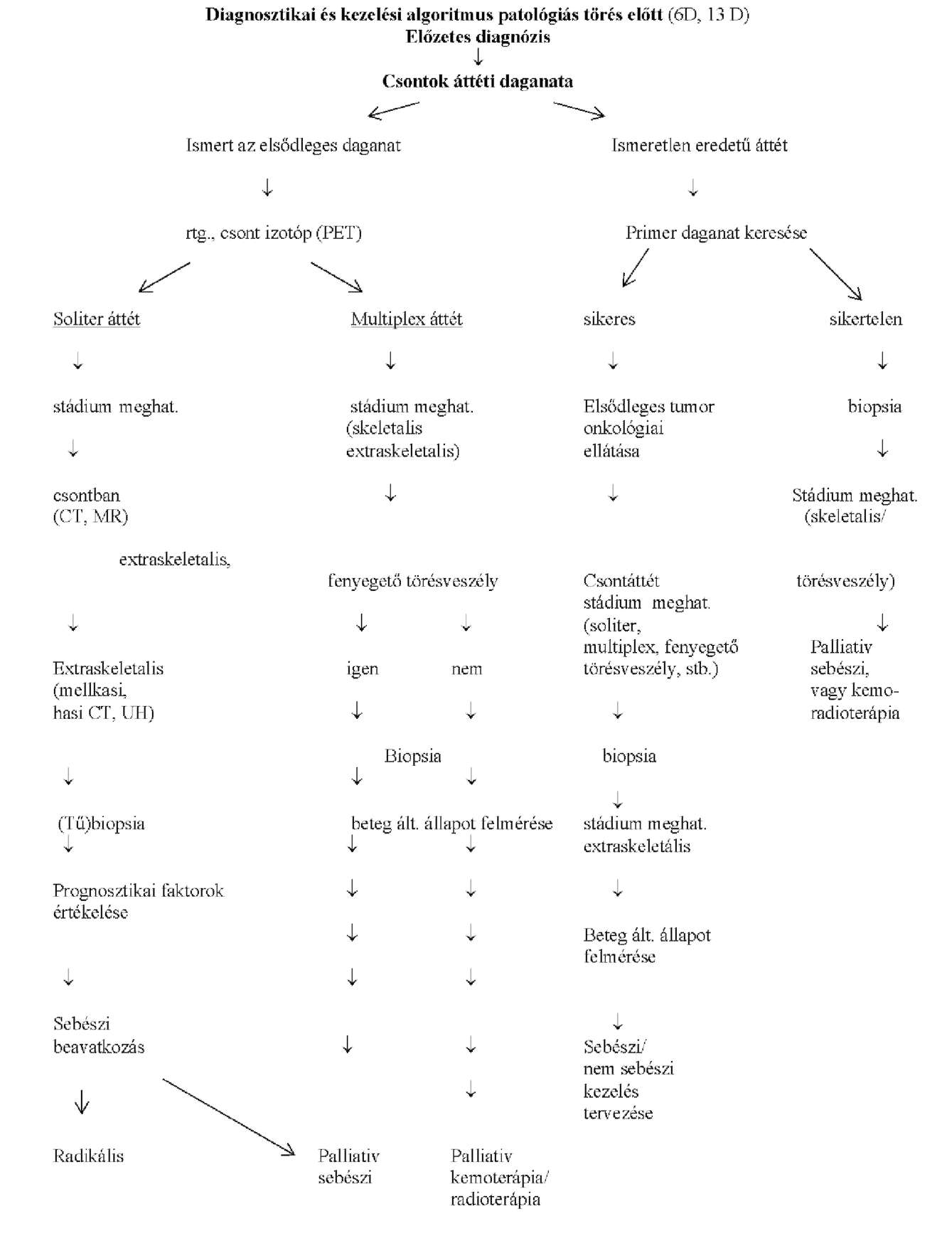
Megjegyzés: előzetes diagnózishoz igen fontos a gondos anamnézis, korábbi betegségek, műtétek explorálása.
A laborértékek kevésbé specifikusabb és hosszú ideig - különösen kis kiterjedésű soliter metastasisoknál - a normál határok között mozoghatnak.
Az első választandó képalkotó vizsgálat mindig a kétirányú summatiós röntgenfelvétel, melyek szükség szerint CT, MR vizsgálattal kell kiegészíteni. Csontizotóp vizsgálat, illetve a lokalizációt pontosabban jelölő SPECT vizsgálatok rendkívül fontosak, elsősorban folyamat soliter, multiplex voltának eldöntésére.
Fenyegető törésveszélyről beszélünk, ha a corticalis destructioja meghaladja az 50%-ot, illetve 2,5 cm-t. Pontosabb Mirels beosztása, mely figyelembe veszi a lokalizációt, fájdalmat, laesio jellegét és a defektus kiterjedését. (9A, 12D, 13D)
3. Patológiai vizsgálatok
Csontmetastasisok felismerésekor az esetek egy jelentős (20-40%) részében a primer tumor ismeretlen. Ilyenkor a csontlaesioból biopsiát végzünk. A szövettani vizsgálat rendszerint ritkán (10-35%) utal az elsődleges daganat szervi lokalizációjára.
Biopsiák formái:
- Aspirációs biopsia: ha technikailag kivitelezhető (a tumor már áttörte a corticalist), ha ismert a primer tumor és a metastasis igazolására van szükség.
Technikai feltétel: citológiában és onkológiában jártas patológus.
- Percután hengerbiopsia, feltárásos sebészi biopsia: a fenti feltételek nem adottak, a diagnózis nem egyértelmű, a primer tumor ismeretlen.
Feltétel: patológus, immunhisztokémiai módszerek, onkológiai konzílium elérhetősége.
- Intraoperativ fagyasztásos metszet és szövettani vizsgálat: ha technikailag kivitelezhető (eltávolított anyag lágyrész), metastasisra van gyanú, de egyűlésben végzett műtétet választunk.
Feltétel: megfelelő szakmai jártassággal bíró patológus, fagyasztó microtom.
Szövettani feldolgozás:
- Hagyományos szövettani módszerek
- Immunhisztokémia és elektromikroszkópia, ha a fenti módszerekkel biztos diagnózis nem adható. III. Kezelés
4. Csontmetastasisok kezelési elvei
4.1. Beteg általános állapotának megítélése: Karnofsky-index alapján.
4.2. Fontosabb prognosztikai faktorok csontáttéteknél: (6D, 9A) Primer tumorra vonatkozók:
- Primer tumor szervi lokalizációja ismert, vagy ismeretlen.
- Primer tumor szöveti malignitási foka.
- Primer tumor szövettana.
- Primer tumor onkológiai értelemben kezelt, kontrollált.
- A primer tumor felismerése és a metastasis közötti idő.
Metastasisra vonatkozók:
- A metastasis soliter, vagy multiplex.
- Patológiás törés fennáll-e.
- Metastasis lokalizációja.
- Metastasis lokális kiterjedése.
- Metastasis növekedési üteme.
- A metastasis kemoterápia érzékenysége.
- A metastasis radioterápia érzékenysége.
- A metastasis hormonterápia érzékenysége (hormonreceptorok stb.).
A beteg általános állapotára vonatkozók:
- Általános belgyógyászati állapot (Karnofsky-index).
- Beteg életkora.
- Beteg pszichéje, kooperációs készsége, stb.
4.3. A sebészi kezelés lehetőségei
(1C, 2B, 3B, 4D, 5B, 7C, 8C, 10B, 11D, 12D, 14B)
4.3.1. Sebészi kezelés célja:
- Fájdalom csökkentése.
- Mozgás - terhelési képesség helyreállítása.
- Daganat radikális eltávolítása, bizonyos feltételek esetén.
- Önellátás biztosítása.
- Ápolhatóság biztosítása.
- Elfogadható életminőség.
4.3.2. Sebészi beavatkozás indikációi:
- Patológiás törés.
- Fenyegető törésveszély, ami megelőző stabilizációt igényel.
- Egyéb palliatív kezelésre nem reagáló kimutatott metastasis.
- Soliter metastasis, ha a kuratív metastasectomia indikációi fennállnak.
- Nagymérvű mozgásbeszűkülés, terhelési képtelenség.
- Aszociális állapotok, nagyfokú fájdalom.
4.3.3. Sebészi beavatkozás kontraindikációi:
- Várható élettartam kevesebb mint 1-3 hónap.
- Rossz általános állapot.
- Multiplex metastasisnál, ha patológiás törésveszély nem áll fenn és a daganat egyéb palliatív kezelésre reagál.
4.3.4. Sebészi kezelés típusai: 4.3.4.1. Palliatív beavatkozások:
- Gerincnél: Laminectomia,decompressio, mint minimál beavatkozás. Laminectomia, decompressio + stabilizáció, jobb prognosztikai feltételek esetén.
- Alsó végtag terhelő hosszú csöves csontjai:
- Ender szegezés: minimál beavatkozás rövid életkiáltásnál az ápolhatóság biztosítására.
Endoprotézis: combfej, combnyak lokalizációnál, célszerű cementes, revíziós, hosszúszárú protéziseket használni. Gamma szegezés: combnyak-intertrochantericus lokalizációnál.
Intramedullaris velőűrszegezés: diaphysealis lokalizációnál. Kombinálható segmentresectioval és intercalaris homograft alkalmazásával, vagy excochleatioval + csontcementtel.
Excochleatio + csontcement és/vagy lemezes rögzítés: diaphysealis lokalizáció, rövid életkilátásnál. Segmentresectio, pótlás homografttal, vagy tumor endoprotézissel: diaphysealis lokalizáció. Segmentresectio + arthrodesis (intramedullaris szegezés, tumor endoprotézis): femur distalis, tibia proximalis, meta-, epiphysis lokalizációnál.
- Felsővégtag nem terhelő csöves csontjainál:
Minimális beavatkozásként kötegszegezés Kirschner drótokkal vagy Ender szeg alkalmazása rövidebb életkilátások esetén. A fenti nagyobb stabilitást biztosító megoldások ritkábban kerülnek alkalmazásra. Medence: Egyszerű resectio: medencelapátra, os pubisra, ülőcsontra lokalizált metastasisnál.
Resectio + excochleatio és a medencegyűrű stabilizálása csontcementtel: acetabulumot elérő medencelapáti lokalizációnál.
Excochleatio, vápafenék kosár Steinmann szegekkel megerősítve, polyetilén vápa, fém szár: ízületbe törő, instabilitást okozó periacetabularis metastasisoknál.
Megjegyzés: A sebészi stratégiatervezésénél fontos figyelembevenni, hogy az alkalmazott módszer kitartson a beteg élete végéig.
4.3.4.2. Amputatio:
Metastasisok esetében ritkán végzünk
Indikációi: Csillapíthatatlan fájdalom.
Funkcióvesztett végtagrész.
Kiterjedt fekélyes lágyrészek, keringészavar.
Acrális lokalizáció.
Súlyos lokális postoperativinfectio.
4.3.4.3.Radikális metastasectomia kurativcéllal Indikáció: Primer tumor onkológiailag kontrollált.
Primer tumor és a metastasis jelentkezése között hosszabb időintervallum. Soliter metastasis.
Patológiás törés nem következett be. Extrasceletalisan egyéb szervben nincs metastasis. Adottak a sebészi radikális tumor eltávolítás lokális feltételei.
Műtéti lehetőségek:
Tumor endoprotézis.
Segmentresectio, pótlás homológ vagy autológ csontgrafttal, stabilizálás lemezzel, vagy intramedullaris szeggel. Homológ masszív osteochondralis graft beültetése. Autológ fibula transpositiója.
4.4. Radioterápia: Indikáció:
- Preoperatív, tumor volumenének csökkentése, fájdalomcsillapítás célzattal.
- Postoperatív: palliatív műtétek után, illetve marginalisan végzett kuratív célzatú műtétek után.
- Fájdalomcsillapító célzattal
4.5. Posztoperatív kemoterápia:
Indikált minden esetben, akár palliatív, akár radikális műtét történt, illetve ha műtétre egyéb okokból nem kerülhetett sor.
Kontraindikációk: 70 év fölötti életkor. Rossz általános belgyógyászati állapot. Ha a daganat kemoterápia resistens.
4.6. Radioizotópok:
Indikáció: Bizonyos pajzsmirigy-, prostata-, emlő rákok disseminalt csontmetastasisainál.
4.7. Hormonkezelés:
Indikáció: Prostata rákok disseminalt csontáttéteinél. Ösztrogén receptor pozitív emlőrákok csontáttétei.
4.8. Bisphosphonatok:
Indikáció: Lyticus, illetve kevert típusú csontmetastasisoknál. Lyticusnál i.v. bisphosphonat, majd localis ellátás (műtét vagy irradiáció), fenntartó bisphosphonat i.v. vagy p.o.
IV. Rehabilitáció
V. Gondozás
5. Csontmetastasisok kezelésének személyi, technikai feltételei
Elsődleges traumatológiai ellátás patológiás törés esetén történhet minden traumatológiai osztályon. A későbbi speciális kivizsgálást célszerű belosztályon, onkológiai osztályon végezni. Minden esetben javasolt multidiszciplináris konzílium onkológus, kemo- és radioterapeuta, patológus és onkológiában jártas sebész részvételével. (6D, 9A, 12D, 13D)
Speciális igényekés műtétek centrumokban tervezhetőek, ahol rendelkezésre áll: CT, MR, izotóp, ultrahang vizsgálati
lehetőség.
Csontbank.
Speciális tumor endoprotézis rendszer.
Megfelelő jártasságú ortopéd-traumatológus sebészi team.
Interdiszciplináris konzílium lehetősége (lásd fent).
6. Csontmetastasisos betegek utánkövetése
Három hónaponkénti kontroll minimum öt évig:
Fizikális vizsgálat.
Laborkontroll.
Kétirányú summatiós röntgen a műtét területéről.
Kétirányú mellkas felvétel, metastasisra gyanú esetén mellkas CT.
Radikális metastasectomia esetén a fenti vizsgálatokon kívül fájdalom jelentkezése esetén csontizotóp vizsgálat, hasi ultrahang is szükséges.
VI. Irodalomjegyzék
1. Bauze AJ, Clayer MT. Treatment of pathological fractures of the humerus with a locked intramedullary nail. J.Orthop Surg.(Hong.Kong.) 2003;11:34-7. (Evidenciaszint: C )
2. Bohm P, Huber J. The surgical treatment of bony metastases of the spine and limbs. J.Bone Joint Surg.Br. 2002;84:521-9. (Evidenciaszint: B )
3. Cheville JC, Tindall D, Boelter C, Jenkins R, Lohse CM, Pankratz VS et al. Metastatic prostate carcinoma to bone: clinical and pathologic features associated with cancer-specific survival. Cancer 2002;95:1028-36. (Evidenciaszint: B )
4. De Geeter K, Reynders P, Samson I, Broos PL. Metastatic fractures of the tibia. Acta Orthop Belg. 2001;67:54-9. (Evidenciaszint: D )
5. Durr HR, Muller PE, LenzT, Baur A, Jansson V, Refior HJ. Surgical treatment of bone metastases in patients with breast cancer. Clin.Orthop Relat Res. 2002;191-6. (Evidenciaszint: B )
6. Esther RJ, Bos GD. Management of metastatic disease of other bones. Orthop Clin.North Am. 2000;31:647-59, ix. (Evidenciaszint: D )
7. Fuchs B, Trousdale RT, Rock MG. Solitary bony metastasis from renal cell carcinoma: significance of surgical treatment. Clin.Orthop Relat Res. 2005;187-92. (Evidenciaszint: C )
8. Ghert MA, Harrelson JM, Scully SP. Solitary renal cell carcinoma metastasis to the hand: the need for wide excision or amputation. J.Hand Surg.[Am.] 2001;26:156-60. (Evidenciaszint: C )
9. Hansen BH, Keller J, Laitinen M, Berg P, Skjeldal S, TrovikCet al. The Scandinavian Sarcoma Group Skeletal Metastasis Register. Survival after surgery for bone metastases in the pelvis and extremities. Acta Orthop Scand.Suppl 2004;75:11-5. (Evidenciaszint: A )
10. Jung ST, Ghert MA, Harrelson JM, Scully SP. Treatment of osseous metastases in patients with renal cell carcinoma. Clin.Orthop Relat Res. 2003;223-31. (Evidenciaszint: B )
11. Liu JK, Apfelbaum RI, Schmidt MH. Surgical management of cervical spinal metastasis: anterior reconstruction and stabilization techniques. Neurosurg.Clin.N.Am. 2004;15:413-24. (Evidenciaszint: D )
12. Manabe J, Kawaguchi N, Matsumoto S,TanizawaT. Surgical treatment of bone metastasis: indications and outcomes. Int.J.Clin.Oncol. 2005;10:103-11. (Evidenciaszint: D )
13. Radford M, Gibbons CL. Management of skeletal metastases. Hosp.Med. 2002;63:722-5. (Evidenciaszint: D )
14. Wedin R. Surgical treatment for pathologic fracture. Acta Orthop Scand.Suppl 2001;72:2p-9. (Evidenciaszint: B )
15. Wenger M. Vertebroplasty for metastasis. Med.Oncol. 2003;20:203-9. (Evidenciaszint: D )
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Dokumentáció, bizonylat
- Járóbeteg szakellátásban: ambuláns lap, kezelő lap.
- Képalkotó vizsgálatok képi és szöveges leletei
- Fekvőbeteg szakellátásban: kórlap, műtéti beleegyezés, műtéti leírás, decursus, zárójelentés.
- Felhasználásra került implantátumok bizonylatai
2. Érintett társszakmákkal való konszenzus Onkológia és onkoterápia, Pathológia, Radiológia.
3. Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Dupuytren contractura ellátásáról
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
I. Alapvető megfontolások
1. A protokoll alkalmazási, érvényességi területe Ortopédia és kézsebészet
2. A protokoll bevezetésének alapfeltételei Ortopéd Szakmai Kollégiumi legitimációja.
Szakmai minimum feltételeknek megfelelő Ortopédiai Osztály.
2. Definició
A Dupuytren korrtractura a tenyéri, ritkábban a talpi aponeurosis hypertrphiaja és heges zsugorodása, melyhez az ujjízületek különböző fokú kontraktúrája társulhat. A folyamat lényege: fibroblaszt proliferáció és kollagén produkció. Az aponeurosis palmaris hosszanti rostkötegei, illetve a bőrhöz vertikálisan húzódó rostok betegszenek meg. (B típusú evidencia-1,9)
2.1. Kiváltó tényezők
oka ismeretlen, de az ismétlődő traumákszerepe nem zárható ki (erős markoló munkát végző embereknél gyakrabban alakul ki). Cukorbetegeknél is gyakoribb az előfordulás. (B típusú evidencia - 4)
1.2. Kockázati tényezők
1.3. 2.1. pontban leírtak.
3. Panaszok
a kéz használhatóságának többnyire lassú, évek alatt kialakuló fukcionális és esztétikai romlása.
4. A betegség leírása
4.1. Érintett szervrendszer
tenyéri bőnye (ritkán a talpi bőnye). Gyakran mindkét kezet szimmetrikusan érinti.
4.2. Genetikai háttér: nem ismert, bár családi halmozódás előfordul.
4.3 Jellemző életkor: elsősorban 30-40 éves kór körül jelentkezik.
4.4 Jellemző nem: férfiaknál gyakoribb, mint nőknél.
II. Diagnózis
1. Anamnézis: a kéz használhatóságának romlása, korlátozódása.
2. Fizikális vizsgálatok: fizikális vizsgálattal a kórkép egyszerűen felismerhető. A tenyér és talp bőrében először heges csomók és azokban behúzódások láthatók, illetve tapinthatók. A betegség előrehaladtával a csomók húrrá állnak össze, az ujakba is belesugároznak, ezzel az MP-és a PIP ízületekben flexíos contracturát okozva. A contrakturák elsősorban MP, kevésbé a PIP és ritkán a DIP ízületekeig is kiterjednek. Az elváltozás leggyakrabban a IV. és az V. ujjsugárban alakul ki, de a többiben is megtalálható.
Osztályozása: Iselin négy fokozatú beosztása szerint történik, melynek alapja és fokmérője az ujjak kisízületeiben kialakult contractura lokalizációja.
3. Kötelező, kiegészítő diagnosztikai vizsgálatok Ilyen vizsgálatokat nem igényel.
4. Képalkotó vizsgálatok
Ilyen vizsgálatokat nem igényel.
5. Diferencial diagnosztika Csomók esetén: -epithel cysta -neurofibroma Contractura esetén: -kamptodactylia
-tiszta tendogen contractura -tiszta arthrogen contractura -bőrheg okozta contractura
6. Diagnosztikai algoritmus
Fizikális vizsgálattal a kórkép egyszerűen felismerhető, egyéb diagnosztikus eljárást nem igényel.
III. Terápia
III/1-2. Konzervatív
1. Gyógyszeres kelezés: nincs
2. Kiegészítő / Alternatív kezelések: az UH kezelés az egyedüli, amely talán a progressziót lassítja.
3. Konzervatív terápiás algoritmus: nincs.
III/3. Műtét
1. Műtéti indikáció: a betegség operatíve kezelendő.
2. Műtéti kontraindikáció
A kéz területére lokalizálódó gyulladásos megbetegedés. Aktív gyulladásos bőrfolyamat A beteg rossz általános állapota, kooperáció hiánya. Ha a műtétet a beteg felvilágosítás ellenére sem akarja.
3. Műtéti előkészítés
A kézsebészeti műtéti előkészítés általános szabályainak betartása mellett speciális előkészítést nem igényel.
4. Műtéti érzéstelenítés Általános, vagy axilláris anesztézia.
5. Műtét (B típusú evidencia - 3,5,6,7,8,9,10.)
A műtéti megoldás lényege a heges aponeurosis eltávolítása. A műtét nyílt feltárásból, kipólyázásos vértelenségben végezhető. Iselin III-IV stádiumú Dupuytren kontraktúráknál kézsebészeti jártassággal rendelkező ortopéd sebész ill. kézsebész asszisztálásával javasolt a műtét elvégzése, hogy lehetőség legyen az esetlegesen felmerülő szövődmény pl.idegsérülés mikrosebészeti ellátására.
A műtét menete
Iselin I-II stádiumban bármilyen kézsebészetben megengedett metszés választható. Az ennél súlyosabb esetekben Millesi szerinti feltárás és/vagy Z plasztika a követendő technika, hogy a műtét végén a bőr lehetőség szerint teljes egészében zárható legyen.
A bőrmetszés után a hegesedett aponeurosist teljes egészében eltávolitjuk, figyelni kell a metacarpusokhoz menő aponeurosís septumok kiírtására is, mert ha azt nem távolítjuk el, az elváltozás recidiválni fog. A hegesedett aponeurosis sok esetben közrefogja az ér-, idegképleteket, így műtét közben nagy az ér, idegsérülés veszélye. Az aponeurosis eltávolítása után a vértelenség felengedése, gondos vérzéscsillapítás szükséges. A bőrzárás javasolt 4/0 atraumás fonallal végezni. Draint a nagyobb beavatkozások esetén célszerű behelyezni. Azokban az esetekben ahol Iselin II. vagy súlyosabb stádium volt, műtét után gipszsínt célszerű felhelyezni az ujjak nyújtott helyzete mellett 7-10 napra. Thrombosis profilaxis nem szükséges.
A műtéti megoldás formái (WHO: 58301, 58230, 58231,58242" 58361, 58400,)
| Subcutan aponeurotomia: | lényege a kiemelkedő feszes köteg átmetszése |
| Végezhető: | súlyos fokú elváltozásnál a végleges műtét előkészítéseként rossz általános állapotú betegnél végleges megoldásként |
| Parciális aponeurectomia: | nagy a recidiva veszélye, nem ajánlott eljárás |
| Komplett aponeurectomia: | ez a választandó megoldás a legtöbb esetben, jó eredményt ad. |
| Aponeurectomia bőrpótlással: | nagy flexios contractura esetén alkalmazható eljárás. |
| Amputáció: | nagyon ritkán jön szóba, csak az V. ujjon végezhető Iselin 4.fokozat esetén. |
6. Posztoperatív teendők
- 2. posztoperatív napig az alkar felpolcolása, a drain(ok) eltávolítása, többi ízület mozgatása a feladat
- 3. naptól 10-12. napig a nem érintett ízületek tornája szükséges.
- varratszedés a 10-12. napon történik
- vezetett gyakorlatok végzése a harmadik hétig
- 3. héttől aktív torna
IV.-V. Rehabilitáció, Gondozás
1. Rehabilitáció és rendszeres ellenőrzés
Gondozás, rehabilitációs kezelés általában nem szükséges.
Szövődménymentes esetekben kontroll vizsgálat 1-2 alkalommal szükséges. (B típusú evidencia - 3, 11)
2. Megelőzés
Cukorbetegeknél, illetve olyan foglakozásuaknál, akiknél a kezet mikrotraumát sorozata éri a korai tünetek keresése, felismerése. Az alkohol és a dohányzás, főleg együttesen a kockázatot növeli. (B típusú evidencia - 2,4)
3. Lehetséges szövődmények Infekció, sebgyógyulási zavar Ideg-, érsérülés
4. Szövődmények kezelése
Fenti szövődmények korai felismerése, azok műtéti korrekciója (idegvarrat), illetve sebgyógyulási zavarnál vagy konzervatív kezelés, vagy/és adott esetben műtéti feltárás.
5. Kezelés várható időtartama/Prognózis Végleges állapot 8-12. hétre alakul ki.
6. Az ellátás megfelelő indikátora
A műtét előtti és utáni mozgásszervi státusz rögzítése biztosítja az állapotváltozás prospektív nyomonkövetését. (mozgástartomány, kézfunkció változása).(B típusú evidencia - 11)
VI. Irodalomjegyzék
1. Udvarhelyi Iván (Szerk.): Fejezetek a felnőttkori ortopédia gyakorlatából. Medicina Könyvkiadó Rt. 1998. 2.Vízkeleti Tibor (szerk.): Az Ortopédia tankönyve. Semmelweis Kiadó. Budapest, 1999. 3. Szendrői Miklós (szerk.): Ortopédia. Semmelweis Kiadó 2006.
Kapcsolódó internetes oldal www.ortopedtarsasag.hu
Evidencia meghatározásnál felhasznált irodalom
1. Augoff K, KulaJ,GoskJ, Rutowski R.: Epidermal growth factor in Dupuytren's disease. Plast ReconstrSurg. 2005 Jan, 115 (1): 128-33.
2. Godtfredsen NS, Lucht H, Prescott E, SorensenTI,GronbaekM.: A prospective study linked both alcohol and tobacco to Dupuytren's disease. J Clin Epidemiol. 2004 Aug, 57 (8):858-63.
3. DraviarajKP,Chakrabarti I.: Functional outcome after surgery for Dupuytren's contracture: a prospektive study. J Hand Surg (Am), 2004 sep, 29 (5):804-8.
4. Geoghegan JM, Forbes J, Clark DI, Smith c, Hubbard R.:Dupuytren's disease risk factors. J Hand Sugg (Br), 2004 Oct, 29(5):423-6.
5. Beyermann K, Prommersberger KJ, Jacobs C, Lanz UB.: Severe contracture of the proximal interphalangeál joint in Dupuytren's diseases: does capsuloligamentous release improve outcome? J. Hand Surg (Br). 2004 Jun, 29 (3):240-3.
6. Meathrel KE, Thoma A.: Abductor digiti minimi involvement in Dupuytren's contracture of the small finger. J. Hand Surg (Am),2004 May, 29 (3):510-3.
7. Skoff HD.: The surgical treatment of Dupuytren's contacture: a synthesis of techniques. Plast Reconstr Surg. 2004 feb, 113 (2):540-4.
8. Ritchie JF,Venu KM, Pillai K,Yanni DH.: Proximal interphalangeal joint release in Dupuytren's disease ot the little finger. J Hand Surg (Br). 2004 Feb, 29 (1):15-7.
9. Pagnotta A, Specchia N, Soccetti A, Manzotti S, Greco F.: Responsiveness of Dupuytren's disease fibroblasts to 5 alpha-dihydrotestosterone. J Hand Surg (Am). 2003 Nov, 28(6):1029-34.
10. FoucherG, Medina J, Navarro R.: Percutaneus needle aponeurotomy: complication and results. J Hand Surg (Br). 2003 Oct, 28 (5):427-31.
11. Sinha R, Cresswell TR, Mason R, Chakrabarti Í.: Functional benefit of Dupuytren's surgery. J. Hand Surg (Br). 2002 Aug, 27(4):378-81.
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Érintett társszakmák
Kézsebészet, Fizioterápia, Gyógytorna.
2. Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Felnőttkori aszeptikus combfej nekrózisról
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
I. Alapvető megfontolások
Szinonímák: Avaszkuláris femurfejnekrózis, Necrosis capitis femoris, Idiopathiás asepticus combfej elhalás, Femurfej necrosis, AVFN.
1. A protokoll alkalmazási, érvényességi területe
- ortopédia, rheumatológia, traumatológia (mozgásszervi betegségekkel foglalkozók)
- radiológia
2. A protokoll bevezetésének alapfeltétele
- A betegség diagnosztikájának és terápiájának egységes szemlélete a mozgásszervi betegségekkel foglalkozó szakmákban.
- A combfejnekrózisos betegek szakmai kompetenciák értelmében végzett gyógyító-megelőző ellátása.
3. Definíció
- A combfej egészének vagy egy részének elhalása vérkeringési zavar, érelzáródás miatt (A szintű evidencia - 29). Ez általában a combfej elülső, felső és oldalsó részét érinti, amely súlyos arthrosishoz vezethet.
- Ettől az entitástól elkülönítendő a mediális combnyaktörést követő combfejelhalás, az ún. poszttraumás fejnekrózis, melyet a "Combnyaktörés kezelésének szakmai protokollja" tárgyal és egy másik beteg populációt érint (idős, osteoporosisos nőbetegek).
3.1. Kiváltó tényezők
Előfordulási gyakorisága: (B szintű evidencia - 1,4,8,10,22,24)
- csípőízületet érintő trauma esetén 11-45% (kivéve mediális combnyaktörést követő fejelhalás)
- alkoholizmus esetén 40%-ban fordul elő, ebből 73%-ban kétoldali
- kortikoszteroid kezelés esetén 5-25%
- vese transzplantáció esetén az első évben 40%, a második évben 85%, 54-80%-ban kétoldali megjelenéssel
- SLE esetén 5-40%
- rheumatoid arthritis esetén 12%
- haemophilia esetén 3%
- További okok: caisson betegség, pankreatitis, koagulopathiák, dialysis, irradiáció, Gaucher-kór, sarlósejtes aneamia, Cushing-kór, óriás sejtes arthritis, hyperurikémia (köszvény), hypercholesterinaemia és lipidaemia, dohányzás, terhesség III. trimesztere
- Létezik továbbá az ún. idiopathiás forma, amikor a fenti okok egyike sem mutatható ki anamnesztikusan
3.2. Kockázati tényezők Lásd előző (3.1.) pont.
4. Panaszok, tünetek, általános jellemzők
- Általában hirtelen kezdődő csípőfájdalom, amelyet néha térdpanaszok előznek meg. A fájdalmas időszakokban sántítás jelentkezik (érintett oldal kímélő jellegű sántítása)
- Az esetek egy részben kétoldali panaszok jelentkeznek változó intenzitással.
- Korai esetben a röntgen felvétel negatív.
- A betegek többsége fiatal vagy középkorú (35-50 év) férfi.
- Az anamnézisben gyakran szerepel túlzott alkoholfogyasztás. (részletesen lásd 3.1. pontban.)
5. A betegség leírása
5.1. Érintett szervrendszer Csípőízület.
5.2. Genetikai háttér Nem ismert.
5.3. Incidencia - prevalencia
- Évente Magyarországon 500-650 újeset, ami növekedni fog a traumák, kortikoszteroid kezelések, transzplantációk esetszámának növekedése és az alkohol fogyasztás növekedése miatt.
- Az esetek 30-70%-a kétoldali.
5.4. Morbiditás, mortalitás: (C szintű evidencia - 10,16)
A csípőízületi protézis beültetés 5%-a fejnekrózis miatt történik. 3 éven belül a diagnózist követően a betegek 50%-a nagy műtéti beavatkozásra szorul. A fermur-fej beroppanása általában 2 évvel a panaszok megjelenése után bekövetkezik.
5.5. Jellemző életkor 30-60 év
5.6. Jellemző nem Férfi:Nő arány 4:1 -5:1
II. Diagnózis
1. Diagnosztikai algoritmusok
- A beteg panaszai és az anamnézis alapján felmerülhet a betegség gyanúja.
- A társ- illetve alapbetegségeket kikérdezéssel, korábbi zárójelentésekkel vagy laboratóriumi vizsgálatokkal lehet bizonyítani.
- Képalkotó vizsgálattal kell bizonyítani a pathoanatómiai eltérést a combfejben. A diagnózis szükséges és elégséges feltétele a combfejben látható elhalt terület (általában háromszög alakú areál).
- A betegség stádiumait a Ficat-féle besorolás tartalmazza (Ficat 0-4 stádium) (B szintű evidencia - 6,7,9)
2. Anamnézis
- A betegekegy részénél a fájdalom hirtelen jelentkezik. A beteg pontosan emlékszik az időpontra. Ez az érelzáródás (infarktus) időpontja.
- A betegek másik részénél a kezdet tünetmentes, a panaszok később a mechanikai eltérés, a fejberoppanása után kezdődnek.
- A fájdalom állásra, járásra, mozgatásra valamilyen mechanikai igénybevételre jelentkezik illetve erősödik. Nyugalomban csökken, megszűnik.
-Amennyiben a fájdalom éjszaka is fennáll synovitis is kíséri a folyamatot. A fájdalom gyakran a farpofa és a térd belső oldalának irányába sugárzik.
3. Fizikális vizsgálat
- A csípők összehasonlító vizsgálata során észlelhető mozgásbeszűkülés, kontraktúra, fájdalom (ami főleg berotációban provokálható), adott esetben végtagrövidülés.
- Az ágyéki gerincet és a térdeket is meg kell vizsgálni (differenciál diagnózis).
4. Kötelező diagnosztikai vizsgálatok 4.1. Laboratóriumi vizsgálatok
- Nincs specifikus laborvizsgálat a combfejnekrózis kimutatásához.
- A 3.1. pontban részletezett alap- illetve kísérő betegségek laboratóriumi eltérései segíthetnek a diagnózis pontosításában és az etiológia tisztázásában (pl. alkoholista beteg májenzim eltérései, hyperlipidaemiás beteg vérzsír eltérései, sarlósejtes anaemiás beteg vérkép eltérései stb.)
4.2. Képalkotó vizsgálatok: (A szintű evidencia - 3,6,10,13.15,23, 26)
- A-P összehasonlító csípő rtg felvétel (obligát) és oldalirányú vagy Lauenstein-felvétel (fakultatív)
- Izotóp vizsgálat (fakultatív)
- MR (obligát-amennyiben a 3.1-ben leírt anamnesztikus adatok és a panaszokegybevágnak, illetve az rtg negatív) (A szintű evidencia - 26)
- UH (fakultatív) -CT, 3D CT (fakultatív)
Amennyiben a hagyományos rtg és az izotóp vizsgálat eredménye negatív, MR elvégzése szükséges a korai diagnózishoz. Az izotóp vizsgálat esetén az elhalás okozta kiesést gyakran elfedi a következményes synovitis okozta dúsulás. UH akkor lehet indokolt, ha kíváncsiak vagyunk, hogy van-e folyadék az ízületben. A folyadék MR-en is jól látható. CT-re illetve 3D CT-re inkább a műtétek tervezésekor lehet szükség a combfej beroppanásának pontos megítélésére. Ilyen esetben végezhetjük az ún. Schneider-felvételeket is, amelyek segítenek a combfej állapotának felmérésében.
4.3. Egyéb: Egyéb vizsgálat általában nem szükséges
5. Kiegészítő diagnosztikai vizsgálatok Általában nem szükséges.
6. Differenciál diagnosztika (A szintű evidencia - 27)
- Amennyiben az elvégzett vizsgálatok nem igazoljákacombfejnekrózist, ki kell zárni első sorban az ágyéki gerincre és a kismedencére lokalizálódó illetve a rheumatológia körébe tartozó sokízületi érintettséget is okozó gyulladásos betegségeket.
- Ezen kívül a csípőízület algodystrophiáját, a csonttumorok közül a chondroblastomát, osteblastomát, osteoclastomát, valamint csontmetasztázisokat, és a bakteriális osteomyelitist.
III. Kezelés
Nem gyógyszeres kezelés
1. A megfelelő egészségügyi ellátás szintje Ortopédiai, traumatológiai és rheumatológiai szakrendelő.
2. Általános intézkedések: nem szükséges
3. Speciális ápolási teendők: nem szükséges
4. Fizikai aktivitás
Érintett végtag tehermentesítése (könyökmankóval), úszás, kerékpározás, gyógytorna a csípőízület vérkeringésének fokozása érdekében.
5. Diéta
Alkoholfogyasztás, dohányzás leállítása, egészséges táplálkozás.
6. Betegoktatás
Felhívni a kockázati tényezőkre a figyelmet. Progresszió esetén műtéti beavatkozástól remélhető állapotjavulás.
III/2. Gyógyszeres kezelés (A szintű evidencia - 25)
1. A megfelelő egészségügyi ellátás szintje Ortopédiai, traumatológiai és rheumatológiai szakrendelő.
2. Speciális ápolási teendők
- Amennyiben a beteg kezelése fekvőbeteg ellátó helyen történik, szokásos kórházi ápolást igényel.
- A csípőízület tehermentesítése miatt szükséges lehet speciális ápolás.
3. Ajánlott gyógyszeres kezelés: (B szintű evidencia - 5,12)
Nem-szteroid gyulladás gátlók (NSAID) - pl. diclofenac, harántcsíkolt izomrelaxánsok- pl. tolperison, keringésjavító szerek - pl. pentoxyfillin, vitaminok
3.1. Kontraindikációk: gyógyszer- vagy hatóanyag túlérzékenység, NSAID nem adható peptikus ulcus, aktív gasztrointesztinális vérzés esetén, myasthenia gravisban nem adható izomrelaxáns
3.2. Lehetséges jelentős interakciók: lítium, digoxin, glükokortikoidok, nifluminsav (Donalgin) együtt szedése a fenti gyógyszerekkel interakciót okozhatnak
4. Kiegészítő/alternatív gyógyszeres kezelés Gyógytorna, fizikoterápiás eljárások.
5. Terápiás algoritmus
Amennyiben a konzervatív módszerek nem segítenek a betegség stádiumától függően többféle műtéti beavatkozás ajánlható.
III/3. Műtét
1. A megfelelő egészségügyi ellátás szintje
Ortopéd sebészeti osztály, traumatológiai osztály, mozgásszervi centrum.
2. Általános intézkedések
- Szokásos műtét előtti kivizsgálás lehetőség szerint ambuláns módon, a választott műtéti időpont előtti hetekben.
- Aneszteziológiai ambulancián a beteg előzetesen jelenjen meg (esetleg bizonyos gyógyszerek szedését fel kell függeszteni).
3. Speciális ápolási teendők
Az egyébként szokásos műtétek utáni ápolásra, ellátásra van szükség műtéti típustól függően (ld. 4.4. pont).
4. Sebészi kezelés HBCs besorolás:
- 08 3750 Csípő, femurműtétek
- 08 4111 Csontbetegségek, arthropathiák
-08 489Z Vázizomrendszeri betegségek (kivéve: osteomyelitis, szeptikus ízületi gyulladások, kötőszöveti betegségek) súlyos társult betegséggel
Műtéti indikáció
- Ficat 1. stádiumban femurfejfelfúrás (core decompression) végezhető [beavatkozás kódja: OENO 57804] (C szintű evidencia - 2, 3, 5, 7, 11, 12, 16, 19, 20, 21) - a szakirodalom ellentmondásos eredményeket közöl e kezelés eredményességéről, a hazai gyakorlatban az utóbbi években nem túl gyakran végzett beavatkozás
- Ficat 2. stádiumban vérellátását megtartott csontlebeny beültetés végezhető [beavatkozás kódja: OENO 5893E] (A szintű evidencia -28, C szintű evidencia -31) -a szakirodalom nem foglal állást egyértelműen e kezelés hatásosságáról, a hazai gyakorlatban az utóbbi években igen ritkán végzett beavatkozás
- Ficat 2-3. stádiumban, ha az elhalás mértéke nem haladja meg az 50%-ot (AP és Lauenstein-felvételen a nekrotikus terület szögösszege nem nagyobb 200 foknál illetve a Schneider 1-es felvételen a femurfej ép) flexiós oszteotómia végezhető [beavatkozás kódja: OENO 57815] (C szintű evidencia - 7,14,16,18,21,30) - a hazai gyakorlatban az utóbbi években már nem végzett beavatkozás
- Ennél nagyobb károsodás esetén és Ficat 4. stádiumban csípőízületi arthroplasztika elvégzése javasolt [beavatkozás kódja: OENO 58150 vagy 58151] (A szintű evidencia - 7, 21, 28) - a hazai gyakorlatban az utóbbi években leggyakrabban végzett beavatkozás
Műtéti előkészítés
- Az ortopédiai műtéknél szokásos előkészítés (lemosás, izolálás, stb.) szükséges.
- Femurfej felfúrás esetén extenziós asztal, flexiós oszteotómiánál oldalfekvés, valamint rtg képerősítő használata szükséges.
- Thrombosis profilaxis megkezdése LMWH készítménnyel a műtét előtti esten minden esetben szükséges (ld. "A thromboemboliák megelőzése és kezelése" c. EüMin Irányelv ajánlásait)
- A beteg felvilágosítása, írásos beleegyezés beszerzése a betegtől.
Műtéti érzéstelenítés
- Általában a műtétek gerinc közeli (spinalis) érzéstelenítésben történnek.
- Ha ez nem lehetséges, narkózisban végezhetők a műtétek.
Műtét
4.4.1. A femurfejfelfúrás lépései
- A beteg asztalra fektetése háton fekvésben.
- A műtéti terület szőrtelenítése és antiszeptikus lemosása
- Izolálás (textil v. egyszer használatos izoláció, incíziós fólia)
- Bőrmetszés a nagytompor alatt a műtéttechnikai eljárásokat ismertető tankönyvek szerint.
- Célzó drótok alkalmazása, rtg kontroll alkalmazása mellett.
- A combnyak és a combfejnekrotikus területeinek megfúrása rtg kontroll alkalmazása mellett.
- A szokásostól eltérő történések, intraoperatív szövődmények ellátása.
- Szívó drain behelyezése, rögzítése.
- Réteges sebzárás.
- A seb környékének lemosása, fertőtlenítése.
- A seb steril fedése, nyomókötés felhelyezése.
- A beteg levétele a műtőasztalról, és kellő óvatossággal ágyba fektetése.
- A műtét után a műtét menetének részletes leírása, csatolása a kórlaphoz.
- Kontroll rtg felvétel készítésre a műtőasztalon, de lehetőleg a műtét napján.
4.4.2. Az ér- izomlebenyes csontbeültetés lépései
- A beteg asztalra történő fektetése háton fekvésben.
- A műtéti terület szőrtelenítése és antiszeptikus lemosása.
- Izolálás (textil v. egyszer használatos izoláció, incíziós fólia).
- Bőrmetszés a nagytompor felett, anterolateralis vagy direkt lateralis feltárás a műtéttechnikai eljárásokat ismertető tankönyvek szerint.
- A csípőízület tokjának megnyitása.
- A combnyakon ablak készítése, nekrotikus terület kikaparása kürett kanállal vagy más alkalmas eszközzel.
- A m.gluteus medius elülső részének leválasztása a csontos tapadással együtt és annak behelyezése az elkészített üregbe. A tokot nem zárjuk.
- A szokásostól eltérő történések, intraoperatív szövődmények ellátása, vérzéscsillapítás, öblítés.
- Szívó drain behelyezése, rögzítése.
- Réteges sebzárás.
- A seb környékének lemosása, fertőtlenítése.
- A seb steril fedése, nyomókötés felhelyezése.
- A beteg levétele a műtőasztalról, és kellő óvatossággal ágyba fektetése.
- A műtét után a műtét menetének részletes leírása, csatolása a kórlaphoz.
- Kontroll rtg felvétel készítésre a műtőasztalon, de lehetőleg a műtét napján.
4.4.3. A flexiós intertrochantericus oszteotómia lépései
- A beteg asztalra történő fektetése oldalfekvésben, stabilan rögzítve.
- A műtéti terület szőrtelenítése és antiszeptikus lemosása
- Izolálás (textil v. egyszer használatos izoláció, incíziós fólia)
- Bőrmetszés és a femur proximális harmadának feltárása a műtéttechnikai eljárásokat ismertető tankönyvek szerint.
- Elővéső behelyezése, szükség szerint célzó drótok alkalmazása, rtg kontroll alkalmazása mellett.
- Alapjával ventral felé néző csonték (20-30 fok) eltávolítása az intertrochantericus területen.
- Elővéső eltávolítása.
- Szögletlemez behelyezése, kompressziós eszköz felhelyezése, kompresszió létrehozása. Csavarok behelyezése rtg kontroll alkalmazása mellett.
- A szokásostól eltérő történések, intraoperatív szövődmények ellátása, vérzéscsillapítás, öblítés.
- Szívó drain behelyezése, rögzítése.
- Réteges sebzárás.
- A seb környékének lemosása, fertőtlenítése.
- A seb steril fedése, nyomókötés felhelyezése.
- A beteg levétele a műtőasztalról, és kellő óvatossággal ágyba fektetése.
- A műtét után a műtét menetének részletes leírása, csatolása a kórlaphoz.
- Kontroll rtg felvétel készítésre a műtőasztalon, de lehetőleg a műtét napján.
4.4.4. Csípőízületi arthroplasztika lépései
- A beteg asztalra történő fektetése háton fekvésben.
- A műtéti terület szőrtelenítése és antiszeptikus lemosása.
- Izolálás (textil v. egyszer használatos izoláció, incíziós fólia).
- Bőrmetszés a nagytompor felett, anterolateralis, posterolateralis, direkt lateralis vagy ún. minimál invazív feltárás a műtéttechnikai eljárásokat ismertető tankönyvek szerint.
- A csípőízület tokjának megnyitása, a nekrotikus combfejreszekciója oszcillációs fűrésszel.
-A medence csontban vápamarás, majd protézis vápa beültetés cementes (idősebb beteg, rossz csontminőség) vagy cement nélküli (fiatalabb beteg, jó csontminőség) technikával.
- A combcsontban a velőűr felreszelése után protézis szár rögzítése cementes vagy cement nélküli technikával. Combfejnecrosisban az ún. felszínpótló csípőprotézisek (surface arthroplasty) alkalmazása nem javasolt.
- Megfelelő nyakhosszúságú protézis fejjel repozíció, mozgásterjedelem, luxációs tendencia vizsgálata.
- A szokásostól eltérő történések, intraoperatív szövődmények ellátása, vérzéscsillapítás, öblítés.
- Szívó drain behelyezése, rögzítése.
- Réteges sebzárás.
- A seb környékének lemosása, fertőtlenítése.
- A seb steril fedése, nyomókötés felhelyezése.
- A beteg levétele a műtőasztalról, és kellő óvatossággal ágyba fektetése.
- A műtét után a műtét menetének részletes leírása, csatolása a kórlaphoz.
- Kontroll rtg felvétel készítésre a műtőasztalon, de lehetőleg a műtét napján. Posztoperatív teendők
- Az ortopédiai műtétek utáni szokásos teendőkre van szükség: posztoperatív megfigyelés, fájdalom csillapítás, folyadék- és elektrolit pótlás, stb.
-Thrombosis profilaxis LMWH készítménnyel a posztoperatív 35-42. napig a MAITTés a MHT ajánlásai alapján (ld. "A thromboemboliák megelőzése és kezelése" c. EüMin Irányelv ajánlásait)
- Perioperatív szakban antibiotikus profilaxis (ált. 1. generációs cephalosporin [pl. cefazolin] készítménnyel iv. 24 órás adagolás 3-4 részre osztva) (lásd. "A műtéti sebfertőzések megelőzése" c. EüMin Irányelv ajánlásait)
5. Fizikai aktivitás
- Műtétek utáni 2. nap torna és mobilizálás megkezdése.
- Általában 9-14 nappal a műtétek után a betegek hazaengedhetők. (Ettől eltérően a hazaengedés korábban ill. később is megtörténhet, az adott helyi eljárásrendnek megfelelően.) Otthon a megtanult torna rendszeres végzése, operált végtag részleges tehermentesítése javasolt 6 hétig (segédeszköz használat).
6. Diéta
- Különleges diétára nincs szükség, de alkoholfogyasztás és dohányzás kerülendő.
7. Betegoktatás
-A beteget megfelelő életmódbeli tanácsokkal kellellátni. A korai posztoperatív szakban a műtét sikerét veszélyeztető élethelyzetek kerülendők.
IV. Rehabilitáció
- Általában az otthoni rehabilitáció elegendő. Gyógytornász igénybe vétele otthoni ápolás keretében javasolt.
- 6-8 hét után, ha az operált ízület funkciója nem megfelelő, kórházi utókezelés szóba kerülhet, ahol a gyógytorna, fizikoterápia, víz alatti torna, szobakerékpár alkalmazható.
- Új és nehezített gyakorlatok csak fokozatosan vezethetők be.
V. Gondozás
1. Rendszeres ellenőrzés: (A szintű evidencia - 21)
- Műtétek után 6 héttel az első, ezt követően 3 hónap múlva a második és további 6 hó múlva a harmadik kontroll javasolt járóbeteg szakrendelésen. Utána 1-2 évente egy alkalommal kontroll vizsgálat javasolt.
- Oszteotómia esetén 1-2 évvel a műtét után a fémeltávolítás szóba kerül.
- Csípő endoprotézis esetén évente rtg kontroll szükséges a protézis aszeptikus lazulásának észlelése céljából.
2. Megelőzés
- Alkoholfogyasztás csökkentése, szteroid szedés esetén a dózis lehető legalacsonyabban tartása.
3. Lehetséges szövődmények
- Súlyos társult betegség (szövődmény) ritkán alakul ki.
-A legyakoribb a thromboemboliás és a szeptikus szövődmény. Ezekelkerülésére thrombosis és antibiotikus profilaxis alkalmazandó.
- Oszteotómia esetén álízület, lemeztörés, kilazulás miatt reoperációra lehet szükség.
- Arthroplasztika esetén a protézis aszeptikus lazulása miatt revíziós műtétre lehet szükség.
4. Kezelés várható időtartama/prognózis
- Korai felismerés esetén, ha sikerül a fejdeformálódását megakadályozni, a prognózis jó.
- Késői felismerés esetén a konzervatív kezelés eredményessége 10% körüli. Általában 3 éven belül valószínűleg műtétre kerülhet sor. Elsősorban az arthroplasztika eredményei jók hosszú távon, ezért a leggyakrabban ezt végezzük.
Az ellátás megfelelőségének indikátorai (szakmai munka eredményességének mutatói)
- Műtéti szövődmények kialakulása (oszteotómia esetén álízület képződés, csípő protézis beültetés esetén specifikus szövődmények)
- Combfejberoppanásának késleltetése core decompression esetén (MR kontroll)
- Ellenoldali csípőízület érintettségének időben történő észlelése
- Betegállományban töltött napok, betegségi nyugdíjazás, mint a gyógyeredmény minőségi mutatói
VI. Irodalomjegyzék
1. Abu-Shakra M, Buskila D, Shoenfeld Y. Osteonecrosis in patients with SLE. Clin Rev Allergy Immunol. 2003 Aug;25(1):13-24. Review.
2. Aigner N, Schneider W, Eberl V, Knahr K. Core decompression in early stages of femoral head osteonecrosis-an MRI-controlled study. Int Orthop. 2002;26(1):31-5.
3. Beltran J, Knight CT, Zuelzer WA, Morgan JP, Shwendeman LJ, Chandnani VP, Mosure JC, Shaffer PB. Core decompression for avascular necrosis of the femoral head: correlation between long-term results and preoperative MR staging. Radiology. 1990 May;175(2):533-6.
4. Bjorkman A, Svensson PJ, Hillarp A, Burtscher IM, Runow A, Benoni G. Factor V leiden and prothrombin gene mutation: risk factors for osteonecrosis of the femoral head in adults. Clin Orthop Relat Res. 2004 Aug;(425):168-72.
5. Castro FP Jr, Barrack RL. Core decompression and conservative treatment for avascular necrosis of the femoral head: a meta-analysis. Am J Orthop. 2000 Mar;29(3):187-94.
6. Erb RE. Current concepts in imaging the adult hip. Clin Sports Med. 2001 Oct;20(4):661-96. Review.
7. Ficat RP. Treatment of avascular necrosis of the femoral head. Hip. 1983: 279-95.
8. Gebhard KL, Maibach HI. Relationship between systemic corticosteroids and osteonecrosis. Am J Clin Dermatol. 2001;2(6):377-88. Review.
9. Hankiss J, Fekete K, Salacz T, Karlinger K, Manninger J. [Early diagnosis and management of femur head necrosis in young adult age] Orv Hetil. 1997 Oct 5;138(40):2521-6.
10. Jones LC, Hungerford DS. Osteonecrosis: etiology, diagnosis, and treatment. Curr Opin Rheumatol. 2004 Jul;16(4):443-9. Review.
11. Lieberman JR. Core decompression for osteonecrosis of the hip. Clin Orthop Relat Res. 2004 mJan;(418):29-33. Review.
12. Mont MA, Carbone JJ, Fairbank AC. Core decompression versus nonoperative management for osteonecrosis of the hip. Clin Orthop Relat Res. 1996 Mar;(324):169-78. Review.
13. Radke S, Kirschner S, Seipel V, Rader C, Eulert J. Magnetic resonance imaging criteria of successful core decompression in avascular necrosis of the hip. Skeletal Radiol. 2004 Sep;33(9):519-23. Epub 2004 Jun 23.
14. Matsusaki H, Noguchi M, Kawakami T, Tani T. Use of vascularized pedicle iliac bone graft combined with transtrochanteric rotational osteotomy in the treatment of avascular necrosis of the femoral head. Arch Orthop Trauma Surg. 2005 Mar;125(2):95-101. Epub 2005 Jan 19.
15. Saini A,Saifuddin A. MRI of osteonecrosis. Clin Radiol. 2004 Dec;59(12):1079-93. Review.
16. Saito S,Ohzono K, Ono K. Joint-preserving operations for idiopathic avascular necrosis of the femoral head. Results of core decompression, grafting and osteotomy. J Bone Joint Surg Br. 1988 Jan;70(1):78-84.
17. Salacz T, Manninger J, Szita J, Hankiss J. [Aseptic femur head necrosis and therapeutic possibilities by using a bone graft with a vascular pedicle] Magy Traumatol Ortop Kezseb Plasztikai Seb. 1993;36(2):129-39.
18. Shannon BD, Trousdale RT. Femoral osteotomies for avascular necrosis of the femoral head. Clin Orthop Relat Res. 2004 Jan;(418):34-40. Review.
19. Simank HG, Brocai DR, Brill C, Lukoschek M. Comparison of results of core decompression and intertrochanteric osteotomy for nontraumatic osteonecrosis of the femoral head using Cox regression and survivorship analysis. J Arthroplasty. 2001 Sep;16(6):790-4.
20. Steinberg ME. Core decompression of the femoral head for avascular necrosis: indications and results. Can J Surg. 1995 Feb;38Suppl 1:S18-24.
21. Stulberg BN, Davis AW, Bauer TW, Levine M, Easley K. Osteonecrosis of the femoral head. A prospective randomized treatment protocol. Clin Orthop Relat Res. 1991 Jul;(268):140-51.
22. Suh KT, Kim SW, Roh HL, Youn MS, Jung JS. Decreased osteogenic differentiation of mesenchymal stem cells in alcohol-induced osteonecrosis. Clin Orthop Relat Res. 2005 Feb;(431):220-5.
23. Vande Berg BC, Malghem J, Lecouvet FE, Maldague B. Magnetic resonance imaging and differential diagnosis of epiphyseal osteonecrosis. Semin Musculoskelet Radiol. 2001;5(1):57-67. Review.
24. Zalavras CG, Vartholomatos G, Dokou E, Malizos KN. Genetic background of osteonecrosis: associated with thrombophilic mutations? Clin Orthop Relat Res. 2004 May;(422):251-5.
25. Tarner IH, Dinser R, Müller-Ladner U. Pharmacotherapeutic aspects of femoral head necrosis Orthopade. 2007 May;36(5):446-50. Review.
26. Reppenhagen S, Kenn W, Reichert J, Raab P, Eulert J, Nöth U. Imaging of avascular necrosis of the femoral head in adults Orthopade. 2007 May;36(5):430,432-4,436-40. Review.
27. Mattes T, Fraitzl C, Ostertag O, Reichel H. Differential diagnoses of avascular necrosis of the femoral head. Articular groin pain in adults Orthopade. 2007 May;36(5):414,416-22. Review.
28. Aldridge JM 3rd, Urbaniak JR. Avascular necrosis of the femoral head: role of vascularized bone grafts. Orthop Clin North Am. 2007 Jan;38(1):13-22, v. Review.
29. Kerachian MA, Harvey EJ, Cournoyer D, Chow TY, Séguin C. Avascular necrosis of the femoral head: vascular hypotheses. Endothelium. 2006 Jul-Aug;13(4):237-44. Review.
30. Zimmermann A, Udvarhelyi I, Lakatos J A korai avascularis combfejnecrosis kezelése flexiós osteotomiával Magy Traumatol Ortop Kézseb Plasztikai Seb 1994, 37 (2): 153-9
31. Zimmermann A, Udvarhelyi I, Végh G, Csákány L A korai avascularis combfejnecrosis kezelése izomlebenyes csontbeültetéssel Magy Traumatol Ortop Kézseb Plasztikai Seb 1994,37 (1): 217
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Dokumentáció, bizonylat
- Járóbeteg szakellátásban: ambuláns lap, kezelő lap.
- Képalkotó vizsgálatok képi és szöveges leletei
- Fekvőbeteg szakellátásban: kórlap, műtéti beleegyezés, műtéti leírás, decursus, zárójelentés.
- Felhasználásra került implantátumok bizonylatai, Magyar Artroplasztika Regiszterbe történő regisztráció
2. Gyakori társbetegségek Lásd 3.1. pont.
3. Érintett társszakmákkal való konszenzus Rheumatológia, traumatológia, radiológia.
4. Evidencia besorolás
A bizonyítékok szintjei
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Habituális patella ficamról
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
I. Alapvető megfontolások
1. A protokollok alkalmazási / érvényességi területe
mozgásszervi betegségekkel foglalkozók: ortopédia, traumatológia, sportorvostan, reumatológia, radiológia
2. A protokollok bevezetésének alapfeltétele Ortopéd Szakmai kollégium legitimációja
Ortopéd szakmai minimum feltételeknek megfelelő ellátási szint
3. Definíció
A térdkalács gyakorlatilag a térd minden hajlítása során laterál felé ficamodik.
3.1.) Kiváltó tényezők
- kongenitális
- lateralis femur condylus hypoplasia
- patellaalta
- patella parva
- iatrogén (m. quadriceps femorisba adott injekció csecsemő vagy kisgyermek korban)
- bénulás
- genu valgum
- lateralizált tuberositas tibiae
3.2.) Kockázati tényezők
mint 3.1. pont
4. Panaszok/Tünetek/Általános jellemzők
A térd minden egyes hajlítása során a patella laterál felé luxálódik. A ficamodás pillanatában a betegnek elakadás érzése van a térdében. Mindez retropatellaris és peripatellaris fájdalommal, instabilitás érzéssel, később retropatellaris krepitációval is járhat.
5. A betegség leírása
5.1.) Érintett szervrendszer(ek) Térd, combizomzat.
5.2.) Genetikai háttér Nem ismert.
5.3.) Incidencia / Prevalencia / Morbiditás / Mortalitás Magyarországon Erre vonatkozó adatokkal nem rendelkezünk.
5.4.) Jellemző életkor és nem
5-9 éves korban, idősebbeknél ritkán, nemi különbség nincs.
II. Diagnózis
1. Diagnosztikai algoritmusok
2. Anamnézis
A gyerekek sokszor nem tudnak a korcsoportjuknak megfelelő sport és tornakövetelményeknek megfelelni. Instabilitás és elakadás érzés, valamint fájdalom lehet az érintett térdben. Tisztázandó, hogy a családban másnál is fordult-e elő, volt-e a gyermeknek alsó végtagi bénulása, sérülése, térdízületi deformitása, illetve kapott-e a combjába injekciót?
3. Fizikális vizsgálatok
A térd minden egyes flexiója során a patella lecsúszik a laterális femur condylusról, azaz laterál felé luxálódik, ugyanakkor a femur facies patellarisa üresen áll. Ez sokszor látható és mindig tapintható is. A patella diszlokációja együtt jár a vastus lateralis és a tractus iliotibialis relatív megrövidülésével. Ha a térdet valgizáljuk és kirotáljuk a flexió során, a ficam még könnyebben bekövetkezik. Extenziósorána patella mindig helyre megy, kivéve, ha patellaalta van, amikor fixáltan luxált vagy subluxált is lehet.
Ha a térdet a patella helybentartása nélkül próbáljuk hajlítani, 30-40° flexiónál elakadást érzünk. A patella helybentartása melletti flexiókor fájdalom jelentkezik. A betegnek sokszor valgus térde van.
4. Kötelező (minimálisan elvégzendő) diagnosztikai vizsgálatok 4.1.) Laboratóriumi vizsgálatok
A diagnózishoz általában nem feltétlenül szükséges. 4.2.) Képalkotó vizsgálatok
2 irányú térd felvétel és axiális patella felvétel 30-60-90° flexióban. 4.3.) Egyéb
4.4.) Preoperatív kötelező vizsgálatok
Rutin műtét előtti kivizsgálás. Bénulásos eredet esetén a bénulás típusának és prognózisának tisztázása.
5. Kiegészítő diagnosztikai vizsgálatok (felhasznált bizonyítékok, azok szintjei) Csípő dysplasia kizárása (a kongenitális változattal társulhat!)
A femoropatellaris ízület porcborítékának, kongruitásának megítélésére MRI vizsgálat. (A típusú evidencia alapján)
6. Differenciál diagnosztika (felhasznált bizonyítékok, azok szintjei)
Recurrens, kongenitális vagy traumás patella luxáció és subluxáció, meniscus sérülés, (A típusú evidencia alapján)
III. Terápia
Nem gyógyszeres kezelés
A típusú evidencia alapján:
1. A megfelelő egészségügyi ellátás szintje
ÁNTSz minimumfeltételekalapján
2. Általános intézkedések
Tartózkodás a m. quadriceps injekciózásától.
3. Speciális ápolási teendők
Patella ablakos térd ortézis használata.
4. Fizikai aktivitás
A m. quadriceps (vastus medialis) erősítése.
5. Diéta Hatástalan.
6. Betegoktatás
A betegség lényegének elmagyarázása a szülőnek és a gyereknek.
III/3. Műtét
A típusú evidencia alapján:
1. A megfelelő egészségügyi ellátás szintje
Fekvőbeteg ellátás / műtéti tevékenység: ÁNTSz működési engedély alapján.
2. Általános intézkedések 2.2.) Műtői körülmények A műtét tárgyi feltételei
Kiemelt sterilitást biztosító műtő, az ÁNTSz minimumfeltételeknek megfelelően felszerelve. A műtét biztonságos kivitelezését biztosító általános műszerkészlet. Leggyakoribb szövődmények ellátásához szükséges műszerek. A műtét személyi feltételei
Sebész, célirányos elméleti és gyakorlati felkészültséggel, minimum egy asszisztens. Műtősnő, műtőssegéd.
Aneszteziológus orvos, valamint asszisztens közreműködése elengedhetetlen.
3. Speciális ápolási teendők
A műtétet követően, a beteg általános belgyógyászati státuszában felmerülő állapotváltozások korrekciójának biztosítása.
Gipszellenőrzés! Sebellenőrzés!
4. Sebészeti kezelés
4.1.) műtéti indikáció Gyakorlatilag minden esetben
4.2.) műtéti előkészítés
Általános belgyógyászati kivizsgálás, szükség szerinti szakorvosi konzíliumokkal kiegészítve. Aneszteziológiai protokoll szerinti előkészítés. 4.3) műtéti érzéstelenítés Aneszteziológiai protokoll leírása szerint
4.4.) műtét Lágyrészműtétek:
A műtét alapvetően 3 alapvető mozzanatból áll: a contractura nyújtása a térdízület laterális tokjának bemetszése. a mediális tok szűkítése.
Ezek számos variációban kerültek leírásra a szakirodalomban. (1,2,3,4,5) Csontműtétek:
Genu valgum esetén a deformáció helyének megfelelően (tibia vagy femur) végzett korrekciós osteotomia Tuberositas tibiae lateralisatio esetén tuberositas tibiae medialisatio (1,2,3,4,5)
4.5.) posztoperációs teendők
A szívódrainen keresztül ürült vérmennyiség regisztrálása, folyadékháztartás (só-elektrolit-, sz.sz. vérpótlás) rendezése, fájdalomcsillapítás, a beteg általános belgyógyászati státuszának ellenőrzése. Infekció és trombózis profilaxis, szükség szerint az alapbetegségek specifikus gyógyszerelése. Röntgen kontroll. Gipsz kontroll érzés-keringés vizsgálattal.
A műtét menetének részletes leírása, a műtéti leírás csatolása kórlaphoz, archiváláshoz. Általában a második posztoperatív napon drain eltávolítás. A gyógytorna és a beteg mobilizálásának elkezdése.
5. Fizikai aktivitás
Végtagrögzítés, gyógytorna és beteg mobilizálás az elvégzett műtét protokollja szerint.
6. Diéta
Önmagában a betegség nem igényel speciális diétát.
7. Betegoktatás
Általános betegtájékoztató szerint. Gyógytornász utasításainak megfelelően.
III/4. Egyéb terápia (pszichoterápia, gyógyfoglalkoztatás stb.) Általában nem szükséges.
IV. Rehabilitáció
Beteg mobilizáció, a térd rögzítése, tornáztatása, terhelése az elvégzett beavatkozástól függően. A rögzítés eltávolítása után fokozatos megterhelés mellett aktív izomtorna, a térd eredeti mozgástartományának, proprioceptivitásávak helyreállítása.
V. Gondozás
1. Rendszeres ellenőrzés
Kötözés sebgyógyulásig, varratszedés. Gipszlevétel után torna. 6-12 hónap után sportolás.
2. Megelőzés
Sportolás, megerőltetés kerülése teljes gyógyulásig.
3. Lehetséges szövődmények
Korai és késői infekció, haematoma, sebgyógyulási zavar, thrombophlebitis, mélyvénás thrombosis, tüdő embólia, igen ritkán ér- és idegkárosodás, recidíva, szalag szakadás, varratelégtelenség. 3.1.) Szövődmények kezelése
A 3. pontban felsorolt szövődmények kezelésének haladéktalan megkezdése a szakma szabályai szerint. Fontosa posztoperatív lokális szövődmények korai ellátása. Infekció gyanúja esetén korai feltárás, alapos debridement és átmosás, majd szívódrainek behelyezése javasolt. Steril haematoma miatt punkció, incízió, illetve a műtőben steril körülmények közötti kiürítés. Sebgyógyulási zavar, illetve bőrnekrózis esetén annak kiterjedésétől függően felületes hámosító kezelés vagy a defektus sebészi ellátása szükséges.
4. Kezelés várható időtartama/Prognózis
A beteg egyedi mozgásszervi státuszából következően egyedi felépülési prognózist kell megállapítani, amelyben törekedni kell az életminőség javításának legrövidebb, de legbiztosabb módjára. A kezelés várható időtartama 6-12 hónap.
5. Az ellátás megfelelőségének indikátorai Nemzetközi protokollok szerinti kiértékelése.
A műtött beteg általános és speciális mozgásszervi állapotának rögzítésének dokumentálása szükséges az állapotváltozás utánkövetése érdekében.
6. Szakmai munka eredményességének mutatói
A beteg aktivitási szintje, a térd mozgásterjedelme a műtét után.
A ficam kiújulásnak gyakorisága.
A térdkalács porcfelszíne degenerációjának mértéke.
A szövődmények elfordulásának gyakorisága.
7. Dokumentáció, bizonylat Kórlap
Ambuláns kezelési lapok Rtg., MRI felvételek Kiegészítő vizsgálatok eredményei Gyógytornász kezelési lap Műtéti leírás
VI. Irodalomjegyzék
1. Tachdjian: Pediatric Orthopedics 2nd Edition Vol. 2. p. 1551-1582.
2. Duparc: Surgical Techniques in Orthopaedics and Traumatology Elsevier. 2002. Vol. 7. Femur and Knee, section 55-520-A-10 - A-20
3. Vízkelety (szerk.): Az ortopédia tankönyve, Semmelweis Kiadó, 1999. 224
4. Campbell's Operative Orthopaedics, 9th Edition Mosby1998 1334-1349
5. Szendrői (szerk.): Ortopédia, Semmelweis Kiadó, 2005. 358-359
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Dokumentáció, bizonylat
- Járóbeteg szakellátásban: ambuláns lap, kezelő lap.
- Képalkotó vizsgálatok képi és szöveges leletei
- Fekvőbeteg szakellátásban: kórlap, műtéti beleegyezés, műtéti leírás, decursus, zárójelentés.
2. Érintett társszakmákkal való konszenzus Gyermekgyógyászat, Traumatológia, Radiológia.
3. Evidencia besorolás
A bizonyítékok szintjei
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Infantilis cerebralis paresisről (ICP)
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
Szinonímák: Little-kór, Spasticus bénulások
I. Alapvető megfontolások
1.1. Gyermekortopédia, ortopédia, gyermekgyógyászat, gyermek ideggyógyászat, rehabilitáció
1.2. Megfelelő tájékozottság a fent említett szakmákban.
1.3. Definíció
Pre-vagy perinatalis agyi károsodás következtében kialakult psychosenso-motoros zavar. B szintű evidencia (1) 3.1. Aktiváló tényezők a betegség különböző formáit és lokalizációját hozzák létre. B szintű evidencia (2)
| A spasticitas csoportosítása és kiváltó oka | ||
| Lokalizáció | Kiváltó ok | |
| Hemiplegia | féloldali | perinatalis agyvérzés |
| Diplegia | két alsó végtag | agyi anoxisa (koraszülöttek) |
| Quadriplegia | mind a négy végtag, egész test | agyi fejlődési rendellenesség |
| Monplegia | egy végtag | |
3.2. Koraszülöttség,elhúzódó vagy gyors, nehéz szülés, központi idegrendszerfejlődési rendellenességei,gyulladások kiválthatják a betegséget. B szintű evidencia (3)
4. A szülők rendszerint a mozgás fejlődés visszamaradását, görcsös vagy éppen petyhüdt állapotot észlelnek. Később a szellemi fejlődés visszamaradását és mozgás zavart is észlelnek.
Előfordul azonban, hogy később, iskolás korban a gyengébb teljesítmény és beilleszkedési zavarok miatt diagnosztizálják a betegséget.
A tünetek kor szerint nagyon eltérőek. C szintű evidencia (4)
5.1. Érintett a központi idegrendszer, elsősorban az agy különböző részei és ennek következtében a hozzá tartozó periféria különböző lokalizáció szerint
A periféria, a végtagok izomzata és az ízületeka fejlődés kapcsán változhatnak, kóros ízületi és végtag állás alakulhat ki. A hasznos mozgás, a járás jelentős mértékben zavart lehet. B szintű evidencia (5,6)
5.2. Genetikai okot ritkán lehet kimutatni, bár agyi fejlődési rendellenességnél előfordulhat. C szintű evidencia (7)
5.3. 0,2-0,3% körül van a hazai előfordulás, súlyos esetekben a mortalitás meghaladja a normál populációét. B szintű evidencia (8,9)
5.4. fél éves kor után lehet csak biztosan megállapítani, vagy kizárni a betegséget. B szintű evidencia (10,11)
5.5. Mindkét nemben egyforma gyakorisággal fordul elő.
II. Diagnózis Anamnézis
Nagyon fontos a terhesség és a szülés körülményeit tisztázni. Terhesség alatti rendellenességek a magzat oxigenizációjának károsításával előidézhetik a központi idegrendszer sérülését. A szülés lefolyásáról is részletesen tájékozódni kell. A szülés elhúzódása vagy rohamos lefolyása, fogó alkalmazása koponyaűri vérzéshez vezethet. A szülőfájások rendellenes ritmusa, pl. ha a méhizomzat összehúzódása túl hosszú ideig tart, a magzat agyi anoxiájához vezethet. A rizikótényezőket azonban kellő kritikával kell értékelni, mert a különböző tényezők után normális és kóros irányban is folytatódhat az agy fejlődése.
A koraszülöttek sérülékenyebbek, így a szülés normális lefolyása alatt is könnyebben szenvednek károsodást. Az újszülött állapotára, az asphyxiára, élesztgetésre, inkubátorba helyezésre, sárgaság fokára, vércserére vonatkozó kérdéseink nyomán kaphatunk felvilágosítást. Ha a csecsemő fejlődésében visszamaradt (nem fordul, nem ül fel, illetve nem a megfelelő időben teszi, gondolnunk kell Little-kórra.
A már járó gyermeknél a leggyakoribb panaszok: az alsó végtagok kereszteződése, hajlított térddel, lábujjhegyen járás. II.2. Fizikális vizsgálat
A betegség különböző súlyosságú lehet. Az idősebb gyermekeknél is alig felismerhető enyhe fokú betegségtől a súlyos, már a születés után észlelhető spasticitásig. A gyermeket először fekvő helyzetben vizsgáljuk. Megtekintésre feltűnhetnek a kényszermozgások, az ízületek jellegzetes tartása. Az ízületek mozgathatóságát az izmok feszülését meghatározzuk. Ezt követően csecsemőkön a nyak-fejtartását vizsgáljuk, idősebbeken az ülést, állást, járást.
Tünetek:
A jellemző tünetek életkorok szerint a következők:
- Újszülöttkorban: kóma, sajátságos sírás, intracranalis nyomásfokozódás tünetei, agyidegek bénulása, normálistól eltérő testhelyzet, reflex- és mozgásfokozódás (aszimmetria), fény hatására elmarad a pislogás, szopásképtelenség, Moro-reflex, palmarisés plantaris fogóreflex hiánya, a fejtartás hiánya függőleges helyzetben. Azokat az újszülötteket, akiknél ezeket a jeleket észleljük, kezelni és ellenőrizni kell.
- Csecsemőkorban: rossz nyaktartás 4 hetes kor után, nyelési és szopási nehézségek, perzisztáló tonusos reflex, 3-4 hónapos kor után Moro-reflex, a kezek állandó ökölbe szorítása. Ha a csecsemőt hónaljánál fogva felemeljük a csípők extensióba és adductióba, a térdek extensióba kerülnek, kezek állandó ökölbe szorítása észlelhető. A térdek hirtelen behajlításra a lábhát vagy a comb elülső felszínének ingerlésére, adductorfeszülés, a lábak equinus spasmusa lép fel. Clonusos ínreflexeka spasticitas jelei.
- 2 éves kor után a Babinski- és Oppenheim-reflex kórjelző. Az ínreflexekfokozottak, a relflexogen zónák kiterjedtek, clonus észlelhető. A felső végtagon rendszerint pronatiós spasmust észlelünk, az alkar nem supinálható teljesen, a tenyerek nem fordíthatók felfelé. Az athetosis első jelei gyakran csaka 2-3. életévben észlelhetők, mint az ujjak, a kéz, a láb sajátságos mozgása. Differenciáldiagnosztikailag elsősorban az adductor-spasmus okoz problémát. Nehéz elkülöníteni a Little-kór okozta adductiós csípőcontracturát a világra hozott csípőficammal vagy dysplasiával együtt járó mozgáskorlátozottságtól. A csípőkről készült röntgenfelvétel eldönti a kérdést.
- Kisgyermekkorban: a korábbi tünetek kifejezettebbek lesznek anélkül, hogy a betegség progrediálna. Enyhe esetekben a következő tünetek lehetnek jelen:
- a gyermek keze ügyetlen,
- járása nem harmonikus,
- térdeit egymáshoz szorítva, flektált térdekkel jár,
- sarkát nem teszi le,
- lábait keresztezi.
Súlyos esetben mentális és motoros retardatio állhat fenn. Scoliosis, kyphoscoliosis alakulhat ki.
Fontos megállapítani a gyermek szellemi fejlettségének fokát és mozgáskészségét is, mert jelentősen befolyásolja a kezelési tervet.
11.3. A központi idegrendszer károsodása miatt ajánlott gyermekneurológussal való együttműködés. Szükség lehet lumbalpunctio esetleg elektromyografia elvégzésére.
11.4. Koponya UH vizsgálat, szükség esetén MR kimutatja az agyi károsodást. Elsősorban fejlődési rendellenességeknél fontos.
11.5. Differenciáldiagnosztika szempontjából felmerülhet spinalis izomatrophia, herediter sensomotoros betegségek, idiopatias v. familiaris lábujjhegyen járás, familiaris spasticus paraplegia.
11.6. Diagnosztikus algoritumus
Pontos terhességi szülési, újszülöttkori anamnézis felvétel. Fizikális vizsgálat
Tonusvizsgálat
Reflexvizsgálat
A gyermek mozgás és szellemi fejlődésének pontos követése. III. Terápia
III.1.1. Speciális intézetek, fejlődésneurológiai és neurorehabilitációs osztályok, Mozgássérültek Pető András Nevelőképző és Nevelőintézete és ennek részlegei, egyéb hasonló profilú szerveződések, gyermekortopédiai osztályok.
III.1.2.Célszerű a súlyosabb betegek intézeti elhelyezése, esetleg hétvégi szabadságolással.
III.1.3.A pontos diagnózis felállítása esetleg hosszabb időt vehet igénybe. A konduktív pedagógia módszerének alkalmazása.
Csoportos fejlesztési programok, melynek keretében oldható meg a diéta, a fizikai és szellemi aktivitás fokozása és az oktatás is.
III.2. Gyógyszeres kezelés
Gyermekorvos, ideggyógyász, ortopéd szakorvos, rendelőintézetben vagy kórházi osztályon alkalmazhat gyógyszeres kezelést. Spasticus betegeknek izomlazítók: Mydeton, Baclofen, Silurid adhatók. Meg kell állapítani az optimális adagot.
Botullin toxin befecskendezése az erősen spasticus izmot beidegző ideg mellé eredményes lehet. C szintű evidencia (12,13)
Beültethető a testbe tartály Baclofen részére, amelyből fokozatosan adagolható. C szintű evidencia (14,15)
Ezek a gyógyszerek aluszékonyságot, nyálcsorgást okozhatnak. Csökkenteni kell az adagot, vagy abbahagyni a kezelést.
III.2.4.Kiegészítő/alternatív gyógyszeres kezelés
Nyugtatók is adhatók. Jó hatású a zsálya főzettel való borogatás és fürdetés.
III.2.5.Terápiás algoritmus
- Pontos diagnózis megállapítása és
- Korai kezelés a fejlődésneurológiai és neurorehabilitációs osztályok keretében.
- A Mozgássérültek Pető András Nevelőképző és Nevelőintézetében vizsgálat és konzervatív kezelési javaslat kialakítása, ennek megfelelően kezelés megszervezése. (Konduktívpedagógiai módszer)
- Fél-egy évente ortopédiai ellenőrzés, amennyiben lehetséges a gyermekortopédiai sebészeti ellátásban jártas szakorvos és kézsebész, vagy kézsebészeti műtétekben is jártas ortopéd szakorvos által végezve, és alkalmas időpontban a cerebral paresises betegek műtétre irányítása.
- A rendszeres, folyamatos kontrollvizsgálatoknak megfelelően a cerebral paresises gyermekek korszerű segédeszközökkel, orthesisekkel való ellátásának biztosítása a gyermekortopédiában járatos szakorvos véleménye
alapján. (AFO, cipőbe helyezhető AFO, négykörsines járógép, medencekosaras járógép, alsó végtagi, felső végtagi sínek, éjszakai korrekciós sínek, cipők, Swash-készülék, csípőtávolító eszközök, ülőfűző, ültetőmodul, korzett)
- Közepesen súlyos ill. súlyos cerebral paresis esetén javasolt a csípők esetleges subluxációs változásának megítélése céljából évente csípő röntgenfelvételt készíteni és így követni a csípők állapotát, hogy időben preventív műtétre kerülhessen sor, vagy időben megtörténhessék a csípők egyéb ortopéd sebészeti ellátása.
- Nagy jelentőséggel bírna, ha hazánkban is lehetségessé válna, a cerebral paretikus betegekjárásanalízisére alkalmas mozgásanalitikai labor kialakítása, mely jelentősen javítaná a spasztikus betegeknél végzendő speciális ortopédiai műtétek indikációjának biztonságát, egyben lehetőséget teremtene a műtéti eredményesség mérésére és a spasztikusoknál alkalmazható segédeszközök, orthesisek alkalmasságának és szükségességének objektív megítélésére.
III.3.1.Infantilis cerabralis paresis betegeken a szükséges műtéteket, elsősorban nagy tapasztalattal rendelkező gyermekortopédiai osztályokon tanácsos végezni, bizonyos beavatkozásokat idegsebészeten illetve kézsebészeti jártassággal bíró osztályon.
III.3.2.Ezeka betegek különleges ápolást, gondozást igényelnek a műtételőtt és után is, ezért gyakran szülővel együtt ajánlatos felvenni.
III.3.3.A gyermekeket a lehető legrövidebb ideig hospitalizáljuk. Többnyire gipszkötésben vannak. 1-2 héttel a műtét után lehetőleg állítsuk fel a gyermekeket, járassuk. Kézműtét után lehetőség szerint naponta tornáztassuk az operált végtagot gyógytornász irányításával, majd helyezzük vissza a gipszsinbe..
III.3.4.Sebészi kezelés
III.4.1.Műtéti indikáció
Műtétet lehet preventív, az ápolást megkönnyítő, a segédeszköz viselését megsegítő, és kuratív céllal végezni. Megelőző műtétként, tenotomiákat, ínátültetést, osteotomiákat végezhetünk spasmus, kontraktúra oldására és a másodlagos deformitások, kóros állapotok megelőzésére. Ezek:
Nyílt adductor tenotomia Térd flexor tenotomia
Achilles tenotomia vagy m. gastrocnemius recessio Varisalo femurosteotomia
Vállízületi adductios és berotatiós contractura oldása
Könyökízület flexiós contracturájának oldása
Alkari pronatios contractura oldása
Csuklóízületi flexiós contractura oldása, ínáthelyezés
Ujjak spasticus contracturájának oldása
Hüvelykujjadductiós contracturájának oldása
A felsorolt műtétek végezhetők kuratív céllal is.
A spasticusok kezelésében nagyon fontos szerep jut az ortopédiai műtéteknek. A műtét típusának kiválasztása mellett az időpont is igen lényeges. Megfelelő időben elvégezve egy műtétet, megelőzhetjüka már nehezebben korrigálható deformitások kialakulását. A spasticus gyermek jellegzetes ízületi állása vagy contracturája a következő:
- Sagittalis síkban: fokozott lordosis, hajlított csípő, hajlított térd, equinus helyzetű láb. Az alsó végtag izmai zárt kinetikus láncot képzenek. Ahhoz, hogy a súlypont az alátámasztási pont fölé kerüljön, az egyik ízület ilyen irányú kóros helyzetét kényszerűen követi a másik két ízületé is. Éppen ezért gyakran mind a három ízületben meg kell oldani a kóros helyzetet, illetve contracturát.
- Frontalis síkban: a csípőadductorokfeszülését vagy contracturájátészleljükés a sarkak valgus vagy varus helyzetben lehetnek, rendszerint az equinus contractura kompenzációjára.
- Horizontális síkban: a csípők befelé rotált tartását láthatjuk, ami az adductiós spasmussal együtt a járást megnehezíti.
A spasticus gyermekek gyógyításában gyakrabban alkalmazott műtéti eljárások a következők. C szintű evidencia (16,17,18)
Az adductiós csípőconractura vagy -spasmus megoldására az adductorok nyílt tenotomiája végezhető, szükség esetén a n. obturatorius elülső ágának átmetszésével. A rendszerint fennálló, flexiós csípőcontractura megoldására ugyanabból a metszésből a m. iliopsoas is tenotomizálható.
Az adductorok nyílt tenotomiája elvégezhető 2 éves kor után, ha a csípők abductiója 30 fok alá csökkent. A műtéttel megakadályozhatjuk a coxa valga, subluxatio, luxatio kialakulását. Ha már kialakult kisebb fokú coxa valga és subluxatio, a tenotomia után normalizálódhatnaka csípőízületi viszonyok. Ha az adductor tenotomiát nem végezzük el időben, a tartósan fennálló adductor túlsúly következtében a combnyak kiegyenesedik, és a femurfejfokozatosan subluxálódikvagy luxálódik. Ebben az esetben a nyílt adductor tenotomia mellett már a subluxatiót, illetve luxatiót is meg kell oldani.
A coxa valgát és subluxatiót varizáló derotatiós osteotomiával korrigálhatjuk. Itt is belső rögzítést alkalmazunk, de szükség van gipszkötésre is. C szintű evidencia (19)
A luxatiót nyílt repositióval oldjuk meg. Rendszerint szükség van rövidítéses, varizáló femurosteotomiára is. A vápa általában jól fejlett, így a repositio elég stabil. Ha a vápa sekély, második ülésben Pemberton vagy Chiari-féle medenceosteotomia végezhető. C szintű evidencia (20)
A csípőízomzat egyensúlyzavarának gyakori következménye az alsó végtagok befelé rotált tartása, mely járáskor fokozottabban jelentkezik. Az adductor izomzat eredésének hátrahelyezése az ülőcsontra jól korrigálhatja a funkciózavart. Idősebb gyermekeknél a befelé rotatiós contractura megoldására már szükség lehet derotatiós femurosteotomiára is. Serdülő és felnőtt korban járásképtelen betegeken csípőfájdalom miatt a luxált femurfejet reszekálhatjuka kistrochanter alatt. C szintű evidencia (21)
A térdekflexiós spasmusa és contracturája a hajlítóizomok tenotomiájával oldható meg. A spasmus fokától függően a m. semitendinosust, semimembranosust, gracilist és bicepset vagy ezek közül kettőt, hármat tenotomizálunk. A térdflexor tentomiája után 4 hétig gipszkötést alkalmazunk, azonban a gyermek már ebben felállhat, járhat. C szintű evidencia (22)
Ha a gastrocnemius spasmus vagy contarcura is fennáll, a térdflexorok tenotomiájával együtt leválasztjuk a gastrocnemius fejek eredését is. Idősebb gyermekeknél, felnőtteknél a térdízületi tok contracturája is fennállhat, és szükség lehet a hátsó ízületi tok bemetszésére is. C szintű evidencia (22)
A lábak equinus spasmusa és contracturája a leggyakoribb következménye a spasticitásnak. Ha a gyermek lábujjhegyen jár, a kis támaszkodási felület miatt bizonytalan a járása, nehezebben tanul meg járni. Vizsgálat alapján eldönthető, hogy az equinus spasmus vagy contractura kialakulásában a tricpes surae teljes egészében részt vesz-e vagy a m. soleus, vagy gastrocnemiusok vannak-e túlsúlyban.
Az equinus contracturát és spasmust leggyakrabban achillotomiával oldjuk meg. Ritkábban kerül sor a gastrocnemiusfejek leválasztására, esetleg denervatióval együtt vagy aponeurosisának haránt átmetszésére. Ezt akkor végezhetjük, ha a gastrocnemius vagy Silferskiöld-jel pozitív: nyújtott térddel a láb equinusban van, hajlított térd mellett extendálható, akár a 0§-on túl 20-30 fokkal is.
Az equinus állással együtt a sarok valgus vagy varus helyzetbe kerülhet. Az equinus contractura megoldásával ez is korrigálható.
A sarok valgitása korrigálható a sinus tarsiba helyezett csontléccel (Grice-műtét).
Az achillotomiát feltárással és nagyon pontos beállítással kell elvégezni. Subcutan (három pontos Achillotomia) végzett achillotomia után az invégekösszevarrása nélkül a lábcalcaneus helyzetbe kerülhet, és az addig lábujjhegyen járó gyermek járásképtelen lesz. Csak ott ajánlatos végezni, ahol a nyílt műtéttel nagy tapasztalattal rendelkeznek. A túl korán elvégzett hosszabbítás, vagy a kelleténél jobban meghosszabbított Achilles-ín hasonló eredményhez vezethet. Abban az esetben viszont, ha nem végezzük el időben az achillotomiát, a sarok equinus állását az előláb dorsalflexiója korrigálja, és a láb súlyos deformitása, sajkaláb alakul ki. A deformálódott láb formai és funkcionális javítása a lábtőízületek modelláló resectiójával érhető el a növekedés befejezése után. A műtét után 3 hónapra járógipszet helyezünk fel, de már 3 hét múlva járhat a beteg. C szintű evidencia (18)
Súlyos scoliosis, kyphoscoliosis is kialakulhat főleg a járóképtelen betegeken. Ezek műtéti kezelése olyan helyen ajánlható, ahol ebben megfelelő gyakorlat van.
A spasticus gyermekek műtét után általában 3-4 hétre gipszkötést kapnak, de már a 10. nap után felállítjuk és lehetőség szerint járatjuk őket. A szükséges műtéteket igyekszünk egy időben elvégezni (4-6 műtétet is), hogy az immobilizáció a legkisebb kiesést okozza a gyermek mozgásfejlődésében.
Fontos hangsúlyozni és a szülőkkel is megbeszélni, hogy az ortopédiai műtétekkel a lehetőséget teremtjük meg ahhoz, hogy a gyermek mozgása, járása javuljon, de a műtéti eredmény hasznosításához még hosszú és kitartó gyakorlás szükséges.
Gipszlevételre a gyermekeket többnyire ismét felvesszük, és a kezdő lépéseket gyógytornász vezetésével itt teszi meg.
A további gyakorlatozás, a torna azonban otthon, a szülő irányításával vagy speciális intézetekben történik.
Felső végtagon ritkábban kerül sor műtétre.
A felső végtagon megfigyelhető deformitások:
Váll: berotatio, adductio
Könyök: flexio
Alkar: pronatio
Csukló: flexio, ulnar deviatio
Ujjak: flexio, esetenként hattyúnyak deformitás
Hüvelykujj: adductio, flexio
A kéz funkciójának javítására a következő beavatkozások végezhetők:
Vállízületi adductios és berotatiós contracturájának oldása a pectoralis major és subscapularis izom leválasztásával; Könyökízület flexiós contracturájának oldása a biceps izom Z-tenotómiájával;
Alkari pronatios contractura oldása a pronator teres izom leválasztásával, illetve supinator izomként való áthelyezésével;
Csuklóízületi flexiós contractura oldása, ínáthelyezéssel, legtöbbször a flexor carpi ulnaris ín befűzése az extensor carpi radialis ínba, történik, de felhasználható még a musculus brachioradialis vagy a musculus pronator teres ina is. A további csuklócontractura és -spasmus megszüntetése céljából a flexor carpi radialis inon Z-tenotomia végezhető illetve a feszülő palmaris longus in átvágható.
Ujjak spasticus contracturájának oldása a felületes és mély ujjhajlító inak és szükség esetén a flexor pollicis longus in Z-tenotómiájával végezhető. Ha az ujjak extensiója gyenge, a leválasztott flexor carpi ulnaris inat fűzzük be az extensor digitorum communis inaiba és a csukló extensió más innal pl. musculus brachioradialis vagy pronator teres innal pótolható.
Hüvelykujj adductiós contracturájának oldása az adductor pollicis in oldásával vagy az 1. és 2. metacarpus közé beültetett csontléccel történhet.
A kézműtétek célja a funkció javítás, de higéniai és esztétikai szempontok is figyelembe vehetők a műtéti terv felállításakor. A műtét előtt EMG használható a pontosabb izomaktivitás megítélésére. Botulin toxin is adható a spastikus izmokba, szimulálva ezzel az inhosszabbítás eredményességét. A kéz funkcióját a mindennapi élettevékenységben lehet megítélni. A műtét előtti állapotot össze kell hasonlítani a műtét utánival, lehetőleg standardizált körülmények között.
(és a m. pronator teres. Szóba jöhet a csuklóízület elmerevítése korrigált helyzetben. C szintű evidencia (23,33)
A kéz fogóképességét javíthatja a hüvelykujj adductiós helyzetének korrekciója. Műtétek előtt gondosan
tanulmányozzuk, hogy a tervezett helyzetben valóban javul-a a kéz funkciója. )
A deformált lábak funkciójának javítására gyakran rendelünk ortopéd cipőt, és egyes esetekben járógéppel lehet a térd- vagy bokaízületet stabilizálni, vagy a kóros mozgásokat kiiktatni. A kezelés minden fázisában adhatók a spasticitást csökkentő gyógyszerek.
A spasticus betegek egy része jól megtervezett kezeléssel önellátóvá tehető, sőt elérhetjük azt is, hogy a termelőmunkában részt vegyenek. Megfelelő gondossággal kiválasztható az állapotuknak és képességeiknek leginkább megfelelő foglalkozás.
Fontos az optimális időpont megválasztása és a pontos dozírozás. Bizonyos műtétek felnőtt korban is végezhetők.
A műtét csak egy állomás a kezelésben és az eredmény a gyermek mozgás és szellemi fejlődésétől függ. Lényegesen megkönnyítheti a gyermek mozgását.
III.4.2.A műtéti előkészítés fontos része a jó szellemi fejlettségű gyermeknél a műtét menetének megbeszélése. A szülőket is alaposan kell tájékoztatni és megszervezni a műtét utáni ellátást. Intézetben lévő gyermekek is gyakran hazakerülnek arra a 4 hétre, amíg gipszben vannak.
III.4.3.A műtét általában általános anaesthesiában történik. Nagyobb gyerekeken lumbal anaesthesia is megkísérelhető.
III.4.4.4.A gyakoribb ortopédiai műtéteket felsoroltuk. Fontos a precíz technika és ínmeghosszabbításnál a meghosszabbítás mértéke. Selectiv dorsalis rhizotomia végezhető diplegiás 4 évnél idősebb járóképes gyermeknél, akiknél jelentős fokú spasticitás áll fenn. Ezt a műtétet ajánlatos kellő tapasztalattal rendelkező idegsebésszel végeztetni.
III.4.4.5.Ortopédiai műtétek után a gyermekek általában 4 hétig gipszkötésben vannak. Történnek kísérletek a rövidebb rögzítésre és hosszabb kórházi tartózkodásra tornával
A gipszben a gyermekek forgathatók, felállíthatók, sőt még járathatók is. Kerekes székben kivihetők a szabadba. Fél-egy évente ellenőrzendők a betegek.
Fizikai aktivitásukat biztosítani kell és lehetőleg normál iskolába járjanak.
IV. Rehabilitáció
Szem előtt kell tartani, hogy a spasztikus gyermekből spasztikus felnőtt lesz. Erre a felnőtt életre, tanulásra, kereső foglalkozásra, párválasztásra, terhességre kell felkészíteni őket. Szükség lehet ortézissel való ellátásra. C szintű evidencia (24)
A betegeket fél-egy évente ellenőrizni kell és megelőzni újabb deformitások kialakulását.
A műtétek lehetnekelégtelenek, de túlkorrekció is előfordul. Ez utóbbi rosszabb állapotot okozhat, mint a műtét előtti. Az ismételten kialakuló kontraktúrák újabb műtéttel korrigálhatóak.
A spasticus betegekkel életük végéig foglalkozni kell, bár lehetnek hosszú évekig tartó periódusok, amikor semmi kezelésre nincs szükség. A kor előrehaladtával, esetleg a testsúly fokozódásával egyre gyakrabban jelentkeznek panaszok.
V. Gondozás
Az ellátás indikátora
Korai diagnózis (legkésőbb "éves kor).
Kezelés és ellenőrzés megfelelő intézetben.
Szükség szerint gyógyászati segédeszköz ellátás.
Preventív műtétek időben elvégezve.
Secunder deformitások megelőzése.
Önellátóvá tétel.
Normál iskola.
Kereső foglalkozás.
Családalapítás.
VI. Irodalomjegyzék
1. MacKeith RC, Polani PE: Cerebral palsy. Lancet, 1958,1:61.
2. BaxM: Terminology and classification of cerebral palsy. Dev.Med.Child Neurol., 1964,6:295-297.
3. Nelson KB, Leviton A: How much of neonatal encephalopathy is due to birth asphyxia? Am J Dis Child 1991,
145:132-136.
4. Damiano DL, Kelly LE, Vaughn CL: Effects of quadriceps Femoris Muscle Strengthening on crouch gait in children with spastic diplegia. Physical Therapy, 1995, 75(8): 658-671.
5. Rosenbaum PL, Walter SD, Hanna SE et al: Prognosis for gross motor function in cerebral palsy: creation of motor development curves. JAMA, 2002, 288:1357-1363.
6. Brown JK, Minnus RA: Mechanisms of deformity in children with cerebral palsy. Seminars in Orthopaedics, 1989,14(4): 236-255.
7. Fink JK: Hereditary spastic paraplegia. Neurol. Clin., 2002, 20: 71126.
8. Winter S, Autry A, Boyle C, Yeargin Allsopp M: Trends in the prevalance of cerebral palsy in a population based study. Pediatric, 2002,110:12205.
9. Nelson KB: The epidemiology of cerebral palsy in term infants. Men. Retard Dev. Disabil. Res. Rev., 2002,8:14650.
10. Johnson DC, Damiano DL, Abel MF: The evolution of gait in childhood and adolescent cerebral palsy. J. Pediatr. Orthop., 2002,22:677-682.
11. Bell KJ, Ounpuu S, DeLuca PA, Romness MJ: Natural progression of gait in children with cerebral palsy. J. Pediatr. Orthop., 2002,22:677-82.
12. Cosgrove AP, Corry IS, Graham HK: Botulinum toxin in the management of the lower limb in cerebral palsy. Dev. Med. Child Neurol., 1994, 36: 386-396.
13. Koman LA, Mooney JF, Paterson Smith B., Walker F, Leon JM and the BOTOX Study Group: Botulinum toxin type A neuromuscular blockade in the treatment of lower extremely spasticity in cerebral palsy: a randomized, double-blind, placebo-controlled trial. Botox Study Group, J. Pediatr. Orthop., 2000,17:108-115.
14. Albright AL,Cervi A, Singletary J: Intrathecal baclofen for spasticity in cerebral palsy. JAMA, 1991,265:1418-1422.
15. Armstrong RW, Steinbok P, Cochrane DD et al: Intrathecally administered baclofen for treatment of children with spasticity of cerebral origin. J. Neurosurg. 1997,87:409-414.
16. Rodda J, Graham HK: Classification of gait patterns in spastic hemiplegia and spastic diplegia: a basis for management algorithm. Eur J Neurol 2001,8:98-108.
17. Nene AV, Evans GA, Patrick JH: Simultaneous multiple operations for spastic diplegia: outcome and functional assessment of walking in 18 patients. J. Bone Joint Surg. (Br.), 1993: 75-B: 488-494.
18. Abel MF, Damiano DL, Pannunzio M, Bush J: Muscle-tendon surgery in diplegic cerebral palsy: functional and mechanical changes. J. Pediatr. Orthop, 1999,19: 366-375.
19. Ounpuu S, DeLuca P, Davis R, Romness M: Long-term effects of femoral derotation osteotomies: an evaluation using three-dimensional gait analysis. J. Pediatr. Orthop, 2002,22:139-145.
20. Cooperman DR, Bartucci E, Dietrick E, Millar EA: Hip dislocation in spastic cerebral palsy: Long term consequences. J. Pediatr. Orthop. 1987, 7: 268-276.
21. Wildmann RF, Do TT, Doyle SM, Burke SW, Root L: Resection arthroplasty of the hip for patients with cerebral palsy: an outcome study. J. Pediatr. Orthop., 1999,19: 805-810.
22. Beals RK: Treatment of knee contracture in cerebral palsy by hamstring lengthening, posterior capsulotomy, and quadriceps mechanism shortening. Dev. Med. Child Neurol., 2001,43(12): 802-805.
23. Boyd RN, Morris ME, Graham HK: Management of upper limb dysfunction in children with cerebral palsy: a systematic review. Eur. J. Neurol., 2001,8(Suppl. 5): 150-166.
24. Anderson C, Mattsson E: Adults with cerebral palsy: a survey describing problems, needs and resources, with special emphasis on locomotion. Dev.Med.Child Neurol., 2001,43: 76-82.
25. Bleck E.E.: Orthopaedic Management in Cerebral Palsy. Mackeith Press, Oxford, 1987.
26. Cahuzae M.: L'enfant infirme moteur d'origine cerebral. Masson, Paris, 1977.
27. Canale T.S., Beaty J.H.: Operative Pediatric Orthopaedics. Mosby Year Book, St.Louis, 1991.
28. Sharrard W.J.W.: Paediatric Orthopaedics & Fractures. Blackwell Scientific Publications, Oxford & Edinburg, 1993.
29. Tachdjian M.O.: Pediatric Orthopedics. W. B. Saunders Co. Philadelphia, London, Toronto, 1990.
30. Thom H.: Die infantilen Zerebralparesen. 2. kiadás,Thieme, Stuttgart, 1982.
31. Vízkelety T.: Gyermekortopédia. Medicina, Budapest, 1994.
32. Vízkelety T. (szerk.): Az ortopédia tankönyve. Semmelweis Kiadó, Budapest, 2002.
33. Nachemson AK. Tendon Transfers in Cerebral Palsy. In Fridén, ed. Tendon Transfers in Reconstructive Hand Surgery. London and New York: Taylor&Francis, Federation of European Societies for Surgery of the Hand, 2005:133-148.
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Gyakori társbetegségek. Rossz fogazat, epilepszia, hydrocephalus.
2. Társszakmák: gyermekgyógyászat, gyermek (fejlődés) neurológia, idegsebészet, rehabilitáció.
3. Dokumentáció, bizonylat
- Járóbeteg szakellátásban: ambuláns lap, kezelő lap.
- Képalkotó vizsgálatok képi és szöveges leletei
- Fekvőbeteg szakellátásban: kórlap, műtéti beleegyezés, műtéti leírás, decursus, zárójelentés.
4. Evidencia besorolás
A bizonyítékok szintjei
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
A kézízületi synovitisekről és tenosynovitisekről
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
I. Alapvető megfontolások
A betegségek diagnosztizálása, alapkezelése a rheumatológia feladata, azzal a megkötéssel, hogy a klinikai képtől, lefolyástól függően időszakos ortopéd-sebészeti vizsgálat is szükséges a műtéti terv (sokszor ez sorozat műtétet jelent) meghatározásához..
1. A protokoll alkalmazási, érvényességi területe Ortopédia, reumatológia és kézsebészet
2. A protokoll bevezetésének alapfeltételei Ortopéd Szakmai Kollégiumi legitimációja
Szakmai minimum feltételeknek megfelelő Ortopédiai Osztály.
3. Definíció
Az ízületek és az ínhüvelyek synovialis rétegének a gyulladása.
3.1. Kiváltó tényezők: az okok tisztázása a reumatológia feladata (RA, arthritis psoriatica, erozív osteoarthritis, arthritis urica, egyéb kristály indukálta synovitis stb.)
4. Panaszok: az érintett ízület(ek), illetve ínhüvely(ek) területének duzzanata, mely fájdalmat és mozgáskorlátozottságot okoz.
5. A betegség leírása
5.1. Érintett szervrendszerek: a csukló és a kéz kisízületek, valamint a nyújtó és a hajlító inakinhüvelyei.
5.2. Genetikai háttér: egyes kiváltó betegségeknél lehetséges.
5.3. Morbiditás: az RA a felnőtt lakosság 1%-át érinti.
5.4. Jellemző nem: az RA nőknél 3x gyakrabban fordul elő, mint a férfiaknál. (B típusú evidencia - 10)
II. Diagnózis
1. Anamnézis: a kiváltó okok miatt változatos.
2. Fizikális vizsgálat: Különböző megbetegedésekben synovitis miatt duzzanatok léphetnek fel a csuklóízületben, illetve a kéz kisízületeiben, valamint tenosynovitis miatt láthatóan (elsősorban) a kézháton, vagy radialisan illetve tenyéri oldalon. Ezen elváltozások elsősorban rheumás betegségekben alakulnak ki.
A korai rheumatoid arthritis diagnózisát a kórtörténet és a fizikális vizsgálat - s nem a laboratóriumi eredmények -alapján kell felállítani. Az utóbbiak legjobb esetben megerősítik a klinikai feltételezést.
3. Kötelező diagnosztikai vizsgálatok
3.1. Laboratóriumi vizsgálatok: egyes esetekben a feltételezett diagnózist megerősíthetik (RA test, se. húgysav, stb.).
3.2. Képalkotó vizsgálatok: Osteografiás felvételek az RA diagnozisát alátámaszthatják és megerősíthetik, differenciáldiagnosztikai szempontból egyéb betegségekre hívhatja fel a figyelmet a kisízületi lokalizáció és radiológiai kép alapján (pl.: EOA, arthtritis psoriatica, köszvény stb.)
További speciális képalkotó eljárásra: MRI, UH, izotóp (háromfázisú csontscan: lágyrész és/vagy csontérintettség kimutatására) vizsgálatra általában rutinszerűen nincs szűkség. (lehetséges fenyegető szövődmények kimutatására: ínszakadás, kollapsus deformitások) (B típusú evidencia - 1,2,3,5,6,)
4. Diagnosztikai algoritmus: 1-2 pontban leírtak.
III. Terápia
III/1. Nem gyógyszeres kezelés
Egyes synovitist kiváltó betegségeknél, pl. köszvény esetében speciális diéta (purin szegény) szükséges. IN/2. Gyógyszeres kezelés
1. Ajánlott gyógyszeres kezelés: A synovitist kiváltó kimutatott kórkép megfelelő gyógyszeres kezelése, pl.RA esetében: NSAID, analgetikum, bázisterápia (reumatológia feladata).
2. Kiegészítő kezelés: Fizióterápia, gyógytorna.
III/3. Műtét
1. A megfelelő egészségügyi ellátás szintje: a konzervatív kezelés elsősorban járóbeteg ellátást igényel, az operatív kezelés ortopéd, kézsebészeti műtői feltételekkel végezhető.
2. Műtéti kezelés elvei
Synovectomiát (Larsen 0-3 stádiumig végezhető [ettől súlyosabb esetekben már arthroplasztika, rész-, vagy teljes arthrodezis jön szóba]) és tenosynovectomiát leggyakrabban RA-ban végzünk, ezért ezen kórképeket taglaljuk részletesen. Egyéb kóreredetek esetén a műtéti kezelés, utókezelés, gondozás hasonló elvek alapján történik 2.1. Műtéti indikáció: 4-6 hónapos eredménytelen konzervatív kezelés.
2.2 Műtéti előkészítés: A kézsebészeti műtéti előkészítés általános szabályainak betartása mellett esetenként speciális előkészítés is szükséges (RA: steroid).
2.3 Műtéti érzéstelenítés: -általános, vagy axilláris anaestesia, esetenként Oberst féle vezetéses érzéstelenítés.
2.4 Műtét: általános feltételek: műtéti terület kipólyázásos vértelensége, kézsebészeti alap műszerkészlet, atraumás varróanyag.
I. Rheumatoid arthritis következtében kialakult kézízületi synovitisek sebészi kezelése (WHO 58051, 58052) (A típusú evidencia - 14,16, B típusú evidencia - 4,8,12)
Csuklóízület esetén a betegség döntően a radiocarpalis ízületben jelentkezik, kisebb mértékben az intercarpalis ízületek is érintettek lehetnek. Gyakran észleljükaz ún. ulnafejsyndromát is. A carpometacarpalis ízületi sorban ritkán jelentkezik ez a kórfolyamat. Az MP, PIP és DIP ízületek synovitise nagyon jellegzetes és a leggyakrabban látott klinikai kép is.
Az MP ízületi sorban a synovitis legtöbbször egyszerre jelentkezik a N-NI-IV-V. ízületekben. A duzzanat, a synovialis folyadék ballotálhatósága, a fájdalom és mozgáskorlátozottság minden ízületben jellegzetes tünet. A PIP ízületek synovitisének következménye a gomblyuk és hattyúnyak deformitás kialakulása valamelyik sugárban. DIP ízületek esetén a duzzanat, illetve a synovialis folyadék megjelenése sokszor nem markáns, és csak az extensor in szakadása által kiváltott végperc flexios helyzet jellegzetes.
Konzervatív kezelés
A betegek az esetek döntő többségében - a kezdeti stádiumban - konzervatív terápiában részesülnek. A terápiát rheumatológus szakorvos indikálja és kíséri nyomon.
Műtéti kezelés Indikáció
Négy-hat hónapja fennálló, illetve ismétlődő és konzervatív therápiára nem gyógyuló kórfolyamat esetén synovectomia indikált, függetlenül attól, hogy a kéz melyik ízületére vagy ízületeire lokalizált a kórfolyamat. (B típusú evidencia -13) Kontraindikáció
- A synovectomia elvégzéséneka legtöbb esetben nincs kontraindikációja. A jellegzetes ízületi synovitis rendszerint a betegség korai fázisában jelentkezik, így cardiovascularis betegség, a légzőszervek betegségei, magas kor, vagy súlyos polyarthritis még nem jelentkezik - mint általános kontraindikációs tényező.
- A sebészi kezelés kontraindikált - vagy csak korlátozott -, ha a beteg nem kooperáló és nem motivált. (B típusú evidencia - 13)
A műtét menete
Az ajánlott bőrmetszés vezetése a csuklóízület dorsalis oldalán hosszanti S alakú, az MP sor felett haránt irányú, a PIP ízületek felett hosszanti ívelt.
Lehetőleg a teljes ízületi belhártya eltávolítására kell törekedni. Ennekazért van nagy jelentősége, mert a visszamaradó synovialis hártya a recidíva matrixa és motorja is egyben.. A synovectomia elvégzése mellett gyakran szükséges az inak centralizációja, leválasztása, áthelyezése, oldalszalag plasztika, stb. elvégzése is. Bőrzárás javasolt 4/0-ás atraumás fonallal végezni, drain(ok) behelyezése után.
Posztoperatív kezelés
Ebben a fázisban, a speciális betegség gyógytornájában már - lehetőleg - járatos szakember közreműködése célszerű. Nem elég csak a műtéti területtel foglalkozni, a szomszédos ízületek mozgatása a műtétet követő napon kezdődik el. Az operált ízület esetén szem előtt kell tartani a fokozatosság elvét: nem szabad fájdalmat okozni. Sorrendiség:
1. műtét utáni első napon innervációs gyakorlatok megkezdése indokolt.
2. 2.naptól óvatos passzív mozgatás
3. 3.-4.naptól úgynevezett aktív mozgatás a gravitáció kikapcsolásával
4. 5.-6.napon majd a gravitációval szemben is
5. 8. naptól az ellenállással szemben végzett aktív gyakorlatok következnek.
MP ízületi sor synovectomia esetén az 5. posztoperatív naptól dinamikus tornáztató készülék használata is javasolt. Utókezelés
12 hétig javasolt három hetes felülvizsgálati intervallumokkal. Ilyenkora funkció ellenőrzésén, valamint a gyógytorna irányításán van a hangsúly, speciális vizsgálatok elvégzésére rendszerint nincs szűkség.
A rheumatoid arthritis következtében kialakult tenosynovitis sebészi kezelése
A. Tenosynovítis a feszítő oldalon
Az ízületekhez hasonlóan már a betegség korai szakaszában jelentkezhet az ínhüvelyek érintettsége is. A folyamat a feszítő oldalon rendszerint szembetűnő, a retinaculum extensorumtól distalisan hirtelen kiemelkedő duzzanat észlelehető, mely a metacarpusok közepéig terjed.
A műtéti kezelés indikációja, technikája (WHO:58332) (A típusú evidencia - 11, B típusú evidencia - 9)
Itt is érvényes alapelv: 4-6 hónapos eredménytelen konzervatív kezelés után műtéti megoldás indikált, de itt a hangsúly erősebb, mint ízületi synovitísben: a háttérben súlyos szövődmény - az inak ruptúrája fenyeget. A műtéti technikánál figyelni kell az inak elemi kollagén rostjai közé besugárzó synoviális hártyára is - ennek eltávolítása subtilis technikát kíván. A metacarpusokon - mint alapon - fekvő involvált synovialis membránt szintén eltávolítjuk, mert a folyamat innen is recidiválhat.
Posztoperatív kezelés Sorrendiség:
1. A műtét után felhelyezett kötésben a csuklóízület 20°-osextenzióban,azMPésPIP ízületek 50°-os flexióban vannak.
2. A második posztoperatív naptól kezdve az ujjbegyeknek ellenállást adva innervációs gyakorlatokat indítunk.
3. A 4. postoperatív napon a kötés eltávolítása után tehermentesített helyzetben vezetett aktív flexió - extensió gyakorlása kezdődik el.
Utókezelés
Nyolc hétig javasolt 2 hetes felülvizsgálati intervallumokkal. A gyógytorna, illetve az elért funkció controllja szükséges, speciális vizsgálatokra rendszerint nincs szükség.
B. Tenosynovitis a hajlító oldalon
Rendszerint az ujjak ínhüvelyeinek területén jelentkezik flexor oldali tenosynovitis. Ilyenkor azonnal funkciózavar lép fel csúszászavarokkal illetve előfordulhat az ujjak akadása is, "pattanó ujj" -digitus-saltans syndroma. A diagnózist egyszerű fizikális vizsgálat is biztosíthatja, az alapbetegséget illetően utalunk az előzőekben felvázolt eljárásra. Eredménytelen konzervatív kezelés esetén műtétet indikálunk. (A típusú evidencia -15)
Műtéti technika
Tenosynovitis esetén cikk-cakk metszésből feltárjuk a területet a tenyértől a DIP ízületig és radikális tenosynovectomiát végzünk. A húrjelenség elkerülésére az ínhüvely 1-1 gyűrűjét megkíméljük. Digitus saltans -syndroma esetén az A1 inhüvelyt hasítjuk be ulnarisan.
Posztoperatív kezelés
(8 napig gipszsín rögzítés szükséges, de a 3. naptól kezdve a) Korai torna megkezdése javasolt. (úgy, hogy erre az időre a végtagot kiemeljük a rögzítő gipszsínből.)
Utókezelés
(12) 4-6 hétig javasolt, két hetes felülvizsgálati intervallumokkal: a gyógytorna, illetve az elért funkció kontrollja szükséges.
C. Tenosynovitis a radialis oldalon: De Quervain-syndroma
A musculus abductor pollicis longus és a musculus extensor pollicis brevis ina az első dorsalis extensor csatornában közös inhüvelyben fut. Amennyiben tenosynovitis következményeként térszűkítő folyamat alakul ki de Quervain syndrómáról beszélünk. A diagnózist egyszerű fizikális vizsgálat is biztosíthatja, a processus styloideus radii területén nyomásérzékenység alakul ki. A hüvelykujj fixálásával egyidőben a kéz ulnarductióba hozva a processus styloideus radii fölött nagy fájdalom jelentkezik (Finkelstein-teszt). Eredménytelen konzervatív kezelés esetén műtétet indikálunk.
Műtéti technika
A közös inhüvely hosszanti felhasítása és az inak szabaddá tétele.
Posztoperatív kezelés
Korai torna megkezdése javasolt.
Utókezelés
Korai gyógytorna, jegelés.
IV.-V. Rehabilitáció, Gondozás
1. Rehabilitáció és rendszeres ellenőrzés
Az alapgondozás a reumatológia feladata, azzal a megkötéssel, hogy adott, választott időben elvégzett műtét(ek) az orvosi rehabilitáció igen fontos láncszemétjelentik. (C típusú evidencia - 7)
2. Megelőzés
Fontos szempont a helyes diagnózis gyors felállítása, annak megfelelő kezelése, így ezzel a súlyos kézízület deformítások megelőzése.
3. Lehetséges szövődmények
Sebgyógyulási zavar. ízületi mozgáspálya beszükülése (korai gyógytorna!)
4. Szövődmények kezelése
Sebrevízió, sebátmosás, drainálás a gyógyszeres kezelés mellett.
5. Kezelés várható időtartama / Prognózis Lásd az utókezelési részeknél.
6. Az ellátás megfelelőségének indikátora
A műtött beteg speciális mozgásszervi státuszának a rögzítése biztosítja az állapotváltozás prospektív nyomonkövetését. (fájdalom mértékének változása, mentessége, mozgástartomány, kézfunkció változása)
VI. Irodalomjegyzék
1. Gömör Béla (szerk.): Reumatológia. Medicina Könyvkiadó Rt. 2001.
2. Vízkeleti Tibor (szerk.): Az Ortopédia tankönyve. Semmelweis Kiadó. Budapest, 1999.
3. Udvarhelyi Iván (szerk.): Fejezetek a felnőttkori ortopédia gyakorlatából Medicina Könyvkiadó RT. Budapest, 1998
4. Szendrői Miklós (szerk.): Ortopédia. Semmelweis Kiadó 2006.
Kapcsolódó internetes oldal www.ortopedtarsasag.hu
Evidencia meghatározásnál felhasznált irodalom
1. McQeen F, Ostergaard M, Peterfy C.: Pitfalls in scoring MR images of rheumatoid arthriti wrist and metacarpophalangeal joints. Ann Rheum Dis. 2005 febr, 64 Suppl 1:148-55.
2. Gibbon WW.: Application of ultrasound in arthritis. Semi Musculoskelet Radol. 2004 Dec, 8 (4) :313-28.
3. Teefey SA, Middleton WD, Patel V, Hildebolt CF, Boyer MI.: The accuracy of high-resolution ultrasound for evaluating focal lesions of the hand and wrist. J Hand Surg (Am). 2004 May, 29(3):393-9.
4. King JA,Tomaino MM.: Surgical treatment of the rheumatoid thumb. Hand Clin. 2001 May, 17 (2):275-89.
5. Rasmussen OS.: Sonography of tendons. Scand J Med Sci Sports.2000 Dec, 10(6):360-4.
6. Terslev L, Torp-Pedersen S, Savnik A, von der Recke P.:Doppler ultrasound and magnetic resonance imaging of synovial inflammation of the hand in rheumatoid arthritis: a comparative study. Arthritis Rheum. 2003 Sep, 48(9):434-41.
7. Alderman AK, Ubel PA, Kim HM, Fox DA, Chung KC.: Surgical management of the rheumatoid hand: consensus and controversy among rheumatologist and hand surgeons. J Rheumatol. 2003 Jul, 30 (7):1464-72.
8. AllendeC, Le Viet D.: Extensor carpi ulnaris problems at the Wrist-classification, Surgical Treatment and Results. J Hand Surgery. 2005 Jun 30 (3):265-272.
9. Richards RA, Wilson RL.: Management of extensor tendons and the distal radioulnar joint in rheumatoid arhritis. J of American Society for Surgery of the Hand. 2003 Aug 3 (3):132-144.
10. Palmer KT.:Pain in the forearm, wrist and hand. Best Practice and Research Clinical Rheumatology. 2003 Febr 17 (1):113-135.
11. Howard LD.:Surgical treatment of rheumatic tenosynovitis. Am. J Surg. 1955.89:1163-1168.
12. Jakubowski S, Pongowska J.: Indikationen zur Synovectomie bei PCP. Orthop.1973. 2:6-11.
13. Vainio K.: Indications and contraindications for surgery in rheumatoid arthritis. Rheumatism. 1966.22:10-21.
14. Cordes U, Koob E, Wessels D.:Die operative Synovectomie der Fingergelenke -ein unverzicht-bares Therapieverfahren in der Rheumachirurgie, wie Langzeit-Nachuntersuchungsergebnisse beweisen. Orthop. Praxis 1990.1:11-16.
15. Gray R, Gottlieb N.: Handflexortenosynovitis in rheumatoid arthritis. Arthritis Rheum. 1977. 20:1003-1012.
16. Gschwend N.: Late results of synovectomy of wrist, MP and PIP joints. Multicenter study. Clin. Rheumatol. 1985. 4:23-52.
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Érintett társszakmák
Reumatológia, illetve reumasebészetben járatos kézsebész, Fizioterápia - Gyógytorna. Evidencia besorolás
A bizonyítékok szintjei
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Meniscus sérülés ellátásáról
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium Szinonimák:
A térdízület félhold alakú porcának szakadása, Porcsérülés, Porcszakadás
I. Alapvető megfontolások
1. A protokoll alkalmazási, érvényességi területe
- Ortopédia, traumatológia, sportsebészet (mozgásszervi sebészettel foglalkozók)
- Reumatológia
- Radiológia
2. A protokoll bevezetésének alapfeltétele
- A betegség diagnosztikájának és terápiájának egységes szemlélete a mozgásszervi betegségekkel foglalkozó szakmákban.
- A meniscus sérült betegek szakmai kompetenciák értelmében végzett gyógyító-megelőző ellátása.
3. Definíció
- A térdízület külső vagy belső oldali félhold alakú porcának szakadása. Lehet traumás (akut) vagy degeneratív eredetű.
3.1. Kiváltó tényezők
- Traumás: A térdízületet érő hirtelen, indirekt erőhatás.
- Leggyakrabban: rotáció
- Degeneratív: A térdízület tartós túlterhelése, ismétlődő mikrotraumák.
- Leggyakrabban: sport, fizikai munka.
3.2. Kockázati tényezők
- Krónikus térdízületi instabilitás
- Alsó végtagi tengely deformitások
- Túlsúly
- Térdízületi artrózis
- Discoid meniscus
4. Panaszok, tünetek, általános jellemzők:
- Típusos panaszok:
- fájdalom, jellemzően az ízületi résben (mediális vagy laterális)
- kattanás,
- ízületi elakadásérzés,
- ízületi kimozdulásérzés
- Típusos tünetek:
- ízületi rés érzékenysége,
- mozgáskorlátozottság, elakadás (ízületi blokk)
- kattanás, roppanás
- elmozduló terime
- duzzanat
- Általános jellemzők:
5. A betegség leírása
A térd külső és belső oldalán elhelyezkedő meniscusok fontos szerepet játszanak a térd működésében. E képletek funkciói:
- A comb- és a sípcsont közötti alaki különbség mérséklése (illeszkedésjavítás, térkitöltés)
- Az ízületi felszínek közötti nyomás egyenletesebb elosztása (felületnövelés)
- Az ízületi felszíneket érő mechanikai sokk elnyelése, mérséklése (erőelnyelés, erőtranszformálás)
- a szinoviális folyadék áramlásának segítése (áramlásszabályozás)
- a térd stabilizálása (stabilizálás, fékezés)
- proprioceptív funkció
A meniscusok szakadása akut illetve krónikus megterhelés hatására alakul ki. (I./3.1.)
Akut (traumás) szakadás főleg fiatalokon, leggyakrabban sportolókon jön létre. Férfiak körében gyakoribb.
A degeneratív szakadás általában idősebb korban, tartós megterhelésre fokozatosan alakul ki.
A mediális meniscus degeneratív szakadása is gyakoribb férfiakon.
A szakadás kialakulhat a meniscus vérellátással rendelkező, illetve a vérellátással nem rendelkező zónájában.
A szakadás kialakulhat nagy erőbehatásra ép, vagy viszonylag kis erőbehatásra degenerált állományú meniscuson. A szakadás lehet lebenyes, vagy radier-, horizontális-, vertikális irányú.
Tekintettel a meniscusokszámos funkciójára szakadásuk esetén a meniscus megtartására illetve a minél takarékosabb reszekcióra kell törekedni. (5,-B, 7-B,9-C evidencia szint)
Refixáció elsősorban a 4 cm-nél rövidebb, egyébként ép állományú, a vascularis zónában létrejött meniscus szakadás esetén indokolt.
5.1. Érintett szervrendszer: Térdízület.
5.2. Genetikai háttér: Nem ismert.
5.3. Incidencia - prevalencia - morbiditás - mortalitás: Pontosan nem ismert
5.4. Jellemző életkor:
- Traumás: fiatal felnőttkor (18-25 év)
- Degeneratív: 30-50 év
5.5. Jellemző nem: Férfiaknál gyakoribb.
II. Diagnózis
1. Anamnézis:
Általános (mint minden betegségnél)
- fontos kérdések: korábbi vagy fennálló ízületi betegségek, anyagcsere betegségek, végtagi keringési betegségek Speciális
- korábbi térdízületi sérülés vagy betegség, korábbi térdízületi panaszok, kezelések, műtétek (lásd még I./3.2. pont)
- a jelenlegi sérülés vagy a panaszok (I./4. pont) kialakulásának pontos körülményei (mechanizmusa) és sorrendje, a panaszok pontos lokalizációja
2. Fizikális vizsgálat: (2,-D 11,-C evidencia szint)
Az alábbi vizsgálatokat mindkét térdízületen el kell végezni. A két oldalon észlelt tünetek és vizsgálati lelet összehasonlításából következtethetünk a kóros elváltozásokra.
Megtekintés
- Álló és fekvő helyzetben, valamint aktív mozgás közben
- Fontos látható tünetek: tengely deformitások, diffúz ízületi duzzanat vagy látható körülírt cysta, combizom hipotrófia
- Artrótikus deformitás, a patella helyzeti és mozgási rendellenességei, korábbi beavatkozások hegei
- Akut sérülés esetén: traumás bőrelváltozások, bevérzések Tapintás
- A nyomásérzékenység vizsgálata, pontos lokalizációja
- Körülírt képletek tapintása (meniscus-lebeny, cysta, szabadtest, perem-osteophyta, synovialis plica)
- A patella ballotálhatóságának vizsgálata (az ízületi folyadékgyülem mennyiségének meghatározására) Duzzanat, izületi folyadékgyülem esetén körfogat mérés ugyanazon magasságban mindkét oldalon, a mérés magasságának és eredményének írásban történő rögzítése cm-ben a későbbi változás megítélésére.
- A patella helyzetének, mozgásának és mobilitásának vizsgálata Mozgásvizsgálat
- A térd aktív és passzív mozgásterjedelmének vizsgálata, meghatározása fokokban, az eredmény írásbeli dokumentálása.
- A passzív mozgás-végpont minőségének vizsgálata (rugalmas, kemény)
- Helyi érzéstelenítéssel kiegészíthető a mozgásvizsgálat az oldalszalag-sérülés elkülönítésére
- Crepitatio vizsgálata mozgás közben az egyidejűleg fennálló ízfelszíni porckárosodás megítélésére.
Stabilitás vizsgálat
- A térdízület anteroposterior és oldalirányú stabilitásának vizsgálata akut vagy krónikus szalagsérülés megállapítására, elkülönítésére. (Lachman-teszt, elülső és hátsó asztalfiók tünet, varus-valgus stressz-teszt, aktív quadriceps-teszt, pivot shift-teszt)
Kétes esetekben, amennyiben a feltételek adottak
- objektív stabilitás vizsgálat (arthrometria)
- érzéstelenítésben végzett stabilitás vizsgálat (akut sérülés esetén) Speciális tesztek (a meniscus szakadásának diagnosztizálására)
- A mediális meniscus szakadására utaló tünetek és tesztek:
- a mediális ízületi résben a meniscus bázisának direkt nyomásérzékenysége
- a lábszár kirotációjára, varizálására a mediális ízületi résben jelentkező fájdalom, kattanás
- tapintható mozgó terime a mediális izületi résben
- cysta a mediális izületi résben (meniscus szakadáshoz társuló meniscus cysta esetén)
- A laterális meniscus szakadására utaló tünetek és tesztek:
- a laterális ízületi résben a meniscus bázisának direkt nyomásérzékenysége
- a lábszár berotálására, valgizálására a laterális ízületi résben jelentkező fájdalom, kattanás
- tapintható mozgó terime a laterális izületi résben
- cysta a laterális izületi résben (meniscus szakadáshoz társuló meniscus cysta esetén)
3. Kötelező diagnosztikai vizsgálatok:
3.1. Laboratóriumi vizsgálatok:
- Nincs specifikus laborvizsgálat a meniscus sérülés kimutatásához.
- Differenciál diagnosztikai szerepe lehet nem tisztázott ízületi duzzanat és/vagy fájdalom esetén.
3.2. Képalkotó vizsgálatok:
- Röntgenfelvétel
- Annak ellenére, hogy a meniscus szakadásának direkt radiológiai jele nincs az anteroposterior és az oldalirányú natív felvétel meniscus sérülés gyanúja esetén elvégzendő a hasonló klinikai tüneteket okozó intraartikuláris (ízületbe hatoló törés, osteochondritis, ízületi szabadtest, artrózis) és/vagy extraartikuláris (Stieda-Pellegrini árnyék, csont tumorok és tumorszerű elváltozások) eltérések megítélésére
- Esetenként axiális patella felvétel, alagút felvétel, terheléses felvétel is szóba jön
- Mágneses rezonancia vizsgálat (6-B evidencia szint)
- Rutinszerűen nem szükséges.
- Bizonytalan tünetek, nem egyértelmű fizikális vizsgálati lelet esetén indokolt. (Figyelembe kell azonban venni, hogy az MRI hiperszenzitíva meniscus elváltozások megítélésében. Az MRI felvételen szakadtnak vagy degeneráltnak látszó esetek egy részében műtétkor a meniscusok mind megtekintéssel, mind tapintással épek lehetnek.)
- Ultrahang vizsgálat (3,-C,6-B evidencia szint)
- Csak a meniscus cystával együtt előforduló degenerált meniscus szakadás gyanúja esetén jön szóba megfelelő teljesítményű készülék és gyakorlott vizsgáló esetén, mivel találati pontossága egyébként alacsony
- Artroszkópia
- Kétes esetekben diagnosztikus artroszkópia indokolt, mely beavatkozás lehetőséget biztosít a meniscus sérülésének ellátására is.
3.3. Egyéb: Egyéb vizsgálat általában nem szükséges
4. Kiegészítő diagnosztikai vizsgálatok: Általában nem szükséges.
5. Differenciál diagnosztika: (2,-B, 4-D,10-C evidencia szint )
- Intraartikuláris elváltozások
- porcfelszín károsodás (chondromalacia) a terhelő felszíneken vagy a patellán
- ízületi szabadtest
- plica synovialis (mediopatellaris, laterális, egyéb)
- a synovialis hártya egyéb elváltozásai (synovioma, stb.)
- a csontok elváltozásai (osteochondralis törés, tumor)
- elülső keresztszalag szakadás, ízületi tok sérülése, oldalszalagok sérülése
- artrózis
- Extraartikuláris elváltozások
- Véna saphena magna phlebitis
- Nervus saphenus szindróma
- Térd körüli tendinitisek és insertiopathiák (flexor tendinitis, ugrótérd szindróma)
- Iliotibiális szalag szindróma
- Szisztémás betegségek (amelyek ízületi fájdalommal és/vagy duzzanattal járnak)
- Krónikus nem specifikus synovitisek
- Reaktív synovitisek
- Anyagcsere betegségek
6. Diagnosztikai algoritmusok
- A meniscus sérülés az anamnézis és a fizikális vizsgálat alapján az esetek többségében diagnosztizálható. Röntgenfelvétel ilyen eseteknél is kötelező.
- Az adekvát konzervatív kezelés ellenére fennálló, bizonytalan, meniscus szakadásra utaló térdpanaszok, és nem egyértelmű fizikális vizsgálati lelet esetén MR vizsgálat végzése javasolt.
- Adekvát konzervatív kezelés ellenére fennálló panaszok és negatív vagy nem egyértelműen pozitív MRI eredmény esetén kétséges esetekben diagnosztikus artroszkópia végzése indokolt.
III. Terápia
A meniscus szakadás kezelése alapvetően műtéti: a szakadt rész refixációja vagy eltávolítása. Konzervatív kezelés csak a beteg rossz általános állapota, műtétet elutasító magatartása, kooperációs hiánya, a szervezetében lévő gyulladásos tünetek esetén jön szóba. III/1. Nem gyógyszeres kezelés:
- Akut tünetek esetén: térd kímélet, jegelés
- Erős fájdalom esetén az izület rögzítése (rugalmas pólya, brace, gipsz) III/2. Gyógyszeres kezelés:
- Erős fájdalom esetén fájdalomcsillapítók adása III/3. Műtét: (7-B,8-B evidencia szint)
Mivel a minimál invazív technikával, artroszkóp segítségével végzett műtét során sokkal kisebb szöveti károsodás mellett a beavatkozás precízebben, gyorsabban elvégezhető, a nyílt feltárásos műtét csak igen ritkán jön szóba. A műtét történhet kórházi bennfekvés alatt, illetve "egynapos" sebészeti beavatkozásként.
1. A megfelelő egészségügyi ellátás szintje:
- Artroszkópos felszereléssel és jártassággal rendelkező ortopéd sebészeti osztály vagy traumatológiai osztály.
A meniscus sérülések reszekciója csaknem minden esetben artroszkóp segítségével elvégezhető. A visszavarrásra alkalmas esetekben a szakadt rész refixációjához speciális eszközökre és az átlagosnál nagyobb artroszkópos jártasságra van szükség. A meniscus sérülések ellátására emiatt artroszkóppal és megfelelő artroszkópos sebészi jártassággal rendelkező ortopéd és baleseti sebészeti osztályokon kerülhet sor.
2. Általános intézkedések:
- Szokásos műtét előtti kivizsgálás lehetőség szerint ambulanter. 3.Speciális ápolási teendők:
- Nincs
Sebészi kezelés:
4.1. Műtéti indikáció:
- a meniscus szakadására utaló típusos tünetek: beakadt térd, rendszeresen ismétlődő ízületi blokk, ízületi résben jelentkező fájdalom, duzzanat
- fizikális vizsgálat során tapintható (elmozduló) meniscus-lebeny, ízületi rés nyomásérzékenység, pozitív meniscus tesztek, ízületi mozgás beszűkülés
- konzervatív kezelésre nem reagáló ízületi fájdalom, bizonytalan meniscus tesztek, a fájdalmat magyarázó egyéb elváltozás hiánya, pozitív MRI lelet
- WHO 58040, 58041, 58042, 58043, 58044 Műtéti kontraindikáció
- a térdízület lágyrészeinek és/vagy csontjainak gyulladásos megbetegedése
- a szervezetben zajló bármilyen gyulladásos elváltozás
- a beteg rossz általános állapota (kardiális dekompenzáció, szepszis, trombózis stb.)
- meniscus reszekció ellenjavallt:fiatal beteg visszavarrásra alkalmas meniscus szakadása,amennyiben a refixációhoz a személyi és tárgyi feltételek adottak, vagy rövid időn belül - akár más intézetben - megteremthetők
- kooperáció hiánya a beteg részéről
4.2. Műtéti előkészítés:
- Az artroszkópos műtéteknél szokásos előkészítés.
- A beteg felvilágosítása, írásos beleegyező nyilatkozat.
4.3. Műtéti érzéstelenítés:
- A műtét történhet narkózisban, gerincvelői-, vezetéses-, vagy válogatott esetekben lokális érzéstelenítésben.
4.4. Műtét:
- A műtét történhet vértelenítésben vagy vértelenítés nélkül.
- A beteg fektetése háton, nyújtott vagy lógatott alsó végtag mellett, történik
- A végtag antiszeptikus lemosása, izolálása a szakma szabályai szerint történik.
- Standard behatolási kapuk alkalmazása mellett diagnosztikus artroszkópiát végzünk a szakma szabályainak megfelelően.
- Meniscus szakadás esetén a meniscus szakadt, károsodott centrális részét artroszkópos vágóeszközzel (olló, kés, shaver, elektromos tapintó-vágó horog, lézer, vaporizátor stb.) takarékosan, lépcsőmentesen, ív alakban úgy kell eltávolítani, hogy minél több ép perifériás rész maradjon meg, és a reszekció során az ízfelszíni porc ne károsodjon.
- Discoid meniscus szakadása esetén a szakadt részt úgy kell eltávolítani, hogy a megmaradt meniscus félhold alakú legyen, és ez mozgáskor ne csípődjön az ízfelszínek közé.
- Amennyiben a szakadás kiterjedése, elhelyezkedése, a meniscus állaga, a beteg életkora lehetővé teszi a meniscus megtartását, valamint ehhez a személyi és tárgyi feltételek adottak, a meniscus refixációját el kell végezni.
- Ha a meniscus ruptúrájához más sérülés (szalagszakadás, porcsérülés) is társul, akkor ezeket a szakma szabályai szerint egy-, vagy külön ülésben kell ellátni.
- Artroszkópos meniscus reszekció után az ízület drenálása egyéni elbírálást igényel. A behatolási portálok sebszéleit varrattal vagy a sebszéleket összefektető ragasztócsíkokkal egyesítjük. Kis behatolási seb esetén a fedőkötés is elegendő.
- A seb steril fedése, nyomókötés felhelyezése.
4.5. Posztoperatív teendők:
- Posztoperatív megfigyelés, fájdalomcsillapítás.
- Az operált végtag felpolcolása, a térd jegelése, az ízület aktív tornáztatása.
- Az egyébként egészséges térdű betegek a lokális anesztéziában végzett izolált artroszkópos meniscus reszekció után a műtött végtagjukat azonnal, a gerincvelői érzéstelenítés után a végtag izomerejének visszatérte, a narkózisban végzett műtét után a stabil járóképesség visszanyerése után terhelhetik.
- A műtét után a drént 6-24 órával, a varratokat 5-10 nap elteltével kell eltávolítani.
- Trombózis profilaxis: rugalmas pólyázás lábujjtól térd fölé folytonosan, aktív vénás torna, korai mobilizálás. Gyógyszeres profilaxis rutinszerűen nem indokolt.
A rizikó csoportba tartozó betegek esetén a gyógyszeres profilaxist egyéni elbírálás alapján kell alkalmazni.
5. Fizikai aktivitás:
Műtét utáni 2. napon a természetes életmód nem korlátozott, de térdkímélet indokolt.
6. Diéta:
Nincs speciális diéta.
7. Betegoktatás:
- Általános tanácsadás a térdízület terhelhetőségére vonatkozóan minden esetben szükséges.
- Speciális tanácsadás indokolt magas szintű sporttevékenység és nehéz fizikai munka illetve társsérülések ellátása esetén.
IV. Rehabilitáció
Meniscus reszekció után speciális utókezelésre általában nincs szükség. Csak kifejezett izomsorvadással járó esetekben jön szóba fizikoterápia, gyógytorna.
Magas szintű sporttevékenység folytatásához intenzív gyógytorna és sportrehabilitáció szükséges.
V. Gondozás
1. Rendszeres ellenőrzés
Szövődménymentes esetben kontroll vizsgálat általában egy, ritkán több alkalommal szükséges. Az első kontroll ideje a varratszedés időpontja.
2. Megelőzés
A meniscus sérülés primer prevenciójának tekinthető a fontos rizikótényezők megszűntetése (I./3.2. pont). Legfontosabb ezek közül a krónikus térdízületi instabilitás műtéti kezelése.
3. Lehetséges szövődmények: (1-B evidencia szint )
- ideg-, érsérülések
- sebgennyedés
- kompartment szindróma
- izomatrófia
- trombózis
- synovitis
3.1. A szövődmények kezelése
Megfelelő műtéti technika, gyakorlottság mellett az ideg,érsérülések,a sebgennyedés,a kompartment szindróma, az izomatrófia előfordulása igen ritka. E szövődményeket a szakma szabályai szerint kell ellátni.
4. Kezelés várható időtartama / prognózis:
- A kezelés várható időtartama
- Az egyébként egészséges térdű, izolált meniscus reszekción átesett betegek az átlagos, hétköznapi aktivitást, a műtétet követő 1-4. héten, a nehéz fizikai munkát, a sportolást a 3-6. posztoperatív héten kezdhetik el fokozatosan.
- Társsérüléssel (szalagszakadás, porckárosodás) járó esetekben a posztoperatív kezelés, a munkába, sportba való visszaállás időpontja a társsérüléstől függően a fenti protokolltól eltér.
- Prognózis
- Az izolált meniscus reszekció után ritkán, a szubtotális és a totális meniscus eltávolítást követően szinte mindig artrózis kialakulására kell számítani.
- Rosszabb az artrózis prognózisa a túlsúlyos, a fizikai munkát végző illetve a nagy megterhelést jelentő sportot űző betegek esetében.
- Súlyosabb fokú a postmeniscectomiás artrózis a szalag- és porcfelszín-sérüléssel szövődött meniscus szakadások esetében.
5. Az ellátás megfelelőségének indikátorai (szakmai munka eredményességének mutatói)
1. A szövődmények gyakorisága
2. A táppénzes idő tartama
3. A refixáció eseten a sikeres esetek aránya
6. Dokumentáció, bizonylat
- Járóbeteg szakellátásban: ambuláns lap, kezelő lap,
- Képalkotó vizsgálatok képi és szöveges leletei, foto dokumentáció, vagy adathordozón archivált (hajlékony lemez, CD, DVD ) dokumentáció
- Fekvőbeteg szakellátásban: kórlap, műtéti beleegyezés, műtéti leírás, (opcionálisan foto, video, vagy computeres dokumentáció) decursus, zárójelentés.
VI. Irodalomjegyzék
1. Austin KS: Complications of arthroscopic meniscal repair. Am J Sports Med, 1993.21 (6): 846-48.
2. Az ortopédia tankönyve. (Szerk: Vízkelety) Alliter Kiadói és Oktatásfejlesztő Alapítvány, Bp. 2002.
3. Azzoni R,Cabitza P. Is there a role for sonography in the diagnosis of tears of the knee menisci? J Clin Ultrasound 2002; 30: 472-6.
4. Berkes I.: Sportsebészet. In: Jákó P.(szerk): A sportorvoslás alapjai. 1998. Bp. OSE1117-265.
5. DeHaven KE. Meniscus repair. Am J Sports Med 1999; 27: 242-250.
6. De Maeseneer M, Lenchik L, Starok M, Pedowitz R, Trudell D, Resnick D.
Normal and abnormal medial meniscocapsular structures: MR imaging and sonography in cadavers. AJR Am J Roentgenol. 1998; 171 (4): 969-76.
7. Howell JR, Handoll HH Surgical treatment of the knee in adults. Cochrane Database Syst Rev 2000; 2:1353.
8. Newman AP: Principles and Decision Making in Meniscal Surgery Arthroscopy, 1993. 9 (1): 33-51.
9. Rockborn P, MessnerK. Long-term results of meniscus repair and meniscectomy: a 13-year functional and radiographic follow-up study. Knee Surg Sports Traumatol Arthrosc 2000; 8:2-9.
10. Reumatológia. (Szerk: Gömör) Medicina, Bp. 2001.
11. Scholten RJ, Deville WL, Opstelten W, Bijl D, van der Plas CG, Bouter LM. The accuracy of physical diagnostic tests for assessing meniscal lesions of the knee: a meta-analysis. J Fam Pract. 2001; 50 (11): 938-44.
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Érintett társszakmákkal való konszenzus: Traumatológia, sportorvostan, radiológia
2. Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Perthes-kórról
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
Szinonimák: Osteochondritis capitis femoris juvenilis Legg-Calvé-Perthes betegség BNO: M9120
I. Alapvető megfontolások
1. A protokoll alkalmazási/érvényességi területe Gyermekortopédiai ellátás.
2. A protokollok bevezetésének alapfeltétele Gyermekortopédiai klinikumok, klinikai centrumok.
3. Definíció
A proximalis femur epiphysis elhalása gyermekkorban, mely a combfejdeformálódásához vezethet.
3.1. Kiváltó tényezők:
A combcsont proximális epiphysisének vérellátást gátló tényezők (trauma, felsőlégúti hurutot vagy egyéb gyermekkori lázas betegséget követő következményes immun-synovitis) vezetheti be.
Mint a juvenilis osteochondrosis csoport csípőizületet érintő tagja ismeretlen okból is létrejöhet, az esetek jelentős részében.
Herediter thrombophiliák szerepe mindmáig ellentmondásos. (C típusú evidencia, 4)
3.2. Kockázati tényezők:
A gyermekkorban lezajló, többnyire egyoldali, felsőlégúti hurutot követő transitoricus coxitis. A transitoricus coxitis gyógyulása után is 3 hónapig observatio szükséges, mivel a Perthes betegség kb. 15 %-ában a korábban lezajlott transitoricus coxitis, mint kóroki tényező szerepel.
4. Panaszok (tünetek), általános jellemzők
Legjellemzőbb a hetek vagy hónapok óta fennálló, intermittáló furcsa járás vagy sántítás. Az esetek egy részében a gyermek nem is panaszkodik fájdalomról. A sántítás és a furcsa járás a kezdeti időszakban pihenésre átmenetileg megszűnik. Emiatt néha hetek, vagy hónapok telnekel, amíg a gyermekorvoshoz kerül. Jellemző, hogy a gyermek nem a csípőizületben, hanem a combban, ill. a térdben jelzi a fájdalmat (nervus obtoratorius miatt). Ezért általános szabály, hogy gyermekkori térdfájdalom esetén a csípőizületeket is gondosan meg kell vizsgálni. Ritkábban akut csípőizületi fájdalommal hozzák a gyermeket, esetleg nem is tud rálépni az alsó végtagra. Ezen esetekben a primérvagy secunder synovitis uralja a klinikai képet. A panaszoknak akkor is jelentőséget kell tulajdonítani, ha a vizsgálat során semmi értékelhető klinikai eltérést nem találunk, mivel az intermittáló jelleg miatt a vizsgálat történhet panaszmentes időszakban. Negatív status esetén is ezért célszerű pár hét múlva kontroll vizsgálatra visszakérni a gyermeket.
5. A betegség leírása
5.1. Érintett szervrendszer:
A gyermekkori, még fejlődésben lévő femur proximális epiphysise.
5.2. Genetikai háttér: Genetikai ok nem mutatható ki.
5.3. Incidencia/prevalencia/Morbiditás/Mortalitás Magyarországon:
A mérsékelt égöv betegsége, mind az északi, mind a déli féltekén. A kiegyensúlyozottabb éghajlattal rendelkező hideg égövben, valamint a meleg égövben nem fordul elő. Hazai gyakorisága 1%-ra tehető, a második leggyakoribb gyermekkori csípőizületi betegség.
5.4. Jellemző életkor:
3-13 éves kor között fordul elő.
5.5. Jellemző nem:
Fiúknál 3-szor gyakoribb, mint lányoknál.
II. Diagnózis
1. Diagnosztikai algoritmusok
- anamnézis,
- fizikális vizsgálat,
- radiológiai vizsgálat: ap. és Lauenstein összehasonlító csípőizületi felvétel.
2. Anamnézis
A szülő elmondása szerint a gyermeksántít, néha csak intermittáló jelleggel; azonban az esetek egy részében a sántítás mellett csípőizületi, comb- és térdfájdalmakról panaszkodik.
3. Fizikális vizsgálatok
Járásvizsgálatkor a gyermek kisfokú kímélő jellegű sántítása látható az érintett, panaszolt oldalon. Hanyatt fekvő helyzetben a csípőízületek összehasonlító mozgásvizsgálatát végezzük el. Nyújtott csípőkés térdek mellett a lábakat megfogva, csípőizületi összehasonlító berotatiót próbálunk előidézni, melynek során az érintett oldalon kevésbé rotálható befelé irányba a csípőízület. Ilyenkora lábak befelé fordulását, ill. a térdizületek, térdkalács befelé fordulását vizsgáljuk, összehasonlító formában. Jellemző lehet még a kisfokú extensiós és abductiós mozgáskorlátozottság. Az extensio kiesését (flexios contractura) az ellenoldali csípőizület teljes flexioja során figyeljük, ilyenkor az érintett, azaz ellenoldali comb a vizsgálóasztaltól kissé elemelkedik. Az abductio vizsgálata történhet nyújtott csípők és térdek mellett, összehasonlítva; vagy 90 fokig hajlított csípőhelyzetben végezve az abductiot, szintén összehasonlítva (Lorenz-abductio). Előrehaladott, ill. elhanyagolt esetben a comb, a far izomzata atrophiás lehet, továbbá kisfokú végtagrövidülés mérhető. A végtagrövidülésnél a spina iliaca anterior superior és belbokák közötti összehasonlító távolságot mérjük le centiméterrel.
A hosszkülönbséget részben a valódi csontos megrövidülés, részben az izületi zsugorodások okozzák.
4. Kötelező (minimálisan elvégzendő) diagnosztikai vizsgálatok: (B típusú evidencia, 5-10,12,16)
4.1. Laboratóriumi vizsgálatok:
Megelőzően, 1-2 héten belül lezajlott felsőlégúti hurut vagy torokgyulladás
okozhat kissé emelkedett vörösvérsejt-süllyedést és a vérkép balratolódását. A Perthes betegségnél nem jellemző a laboratóriumi elérés.
4.2. Képalkotó vizsgálatok:
Perthes betegség gyanúja esetén összehasonlító ap. és Lauenstein csípőfelvételek készítése szükséges. Gyakran az ap. felvételen nem találunk érdemi eltérést. Kezdődő esetekben a proximális epiphysis magassága csökkenhet, scleroticussá, esetleg fragmentálttá válhat. Mindez sokkal jobban látható a Lauenstein felvételen, mivel partialis Perthes betegségnél, a proximális epiphysis elülső részét érintő folyamat esetén Lauenstein felvételen jobban vizualizálható azepiphysis strukturális zavara, a mögötte elhelyezkedő posterior,ép rész ilyenkor különállóan vetül. A röntgenfelvételen látható elváltozások döntően meghatározzák a betegség végeredményét, mivel számos
rizikófaktor jelenléte dokumentálható: - a combfej érintettségének nagysága: 25, 50, 75 és 100 %-os érintettség a progresszív esetek fokozatait mutatják, A subchondralis fissura kiterjedését károsodás nagyságával hozzák összefüggésbe. (12)
Epiphysis acetabulumból történő lateralis kiboltosulása, A 3 pillér elméletet ismertetve a lateralis pillér érintettsége mindig rosszabb prognózisra utal, a medialis érintettsége szinte mindig a jóindulatúság jele - magyarul nem mindegy hogy az a 25% hol van.
Nemcsak az epiphysisre, hanem a metaphysisre is terjedő folyamat rosszabb kezelési végeredményeket jelent.
A korai radiológiai jelek és a késői eredmény összevetésére több gyakorlatban használatos elmélet is megtalálható. Úttörő munkát végzett Catteral. (16) Napjainkban a Herring-féle osztályozás is teret nyer, mely segítséget nyújt a prognózis és terápiás döntés mérlegelésekor is.
4.3. Egyéb vizsgálatok közül (B típusú evidencia, 26-28.)
Kétséges esetekben a csontizületi scintigraphia lehet mérvadó, a Perthes betegség korai stádiumában radiológiailag még nem látunk eltérést, ugyanakkor a combfej keringésének részleges vagy teljes megszűnése nagyon jól látható perfúziós zavar formájában a csontizületi scintigraphián.
A csípőizületi szonográfia az izületi tokon belüli folyadék mennyiségéről, és a porcos fej egyenetlenségeiről szolgálhat információval.
Az MRI vizsgálattal korán kimutatható a combcsont fej vérellátásának kiesése, annak kiterjedése. (26.27.28.)
5. Kiegészítő diagnosztikai vizsgálatok: (B típusú evidencia, 10) Arthrographia nem ad többletinformációt, emellett invazív vizsgálatot jelent.
CT vizsgálat hasznos lehet a ritka késői szövődményként jelentkező combfejosteochondritisdissecans diagnózisában.
6. Differenciál diagnosztika:
- Dyspslasia epiphysealis capitis femoris:
gyermekkorban észlelhető, nem leépülési, hanem fej-felépülési zavar. Lényege, hogy egyik oldali csípőizületben a proximalis femurepiphyis nem egy, hanem 2 vagy 3 csontmagból fejlődik. Intermittáló synovitist és intermittáló sántítást okozhat. A röntgenfelvételen nagyon hasonló elváltozás látható, mint Perthes betegség esetében (Perthes like syndroma). A Lauenstein felvételen azonban nagy biztonsággal megállapítható, hogy 2 vagy 3 körülírt csontmag alkotja a proximalis epiphysist. Jellemző továbbá a differenciál diagnózis során, hogy általában érdemi mozgáskorlátozottságot nem találunk a csípőizületben. Elkülönítése azért szükséges, mivel ezen kórkép kizárólag konzervatív kezelést, esetleg csak megfigyelést igényel.
- multiplex epiphysealis dysostosis:
Kétoldali folyamat, szintén intermittáló panaszokat okozhat, és a radiológiai kép ugyanaz, mint az előző kórformánál, csak kétoldali az elváltozás. Jellemző ezen esetekben a kisfokú coxa vara. Szintén jellemző, hogy érdemi mozgáskorlátozottságot nem találunk. A diagnózis a test egyéb epiphysiseiről készített röntgenfelvétel segítségével megerősíthető. Szintén csak megfigyelést igényel.
III. Terápia
Nem gyógyszeres kezelés
1. A megfelelő egészségügyi ellátás szintje: Gyermekortopédiai centrum.
2. Általános intézkedések:
Nem szükséges azonnali fektetés, mint az epiphyseolysisnél, de ajánlott hogy személyesen átadva, a beteget ortopéd/gyermek-ortopéd centrumba irányítsák.
3.Speciális ápolási teendők: Nincsenek.
4.Fizikai aktivitás:
A fizikai aktivitás korlátozása Nincs szükség fektetésre. A célzott terheléstől való mentesítés javasolt
5.Speciális diéta nem szükséges.
6.Betegoktatás:
Szülőknek elmondjuk, hogy a combfej elhalásos betegségéről van szó, mely pihenést igényel, további teendőket a regionális centrumban határozzák meg.
III./2. Gyógyszeres kezelés
1.A megfelelő egészségügyi ellátás szintje: Regionális gyermekortopédiai centrum.
2.Gyógyszeres terápiája a betegségnek nem ismeretes. Kifejezett fájdalom esetén a gyermek korának megfelelő dózisban non-steroid gyulladáscsökkentő adható.
III/3. Műtét: (B típusú evidencia, 1,6-13)
1. Megfelelő egészségügyi ellátás szintje: Regionális gyermekortopédiai centrum.
2. Általános intézkedések:
Fektetés. Akut szakban panasz esetén az extenzió jó hatású. Tehermentesített helyzetben mozgatás,(kerékpár, CPM)
3. Speciális ápolási teendők: Nincsenek.
4. Sebészeti kezelés: Műtéti indikáció:
- A proximális femur epiphysis centralisatióját biztosító varisaló-derotaló intertrochantericus femur osteotomia indikált, 6 éves kor felett a derotáció nem indokolt.
- A beteg korától a betegség tipusától fűggően femur/medence/ kombinált műtéti kezelés javasoltható
- VDRO
- Pemberton
- Salter
- Triple osteotomia
- 50 %-nál kisebb combfejnecrosisok esetében a konzervatív és a sebészeti kezelés azonos végeredményt mutat. Ezért 50 %-nál kisebb combfej érintettség esetén megfigyelés javasolt, míg nagyobb combfejnecrosis esetén mérlegelendő a varisaló-derotaló osteotomia elvégzése. A 10 éves kor feletti Perthes betegség esetén csaknem minden létező kezelési formánál kedvezőtlen klinikai végeredményeket találunk. Minden Pertheses eset egyéni mérlegelést igényel. Amennyiben funkcionális-abductiós és berotatiós röntgenfelvételen a combfej centralizációja biztosítható, a varisaló-derotaló osteotomia szóba jön. Amennyiben a combfej lateralis kiboltosulása jelentős, és a combfej centralizálása nem biztosítható, a medenceosteotomiák valamely formája (Salter vagy Pemberton).
- A Chiari osteotomia ritkán jöhet szóba. 10 éves kor alatt ad rossz eredményeket, előnye viszont, hogy a combfej befedését úgy biztosítja, hogy nem növeli a kompressziót, csak a teret.
- Alternatív megoldási lehetőség, hogy a fennálló necrosis ellenére műtéti beavatkozást nem végzünk, hanem csak megfigyelést és a fizikális aktivítás korlátozását (iskolai torna alóli felmentés), és csaka kialakult végállapot kialakulása után próbáljuk a combfej befedését biztosítani műtéti úton.
Műtéti előkészítés: Műtéti előkészítésként
- negatív vérkép,
- negatív EKG, és
- gyermekgyógyászati vagy anaesthesiológus szakvélemény szükséges az altathatóságról.
Műtéti érzéstelenítés:
A műtétet narkózisban kell végezni.
Műtét: ( Varisalo derotaciós femur osteotomia)
A trochanter csúcsától distal felé induló tengelyirányú bőrmetszés ejtünk. Ezután a fascia lata hossz-, esetleg haránt irányú behasítását végezzük. Avastus lateralis rostjai között tengelyirányba behatolva, azokat két irányba elkampózva a periosteumot a trochantertől distal felé hosszirányban behasítjuk, majd hüvelyszerűen, kampók védelme mellett oldalra letoljuk. Képerősítő kontrollja mellett intertrochantericusan haránt osteotomiát végzünk, majd intertrochantericusan a funkcionális felvétel által igényelt méretű, mediál felé néző csontéket távolítunk el. A proximális femurvéget 10-15 fokkal befelé rotáljuk, és ebben a helyzetben a csontvégeket stabil osteosynthesissel rögzítjük (szöglemez vagy egyéb stabil lemez). Képerősítő kontrollja után - centralizálás megítélése céljából -réteges rekonstrukciót végzünk, majd steril fedőkötést. Gyermekkorban a bőr zárási technikájától függetlenül nagy a keloid-képzés hajlama, az esetek 90 %-ában a csípőtájékon kialakul.
Posztoperációs teendők:
- Stabil belső rögzítés esetén külső rögzítés - gipszkötés - nem szükséges.
- Amennyiben nem stabil a rögzítés, 4-6 hétre medencegipsz szükséges.
- A műtét után csak fájdalomcsillapítás szükséges, és a fájdalom megszűnése után
(1-3 nap) terhelés nélküli mankózás engedélyezhető, a csípő gyógytornáztatása mellett.
- A terhelés nélküli mankózás az osteotomia csontos átépüléséig szükséges. Gyermekkorban ez 6-12 hétig tart.
5. Fizikai aktivitás
A radiológiailag igazolt csontos átépülésig csak fekvő helyzetben végzett csípőtorna, valamint mankóval, terhelés nélküli járás engedélyezhető.
6. Diéta
Nem szükséges.
7. Betegoktatás
A fent említettek betartása szükséges.
III/4. Egyéb terápia: (B típusú evidencia 1,6, 9,10,17)
Alternatív kezelésként a betegség lezajlásának ideje alatt, a csípőizületet tehermentesítő, abdukciot és berotatiot (centralizációt) biztosító járógép viselése jön szóba, ha a femur fej beforgatható a vápába. Ezt abdukciós-berotációs helyzetben készült összehasonlító rtg felvétellel ellenőrizhetjük. Következetes járógép viseltetéssel a műtéti beavatkozások egy része elkerülhető. A műtéti kezelés - varisalo-derotalo osteotomia - 8-12 héttel a műtét után szabad járást, és terhelést biztosít. Emellett rendszeres csípőizületi torna szükséges.
Tekintettel arra, hogy a betegség lezajlása (3-5 év) hosszadalmas, a járógép ilyen hosszú fenntartása mérlegelendő.
IV. Rehabilitáció
Rehabilitáció csak abban az esetben szükséges, amikor a választott kezeléstől függetlenül jelentős csípőizületi mozgáskorlátozottság maradt vissza. Ez általában 10 éves kora felett jelentkező Perthes betegségnél várható. Ilyen esetekben gyermek-ortopédiai osztályon konzervatív kezelés javasolt.
V. Gondozás
1. Rendszeres ellenőrzés:
A Perthes betegség lezajlása után a gyermekkor végéig (14-16 év) évenkénti, rendszeres ortopédiai ellenőrzés szükséges. Konzervatív kezelés - járógép - esetében a járógép elkészülte után szükséges orvosi ellenőrzés, majd ezt követően 3 havonként. Röntgenfelvétel készítése legkorábban félévenként szükséges, kivéve, ha váratlan panasz jelentkezik. A műtéti kezelés után kontroll vizsgálat várható a csontosodás bekövetkeztekor (6-12 hét között), majd utána fél év múlva, azt követően évenként szükséges. A műtét után általában fél-egy évvel a fémlemez műtéti eltávolítása szükséges, melyet követően szabad járás engedélyezhető.
2. Megelőzés:
A Perthes betegséget általában megelőzni nem lehet. Korábban lezajlott és gyógyult transitoricus coxitis esetében azonban a gyógyulást követően 3 hónap múlva vissza kell rendelni, és csípőizületi összehasonlító röntgenfelvétel készítése szükséges.
3. Lehetséges szövődmények: (B típusú evidencia 18-22. 25) 3.1.Szövődmények kezelése:
Konzervatív kezelés esetében a lehetséges szövődmények a combfejellapulása és csípőizületi mozgáskorlátozottság kialakulása. Műtéti kezelésnél (varisalo-derotalo osteotomia) a műtét után az operált alsó végtag 0,5-1 cm-rel megrövidül.A nagytompor relatív, majd később valódi magasabbra helyeződése miatt kialakul aTrendelenburg tünet.
A rövidülés az esetek többségében a gyermekkor hátralévő részében megszűnik, vagy jelentősen csökken. A leggondosabb kezelés ellenére is a combfej ellapulása, kiboltosulása és a csípőizület mozgáskorlátozottsága visszamaradhat. Ennek kezelése a rendszeres gyógytorna, továbbá az iskolai torna alóli részleges felmentés (felsővégtag tornát végezhet).
A magas trochanter állás és következményes Trendelenburg tünet kezelésére tompor csavaros növekedés gátlás (18.19.20.21.22.) vagy a növekedés bezáródása után tomporlehelyezés (.25.) ajánlható.
4. A kezelés várható időtartama/prognózis: (B típusú evidencia 6,7,10)
Konzervatív kezelés esetén a kezelés várható időtartama 3-5 év. Műtéti kezelés esetében 1,5-2 év. Ugyanakkor a növekedés befejeződéséig folyamatos ellenőrzés szükséges. A prognózis attól függ, hogy a combfej epiphysise a felépülés után milyen remodellációra képes az acetabulumban. Ennek megítélése ma még objektív módszerekkel nem lehetséges. Korábban meglévő rizikótényezők esetén nagyobb a pathológiás inkongruencia kialakulásának esélye, ami ellapult és egyenetlen felszínű combfejet jelent. Jó kezelési eredménynek tekintjük, amikor a combfej ugyan ellapult valamilyen mértékben, de újra épülve az acetabulum alakjára negatív körkörös remodellációt mutat, mely jól mozgó csípőt és jó funkciót biztosít (fiziológiás inkongruencia). Ezen esetekben, a felnőttkorban coxarthrosis kialakulása általában nem várható. Patológiás inkongruencia esetében azonban a felnőttkorban secunder coxarthrosis kialakulása valószínű. A növekedés befejezését követően észlelhető fej-vápa aránytalanság esetén mérlegelhető, a fej jobb befedésére, valamilyen medence osteotomia
A femur nyak lecsökkent növekedési erélye és a nagytompor változatlan fejlődése olyan aránytalanságot okoz a proximális femurvégen, ami a Trendelenurg tünet megjelenésével és fokozódásával jár. Az egyre magasabb tomporon tapadó gluteusok insufficienssé válnak. Ennek a folyamatnak a megelőzésére, rendszerint a femur osteotomia során behelyezett fémek eltávolítása idején növekedésgátló céllal megcsavarozhatjuk a nagytomport. Az így kikapcsolt növekedési zóna nem okoz további állapotromlást.
5. Az ellátás megfelelősségének indikátorai:
A szakmai munka eredményességének mutatói a csípőizületi panaszok megszűnése, a csípőizület mozgásainak teljes helyreállása vagy kisfokú mozgáskorlátozottság visszamaradása (abductio és berotatio kisfokú korlátozottsága), valamint röntgenfelvételen a centrálisan elhelyezkedő, kissé ellapult, de körkörös combfej kialakulásának mértéke a mutató.
6. Dokumentáció, bizonylat:
- Első jelentkezéskor ambuláns vizsgálati lelet,
- AP és Lauenstein összehasonlító csípőizületi röntgenfelvétel,
- Ahol szükséges volt, csípőizületi scintigraphia,
- Műtét után az osteotomia csontos átépülés dokumentáló röntgenfelvétel,
- A combfejátépülése után készített csípőizületi röntgenfelvétel,
- A növekedés befejeződésekor (15-16 év) készített záró röntgenfelvétel.
7. Egyéb megjegyzések:
1. Izolált betegségről van szó.
2. Érintett társszakmák:
Speciális gyermekortopédiai megbetegedés.
VI. Irodalomjegyzék
1. Bellyei Á., Mike Gy.: Weight bearing in Perthes'disease, Orthopedics, 1991,14:19-22
2. H. Kitoh, T. Kitakoji, M. Katoh, and Y. Takamine Delayed ossification of the proximal capital femoral epiphysis in Legg-Calvé-Perthes' disease J Bone Joint Surg Br, Jan 2003; 85-B: 121 -124.
3. F. Lecuire The long-term outcome of primary osteochondritis of the hip (Legg-Calvé-Perthes' disease) J Bone Joint Surg Br, Jul 2002; 84-B: 636 - 640.
4. S. Hayek, G. Kenet, A. Lubetsky, N. Rosenberg, S. Gitel, and S. Wientroub Does thrombophilia play an aetiological role in Legg-Calvé-Perthes disease? J Bone Joint Surg Br, Jul 1999; 81-B: 686-690.
5. John A. Herring, Hui Taek Kim, and Richard Browne Legg-Calvé-Perthes Disease. Part I: Classification of Radiographs with Use of the Modified Lateral Pillar and Stulberg Classifications J. Bone Joint Surg. Am., Oct 2004; 86:2103-2120.
6. John A. Herring, Hui Taek Kim, and Richard Browne Legg-Calvé-Perthes Disease. Part II: Prospective Multicenter Study of the Effect of Treatment on Outcome J. Bone Joint Surg. Am., Oct 2004; 86:2121 - 2134.
7. J.T.Guille, G.E. Lipton,G. Szökeet al. Legg-Calvé-Perthes Disease in Girls. A Comparison of the Results with Those Seen in Boys J. Bone Joint Surg. Am., Sep 1998; 80:1256 - 1263.
8. Jeroen G. Neyt, S.L. Weinstein, et al. Stulberg Classification System for Evaluation of Legg-Calvé-Perthes Disease: Intra-Raterand Inter-Rater Reliability J. Bone Joint Surg. Am., Sep 1999; 81:1209- 16.
9. JA Herring The treatment of Legg-Calve-Perthes disease. A critical review of the literature J. Bone Joint Surg. Am., Mar
1994; 76: 448 - 458.
10. DR Wenger, WT Ward, and JA Herring Legg-Calve-Perthes disease J. Bone Joint Surg. Am.,Jun 1991; 73: 778-788.
11. M Clancy and HH Steel The effect of an incomplete interochanteric osteotomy on Legg-Calve-Perthes disease J. Bone Joint Surg. Am., Feb 1985; 67: 213-216.
12. RB Salter and GH Thompson Legg-Calve-Perthes disease. The prognostic significance of the subchondral fracture and a two-group classification of the femoral head involvement J. Bone Joint Surg. Am., Apr 1984; 66:479 - 489.
13. PD Sponseller, SS Desai, and MB Millis Comparison of femoral and innominate osteotomies for the treatment of Legg-Calve-Perthes disease J. Bone Joint Surg. Am., Sep 1988; 70:1131 - 1139.
14. MP McAndrew and SL Weinstein A long-term follow-up of Legg-Calve-Perthes disease J. Bone Joint Surg. Am., Jul 1984; 66: 860 - 869.
15. SD Stulberg, DR Cooperman, and R Wallensten The natural history of Legg-Calve-Perthes disease J. Bone Joint Surg. Am., Sep 1981; 63:1095 - 1108.
16. BE Van Dam, RJ Crider, JD Noyes, and LJ Larsen Determination of the Catterall classification in Legg-Calve-Perthes disease J. Bone Joint Surg. Am., Jul 1981; 63: 906-914.
17. FB Kelly, STCanale, and RR Jones Legg-Calve-Perthes disease. Long-term evaluation of non-containment treatment J. Bone Joint Surg. Am., Apr 1980; 62: 400 - 407.
18. Lloyd-Roberts GC, Wetherill MH, Fraser M. Trochanteric advancement for premature arrest of the femoral capital growth plate. J Bone Joint Surg Br. 1985;67:21Y 24
19. Gage JR, Cary JM. The effect of trochanteric epiphyseodesis on growth of the proximal end of the femur following necrosis of the capital femo.ral epiphysis. J Bone Joint Surg Am. 1980;62:785Y794.
20. Fernbach SK, Poznanski AK, Kelikian AS, et al. Greater trochanteric overgrowth: development and surgical correction. Radiology. 1985;154: 661Y 664
21. Dorien Schneidmueller, MD,* Claus Carstens, MD, PhD,T and Marc Thomsen, MD, PhDT Surgical Treatment of Overgrowth of the Greater Trochanter in Children and Adolescents J Pediatr Orthop & Volume 26, Number 4, July/August 2006
22. Takata K, Maniwa S, Ochi M. Surgical treatment of high-standing greater trochanter. Arch Orthop Trauma Surg. 1999;119:461Y463.
23. Hasler CC, Morscher EW. Femoral neck lengthening osteotomy after growth disturbance of the proximal femur. J Pediatr Orthop B. 1999;8:271Y 275.
24. Niethard FU. Overgrowth of the greater trochanter. Mapfre Medicina. 1995;6:229Y 231.
25. Szepesi K, Fazekas K, Biro B,etal. Distal transfer of the greater trochanter for the correction of trochanteric overgrowth. Acta Chir Hung. 1992Y 93;33:125Y 133.
26. RannerG, Fotter R, Linhart W, Ebner F. Radiologic diagnosis of Perthes disease. Radiologe. 1994 Jan;34(1):21-9.
27 Ranner G. Osteochondrosis deformans coxae juvenilis (Legg-Calvé-Perthes disease) in the MR tomogram: diagnosis and follow-up assessment correlated with x-rays and skeletal scintigraphy] Rofo. 1990 Aug;153(2):124-30. 28. Kramer J, Hofmann S, Scheurecker A, Tschauner C. Perthes disease Radiologe. 2002 Jun;42(6):432-9.
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Dokumentáció, bizonylat
- Járóbeteg szakellátásban: ambuláns lap, kezelő lap.
- Képalkotó vizsgálatok képi és szöveges leletei
- Fekvőbeteg szakellátásban: kórlap, műtéti beleegyezés, műtéti leírás, decursus, zárójelentés.
- Felhasználásra került implantátumok bizonylatai
2. Érintett társszakmákkal való konszenzus Gyermekgyógyászat, Radiológia.
3. Evidencia besorolás
A bizonyítékok szintjei
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Epiphyseolysis capitis femoris juvenilis ellátásáról
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
Szinonímák:
Coxa vara adolescens
Serdülőkori femur fej elcsúszás
I. Alapvető megfontolások
1.1. Ortopédia, traumatológia, gyermekgyógyászat
1.2. Jó szakmai tájékozottság az említett három szakmában.
1.3. Definició
A femurfej epiphysise a combnyakon hátra és lefelé fordul és csúszik fokozatosan (lenta v. chronica) vagy hirtelen (acuta).
1.3.1. Kiváltó tényezők
A betegség oka átmeneti hormonális zavar, melynek lényege a növekedési hormon túlsúlya a sexuál hormonokkal szemben. E hormon hatására a növekedési porc kiszélesedik és az itt érvényesülő nyíró erő hatására az epiphysis a nyakon elfordul1(B szintű evidencia).
1.3.2. Kockázati tényezők
A praepubertásban fordul elő a fent említett hormonális zavar és a leggyorsabb növekedés idején fiúknál 13-15, lányoknál 11-13 év között a leggyakoribb a betegség. Lányoknál a menstruáció után nem fordul elő. Bizonyos endokrin betegségek (dystrophia adiposogenitalis, pubertáskori eunuchoidismus, pubertáskori gigantizmus, kasztráció után, anyagcsere betegségben gyakran fordul elő2(B szintű evidencia).
1.4. Panaszok, tünetek, általános jellemzők
A gyermekek comb, térd, csípőfájdalomról panaszkodnak. Az akut formánál elesik nem tud lábra állni.
Az alsó végtag kifelé fordul, Drehmann tünet észlelhető3. A gyerekek rendszerint túlsúlyosaka secunder nemi jellegek
megjelenése késik.
1.5.1. Érintett szervrendszer Csípőízület, proximális femurvég
1.5.2. Genetikai háttér: Ha a családban előfordult a következő gyermeknél a valószínűség 7:1.
1.5.3. Előfordulás: 0,5-1%, az esetek 1/3-ában kétoldali, közvetlen mortalitás nincs.
1.5.4. Jellemző életkor: fiúknál 13-15 év, lányoknál 11-13 év között.
I.5.5. Fiúknál kétszer gyakoribb, mint lányoknál.
II. Diagnózis
Anamnézis
Epiphyseolysis lenta esetében a gyermekek rendszerint hosszabb ideje fennálló panaszokkal jönnek. Leggyakrabban térd- és combfájdalomról, ritkábban csípő fájdalomról panaszkodnak, vagy a fáradékonyság miatt a tornaórán nem tudnak megfelelni a követelményeknek. Gyakran észlelik a szülők, hogy a gyermek furcsán megy, sántít. A "másik" oldalon is kialakulhat a betegség, nem ritkán egy-másfél évvel később, ezért az "ép" oldalt is figyelni kell.
Ha a 11-16 éves elhízott, nemi érésben visszamaradt vagy eunuchoid alkatú gyermek comb-, térd-, csípő-, lábszárfájdalmakról, fáradékonyságról panaszkodik, feltétlenül gondoljunk epiphyseolysisre. Az epiphyseolysis előfordulhat azonban teljesen normál alkatú gyermekeken és ritkán fiatalabb korban is4(B szintű evidencia).
11.2. Fizikális vizsgálatok
A klinikai és röntgentünetekegy részét is azepiphysis hátrafelé fordulása magyarázza. Már megtekintéskor feltűnhet, hogy a gyermek a beteg oldali alsó végtagját kifelé forgatott helyzetben tartja, ami különösen kifejezett lehet járás közben. Az epiphysis hátrafordulása miatt ugyanis, mivel a femurfejhátrafelé nem tud kifordulni a vápából, a végtag fordul kifelé.
A csípőízület mozgását háton fekvő helyzetben vizsgáljuk. A csípőízület hajlítása közben epiphyseolysis esetén a végtag abductiós és kifelé forgatott helyzetbe kerül3(C szintű evidencia). Ez a kényszermozgás - Drehmann-tünet -ugyancsak a combfej hátrafelé fordulásának következménye, és már kezdeti stádiumban jelen van. Állandó tünet a végtag befelé rotatiójának korlátozottsága. Ez vizsgálható nyújtott csípő és térd, vagy 90 fokban hajlított csípő és térd mellett. Jól észlelhető a mozgáskorlátozottság, ha a két oldalt összehasonlítva vizsgáljuk. Míg normálisan 30-50 fok a kifelé és befelé rotatio, addig epiphyseolysis esetén a befelé rotatio korlátozott és ez gyakran olyan fokú, hogy a végtag kifelé rotatiós helyzetéből középállásig sem forgatható be. Ha a gyermeket a vizsgálóasztalra térdeltetjük, azt látjuk, hogy lábszárai keresztezik egymást. A végtag kifelé fordulása az epiphysis hátrafordulásának következménye. A combfejígy helyezkedik el centrálisan a vápában. Rendszerint korlátozott a csípőízület abductiója és extensiója is.
Epiphyseolysis acuta esetén a gyermek rendszerint elesik és nem tud lábra állni. A traumának az epiphysis dislocatiójában nincs lényeges szerepe,sőt arra is következtethetünkazanamnesisből,hogy a beteg azért esikel, mert bekövetkezett az epiphysis elcsúszása. Az akut elcsúszást olyan tünetek előzhetik meg, amelyek arra utalnak, hogy a teljes elcsúszás hónapok óta fennálló epiphyseolysis lenta talaján következett be (akut elcsúszás krónikus előzménnyel).
Vizsgálatkor a combnyaktöréshez hasonló állapotot észlelünk. A végtag kifelé forgatott helyzetben van, a csípőízület fájdalma miatt a beteg végtagját nem mozgatja, illetve mozgáskísérletre fájdalmat jelez. Ilyen esetben a beteg rendszerint azonnal ortopédiai osztályra kerül, ahol megfelelő ellátásban részesül. Amennyiben a beteg nem kerül orvoshoz, napok múlva a fájdalom csökkenése után felkel és járni kezd. A végtag kifelé fordult helyzete, megrövidülése és a csípőízületben fennálló mozgáskorlátozottság mutatja a lezajlott eseményt.
11.3. Kötelező vizsgálatok
Ha a betegség másodlagos, akkor szükség lehet csont-anyagcsere és endokrin vizsgálatokra.
11.3.1. Laboratóriumi vizsgálatokra csak a másodlagos formáknál van szükség az alapbetegség tisztázására. Renális rachitisnél és endokrin betegségekesetén szükséges a megfelelő laborvizsgálatokat elvégezni5,6(B szintű evidencia).
11.3.2. Képalkotó vizsgálatok
Röntgentünetek: Epiphyseolysis gyanúja esetén a betegség fennállásának igazolása és az elcsúszás fokának megítélése céljából összehasonlító röntgenfelvételt készíttetünk a-p és Lauenstein-helyzetben (vagy oldalirányút). Azért kell mind a két csípőről felvételt készíteni, mert gyakran a látszólag ép csípő is érintett. A Lauenstein-helyzetben készült vagy oldalirányú felvételre pedig azért van szükség, mert amíg az a-p képen kezdeti stádiumban gyakran nem látható értékelhető elváltozás, addig a Lauenstein-helyzetben készült képen már kisfokú hátrafordulás is kimutatható7(C szintű evidencia).
Az elcsúszás, ill. elfordulás mértéke szerint megkülönböztethetünk fenyegető (e.imminens) kezdődő (e. incipiens), mérsékelt és súlyos formát, teljes elcsúszást8(B szintű evidencia).
A legkoraibb, még a dislocatiót megelőző, nehezen értékelhető korai röntgentünet a növekedési porc kiszélesedése és a combnyak metaphysisének fellazulása (epiphyseolysis imminens).
A röntgenképen már minimális elcsúszás is jól felismerhető. Először az epiphysis csak elfordul hátrafelé anélkül, hogy elcsúszna. Ez az a-p képen úgy jelentkezik, hogy az epiphysis magassága kisebb és a nyak felső szélének meghosszabbításából adódó vonal nem metsz le egy szegmentumot a fejből.
Lauenstein-felvételen az elcsúszás, illetve elfordulás kifejezettebb. Az epiphysis alapja normálisan merőleges a nyak tengelyére. Epiphyseolysis esetében a két vonal által bezárt szög hátrafelé kisebb 90 foknál, és annál kisebb, minél nagyobb a hátrafordulás (epiphyseolysis incipiens).
Nagyobb fokú elfordulás és elcsúszás esetén már az a-p képen is jól látható a dislocatio. Az epiphysis magassága csökkent, a nyakhoz viszonyítva lejjebb került és alapjával szemben helyezkedik el, ami kerek vetületként jól látható. Lauenstein-felvételen látható, hogy teljes elcsúszás esetén az epiphysis hátsó széle a fossa trochantericába támaszkodik.
Akut epiphyseolysis esetén általában teljes elcsúszás látható. Ilyen esetben, ha Lauenstein-felvétel nem készíthető, oldalirányú felvétel ad pontos tájékoztatást az epiphysis helyzetéről.
MR, CT és ultrahang vizsgálatra csak rendkívüli esetben van szükség. Általában elegendő információt ad az a-p és Lauenstein helyzetben készült (vagy oldalirányú) röntgenfelvétel.
11.4. Kiegészítő diagnosztikai vizsgálatokra csak a másodlagos formákban van szükség.
11.5. Differenciál diagnosztika
A veszélyeztetett korcsoportban bizonytalan comb, térd, csípő fájdalom esetén gondolni kell a betegségre. Minden
térdpanaszos betegnél meg kell vizsgálni a csípőket is9(B szintű evidencia).
Perthes kór
Csípőizületi gyulladás
Tranzitórikus csípőízületi gyulladás
Idiopatiás csípő osteoporosis
Rheumatoid arthritis
Protrusio acetabuli
merülhetnek fel.
11.6. Diagnosztikai algoritmus:
- Panaszok meghallgatása értékelése (gyakran comb, térdfájdalom van)
- A beteg megtekintése (alkat, secunder nemi jelleg, alsóvégtag rotációs állása)
- Beteg vizsgálata (térd, comb, csípő)
- A-p összehasonlító és Lauenstein helyzetben készült (vagy oldalirányú) csípő röntgenfelvétel.
III. Terápia
III/1. A betegség műtétileg kezelendő
Az említett korosztályban, prépubertásban, pubertásban lévő gyermekekre fokozottabban kell figyelni, különösen, ha az említett alkati sajátosságot mutatják.
III/2. Eddig eredményesen alkalmazott gyógyszeres kezelésről nem számoltak be. III/3. Műtét
A betegek műtéti ellátása ortopédiai és traumatológiai osztályon történhet. A betegség észlelésekor a gyermeket azonnal a megfelelő osztályra kell utalni.
Kezelés
A konzervatív kezelési eljárásoktól eredmény nem várható. Előfordul, hogy fekvő betegeknél is fokozódik az elcsúszás. Helyes, ha lefektetjük a beteget arra az időre is, amíg ortopédiai osztályra kerül, mert epiphyseolysis lentának minősített esetben is fennáll a veszélye annak, hogy az elcsúszás hirtelen teljessé válik, epiphyseolysis acuta esetén pedig röviddel az elcsúszás után még lehetőség van a repositióra.
Gondosan kell vizsgálni a "másik", látszólag egészséges oldalt és a legkisebb jel esetén egyidejűleg, mintegy prventíve szintén meg kell operálni.
Műtéti indikáció
Kisfokú dislocatio esetén, ha az elmozdulás még nem nagy fokú a Lauenstein-felvételen az epiphysis hátrafelé fordulása még nem nagyobb 30 foknál vagy az elcsúszás még nem haladja meg a nyakszélesség 1/3-át, akkor az adott helyzetben (in situ epiphyseodesis) a nyakon keresztül az epiphysisbe vezetett Kirschner-drótok, AOspongiosa csavar vagy speciális, e célra készült csavar megakadályozzák a további elmozdulást és elősegítik a növekedési porc gyors elcsontosodását. Kanülált csavart képerősítő segítségével percutan is be lehet vezetni. A műtétet általános érzéstelenítésben, vagy lumbal anaesthesiában végezzük.
Műtét után csökken a kifelé rotatiós contractura és idővel a femurfejmodellálóátépülése is javít a helyzeten10(B szintű evidencia). A gyermek a műtét utáni 2. napon mankóval felkelhet, 3 hét múlva már részlegesen terhelve járhat, iskolába mehet, 3 hónap múlva normális életet élhet. 1-2 év alatt általában elcsontosodika növekedési porc, és utána a drótok, illetve a csavarok eltávolíthatók.
Az in situ epiphyseodesis elvégezhető amíg technikailag lehetséges, ha még nem teljes az elcsúszás.
Nagyobb fokú elcsúszás esetén azonban megnyugtató megoldás csak az elmozdulás korrekciójától várható. Minél közelebb történik a korrekció (a csont átvésése és repositio) az elmozdulás helyéhez, annál tökéletesebb anatómiai eredmény érhető el. A fedett vagy nyílt repositiónak és combnyak-osteotomiának viszont nagy a veszélye, mert sérülhet a fej vérellátása, és gyakran a combfejvagy az ízületi porc ischaemiás necrosisa alakul ki. A legjobb eredmény az epiphysis Dunn szerinti repositiójától11(C szintű evidencia) és a combnyak ék-osteotomiájától várható, amikor a combnyak hátsó felszínén haladó ereket biztosabban megóvhatjuk a sérüléstől12(B szintű evidencia).
A kis trochanter alatt végzett osteotomiával is korrigálhatjukafemurfejvápához való viszonyát és a végtag kifelé rotált helyzetét. Veszélytelen eljárás, de kevésbé javítja a femurfej-vápa viszonyát.
Osteotomiánál általában belső rögzítést alkalmazunk, azonban ritkán gipszkötésre is szükség lehet.
Epiphyseolysis acuta esetén 1 héten belül megkísérelhető a fedett vagy nyílt repositio, eredményei azonban nem megnyugtatók. A helyretételt észlelés után (acut esetben) a lehető legrövidebb időn belül kell elvégezni, de nagyon óvatosan, lassan. Gyakori az epiphysis vagy az ízületi porc necrosisa, mely az ízület mozgásának jelentős beszűküléséhez vezet. Repositio után az epiphysist hasonló módon kell rögzíteni a combnyakon, mint epiphyseolysis lenta esetén.
A legjobb eredményt akkor kapjuk, ha korán, még kisfokú elmozdulás esetén korrekció nélkül végezzük el a rögzítést, az epiphyseodesist. Így megakadályozzuk a további elcsúszást, nem károsítjuk a femurfejvérellátását, gyors záródásra serkentjük a növekedési porcot és lehetőséget adunk a modelláló átépülésre.
Ha deformitás nélkül gyógyul a beteg teljes fizikai terhelés lehetséges. Deformálódás esetén kímélet szükséges.
IV. Rehabilitáció
V. Gondozás
Minden olyan esetben, amikor nem tökéletes a gyógyulás a másodlagos coxarthrosis veszélye miatt gondosan figyelni kell a beteget és fokozott fizikai igénybevételtől óvandó.
Törekedni kell arra is, hogy a betegek ne hízzanak el, mert az is fokozza a csípők terhelését. Szövődmények előfordulnak a lenta és az akut formában is.
A lenta formában az elcsúszás fokától függően a csípőízület mozgáskorlátozottsága, a femurfejdeformálódása alakulhat ki előrevetítve a szekunder coxarthrosis felléptét.
Akut elcsúszás esetén ha nem történik repositio vagy nem elég sikeres, az előbb említett helyzet áll fenn.
Repositio esetén az esetek jelentős részében epiphysis necrosis vagy az ízületi porc pusztulása következik be súlyos mozgáskorlátozottsággal és deformitással.
Mérlegelni kell akut teljes elcsúszás esetén, hogy a nyílt vagy fedett repositiótól vagy egy későbbi osteotomiától várható-e jobb eredmény.
Az in situ epiphyseodesis után 3 hónap múlva a gyermekek már normál életet élhetnek és a növekedési porc elcsontosodása után a teljes fizikai terhelés engedélyezhető, ha az ízület alakilag ép. Egy rögzítő csavar esetén ritkább, több csavar után gyakoribb az izületbe történő penetráció miatt az izületi porc károsodása.
A szakmai munka eredményességének mutatói között első helyen kell említeni a korai diagnózis és kezelés fontosságát. A mintegy "preventiv epiphyseodesissel" tökéletes vagy közel tökéletes eredmény érhető el.
A csekély fokú elcsúszás után is jó eredmény várható, de minél nagyobb az elcsúszás foka, annál nagyobb lesz a femurfejdeformálódása és a felnőttkori arthrosis.
VI. Irodalomjegyzék
1. Weiner D.; Pathogenesis of slipped capital femoral epiphysis: current concepts. J Pediatr Orthop B. 1996 Spring;5(2):67-73.
2. Mann DC.; Endocrine disorders and orthopedic problems in children. CurrOpin Pediatr. 1996 Feb;8(1):68-70.
3. Drehmann F.; Drehmann's sign. A clinical examination method in epiphysiolysis (slipping of the upper femoral epiphysis). Description of signs, aetiopathogenetic considerations, clinical experience (author's transl)] Z Orthop Ihre Grenzgeb. 1979 Jun;117(3):333-44.
4. Ledwith CA, Fleisher GR.; Slipped capital femoral epiphysis without hip pain leads to missed diagnosis. Pediatrics. 1992
Apr;89(4 Pt 1):660-2.
5. Oppenheim WL, Bowen RE, McDonough PW, FunahashiTT, Salusky IB.; Outcome of slipped capital femoral epiphysis in renal osteodystrophy. J Pediatr Orthop. 2003 Mar-Apr;23(2):169-74.
6. Burrow SR, Alman B, Wright JG.; Short stature as a screening test for endocrinopathy in slipped capital femoral epiphysis. J Bone Joint Surg Br. 2001 Mar;83(2):263-8.
7. Bloomberg TJ, Nuttall J, Stoker DJ.; Radiology in early slipped femoral capital epiphysis. Clin Radiol. 1978 Nov;29(6):657-67.
8. Boero S, Brunenghi GM, Carbone M, Stella G, Calevo MG.; Pinning in slipped capital femoral epiphysis: long-term follow-up study. J Pediatr Orthop B. 2003 Nov;12(6):372-9.
9. Matava MJ, Patton CM, Luhmann S, Gordon JE, Schoenecker PL.; Knee pain as the initial symptom of slipped capital femoral epiphysis: an analysis of initial presentation and treatment. J Pediatr Orthop. 1999 Jul-Aug;19(4):455-60.
10. Jones JR, Paterson DC, Hillier TM, Foster BK. Remodelling after pinning for slipped capital femoral epiphysis. J Bone Joint Surg Br. 1990 Jul;72(4):568-73.
11. Dunn DM. The treatment of adolescent slippeng of the upper femoral epiphysis J Bone Joint Surg Br. 1964 Nov;46:621-9.
12. Uglow MG., Clarke NMP.;The management of slipped capital femoral epiphysis J Bone Joint Surg Br. 2004 Jul;
13. Canale T.S., Beaty J.H.; Operative Pediatric Orthopaedics. Mosby Year Book, St.Louis, 1991.
14. Sharrard W.J.W.; Paediatric Orthopaedics & Fractures. Blackwell Scientific Publications, Oxford &Edinburg, 1993.
15. Tachdjian M.O.; Pediatric Orthopedics. W. B. Saunders Co. Philadelphia, London, Toronto, 1990.
16. Vízkelety T.; Gyermekortopédia. Medicina, Budapest, 1994.
17. Vízkelety T. (szerk.); Az ortopédia tankönyve. Semmelweis Kiadó, Budapest, 2002.
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Gyakori társbetegségek: Szekunder formáknál Prepubertáskori endokrinzavar Csont anyagcsere betegségek
2. Érintett társszakmák: traumatológia, Gyermekorvosok, Iskolaorvosok, Reumatológusok
3.
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Az Egészségügyi Minisztérium
szakmai protokollja
Subacromialis impingement ellátásáról
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
Szinonimák: subacromialis ütközési szindróma
I. Alapvető megfontolások
1. A protokoll alkalmazási, érvényességi területe
- Ortopédia, traumatológia, rheumatológia
- Családorvos - kompetencia szintnek megfelelően
2. A protokoll bevezetésének alapfeltétele
- Ortopéd Szakmai Kollégium legitimációja
- Ortopéd szakmai minimum feltételeknek megfelelő ellátás szerint
3. Definíció
Subacromialis impingement syndroma alatt a válltájéknak típusosan a kar elevatioja és rotációja közben jelentkező, esetlegesen a felkarba sugárzó fájdalmas tünetcsoportot értjük. Jellemző, hogy a fájdalmak ágynyugalomban tovább fokozódhatnak, mely a beteg éjszakai nyugalmát zavarja.
3.1. Kiváltó tényezők (B típusú evidencia)
A kórkép lényege a tuberculum maius és acromion közötti tér beszűkülése, melynek oka lehet a két csont közötti lágyrészek megvastagodása (rotátorköpeny tendinitise, subacromialis bursa gyulladása), az acromion csontos elváltozása (Bigliani III-as acromion, illetve a coraco-acromialis szalag elcsontosodása, tuberculum majus deformálódása), a rotátorköpeny centralizáló funkciójának károsodása (izmok gyengülése vagy bénulása, inak szakadása), az inak valamint a glenohumeralis ízület tokjának zsugorodásából adódó kontraktúra a humerusfej cranialis elmozdulása folytán okozhat ütközést. További okok lehetnek a vállöv rendellenes tartása, valamint a vállízületi instabilitás egyes formái.
3.2. Kockázati tényezők
- Életkor - betegség típusosan a 4. évtizedtől jelentkezik és az életkor előrehaladtával egyre gyakoribb.
- Tartós fejfeletti munkavégzés, sportolás.
- Repetitív trauma (bizonyos sportok, vibrációs ártalom stb.).
4. Panaszok, tünetek, általános jellemzők
- Jellemző panasz a kar elevatioja során annak középtartományában fellépő fájdalom az úgynevezett fájdalmas mozgásív.
- Ugyancsakjellegzetes az éjszakai fájdalom, melyre a beteg többször felébred, és nem tud az érintett oldalra feküdni.
- A fájdalom típusosan a m. deltoideus tapadása felé sugárzik.
- A napi életvitel különböző mozdulatai (mosakodás, öltözködés, vezetés stb.) is provokálhatják a fájdalmat.
- Egy és kétoldali megjelenés lehetséges.
5. A betegség leírása
A subacromialis tér beszűkülése következtében a tuberculum majus humeri és a rajta tapadó inak (rotátorköpeny) a kar elevatioja során továbbá nyugalmi, ellazult helyzetben is az acromion alsó felszínével és a coraco-acromialis szalaggal ütközik. A kóros érintkezés következményeként a subacromialis bursa chronicus gyulladása, megvastagodása, továbbá a rotátorköpeny ödémás megvastagodása (tendinitis), később felrostozódása, részleges vagy teljes vastagságú szakadása alakulhat ki, mely önmagában is fenntartója lehet a folyamatnak.
5.1. Érintett szervrendszerek
- A subacromialis teret alkotó csontok : humerusfej, acromion, processus coracoideus
- Coraco-acromialis szalag
- Subacromialis-subdeltoidealis bursa
- Rotátorköpeny izmai és inai (elsősorban a m. supraspinatus továbbá az m. infraspinatus és a m. subscapularis)
- Egész vállövi izomzat
5.2. Genetikai háttér Genetikai háttér nem ismeretes.
5.3. Incidencia / Prevalencia / Morbiditás / Mortalitás Magyarországon
A negyedik életévtizedtől előrehaladva fokozatosan növekvő incidencia. Ritkábban fiatalabb korban is előfordulhat (sportolók, fizikai munkások). Nő:férfi arány lényegében azonos.
II. Diagnózis
1. Diagnosztikus algoritmusok
A subacromialis impingement syndroma diagnózisa pontos anamnesis felvétellel, gondos fizikális vizsgálattal és standard radiológiai vizsgálatokkal az esetek többségében biztonsággal felállítható. A vizsgálatokat a következő sorrendben, az alábbiak figyelembe vételével kell végezni.
2. Anamnesis
Vizsgálni kell a panaszok kezdetének körülményeit, esetlegesen a rotátorköpeny szakadásra utaló sérülések körülményeit, az erőbehatás jellegét vagy éppen hiányát, a beteg foglalkozását, munkakörülményeit, sporttevékenységét, az esetleges orvosi ellátással kapcsolatos dokumentumokat. Külön figyelmet kell szentelni a fájdalom jellegére, jelentkezésére és a funkciózavarra.
3. Fizikális vizsgálat
Az alábbi vizsgálatokat mindkét vállízületen el kell végezni. A két oldalon észlelt tünetek és vizsgálati lelet összehasonlításából következtethetünk a kóros elváltozásokra.
A vizsgálat megtekintéssel kezdődik, mely során megfigyeljük az esetleges nyugalmi alaki eltéréseket, izomsorvadást, tartási rendellenességeket. Ugyanezt megfigyeljük az aktív mozgások során. Az aktív mozgásterjedelmet ezután összehasonlítjuk a passzív mozgásterjedelemmel, közben figyeljük a mozgás kiváltotta esetleges fájdalmat és egyéb kóros eltéréseket (pl. intraarticularis roppanás, subacromialis crepitatio, subluxatio). Vizsgáljuk a lapocka mozgató, a rotátorköpeny és a m. deloideus erejét és a válltájék egyes pontjainak nyomásérzékenységét. A vizsgálat része egy tájékozódó felső végtagi neurológiai vizsgálat is.
4. Kötelező diagnosztikai vizsgálatok
Anamnezis értékelése, fizikális vizsgálat, képalkotó diagnosztika, szükség esetén kiegészítve laboratóriumi vizsgálattal.
4.1. Laboratóriumi vizsgálatok
Nem feltétlenül szükségesek.
Amennyiben a diagnozis alátámasztásához szükséges, végezhető általános laborvizsgálat, speciális tesztek, továbbá a subacromialis bursa és a glenohumeralis ízületi punctatum vizsgálata (általános és bacterilógiai szempontból)
4.2. Képalkotó eljárások
Minimális követelmény az érintett váll 2 irányú röntgenfelvétele, ami lehetőség szerint a glenohumeralis ízület antero-posterior és axillaris felvétele.
Szükség esetén kiegészíthető scapula lateralis felvétellel vagy egyéb speciális ferde felvételekkel. Kétes esetben elvégzendő az ép oldal összehasonlító röntgen vizsgálata. (B típusú evidencia).
5. Kiegészítő diagnosztikus vizsgálatok (B típusú evidencia).
Kétes diagnózis esetén, vagy a társsérülések tisztázása végett lehet rá szükség
- Vállöv ultrahang vizsgálata a rotátorköpeny és labrum állapotáról ad információt
- MRI vizsgálat a rotátorköpeny és labrum állapotáról valamint a csontok állapotáról ad információt
- CT és CT arthrogramm a labrum és a csontos anatómiáról ad információt
- Arthroscopos vizsgálatra ritkán, de szükség lehet azonban ez lehetőség esetén már a műtéti kezelés részét képezi.
6. Differenciál diagnosztika (B típusú evidencia)
- Rotátorköpeny szakadás
- Cervico-brachialis szindróma
- Thoracic outlet szindróma
- Glenohumeralis arthorsis
- Acromio-clavicularis arthrosis
- Rheumatoid arthritis
- Humerusfej necrosis
- Adhesivcapsulitis (befagyott váll)
- Válltáji tumorok
- Egyéb válltáji gyulladásos elváltozások (köszvény, tendinitis calcificans stb.)
- Infectio (pyogen fertőzés, tuberculosis stb.)
- Bármely válltáji fájdalommal járó kórkép.
III. Terápia
Nem gyógyszeres kezelés
1. A megfelelő egészségügyi ellátás szintje ÁNTSz minimumfeltételek alapján
2. Általános intézkedések (B típusú evidencia)
Konzervativ kezelési lehetőségek alkalmazása: fizio-, balneo terápia, manuálterápia, magnetoterápia, psychoterápia, életmódterápia. Mozgásjavító torna mozgásbeszűkülés esetén. Izomerősítő torna a rotátorköpeny gyengülése esetén.
3. Speciális ápolási teendők
Mozgássérült állapotának súlyosságától függő mértékű segédeszközzel ellátása.
4. Fizikai aktivitás (C típusú evidencia)
A panaszokat kiváltó sport vagy munkatevékenység körülményeinek felülvizsgálata, módosítása, szükség esetén szüneteltetése.
5. Diéta
Az estleges testsúlyfelesleg csökkentéséhez szükséges mértékben. Esetleges anyagcsere zavarok rendezése.
6. Betegoktatás (B típusú evidencia)
Általános betegtájékoztató, felvilágosítás, tanácsadás, életmódterápia.
III/2. Gyógyszeres kezelés
1. A megfelelő egészségügyi ellátás szintje ÁNTSz minimumfeltételekalapján
2. Speciális ápolási teendők
Csakfokozott óvatossággal és kiemelt sterilitás mellett végezhető ízületi punkció. Hasonló megfontoltságot igényel az intraartikulási injekciós therapia.
3. Ajánlott gyógyszeres kezelés (B típusú evidencia)
Per os steroid és nonsteroid gyulladáscsökkentők mérséklik a rotátorköpeny valamint a subacromialis bursa ödémás megvastagodását valamint a csökkentik a subacromialis bursában lévő folyadékszaporulatot. Mindkét mechanizmus hozzájárul az ütközés és a fájdalmak csökkentéséhez.
Subacromialis térbe adott steroid injectio hasonló mechanizimus alapján fejti ki hatását. Steril körülmények között adható.
3.1. Kontraindikációk
- Általános gyógyszer tájékoztató szerint.
- Bakteriális eredetű gyulladás.
IN/3. Műtét
1. A megfelelő egészségügyi ellátás szintje Járóbeteg ellátás: ÁNTSz működési engedély alapján.
Fekvőbeteg ellátás / műtéti tevékenység: ÁNTSz működési engedély alapján.
2. Általános intézkedések
2.1.A műtét tárgyi feltételei
- Kiemelt sterilitást biztosító műtő, az ÁNTSz minimumfeltételeknek megfelelően felszerelve.
- A műtét biztonságos kivitelezését biztosító általános műszerkészlet.
2.2. A műtét személyi feltételei
- Minősített műtéti eljárás, amelynek végzésére olyan (szak)orvos vállalkozhat, aki az műtétek kivitelezésében alapos tapasztalatot szerzett. Képes a műtét biztonságos kivitelezésére és a műtét során adódó szövődmények, komplikációk ellátására.
- Egy vagy több műtéti asszisztens.
- Anaesthesiológus orvos.
- További szakemberek: gyakorlott műtősnő, műtőssegéd.
3. Speciális ápolási teendők
A műtétet követően, a beteg általános belgyógyászati statusában felmerülő állapot-változások korrekciójának biztosítása.
4. Sebészeti kezelés (B típusú evidencia) 4.1. Műtéti indikáció
Minimum 3 hónap eredménytelen konzervatív kezelés esetén jön szóba műtét.
A műtéti indikáció felállításánál és a műtéttípus megválasztásánál a szakirodalmi utasításokat követjük. Partialis laesio esetén elegendő a részlegesen szakadt rész kimetszése és acromion plasztika. A műtétet végezhetjük nyitottan vagy arthroscoposan. Teljes szakadás esetén amennyiben a szakadás kiterjedése és a szakadt ínak állaga megengedi, törekedni kell a rotátorköpeny varratára. Rekonstruálhatatlan szakadás esetén a subacromialis tér nyitott vagy arthroscopos debridement-ja jön szóba.
4.2. Műtéti kontraindikáció
- A vállízület lágyrészeinek és/vagy csontjainak gyulladásos megbetegedése.
- Pustula, pyoderma a beteg bőrén bárhol.
- A beteg rossz általános állapota (cardiális decompensatio, sepsis, thombosis gyanúja).
- Rossz kooperációs készség.
4.3. Műtéti előkészítés
Általános belgyógyászati kivizsgálás, szükség szerinti szakorvosi konzíliumokkal kiegészítve. Anaesthesiologiai protokoll szerinti előkészítés.
4.4. Műtéti érzéstelenítés:
A műtét végezhető általános érzéstelenítésben (altatás bármely formájában) valamint vezetéses érzéstelenítésben (interscalenicus blokád) az anaesthesiologiai protokoll leírása szerint
4.5. Műtét
Beavatkozás neve: acromionplastica szükség esetén a rotátorköpeny rekonstrukciója, részleges sérülés esetén annak ellátása.
A diagnózis és technikai lehetőségek függvényében lehet arthroscopos vagy nyitott műtét Arthroscopos műtét:
Eszközigény: hidegfényoptikás videorendszer, speciális kézi műszer készlet, shaver, műtői tartozékok, folyadékpumpa, vízmentes izolálás
Az arthroscopos subacromialis decompressiot vagy az arthrocopos debridemant az irodalmi hivatkozásban listázott műtéttani könyvekben leírt műtéti technikát követve végezzük.
Nyitott acromionplasztika (+/- rotátorköpeny rekonstrukció)
Eszközigény: vállsebészeti feltáró alaptálca, speciális kézi műszer készlet, vízmentes izolálás, műtői alapfelszereltség, diatermiás eszköz.
Az indikációs szempontokat és a műtéttechnikai leírást az irodalmi hivatkozásban szereplő szakkönyvek tartalmazzák.
4.6. Posztoperációs teendők
- A műtét menetének részletes leírása, a műtéti leírás csatolása kórlaphoz, archiváláshoz.
- A közvetlen postoperatív szakban fokozott felügyelet szükséges: szívódrainen keresztül ürült mennyiség regisztrálása, folyadékháztartás (só-elektrolit, sz.sz. vérpótlás) rendezése, fájdalomcsillapítás, a beteg ált. belgy. statusának ellenőrzése érdekében.
- A postoperatív szakban a műtött végtagot levehető kartartóval, Dessault kötéssel vagy Gilchrist kötéssel immobilizáljuk.
- Kórházi ápolás 2-5 nap.
- Amennyiben alkalmaztunk draint azt a műtét után 24 órával, a varratokat 10-12 nap elteltével kell eltávolítani.
- A műtét után thrombosis profilaxis rutinszerű alkalmazása nem szükséges. A thrombosis szempontjából rizikó csoportba tartozó betegek esetén a profilaktikus antithrombotikus kezelést egyéni elbírálás alapján kell alkalmazni.
5. Fizikai aktivitás
A műtéti típustól függően, a szakkönyvek iránymutatása alapján a rögzítési idő 1-6 hét lehet, mely időtartam alatt bizonyos előírt mozgások megengedettek. A rögzítés megszűntetése után a szakkönyvek útmutatása alapján, a műtéti típustól függően kell utókezelés végezni.
6. Diéta
Általános, vagy belgyógyászati indikációnak megfelően, dietetikai előírások szerint.
7. Betegoktatás
Általános betegtájékoztató szerint. III/4. Egyéb terápia
A beteg életkorához és fizikai aktivitási szintjéhez (munka, sport) szükséges tevékenység betanítása. Az életkörülmények, munka és sporttevékenység szükség szerinti módosítása.
IV. Rehabilitáció
A kórházi tartózkodás alatt
A beteg önálló járóképességénekés önellátásának elérése fekvőbeteg osztályon, rehabilitációs részlegen, vagy házi ápolás keretében. Késői rehabilitáció
A beteg állapotának folyamatos ellenőrzése, utánkövetése, s amennyiben szükséges utókezelésre, gyógytorna kezelésre juttatása, otthoni ápolás elősegítése, sz.e. gyógyszeres kiegészítő kezelés. Végső cél a munkába való visszaállítás illetve a szokásos napi tevékenységi szint elérése.
V. Gondozás
1. Rendszeres ellenőrzés
Szövődmény mentes esetben kontroll 4 alkalommal szükséges. Az első kontroll ideje a varratszedés időpontja, majd 6 hét, 12 hét és 6 hónap.
A kontrollvizsgálatok során elegendő a fizikális vizsgálat. Radiológiai, laboratóriumi, vagy egyéb vizsgálatra csak szövődmények gyanúja esetén van szükség.
Társsérüléssel (ficam, törés, idegi sérülés) járó esetekben a postoperatív kezelés, a munkába, sportba való visszaállás időpontja a társsérüléstől függően a fenti protokolltól eltér.
2. Megelőzés
A betegséghez vezető kiváltó okok megszűntetése.
Az utókezelés során betanított gyógytorna otthoni rendszeres folytatása.
3. Lehetséges szövődmények
- Korai szövődmények:
- Infekció (valószínűsége 1% hagyományos műtőben)
- Haematoma
- Sebgyógyulási zavar
- Késői szövődmények:
- Rotátorköpeny szakadása
- Mozgásbeszűkülés
3.1. Szövődmények kezelése
Fontos a postoperatív localis szövődmények korai ellátása. Infectio gyanúja esetén korai feltárás, alapos debridement és átmosás majd szívódrainek behelyezése javasolt. Steril haematomát a műtőben steril körülmények között kell kiüríteni. Sebgyógyulási zavar, illetve bőrnecrosis esetén annak kiterjedésétől függően felületes hámosító kezelés vagy a defectus sebészi zárása szükséges (szükség esetén igénybe véve plasztikai sebész segítségét.) A késői szövődmények ellátását az adott betegségre vonatkozó szakmai szabályok szerint kell végezni.
4. Kezelés várható időtartama / Prognózis
A betegek az átlagos fizikai megterhelést igénylő munkát a műtétet követő 4-6 héten, a nehéz fizikai munkát, a sportolást a 3-6. postoperatív hónapban kezdhetik el.
5. Ellátás megfelelőségének indikátorai
A kezelés eredményességét a fájdalmak és funkciózavar megszűnése valamint a korábbi fizikai aktivitáshoz (munka, sport) való visszatérés jelentik.
VI. Irodalomjegyzék
1. Vízkelety: Az orthopaedia tankönyve Semmelweis Kiadó, 2002.
2. Campbell's Operative orthopaedics
3. Traumatológia tankönyv (szerk.: dr. Renner Antal) Medicina 2003.
4. Bulstrode et al.: Oxford Textbookof Orhopaedics and Trauma. Oxford University Press 2002.
5. Rockwood-Matsen: The Shoulder, Saunders 1990
6. Hawkins: Atlas ofshouldersurgery, Mosby 1996
7. A Magyar Thrombosis és Haemostasis Társaság Konszenzus nyilatkozata a thromboemboliák megelőzése és kezeléséről 2001.
Kapcsolódó internetes oldalak Kapcsolodó internetes oldalak www.ortopedtarsasag.hu www.gyogytorna.lap.hu www.egeszseg.lap.hu
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Gyakori társbetegségek Tankönyvi adatoknak megfelelően
2. Érintett társszakmák
Traumatológia, Reumatológia, Fizioterápia, Gyógytorna, Radiológia
3. Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Térdarthrosis ellátásáról (arthrosis deformans genus)
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
Szinonimák: Gonarthrosis, Térdartrózis, Térdízületi artrózis I. Alapvető megfontolások
1. A protokoll alkalmazási, érvényességi területe
- Ortopédia, traumatológia, rheumatológia
- Családorvos - kompetencia szintnek megfelelően
2. A protokoll bevezetésének alapfeltétele
- Ortopéd Szakmai Kollégium legitimációja
- Ortopéd szakmai minimum feltételeknek megfelelő ellátás szerint
3. Definíció:
- A térdízületet alkotó három csont (femur distalis vége, tibia proximalis vége és a patella) ízfelszínét borító hyalin-porc integritásának megbomlása, mely végső stádiumában elvezet a porcfelszín fokozatos pusztulásához és a végállapot a porcfosztott, szklerotikus,eburneált, deformált csontfelszin. Érintett rendszerint az ízületi tok,asynovialis hártya, az oldal- és keresztszalagok valamint az izomzat is.
3.1. Kiváltó tényezők
- A primer gonarthrosis pontos kóreredete tisztázatlan, kialakulásának időpontja genetikailag determinált, de exogén tényezők, mint a testsúly, foglalkozás, mindennapi igénybevétel is jelentős szereppel bír. Az életkor előrehaladtával a porcsejtek funkciója változik, proteoglykánok termelése csökken, így a porc kollagén hálózatának integritása sérül, víztartalma csökken.
- Epidemiológiai adatok (Gunther et al. 1999, 2002.) alapján e primer arthrosis teszi ki az összes műtétileg kezelt arthrosisok 65-75%-át, míg a többi az úgynevezett szekunder arthrosis, azaz prearthrotikus elváltozások és egyéb betegségek következményei.
3.2. Kockázati tényezők (B típusú evidencia - 9)
- Leggyakoribb kockázati tényezőket az úgynevezett prearthroticus elváltozások jelentik
- Posttraumás állapotok -Jelentős túlsúly
- Gyulladások (RA, JCA, specifikus és bakteriális arthritis)
- Tengely deformitások (genua vara, valga)
- Postmeniscectomiás állapot
- Condylus necrosis
-Térdízületi instabilitás (elülső keresztszalag hiány, oldalszalag elégtelenség, bizonyos neuromuscularis betegségek)
- Anyagcsere betegségek, csontdysplasiák (osteomalacia, Paget-kór, fibrosus dysplasia, dysplasia epiphysealis multiplex., stb.)
- Arthropathiák (neurogén, haemophiliás, köszvényes)
- Gyermekkori térdízületi betegségek (Tibia vara epiphysarea, osteochondritis dissecans)
-Tumoros térdízületi destrukció, tumorszerű elváltozások (Óriássejtes csonttumor, synovitis villonodularis, synovialis chondromatosis)
4. Panaszok, tünetek, általános jellemzők
- Térdfájdalom, duzzanat, mozgásterjedelem beszűkülés, instabilitás a fő tünetek.
- Mindezek eredményeképpen nehezített terhelés egészen a járásképtelenségig fokozódva.
- Egy- és kétoldali megjelenés lehetséges. -Társulhat egyéb ízületekarthrosisával (ld. etiológia).
5. A betegség leírása
A degeneratív folyamatban leginkább a porcszövet károsodása ismert. Ez rendszerint a terhelési zónában kezdődik, majd később a defektus mérete növekszik. A porc elvékonyodik, elveszti sima, fénylő jellegét, és sárgás-barnán elszíneződik. Felszíne felrostozódik, majd feltöredezik, fissurák keletkeznek, később porcfekélyek alakulnak ki. A folyamat előrehaladtával a porcfelszín fokozatosan elpusztul és a végállapot a porcfosztott, szklerotikus, eburneált csontfelszín. Széli részeken osteophyták képződnek, csonton belül szklerózis, ill. ciszták alakulhatnak ki.
5.1. Érintett szervrendszerek
A térdízületet alkotó csontok: Femur distalis vég, Tibia proximalis vég, Patella. Synovialis hártya, ízületi tok, szalagok, ízület körüli izomzat.
5.2. Genetikai háttér
Pontos kromoszóma lokalizáció nem ismeretes, családi halmozódás előfordul
5.3. Incidencia / Prevalencia / Morbiditás / Mortalitás Magyarországon
A negyedik életévtizedtől előrehaladva fokozatosan növekvő incidencia. Egyes felmérések szerint 65-74 éves populációban a gonarthrosis radiológiai tüneteinek prevalenciája 20-34%, míg klinikai tünetekkel is együtt járó, radiológiailag igazolt gonarthrosis prevalenciája 7,8-15% (Kellgren). Mozgásszervi érintettség a magyar populációban az alapellátást felkeresők között kb. 15%-os Nő:férfi arány 3:1.
Hazánkban az ortopédiai osztályokon évi kb. 3000-3500 endoprotézis beültetést végeznek.
II. Diagnózis 1. Anamnezis
A klinikai tünetek megjelenése és intenzitása függ a kiváltó októl és az elváltozás mértékétől. Fájdalom kezdetben csak mint "indítási fájdalom" jelentkezik, felálláskor, ill. a járás kezdetén. Később a fájdalom fokozódhat, huzamosabb megterhelésre, lépcsőn járáskor. Az állandósult fájdalom előrehaladt folyamatot jelezhet, persistáló, ízületi duzzanattal kisérve. A fájdalom intenzitása függ a beteg egyéni tűrőképességétől. Éles fájdalom jelentkezhet mérsékelt elváltozás mellett, máskor a súlyos degeneratív elváltozást a beteg hosszabb ideig mérsékelt fájdalommal tűri. A fájdalom lokalizálódhat az érintett ízületi résre, lehet retropatellarisan, leggyakrabban azonban a betegek általános térdízületi fájdalmat említenek.
Duzzanat megjelenése arthrosisban a degeneratív, levált porcrészletek indukálta synovitis következménye. Legtöbbször az egész térdízület bedagad, a patella ballotálható a folyadék suprapatellarisan kitapintható. A folyadékkal telt ízületet a beteg enyhén flectált helyzetben tartja, mivel az ellazított szalagok mellett mérsékeltebb a feszülés érzése.
Mozgásterjedelem beszűkülés kezdetben csak időnkénti elakadásban jelentkezik, később csökken a flexió végpontja, majd extenzió kiesése alakul ki a széli exostosisok megjelenésével egyidejűleg. A mozgásterjedelem beszűkülése megnehezíti a járást. Az extenzió elmaradás csökkenti a végtag terhelhetőségét. A flexiós tartomány csökkenése az ülő helyzetből felemelkedés képtelenségét eredményezi.
Tapintással már kezdeti arthrosisban retropatellarisan ill. az érintett ízületi résnek megfelelően enyhébb-durvább crepitáció észlelhető. A bőrhőmérséklet emelkedés inflammált folyamatra utal.
Térdízületi instabilitáshoz vezet a recidiváló folyadékgyülem kiváltotta tok és szalagrendszer lazulás. A femur és tibia condylus széli részein megjelenő exostosis fájdalmas feszességet ad az ízületnek, később azonban az ízületi felszín pusztulása oldalszalag deficitet eredményez. Az intercondylaris régióban megjelenő exostosisoknak gyakran áldozatul esik az elülső keresztszalag. Ezért az előrehaladt arthrosisban legtöbbször rotaciós instabilitás észlelhető.
2. Fizikális vizsgálatok
Térdízület (alsóvégtag) tengelyállás vizsgálat, duzzanat, bőrhőmérséklet, mozgáspálya vizsgálat, patella elmozdulás vizsgálata, instabilitás mértéke, milyensége.
3. Kötelező diagnosztikai vizsgálatok
Anamnezis értékelése, fizikális vizsgálat, képalkotó diagnosztika, szükség esetén kiegészítve laboratóriumi (általánosul ízületi punctatum) vizsgálattal.
3.1. Laboratóriumi vizsgálatok Nem feltétlenül szükségesek.
Amennyiben a diagnozis alátámasztásához szükséges, végezhető általános laborvizsgálat, speciális tesztek, továbbá az ízületi punctatum vizsgálata (általános és bacterilógiai szempontból)
3.2. Képalkotó vizsgálatok
A műtéti indikáció felállításához szükséges mindkét térdízületről kétirányú összehasonlító röntgenfelvétel készítése, kiegészítve szükség szerint terheléses (álló), ill. egyéb speciális felvételekkel (tartott, alagút) (A típusú evidencia - 5,6). Tengelyállás megítéléséhez , un. hosszú rtg. felvétel készíthető - a teljes alsó végtagról. Az ízületi képalkotó diagnosztikában további lehetőségek az UH, CT, MRI, scintigráfia csak ritkán jönnek szóba, elsősorban differenciáldiagnosztikai problémák esetén.
4. Kiegészítő diagnosztikai vizsgálatok
A térdízületi diagnosztikában speciális lehetőség az ízületi arthroscopia, amely jelenthet diagnosztikai beavatkozást, gyakrabban azonban a klinikai diagnózis eredményeképpen arthroscopos műtéti beavatkozás végezhető (ízület átöblítése, debridement, porckárosodás ellátása, stb.) (B típusú evidencia - 5,6)
5. Differenciál diagnosztika
A differenciáldiagnózisban az alábbi betegségek kerülnek szóba:
| Infect arthritisek | - Pyogen (septicus) arthritisek - Tuberculosis - Whipple kór - Gombás arthritisek |
| Gyulladásos vagy reaktív arthritisek (nem infect arthritisek) | - Systemas betegségek: R.A., SNSA - Sarcoidosis - Synovitis villonodosa pigmentosa - Nodularis tenosynovitis - Synoviális chondromatosis |
| Anyagcsere betegségek ízületi manifesztációval | - Amyloidosis - Köszvény - CPPD kristály indukálta arthropathia - Hydroxyapatit okozta lerakódások az ízületben. - Ochronosis |
| Arthropathiák | - Neurogen, hemophyliás, anyagcsere-zavar okozta |
| Csontnecrosisok |
6. Diagnosztikai algoritmusok
Anamnezis - fizikális vizsgálat - képalkotó diagnosztika - sz.e. laborvizsgálat - arthroscopia.
III. Kezelés
Nem gyógyszeres kezelés
1. A megfelelő egészségügyi ellátás szintje ÁNTSz minimumfeltételekalapján
2. Általános intézkedések (B típusú evidencia -1,8)
Konzervativ kezelési lehetőségek alkalmazása: gyógytorna, fizio-, balneo terápia, manuálterápia, magnetoterápia, psychoterápia, életmódterápia.
3. Speciális ápolási teendők
Mozgássérült állapotának súlyosságától függő mértékű segédeszközzel ellátása.
4. Fizikai aktivitás
Törekedni kell a mozgássérült segédeszköz nélkül, vagy annak segítségével történő minél teljesebb fizikai aktivitásának biztosítására, ill. annak elősegítésére.
5. Diéta (B típusú evidencia - 8)
Az estleges testsúlyfelesleg csökkentéséhez szükséges mértékben.
6. Betegoktatás (B típusú evidencia - 8)
Általános betegtájékoztató, felvilágosítás, tanácsadás, életmódterápia.
IN/2. Gyógyszeres kezelés
1. A megfelelő egészségügyi ellátás szintje ÁNTSz minimumfeltételekalapján
2. Speciális ápolási teendők
Tekintettel arra, hogy steril gyulladásos folyamat eredménye a folyadékgyülem, csak fokozott óvatossággal és kiemelt sterilitás mellett végezhető ízületi punkció. Hasonló megfontoltságot igényel az intraartikulási injekciós therapia.
3. Ajánlott gyógyszeres kezelés
Asteroid és nonsteroid gyulladáscsökkentők mérséklikaz ízületi exsudatum újratermelődését, a fájdalmat enyhitik, de tartós alkalmazásuk mellett az arthrosis progrediálhat a jól észlelhető és fenyegető tünetek nélkül! Steroid injectio javallata az exsudativ synovitis, ha az ízületi folyadékgyülem NSAID-dal nem szűntethető meg. Steril körülmények között adható. (B típusú evidencia - 4,7) Kontraindikáció: bakteriális eredetű synovitis.
Per os, illetve intraartikulárisan alkalmazható chondroprotektiv szerek a kezdeti porclaesió esetén alkalmazhatók. A kezelés eredményessége csak a kiváltó ok egyidejű megszüntetésével remélhető. (A típusú evidencia - 3) A konzervatív kezelés előnye az, hogy a betegség korai szakaszában a tünetek és panaszok jól befolyásolhatók. Előrehaladt arthrosisban viszont az izomerősítés és gyógytorna jó előkészítője az eredményes műtéti megoldásnak.
3.1. Kontraindikációk
Általános gyógyszer tájékoztató szerint.
III/3. Műtét
1. A megfelelő egészségügyi ellátás szintje
Járóbeteg ellátás: ÁNTSz működési engedély alapján.
Fekvőbeteg ellátás / műtéti tevékenység: ÁNTSz működési engedély alapján.
2. Általános intézkedések A műtét tárgyi feltételei
Kiemelt sterilitást biztosító műtő, az ÁNTSz minimumfeltételeknek megfelelően felszerelve.
A műtét biztonságos kivitelezését biztosító általános műszerkészlet.
Az esetleges implantáció kivitelezéséhez szükséges speciális műszerkészlet.
A tervezett implantációs eszköz teljes méretválasztékából egy sorozat.
Leggyakoribb szövődmények ellátásához szükséges műszerek, implantátumok megléte.
A műtét személyi feltételei
Minősített műtéti eljárás, amelynek végzésére olyan (szak)orvos vállalkozhat, aki az implantációs műtétek kivitelezésében alapos tapasztalatot szerzett. Az implantáció területén olyan gyakorlata van, hogy képes a műtét biztonságos kivitelezésére és a műtét során adódó szövődmények, komplikációk ellátására. Egy vagy több műtéti asszisztens. Anaesthesiológus orvos.
További szakemberek: gyakorlott műtősnő, műtőssegéd.
3. Speciális ápolási teendők
A műtétet követően, a beteg általános belgyógyászati statusában felmerülő állapot-változások korrekciójának biztosítása.
4. Sebészeti kezelés
Prearthrosisban végzett preventív műtétek
Az arthroscopia így fokozatosan a térdízületi differenciál diagnosztika egyik leglényegesebb láncszemévé vált, mivel alkalmazásával az intraartikulás diagnózist követően közvetlenül therapiás-operatív beavatkozásra van mód. A preventiv műtétek célja, az arthroticus elváltozás kialakulásának, ill. progressziójának megakadályozása. A beavatkozás jellege a kiváltó októl függ, így térd instabilitás esetében oldalszalagok, keresztszalagok rekonstrukciója, meniscus lesio esetén partialis meniscectomia,vagy meniscus visszavarrása, ízületbe hatoló törések esetén anatómiás rekonstrukció, bakteriális arthritis esetén synovectomia, gyógyszeres kezelés, stb.
Az alsóvégtag tengelydeformitásai esetén tengelykorrekciót végzünk, s ezzel a frontalis sikban centralizáljuk az alsó végtag mechanikai tengelyét, amelynek eredményeképpen kiegyenlítődik a terhelés mindkét szektorban, azaz csökken az egységnyi felületre jutó terhelés. A patella degeneratív elváltozásai esetén, ha a kiváltó okot /pl. avt.-i tengelydeformitás/nem sikerül időben megszüntetni, hosszabb-rövidebb időn belül térdízületi panarthrosis alakul ki. Ennek megakadályozását célozzák az időben elvégzett proximalis és distalis tehermentesitő mütétek. A fenti beavatkozások indikációit és kontraindikációit lásd egyéb szakmai protokollokban, kézi könyvekben.
Chondropathiáknál, körülírt porcdefektusoknál, arthrosis kezdeti stádiumában végzett műtétek (C szintű evidencia -11)
- synovectomia: incikációja egyéb konzervatív kezeléssel nem befolyásolható proliferatív, vagy folyadékgyülemmel járó synovitis
- arthroscopia: végezhető diagnosztikus céllal, kiegészíthető ízület átöblítésével, debridementtel, porcfekélyek széleinek lesimításával (shavelés), porcfekélyek felfúrásával, microfracturájával
lateralis retinaculum bemetszése: patellofemoralis chondropathia, lateralizált feszes alacsony állású patella esetén
- magas tibia, ill. supracondylar femur osteotomia: tengely deformitások esetén fiatalabb érett korban, ha még nem alakult ki a porcfelszín teljes subchondralis csontig történő lepusztulása
- mozaik plastica: körülírt 2-2,5 cm átmérőjű (fokális chondralis és/vagy osteochondralis) porcdefektusok esetén 40 év alatt
- autológ chondrocyta transplantatio: nagyobb 3-4 cm átmérőjű körülírt porcdefektusok esetén (jelenleg még kísérletes stádiumban van, igen költséges)
Műtéti beavatkozások gonarthrosis késői stádiumában
1. Lateralis retinaculum release: ritkán indikált, ha a beteg általános belgyógyászati állapota total endoprothesis beültetését nem engedi meg és elsősorban feszes patella, retropatellaris fájdalom dominál.
2. Arthrodesis: ritkán végezzük, mivel a mozgó ízület megtartására törekszünk. Rendszerint septicus szövődmények eredménytelen kezelése után, nagy csontvesztést követően, vagy olyan esetben végezzük, ahol egy jól terhelhető végtag elérése az elsődleges cél.
3. Arhtroplastica (C szintű evidencia - 5,10)
- Szánkó protézis (unicompartmentális protézis)
- Teljes felszínpótló protézisek
- Csuklós protézis
A degeneratív és destruktív elváltozások késői fázisaiban, amikor már jelentős mértékben károsodott az ízületi porcfelszín és végső soron az ízületi funkció dezintegrációja következett be, endoprothetikai megoldást kell választani. Ennek célja a panaszok csökkentésén túl a végtag biomechanikájának, funkciójának rekonstrukciója.
- Szánkó protézis indikációja: egy compartmentre korlátozódó arthrosis
Kontraindikációk: 10-15 fokot meghaladó tengelydeformitás (fixált varus), 10 fokot meghaladó flexios contractura, elülső keresztszalag hiány, oldalszalag elégtelenség, patellofemoralis arthrosis, panarthrosis, kiterjedt condylus necrosis, jelentős obesitas, súlyos osteoporosis, ha a folyamat rohamos progressziója várható.
- Teljes felszínpótló protézis indikációja: panarthrosis, csonthiányból és/vagy szalag elégtelenségből adódó instabilitás.
Kontraindikáció: súlyos szalag elégtelenség, kiterjedt csontdefektus, localis septicus folyamat, arthrodesis utáni állapot, extensor izomfunkció elégtelensége, súlyos contracturák.
Fajtái: hátsó keresztszalag megtartó forma, hátsó keresztszalag pótló forma, szuper stabilizációs forma (semiconstrained).
- Csuklós (zsanéros, constrained) protézis indikációja: a kereszt- és oldalszalagok teljes elégtelensége, jelentős csonthiány, ha az arthrosis a fenti protézisekkel biztonsággal nem operálható.
4.1. Általános műtéti indikációk
A térdízület arthrosis sebészi kezelése indokolt, amikor a konzervatív kezelésre nem csökken a fájdalom, terhelési nehezítettség, a mozgástartomány beszűkülés, instabilitás (tok és szalagrendszer meggyengülése), valamint a következményes izomatrophia - már nem tolerálható életminőség-csökkenést eredményez a beteg életvitelében és a sebészi beavatkozás eredményességének megítélése meghaladja a kockázati tényezők mértékét. A beteg panaszai, a klinikai tünetek és a képalkotó eljárásokkal készített felvételek alapján az ízület funkciója, konzervatív kezeléssel, vagy más eljárással helyre nem állítható.
A térdízületi arthroplastica akkor jön számításba amikor a funkcióromlás hátterében olyan morfológiai elváltozás szerepel, amelyet konzervatív kezelési eljárásokkal eredményesen befolyásolni nem tudunk és további javulás már nem várható. Ezért a jelentősen degenerált vagy destruált térdízületek esetében gyakran a rehabilitáció egyetlen lehetősége, az endoprothesis beültetés.
Az endoprothesis beültetés megítélését differenciált módon kell kezelni: a klinikai tünetek, radiológiai eltérések és az intraoperativ lelet összehangolásával.
4.2. Műtéti kontraindikáció
A térdízületi endoprothesis implantációját kontraindikáló tényezők. Általános tényezők:
- A beteg kooperálóképességének hiánya. Amennyiben a beteg képtelen a postoperatív együttmüködésre az operatőr és a gyógytornász utasításainak végrehajtására, a teherviselés fokozatosságának betartására, nem várható jó eredmény, akármilyen típusú implantátumot ültetünk be. A várható komplikációk leküzdése után az eredmény rosszabb lehet, mint a kiindulási állapot. Ezekben az esetekben alternatív megoldást kell keresni. Ez lehet térdtok viselete, vagy konzervatív kezelés.
- Az elhízott túlsúlyos betegnél nagyobb a perioperativ szövődmény rizikója, az intraoperatív technikai problémák előfordulása, a prothezis lazulás valószínűsége. Mindezek alapján érthető, ha a sebész a súlycsökkenésig elhalasztja a műtétet. Természetesen az is igaz, hogy a fájdalom miatt csökkent aktivitású betegnél nehéz a testsúlycsökkenést elérni.
- Az alsó végtagi varicositas fokozza a mozgásszervi betegek műtétjei után előforduló thrombozis veszélyét. A thromboemboliás szövődmények rizikójánakcsökkentése érdekében a súlyosabb esetekben célszerűbb a műtételőtt érsebész szakvéleményét kikérni, és thrombozis profilaxist végezni.
A térdprothesis beültetést abszolút kontraindikáló tényezők.
- Súlyos cardiorespiratorikus megbetegedés.
- Aktiv szeptikus állapot.
- Súlyos végtagkeringési zavar.
- Neurogen arthropathia
- Neurológiai, posttraumás, vagy idiopathias okból kiesett quadriceps funkció.
- Ankylotizalt térdízület
Ilyenkor a sebésznek le kell mondania az arthroplasztikáról és alternatív megoldást kell keresnie.(Konzervatív kezelés folytatása, antiflogisztrikum, különböző térdrögzítők, speciális segédeszközök alkalmazása)
4.3. Műtéti előkészítés
Általános belgyógyászati kivizsgálás, szükség szerinti szakorvosi konzíliumokkal kiegészítve. Anaesthesiologiai protokoll szerinti előkészítés. Antibiotikus- és thrombozis profilaxis útmutatásai alapján.
4.4. Műtéti érzéstelenítés Anaesthesiologiai protokoll leírása szerint
4.5. Műtét (térdízületi arthroplastica)
A műtét kivitelezése a műtéttechnikai leírásoknak megfelelően:
- A beteg asztalra történő fektetése, rögzítése.
-A műtéti területen a bőrszőrtelenítéseés fertőtlenítése. (Előírt fertőtlenítőszerrel combtól bokáig, sz.sz.a lábat is.). A sterilitás szabályainak betartásával az operálandó terület izolálása, inciziós fólia felhelyezése.
- Az ízület feltárása, az ismert műtéttechnikai leírásoknak megfelelően.
-Az elülső és hátsó keresztszalag állapotától, a térdízület instabilitásától, illetve a degeneratív folyamat kiterjedésétől függő protézis típus megválasztása.
- A kiválasztott protézis femoralis, tibialis és esetleg a patelláris komponenseinek megfelelő hely kialakítása (speciális célzó eszközök használata).
- A protézis próba-komponenseinek beillesztése és próba (stabilitás, mozgástartomány). A fiziológiás tengelyállást továbbá a stabilitást biztosító kiegészítő lágyrész felszabadítások elvégzése.
- A megfelelő méret kiválasztása után a végleges protézis-komponensek beültetése, rögzítés cementezéses, vagy cementnélküli technikával.
- Szívódrainek behelyezése, rögzítése, majd réteges sebzárás.
- A seb környékének lemosása, fertőtlenítése, steril fedése.
- A végtagra rugalmas pólya felhelyezése (mechanikus thrombozis profilaxis).
4.6. Posztoperációs teendők
- A műtét menetének részletes leírása, a műtéti leírás csatolása kórlaphoz, archiváláshoz.
- A beültetett implantatum helyzetének ellnőrzése kontroll képalkotó eljárással, legkésőbb 72 órán belül..
- A beültetetett implantátum dokumentálása műtéti leíráson, archiváláshoz.
- A közvetlen postoperatív szakban fokozott felügyelet szükséges: szívódrainen keresztül ürült mennyiség regisztrálása, folyadékháztartás (só-elektrolit, sz.sz. vérpótlás) rendezése, fájdalomcsillapítás, a beteg ált. belgy. statusának ellenőrzése érdekében.
- Antibiotikus , thrombozis profilaxis, sz.sz. alapbetegség spec. gyógyszerelése.
4.7. A térdprotézis beültetés lehetséges szövődményei
1. Intraoperatív: keresztszalag, oldalszalagok átmetszése, érsérülés, condylusok lerepesztése. Egyes komponensek rossz helyzetben történő beültetése.
2. Korai posztoperatív: A térdízület kereszt, ill. oldalszalagjainak utólagos megnyúlása, szakadása. Kiváltó oka a térdízületi arthrózis, ill. gyulladás progressziója, a prímer műtét residuális tengelydeformitása. Megoldása a protézis revíziója, tengelykorrekciója, magasabb constrained fokozatú implantátum beépítése. Inoperabilitás esetén brace viseltetése.
A protézis luxációja: alulméretezett femorális komponens, alacsony tíbiakomponens okozhatja. Kezelése repozíció, brace-viselés, ismétlődés esetén revízió a megfelelő irányelvek figyelembevételével.
Előfordulhat ezen felül térdízületi feszítő hematoma, melynek lebocsátása szükséges, sebgyógyulási zavar, mélyvénás thrombosis.
3. Késői komplikáció: Aszeptikus lazulás: rendszerint 10 éves körüli túlélés után várható. (C szintű evidencia -10) A korai aszeptikus lazulás rendszerint suboptimális tengelyállás következménye, a kezelés korai revízió, a tengelyállás korrekciója, lágyrész-balance biztosítása.
Szeptikus komplikáció: korai (akut, szubakut) és késői formában jelentkezik.
Korai, akut forma: műtéttől négy héten belül, kifejezett lokális gyulladásos tünetekkel jelentkezik. A mikrobiológiai diagnózis megérkezéséig széles spektrumú antibiotikum terápia, ízületi feltárás, debridement esélyt ad a protézis megmaradására a kórokozó virulenciájától függően.
Szubakut forma: a műtét utáni 4-12. hétben kezdődik, lappangva, mitigált lokális tünetek (fájdalom, duzzanat, bőrhőmérséklet emelkedés, esetleg bőrpír, mozgáskorlátozottság), de a laborleletekben We- emelkedés, magas CRP, thrombocytaszám kíséretében. A röntgen és izotópvizsgálat nem jellemző, később gallium és indiummal jelzett fehérvérsejtes izotóp vizsgálat kórjelző lehet. Punkció, mikrobiológiai diagnózis szükséges, célzott antibiotikum terápia, feltárás megkísérlendő a protézis megmentésére. A szubakut gyulladás gyakran átmegy krónikusba, és ekkora protézis eltávolítása, célzott antibiotikummal dúsított csontcement "spacer" behelyezése, tartós antibiotikum kezelés szükséges. A gyulladás szanálása után (ismételt negatív leoltások, laborértékek rendeződése, klinikai tünetek regressziója) a reimplantáció megkísérelhető, rendszerint 6-12 héttel az implantátumok eltávolítását követően. Ha erre nincs remény (többszörös flóra, Gram negatívcoccusok),arthrodesis vagy reszekciósarthroplasztika a megoldás. Késői (hematogén) gyulladás rendszerint a protézis radiológiai kilazulásával, lokális és általános gyulladásos tünetekkel, jellemző laborparaméterekkel jár.(ld.fenti). Kezelése teljes debridement, protézis eltávolítás, egy- vagy kétüléses protézis csere. A szeptikus komplikációk kezelése hónapokat vesz igénybe, 80-90%-ban eredményes.
5. Fizikai aktivitás
A gyógytorna kezelés megkezdése előtt orvosi vélemény szükséges, hogy a műtéti körülmények függvényében, egyéni megítélés és mérlegelés alapján, a beteg az operált végtagját teljes testsúllyal mikortól terhelheti.
Első nap izometriás, véna és légzőtorna, flexios-extensios gyakorlatok, egyedi megítélés szerint. Második nap torna, mobilizálás folytatása. (B szintű evidencia - 5)
További mobilizálás, járás megkezdése tehermentesítés mellett.
Kontroll vizsgálatok alapján egyénileg meghatározott fokozatos terhelési program szerint.
6. Diéta
Általános, vagy belgyógyászati indikációnak megfelően, dietetikai előírások szerint.
7. Betegoktatás
Általános betegtájékoztató szerint. Implantátum egyedi előírásainak megfelelően. Gyógytornász utasításainak megfelelően.
IV. Rehabilitáció
Rehabilitációs igény
A kórházi tartózkodás alatt: a beteg önálló járóképességének és önellátásának elérése fekvőbeteg osztályon, rehabilitációs részlegen, vagy házi ápolás keretében. Késői rehabilitáció
A beteg állapotának folyamatos ellenőrzése, utánkövetése, s amennyiben szükséges utókezelésre, gyógytorna kezelésre juttatása, otthoni ápolás elősegítése, sz.e. gyógyszeres kiegészítő kezelés.
V. Gondozás
1. Rendszeres ellenőrzés
A beteg általános mozgásszervi állapotának, az operált ízület rendszeres felügyelete, utánvizsgálata szükséges a műtétet követő 6-12 héten, majd fél év, egy évvel később. Ezt követően panaszok esetén ill. egy-két évente.
Röntgenkontroll közvetlen műtét után, fél-egy év múlva, ill. panasz esetén és az operáló osztály útmutatása szerint.
2. Megelőzés
Bekövetkező állapotromlás esetén haladéktalan beavatkozás szükséges: utókezelés, rehabilitáció, sz.e. reoperáció.
3. Lehetséges szövődmények
Infekció (korai) valószínűsége 3-5% hagyományos műtőben.
Késői infekció, haematoma, sebgyógyulási zavar, thrombophlebitis, mélyvénás thrombosis, tüdő embólia, femur, illetve tibia condylus törés, igen ritkán ér- és ideg károsodás, protézis törés.
4. Szövődmények kezelése
A 4.pontban felsorolt szövődmények kezelésének haladéktalan megkezdése szükséges.
Fontos a postoperatív localis szövődmények korai ellátása. Infectio gyanúja esetén korai feltárás, alapos debridement és átmosás majd szívódrainek behelyezése javasolt. Steril haematomát a műtőben steril körülmények között kell kiüríteni. Sebgyógyulási zavar, illetve bőrnecrosis esetén annak kiterjedésétől függően felületes hámosító kezelés vagy a defectus sebészi zárása szükséges (szükség esetén igénybe véve plasztikai sebész segítségét.)
5. Kezelés várható időtartama/Prognózis
Az implantációs technikától függően, továbbá a beteg egyedi mozgásszervi statusából következően egyedi felépülési prognózist kell megállapítani, amelyben törekedni kell az életminőség javításának legrövidebb, de legbiztosabb módjára.
6. Az ellátás megfelelőségének indikátorai
Műtét utáni fájdalommentesség, mozgástartomány. Beültetett protézis helyzete (rtg.), lágyrész balance. Nemzetközi térdvizsgálati protokollok kiértékelése (knee scorok).
A műtött beteg általános és speciális mozgásszervi állapotának rögzítésének dokumentálása szükséges az állapotváltozás utánkövetése érdekében.
Az Arthroplasztika Regiszter használata segítségével rögzíthető a beteg és implantátum túlélési görbéje és a nemzetközi eredményekkel összehasonlítás végezhető.
VI. Irodalomjegyzék
1. Gunther KP, Puhl W, Brenner H, Sturmer T.: Clinical epidemiology of hip and knee osteoarthritis:The Ulm Osteoarthritis Study. Zeitschrift für Rheumatologie 61 (3): 244-249,2002.
2. Gunther KP, Sturmer T, RepteCT, NaumannT, Kinzl L., Puhl W.: Prevalenceof local riskfactorsin patients withadvanced hip and knee osteoarthritis in the Uim osteoarthritis study. Aim of study. Zeitschrift für Orthopadie und Ihre Grenzgebiete 137(6): 468-473,1999.
3. Vízkelety T. (szerk.): Az ortopédia tankönyve. Semmelweis Kiadó, 2002. Kapcsolodó internetes oldalak www.ortopedtarsasag.hu www.gyogytorna.lap.hu www.egeszseg.lap.hu Evidencia meghatározásánál felhasznált irodalom
1. Petrella RJ. Is exercise effective treatment for osteoarthritis of the knee? British Journal of Sports Medicine 2000,34(5), 326-331
2. The Database of Abstracts of Reviews of Effectiveness (University of York), Database no.: DARE-20002058. In: The Cochrane Library, Issue 2,2002. Oxford: Update Software
3. Towheed TE, Anastassiades TP, Shea B, Houpt J, Welch V, Hochberg MC. Glucosamine therapy for treating osteoarthritis. Cochrane Database Syst Rev. 2004;(2):CD002946.
4. The Database of Abstracts of Reviews of Effectiveness (University of York), Database no.: DARE-980948. In: The Cochrane Library, Issue 2,2000. Oxford: Update Software
5. Callahan CM, Drake BG, Heck DA, Dittus RS. Patient outcomes following unicompartmental or bicompartmental knee arthroplasty: a meta-analysis. J Arthroplasty 1995;10:141-150
6. The Database of Abstracts of Reviews of Effectiveness (University of York), Database no.: DARE-950771. In: The Cochrane Library, Issue 4,1999. Oxford: Update Software
7. Towheed TE, Hochberg MC. A systematic review of randomised controlled trials of pharmacological therapy in osteoarthritis of the knee, with an emphasis on trial methodology. Semin Arthritis Rheum 1997;26:755-770
8. The Database of Abstracts of Reviews of Effectiveness (University of York), Database no.: DARE-970656. In: The Cochrane Library, Issue 4,1999. Oxford: Update Software
9. Roos H, Lauren M, Adalberth et al. Knee osteoarthritis after meniscectomy. Prevalence and radiographic changes after twenty-one years compared with matched controls. Arthritis Rheum 1998;41:687-693
10. Jordan KM, Arden NK, Doherty M, Bannwarth B, Bijlsma JW, Dieppe P,Gunther K, Hauselmann H, Herrero-Beaumont G, Kaklamanis P, Lohmander S, Leeb B, Lequesne M, Mazieres B, Martin-Mola E, Pavelka K, Pendleton A, Punzi L, Serni U, Swoboda B, Verbruggen G, Zimmerman-Gorska I, Dougados M: EULAR Recommendations 2003: an evidence based approach to the management of knee osteoarthritis: Report of a Task Force of the Standing Committee for International Clinical Studies Including Therapeutic Trials (ESCISIT). Ann Rheum Dis. 2003 Dec;62(12):1145-55.
11. Brouwer RW, Jakma TSC, Bierma-Zeinstra SMA, Verhagen AP, Verhaar Jan. Osteotomy for treating knee osteoarthritis. In: The Cochrane Library, Issue 1,2005. Chichester, UK: John Wiley & Sons, Ltd.
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Gyakori társbetegségek Tankönyvi adatoknak megfelelően
2. Érintett társszakmák
Traumatológia, Reumatológia, Fizioterápia, Gyógytorna, Radiológia
3. Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
A csípőficamról
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
Szinonimák: A csípő fejlődési dysplasiája (angol rövidítése DDH) Veleszületett csípőficam (angol rövidítése CDH) A csípő dysplasiás fejlődése Luxatio coxae congenita Dysplasia coxae congenita Instabil csípő
A csípőízület hibás fejlődése
I. Alapvető megfontolások
1. A protokoll alkalmazási/érvényességi területe Ortopédia, gyermekgyógyászat, radiológia.
2. A protokoll bevezetésének alapfeltétele
Jól szervezett szűrővizsgálat, UH vizsgálat lehetősége, jól működő gyermekortopédiai osztályok és rendelések.
3. Definíció
Acsípőízület olyan állapota, amelyben a csípő alkotóelemei nem fejlődnek adekvát módon. Két jellemző komponens van:
- Az acetabulum tető meredeksége, sekély ízvápa.
- A csípőízület lazasága, amely lehetővé teszi a femurfejkicsúszását a vápából.
3.1. Kiváltó tényezők Öröklődés.
Mechanikai, külső tényezők, intrauterin, relatív térszűkület, a születés után az alsó végtagok szoros összepelenkázása.
3.2. Kiváltó és kockázati tényezők (B szintű evidencia - 5,15 ,17) Női nem
Családi előfordulás
Farfekvéses szülés
Egyéb intrauterin térszűkület
Torticollis, 7-es szindróma
Alsó végtagi fejlődési rendellenességek
4. Panaszok, tünetek, általános jellemzők
A szülők a csípők aszimmetriáját, az alsóvégtagok kifelé fordulását, esetleg rövidülését észlelik, az újszülött vagy csecsemő az érintett végtagját kevésbé mozgatja.
5. A betegség leírása
5.1. Az érintett szervrendszerek: csípő, alsó végtag
5.2. Genetikai háttér: (B szintű evidencia - 6)
Polygen öröklődés figyelhető meg. A polygen öröklődés szabályai szerint valószínűsíthető a csípőficamos családban az előfordulás a születendő gyermeknél. 5.3.1. Incidencia: (B szintű evidencia -16,18)
Az élve szülöttekre szokták megadni a veleszületett csípőficam gyakoriságát. Az adatok rendkívül eltérőek és nem csak aszerint, hogy csak a valódi ficamot, vagy az instabil csípőt és a dysplasiát is beszámítják. Magyarországon az utolsó felmérés alkalmával (1977) 1.5%-ban találtak luxatiot, instabil csípőt vagy dysplasiát. Az utolsó évek észlelése szerint, UH vizsgálatot is felhasználva, ez a szám lényegesen csökkent (0,2-0,5%). 5.3.2. Morbiditás, mortalitás: a secunder coxarthrosis leggyakoribb kiváltó oka.
5.4. Születés után felismerhető a luxatio és az instabil csípő. UH-val a dysplasia is.
5.5. Jellemző nem: Leányoknál négyszer-hatszor gyakoribb, mint fiúknál. (B szintű evidencia -15)
II. Diagnózis
1. Diagnosztikus algoritmus (lásd. később)
2. Anamnézis
A terhesség és szülés körülményeiről tájékozódunk. Farfekvés, farfekvéses szülés rizikótényezők. Ha a családban volt már csípőficam, előfordulásának nagyobb a valószínűsége. A szülők gyakran említenek alsó végtag aszimmetriát, egyik alsó végtagnak a rövidülését, ráncaszimmetriát. Egyik alsó végtag mozgása csökkent lehet a másikhoz képest.
3. Fizikális vizsgálat
Az anya azon megfigyelése mögött, hogy a csecsemő egyik alsó végtagját kevésbé mozgatja, gyakran dysplasia vagy ficam rejtőzik. A csípőficam az általános mozgásfejlődésben is (ülés, állás, járás) okozhat visszamaradást. A pelenkából vizsgálatra kibontott csecsemőt először megtekintjük. A végtagokaszimmetrikus helyzete, a kóros oldali végtag kifele rotatiós tartása, ráncaszimmetriája dysplasia vagy ficam gyanúját keltheti. A kóros oldalon több a ránc és mélyebbek, mint az ellenkező oldalon és lányoknál az inguinalis redő elfedheti a nagyajkat
A combok háti oldalán jelentkező ráncaszimmetria, amely akkor is fennáll, ha a végtagokat szimmetrikus helyzetbe hozzuk, már biztosabban értékelhető. Feltűnhet, hogy a csecsemő egyik alsó végtagját kevésbé mozgatja. Ha az egyik csípőízületben abductios contractura áll fenn, a végtagokat összetéve a másik, az adductioban levő rövidebbnek látszik. Szimmetrikus helyzetben ez a látszólagos hosszkülönbség eltűnik. Az abductios csípőcontractura jelentősége abban van, hogy az ellenkező oldali adductios helyzet dysplasia kialakulására hajlamosít.
A csípőket a vizsgálóasztalra fektetett csecsemővel szemben állva vizsgáljuk. Megfogjuk mindkét lábszárát és erőszak nélkül, az esetleg feszítő csecsemő ellenállását fokozatosan legyőzve, a térdeket maximálisan, a csípőket 90o-ig behajlítjuk.
Ezután megfigyelhetjük, hogy a térdek egy magasságban vannak-e, majd caudalis irányból megtekintjük a csípők kontúrját. Luxatio esetében a nagy tompor tájéka a csípő kontúrjából előemelkedik.
A csípők 90o-os flexios helyzeténekés a térdek teljes flexiojánakelérése után a combokat egymástól eltávolítjuk. Ha a csecsemő nem feszít, a csípők ép viszonyok mellett 70-90o-nyit abducálhatók. Ha a csecsemő megfeszíti izomzatát, esetleg csak20-30o-os abductio érhető el. A vizsgálat óvatosan végzendő, mert a combcsont proximalis részén törést is lehet okozni. A lehetséges abductio fokát megállapítjuk úgy is, hogy közben a flexios helyzetet csökkentjük és fokozzuk.
Instabil csípőnél a csípőízület lazasága miatt a combfej könnyen elhagyja a vápát. A luxalhatóság vizsgálatához behajlítjuk a csípőket, és a maximálisan behajlított térdeket átfogjuk úgy, hogy hüvelykujjunka comb belső oldalán, a többi négy ujjpedig a nagy trochanter tájékán van. Az egyik kezünkkel tartott combbal rögzítjük a medencét, a másik kezünkkel pedig vizsgáljuk az ellenoldali csípőt. Végezhető a vizsgálat úgy is, hogy egyik kezünkkel átfogva a gátat rögzítjüka medencét. Ha ebből a helyzetből a comb proximalis részét hüvelykujjunkkal oldalfelé és az egész combot a comb tengelyének irányában hátrafelé nyomjuk, luxalható csípő esetén a fej kis zökkenés kíséretében elhagyja a vápát. Ellenkező irányú mozgatásra a combfej reponálódik. Az oldalirányú mozgatás a vizsgáló kéz pronatios-supinatios. Előfordul, hogy vizsgálat közben csak azt észleljük, hogy a femurfej eltávolodik a vápából, de nem hagyja el. Ezekből a laza csípőkből is gyakrabban alakul ki ficam, mint a normális csípőknél. Luxatio esetén távolításkor a combfej zökkenés kíséretében reponálódhat, adductiora pedig elhagyja a vápát. A zökkenést olykor kattanásszerű hang kíséri. Ez a repozíciós-luxatios jel (Ortolani-tünet).
Külön-külön is megvizsgáljuk mindkét oldalt. A csípőket abducáljuk úgy is, hogy közben a femurt hossztengelyének irányában meghúzzuk és a nagy tompor tájékára előrefelé irányuló nyomást gyakorolunk. Így reponálódhat a femurfejakkor is, amikor egyszerű abductiora nem sikerült repozíciós jelet észlelni.
Egyéb jelek, mint a magasan tapintható nagytompor, a Lorenz-abductio nagyfokú korlátozottsága ficam fennállására utalnak. Idősebb csecsemőkön és kisgyermekeken veleszületett csípőficamnál is olyan mérvű adductios contractura alakulhat ki, hogy abductiora a repozíció nem jön létre. Ha nem túl nagy az adductor-feszülés, a combfej repozíciós manőverrel a vápába juttatható, és így biztosan megállapítható a ficam. Tekintve, hogy az erőszakolt repozíció a femurfejet sértheti, helyesebb a pontos kórisme érdekében inkább röntgenfelvételt készíteni. A vizsgálat utolsó fázisaként a csecsemőt hasra fordítjuk és megvizsgáljuk, hogy a csípők adducálhatók-e. Egyik oldalon a csípőízületet abductioba hozzuk, majd megnézzük, hogy a másik oldal a középvonalon túl adducálható-e. A vizsgálatot mindkét oldalon elvégezzük.
Az instabil csípő és a luxatio fizikális vizsgálattal felismerhető. Dysplasia azonban teljes biztonsággal csak ultrahanggal vagy röntgenfelvétel alapján kórismézhető.
Dysplasia gyanúja merül fel, ha:
1. a hason fekvő csecsemőn feltűnő ráncaszimmetria van és a csípőket megtapintva, azokat aszimmetrikusnak találjuk;
1. a csípők Lorenz-abductioja (hajlított helyzetben végzett abductio) korlátozott, kevesebb, mint 60o;
2. abductios pelenkázásra vagy betétes Rugi-nadrág viselésére a contractura nem oldódik.
Az anamnesisben szereplő adatok vagy a vizsgálat alkalmával észlelt tünetek alapján felmerült dysplasia gyanúja esetén indokolt az ultrahangos vizsgálat és szükség szerint 4 hónapos kor körül az ortopéd szakorvos készíthet röntgenfelvételt.
A subluxatio klinikai tünetei lényegében megegyeznek a dysplasia tüneteivel, de kifejezettebbek lehetnek. A már álló, járó gyermeknél a Trendelenburg-tünet is vizsgálandó. Ha a gyermek egyik lábát felemeltetjük, normál körülmények között a felemelt oldali glutealis vonal a vízszintes fölött van, az álló oldali csípő abductorok insufficienciája esetén lesüllyed.
4. Kötelező diagnosztikai vizsgálatok, szűrővizsgálatok - a csípőficam szűrővizsgálati rend algoritmusa Magyarországon
Folyamatosan valósult meg az egész országban ez a szűrővizsgálati rend. Ennek a rendszernek fontos eleme az, hogy minden újszülöttet megvizsgál amennyiben lehetséges ortopéd szakorvos, vagy a csecsemő csípő vizsgálatában járatos orvos, családorvos a szülészeti osztályon az élet 1. hetében, majd 3-4 hetes és 3-4 hónapos korban. Rizikófaktor vagy kóros állapot észlelése esetén ortopéd szakorvoshoz kerül a csecsemő olyan korán, amilyen korán csak lehet, mert a kezelési eredményekannál jobbakés a kezelési idő annál rövidebb, minél korábban kezdjük. Az újszülöttkortól követhető a csípők fejlődése ultrahanggal és korán diagnosztizálható a dysplasia is. Az UH vizsgálat feltétlenül indokolt rizikó tényezők esetén, ill. közvetlenül a születés után észlelhető minden laza, instabil csípő esetén, különösen akkor, ha 2-3 hét alatt az állapot nem rendeződik. Kialakítható olyan rendszer is, hogy minden újszülöttnél, csecsemőnél elvégezzék az UH vizsgálatot a kötelező szűrővizsgálat részeként. Ettől várható az, hogy a semmi más módon fel nem ismerhető dysplasiákat is diagnosztizáljuk és kezelésbe vegyük. A teljes körű csípő szonográfiás szűrővizsgálatot 4-6 hetes korban ajánlott elvégezni éppen azért, hogy a észlelt elváltozások az idejekorán megkezdett kezelésre 3 hónapos kor betöltéséig gyógyuljanak.
4.1. Speciális laboratóriumi vizsgálatok nem szükségek
4.2. Képalkotó vizsgálatok
Ultrahangvizsgálat (B szintű evidencia - 7,8,10,11,12)
A vizsgálat statikus és dinamikus módon végezhető. Az ultrahangképek helyes értékelésének, összehasonlíthatóságának előfeltétele, hogy a vizsgálat standard körülmények között, lineáris transducerek alkalmazásával történjenek.
A statikus vizsgálathoz az újszülöttet vagy csecsemőt oldalfekvésben, a csípő enyhén behajlított és berotált állapotában kell a vizsgálathoz elhelyezni (célszerű speciális fektető használata). A transducert először a test hossztengelyével párhuzamosan helyezzük a trochanter major fölé. Ezt követően a vizsgálófej előre- és hátrafordításával áttekintjükaz elülső és hátsó csípőszektort. Így lényegében három különböző síkban térképezzük fel a csípőizületet. Amennyiben lehetőség van rá és a technikai feltételek biztosítottak, ajánlott a standard síkban a csípőkről egy-egy felvételt készíteni. Ennek - a status dokumentálás mellett - azért van jelentősége, mert a pontos, kvantitatív jellemzés csak bizonyos segédvonalak megszerkesztése és szögek meghatározása útján lehetséges az elváltozást mutató csípők esetében. Modernebb készülékek ezt maguk elvégzik. Az újszülöttek és csecsemők csípőízületének ultrahangvizsgálatára a lineáris transducer ajánlott, mely lehetőséget ad a különböző időpontban végzett vizsgálat eredményeinek összehasonlítására. A statikus vizsgálati módszer mellett végezhető dinamikus UH-os csípővizsgálat is a sonographiás instabilitás megítélésére.
Röntgentünetek (A szintű evidencia -19,20)
Röntgenfelvételt általában 4 hónapos kor körül, ill. négy hónapos kort követően végeztetünk, amennyiben nem áll rendelkezésre UH vizsgálati lehetőség. Felvételt ajánlatos készíteni minden olyan esetben amelyben csípő dysplasia vagy luxatio gyanúja merült fel, a családi anamnesis pozitív (a családban csípőficam fordult elő), intrauterin térszűkületre utaló tartási rendellenesség állt fenn, ultrahanggal és a fizikális vizsgálattal a kórisme megnyugtató módon nem állapítható meg.
A röntgenfelvétel készítésekor ügyelni kell arra, hogy a felvétel az alsó végtagok szimmetrikus helyzetében készüljön. Nagyon fontos, hogy a patellák felfelé nézzenek, azaz a végtagok rotatios középállásban legyenek, mert a kifelé rotált végtagállásban készült kép megtévesztő lehet. Ugyancsak zavarja a kép értékelhetőségét, ha az alsó végtagok leszorítása miatt a medence előrebillen.
A röntgenfelvétel értékeléséhez megfelelő gyakorlat szükséges és elengedhetetlen, hogy az ortopéd orvos ne csak a leletet kapja meg, hanem a felvételt is lássa. Annakeldöntéséhez, hogy pl. enyhébb fokú dysplasia esetén szükséges-e kezelés, ill. milyen kezelést alkalmazzunk, a felvételt is meg kell tekinteni és összevetni a fizikális leletekkel. Röntgenfelvételen látható enyhe fokú dysplasia spontán is gyógyulhat.
A vápatető meredeksége: ép viszonyok között a vápatetőszög (a vápatető mentén húzott vonal és az Y-vonal által bezárt szög) 4-10 hónapos kor között 30o-nál kisebb, dysplasia esetén nagyobb. (Az Y-vonal az Y-porcokat összekötő egyenes.) A vápatető íveltségének és lateralis sarkának hiánya vagy fejletlensége dysplasiára utal. Afemurfejcsontmagja 4-8 hónapos kor között jelenik meg. Késése vagy fejletlensége dysplasia jele lehet. A vápatető meredeksége és a femurfejcsontmagjának késése vagy hypoplasiaja különösen jól értékelhető egyoldali esetekben. E két tünet a vápa, ill. a combfej fejlődési zavarának következménye. Gondolni kell arra, hogy a röntgenfelvétel csak közvetett tájékoztatást ad az ebben a korban még túlnyomórészt porcos ízületi vápa és fej viszonyáról. Luxatio esetén a femurfeja vápához viszonyítva felfelé és oldalfelé mozdul el. Dysplasiaban a diszlokáció jelentéktelen lehet.
CTés MR vizsgálatra csak kivételesen van szükség.
5. Differenciál diagnosztika
El kell különíteni a teratológiás ficamtól, a gennyes csípőízületi gyulladás distensios luxátiójától, paralyticus ficamtól, spasticus betegek csípőficamától. A szindrómák részjelenségeként fellépő ficamtól. Combnyak, combcsont töréstől és egyéb gyermekkori csípőbetegségektől.
6. Diagnosztikai algoritumus: lásd. II/4 pontban.
III. Terápia
1.1. Gyermekortopédiai rendelések, osztályok, gyermekorvosok, neonatológia.
1.2. Az újszülöttosztályt ellátó orvosnak, majd a körzeti gyermekorvosnak meg kell vizsgálnia a csípőket a születés utáni 2-4. napon, ill. a 3. héten és a 4. hónapban. Általános intézkedések a szűrővizsgálati rend szerint.
1.3. Speciális ápolási teendők: a csípők szétpelenkázása.
1.4. Szabad csípőmozgás biztosítása.
1.5. A szülőket megtanítják a helyes pelenkázásra és gondozásra.
2. Gyógyszeres kezelés nem alkalmazható.
3. Speciális konzervatív kezelés
3.1. Ha a csípőkben rendellenességet észlelnek - elsősorban luxalhatóság vagy luxatio tünetét -, a csecsemőt azonnal ortopédiai rendelésre kell irányítani, ahol korán elkezdve a kezelést, a ficam teljes kifejlődése megelőzhető, ill. a már kialakult ficam meggyógyítható. Az a cél, hogy minden dysplasiás, instabil csípős, ill. ficamos csecsemő kezelését 1 hónapos kor előtt elkezdjük.
A kezelés alapelve: minél korábban elkezdeni és a legkíméletesebb módszerrel végezni. A kettő egymással szorosan összefügg, tekintve, hogy a legfiatalabb korban alkalmazható a legkíméletesebb kezelési módszer. A korán kezdett kezelés rendszerint rövidebb ideig tart és ez is a kíméletességet jelenti.
Minden esetben javasoljuk a csípők intenzív tornáztatását, szétpelenkázását és a pólyapárna helyett angolpólya, hálózsák, rugdalódzó használatát, mert így kedvező feltételeket teremtünk a csípők normális fejlődéséhez. Ha laza csípőt, luxalható csípőt vagy luxatios jelet észlelünk közvetlen a születés után a fentiek mellett rugi-bugyit ill. terpesznadrágot javaslunk. (B szintű evidencia - 7)
2-3 hetes korban megismételjük a vizsgálatot, és ha a tünetek megszűntek, tehát nem luxalható a csípő, nem észlelhető luxatios-repozíciós jel, továbbra is csak az előbb ajánlottakat javasoljuk. 60-70 %-ban észleljük a repozíciós-luxatios jel, a luxalhatóság megszűnését csupán a rugi-bugyit, terpesznadrágot, szétpelenkázást, ill. intenzív tornakezelést alkalmazva. Ultrahanggal ellenőrizzüka csípők fejlődését és szükség szerint 4 hónapos korban a csípőről röntgenfelvételt is készíttetünk. A tapasztalatok szerint azokban az esetekben, amelyekben újszülöttkorban luxatios repozíciós jel vagy laza csípő volt észlelhető, de néhány nap múlva a tünet megszűnt, a fejlődés további menete normális, és nem alakul ki ficam.
Ha a tünet megszűnte ellenére a 2-4 hetes korban készült UH felvétel vagy a 4 hónapos korban készült röntgenfelvétel dysplasia jeleit mutatná, ezeknél a csecsemőknél korai esetben valamilyen terpesznadrágot vagy Pavlik-kengyelt, ill. a 4 hónapos csecsemőknél Pavlik-kengyelt alkalmazunk. (B szintű evidencia - 7)
Ha a 2-3 hetes korban végzett vizsgálat alkalmával azt észleljük, hogy fennáll a luxalhatóság vagy a luxatio jele, Pavlik-kengyelt alkalmazunk. 2-3 hetes vagy idősebb csecsemőnél a Pavlik-kengyel jó eredménnyel alkalmazható a világra hozott csípőficam vagy dysplasia gyógyítására. Tisztában kell azonban lenni azzal, hogy ez individuális kezelési módszer, és a csecsemő ilyenkor fokozottabb gondozást igényel. A kezelést általában ambulanter végezzük. (B szintű evidencia -7)
A méret szerint kiválasztott Pavlik-kengyelt úgy adjukfel, hogy a haránt mellpánt a mellbimbók magasságában legyen. A vállpántok hátul keresztezik egymást, és bekapcsolva a mellpánt megfelelő helyzetét biztosítják. Ezt követően a szíjakat felhelyezzük a lábakra, lábszárakra és hozzákapcsoljuk a mellpánthoz. A beállítás esetenként változhat. Általános elvként azonban leszögezhetjük, hogy úgy kell a készüléket beállítani, hogy 90o-os, olykor ennél valamivel nagyobb flexios helyzetet biztosítson a csípőízületekben. Ügyelni kell arra, hogy a térd alatti harántszíja térdárokban ne vágjon be, a belső szíja térdtől medialisan helyezkedjék el. A szíja sarokról gyakran hátrafelé lecsúszik. Ez megakadályozható, ha a belső oldalszíjat megfelelő helyen az alsó harántszíjhoz rögzíttetjük. Figyelni kell arra is, hogy az anya úgy öltöztesse a csecsemőt, hogy a ruházat, pl. szűk rugdalózó, ne akadályozza csípők abductioját.
A Pavlik-kengyel feladása után lehetőség szerint 1-2 nap, de legkésőbb 1 hét múlva ellenőrizzük a csecsemőt. Addig szükséges a gyakori ellenőrzés, amíg a repozíció létre nem jön, ill. a femurfej nem rögzül a vápában. A csípőízület helyzetének változtatásával (a flexio fokozásával vagy csökkentésével, a berotatio fokozásával) meggyorsítható arepozíció, ill. retentio. Kezdetben a szíjak megnyúlnak, és ezért szükséges újabb beállítás.
Ha a femurfejrögzült a vápában és már nem luxálódik, elegendő a csecsemőt 2 hetenként, havonta ellenőrizni.
A Pavlik-kengyel feladása után megjelöljük a szíjon, hogy a csat melyik lyukba van bekapcsolva. Helyes, ha a szülő első ízben előttünk pelenkázza be a csecsemőt, és azt ellenőrizzük. A szíjaknak a pelenkán és pelenkanadrágon kívül kell maradniuk.
1-2 napig engedélyezhetjük, hogy a csecsemőről időnként levegyéka kengyelt, ha nehezen szokja meg. Erre azonban ritkán kerül sor. A napi fürdetésre levehető a kengyel, és ha a retentio már bekövetkezett, 1-2 órát naponta kengyel nélkül hagyjuk a csecsemőt. Ha azt észleljük, hogy a csípőkben flexios contractura alakult ki, napi 2-3 órára hagyjuk szabadon a csecsemőt.
Ritkán előfordul, hogy - miután a femurfej reponálódott - a csecsemő csípőjét nem vagy kevésbé mozgatja, esetleg duzzadt is a csípőtájék. Ennek különösebb jelentősége nincs. Általában néhány nap alatt visszatér a teljes mozgás és a duzzanat megszűnik.
4-6 hetente UH-al vagy 3 hónap elteltével röntgenfelvétellel ellenőrizzük a csípők fejlődését. Ha a Pavlik-kengyel hatására a csípőkben flexios contractura alakult ki, a röntgenfelvétel előtt 1 héttel éjszakára elhagyjuk a kengyelt, így megszűnik a zsugorodás és a röntgenfelvétel a csípők normál állásában készíthető el.
Ha a kezelést 1 hónapos kor előtt kezdtük, az esetek túlnyomó többségében 3 hónap alatt teljes gyógyulást tudunk elérni és a kengyel elhagyható. Minél később kezdjük a kezelést, annál hosszabb időre, pl. 3 hónapos kor után az esetek felében mártöbb, mint 3 hónapi kezelésre van szükség. A Pavlik-kengyeltcsakaddig alkalmazhatjuk,amíg a csecsemő fekszik. Ha már felül és még további kezelésre van szükség, a csípők abducalt helyzetét biztosító merevebb készüléket (abductios sín) rendelünk.
A korai kezelés fontosságát mutatja az a tény, hogy ha a kezelést Pavlik-kengyellel tudjuk végigvinni, a femurfejnem károsodik, osteochondritise csak elvétve fordul elő. Ezzel szemben, ha abductios készülékhasználatára kényszerülünk, már 2-3 %-ban fellép osteochondritis. Ez ugyan elenyészően csekély a még 15-20 évvel ezelőtt is alkalmazott lorenzi kezelési módszernél megfigyelt 20-80 %-os gyakorisághoz képest, de ez is elkerülhető, ha a csecsemőket 1 hónapos kor előtt kezelésbe vesszük. Az osteochondritis a femurfejdeformálódását okozza, és már gyermekkorban panaszokat okozhat, később pedig a csípőízület arthrosisához vezet. (B szintű evidencia - 21)
Helyenként Frejka-párnát is használnak a csípőficam kezelésére. A hazánkban jelenleg forgalomban levő típusnál vastag habszivacs betét tartja a csípőket flectált-abducált helyzetben. Kevésbé biztosítja a csípők szimmetrikus abducált helyzetét, mint a Pavlik-kengyel.
Elég elterjedt és újszülött kortól alkalmazható a Barlow és van Rosen által ajánlott, a csípőket abductios helyzetben tartó sín, ill. a coxa.flex készülék.
Idősebb csecsemőkön, ill teratológiás ficam esetén a Pavlik-kengyel hatástalansága miatt kerülhet sor az "over-head"-kezelésre. Ez végezhető intézetben, de otthon is. Ha a körülmények megfelelőek, inkább az otthoni kezelést választjuk, tekintve, hogy rendszerint több hétre van szükség, és a csecsemő számára az otthon előnyösebb, mint a kórházi környezet. Ez a kezelés abból áll, hogy a csecsemő alsó végtagjára cinkenyv vagy egyéb, a bőrhöz tapadó kötést helyezünk fel, majd ezen kötéssel egy speciális kerethez vagy az ágy széléhez - kezdetben hosszában, majd az abductio fokozására keresztben - a lábakat felkötjük úgy, hogy a csecsemő saját testsúlya nyújtsa a csípő körüli izmokat. Így a test súlyával - közben mozogva is - a csípő körüli izmok nyújtásával kedvezőbb feltételek alakulnak ki, és repozíciós manőver nélkül is bekövetkezik a spontán repozíció. Ha az adductorok kellőképpen megnyúlnak és repozíció jött létre, Lorenz-helyzetben (flectált, abducált csípők) vagy abducalt befelé rotált helyzetben, abductios készülékben vagy gipszkötésben (Fettweiss: Sitz-hock gipsz, (guggoló helyzetben), Salter: human positioban) 4 hétre rögzítjük a csípőket. Abductios készüléket viseltetünk, amíg az ízület normális viszonyai ki nem alakulnak. Hazai tapasztalataink nem túl jók ezzel a módszerrel. (C szintű evidencia - 22)
Ma már csak kivételes esetben kerül sorsubcután adductortenotomiára, fedett repozícióra és gipszkötésre. Ha mégis szükséges, helyes előkészítésként "over-head"-kezelést alkalmazni és 2-4 hét után elvégezni a helyretételt. Amennyiben megbízható sonographiás vizsgálat áll rendelkezésre, megvalósíthatóvá válik az a cél, hogy a kezelést minden esetben a sonogrammok értékelése alapján kezdjük meg, ennek segítségével határozzuk meg a kezelés időtartamát és válasszuk meg magát a kezelési eszközt is és így egyénre szabott kezelést alkalmazzunk.
4. Műtét
Az 1 éves kor után kezdett konzervatív kezelés eredményei saját tapasztalataink szerint annyira kedvezőtlenek, hogy ilyenkor inkább műtéti megoldás javasolt. Műtét végezhető, mihelyt kiderül, hogy konzervatív kezeléssel nem érhető el jó eredmény.
A világra hozott csípőficam, ill. a konzervatív kezelés után visszamaradt dysplasiás komponensek megoldására a következő műtétek végezhetők.
4.1. A megfelelő egészségügyi ellátás szintje: Ortopéd osztály
4.2. Általános intézkedések
Szokásos műtét előtti kivizsgálás ambulanter, a tervezett időpont előtti 2 hétben.
4.3. Speciális ápolási teendők
A gyakran alkalmazott medencegipszből adódnak.
4.4. Műtéti indikáció (B szintű evidencia - 23)
Luxatio esetén véres (műtéti) repositio, gyakran varisáló derotatios femur osteotomiával (belső rögzítéssel), esetleg medence osteotomiával együtt.
Coxa valga, subluxatio esetén varisáló derotatios osteotomia belső rögzítéssel. Csípődysplasia/meredek vápatető esetén medenceosteotomia, vápatetőképzés.
4.5. Műtéti előkészítés
Ortopédiai műtéteknél szokásos előkészítés. Képerősítő használata szükséges lehet. Hozzátartozó felvilágosítása.
4.6. Műtéti érzéstelenítés: rendszerint általános anaesthesia.
4.7. Műtétek (B szintű evidencia - 23)
Nyílt műtéti repozíció. (WHO 58162) Az ízület feltárása és az ízületi tok megnyitása után a vápabemenetet szűkítő és a vápát kitöltő lágyrészeket eltávolítjuk. A vápabementet szűkítő és a csípőficam patomechanizmusában is szerepet játszó m. iliopsoast leválasztjuk. A szabaddá tett vápába reponáljuka femurfejet,zárjukaz ízületi tokot, és a m. iliopsoas inát a combnyak elülső felszínére a tokhoz levarrjuk.
A ficammal vagy dysplasiával rendszerint együttjáró coxa valga és fokozott antetorzió korrekciójára elvégezhető a femurvarisalo-derotatios osteotomiája. Magasabb ficam esetén szükség lehet a femur rövidítésére, hogy a repozíciót feszülésmentesen érjük el. A sekély vápa, meredek vápatető korrekciójára egyidejűleg medenceosteotomia vagy acetabulum plasztika is végezhető. A műtét után röntgenfelvételen ellenőrizzüka repozíciót és azosteotomiát, majd medencegipszet helyezünk fel. Fiatalabb korban, 18 hónapos korig, a műtét végén igyekszünk a tokot olyan szorosan zárni, hogy reluxatio ne legyen lehetséges. Ha sem a medencén, sem a femuron nem végeztünk műtétet, nem alkalmazunk gipszkötést, hanem Pavlik kengyelt vagy abductios sínt helyezünk a gyermekre és ezzel folytatjuk a kezelést amíg az izület kifejlődik, vagy későbba medencén vagy/és a femuron szükséges lesz műtétet végezni a reziduális dysplasia konvekciójára. Műtét után 1 hétig a gyermek kórházban, 3 hétig otthon fekszik gipszben. Gipszlevételre ismét felvesszük, és a gipszeltávolítás után röntgenfelvételen ellenőrizzüka repozíciót és az osteotomia gyógyulását.
Ezután a csípőízület mozgásának helyreállítása céljából a gyermeket tornáztatjuk, 1-2 hét alatt a mozgás rendszerint már annyira javul, hogy a további tornát a szülő otthon végezheti, miután az osztályon azt megtanulta. Helyes, ha a műtét után a gyermek fokozatosan kezdi terhelni a csípőjét. Az ízületi tok megfelelő zsugorodása és az izmok tónusa megakadályozza a reluxatiot.
A műtét utáni 3. hónap végén újból ellenőrizzüka gyermeket, sekkor már szabadon járhat, terhelheti a csípőjét. A 3-6. hónap között eltávolítjuk a fémsínt és a csavarokat. A továbbiakban 1/2-1 éves időközben ellenőrizendő a gyermek.
Varisalo-derotatios osteotomia. (57813-9) A femurnyak valgitása és fokozott antetorziója a konzervatív kezelés után is visszamaradhat. Törekedni kell arra, hogy a femurfejcentrális helyzetét a vápában biztosítsuk, mert ezzel a további fejlődés kedvező feltételeit teremtjük meg, és az ízfelszínek kongruenciájának javításával a későbbi arthrosist megelőzhetjük.
A csípőízületekről abducált, befelé rotált helyzetben röntgenfelvételt készítünk, és ennek alapján megállapítjuk azt a helyzetet, melyben a combfejoptimálisan helyezkedikel a vápában. Műtéttel ezt a helyzetet hozzuk létre oly módon, hogy a kistompor magasságában a femurt átfűrészeljük, majd medialis bázisú ék kivételével biztosítjuk a szükséges varisálást. A proximalis femurrészt az optimális helyzetig befelé forgatjuk és a distalis részt a végtag középállásában egyesítjük a felső véggel. Többnyire olyan belső rögzítésre kerül sor, ami a gipszkötést feleslegessé teszi. A gyermek 1 heti kórházi tartózkodás után otthon még 3-4 hétig fekszik, nem terhelheti a csípőjét. Ellenőrző vizsgálat, röntgenfelvétel után felállhat, járhat. Idősebb, 10-14 éves gyermekeknél már 5-6 hét szükséges az osteotomia gyógyulásához.
(B szintű evidencia -13)
- Medenceosteotomiák. (8160, 5867) A vápatető meredek lehet az ízület egyéb részeinek jó fejlettsége mellett, de a meredekség luxatioval vagy a proximalis femurvég fejlődési zavarával együtt is fennállhat. Ha a repozíció és a varisalo-derotatios osteotomia után a vápatető meredeksége nem csökken, szükségessé válhat ezt műtétileg korrigálni.
- Kisgyermekeknél 2-4 éves korban Salter szerint a csípőcsont testét a vápa felett átfűrészeljük és a vápát magába foglaló distalis részt úgy forgatjuk el, hogy a vápatető előbbre és a vízszinteshez közelebb kerüljön. E helyzetében a csípőlapátból vett csontékkel és Kirschner-dróttal rögzítjük.
- Pemberton szerint a vápa fölött pericapsularisan az Y-porcig véssük át a csípőcsontot és a vápát laterál és előrefelé hajlítjuk és ebben a helyzetben a csípőlapátból vett csontékkel kitámasztjuk. Többet lehet korrigálni mint a Salter műtéttel.
- Dega a vápatető részleges átvésésével és lehajlításával korrigálja a vápatető meredekségét. 4 hét rögzítés szükséges medencegipszben.
- Idősebb gyermekeknél és felnőtt korban a Chiari szerint végzett medenceosteotomia biztosítja a femurfejmegfelelő támaszkodását. A csípőcsontot ebben az esetben az ízületi tok fölött ferdén átvéssük és az alsó részt mediál felé betoljuk. A felső rész vésett felszíne az ízületi tokkal érintkezve biztosítja a támaszkodást. Egy spongiosa csavarral rendszerint kellő rögzítést érünk el és nem szükséges medence gipszet adni.
-Jól korrigálható a vápa helyzete hármas medenceosteotomiával, amikor mind a három vápát alkotó csontot átvágjuk és a vápát magában foglaló részt optimális helyzetbe állítjuk.
(C szintű evidencia - 24)
Vápatetőképzés. (58161) Különböző formáival - a vápatető lehajlításával vagy a vápatetőt csontlemezzel kiegészítve -elérhető a meredek vápatető korrekciója és nagyobb érintkezési felszín. A medence osteotomiák elterjedésével háttérbe került.
A felsorolt műtétek jó eredményt adhatnak és mindenképpen jobbak, mint a későn kezdett konzervatív kezelés eredményei. Ne tévesszük azonban soha szem elől, hogy a műtétekkel soha sem érhetünk el olyan tökéletes gyógyulást, mint amilyet az 1 hónapos kor előtt kezdett Pavlik-kezeléstől várhatunk. Ezért a csípőficamot és a dysplasiát minél korábban, újszülöttkorban, de legkésőbb 1-3 hónapos korban kell felismerni és Pavlik-kengyellel lehetőleg 3 hónap alatt meggyógyítani. Jó munkánk eredményét fogja jelezni, ha az ortopédiai osztályokról eltűnnek az operálandó csípőficamos gyermekek.
4.8. Komplikációk
Speciális komplikációkra számítani nem kell. Szeptikus szövődmények nem gyakoribbak, mint egyéb műtéteknél. Különösebb vérzés veszély a szokásos feltárásoknál nincs. Femur osteotomia után a combcsont proximalis részének növekedési zavara, rövidülés vagy túlnövekedés előfordul.
IV. Rehabilitáció
V. Gondozás
1. Rendszeres ellenőrzés szükséges mind a konzervatív, mind a műtéti kezelés után.
2. A felkelés és igénybevétel megfelelő irányításával elkerülhető a kóros helyzetek kialakulása.
3. Előfordulhat mind konzervatív, mind műtéti kezelés után a femurfejcsontmagjának kórosodása, osteochondrosis, coxa vara, coxa valga subcapitans, fokozott antetorsio kialakulása. A felsorolt állapotok a végtag rövidülését aokozhatja, de előfordul hosszabbodás is, főleg femur osteotomia után.
3.1. A szövődmények, sekély vápa, a rossz irányú vápa, a femurfejproximális végének deformálódása műtéttel kezelhető, de az eredmény ritkán tökéletes.
4. A kezelés várható időtartama: (B szintű evidencia - 7)
Az egy hónapos kor alatt kezelésbe vett gyermekek általában 3 hónapon belül és tökéletesen meggyógyulnak. Minél idősebb korban kezdjük a kezelést, annál tovább tart és annál kevésbé lehet tökéletes gyógyulásra számítani.
Műtétek után gyakran szükséges 4-6 hétre gipszkötést alkalmazni, belső rögzítéssel együtt. Rögzítésre használt fém síneket és csavarokat "-1 évvel a behelyezés után lehet eltávolítani.
Tökéletes eredmény elsősorban az 1 hónapos kor alatt kezdett Pavlik kengyellel végzett kezeléstől várható.
5. Fizikai aktivitás
A műtét másnapjától aktív-passzív torna kezdehtő. A gyermekek gipszben felállíthatók egy héttel a műtét után. A fixateur externe alkalmazása gondos ápolást igényel a kórházban és otthon is.
6. A megfelelő ellátás indikátora
- A jól szervezett szűrővizsgálatok: minden újszülöttnek az élet első hónapjában olyan orvoshoz kell kerülni, akik biztosan tudják diagnosztizálni a csípőficamot.
- Minden újszülöttet és csecsemőt, akinél rizikófaktor áll fenn UH-val is meg kell vizsgálni csípő dysplasia kizárására.
- A csípőficam műtéteket optimális időben kell elvégezni. Műtéti repositiót nem később, mint 6 hónapos korban, a femur és medence osteotomiákat akkor, amikor spontán korrekcióra már biztosan nem lehet számítani. Ezen beavatkozások időbeni elvégzése mutatja az ellátás színvonalát.
- Az anatómiai és a funkcionális eredmény jó mutatója a megfelelő ellátásnak.
7. Gyakori társbetegségek
Ízületi lazaság, teratológiás ficamnál különböző szindrómák. Érintett társszakmák: gyermekgyógyászat, radiológia.
VI. Irodalomjegyzék
1. Vízkelety T. (szerk.): Az ortopédia tankönyve. Semmelweis Kiadó, Budapest, 1995.
2. Vízkelety T.: Gyermekortopédia (3. kiadása) Medicina. Budapest, 1994.
3. Sharrard W.J.W.: Paediatric Orthopaedics and Fractures. Blackwell Scientific Publications Oxford and Edinburg, 1993.
4. Tachdjian M. O.: Pediatric Orthopedics W. B. Saunders Co. Philadelphia, London, Toronto, 1990.
5. Aronsson, David D., Goldberg, Michael J. Developmental dysplasia of the hip. Pediatrics, 1994 Aug; 94(2):201-8.
6. Beals, RK. Familial Primary Acetabular Dysplasia and Dislocation of the Hip. Clin Orthop. 2003 Jan. (406):109-15,
7. Graf R. Developmental hip disorders in infants. Diagnosis and therapy Orthopade. 1997 Jan;26(1):1.
8. Hensinger RN. The changing role of ultrasound in the management of developmental dysplasia of the hip (DDH) J Pediatr Orthop. 1995 Nov-Dec;15(6):723-4.
9. Jones D. Neonatal detection of developmental dysplasia of the hip (DDH) J Bone Joint Surg Br. 1998 Nov;80(6):943-5.
10. Niethard FU. Ultrasound and clinical screening for hip dysplasia-dislocation Z Orthop Ihre Grenzgeb. 1998 Nov-Dec;136(6):485-6.
11. Roposch A. Twenty years of hip ultrasonography: are we doing better today? J Pediatr Orthop. 2003
Nov-Dec;23(6):691-2.
12. Rosendahl K. Ultrasoundin the diagnosisofdevelopmental dysplasia ofthehip (DDH). Acta Radiol. 2004Apr;45(2):118.
13. Soballe K. Pelvic osteotomy for acetabular dysplasia. Acta Orthop Scand. 2003 Apr;74(2):117-8.
14. Wedge JH. Hip joint acetabular dysplasia. J Pediatr Orthop. 1997 Mar-Apr;17(2):141-2.
15. Wilkinson JA Etiologic factors in congenital displacement of the hip and myelodysplasia. Clin Orthop. 1992 Aug. (281):75-83.
16. Czeizel E. Vizkelety T. Incidence of congenital hip dislocation in Hungary. Orv Hetil. 1988 Nov. 129(48):2605,
17. Wynne-Davies R. Acetabular dysplasia and familial joint laxity: two etiological factors in congenital dislocation ofthe hip. A review of 589 patients and their families. J Bone Joint Surg Br. 1970 Nov; 52(4):704-16.
18. Wynne-Davies R. The epidemiology of congenital dislocation of the hip. Developmental Medicine & Child Neurology. 1972 Aug. 14(4):515-7.
19. Bertol P. Macnicol MF. Mitchell GP. Radiographic features of neonatal congenital dislocation of the hip. J Bone Joint Surg Br. 1982.Febr. 64(2):176-9.
20. Wiberg G Relation between congenital subluxation of of the hip and arthritis deformans. Acta Orthop Scand 1939. 10:351-71.
21. O'Brien T, Millis MB, Griffin PP. The early identification and classification of growth disturbances of the proximal end of the femur.. J Bone Joint Surg Am. 1989.Aug. 68:970-80.
22. Tonnis D. An evaluation of conservative and operative methods in the treatment of congenital hip dislocation. Clin Orthop. 1976 Sep. (119):76-88.
23. ScagliettiO, Calandriello B. Open reduction of congenital dislocation of the hip. J Bone Joint Surg Br. 1962. 64(2):257-83.
24. Staheli LT. Chew DE. Slotted acetabular augmentation in childhood and adolescence. J Pediatr Orthop. 1992 Sep-Oct. 12(5):569-80.
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Veleszületett dongaláb ellátásáról
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
Szinonímák: Pes equinovarus congenitus BNO: Q6600
I. Alapvető megfontolások
l. A protokoll érvényességi területe ortopédiai betegellátással foglalkozó járó- és fekvőbeteg intézmények, újszülött ellátással foglalkozó osztályok, neonatológus, gyermekgyógyászok, gyermeksebészek működési területében.
2. Az irányelv bevezetésének alapfeltétele a veleszületett dongaláb graduális, vagy postgraduális formában történő ismereteinek megszerzése.
3. Definíció
A veleszületett dongaláb a láb leggyakoribb fejlődési rendellenessége, amely a születés után azonnal könnyen felismerhető, és a láb valamennyi izületét érintő kontrakturák sorozatából áll. Kiváltó tényezői pontosan nem ismertek.
4. Panaszok, tünetek, általános jellemzők:
- a születés után feltűnik a láb befelé fordulása,
- az újszülöttkor szűrő vizsgálatok során a következő jellegzetes kontaktura sorozatokat találjuk,
- equinus: a láb a felső ugróízületben flexios helyzetben rögzült, a sarok magasan áll,
- varus: az alsó ugróizületben a sarok befelé fordul egyúttal supinálódik is,
- adductus: az előláb a Chopart-ízületben mediál felé hajlik és supinálódik,
- plantiflexus: amely az equinusban levő lábtőhöz képest az előláb Chopart-, illetve Lisfranc-ízületben bekövetkezett további talpi hajlítását jelenti.
Ennek következtében a láb "bab" alakú a külső talpszél konvex, belső talpszél konkáv. A sarok magasan áll a sarokgumó alig tapintható, helyén elsősorban zsírszövet észlelhető.
A veleszületett dongaláb öt típusa különíthető el.
1. Tüneti dongaláb:
Legtöbbször valamely szindróma részjelenségeként észleljük, monogén, vagy kromoszomális ártalom okozata multiplex rendellenesség tünetét képezi.
A leggyakrabban arthrogryposis multiplex congenitánál, vagy Larsen szindrómánál kerül felismerésre.
A korai konzervatív kezelés számára, általában rezisztens, műtéti beavatkozással kiegészítve, csak az esetek egy
részében érhető el jó eredmény.
2. Teratológiai dongaláb:
Az intrauterin élet korai szakaszában tehát a morfogenesis alatt ható teratogén noxak következménye. Jellegzetessége, hogy az érintett végtag egyéb igen változatos képet nyújtó rendellenességével társulhat, ez a típus nem öröklődő a kezelés számára a legrosszabb prognózisú csoport, teljes anatómiai gyógyulás nem biztosítható.
3. Tartási dongaláb:
Valamilyen intrauterin mechanikai hatás okozta tartási deformitásról van szó. Klinikailag a nagyfokú képlékenység jellemzi a sarokcsont jól látható és tapintható.
A konzervatív kezelésre jól reagál, rövid idő alatt teljes anatómiai korrekció biztosítható, tehát a legjobb indulatú forma.
4. Másodlagos dongaláb:
Lényegében itt is tartási dongaláb kialakulásáról van szó, melynek kialakulását a magzat valamely egyéb rendellenessége megkönnyíti, ezek a következők lehetnek.
Elsődleges neuromuscularis ártalom pl. congenitalis myotonicus distrophya.
Másodlagos neuromuscularis ártalom pl. spina bifida cysitica.
Oligohydramnion, pl. veseaplasia, magzatvízcsorgás, ilyenkor az amnion folyadék nyomáskiegyenlítő hatása nem érvényesül.
Részben a magzat mozgási lehetőségei szűkülnek be.
5. Strukturális dongaláb:
Amely etiológiailag és patológiailag, valamint klinikailag önálló egységet képez.
Az ortopédiai gyakorlatban előforduló dongalábak legnagyobb részét ez a típus teszi ki.
Azt is mondhatjuk, hogy a strukturális dongalábnál az újszülötteknek, illetve gyermeknek nincs egyéb fejlődési rendellenessége, csak dongalába.
A születést követően könnyen felismerhető, ez esetben a kezelésre való reagálás alapján két típusát különítjük el, reguláris forma: a kezelésre jól reagál , rebbelis forma: a kezelésnek ellenáll.
5.2. Genetikai háttér:
A veleszületett strukturális dongaláb esetében az etiológiát illetően csak feltételezett elméletek vannak, ezeket az alábbiakban foglalhatjuk össze: B szintű evidencia (4,5,11,18)
- mechanikus okok,
- endogén okok,
- multifactoriális ok (genetikai + környezeti hatás)
Leginkább elfogadott etológia a multifaktoriális eredet, amely szerint, a veleszületett dongaláb létrejöttéhez genetikai predispozició és környezeti hatások együttes jelenlétére van szükség.
A provokáló tényezőket meglehetősen jól ismerjük (méhen belüli élet malpozíciói) addig a genetikai, predispozició
mibenlétére, csak feltételezésekre támaszkodhatunk:
(pl. osteogén ok: talus-nyak medialis elhajlása,
vascularis ok : a sinus tarsi ereinek hypoplasiája,
neurogén ok: a peroneus izomcsoport perifériás beidegzési zavara,
hormonális ok: izületi lazaság,
kötőszöveti ok: a társuló minor kötőszöveti rendellenességek, pl. lágyéksérv magasabb gyakorisága utalhat erre. Valószínűleg együttes hatásukkal kell számolni, mivel öröklődésük leginkább a polygen öröklődési módnakfelel meg. A veleszületett dongaláb családi halmozódást is mutat. C szintű evidencia (18)
Az ismételt előfordulás kockázata a családi terheltség függvénye, minél több veleszületett dongaláb fordul elő az index családjában annál nagyobb az adott család genetikai terheltsége és ennek megfelelően annál gyakrabban várható a veleszületett dongaláb újabb jelentkezése.
Így, ha már egy testvérpár érintett, akkor a várható, ismételt előfordulás 3-5 %, ha valamelyik szülőnek veleszületett dongalába van a kockázat 2 %, viszont ha egy szülő, plusz egy testvér érintett, akkor az ismételt előfordulás kockázata 25 %-ra tehető.
5.3 Incidencia:
Irodalmi adatok alapján europoid lakosságban a gyakoriság 1-2 ezrelék közé tehető, hazai gyakorisági értékek is vannak, amely szerint hazánkban 1,25 ezrelékre tehető a gyakoriság. C szintű evidencia (2,18) Gyakorisági szempontból a dongaláb rasszikus tulajdonságokat is mutat. A Polinéziai rasszhoz tartozó Maorikban előfordulásuk 6-7 ezrelék.
A veleszületett dongaláb már a születés pillanatában jelen van, és a fiú leány arány 2:1 -hez tehető.
Az esetek nagyobb része kétoldali, de közel azonos arányban fordul elő, jobb vagy bal oldali dongaláb is.
II. Diagnózis
A diagnosis felállításához elegendő inspekció és fizikális vizsgálat.
Az anamnesis felvételénél ajánlatos kitérni a családi anamnesisre, amennyiben a családban előfordult-e dongalábas eset.
A fizikális vizsgálat során az általános ortopédiai vizsgálaton belül ki kell terjedni a láb vizsgálatára, amely a kontrakturák fokának meghatározását kell, hogy tartalmazza, illetve a láb rigiditását, mobilitását, és a passzív mozgatásra való lazulását, kontrakturák kimozgatását, illetve az aktív izomerő figyelését bőringerek alkalmazásával. Laboratóriumi vizsgálatokra a diagnosis felállításához nincs szükség.
A képalkotó vizsgálatok közül a röntgen vizsgálat, a diagnosis felállításához nem szükséges, újszülött korban rtg. felvételt ebből a célból nem végzünk, viszont a kezelési eljárások folyamán, különösképpen a konzervatív kezelés eredményének megítélésére, illetve a műtéti terv felállításához a lábról antero posterior és oldalirányú röntgen felvételt kell készíteni. Idősebb gyermekeknél, a járás kialakulása után a pontosabb pathoanatómiai viszonyok tisztázásra terhelt lábbal is készíthetők rtg. felvételek.
Csecsemőkorban a lábtő csontok közül, a calcaneus, talus, valamint az os cuboideum csontmagja van jelen, az os naviculare még csontmaggal nem rendelkezik.
A röntgenfelvételen mind AP. mind oldal vetületben meg tudjuk határozni, az un. talocalcanealis szögeket. Dongaláb esetében ezek a szögek a normálisnál kisebbek.
Az AP talocalcanealis szög nagysága, ha nem éri el a 15 fokot, abban az esetben indirekt módon azt jelentheti, hogy az os naviculare, amely ebben az időszakban még porcos a talus fejtől medialis irányba subluxalt, vagy luxalt helyzetben található.
Óvodás, vagy iskolás korban az előbb említett két szögértéken túl az un. talo-metatarsalis, illetve naviculo-metatarsalis szögeket határozhatunk, meg, amelyeknek a jelentősége az adductus kontraktura radiológiai elemzéséhez nyújt segítséget, amelyből kezelési konzekvenciát vonhatunk el.
Computer tomográf, vagy MR-vizsgálatra a legritkább esetben van szükség, legfeljebb akkor, ha különleges rotációs izületi viszonyokat kell meghatározni.
Differenciál diagnosztikailag el kell különíteni a láb egyéb varus irányú tartási rendellenességeit, ezek a pes adductus, vagy metatarsus varus, vagy magyarul nevezzük "sarlólábnak" is.
Ennek az a jellemzője, hogy az előláb a Chopart-ízületben adductusban és supinatusban helyezkedikel, de a sarok soha nincs equinusban és varusban,sőt a sarok ebben az esetben valgus helyzetben van.
A differenciál diagnosztika azért fontos, mert a pes adductus a legtöbb esetben nem igényel a dongalábhoz hasonló konzervatív, de főleg műtéti kezelést.
A pes adductus passzív és aktív gyógytornájával, a legtöbb esetben eredmény érhető el.
Pes supinatus vagy "mászóláb", amely a Chopart-ízület veleszületett supinatios kontrakturája, a sarok itt enyhe varusban van, de equnius kontraktura nincs.
Már pedig olyan dongaláb nem létezik, amelynél az equnius kontaktura veleszületetten ne lennejelen. A kezelési elvek ugyanazok, mint a pes adductusnál.
III. Terápia
A terápiás elvek:
1. Priméren konzervatív.
a) hagyományos redresszió
b) Ponseti-szerinti redresszió
2. Műtéti kezelés
A. Primér műtét
a. Postero-medialis felszabadítás
b. Achillotomia (csak Ponseti-technika esetében)
B. Reoperatio, idősebb gyermek műtéte
C. A láb növekedésének befejeződése után
3. Szervezett gondozás.
III. l. A konzervatív kezelés részletes leírása. B szintű evidencia (9,10,13,14)
Újszülött korban a születés után azonnal, ha egyéb kizáró ok nincs, már az újszülött osztályon a láb passzív tornáztatása, mozgatása a kontrakturákkal ellentétes irányban.
Ezt végezheti az újszülött osztály nővére, gyógytornász de a szülő is.
A talp bőrének ingerlésre (puha fogkefével, de lehet ujjal is) aktív lábmozgások kiváltása.
a)
Szakaszos redresszio kezdete, mihelyt az újszülött bőre bírja, lehetőleg legkésőbb az 5-7. napon (amikora gyermeket a szülészeti intézményből otthonába bocsátják) a csecsemő útja az ortopéd szakrendelésre vezessen. A szakaszos redressziót magyarországi gyakorlat szerint ortopéd orvos végezze, ez lehet felügyelet mellett nem szakorvos is. A szakaszos redressziós módja történhet a Lorenzi-elveknek megfelelően, technikailag fordított sorrendben, előbb az előláb inflexus, adductusa, supinatusa, majd végül az equinus.
Elfogadott az a redressziós módszer is, amely az újszülött lábán az egy ülésben kivihető összes kontaktura csökkentésére vagy megszüntetésére irányul, tehát "amit a láb elbír".
b)
Ismert és manapság világszerte elterjedt a dongaláb kezelésében az ún. Ponseti módszer. A gipszredresszióra vonatkozó általános elvek úgy mint a gipsz megfigyelése, a szülőknek adott tanácsok, a lábak polcolása és a heti gipszváltás eredetiek szerint érvényesek. Ponseti-szerinti gipszelés esetén:
Első gipsz a cavus correkcio - kivitelezése az előláb supinalt helyzetbe hozása az equinus korrekció ebben
a fáziban nem követelmény.
Második gipsz tartsd a lábat supinatioban és a talus fején ellentartva a lábat vidd abductioba, az equinust nem kell korrigálni de ameddig könnyen tartható addig korrigálható.
Harmadik gipsz vidd tovább a lábat abductioba, ne pronálj, óvatos equinus korrekció lehetséges. Negyedik gipsz további abdukcióba visszük a lábat. Ötödik gipsz elérjük az abdukciós véghelyzetet.
FONTOS: Ne pronáljukazelőlábat!
A nyomáspont nem a calcaneocuboideális ízület, hanem a talus fej.
A korrekció kézzel elérhető, a gipsz célja nem az erőltetett korrekció, hanem a kézi redresszióval elért eredmény megtartása.
Optimális esetben az ötödikgipsz után csaka sarok felcsapottsága maradhat meg, azaz az equinus kivételével minden elem lényegében korrigálható.
Mindkét esetben az elért eredményt alápárnázott körkörös gipszkötésben rögzítjük a térd 90 fokos hajlított helyzete mellett combközép, combtőtől az ujjak végéig, úgy, hogy az ujjak lábháti része látható legyen.
A gipszredresszióhoz szükséges műtősséged, illetve a szülő részvétele, narcosisra nincs szükség.
Célszerű a gipszredresszió után 20-30 perces várakozása rendelőnél és a begipszelt láb megtekintése, szükség szerint, ha keringési zavar van, akkor a gipsz eltávolítása.
A láb duzzanat lehetőségére felhívni a szülő figyelmét, ha a csecsemő sokat sír azonnal forduljon orvosához. A fektetési szempontok: láb felpolcolása ugyancsak szülői felvilágosítást igényel.
Kezdetben kb. 2-3 hónapos korig a gipszeket és a redressziót hetente elvégezzük, manuális menővérek után újabb gipszeket helyezünk fel. A gipszcserék között általában nincs szükség 1-2 hetes szünetek beiktatásra, a láb "pihentetésére".
A láb növekedését figyelemmel kell kísérni, ha lehetséges, akkor a gipszet 3 hónapos kor után 2-3 hétig fent lehet tartani.
A hagyományos gipszredressziót féléves korig érdemes végezni, de csakakkor ha a manuális redresszio során reményt látunk az equinus korrigálására is.
Ügyelni kell arra, hogy a lábat ne hozzuk, "hintaláb" helyzetbe, azaz a Chopart-ízület dorsalis irányú subluxatiojátel kell kerülni.
Az elért eredményről, vagy ha bármi kétségünk van, célszerű antero-posterior és oldalirányú rtg. felvétellel meggyőződni.
Féléves kor után a maradvány tünetek miatt műtéti beavatkozás szükséges.
Amennyiben csecsemőkorban, vagy kisgyermek korban kezeletlen dongalábbal találkozunk a konzervatív módszer alkalmazása, ugyan az, mint újszülött korban, ezekben az esetekben a gipszredresszió csak a kontrakturák csökkentésére alkalmas és jobb feltételeket teremt a műtéti kezeléshez.
Recidiv dongalábas esetekben, vagy műtéti reoperációk után szükség lehet tartós gipszrögzítésre, bizonyos esetekben az úgynevezett Kite metódussal (a gipszkötésből kivett ék után elvégzett manuális korrekció és az ellentétes oldalra behelyezett gipszék rögzítése.)
A gipszredresszió során bármelyik életkorban fellépő dermatitis esetén, szükség van a bőr pihentetésére, ilyenkor műanyagsínt adhatunk, amely célszerű, ha térdet is magába foglalja derékszögig hajlított helyzetben. Műanyagsínt bármikor használhatunk a láb plantigrad helyzetének biztosítására.
A konzervatív, vagy műtéti kezelés befejezése után a lábat és az izmokat mozgatni, illetve erősíteni kell, különböző fizioterápiás módszerekkel, elsősorban gyógytornával.
A járáshoz a legtöbb esetben elegendő konfekció cipő, de szükség lehet úgy nevezett antivarus cipőre is, amely egyenes talptengelyű és a belső oldalon előrevezetett kéregrésze van.
Residualis, vagy recidiv esetekben szükség lehet lábra mintázott ortopéd cipőre is, amely legtöbbször egyenes talptengelyű, a belső oldalon kéreg része van, és előrevezetett pronatios sarka.
III.2. Műtéti kezelés elvei B szintű evidencia (1,2,12,14,16,17)
A. Primér műtét
a) Féléves kortól a konzervatív kezelés folytatásaként postero-medialis lágyrész felszabadítás. A műtét célja teljes korrekció elérése, a deformitást fenntartó valamennyi komponens, kontraktúra megszüntetése.
b) Ponseti-technika esetében, 6 hetes kortól, az Achillotomia célja az equinus kontraktura megoldása.
B. Reoperatio, idősebb gyermek műtéte
Csak Idősebb gyermeknél vagy recidiva esetén reoperáció során kiterjesztett lágyrész műtét. 5 éves kor után szükséges lehet a laterális oszlop rövidítése Evans szerint a calcaneocuboideális izület ékreszekciójával az adductus állás korrekciójára. Egyéb műtéti megoldások is alkalmazhatók a laterális és mediális talpél hosszúságának kiegyenlítésére (pl. lateralis záró, medialis nyíló ék osteotomia).
A peroneus izmok gyengesége esetében a m.tibialis anterior átültetése is indokolt lehet az előláb deformitásának megoldására, a láb külső élén való járás korrekciójára. Feltétele a passzívan korrigálható supinatus helyzet, valamint az extensio lehetősége a felső ugrózületben.
C. A láb növekedésének befejeződése után
A láb növekedésének befejeződése után subtalaris- és Chopart-ízületi arthrodesis ékreszekcióval.
A. Primér műtéti korrekció
a) Postero-medialis felszabadítás
Indikáció
A műtét végzése indikált, ha konzervatív módszerekkel nem tudtukeredményesen korrigálni a deformitásokat. Erősen deformált lábakat célszerű 6-7 hónapos korig megoperálni.
Enyhébb deformitások konzervatív kezeléssel idősebb korig is egyensúlyban tarthatók.
Kétéves kor fölött a primer műtét indikációja már csak ritkán merül föl, leginkább akkor, ha korábban elmulasztottákaz indokolt műtéti korrekciót elvégezni.
Műtéti technika
Vértelenségen operálunk. A gyakorlatban leginkább elterjedt feltárás az Achilles-ín mediális széle mentén haladó és a belbokát megkerülő, a láb mediális oldalára kanyarodó bőrmetszés. Csecsemőkön a Cincinnati-metszés hasonlóan jó feltárást ad a kiterjedt deformitásokhoz, és ez után alakul ki kozmetikailag a legjobb heg.
A műtét célja az összes fennálló kontraktura, deformitás lehető legteljesebb megoldása. Ezt az izületi tokok bemetszésével, inak meghosszabbításával, átvágásával, illetőleg tapadásukról való leválasztásával érjük el. A műtéti technika szempontjából indokolt külön figyelni a dongalábas deformitás 3 megkülönböztethető komponensére, melyek mindegyikét maradéktalanul meg kell oldanunk.
A) A talocruralis izületben alapvetően equinus kontaktura áll fenn.
B) Subtalarisan a lábtőben alakul ki a legfontosabb dongalábas deformitás.
Acalcaneus varusba fordul és elülső pólusa medial felé rotálódik,a naviculare medial felé subluxálódika talusfejről, a cuboideum és a több lábtőcsont adductusba kerül és supinatioba.
C) A lábközép és az előláb a lábtőt követve aductusba, supinatioba kerül és flexios helyzetbe.
A különböző deformitások fennállásától függően a korrekció elérésére az alább felsorolt izületi tokok bemetszését végezhetjük el szükség szerint: a talocruralis és talocalcaneáris izület hátulsó és medialis tokja, a talonavicularis, valamint a calcaneo-cuboidalis izületek tokjainak bemetszése, a ligamentum bifurcatum, a peroneus ínhüvely és a tibiofibularis syndesmosis bemetszése. Szükséges lehet a naviculre az első ékcsont és első metatarsus közötti tokok medialis bemetszése is.
Az Achilles-inat, a tibialis posterior, flexor hallucis és digitorum longus inait inát szükség szerint meghosszabbítjuk. Esetleg az abductor hallucis inának átvágásával együtt szükséges lehet a talpi aponeurosis és a rövid talpizmok eredésének leválasztása a tuber calcaneiről.
4-5 éves kor alatt a csontok alaki deformitása még kevésé kifejezett, ezért csak lágyrész műtétet végzünk. Amennyiben erősen kiterjesztett műtétre volt szükség a korrekció eléréséhez, a korrigált helyzetet dróttűzéssel is biztosíthatjuk.
Gondos vérzéscsillapítás után sebzárás, rögzítés gipszsínben, lehetőleg korrigált helyzetben. Amennyiben a bőr feszül, nem teljes korrekcióval is megelégszünk a következő gipszcseréig.
Utókezelés
Ha a láb nem duzzadt és a seb megnyugható, 3-4 nap után már hazabocsáthatjuk a beteget gipszsínben. Körkörös gipszet teljes korrekcióban csak a duzzanat teljes lelohadása után alkalmazunk. A bőr feszességének csökkenésével a korai postoperativ időszakban gipszcserékkel a lábat fokozatosan korrigálhatjuk a műtét során észlelt helyzetig. A tűződrótokat legalább 4 hétig tartsuk benn, de lehet tovább is.
A preoperativ deformitások mértékétől és a beteg korától függően gipszrögzítés 4-12 hétig szükséges. b) Achillotomia (csak Ponseti-technika esetében)
Az Achillotomiát - percután - a sarokcsont felett egy-másfél centivel célszerű elvégezni medialról lateral felé. A lábat maximálisan dorsalflectaljuk. Időnként "pattanás" érzés észlelhető az ín átvágásakor. Általában 10-25 fokdorsalflexió válik azonnal elérhetővé. Szükség esetén ragasztócsík rakható a sebre.
Utókezelés
Ponseti szerinti kezelés esetén az Achilles teljes műtéti átvágása után általában 3 hét gipsz javasolt, maximálisan abducalt és 20 fokban dorsalflectált helyzetben. Az extensio javítása érdekében a gipsz cserélhető.
A Ponseti technikánál 3 hét gipszrögzítés után 3 hónapig abductios-dorsalflexiós helyzetű Ponseti-elvű brace javasolt folyamatosan, azután csak éjjel, illetve nappal néhány órában mintegy 3-4 éves korig.
B. Reoperáció
Reoperáció szükségessé válhat akár fél-egy évvel az elégtelen primer műtéti korrekció után, vagy ritkábban később a primer műtét után kialakult recidívák miatt rebellis dongalábakon.
A reoperáció heges környezetben technikailag nehezebb a primer műtétnél és az eredmény sem biztosan azonos a primer műtétével.
Műtéti technika
A reoperáció során ugyanazokat az elveket kell szem előtt tartani, mint a primer műtétnél és a műtét technikai megoldása is azonos. Ugyanúgy a fennálló deformitások korrekciójához szükséges beavatkozásokat kell elvégezni. Idősebb gyermekeken, általában 5 éves kor fölött, szükség lehet, a tökéletesebb korrekció eléréséhez, a lateralis oszlop megrövidítésére: a calcaneo- cuboidalis izület. resecálására. Az előláb adductus deformitásának korrekcióját biztosítja, és az újabb recidiva kialakulását eredményesen akadályozza meg a musculus tibialis anterior inának a lábhátra, valamelyik metatarsusra való átültetése is.
Utókezelés
Elvei azonosak a primer műtétnél alkalmazottakkal, de hosszabb gipszrögzítés szükséges, általában 2-3 hónap.
3. Műtéti korrekció a láb növekedésének befejeződése után.
Idősebb gyermekeken, serdülőkorban és ezt követően az izületi kontrakturák oldásával már alig érhető el korrekció, eredményt elsősorban csontos műtéttel biztosíthatunk. A műtét lényeg a subtalaris- és Chopart-ízületekből megfelelő nagyságú és irányú csontos ékek kivésése és az izületek elmerevítése a korrigált helyzetben. 3 hónapi postoperatív gipszrögzítés szükséges.
IV. Rehabilitáció
Szervezett körülmények között erre a feladatra szakosodott speciál dongaláb szakrendelésen célszerű végezni.
Az ortopéd szakorvos vagy rezidens orvos mellett szükséges gyógytornász és műtőssegéd bevonása a munkába. C szintű evidencia (14)
1. Rehabilitáció: gyógytornász végezteti a gyakorlatokat, betanítja a szülőknek. A fizioterápia szempontjai:
- Kontraktura oldása,
- Passzív korrekciós mozgatás,
- Aktív korrekciós mozgatás kiváltása,
- A lábszár a lábizmok erősítése,
- A gyengült izomcsoportok elektromos ingerlése,
- Járástanítás-járáskorrekció,
- Passzívtartó és rögzítősínek alkalmazása,
- életmódbeli tanácsok, pályaválasztási tanácsadás.
V. Gondozás
1. Ajánlott sportok Rendszeres izomerősítő lábtorna, Rövid és hosszú távfutás, Kerékpározás, Labdajátékok.
2. Ortopédcipő ellátás
Az esetek egy részében konfekció cipő is elegendő.
A sarok varus, előáb adductus esetén a külső talpszél túlterhelésének esetleges kifekélyesedésének megakadályozására, a járókép javítására szükséges egyenes talptengelyű ortopéd cipő, előre vezetett pronációs sarokkal, a belső oldalon a befelé fordulást akadályozó kéreggel, a fokozottabb terhelésnek kitett részeken belső laticel béleléssel.
A csecsemő, illetve kisgyermekkorban az elért eredmények megtartására, redresszáló cipő, műanyagsín, illetve antivarus cipő használható.
3. Lehetséges szövődmények
A kezelések során gipsz alatt dermatitis, decubitus, bőrsérülés a gipsz eltávolítás közben.
Műtétek után, mint minden sebészi beavatkozás után előforduló szövődmény itt is jelen lehet.
Az atrófiás lábszár izomzat műtét után is atrófiás marad, ez egyoldali esetben feltűnő lehet. Ez tulajdonképpen a dongaláb patológiájának része, nem tekinthető szövődménynek.
A láb hossznövekedése is gátolt lehet.
4. A kezelés várható időtartama
Ha a kezelésbevétel perinatalis korban elkezdődött, az aktív kezelés (konzervatív és műtéti) kb. a járás tanulás idejéig 1-1,5 évig tart, amelyet a gondozás követ a láb növekedésének befejeződéséig. Az utókezelés a Ponseti módszer szerint általában 3 éves korig tart.
5. A szakmai munka eredményességének mutatói: C szintű evidencia (8)
Recidivák száma. Reoperációk gyakorisága. Az eredményes kezelés ideális kritériuma: A láb izületeiben kontraktura nincs.
A láb alakja normális, a beteg járása harmonikus, sarkát, talpát terhelve jár, fájdalma nincs Radiológiailag közel normális ATC-OTC TM. szögek.
VI. Irodalomjegyzék
1. Bensahel H,Csukonyi Z, Desgrippes Y,Chaumien JP: Surgery in residual clubfoot: one-stage medioposterior release "a la carte". J Pediatr Orthop, 1987;7:145-148.
2. Chesney DJ, Barker SL, Macnicol MF, Porter RW, Maffulli N: Management of congenital talipes equinovarus in Scotland: a nationwide audit. Surg J Coll Surg Edinb Irel, 2004;2:47-51.
3. Crawford AH, Marxen JL, Osterfeld DL: The Cincinnati incision: a comprehensive approach for surgical procedures of the foot and ankle in childhood.. J Bone Joint Surg, 1982;64-A:1355-1365.
4. Czeizel A, Bellyei A, Kranicz J, et al.: Confirmation of multifactorial threshold model for congenital structural talipes equinovarus. J Med Genet, 1981;18:99-100.
5. Dietz F: The genetics of idiopathic clubfoot. Clin Orthop Rel Res, 2002;401:39-48.
6. Dobbs MB, Rudzki JR, Purcell DB, Walton T, Porter KR, Gurnett CA: Factors predictive of outcome after use of Ponseti method for the treatment of idiopathic clubfeet. J Bone Joint Surg, 2004;86-A:22-27.
7. Herzenberg JE, Radler C, Bor N: Ponseti versus traditional methods of casting for idiopathic clubfoot. J Pediatr Orthop, 2002;22:517-521.
8. Heilig MR, Matern RV, Rosenzweig SD, Bennett JT: Current management of idiopathic clubfoot questionnaire. J Pediatr Orthop, 2003;23:780-787.
9. Karski T, Wosko I: Experience in the conservative treatment of congenital clubfoot in newborns and infants. J Pediatr Orthop, 1989;9:134-136.
10. Kite JH: Non-operative treatment of congenital clubfeet: A review of one hundred cases. South Med J, 1930;23:337-345.
11. Lochmiller C, Johnston D, Scott A, Risman M, Hecht JT: Genetic epidemiology study of idiopathic talipes equinovarus. Am J Med Gen, 1998;79:90-96.
12. McKay DW: New concept of an approach to clubfoot treatment: section II. Correction of the clubfoot. J Pediatr Orthop, 1983;3:3-10.
13. Ponseti IV, Smoley EN: Congenital clubfoot: the result of treatment. J Bone Joint Surg, 1963;45-A:261-273.
14. Ponseti IV: Current concepts review. Treatment of congenital clubfoot. J Bone Joint Surg, 1992;74-A:448-453.
15. Tachdjian MO: The foot and leg. In:Pediatric Orthopedics. WB Saunders Company, Philadelphia, 1972; 2477-2510.
16. Turco VJ: Surgical correction of resistant clubfoot: a one stage posteriomedial release with internal fixation. J Bone Joint Surg, 1971;53-A:497-503.
17. Vízkelety T, Szepesi K: Reoperation in treatment of clubfoot. J Pediatr Orthop, 1982;2:144-147.
18. Wynne-Davies R: Family studies and the cause of congenital club foot: Talipes equinovarus, talipes calcaneo-valgus and metatarsus varus. J Bone Joint Surg, 1964;46-B:445-463.
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Társszakmák: gyermekgyógyászat, gyermek (fejlődés) neurológia, rehabilitáció.
2. Dokumentáció, bizonylat
- Járóbeteg szakellátásban: ambuláns lap, kezelő lap.
- Képalkotó vizsgálatok képi és szöveges leletei
- Fekvőbeteg szakellátásban: kórlap, műtéti beleegyezés, műtéti leírás, decursus, zárójelentés.
3. Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
A csonttumorokról
Primer csonttumorokról és tumorszerű elváltozásokról
(1. módosított változat)
Készítette: az Ortopédiai Szakmai Kollégium
I. Alapvető megfontolások
1. Általános elvek
1.1. Szövettani osztályozás
A szövettani osztályozás a csonttumorok WHO 1995. ill. 2002. kiadású klasszifikációja szerint történik. Ennek alapját a csonttumorok szöveti eredete, ill. az a tény adja, hogy milyen anyagot termel maga a tumor. Másik fontos besorolási forma, hogy a jóindulatú tumorok latens, aktív, vagy agresszív csoportba tartoznak-e, ill. hogy a rosszindulatú tumorok alacsony, közepes, vagy nagy malignitással bírnak-e (Evidencia szint 11B, 12A).
| A csontdaganatok WHO osztályozása | |
| I. Csontképző tumorok | Malignitási fok |
| Benignus | |
| 1. Osteoma | latens |
| 2. Osteoid osteoma | aktív |
| 3. Benignus osteoblastoma | aktív, esetenként agresszív |
| Malignus | |
| 1. Konvencionális, centrális osteosarcoma | nagy malignitású |
| 2. Periostealis osteosarcoma | közepes malignitású |
| 3. Nagy malignitású csontfelszíni osteosarcoma | nagy malignitású |
| 4. Juxtacorticalis (parostealis) osteosarcoma | alacsony malignitású |
| 5. Szekunder osteosarcoma | nagy malignitású |
| 6. Centrális, jól differenciált osteosarcoma | alacsony malignitású |
| 7. Dedifferenciált osteosarcoma | nagy malignitású |
| 8. Extraossealis osteosarcoma | nagy malignitású |
| II. Porcképző tumorok | |
| Benignus | |
| 1. Chondroma | latens, esetenként aktív |
| 2. Osteochondroma | aktív (csontérés után latens) |
| 3. Chondroblastoma | aktív, agresszív |
| 4. Chondromyxoid fibroma | aktív, agresszív |
| Malignus | |
| 1. Chondrosarcoma (centrális és perifériás) | 60% alacsony-, |
| 20% közepes-, | |
| 20% nagy malignitású | |
| 2. Secunder chondrosarcoma | alacsony malignitású 90%, |
| nagy malignitású 10% | |
| 3. Perifériás, vagy juxtacorticalis | alacsony-, |
| chondrosarcoma | közepes malignitású |
| 4. Mesenchymalis chondrosarcoma | |
| nagy malignitású | |
| 5. Világos-sejtes chondrosarcoma | alacsony malignitású |
| 6. Myxoid chondrosarcoma | közepes, ill. |
| nagy malignitású | |
| 7. Dedifferenciált chondrosarcoma | nagy malignitású |
| III. Óriássejtes tumor (osteoclastoma) | |
| Intermedier dignitású | 80 %-ban benignus, 20 %-ban malignus, |
| vagy malignusan transzformálódó forma | |
| IV. Csontvelő eredetű tumorok | |
| 1. Ewing sarcoma | nagy malignitású |
| 2. Malignus lymphoma (reticulum sejt sarcoma) | közepes malignitású |
| 3. Myeloma multiplex | közepes malignitású |
| V. Ér eredetű tumorok | |
| Benignus | |
| 1. Haemangioma | latens, aktív |
| 2. Lymphangioma | latens, aktív |
| 3. Glomus tumor (glomangioma) | aktív |
| Semimalignus | |
| 1. Haemangioendothelioma | aktív, agresszív |
| 2. Haemangiopericytoma | aktív, agresszív |
| Malignus | |
| 1. Malignus haemangioendothelioma | alacsony, közepes malignitású |
| 2. Malignus haemangiopericytoma | alacsony, közepes malignitású |
| 3. Angiosarcoma | nagy malignitású |
| VI. Egyéb kötőszöveti eredetű tumorok | |
| Benignus | |
| 1. Desmoplasticus fibroma | aktív, agresszív |
| 2. Lipoma | latens, aktív |
| Malignus | |
| 1. Fibrosarcoma | alacsony, közepes, nagy malignitású |
| 2. Liposarcoma | alacsony, közepes, nagy maligntiású |
| 3. Malignus mesenchymoma | nagy malignitású |
| 4. Malignus fibrosus histiocytoma | közepes, nagy malignitású |
| 5. Differenciálatlan sejtes sarcoma | nagy malignitású |
| VIIÍ. Egyéb tumorok | |
| 1. Chordoma | alacsony malignitású |
| 2. Adamantinoma | alacsony malignitású |
| 3. Neurilemmoma (Schwannoma) | aktív, agresszív |
| 4. Neurofibroma | aktív, agresszív |
| Tumorszerű csontelváltozások | |
| 1. Solitercsontcysta | latens, aktív |
| 2. Aneurysmás csontcysta | aktív, agresszív |
| 3. Juxtacorticalis csontcysta (intraossealis ganglion) | latens, aktív |
| 4. Metaphyseal fibrosus defectus (nem ossificalódó csontfibroma) | latens, aktív |
| 5. Eosinophil granuloma | latens, aktív, agresszív |
| 6. Fibrosus dysplasia | aktív, agresszív |
| 7. Myositis ossificans | latens, aktív |
| 8. Hyperparathyreoidismus okozta barna tumor | aktív, agresszív |
| 9. Intraossealis epidermoid cysta | latens, aktív |
| 1.2. Csonttumorok stádium besorolása (Enneking szerint) | |
| (Evidencia szint 11A, 12A) |
| A., Jóindulatú csont tumorok: | latens | |
| aktív | ||
| agresszív | ||
| B., Rosszindulatú csont tumorok: | ||
| I.A. G1 | TI | M0 |
| I. B G1 | T2 | M0 |
| II. A G2 | T2 | M0 |
| II. B G2 | T2 | M0 |
| III. A G1-2 | TI | Ml |
| IV. B G1-2 | T2 | Ml |
ahol G1 az alacsony-, a G2 a nagy szöveti malignitást, T1 a rekeszen belüli-, a T2 a rekeszen kívüli, az M0 távoli áttétek hiányát, az M1 távoli áttéteket jelent (Evidencia szint 12A).
Az UICC által ajánlott TNM séma a myeloma multiplex, a peri- és a parostealis sarcoma kivételével a csontdaganatok nagy részére szintén alkalmazható.
TNM klinikai klasszifikáció.
T - primer tumor
| TX | Primer tumor nem ítélhető meg |
| T0 | Nincs kimutatható primer tumor |
| TI | A tumor a corticaslist nem töri át |
| T2 | A tumor a corticalison túlterjed |
N - regionális nyirokcsomók
| NX | A régionális nyirokcsomók nem ítélhetők meg |
| N0 | Nincs régionális nyirokcsomó áttét |
| NI | A régionális nyirokcsomóban áttét van |
M - távoli áttét
| MX | Távoli áttét nem ítélhető meg |
| M0 | Nincs kimutatható távoli áttét |
| Ml | Kimutatható távoli áttét van |
WHO által javasolt histopathológiai grading
| GX | A differenciáció grading-je nem ítélhető meg |
| G1 | Jól differenciált |
| G2 | Mérsékelten differenciált |
| G3 | Rosszul differenciált |
| G4 | Nem differenciált |
TNM stádium rendszer
| Stádium I.A | G1,2 | T1 | N0 | M0 |
| Stádium I.B | G1,2 | T2 | N0 | M0 |
| Stádium II.A | G3,4 | T1 | N0 | M0 |
| Stádium II.B | G3,4 | T2 | N0 | M0 |
| Stádium III. | Nem definiált | |||
| Stádium IV.A | Bármely G | bármelyT | N1 | M0 |
| Stádium IV.B | Bármely G | bármelyT | bármely N | M1 |
A chondrosarcomák histopathológiai osztályozása
| Grade I. | Jól diffrenciált. A normális porcra nagyfokban hasonlító elváltozás, a magok kicsik, sötétre festődnek, sejtdús területek, ill. osztódó alakok hiányoznak. |
| Grade II. | Közepesen differenciált. Az előbbieknél kevésbé differenciált forma, nagyobb magokkal, cellularis területekkel. Az osztódó alakok száma kettőnél kevesebb 10 nagy nagyítású látótérben |
| Grade III. | Rosszul differenciált. Osztódó és cellularis területeket tartalmazó, szövetileg könnyen felismerhető malignus tumor |
II. Diagnózis
2. Diagnosztikai teendők (Evidencia szint 12A, 28B)
2.1. Diagnosztikai algoritmus a pontos diagnózis elérése céljából
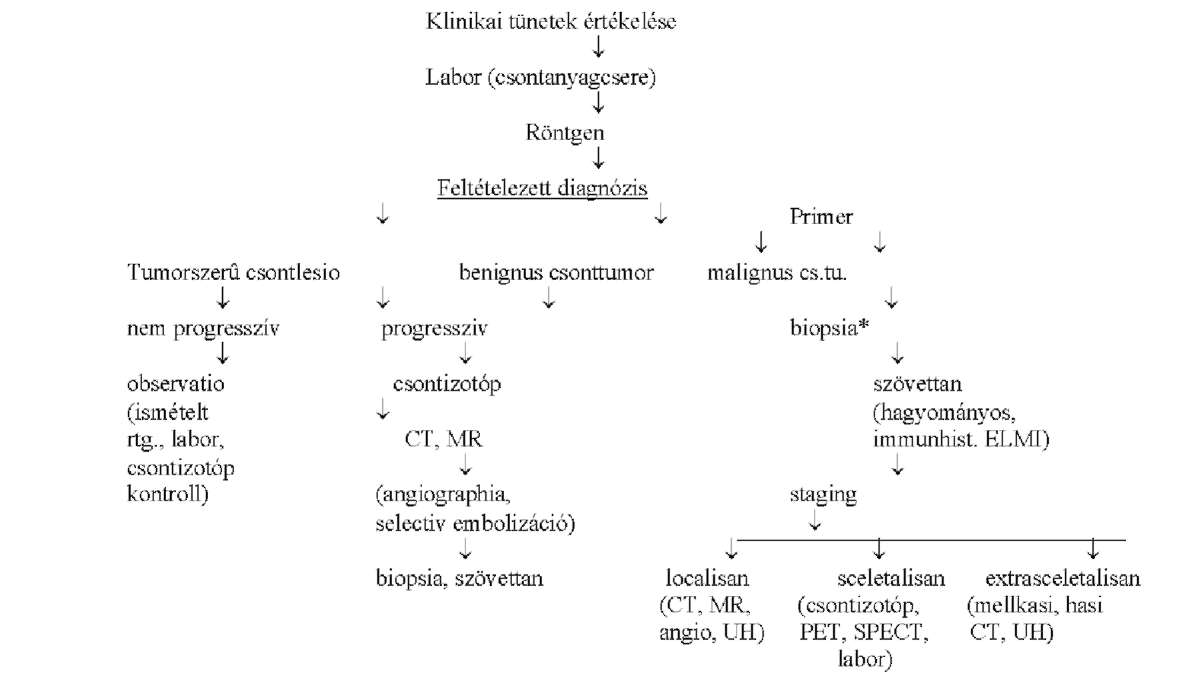
*Megjegyzés:osteo- és Ewing sarcomáknál,ahol preoperativ kemoterápia a kezelés szerves része, a biopsia megelőzi a CTés MR vizsgálatokat. Egyébként a biopsia a diagnosztikus sor utolsó láncszeme.
A diagnosztikai vizsgálatok malignus tumorok esetében részben átfedik egymást, részben egymásból adódnak. Szét lehet választani a vizsgálatok sorrendjét idő függvényében, ill. az előző vizsgálatok eredményétől függően.
- Anamnesis
- Fizikális vizsgálat
EKG és laboratóriumi vizsgálatok (teljes vérkép, süllyedés, máj-, vesefunkciók, szérum kalcium, foszfor, alkalikus foszfatáz szükség szerint kiegészítve speciális laborvizsgálatokkal így: prosztatikus eredetű savi foszfatáz, immun elektroforézis, szérum elektroforézis, vizeletben Bence- Jones fehérje, alfafötoprotein, egyéb tumor markerek stb.)
- Érintett csontokról 2 ir. rtg., szükség szerint CT, MR.
- Szükség szerint (lásd: részletes részt) csontizotóp vizsgálat (háromfázisú csontizotóp, SPECT)
- Szükség szerint angiográfia, szelektív embolisatio.
- 2 ir. mellkas rtg. felvétel (tüdő metastasis gyanúja esetén mellkas CT)
2.2. Patológiai vizsgálatok (Evidencia szint 8A, 12A, 16C, 28B)
2.2.1. Műtét előtti szövettani vizsgálat (biopsia)
Minden esetben indokolt az onkoterápia előtt. Csonkoló műtétet, amputatiot szövettani vizsgálat (műtét előtti, vagy intraoperatív) nélkül csak kivételes esetben végezhetünk (pl. ha a daganat kiterjedése, mérete, fennálló keringési zavar stb. meghatározza a sebészi beavatkozás formáját).
Biopsiák formái:
1. Aspirációs cytológia:
Feltétele: cytológiában jártas patológus Indikációk:
Egyértelmű klinikai-radiológiai tumor megjelenés esetén a diagnózis
- alátámasztására
- ismert primer tumor csontáttétének diagnosztizálására
2. Percutan hengerbiopsia: Indikációk: - szolid tumor
- metastasis igazolására ismert primer tumor esetén
3. Sebészi nyílt feltárásos szöveti mintavétel
Megjegyzés: az előbbi szövettani mintavétel formáknál, ha kétség merül fel a szövettani diagnózist illetően, ill. ha klinikai-radiológiai kép és a szövettani diagnózis nem felel meg egymásnak, akkor minden esetben nyílt feltárásos szövettani mintavétel szükséges.
Biopsia szövettani feldolgozása:
Pufferolt formalinban fixált, paraffinba ágyazott metszetek, hagyományos festés. Szükség szerint (ha a pontos diagnózis megkívánja):
- Immunhisztokémia
- Elektromikroszkópia
- Cytomorphometria ("borderline", intermedier dignitású daganatoknál, pl. órisássejtes csonttumor)
- Molekulár biológiai vizsgálatok (kromoszóma rendellenesség, P53 expresszió, stb.)
2.2.2. Műtét alatti szövettani vizsgálat Indikáció:
- a tumor dignitásának a megítélésére.
- sebészi metszésvonal, resectios szél tumormentességének bizonyítására.
Feltétel: fagyasztó mikrotom ebben járatos patológus
2.2.3. Műtét utáni szövettani vizsgálat (Evidencia szint 5A, 12A)
A műtéti úton eltávolított specimen részletes szövettani feldolgozása, a daganat kemotherápia érzékenységének meghatározása. Praeoperativ kemotherápia után osteosarcoma és Ewing sarcoma, valamint malignus fibrosus histiocytoma esetében jön elsősorban szóba.
A daganat kemoterápia érzékeny, ha az eltávolított tumor teljes keresztmetszetét mikroszkóppal, semiquantitatív módszerrel vizsgálva a túlélő tumorsejtek 10 százalék alatt vannak. Mérsékelten érzékeny a daganat, ha a túlélő tumorsejtek 10-50 százalék között mozognak és kemotherápiára nem reagál a daganat, ha a túlélő tumorsejtek 50 százalék fölött vannak.
2.3. Diagnosztikai algoritmus a praeoperatív kemoterápia előtt vagy alatt A daganat stádiumának meghatározása:
- Fizikális vizsgálat, laboratóriumi vizsgálatok, mellkas rtg.
- Kétirányú rtg. a tumorról
- CT vizsgálat a primer tumorról
- Szükség esetén MR vizsgálat a primer tumorról
- 3 fázisú csontizotóp vizsgálat a tumor kiterjedésének megítélésére, egyéb sceletalis metastasisok kimutatására, valamint a neoadjuváns kemotherápia eredményességének megítélésére a kezelés 2. és 8. hetében
- Szükség szerint mellkas CT (mellkas rtg.-n met. gyanú esetén)
- Hasi ultrahang a kismedencei paraaorticus nyirokcsomók, máj, lép érintettségének tisztázására
2.4. Diagnosztikai algoritmus a postoperatív kemotherápia után
- Fizikális vizsgálat, laboratóriumi vizsgálatok (különös tekintettel a csontanyagcserére), mellkas rtg.
- Csontizotóp vizsgálat
- Amennyiben végtagmegtartó műtét volt, úgy adott időpontokban (lásd később a részletes részben) 2 ir. rtg. felvétel, esetleg CT vizsgálat, angiográfia a recidívák kimutatására
- Tüdő CT a felismeréskor már jelenlevő tüdő áttétek utánkövetésére.
- Amennyiben csupán tumor megkissebítendő műtétet végeztek, vagy a beteg sebészi kezelésbe nem egyezett bele, úgy tumor nagyságának, növekedési ütemének, ill. a kettőződési és felezési idő meghatározása céljából
2.5. Diagnosztikai algoritmus végtagmegtartó műtét indikációjához
- Az érintett csontról 2 ir. rtg. felvétel
- Daganat kiterjedésének, a csontdestructio mértékének meghatározása CT vizsgálattal
- Intramedullaris és lágyrész kiterjedésének, ill. esetleges skip metastasisnak,az ér-, idegképletekhez való viszonyának kimutatására MR felvétel
- Amennyiben fennáll az ér-, idegképletek befogásának veszélye, vagy végtagkeringési zavar van, úgy angiográfia is. (Kombinálható szuper szelektívangiográfiával,cytostaticum beadásával, ill. a daganatot ellátó erekembolizációjával).
- Csontizotóp vizsgálat egyéb skeletalis metastasisok kimutatására
- Mellkas 2 ir. rtg. mellkasi áttétek kimutatására, amennyiben gyanú van, úgy mellkas CT is
- Hasi UH vizsgálat parenchymas szervekés hasi nyirokcsomók érintettségének kizárására
2.6. Diagnosztikai algoritmus metastasectomia előtt
- Laboratóriumi vizsgálatok
- Summatios mellkas rtg.
- Izotópos, UH és CT vizsgálatok (szükség szerint MR) annak kizárására, hogy az ismert szervi áttéten kívül másutt a szervezetben kimutatható nagyságú metastasis van
- Pulmonális metastasisoknál, vagy annak gyanújánál 2 ir. mellkas felvételen kívül mellkas CT vizsgálat annak igazolására, hogy a kimutatható áttétek száma 15-nél nem több, valamint az áttétek növekedési üteme, kettőződési ideje 30 napnál kisebb
III. Kezelés
3. A kezelés általános elvei
(Evidencia szint 5A, 7A, 8A, 12A, 15B, 28B, 29A, 33C, 34B)
Magyarországon évente mintegy 15-20 újosteosarcoma, kb. 10-12 chondrosarcoma és 5-10 Ewing sarcoma fordul elő. Éppen a ritka megbetegedési arány miatt a betegek ellátása minden országban központosított. Hazánkban az OOI-ben, a SE Ortopédiai Klinikáján és a II. Gyermekklinikán együttműködve az OORI-val, illetve a többi egyetemi centrumban történik a primer csonttumoros betegek komplex kezelése. A magas malignitási fokú betegség multidiszciplináris kezelése komplex diagnosztikából, szükség szerint chemotherápiából, az adott műtéti terület ellátásából, a beteg testi/lelki rehabilitálásából,a későbbi áttétek megelőzéséből áll. Ismeretes, hogy azosteosarcoma kezeletlenül a betegek 100%-ában 1 éven belül halálhoz vezet. Az önmagában végzett műtéti beavatkozás (amputatio) az érintettek 20%-ában ad csak 5 éves túléléshez lehetőséget, az operációt kiegészítő pre-és postoperativ chemotherapia 70-80%-os 5 éves túlélést tesz lehetővé. A korán felismert esetek kb. 60-75%-ban lehetőség nyílik végtagmegtartó műtétetek végzésére is. Ezt a képalkotó eljárások (CT, MR) fejlődése, a hatásos chemotherapia és a sebészi rekonstrukciós technika fejlődése (csontbank, tumor endoprothesis, stb.) tette lehetővé.
3.1. Csontdaganatok és daganatszerű elváltozások kezelése:
| 3.1.1. Tumorszerű csont elváltozások | Terápia |
| Solitercsontcysta | Deposteroid intracysticusan |
| vagy excochl. spong. plast. | |
| Aneurysmas csontcysta | Excochl. spong. |
| plast., vagy selectiv embolisatio | |
| Juxtacorticalis csontcysta (intraossealis ganglion) | Excochl., spong. plast. |
| Metaphyseal fibrosus defectus | Observatio, vagy |
| (nem ossificalódó csontfibroma) | excochl. spong. plast. |
| Eosinophil granuloma | Excochl. spong. plast. |
| Fibrosus dysplasia | Excochl., spong. plast., |
| vagy observatio | |
| Myositis ossificans | Observatio, vagy resectio |
| Hyperparathyreoidismus okozta barna tumor | Oki terápia és oberv., |
| vagy excochl. spong. plast. | |
| Intraossealis epidermoid cysta | Excochl. spong. plast. |
3.1.2. Benignus tumorok:
| Diagnózis: | Excochleatio | En bloc resectio |
| (spongiosa plastica) | ||
| Osteoid osteoma | + | |
| Osteoblastoma | + | + |
| Enchondroma | + | |
| Osteochondroma | + | |
| Chondroblastoma | + | + |
| Chondromyxoid fibroma | + | + |
| Óriássejtes csonttumor | + | + |
| Haemangioma | + | |
| Lymphangioma | + | |
| Glomus tumor | + | |
| Lipoma | + | |
| Desmoplaticus fibroma | + | + |
| Haemangioendothelioma | + | |
| Haemangiopericytoma | + |
Megjegyzés: Latens és aktív stádiumú benignus csonttumoroknál elsősorban excochleatiot végzünk (szükség szerint spongiosa plasticával), míg agresszív stádiumnál en bloc resectiot. Átfedések vannak bizonyos tumorfajtáknál (pl. óriássejtes csonttumor), mivel aktív és agresszív stádiummal is rendelkezhetnek, valamint figyelembe kell venni a tumor ízület közeli lokalizációját is, fel kell mérni az ízület megtartás lehetőségét, recidíva veszély nagyságát.
3.1.3. Malignus tumorok:
| Grade 1 tumorok: | Sebészi | Chemoth. | Radioth. |
| chondrosarcoma (grade I) | + | ||
| chordoma | + | ||
| adamantinoma | + | ||
| parostealis és alacsony | |||
| malignitású osteosarcoma | + | ||
| világos sejtes chondrosc. | + | ||
| Grade 2 tumorok: | |||
| Osteosarcoma | + | + | |
| Ewing sarcoma, PNET | + | + | + |
| Chondrosarcoma (gr. II-III) | + | -(+ ?) | + (?) |
| MFH | + | + | + (?) |
A sebészi kezelés típusai
Biopsia (feltárásos sebészi, esetenként percutan tűbiopsia, aspiraciós cytologia).
Daganat eltávolítása.
Végtagmegtartó műtét és rekonstrukció
Amputáció, exarticulatió, rotációs plastica
Metastasectomia.
3.2. Daganat eltávolítása
3.2.1. Palliatív műtétek: Általános indikációk:
- generalizált tumoros folyamat
- Ismeretlen primer tumor csontáttéte
- Belgyógyászati kontraindikáció, beteg általános állapota
- Tumor localis kiterjedése
Palliatív műtétek fajtái:
- Osteosynthesis (patológiás törés esetén)
- Stabilizáló műtétek (fenyegető törésveszély esetén)
- Amputáció
Ajánlott műtétek: velőűr szegezés
- Velőűr köteg szegezés
- Ender szegezés
- Lemezelés, fix szögletű lemez
- A fenti eljárások kombinálása a tumoros góc feltárásával, kikaparásával és a csontdefektus csontcementtel történő kitöltésével
3.2.2. Tumort megkisebbítő műtét, tudottan intralaesionális beavatkozás Indikációi:
- Jóindulatú agresszív, de technikailag irrezekábilis tumorok (pl. desmoid) Inoperabilis, alacsony malignitású tumorok (pl. chondrosarcoma)
- Ha a beteg az amputatioba, hemipelvectomiába nem egyezik bele, és egyidejűleg alacsony malignitású tumorról van szó (pl. chondrosarcoma)
3.2.3. Csonkoló műtétek
- amputatio (exarticulatio)
- rotatios plastica (amputatioval egyenértékű, jobb rehabilitációt biztosít) Általános indikáció:
- ha radikális tumormentességet másképpen nem lehet elérni
palliatív céllal a beteg fájdalmainak csökkentésére, ápolhatóságának biztosítására
3.2.4. Végtagmegtartó műtétek
- Végtagmegtartó műtétek ellenjavallatai:
1. Lágyrészeket, izmokat messze beszűrő, a subcutist elérő daganat, mely sebészi radikalitást lehetetlenné tesz.
2. Ér-, idegképletek beszűrése.
3. Sebészi radikalitás ugyan elérhető, de rekonstrukcióra nincs lehetőség
4. Beültetett csontot, protézist nem tudjuk lágyrészekkel fedni.
5. A beteg rossz általános állapota.
- Relatív ellenjavallat:
Érintett terület egyidejű osteomyelitise
ha az adott tumor nagy malignitású, és kemoterápiára resistens (osteosarcoma, Ewing sarcoma, malignus fibrosus histiocytoma egyes esetei) Egyidejű távoli áttét(ek) Pathológiás törés
Az adott tumor progressziója praeoperatív kemoterápia alatt (CT, izotóp)
Áttét esetén, ha a primer tumor nem ismert, vagy ismert, de onkológiailag ellátatlan
3.3. Rekonstrukciós műtétek (Evidencia szint 10A, 34B, 36A) Ajánlott műtétek:
| 3.3.1. Diaphysis pótlására: | 1. autológ fibula (érnyeles lebennyel, vagy anélkül |
| 2. Homológ csontszegment | |
| 3. Modul rendszerű tumor endoprotézis | |
| 4. Autoklávozott resekátum |
3.3.2. Epi- metaphysis pótlására:
| 1. | Resectios arthrodesis Juvara szerint |
| 2. | Total arthroplastica, vagy haemiarthroplastica |
| 3. | Masszív osteochondralis graft |
| 4. | Autológ fibula transposito (radius dist. vég, illetve fibula dist. vég, illetve |
| humerus proximalis rész pótlására) |
3.3.3. Rekonstrukciós lehetőség belső haemipelvectomiánál:
- Medencelapát prox. kétharmadának resectioja esetén a medencegyűrű intakt marad, resectio nem szükséges.
- symphysis, os pubis és/vagy ülőcsont resectioja után rekonstrukció nem szükséges.
- Az incisura ischiadica tájéki defektusok pótlása: autológ fibulával, másik oldali medencelapát darabbal, homológ medencecsont idommal ajánlott.
3.3.4. Periacetabularis resectiok után a defektus pótlása lehetséges:
- A műtéti resecatummal autoklávozás után
- Homológ medencecsont szegmenttel
- Fém medenceprotézissel
- Arthrodesissel, amikor a femurfejet az os ileum csonkjához rögzítjük
3.4. Metastasectomia
Ellenjavallatok:
- irrezekábilis primer tumor
- más szerv, szervek egyidejű áttéte (relatív kontraindikáció)
- az elsődleges műtét időpontja és az áttét megjelenése között 6 hónapnál kevesebb idő telt el (relatív kontraindikáció)
- 15-nél több tüdőáttét jelenléte
- 30 napnál rövidebb kettőződési idejű áttétek Onkológiai radikalitással nem operálható daganat áttét
3.5. A csonttumorok sugárkezelése 3.5.1. A tumor radioterápiája
1. Radioszenzitív daganatok (Ewing sarcoma, malignus fibrosus hystiocytomama, stb.)
2. Végtagmegtartó műtéteknél a definitív műtétet megelőzően a tumorra és az érintett egész csontra (Ewing sarcoma)
3. Ha a definitív műtét resectios vonala (postoperatív szövettani vizsgálat) tumorral kontaminált
Relatív kontraindikáció: Masszív fémanyagok, protézisek jelenléte a besugározandó terület körül. Radioterápia a régióra:
- Bizonyítottan érintett nyirokcsomók esetén
- Műtét után, vagy helyett (ha sebészi beavatkozás nem történhetett)
3.5.2. Kombinált radio- és kemoterápia: indikációk:
- ha a beteg műtétbe nem egyezik bele
- a műtét nem lehetséges a daganat kiterjedése miatt
-törzsközeli localisatiojú Ewing sarcoma,osteosarcoma (sacrum,gerinc localisatio)
- Palliatív radioterápia javasolt:
Tumor indukálta fájdalom csökkentésére, fenyegető törésveszély esetén, vagy ha műtét nem jön szóba (multiplex metastasis és/vagy inoperabilis primer tumor, stb.)
Ewing sarcoma: az érintett csont teljes egészének besugárzása a preoperatív időszakban 30-50 gray összdózissal végtagmegtartó műtét esetén.
Törzsközeli (gerinc,sacrum) lokalizációnál szóbajön csakchemo-és radiotherapia is, ilyenkor 80-100 grayösszdózissal. Malignus fibrosus histiocytoma, nagy malignitású chondrosarcomákesetén, ha a műtét technikai okokból nem kellő radikalitású, a tumorágy ill. visszamaradó csont masszív besugárzása.
3.6. Csonttumorok kemoterápiája
(Evidencia szint 4B, 5A, 7A, 15B, 19C, 25B, 28B, 31B, 36A)
3.6.1. A citosztatikus kezelés általános elvei
Indokolt adni minden úgynevezett kemoterápia szenzitív csonttumorok esetében (osteosarcoma, Ewing sarcoma, malignus fibrosus hystiocytoma, mesenchymalis chondrosarcoma, stb.).
Ewing sarcoma, ill. osteosarcoma esetében már felismeréskor már 70-80 %-ban a tüdőben jelen vannak mikrometastasisok. Ennek megfelelően korábban az 5 éves túlélési eredmény radikális csonkoló műtéti beavatkozások után is 10-20 százalék körül mozgott. Azadjuváns, újabban a neoadjuváns polikemoterápia bevezetése (Methotrexat, Ifosfamide, Adriamycin, Cisplatin) az 5 éves túlélésben jelentős pozitív változásokat (osteosarcománál 70-80 százalék, Ewing sarcománál 60-65 százalék) eredményezett.
Irodalmi-statisztikai adatok alapján az optimális kemoterápiát a definitív műtét előtti intenzív neoadjuváns, majd a műtétet követő adjuváns kezelés jelenti.
3.6.2. A neoadjuváns (praeoperatív) kezelés elve:
- Megkisebbíti a primer daganat méretét. Az esetekegy részében amputatio helyett végtagmegtartó műtét végzése válik lehetővé.
- A megelőző biopsia során leszakadó és keringésbe kerülő daganatsejteket elpusztítja
- Hat a tüdőben lévő mikrometastasisokra
- Lehetőséget ad a definitív műtétnél a tumor eltávolítását követően szövettani kiértékelésre, tehát a daganat kemoterápia érzékenységének meghatározására. Ezáltal az adjuváns kemoterápiában változtathatunk, ha a daganat a praeoperatív kemoterápiára rosszul reagált
- Lehetősége ad a sebész számára a definitív műtétre, rekonstrukcióra történő felkészülésre (homológ csont, tumorprotézis beszerzése)
3.6.3. Az adjuváns kezelés elve
- Elpusztítja a definitív műtétnél keringésbejutó daganatsejteket.
- Elpusztítja a már meglévő áttéteket.
3.6.4. A citosztatikus protokollok
Európában az osteosarcoma és a Ewing sarcoma kezelésére leginkább elterjedt a COSS protokoll, ill. CESS protokoll (cooperatív osteosarcoma study). A fenti protokollok mellett azonban Amerikában, ill. egyes országokban több fajta hasonló összetételű gyógyszer kombinációk terjedtek el (USA: Rosen: T-9, T-11 protokollok osteosarcomákra).
3.7. Malignus csonttumorok kezelésének személyi, technikai feltételei
Primer malignus csonttumorok kezelése lehetőleg csonttumor centrumban történjék.
Ennek oka: primer csonttumorok ritkák, osteosarcománál évi 15, Ewing sarcománál évi 5-8, chondrosarcománál évi 8-12 újesettel számolhatunk Magyarország 10 milliós lakosságára vonatkoztatva. Csak centrumban biztosítható az évi megfelelő műtéti szám, megfelelő terápiás javaslat, interdiszciplináris együttműködés különböző szakemberek (ortopéd sebész, patológus, radiológus, általános sebész, rehabilitációs szakember, onkológiai belosztály, gyerekorvos) között.
Diagnosztikai és terápiás feltételek:
- Lehetőség immunhisztokémiára, elektomikroszkópiás vizsgálatra
- Elérhető CT, MR, három fázisú izotóp vizsgálat
- Szükség szerint angiográfia
- Tumorprotézis készlettel rendelkezzenek
- Rendelkezésre álljon, vagy beszerezhető legyen homológ csontgraft (csontbank) Személyi feltételek:
- Onkológiai, ill. onkológiai sebészi előképzettség
- Rekonstrukciós műtéttechnikában való jártasság
- Műtéti szövődmények ellátására lehetőség (társszakmák jelenléte)
- Csonttumor diagnosztikában járatos patológus, radiológus, konzíliumra lehetőség
- Elérhető radio-, ill. kemoterápia, az ezt adó szakemberek konzíliumával
3.8. Csonttumoros betegek utánkövetése (Evidencia szint 7A, 8A, 20D, 22B, 30D, 33C, 36A)
3.8.1. Benignus, latens és aktív csonttumorok sebészi kezelését követő utánkezelés.
-3, majd 6 hónap után, illetve a defectus nagyságától függően a sebész egyéni megítélése szerint kellő időszakonként a recidíva kizárására és a csontos átépülés nyomonkövetésére kétirányú rtg. felvétel a műtéti területről
- Műtét utáni panaszok persistálása esetén kétirányú rtg. felvétel, szükség szerint kontroll CT visszamaradó laesio (pl. osteoid osteoma nidusa) kimutatására
-További 6 hónaponkénti kontroll,összességében 3 évig (kétirányú kontroll rtg.)
3.8.2. Benignus agresszív csonttumorok, ill. tumorszerű csontelváltozások utánkövetése
- megegyezik az előbbivel utánkövetés azonban minimum 5 évig szükséges
3.8.3. Alacsony malignitású csontsarcomák (chondrosarcoma, adamantinoma, haemangioendotelioma, stb.) utánkövetése.
- Rekonstrukciós műtét esetén a csontátépülés vizsgálatára kétirányú kontroll rtg. 3, 6 hónappal műtétet követően
- Első 3 évben háromhavonként kontroll vizsgálatok (lásd korábban). Félévenként mellkas kétirányú rtg., szükség szerint tüdőáttét gyanúja esetén tüdő CT, a műtétet követő minimum 6-8 évig rendszeres kontroll évente (késői metastasisok!)
- Helyi recidíva esetén lásd a teljes primer műtét előtti diagnosztikai algoritmust
3.8.4. Nagy malignitású csontsarcomákesetén tekintettel a daganat gyors növekedésére, valamint arra a tényre, hogy a recidívák és áttétek rendszerint a primer műtétet követően 1,5-3 éven belül jelentkeznek az alábbi algoritmus javasolt:
- Az első két évben 3 hónaponkénti kontroll javasolt: laborvizsgálat (süllyedés, szérum alkalikus foszfatáz), kétirányú mellkas felvétel (gyanú esetén mellkas CT), kétirányú rtg. a műtéti területről
- 2-5 évig terjedő időszakban félévenként laborvizsgálat, mellkas rtg., háromfázisú csontizotóp vizsgálat. Localis recidíva gyanúja esetén, amennyiben lehetséges CT, MR, szükség esetén ismételt biopsia, ill. angiográfia
- 3-6 évig félévente rtg., izotóp vizsgálat a műtéti területről és a mellkasról (szükség szerint kiegészíthető mellkas CT-vel, hasi UH-val)
Megjegyezés: chondrosarcomán kívül Ewing sarcoma is adhat 6-8 év után késői metastasisokat. Amennyiben a beteg kezelése során kemoterápiát is kapott, úgy a kemoterápiát követő 5. évtől postkemoterápiás daganatok lehetőségére is gondolnunk kell (Ewing sarcoma esetében ez kb. 10 százalék).
4. Diagnosztikai és kezelési algoritmus egyes csonttumoroknál
4.1. Osteoid osteoma és benignus osteoblastoma (Evidencia szint 12A, 14A, 16C)
Diagnosztika: lásd általános rész (2)
Megjegyzés: fizikális vizsgálat, laborvizsgálatok (rendszerint negatívak) szalicilát teszt kétirányú szummációs rtg. felvétel bizonytalan esetben, ha centrális nidus nem ábrázolódik CT vizsgálat (medence, gerinc és vállövi localisationál CT kötelező) differenciál diagnosztikai szempontból, ha a klinikopatológiai kép nem egyértelmű csontizotóp vizsgálat Kezelés: Sebészi, a nidus excochleatioja, vagy épben történő resectiója. Szükséges tárgyi feltétel: képerősítő.
Utánkövetés: lásd általános rész (3.8).
4.2. Konvencionális centrális nagy malignitású osteosarcoma (Evidencia szint 4B, 7A, 22B, 25B, 26B, 29A)
Diagnosztika: lásd általános rész (2)
Megjegyzés:
- Kétirányú szummációs rtg. felvétel már gyakran felveti a helyes diagnózist
- CT a csont corticalis destrukciójának kimutatására
- Végtagmegtartás eldöntésénél MR vizsgálat (lágyrészkiterjedés, intramedullaris kiterjedés, skip metastasisok kimutatása)
- Szükség szerint angiográfia
- Biopsia (feltárásos sebészi biopsia, esetleg percutan henger)
-További prae-és postoperatívdiagnosztikai lépések, ill. a tumor stádiumának meghatározása, lásd általános rész (2) Kezelés:
- praeoperatív kemoterápia definitív műtét, postoperativ kemoterápia
- Enormis méretű tumorok esetén, amputáció, majd postoperatív kemoterápia
- Törzsközeli inoperabilis osteosarcomáknál (sacrum, gerinc) kemoterápia.
Utánkövetés: műtétet követő minimum 5 évig (3.8).
4.3. Csontfelszíni (surface) nagy malignitású osteosarcoma Diagnosztika: lásd általános rész (2)
Megjegyzés:
CT minden esetben szükséges a korrekt diagnózis felállításához!
Kezelés: szendvicsterápia: praeoperatív kemoterápia:
- definitív műtét
- postop. kemoterápia
Utánkövetés: lásd általános rész (3.8.)
4.4. Periostealis osteosarcoma Diagnosztika: lásd általános rész (2). Megjegyzés:
CT minden esetben szükséges a pontos diagnózishoz!
Kezelés: a daganat radikális sebészi eltávolítása, majd kemoterápia megpróbálható, de jelentős irodalmi tapasztalat nem áll rendelkezésre.
Utánkövetés: lásd általános rész (3.8.)
4.5. Parossealis osteosarcoma Diagnosztika: lásd általános rész (2) Megjegyzés:
- CT a korrekt diagnózishoz minden esetben szükséges. Kezelés: kizárólag sebészi (radikálisan, vagy szélesen az épben)
Megjegyzés: ritka esetben parossealis osteosarcoma másodlagosan dedifferenciálódhat, ilyenkor pulmonalis metastasisok kezelésére kemoterápia is szóba jön.
Utánkövetés: lásd általános rész (3.8.)
4.6. Alacsony malignitású centrális osteosarcoma Diagnosztika: lásd általános rész (2) Megjegyzés:
Pontos diagnózist csak a szövettani gondos elemzés ad! Kezelés: sebészi (radikálisan, vagy szélesen az épben).
Megjegyzés: végtagmegtartás rendszerint lehetséges (indikációk, kontraindikációk lásd általános rész). Utánkövetés: lásd általános rész (3.8.)
Megjegyzés: alacsony malignitású osteosarcoma ritkán, de átmehet nagy malignitásúba, ilyenkor kemoterápia indokolt.
4.7. Szekunder osteosarcoma (postirraditatios fibrosus dysplasia, M. Paget, óriássejtes tumor talaján kialakuló stb.) Diagnosztika: lásd általános rész (2)
Megjegyzés: anamnesis rendkívüli jelentőségű!
Kezelés: kombinált praeoperatív és postoperatív kemoterápia, valamint radikális sebészi kezelés (túlélés így is igen szerény).
Utánkövetés: legalább 10 évig (3.8.)
4.8. Enchondroma, hosszú csöves csontok centrális chondromája Diagnosztika: lásd általános rész (2).
Kétirányú rtg. felvétel: diagnózist valószínűsíti. Kezelés: exchochleatio, spongiosa plastica.
Megjegyzés: a hosszú csöves csontok úgynevezett centrális chondromájánál célszerű citofotometriát végezni, amennyiben aneuploidia áll fenn és a tumor recidivál, úgy az épben történő resecio szóba jön.
Utánkövetés: lásd általános rész (3.8.)
4.9. Osteochondroma (11A, 32C) Diagnosztika: lásd általános rész (2)
Megjegyzés: kétirányú szummációs rtg. felvétel (medence, lapocka, gerinc localisationál CTis). Malignizáció gyanúja esetén háromfázisú izotóp vizsgálat, esetlegesen MR vizsgálat is indokolt. Szövettani vizsgálat: grading!
Kezelés: kizárólag sebészi, az elváltozás alapjáról történő leválasztása.
Megjegyzés: szekunder malignizáció, másodlagos chondrosarcoma fennállásánál lágyrészköpennyel együtt célszerű a daganatot csontos alapjáról levésni.
Multiplex formánál nem kell törekedni minden egyes osteochondroma eltávolítására. Indikációk: - Nagy méret (malignizációra gyanús)
- Környező ér, ideg, izom, ín nyomása okozta panaszok
- Szomszédos csontok nyomása, tengelydeformitás
Utánkövetés: lásd általános rész (3.8.)
4.10. Chondroblastoma (Evidencia szint 5A, 12A, 23C) Diagnosztika: lásd általános rész (2) Megjegyzés:
Kétirányú szummációs rtg. felvétel, szükség szerint tomográfiával, ill. MR felvétellel kiegészítve (izületi felszín érintettsége!).
Kezelés: amennyiben az izületi felszínt, a subchondralis csontot a folyamat nem érinti az épben történő resectio javallt. Az ízületi felszín érintettsége esetén transarticularis feltárásból excochleatio, spongiosa plastica, ízületi felszín pótlása (crista idom, mozaik plastica), vagy excochleatio és a defektus csontcementtel történő kitöltése.
Utánkövetés: lásd általános rész (3.8.)
4.11. Chondromyxoid csontfibroma Diagnosztika: lásd általános rész (2) Megjegyzés:
Kétirányú szummációs rtg. felvétel (szükség szerint CT vizsgálattal kiegészítve). A rendszerint benignus radiomorphológiai kép miatt előzetes biopsia nem szükséges. Pontos diagnózist a szövettani vizsgálat ad.
Kezelés: sebészi, excochleatio, spongiosa plastica, recidívák esetén az épben történő resectio, vagy a defektus csontcementtel történő kitöltése javasolt.
Utánkövetés: lásd általános rész (3.8.).
4.12. Chondrosarcoma,
konvencionális, centrális, vagy perifériás (alacsony malignitás) (Evidencia szint 5A, 8A, 10A, 12A,27B, 34B)
Diagnosztika: lásd általános rész (2)
Megjegyzés:
Kétirányú szummációs rtg. felvétel már felveti az alacsony malignitású chondrosarcoma lehetőségét. CT felvétel a csontdestructio és lágyrészkiterjedés megítélésére
Végtagmegtartó műtét esetén MR vizsgálat fontos (nagy malignitású chondrosarcomák intramedullaris kiterjedése lényegesen nagyobb lehet mint azt a CT felvétel mutatja). Csontizotóp vizsgálat.
Szövettani vizgálat: célszerű előzetes feltárásos biopsia a malignitási fok meghatározásáral!
Aspirációs citológia egyértelmű klinikoradiológiai kép esetén szóba jön, intraoperatív fagyasztásos metszet megkísérelhető, de technikai okok miatt nem mindig értékelhető.
Kezelés: alacsony malignitású formáknál kizárólag sebészi, nagy malignitású formáknál, ill. dedifferenciált formáknál radikális sebészi, rendszerint amputatio, kemoterápiával kiegészítve. Utánkövetés: lásd általános rész (3.8.)
4.13. Myxoid chondrosarcoma, mesenchymalis chondrosarcoma, dedifferenciált chondrosarcoma (nagy malignitás) Diagnosztika: lásd általános rész (2)
Megjegyzés: a tumor intramedullaris kiterjedésére, skip metastasisokjelenlétére, lágyrészkiterjedésre vonatkozóan az MR vizsgálat lényegesen informatívabb, mint a CT.
Kezelés: elsősorban sebészi, kemoterápia, ill. radioterápia megpróbálható mesenchymalis chondrosarcománál és tüdő áttéteknél, de nem áll elég irodalmi adat rendelkezésre a hatásosságot illetően.
Utánkövetés: lásd általános rész (3.8.)
4.14. Világossejtes chondrosarcoma Diagnosztika: lásd általános rész (2) Megjegyzés:
Szummációs rtg. felvétel (rendszerint nem informatív), daganat kiterjedésére CT, MR egyaránt megfelelő vizsgálat. Pontos diagnózist csak az előzetes biopsia szövettani vizsgálata ad.
Kezelés: kizárólag sebészi (tekintettel a daganat alacsony malignitására, végtagmegtartás sokszor szóba jön). Radikalitás: szélesen az épben.
Utánkövetés: lásd általános rész (3.8.)
4.15. Óriássejtes csonttumor
(Evidencia szint 1A, 2C, 3C,6B, 18C, 21B, 32B, 37B)
Diagnosztika: lásd általános rész (2)
Megjegyzés: kétirányú szummációs rtg. felvétel már felveti a helyes diagnózist.
a tumor kiterjedésének megítélésére CT, vagy MR alkalmas, ez utóbbi differenciál diagnosztikai jelentőségű az aneurysmás csontcystáktól történő elkülönítéshez. A subchondralis terjedést, izület érintettségét legjobban MR mutatja.
Szövettani vizsgálat: rendszerint nem lehet következtetni a daganat biológiai viselkedésére, csak az egyértelműen malignus, vagy malignizálódott formákat lehet elkülöníteni. Ha lehetőség van célszerű mitosis index számolást, ill. DNS citofotometriát végezni.
Kezelés: sebészi
- Intermedier formánál excochleatio, spongiosa plastica lehetőleg az izületi felszín megtartásával. A recidívák csökkentése érdekében adjuváns phenolos öblítés, ill. csontcementtel történő kitöltés javasolt. Ismételt recidíváknál épben történő resectio szóba jön.
- Bizonyos esetekben (törzsközeli formák, sacrum localisatio, periacetabularis érintettség) az egyedüli lehetséges intralaesionális sebészi beavatkozást radioterápiával lehet kiegészíteni.
- Primeren malignus, vagy másodlagosan malignizálódott órisássejtes csonttumoroknál a tumor radikális resectioja mellett prae- és postoperaítiv kemoterápia is szóba jön.
Utánkövetés: lásd általános rész (3.8.)
4.16. Ewing sarcoma
(Evidencia szint 5A, 8A, 10A, 12A, 13A, 35D) Diagnosztika: lásd általános rész (2)
Megjegyzés: tekintettel arra, hogy a Ewing sarcoma gyakran több csontot érintő generalizált megbetegedés, ezért az érintett csont biopsiáján kívül javasolt, sternum biopsia, ill. csípőlapátból származó biopsia (aspirációs citológia) végzése is. A hagyományos kétirányú rtg. felvételen kívül minden esetben szükséges háromfázisú csontizotóp vizsgálat, CT helyett inkább MR ajánlott az intra- és extraossealis kiterjedés megítélésére.
- Szövettani vizsgálatot célszerű kiegészíteni immunhisztokémiával (pnet = primitiv neuroectodermalis tumortól történő elkülönítés érdekében).
(A Ewing sarcoma egyértelmű igazolása: kromoszóma vizsgálattal; 11-22-es kromoszóma translocatio, ahol erre lehetőség van.)
Kezelés:
- komplex: praeoperatív kemoterápia, majd teljes csont besugárzás, majd tumoros csontszegment resectioja, vagy amputatio, majd postoperatívkemoterápia.
- Recidívák esetén amputáció, ill. kemoterápia és radioterápia ajánlott.
- Törzsközeli localisationál (sacrum, csigolyák) mérlegelni kell a sebészi beavatkozás mértékét, tudunk-e radikálisak lenni. Ha nem, úgy kemoterápia és radioterápia kombinációja ajánlott.
Utánkövetés: lásd általános rész (3.8.)
Megjegyzés: Ewing sarcománál nem ritka a primer műtétet követő 8-10 év utáni recidívák fellépte sem, ill. kemoterápiát követően 5-7 évvel másodlagos, elsősorban vérképzőszervi daganatok (leukémia, lymphoma megjelenése).
4.17. Csontok malignus lymphomája (reticulum sejt sarcoma) Diagnosztika: lásd általános rész (2)
Megjegyzés:
szövettani vizsgálat: immunhisztokémia végzése kötelező.
Kezelés: praeoperatív kemoterápia (lymphoma fajtájának megfelelően), az érintett csontsegment resectioja, vagy amputatioja, majd postoperatív kemoterápia.
Utánkövetés: lásd általános rész (3.8.)
4.18. Myeloma multiplex (Evidencia szint 12A, 34D) Diagnosztika: lásd általános rész (2).
Megjegyzés: speciális laborvizsgálatok, sternum punctio rendszerint diagnózishoz vezet, feltárásos sebészi biopsia nem szükséges, csak atípusos soliter elváltozásoknál aspirációs cytológia javasolt.
Kezelés: elsősorban konzervatív, kemoterápia.
Sebészi kezelés szóba jön soliter, nem generalizált formáknál, valamint multiplex formáknál fenyegető patológiás törésveszély esetén (stabilizálás), ill. patológiás törésnél (osteosynthesis). Minden esetben kemoterápiával kiegészítve.
Utánkövetés: lásd általános rész (3.8.)
4.19. Ér eredetű jóindulatú tumorok (haemangioma, lymphangioma, glomus tumor)
Diagnosztika: lásd általános rész (2)
Megjegyzés:
Szummációs rtg. felvétel karakterisztikus lehet, feltárásos biopsia nem jellegzetes eseteknél szükséges.
Kezelés: csigolyák haemangiomája és lymphangiomája rendszerint melléklelet, csak observatiot igényel, egyébként excochleatio, spongiosa plastica. Műtét előtti szuperszelektív angiográfia embolizáció céljából mérlegelendő.
Megyjegyzés: radioterápia tilos (secunder malignizáció).
Utánkövetés: lásd általános rész (3.8.)
4.20. Haemangioendothelioma, haemangiopericytoma Diagnosztika: lásd általános rész (2)
Megjegyzés:
Szummációs rtg. (rendszerint nem jellegzetes), végleges diagnózist rendszerint feltárásos biopsia ad. Kezelés: sebészi, resectio szélesen az épben.
Megjegyzés: radioterápia tilos (malignizáció, dedifferenciáció veszélye). Utánkövetés: lásd általános rész (3.8.)
4.21. Angiosarcoma Diagnosztika: lásd általános rész (2)
Megjegyzés: csontok diffúz osteoporosisa, ill. hypoglykaemiás rohamok jellemző kísérői e tumorféleségnek.
Kezelés: sebészi, radikális (rendszerint amputatio). Kemoterápia és radioterápia eredményessége kétséges.
Utánkövetés: lásd általános rész (3.8.)
4.22. Intraossealis lipoma Diagnosztika: lásd általános rész (2) Megjegyzés:
A szummációs kétirányú rtg. felvétel felvetheti gyanúját.
Előzetes biopsia rendszerint nem szükséges a benignus radiomorfológia miatt.
Kezelés: excochleatio, spongiosa plastica.
Utánkövetés: lásd általános rész (3.8.)
4.23. Desmoplasticus fibroma Diagnosztika: lásd általános rész (2) Megjegyzés:
A kétirányú szummációs rtg. felvétel (rendszerint nem informatív). Tumor kiterjedésének megítélésére CT szükséges lehet. Végleges diagnózist szövettani vizsgálat hoz.
Kezelés: excochleatio és spongiosa plastica, vagy resectio szélesen az épben. Utánkövetés: lásd általános rész (3.8.).
4.24. Malignus fibrosus histiocytoma (csontban) (MFH) (Evidencia szint 5A, 8A, 12A)
Diagnosztika: lásd általános rész (2)
Megjegyzés:
Szummációs rtg. felvételeken kívül daganat kiterjedésének megítélésére elsősorban MR alkalmas.
MFH diagnózist csak akkor adhatunk, ha a definitív műtéti resecatumban részletes szövettani feldolgozással sem
sikerül tumoros osteoidot kimutatni.
Csontizotóp vizsgálat is szükséges.
Regionális nyirokcsomók érintettek lehetnek, ezért UH vizsgálat javasolt.
Kezelés: osteosarcomáéval megegyező praeoperatív kemoterápia, majd műtét, majd postoperatív kemoterápia. Nyirokcsomó érintettségnél lymphadenectomia, majd regionális irradiatio is szóba jön.
Utánkövetés: lásd általános rész (3.8.)
4.25. Fibrosarcoma, liposarcoma, malignus mesenchymoma, differenciálatlan sejtes sarcoma
Diagnosztika: lásd általános rész (2)
Megjegyzés:
CT és MR mindenképpen indokolt.
Szövettani vizsgálat döntő a tumor malignitási fokának meghatározására. Immunhisztokémiai vizsgálat szükséges a szöveti eredet tisztázására.
Kezelés: sebészi, radikális resectio, nagy malignitású formáknál kemoterápia megkísérelhető (eredménye irodalmi adatok alapján vitatott).
Utánkövetés: lásd általános rész (3.8.)
4.26. Chordoma (Evidencia szint 12A) Diagnosztika: lásd általános rész (2) Megjegyzés:
- Labor és kétirányú szummációs felvétel a típusos localisatio (sacrum, gerinc) felveti a helyes diagnózist.
- Csontdestrukció kimutatására CT vizsgálat.
- A tumor intramedullaris és lágyrészkiterjedését legjobban MR vizsgálattal ítélhetjük meg.
-Amennyiben érképletek befogására gyanú van angiográfia szükséges, szükség lehet praeoperatívembolizációrais.
Kezelés: sebészi.
Megjegyzés: a választandó műtéti radikalitás mértéke mérlegelendő, mivel a daganat alacsony malignitású, ill. kiindulási helye miatt rendszerint fontos idegrostokat szűr be. A daganat radio- és kemoterápiára kevéssé érzékeny.
Utánkövetés: lásd általános részt (3.8.)
4.27. Hosszú csöves csontok adamantinómája Diagnosztika: lásd általános rész (2) Megjegyzés:
Kétirányú szummációs rtg. felvétel rendszerint felveti a helyes diganózist. MR, CT rendszerint nem szükséges.
Szövettani vizsgálat műtét előtt fontos: speciális festések, immunhisztokémia szükséges.
Kezelés: sebészi, daganat resectioja szélesen az épben. A daganat kemoterápia és radiorezisztens.
Tekintettel, hogy a daganat 99%-ban a tibiában fordul elő, ajánlott műtétek: tibia resectioja és a csontdefektus pótlása az ellenoldali fibulával (érnyeles, vagy nem érnyeles), vagy az azonos oldali fibulával (érnyeles, izommal fedett formában).
Utánkövetés: lásd általános rész (3.8.)
Megjegyzés: tapasztalataink szerint adamantinóma nem ritkán recidivál, 10-16 évvel a primer műtét után is, ezért utánkövetési idő minimum 20 év legyen.
4.28. Neurilemmoma, neurofibroma Diagnosztika: lásd általános rész (2)
Megjegyzés: Anamnesis fontossága (neurofibromás csomók, scoliosis jelenléte, családi öröklődés, stb.).
Csontokról kétirányú szummációs rtg. felvétel.
Az elváltozás ritkán destruktív, ilyenkor szükség lehet CT vizsgálatra is.
Korrekt diagnózis csak szövettani biopsiás anyagból várható (speciális festések, immunhisztokémia). Kezelés: sebészi, resectio az épben.
Megjegyzés: radio- és kemoterápia rezisztens. Malignizáció előfordulhat esetenként műtétet követően is. Utánkövetés: lásd általános részt (3.8.)
4.29. Tumorszerű csontelváltozások (Evidencia szint 12A, 17C, 33C)
4.29.1. Solitaer (juvenilis) csontcysta Diagnosztika: lásd általános rész (2)
Megjegyzés: Kétirányú szummációs rtg. felvétel gyakran típusos, pontos diagnózist ad. Labor negatív. Típusos localisatio és életkor esetén CT és MR nem szükséges. Diagnosztikus punctio (serosus folyadékgyülem) megerősíti a diagnózist.
Kezelés: deposteroid injectio adása direkt a cystába.
Ritkán, atipusos esetekben sebészi feltárás, excochleatio, spongiosa plastica.
Megjegyzés: a juvenilis csontcysta rendszerint patológiás töréssel kerül felismerésre, így először törés gyógyítása javasolt konzervatív módszerekkel (gipszrögzítés), majd callusképződés után a cysta injectiós kezelése következik a fentiek szerint.
Utánkövetés: 3 hónaponként rtg. kontroll a cysta átépülésének monitorozására, amennyiben a cysta átépülése elhúzódó, vagy tökéletlen úgy a szteroid kezelést 3-5-ször megismételhetjük.
4.29.2. Aneurysmás csontcysta Diagnosztika: lásd általános rész (2)
Megjegyzés: Laborértékek (emelkedett alkalikus foszfatáz szint). CT vizsgálat: a laesiot körülvevő keskeny csonthéj jellegzetes.
MR vizsgálat: jellemző a cysta kötőszövetesen septalt volta, valamint a folyadék nivókaz egyes üregekben.
A cysta direkt punctioja: kezdetben túlnyomással ürül a cysta bennéke. A sanquinolens folyadékgyülem nyomása
20-50 vízcm-t is elérhet.
Aspirációs cytológia negatívitása nem szól a laesio ellen.
Bizonytalan esetben feltétlenül feltárásos biopsia, szövettani vizsgálat indokolt a gyakori secundaer cysták miatt. Angiográfia: egyrészt diagnosztikai célt szolgál, (normovascularisalt, ritkában hypo-, gyakrabban hypervascularisaltaz elváltozás), másrészt lehetőséget nyújt egyidejűleg a cysta embolisatiójára is.
Kezelés: amennyiben lehetséges resectio az épben, vagy excochleatio és spongiosa plastica. Radioterápia tilos malignisatio miatt. Szóba jön a cystát ellátó erekembolisatioja.
Utánkövetés: lásd általános rész (3.8.1.)
4.29.3. Juxtacorticalis csontcysta (intraossealis ganglion)
Diagnosztika: lásd általános rész (2)
Megjegyzés: Kétirányú szummációs rtg. felvétel típusos. Szükség lehet CT-re az izülettel való összeköttetés bizonyítására.
Csontizotóp enyhe pozitívitása differenciál diagnosztikailag segíthet egyéb tumoroktól történő elkülönítésben.
Kezelés: panaszt nem okozó esetekben observatio. Egyébként feltárás, excochleatio, spongiosa plastica.
Utánkövetés: lásd általános rész (3.8.1.)
4.29.4. Metaphysealis fibrosus defectus (nem ossificalódó csontfibroma)
Diagnosztika: lásd általános rész (2)
Megjegyzés: Kétirányú szummációs rtg. felvétel diagnosztikus értékű.
Amennyiben az elváltozás nagyobb kiterjedésű és fenyegető törésveszély áll fenn, úgy a pontos kiterjedés megítéléséhez CT vizsgálat javallt.
Kezelés: panaszt nem okozó, törésveszéllyel nem járó formáknál elegendő az observatio.
Megjegyzés: csont átmérőjének kétharmadát meghaladó kiterjedésű laesioknál excochleatio, spongiosa plastica javallt a fenyegető törésveszély miatt. Patológiás törés esetén a törést kezelhetjük konzervatívan, gyakran a törés gyógyulásával a defektus is átépül. Ha osteosynthesisre van szükség, úgy azt kombináljuk a cysta kikaparásával, spongiosa plasticával.
Utánkövetés: lásd általános rész (3.8.1.)
4.29.5. Eosinophil granuloma Diagnosztika: lásd általános rész (2)
Megjegyzés: Labor (eosinophilia, alkalikus foszfatáz emelkedett).
Kezelés: soliter formáknál excochleatio, spongiosa plastica, multiplex formáknál egyénileg mérlegelendő, a törésveszéllyel járó gócok sebészi feltárása indokolt. Egyébként szisztémás kezelés (kemoterápia).
Utánkövetés: soliter elváltozásoknál 2-3 év, multiplex formáknál tekintettel a lényegesen rosszabb prognózisra a beteg egész életében.
4.29.6. Fibrosus dysplasia Diagnosztika: lásd általános rész (2)
Megjegyzés: Kétirányú szummációs rtg. felvétel gyakran típusos, diagnosztikus értékű.
Labor: emelkedett alkalikus foszfatáz, de nem minden esetben.
Nagykiterjedésű elváltozásoknál műtétet megelőzően MR vizsgálat szóba jön.
Malignisatio gyanújakor teljes diagnosztikai paletta, CT, MR, csontizotóp vizsgálat szükséges lehet.
Ha a klinikoradiológiai kép egyértelmű előzetes biopsiától, szövettani vizsgálattól eltekinthetünk.
Kezelés:
1. Kis kiterjedésű, növekedési hajlamot nem mutató fibrosus dysplasiáknál (típusos localisato femurnyak, felkar prox. harmad) elég a rendszeres kontroll vizsálat.
2. Nagyobb kiterjedésű és növekedésre hajlamos formáknál feltárás, excochleatio, spongiosa plastica, szükség szerint crista idommal extraossealis megtámasztás, stabilizálás.
Malignisatio veszélye esetén praeoperatív biopsia. A szövettan ismeretében a malignus elváltozás szöveti jellegének megfelelő terápia: radikális resectio az épben és/vagy kemoterápia.
Utánkövetés: növekedési hajlamot nem mutató kis kiterjedésű elváltozásoknál félévente, majd évente egyszer 5-8 évig, agresszív növekedést mutató elváltozásoknál félévente kb. 5 évig műtétet követően. Malignus formáknál lásd általános rész, malignus csontdaganatok.
4.29.7. Myositis ossificans Diagnosztika: lásd általános rész (2)
Megjegyzés: Labor (emelkedett süllyedés, balratolt vérkép).
Kétirányú szummációs rtg. felvétel (akut stádiumban két hetenként célszerű megismételni).
Műtéti beavatkozás, vagy bizonytalan klinikoradiológiai kép esetén CT vizsgálat, csontizotóp vizsgálat.
Nem típusos esetben feltárásos sebészi biopsia, szövettani vizsgálat javallt a felismerését követően.
Kezelés: florid stádiumban (első 8-12 hét) lehetőleg tartózkodjunk a végleges sebészi megoldástól. Kiérett stádiumban a sebészi beavatkozást az elváltozás épben történő kimetszése jelenti.
Indikációk: ha izületi mozgáskorlátozottságot okoz, nem tudja ellátni mindennapi munkáját, fájdalmas kontraktúráknál.
Megjegyzés: a műtétet követő ismételt kiújulási veszély nagy, ennek csökkentése érdekében nem szteroid gyulladáscsökkentők (pl. Indometacinum), kis dózisú frakcionált rtg. besugárzás javallt a közvetlen perioperativ időszakban.
Utánkövetés: lásd általános rész (3.8.1.)
4.29.8. Hyperparathyreoidismus okozta barna tumor Diagnosztika: lásd általános rész (2)
Megjegyzés: Labor (süllyedés, szérum kalcium, foszfor, alkalikus foszfatáz emelkedett, szérum parat hormonszint meghatározás).
Kétirányú szummációs rtg. felvétel az érintett csontról, ill. kéz rövid csöves csontjairól (corticalis elvékonyodása, felrostozódása, spongialisatioja, apróbb cysták jelenléte). CT csak nagyobb törésveszéllyel járó cysták esetén. Biopsia, ha a klinikai, radiológiai kép nem egyértelmű.
Kezelés: elsősorban konzervatív, a hormonális státusz rendezése, vagy egyéb etiológiai faktor kiküszöbölése, kalcium szubsztituició.
Patológiás törésveszélynél csont stabilizálása, ill. törés esetében osteosynthesis szóba jön. Utánkövetés: alapfolyamattól függően 3-5 év, vagy még tovább.
4.29.9. Intraossealis epidermoid cysta Diagnosztika: lásd általános rész (2)
Megjegyzés: A képalkotó eljárások rendszerint nem adnak korrekt diagnózist, csak az eltávolított anyag szövettani vizsgálata.
A laesio benignitása rendszerint egyértelmű, ezért előzetes biopsia nem szükséges.
Kezelés: excochleatio, szükség szerint spongiosa plastica.
Utánkövetés: lásd általános rész (3.8.1.)
4.29.10. Paget-kór
Diagnosztika: lásd általános rész (2)
Megjegyzés: Kétirányú szummációs rtg. felvétel az érintett csontokról gyakran már diagnosztikus értékű. Laborvizsgálat (szérum kalcium, foszfor, alkalikus foszfatáz, süllyedés).
CT csak ritkán szükséges, amennyiben a klinikai, radiológiai kép nem egyértelmű és a folyamatot tumortól kell eldifferenciálni.
Biopsia: a szövettani vizsgálat megerősíti a diagnózist.
Malignisatio gyanúja esetén teljes diagnosztikai paletta: CT, MR, csontizotóp vizsgálat szükséges. Biopsia ilyenkor feltétlenül indokolt az érintett területről.
Kezelés: rendszerint konzervatív, gyógyszeres.
Megjegyzés: hosszú csöves csontok rendszerint 30 foknál nagyobb görbülete esetén patológiás infractio, ill. törés megelőzésére szóba jön ortézis adása, illetve tengelykorrekciós osteotomia.
Utánkövetés: kontroll rtg. vizsgálat fél, ill. egy évente szükséges betegség progressziójának, ill. terápia megítélésének céljából. A betegség krónikus lefolyása miatt az utánkövetés 5-10 évig, esetleg még tovább is szükséges lehet.
IV. Rehabilitáció
V. Gondozás
VI. Irodalomjegyzék Primaer csonttumorok
1. Becker,W.T.; Dohle,J.; Bernd,L.; Braun,A.; Cserhati,M.; Enderle,A.; Hovy,L.; Matejovsky,Z.; Szendroi,M.;Trieb,K.;Tunn,P.U. Local recurrence of giant cell tumor of bone after intralesional treatment with and without adjuvant therapy. J.Bone Joint Surg.Am. 2008; 90:1060-1067 (Evidenciaszint: A)
2. Blackley HR, Wunder JS, Davis AM, White LM, Kandel R, Bell RS. Treatment of giant-cell tumors of long bones with curettage and bone-grafting. J.Bone Joint Surg.Am. 1999;81:811-20. (Evidenciaszint: C)
3. Campanacci M, Baldini N, Boriani S, Sudanese A. Giant-cell tumor of bone. J.Bone Joint Surg.Am. 1987;69:106-14. (Evidenciaszint: C)
4. Campanacci M, Ruggieri P. [Osteosarcoma]. Z.Orthop.Ihre.Grenzgeb. 1992;130:259-64. (Evidenciaszint: B)
5. Coombs R, Friedlander G. Bone tumour management. Butterworth and Co., 1987. (Evidenciaszint: A)
6. Dahlin DC. Caldwell Lecture. Giant cell tumor of bone: highlights of 407 cases. AJR.Am.J.Roentgenol. 1985;144:955-60. (Evidenciaszint: B )
7. Damron TA, Pritchard DJ. Current combined treatment of high-grade osteosarcomas. Oncology Huntingt. 1995;9:327-43. (Evidenciaszint: A)
8. Dominkus M, Kainberger F, Lang S, Kotz R. [Primary malignant bone tumors. Clinical aspects and therapy. Vienna Bone Tumor Registry]. Radiologe 1998;38:82. (Evidenciaszint: A)
9. Eckardt JJ, Grogan TJ. Giant cell tumor of bone. Clin.Orthop. 1986;45-58. (Evidenciaszint: B)
10. Enneking W.F. Limb salvage in musculoskeletal onkology. 1987. Churchill Livingstone. Ref Type: Generic (Evidenciaszint: A)
11. Enneking WF, Spanier SS, Goodman MA. TI - A system for the surgical staging of musculoskeletal sarcoma. 1980. (Evidenciaszint: B)
12. Enneking, W. F. Musculoskeletal Tumor Surgery. 1983. Churchill Livingstone. Ref Type: Generic (Evidenciaszint: A)
13. Fuchs B, Valenzuela RG, Inwards C, Sim FH, Rock MG. Complications in long-term survivors of Ewing sarcoma. Cancer 2003;98:2687-92. (Evidenciaszint: A)
14. Gitelis S, Schajowicz F.Osteoid osteoma and osteoblastoma. Orthop.Clin.North Am. 1989;20:313-25. (Evidenciaszint: A)
15. Glasser DB, Lane JM, Huvos AG, Marcove RC, Rosen G. Survival, prognosis, and therapeutic response in osteogenic sarcoma. The Memorial Hospital experience. Cancer 1992;69:698-708. (Evidenciaszint: B)
16. Greenspan A. Benign bone-forming lesions: osteoma, osteoid osteoma, and osteoblastoma. Clinical, imaging, pathologic, and differential considerations. Skeletal Radiol. 1993;22:485-500. (Evidenciaszint: C )
17. Kransdorf MJ, Sweet DE. Aneurysmal bone cyst: concept, controversy, clinical presentation, and imaging. AJR AmJ.Roentgenol. 1995;164:573-80. (Evidenciaszint: C)
18. Lausten GS, Jensen PK, Schiodt T, Lund B. Local recurrences in giant cell tumour of bone. Long-term follow up of 31 cases. Int.Orthop. 1996;20:172-6. (Evidenciaszint: C)
19. Leung S, Marshall GM, al Mahr M, Tobias V, Lee DB, Hughes DO. Prognostic significance of chemotherapy dosage characteristics in children with osteogenic sarcoma. Med.Pediatr.Oncol. 1997;28:179-82. (Evidenciaszint: C)
20. Lewis VO. Limb salvage in the skeletally immature patient. Curr.Oncol.Rep. 2005;7:285-92. (Evidenciaszint: D)
21. Malawer MM, Bickels J, Meller I, Buch RG, Henshaw RM, Kollender Y. Cryosurgery in the treatment of giant cell tumor. A long-term followup study. Clin.Orthop. 1999;176-88. (Evidenciaszint: B)
22. Marsden FW, Stephens FO, McCarthy SW, Ferrari AM. IIB osteosarcoma. Current management, local control, and survival statistics-the Australian experience. Clin.Orthop. 1991;113-9. (Evidenciaszint: B)
23. Masui F, Ushigome S, Kamitani K, Asanuma K, Fujii K. Chondroblastoma, a study of 11 cases. Eur J Surg Oncol 2002 Dec;28(8):869-74. 2002. (Evidenciaszint: C )
24. McDonald DJ, Sim FH, McLeod RA, Dahlin DC. Giant-cell tumor of bone. J.Bone Joint Surg.Am. 1986;68:235-42. (Evidenciaszint: B )
25. Meyer WH, Malawer MM. Osteosarcoma. Clinical features and evolving surgical and chemotherapeutic strategies. Pediatr.Clin.North Am. 1991;38:317-48. (Evidenciaszint: B )
26. Picci P, Sangiorgi L, Bahamonde L, Aluigi P, Bibiloni J, Zavatta M et al. Risk factors for local recurrences after limb-salvage surgery for high-grade osteosarcoma of the extremities. Ann.Oncol. 1997;8:899-903. (Evidenciaszint: B)
27. Pring ME, Weber KL, Unni KK, Sim FH.TI - Chondrosarcoma of the pelvis. A review of sixty-four cases. (Evidenciaszint: B)
28. Saeter G. ESMO Minimum Clinical Recommendations for diagnosis, treatment and follow-up of osteosarcoma. Ann.Oncol. 2003;14:1165-6. (Evidenciaszint: B )
29. Solheim OP, Saeter G, Elomaa I, Alvegard TA. The treatment of osteosarcoma: present trends. The Scandinavian Sarcoma Group experience. Ann.Oncol. 1992;3 Suppl 2:S7-11. (Evidenciaszint: A )
30. Szendroi M. New aspects in the treatment of bone sarcomas. Acta Med.Hung. 1994;50:237-44. (Evidenciaszint: D)
31. Szendroi M, Papai Z, Koos R, Illes T. Limb-saving surgery, survival, and prognostic factors for osteosarcoma: the Hungarian experience. J.Surg.Oncol. 2000;73:87-94. (Evidenciaszint: B )
32. Szendroi M, Kiss J, Antal I. TI - Surgical treatment and prognostic factors in giant-cell tumor of bone. Acta Chir Orthop Traumatol Cech 2003;70(3):142-50. 2003. (Evidenciaszint: B)
33. van der Eijken JW. Strategy in the treatment of benign bone tumors: an overview. [Review] [19 refs] [Editorial. Review. Review, Tutorial] . (Journal of Pediatric Orthopaedics, Part B. 7(4):249-52, 1998 Oct.Editorial. Review. Review, Tutorial.). 2005. Ref Type: Generic (Evidenciaszint: C)
34. Veth R, van Hoesel R, Pruszczynski M, Hoogenhout J, Schreuder B, Wobbes T. Limb salvage in musculoskeletal oncology. Lancet Oncol. 2003;4:343-50. (Evidenciaszint: B)
35. Wagner LM, Neel MD, Pappo AS, Merchant TE, Poquette CA, Rao BN et al. Fractures in pediatric Ewing sarcoma. J.Pediatr.Hematol.Oncol. 2001;23:568-71. (Evidenciaszint: D )
36. Winkler K, Bieling P, Bielack S, Delling G, Dose C, Jurgens H et al. Local control and survival from the Cooperative Osteosarcoma Study Group studies of the German Society of Pediatric Oncology and the Vienna Bone Tumor Registry. Clin.Orthop. 1991;79-86. (Evidenciaszint: A)
37. Wuisman P, Harle A, Nommensen B, Reiser M, Erlemann R, Roessner A et al. [Giant cell tumor of bone. An analysis of 69 cases]. Z.Orthop. 1989;127:392-5. (Evidenciaszint: B )
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Dokumentáció, bizonylat
- Járóbeteg szakellátásban: ambuláns lap, kezelő lap.
- Képalkotó vizsgálatok képi és szöveges leletei
- Fekvőbeteg szakellátásban: kórlap, műtéti beleegyezés, műtéti leírás, decursus, zárójelentés.
- Felhasználásra került implantátumok bizonylatai
2. Érintett társszakmákkal való konszenzus Onkológia és onkoterápia, Pathológia, Radiológia.
3. Evidencia besorolás
A bizonyítékok szintjei
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Lábtő betegségek ellátásáról
Készítette: az Ortopédiai Szakmai Kollégium
I. Alapvető megfontolások
1. A tevékenység alkalmazási/érvényességi területe
Ortopédia, traumatologia, sebészet (mozgásszerekkel foglalkozó területek)
2. A protokoll bevezetésének alapfeltétele
A betegség diagnosztikájának és terápiájának egységes szemlélete a mozgásszervi betegségekkel foglalkozó szakmákban.
Az egyes betegségek a lábtőben szövet szerint csoportosíthatók. Ezek csoportosításával egységes szemlélet alakítható ki.
3. Definíció:
A lábtő különböző kiváltó tényezők miatti megbetegedése. 3.1.) Kiváltó tényezők: Fejlődési rendellenességek
Növekedési zavarok
Gyulladásos betegségek
Bénulások okozta eltérések
Degenerativ betegségek
Daganatos betegségek
Általános betegségek lábon megjelenő tünetei (érbetegségek, cukorbetegség, ideggyógyászati eltérések) Posttraumás állapotok
3.2.) Kockázati tényezők:
Általános kockázati tényezőt jelent minden olyan betegség, vagy krónikus kórosállapot, mely a 3.1 pontban megjelölt kiváltó tényezők megvalósulását elősegíti.
4. Panaszok/Tünetek/Általános jellemzők
A lábtő panaszok a betegségtől, vagy deformáltságtól függően terhelési zavart/vagy képtelenséget, cipőviselési zavart/vagy képtelenséget, járászavart/vagy képtelenséget okoznak
A tünetek a deformitásnak ill. a panaszoknak megfelelően alaki eltérésben, ízületi mozgáscsökkenésben vagy merevségben, érzészavarban, helyi fájdalomban nyilvánulnak meg.
5. A betegség leírása
A lábtőben előforduló betegségek az érintett anatómiai struktúrák és kóreredet szerint csoportosíthatók (A típusú evidencia: 1,9/a,15,15/a,20) A konzervativés műtéti kezelés is eszerint alakítható ki
5.1.)Az érintett szervrendszer: lábtő (a felső ugróízülettől distalisan, a Lisfranc ízület vonaláig elhelyezkedő testrész)
5.2.) Genetikai háttér: a lábon előforduló elváltozások részben családi hajlam, részben valódi genetikai összefüggés, részben csíraártalom alapján alakulnak ki. (az embrio 4-8 hetes kora között történik meg a végtagok kifejlődése,- a felső és az alsó végtag párhuzamosan fejlődik.)
5.3.)Incidencia/Prevalencia/Morbiditás/Mortalitás Magyarországon
Erre vonatkozóan a láb betegségei szempontjából csak bizonytalan, hozzávetőleges értékek állnak rendelkezésre. 5.4.) Jellemző életkor:
Az egyes elváltozások más-más életkorban jelentkezhetnek:
- fejlődési rendellenességek: a születés után azonnal
- csontosodási zavarok: csak növekedő szervezetben 1-16 éves kor között
- statikai elváltozások: valamennyi életkorban
- primer mozgásszevi daganatok (fiatalkori dominanciáva) bármely életkorban
- gyulladásos,-bénulásos,-posttraumás (ill. szisztémás betegségek helyi tünetei) bármely életkorban
- degenerativ betegségek a 30 életév felett
5.5.) Jellemző nem: az egyes eltérések között van nemi dominancia (pl. gacsos láb-nőknél gyakoribb;).
II. Diagnózis
A lábtő betegségeiben legfontosabb diagnosztikai eljárások:
1. A fizikális vizsgálat.
2. Kiegészítő vizsgálatok: röntgen (standard két ir és kivetített felvételek, szükség esetén funkcionális és tartott felvételek); Csont alaki elváltozásokesetén CT vizsgálat, lágyrész ill. a csontok keringési állapotának vizsgálatára az MR és az izotop vizsgálata válhat szükségessé. Inak, szalagok betegsége, sérülése és tumoros elváltozások esetén ultrahand diagnosztika segíthet. Differenciál diagnosztikában az egész test mozgásszerveinekállapotát kell megítélni.
1. Diagnosztikai algoritmusok
1.A beteg panaszai és az anamnézis alapján felmerül a betegség gyanúja.
2.A társ- illetve alapbetegségeket kikérdezéssel, korábbi zárójelentésekkel vagy laboratóriumi vizsgálatokkal lehet bizonyítani.
3.Fizikális vizsgálat megerősíti vagy elveti a korábbi gyanút. Felvetheti további speciális vizsgálatok szükségességét 4.Speciális vizsgálatok képalkotók: (rtg, CT, MR, izotop. UH, stb) pedobarográfia.
2. Anamnézis
A lábbetegségek kórelőzményében a lokális panaszokra utaló adatok mellett az általános kórelőzmény is döntő. Számos betegség kérői stádiumában a lábon is előforduló tüneteket okoz pl. diabetes, tabes dorsalis, stb.
3. Fizikális vizsgálat
Minden lábbetegség esetén a lábat egyrészt terhelt nyugalmi helyzetben, másrészt járás közben egyaránt megtekintjük. A fizikális vizsgálat döntő része a tapintás és az aktív és passzív mozgástartomány vizsgálata, a keringési és érzési állapot felmérése, mely kiterjed a lábszárra is.
4. Kötelező diagnosztikai vizsgálatok
4.1.) Laboratoriumi vizsgálatok:- az aktuális általános paraméterek rögzítése
- a tüneteknek megfelelően célzott vizsgálatok (pl. húgysavszint köszvény gyanújánál, vércukorszint diabetes gyanújánál)
4.2.) Képalkotó vizsgálatok:
Két irányú rtg felvétel minden esetben kötelező. (részben közvetlen diagnosztikai jelleggel, részben differenciál diagnosztikai célból)
Az egyes deformitásoknak megfelelően harmadik, vagy negyedik vetület is szükséges lehet, ill. a láb terhelt és terheletlen állapotának összehasonlítására további felvételek.
Lágyrészek sérülései esetén (elsősorban szalag és/vagy tok sérülés esetén) tartott felvételek válhatnak szükségessé. A csontok finomabb stukturáinak elváltozása esetén CT ill. 3D CT alapvető lehet a therápia eldöntésében. Lágyrész sérülések, deformitás, defektus esetén és a daganatok diagnosztikájában az MR vizsgálat elengedhetetlen lehet
Gyulladások, tumorok diagnosztikájában az izotop vizsgálat (scintigraphia) válhat szükségessé.
4.3,.) Más disciplinák konziliumait a tervezett konzervativ vagy műtéti kezelés előtt egyes esetekben szükséges ill.
célszerű kikérni.
5. Kiegészítő diagnosztikai vizsgálatok:.Ritkán szükségesek: pl. pedobarográfia.
6. Differenciál diagnosztika: A feltételezett kóreredet elkülönítésére végzett vizsgálatok rendszerint megegyeznek az kötelező diagnosztikai eljárásokkal, melyeket a konzíliumok ajánlásai alapján célszerű kiegészíteni. Diagnosztikai algoritmusok: A különböző elváltozások esetén végzendő vizsgálatok sora az egyes betegségek esetén más és más.
III Terápia
III/1 Nem gyógyszeres kezelés
1. A megfelelő egészségügyi ellátás szintje
Ortopédiai, traumatológiai és reumatológiai szakrendelő, gyermekkorban: gyermekorvosi, iskolaorvosi szakrendelés..
2. Általános intézkedések: Születéskor gyermekorvosi, majd később: iskolaorvosi és munkahelyi orvosi szűrés, tünet esetén szakorvoshoz irányítás.
3. Speciális ápolási teendők: nincsenek.
4. Fizikai aktivitás: a prevenció része
5. Diéta: egyes betegségek kezelésének része (köszvény, diabetes)
6. Betegoktatás: Elsősorban a sokakhoz eljutó médiumokon keresztül-televízio
Sokak által látogatott helyeken szórólap formában-háziorvosi rendelő
Iskolaorvosi rendelő.
Üzemorvosi rendelő.
Iskolai egészségnevelés keretében
III/2 Gyógyszeres kezelés
A lábtő betegségeinek kezelésében viszonylag kevés tere van a gyógyszeres kezelésnek, ez lényegében megegyezik a mozgásszervek betegségek kezelésében használt elvekkel.
1. Megfelelő egészségügyi ellátás szintje: Szakorvosi rendelő, ill. egyszerűbb, visszatérő esetben szakorvosi útmutatás alapján háziorvos,
2. Speciális ápolási teendők: Egyes hosszasan gyógyuló lokális elváltozások rendszeres gondozása (pl diabeteses láb): Szakorvosi rendelő.
3. Ajánlott gyógyszeres kezelés
Nem-szteroid gyulladás gátlók (NSAID) - pl. diclofenac, Harántcsíkolt izomrelaxánsok - pl. tolperison, Vitaminok
3.1. Kontraindikációk: Általános alkalmazás: gyógyszer- vagy hatóanyag túlérzékenység, NSAID nem adható peptikus ulcus, aktív gasztrointesztinális vérzés esetén, myasthenia gravisban nem adható izomrelaxáns
Lokális alkalmazás: a lábon a lokális szteroidok alkalmazása a strukturális károsodás veszélye miatt ínak, ínhüvelyek, izületek esetében kontraindikált. Más esetekben maximum 1-2 alkalommal adható (pl. perioszteális izgalom csökkentésére, Morton neuralgia esetén).
3.2. Lehetséges jelentős interakciók: Az alkalmazott gyógyszerelés egyes gyógyszereinek leírása szerint.
4. Kiegészítő kezelés: Nem gyógyszeres kezelésnek tekinthetők a lábtőbetegségek gyógyászati segédeszközzel való ellátása, azok elkészítésének és viselésének rendszeres ellenőrzése szükség esetén megújítása.(A típusú evidencia:7,12,15,15/a)
III./3 Műtéti kezelés
A lábtőben leggyakrabban a felső ugróízület, az alsóugróízület fájdalmas arthrosisa, pes planus fixatus, -ritkábban fejlődési rendellenességek, bénulások és daganatok miatt végzünk műtéteket. Leggyakoribb műtéti tipus az ízületi arthrodesis.
Az arthrodesisek kiterjesztését a károsodott ízület és a láb statikai helyreállítása szabja meg. Egyéb eljárásoka lábtő lágyrészeit: inakat, ínhüvelyeket, perifériás idegeket érintik.
Műtéti indikáció: Műtét indokolt, a./ ha a sebészeti eljárás eredményeként várható a beteg gyógyulása, vagy állapotánakjelentős javulása. b./ ha annakelmaradása a beteg állapotának lényeges romlását, vagy más deformitások vagy panaszok megjelenését eredményezi.
Műtéti kontraindikáció: Olyan lokális vagy általános betegség egyidejű fennállása, ami a tervezett műtét sikerét veszélyezteti vagy a beteg általános állapotának romlását eredményezheti. Ellenjavallt a műtéti kezelés beteg kooperációs képességének hiánya esetén is.
A lábtőben végzett arthrodesisek kiterjedhetnek több ízületre, de korlátozódhatnak egy ízületre is (talonavicularis, vagy calcaneocuboidealis ízület.)
+Ízületi protézis műtéte:
Az arthrodesisek mellett a felső ugróízületben elsősorban posttraumás arthrosis esetén total ízületpótló prothesisek behelyezésére is sor kerülhet.
Ezen prothesis műtétek végzésének feltétele a mozgató és rögzítő izom-szalag apparátus épsége.
1. Megfelelő ellátás szintje: Elkülönített, steril műtővel rendelkező, befekvésre alkalmas gyógyintézet (szakmai kollégium akkreditáltsága és ÁNTSZ engedélye alapján) A lábtő műtétek ellátási szint szempontjából elkülönített műtővel rendelkező ortopédiai vagy traumatologiai osztályokhoz tartoznak. Egyes bonyolultabb műtéteket (pl. prothesis) II és III ellátási szintű osztályokspeciális felszerelés birtokában megfelelő előképzettség mellett végezhetik.
2. Általános intézkedések
1. A műtét végzésére jogosult
A megfelelő szakorvosi vizsgával és megfelelő jártassággal bíró, Intézeti vagy ÁNTSZ engedéllyel rendelkező orvos. (ortopéd, traumatologus szakorvos, vagy szakorvosi felügyelet mellett szakorvos jelölt. Általános sebészi szakorvosi képesítés szakorvosjelölti szintnek tekintendő.)
2. Műtéti beleegyezés:
A beteggel tudatni kell az elvégzendő műtét lényegét, a műtéttel járó valamennyi a beteget érintő tényt (rögzítés, tehermentesítést), az esetlegesen előforduló leggyakoribb szövődményt és az annakelhárítására tett intézkedéseket (tromboprofilaxis, stb) a műtét utáni várható gyógytartamot és a műtét következtében előálló végleges mozgásállapotot.-arthrodesis-, a várható teljes munkaképesség visszanyerésének időtartamát, szükséges további kezelések stb. A műtét elmaradásával járó veszélyt vagy annak kockázatát) A felvilágosítás alapján a betegnek aláírásával igazolni kell, hogy a műtétbe beleegyezik.
3. Műtői körülmények
1. A körülményekre a sebészet szabályai irányadók. Steril ízületi műtétek végzésére csakolyan műtőhelyiség alkalmas, melyet más betegségek műtéteihez nem használnak(pl bél,urogenitalis, nőgyógyászati stb.) A műtőhelyiségnek kellő tágasságúnakkell lennie, hogy a felhasználásra kerülő műszerek, gépek elférjenek, a műtő személyzetet mozgásukban ne korlátozzák. Kellő világítás szükséges (mennyezeti fény+műtőlámpa)
2. Lábtő műtéteket egy operáló orvos és minimálisan egy, optimálisan két aszisztens végezze. A műtétnél műtősnő és egy műtősegéd kell hogy jelen legyen.
3. Műtéti előkészítés: ez a folyamat magába foglalhat megelőző tornakezelést, segédeszköz viselést és általános (belgyógyászati, bőrgyógyászati) kezelést. Közvetlenül a műtétet megelőzően a bőr letisztítása és a műtőhelyiségbe való érkezésig védelme szükséges.
(A típusú evidencia:4,8,15,15a)
4. Érzéstelenítés
A műtéteket általános, vagy regionális érzéstelenítésben, vértelenségben szükséges végezni. Ritkán, localis anaesthesia is végezhető.
Helyi érzéstelenítés: csak a legkisebb, felületesen elhelyezkedő képleteken végzett műtét esetén ajánlható (bőr, kisebb ujjak);vezetésés érzéstelenítiés: a lábat ellátó érzőidegek blokádja, ami mellett nagyobb beavatkozások is elvégezhetők, esetenként vértelenített műtéti területen. Regionális érzéstelenítés: az operálandó végtag teljes hosszára kiterjedő érzéstelenítés (spinál, vagy epidural anaesthesia) körülményei között a láb valamint a lábszár vérteleníthető, így a legbiztonságosabb sebészi - anatomiai körülmények biztosíthatók. Narcosis: a regionális érzéstelenítéssel egyenértékű érzéstelenséget ad. (A típusú evidencia:4,8,15,15a)
5. Nagyobb kiterjedésű, várhatóan utóvérzéssel járó műtéteknél szívó drain behelyezés és a műtét befejezése előtt a vértelenség felengedése szükséges.
Az operált lábakat fel kell polcolni (párnán vagy Braun szánkón)
6. Nagyobb kiterjedésű műtétek után a kívánatos ágynyugalom időtartamát a traumatizált szövetek milyensége, kiterjedése, az érzéstelenítés milyensége határozza meg.
7. Rögzítés: Egyes műtéteket követően az operált végtagot, vagy ízületet rögzíteni szükséges. Ez történhet a műtét során behelyezett fémanyagokkal -belső rögzítés, vagy a sebzárás után felhelyezett külső rögzítéssel-gipsszel. A gipszrögzítés a műtét után csaksín, vagy felvágott körkörös gipsz lehet, melyet az első napon óránként ellenőrizni kell. A rögzítés mellett a végtag tehermentesítése is szükséges.
8. A műtét után a fizikai aktivitást minél előbb helyreállítják.
3. Speciális ápolási teendők
A sebkezelésre és a végtag rögzítésére vonatkozó kezelési teendők
4. Fizikai aktivitás: a műtéteket követően az aktivitást minél előbb vissza kell állítani. Láb műtétek után rendszerint egy nappal mára betegek felkelthetők és lábukat terhelve, vagy tehermentesítve járhatnak (a műtét fajtájától függően az operáló orvos utasítása alapján).
A korai mobilizációban test távoli járási segédeszközök (mankó, járókeret -bot) használhatók.
5. Diéta: Láb műtétet követően egy nappal már semmiféle diétára nincs szükség.
6. Betegoktatás: A láb műtétjei előtt szükséges mindazon tények ismertetése, melyek a teljes kezelési folyamatban szóbajönnek. (rögzítés, megfigyelés, várható szövődmények tünetei, az azonnali kontroll vizsgálat szükségessége, a sebellenőrzés ideje, varratszedés ideje, további rehabilitáció, gyógyászati segédeszközök szükségessége stb.).
III/4 Egyéb terápia: a beteg korábbi állapotának megfelelően, egyéb krónikus betegség fennállása esetén annak megfelelő gyógyszeres, vagy egyéb kezelés folytatása.
IV. Rehabilitáció
A lábtő műtéteket követően a betegnek gyógytornát is magába foglaló rehabilitációs kezelésre van szüksége, melyet erre a célra szervezett fiziotherápiás osztályok vagy ambulans rendelők végeznek. A lábműtétek utáni rehabilitáció szakképzett gyógytornászok segítségével rendszeres kontroll vizsgálat alapján történik (A típusú evidencia:1,7,24B típusú evidencia:22)
V. Gondozás
1. Rendszeres ellenőrzés
A lábtő területén végzett műtét után az operált beteg posztoperatív gondozása, a seb ellenőrzése, a rögzítés ill. tehermentesítés az operáló osztály hatáskörébe tartozik. (kívánatos, hogy az operáló orvos végezze az ellenőrző vizsgálatokat)
A rögzítés formáját és időtartamát az operáló sebész a használt módszer, a napi klinikai gyakorlat, a szakirodalom ajánlásai, és a saját tapasztalatai alapján állapítja meg.
A lábtő területén lágyrész műtétek után maximálisan 4- 6, csontműtétek után 10-12 hét külső rögzítés válhat szükségessé.
A műtétet végző orvosnak a kezelés folyamán a beteg állapotáról (keresőképességéről) a háziorvost folyamatosan tájékoztatnia kell.
Az operáló orvosnak ill. osztálynak a teljes gyógyulás eléréséig ellenőriznie kell a beteget, vagy szakmai kapcsolatban lévő szakrendelésre kell utalnia.
2. Megelőzés
A kezelés során felléphető nem kívánt kísérőjelenségek (szövődmények, nem megfelelő gyógyulás) megelőzését szolgálják a rendszeres kontroll vizsgálatok és konzíliumok.
3. Lehetséges szövődmények
A gyógykezelési eljárások és a műtétek mindegyikének lehet szövődménye. 3.1. Lehetséges szövődmények:
Műtéti kezelés esetén a leggyakoribb a thromboemboliás és a szeptikus szövődmény. A trombózis elkerülésére thrombosis profilaxis alkalmazandó az Eü Minisztérium Tromboembóliák megelőzése és kezelése című szakmai protokoll 3.5.4. pontja alapján (A szintű evidencia).
A szeptikus szövődmény megelőzésére az aszepszis antiszepszis műtéti szabályinak betartása mellett a szövetkímélő műtéti technika alkalmazása mellett egyes esetekben szóba jöhet antibiotikus profilaxis (de nem rutinszerűen). Oszteotómia esetén álízület, lemeztörés, kilazulás miatt reoperációra lehet szükség.
Szövődmény jelentkezése esetén az operáló intézetnek (lehetőleg az operáló orvosnak!) haladéktalanul a beteg rendelkezésére kell állnia
A szövődmény kezelése annak természetétől függ, de haladéktalanul el kell végezni.
VI. Irodalomjegyzék:
1. Rohmiller MT, Callahan BS. The reverse sural neurocutaneous flap for hindfoot and ankle coverage: experience and review of the literature. Orthopedics. 2005 Dec;28(12):1449-53. Review.
2. Berkowitz MJ, Kim DH. Process and tubercle fractures of the hindfoot. J Am Acad Orthop Surg. 2005 Dec;13(8):492-502. Review.
3. Mengiardi B, Pfirrmann CW, Zanetti M. MR imaging of tendons and ligaments of the midfoot. Semin Musculoskelet Radiol. 2005 Sep;9(3):187-98. Review.
4. Younger AS, Hansen ST Jr. Adult cavovarus foot. J Am Acad Orthop Surg. 2005 Sep;13(5):302-15. Review. 5 Malerba F, De Marchi F. Calcaneal osteotomies. Foot Ankle Clin. 2005 Sep;10(3):523-40, vii. Review.
6. Jeng CL,Vora AM, Myerson MS. The medial approach to triple arthrodesis. Indications and technique for management of rigid valgus deformities in high-risk patients. Foot Ankle Clin. 2005 Sep;10(3):515-21, vi-vii. Review.
7. Karges DE. Current concepts for treatment of the painful flatfoot in the elderly. Mo Med. 2005 May-Jun;102(3):236-9. Review.
8. Joseph TN, Myerson MS. Correction of multiplanar hindfoot deformity with osteotomy, arthrodesis, and internal fixation. Instr Course Lect. 2005;54:269-76. Review.
9. Lee MS. Posterior calcaneal displacement osteotomy for the adult acquired flatfoot. Clin Podiatr Med Surg North Am. 2005 Apr;22(2):277-89, vii. Review.
10. Stengel D, Bauwens K, Ekkernkamp A, Cramer J. Efficacy of total ankle replacement with meniscal-bearing devices: a systematic review and meta-analysis. Arch Orthop Trauma Surg. 2005 Mar;125(2):109-19. Epub 2005 Feb 3. Review.
11. Kennedy JG, Knowles B, Dolan M, Bohne W. Foot and ankle injuries in the adolescent runner. Curr Opin Pediatr. 2005
Feb;17(1):34-42. Review.
12. Mouhsine E, Djahangiri A,Garofalo R. Fracture of the nonfusedostrigonum,a rare cause of hindfoot pain. A case report and review of the literature. ChirOrgani Mov. 2004 Apr-Jun;89(2):171-5. Review. English, Spanish.
13. Pisani G, Pisani PC, Parino E Sinus tarsi syndrome and subtalar joint instability. Clin Podiatr Med Surg North Am. 2005 Jan;22(1):63-77,vii. Review.
14. Weinfeld SB. Surgical approaches to the talus. Foot Ankle Clin. 2004 Dec;9(4):703-8, v. Review.
15. Ledoux WR, Sangeorzan BJ. Clinical biomechanics of the peritalar joint. Foot Ankle Clin. 2004 Dec;9(4):663-83, v. Review.
16. Lawrence SJ. Open calcaneal fractures. Orthopedics. 2004 Jul;27(7):737-41; quiz 742-3. Review.
17. Drizenko A, Demondion X, Luyckx F,Mestdagh H,CassagnaudX. The communicating branches between the sural and superficial peroneal nerves in the foot: a review of 55 cases. Surg Radiol Anat. 2004 Dec;26(6):447-52. Review.
18. MandracchiaVJ, NicklesWA, Mandi DM, Jaeger AJ, Sanders SM. Treatment of nonunited hindfoot fusions. Clin Podiatr Med Surg North Am. 2004 Jul;21(3):417-39, vii. Review.
19. Lamm BM, Paley D. Deformity correction planning for hindfoot, ankle, and lower limb. Clin Podiatr Med Surg North Am. 2004 Jul;21(3):305-26, v. Review.
20. Strash WW, Berardo P. Radiographic assessment of the hindfoot and ankle. Clin Podiatr Med Surg North Am. 2004 Jul;21(3):295-304,v. Review.
21. Mády F. Klinikai pontrendszer alkalmazása a láb betegségeinek megítélésében. Magyar Trauma.: 46. 343-348. 2003
22. Mark S. Myerson Foot and Ankle Disorders W.B.Saunders Company 2000
23. PritschT,Maman E, Steinberg E, Luger E. [Posterior tibial tendon dysfunction]Harefuah. 2004 Feb;143(2):136-41,165. Review. Hebrew.
24. Mullen JE, O'Malley MJ. Sprains-residual instability of subtalar, Lisfranc joints, and turf toe. Clin Sports Med. 2004 Jan;23(1):97-121. Review.
25. Castro MD. Arthrodesis of the navicular. Foot Ankle Clin. 2004 Mar;9(1):73-83. Review.
26. Maes R, AverousC,Copin G. [Lateral peritalar luxation: prognostic evaluation and therapeutic approach. Review of the literature based on a clinical case] Rev Med Brux. 2003 Dec;24(6):458-63. Review. French.
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Gyakori társbetegségek: Lásd tankönyvi adatok. (A típusú evidencia: 9a,15,15a,20,24)
2. Érintett társszakmákkal való konszenzus Rheumatológia, traumatológia, radiológia, aneszteziológia.
3. Dokumentáció, bizonylat
- Járóbeteg szakellátásban: ambuláns lap, kezelő lap.
- Képalkotó vizsgálatok képi és szöveges leletei
- Fekvőbeteg szakellátásban: kórlap, műtéti beleegyezés, műtéti leírás, decursus, zárójelentés.
- Felhasználásra került implantátumok bizonylatai
4. Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
A lúdtalp (pes planus) ellátásáról
Készítette: az Ortopédiai Szakmai Kollégium
I. Alapvető megfontolások
1. A tevékenység alkalmazási/érvényességi területe
Ortopédia, gyermekgyógyászat, iskolaorvoslás (mozgásszervekkel foglalkozó területek)
2. A protokoll bevezetésének alapfeltétele
A betegség diagnosztikájának és terápiájának egységes szemlélete a mozgásszervi betegségekkel foglalkozó szakmákban.
3. Definíció
3.1. A láb boltozatos szerkezetének megbomlása, a hosszanti és/vagy harántboltozat lesüllyedése a sarokcsont gacsos (valgus) helyzetével. Kiváltója alkati tényezők mellett fejlődési,-növekedési,-csontosodási zavar lehet.
3.2. Kockázati tényezők:
Általános kockázati tényezőt jelent minden olyan betegség vagy krónikus kóros állapot, mely a lábszár és a láb izomzatának és szalagrendszerének meggyengüléséhez vezet
4.Panaszok/Tünetek/Általános jellemzők:
A lábboltozatok lesüllyedése különböző mértékű lehet. Kórosnak csak a panaszokat okozó nagyobb mértékű boltozatsüllyedés tekinthető. Gyermekkorban a lábboltozatok laposabb volta normálisnak tekinthető. A láb boltozatainak kialakulása a 9-10. életévre tehető.
A tünetek a deformitásnak ill. a panaszoknak megfelelően alaki eltérésben, ízületi mozgáscsökkenésben vagy merevségben, helyi fájdalomban, esetleg bőrkeményedések(clavus) képződésében nyilvánulnak meg. Jellemző tünet a sarkak valgus helyzete, mely lábujjhegyen állásnál sem tér vissza a középvonalba.
5. A betegség leírása
Az lábboltozat elváltozásai előforduló betegségek az érintett anatómiai struktúrák és kóreredet szerint csoportosíthatók (B típusú evidencia: 1,2,3,7,15) A konzervatív és műtéti kezelés is eszerint alakítható ki 5.1.)Az érintett szervrendszer: a láb csontváza, szalagjai, a külső (lábszár) és a belső izomzata
5.2.) Genetikai háttér: a láb boltozaton előforduló elváltozások részben családi hajlam, részben valódi genetikai összefüggés, részben csíraártalom alapján alakulnak ki. (az embryo 4-8 hetes kora között történik meg a végtagok kifejlődése,- a felső és az alsó végtag párhuzamosan fejlődik.)
5.3.)Incidencia/Prevalencia/Morbiditás/Mortalitás Magyarországon
Erre vonatkozóan a láb betegségei szempontjából csak bizonytalan, hozzávetőleges értékek állnak rendelkezésre. Az általános kép alapján a lábboltozatok eltérései jelentik a mozgásszervek leggyakoribb elváltozásait.
5.4.) Jellemző életkor:
Az egyes pes planus formák más-más életkorban jelentkezhetnek:
- gyermekkori: 5-7 éves kor között
- csontosodási zavarok: csak növekedő szervezetben 1-16 éves kor között (tarsalis coalitiohoz kötött pes planus fixatus)
- statikai elváltozások: valamennyi életkorban, de túlnyomó részben a serdülőkor után,
- gyulladásos,-bénulásos,-poszttraumás (pes planus inflammatus, -fixatus)
- degenerativ betegségek a 30. életév felett
II. Diagnózis
A pes planus diagnosztikájában a fizikális vizsgálatnak, az aktív és passzív mozgásvizsgálatnak van elsődleges tere. Kiegészítő vizsgálat a terhelt és nem terhelt állapotban végzett rtg vizsgálat.
1. Diagnosztikai algoritmusok
1. A beteg panaszai és az anamnézis alapján felmerül a betegség gyanúja.
2. A társ- illetve alapbetegségeket kikérdezéssel, korábbi zárójelentésekkel vagy laboratóriumi vizsgálatokkal lehet bizonyítani.
3. Fizikális vizsgálat megerősíti vagy elveti a korábbi gyanút. Felvetheti további speciális vizsgálatok szükségességét
4. Speciális vizsgálatok képalkotók: (rtg, CT, MR, izotóp. UH, stb) pedobarográfia.
2. Anamnézis
A pes planus kórelőzményében a lokális panaszokra utaló adatok mellett a fejlődési kórelőzmény is döntő.
3. Fizikális vizsgálat
Pes planus esetén a lábat egyrészt terhelt nyugalmi helyzetben, másrészt járás közben egyaránt megtekintjük. A fizikális vizsgálat döntő része a tapintás, és az aktív és passzív mozgástartomány vizsgálata a láb valamennyi ízületében. Külön figyelmet érdemel a tibialis posterior izom funkció vizsgálata. A keringési és érzési állapot felmérése, mely kiterjed a lábszárra is.
4. Kötelező diagnosztikai vizsgálatok
4.1.) Laboratóriumi vizsgálatok: lúdtalp esetén laboratóriumi vizsgálatra nincs szükség 4.2.) Képalkotó vizsgálatok:
Két irányú rtg felvétel minden esetben ajánlott. Nagyobb fokú eltérés, vagy merev lúdtalp esetén a félferde lábtő felvétel ad információt az esetleges tarsalis coalitióról.
Fedett ínszakadáshoz társuló szerzett pes planus esetében UH vizsgálat szükséges.
4.3,.) Egyes esetekben más disciplinák konziliumait szükséges ill.célszerű kikérni.(pl. neurologia)
5. Kiegészítő diagnosztikai vizsgálatok:.Ritkán szükségesek: pl. pedobarográfia. (B típusú evidencia: 1, 4, 5, 6, 15)
6. Differenciál diagnosztika: A feltételezett kóreredet elkülönítésére végzett vizsgálatok rendszerint megegyeznek az kötelező diagnosztikai eljárásokkal, melyeket a konzíliumok ajánlásai alapján célszerű kiegészíteni.
III Terápia
Nem gyógyszeres kezelés
1. A megfelelő egészségügyi ellátás szintje
Felnőtt és gyermekortopédiai szakrendelő, gyermekkorban: gyermekorvosi, iskolaorvosi szakrendelés.
2. Általános intézkedések: kisgyermek korban gyermekorvosi, majd később: iskolaorvosi és munkahelyi orvosi szűrés. Panasz, tünet esetén szakorvoshoz irányítás.
Célzott pes planus szűrővizsgálatra nincs szükség. Ortopéd szakorvos jelenléte nélkül végzett szűrővizsgálat eredményeként lúdtalpbetét rendelése káros, ezért nem kívánatos (tömeges ún. számítógépes szűrés!)
3. Speciális ápolási teendők: nincsenek.
4. Fizikai aktivitás: a prevenció része
5. Diéta: nincs rá szükség.
6. Betegoktatás: Elsősorban a sokakhoz eljutó médiumokon keresztül - televízió
Sokak által látogatott helyeken szórólap formában - háziorvosi rendelő
Iskolaorvosi rendelő.
Iskolai egészségnevelés keretében
III/2 Gyógyszeres kezelés
A pes planus kezelésében viszonylag kevés tere van a gyógyszeres kezelésnek, ez lényegében megegyezik a mozgásszervek betegségek kezelésében használt elvekkel. Fájdalmas panaszok esetén tüneti analgetikus kezelés szükségessé válhat.
1. Megfelelő egészségügyi ellátás szintje: Szakorvosi rendelő, ill. egyszerűbb, visszatérő esetben szakorvosi útmutatás alapján háziorvos,
2. Speciális ápolási teendők: Legtöbbször nincs. (Szakorvosi rendelő)
3.Gyógyászati segédeszközzel (lúdtalpbetéttel) való kezelés: (B típusú evidencia 8, 9, 10, 11) A panaszos, mobilis pes planus esetén a betegeket lúdtalpbetéttel szükséges ellátni. A lúdtalpbetétet csak orvos rendelhet.
3.1. Kisgyermek korban lúdtalpbetétre a legtöbb esetben nincs szükség. A sarok valgus helyzeténél a cipősarok külső oldalára helyezett supináló cipősarok viseltetése kedvező. A talp tornáztatása javasolt.
3.2. Mobilis lábnál, nagyobb sarok valgus esetén sarokfogós betét viseltetése indokolt.
3.3. Serdülő és felnőtt korban kisebb, vagy közepesfokú panaszmentes pes planus esetén betét viselésére általában nincs szükség.
3.4. felnőtt korban fájdalmas pes planusnál kezdeti kezelésre rugalmasabb, később merevebb betét viselése javasolt.
3.5. Fájdalmas, merev, deformált pes planusos láb esetén egyedi lábágy készítése és viselése indokolt.
Betét rendelésére jogosult az egészségbiztosítási pénztárral szerződésben álló ortopéd szakorvos. 4. Ajánlott gyógyszeres kezelés:
Fájdalmas gyulladásos lúdtalp esetén (pes planus inflammatus) szükségessé válhat:
Analgetikum - pl. paracetamol
Nem-szteroid gyulladás gátlók (NSAID) - pl. diclofenac
Harántcsíkolt izomrelaxánsok - pl. tolperison
4.1. Kontraindikációk: Általános alkalmazás: gyógyszer- vagy hatóanyag túlérzékenység, NSAID nem adható peptikus ulcus, aktív gasztrointesztinális vérzés esetén, myasthenia gravisban nem adható izomrelaxáns
4.2. Lehetséges jelentős interakciók: Az alkalmazott gyógyszerelés egyes gyógyszereinek leírása szerint.
III./3 Műtéti kezelés:
Pes planus esetén műtét indokolt:
1. A lábboltozatok teljes hiányát eredményező merev gyermekkori lúdtalp
2. Tarsalis coalitio okozta lúdtalp
3. Szerzett felnőttkori lúdtalp (m.tibialis posterior szakadás)
Megfelelő ellátás szintje: Elkülönített, steril műtővel rendelkező, befekvésre alkalmas gyógyintézet (szakmai kollégium akkreditáltsága és ÁNTSZ engedélye alapján). Lúdtalp miatt végzendő műtét egynapos sebészet keretében nem végezhető.
A pes planus miatt végzett műtétekkel kapcsolatosan mindenben irányadó a "Lábtő betegségekszakmai protokollja".
IV. Rehabilitáció
V. Gondozás
VI. Irodalomjegyzék
1. Duckworth: Pedobarography 108-131. Helal B., Wilson D. The Foot Churchill Livingstone 1988
2. Helal B. Wilson D. The Foot Churchill Livingstone 1988
3. Hunt G. C. Physical therapy of the Foot and Ankle Churchill Livingstone 1988
4. King J.B., Leuack B.: Hindfoot disorders 542-550. In: Helal B., Wilson D.: The Foot Churchill Livingston 1988.
5. Mády F: Klinikai pontrendszer alkalmazása a láb betegségeinek megítélésében. Magyar Trauma.: 46. 343-348. 2003
6. Myerson M.S.: Foot and Ankle Disorders W.B.Saunders Company 2000
7. Regnauld B.: Instrumentation, Technique and Surgical Approach 550-565. The Foot. Springer Verlag 1986.
8. Regnauld B. The Foot Springer-Verlag 1986
9. Tóth K: Ortopéd cipők, betétek 79-81. In: Szendrői M. Ortopédia Semmelweis Kiadó 2005.
10. Tóth K.: Felnőttkori lábdeformitások 392-403. In: Szendrői M. Ortopédia Semmelweis Kiadó 2005
11. Turek S.L. Orthopaedics Principles and Their Application Metatarsalgia 1436-1457. J.B. Lippincott Company Philadelphia
12. Wu K.K. General Consideration of Foot Surgery 1-27. In: Surgery of the Foot Lea and Febiger 1986.
13. Wu K.K. Surgery of the Tarsal Region 175-237. In: Surgery of the Foot Lea and Febiger 1986.
14. Wu K.K. Principles of Nonsurgical Treatment of Foot Problems 3-7. In: Surgery of the Foot Lea and Febiger 1986.
15. Wu K.K. Principles of the Foot Surgery 17-26. In: Surgery of the Foot Lea and Febiger 1986.
16. Wu K.K. Surgery of the Foot Lea and Febiger 1986.
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Dokumentáció, bizonylat
- Járóbeteg szakellátásban: ambuláns lap, kezelő lap.
- Képalkotó vizsgálatok képi és szöveges leletei
- Fekvőbeteg szakellátásban: kórlap, műtéti beleegyezés, műtéti leírás, decursus, zárójelentés.
2. Érintett társszakmákkal való konszenzus Gyermekgyógyászat.
3. Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Hanyagtartásról
Készítette: az Ortopédiai Szakmai Kollégium
Szinonímák Helytelen testtartás Tartási kyphosis Kypholordoticus tartás
I. Alapvető megfontolások
1. A protokollok alkalmazási / érvényességi területe Magyarország, ortopédiai betegellátó-hálózat.
2. A protokollok bevezetésének alapfeltétele Kiépült ortopéd szakorvosi hálózat.
3. Definíció
A hanyagtartás a biomechanikailag helyes testtartástól eltérő olyan tartási zavar, mely nem takar gerincbetegséget, hanem pusztán a testtartásért felelős csontos és szalagos elemek fiziológiástól eltérő állapota, valamint a testtartásért felelős izmok elégtelen működésére vezethetők vissza. A helyes testtartás az egyes testrészek egymáshoz viszonyított dinamikus egyensúlyi állapota, melyet -alkati különbözőségek mellett -a testtartásért felelős izmok állandó, szemmel alig látható, sokirányú tevékenysége tart fenn. Eközben az ízületi tokok és szalagok feszülése a fiziológiásnak megfelelő, a tartásért felelős izmok harmonikus együttműködése miatt az izomzat erőkifejtése minimális, az ízületi felszínek terhelése így minimális. A tartáshiba túlnyomórészt funkcionális, korrigálható, reverzibilis. Biomechanikailag helyes testtartás esetén a test súlyvonala a processus mastoideus -cervicodorsalis junctio-dorsolumbális átmenetben lévő csigolyatest-sacroiliacalis izület előtt, kissé a csípőizület mögött halad, a térdizület elülső felén át, a talus előtt, a talpig. Normál testtartásban a súlyvonalhoz képest a térdek nyújtott helyzetben vannak, a verticalis medence inclinatio (medencedőlés) 60 fok, a has lapos, feszes, a vállak egy szintben vannak, a fej egyenes állásban, a medencesík középvonalában helyezkedikel.
3.1.) Kiváltó tényezők(A típusú evidencia 2,17,20,23,24) Inaktivitás, mozgásszegény életmód.
3.2.) Kockázati tényezők
Gyenge (nem eléggé erős és nem kellően nyújtható) izomzat és szalagok.
4. Panaszok/Tünetek/Általános jellemzők
A tartáshiba nem jelent betegséget, gyakran panaszmentes. Ha mégis panaszt okoznak, azok nyaki, háti és deréktáji fájdalmakban nyilvánulnak meg. A leggyakoribb tartáshiba általános jellemzői között a gyengén fejlett izomzat, előretartó fej, horpadt mellkas, előreforduló vállak, ellazult és előreálló has, fokozott lumbalis lordosis szerepelnek.
5. A betegség leírása
5.1.) Érintett szervrendszer(ek) Az érintett szervrendszerek (A típusú evidencia,1-24): A nyaki, háti, a lumbalis gerinc, vállak, medence, és alsó végtagok.
5.2.) Genetikai háttér Nem ismert.
5.3.) Incidencia / Prevalecia / Morbiditás / Mortalitás Magyarországon
Az evidence based medicine kritériumainak megfelelő adat kevés, így az előfordulási gyakoriság nagyfokú szórást mutathat. Hazánkban 20-30 % a gyakoriság, kissé emelkedő. (C típusú evidencia 1,11,17,22). Ha az objektív jelként értékelhető szimmetrikus, rögzült mellkasi behúzódással jellemezzük a hanyag tartást, és különválasztjuk a háti kyphosis fokozott, de aktívan korrigálható változataitól, akkor az előfordulás gyakorisága 7% (C típusú evidencia 11) 5.4.) Jellemző életkor
Az esetek túlnyomó többsége a gyermekkor második felében, 10 éves kor felett jelentkezik. Fiúkés lányok esetében a gyors növekedés szakaszában emelkedő előfordulási gyakoriságú.
A gyors növekedés utáni fejlődési szakaszban fiúk esetében számuk tovább emelkedik, lányok esetében lecsökken (B típusú evidencia 14)
5.5.) Jellemző nem
Nincs nemi eltérés a gyakoriságban.
II. Diagnózis
1. Diagnosztikai algoritmusok
2. Anamnézis
A gyermeket a szülők általában rossz tartása, púpos hát, esetleg háti, deréktáji fájdalom miatt hozzák orvoshoz. Gyakori, hogy a házi-gyermekorvos más vizsgálat kapcsán észlel eltérést, vagy célzott iskolai szűrés emeli ki, további vizsgálatra.
3. Fizikális vizsgálatok
A fokozott háti kyphosissal járó tartáshibára jellemző, hogy a beteg képes háti domborulatát aktívan korrigálni. A vizsgálatot úgy végezzük, hogy felkérjük az alsónadrágig levetkőzött gyermeket, hogy álljon egyenesen: farizmát szorítsa össze, hasizmát húzza be, vállait húzza hátra de, ne húzza fel, fejét tartsa egyenesen. Ilyenkor a tartás normalizálódik.
Felkérjük, hogy 90 fokban, csípőben hajoljon előre, kinyújtott karokkal és vállakkal, majd a kyphosis csúcspontján lefelé megtámasztva a gerincet, felszólítjuk a gyermeket, hogy felső végtagjainak és fejének emelésével fokozatosan homorítson. Ép viszonyok között a gerinc homorúvá válik. Ez az aktív korrekció. Passzív korrekció esetén a vizsgáló, az előre kinyújtott karokat könyök magasságban alátámasztva, és csak a hátra lefelé ható nyomást kifejtve képes korrekciót elérni.
Másikjellemző klinikai tünet a Mathias-teszt pozitivitása. A beteget oldalról megtekintve felkérjük, hogy medencéjét a középállásban stabilizálva mindkét karját tartsa nyújtott helyzetben előre. Normál esetben 30 másodperc elteltével nem észlelünkváltozást a tartásban. Helytelen tartás esetében ez idő alatt a háti domborulat és vagy ágyéki homorulat fokozódik, a lapockák "szétcsúsznak", elállóvá válnak.
4. Kötelező (minimálisan elvégzendő) diagnosztikai vizsgálatok 4.1.) Laboratóriumi vizsgálatok nem szükségesek
Gyógyszerek, amelyek befolyásolhatják a laboratóriumi eredményeket Betegségek, amelyek befolyásolhatják a laboratóriumi eredményeket 4.2.) Képalkotó vizsgálatok nem szükségesek 4.3.) Egyéb
Mérőeszközök használata (Debrunner kyphometer, 3D ultrahang topográphia, inclinometer) (C típusú evidencia 6)
5. Kiegészítő diagnosztikai vizsgálatok
Tekintettel arra, hogy a klinikai vizsgálat egyértelmű diagnózist biztosít, nem szükséges.
6. Differenciál diagnosztika
Amennyiben panasz, vagy egyéb szintű mozgáskorlátozottságok is fennállnak, a fokozott kyphosis irreguláris vagy szegmentre terjedő, a fizikális vizsgálatkor csak passzívan korrigálható a fokozott domborulat, akkor felmerül a Scheuermann betegség lehetősége. Ebben az esetben röntgenfelvétel biztosítja a diagnózist.
III. Terápia
Nem gyógyszeres kezelés
1. A megfelelő egészségügyi ellátás szintje Ortopédiai szakrendelés.
2. Általános intézkedések
A mozgásszegény életmód megszüntetése mindennapi iskolai testneveléssel, testmozgással.(B típusú evidencia 1-24). Iskolai testnevelésbe beépített tartásjavító gyakorlatok rendszeres végzése, melyet a testtartásért felelős izmok erejét és nyújthatóságát vizsgáló tesztgyakorlatok alkalmazása hasznosan egészít ki. (C típusú evidencia 5,9,16,17,18,21). Az egyre általánosabb informatikai technológiához szükséges megfelelő ülőpozíció (B típusú evidencia 3,10,13,15), az iskolai hátizsák helyes pozícionálása ( C típusú evidencia 4,8) és megfelelő súlyának meghatározása (Testsúly 10%-a D típusú evidencia 4,8) fontos.
3. Speciális ápolási teendők nincs
4. Fizikai aktivitás
Az iskolai testnevelésre vonatkozó általános intézkedéseken kívül otthoni, rendszeres, naponta végzett, gyógytornász által betanított tartásjavító torna is javasolható. Otthoni függeszkedési lehetőség a vállöv és hasizmok fokozatos erősítéséhez. Emellett úszás, elsősorban a váltott karú úszásnemek végzése javasolt. Iskolai tornát végezhet. Rendszeres sporttevékenység javasolt, előnyösek a nyújtózkodó labdajátékok.
5. Diéta
6. Betegoktatás
Igen lényeges a szülővel és gyermekkel megértetni, hogy nem betegségről, hanem átmeneti állapotról van szó, és a jó tartás kialakítása nagyrészt az iskolai testnevelés megfelelő működésén múlik, melyet a gyermek, otthoni gyógytornával, iskolán kívüli úszással és egyéb sporttal tud eredményesen kiegészíteni.
III/2. Gyógyszeres kezelés Nem szükséges
III/3. Műtét Nem szükséges
III/4. Egyéb terápia (pszichoterápia, gyógy-foglalkoztatás stb.)
A rendszeresen végzett tartásjavító torna (a testtartásért felelős izmok erősítését és nyújtását szolgáló speciális gyakorlatokalkalmazása, mely magában foglalja a hasizom, a m. erector spinae és a m. gluteus maximus erősítését is) (B szintű evidencia 2,20), valamint az úszás és az egyéb sportmozgások az esetek jelentős részében képesek az elváltozás korrigálására. Az aktív torna izom-erősítő és izom nyújtó gyakorlatai mellett szükség lehet a kontrakturás izmok passzív oldására is (triceps surae, ischiocrurális izmok, pectoralis izomzat, nyaki flexorok, trapesius, lapockarögzítő izmok.(B típusú evidencia 2).
IV. Rehabilitáció
V. Gondozás
1. Rendszeres ellenőrzés. A helytelen testtartást félévenként szükséges ellenőrizni orvosilag, akár csak sport, fokozott fizikai aktivitás javasolt, akár gyógytornakezelés történik.
2. Megelőzés
A megelőzés lehetőségei a szülők és az iskola kezében vannak. Iskolán kívüli sport és egyéb rendszeres mozgás, mindennapi iskolai testnevelés/testmozgás, a testnevelésbe építve rendszeres speciális tartásjavító torna végzése, az ülve töltött idő csökkentése, megfelelő testhelyzet üléskor, az iskolatáska megfelelő súlyának betartása, az iskolatáska megfelelő viselése, a megfelelő iskolai és otthoni bútorok jelentik a megelőzést.
3. Lehetséges szövődmények
3.1.) szövődmények kezelése
A serdülőgyermek gyakran elutasítja az együttműködést, vagy nem végzi rendszeresen a gerinctorna gyakorlatokat. Ezért fontos az iskolai testnevelés struktúrájának olyan változtatása, mely a már ma is létező szabályozásoknak megfelelően végezné szakmai tevékenységét. (243/2003. (XII. 17.) Kormányrendelet a Nemzeti alaptanterv kiadásáról, bevezetéséről és alkalmazásáról)
4. Kezelés várható időtartama / Prognózis
A kezelés időtartama a növekedés befejeződéséig tart, félévenkénti ellenőrzéssel és orvosi megbeszéléssel együtt. A növekedés befejeződése után is rendszeres gerinctorna, sportolás javasolt, és csak panasz esetén javasolt kontroll vizsgálat.
5. Az ellátás megfelelősségének indikátorai Szakmai munka eredményességének mutatói
- A szülő és gyermek által a vizsgálatok során elmondott psyches egyensúlyi helyzet.
- A szimmetrikus mellkas deformitás csökkenése, eltűnése.
- Klinikailag a progresszió leállása, vagy lassulása, a Mathias-teszt negatív eredménye.
6. Dokumentáció, bizonylat
- Az ambuláns vizsgálati leletek eredménye,
- A klinikailag kimért görbület foka, (B típusú evidencia 2,20)
VI. Irodalomjegyzék
1. Andrássy Ilona: A Budapest XII. kerületi iskolai mozgásszervi szűrővizsgálatok során szerzett tapasztalataim. Magyar Traumatológia, Ortopédia 2003. 46. 2.139-146
2. Bernbeck R ,Dahmen G.:Kinder Orthopadie.3.Edition.1983
3. Briggs A; Straker L; Greig A.: Upper quadrant postural changes of school children in response to interaction with different information technologies. Ergonomics. 2004; 47(7):790-819 (ISSN: 0014-0139)
4. Chansirinukor W; Wilson D; Grimmer K; Dansie B.: Effects of backpacks on students: measurement of cervical and shoulder posture.Aust J Physiother. 2001; 47 (2):110-6 (ISSN: 0004-9514)
5. Domján L., Bálint P.: Serdülők tartásának javítása a hátizom erősítésével. Gyermekgyógyászat 1990,41,221-226
6. McEvoy MP; Grimmer K.: Reliability of upright posture measurements in primary school children. BMC Musculoskelet Disord. 2005; 6(1):35 (ISSN: 1471-2474)
7. Feingold AJ; Jacobs K.:The effect of education on backpackwearing and posture in a middle school population. Work. 2002; 18(3):287-94 (ISSN: 1051-9815)
8. Grimmer K; Dansie B; Milanese S; Pirunsan U; Trott P.: Adolescent standing postural response to backpack loads: a randomised controlled experimental study. BMC Musculoskelet Disord. 2002; 3:10 (ISSN: 1471-2474)
9. Gardi Z; Feszthammer A; DarabosnéTim I;Tóthné Steinhausz V; Somhegyi A; Varga PP.: Primary prevention program of the Hungarian Spine Society-part I. Scientific background of the posture correction exercise scheme] Ideggyógy Sz. 2005; 58(3-4):105-12 (ISSN: 0019-1442)
10. Marcus M; Gerr F; Monteilh C; Ortiz DJ; Gentry E; Cohen S; Edwards A; Ensor C; Kleinbaum D.: A prospective study of computer users: II. Postural risk factors for musculoskeletal symptoms and disorders. Am J Ind Med. 2002;41(4):236-49 (ISSN: 0271-3586)
11. Marschalkó Péter és mtsai.: Mozgásszervi adatgyűjtés tapasztalatai általános iskolai korcsoportokon MOT 46. Kongresszusa Budapest, 2003 (Előadás)
12. Murphy S; Buckle P; Stubbs D.: The use of the portable ergonomic observation method (PEO) to monitor the sitting posture of schoolchildren in the classroom. Appl Ergon. 2002; 33(4):365-70 (ISSN: 0003-6870)
13. Murphy S; Buckle P;Stubbs D.: Classroom posture and self-reported backand neck pain in schoolchildren. Appl Ergon. 2004; 35(2):113-20 (ISSN: 0003-6870)
14. Poussa MS; Heliövaara MM; Seitsamo JT; Könönen MH; Hurmerinta KA; Nissinen MJ.: Development of spinal posture in a cohort of children from the age of 11 to 22 years.Eur Spine J. 2005; 14(8):738-42 (ISSN: 0940-6719)
15. RoweG; Jacobs K.: Efficacy of body mechanics education on posture while computing in middle school children. Work. 2002; 18(3):295-303 (ISSN: 1051-9815)
16. Somhegyi A; Tóth J; Makszin I; Gardi Z; Feszthammer A; DarabosnéTim I;Tóthné Steinhausz V;Tóthné Szabó K; Varga PP.: [Primary prevention program of the Hungarian Spine Society-Part II. A prospective controlled study of exercises for the improvement of posture] Ideggyogy Sz. 2005; 58(5-6):177-82 (ISSN: 0019-1442)
17. Somhegyi A., Varga P.P.: A Gerincgyógyászati Nemzeti Központ Országos Prevenciós Programja. Népegészségügy1999, 23-27
18. Somhegyi A.: Tartáskorrekció. Magyar Gerincgyógyászati Társaság 2003
19. Straker L; Briggs A; Greig A.: The effect of individually adjusted workstations on upper quadrant posture and muscle activity in school children. Work. 2002; 18(3):239-48 (ISSN: 1051-9815)
20. Tachdjian.:PediatricOrthopedics.2.Edition 1972
21. Tóth J.: Gerinciskola .1995 Biogál Gyógyszergyár Rt, Debrecen
22. Viola S és mtasai: Iskolai mozgásszervi szűrővizsgálatok eredményei. Gyermekkori Gerincdeformitásokat Kutatók Magyarországi Egyesület Kongresszusi előadásai 2000,2002,2004 években
23. Vízkelety T. (szerk): Az ortopédia tankönyve. Semmelweis Kiadó, 2002.
24. Vízkelety T.: Gyermekortopédia. Medicina Kiadó, 1994.
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Gyakori társbetegségek
A hanyagtartás többször egyéb tartási rendellenességekkel társul: Pectus carinátum Pectus excavatum Aszimmetriás mellkas Funkcionális scoliosis
2. Érintett társszakmákkal való konszenzus
A körzeti orvosok és iskolaorvosok szintjén, annak elfogadtatása, hogy a helytelen testtartás nem betegség, hanem állapot, és az iskolai közösségből (a normál iskolai testnevelésből) való kiemelés lelkileg ártalmas. Iskolai testnevelésben vegyen részt, annak kell tartalmaznia a speciális tartásjavító tornát, valamint annak kiegészítéseként javasolt a rendszeres sport.
3. Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Elöláb betegségek ellátásáról
Készítette: az Ortopédiai Szakmai Kollégium
I. Alapvető megfontolások
1. A tevékenység alkalmazási/érvényességi területe:
Ortopédia, traumatologia, sebészet (mozgásszevekkel foglalkozó területek)
2. A protokoll bevezetésének alapfeltétele:
A betegség diagnosztikájának és terápiájának egységes szemlélete a mozgásszervi betegségekkel foglalkozó szakmákban.
Az egyes betegségek az előlábon szövet szerint csoportosíthatók. Ezek csoportosításával egységes szemlélet alakítható ki.
3. Definíció:
A előláb különböző kiváltó tényezők miatti megbetegedése.
3.1.) Kiváltó tényezők: Fejlődési rendellenességek
Növekedési zavarok
Gyulladásos betegségek
Bénulások okozta eltérések
Degenerativ betegségek
Daganatos betegségek
Általános betegségek lábon megjelenő tünetei (érbetegségek, cukorbetegség, ideggyógyászati eltérések) Posttraumás állapotok Statikai rendellenességek
3.2.) Kockázati tényezők:
Általános kockázati tényezőt jelent minden olyan betegség, vagy krónikus kórosállapot, mely a 3.1 pontban megjelölt kiváltó tényezők megvalósulását elősegíti.
4. Panaszok/Tünetek/Általános jellemzők:
Az előláb panaszok a betegségtől, vagy deformáltságtól függően terhelési zavart/vagy képtelenséget, cipőviselési zavart/vagy képtelenséget, járászavart/vagy képtelenséget okoznak.
A tünetek a deformitásnak ill. a panaszoknak megfelelően alaki eltérésben, ízületi mozgáscsökkenésben vagy merevségben, érzészavarban, helyi fájdalomban, esetleg fekélyek képződésében nyilvánulnak meg.
5. A betegség leírása:
Az előlábon előforduló betegségek az érintett anatómiai struktúrák és kóreredet szerint csoportosíthatók (A típusú evidencia: 1,9/a,15,15/a,20) A konzervativés műtéti kezelés is eszerint alakítható ki
5.1.)Az érintett szervrendszer: előláb (a Lisfranc ízület vonalától distalisan elhelyezkedő testrész, mely magába foglalja a metatarsusokat és az ujjakat)
5.2.) Genetikai háttér: a lábon előforduló elváltozások részben családi hajlam, részben valódi genetikai összefüggés, részben csíraártalom alapján alakulnak ki. (az embrio 4-8 hetes kora között történik meg a végtagok kifejlődése,- a felső és az alsó végtag párhuzamosan fejlődik.)
5.3.) Incidencia/Prevalencia/Morbiditás/Mortalitás Magyarországon
Erre vonatkozóan a láb betegségei szempontjából csak bizonytalan, hozzávetőleges értékek állnak rendelkezésre. 5.4.) Jellemző életkor:
Az egyes elváltozások más-más életkorban jelentkezhetnek:
- fejlődési rendellenességek: a születés után azonnal
- csontosodási zavarok: csak növekedő szervezetben 1-16 éves kor között
- statikai elváltozások: valamennyi életkorban, de túlnyomó részben a 2 évtized után,
- primer mozgásszevi daganatok (fiatalkori dominanciáva) bármely életkorban
- gyulladásos,-bénulásos,-posttraumás (ill. szisztémás betegségek helyi tünetei) bármely életkorban
- degenerativ betegségek a 30 életév felett
5.5.) Jellemző nem: az egyes eltérések között van nemi dominancia (pl. hallux valgus-nőknél gyakoribb;). II.
Diagnózis
Az előláb betegségeiben legfontosabb diagnosztikai eljárások:
1. A fizikális vizsgálat.
2. Kiegészítő vizsgálatok: röntgen (standard két ir és kivetített felvételek, szükség esetén funkcionális és tartott felvételek); Csont alaki elváltozásokesetén CT vizsgálat, lágyrész ill. a csontok keringési állapotának vizsgálatára az MR és az izotop vizsgálata válhat szükségessé. Inak, szalagok betegsége, sérülése és tumoros elváltozások esetén ultrahang diagnosztika segíthet. Differenciál diagnosztikában az egész test mozgásszerveinekállapotát kell megítélni.
1. Diagnosztikai algoritmusok
1.A beteg panaszai és az anamnézis alapján felmerül a betegség gyanúja.
2.A társ- illetve alapbetegségeket kikérdezéssel, korábbi zárójelentésekkel vagy laboratóriumi vizsgálatokkal lehet bizonyítani.
3.Fizikális vizsgálat megerősíti vagy elveti a korábbi gyanút. Felvetheti további speciális vizsgálatok szükségességét 4.Speciális vizsgálatok képalkotók: (rtg, CT, MR, izotop. UH, pedobarográfia, stb).
2. Anamnézis
A lábbetegségek kórelőzményében a lokális panaszokra utaló adatok mellett az általános kórelőzmény is döntő. Számos betegség késői stádiumában az előlábon is előforduló tüneteket okoz, pl. diabetes, köszvény, stb.
3. Fizikális vizsgálat
Minden lábbetegség esetén a lábat egyrészt terhelt nyugalmi helyzetben, másrészt járás közben egyaránt megtekintjük. A fizikális vizsgálat döntő része a tapintás és az aktív és passzív mozgástartomány vizsgálata a láb valamennyi ízületében. A keringési és érzési állapot felmérése, mely kiterjed a lábszárra is.
4. Kötelező diagnosztikai vizsgálatok:
4.1.) Laboratóriumi vizsgálatok: - az aktuális általános paraméterek rögzítése
- a tüneteknek megfelelően célzott vizsgálatok (pl. húgysavszint köszvény gyanújánál, vércukorszint diabetes gyanújánál)
4.2.) Képalkotó vizsgálatok:
Két irányú rtg felvétel minden esetben kötelező. (részben közvetlen diagnosztikai jelleggel, részben differenciál diagnosztikai célból)
Az egyes deformitásoknak megfelelően harmadik, vagy negyedik vetület is szükséges lehet, ill. a láb terhelt és terheletlen állapotának összehasonlítására további felvételek.
Lágyrészek sérülései esetén (elsősorban szalag és/vagy tok sérülés esetén) tartott felvételek válhatnak szükségessé. A csontok finomabb stukturáinak elváltozása esetén CT ill. 3D CT alapvető a therápia eldöntésében. Lágyrész sérülések, deformitás, defektus esetén és a daganatok diagnosztikájában az MR vizsgálat elengedhetetlen Gyulladások, tumorok diagnosztikájában az izotop vizsgálat (scintigraphia) szükséges.
4.3.) Más disciplinák konzíliumait a tervezett konzervatív vagy műtéti kezelés előtt egyes esetekben szükséges ill.célszerű kikérni.(pl angiologia, bőrgyógyászat)
5. Kiegészítő diagnosztikai vizsgálatok:. Ritkán szükségesek: pl. pedobarográfia.
6. Differenciál diagnosztika: A feltételezett kóreredet elkülönítésére végzett vizsgálatok rendszerint megegyeznek a kötelező diagnosztikai eljárásokkal, melyeket a konzíliumok ajánlásai alapján célszerű kiegészíteni. Diagnosztikai algoritmusok: A különböző elváltozások esetén végzendő vizsgálatok sora az egyes betegségek esetén más és más.
III. Terápia
Nem gyógyszeres kezelés:
1. A megfelelő egészségügyi ellátás szintje:
Ortopédiai, traumatológiai és reumatológiai szakrendelő,gyermekkorban: gyermekorvosi, iskolaorvosi szakrendelés..
2. Általános intézkedések: Születéskor gyermekorvosi, majd később: iskolaorvosi és munkahelyi orvosi szűrés, tünet esetén szakorvoshoz irányítás.
3. Speciális ápolási teendők: nincsenek.
4. Fizikai aktivitás : a prevenció része
5. Diéta: egyes betegségek kezelésének része (köszvény, diabetes)
6. Betegoktatás: Elsősorban a sokakhoz eljutó médiumokon keresztül-televízio
Sokak által látogatott helyeken szórólap formában-háziorvosi rendelő
Iskolaorvosi rendelő.
Üzemorvosi rendelő.
Iskolai egészségnevelés keretében
IN/2 Gyógyszeres kezelés: Az előláb betegségeinek kezelésében viszonylag kevés tere van a gyógyszeres kezelésnek, ez lényegében megegyezik a mozgásszervek betegségek kezelésében használt elvekkel.
1. Megfelelő egészségügyi ellátás szintje: Szakorvosi rendelő, ill. egyszerűbb, visszatérő esetben szakorvosi útmutatás alapján háziorvos.
2. Speciális ápolási teendők: Egyes hosszasan gyógyuló lokális elváltozások rendszeres gondozása ( pl diabeteses láb): Szakorvosi rendelő.
3. Ajánlott gyógyszeres kezelés:
Nem-szteroid gyulladás gátlók (NSAID) - pl. diclofenac, Harántcsíkolt izomrelaxánsok - pl. tolperison, Vitaminok
3.1. Kontraindikációk: Általános alkalmazás: gyógyszer- vagy hatóanyag túlérzékenység, NSAID nem adható peptikus ulcus, aktív gasztrointesztinális vérzés esetén, myasthenia gravisban nem adható izomrelaxáns
Lokális alkalmazás: az előlábon a lokális szteroidok alkalmazása a strukturális károsodás veszélye miatt ínak, ínhüvelyek, izületek esetében kontraindikált, ezért tilos. Más esetekben maximum 1-2 alkalommal adható (pl. Morton neuralgia esetén).
3.2. Lehetséges jelentős interakciók: Az alkalmazott gyógyszerelés egyes gyógyszereinek leírása szerint.
4. Kiegészítő kezelés: Nem gyógyszeres kezelésnek tekinthetőkaz előláb betegségek gyógyászati segédeszközzel való ellátása, azok elkészítésének és viselésének rendszeres ellenőrzése szükség esetén megújítása A típusú evidencia:7,12,15,15/a
III./3 Műtéti kezelés:
Azelőlábon több betegség is műtéti kezelést igényel: leggyakoribb a hallux valgus, a hallux rigidus, a digitus malleus,a metatarsalgia és ezek kombinációi.
1. Megfelelő ellátás szintje: Elkülönített, steril műtővel rendelkező, befekvésre vagy egynapos sebészeti ellátásra alkalmas gyógyintézet (szakmai kollégium akkreditáltsága és ÁNTSZ engedélye alapján) Az előláb műtétek ellátási szint szempontjából elkülönített műtővel rendelkező ortopédiai vagy traumatologiai osztályokhoz és egynapos sebészeti rendelőkhöz tartoznak. Egyes bonyolultabb előláb műtéteket csak II és III ellátási szintű osztályok speciális felszerelés birtokában megfelelő előképzettség mellett végezhetnek.(pl. tumor, nagyobb kiterjedésű osteotomiákkal járó előláb reconstructio, diabeteses láb elváltozások. stb)
2. Általános intézkedések:
1.A műtét végzésére jogosult a megfelelő szakorvosi vizsgával és megfelelő jártassággal bíró, intézeti vagy ÁNTSZ engedéllyel rendelkező orvos. (ortopéd, traumatologus szakorvos, vagy szakorvosi felügyelet mellett szakorvosjelölt. Általános sebészi szakorvosi képesítés szakorvosjelölti szintnek tekintendő.)
2.Műtéti beleegyezés: a beteggel tudatni kell az elvégzendő műtét lényegét, a műtéttel járó valamennyi a beteget érintő tényt (rögzítés, tehermentesítést), az esetlegesen előforduló leggyakoribb szövődményt és az annak elhárítására tett intézkedéseket (tromboprofilaxis, stb) a műtét utáni várható gyógytartamot és a műtét következtében előálló végleges mozgásállapotot.-arthrodesis-, a várható teljes munkaképesség visszanyerésének időtartamát, szükséges további kezelések stb. A műtét elmaradásával járó veszélyt vagy annak kockázatát) A felvilágosítás alapján a betegnek aláírásával igazolni kell, hogy a műtétbe beleegyezik.
3. Műtői körülmények:
1. A körülményekre a sebészet szabályai irányadók. Steril ízületi műtétek végzésére csakolyan műtőhelyiség alkalmas, melyet más betegségek műtéteihez nem használnak(pl bél,urogenitalis, nőgyógyászati stb.) A műtőhelyiségnek kellő tágasságúnakkell lennie, hogy a felhasználásra kerülő műszerek, gépek elférjenek, a műtő személyzetet mozgásukban ne korlátozzák. Kellő világítás szükséges (mennyezeti fény+műtőlámpa)
2. Az előláb műtéteket egy operáló orvos és egy aszisztens végezze. A műtétnél műtősnő és egy műtősegéd kell, hogy jelen legyen.
3. Műtéti előkészítés: ez a folyamat magába foglalhat megelőző tornakezelést, segédeszköz viselést és általános (belgyógyászati, bőrgyógyászati) kezelést. Közvetlenül a műtétet megelőzően a bőr letisztítása és a műtőhelyiségbe való érkezésig védelme szükséges.
(A típusú evidencia:4,8,15,15a)
4. Érzéstelenítés: A műtéteket általános, vagy regionális érzéstelenítésben, vértelenségben szükséges végezni. Ritkán, localis anaesthesia is végezhető.
Helyi érzéstelenítés: csak a legkisebb, felületesen elhelyezkedő képleteken végzett műtét esetén ajánlható (bőr, kisebb ujjak);vezetésés érzéstelenítiés: a lábat ellátó érzőidegek blokádja, ami mellett nagyobb beavatkozások is elvégezhetők, esetenként vértelenített műtéti területen. Regionális érzéstelenítés: az operálandó végtag teljes hosszára kiterjedő érzéstelenítés (spinál, vagy epidural anaesthesia) körülményei között a láb valamint a lábszár vérteleníthető, így a legbiztonságosabb sebészi - anatomiai körülmények biztosíthatók. Narcosis: a regionális érzéstelenítéssel egyenértékű érzéstelenséget ad. Az előláb közepes vagy nagyobb műtéteinél vértelenség ajánlott. (A típusú evidencia: 4,8,15,15a)
5. Nagyobb kiterjedésű, várhatóan utóvérzéssel járó műtéteknél gumiszalag drain behelyezés és a műtét befejezése előtt a vértelenség felengedése szükséges.
A műtétet követően az operált láb felpolcolása ajánlott (párnán vagy Braun szánkón).
6. Nagyobb kiterjedésű műtétek után a kivánatos ágynyugalom időtartamát a traumatizált szövetek milyensége, kiterjedése, az érzéstelenítés milyensége határozza meg.
7. Rögzítés: Egyes műtéteket követően az operált végtagot, vagy ízületet rögzíteni szükséges. Ez történhet a műtét során behelyezett fémanyagokkal -belső rögzítés, vagy a sebzárás után felhelyezett külső rögzítéssel-gipsszel. Előláb műtétek után gipszrögzítés csak ritkán szükséges. Megfelelő kezelőcipő kellő rögzítést és tehermentesítést ad.
8. A műtét után a fizikai aktivitást minél előbb helyreállítják.
4. Speciális ápolási teendők: A sebkezelésre és a végtag tehermentesítésére vonatkozó kezelési teendők
5. Fizikai aktivitás: a műtéteket követően az aktivitást minél előbb vissza kell állítani. Az előláb műtétek után rendszerint egy nappal már a betegek felkelthetők és lábtő terheléssel, vagy teljes tehermentesítéssel járhatnak (a műtét fajtájától függően az operáló orvos utasítása alapján).
A korai mobilizációban test távoli járási segédeszközök (mankó, járókeret -bot) használhatók.
6. Diéta. Láb műtétet követően egy nappal már semmiféle diétára nincs szükség.
7. Betegoktatás: A láb műtétjei előtt szükséges mindazon tények ismertetése, melyek a teljes kezelési folyamatban szóba jönnek. (rögzítés, megfigyelés, várható szövődmények tünetei, az azonnali kontroll vizsgálat szükségessége, a sebellenőrzés ideje, varratszedés ideje, további rehabilitáció, gyógyászati segédeszközök szükségessége stb.).
III/4 Egyéb terápia: a beteg korábbi állapotának megfelelően, egyéb krónikus betegség fennállása esetén annak megfelelő gyógyszeres, vagy egyéb kezelés folytatása.
IV. Rehabilitáció
Az előláb műtéteket követően a betegnek gyógytornát is magába foglaló rehabilitációs kezelésre van szüksége, melyet erre a célra szervezett fiziotherápiás ambulans rendelők végeznek. A lábműtétek utáni rehabilitáció szakképzett gyógytornászok segítségével rendszeres kontroll vizsgálat alapján kívánatos. (A típusú evidencia:1,7,24, B típusú evidencia:22)
V. Gondozás
1. Rendszeres ellenőrzés
Az előláb területén végzett műtét után az operált beteg posztoperativ gondozása, a seb ellenőrzése, a rögzítés ill. tehermentesítés az operáló osztály hatáskörébe tartozik. (kívánatos, hogy az operáló orvos végezze az ellenőrző vizsgálatokat)
A tehermentesítés formáját és időtartamát az operáló sebész a használt módszer, a napi klinikai gyakorlat, a szakirodalom ajánlásai, és a saját tapasztalatai alapján állapítja meg.
Az előláb területén lágyrész műtétek után maximálisan3-4, csontműtétek után 4-5 hét külső rögzítés válhat szükségessé.
A műtétet végző orvosnak a kezelés folyamán a beteg állapotáról (keresőképességéről) a háziorvost folyamatosan tájékoztatnia kell.
Az operáló orvosnak ill. osztálynak a teljes gyógyulás eléréséig ellenőriznie kell a beteget, vagy szakmai kapcsolatban lévő szakrendelésre kell utalnia.
2. Megelőzés:
A kezelés során felléphető nem kívánt kísérőjelenségek (szövődmények, nem megfelelő gyógyulás) megelőzését szolgálják a rendszeres kontroll vizsgálatok és konzíliumok.
3. Lehetséges szövődmények:
A gyógykezelési eljárások és a műtétek mindegyikének lehet szövődménye. 3.1. Lehetséges szövődmények:
Műtéti kezelés esetén a leggyakoribb a thromboemboliás és a szeptikus szövődmény. A trombózis elkerülésére thrombosis profilaxis alkalmazandó az Eü Minisztérium Tromboembóliák megelőzése és kezelése című szakmai protokoll 3.5.4. pontja alapján (A szintű evidencia).
A szeptikus szövődmény megelőzésére az aszepszis antiszepszis műtéti szabályinak betartása mellett a szövetkímélő műtéti technika alkalmazása mellett egyes esetekben szóba jöhet antibiotikus profilaxis ( de nem rutinszerűen). Oszteotómia esetén (álízület, lemeztörés, kilazulás miatt) reoperációra lehet szükség.
Szövődmény jelentkezése esetén az operáló intézetnek (lehetőleg az operáló orvosnak!) haladéktalanul a beteg rendelkezésére kell állnia.
A szövődmény kezelése annak természetétől függ, de haladéktalanul el kell végezni.
4. Az előláb leggyakoribb betegségei:
Az előlábon az alábbi deformitások fordulnak elő, melyek legtöbb esetben műtéttel gyógyíthatók:
1. hallux valgus (gacsos lábujj vagy bütyök),
2. metatarsalgia,
3. digitus malleus (kalapácsujj)
4. hallux rigidus
1. Hallux valgus:
Definició: Azöregujjolyan deformitása mely a normál helyzettől laterál felé eltérő halluxt jelent, az I metatarsustarsuló várusz eltérésével együtt, vagy nélküle.
1. Műtéti indikáció:
a./ hallux valgus esetén műtét indokolt, ha a betegnek cipőviselési nehézsége és/vagy, b./ terhelésre jelentkező fájdalma és / vagy, c./gyakran gyulladást okozó bursitise és / vagy,
d./ az öregujjhibás állásával összefüggő egyéb deformitása (dig II. superductus) van. e./ kizárólag kozmetikai panasz csak eseti műtéti indikációt jelent.
2. Ellenjavallt a műtét:
a./ ha a várható javulás nincs arányban a műtéti kockázattal.
b./ ha vasculáris tünetekkel jelentkező diabetes áll fenn
c./ ha perifériás érkárosodás (makro vagy mikroangiopathia) észlelhető
d./ ha a műtéti területet érintő bőrbetegség (gombásodás, fertőzés, ekcéma) észlelhető.
e./ ha a műtéthez szükséges kooperáció az orvos megítélése szerint a beteg oldaláról nincs meg (megfelelő tisztálkodás hiánya, tehementesítés szabályainak nem betartása, stb).
3. Alternativtherapia:
Egyedi ortopéd cipő készíttetése
Súlyos előláb deformitás mellett egyedi lábággyal kiegészített ortopéd cipő viseltetése. Diabeteses neuropathia esetén total kontakt betétes ortopéd cipő készíttetése
A hallux valgus kezelésére mértékadó szerzők több mint 200 műtéti típust írtak le. Ezek közül a beteg számára az elváltozás súlyossága és a műtétet befolyásoló általános és lokális tényezők figyelembe vételével a leginkább célravezetőt kell kiválasztani. A helyes műtéti típus kiválasztásához alapos lábsebészeti szakmai jártasság szükséges.
2. Metatarsalgia:
(A típusú evidencia:5,10,11,17,19)
Definició: Metatarsalgiának nevezzük a harántboltozat lesüllyedése miatt kialakult, a talp felől (töbnyire) a II,-III-IV-es metatarsus fejre lokalizálódó fájdalmakat.
1. Műtéti indikáció:
a./ metatarsalgia esetén műtét indokolt, ha a betegnek cipőviselési nehézségei és / vagy, b./ terhelésre jelentkező állandó fájdalmai és / vagy, c./fájdalmas talpi clavusa és / vagy,
d./ a merev harántboltozattal összefüggő egyéb deformitása (MP luxatio, deviatio) van.
2. Ellenjavallt a műtét:
a./ ha a harántboltozat mobilis és a beteg betétet még nem viselt.
b./ ha vasculáris tünetekkel jelentkező diabetes áll fenn
c./ ha perifériás érkárosodás (makro- vagy mikroangiopathia) észlelhető
d./ ha a műtéti területet érintő bőrbetegség (gombásodás, fertőzés, ekcéma)észlelhető.
e./ ha a műtéthez szükséges kooperáció az orvos megítélése szerint a beteg oldaláról nincs meg (megfelelő tisztálkodás hiánya, tehementesítés szabályainak nem betartása, stb).
3. Alternativtherapia:
Egyedi ortopéd cipő készíttetése merev betéttel
Súlyos előláb deformitás mellett egyedi lábággyal kiegészített ortopéd cipő viseltetése. Diabeteses neuropathia esetén total kontakt betétes ortopéd cipő készíttetése
4. A metatarsalgia műtéti kezelésére több műtéti típust tartalmaznak a megfelelő tankönyvek. Ezek lényege, hogy a deformitást létrehozó anatómiai elváltozást szünteti meg. A helyes műtéti típus kiválasztásához alapos lábsebészeti szakmai jártasság szükséges
3. Digitus malleus
(A típusú evidencia:2,8,16,19)
Definicio: Digitus malleus (kalapácsujj,) az előláb izomegyensúlyának megbomlása miatt kialakuló deformitás, melyre az MP izületi hyperextenzió, PIP izületi hyperflexió jellemző, a DIP izület hyperflexiós vagy normál helyzetével.. A panaszok lányege, hogy a kontrakturában lévő ujjat a cipő egy ponton nyomja, ami fájdalmas clavus kialakulásához vezet.
1. Műtéti indikáció:
a./digitus malleus esetén műtét indokolt, ha a betegnek cipőviselési vagy, b./ terhelésre jelentkező állandó fájdalmai és / vagy, c./fájdalmas PIP ízületi clavusa és / vagy,
d./ a merev harántboltozattal összefüggő egyéb deformitása (MP luxatio, deviatio) van.
2. Ellenjavallt a műtét:
a./ ha a harántboltozat mobilis és a beteg betétet még nem viselt.
b./ ha vasculáris tünetekkel jelentkező diabetes áll fenn
c./ ha perifériás érkárosodás (makro- vagy mikroangiopathia) ézlelhető
d./ ha a műtéti területet érintő bőrbetegség (gombásodás, fertőzés, ekcéma)észlelhető.
e./ ha a műtéthez szükséges kooperáció az orvos megítélése szerint a beteg oldaláról nincs meg (megfelelő tisztálkodás hiánya, tehementesítés szabályainak nem betartása stb).
3. Alternatív therapia:
Egyedi ortopéd cipő készíttetése merev betéttel
Súlyos előláb deformitás mellett egyedi lábággyal kiegészített ortopéd cipő viseltetése. Diabeteses neuropathia esetén total kontakt betétes ortopéd cipő készíttetés
4. A digitus malleus műtéti kezelésére több műtéti típust tartalmaznaka megfelelő tankönyvek. Ezek lényege, hogy a deformitást létrehozó anatómiai elváltozást szünteti meg. A helyes műtéti típus kiválasztásához alapos lábsebészeti szakmai jártasság szükséges
4. Hallux rigidus
( A típusú evidencia:2,8,16,19)
Hallux rigidusnak nevezzük azt az állapotot, melyben az öregujjalapízületénk mozgáspályája korlátozott, az ujj feszítése csökkent vagy megszűnt, emiatt a lépés utolsó fázisában az öregujjelrugaszkodása nem vagy alig lehetséges, emiatt a betegek járása korlátozott, fájdalmas. Anatómiailag ezt az állapotot az ízületi tok zsugorodása, az ízület artrozisa hozhatja létre. Gyakran társul a hallux rigidushoz az ízület körüli csontkinövés, mely a mozgászavar mellett helyi nyomásos fájdalmat is kivált.
1. Műtéti indikáció:
a./ hallux rigidus esetén műtét indokolt, ha a betegnek járási vagy cipőviselési panasza van,
b./ terhelésre jelentkező állandó fájdalmai és / vagy,
c./fájdalmas MP ízületi clavusa és / vagy,
d./ a merev alapízülettel összefüggő egyéb deformitása van.
2. Ellenjavallt a műtét:
a./ ha az öregujjkellően mobilis és a beteg betétet még nem viselt.
b./ ha vasculáris tünetekkel jelentkező diabetes áll fenn
c./ ha perifériás érkárosodás (makro- vagy mikroangiopathia) ézlelhető
d./ ha a műtéti területet érintő bőrbetegség (gombásodás, fertőzés, ekcéma)észlelhető.
e./ ha a műtéthez szükséges kooperáció az orvos megítélése szerint a beteg oldaláról nincs meg (megfelelő tisztálkodás hiánya, tehementesítés szabályainak nem betartása, stb).
3. Alternativtherapia:
Egyedi ortopéd cipő készíttetése merev betéttel gördülőtappal
Súlyos előláb deformitás mellett egyedi lábággyal kiegészített ortopéd cipő viseltetése. Diabeteses neuropathia esetén total kontakt betétes ortopéd cipő készíttetés
4. A hallux rigidus műtéti kezelésére több műtéti típust tartalmaznak a megfelelő tankönyvek. Ezek lényege, hogy a deformitást létrehozó anatómiai elváltozást szünteti meg. A helyes műtéti típus kiválasztásához alapos lábsebészeti szakmai jártasság szükséges
VI. Irodalomjegyzék
1. Vinel H. [What are the surgical indications in podiatry?] Ann Dermatol Venereol. 2005 Oct;132(10 Pt 1):775-81. Review. French. No abstract available.
2. Tauveron P, Lelievre G. [Deformities and deviations of the feet and their consequences] Ann Dermatol Venereol. 2005 Oct;132(10 Pt 1):762-6. Review. French. No abstract available.
3. Correll J, Berger N. [Diagnosis and treatment of disorders of the foot in children] Orthopade. 2005 Oct;34(10):1061-72; quiz 1073-4. Review. German.
4. Ferrari J. Bunions. Clin Evid. 2005 Jun;(13):1377-87. Review. No abstract available.
5. Robinson AH, Limbers JP. Modern concepts in the treatment of hallux valgus. J Bone Joint Surg Br. 2005 Aug;87(8):1038-45. Review. No abstract available.
6. Trnka HJ, Hofstatter S. [The modified Lapidus arthrodesis] Orthopäde. 2005 Aug;34(8):735-41. Review. German.
7. Fuhrmann RA, Roth A, Venbrocks RA. [Metatarsalgia. Differential diagnosis and therapeutic algorithm] Orthopade. 2005 Aug;34(8):767-8, 769-72,774-5. Review. German.
8. Stinus H, Weber F. [Inserts for foot deformities] Orthopade. 2005 Aug;34(8):776-8,780-1. Review. German.
9. Wulker N, Suckel A. [Metatarsal osteotomies for hallux valgus] Orthopade. 2005 Aug;34(8):726, 728-34. Review. German.
10. Arnold H. [Lesser toe deformities. Definition, pathogenesis, and options for surgical correction] Orthopade. 2005 Aug;34(8):758-66. Review. German.
11. Marks RM. Arthrodesis of the first metatarsophalangeal joint. Instr Course Lect. 2005;54:263-8. Review.
12. Ajis A, Koti M, Maffulli N. Tailor's bunion: a review. J Foot Ankle Surg. 2005 May-Jun;44(3):236-45. Review.
13. Roukis TS. Metatarsus primus elevatus in hallux rigidus: fact or fiction? J Am Podiatr Med Assoc. 2005 May-Jun;95(3):221-8. Review.
14. Roukis TS. Central metatarsal head-neck osteotomies: indications and operative techniques. Clin Podiatr Med Surg North Am. 2005 Apr;22(2):197-222, vi. Review.
15. Rockett MS, Goss LR. Midshaft first-ray osteotomies for hallux valgus. Clin Podiatr Med Surg North Am. 2005 Apr;22(2):169-95,v. Review.
16. Hetman J, Myer KD. The distal metatarsal osteotomy for the treatment of hallux valgus. Clin Podiatr Med Surg North Am. 2005 Apr;22(2):143-67, v. Review.
17. Sammarco VJ, Nichols R. Orthotic management for disorders of the hallux. Foot Ankle Clin. 2005 Mar;10(1):191-209. Review.
18. Barouk LS, Barouk P, Baudet B, Toullec E. The great toe proximal phalanx osteotomy: the final step of the bunionectomy. Foot Ankle Clin. 2005 Mar;10(1):141-55. Review.
19. Edwards WH. Avascular necrosis of the first metatarsal head. Foot Ankle Clin. 2005 Mar;10(1):117-27. Review.
20. Esway JE, Conti SF. Joint replacement in the hallux metatarsophalangeal joint. Foot Ankle Clin. 2005 Mar;10(1):97-115. Review.
21. Mády F. Szempontoka hallux valgus kezelési módjának megválasztásában Magyar Trauma.: 41.462-464.1998.
22. Mády F. A hallux valgus műtétek utáni rehabilitációs kezelésről Rehabilitáció 1999. 9.70-71
23. Mády F. Klinikai pontrendszer alkalmazása a láb betegségeinek megítélésében. Magyar Trauma.: 46. 343-348. 2003
24. Mark S. Myerson Foot and Ankle Disorders W.B.Saunders Company 2000
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Gyakori társbetegségek: Lásd tankönyvi adatok. (A típusú evidencia:9a,15,15a,20,24)
2. Érintett társszakmákkal való konszenzus
Rheumatológia
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
3. Dokumentáció, bizonylat
- Járóbeteg szakellátásban: ambuláns lap, kezelő lap.
- Képalkotó vizsgálatok képi és szöveges leletei
- Fekvőbeteg szakellátásban: kórlap, műtéti beleegyezés, műtéti leírás, decursus, zárójelentés.
- Felhasználásra került implantátumok bizonylatai
4. Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
A könyök betegségeiről
Készítette: az Ortopédiai Szakmai Kollégium
I. Alapvető megfontolások
1. A tevékenység alkalmazási/érvényességi területe
ortopédia, traumatológia, sebészet (mozgásszervi betegségekkel foglalkozók)
2. A protokoll bevezetésének alapfeltétele
A betegségek diagnosztikájának és terápiájának egységes szemlélete a mozgásszervi betegségekkel foglalkozó szakmákban.
Az egyes betegségek a könyökízület környékén testtáj és szövet szerint csoportosíthatók. Ezek csoportosításával egységes szemlélet alakítható ki.
3. Definíció: A könyök egészének vagy egy részének különböző kiváltó tényezők miatti megbetegedése. 3.1.) Kiváltó tényezők: Fejlődési rendellenességek
Növekedési zavarok
Gyulladásos betegségek
Bénulások okozta eltérések
Degeneratív betegségek
Perifériás idegek kompressziója okozta eltérések
Daganatos betegségek
Általános betegségek könyökön megjelenő tünetei (anyagcsere betegségek, bénulásos eltérések) Posttraumás állapotok
3.2.) Kockázati tényezők:
Általános kockázati tényezőt jelent minden olyan betegség, vagy krónikus kóros állapot, mely a 3.1 pontban megjelölt kiváltó tényezők megvalósulását elősegíti.
4. Panaszok/Tünetek/Általános jellemzők:
A könyök panaszai a betegségtől, vagy deformáltságtól függően terhelési zavart/vagy képtelenséget, mozgáskorlátozottságot, a felső végtag használhatóságának csökkenését okozzák.
A tünetek a deformitásnak ill. a panaszoknak megfelelően alaki eltérésben, ízületi mozgáscsökkenésben vagy merevségben, érzészavarban, helyi fájdalomban nyilvánulnak meg.
5. A betegség leírása
A könyökízület környékén előforduló betegségek az érintett anatómiai struktúrák és kóreredet szerint csoportosíthatók (A típusú evidencia) A konzervatív és műtéti kezelés is eszerint alakítható ki
5.1.) Az érintett szervrendszer: könyökízület (a felkar alsó ízületi vég, az orsócsont és a singcsont felső ízületi vég közös ízületi üregbe eső része, valamint ezek közvetlen környéke)
5.2.) Genetikai háttér: a könyökön előforduló elváltozások részben családi hajlam, részben valódi genetikai összefüggés, részben csíraártalom alapján alakulnak ki. (az embrio 4-8 hetes kora között történik meg a végtagok kifejlődése, - a felső és az alsó végtag párhuzamosan fejlődik.)
5.3.) Incidencia/Prevalencia/Morbiditás/Mortalitás Magyarországon
Erre vonatkozóan a könyök betegségei szempontjából csak bizonytalan, hozzávetőleges értékek állnak rendelkezésre. A könyökízületen észlelhető betegségek előfordulási gyakorisága bizonyos foglalkozások esetében különösen gyakori (pl a felső végtagot terhelő fizikai munkák: felszolgáló, asztalos, egyes sportok, pl: tenisz, golf stb.)
5.4.) Jellemző életkor:
Az egyes elváltozások más-más életkorban jelentkezhetnek:
- fejlődési rendellenességek: a születés után azonnal
- csontosodási zavarok: csak növekedő szervezetben 1-16 éves kor között
- túlterheléses elváltozások: valamennyi életkorban
- primer mozgásszevi daganatok (fiatalkori dominanciáva) bármely életkorban
- gyulladásos,bénulásos,posttraumás (ill. szisztémás betegségek helyi tünetei) bármely életkorban
- degenerativ betegségek a 30 életév felett
- anyagcsere betegsségek (pl. köszvény) általában az élet második felében.
5.5.) Jellemző nem: az egyes eltérések között van nemi dominancia (pl. teniszkönyök férfi dominanciával fordul elő) II. Diagnózis
1. Diagnosztikai algoritmusok
1.1. A beteg panaszai és az anamnézis alapján felmerül a betegség gyanúja.
1.2. A társ- illetve alapbetegségeket kikérdezéssel, korábbi zárójelentésekkel vagy laboratóriumi vizsgálatokkal lehet bizonyítani.
1.3. Fizikális vizsgálat megerősíti vagy elveti a korábbi gyanút. Felvetheti további speciális vizsgálatokszükségességét 1.4.. Speciális vizsgálatok képalkotók: (rtg, CT, MR, izotóp. UH, stb)
2. Anamnézis
A könyökbetegségek kórelőzményében a lokális panaszokra utaló adatok mellett az általános kórelőzmény is döntő. Számos betegség kérői stádiumában a könyökön is előforduló tüneteket okoz (pl.a nyaki borda, a köszvény nyaki discus hernia stb.)
3. Fizikális vizsgálat
Minden felső végtagi betegség esetén a végtagot és a végtag övet egyrészt nyugalmi helyzetben, másrészt mozgás közben egyaránt megtekintjük. A fizikális vizsgálat döntő része a tapintás és az aktív és passzív mozgástartomány vizsgálata, a keringési és érzési állapot felmérése. Különös figyelemmel vagyunk a localis nyomásérzékenységre és a
kóros irányú mozgásokra, melyek a tapintásos vizsgálat részei. A könyök körüli izmok erejét a vizsgálati skála (0-5) alapján írjuk le.
4. Kötelező diagnosztikai vizsgálatok:
4.1.) Laboratóriumi vizsgálatok:
- az aktuális általános paraméterek rögzítése
- a tüneteknek megfelelően célzott vizsgálatok (pl.húgysavszint köszvény gyanújánál) 4.2.) Képalkotó vizsgálatok:
Két irányú rtg felvétel minden esetben kötelező. (részben közvetlen diagnosztikai jelleggel, részben differenciál diagnosztikai célból)
Az egyes deformitásoknak megfelelően a típusostól eltérő vetület is szükséges lehet, ill. a könyök szalagrendszerének megítélésére tartott felvételek készíthetők.
Ugyancsak szükségessé válhat differenciál diagnosztikai célból a szomszédos testtájak (felkar, alkar, nyaki gerinc) képalkotó vizsgálata.
A csontok finomabb stukturáinak elváltozása esetén CT ill. 3D CT alapvető a therápia eldöntésében.
Lágyrész sérülések, deformitás, defektus esetén és a daganatok diagnosztikájában az MR vizsgálat elengedhetetlen
Gyulladások, tumorok diagnosztikájában az izotóp vizsgálat (scintigraphia) szükséges.
4.3,.) Más disciplinák konziliumait a tervezett konzervatív vagy műtéti kezelés előtt egyes esetekben célszerű kikérni.
5. Kiegészítő diagnosztikai vizsgálatok:.Ritkán szükségesek.(pl daganatnál aspirációs cytologia)
6. Differenciál diagnosztika: A feltételezett kóreredet elkülönítésére végzett vizsgálatok rendszerint megegyeznek az kötelező diagnosztikai eljárásokkal, melyeket a konzíliumok ajánlásai alapján célszerű kiegészíteni. Diagnosztikai algoritmusok: A különböző elváltozások esetén végzendő vizsgálatok sora az egyes betegségek esetén más és más.
III. Terápia
Nem gyógyszeres kezelés:
1. A megfelelő egészségügyi ellátás szintje
Ortopédiai, traumatológiai és reumatológiai szakrendelő, gyermekkorban: gyermekorvosi, iskolaorvosi szakrendelés.
2. Általános intézkedések: Születéskor gyermekorvosi, majd később: iskolaorvosi és munkahelyi orvosi szűrés, tünet esetén szakorvoshoz irányítás.
3. Speciális ápolási teendők: nincsenek.
4. Fizikai aktivitás a prevenció része (óvatos, irányított tornák, erősítések)
5. Diéta: egyes betegségek kezelésének része (köszvény, diabetes)
6. Betegoktatás: Elsősorban a sokakhoz eljutó médiumokon keresztül-televízió
Sokak által látogatott helyeken szórólap formában-háziorvosi rendelő
Iskolaorvosi rendelő.
Iskolai egészségnevelés keretében (külön a könyök ízület betegségei nem igényelnek beteg oktatást, inkább az általános mozgásszervi betegségek prevenciójának keretében szükséges erről a testtájról is említést tenni.)
III/2 Gyógyszeres kezelés
A könyök betegségeinek kezelésében viszonylag kevés tere van a gyógyszeres kezelésnek, ez lényegében megegyezik a mozgásszervek betegségek kezelésében használt elvekkel.
1. Megfelelő egészségügyi ellátás szintje: Szakorvosi rendelő, ill. egyszerűbb, visszatérő esetben szakorvosi utmutatás alapján háziorvos.
2. Speciális ápolási teendők: Egyes hosszasan gyógyuló lokális elváltozások rendszeres gondozása ( pl epicondylitis): Szakorvosi rendelő.
3. Ajánlott gyógyszeres kezelés:
Nem-szteroid gyulladás gátlók (NSAID) - pl. diclofenac, Harántcsíkolt izomrelaxánsok - pl. tolperison, Vitaminok
3.1. Kontraindikációk: Általános alkalmazás: gyógyszer- vagy hatóanyag túlérzékenység, NSAID nem adható peptikus ulcus, aktív gasztrointesztinális vérzés esetén, myasthenia gravisban nem adható izomrelaxáns
Lokális alkalmazás: a könyökön a lokális szteroidok alkalmazása a strukturális károsodás veszélye miatt ínak, ínhüvelyek, izületek esetében kontraindikált. Más esetekben maximum 1-2 alkalommal adható (pl. entesopahiák: teniszkönyök, golfkönyök).
3.2. Lehetséges jelentős interakciók: Az alkalmazott gyógyszerelés egyes gyógyszereinek leírása szerint.
4. Kiegészítő kezelés: Nem gyógyszeres kezelésnek tekinthetők a könyökbetegek gyógyászati segédeszközzel való ellátása, azok elkészítésének és viselésének rendszeres ellenőrzése szükség esetén megújítása.(A típusú evidencia)
III/3 Műtét:
1. Megfelelő ellátás szintje: Elkülönített, steril műtővel rendelkező, az egynapos sebészet, vagy befekvésre alkalmas gyógyintézet (szakmai kollégium akkreditáltsága és ÁNTSZ engedélye alapján) Gyakoribb, egyszerűbb ellátást igénylő esetekben valamennyi ortopédiai osztály elláthatja a betegeket. Tumor, fejlődési rendellenességek, izűleti protetika a legmagasabb ellátási szintre tartozik.
2. Általános intézkedések: A műtét végzésére jogosult a megfelelő szakorvosi vizsgával és megfelelő jártassággal bíró, intézeti vagy ÁNTSZ engedéllyel rendelkező orvos. (ortopéd-traumatologus-sebész)
A beteggel tudatni kell a műtéti kezelés indikációját, szövődményeinek veszélyét, a műtéttel együttjáró valamennyi, a beteget érintő tényt (várható gyógyulási idő, rögzítés vagy tehermentesítés szükségessége, mikéntje, a várható teljes munkaképesség visszanyerésének időtartama, szükséges további kezelések stb. A műtét elmaradásával járó veszély vagy kockázat) és a betegnek aláírásával igazolni kell, hogy a műtétbe beleegyezik.
3. Speciális ápolási teendők: A sebkezelésre és a végtag rögzítésére vonatkozó kezelési teendők
4. Sebészeti kezelés:
4.1. Műtéti indikáció: Műtét indokolt,
a./ ha a sebészeti eljárás eredményeként várható a beteg gyógyulása, vagy állapotának jelentős javulása.
b./ ha annakelmaradása a beteg állapotának lényeges romlását, vagy más deformitások vagy panaszok megjelenését eredményezi.
Kontraindikáció: A beteg kooperációs képességének hiánya. Általános okok, amik bármilyen választott műtét kontraindikációját jelentik.
4.2. Műtéti előkészítés: a szükséges műtétre a könyököt elő kell készíteni. Ez a folyamat magába foglalhat megelőző tornakezelést, segédeszköz viselést és általános (belgyógyászati, bőrgyógyászati) kezelést.
Közvetlenül a műtétet megelőzően a bőr letisztítása és a műtőhelyiségbe való érkezésig védelme szükséges. (A típusú evidencia)
4.3. Műtéti érzéstelenítés: helyi érzéstelenítés: csak a legkisebb, felületesen elhelyezkedő képleteken végzett műtét esetén ajánlható (bőr, kisebb, a bőr szintje alatti lágyrész tumorok).
Regionális érzéstelenítés: az operálandó végtag teljes hosszára kiterjedő érzéstelenítés (axillárisvagy supraclavicularis plexus blockad) körülményei között a könyök vérteleníthető, így a legbiztonságosabb sebészi - anatomiai körülmények biztosíthatók. (A típusú evidencia)
Narcosis: a regionális érzéstelenítéssel egyenértékű érzéstelenítési módszer.
4.4. A műtét: Arra előkészített, vértelenített végtagon, steril körülmények között, steril műszerekkel végzett tevékenység. A körülményekre a sebészet szabályai irányadók. Steril ízületi műtétek végzésére csak olyan műtőhelyiség alkalmas, melyet más betegségek műtéteihez nem használnak (pl bél, urogenitalis, nőgyógyászati stb.) A műtőhelyiségnek kellő tágasságúnak kell lennie, hogy a felhasználásra kerülő műszerek, gépek elférjenek, a műtő személyzetet mozgásukban ne korlátozzák. Kellő világítás szükséges (mennyezeti fény+műtőlámpa)
A könyökön végzett műtétekhez 1. szakorvos, 2. egy asszisztens (orvos vagy növendék), 3. műtősnő 4. műtősegéd szükséges.
4.5. Műtét utáni teendők: A műtétet követően közvetlenül (a legkisebb műtét után is legalább 2-3 órát) a beteg feküdjön, operált végtagját polcolja fel.
Nagyobb kiterjedésű műtétek után a kívánatos ágynyugalmat a traumatizált szövetek milyensége, kiterjedése, az érzéstelenítés fajtája határozza meg.
Rögzítés: Egyes műtéteket követően az operált végtagot, vagy ízületet rögzíteni szükséges. Ez történhet a műtét során behelyezett fémanyagokkal -belső rögzítés, vagy a sebzárás után felhelyezett külső rögzítéssel-gipsszel. A gipszrögzítés a műtét után csak sín, lehet, melyet az első napon óránként ellenőrizni kell. Az operált felső végtagot fel kell polcolni (párnán), álló betegen háromszög kendővel.
5. Fizikai aktivitás: a műtéteket követően az aktivitást minél előbb vissza kell állítani. A könyök műtétek után 2-3 órával a betegek felkelthetők. Az operált végtagot háromszög kendővel rugalmasan rögzíteni, megtámasztani szükséges.
6. Diéta. Könyök műtétet követően egy nappal már semmiféle diétára nincs szükség.
7. Betegoktatás: A könyök műtétjei előtt szükséges mindazon tények ismertetése, melyeka teljes kezelési folyamatban szóba jönnek. (rögzítés, megfigyelés, várható szövődmények tünetei, az azonnali kontroll vizsgálat szükségessége, a sebellenőrzés ideje, varratszedés ideje, további rehabilitáció, gyógyászati segédeszközök szükségessége stb.).
III/4. Egyéb terápia: nem szükséges.
III/5. Az ellátás megfelelőségének indikátorai: Szakmai munka eredményességeinek mutatói
A könyök betegségeinek eredményességét az egyes kezelési eljárások függvényében lehet értékelni. Az egyes könyökízületi betegségek kezelésének szempontjai
1. Gyakori társbetegségek: Rheumatoid arthritis, Köszvény
2. Érintett társszakmákkal való konszenzus Rheumatológia, traumatológia, radiológia
3. Egyéb megjegyzések: Mivel a könyökön végzett műtétek rendkívül sokfélék lehetnek, a leggyakrabban előforduló betegségeket az alábbiakban a specialitásaikvonatkozásában részletezzük. Minden egyéb vonatkozásban az általános protokoll vonatkozik rájuk.
3/ Az ízület üregén kívüli műtétei:
Leggyakoribb, műtéti kezelést igénylő, ízület üregén kívüli betegségek a könyökön
1. Entesopathiák ( epicondylitis humeri- tenisz,- és golf könyök)
2. Bursitisek (bursitis olecrani)
3. Perifériás idegekcompressiója (alagút sy-k)
4. Posttraumás állapotok (hegek, szalagcontracturák)
5. Izület közeli (extraarticularis) csonttumorok
6. Izület közeli (extraarticuláris) lágyrész tumorok
Műtéti kezelés:
1. Epicondylitis humeri
(A típusú evidencia: 1,3,7,9,11,14,16,19,24, B típusú evidencia: 21,22,23)
Definíció: A radiális és ulnaris epicondylus területének periostitise (entesopathiája)
1. Műtéti indikáció:
a./epicondylitis humeri esetén műtét indokolt, ha a betegnek a kézujjakszorítása közben könyöktáji fájdalmai vannak, a kéz használhatósága emiatt csökkent.
b./a konzervativ kezelési lehetőségek egyik sem hozott tartós gyógyulást
2. Ellenjavallt a műtét:
a./ ha perifériás érkárosodás (makro vagy mikroangiopathia) ézlelhető
b./ ha a műtéti területet érintő bőrbetegség (gombásodás, fertőzés, ekcéma) észlelhető.
3. Alternatív therápia:
a./ Pihentetés, rögzítés, NSAID localisan és per os. b./ Ismételt localis steroid (Diprofos)
2. Bursitis olecrani
(A típusú evidencia:5,10,11,17,19)
Definíció: Az olecranon felett, a bőr alatt elhelyezkedő bursa gyulladásos, vagy posttraumás megnagyobbodása.
1. Műtéti indikáció:
a./. ismételten feltelődő tömlő
b./ spontán, vagy érintésre jelentkező fájdalom
2. Ellenjavallt a műtét:
a./ ha a műtéti területen seb van.
b./ ha a műtéti területet érintő bőrbetegség (gombásodás, fertőzés, ekcéma) észlelhető. c.J ha a beteg olyan általános állapotban van, melyet a műtét rontana
3. Alternativ therapia: a./ punctio, nyomókötés
b./ punctio, localis szteroid adás
3. Perifériás ideg compressio (A típusú evidencia:2,8,16,19)
A könyökízület területén szűk anatómiai csatornákban fut a n. radiális (supinator csatorna), a n.medianus (retinaculum flexorum), n. ulnaris (sulcus n. ulnaris). Ezek a csatornák szerteágazó okok eredményeként beszűkülhetnek. A szűkület közös tünete a kompresszió alá került ideg részleges, vagy teljes funkció kiesése.
1. Műtéti indikáció:
Konzervatív kezelésre nem javuló izomgyengülés, izomatrofia, érzészavar, érzéskiesés.
2. Ellenjavallt a műtét:
Minden esetben, mely általánosságban a könyökízületi műtétek ellenjavallata. Speciális ellenjavallat nincs.
3. Alternatív therápia:
Localis non steroid kenőcsök, NSAID peros. Átmeneti rögzítés.
4. Az idegkompressiok műtétjeinek közös lényege: az ideget az ép felől megközelítve a leszorítás alól felszabadítják. Nagyfokú kompresszió esetén az ideg kábeleinek szétválasztása is szükségessé válhat.
A műtét végzése kézsebészeti, ill. perifériás idegsebészeti jártasságot igényel.
4. Posttraumás állapotok. Hegek
(A típusú evidencia: 6,8,12,15b,18a,19)
A sérüléseket követően a könyökízület környékén gyakoriaik a mozgászavart okozó hegek, és az ízület mozgásait akadályozó szalagkontraktúra.
1. Műtéti indikáció:
Indokolt a műtéti kezelés, ha a hegek kimetszése, megfelelő plasztikai eljárással kiegészítve az ízület mozgáspályájánakjavulását eredményezheti. Hasonlóan szükséges műtét végzése, ha a szalag kontractura műtétileg oldható.
2. Ellenjavallt a műtét:
a./ ha perifériás érkárosodás (makro- vagy mikroangiopathia) észlelhető
b./ ha a műtéti területet érintő bőrbetegség (gombásodás, fertőzés, ekcéma) észlelhető.
3. Alternatív therapia: Tornakezelés, paracordináció betanítása, A bőr hegeinek fokozatos nyújtása.
4. A posttraumás állapotok kezelésében traumatológiai, ortopédiai, plasztikai sebészeti jártasság szükséges.
5. Extraarticularis lágyrésztumorok
A könyökízület környékén lévő lágyrésztumorok műtéti ellátásában a tumor dignitásának ismerete szükséges. A diagnosztikus lehetőségeket kívánatos aspirációs cytopathologiai vizsgálattal kiegészíteni.
1. Műtéti indikáció:
Kisebb kiterjedésű lágyrésztumorok esetén a teljes tumor primer eltávolítása javasolt.
Nagyobb kiterjedésű tumor esetén a teljes eltávolítást biopsia és szövettani vizsgálat kell, hogy megelőzze.
2. Ellenjavallt a műtét: Minden olyan esetben, melyeket már említett a protokoll.
3. Alternetiv terápia: tumorok esetén, benignus tumor esetébe szoros observatio mellett a műtét halasztható, malignitás gyanuja esetén ez nem megengedett.
6. Extraarticuláris csonttumorok
A könyökízület körüli csont tumorok kezelésére a lágyrész tumorokkal azonos szempontok érvényesek A csont tumorok esetén a tűbiopszia nem minden esetben végezhető.
3/b Izületen belüli betegségek
1. Könyökízületi arthrosis
2. Synoviális chondromatosis
3. Osteochondritis dissecans
4. Rheumatoid arthritis
5. Izületi felszínt érintő posttraumás állapotok
Az ízületi üregen belüli betegségek esetén a következő műtétek végezhetők: arthrotomia, synovectomia, arthroplastica
Műtéti indikáció:
1. a műtét segítségével a kóros állapot megállítható, progresszív betegség esetén annak romlása megelőzhető
2. a műtét segítségével a már kialakult deformitás megszüntethető vagy javítható 3..tönkrement ízületi felszínek funkciójának pótlása arthroplastica segítségével (auto v. alloplasztika)
Műtéti ellenjavallat:
1. Minden olyan localis és általános körülmény, amit a protokoll említ
2. Olyan körülmény, mely a kívánt eredményt veszélyezteti
IV. Rehabilitáció
A könyök műtétek utáni rehabilitáció gyógytornászok segítségével rendszeres kontroll vizsgálat alapján történik (B típusú evidencia)
V. Gondozás
1. Rendszeres ellenőrzés
Minden könyökműtét után lehetőleg a 10-14. nap között a varratokat el kell távolítani.
Az egyes csontműtétek után a végtagot, a végtagrészt megfelelő ideig tehermentesíteni és/vagy rögzíteni szükséges. Az könyökízületen végzett műtétek után a csontgyógyulás várható gyógytartama hat - nyolc hét. Külső rögzítéssel (gipsz) és /vagy a végtag rugalmas rögzítésével tölti el a beteg.
A könyökön végzett ín-izom műtétek gyógyulási ideje 3-5 hét. Ennyi ideig szükséges rögzíteni azokat, ezután megkezdhető a teljes rehabilitáció.
A műtétet igénylő elváltozástól, a műtét során észlelt leletektől függően a műtőorvos egyéni megítélése irányadó az egyes esetek rögzítésének időtartamáról függően.
Az operáló orvosnak ill. osztálynak a teljes gyógyulás eléréséig ellenőriznie kell a beteget, vagy szakmai kapcsolatban lévő szakrendelésre kell utalnia.
2. Megelőzés
A kezelés során felléphető nem kívánt kísérőjelenségek (szövődmények, nem megfelelő gyógyulás) megelőzését szolgálják a rendszeres kontroll vizsgálatok és konzíliumok.
3. Lehetséges szövődmények
A gyógykezelési eljárások és a műtétek mindegyikének lehet szövődménye. 3.1. Lehetséges szövődmények:
Műtéti kezelés esetén a leggyakoribb a thromboemboliás és a szeptikus szövődmény. A trombózis elkerülésére trombosis profilaxis alkalmazandó az Eü Minisztérium Tromboembóliák megelőzése és kezelése című szakmai protokoll 3.5.4. pontja alapján (A szintű evidencia). A szeptikus szövődmény megelőzésére az aszepszis-antiszepszis műtéti szabályinak betartása és a szövetkímélő műtéti technika alkalmazása mellett egyes esetekben szóba jöhet antibiotikus profilaxis ( de nem rutinszerűen).
Oszteotómia esetén álízület, lemeztörés, kilazulás miatt reoperációra lehet szükség
Szövődmény veszély esetén a kezelő intézetnek haladéktalanul a beteg rendelkezésére kell állnia. A szövődmény kezelése annak természetétől függ, de haladéktalanul el kell végezni.
VI. Irodalomjegyzék
1. Cassas KJ,Cassettari-Wayhs A. Childhood and adolescent sports-related overuse injuries. Am Fam Physician. 2006 Mar 15;73(6):1014-22. Review.
2. Carson S, Woolridge DP, Colletti J, Kilgore K. Pediatric upper extremity injuries. Pediatr Clin North Am. 2006 Feb;53(1):41-67, v. Review.
3. Bilic R, Kolundzic R. [Emergencies in orthopaedic surgery of hand, forearm and elbow] Lijec Vjesn. 2005 Jul-Aug;127(7-8):181-5. Review. Croatian.
4. Colombini D, Menoni O, Occhipinti E, Battevi N, Ricci MG, Cairoli S, Sferra C, Cimaglia G, Missere M, Draicchio F, Papale A, Di Loreto G, Ubiali E, Bertolini C, Piazzini DB. [Criteria for classification of upper limb work-related musculo-skeletal disorders due to biomechanical overload in occupational health. Consensus document by an Italian Working Group] Med Lav. 2005;96 Suppl 2:5-26. Review. Italian.
5. Gramstad GD,GalatzLM. Management of elbow osteoarthritis. J Bone Joint Surg Am. 2006 Feb;88(2):421-30. Review.
6. Winter M, Balaguer T, Tabutin J. Bilateral patella cubiti. A case report. J Bone Joint Surg Am. 2006 Feb;88(2):415-7. Review. No abstract available.
7. OussedikS, Haddad F.Aspiration of the elbow joint. Br J HospMed (Lond). 2006 Jan;67(1):M12-3. Review. No abstract available.
8. Handoll HH, Koscielniak-Nielsen ZJ. Single, double or multiple injection techniques for axillary brachial plexus blockfor hand, wrist or forearm surgery. Cochrane Database Syst Rev. 2006 Jan 25;(1):CD003842. Review.
9. Hoppenrath T, Ciccone CD. Is there evidence that phonophoresis is more effective than ultrasound in treating pain associated with lateral epicondylitis? Phys Ther. 2006 Jan;86(1):136-40. Review. No abstract available.
10. Aslan G,Tuncali D, Cigsar B, Barutcu AY, Terzioglu A. The propeller flap for postburn elbow contractures. Burns. 2006 Feb;32(1):112-5. Epub 2005 Dec 27. Review.
11. Saw A. Extracorporeal shock wave therapy for musculoskeletal pathology-a literature review. Med J Malaysia. 2005 Jul;60 Suppl C:8-10. Review.
12. Polizzi A, Pavone P, Ciancio E, La Rosa C, Sorge G, Ruggieri M. Hypertrichosis cubiti (hairy elbow syndrome): a clue to a malformation syndrome. J Pediatr Endocrinol Metab. 2005 Oct;18(10):1019-25. Review.
13. Hobbs DL. Fat pad signs in elbow trauma. Radiol Technol. 2005 Nov-Dec;77(2):93-6. Review. No abstract available.
14. Tan V, Daluiski A, Capo J, Hotchkiss R. Hinged elbow external fixators: indications and uses. J Am Acad Orthop Surg. 2005 Dec;13(8):503-14. Review.
15. Safran M, Ahmad CS, Elattrache NS. Ulnar collateral ligament of the elbow. Arthroscopy. 2005 Nov;21(11):1381-95. Review.
16. Jones GL. Upper extremity stress fractures. Clin Sports Med. 2006 Jan;25(1):159-74, xi. Review.
17. Jacobson JA, Miller BS, Morag Y. Golf and racquet sports injuries. Semin Musculoskelet Radiol. 2005 Dec;9(4):346-59. Review.
18. Ouellette H, Kassarjian A, Tretreault P, Palmer W. Imaging of the overhead throwing athlete. Semin Musculoskelet Radiol. 2005 Dec;9(4):316-33. Review.
19. Stasinopoulos D, Stasinopoulou K, Johnson MI. An exercise programme for the management of lateral elbow tendinopathy. Br J Sports Med. 2005 Dec;39(12):944-7. Review.
20. KovacicJ, Bergfeld J. Return to play issues in upper extremity injuries. Clin J Sport Med. 2005 Nov;15(6):448-52. Review.
21. Jenabzadeh AR, Haddad FS. Injuries around the elbow. Br J Hosp Med (Lond). 2005 Oct;66(10):M54-5. Review. No abstract available.
22. Allen SD, Harvey C, O'Regan D. Interpretation of elbow and forearm radiographs. Br J Hosp Med (Lond). 2005 Oct;66(10):M50-3. Review. No abstract available.
23. Deleuze A, Gentili ME. [Regional block for the elbow, wrist and hand] Ann Fr Anesth Reanim. 2006 Feb;25(2):242-8. Epub 2005 Oct 25. Review.
24. McCarty LP, Ring D, Jupiter JB. Management of distal humerus fractures. Am J Orthop. 2005 Sep;34(9):430-8. Review.
25. Caine DJ, Nassar L. Gymnastics injuries. Med Sport Sci. 2005;48:18-58. Review.
26. Utukuri MM, Goddard NJ. Haemophilic arthropathy of the elbow. Haemophilia. 2005 Nov;11(6):565-70. Review.
27. Buchbinder R, Green SE, Youd JM, Assendelft WJ, Barnsley L, Smidt N. Shock wave therapy for lateral elbow pain. Cochrane Database Syst Rev. 2005 Oct 19;(4):CD003524. Review.
28. Shin AY, Spinner RJ, Steinmann SP, Bishop AT. Adult traumatic brachial plexus injuries. J Am Acad Orthop Surg. 2005 Oct;13(6):382-96. Review.
29. Vízkelety Tibor Az Ortopédia Tankönyve Semmelweis kiadó Budapest 1995
30. Szendrői Miklós (szerk.) Ortopédia szakkönyv Semmelweis kiadó Budapest 2006
31. Udvarhelyi Iván Fejezetek a felnőttkoi ortopédia gyakorlatából
32. Duprac J. Surgical Techniques in Orthopaedics and Traumatology vol.4. Elsevier 2002
33. Domán I.,KoósZ.,Bálint L. Teniszkönyök miatt végzett műtétek hosszú távú eredményei Magyar Trauma 44.9-14.2001
34. Vidó S. Új tipusú rádiusfejprotézis Magyar Trauma 47.83-89 .2004
Kapcsolódó internetes oldalak:
http://www.sign.ac.uk/guidelines/index.html
A szakmai protokoll érvényessége: 2010. szeptember 30.
1. Dokumentáció, bizonylat
- Járóbeteg szakellátásban: ambuláns lap, kezelő lap. •Képalkotó vizsgálatok képi és szöveges leletei
- Fekvőbeteg szakellátásban: kórlap, műtéti beleegyezés, műtéti leírás, decursus, zárójelentés.
- Felhasználásra került implantátumok bizonylatai
2. Érintett társszakmákkal való konszenzus Onkológia és onkoterápia, Pathológia, Radiológia.
3. Evidencia besorolás
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Author: Toimitus
Article ID: inf04223 © 2005 Duodecim Medical Publications Ltd
Az Egészségügyi Minisztérium
szakmai protokollja
Gerincdeformitásokról Scoliosiséskyphosis
Készítette: az Ortopédiai Szakmai Kollégium
I. Alapvető megfontolások
1. A protokollok alkalmazási / érvényességi területe ortopédia család-, és iskolaorvos kompetencia szintnek megfelelően
2. A protokollok bevezetésének alapfeltétele Ortopéd Szakmai kollégium legitimációja
Ortopéd szakmai minimum feltételeknek megfelelő ellátási szint
3. Definíció
Scoliosis: gerinc térbeli deformítása.
Funkcionális scoliosis: Az oldalirányú görbület fekve megszűnik, a vizsgáló által vagy a betegálatal akaratlagosan korrigálható. Bordapúp előrehajolva nincs.
Strukturális scoliosis: A gerinc mindhárom fő síkban deformálódik. Oldalirányú elhajlás, lordotizáció és a horizontális síkban torqualódás jellemzi, melyhez a csigolyatesteken belüli torzió is társul. Következményesen thoracalisan bordapúp, lumbalisan izompúp jön létre.
3.1.) Kiváltó tényezők
nagyobb részük ismeretlen etiológiájú
- ismeretlen etiológiájú funkcionális scoliosis
- idiopathiás strukturális scoliosis (a strukturális scoliosisok 80-85 %-a) ismert etiológia
- ismert etiológiájú funkcionális scoliosis: alsó végtag funkcionális vagy abszolút rövidülése okozza. Hosszan fennálva struktúrálissá válhat.
- ismert etiológiájú strukturális scoliosisok
Congenitális scoliosisok: Veleszületett csigolyafejlődési rendellenessség talaján alakul ki (ékcsigolya, félcsigolya, részleges vagy teljes blokkcsigolya)
Neuromuscularis scoliosisok: Idegrendszeri betegségekhez társultan (polyomyelitis anterior acuta, ICP, Friedrich ataxia, Charcot-Marie- Tooth betegség, syringomyelia, myelomeningocele). Izombetegségekhez társultan (arthrogryposis, dystrophia musculorum progressiva, spinalis muscularis atrophia, gerincvelő sérülés). Rendszerbetegségekhez társuló scoliosisok: Marfan sy., neurofibromatosis, osteogenesis imperfecta.
3.2.) Kockázati tényezők
Fokozott fizikai igénybevétel, helytelen testtartás, gerincközeli és törzs izomzatának nem megfelelő állapota.
4. Panaszok/Tünetek/Általános jellemzők
A panaszok és tünetek általában a scoliosis etiológiájától és a deformitás nagyságától függnek. Különösen fontos a neurologiai tünetek értékelése, melyek vagy az alapbetegségből adódóan, vagy elsősorban congenitalis csigolya malformációk okozta gerinvelői vagy gyöki compressio talaján alakulnak ki. A döntő többséget alkotó idiopathiás struktúrális scoliosis rendszerint nem fájdalmas, a betegek a deformitás miatt jelentkeznek, vezető tünetek a gerinc deformitás és következményesen a mellkas deformálódása.
5. A betegség leírása
5.1.) Érintett szervrendszer(ek)
vázrendszer: gerinc (osztályozás lokalizáció szerint)
- funkcionális scoliosis:
- balra convex, nagy ívű thoracolumbalis
- strukturális scoliosis:
- jobbra convex háti (Th6-Th12)
- balra vagy jobbra convex lumbalis (Th11/12- LIV-V)
- jobbra convex háti, balra convex lumbalis (Th4-LIV)
- jobbra convex dorsolumbalis (Th6-LII)
légzőszervek keringési rendszer
5.2.) Genetikai háttér
Idiopathisás esetekben pontos genetikai háttér nem ismert.
5.3.) Incidencia / Prevalecia / Morbiditás / Mortalitás Magyarországon A népesség 5 %o-ében észlelhető. Lányoknál nyolc-tízszer gyakoribb.
5.4.) Jellemző életkor és nem Infantilis scoliosis: 1-3 éves kor között kezdődik. Juvenilis scoliosis: 3-10 éves kor között jelentjezik. Adolescens scoliosis: 10 éves kor felett kezdődik. Újabban 2 megjelenési forma:
Korai megjelenésű görbület: 6 éves kor előtt jelentkezik Késői megjelenésű forma: 6 éves kor után jelentkezik.
II. Diagnózis
1. Diagnosztikai algoritmusok
Anamnezis - fizikális vizsgálat - képalkotó diagnosztika - etiologiától függően kiegészítő vizsgálatok - sz.e. laborvizsgálat .
2. Anamnézis
Családban való előfordulás. Gerindeformitás észlelésének időpontja, az azóta eltelt időben a görbület progressziója. Eddigi kozervatív kezelések (torna, fűzőkezelés) és azok eredményessége. Eddigi műtéti kezelések és azok eredményessége. Szubjektív panaszok megléte (fájdalom, neurológiai tünetek). Társuló betegségek (kórok is lehet) megléte, légzés, keringés károsodott volta. Lányoknál menstruációs ciklus megléte.
3. Fizikális vizsgálatok
Inspectio: Levetkőztetett betegen gerinc és mellkas megtekintése elölről, hátulról, oldalról. Vállcsúcsok, scapulák, christák magassága. Törzs-kar háromszög szimmetriája. Bőrelváltozások keresése (cafe-au-lait foltok).
Palpatio: Csigolyák proceessus spinosusainak végigtapintása, mely a görbületet kirajzolja. Nyomási, ütögetési érzékenység keresése. Előrehajolva thoracalisan bordapúp, lumbalisan izompúp keresése, mérése. Görbület kompenzáltságának megítélése függőónnal.
Görbület mobilitásának megítélése tarkónál fogva való megemeléssel és bending tesztekkel. Durva neurológiai vizsgálat.
Alsó végtagok hosszának mérése, alsó végtagi nagyizületek vizsgálata.
4. Kötelező (minimálisan elvégzendő) diagnosztikai vizsgálatok (felhasznált bizonyítékok, azok szintjei) 4.1.) Laboratóriumi vizsgálatok
A diagnózishoz általában nem feltétlenül szükséges.
4.2.) Képalkotó vizsgálatok
2 irányú teljes gerinc Rtg, valamint scoliosis esetén oldal irányú, kyphosis esetén antero-posterior Bending felvétel. 4.3.) Egyéb
légzésfunkciós vizsgálat
4.4.) Preoperatív kötelező vizsgálatok
teljes rutin nagylabor vizsg., negatív bakterologiai vizsgálatok (garat, vizelet), EKG, mellkas rtg
5. Kiegészítő diagnosztikai vizsgálatok (felhasznált bizonyítékok, azok szintjei) Etiológiától függően: Teljes és részletes neurológiai vizsgálat (pl.: neurofibromatosis) CT, esetleg 3D rekonstrukcióval (pl.: fejlődési rendellenesség).
MRI neurológiai érintettség valószínűsége esetén (pl.:neurofibromatosis, diastematomyelia). Szív UH (pl.: Marfan szindróma, myopathiák). csontdenzitás mérés (DEXA)
6. Diferenciál diagnosztika (felhasznált bizonyítékok, azok szintjei) III. Terápia
III/1. Nem gyógyszeres kezelés (felhasznált bizonyítékok, azok szintjei)
1. A megfelelő egészségügyi ellátás szintje
Járóbeteg ellátás (ambuláns tevékenység: ÁNTSZ működési engedély alapján)
Előnyös lehet, a fűző megszoktatása, fizioterápiás kezelésekotthoni egyéni tornaprogram összeállítása, begyakorlása, bővítése idejére, Ortopéd osztályos felvétele is.
Indikációja:
- 10-40° közötti görbületek
- Risser0-3stádium
- Műtéti kontraindikáció esetén a sceletális érettség befelyeződéséig.
2. Általános intézkedések
A járóbeteg ellátással szoros kapcsolatban gyógyászati segédeszközt (fűző) méretre gyártó cég jelenléte.
3. Speciális ápolási teendők
Gyógytornász által irányított speciális gerinctorna.
4. Fizikai aktivitás
Iskolai testnevelés alóli felmentés indokolatlan! Rendszeres hát és hasizom erősítő torna javallt.
5. Diéta
Az idiopátiás scoliosisokban a jelen ismeretek szerint sem a D vitamin, sem a Ca, Mg, vagy fehérjebevitel forszírozása nem csökkenti a progressziót. B-C szintű evidencia (5)
6. Betegoktatás
A fűzőkezelés tényleges eredményeinek, várható hatásának ismertetése.
7. Kezelés
7.1. Az alapbetegség kezelésének folytatása
Ismert etiológiájú scoliosisok esetében az alapbetegség gyógyszeres terápiáját folytatni szükséges, amennyiben erre szükség és mód van (pl. Cystas Fibrosis). A neuromuszkuláris betegségekben, bizonyos esetekben adható szteroidok nem csak a betegség természetes lefolyását változtatják meg, de a scoliosis megjelenésének idejét is, ill. a terhelhetőséget is. Erre az alapbetegséget kezelő szakorvos döntése alapján kerül sor, azonban erről a scoliosis kezelését végző szakembereknek is tudnia kell.
7. 2. A scoliosis kezelése és a szövődmények megelőzése
Scoliosis kezelés módját a scoliosis nagysága határozza meg.
Az ismert ún.secunder és az ismeretlen eredetű soliosisok igen eltérő ütemben progrediálnak, ezért az egyes kezelési módok eltérő súllyal szerepelnek a gyógyításukban.
A súlyos, torziós scoliosis a mellkasdeformitás miatt hozzájárulhat a légúti betegségek súlyosabb lefolyásához, ezért ilyen betegeknél fokozott figyelmet érdemel a légzőtorna felügyelete, akut betegség esetén a váladékoldás gyógyszeres kezelése és a váladék eltávolítás, fizioterápia segítségével történő biztosítása. Fájdalommal járó esetekben gyógyszeres csillapítás, ill. lazító TENS kezelés, masszázs egészítheti ki a terápiát. C szintű evidencia (6)
Mozgásterápia:
Az erőnlét javításának legfontosabb eszköze a mozgás. A fizioterápia a betegség etiologiájától, a beteg életkorától és általános állapotától függően egyéni és csoportos formában érhető el. Alapja a gyógytorna, mely különböző módszerekkel segíti a mozgás során a gerinc élettani mozgástartományának megőrzését (túlmobilizálás a progressziót fokozza káros, kivéve a műtéti előkészítést), a deformitás csökkentését (pl. PNF, Schroth). A fizioterápia 20-40 Cobb fok közt fűzőkezeléssel kiegészítve, 40 fok felett műtéti előkészítésként és utókezelésként minden betegnek szükséges. A fizioterápia eredményét a betegség etiologiája mellett a beteg kooperációja és a terapeuta által választott módszerben való jártassága is befolyásolja. A gyógytorna rövidtávú előnye a javuló tüdőfunkció, csökkenő fájdalom, a progresszió csökkenése, esetleg megállása, javuló tartás, csoportos torna esetén pszichés támogatás a "sorstársak" részéről. A szintű evidencia (7,8,11) C szintű evidencia (9,10)
- Az erőnlétet javítja a szárazföldi foglalkozások mellett végezhető gyógyúszás is, erre külön képesítéssel rendelkező oktató vezetésével. Jelen szabályozás szerint scoliosis miatt 2x52 alkalom javasolható (írható fel receptre), melyet heti 2 alkalommal 45 perces foglakozások keretében lehet igénybevenni biztosítói támogatással 18 év alatt. Ezt követően már csak 15 alkalommal vehető igénybe fürdőkezelés részeként támogatott formában az úszás. Ez azonban nem helyettesítheti a scoliosis kezelését!
- Iskolai gyógytestnevelés: Az alapbetegség függvényében törekedni kell arra, hogy minél kevesebb korlátozással éljenek a betegek, így helytelen gyakorlat a scoliosis miatt testnevelés alóli felmentés, ha más ezt nem indokolja. Szükség lehet azonban könnyítésre a gerinc hosszirányú terhelésével járó gyakorlatok esetén, vagy gyógytestnevelés elbírálására. D szintű evidencia (4)
- Sport: Súlyos deformitással járó esetekben a féloldalas sportok megfontolandók, ill. célszerű a kondicionálóterem használatánál megfelelő edző segítségének kikérése. Hobbi szinten a sportolás mindenképpen ajánlott a gerinctorna gyakorlatainak végzése mellett. C szintű evidencia (15)
7. 3. Önellátás elérése
A mindennapi élettevékenységekben a scoliosis általában nem okoz nehézségeket, problémákat, de a fűzőkezelés kezdetén az öltözködés, cipőfűzés, lehajlás valamiért ill. a toalett használat nehézkes lehet.
A műtéti kezelés után, az elmerevített gerincszakasz hosszától függően kiesik a gerinc mozgása, így a még mozgó szakaszok és a végtagi nagyizületek optimális ergonómiai kompenzációs mozgásának segítése a terapeuta feladata.
7. 4. Mobilitás biztosítása
A scoliosis a mobilitást általában nem befolyásolja.
Egyes secunderscoliosisoknál,ahol a beteg kerekesszék használatára szorul, a kialakuló súlyos torziós deformitások a beteg ülés biztonságát, a kerekesszék használatátnál a hajtást jelentősen zavarhatják..
7. 5. Állapot elfogadtatása (lelki vezetés) és az annak megfelelő életvitel elsajátítása
A scolosis kezelésében a rendszeres gyógytorna elfogadása, a fűző kezelés elviselése gondot jelenthet különösen az adolescens korosztályban, nagyon fontos a betegek lelki vezetése,támogatása. A scoliosis miatt kezelt beteg nagy része ambuláns formában ellátható, ami segíti az együttműködést. Az állapot nyomon követése csak rendszeres gondozás mellett biztosítható, ami a növekedés befejeződésig 3-6 havonta végzett fizikális vizsgálatot és évente röntgen kontrollt jelent. A fűzőkezelést igénylő esetekben a fűző cseréje esetén is szükséges kontroll röntgen, a korrekció mértékének ellenőrzésére. B-C szintű evidencia (5)
Szervezett gyógytorna, legalább heti 2 alkalommal szükséges a kezelés teljes tartama alatt. A betanult gyakorlatokat azonban otthon, naponta végezni kell! Egyéni torna szükséges nagyon fiatal páciensek esetén a kialakulatlan izomérzet miatt a korrekció megtanítására és gyors növekedés esetén, fokozott progresszió mellett. Ez legalább 2-3 hétig, heti 5 alkalommal, gyógytornász segítésével végzett foglalkozást jelent. Amennyiben a beteg/család kooperációja nem megfelelő, a konzervatív terápia eredménytelensége esetén műtéti kezelés javíthat az állapoton, de itt is fontos a megfelelő konzervatív előkészítés és utókezelés, ilyenkor intézeti keretek közt. Mindkét esetben javasolt a rossz kooperáció okának pontos felderítése, az esetleges ismerethiány miatti kommunikációs probléma kezelése, a beteg és családjának képzése. C szintű evidencia (16)
7. 6. Segédeszközök biztosítása
Fűzőkezelés
Strukturális scoliosisban 20 Cobb fok feletti görbület az esetek több mint felében a konzervativ kezelés elmaradása esetén progrediál. B-C szintű evidencia (5)
Idiopáthiás scoliosis esetén a romlás mértéke és sebessége függ a görbület formájától és nagyságától, a beteg életkorától, nemétől, a maturáltság fokától, a várható növekedés mértékétől, a menarche-tól eltelt idő hosszától, a kezelés kezdetének időpontjától, az alkalmazott kezeléstől. A szintű evidencia(7,8). A fűzők egyedi gipszminta után, magas hőfokon lágyuló műanyagból készülnek. Az idiopátiás scoliosis fűző kezelésének szabályai:
- Jelentős progressziónál (fél év alatt több mint 5 Cobb fok), amint eléri a görbület a 20 Cobb fokot, el kell kezdeni a fűzőkezelést.
- A görbületnek megfelelő típusú fűző használata ajánlott.
- Viselési idő: 18- 20 óra / nap. Kezelőorvosi kontroll vizsgálat 3-4 havonta.
- Röntgenfelvételek készítése két irányból, álló helyzetben évente, de újfűző készítése előtt mindig, valamint az új fűző feladását követően 6-8 héttel.
- Állapotváltozáskor (magasság-, súlynövekedés, görbület nagyságának jelentős változása) fűzőcsere.
- Fűzőkezelés folytatása a csontérettség eléréséig szükséges
-40 -50 Cobb foknál nagyobb görbületeket már ne kezeljünk fűzővel.
A progresszió lassítására a 40 fok alatti görbületek esetén a tanulmányok egy része szerint a fűzőkezelés alkalmas. A szintű evidencia (7,8,17) B szintű evidencia (21,22)B-C szintű evidencia (5)C szintű evidencia (6,19,20,23) Fűző típusok strukturális scoliosis kezelésére:
Boston korzett- rövid műanyagfűző, kétféle formája van. Hátul nyitható formájában, elsősorban a thoracolumbalis és lumbalis gerinc frontális és sagittalis irányú strukturális görbületeinél alkalmazható, amikor a görbület csúcspontja a Th X. csigolya alatt helyezkedik el. A korzett, elől nyitható formája az ágyéki gerincszakasz rögzítésére szolgál. Kifejezetten csökkenti a lumbalis lordosis mértékét.
Charlestone korzett - a gerinc egyívű, mobilis , a háti-ágyéki átmenetében elhelyezkedő strukturális, scoliotikus görbületének kezelésére alkalmas. A fűző a beteget túlkorrigált helyzetben tartja, ezért csakfekve, elsősorban éjszakai viseletre alkalmas, mobilis és relatíve kicsi, maximum 25 Cobb fokos görbületek esetén ajánlott.
Cheneau korzett - a leggyakrabban alkalmazott fűző, amely alkalmas, mind a frontális (scoliosis), mind a sagittális (kyphosis, lordosis) síkban elhelyezkedő strukturális gerincgörbületek korrekciójára. Álltartóval kiegészítve, nemcsaka háti és ágyéki, hanem a nyaki gerinc görbületeinek korrekcióját is lehetővé teszi. Hátránya, hogy jelentősen akadályozza a mellkas normális fejlődését.
Stagnara (lyoni) korzett-a törzs elülső és hátsó oldalán, a középvonalban futó 1 -1 fémsínből és a fémsínekhez rögzített korrekciós pelottákból áll. Alkalmas strukturális scoliosis kezelésére, valamint az ideg-izom eredetű scoliosisok elsődleges kezelésére szolgál. Műtétek utáni rögzítésre is használják. Kiegészíthető nyakgyűrűvel. Némi módosítással nyílirányú strukturális gerincgörbületek (pl. Scheuermann féle betegség) korrekciójára is alkalmassá tehető. Milwaukee korzett -bármilyen irányú és lokalizációjú görbület kezelésére alkalmazható, fiatal korban, a mellkas fejlődésének befejeződése előtt. A fűző medencekosárból, nyakgyűrűből, összekötő sínekből és a görbületeknek megfelelően elhelyezett korrekciós párnákból áll. A nyakgyűrű, amely kilátszik a ruhából, súlyos lelki problémákat okozhat a serdülőknél. A nyakgyűrű használata csak a magas háti görbületeknél (csúcscsigolya a Th 5. csigolya felett) ill. a nyaki folyamatoknál kötelező. Az egyetlen korzett, mely nem befolyásolja károsan a mellkas fejlődését. Hibája még a korzettnek, hogy a háti gerinc, idiopathias scoliosisnál jelentkező ellaposodását nehezen lehet vele megelőzni, valamint az, hogy kompenzatórikus görbületek megjelenését segíti elő.
Merev fűzők előnyei
- A korszerű, korrekciós fűzők képesek 3D korrekcióra, a Milwaukee-t kivéve. Az elsődleges korrekció már a feladást követően azonnal jelentkezik, de a teljes korrekció,6 hét múlva készült fűzős röntgenfelvétellel mutatható ki
Merev fűzők hátrányai
- Neuromuscularis eredetű scoliosisban a merev fűzők bár "kényszerítenek" a korrigált tartásra csak rövid ideig képesek a progressziót lassítani, ugyanakkor járógéppel kegészítve elősagíthetik az ideg-izom eredetű scoliosisban szenvedő betegek vertikalizációját.
- Jelentősen befolyásolják a mellkas normális fejlődését.
- Serdülőkorú pácienseknél a kortárs közösség elutasításától való félelem gátolhatja a nappali viselést. A szintű evidencia (7,8,17) B szintű evidencia (21,22)B-C szintű evidencia (5) C szintű evidencia (6,12,18,19,20,23)
Rugalmas fűzők
A merev műanyagfűzők mellett léteznek rugalmas, dinamikus fűzők is. Az ezzel kapcsolatos eredmények ellentmondóak. C szintű evidencia (24)
Rugalmas fűzőkezelés előnyei
- A merev fűzőkkel szemben előnye, hogy gyakorlatilag láthatatlan, minden mozgás kivitelezhető benne, így a 20 órás viselés könnyebben megoldható, könnyebb a gerinc rugalmasságát megőrizni.
Rugalmas fűzőkezelés hátrányai
- Szűk az indikációs területe, a felhelyezést követően azonnal nem észlelhető a javulás, nem korrigál minden síkban, a napi felvétele nagyobb odafigyelést kíván (pántok, tépőzárak pontos elhelyezése, a medenceöv gondos beállítása) és a toalett használat bonyolult.
- Csak kifejezetten mobilis, kis görbületek (20 fok alatti görbületek) kezelésére ajánlott. Szociális intézkedések kezdeményezése
A fűzőkezelés időtartamára, ill. korrekciós gerincműtét után 1 évig, a jelenlegi szabályozás szerint közgyógyellátási igazolvány és emelt összegű családi pótlék igényléséhez igazolás adható.
Amennyiben a terápia lakóhelyen nem biztosított, a közlekedéshez TB támogatás vehető igénybe, a kezelő intézmény igazolásával,utólagos elszámolással.
III/2. Műtét [A szintű evidencia (1;2;3)]
1. A megfelelő egészségügyi ellátás szintje
Fekvőbeteg ellátás / műtéti tevékenység: ÁNTSz működési engedély alapján.
2. Általános intézkedések 2.1.) Műtői körülmények
A műtét tárgyi feltételei
Kiemelt sterilitást biztosító műtő, az ÁNTSz minimumfeltételeknek megfelelően felszerelve.
A műtét biztonságos kivitelezését biztosító általános műszerkészlet.
Az esetleges implantáció kivitelezéséhez szükséges speciális műszerkészlet.
A tervezett implantációs eszköz teljes méretválasztékából egy sorozat.
Leggyakoribb szövődmények ellátásához szükséges műszerek, implantátumok megléte.
Műszerek és berendezések:
Minimum: Speciális gerincsebészeti műtőasztal
Elektrokoaguláló
Központi szívás
Rtg képerősítő
Rtg
Standard műszerkészlet Optimum: A fentiek plussz Cell saver
Intraoperatív neurofiziológia lehetősége (SEP, MEP) 2.2.) Személyzeti kívánalmak
Sebész, célirányos elméleti és gyakorlati felkészültséggel. Anaesthesiológus orvos, valamint asszisztens jelenléte elengedhetetlen.
Egyéb szakemberek, célirányú (szakképzett műtős) képzettséggel, míg SEP és MEO használata esetén speciálisan képzett szakasszisztens kívánatos.
3. Speciális ápolási teendők
A műtétet követően, a beteg általános belgyógyászati statusában felmerülő állapot-változások korrekciójának biztosítása
4. Sebészeti kezelés 4.1.) műtéti indikáció Dorzális feltárás:
6 éves kor alatt bizonyítottan progrediáló görbületek esetén azonnal, növekedő implantátummal, fúzió nélkül. 6 éves kor alatt Thoracalis Insufficiencia Szindróma (TIS) megléte esetén vagy növekedő implantátummal, fúzió nélkül.vagy Vertical Expandable Prosthetic Titanium Rib (VEPTR) implantátummal a légzésfunkció mielőbbi javítása érdekében.
Scoliosis esetén 35 Cobb fokot meghaladó bármely irányú strukrturális görbület etiológiától függetlenül, vagy évente legalább 10 fokot meghaladó dokumentált progresszió, Risser3-5stádiumban.
Kyphosis esetén 55 - 75 Cobb fokot meghaladó reguláris kyphosis, relatív indikáció, míg 75 Cobb fokot meghaladó reguláris kyphosis absolút indikáció, Risser3-5 stádiumban. 20 Cobb fokot meghaladó anguláris kyphosis. Ventrális feltárás:
6 éves kor alatt Thoracalis Insufficiencia Szindróma (TIS) megléte esetén Vertical Expandable Prosthetic Titanium Rib (VEPTR) implantátummal a légzésfunkció mielőbbi javítása érdekében.
Scoliosis esetén 100 Cobb fokot meghaladó görbület, kifejezetten merev 80 - 100 fokos görbület. Risser0-3 stádiumokban bármely görbület a Crancshaft fenomén kivédése céljából. Kyphosis esetén minden anguláris kyphosis, növekedés befejeztével minden reguláris kyphosis.
4.2.) műtéti előkészítés
Általános belgyógyászati kivizsgálás, szükség szerinti szakorvosi konzíliumokkal kiegészítve. Anaesthesiologiai protokoll szerinti előkészítés. Antibiotikus- és thrombosis profilaxis útmutatásai alapján.
4.3) műtéti érzéstelenítés Anaesthesiologiai protokoll leírása szerint
4.4.) műtét
Dorsalis feltárás: (A generikus lépéseket követően)
1 A beteg asztalra történő fektetése (hason fekvés).
2 A műtét alatti folyamatos húzás (Húzás a fejen: Halo tractio: az esetek jelentős részében Halo szükséges, és csak kivételes esetben helyettesíthető Halo trakció Glisson-függesztővel történő húzással). Irányának és nagyságának beállítása mind a fejen, mind az alsó végtagokon (max. a testsúly 1/3-a).
3 A műtéti terület bőrfertőtlenítése.
4 A műtéti terület izolálása.
5 Bőrmetszés.
6 Subcutison történő áthaladás.
7 Fascia medián, vagy paramedián síkban való bemetszése.
8 Paravertebralis izomzat egy-vagy kétoldali leválasztása, a kisizületekfelszabadítása.
9 Intraoperatív Rtg készítése szintmeghatározás céljából.
10 A műtét speciális lépései (lásd alább részletezve).
11 Szívódrain, - drainek behelyezése és kiöltése.
12 A fascia és ezen keresztül a paravertebralis izomzat csomós öltésekkel történő zárása.
13 A subcutis folyamatos öltéssel történő zárása.
14 A bőr folyamatos öltéssel való zárása.
15 A sebkörnyék lemosása.
16 A seb fedése.
A műtétek speciális lépéseinek részletezése (10. pont): 10/1. Multiszegmentális egyoldali spondylodesis + graft *.
(A hátsó ívek és nyúlványok egyoldali dekortikálása + graft / saját csont, biocoral/ + gipszágy + fűző az utókezelés részeként).
10/2. Csontgraft* augmentáció.
(Ugyanaz mint az 1/1, csak 2.3.4. lépésként max 9 hónapos intervallumokban végzendő). 10/3. Instrumentárium spondylodesis nélkül
(Végponti csigolyák feltárása + implantátumok helyének elkészítése + implantátum behelyezések/kapcsok csak a végponti csigolyákon/ + subcutan rúd behelyezés + korrekció + gipszágy + fűző az utókezelés részeként)
10/4. Correctio a spondylodesis nélküli műtét után
(Ugyanaz mint az 1/3. Instrumentárium és subcutan rúd behelyezése nélkül. Szükség szerint évente 1- 2 alkalommal végezhető).
10/5. Posterior multisegmentális instrumentárium (3D) + spondylodesis + graft*
(Implantátumok helyének elkészítése + implantátum behelyezés/mindig poliszegmentálisan/+ korrekciós rúdforma kialakítása + rúd behelyezés + korrekció + wake-up teszt + 2. rúd behelyezés + ívek, nyúlványok dekortikálása, kisizületek szanálása + graft + rúdösszekötők felhelyezése).
10/6. Posterior osteotomia + posterior multisegmentalis instrumentárium (3D) +spondylodesis + graft* (Mono vagy multiszegmentális hátsó osteotomia + idegelemek felszabadítása + 1/5).
10/7. Posterior osteotomia előzőleg fuzionált gerinc esetében + posterior multisegmentális instrumentárium (3D) + spondylodesis + graft*.
(Instrumentárium eltávolítása + mono vagy multisztegmentális hátsó osteotomia + idegelemek felszabadítása + új implantátumok helyének elkészítése + új implantátum behelyezés/mindig poliszegmentálisan/ + korrekció /ha lehetséges/ + wake-up teszt + 2. rúd behelyezés + dekortikálás + graft + rúdösszekötőkfelhelyezése).
- Graft nyerés miatt ahol ez szükséges a műtétek az alábbi lépésekkel egészülnek ki.
(Bőrmetszés a crista ilei felett + a periosteum és a csípőlapát hátsó felszínén tapadó izmok letolása + csontnyerés + izom rekonstrukció + szívódrainage + réteges sebzárás)
Ventrális feltárás: (transthoracalis, thoracoabdominális, retroperitonealis, costotransversectomiás, transperitonealis)
(A generikus lépéseket követően)
1. A beteg asztalra történő fektetése (oldal fekvés: transthoracalis, thoracoabdominalis, retroperitonealis, costotransversectomiás behatolás/mindig a concáv oldalon/, hanyatt fekvés: transperitoneális behatolás).
2. A műtét alatti folyamatos húzás irányának és nagyságának beállítása mind a fejen**, mind az alsó végtagokon (max. a testsúly 1/3-a).
3. A műtéti terület bőrfertőtlenítése.
4. A műtéti terület izolálása.
5. Bőrmetszés (mind a convex oldalon a bordalefutásnak megfelelően: transthoracalis behatolás: a görbületi punctum maximumából számított borda, thoracoabdominalis behatolás: X. borda, retroperitonealis behatolás: XII. borda, costotrransversectomiás behatolás: a punctum maximumon, transperitonealis behatolás: medián laparotomia).
6. Subcutison történő áthaladás.
7. Borda subperiosteális feltárása (transthoracalis, thoracoabdominális, retroperitonealis behatolás). Bordák és proseccus transversusok subperiosteális feltárása (costotransversectomiás behatolás). Linea alba átmetszése (transperitonealis behatolás).
8. Bordaresectio. Costotransversectomia.
Peritoneum megnyítása (transperitonealis behatolás).
9. Parietalis pleura bemetszése (transthoracalis behatolás)
Parietalis pleura bemetszés + rekeszleválasztás (thoracoabdominalis behatolás). Áthaladás a hasfali izomzaton + peritoneum lepreparálása (retropertitonealis behatolás). Fali peritoneum átmetszése az L IV-LV magasságában (transperitonealis behatolás).
10. A műtét speciális lépései (lásd alább részletezve)
11. Rekesz rekonstrukció (csak thoracoabdominális behatolás).
12. Mellkasi szívódrain (transthoracalis, thoracoabdominális behatolás), - és/vagy drainek behelyezése és kiöltése.
13. A pleura recostructio és mellüreg zárása csomós öltésekkel (transthoracalis, thoracoabdominalis behatolás). Hasfali izomzat zárása csomós öltésekkel (retroperitonealis behatolás).
Linea akba zárása csomós öltésekkel (transperitonealis behatolás).
14. A subcutis folyamatos öltéssel történő zárása.
15. A bőr folyamatos öltéssel való zárása.
16. A sebkörnyék lemosása.
17. A seb fedése.
A műtétek specialis lépéseinek részletezése (10. pont): 10/1. Anterior corpodesis + graft***.
(Fali pleura/peritoneum lepreparálása + segmentális érképletek ligaturája + periosteum lepreparálása + intervertebral discusok eltávolítása + vérzéscsillapítás + graft*** + periosteum reconstructio + pleura/peritoneum reconstrukcio).
10/2. Anterior corpodesis csigolyatestbe ékelt grafttal****.
(Fali pleura/pertitoneum lepreparálása + segmentális érképletek ligaturája + periosteum lepreparálása + intervertebrális discusok eltávolítása + vérzéscsillapítás + vályulat képzés a feltárt csigolyákban + graft**** beékelés + graft*** + periosteum reconstructio + pleura/peritoneum reconstrukcio).
10/3. Anterior corpodesis kitámasztó grafttal****
(Fali pleura/peritoneum lepreparálása + segmentális érképletek ligaturája + periosteum lepreparálása + intervertebrális discusok eltávolítása + vérzéscsillapítás + graft**** beékelés a végponti csigolyákban + csigolyatest felépítés + graft*** + periosteum reconstructio + pleura/peritoneum reconstructio)
10/4. Anterios osteotomia + corpodesis kitámasztó graft****
(Fali pleura/peritoneum lepreparálása + segmentális érképletek ligaturája + periosteum lepreparálása + intervertebral discus maradványok felkeresése + discus maradványok eltávolítása + osteotomia + vérzéscsillapítás + graft**** beékelés a végponti csigolyákban + csigolyatest felépítés + graft*** + periosteum reconstructio + pleura/peritoneum reconstrukcio)
10/5. Anterior decompresio + corpodesis kitámasztó grafttal****
(Fali pleura/peritoneum lepreparálása + segmentális érképletek ligaturája + periosteum lepreparálása + intervertebral discuzs maradványokfelkeresése + discus maradványokeltávolítása + csigolyatest hátsó részleteinek eltávolítása + idegelemek felszabadítása + vérzéscsillapítás + graft**** beékelés a végponti csigolyákban + graft*** + periosteum reconstructio + pleura/peritoneum reconstrukcio).
10/6. Anterior csigolyatest resectio + corpodesis kitámasztó grafttal****
(Fali pleura/peritoneum lepreparálása + segmentális érképletek ligaturája + periosteum lepreparálása + intervertebrális discusok felkeresése + discusresectio + csigolyatest eltávolítása + idegelemek felszabadítása + vérzéscsillapítás + graft**** beékelés a végponti csigolyákban + graft*** + periosteum reconstructio + pleura/peritoneum rekonstructio).
10/7. Anterior instrumentarium + corpodesis
(Fali pleura/peritoneum lepreparálása + segmentális érképletek ligaturája + periosteum lepreparálása + intervertebrális discusok felkeresése + discusresectio + vérzéscsillapítás + implantátumok helyének elkészítése + implantátumok behelyezése/mindig poliszegmentálisan/ + rúd behelyezés + korrekció + graft*** + periosteum reconstructio + pleura/peritoneum rekonstructio).
Húzás*** a fejen: Halo tractio
(10/1 - 10/7 műtétek esetén mindig Halo szükséges, míg a 10/7 műtét esetén a Halo helyettesíthető Glisson-függesztővel történő húzással is).
Graft***
(A resecált borda őrlemény)
Graft**** nyerés miatt ahol ez szükséges a műtétek az alábbi lépésekkel egészülnek ki.
(Bőrmetszés egy vagy mindkét tibia felett + a periosteum lepreparálása + csontspán nyerés /1-1,5 cm széles. A tibia teljes hosszát kitévő spán, a tibia él intaktságának megőrzésével / + periosteum reconstructio + réteges sebzárás).
Megjegyzendő, hogy a fúziókhoz szükséges csontot kiegészítő, vagy teljességgel kiváltó természetes (pl.: korall alapú hydroxiapatit) és/vagy mesterséges alapanyagú (hydroxiapatit) helyettesítő termékek is használhatóak, melyek használata esetén a graft****... lépés természetesen kimarad. (A használatot nehezíti a finanszírozás hiánya).
Az anterior feltárások (10/2 - 10/6-os számú műtétek) után egy bentfekvés során valamilyen hátsó feltárásból végezhető korrekciós spondylodesis mindig szükséges.
A 10/1, valamint a 10/7 számú műtétek esetén szükséges lehet egy bentfekvés alatt elvégzett hátsó korrekciós spondylodesis is.
Egyedi műtétek:
1. vascularizált borda graft anterior behelyezés, vagy
2. thoracoplastica egyedi esetben szükségessé válhat a gerincdeformítások korrekciójának növeléséhez.
3. Thoracoscopos mellkasi felszabadító műtét (fejlesztés alatt)
4.5.) posztoperációs teendők
ITO szükségessége: Az anterior feltárások (10/2 - 10/6-os számú műtétek) után egy bentfekvés során valamilyen hátsó feltárásból végezhető korrekciós spondylodesis mindig szükséges. A 2. műtét elvégezhetőségéig (max 10 nap) intenzív osztályos elhelyezés, vagy folyamatos postoperatív őrzés szükséges.
A közvetlen postoperatív szakban fokozott felügyelet szükséges: szívódrainen keresztül ürült mennyiség regisztrálása, folyadékháztartás (só-elektrolit, sz.sz. vérpótlás) rendezése, fájdalomcsillapítás, a beteg ált. belgy. statusának ellenőrzése érdekében.
Antibiotikus, thrombozis profilaxis, sz.sz. alapbetegség spec. gyógyszerelése.
A beültetett implantatum helyzetének ellnőrzése kontroll képalkotó eljárással, legkésőbb 24 órán belül.
Ventrális feltárás után testüregi drainen ürült mennyiség regisztrálása. Kórtermi nativ mellkas rtg a postoperatv 1. napon és mellkas drain kihúzása előtt.
A műtét menetének részletes leírása, a műtéti leírás csatolása kórlaphoz, archiváláshoz. A beültetetett implantátum dokumentálása műtéti leíráson, archiváláshoz.
5. Fizikai aktivitás
Postoperatív torna, vénás torna, légzőtorna és mobilizálás gyógytornász protokoll szerint, orvosi vélemény alapján. Kontroll vizsgálatok alapján egyénileg meghatározott fokozatos terhelési program szerint.
6. Segédeszköz igény: Nem megfelelő minőségű, porotikus csontok esetén, vagy féloldali dézisek esetén postoperatív gipszágy, valamint postoperatív fűző viselése javasolt.(pl.: neurofibromatosis esetén a műtétet követő 1 évig).
7. Diéta
Általános, vagy belgyógyászati indikációnak megfelelően, dietetikai előírások szerint.
8. Betegoktatás
Általános betegtájékoztató szerint. Implantátum egyedi előírásainak megfelelően. Gyógytornász utasításainak megfelelően.
III/4. Egyéb terápia (pszichoterápia, gyógyfoglalkoztatás stb.)
IV. Rehabilitáció
Korai: Második naptól a spinalis izombalance helyreállítása
Késői: 6. Héttől óvatos, fokozatos terhelés mellett hát és hasizom erősítő torna, rendszeres úszás. Gondozás: Évente legalább egy alkalommal végzett teljes gerinc vizsgálat rtg. kontrollal kiegészítve.
V. Gondozás
1. Rendszeres ellenőrzés
A beteg általános mozgásszervi állapotának, az operált gerinc rendszeres felügyelete után vizsgálata szükséges a műtétet követő 6-12 héten, majd fél év, egy évvel később. Ezt követően panaszok esetén ill. egy-két évente. Röntgenkontroll közvetlen műtét után, fél-egy év múlva, ill. panasz esetén és az operáló osztály útmutatása szerint.
2. Megelőzés
Bekövetkező állapotromlás esetén haladéktalan beavatkozás szükséges: utókezelés, rehabilitáció, sz.e. reoperáció.
3. Lehetséges szövődmények
Korai és késői infekció, haematoma, sebgyógyulási zavar, thrombophlebitis, mélyvénás thrombosis, tüdő embólia, igen ritkán ér- és ideg károsodás, implantátum lazulás/törés.
4. Szövődmények kezelése
A 4. pontban felsorolt szövődmények kezelésének haladéktalan megkezdése szükséges.
Fontos a postoperatív localis szövődmények korai ellátása. Infectio gyanúja esetén korai feltárás, alapos debridement és átmosás majd szívódrainek behelyezése javasolt. Steril haematomát a műtőben steril körülmények között kell kiüríteni. Sebgyógyulási zavar, illetve bőrnecrosis esetén annak kiterjedésétől függően felületes hámosító kezelés vagy a defectus sebészi zárása szükséges.
5. Kezelés várható időtartama/Prognózis
A beteg egyedi mozgásszervi statusából következően egyedi felépülési prognózist kell megállapítani, amelyben törekedni kell az életminőség javításának legrövidebb, de legbiztosabb módjára.
6. Az ellátás megfelelőségének indikátorai
Gerindeformitás megszűnése vagy jelentős csökkenése, kompenzálttá válása. Fájdalommentesség, neurologiai deficit hiánya.
Nemzetközi protokollok kiértékelése.
A műtött beteg általános és speciális mozgásszervi állapotának rögzítésének dokumentálása szükséges az állapotváltozás utánkövetése érdekében.
Szakmai munka eredményességének mutatói
(folyamat-, eredmény indikátorok EüK.2003.V.29- számában megjelent indikátorok mintájára kérjük megadni)
VI. Irodalomjegyzék
1. Bradford DS., Lonstein JE., Moe JH., Ogilvia JW., Winter RB: Moe's Textbook of Scoliosis and other Spinal Deformities Second edition, 1987. W.B. Saunders Co. Philadelphia, London, Toronto.
2. DeWald RL., Arlet V., Carl AL., O'Brien MF: Spinal Deformities. The Comprehensive text. 2003. Thieme, New York, Stuttgart.
3. Weinstein SL: The pediatric Spine. Principles and Practice 1995. Raven Press, New York.
4. A testnevelés kategóriákba sorolás szempontjai. Az Országos Gyeremekegészségügyi Intézet szakmai irányelve 2007
5. Szendrői M. (szerk): Az Ortopédia Tankönyve, Semmelweis Kiadó, Budapest, 2005.
6. Orosz M: Az idiopathias scoliosis kezelése Gyermekgyógyászat 2005; 6: 649-655
7. Rowe DE, Bernstein SM, Riddick MF et al.: A meta-analysis of the efficacy of non-operative treatments for idiopathic scoliosis. J Bone Joint Surg Am 1997; 79: 664-74.
8. Lenssinck ML, Frijlink AC, Berger MY.: Effect of bracing and other conservative interventions in the treatment of idiopathic scoliosis in adolescents: a systematic review of clinical trials. Phys Ther 2005; 85:1329-39.
9. Nagy Sz.: Az idiopathias scoliosis korszerű, komplex mozgásterápiája Gyermekgyógyászat, 2005; 6: 657-665.
10. Rigo M, Reiter Ch, Weiss HR.: Effect of conservative management on the prevalence of surgery in patients with adolescent idiopathic scoliosis. Pediatr Rehabil 2003; 6: 209-14.
11. Maruyama T, Kitagawa T, Takeshita K.: Conservative treatment for adolescent idiopathic scoliosis: can it reduce the incidence of surgical treatment? Review. Pediatr Rehabil 2003; 6: 215-9.
12. O'Neill PJ, Karol LA, Shindle MK.: Decreased orthotic effectiveness in overweight patients with adolescent idiopathic scoliosis. J Bone Joint Surg Am 2005;87:1069-74.
13. Illés T.: A gerincdeformitások 3 dimenziós analízise és műtétti terápiája MTA Doktori disszertáció 2003
14. Jeszenszky D: A gerincdeformitások műtéti kezelése neuromuscularis betegségekben Gyermekgyógyászat, 2005; 5: 523-530.
15. Weiss HR, Weiss G, Schaar HJ.: Incidence of surgery in conservatively treated patients with scoliosis. Pediatr Rehabil 2003; 6: 111-8.
16. Reichel D, Schanz J: Developmental psychological aspects of scoliosis treatment. Pediatr Rehabil 2003; 6: 221-5.
17. Weiss HR, Negrini S, Hawes MC et al.: Physical exercises in the treatment of idiopathic scoliosis at riskof brace treatment - SOSORT consensus paper 2005. Scoliosis 2006;1:1748-7161.
18. Karol LA.: Effectiveness of bracing in male patients with idiopathic scoliosis. Spine 2001; 26: 2001-5.
19. Weiss HR, Weiss GM.: Brace treatment during pubertal growth spurt in girls with idiopathic scoliosis (IS): a prospective trial comparing two different concepts. Scoliosis 2005; 8:199-206.
20. Howard A, Wright JG, Hedden D. :A comparative study of TLSO, Charleston, and Milwaukee braces for idiopathic scoliosis. Spine 1998;23:2404-11.
21. Nachemson AL, Peterson LE.: Effectiveness of treatment with a brace in girls who have adolescent idiopathic scoliosis. A prospective, controlled study based on data from the Brace Study of the Scoliosis Research Society. J Bone Joint Surg
Am 1995; 77: 815-22.
22. Yrjonen T, Ylikoski M, Schlenzka D.:Results of brace treatment of adolescent idiopathic scoliosis in boys compared with girls: a retrospective study of 102 patients treated with the Boston brace. Eur Spine J 2007; 16:393-7. Epub 2006 Aug 15.
23. Janicki JA, Poe-Kochert C, Armstrong DG.: A Comparison of the Thoracolumbosacral Orthoses and Providence Orthosis in the Treatment of Adolescent Idiopathic Scoliosis: Results Using the New SRS Inclusion and Assessment Criteria for Bracing Studies. J Pediatr Orthop 2007; 27: 369-374.
24. Coillard C, Vachon V, Circo AB, Beauséjour M, Rivard CH: Effectiveness of the SpineCor brace based on the new standardized criteria proposed by the scoliosis research society for adolescent idiopathic scoliosis. J Pediatr Orthop. 2007; 27:375-9
Kapcsolódó internetes oldalak www.ortopedtarsasag.hu
A szakmai protokollok érvényessége: 2010. szeptember 30.
| A bizonyítékok szintjei | ||
| Kód | Szint | Definíció |
| A | Erősen megalapozott tudományos bizonyíték | Többszörösen releváns, minőségi tudományos tanulmány, homogén eredményekkel |
| B | Közepesen megalapozott tudományos bizonyíték | Legalább egy releváns, minőségi tanulmány vagy több adekvát tanulmány |
| C | Korlátozottan megalapozott tudományos bizonyíték | Legalább egy adekvát tudományos tanulmány |
| D | Nem áll rendelkezésre megalapozott tudományos bizonyíték | További információk szakértői elemzése |
Az Egészségügyi Minisztérium
szakmai irányelve
A számított GFR (eGFR) bevezetésével kapcsolatos ismeretekről útmutató laboratóriumi szakemberek számára
Készítette: a Magyar Laboratóriumi Diagnosztikai Társaság, a Magyar Nephrológiai Társaság és a Magyar Diabetes Társaság
Az idült vesebetegség (CKD) gyakori, legtöbbször progresszív, korai érelmeszesedéshez és halálozáshoz vezető betegség, melynek lefolyásában a glomerulus filtrációs ráta (GFR) alapján 5 stádiumot különböztetünk meg (1. táblázat). A szérum kreatinin (Scr) nem elég érzékeny jelzője a GFR csökkenésének. A CKD 3-5. stádiumában a számított GFR (eGFR) pontosabban becsüli a valódi GFR-t, mint a vizeletgyűjtéssel mért kreatinin clearance. CKD rizikója esetén az eGFR meghatározása, és ennek eredményétől függően nephrológiai konzílium ill. gondozás szükséges.
1. táblázat: Az idült vesebetegség stádiumai
| Stádium | Jellemző | GFR ml/perc/1,73m2 | Főbb tünetek | Gyakoriság (%) | Teendők |
| 1. | vesebetegség norm. v. magas GFR-rel | >90 | alap-betegség | 3,3 | diagnózis, kezelés |
| 2. | vesebetegség csökkent GFR-rel | 60-89 | hypertonia CV rizikót | 3,0 | progresszió és CV rizikó csökkentés |
| 3. | mérsékelt veseelégtelenség | 30-59 | anaemia osteodystr. | 4,3 | fentiek + szövődmények kezelése |
| 4. | súlyos veseelégtelenség | 15-29 | hyperK oedema | 0,2 | fentiek + felkészülés vese-pótló terápiára |
| 5. | végstádiumú veseelégtelenség | <15v. dialízis | malnutritio uraemia | 0,1 | transzplantáció dialízis |
Jelen útmutató célja, hogy az eGFR számítása és alkalmazása épüljön be a rutin klinikai gyakorlatba, továbbá, hogy az eGFR számítását és eredményének közlését a magyarországi laboratóriumok szakszerűen, és a hazai és nemzetközi irányelvajánlásoknak megfelelően végezzék.
Háttér
A vesefunkció legjobb jelzője a GFR, melynek meghatározása a mindennapi gyakorlatban körülményes (izotóp clearance vizsgálatok) és pontatlan (kreatinin clearance 24 órás vizeletgyűjtésből). Ezért 2005-ben a MANET az MLDT-vel közösen kidolgozott egy ajánlást, mely javasolta a GFR képletekkel történő számítását, és ennek rutinszerű közlését a laboratóriumi leleten (1). A MANET és MLDT ajánlás kimunkálása óta számos cikk jelent meg, mely felhívja a figyelmet a kreatinin módszerek standardizációs problémája miatti eGFR meghatározás pontatlanságaira, emiatt a CKD stádiumok klasszifikációs hibáira és az eGFR alkalmazhatóságának limitációira (2-3). A problémák megoldására folyamatban van a kreatinin módszerek nemzetközi standardizációja és időközben a hagyományos számítási képleteket is felülvizsgálták (4-5). 2006-tól amerikai és brit útmutatók is egyértelműen ajánlják a MDRD (Modification of Diet in Renal Disease) egyenlettel történő eGFR számítást (6-8). Az eGFR orvosi diagnosztikai laboratóriumokban történő számítása és az eredmény automatikus közlése azért is célszerű, mert a Scr értéke függ a meghatározására alkalmazott módszer referencia standardra való visszavezethetőségétől. Így az újScr módszerek esetén módosított MDRD képlet alkalmazása szükséges.
Miért szükséges a GFR ismerete?
A CKD a lakosság több mint 10 %-át érinti, és a betegek többségében a vesefunkció is beszűkült. Ennek oka az atherogenetikus nephropathiák (leginkább diabetes mellitusban, hypertoniában, érbetegségben jelentkező vesekárosodás) számának drámai megemelkedése. A klasszikus vesetünetek hiánya miatt a betegség későn, sokszor csaka végstádiumban kerül felismerésre. Ugyanakkor már az enyhe - mérsékelt veseelégtelenség is jelentősen fokozza az atherosclerosis kockázatát, szövődményekhez, korai halálozáshoz vezet. A GFR csökkenés kimutatásával és az időben elkezdett nephrológiai gondozással lehetőség van a vesefunkció romlás megállítására vagy progressziójának
csökkentésére, a szövődmények kezelésére, a vesepótló kezelés időben történő elkezdésére, módjának megválasztására. Mindezektől a betegek morbiditásának és mortalitásának csökkenése várható.
Hogyan történik az eGFR számítása?
A szakirodalomban és a klinikai gyakorlatban számos eGFR kalkulációs módszer ismert: pl. Schwartz-Counahan, Cockroft-Gault, MDRD (Modification of Diet in Renal Disease) és az ún. 4-változós (4v) MDRD formulák. Nemzetközi és hazai ajánlások ezek közül felnőttekben (18 év felett) minden Scr vizsgálat kérésekora 4v MDRD, Scr módszerfüggő változatának megfelelő formulával számolt eGFR automatikus megadását és klinikai használatát javasolják (1,6-8). A 4v MDRD kinetikus Jaffé Scr módszerre vonatkozó számítási képlete az ún. "186-os MDRD formula":
eGFR =186 x(kreatinin x 0,0113)-1.154x(kor)-0.203x0,742 ha nő (x1,21 ha fekete rassz) ahol: GFR (ml/min/1,73m2); kreatinin (mmol/l); kor (év)
Az eGFR eredmény számításakor figyelembe kell venni, hogy a fent említett 4v MDRD-186-os formulát a klasszikus kinetikus Jaffe-féle kreatinin módszerre dolgozták ki. Ezek a hagyományos Jaffé kreatinin módszerek az ún. pszeudo-kromogének jelenléte miatt a valósnál magasabb Scr értékeket mérnek. Az izotóp-dilúciós-tömegspektrográfiás (ID-MS) "gold standard" kreatinin módszerekkel meghatározott, pontosabb Scr értékeket közelítik ma már az enzimatikus és kompenzált kinetikus Jaffé módszerek, melyek azonban kb. 24-26 umol/L-rel alacsonyabb Scr koncentrációt adnak, mint a hagyományos kinetikus Jaffé módszerek.
Ebből adódóan, az ismert és elterjedt (ma már zseb-kalkulátorokon és interneten is rendelkezésre álló) GFR számítási képletekben az újabb, a referencia módszerrel ugyan jobban korreláló, de alacsonyabb Scr értékek nem használhatóak, mert a GFR-t fölébecsülnék. Ezért 2006-tól felnőttekre a módosított 4v MDRD ("175-ös") formula javasolt, amennyiben a laboratórium az ID-MS módszerre kalibrált és azzal jobban korreláló (pl. enzimatikus vagy kompenzált kinetikus Jaffé) kreatinin módszert használja (5-8).
A 4v MDRD ID-MS referencia eljárásra visszavezethető Scr módszerre vonatkozó számítási képlete az ún. "175-ös MDRD formula":
GFR=175x(Scrx0,0113)-1.154x(kor)-0.203x0,742 ha nő (x1,21 ha fekete rassz) ahol: GFR (ml/min/1,73m2); kreatinin (mmol/l); kor (év)
A számítási képletek megtalálhatók az alábbi web oldalakon www.mldt.hu és www.nephrologia.hu www.nkdep.nih.gov/professionals/gfr_calculators/index.htm
Mikor javasolt az eGFR vizsgálata?
Ismert vesebetegség követésére, vagy vesebetegségre utaló tünet észlelésekor. Szűrővizsgálatként (vesebajra utaló jel hiányában is) az alábbi betegekben:
1. Diabetes mellitus
2. Hypertonia
3. Atherosclerosis (coronaria, agyi, alsóvégtagi)
4. Szívelégtelenség (NYHA III-IV)
5. Anaemia (ismeretlen okú)
6. Urológiai betegség (prostata hyperplasia, egyéb húgyúti obstructio, műtét)
7. Terhelő családi anamnézis (pl. polycystas vesebetegség)
8. Potenciálisan vesekárosító vagy döntően vesén kiválasztódó szer alkalmazásakor (pl. kontrasztanyag, cyclosporin, metformin, fibratok, ACEI/ARB, NSAID, kombinált fájdalomcsillapítók)
A laboratóriumok feladatai az eGFR bevezetése kapcsán (9)
- A laboratórium feladata az eGFR számítása, melyhez a 4vMDRD formula kreatinin módszerfüggő változata ajánlott.
- Klasszikus, ID-MS referencia eljárásra nem visszavezethető, kinetikus Jaffe kreatinin módszer esetén a 4vMDRD-186 formulát,
- az újabb, ID-MS referencia eljárásra visszavezethető kreatinin (pl. enzimatikus, kompenzált Jaffé) módszer esetén a módosított 4-v MDRD-175 formulát kell használni.
- A hazai orvosi laboratóriumok számára javasolt az ID-MS-re kalibrált kreatinin módszer és az ennek megfelelő 4-v MDRD-175 formula alkalmazása. A Scr módszer visszavezethetőségének igazolása a gyártó feladata (pl. kalibrálási bizonyítvány bemutatásával).
A zseb-kalkulátorokon vagy interneten is rendelkezésre álló GFR számítási képletekben (pl. Cockroft-Gault, vagy 4v MDRD-186 formulák) az ID-MS-re visszavezethető kreatinin értékek nem alkalmazhatók! Javasoljuk, hogy erre a laboratóriumok hívják fel a velük kapcsolatban álló klinikusok figyelmét.
- A laboratóriumoknak törekedni kell a Scr eredmények torzításának csökkentésére és reprodukálhatóságának javítására a laboratóriumok között és azon belül. Az eGFR pontos becslése érdekében max. megengedett analitikai hiba minden Scr koncentráció tartományban: reprodukálhatóság (CV) <8%, és torzítás (bias, ID-MS-hez képest) <5%.
- Minden laboratóriumnak, saját módszere ismeretében, validálnia kell az alkalmazott eGFR képletet.
(A kreatinin módszerek ID-MS módszerrel való korrelációját, ill. az eGFR erre való átszámítását a UK NEQAS brit laboratóriumi összehasonlító tanulmányok alapján közölte (5). A UK NEQAS általjavasolt korrekció a standard ID-MS módszerre csak akkor megbízható, ha a laboratórium szigorúan követi a gyártó leírását!)
- Az eGFR meghatározás külső minőségellenőrzési programban való részvétele, és a hazai laborok teljesítményének mérése és összehasonlítása kívánatos.
A laboratóriumok feladatai az eGFR eredmények közlése kapcsán (9)
- A Scr értékét egész számra kerekítve (tizedesjegy nélkül) umol/L-ben kell megadni a laboratóriumi leleten a beteg nemének megfelelő referencia tartománnyal együtt.
- Az eGFR-t a laboratórium a kérőlapon szereplő nem és életkor ismeretében - nem fekete rasszt feltételezve - egész számként, ml/perc/1,73 m2 egységben adja meg. Az egyenlet már a testfelszínre korrigált GFR-t adja meg, nem szükséges normálni.
- MDRD formulák nem használhatóak 18 éves kor alatt.
- A testhossz ismeretében a gyermek nefrológusoknakjavasolható a Schwartz képlet három újkorfüggő változata a kreatinin módszer figyelembe vételével, de gyermekek GFR számítása a laboratóriumnak nem ajánlott (10).
- A rasszra történő átszámítás módja a leleten megjegyzésben adható meg. Fekete rassz esetén, a nagyobb izomtömeg miatt, a laboratórium által megadott eGFR értéket 1,21-gyel kell szorozni. Mivel hazánkban ez ritkán szükséges, javasolt, hogy a fenti korrekciót a rassz ismeretében a klinikus végezze el.
- 4v MDRD formulával számított eGFR esetén számszerű eredményközlés csak60ml/perc/1.73m2 alatt megbízható és javasolt. Amennyiben az eGFR értéke nagyobb, mint 60 ml/perc/1,73m2, a számszerű érték helyett a leleten automatikusan az eGFR >60 ml/perc/1,73m2 megjelölés ajánlott.
- Az MDRD képletet ugyanis kizárólag vesebetegek vizsgálata alapján határozták meg. Normál vagy enyhén csökkent GFR esetén, azaz 60 és 90 ml/perc/1.73m2 tartományban az MDRD képlet nem validált, és az eGFR eredmények nagy bizonytalanságot mutathatnak. (Például, az eGFR 60ml/perc értéknél -9%-tól -13,5%-ig torzít a kreatinin kalibrációtól, beteg nemétől, korától, rassztól, függően [11]. 60-90 ml/perc tartományban ez a torzítás még megfelelő kreatinin kalibráció esetén is elérheti a 30%-ot [12,13].)
- Numerikus eredmény a 60 és 90 ml/perc/1.73m2 tartományban ezért csak a laboratórium és a klinikus (nephrológus, belgyógyász) közötti párbeszéd alapján, a klinikus külön kérésére adható meg és interpretálható. E tartományban csak IDMS-re visszavezethető kalibráció esetén javasolt az eGFR számszerű értékét megadni és interpretálni. (ld.: www.nkdep.nih.gov/labprofessionals/ commutabilitystudy.htm).
- Ilyen esetekben fel kell hívni a klinikus figyelmét - pl. körlevél, továbbképzés, személyes konzultáció, leleten feltüntetett megjegyzés révén -, hogy az eGFR 60-90ml/perc/1,73m2 értéke önmagában még nem biztos jele a CKD-nak, amennyiben nincs más erre utaló klinikai tünet vagy diagnosztikai jel. A vesekárosodás lehetőségét ilyenkor egyéb tesztekkel (proteinuria,cystatin C, GFR mérés egyéb-pl. izotópos vagy kreatinin clearance-módszerekkel, stb.) szükséges vizsgálni.
- A GFR 90 ml/perc/1,73 m2-t meghaladó értéke esetén numerikus eredmény kiadását a fent ajánlott képletekkel semmilyen körülmények között nem javasoljuk; számszerű érték helyett a leleten az eGFR >90 ml/perc/1,73m2 megjelölés ajánlott.
-GFR >90 ml/perc/1,73 m2 esetén a vizelet fehérjéinek ultraszenzitív meghatározása nyújtja a legjobb eredményt a tünetmentes CKD felismerésére.
- Betegek monitorozása esetén - a Scr meghatározás eltérő módszerei miatt - a vizsgálatot és így az eGFR meghatározást is célszerű mindig ugyanabban a laboratóriumban végeztetni.
- A laboratórium felelőssége, hogy a klinikus kollegákat írásban (pl. körlevél, tájékoztató, internet) tájékoztassa az eGFR számítás módjáról és a Scr módszerfüggőségéből adódó potenciális hibaforrásairól, valamint az eGFR alkalmazhatóságának korlátairól és az ezzel kapcsolatos további teendőkről. Ehhez nyújt segítséget az MLDT-MANET-MDT orvosoknak szóló hivatalos tájékoztató kiadványa is (www.mldt.hu és www.nephrologia.hu).
A meghatározás pontatlansága miatt mikor nem javasolt az eGFR alkalmazása?
1. Akut veseelégtelenség.
Teendő: gyanú esetén sürgős nephrológiai beutalás.
2. Hypervolaemiás, oedemas állapotok (pl. szívelégtelenség, nephrosis, terhesség): alacsony Scr miatt félrevezetően magas eGFR.
Teendő: oedema megszüntetése után Scr ismétlése. Terhességben a Scr felső határa 70 u.mol/l.
3. Hypovolaemias állapotok (pl. szomjazás, dehydráció): magas Scr miatt félrevezetően alacsony eGFR. Teendő: Scr ismétlése rehidrálást követően.
4. Izomvesztéssel járó állapotok (pl. amputáció, súlyos alultápláltság, paraparesis): alacsony Scr miatt félrevezetően magas eGFR.
Teendő: clearance vizsgálatok vagy cystatin C meghatározása.
Hogyan értékelendő az eGFR eredménye, mik a teendők az egyes esetekben?
eGFR >60 ml/perc/1,73 m2 : jelentős vesefunkció romlás nincs
Teendő: vesekárosodásra utaló egyéb jel (proteinuria, haematuria, rendellenes vese ultrahang) keresése; amennyiben ez nem észlelhető, az eGFR ismétlése évente.
CKD gyanúja esetén nephrológiai konzílium kérése, a vesefunkció pontosabb megítélésére és követésére clearance vizsgálat vagy cystatin C meghatározás végzése.
eGFR 30-59 ml/perc/1,73 m2 : mérsékelt veseelégtelenség CKD biztos, egyéb jel hiányában is, ha 3 hónapon túl is fennáll. A kardiovascularis betegségek önálló, súlyos rizikótényezője.
Teendő: nephrológiai konzílium kérése, javaslata alapján a CKD progressziójának csökkentése, szövődményeinek kezelése, az eGFR kontrollja legalább félévente.
eGFR 15-29 ml/perc/1,73 m2 : súlyos veseelégtelenség
A végstádiumú veseelégtelenségbe való átmenet nem megállítható.
Teendő: a beteg rendszeres nephrológiai gondozásra szorul, a korábbi feladatokon túl fel kell készülni a vesepótló kezelésre is, legalább 3 havonta szükséges eGFR kontroll.
eGFR <15 ml/perc/1,73 m2: végstádiumú veseelégtelenség Vesepótló kezelés elkezdése mérlegelendő.
Teendő: szoros, 1-3 havonta történő nephrológiai gondozás, ennek során eGFR meghatározás is. Vesepótló kezelés elkezdése klinikai tünetektől függően diabetes nephropathiában általában 10-15 ml/perc/1,73m2, egyéb betegekben 8-12 ml/perc/1,73m2 esetén indokolt. Dializált betegben az eGFR nem alkalmas a maradék vesefunkció megítélésére.
Irodalom:
1. Javaslat a vesefunkció laboratóriumi vizsgálatára felnőttekben. Nephrológiai Útmutató Szerk: Túri S., Mátyus J., Kiss I., Kárpáti I. Medition 2005; 5-9.
2. Lamb E J: Challenging time in renal medicine. Ann. Clin. Biochem 2005; 42:318-320.
3. Lamb E J, Wood J et al: Susceptibility of eGFR to variations in creatinine methodology. Ann. Clin. Biochem 2005; 42: 11-18.
4. Froissart M.C: The New Mayo Clinic Equation for eGFR. Ann. Internal Med.2005; 142:679.
5. UK NEQAS javaslatai az eGFR Scr módszer-függő számítására: www.ukneqas.org.uk
6. Burden R,Tomson C: Identification, management and referral of adults with chronic kidney disease: concise guidline. Clin.Med. 2005; 5: 635-42. www.renal.org/CKDguide/full/UKCKDfull.pdf
7. National Kidney Foundation, USA K/DOQI útmutatója: Centers for Medicare and Medical services (CMS~OEP): CMS-2728, ESRD program, 2005. május
8. National Kidney Disease Education Program, Suggestions for Laboratories www.nkdep.nih.gov/resources /laboratory_reporting.htm
9. Myers GL, Miller WG, Coresh J, Fleming J. et al. for the National Kidney Disease Education Program Laboratory Working Group. Recommendations for Improving Serum Creatinine Measurement: A Report from the Laboratory Working Group of the National Kidney Disease Education Program. Clin Chem 2006; 52(1): 5-18.
10. Schwartz képlet és eGFR kalkulátor (NB: ID-MS-re visszavezethető kreatininre nem validált!): http://www.nkdep.nih.gov/professionals/gfr_calculators/gfr_children.htm
11. K. Murthy, L.A. Stevens et al.:, Variation in the serum creatinin calibration. Kidney International 2005;68:1884-1887.
12. P. Delanaye, J.M. Krzesinski.: The New Mayo Clinic Equation for Estimating Glomerular Filtration Rate. Ann. Internal Medicine 2005;142(8): 679-680.
13. Oláh A, Fodor B, Horváth A: A szérum kreatinin meghatározás kihívásai és korlátai. Orvosi Hetilap 149/7 (2008) 317-323. (Amennyiben időközben újbizonyítékokjelennek meg a szakirodalomban, az útmutató frissítését a kiadók biztosítják).
A szakmai irányelv érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai irányelve
A számított GFR (eGFR) bevezetéséről útmutató a háziorvosok és szakrendelések (diabetes, hypertonia, kardiológia, urológia) számára
Készítette: a Magyar Laboratóriumi Diagnosztikai Társaság, a Magyar Nephrológiai Társaság és a Magyar Diabetes Társaság
Jelen útmutató célja, hogy a glomerulus filtrációs ráta (GFR) számítása (eGFR), és alkalmazása épüljön be az alap és szakellátásba. Az idült vesebetegség (CKD) gyakori, legtöbbször progresszív, korai érelmeszesedéshez és halálozáshoz vezető betegség, melynek lefolyásában a GFR alapján 5 stádiumot különböztetünk meg (1. táblázat). A szérum kreatinin (Scr) nem elég érzékeny jelzője a GFR csökkenésének. A CKD 3-5. stádiumában az eGFR pontosabban becsüli a valódi GFR-t, mint a vizeletgyűjtéssel mért kreatinin clearance. CKD rizikója esetén az eGFR meghatározása, ennek eredményétől függően nephrológiai konzílium ill. gondozás szükséges.
1. táblázat: Az idült vesebetegség stádiumai
| Stádiu m | Jellemző | GFR ml/perc/1,73m2 | Főbb tünetek | Gyakorisá g (%) | Teendők |
| 1. | vesebetegség norm. v. magas GFR-rel | >90 | alap-betegség | 3,3 | diagnózis, kezelés |
| 2. | vesebetegség csökkent GFR-rel | 60-89 | hypertonia CV rizikót | 3,0 | progresszió és CV rizikó csökkentés |
| 3. | mérsékelt veseelégtelenség | 30-59 | anaemia osteodystr. | 4,3 | fentiek + szövőd-mények kezelése |
| 4. | súlyos veseelégtelenség | 15-29 | hyperK oedema | 0,2 | fentiek + felkészülés vesepótló kezelésre |
| 5. | végstádiumú veseelégtelenség | <15 v. dialízis | malnutritio uraemia | 0,1 | transzplantáció dialízis |
Háttér
A vesefunkció legjobb jelzője a GFR, melynek meghatározása a mindennapi gyakorlatban körülményes (izotóp clearance vizsgálatok) és pontatlan (kreatinin clearance 24 órás vizeletgyűjtésből). Ezért 2005-ben a MANET az MLDT-vel közösen kidolgozott egy ajánlást, mely javasolta a GFR képletekkel becsült számítását, és ennek rutinszerű közlését a laboratóriumi leleten. 2006-tól amerikai és brit útmutatók is egyértelműen ajánlják a MDRD (Modification of Diet in Renal Disease) egyenlettel megadott eGFR alkalmazását. A számítás orvosi diagnosztikai laboratóriumokban történő végzése és az eredmény laborleleten való automatikus közlése azért is célszerű, mert a Scr értéke függ az alkalmazott mérőmódszertől, így újlaboratóriumi módszerekesetén módosított képlet alkalmazása szükséges.
Miért szükséges a GFR ismerete?
A CKD a lakosság több mint 10 %-át érinti, és a betegek többségében a vesefunkció is beszűkült. Ennek oka az atherogenetikus nephropathiák (leginkább diabetes mellitusban, hypertoniában, érbetegségben jelentkező vesekárosodás) számának drámai megemelkedése. A klasszikus vesetünetek hiánya miatt a betegség későn, sokszor csaka végstádiumban kerül felismerésre. Ugyanakkor már az enyhe - mérsékelt veseelégtelenség is jelentősen fokozza az atherosclerosis kockázatát, szövődményekhez, korai halálozáshoz vezet. A GFR csökkenés kimutatásával és az időben elkezdett nephrológiai gondozással lehetőség van a vesefunkció romlás megállítására vagy progressziójának csökkentésére, a szövődmények kezelésére, a vesepótló kezelés időben történő elkezdésére, módjának megválasztására. Mindezektől a betegek morbiditásának és mortalitásának csökkenése várható.
Hogyan történik az eGFR laboratóriumi kérése és megadása?
1. Felnőttekben (18 év felett) minden Scr vizsgálat kérésekora laboratóriumok automatikusan megadják az eGFR-t, a Scr módszertől függő képlet alapján. A számítási képlet megtalálható: www.mldt.hu és www.nephrologia.hu oldalakon.
Klasszikus kinetikus Jaffe kreatinin módszerhez a 4-változós MDRD-186 formulát, az új ú.n. IDMS referencia eljárásra kalibrált kreatinin módszerek (pl. enzimatikus, kompenzált Jaffé) esetén a módosított 4v MDRD-175 formulát használják. A zseb-kalkulátorokon is rendelkezésre álló GFR számítási képletekben (pl. a régi Cockroft-Gault formula) az újabb módszerekkel mért kreatinin értékek nem alkalmazhatók.
Fentiek alapján klinikusoknak nem javasoljuk a zseb- vagy egyéb internetes eGFR kalkulátorok alkalmazását, amennyiben nem ismerik a Scr mérés pontos módszerének és kalibrátorának megfelelő helyes képletet.
2. Az eGFR-t a laboratórium a kérőlapon szereplő nem és életkor ismeretében, nem fekete rasszt feltételezve, egész számként, ml/perc/1,73 m2 egységben adja meg.
Fekete rassz esetén a laboratórium által megadott értéket 1,21-gyel szorozni kell a nagyobb izomtömeg miatt.
3. 4v MDRD formulával számított eGFR esetén számszerű eredményközlés 60 ml/perc/1.73m2 alatt megbízható és javasolt. Amennyiben az eGFR értéke nagyobb, mint 60 ml/perc/1,73m2, a számszerű érték helyett a leleten automatikusan az eGFR 60 ml/perc/1,73m2 megjelölés ajánlott.
Az MDRD képletet ugyanis kizárólag vesebetegek vizsgálata alapján határozták meg. Normális vagy enyhén csökkent GFR esetén, azaz 60 és 90 ml/perc/1.73m2 tartományban, az MDRD képlet nem validált, és az eGFR eredmények nagy bizonytalanságot mutathatnak. (Például, az eGFR 60ml/perc értéknél -9%-tól -13,5%-ig torzít a kreatinin kalibrációtól,
beteg nemétől, korától, rassztól, függően [4]. 60-90 ml/perc tartományban ez a torzítás még megfelelő kreatinin kalibráció esetén is elérheti a 30 %-ot [5].)
4. Numerikus eredmény a 60 és 90 ml/perc/1.73m2 tartományban ezért csaka laboratórium és a klinikus (nephrológus, belgyógyász) közötti párbeszéd alapján, a klinikus külön kérésére adható meg és interpretálható. Ilyen esetekben fel kell hívni a figyelmet, hogy az eGFR 60-90ml/perc/1,73m2 értéke önmagában még nem biztos jele a CKD-nak, amennyiben nincs más erre utaló klinikai tünet vagy diagnosztikai jel. A vesekárosodás lehetőségét ilyenkor egyéb tesztekkel (proteinuria, cystatin C, GFR mérés egyéb - pl. izotópos vagy kreatinin clearance - módszerekkel, stb.) szükséges vizsgálni.
5. A Scr meghatározás eltérő módszerei miatt a vizsgálatot és így az eGFR meghatározást - különösen a vesefunkció rendszeres monitorozása esetén - célszerű mindig ugyanabban a laboratóriumban végeztetni.
Mikor javasolt az eGFR vizsgálata?
Ismert vesebetegség követésére, vagy vesebetegségre utaló tünet észlelésekor. Szűrővizsgálatként (vesebajra utaló jel hiányában is) az alábbi betegekben:
1. Diabetes mellitus
2. Hypertonia
3. Atherosclerosis (coronaria, agyi, alsóvégtagi)
4. Szívelégtelenség (NYHA III-IV)
5. Anaemia (ismeretlen okú)
6. Urológiai betegség (prostata hyperplasia, egyéb húgyúti obstructio, műtét)
7. Terhelő családi anamnézis (pl. polycystas vesebetegség)
8. Potenciálisan vesekárosító vagy döntően vesén kiválasztódó szer alkalmazásakor (pl. kontrasztanyag, cyclosporin, metformin, fibratok, ACEI/ARB, NSAID, kombinált fájdalomcsillapítók)
Mikor nem javasolt pontatlansága miatt az eGFR alkalmazása?
1. akut veseelégtelenség. Teendő: gyanú esetén sürgős nephrológiai beutalás.
2. hypervolaemiás,oedemas állapotok (pl. szívelégtelenség, nephrosis, terhesség): alacsony Scr miatt fals magas eGFR. Teendő: oedema megszüntetése után Scr ismétlése. Terhességben a Scr felső határa 70 umol/l.
3. hypovolaemias állapotok (pl. szomjazás vérvétel előtt): magas Scr miatt fals alacsony eGFR. Teendő: Scr ismétlése rehidrálást követően.
4. izomvesztéssel járó állapotok (pl. amputáció, súlyos alultápláltság, paraparesis): alacsony Scr miatt fals magas eGFR. Teendő: clearance vizsgálatok vagy cystatin C meghatározása.
Hogyan értékelendő az eGFR eredménye, mik a teendők az egyes esetekben?
eGFR >60 ml/perc/1,73 m2: jelentős vesefunkció romlás nincs
Teendő: vesekárosodásra utaló egyéb jel (proteinuria, haematuria, rendellenes vese ultrahang lelet) keresése; amennyiben ez nem észlelhető, az eGFR ismétlése évente.
CKD gyanúja esetén nephrológiai konzílium kérése, a vesefunkció pontosabb megítélésére és követésére clearance vizsgálat vagy cystatin C meghatározás végzése.
eGFR 30-59 ml/perc/1,73 m2 : mérsékelt veseelégtelenség CKD biztos, egyéb jel hiányában is, ha 3 hónapon túl is fennáll. A kardiovascularis betegségek önálló, súlyos rizikótényezője.
Teendő: nephrológiai konzílium kérése, javaslata alapján a CKD progressziójának csökkentése, szövődményeinek kezelése, az eGFR kontrollja legalább félévente.
eGFR 15-29 ml/perc/1,73 m2 : súlyos veseelégtelenség
A végstádiumú veseelégtelenségbe való átmenet nem megállítható.
Teendő: a beteg rendszeres nephrológiai gondozásra szorul, a korábbi feladatokon túl fel kell készülni a vesepótló kezelésre is, legalább 3 havonta szükséges eGFR kontroll.
eGFR >15 ml/perc/1,73 m2: végstádiumú veseelégtelenség Vesepótló kezelés elkezdése mérlegelendő.
Teendő: szoros, 1-3 havonta történő nephrológiai gondozás, ennek során eGFR meghatározás is. Vesepótló kezelés elkezdése klinikai tünetektől függően diabetes nephropathiában általában 10-15 ml/perc/1,73m2, egyéb betegekben 8-12 ml/perc/1,73m2 esetén indokolt. Dialízált betegben az eGFR nem alkalmas a maradék vesefunkció megítélésére.
Irodalom:
1. Javaslat a vesefunkció laboratóriumi vizsgálatára felnőttekben. Nephrológiai Útmutató Szerk: Túri S., Mátyus J., Kiss I., Kárpáti I. Medition 2005; 5-9.
2. Az angol Royal College of Physicians 2006-os ajánlása: www.renal.org/CKDguide/full/UKCKDfull.pdf
3. National Kidney Disease Education Program, Suggestions for Laboratories www.nkdep.nih.gov/resources /laboratory_reporting.htm
4. K. Murthy, L.A. Stevens etal.:, Variation in the serum creatinin calibration. Kidney International 2005;68:1884-1887.
5. P. Delanaye, J.M. Krzesinski.: The New Mayo Clinic Equation for Estimating Glomerular Filtration Rate. Ann. Internal Medicine 2005;142(8): 679-680.
(Amennyiben időközben újbizonyítékok jelennek meg a szakirodalomban az útmutató frissítését a kiadók biztosítják.) A szakmai irányelv érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai irányelve
A tuberkulózis mikrobiológiai diagnosztikájáról
Készítette: az Orvosi Mikrobiológiai Szakmai Kollégium
I. Alapvető megfontolások
1. A protokoll alkalmazási / érvényességi területe
1.1. A protokoll témája a tuberkulózis mikrobiológiai diagnosztikája a járó- és fekvőbeteg szakellátásban.
1.2. A protokoll célja az egységes hazai gyakorlat kialakítása, figyelembe véve a témában meghatározó jelentőségű nemzetközi (WHO, IUATLD, EuroTB, ECDC) és más külföldi szervezetek(CDC, FDA) ajánlásait és azérvényben lévő hazai rendelkezéseket.
1.3. A protokoll célcsoportjai (a protokollt alkalmazó ellátók köre): mikrobiológiai laboratóriumok mycobacteriológiai részlegei,önálló mycobacterologiai laboratoriumok, klinikai osztályok,szakrendelők, pulmonológiai gondozó hálózat
1.4. Ellátottak: tuberkulózis fertőzés és megbetegedés gyanúja, tuberkulózissal fertőzöttek, tuberkulózis betegségben szenvedők, tuberkulózis betegségre veszélyeztetettek.
1.5. A protokollt alkalmazó ellátók: mycobacteriológiai diagnosztikát végző mikrobiológiai laboratóriumok.
1.6. Ellátási szint: II. és III. kompetencia szintű mikrobiológiai laboratóriumok, melyek mycobacteriológiai diagnosztikát, mycobacteriológiai laboratóriumi szakellátást végeznek.
2. Definíciók
- Bakteriológiailag igazolt eset
- Bakteriológiailag nem igazolt eset
- Újonnan igazolt eset
- Korábban tuberkulózis miatt már kezelt eset
- Antituberculotikum rezisztens tuberkulózis, polyrezisztens, multi-drug rezisztens (MDR) és extensively-drug rezisztens (XDR) eset
II. Diagnosztikai eljárások
Tuberkulózis gyanúja esetén a mikrobiológiai diagnosztikai módszerek széles skálájával és korszerű technikáinak felhasználásával (direkt mikroszkópos vizsgálatok, tenyésztés, identifikálás, nukleinsav amplifikációs technikák) törekedni kell arra, hogy a fertőző ágenst a lehető legrövidívebbidőn belül igazoljuk, és a definitív diagnózist követően a rezisztencia vizsgálatok eredményét a kezelő orvossal közöljük.
Kötelező (minimálisan elvégzendő) mikrobiológiai diagnosztikai vizsgálatok és azok gyakorisága A tuberkulózis definitív diagnózisa felállításának alapfeltétele a M. tuberculosis-nak a beteg testnedveiből (köpet, pleurális folyadék, vizelet, hörgőmosó folyadék, stb) tenyésztéssel történő kimutatása, vagy a kórokozó direkt nukleinsav amplifikációs módszerekkel történő detektálása direkt mikroszkópos vizsgálattal kapott saválló pozitivitás mellett. A diagnózis felállításához minimum három, maximum öt adekvát vizsgálati mintára van szükség. A terápiában még nem részesült, vagy két hónapnál kevesebb ideig kezelt beteg első M. tuberculosis tenyészetéből a kezdeti rezisztencia vizsgálatok kötelezően elvégzendők. Ismert fertőzés fennállásakor pedig követni kell a beteg fertőzőképességét (mikroszkópos vizsgálatok), és monitorozni kell a gyógyulás folyamatát (tenyésztés és rezisztencia vizsgálatok). A kezelés 4. hónapját követően is baktériumot ürítő beteg esetén a rezisztencia vizsgálat megismétlendő. A beteg akkor tekinthető gyógyultnak, ha a kezelés alatt, illetve annak befejezése után megfelelő számú negatív tenyésztési lelettel igazolták, hogy nem ürít baktériumot.
1. Szakmai háttér
A mycobacteriológiai laboratóriumok alapvető szerepet játszanak a tuberkulózis elleni hatékony védekezésben, hiszen a definitív klinikai diagnózis felállításához nélkülözhetetlen feltétel a kórokozó baktérium izolálása és identifikálása. A mycobacteriológiai vizsgálatok elengedhetetlen információkat szolgáltatnak az antituberkulotikum kezelés összetételének meghatározásához, valamint a kezelés hatásosságának monitorozásához is, részben a kórokozó kimutathatóságával, részben az izolálást követő rezisztencia vizsgálatok eredményeivel. Magyarországon a bakteriológiailag igazolt TBC-s betegek aránya évek óta mindössze 46 % körüli értéken van. Ennek okai között szerepet játszik, hogy az ország legtöbb TBC laboratóriumában jelenleg alkalmazott bakteriológiai módszerek érzékenysége nem megfelelő illetve, hogy a betegekegy jelentős százalékában (bakteriológiailag negatív esetek egyharmadában) egyáltalán nem készül tenyésztés, illetve az adatközlés nem megfelelő. További gond, hogy a tenyésztés és az ebből végzett rezisztencia meghatározás átfutási ideje klinikai szempontból elfogadhatatlanul hosszú. Így a terápia rezisztens betegek időbeni felismerése, illetve érzékeny mycobacterium okozta fertőzés esetében a kezelés 8. hetének végén szükséges gyógyszer kombináció szűkítés, valamint a kezelés hatékonyságának megfelelő monitorozása megoldatlan. Ezt a megállapítást támasztják alá a gyógyszeredmények, melyek szerint a gyógyult betegek aránya nem éri el a 60 %-t, a nemzetközi 80 %-os elvárásokkal szemben.
2. Bakteriológiai vizsgálatok
2.1 Mintavétel, mintatovábbítás, tárolás (1-3)
A tuberkulózis és az egyéb mycobacterialis fertőzések megbízható, pontos és főleg gyors mikrobiológiai diagnosztikájának alapja a megfelelő mennyiségű, minőségű, és kellő számú minta továbbítása a laboratóriumba. Az inadekvát mintavételből fakadó problémákat a legmodernebb molekuláris biológia módszerek sem képesek kiküszöbölni. Nagyon fontos, hogy a minták késedelem nélkül megérkezzenek a laboratóriumba, mivel egyes vizsgálatok átfutási idejét (pl. mikroszkópos vizsgálat és direkt nukleinsav amplifikáció eredménye 24 órán belül) és minőségét (tenyészetek befertőződése) nagyban befolyásolhatja, ha a vizsgálati anyagot a laboratórium mintavételt követő 24-48 órán belül nem kapja kézhez.
Mycobacteriológiai vizsgálatra alkalmatlan a nyálköpet, a gyűjtött köpet, a tamponnal vett garat- és sebváladék. A reggeli, ébredés utáni köpet begyűjtésére kell törekedni. A felköhögött köpetet a beteg ürítse az erre a célra rendszeresített steril edénybe. A legmegfelelőbb a 30-50 ml térfogatú, steril, milliliteres beosztású, kónuszos aljú, csavaros fedelű, műanyag centrifugacső. Optimális esetben a köpet 5-10 ml térfogatú. Ügyelni kell a mintavételi csövek megfelelő címkézésére az azonosíthatóság érdekében. A mintavételi edények 1-2 órán át szobahőmérsékleten, 24-72 órán át 2-8°C-n hűtőben tárolandók. Nagyobb nyári meleg esetén érdemes azonnal hűtőszekrényben tárolni a mintákat. Amennyiben a laboratórium nem házon belül van, akkor a centrifuga csöveket jól zárható fémtartályokba, majd ezeket papírdobozba csomagolva a megfelelő kísérő papírokkal ellátva kell továbbítani a laboratórium részére. Egyebekben 121/ 2000 Postaügyi értesítő 32. "Fertőző anyagok kezelése" című utasítása a mérvadó. A kísérőlap feltétlenül tartalmazza a beteg adatai mellett, hogy a kért vizsgálat célja a diagnózis felállítása/megerősítése, vagy a kezelés eredményességének ellenőrzése. Fel kell tüntetni azt is, hogy korábban tuberkulózis miatt nem kezelt, vagy tuberkulózis miatt már korábban is kezelt betegtől származik-e a vizsgálatra küldött minta. Ha ismert, fel kell sorolni azokat az antituberkulotikumokat (legfőképpen a rifampicin vonatkozásában) is, amelyekre a beteg izolátuma a korábbi vizsgálatok során rezisztens volt. Utóbbi információk kiemelten fontosak a rezisztencia vizsgálatok indítása és értékelése szempontjából a laboratórium és a klinikus számára is. Amennyiben a beteg alkalmatlan értékelhető köpet adására úgy meg lehet kísérelni hypertoniás (5-10%) sóoldattal való inhaláltatást követően ún. indukált köpet gyűjtését, illetve ébredés utáni, még az ágyban levett éhgyomori gyomorbennék aspirátum (és nem mosás) nyerését. Négy órát meghaladó tárolás esetén a gyomorsav mycobacteriumokat is elölő hatását 100 mg steril szódabikarbona segítségével semlegesíteni kell.
A köpeten kívül a leggyakrabban beküldésre került minták a következők: bronchusmosó folyadék, bronchoalveoláris lavage, pleurális, pericardiális vagy ascites folyadék (steril edényben, utóbbi három esetében 0,2 mg/ml steril heparin hozzáadásával vagy közvetlenül folyékonytáptalajba oltva), vizelet (> 40 ml, reggeli középsugár vagy katéteres, nem gyűjtött, nem katéter zsákból, kellő genitális toalettet követően), széklet (> 1 g), liquor (> 2-5 ml), seb vagy tályogváladék (steril fecskendőbe felszívva amennyit csak lehetséges), menstruációs folyadék, biopsziás minta (nem formalinba ágyazott, csak fiziológiás sóoldatban). A ritkábban előforduló minták esetében a mintavétel előtt érdemes a laboratórium tanácsát kérni a mintavételi, tárolási és szállítási előírásokat illetően.
A mikroszkópos vizsgálatokat minden alkalommal három különböző alkalommal levett mintából, a tenyésztéseket öt különböző alkalommal levett mintából kell végezni.
2.2 A minta előkezelése: homogenizálás, dekontaminálás (1-4,6)
A minta előkezelése, homogenizálása, dekontaminálása a fertőzés veszély elkerülése érdekében laminális box-ban (minimálisan BSL2) kell hogy történjen.
A mycobacteriumok osztódási ideje meglehetősen hosszú (16-20 óra) ezért a nem steril testtájékokról származó minták (pl. köpet, vizelet, széklet) nem mycobacteriális, ún. kontamináns baktériumai számottevően gyorsabb növekedési ütemüknek köszönhetően könnyen túlnőhetik az adott klinikai minta mycobacteriumait. Az álnegatív eredmények elkerülése céljából a mycobacteriológiai laboratóriumok ezeket a klinikai mintákat ún. dekontaminációs eljárásnak vetik alá. A dekontamináció steril minták esetében (pl. liquor, pleurális folyadék) nem szükséges. A dekontaminálás során alkalmazott vegyszerek a kontamináns baktériumok vagy gombák elölésén kívül segítenek a gyakran erősen purulens minták homogenizálásban, valamint a centrifugálási lépések közbeiktatásával azok koncentrálásában is. A dekontaminálás hatékonyságát befolyásolja az alkalmazott reagens toxicitása, expozíciós ideje, és a centrifugálási lépés során keletkező hő károsító hatása. Mindezektől függően még a legenyhébbnek számító dekontaminálási módszer a N-Acetyl-L-Cystein-NaOH (NALC-NaOH) is elpusztítja a minta mycobacterium tartalmának legalább 33%-át, míg erősebb reagensek (pl. klórhexidin digluconikum) alkalmazása esetén ez az érték könnyen 70%-ra emelkedhet, amely jelentősen csökkentheti a tenyésztés érzékenységét. A táptalaj beszennyeződés mértékéből következtetni lehet az alkalmazott eljárás helyességére. Így szilárd táptalajon a 3%-nál alacsonyabb, ill. folyékony táptalajt használva az 5-8 %-nál alacsonyabb kontaminációs ráta esetén a dekontaminálás túl erős, míg az ezen értékek feletti arány túl gyenge dekontaminálásra utal.
Többféle előkezelési technika ismert. A hazai TBC tenyésztéssel foglalkozó laboratóriumok 1976 óta egységesen a klórhexidinum-digluconatos eljárást alkalmazzák, ami a maga idejében egyszerűsége, olcsósága miatt megfelelő választás volt. A módszer nem túl munkaigényes, egyszerűen kivitelezhető, nem kell a vizsgálati anyagot centrifugálni, semlegesíteni,ezért tömeges minta feldolgozására is kiválóan alkalmas. Számításba kell azonban venni, hogy közel 30 évvel ezelőtt a laboratóriumok a mai mintaszámnak több mint hússzorosát dolgozták fel. A módszer hátránya, hogy jobban károsítja a mycobacteriumokat, minta NALC-NaOH technika, és csakszilárd alapú tenyésztéshez alkalmazható. A két eljárás összehasonlító vizsgálata szerint a LJ-en történő tenyésztés pozitivitásának aránya közel duplájára emelkedett a NALC-NaOH előkezelés mellett. A klórhexidines módszer folyékony táptalajon történő tenyésztésre alkalmatlan (roncsolja a táptalajt), így napjainkban az újabb folyékony alapú táptalajok hazai elterjesztésének gátjává vált. Ezen okok miatt a CDC, valamint a jelentősebb nyugat-európai mycobacteriológiai referencia laboratóriumok is a NALC-NaOH előkezelést ajánlják. A folyékony tenyésztő rendszerek rutinszerű alkalmazásának feltétele az adekvat előkezelési technika használata, ezért elengedhetetlen ennek az újmódszernek a fokozatos hazai bevezetése.
Bizonyos betegcsoportok megkülönböztetett figyelmet igényelhetnek a dekontaminálás vonatkozásában. Így például a cisztikus fibrózisban szenvedő betegek légúti mintájából egyre gyakrabban kerül izolálásra klinikai szignifikanciával (pl. transzplantálhatóság kérdése) bíró Nem Tuberculosist okozó Mycobacterium (NTM). Azonban a betegek 80%-ban a minta P. aeruginosa-t is tartalmaz, amely könnyedén túlnövi a tenyésztés során a mintában jelenlévő NTM-ot, és álnegatív tenyésztéshez vezet még a rutinszerűen alkalmazott dekontaminálási módszerek mellett is. Ezért az ilyen betegekesetében speciális 5%oxálsavas kezeléssel kiegészített dekontaminálás javasolt.
2.3 Direkt vizsgálatok
2.3.1 Mikroszkópos vizsgálatok (1-3,6, 9-12)
A direkt mikroszkópos vizsgálat a mycobacteriológiai vizsgálatok legolcsóbb, legegyszerűbben kivitelezhető és leggyorsabb módszere. Egyes laboratóriumokban a minta a dekontaminálás elhagyásával, közvetlenül kerül mikroszkópos vizsgálatra, az így készült keneteket direkt keneteknek, az így végzett vizsgálatotokat direkt mikroszkópos vizsgálatnak nevezzük. A mikroszkópos vizsgálat leggyakoribb módja azonban hogy a minták dekontaminálásra kerülnek és a mikroszkópos kenet nem közvetlenül a klinikai mintából, hanem a minta előkezelt, centrifugált üledékéből készül. Magasabb érzékenysége miatt a direkt módszerrel szemben ez a módszer választandó, azonban tudni kell, hogy a dekontaminálás során felhasznált steril desztillált víz tartalmazhat elölt saválló környezeti baktériumokat, amelyek fals pozitívvá tehetik a kenetet, ezért ilyenkor szűrt, steril desztillált víz használata ajánlott. A kenetkészítést követően a festés a Ziehl-Neelsen (ZN), Kinyoun-féle karbol fukszin alapú vagy auramin alapú fluoreszans eljárásokkal történhet. A Kinyoun-féle festés alacsony érzékenysége miatt nem ajánlott módszer. A ZN festést követően a mycobacteriumok vörös pálcákként észlelhetőek a kék, vagy zöld háttér kontrasztja mellett. Az auramin festést követően a mycobacteriumok sárgás-zölden fluoreszkálnak fekete háttér mellett. A fluoreszans mikroszkópia elsősorban azon laboratóriumok számára ajánlható, amelyek nagy esetszámmal dolgoznak. A sötét háttér mellett ugyanis a mycobacteriumok könnyebben észlelhetők, a fluoreszcens mikroszkóp látótere nagyobb, mindezek miatt egy-egy kenet áttekintése gyorsabb. Ez a módszer azonban még a ZN vizsgálathoz képest is nagyobb gyakorlatot igényel, a kevésbé tapasztalt vizsgáló gyakran jelez vissza álpozitív eredményt, a fluoreszcein festékrögöket nézve baktériumnak. Emellett, a fluoreszcens festés a karbol fukszinhoz képest sokkal jobb hatásfokkal képes megfesteni az antituberkulotikum kezelés miatt már károsodott saválló baktériumokat, így a mikroszkópos pozitivitás a fluoreszcens festés mellett hosszabb ideig detektálható egy kezelt beteg esetében, amely nem feltétlenül jelenti azt, hogy a kezelés inadekvát vagy a beteg még mindig fertőző. További eltérés a ZN festéshez képest, hogy a mintában esetlegesen jelenlévő vér álpozitivitást okozó fluoresceinciát eredményezhet. Mindezek miatt minden újonnan felismerésre került beteg esetében a fluoreszcens mikroszkópos pozitivitást ZN vizsgálattal meg kell erősíteni.
2.2.1/a Módszer érzékenysége, specificitása: A mikroszkópos vizsgálat legnagyobb hátránya, hogy nem kellően érzékeny és a negatív eredmény kiadásához minimum 100-300 látótér áttekintése szükséges, ami meglehetősen munkaigényes. A mikroszkópos vizsgálat érzékenysége az adott beteg populáción belül a kiterjedt tuberkulózisban szenvedő betegek hányadától, a vizsgált minta típusától (felsőlégúti vs. mélylégúti), a mintagyűjtés minőségétől, a mycobacteriumok mintán belüli számától, az alkalmazott dekontaminálási és centrifugálási módszertől (cytocentrifugálás), a centrifuga minőségétől (legalább 3000 x g) függően 50-75%. Míg a pozitív mikroszkópos eredmény a tuberkulózis preszumptív diagnózisa mellett szól, addig a negatív eredmény, az alacsony érzékenységi mutató miatt, nem zárja ki a tuberkulózis lehetőségét. Legalább 10.000 mycobacterium milliliterenkénti jelenléte szükséges ahhoz, hogy egy kenet teljes átvizsgálását követően legalább néhány saválló pálcát találjunk. A mikroszkóposan pozitív betegek tehát megkülönböztetett figyelmet igényelnek, hiszen az általuk ürített baktérium mennyiség miatt ezek a betegek a legfertőzőbbek. Éppen ezért, hogy az ilyen esetben szükséges izolációs lépések időben foganatosíthatóak legyenek, a mikroszkópos vizsgálat eredményét a laboratórium 24 órán belül vissza kell, hogy jelezze a vizsgálatkérő számára.
Nem szabad elfeledkeznünk azonban arról a tényről sem, hogy a mikroszkópia nem képes különbséget tenni élő és élettelen mycobacterium között. Így egy megfelelően kezelt és ellenőrzött beteg esetében a mikroszkópos vizsgálat negatívvá válást követő esetleges pozitivitása nem feltétlenül a klinikai állapot romlásának a jele. Ugyancsak fontos szem előtt tartani azt a tényt is, hogy a mikroszkópos vizsgálat nem tud különbséget tenni a M. tuberculosis complexés NTM-ok között. Azaz a kenet pozitivitás atípusos Mycobacterium jelenlétének eredménye is lehet, amely nem biztos, hogy klinikai fontossággal bír. Egy hazai felmérés szerint ugyan Magyarországon a mikroszkópos vizsgálat pozitivitásának hátterében az esetek több mint 90 %-ában M. tuberculosis jelenléte igazolható tenyésztéssel, de HIV fertőzött vagy egyéb immunszuprimált betegek esetében, vagy olyan földrajzi területeken, ahol bizonyos NTM előfordulási gyakorisága magas, mindig gondolni kell NTM jelenlétére is. Emellett az aerob Actinomycetaceae-k, legionellák egyes fajai is saválló pozitivitást mutathatnak. Mindezek miatt a mikroszkópos vizsgálat eredményét saválló baktérium pozitív vagy negatív megjelöléssel kell visszajelezni.
2.2.1/b Minőségbiztosítás: Pozitív és negatív kontrollt kell alkalmazni minden újfesték sarzs használatánál. Minden kenet pozitív mintát és a negatívak legalább 10%-át egy másodikvizsgálónakellenőriznie kell. Ugyancsakfigyelemmel kell kísérni a mikroszkóposan pozitív és tenyésztéssel negatív betegek arányát is. Az ilyen betegek (elsősorban az újonnan nyilvántartásba vett betegekről van szó) arányának kevesebb, mint 1%-nak kell lennie. Az ennél magasabb arány dekontaminálási, tenyésztési (táptalaj minőség, rövid inkubációs idő) hibát, nehezen tenyészthető NTM (pl. M. haemophilum, M. genavense) jelenlétét vagy laboratóriumi keresztfertőzést jelezhet.
2.3.2 Direkt nukleinsav-amplifikációs módszerek (2,6,7,12,14,15)
A direkt nukleinsav amplifikációs módszereknek (DNAM) a mycobacteriológiában való alkalmazása a lassan tenyészthető M. tuberculosis és a bizonyos speciális tenyésztési feltételeket igénylő, ezért nehezen izolálható NTM-ok direkt (közvetlenül a klinikai mintából) történő detektálásának gyors, 24 órán belüli kivitelezésének lehetőségét teremtette meg.
A módszer minden mintából történő rutinszerű alkalmazása szükségtelen. Mikroszkópos vizsgálattal pozitívnak bizonyuló mintából csak akkor javasolt a teszt elvégzése, ha olyan betegről van szó, akinél NTM kóroktani szerepe vetődik fel (pl. HIV fertőzött, transzplantált beteg, cisztikus fibrózis esetében). A tesztek érzékenysége a mikroszkóposan pozitív légúti minták esetében közel 100 %. Mikroszkóposan negatív minták esetében csak akkor végezzünk ilyen vizsgálatot, ha a tuberkulózis diagnózisának felállítása komoly differenciáldiagnosztikai problémát jelent a rendelkezésre álló egyéb klinikai adatok tükrében. A tesztek érzékenysége ezen betegcsoport esetében függ az alkalmazott módszertől, mérvadó irodalmi adatok alapján 70-90 %. Az eredmények értékelése minding individuálisan történjék. Elengedhetetlen hogy a direkt nukleinsav amplifikációs vizsgálatra kerülő mintákból a mikroszkópos és tenyésztéses vizsgálatok is elvégzésre kerüljenek.
A módszerek légúti vizsgálati anyagokra vannak validálva, érzékenységük extrapulmonális minták esetében alacsonyabb. Extrapulmonális kórképekben a módszer szenzitivitását jelentősen csökkenti a minta jellemzően alacsonyabb csíraszáma, és az amplifikációt gátló inhibítorokjelenléte, amelyekaránya szignifikánsan magasabb, mint a légúti anyagokban.
A központi idegrendszer tuberkulózisa a humán gümőkór legveszélyesebb formája, ezért ebben a kórképben a gyors diagnózis felállítása kiemelkedően fontos. A publikált esetek alacsony száma és a módszerek elégtelen szenzitivitása miatt a meningitis basilaris diagnózisánakgyors felállítására jelenleg nincs nemzetközileg ajánlott módszer. Az utóbbi időben megjelent metaanalízis megállapítása szerint a DNAM technikák érzékenysége extrapulmonális esetekben a vizsgáló helyektől és módszerektől függően széles határok között (27-85 %) mozog. Meningitisben átlagosan 56 % körüli.
A Pulmonológiai Szakmai Kollégium a módszerek indikációjára vonatkozó 2000-ben kiadott korábbi állásfoglalása továbbra is mérvadó. Ennek megfelelően a DNAM indikációi:
- Mikroszkóposan negatív, akut súlyos állapotú betegnél tuberkulózis gyanúja esetén (pl. lélegeztetést igénylő pneumonia)
- Bármilyen rendkívüli sürgősséget igénylő esetben (pl. nem tüdőbetegellátó intézmény ellátására szoruló beteg esetében)
- Mikroszkóposan pozitív immunszuprimáltaknál NTM fertőzés fokozottabb veszélye miatt
- Szervtranszplantált betegeknél
- Fertőzési veszély vélelmének kizárására fokozottan veszélyeztetettek védelmében (mikroszkópos negativitás mellett)
A DNAM legfontosabb előnye, hogy 6-8 órán belül elvégezhetőek, ezért a klinikus részéről elvárható, hogy az eredmények még a mintafeldolgozás napján, de legkésőbb 24 órán belül visszajelzésre kerüljenek. Jelenleg többféle kereskedelmi teszt van forgalomban, (Amplicor PCR-Roche Molecular Systems, Amplified Mycobacterium Tuberculosis Direct Test AMTD-Gen-Probe Inc., BDProbeTec-Becton-Dickinson, GenoType Mycobacteria Direct-HAIN, Genotype MTBDRplus-HAIN), amelyek a minta előkezeléséből, nukleinsav izolálásából, amplifikációból és detektálásból állnak, és minden egyes kit lépésenként más-más módszert alkalmaz. Egyes tesztek csak a M. tuberculosis complexet detektálják, mások a M. tuberculosis complexet és az isonicid (INH) és a rifampicin (RMP) rezisztenciához társuló mutációkat is, és megint mások a M. tuberculosis complexen belüli specieseket, ill. a
gyakori és klinikailag releváns nem tuberkulózist okozó mycobacteriumokat (NTM) is képesek kimutatni. A módszerek szenzitivitása alapvetően a kenet pozitivitásának függvénye, de az alkalmazott tesztenként is változó.
2.4 Tenyésztés (1-6, 9,11,12)
A mycobacteriológiai vizsgálatok következő lépése a dekontaminált minta tenyésztése, amely továbbra is nélkülözhetetlen a következő okok miatt:
- a tenyésztés érzékenysége nagyságrendekkel nagyobb, mint a mikroszkópos vizsgálatoké,
- a M. tuberculosis complexen belüli differenciáláshoz, a különböző NTM azonosításához, a molekuláris epidemiológiai vizsgálatok elvégzéséhez (DNS ujjlenyomat vizsgálat) megfelelő mennyiségű biomasszára van szükség, amelyet a tenyésztés biztosít,
- a rezisztencia vizsgálatok elvégzéséhez élő kórokozót ugyancsak a tenyésztés biztosít.
A mycobacteriumok izolálására használt talán legismertebb táptalaja tojás alapú, szilárd Löwenstein-Jensen (LJ) táptalaj. Az agar alapú táptalajok, mintamilyen a Middlebrook7H10 vagy 7H11 agar, a LJ táptalajhoz képest a némileg gyorsabb tenyésztési idő, és a transzparenciájuk folytán megvalósítható egyszerűbb kolónia morfológia vizsgálat lehetősége miatt kedveltek. Mindazonáltal, ezeken a hagyományos szilárd táptalajokon a M. tuberculosis telepei általában 3-6 hét elteltével jelennek csak meg. Az izolálást követő identifikálás, majd rezisztencia meghatározás további 3-6 héttel növelheti ezt az amúgy is tetemes tenyésztési időt. Mindemellett vizsgálatok azt is igazolták, hogy csakszilárd táptalajon tenyésztve a klinikailag egyértelműen tuberkulózisként diagnosztizált betegek mintáit mintegy 20-30%-ban nem sikerült a M. tuberculosis izolálása. Ez az adat világosan jelzi, hogy a szilárd táptalajon való tenyésztés érzékenysége, bár lényegesen jobb, mint a mikroszkópos vizsgálaté, mégsem haladja meg a 70-80%-ot. A CDC és a WHO jelenlegi ajánlása az, hogy a TBC izolálása, identifikálása valamint az ezt követő rezisztencia vizsgálatok lehetőleg a mintavétel időpontjától számított 2-3 (izolálás, identifikálás) illetve 2-5 (rezisztencia meghatározás) héten belül történjenek meg. Ez az átfutási idő nélkülözhetetlen ahhoz, hogy a klinikus a kezelés nyolcadik hetének végén el tudja dönteni, hogy az alkalmazott négyes kombinációból biztonsággal elhagyhatja-e a pyrazinamidot (PZA) és az ethambutolt (EMB). Ahhoz, hogy ez az ajánlás a gyakorlatban is megvalósítható legyen, nélkülözhetetlen az újabb, folyékony táptalaj alapú rendszerek rutinszerű alkalmazása. Folyékony táptalajon tenyésztve, a tenyésztési idő a minta mycobacterium tartalmától függően 1-3 hétre rövidíthető. Emellett a folyékony táptalajok szenzitivitása 90% feletti. Hátrányuk, hogy jóval hajlamosabbak a befertőződésre. 2.4/a Módszer érzékenysége
Bár a folyékony táptalajok alkalmazása jelentősen csökkenteni képes a tenyésztési időt, szilárd táptalajra azért továbbra is szükség van, mivel bizonyos törzsek nem növekednek jól folyékony miliőben. A tenyésztés érzékenységét jelentősen befolyásolja a szilárd táptalajpH értéke is. Felmérések azt jelzik, hogy a rutinszerűen alkalmazott pH 7-es LJ táptalaj nem felétlenül alkalmas minden Mycobacterium optimális tenyésztésére. Így olyan helyeken, ahol bizonyos NTM okozta megbetegedésekgyakoribbak(pl. HIV fertőzöttek), vagy endémiásakszükség lehet egy savanyú pH érékű LJ-re vagy a pH 6 értékű Ogawa (Japánban elterjedt tojás alapú táptalaj) táptalajra való leoltásra is. A szilárd táptalaj további előnye, hogy a növekedés kvantitatív formában is visszajelenthető, a kolónia morfológia és a pigment termelés is vizsgálható, illetve kellő biomassza biztosítható az identifikálást segítő biokémiai tesztekhez. Önmagában tehát sem a szilárd, sem a folyékony táptalaj érzékenysége nem éri el a 100%-ot, azaz mindkét táptalajtípus esetében előfordulhatnak olyan törzsek, amelyek vagy csak az egyik vagy csak a másik táptalajtípuson képesek növekedni. Ez az oka, hogy jelenleg a nemzetközi ajánlásoknak megfelelően a mycobacteriumok izolálása szilárd és folyékony táptalaj kombinációján kell, hogy alapuljon a kórokozó minél gyorsabb és érzékenyebb detektálása, valamint a rezisztencia vizsgálatok minél gyorsabb elvégezhetősége érdekében. Amennyiben a beoltott szilárd vagy folyékony táptalajokon növekedés nem észlelhető, úgy negatív tenyésztési eredmény 8 illetve 6 hetes inkubálást követően adható ki.
2.4/b Minőségbiztosítás az előkezelési és tenyésztéses vizsgálatok ellenőrzéséhez Általános:
- Összes eszköz és berendezés szabályozott időközönkénti kontroll vizsgálatát el kell végezni, különös tekintettel a laminális boxokra és a centrifugákra
Naponként:
- Reagensek lejárati idejének kontrollja: a NALC-ot mindig a munkafolyamat kezdetén kell a NaOH-hoz adni, NALC-NaOH oldatot 24 órán túl nem szabad felhasználni
- Monitorozni kell a szennyezett minták százalékos előfordulását: ha 10 előkezelt mintát véres táptalajra inokulálunk, 24-48 óra múlva szennyező baktérium nem, ill. minimális mennyiségben tenyészhet csak ki.
- Ha ismételten azonos szennyező baktérium tenyészik ki, ellenőrizni kell az összes felhasznált reagens sterilitását.
- A dekontaminálás kezdetén és végén 1-1-cső (5 ml) steril desztillált víz ill, fiziológiás só oldattal is el kell végezni a munkafolyamatot.
- Az előkezeléshez használt reagenseket a munkafolyamat előtt véres agárra kell oltani.
- Ellenőrizni kell a táptalajok és reagensek lejárati idejét.
- Minden új, házilagosan gyártott táptalajsarzs minőségi vizsgálatát M. fortuitum (ATCC 6841), egy gyorsan növő NTM-el ajánlott elvégezni.
- A kereskedelmi forgalomban kapható, minőségbiztosítási bizonylattal ellátott táptalajokat nem szükséges ellenőrizni, de a felhasznált táptalajok gyártási számát fel kell jegyezni.
Hetente:
- Meg kell határozni a szennyezett tenyészetek százalékos előfordulását. Szilárd táptalaj esetén a 5%, folyékony táptalaj esetén a 8-10 % kontamináció inadekvát előkezelési munkafolyamatra utal.A<3°% szennyeződés túl erős dekontaminációt jelez.
Havonta:
- Monitorozni kell a M. tuberculosis pozitív tenyészetek számát.
- Monitorozni kell a kenetben pozitív és tenyésztéssel negatív minták számát. Ha az ilyen minták száma meghaladja az 1 %-ot, ez túl erős előkezelésre, megfelelő minőségű táptalajokra, különleges igényű mycobacteriumokra, vagy antituberculotikum kezelés alatt álló beteg mintájára utal.
- Monitorozni kell a kenet negatív, tenyésztéssel pozitív minták számát. Az elvárhatóság kb. 30%. Monitorozni kell a kenet negatív és mindössze egy pozitív tenyészettel rendelkező betegek számát.
- Monitorozni kell a kenetben és tenyésztéssel is pozitív esetek arányát. Az elvárt mérték 95 %.
- Monitorozni kell a tenyészetek pozitívvá válásának idejét külön a szilárd és folyékony táptalajok esetében mind kenet pozitív, mind a kenet negatív mintáknál
A fenti értékektől való szignifikáns eltérés nem megfelelő előkezelési eljárásra, vagy fals pozitív tenyészetek előfordulására utal.
Fals pozitív tenyészetek előfordulása kenet pozitív mintákkal történő kontamináció következtében: A mycobacteriológiai laboratóriumokban az előkezelési és tenyésztéses eljárások során a vizsgálati anyag keresztfertőzése következtében fals pozitívvá válhat. A fals pozitív tenyészetek elfogadható aránya kb. 3 %. A keresztfertőzés létrejöhet az előkezelőszer adagolása, vagy a semlegesítés során az aerosol képződés miatt, esetleg a reagens csövek, vagy oldatok kontaminálódhatnak saválló baktériummal. Ez utóbbiak könnyen szennyeződhetnek a vízben gyakran előforduló atípusos mycobakteriumokkal (M. gordonae, M. xenopi), ha a felhasznált víz nem volt steril. A vizsgálati anyagok átfertőződésének esélyét csökkenti, ha a laminális boxban kisebb mennyiségű reagenst használunk, a manipulációk során alkalmanként csak egy minta csöve van nyitva, és a centrifuga csövek zárókupakját lassan nyitjuk ki az aerosol képződés csökkentése érdekében.
2.5 Identifikálás (1-3,6,11,12)
2.5.1 Identifikálás hagyományos módszerrel
A különböző Mycobacterium fajok egymástól valóelkülönítésének,identifikálásának hagyományos útját a különböző hőmérsékleti szinteken mutatott növekedési sajátságok, a telepmorfológia és pigment termelés vizsgálata, valamint különböző enzimaktivitás vagy növekedésgátlás kimutatását célzó biokémiai reakciók elvégzése jelenti. Ezeknek a hagyományos identifikálási teszteknek a legnagyobb hátránya, hogy elvégzésük jelentős mennyiségű biomasszát igényel, amely szubkultúrákra való átoltással és a primér izolálást követően még további több hetes tenyésztéssel és időveszteséggel jár. Emellett a vizsgálatok elvégzése munkaigényes, az eredmények értékelése sok esetben szubjektív. Az utóbbi évek során nagy számban írtakleolyan újNTM törzseket, amelyek identifikálása a hagyományos módszerek segítségével egyáltalán nem lehetséges, ezeket a fajokat csak az új molekuláris biológiai módszerek alkalmazásával lehet felismerni. Mindezen okok miatt a hagyományos identifikálási módszerek szerepe világszerte igen jelentősen visszaszorulóban van. A M. tuberculosis complex identifikálására és az ehhez szükséges alapvető hagyományos identifikálási módszerek elvégzésére (niacin, nitrát reduktáz teszt) minden mycobacteriológiai laboratóriumnak képesnek kell lennie. Az átfutási idő mérséklésére azonban hazai viszonylatban is meg kell teremteni a molekuláris vagy egyéb gyors identifikálási módszerekhez való hozzáférés lehetőségét legalább a magasabb kompetenciájú, regionális laboratóriumok számára.
2.5.2 Identifikálás molekuláris biológiai és egyéb technikákon alapuló módszerekkel
A kereskedelmi forgalomban napjainkban többféle identifikáló teszt kapható, amelyek különböző géntechnikai, kromatográfiás, vagy tömegspektrografiás módszert alkalmaznak a mycobacterium speciesek azonosítására.
2.5.2.1 Nukleinsav hibridizációs módszer:
A kereskedelmi forgalomban hozzáférhető AccuProbe (Gen-Probe Inc., San-Diego, CA) nukleinsav hibridizációs teszt bevezetése jelentősen meggyorsította a M. tuberculosis complex, a M. avium complex, a M. gordonae,ésa M. kansasii identifikálását. Mivel a teszt nem alkalmaz amplifikációs lépést így közvetlenül a klinikai mintából való kórokozó kimutatásra alkalmatlan, pozitivitásához legalább 105 számú baktérium jelenléte szükséges. A teszt azonban kiválóan alkalmas a pozitív folyékony vagy szilárd tenyészetek esetében (ahol a teszt érzékenységéhez szükséges baktérium mennyiség többszöröse rendelkezésre áll) a kitenyészett saválló baktérium identifikálására 1-2 órán belül.
2.5.2.2 Reverz hibridizáción alapuló identifikáló tesztek:
A tesztek során a speciális DNS szakaszt sokszorozzuk PCR segítségével, majd a DNS terméket egy tesztcsíkon elhelyezett, az egyes mycobacteriumokra specifikus próbákkal hibridizáltatjuk. Ez a rendszer a GenoType MTB-HAIN módszer esetében a M. tuberculosis complex-en kívül az összes jelenleg ismert klinikailag szignifikáns NTM kimutatására is alkalmas. Az InnoLipa (Innogenetics) módszerrel a M. tuberculosis complex, a M. avium, a M. intracellulare, a M. kansasii, a M. xenopi, a M. gordonae, a M. scrofulaceum, és M. chelonae azonosítható.
2.5.2.3 DNSszekvenálás:
A DNS szekvenálás a mycobacteriumok identifikálásának jelenleg a legpontosabb módszere. Az egyes törzsek azonosításán kívül információval szolgál az egyes fajok filogenetikájáról és rokonsági fokáról is. A DNS szekvenálás során egyes gének olyan fajspecifikus szakaszainak bázissorrendjét határozzák meg, amelyet azután már ismert és jól karakterizált törzsek bázissorendjével vetnek össze. A referencia bázissorend adatbázis összeállítása történhet "házilagosan", de kereskedelmi forgalomban árult adatbázisok is rendelkezésre állnak. A rutinalkalmazásban mintegy referencia módszerként legelterjedtebb DNS szekvenálás a 16S rRNS hypervariábilis régiójának vizsgálatán alapszik. Automata DNS szekvenáló műszer segítségével a vizsgálat 1-3 nap alatt elvégezhető. A DNS szekvenálás lehetővé tette olyan NTM fajok felfedezését is, amelyek nem vagy nagyon nehezen tenyészthetőek, potenciálisan patogének, vagy egyelőre még nem kellően karakterizáltak, nem minden szempontból ismertek (patogenitás, rezervoár, transzmisszió stb.). A módszer alkalmazása referencia laboratóriumban indokolt.
2.5.2.4 Magas hatékonyságú folyadék kromatográfia (high-performance liquid chromatography; HPLC):
A Mycobacterium sejtfala fajonként változó és specifikus mycolsav összetételének gyors és pontos vizsgálati lehetőségét kínálja a HPLC, amellyel számos ismert, sőt új, korábban még azonosítatlan Mycobacterium faj identifikálása lehetséges. A HPLC berendezés megléte esetén a mérés olcsó és gyors, 2 órán belül elvégezhető. A módszer hátránya, hogy a szükséges műszer költséges és az eredmények értékelése gyakorlatot, nagy tapasztalatot igényel. A módszer alkalmazása referencia laboratóriumban indokolt.
2.5.2.5 A tömeg-spektrometriás módszer egy olyan új, modern technika, amellyel a lézerrel ionizált sejt komponensek tömegét mérik, az eredményt egy detektoron regisztrálják, így megkapják az egyes speciesekre jellemző spektrum profilt. Egy software segítségével a spektrum profil alapján a törzs beazonosítható. A módszer alkalmazása referencia laboratóriumban indokolt.
2.5.2.6 A Capilia TB Test (Tauns, Numazu, Japan Nippon Becton-Dickinson Tokio:
Az egyszerű és gyorsan elvégezhető, immunkromatografiás assay a M. tuberculosis complex-et különíti el a NTM törzsektől. A módszer a M. tuberculosis törzsekre specifikus MPB64 protein és a gén által termelt monoklonális antitestek reakcióján alapszik. Pozitív reakció esetén a cellulóz membránhoz kötött anti-MPB64 monoklonális antitestek reakcióba lépnek a MPB64 proteinnel, és 15 percen belül egy piros gyűrű válik láthatóvá. A módszer specificitása a vizsgálatok szerint 100 %, és a szenzitivitása is 90 % feletti.
2.6 A M. tuberculosis és az NTM genotipizálása, molekuláris epidemiológiai vizsgáló módszerek (2,6)
Az utóbbi években a DNS ujjlenyomat vizsgálat, a PCR alapú spoligotyping és VNTR-MIRU, (Variable Numbers of Tandem Repeats of Mycobacterial Interspersed Repetitive Units) valamint a tömeg spektrometriás módszerek segítségével lehetségessé válta M. tuberculosis nagy pontosságú tipizálása. Aspoligotyping és VNTR-MIRU technikák a PCR-el amplifikált DNS-t detektálják. Aspologotipizálás dot blot módszerrel mutatja ki a speciális DR locuson a spacer szekvenciák jelenlétét, vagy hiányát, a VNTR-MIRU a különböző számban ismétlődő mycobacteriális repetitív egységeket detektálja azok mérete alapján. Ezekkel a módszerekkel az izolátumok un. clusterekbe sorolhatók, és a clonális tipizálásra kiválóan alkalmasak. A tömeg-spektrometriás módszerrel a lézerrel ionizált sejt fehérje komponensek tömegét mérik, egy detektoron regisztrálják, így megkapják a mycobacterium spektrum profilját, azaz a specifikus ujjlenyomatát. Jelenleg a molekuláris epidemiológia arany standard módszere a DNS ujjlenyomat Restriction Fragment Length Polymorphism (RFLP) vizsgálat. Az enzimemésztés során nyert fragmentumok molekuláris mérete oly módon variálódik, hogy két nem rokon M. tuberculosis törzs egymástól eltérő mintázatot mutat a jelölt IS6110 próbával való hibridizációt követően. A DNS ujjlenyomat vizsgálatot sikeresen alkalmazzák különböző járványok vizsgálatára, a tuberkulózis aktív transzmissziójat befolyásoló rizikó tényezők vizsgálatára (pl. antituberkulotikum rezisztencia), a konvencionális módszerekkel azonosíthatatlan kontaktok kiszűrésére és ezáltal a fertőzési lánc felderítésére, különböző veszélyeztetett szubpopulációkon belül a tuberkulózis transzmisszójának vizsgálatára, és a laboratóriumi keresztfertőzések okozta téves diagnózisok kiszűrésére. Az ezekben a helyzetekben szükséges prevenciós lépések meghatározásához és megtételéhez hazánkban is szükséges a molekuláris epidemiológiai vizsgálatok bevezetése legalább a referencia laboratóriumban.
2.7 Rezisztencia meghatározás (1-3,8,9,11,12) 2.7.1 Alapfogalmak
Az eddigi genetikai vizsgálatok szerint a M. tuberculosis antituberkulotikumokkal szembeni rezisztenciájának megjelenéséért vagy a gyógyszer támadáspontját kódoló génekben, vagy a gyógyszer aktiválásáért felelős enzimeket kódoló génekben kialakuló spontán pontmutációk a felelősek. A rezisztenciával kapcsolatos pontmutációk, deléciók és inzerciókaz összes első vonalbeli szernél (isonicid (INH), rifampicin (RMP), pyrazinamid (PZA), ethambutol (EMB) és már néhány másodvonalbeli újabb szernél (streptomycin, ethionamid, fluorokinolonok, makrolidek,) is felismerésre kerültek.
Mindezek alapján nagyvalószínűséggel kizárható egy olyan egyedüli gén jelenléte, amelynek mutációi önmagukban vezetnének a polirezisztens (rezisztencia RMP mellett több más antituberculotikummal szemben) illetve a multidrug rezisztens (MDR) (rezisztencia legalább INH-val és RMP-el szemben; MDR) fenotípus kialakulásához. Az extensively-drug rezisztens (XDR) Mycobacterium törzsek (rezisztencia RMP és INH mellett fluoroquinolonokra, és iv. adagolható kanamycin, capreomycin és amikacin-ra) megjelenése és terjedése tovább erősíti azt az igényt, hogy a rezisztencia vizsgálat minden először izolált törzs esetében megtörténjen. Úgy tűnik, hogy a MDR és XDR több, egymással párhuzamosan, illetve lépcsőzetesen kialakuló mutációk sorozatának az eredménye a különböző génszakaszokon. Rezisztencia leggyakrabban a nem megfelelő gyógyszeres kombináció és dózis, a beteg nem megfelelő compliance következtében, az egyébként természetes körülmények között is mindig előforduló, de csak igen kis kópiaszámban jelenlévő mutáns törzsek szelektálódásával alakul ki.
A Nemzeti Tuberkulózis Program szabályozásának megfelelően minden újonnan felismerésre került, tuberkulózisban szenvedő beteg elsőként izolált tenyészeteiből kötelezően rezisztencia vizsgálatokat kell végezni (kezdeti rezisztencia
vizsgálat). Ellenőrző rezisztencia vizsgálatok végzése akkor szükséges, ha a beteg kontroll tenyésztései a kezelés negyedik hónapja után is pozitivitást mutatnak, illetve ha radiológiai állapotromlás vagy reaktiváció jelei észlelhetők. Rezisztens Mycobacterium okozta infekció veszélye merül fel akkor, ha
- a beteg ismert rezisztens M. tuberculosis okozta infekcióban szenvedő beteg kontaktja,
- a beteg korábban már antituberkulotikum kezelést kapott,
- a beteg az alkalmazott antituberkulotikum kezelés ellenére progressziót mutat (tenyésztései a három hónapos kezelés után is pozitívak),
- a beteg olyan országból származik, ahol a rezisztens Mycobacterium okozta infekció gyakorisága magas.
2.7.2 Szilárd és folyékony alapú rezisztencia vizsgálat, a vizsgálat átfutási ideje
2.7.2.1 A szilárd táptalajon (proportios módszer) végzett rezisztencia-meghatározás bár pontos, de meglehetősen idő (az izolálást követő további 3-5 hetes tenyésztés) és munkaigényes. A vizsgálat biomassza igénye miatt szükség van az identifikált kórokozó LJ vagy egyéb szubkultúrán történő felszaporítására, vagy ha a M. tuberculosis NTM-al együtt ún. kevert tenyészet formájában került izolálásra, akkor a tenyészetnek az álrezisztenciához vezető NTM-tól való megtisztítására, ami újabb több hetes időveszteséget okozhat.
2.7.2.2 Folyékony alapú rezisztencia vizsgálatok
A Bactec MGIT, a radiometriás Bactec 460 TB, vagy a Bact/Alert rendszer segítségével az öt elsővonalbeli antituberkulotikumon kívül a másodrendű szerek többségével szembeni rezisztencia vizsgálatok kb. 4-6 nap alatt elvégezhetők, és a klinikus számára visszajelezhetők.
Mind az antituberculoticum-érzékeny, mind a rezisztens kórokozót hordozó betegek esetében az adekvát kezelés folytatásához, a beteg compliance-nak megtartásához és javításához kívánatos, hogy a rezisztencia vizsgálatok eredményei mihamarabb, de a mintavételtől számított legkésőbb 8 héten belül rendelkezésre álljanak. Ehhez a kórokozó izolálásához, identifikáláshoz és a rezisztencia vizsgálatokhoz alkalmazott gyorsabb átfutási időt biztosító újabb módszerek hazai rutinszerű bevezetése szükséges. 2.7.2.2./a Külső minőségi kontroll
A rezisztencia vizsgálatok megbízhatósága kiemelten fontos, ezért elengedhetetlen, hogy minden rezisztens izolátum kontroll vizsgálata megtörténjen és a vizsgálat eredménye a Referencia Laboratóriumban megerősítésre kerüljön. Különösen fontos a MDR törzsek rezisztenciájának minőségi kontrollja. Az MDR törzsekellenőrző vizsgálata mellett a Referencia Laboratórium automatikusan elvégzi a másodvonalbeli szerekkel szembeni rezisztencia meghatározást is, ezért ezen törzseknek a Referencia Laboratóriumba történő továbbítása kötelező.
2.7.3 Rezisztencia meghatározás géntechnikai módszerrel (13)
A rifampicin (RMP) kulcsfontossággal bír a tuberkulózis kezelésében és a gyógyszerrel szembeni rezisztencia mihamarabbi felismerése vitális a beteg számára. Mindemellett a RMP monorezisztencia ritka, a RMP rezisztencia leggyakrabban polirezisztencia vagy az INH rezisztenciához társulva MDR formájában jelentkezik. Így a RMP rezisztencia gyors kimutatása nemcsak a kezelés optimalizálása szempontjából, hanem a legveszélyeztetettebb MDR törzs okozta megbetegedésben szenvedő betegek gyors azonosítása szempontjából is fontos. A RMP rezisztenciát okozó mutációknak a kimutatása néhány órán belül elvégezhető az rpoB gén specális szakaszának DNS szekvenálásával, vagy a PCR és reverz hibridizáción alapuló (GenoType HAIN és Inno-LiPA Rif TB Innogenetics) line probe assay-k segítségével. Az újabb kereskedelmi forgalomban kapható tesztek a rifampicin rpoB génjének és az isonicid (INH) katG és inhA génjének mutációját szimultán is képesek kimutatni az izolált törzsből (GenoType MTB DR HAIN) és közvetlenül a mikroszkópos vizsgálattal saválló pozitívnak bizonyult beteg mintájából is (GenoType MTB DRplus HAIN).
A MDR tuberculosis fenyegető mértékű globális terjedése miatt, a gyors rezisztencia eredményekhez való hozzájutás érdekében a WHO újdiagnosztikai algoritmus bevezetését javasolja elsősorban a mikroszkópos vizsgálattal saválló pozitív betegekesetében. A WHO állásfoglalása szerint:
- A line probe assay-k alkalmasságát a mikroszkóposan pozitív esetek RMP, ill. INH + RMP rezisztencia detektálására megfelelő számú evidencián alapuló vizsgálattal bizonyították
- A módszerek bevezetését a referencia laboratóriumokban ill. a technikailag jól felszerelt és képzett munkaerővel rendelkező mikrobiológiai laboratóriumokban ajánlják
- Ha a line probe assay érzékeny törzset detektál, az érzékeny M. tuberculosis okozta infekció diagnózisa elfogadható, és a kezelés az elsőrendű szerekkel azonnal megkezdhető
- Ha a line probe assay rezisztens törzset detektál, további tenyésztés, majd a kitenyészett törzsből az első- és másodrendű szerek iránti rezisztencia vizsgálat is azonnal elvégzendő
- A szükséges közegészségügyi intézkedések késedelem nélkül beindíthatók
A M. tuberculosis-sal szemben a NTM esetében - egyes kivételektől eltekintve (M. avium, M. kansasii, gyorsan növő NTM-k) - a rutinszerű rezisztencia meghatározása megfelelően standardizált módszerek hiányában nem javasolt. Az 1. ábra a mycobacteriumok okozta infekciók egyszerűsített diagnosztikus sémáját, algoritmusát mutatja.
2.8. Látens-és aktív tuberculosis fertőzés kimutatása immunológiai módszerekkel
A kereskedelmi forgalomban levő technikák (T-SPOT-TB és Quantiferon-TB Gold) olyan gyors vértesztek, amelyek a M. tuberculosis specifikus antigénjei által aktivált immunsejtek (T sejtek) fokozott jelenlétét, ill. a sejtek által termelt y interferon kimutatását teszik lehetővé. A tesztek a Mantoux próbát helyettesítik, de annál határozottan specifikusabb módszerek, fajlagosságukat a BCG vaccináció,és az atípusos mycobacteriumok (NTM) okozta infekciók többsége nem befolyásolja. Immunszuprimált betegeken a módszer érzékenysége még nem kellően bizonyított.
A protokoll bevezetésének feltételei
A tárgyi és személyi feltételeket a kompetencia szinteknek megfelelően a 15/2004 ESZCSM rendelet tartalmazza.
1. Tárgyi feltételek
A Mycobacterium diagnosztika az ország egész területén elérhető, jelenleg összesen 10 TBC Tenyésztő Laboratórium és a Nemzeti Mycobacteriológiai Referencia Laboratórium működik. A TBC tenyésztő laboratóriumok alkalmasak direkt mikroszkópos, tenyésztéses vizsgálatok végzésére és legalább a M. tuberculosis identifikálására, egyes laboratóriumok rezisztencia vizsgálatokat is végeznek. Egyes III. kompetencia szintű mikrobiológiai laboratóriumok néhány molekuláris genetikai vizsgálat végzésére is alkalmasak. A Referencia Laboratóriumban történik a rezisztens törzsek kontroll vizsgálata, az atípusos Mycobacterium (NTM) törzsek identifikálása, egyes esetekben rezisztencia vizsgálata, és a molekuláris technikák alkalmazása. (direkt kimutatás, species identifikálás, rezisztencia gének detektálása, tipizálás epidemiológiai érdekből)
2. Személyi feltételek
A kompetencia szinteknek megfelelő személyi feltételek: a 15/2004 ESZCSM rendelet szerinti megfelelő számú diplomás és egészségügyi szakdolgozó
3. Szakmai képzési feltételek
A jelen protokoll oktatása a szakorvosképzés, egyéb diplomásképzés és továbbképzés keretében történik A diagnosztikus vizsgálatok megfelelőségének indikátorai
- Direkt mikroszkópos, tenyésztéses és genetikai vizsgálatok eredményinek összevetése (szenzitivitás, specificitás, pozitív és negatív prediktív érték)
- A bakteriológiailag igazolt esetek aránya a regisztrált esetekhez viszonyítva.
- Tenyésztéssel pozitív esetekben a rezisztencia vizsgálatok aránya.
III. Irodalomjegyzék
1. Kent, P. T., and G. P. Kubica. 1985. Public health mycobacteriology. A guide for a level III laboratory. Center for Disease Control, Atlanta, GA.
2. Dunlap, N. E., J. Bass, P. Fujiwara, P. Hopewell, J. Horsburgh, C.R., M. Salfinger, and P. M. Simone. 2000. Diagnostic standards and classification of tuberculosis in adults and children. This official statement of the American Thoracic Society and the Centers for Disease Control and Prevention was adopted by the ATS Board of Directors, July 1999. This statement was endorsed by the Council of the Infectious Disease Society of America, September 1999. Am. J. Respir. Crit Care Med. 161:1376-1395.
3. Metchock, B. G., F. S. Nolte, and J. Wallace, R.J. 1999. Mycobacterium, p. 399-437. In P. R. Murray, E. J. Baron, M. A. Pfaller, F. C. Tenover, and R. H. Yolken (ed.), Manual of Clinical Microbiology, 7th ed. American Society for Microbiology, Washington, D.C.
4. Szabó, N., Lipót Z., Vámos M., Nagy J. 2003. A mycobacteriumok tenyésztésének hatásfoka különböző előkezelési eljárások és tenyésztési módszerek függvényében. Medicina Thoracalis 56: 188-192.
5. Somoskovi, A., C. Kodmon, A. Lantos, Z. Bartfai, L. Tamasi, J. Fuzy, and P. Magyar. 2000. Comparison of recoveries of Mycobacterium tuberculosis using the automated BACTEC MGIT 960 system, the BACTEC 460 TB system, and Lowenstein-Jensen medium. J. Clin. Microbiol. 38:2395-2397.
6. Somoskovi, A., J. Mester, Y. M. Hale, L. M. Parsons, and M. Salfinger. 2002. Laboratory diagnosis of nontuberculous mycobacteria. Clin. Chest Med. 23:585-597.
7. 2000. Update: Nucleic acid amplification tests for tuberculosis. MMWR Morb.Mortal.Wkly.Rep. 49:593-594.
8. Mester, J., Vadász I., Bártfai Z., Ködmön CS., Somoskövi Á.. 2002. A Mycobacterium tuberculosis antituberkulotikum-rezisztenciájának molekuláris alapjai. Medicina Thoracalis 55:30-36.
9. Fodor T., Lőrinczi I., Szikra L. A Mycobacterium tuberculosis és egyéb típusos mycobacterium fertőzések bakteriológiai vizsgálatának módszerei. 555-557. old. In: Czirók É. (szerk.): Klinkai és járványügyi bakteriológia kézikönyv. Melánia, Budapest 1999.
10. National plan for reliable tuberculosis laboratory services using a systems approach Morb. Mortal. Wkly.Rep. 54: No: RR-6. 2005.
11. Drobniewski F.A., Hoffner S., Rüsch_Gerdes S., Skenders G., Thomsen V. and the WHO European Laboratory Strengthening Task Force. Recommended standards for modern tuberculosis laboratory services in Europa. Eur.Respir J. 28. 903-909. 2006.
12. Somoskövi Á., Szabó N., Nagy E.: A tuberkulózis mikrobiológiai diagnosztikájának irányelvei. A Tüdőgyógyászati Szakmai Kollégium és az Orvosi Mikrobiológiai Szakmai Kollégium közös állásfoglalása. Med. Thor. 57. 116-137. 2004.
13. World Health Organization: Molecular line probe assays for rapid screening of patients at risk of multidrug-resistant tuberculosis (MDR-TB) policy statement 27 June 2008.
14. Pai M., L.L Flores, Pai N., Hubbard A., Riley L.W., Colford J.M. Jr. 2003 Diagnostic accuracy of nucleic acid amplification tests for tuberculosis meningitis: a systematic review and meta-analysis. Lancet Infect.Dis 3:633-643.
15. Rock R.B., Olin M., Baker C.A., Molitor T.W., Peterson P.K. 2008. Central nervous system tuberculosis: Pathogenesis and clinical aspects. Clin.Microbiol.Review 21:243-261.
A szakmai irányelv érvényessége: 2009. szeptember 30.
1. A protokoll fejlesztés módszerei:
1.1. A nemzetközi szervezetek (WHO, IUATLD, CDC, ECDC) és tekintélyes külföldi un. supranacionális laboratóriumokés társaságok (CLSI) által kiadott irányelvek alapján, azokat az irodalmi hivatkozásokat vettük figyelembe, amelyek megfelelnek a fenti irányelveknek.
1.2. A felhasznált nemzetközi irányelveket a hazai nemzeti tuberculosis programban foglaltaknak megfelelően adaptáltuk.
1.3. A mycobacteriumok okozta infekciók egyszerűsített diagnosztikus sémáját az 1. ábra mutatja
1.4. Az protokollban használt röviditések: WHO = World Health Organisation
IUATLD = International Union against Tuberculosis and Lung Disease
CDC = Center for Disease Control and Prevention
EuroTB = Európai Tuberculosis Surveillance Központ
ECDC = European Centre for Diseases Control and Prevention
NTM = Non Tuberculous Mycobacterium
DNAM = Direkt Nukleinsav Amplifikációs Módszerek
CLSI = Clinical and Laboratory Standards Institute
FDA = Food and Drug Administration
VNTR-MIRU = Variable Numbers of Tandem Repeats of Mycobacterial Interspersed Repetitive Units
Mycobacteriumok okozta infekciók diagnosztikus sémája
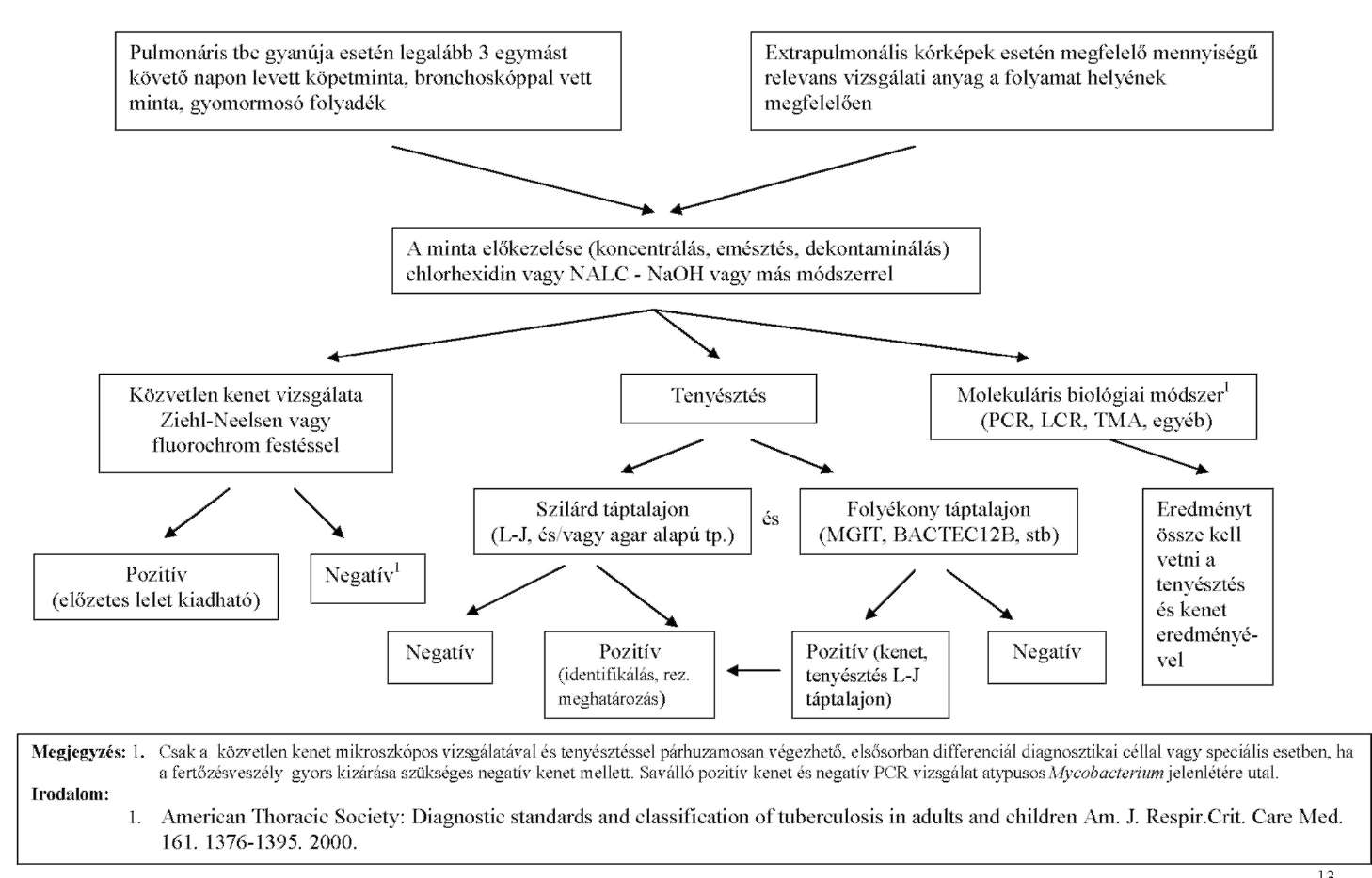
Az Egészségügyi Minisztérium
szakmai irányelve
A felsőlégúti infekciók bakteriológiai diagnosztikájáról
Készítette: az Orvosi Mikrobiológiai Szakmai Kollégium
I. Alapvető megfontolások Bevezetés
A mikrobiológiai laboratóriumok egyik leggyakoribb mintacsoportja a felsőlégúti minták. Ez részben a felsőlégúti infekciók gyakori volta miatt, részben az egyszerű mintavétel miatt alakult így. A minta könnyű hozzáférhetősége azt sugallhatja, hogy a mélyebb légutak infekcióit is megpróbálják felszínesebb mintából kimutatni. Az irányelv célja, hogy tisztázza, melyek azok a kórállapotok, és azok a felsőlégúti minták, amelyeknél a bakteriológiai diagnosztikai laboratórium segítséget tud nyújtani.
Célcsoport
Mikrobiológiai diagnosztikát végző diplomás szakember, mikrobiológiai diagnosztikát igénybevevő klinikus.
Az irányelv tagolása a klinikai kórképekalapján
1. A garat betegségeinek mikrobiológiai diagnosztikája
1.1. A tonsillo-pharyngitis kórokozójának kimutatása
1.1.1. A S. pyogenes okozta tonsillo-pharyngitis mikrobiológiai igazolása
1.1.2. A N. gonorrhoeae okozta tonsillo-pharyngitis mikrobiológiai igazolása
1.1.3. A Plaut-Vincent angina mikrobiológiai diagnosztikája
1.1.4. A torok diphtheria mikrobiológiai diagnosztikája
1.1.5. A pertussis mikrobiológiai diagnosztikája
1.2. A hordozó állapotok vizsgálata
1.2.1. A S. aureus orr, torok hordozás kimutatása
1.2.2. A N. meningitidis nasopharyngeális hordozás kimutatása
1.3. A szájüregi candidiasis mikrobiológiai diagnosztikája
2. A para- retropharyngealis tályog mikrobiológiai diagnosztikája
3. Az otitis externa mikrobiológiai diagnosztikája
4. Az otitis media mikrobiológiai diagnosztikája
5. A sinusitis maxillaris mikrobiológiai diagnosztikája
6. Az epiglottitis mikrobiológiai diagnosztikája
II. Diagnózis
1. A garat betegségeinek diagnosztikája
1.1. A tonsillo-pharyngitis kórokozójának kimutatása
Bevezetés
A tonsillo-pharyngitis (tonsillitis, pharyngitis) az egyik leggyakoribb betegség, amivel a betegek orvoshoz fordulnak. A fertőzéses eredetű tonsillo-pharyngitisekdöntő részét vírusokokozzák (rhinovírus,coronavírusok,adenovírusok, HSV, parainfluenza vírusok, influenza vírusok, Coxsackie A vírus, EBV, CMV, HIV-1). Kisebb részben baktériumok Streptococcus pyogenes (group A Streptococcus, (GAS), a C, G csoportú, béta-haemolizáló streptococcusok, az Arcanobacterium haemolyticum, Yersinia enterocolitica, Neisseria gonorrhoeae, Corynebacterium diphtheriae, Corynebacterium ulcerans, Chlamydophila pneumoniae (régen: Chlamydia pneumoniae), Mycoplasma pneumoniae, Treponema pallidum, kevert anaerob baktériumok (fusobacteriumok, spirochetak) a kórokozók, míg az esetek közel 30%-ában nincs kimutatható etiológiai ágens (19).
A bakteriológiai mintavétel indikációja
Ha a klinikai kép, környezeti anamnézis (pl: skarlát), laborleletek alapján felmerül akut bakteriális tonsillo-pharyngitis (lásd az Irányelv a heveny tonsillopharyngitis antimikróbás kezeléséhez (27).)
- Rheumás lázon átesett beteg tonsillo-pharyngitise
- Gonorrhoeás tonsillo-pharyngitis gyanúja
- Egyoldali necrotizáló folyamat esetén Plaut-Vincent angina diagnosztikájára
- Diftéria gyanú esetén, elsősorban külföldi betegeknél
Minta
Torokváladék
A mintavétel módja tenyésztéshez és antigén kimutatáshoz:
A beteg fejének rögzítése (ha nem kooperál), nyelvének lapoccal történő lenyomása mellett, miközben a beteg maximálisra nyitott szájjal "e" hangot ad, vattapálcával a tonsillákat, a tonsillacsonkot, a hátsó garatívet letöröljük, elsősorban a kóros területeken. Az uvula érintését kerülni kell az öklendezés elkerülése érdekében. A szájüreg egyéb területeinek (nyelv, bucca, lágyszájpad) érintése a normál szájüregi flóra túlzott jelenlétét eredményezi, így a kórokozó kimutatásának esélye romlik. A tenyésztés és a gyors, az antigén kimutatására szolgáló teszt érzékenységét nagyban befolyásolja a mintavétel technikája (29). Az antigén kimutatást szolgáló teszt tartalmazza az erre a célra készített vattapálcát.
A minta tárolása, szállítása
- ha N. gonorrhoeae kimutatása nem cél a vattapálca bármyilyen bakteriológiai transzport (Amies, Stuart) közegben 48 óráig szobahőn,
- ha N. gonorrhoeae kimutatásra van igény, a vattapálca aktív szenet tartalmazó transzport közegben, vagy gonorrhoea transzport táptalajon 24-48 óráig szobahőn tartható, a hűtését kerülni kell,
- Plaut-Vincent angina esetén, ha a minta 12 órán belül nem kerül a laboratóriumba, a vattapálcát 2 tárgylemezre kell kikenni, és azokat szobahőn történő szárítás után a laboratóriumba juttatni
Az egyes entitások külön-külön történő tárgyalását az indokolja, hogy a tárgyalt kórképek mikrobiológiai diagnosztikája eltérő, nem feltétlenül része a rutin feldolgozásnak. A mikrobiológiai laboratóriumok által igényelt járulékos információk (immunológiai státusz, utazási anamnézis, stb.) segítséget nyújtanak abban is, hogy a mikrobiológus is gondolhasson a ritkább kórokozók oki szerepére, és ennek diagnosztikájára a klinikus figyelmét is felhívhassa.
1.1.1. A Streptococcus pyogenes (S. pyogenes) okozta tonsillo-pharyngitis mikrobiológiai igazolása Megfontolás
A közönségesen előforduló bakteriális tonsillo-pharyngitisek közül az egyetlen a S. pyogenes okozta forma az, amelynél az antibakteriális terápia igazoltan indokolt (13). A kezeléstől a következő előnyök várhatóak:
1. megelőzi az akut rheumás láz kialakulását,
2. megelőzi a suppuratív szövődményeket,
3. megszünteti a klinikai tüneteket,
4. csökkenti a baktérium terjedésének lehetőségét a szoros kontaktok között,
5. csökkenti a nem megfelelő antibiotikum terápia okozta mellékhatásokat (3).
Az akut rheumás láz a tünetek jelentkezésétől számított 9 napon belül megelőzhető, így a mikrobiológiai diagnózis kivárása nem jelent kockázatot a terápia késlekedése miatt (39)
A S. pyogenes a torokfájások 5-40%-ában kórokozó. Leggyakrabban az 5-15 éves korosztályban fordul elő (25-40%), a 15-35 éves korosztályban 10-20%, 35 év felett 5-6%, 3 éves kor alatt gyakorlatilag nem fordul elő. Télen és kora tavasszal halmozódik, járványokat okozhat fiatal zárt közösségekben (katonaság, diákszállók) (11) A S. pyogenes tonsillo-pharyngitist általában nem kíséri orrfolyás, köhögés, conjunctivitis. Szuppuratív szövődménye a parapharyngealis tályog és a sepsis, autoimmun poststreptococcalis betegségek a rheumás láz és a glomerulonephritis.
Az egyéb béta hemolizáló streptococcusok közül a C és G csoportú Streptococcus esetén bizonyított tonsillo-pharingitisben betöltött kóroki szerepe, ill. a béta-hemolizáló Arcanobacterium haemolyticum is okozhat tonsillo-pharyngitist. A C csoportú Streptococcus idősebb gyermekekben, zárt közösségben fordul elő gyakrabban; járványos, étel közvetítette infekciót is leírtak. A G csoportú Streptococcust elsősorban étel közvetítette járványok kapcsán tartják kórokozónak. Rheumás lázat egyik baktérium esetén sem igazoltak szövődményként, és akut glomerulonephritist is csak a C csoportú Streptococcus okozta pharyngitis kapcsán igazoltak. Ezen kórokozók esetén az antibiotikum kezelés hasznossága nem egyértelműen igazolt (17)
Diagnosztika
A S. pyogenes okozta tonsillo-pharyngitis igazolásához a kórokozót, vagy annak alkotórészeit kell kimutatni a torokból nyert mintából. Az etiológiai diagnózis két pillérre épül:
- a "betegágy mellett" elvégezhető kórokozó specifikus antigén kimutatásra,
- és a gold standard módszerre, a tenyésztésre.
- A diagnosztikában nem alkalmazzáka direkt kenetvizsgálatot, mert a baktérium csíraszáma a torokban ritkán éri el a kenetben való detektálhatóság határát, a módszer nem elég érzékeny, és az esetlegesen kenetben látható S. pyogenes nem elkülöníthető mikroszkópos morfológiai kép alapján egyéb streptococcusoktól, tehát nem specifikus.
Az AST (Antistreptolysin) detektálása nem része az akut tonsillopharyngitis diagnosztikájának, mert heveny gyulladás esetén nincs kimutatható ellenanyag titer emelkedés a vérben. A vizsgálat csak az autoimmun poststreptococcalis betegségek diagnosztikájában használható (13).
Direkt kórokozó antigén kimutatás
Számos gyári gyorsteszt áll rendelkezésre a kórokozó antigénjeinek direkt kimutatására. Módszereik: latex agglutináció, enzim-immunoassay-ek, immunkromatográfiás tesztek. Érzékenységük függ az alkalmazott módszertől" 60-95% között mozog; fajlagosságuk 99% körüli. Ezek a rendelőben vagy a betegágy mellett elvégezhető vizsgálatok, és általában magas költségük miatt nem ajánlotta mikrobiológiai laboratóriumban az alkalmazásuk. Ezen teszteket kimondottan a betegeket vizsgáló szakemberek részére alakították ki úgy, hogy a gyári kitben az elvégzéshez szükséges összes eszköz rendelkezésre áll, és elvégzésük olyan egyszerű, hogy a korábban laboratóriumi tevékenységet nem végzők is nagy biztonsággal használhatják. Magyarországon ezen tesztek elterjedését akadályozza, hogy csak laboratóriumokszámolhatjákel a vizsgálatot az OEP finanszírozás jelenlegi rendszere szerint. A pozitív gyorsteszt eredmény - megfelelő klinikai kép esetében - igazolja a GAS pharyngitist, a negatív eredmény azonban nem zárja azt ki, a viszonylag alacsony érzékenysége miatt. Egyes vizsgálatok azonban 3 éves kor alatt, ill. felnőtt korban a S. pyogenes okozta tonsillo-pharyngitis igen alacsony incidenciája, és a rheumás láz előfordulásának extrém ritka volta miatt nem ajánlják a negatív gyorsteszt eredményének konfirmálását tenyésztéssel (4).
Tenyésztés:
A mikrobiológiai diagnózis gold standardja a torok váladék tenyésztése 5% véres agaron, 5% CO2 atmoszférában 48 óráig. Megfelelően végezve a vizsgálatot a tenyésztés érzékenysége 90-95%. Az előzetes antibiotikum terápia nagymértékben rontja a tenyésztés érzékenységét. Szelektív táptalajok (Na-azid, nalidixsav, oxolinsav, polymyxin-B, colistin-sulfat, neomycin tartalmú véres agar) alkalmazása, anaerob inkubáció egyes vizsgálatok szerint a tenyésztés érzékenységét növelik (43,30), míg más, költség hatékonyság irányában végzett vizsgálatok nem tartják ezt indokoltnak (40,18). A vizsgálat elvégzése indokolt, ha
- nincs antigén kimutatási gyorsteszt,
- negatív (3 éves kor felett) vagy nem értékelhető az antigén kimutatás,
- macrolid/lincosamid antibiotikumot választ a kezelőorvos, mivel ezen szerekkel szemben a GAS érzékenysége csak 86,7%, ill. 86,8% (OEK Surveillance rendszerben jelentett 2006- évi adatok 5664, ill 5702 törzs vizsgálatával), az éves jelentések alapján ez a rezisztencia szignifikánsan nem változik (24).
Rezisztencia vizsgálat.
A S. pyogenes penicillin érzékenysége 100%-ban megtartott, tesztelése elsősorban az identifikálásban nyújt segítséget. A macrolid/lincosamid rezisztencia lehetősége miatt ezen antibiotikumok hatékonyságát vizsgálni kell. A trimethoprim/sulfamethoxazol nem hatékony a S. pyogenes-re, tesztelése csak diagnosztikai célból indokolt. A tetracyclinek használata a Mycoplasma és Chlamydia kóroki szerepénekfelmerülése miatt nem csökkent. A tetracyclin érzékenység tesztelése indokolt, mert a 2006. évi magyarországi adatok szerint csak 76,6%-a a hazai törzseknek érzékeny. Empirikus terápiára S. pyogenes okozta fertőzés gyanúja esetén csak a penicillin jön szóba (24).
Eredményközlés (várható ideje):
- Béta-hemolizáló Streptococcus nem tenyészett ki. (48 óra múlva)
- Streptococcus pyogenes tenyészett ki. A kitenyészett mennyiség közlése. A rezisztencia vizsgálat eredményei közül a penicillin, erythromycin és clindamycin érzékenységét indokolt közölni elsődlegesen.(min. 48 óra).
- C vagy G csoportú béta-hemolizáló Streptococcus vagy A. haemolyticum tenyészett ki. A kitenyészett baktérium mennyiségének közlése. A rezisztencia vizsgálat eredmény közlése. (min. 48 óra)
Eredmény értékelése:
A GAS hordozás egészségeseknél 10% alatt van. Leggyakrabban a 6-14 éves korosztályt érinti, ritkább a tonsillectomián átesettek S. pyogenes hordozása (2). Hordozóknál a kitenyészett baktérium csíraszáma alacsonyabb, mint akut infekció esetén, ezért a baktérium mennyisége segít a kórokozó szerep eldöntésében is. A hordozás mikrobiológiai diagnosztikát és kezelést nem igényel, mert hordozóknál az akut rheumás láz valószínűsége elenyésző (44) A béta-haemolizáló Streptococcus agalactiae (GBS) kóroki szerepét a tonsillo-pharyngitisben nem sikerült eddig igazolni, a hordozásának közlése félrevezető eredmény, kiadása csak 3 hónapos kor alatt az invazív GBS fertőzések miatt indokolt.
1.1.2. A N. gonorrhoeae okozta tonsillo-pharyngitis mikrobiológiai igazolása
Megfontolás
A gonorrhoeás tonsillo-pharyngitis ritka kórkép, szexuálisan aktív, fiatal felnőtteknél kell elsősorban gondolni rá, a vizsgálatot indikáló orvosnak külön kell kérnie a Neisseria gonorrhoeae irányában történő tenyésztést, mert speciális táp- ás atmoszféra igényű a baktérium. A baktérium béta-laktám, tetracyclin és fluorokinolon érzékenysége nem megjósolható, minden esetben tesztelni kell. A N. gonorrhoeae okozta tonsillo-pharyngitis STD kórkép, ennek megfelelően kell járványügyileg eljárni.
Diagnosztika
A baktérium tenyésztése speciális táptalajt igényel (GC csokoládé agar). Szelektív táptalaj (Thayer-Martin agar, módosított Thayer-Martin agar, Martin-Lewis agar, New York City táptalaj) alkalmazása nélkül a kísérőflóra miatt a tenyésztés nem elég érzékeny módszer. A tenyésztési idő a lassan növő tápigényesebb típusok miatt 72 óra (45)
A kórokozó tenyésztése mellett a molekuláris vizsgálatokszerepe nőtt. Mind nukleinsav hibridizációs, mind nukleinsav amplifikációs próbák forgalomban vannak N. gonorrhoeae kimutatására genitális mintákból. Az amplifikációs próbák érzékenysége és fajlagossága 90% felett van a genitális minták esetén, ezért a ruin diagnosztika részét képezik. Az extragenitális mintákból, különösen a torokváladékból a CDC nem javasolja a molekuláris vizsgálatot, mert a normál flóra tagjait képező apatogén neisseriák gyakran álpozitív eredményt adnak. A molekuláris vizsgálatok nem adnak információt a baktérium érzékenységéről sem, ezért a gold standard tenyésztést nem helyettesíthetik.
Eredményközlés (várható ideje):
- N. gonorrhoeae nem tenyészett ki. Ez az eredmény akkor közölhető, ha egyéb baktériumoktúlszaporodásával nem kell számolni. (72 óra múlva)
- A tenyésztés sikertelen volt normál torokflóra vagy sarjadzó gomba túlnövése miatt. A vizsgálat ismétlése javasolt.
(72 óra)
- N. gonorrhoeae tenyészett ki. Rezisztencia eredményben a penicillin, a cefixim (vagy cefpodofim), ceftriaxon (vagy cefotaxim), a cefuroxim (vagy cefoxitin),a ciprofloxacin (vagy ofloxacin) és a tetracyclin szerepeljen. (min. 48 óra)
1.1.3. A Plaut-Vincent angina mikrobiológiai diagnosztikája Megfontolás
A Plaut-Vincent anginát (necrotizáló ulceratív gingivostomatitis) vegyes anaerob, mikroaerofil baktériumflóra, spirochaeták, fusobacteriumok okozzák. Hirtelen kezdődő egyoldali, nekrotizáló folyamat. Tenyésztéssel való izolálásuk nem célravezető, miután ezek lassan növő, nehezen tenyészthető mikróbák, melyeket a normál torokflóra tagjai könnyen túlnőnek. A kórkép igazolására a kóros torokképletből vett minta festett kenetének mikroszkópos vizsgálata elegendő. Torokváladék, szájüregi váladékfeldolgozása ez irányban csak kezelőorvos kérése esetén történik meg, nem a rutin laboratóriumi feldolgozás része a vizsgálat, ezért a kezelőorvosnak tájékoztatni kell a laboratóriumot ezirányú kérés esetén. A bakteriális fertőzéstől el kell különíteni az allergiás, autoimmun, virális és a kemoterápia okozta akut szájüregi ulcerációt (42).
Diagnosztika
Kettő kenet készítése, szárítás, hőfixálás, festés karbolfukszin 10x-es hígításával 5 percig. Eredményközlés (várható ideje):
- Mikroszkópos vizsgálattal Plaut-Vincent angína nem valószínűsíthető (aznapi eredmény)
- Mikroszkópos vizsgálattal Plaut-Vincent angína valószínűsíthető (aznapi eredmény). A pozitív eredményről a kezelőorvost célszerű szóban is tájékoztatni.
1.1.4. A torok diphtheria mikrobiológiai diagnosztikája Megfontolás
Diphtheriát Magyarországon nagyon ritkán diagnosztizálnak. Az elmúlt 4 évben egyetlen egy esetet sem jelentettek be (25). Elsősorban a behurcolt esetek bármikor előfordulhatnak. A klasszikus álhártya hiányozhat, klinikai megjelenése utánozhatja a streptococcus pharyngitist. A kórkép elkülönítendő a mononucleosisos toroktól, a Plaut-Vincent anginától és a soortól is. A diphtheria toxin által okozott betegség. A Corynebacterium diphtheriae izolálása önmagában nem bizonyító erejű a kórképet illetően, a törzs toxintermelését is igazolni kell. Akut szakban a natív vérből kimutatott ellenanyag inkább védettséget, mint a kórkép igazolását jelenti. A rekonvalescens savó titeremelkedése igazolhatja a kórképet. Raritás, de egyéb corynebacterium fajok (C. ulcerans, C. pseudotuberculosis) termelhetnek diphtheria toxint, és a klasszikus betegség tüneteit kialakíthatják (37).
AC. diphtheriae kimutatása nem rutin mikrobiológiai feladat, a kezelőorvosnaktájékozódnia kell, hogy a laboratórium felkészült-e a diagnosztikára, és azt külön kérnie kell.
Minta
Álhártya a torokból, vagy nasopharyngeális váladék; 3 mintavétel ajánlott a kórkép kizárására
Mintavétel lásd:1.1. mintavétel
vagy: nasopharyngeális minta: Csak a flexibilis kifejezetten nasopharyngeális váladék vételére fejlesztett mintavevő alkalmas a nasopharynx megmintázására. A beteg a mintát vevővel szembe leül egyenes fejtartással. A beteg orrának hegyét hátrafelé nyomjuk, bevezetjük az egyik orrnyílásba a mintavevőt a beteg orrának kb. 1,5x-ös hosszában. Akkor járunk biztosan kellő magasságban, ha a betegnél tüsszentési ingert váltunk ki. A visszahúzott pálcát transzport közegbe tesszük. A gyapot alapú vattapálca gátolja a baktérium szaporodását, tenyésztéshez nem ajánlott. PCR-hez Dacron tampon ajánlott, mivel a Ca-alginát PCR-t gátló anyagokat tartalmaz.
A minta tárolása, szállítása
- a transzport közegben tárolt vattapálca 24-48 óráig szobahőn tartható.
Diagnosztika
Tenyésztés. A C. diphtheriae tenyésztéséhez szelektív, differenciáló táptalajok (Clauberg, Loeffler) használata szükséges. Identifikálásához speciális festést alkalmazunk (Neisser festés). Végleges mikrobiológiai eredményt csak toxint kimutató laboratórium adhat. Toxin kimutatására a gold standard módszer az Elek próba (agar gél precipitáció). A toxin kimutatható ELISA-n vagy immunkromatográfián alapuló módszerrel is.
PCR. A C. diphtheriae toxinjának génje egy bakteriofágon található. Tekintve, hogy más coryneform baktériumok is hordozhatják azt, a vizsgálati mintából történt közvetlen toxinkimutatás álhártya nélkül nem bizonyítja, csak valószínűsíti az infekciót. A PCR vizsgálattal az izolált C. diphtheriae-ból is kimutatható a toxin gén (tox) vagy a termelés regulációjáért felelős génszakasz (dtxR) (37,38).
Rezisztencia vizsgálat. Az antibiotikum terápia a kezelés része, de nem elsődleges eleme. Tesztelni kell a baktérium penicillin erythromycin és clindamycin érzékenységét (34).
Ellenanyag kimutatás. Magyarországon a populáció átoltott diphtheria ellen, ezért toxin elleni antitest nem igazolja az akut fertőzést. ELISA alapú IgG kvantitatív vizsgálattal az akut fázis és a rekonvalescens szak közötti 4x-es titeremelkedés valószínűsítheti, de nem bizonyítja az infekciót. Vero sejten antitest neutralizációs módszerrel funkcionális diphtheria ellenanyag vizsgálat végezhető.
Eredmény közlés (várható ideje):
- Corynebacterium diphtheriae nem tenyészett ki. (48 óra)
- Corynebacterium. diphtheriae tenyészett ki. Érzékenységi vizsgálat eredménye. Toxinkimutatás folyamatban. (min. 48 óra). Pozitív eredmény közlés szóban is.
- Toxintermelő C. diphtheriae tenyészett ki. (min. 72 óra). Pozitív eredmény közlés szóban is. 1.1.5. A pertussis mikrobiológiai diagnosztikája
Megfontolás
A pertussis rendkívül fertőző, elhúzódó légúti betegség, melyet a Bordetella pertussis mellett a B. parapertussis is okozhat. A kórkép világszerte, minden életkorban előfordulhat. Csecsemőkben súlyos, magas letalitású a betegség. Magyarországon a kötelező védőoltás miatt a betegség incidenciája alacsony, évente 20-50, klinikailag igazolt esetet jelentenek. Megjelenésére elsősorban a fiatal felnőttek között kell számítani (25). A pertussishoz hasonló lefolyású légúti megbetegedést okoznak egyes adenovírusok is. A betegség típusosan 3 szakaszban zajlik: a kezdeti hurutos szakaszt a paroxizmális köhögési szak, majd a lassú rekonvalescens szakasz követi. Oltott felnőttekben a betegség atípusosan zajlik. A pertussisra elhúzódó, különösen a hányással befejeződő köhögési rohamok esetén fiatal felnőtteknél is gondolni kell.
Minta
1) Hurutos szakban:
a) Nasopharyngeális váladéktenyésztésre és PCR vizsgálatra. Torokváladékból a baktérium kimutatási esélye rosszabb.
b) Vérsavó, antitest kimutatásra
2) Paroxizmális szakban:
a) Nasopharyngealis minta PCR vizsgálatra.
b) Vérsavó, antitest kimutatásra
Mintavétel
lásd.1.1.4. Nasopharyngealis minta vétele Mintaszállítás, tárolás
- Csak transzport közegen (legjobb a Rogen-Lowe agar), vagy Bordet-Gengou táptalajon szállítva van esélye az izolálásnak.
- A vérsavót 48 óráig +4 oC-on, azon túl -20 oC-on szállítandó, tárolandó
Diagnosztika
Tenyésztés. Csak a kezdeti, catarrhalis fázisban van értelme. A tenyésztés Bordet-Gengou táptalajon történik 35 0C-on. A táptalajt cefalexinnel (0,04 g/l) kiegészítve a kísérő flóra visszaszorítása eredményes. Az inkubációs idő min. 1 hét. Molekuláris vizsgálat. A PCR-rel történő kimutatás a rutin diagnosztika része. Előnye:
- érzékenyebb a tenyésztésnél,
- torokváladék is jó minta,
- a minta szállítása történhet szárazon vagy fiziológiás sóoldatban is,
- a paroxizmális fázisban is van esélye a kórokozó kimutatásának,
- antibiotikum terápia megkezdését követően is lehet sikeres a baktérium kimutatása.
Szerológiai vizsgálat. A diagnosztika legegyszerűbb és legelterjedtebb módja a kórokozó specifikus antitestek kimutatása. A pertussis toxin (PT) elleni antitestválasz fajspecifikus, míg a filamentosus haemagglutinin (FHA), a pertactin (PRN) és a fimbrialis adhaesinek (FIM) elleni antitestválasz vagy nem kielégítő, vagy nem fajspecfikus. Savópár vizsgálatával azanti-PT4x-es titeremelkedése, vagy a másik három antigén közül legalább kettővel szembeni 4x-es titeremelkedés igazolja a pertussist. Egyszeri emelkedett IgG válasz csak valószínűsíti a kórképet, az IgA emelkedés ilyenkor megerősítheti a diagnózist. Pertussis fertőzés igazolt,
- ha a nasopharyngealis váladékból a B. pertussis kitenyészett,
- ha a minta PCR pozitív,
- ha az akut és rekonvalescens savók között a titeremelkedés 4x-esaz anti-PT antitestben, vagy a többi antigén közül legalább kettővel szemben.
Pertussis fertőzés valószínű,
- Ha egyszeri savóvizsgálattal magas IgA és IgG ellenanyag mutatható ki a vizsgált antigénekkel szemben a paroxizmális szakban. (6)
1.2. A hordozó állapotok vizsgálata
Megfontolás
Kizárólag epidemiológiai jelentőségű a Staphylococcus aureus (S. aureus), a légúti patogén baktériumok, a N. meningitidis hordozás vizsgálata. A S. aureust az elülső orrjáratból, torokból, axilláris, perianalis tájékról lehet leggyakrabban izolálni. A rezisztencia vizsgálatnak elsősorban a methicillin rezisztens törzsek kiszűrésében van szerepe. A légúti patogének és a N. meningitidis leggyakrabban a nasopharynxból izolálhatók, A sarjadzó gombák torokhordozásának vizsgálata immunkompromittáltaknál része a későbbi invazív gomba fertőzés megjóslására végzett surveillance vizsgálatoknak. Immunkompetenseknél a sarjadzógomba a normál torokflóra tagja, vizsgálata csak soor esetén indokolt.
1.2.1. A S. aureus orr, torok hordozás kimutatása
Minta
Orr váladék tenyésztésére kizárólag a S. aureus hordozás kimutatás céljából indokolt. Mintavétel
Előzetesen benedvesített vattapálcával az orrüreg elsőharmadát (mindkettőt) át kell törölni Torok váladék: Lásd 1.1.1.
Mintaszállítás, tárolás (orr/torok)
A vattapálca transzport közegben 72 óráig tárolható szobahőmérsékleten.
Diagnosztika
Tenyésztés. A mintát direkt leoltás mellett szelektív, dúsító közegbe is ajánlott leoltani, amit 24 óra múlva, bedúsulás után ki kell oltani. A felhasznált táptalaj ill. dúsító közeg kiválasztása attól is függ, hogy a S. aureus vagy az MRSA hordozást kívánjuk vizsgálni. Dúsító közegnek 6,5% NaCl tartalmú Müller-Hinton buillont javasolnak, MRSA szűrés esetén kiegészítve oxacillinnel. A dúsítás a tenyésztés érzékenységét 12-24%-kal javítja az egyes irodalmi közlemények alapján. Agar lemeznek sósagart, sós-véres agart, oxacillinnel vagy anélkül, lipovitellin Chapman sós agart, vagy kereskedelmi forgalomban beszerezhető Staphylococcus vagy MRSA chromagart lehet használni. A kereskedelmi forgalomban kapható MRSA chromagarokban az antimikróbás szerek gyorsan bomlanak, esetenként lejárati időn belül MRSA-nak bizonyul az MSSA, ezért az MRSA eredményt mindig konfirmálni kell a PBP 2' protein kimutatásával latex agglutinációval, ennek kétséges eredménye esetén mecA gén detektálással. A methicillin rezisztencia szűrésére korongdiffúziós módszerrel a 30 μg-os cefoxitin korong javasolt 35 oC-on, Müller-Hinton agaron (33,31,5,10). Molekuláris vizsgálat
Az MRSA kórházi terjedésének megelőzésére a javasolt a beteg kórházi felvétele, elhelyezése előtti MRSA szűrése azokban az országokban, olyan területeken, ahol gyakori az MRSA előfordulása. Erre a célra a molekuláris vizsgálatok tűnnek alkalmasnak, melyekkel 2-3 órán belül kizárható a beteg MRSA hordozása. A kereskedelmi forgalomban kapható, valós idejű PCR vizsgálatokon alapuló módszerek zárt rendszerűek, a DNS tisztítástól az amplifikáción át a detekciós lépéig automatában zajlanak, nem igényelnek különösebb molekuláris módszer ismeretet, kevésbé érzékenyek a kontaminációra, magas specificitású és szenzitivitású vizsgálatok. Alkalmazásuknak leginkább áruk szab határt (34,21,41).
Eredményközlés (várható ideje):
- S. aureus nem tenyészett ki (48 óra múlva)
- S. aureus tenyészett ki + érzékenységi adatok (min. 48 óra)
- MRSA nem tenyészett ki (24 óra múlva)
- MRSA tenyészett ki (min. 48 óra). Szóbeli közlés is indokolt
1.2.2. A N. meningitidis (nasopharyngealis) hordozásának kimutatása Minta
Nasopharyngealis váladék
Mintavétel lásd:1.1.4.
Minta szállítása, tárolása
Transzport közegben (szenes Amies vagy Stuart) vagy transzport táptalajon (Neisseria szelektív agar, lásd 1.1.2) szobahőn vagy termosztátban 24 óráig. Hűtést kerülni kell!
Diagnosztika
Tenyésztés. A N. meningitidis tápigényes, érzékeny baktérium. 5-7%-os széndioxid atmoszférát igényel. Nasopharyngealis minta esetén számolni kell a kísérő baktérium flóra túlnövésével, ezért célszerű szelektív táptalajt használni (módosított Thayer-Martin trimethoprimmel, vancomycinnel, colistinnal, amphotericinnel kiegészítve). A baktérium szerotípusának meghatározása a diagnosztika részét kell, hogy képezze. Ha a laboratórium nem rendelkezik szerotipizálási lehetőséggel, a törzset tovább kell küldeni ezen vizsgálat céljából.
Eredményközlés (várható ideje):
- N. meningitidis nem tenyészett ki. (48 óra múlva)
- N. meningitidis tenyészett ki. Szerotípus eredménye. Rezisztencia eredményben a ceftriaxon, cefixim, rifampicin és ciprofloxacin is szerepeljen. (min. 48 óra)
Eredmény értékelése
-AN. meningitidis nasopharyngeal hordozása nem igazolja, hogy a páciens esetleges invazív fertőzését a baktérium okozza. Nincs egységes álláspont arra vonatkozóan, hogy mi a teendő a N. meningitidis- t hordozó paciensekkel járvány mentes időben.
1.3 . A szájüregi candidiasis mikrobiológiai diagnosztikája
Megfontolás
Gyakori kora- és újszülöttekben, csökkent védekezőképességű betegekben, idősekben (elsősorban műfogsort viselőkben). A lepedékes elváltozásban sok gombaelem található, ezért direkt mikroszkópos vizsgálattal meggyorsítható a diagnosztika. Ép immunitású betegeknél szájüregi gomba vizsgálat típusos klinikai kép hiányában nem indokolt.
Csökkent védekezőképességű betegek gomba surveillance vizsgálatának részét képezi a torokváladék szűrése. Minta
Szájüregi lepedék vagy immunkompromittáltaknál torok váladék Mintavétel
Vattapálcával a lepedékes területről törlést venni, lehetőleg nem érintve ép szájnyálkahártyát Torokváladék lásd 1.1.
Minta tárolás, szállítás
Transzport közegben, szobahőmérsékleten 72 óráig tárolható a vattapálva. Diagnosztika
Szájüregi candidiasisnál, ha a beteg nem csökkent védekezőképességű, elegendő a gomba jelenlétének igazolása. Ilyen esetben - bár a kenet érzékenysége kisebb, mint a tenyésztésé - a kenet metilénkék festéssel történt vizsgálata elegendő. Csökkent védekezőképességű betegeknél a vizsgálati mintát Sabouraud táptalajon tenyészteni kell, és a kitenyészett sarjadzó gombát species szintig identifikálni kell. Az izolátumból rezisztencia vizsgálatot nem kell végezni.
Eredményközlés (várható ideje):
- Mikroszkópos vizsgálattal sarjadzó gomba elemek nem láthatók (aznapi eredmény)
- Mikroszkópos vizsgálattal sarjadzó gomba elemekés/vagy pszeudohifák láthatók (aznapi eredmény)
- Sarjadzó gomba nem tenyészett ki (7 nap múlva)
- Species szintű gombaidentifikálás eredményének közlése. A species szintű identifikálásnak elsősorban csökkent védekezőképességű betegeknél van jelentősége. Rezisztencia vizsgálat csak speciális esetekben, a kezelőorvossal konzultálva indokolt (min. 72 óra).
2. A para-retropharyngeális tályog mikrobiológiai diagnosztikája
A garat körüli tályog felsőlégúti vagy fogászati fertőzések szövődményeként, nyaki osteomyelitis vagy trauma következményeként alakulhat ki. Leggyakoribb kórokozók a Streptococcus pyogenes és a Staphylococcus aureus. Bármely normál szájflóra tag részese lehet egy kevert aerob-anaerob fertőzésnek (Haemophilus parainfluenzae, Eikenella corrodens, Fusobacterium necrophorum, Peptostreptococcus sp., nem haemolizáló streptococcusok, stb). Actinomycosis és tuberculosis is lehet egy mikrobiológiailag negatív tályog hátterében. A konzervatív kezelés mellett nem javuló kórkép (tályog) sebészi feltárást igényel, mikrobiológiai mintát a műtét alatt kell venni. A garat körüli tályogokdöntően gyermekkorban fordulnakelő,de felnőttkorban is számítani kell rá. Retropharyngealis tályog 6 éves kor előtt alakul ki, utána a virtuális tér, ill. a nyirokcsomók megszűnnek (22,28,12,46).
Minta
Sebészeti feltárásból származó punktátum vagy törlés
Mintavétel
Műtéti feltárásban, sebészeti úton vett minta Mintaszállítás és tárolás
Anaerob transzport közegben szobahőn vagy 2-8 oC-on tárolt minta max. 48 óráig tárolható.
Diagnosztika Tenyésztés.
Az anaerob baktériumok is lehetnek kórokozók, ezért a megfelelően (anaerob diagnosztikára is alkalmasan: zárt fecskendőben vagy transzport közegben) szállított mintát anaerob tenyésztésre is fel kell dolgozni. A normál nasopharyngealis flóra kontamináló szerepére számítani kell, ugyanakkor az alfa-haemolizáló streptococcusok kóroki szerepe sem zárható ki ebben a kórképben. A műtéti mintából gyors tájékozódás érdekében direkt kenetet is kell készíteni Gram szerint festve.
Eredményközlés (várható ideje):
- Direkt kenetben látott baktérium (aznap)
- Aerob baktérium nem tenyészett ki (48 óra múlva)
- Kórokozó baktérium nem tenyészett ki (48 óra múlva)
- Anaerob baktérium nem tenyészett ki (5 nap múlva)
- Kórokozó és antibiotikum érzékenysége (legkorábban 48 óra múlva)
3. Az otitis externa mikrobiológiai diagnosztikája Megfontolás
Az otitis externa a külső hallójárat és/vagy a fül gyulladása illetőleg fertőzése. Vizes sportokat űzők között gyakran fordul elő. A kórkép kialakulását elősegíti a cerumen hiánya, a magas páratartalom, magas hőmérséklet, lokális trauma (fültisztító pálca használata, fülhallgató, hallókészülék használata). Nyári hónapokban gyakrabban fordul elő, trópusokon is gyakrabban kell a kórképre számítani. A leggyakrabban izolált kórokozó a Pseudomonas aeruginosa (~50%) és a Staphylococcus aureus (~25%), Gram-negatív baktériumok, Streptococcus pyogenes és gombák (Aspergillus és Candida fajok) is előfordulnak. Gomba tenyésztés immunkompromittáltak krónikus, malignus folyamatainál indokolt. Anaerob baktériumok nem játszanak kóroki szerepet, ezért anaerob feldolgozás nem jön szóba. Az Amerikai Egyesült Államokban az előfordulás 4/1000 ember, a necrotizáló forma nagyon ritka, azonban a mortalitás ebben a kórformában 20%. A következő klinikai entitásokat különítjük el:
- Az akut diffúz otitis externa, mely a leggyakoribb kórforma, uszodába járók betegsége. Általában bakteriális eredetű, ritkán gombás fertőzés következménye. A 7-12 éves korosztályban fordul elő leggyakrabban.
- Az akut lokalizált otitis externa, más néven furunculosis a hallójárati szőrtüszőgyulladást jelenti.
- A krónikus otitis externa a 6 héten túl sem gyógyuló akut diffúz formának felel meg. Krónikus folyamat gyermekeknél gyakran másodlagos, gennyes, perforált otitis media szövődménye, ez esetben a baktériumok köre megegyezik az otitis media kórokozóival.
- Az ekcematosus otitis externa nem infekciós eredetű, számos bőrgyógyászati kórkép (atópiás dermatitis, psoriasis, lupus erythematosus, ekcema) lokalizálódhat a külső hallójáratra, és okozhat differenciáldiagnosztikai problémát.
- A nekrotizáló, malignus otitis externa infekciós kórkép, amely a hallójárat körüli mély szöveteket is involválja. Elsősorban immunkompromittált felnőttek betegsége (régóta fennálló II. típusú diabetes mellitus, AIDS). Gyakran Pseudomodas aeruginosa vagy penészgombákokozzák. Az Aspergillus fajok mellett a Mucor vagy Rhisopus fajokkal is számolnunk kell. Cellulitis és osteomyelitis eredményeként is kialakulhat a malignus otitis externa (23,26,36, 9).
Minta
Vattapálcával vett külsőfül váladék. Mintavétel
Vattapálcával a külső hallójáratból kell mintát venni, vagy a necrotikus masszát a laboratóriumba beküldeni
Minta tárolás, szállítás
Transzport közegben, szobahőmérsékleten a vattapálca 72 óráig tárolható. Diagnosztika
Tenyésztés aerob baktériumok és penészgombák irányában.
Eredményközlés (várható ideje):
- Aerob baktérium nem tenyészett ki (24 óra)
- Kórokozó baktérium nem tenyészett ki (24 óra)
- Sarjadzó gomba nem tenyészett ki (7 nap)
- Penészgomba nem tenyészett ki (21 nap)
- Kitenyésztett kórokozó + antibiotikum érzékenység (min. 48 óra)
4. Az otitis media mikrobiológiai diagnosztikája Megfontolás
Az akut otitis media leggyakoribb kórokozói a vírusokon (8-25%) túl a S. pneumoniae, H. influenzae, M. catarrhalis, S. pyogenes, S. aureus, Enterobacteriaceae. Krónikus folyamatoknál az anaerob baktériumokkal is számolni kell. A nasopharynxból, orr-, torokváladékból az otitis media kórokozói kortól, etnikumtól, szocio-ökonomiai helyzettől, kórállapottól, földrajzi elhelyezkedéstől, éghajlati-, időjárási viszonyoktól függően változó arányban (1-88%) kitenyészthetőek, ezért ezeka minták nem alkalmasakaz otitis media kórokozójának igazolására (7,16). Az otitis media etiológiai diagnózisához csak a középfül váladék a megfelelő minta. A középfülgyulladás szövődménye lehet mastoiditis, meningitis, fokális vagy diffúz intracraniális gyulladás.
Bakteriológiai mintavétel indikációja
Minden olyan esetben, amikor a pontos bakteriológiai diagnózis és azantimikróbás érzékenység ismerete szükséges, az empirikus antibakteriális kezelés nem elégséges: Csökkent védekezőképességű betegek középfül fertőzése Mastoiditis, meningitis, vagy egyéb intracraniális szövődmények 2 vagy 3 sikertelen antibiotikum kúra után fennálló otitis media (32)
Minta
Középfül váladék Mintavétel
Tympanocentezis után a lándzsa leoltása vagy vattapálcával a kicsurgó váladékot felfogni; legjobb eredményt a vakuténeres mintavétel ad (46%-os pozitivitás szemben a tympanocentesis 6%-os pozitivitásával (1) A spontán perforációt követő váladékozásból nyert minta esetén gyakran kell kontamináns baktérium flórával számolni. Vakuténeres mintavétel: A hallójáratot szívóval meg kell tisztítani a cerumentől, majd Bonain-oldattal dezinficiálni és érzésteleníteni kell a dobhártyát. A sárga szinkódú vakuténeres tűt be kell csavarni a csőtartó harangba, majd a védőhüvely segítségével 45o-os szögben meg kell hajlítani. A natív vérvételi vákumos csövet a helyére kell illeszteni, de nem szabad rányomni. Ezzel a szerelékkel, lehetőleg vizsgáló mikroszkóp alatt kell átszúrni a dobhártyát, a tű lumenét a dobüregben tartva a vakuténeres csövet a csőtartóba kell nyomni. A szerelék eltávolítása, és szétszedése után a vakuténeres csövet be kell küldeni mikrobiológiai feldolgozásra. (1) Ez a minta anaerob tenyésztésre is alkalmas transzport közeg nélkül.
Minta tárolás, szállítás
- transzport közegben tartott minta 48 óráig szobahőmérsékleten tárolható, vakuténeres minta 2-8 oC-on 24 óráig tartható,
- anaerob tenyésztés igénye esetén anaerob transzport közegben 48 óráig szobahőmérsékleten tárolható
Diagnosztika
Középfül váladék tenyésztés aerob, megfelelő minta esetén anaerob módon is. A direkt kenet vizsgálat indokolt, habár ritkán informatív a kórokozó sokszor alacsony csíraszáma miatt, ellenben a kenetvizsgálat pozitív prediktív érteke magas.
Eredmény közlés (várható ideje):
- Direkt Gram-szerint festett kenet eredménye (aznap)
- Aerob baktérium nem tenyészett ki (48 óra)
- Kórokozó baktérium nem tenyészett ki (kontamináns bőrflóra esetén) (48 óra)
- Anaerob baktérium nem tenyészett ki (5 nap)
- Kitenyészett kórokozó(k) megnevezése, rezisztencia eredménnyel (min. 48 óra) 5. A sinusitis maxillaris mikrobiológiai diagnosztikája
Megfontolás
Az akut sinusitis egyike a leggyakrabban kezelést igénylő felsőlégúti betegségeknek. Nasalis intubálás, immunkompromittált állapotok, cysticus fibrosis hajlamosítanak a betegségre. Mintavételre a sinus aspirációt tartják legalkalmasabbnak, az endoszkópos beavatkozások közül a merev eszközzel végzett mintavételnél találtak jobb eredményeket. A sinus aspiratumból akut sinusitisben az esetek 76%-ában mutatható ki kórokozó. A szignifikáns baktérium csíraszám 103/ml, az 1000x-es nagyításban látóterenkénti 20 vagy több granulocyta jellemzi a bakteriális akut sinusitist (8). Az orr váladék nem releváns minta, a sinus váladékkal 64%-os egyezést mutat csak (7). A leggyakoribb kórokozók megegyeznek az akut otitis media kórokozóival. Intubáltaknál, nasogastricus szondát viselőknél kórházi Gram-negatív pálcákra kell számítani. Odontogén eredetű sinusitisben polimikróbás anaerob dominanciájú baktériumflóra valoszínűsíthatő. Gombák okozta invazív sinusitis esetén szükséges mikrobiológiai diagnózis, elsősorban fonalas gombák a kórokozók. A nasopharynx normál flórájának tagjai gyakran kontaminánsok, ezért a csíraszám meghatározás segíthet a patogenitás eldöntésében.
A krónikus siniusitiseknél gyakran nem mutatható ki kórokozó. A krónikus sinusitisekdiagnosztikáját újabban flexibilis endoszkópos beavatkozással (FESS: functional endoscopic sinus surgery) kívánják eredményesebbé tenni.
A gombás sinusitis kórismézése döntően hisztológiára épül a fonalas gombákgyakran sikertelen tenyésztése miatt. Ha felmerül a gomba szerepe (immunkompromittált, diabetes mellitus ketoacidosissal), a tenyésztést minden esetben meg kell kísérelni. Aspergillus, Rhisopus fajok, C. albicans, Fusarium és Alternaria fajok izolálhatók gyakrabban. Az I. típusú diabeteses mellitusban szenvedőknél Mucor és Rhisopus fajok okoznak un. rhinocerebralis mucormycosist, elsősorban ketoacidosra hajlamos betegeknél.
Sinusitist intracraniális, szemüregi és légúti szövődmények követhetnek. Bakteriológiai mintavétel indikációja
- Korrekt, kellő ideig alkalmazott antibiotikum terápia kudarca esetén
- Pansinusitisben
- Bármilyen szövődmény esetén
- Csökkent védekezőképességű betegeknél
- Recidiváló sinusitisben
- Kórházban akvirált sinusitisben
- Súlyos tünetek és toxikus állapotok
- Szuppuratívszövődmények (15,8)
Minta
Sinus aspiratum
Nem alkalmas minta azarcüreggyulladás kórokozójánaka tisztázására az orr,nasopharyngealis és torok váladék,mert ott nem csak a sinusitis kórokozói, hanem hordozott ún. légúti patogén baktériumok is előfordulnak. A mintavétel során nem elkerülhető az orrváladékkal történő kontamináció, melyben lehetnek hordozott un. légúti patogén baktériumok, ezért a kitenyészett baktérium relevanciáját a csíraszámmal jellemzik.
Mintavétel
Az elülső orr és az alsó orrkagyló alatti terület dezinficiálása után lokális anesztetikummal érzésteleníteni az alsó orrkagyló alatti területet (punkció helye). Az antrum középső falát átszúrni 12-es tűvel, a sinus tartalmát fecskendőbe kiszívni (ha szükséges, 1-2 ml steril fiziológiás sóoldattal átmosható a sinus). A fecskendőt lezárva kell juttatni a laboratóriumba (20). Transzportálható a minta vakuteneres csőben, anaerob transzport közegben. Fonalas gomba infekció gyanúja esetén biopsziával nyert szövetmintát kell vizsgálni.
Minta tárolás, szállítás
- transzport közegben, szobahőmérsékleten 48 óráig tárolható
- anaerob tenyésztés igénye esetén anaerob transzport közeg használható
Diagnosztika
A tenyésztési irányt a kért vizsgálat határozza meg, Amennyiben a vizsgálatkérő adatlapon a tenyésztés iránya és a diagnózis nincs feltüntetve a tenyésztést aerob, anaerob, fonalas gomba irányában indítjuk el, ha a beküldött minta tárolása ezt lehetővé teszi. Direkt kenet vizsgálat Gram szerint, melynek eredményközlésében a domináló baktérium jelenlétén kívül a granulocyták mennyiségét is közölni kell. A tenyésztést lehetőleg kvantitatívan kell végezni, és a csíraszámot az eredményben a klinikussal közölni kell. Akut sinusitisnél a szignifikáns csíraszám: 103/ml (20). Krónikus infekcióknál a direkt kenet pozitivitás,ésa direkt leoltás pozitivitási aránya nagyon alacsony a kórokozó kis csíraszáma miatt. Fonalas gomba infekcióknál sokszor csak szövettani mintából lehet a kórokozót kimutatni, ezért forszírozni kell ennek a mintának a mikrobiológiai vizsgálatát.
Eredményközlés (várható ideje):
- A direkt kenetben látható granulocyták jelenlétének és a látható baktériumnak közlése (aznap)
- Aerob baktérium nem tenyészett ki (48 óra)
- Kórokozó baktérium nem tenyészett ki (48 óra)
- Kitenyésztett kórokozó, csíraszáma + antibiotikum érzékenység (min. 48 óra)
- Anaerob baktérium nem tenyészett ki (5 nap)
- Gomba nem tenyészett ki (21 nap)
6. Az epiglottitis mikrobiológiai diagnosztikája Megfontolás
Az epiglottitis leggyakrabban 2-6 év közötti gyermekek fulladással kísért súlyos, szisztémás infekciója. Szinte kizárólagos kórokozó a H. influenzae b, de okozhatja H. influenzae non b szerotípus, S. pneumoniae, S. pyogenes és S. aureus is. Vírusok is lehetnek kórokozók. A kötelező HiB védőoltás óta a betegség előfordulása drámaian lecsökkent. A légúti mintavétel a garat-epiglottis nagyfokú érzékenysége miatt fulladáshoz vezethet, ezért még intenzív terápiás háttér mellett sem célszerű a beavatkozást elvégezni. Az epiglottitis esetén a bakteriémia gyakori, ezért releváns mikrobiológiai minta a haemokultura. A hemokultura vételéről a Mikrobiológiai Szakmai Kollégium által kiadott Véráram infekciók mikrobiológiai diagnosztikája irányelvek tájékoztatnak (14).
Minta visszautasítása:
A felső légúti fertőzések diagnosztikájára beküldött bakteriológiai minták akkor utasíthatóak vissza, ha a minta nem azonosítható, ha nem megfelelő módon, ideig lett tárolva, szállítva. Egyéb esetekben a minta feldolgozásra kerül,és az eredményközlésben jeleznie kell a mikrobiológusnak, hogy az adott mintából kitenyészett baktérium kóroki szerepéről mit tart a klinikai adatok, a minta típusa és a kitenyészett baktérium figyelembe vételével.
| Rövidítések jegyzéke: | |
| AST | Antistreptolysin titer |
| CMV | Cytomegalovirus |
| EBV | Epstein-Barr vírus |
| GAS | Group A Streptococcus (Streptococcus pyogenes) |
| Hib | Haemophilus influenzae b |
| HIV-1 | Human immundeficiencia virus-1 |
| HSV | Herpes simplex virus |
| MH | Müller-Hinton agar |
| MRSA | Methicillin rezisztens Staphylococcus aureus |
| MSSA | Methicillin érzékeny Staphylococcus aureus |
| OEK | Országos Epidemiológiai Központ |
| PCR | Polimeráz-láncreakció |
| STD | Sexually transmitted diseases (szexuális úton átvihető betegségek) |
III. Irodalomjegyzék
1. Balogh L, Rásonyi -Kovács P, Bán É: Akut otitis media bakteriológiai diagnosztikája. Fül- orr- gégegyógyászat. 2005; 51(1):5-7
2. J Begovac, E Bobinac, B Benic et al: Asymptomatic pharyngeal carriage of beta-haemolytic streptococci and streptococcal pharyngitis among patients at an urban hospital in Croatia. Eur J Epidemiol 1993; 9(4):405-10
3. AL Bisno, MA Gerber, JM Gwaltney et al: Practice guidelines for the diagnosis and management of group A streptococcal pharyngitis. Infectious Disease Society of America. CID. 2002; 15:113-125.
4. J AL Bisno et al: Diagnosis and Management of Group A Streptococcal Pharyngitis: A Practice Guideline. CID. 1997; 25:574-83
5. Blanc DS, Wenger A, BilleJ.: Evaluation of a novel medium for screening specimens from hospitalized patientsto detect methicillin-resistant Staphylococcus aureus. J Clin Microbiol. 2003;41(8):3499-502.
6. Budai J: Pertussis. Infekt és Klin Mikrobiol. 2004. december, 119-122
7. K Carroll, L Reimer: Microbiology and laboratory diagnosis of upper respiratory tract infections. CID. 1996; 23:442-8.
8. AW Chow: Infection of the Sinuses and Parameningeal Structures. In: SL Gorbach, JG Bartlett, NR Blacklow: Infectious Diseases.1992. W.B. Saunders Company. 517-530.
9. WB Clark, I Brook, D Bianki, DH Thompson: Microbiology of otitis externa. Otolaryngol Head Neck Surg. 1997; 116(1): 23-5.
10. CLSI: Performance Standards for Antomicrobial Susceptibility Testing; Eighteenth Informational Supplement. 2008;28. M100-S18.
11. J Crump: Pharyngitis. Guideline for clinical care. Univ. Michigan Health System.1996. update2000.
12. Coticchia JM, GetnickGS, Yun RD, et al: Age-, site-, and time-specific differences in pediatric deep neck abscesses. Arch Otolaryngol Head Neck Surg. 2004;130(2):201-7.
13. Az Egészségügyi Minisztérium szakmai protokollja A heveny tonsillopharyngitis antimikróbás kezeléséről. www.eum.hu
14. Egészségügyi Minisztériumi iránylevei: Véráram infekciók http://www.euagazat.hu/portal/server.pt/gateway/ PTARGS_0_270_3491_0_0_18/MIKRO_Veraram_infekciok_P.pdf
15. Fül-orr-gégészeti Szakmai Kollégium, Infektológiai Szakmai Kollégium: Az akut rhinosinusitisek kezelése. Infektológiai útmutató 2005. 45.-51. Medition Kiadó 2005.
16. García-Rodríguez JÁ, Martínez MJF: Dynamics of nasopharyngeal colonization by potencial respiratory pathogens. JAC. 2002. 50; S2, 59-73.
17. MA Gerber, ST Shulman: Rapid diagnosis of pharyngitis caused by group A streptococci. Clin Microbiol Reviews 2004; 17: 571-580
18. MA Gerber: Diagnosis of pharyngitis: methodology of throat cultures. In: ST Shulman ed. Pharyngitis: management in an era of declining rheumatic fever. New York: Praeger, 1984; 61-72.
19. M Gwaltney, AL Bisno: Pharyngitis. In: Mandell 2000.
20. JM Gwaltney JR: Sinusitis. IN: G Mandell, JE Bennett, R Dolin:Principles and Practise of Infectious Diseases. 676-686. Churchill Livingstone 2000.
21. van Hal SJ, Jennings Z, Stark D, et al: MRSA detection: comparison of two molecular methods (BD GeneOhm((R)) PCR assay and Easy-Plex) with two selective MRSA agars (MRSA-ID and Oxoid MRSA) for nasal swabs. Eur J Clin Microbiol Infect Dis. 2008 Jul 29. [Epub ahead of print]
22. Hasegawa J,Tateda M, Hidaka H et al: Retropharyngeal abscess complicated with torticollis: case report and review of the literature. Tohoku J Exp Med. 2007;213(1):99-104.
23. KB. Holter, J. Gick: Management of the patient with otitis externa. J Fam Pract. 2001. 50(4): 353-60.
24. http://www.oek.hu/oek.web?nid=666&pid=1
25. http://www.oek.hu/oek.web?to=1529&nid=509&pid=1&lang=hun
26. E. Hughes, JH Lee: Otitis externa. Pediatr Rev. 2001; 22(6):191-7.
27. Infektológiai Szakmai Kollegium, Gyermekgyógyászati Szakmai Kollegium: Irányelv heveny tonsillopharyngitis antimikróbás kezeléséhez. Infektológiai útmutató 2005. 53.-56. Medition Kiadó 2005.
28. Kamath MP, Bhojwani KM, Kamath SU,et al:Tuberculous retropharyngeal abscess. Ear Nose Throat J. 2007;86(4):236-7.
29. B Kurtz, et al: Importance of inoculum size and sampling effect in rapid antigen detection for diagnosis of Sterptococcus pyogenes pharyngitis. CID. 2000; 38: 279-281
30. BA Lauer et al: Effect of atmosphere and duration of incubation on primary isolation of group A streptococci from throat cultures. J Clin Microbiol 1983;17:338-40
31. van Loo IH, van Dijk S, Verbakel-Schelle I, et al:Evaluation of a chromogenic agar (MRSASelect) for the detection of meticillin-resistant Staphylococcus aureus with clinical samples in The Netherlands. J Med Microbiol. 2007;56 (Pt 4):491-4.
32. M Marcy: New guidelines on acute otitis media: an overview of their key principles for practice. ClevClin J Med. 2004;
71: (suppl 4) S3-S9.
33. Nahimana I, Francioli P, Blanc DS.: Evaluation of three chromogenic media (MRSA-ID, MRSA-Select and CHROMagar MRSA) and ORSAB for surveillance cultures of methicillin-resistant Staphylococcus aureus. Clin Microbiol Infect. 2006;12(12):1168-74.
34. Nguyen Van JC, Kitzis MD, Ly A, et al: Detection of nasal colonization methicillin-resistant Staphylococcus aureus: a prospective study comparing real-time genic amplification assay vs selective chromogenic media. Pathol Biol (Paris). 2006;54(5):285-292.
35. J.D.Osguthorpe,D.R. Nielsen:Otitisexterna: ReviewandClinical Update.Am Family physician, 2006.74 (9). 1510-1516.
36. JD Osguthorpe, DR Nielsen:Otitis externa: review and clinical update. Am Fam Physician. 2006; 74(9):1510-6.
37. CJ Ohuabunwo, KM Bisgard, T Popovi cet al: Diphtheria. In: VPV Surveillance Manual, 3th ed. 2002. Ch1. CDC
38. Protocol for the laboratory diagnosis of C. diphtheriae, Canada: http://www.phac-aspc.gc.ca/publicat/ ccdr-rmtc/98vol24/24s3/24s3h_e.html
39. CH Rammelkamp: Rheumatic heart disease - a challenge. Circulation. 1958; 17:842-851
40. OF Roddey et al: Comparison of throat culture methods for the recovery of group A streptococci in a pediatric office setting. JAMA 1995;274:1863-5.
41. Rossney AS, Herra CM, Brennan GI, et al: Evaluation of the XpertTM MRSA Assay on the GeneXpert Real-Time PCR Platform for Rapid Detection of MRSA from Screening Specimens. J Clin Microbiol. 2008 Aug 6. [Epub ahead of print]
42. L.C. Schneider, A.E. Schneider: Diagnosis of oral ulcer. Mt Sinai J Med. 1998. 65 (5-6):383-7.
43. RH Schwartz et al: Effect of atmosphere of incubation on the isolation of group A streptococci from throat cultures. J Lab Clin Med 1985;106:88-92.
44. B. Schwartz et al: Pharyngitis. Pediatrics 1998; 101:171-174
45. Széll A: Neisseria gonorrhoeae. In: Klinikai és járványügyi bakteriológiai kézikonyv. Szerk: Czirók É. 1999. Melania kiadó. 334-6.
46. Tan PT, Chang LY, Huang YC, et al: Deep neck infections in children. J Microbiol Immunol Infect. 2001;34(4):287-92.
47. DM Whiley, JW Tapsall, TP Sloots: Nucleid Acid Amplification Testing for Neisseria gonorrhoeae. J Mol Diagn. 2006. 8(1):3-15.
Az Egészségügyi Minisztérium
módszertani levele
A tápcsatornából vett diagnosztikus szövetminták kórszövettani feldolgozásáról
(1. módosított változat)
Készítette: a Patológiai Szakmai Kollégium
Bevezetés
A patológiai vizsgálatok fő célja minél több információt szolgáltatni a beteg kezeléséhez. A vizsgálatok nagy többségét a rákmegelőző állapotok és daganatok diagnosztikája képezi. A diagnosztika ezen a területen abban változott, hogy jelenleg molekuláris patológiai módszereket kell alkalmazni elsősorban a daganatok prognosztikai és az egyedi terápia megválasztása céljából. Mindez azt jeleni, hogy a mai stratégiák közül az adott betegnek legmegfelelőbb kezelést csak a korszerű patológiai lelet alapján lehet kiválasztani. A módszertani levél útmutatást kíván adni a tápcsatornából származó biopsziás anyag, valamint a sebészi rezekciós preparátumok korszerű patológiai feldolgozásához, beleértve az elvárható fixálási-, szövet-feldolgozási-, festési-, immunhisztokémiai módszerek alkalmazását és a rosszindulatú daganatok esetében jelenleg alkalmazandó molekuláris patológiai eljárásokat.
1. Általános irányelvek
A tápcsatorna sebészi-daganatpatológiai eljárásai
A) Patológiai staging (pT, pN)
- a tumor kiterjedése
- a nyirokcsomó metasztázisok jelenléte, regionális eloszlása
B) Patológiai grading
- a tumor differenciáltsága (a mirigyes struktúra megtartottsága)
- a sejtmag atípia foka
- nagy nagyítású látóterenkénti mitózisszám
C) Egyéb patológiai prognosztikai faktorok
- a rezekciós szélek épsége
- a daganat növekedési típusa (expanzív - infiltratív, terjedés (vér-, nyirokér-, perineuralis invázió)
- a tumor erezettsége
- proliferációs markerek (Ki67 index, DNS cytometria)
- immunhisztokémiai prognosztika faktorok (p53, E-cadherin, PTEN)
- énelváltozásokhoz társuló jellegzetes szövettani kép (lásd alább)
A tápcsatorna elváltozásainál alkalmazható molekuláris patológiai eljárások célja
A) Patológiai diagnózis segítése
- jellegzetes génátrendeződések kimutatása (lymphomák, sarcomák)
- klonalitás vizsgálat (lymphomák)
- vírusok és baktériumok kimutatása (HPV, Helicobacter és ennek terápiával szembeni rezisztenciája)
B) Prediktívfaktorok
- ploidia (kromoszómális, DNS)
- tumor szupresszor és "mismatch repair" gén mutációk kimutatása (örökletes daganatok)
C) Prognosztikai faktorok
- génexpresszió vizsgálata immunhisztokémiai-, szöveti- vagy mRNS microarray technikával
- génamplifikáció kimutatása (carcinomák)
- microsatellita instabilitás vizsgálat (gyomor- és vastagbélrákok)
- gén mutációk kimutatása (BRAF gén V600E mutáció)
D) A célzott molekuláris terápia segítése
- KRAS gén 12. és 13. codon mutáció kimutatása az anti-EGFR monoklonális ellenanyag kezelés hatásosságának meghatározására
- a cKIT 11. exon vagy a PDGFRA 12. exon Gleevec szenzitív mutációk, továbbá a cKIT9,13,17 exon és PDGFRA 14. exon kevésbé Gleevec szenzitív mutációk vizsgálata
- reisztencia mutációk kimutatása (EGFR 21. exon, PDGFRA 18. exon)
1.1. A tápcsatornából származó biopsziás anyag kórszövettani vizsgálatához szükséges klinikai adatok A kórszövettani vizsgálathoz az alábbi adatokat kell a patológus rendelkezésére bocsátani:
a) A beteg azonosítása
- Név
- TAJ szám
- Születési év, hó, nap
b) A kezelőorvos neve és az a címe, ahova a szövettani leletet várják.
c) A biopszia vagy a műtét időpontja
d) További klinikai adatok:
- Kórelőzmény (pl. előzetes diagnózisok és leletszámok, kezelések, Helicobacter pylori teszt, gluten enteropathia, Crohn-betegség, nehézlánc betegség, szerzett immunhiányos szindróma, más lokalizációjú daganatos betegség).
- Releváns klinikai leletek. Teljes endoszkópos vagy műtéti lelet
- A beküldött minta típusa (cytologia, biopszia, polypectomia, rezekátum) és lokalizációja.
1.2. A tápcsatornából származó biopsziás vagy műtéti preparátumok előkészítése kórszövettani vizsgálatra
A kórszövettani vizsgálatra szánt kis biopsziás mintákat 4%-os pufferezett formalinban fixálva a mintavétel napján, de legkésőbb másnap reggel kell vizsgálatra küldeni. Egy endoszkópos vizsgálat alkalmával vett többszörös biopsziát külön edénybe kell tenni, amin a beteg neve mellett a mintavétel helye is fel van tüntetve. A műtéti preparátumokat lehetőleg fixálatlanul és a műtétet követően haladéktalanul el kell juttatni a patológiára. Az ilyen anyagot felvágva és kiterítve kell fixálásra előkészíteni. Daganatos betegség esetén a serosai (vagy a sebészi) felszínt tussal meg kell festeni, hogy a daganatos terjedés viszonyát a környezethez a metszetekben egyértelműen meg lehessen határozni. Célszerű a preparátumot jelzéssel ellátni és lefényképezni. Daganatszövetből további vizsgálatokra (pl. FISH, DNS cytometria) lenyomati kenetet lehet készíteni, illetve ha a diagnózist nem veszélyezteti, fixálatlan tumorszövet mintát további genetikai vizsgálatok céljára mélyfagyasztva félre lehet tenni. Ha a félretett szövetminta nem diagnosztikus célt szolgál, ehhez a beteg beleegyezését előre meg kell szerezni. A műtéti preparátumok fixálása is 4%-os pufferezett formalinban történik. A fixálást lehetőleg mikrohullámú besugárzással kell elősegíteni. A mikrohullámú besugárzás egyrészt fixáló hatású, másrészt elősegíti a fixálószer gyors penetrációját, ezáltal a sejtstruktúra, és a sejtek makromolekuláinak szerkezete is jobban megőrződik, ami a később szükségessé váló speciális vizsgálatokat sokkal megbízhatóbbá teszi. A műtéti preparátum indításakor a szövettani vizsgálatra kivágott részeket egy sémás rajzon jelölni kell. Carcinoma esetén a műtéti preparátumban fellelhető összes nyirokcsomót meg kell keresni és külön blokkban beágyazni.
1.3. A tápcsatornából származó biopsziás vagy műtéti preparátumok patológiai feldolgozásának általános elve
Az egy alkalommal különböző régiókból vett és külön edényben érkezett többszörös biopsziát külön-külön kell feldolgozni. Ugyanabból a blokkból készült metszeteket egy tárgylemezre a metszés sorrendjében egymásután kell felhúzni. Polypoid képletet a legnagyobb domborulatán felvágva úgy kell indítani, hogy a metszetben a nyél is jól megítélhető legyen,a rezekciós vonalat festékkel kell jelölni. A polypusok teljs feldolgozása szükséges, extrém nagy elváltozás esetén az előző metszés síkjával párhuzamosan vezetett metszéssel kell több blokkot kialakítani. Ha familiáris polyposis szindróma áll fenn carcinoma nélkül, az elváltozást legalább 15 blokkban kell vizsgálni. Ha familiáris polyposis szindróma talaján carcinoma is kialakult, az elváltozás kiterjedtségétől függően 20-30 kivágás szükséges.
Carcinománál meg kell határozni az infiltráció mélységét, a serosa vagy a tumor alatti, illetve az alsó és felső rezekciós sík esetleges érintettségét, valamint az összes (legalább 8) regionális nyirokcsomó állapotát. A tumort úgy kell indítani, hogy annak a legmélyebb infiltrációnak megfelelő teljes harántmetszete vizsgálatra kerüljön. A szomszédos ép nyálkahártyából is indítani kell egy blokkot.
1.4. A formalin-fixált paraffinba ágyazott szöveteken végezhető molekuláris patológiai vizsgálatok a daganatellenes terápia segítése céljából
Megjegyezzük, hogy itt részletes technikai protokollok nem adhatók meg, csak utalunk az eljárások fő lépéseire. A vizsgálatokhoz speciális felszerelésnek, mint valósidejű PCR készülék vagy DNS szekvenátor, továbbá mikrocentrifugának, a hőmérsékletét állítható laboratóriumi inkubátornak és termo-blokknaknak rendelkezésre kell állni. Szükség van a standard laboratóriumi felszerelésekre, mikroliter térfogatú pipetta sorozatra, végül a megfelelő reagens kitekre és egyéb reagensekre, pufferekre, mikrocentrifuga és PCR csövekre.
1.4.1. A szövetminta kiválasztása molekuláris patológiai vizsgálatok céljára
A molekuláris patológiai vizsgálatokat el lehet végezni formalinban fixált és paraffinba ágyazott műtéti anyagon, biopsziás mintákon vagy megfestett cytologiai keneteken. A kenetek a DNS izolálás során megsemmisülnek, mert a lemezekről a sejteket le kell oldani, ezért célszerű azokat előzetesen lefényképezni.
1.4.2. A szövetminta megfelelősége molekuláris patológiai célokra
Törekedjünkfixálatlan szövetminták tárolására, amelyeka legmegfelelőbbek molekuláris genetikai vizsgálatokcéljára. A jól fixált és előkezelt paraffinba ágyazott szövet vagy cytologiai preparátum is alkalmas kiindulási minta. A vizsgálatokat az alábbi tényezők nehezítik:
- A műtéti anyag sokáig állt fixálatlanul, vagy a beleket nem felvágva fixálták.
- A fixálás nem 4%-os neutrális formalinban, vagy jelentősen több mint 8-12 óráig történt.
- A DNS izolálásra kiválasztott mintában a tumorsejt: ép sejt arány túl alacsony.
- Előzetes sugárkezelés, ami egyszálú DNS töréseket okoz.
1.4.3. DNS izolálás
A DNS izolálás módszerét a kiindulási minta minőségéhez kell igazítani. Magas tisztaságú DNS izolálásra alkalmas kitek különböző fajtái, továbbá paraffinba ágyazott szövetekből és kismennyiségű mintákból izoláló, továbbá egyszálú DNS töréseket helyreállító és izoláló speciális kitek a kereskedelemben rendelkezésre állnak. Nagyon jól alkalmazhatók az automata DNS izoláló készülékek is.
1.4.4. A mikroszatellita instabilitás meghatározása és mutáció analízis
Ha a tumorszövetből és az ép szövetekből izolált DNS rendelkezésre áll, az 1998. évi Bethesda konferencia által javasolt öt mikroszatellita marker (BAT-26, BAT-25, D5S346, D2S123 és D17S250) segítségével a mikroszatellita instabilitás vizsgálat elvégezhető. (Boland CR, et al: Cancer Res 58:5248-5257, 1998). Mikroszatellita stabil (MSS) az a daganat, amely egyik fent említett markerrel sem mutat instabilitást. Magasfokú mikroszatellita instabil (MSI-H) acarcinoma,ha legalább két markerrel, alacsony fokú mikroszatellita instabil (MSI-L), ha egy mikroszatellita markerrel mutat instabilitást.
Az elmúlt évek tapasztalatai azt mutatják, hogy valósidejű PCR és olvadáspont analízis technikát alkalmazva a BAT-25
és BAT-26 marker elegendő egy vastagbélrák mikroszatellita státusának korrekt meghatározásához.
Valósidejű PCR technika és olvadáspont analízis szintén nagyon érzékeny és jól alkalmazható a KRAS, a BRAF, az EGFR génmutációk és a tirozin-kináz gátlók vagy a Glivec elleni rezisztencia kimutatására. Az eredményeket szekvenciaanalízissel lehet/kell ellenőrizni. A c-KIT és PDGFRA mutációk vizsgálata jelenleg még szekvenciaanalízissel történik.
1.5. A patológiai lelet általános szerkezete
Minden patológiai lelet készítéséhez bizonyos általános szempontok meghatározhatók. Fel kell tüntetni a kórszövettani azonosító számot, a beérkezés és kibocsátás dátumát, az elváltozás lokalizációját és a készült blokkok számát. A lokalizáció és a blokkok számának ismerete alapvetően fontos információ a metszetek értékelésekor vagy egy második vélemény igénybevétele esetén. Nem tudjuk például meghatározni, hogy egy daganat részlegesen vagy kompletten került-e eltávolításra, a sebészi széleket a betegség érinti-e vagy nem, anélkül, hogy tudnánk a szövettani blokkok számát és a kimetszés helyét. A klinikai adatok rögzítése a szövettani leletben hasznos lehet, ha a diagnózis egy későbbi időpontban újra értékelésre kerül.
A lelet makroszkópos és mikroszkópos leíró része a legtöbb esetben azonos módon szerkeszthető. A makroszkópos leírásnak tartalmaznia kell a minta nagyságát, és az ép, valamint a kóros szövetrészek arányát. Jelölni kell nem csak a kimetszés helyét és számát, hanem azt is, hogy egy blokkból hány metszet készült. A mikroszkópos leírásnak
tartalmaznia kell a szövet típusát, és az alkalmazott speciális módszereket. A gyomor-bél rendszer elváltozásainak szövettani diagnosztikájához jelenleg leggyakrabban felhasznált eljárásoka következők: PAS vagy mucikarmin festés, Gimasa-festés, MUC1, MUC2, pan-CK, CK7, CK20, LCA, CD20, chromogranin, synaptophysin, s-actin, S100 fehérje, CD117, p53, E-cadherin, MLH1, MSH2 immunhisztokémia.
A leletben össze kell foglalni azokat a szöveti jellegzetességeket, amelyek a biztos vagy valószínűsíthető diagnózis és differenciál-diagnózis felállításához szükségesek, továbbá meg kell adni minden olyan információt, amely a klinikus számára később fontos lehet.
Említeni kell a rezekciós szélek állapotát, a metasztatikus terjedést, az elváltozás kialakulásának valószínűsíthető folyamatát és azokat a jellegzetességeket, amelyek a beteg ellátásában fontosak. Ha egy daganat teljes egészében eltávolításra került, a TNM-re alapozott stádiumot is meg kell határozni. A gyomor-béltraktus daganatainak részletesebb kórszövettani diagnosztikáját és molekuláris genetikáját illetően utalunk a WHO Tumours of the Digestive System, lARCPress, Lyon, France kézikönyvre.
Molekuláris patológiai vizsgálatok esetén rögzíteni kell az alkalmazott módszereket, a használt molekuláris markereket, a DNS minőségét meghatározó eljárásokat, a negatív és pozitív kontrollokat, és ha vannak, az elvégzett, az eredményeket megerősítő eljárásokat.
Az összefoglalás vagy a konklúzió - különösen hosszabb leleteknél - rávilágít az értékelés fontos aspektusaira. A molekuláris vizsgálat eredményét közérthető formában kell megadni. Nehéz vagy komplikált esetet bonyolult néhány szóval összefoglalni. Több lehetőség felvetése esetén jelölni kell, hogy mi a vizsgáló preferált véleménye. Azt is érdemes figyelembe venni, hogy a leletet kézbe vevő klinikus rendszerint nem az egész szöveget, hanem csak a konklúziót olvassa el, ezért adott esetben ezen a helyen is rá kell mutatni az esetleges diagnosztikus nehézségekre, hogy ösztönözzük ez által is az egész lelet részletes átolvasását.
A komputerbe írt és központi szerverben tárolt lelet, amely a patológián kívül is hozzáférhető, nincs aláírva. Ilyenkor biztosítani kell, hogy a leletet semmilyen körülmények között se lehessen kívülről megváltoztatni és egy releváns kópiát a Patológiai Osztályon kell tárolni. A legtöbb patológiai lelet nagyon bizalmas, ezért kívülálló a tároló komputer rendszert nem érheti el.
1.6. A kiegészítő leletek készítésének módja és a külső vagy belső konzultáció eredményének közlése
A szövettani anyag további feldolgozása vagy az eset későbbi revíziója során fontos kiegészítő információ keletkezhet. Ilyen például a később elvégzett molekuláris patológiai vizsgálatok eredménye. Ezt helyesebb nem hozzáírni az eredeti lelethez, hanem kiegészítő leletet kell készíteni. Ebben fel kell tüntetni az eredeti leletből megtartott és az esetleg megváltoztatott részleteket, továbbá ki kell emelni azt az új információt, ami a beteg kezelését érintheti. Amennyiben célzott daganatellenes terápia érdekében végeztünk kiegészítő vizsgálatokat, a leletben fel lehet tüntetni, hogy az érvényben lévő szelekciós kritériumok szerint a beteg kiválasztható-e az adott kezelésre. Nehéz esetekben, vagy ha a megfelelő feldolgozásra nincs mód, külső konzultációt igénybe lehet venni. A kísérő levélben fel kell tüntetni az elvégzett szövettani vizsgálat dátumát, a szükséges klinikai adatokat, a klinikai probléma jellegét, a makroszkópos leírást és a küldött blokkokszámát, valamint a kivágás lokalizációját, a munka-diagnózist és a diagnosztikus problémát. Belső konzultáció esetén fel kell tüntetni a megvitatott probléma lényegét és a konzulensek nevét. A leletet először kiadó patológusnak természetesen nem kell feltétlenül egyetértenie a második véleménnyel, a véleménykülönbség lényegét azonban rögzíteni kell.
1.7. A patológiai lelet klinikai következményei
A kórszövettani leletet is figyelembe véve kell dönteni a kezelés módjáról. Ha a kórszövettani lelet alátámasztja a klinikai és endoszkópos diagnózist, alátámasztja a döntést a választott kezelést illetően is. Amennyiben a klinikai és endoszkópos vizsgálatok eredménye és a kórszövettani lelet eltér a választandó eljárás a következő:
a) Ha a kórszövettani lelet daganatos betegséget igazol, a továbbiakban ez a lelet az irányadó. Amennyiben azonban a szövettani diagnózis és a klinikai kép jelentős ellentmondást mutat, a metszetek konzultációs vizsgálata, illetve ismételt mintavétel lehet szükséges.
b) Ha a klinikai és endoszkópos vizsgálat egybehangzó és egyértelmű, ugyanakkor a kórszövettani vizsgálat eredménye bizonytalan vagy negatív, a szövettani anyag újraértékelését, további feldolgozását, második vélemény beszerzését kell kérni vagy újabb biopsziás mintavételt kell végezni. Radikális műtétről vagy agresszív, illetve a beteget más módon megterhelő terápiáról egyértelmű szövettani vélemény birtokában lehet dönteni.
Biopsziából diagnosztizált gasztrointesztinális lymphomák esetén a sebészi rezekció sok esetben a túlélést meghosszabbítja. Az előrehaladott stádium és a sebészi szélek tumoros infiltrációja azonban kedvezőtlen prognosztikai jel, kivéve ha a műtétet követően sugárterápiát vagy kemoterápiát is kapa beteg. A szövettani vizsgálat mellett a PCR alapú diagnózis segítheti a MALT lymphomák konzervatív kezelést követő regressziójának nyomon követését. A PCR vizsgálattal kimutatott klonális B-sejt populáció néha még akkor is megtalálható, ha a szövettani vizsgálat komplett regressziót mutat. Ennek a jelenségnek az a magyarázata, hogy időeltolódás állhat fenn a szövettani és molekuláris regresszió között. Ha szövettani vizsgálattal reziduális lymphoma jelenléte nem igazolható, a kimutatott perzisztáló monoklonális sejtpopuláció további terápiás beavatkozást nem, de időszakos kontrollvizsgálatot indokol.
2. Részletes irányelvek
2.1. Nyelőcső
A nyelőcső alábbi betegségeiben kell endoszkópos biopsziát végezni és szükséges megjelölni, hogy az elváltozás illetve a biopszia helye cm-ben kifejezve milyen távol van a fogsortól:
a) A nyelőcső minden szűkülete esetén az itt található esetleges rákmegelőző állapotok vagy daganatok felderítésére. Amennyiben az eszköz a szűkületen perforáció veszélye nélkül nem vezethető keresztül, legalább abráziós citológiát ajánlatos végezni.
b) Reflux betegség. A gyomorsav és epe reflux miatt az oesophagitis gyakori a nyelőcső alsó harmadában. Ha a gyulladás az egész nyelőcsövet érinti, felmerül az immunhiányos állapot gyanúja. Ilyenkor különféle kórokozókat illetve vírust is keresni kell.
c) Barrett oesophagus. Állandósult reflux következtében alakul ki. A nyelőcső többrétegű laphámja helyén kehelysejteket tartalmazó intesztinális jellegű, nyáktermelő hám jelenik meg, váltakozva laphám szigetekkel. A rövid szegmensű Barrett oesophagus kevesebb, mint 3 cm hosszú. Ilyen esetekben a szövettani diagnózis nehéz lehet, különösen problémás a Barrett-mirigyhám elkülönítése a cardia-nyálkahártya intestinalis metapláziájától. Ilyenkor a diagnózist a károsodott nyálkahártya alatt meglévő nyelőcsőmirigyek és -ductusok jelenléte, valamint immunhisztokémiai vizsgálat (CK7, CK20, CDX2) segítheti.
d) Daganat, vagy annak gyanúja. A nyelőcsőrák leggyakrabban a többrétegű laphámból, ritkán a Barrett nyálkahártyából indul ki. A legtöbb adenocarcinoma Barrett nyálkahártya eredetű, de ettől független nyelőcső kiindulású is lehet. A laphámrák rendszerint polypoid megjelenésű, klinikailag sokszor összetéveszthető lágyrész tumorral vagy gyulladásos polyppal. Laphám papillomák és verrucosus carcinomák, továbbá az egyéb laphámrákok 20-25 százaléka humán papillomavirus (HPV) eredetű.
2.1.1. Az endoszkópos nyelőcső biopszia vagy műtéti rezekátum anyagának előkészítése kórszövettani vizsgálatra (Lásd: Általános irányelvek. Speciális előkészítést nem igényel.)
2.1.2. A nyelőcsőből származó biopsziás vagy műtéti anyag kórszövettani feldolgozásának elvei (Lásd: Általános irányelvek. Speciális előkészítést nem igényel.)
2.1.3. A nyelőcsőből származó biopsziás vagy rezekciós anyag szövettani lelete és az adható fontosabb kórszövettani diagnózisok
a) Gyulladásos elváltozások, Barrett oesophagus és dysplasia esetén a szövettani leletben az alábbiakra kell kitérni: laphámot, junctionalis vagy glanduláris nyálkahártyát tartalmaz-e a metszet,
- van-e kifekélyesedés,
- gyulladásnál annak típusa, súlyossága és kiterjedése,
- kimutatható organizmusok (gomba, vagy vírusfertőzésre utaló inklúziók)
- van-e reflux oesophagitisre utaló jel laphám hyperplasiával,"rete ridges" formációval és a papillák elongációjával,
- felismerhető-e Barrett nyálkahártya, kehelysejteket tartalmazó nyáktermelő hámmal,
- előfordul-e regeneratív hámelváltozás,
- dysplasia esetén annak súlyossági foka (enyhe, súlyos, nem meghatározható),
- szükséges-e újabb biopszia az atypusos hámelváltozások valódi természetének megítélésére.
b) Daganatos betegségek esetén a szövettani leletben az alábbiakra kell kitérni:
- a metszetben lévő ép szövetek jelenléte, különös tekintettel a cardiára,
- a tumor szöveti típusa és differenciáltságának foka,
- a tumor kiterjedése (a nyelőcsőfal infiltrációjának mélysége, érinvázió, a nyirokcsomók érintettsége és a metasztatikus nyirokcsomók száma, a tumor távolsága a rezekciós síkoktól, a TNM-re alapozott tumor stádium),
- prognosztikai faktorok.
Endoszkópos biopszia eseten csak a tumor típusa, differenciáltságának foka, az esetleges érinvázió valamint a metszetben előforduló nem daganatos szövetek és kórokozók jelenléte adható meg. A nyelőcső-gyomor junctio adenocarcinoma külön entitás, a junctio feletti területről kiinduló adenocarcinoma nyelőcső, a régió alatti daganat gyomor eredetű. A tumor prognosztikai faktorai a következők:
- klinikai stádium (ez a legfontosabb prognosztikai jel),
- differenciáltság, a rezekció kiterjedtsége,
- lymphocytainfiltráció (jelenléte kedvezőbb prognózisra utal),
- proliferációs paraméterek (Ki67 jelzési index), DNS ploidia és S-fázis frakció (aneuploid gyorsan proliferáló tumorok kórjóslata kedvezőtlenebb, mint a diploid tumoroké),
- molekuláris faktorok (immunhisztokémiai monoklonális p53 pozitivitás, a HER-2 és int-2 fehérje fokozott megjelenése kedvezőtlen prognosztikai jel).
2.1.4. A nyelőcsőből származó kórszövettani anyag leletének klinikai konzekvenciái
Kezelés szempontjából a nyelőcső laphámrákjai a stádiumtól függően két csoportra oszthatók: (1) Loco-regionalis betegség, amikor a daganat potenciálisan gyógyítható. (2) Előrehaladott betegség a légutak infiltrációjával vagy távoli áttétekkel. Ilyenkor csak palliativ beavatkozás jön szóba. A nyálkahártyára lokalizált laphámrák endoszkópos nyálkahártyarezekcióval is kezelhető, mert ilyenkor a regionális nyirokcsomóáttét kockázata kicsi. Endoszkópos mucosectomia végezhető súlyos dysplasia esetén is. Azon daganat, amelyik a submucosára is ráterjedt vagy még inkább előrehaladott stádiumú, endoszkópos terápiára nem alkalmas, mert a nyirokcsomó áttét valószínűsége több mint 30%. A oesophago-gastricus junctio adenocarcinomáknál szignifikáns összefüggés van a grading és a prognózis között. A jól és a közepesen differenciált tumorral rendelkező betegek 5 éves túlélési aránya kedvezőbb, mint a rosszul differenciált tumort hordozó betegeké.
2.2. Gyomor
A gyomor betegségeiben általában többszörös biopszia a gyakorlat. A szövettani mintavétel az egyes gyomorelváltozásokban azok jellegétől függően a következő legyen:
a) Gastritis chronica esetén:
- a kisgörbület praepyloricus részéből,
- az antrum kis-és nagygörbületéről,
- a corpus nagygörbületéről,
- a subcardialis kisgörbületről.
b) Ulcus ventriculi esetén:
- az ulcus széléről, több helyről,
- az ulcus alapjáról,
- az ulcustól 1 cm-re lévő felső és alsó nyálkahártyából
- az antrum kisgörbületéről.
c) Ulcus duodeni esetén a gyomorból.
d) Rezekált gyomor esetén:
- az anasztomózis területéből,
- a corpus területéből és a subcardialis kisgörbületről.
e) Tumoros folyamat esetén biopszia szükséges annak széléből, belsejéből és a környező ép nyálkahártyából.
f) Polypot lehetőleg egészben el kell távolítani. Biopszia csakakkortörténhet, ha a képlet a rendelkezésre álló eszközzel nem távolítható el. Tisztában kell azonban azzal lenni, hogy ilyenkor a szövettani vizsgálat korlátozott értékű lehet. A gyomornyálkahártya óriásredős megbetegedéseiben (Menetrier-kór, lymphoma) azun."big particle" biopszia ajánlott a redő tetejéből és az árokból, hasonló módon a polypektómiához.
2.2.1. Az endoszkópos gyomorbiopszia vagy műtéti rezekátum anyagának előkészítése kórszövettani vizsgálatra
Az általános irányelvekben megfogalmazottaknál túlmenő speciális előkészítést nem igényel. A mikrohullámmal segített formalinfixálás kifejezetten ajánlott.
2.2.2. A gyomorból származó biopsziás vagy műtéti anyag kórszövettani feldolgozásának elvei (Lásd: Általános irányelvek. Speciális előkészítést nem igényel.)
2.2.3. A gyomorból származó biopsziás vagy rezekciós anyag szövettani lelete és az adható fontosabb kórszövettani diagnózisok
A gyomorból történő endoszkópos biopszia leggyakoribb indikációja a krónikus gastritis, az ulcus és a Helicobacter pylori vagy Helicobacter heilmanii fertőzés következtében kialakult nem-ulcus eredetű dypepsia. A krónikus gastritis többféle osztályozása ismert és használt. Az egyik legegyszerűbb a Wayatt és Dixon osztályozás, ami az etiológiát és a topográfiát kombinálja:
A típusú: anaemia perniciosa-val összefüggő autoimmun gastritis, ami főleg a corpusra lokalizált. B típusú: H. pylori vagy H. heilmanii okozta gastritis, ami főleg az antrumra lokalizált.
C típusú: Kemikáliák-okozta gastritis, ami rendszerint nem-szteroid gyulladásellenes gyógyszerek szedése vagy epés reflux következménye. Ilyenkor a gyulladásos komponens kisfokú, jellemző a nyálkahártya oedema, a mirigyek torzulása, elágazódása, az értágulat és a lamina propria izomrostjainak felszaporodása.
A Sydney krónikus gastritis osztályozás az elváltozás etiológiáját, morfológiáját és endoszkópos kiterjedését veszi figyelembe. Akkor alkalmazható, ha minden régióból legalább két biopsziás szövetminta került eltávolításra. A krónikus gyulladást, a gyulladás aktivitását, az atrófia és az intesztinális metaplázia mértékét enyhe, közepes és súlyos fokozatra oszthatjuk, jelenlétük alapján. A gastritis chronica speciális típusai (lymphocytás, granulomatosus vagy eozinofil) külön kategóriát képeznek. Menetrier betegségben a mirigyek megnyúltak, megcsavarodtak, a nyálkahártya mélyebb rétegeiben cystikusan tágultak, mucinosus metaplázia van a specializált nyálkahártyasejtek helyén és aktív krónikus gyulladás van a lamina propriaban.
A gyomornyálkahártya dysplasia diagnózisa nehéz a jelenlévő kifejezett, esetleg erosiv gyulladás és hámregeneráció miatt, ami maga is dysplasiát utánoz. Dysplasiára utal a mirigystruktúra megváltozása (megcsavarodás, elágazódás, csoportos egymással összefekvő "back to back" mirigyek), a sejtmag atypiája, fokozott mitotikus aktivitás, ami a mirigyek felső részére vagy felszínére is ráterjed.
Krónikus gastritis, fekélybetegség és dysplasia szövettani leletében az alábbiakra kell kitérni:
- a metszetben lévő nyálkahártya típusa (cardia, fundus/corpus, antralis/pyloricus),
- kifekélyesedés van-e,
- a krónikus gyulladás típusa, súlyossága, kiterjedése,
- aktív gyulladás esetén annak súlyossága,
- H. pylori vagy heilmanii jelenléte,
- mirigyatrófia jelenléte és súlyossága,
- intesztinális metaplázia jelenléte, típusa,
- nyálkahártya oedema,
- intraepithelialis lymphocytaszám emelkedés (pl. lymphocytás gastritisben, ritkán Helicobacter fertőzésben)
- a nyálkahártya mirigyek strukturális torzulása,
- értágulat,
- kimutatható egyéb kórokozók (pl. gombák),
- dysplasia jelenléte és súlyossága,
- az esetleges újabb biopszia szükségessége.
A gyomorpolypok lehetnek soliterek, vagy polypózis szindróma részei. Szövettanilag a hám eredetűek a leggyakoribbak, közöttük nem daganatos (hyperplasticus-, hamartomatózus- vagy fundus mirigy polypokat) és daganatos (tubuláris-, villosus-,tubulovillosus- valamint fogazott ("serrated") adenomákat) polypokat különböztetünk meg.
A hyperplastikus polypok gyakoriak, leginkább H. pylori vagy heilmanii fertőzés hatására alakulnak ki. A foveolaris mirigyrégió megnyúlt és megcsavarodott, hámja proliferál, felszíne rendszerint erodált, a mirigyhám egysoros, monomorf, nyáktermelő jellegű. A hyperplastikus polyp talaján a carcinoma kialakulása igen ritka, főleg a dysplasiás területekből indul ki.
A hamartomatózus polypokban a muscularis mucosae izomrostjai felszaporodtak, elágazódnak, a foveoláris mirigyrégió megnyúlik, elágazódik, hyperplasiás vagy cystikusan tágult, a mélyebb mirigyrészek sorvadtak. Ezek a polypok rendszerint a Peutz-Jeghers vagy Cowden szindróma illetve a juvenilis polyposis részjelenségei, ritkák. A rendkívül gyakori, hyperplasiogén jellegű, corpus/fundus területén előforduló fundus mirigy polypban a foveolaris réteg nem érintett, a hyperplasia az oxynticus, mély mirigyeket érinti, bennük fokális,cystikus tágulat alakul ki, és az itt lévő sejtek helyét nyáktermelő sejtek foglalják el. A sporadikus fundus mirigy polyp nem malignizálódik, kiválthatja hosszú idejű protonpumpa-gátló kezelés. Polyposisa esetén benne dysplasia és carcinoma is kialakulhat. Az adenomák valódi daganatok, ritkán fordulnak elő, bennük különböző súlyosságú dysplasiák találhatók, és carcinoma is kialakulhat. A carcinoma jelenlétének valószínűsége az adenoma méretével arányos. Kevesebb, mint 2 cm átmérőjű adenomában a rák előfordulása kb. 2%, a 2 cm-nél nagyobbakban 40-50%. Lapos adenomák nagyobb valószínűséggel alakulnak át carcinomává.
Az előrehaladott gyomorrákokat többféleképpen is osztályozhatjuk. A WHO osztályozás leíró jellegű, e szerint a daganatok lehetnek tubulárisak, papillárisak, mucinózisak vagy pecsétgyűrű sejtesek. Ritka variáns a laphám-, az adenosquamosus- és a differenciálatlan carcinoma. A Laurén osztályozás a carcinomák fejlődésmenetét veszi figyelembe és megkülönböztet inestinális és diffúz típust. A genetikai osztályozás mikroszatellita stabil (MMS) és mikroszatellita instabil (MSI-H) daganatokat különböztet meg. Az MSI-H rákok lehetnek sporadikusak és azMLH1 gén promoter régiójában lévő CpG szigetek rákkal összefüggő metilációja következtében, vagy herediter nem-polypozis colorectalis carcinoma (HNPCC) szindróma részeként alakulhatnak ki és prognózisuk sokkal kedvezőbb, mint az egyéb típusú rákoké.
A korai gyomorrák elkülönítése igen fontos, mert prognózisa rendkívül jó. Lehet bármilyen szövettani típusú, de csaka nyálkahártyára vagy a nyálkahártyára és a submucosára terjed ki, és független a nyirokcsomó státusztól. A nyálkahártyára lokalizált carcinomát a kiterjedése alapján kis mucosa carcinomára (cm) és szuperficiális carcinomára (<4 cm) osztjuk. Ha a korai rák kiterjedten infiltrálja a submucosát, PenA vagy PenB típusról beszélünk. A PenA típusú rákok az ép szöveteket maguk előtt tolva nőnek és kevésbé gyakoriak, mint a PenB típusúak, amelyek sokkal inkább infiltratív növekedésűek. A gyomor egyéb elsődleges daganatai endokrin tumorok, mesenchymalis tumorok vagy lymphomák. A mesencymalis tumorok között kiemelt jelentőségű gasztrointesztinális strómális tumor (GIST), amely lehet lokalizált vagy metasztázist képez, és a tirozin-kináz családba tartozó c-KIT protoonkogén funkciónyerő mutációja következtében alakul ki. A diagnózist a CD117 és CD34 pozitív immunhisztokémia biztosítja, kétséges esetben mutációanalízis végezhető.
A gyomorlimfómák csaknem mindig B-sejtesek, közöttük leggyakoribb a MALT lymphoma. A gyomorpolypok és carcinomák szövettani leletében értelemszerűen az alábbiakra kell kitérni:
- a polyp szövettani jellegzetessége,
- a polyp szöveti típusa (hyperplastikus, hamartomatózus, fundus mirigy típusú, adenoma, stb),
- epiteliális dysplasia jelen van-e, és ha igen, annak súlyossága,
- malignitás fennáll-e a polypban,
- a kimetszés komplett vagy nem,
- a daganat típusa, differenciáltsága és súlyossági fokozata,
- kifekélyesedés van-e,
- nem daganatos nyálkahártya van-e a metszetben,
- a tumorral összefüggő nyálkahártyaelváltozások megfigyelhetők-e,
- szükséges-e újabb biopszia végzése.
2.2.4. A gyomorból származó kórszövettani anyag leletének klinikai konzekvenciái
Idült gastritisben az ismételt biopsziánaka betegség nyomonkövetésében van szerepe. Dysplasia esetén évenkénti kontroll biopszia ajánlott. Azt is figyelembe kell venni, hogy bármely súlyosságú dysplasia hosszú ideig stagnálhat, regrediálhat vagy progrediálhat. Kóros p53 fehérje jelenléte a várható progressziót valószínűsíti. Ha a biopsziás anyagban a dysplasia vagy carcinoma diagnózisa kérdéses, második véleményt is vegyünk igénybe, végső esetben a biopszia megismétlése indokolt. A carcinoma diagnózisa gyomor rezekciót von maga után. Második-harmadik stádiumú MSI-H tumorok esetén az egyébként szokásos adjuváns kezelés hatásossága erősen megkérdőjelezhető. Metasztatikus GIST esetében a terápia optimalizálása érdekében a c-KIT vagy PDGFRA gén funkciónyerő és rezisztenciát okozó mutációjának vizsgálatát el kell végezni. Az alacsony súlyossági fokozatú MALT limfómánál a H. pylori eradikációja az esetek 67-84%-ában remissziót eredményez, főleg azokban az esetekben, amelyekben az elváltozás felszínesen járja át a gyomorfalat. A remisszió ideje 4-6 héttől több hónapig vagy évig változhat, de stabilitása kérdéses.
2.3. Vékonybél és appendix
A vékonybélben a biopsziát az anatómiai elhelyezkedés, a rendelkezésre állóeszköz és az elváltozás jellege együttesen határozza meg. A vékonybél ugyanis - leszámítva a duodénumot, a jejunum rövid felső szakaszát és az alsó ileumkacsot- mintavételre alkalmas fiberoszkóppal nem vizsgálható. Ebből következik, hogy célzottan anyagot venni csak az említett vékonybél szakaszokról lehet. A mintavétel másik módja az un. vak biopszia, amit speciálisan kialakított kapszulával végeznek. Ezzel a módszerrel a vékonybél hosszabb szakaszaiból is vehetünk szövetmintát. Vékonybélbiopsziát a béleredetű felszívódási zavarok kórismézése és a kezelés hatásosságának megítélése, a coeliakia nyomon követése, a vashiányos anaemia vizsgálata, a daganatos betegségek diagnózisa, végül a fertőzéses eredetű diarrhoea felismerése céljából végeznek. Az utóbbi indikációhoz tartozik az AIDS-ben végzett duodénum biopszia is. Daganat gyanúja miatt történő ampulláris és periampulláris biopsziák másik módszertani levélben kerülnek megtárgyalásra.
A vékonybél rezekció leggyakoribb indikációi a Crohn-betegség, az ischaemiás elváltozások, a különféle eredetű stricturák és a daganatok. Ritkán kerül sor rezekcióra diverticulosis, bevérzés vagy rekeszizom betegség miatt. Appendectomiát rendszerint akut appendicitis gyanúja miatt végeznek, de megtörténhet profilaktikus célból is.
2.3.1. Az endoszkópos vékonybél biopszia vagy műtéti rezekátum anyagának előkészítése kórszövettani vizsgálatra A minták speciális orientációjára feltétlenül szükség van, mert ettől függ a bolyhok állapotának helyes megítélése. Éppen ezért a vékonybélbiopsziás szövetmintát a fixálás előtt -sztereómikroszkópos ellenőrzés mellett - szűrőpapíron alapjára kell fektetni, kiteríteni, egy pillanatig megszáradni hagyni, hogy később el ne mozduljon, és csak ezután behelyezni a fixáló oldatba. Ilyen módon eljárva a szövet orientáltan kerül beágyazásra. Elektronmikroszkópos vizsgálat céljára külön vegyünk mintát.
2.3.2. A vékonybélből származó biopsziás vagy műtéti anyag kórszövettani feldolgozásának elvei
Az általános irányelvekben megfogalmazottaknál túlmenő speciális előkészítést nem igényel. Coeliakia esetén négy biopszia vétele javasolt, mert az elváltozás gócos megjelenésű lehet.
2.3.3. A vékonybélből származó biopsziás vagy rezekciós anyag szövettani lelete és az adható fontosabb kórszövettani diagnózisok
A coeliakia jellegzetes szövettani képe a boholyatrófia a felszíni enterocyták károsodásával és a kefeszegély elvesztésével, a bolyhok felszínén az intraepithelialis (CD8+ T-sejtek) lymphocytaszám (IEL) emelkedése (>40/100 epithelsejt),a kripta hyperplasia fokozott mitotikus aktivitással és a krónikus gyulladás, ami a lamina propriát is beszűri. Megjegyzendő, hogy a felsorolt szöveti jelek egyike sem specifikus önmagában coeliakiára, azokat együttesen és igen körültekintően kell értékelni. Másrészt pl. vastag metszetekben gyakran túlértékelhető az egyik legfontosabb eltérés, az IEL-szám mértéke. A diagnózis csak mélyduodenum vagy jejunum minták alapján állítható fel, a nyombél kezdeti szakasza a gyakori pepticus gyulladás miatt erre nem alkalmas. A téves pozitív diagnózis pedig évtizedekig tartó, a beteget megviselő diétát vonhat maga után. Kérdéses esetben érdemes konzíliumi segítséget kérni. Duodénumban a Crohn-betegség szövettani képe rendszerint nem specifikus, leggyakrabban mindössze gócos, aktív gyulladás látható, többnyire granulómák nélkül. Gyanúja leginkábbatípusos lokalizációjú (pl. mélyduodenum) fekélyekesetén merül fel.
A vékonybélpolypok hamartomatózus vagy neoplasztikus eredetűek, a polypoid megjelenésű gyulladásos pseudotumorok ritkák. A Peutz-Jeghers betegség autoszómális domináns öröklődést mutató szindróma, amelyet muco-cutan melanin pigmentáció és főleg a vékonybélben előforduló hamartomatózus polyposis jellemez. A vékonybélen kívüli daganatok kevésbé gyakoriak, ha előfordulnak, a tápcsatorna egyéb régióin kívül a petefészket, a méhnyakat, a heréket, a hasnyálmirigyet és az emlőket érinthetik. A Peutz-Jeghers szindróma mellett 10-18-szor gyakoribb a gastrointesztinális és nem- gastrointesztinális carcinoma. A 19. kromoszómán lévő LKB1 serin/threonin kináz gén heterozigozitásának elvesztése esetén van nagy esély a dysplasiák megjelenésére és azok malignus átalakulásra a Peutz-Jeghers polypban.
Az elsődleges vékonybél daganatok lehetnek jóindulatúak vagy rosszindulatúak és jelentősen ritkábbak, mint a gyomor vagy a vastagbél hasonló tumorai. A vékonybél endocrin tumorai közül a carcinoid tumor a leggyakoribb, mely ebben a lokalizációban rendszerint multiplex, malignus és metasztatizál, serotonin termelése folytán carcinoid szindrómát,agastrintermelő tumorok egy része pedig Zollinger-Ellison szindrómát okoz. Ezeka tumorokagresszívebb biológiai viselkedést mutatnak, mint a nem funkcionáló megfelelőik. Az utóbbiaksokszorjóindulatúakvagy alacsony malignitásúak. Az intesztinális T-sejtes lymphoma kifekélyesedett plakk, vagy szűkület formájában jelenik meg a
proximális vékonybélben. Ezt a betegséget legtöbbször rezekciós preparátumból diagnosztizáljuk. Ritkábban - 6 hónapnál hosszabb klinikai tünetek és gyulladásos bélbetegség gyanúja mellett - csak a gyomorból, duodénumból vagy a colonból származó endoszkópos biopszia áll rendelkezésre. Nehezíti a biopsziából történő diagnózist, hogy a daganatos infiltráció lehet kevéssé kifejezett vagy felszínes, és nem mindig jár cytologiai atypiával. Ilyen esetekben az aberráns fenotípus immunhisztokémiai megjelenítése és a T-sejt receptor (R-lánc) génátrendeződés PCR-rel történő kimutatása vezethet eredményre.
Az appendix tumorai leggyakrabban carcinoidok(tubuláris, pecsétgyűrű sejtes és kevert carcinoid-adenocarcinoma). E tumorok biológiai viselkedésének megítélése nehéz, de az appendixben általában jóindulatúak vagy alacsony malignitásúak, diagnózisuk többnyire véletlen melléklelet. A pecsétgyűrű-sejtes carcinoidok kifejezettebben agresszívek, mint a közönséges megfelelőik, de kevésbé malignusak, mint az adenocarcinomák. A kevert carcinoid-adenocarcinoma kifejezés azokat a daganatokat takarja, amelyek előzetesen fennálló pecsétgyűrű-sejtes carcinoid progressziójából alakultak ki. Ezekben az esetekben az appendix nyálkahártyájában daganatos elváltozás soha nem mutatható ki. A legtöbb pseudomyxoma peritonei (mucinózus anyag található a peritoneum felszínén) az appendix primer nyáktermelő adenocarcinomájánaka peritonealis felszínre történő terjedése következtében alakul ki, de okozhatják az epehólyag, gyomor, vastagbél, hasnyálmirigy, tuba, ovarium, urachus, tüdő és emlő hasonlóan nyáktermelő tumorai is.
A vékonybél biopsziák és rezekciós specimenek szövettani leletében, az elváltozás jellegétől függően, az alábbiakra kell kitérni:
a) Vékonybél biopszia: -a biopsziákszáma,
- kifekélyesedés van-e,
- a bélbolyhok állapota (ép, megrövidült) és szerkezete,
- kripta hyperplasia, boholy- krypta arány,
- a felszíni enterocyták állapota (ép, ellapult, károsodott),
- a kefeszegély megtartott vagy hiányzik,
- intraepiteliális lymphocytaszám (normális, megemelkedett),
- van-e gyulladásos infiltrátum a lamina propriában, ha van, annak eloszlása (gócos, diffúz),
- a gyulladás típusa (nem specifikus, granulomatózus, eozinofil),
- Brunner mirigy hyperplasia, gyomormirigy metaplázia,
- azonosított fertőző ágensek (pl. Giardia lamblia),
- ritka elváltozások (R-lipoproteinaemia, Wipple-kór, amyloidosis)
- daganatok.
b) Vékonybél rezekciós preparátum
- a gyulladásos beszűrődés típusa, eloszlása, súlyossága,
- a nyálkahártyafekély típusa, mélysége,
- elhalás (nyálkahártyára lokalizált, transzmuralis),
- submucosa elváltozások (fibrózis, neuron hyperplasia),
- érelváltozások (dilatáció, pangás, vasculitis),
- a serosa elváltozásai (abscessus, fibrosis, fibrin depositum)
- a polyp vagy tumor típusa,
- az infiltráció kiterjedtsége (mélység, rezekciós síkok, serosa érintettsége), -van-e érinvázió,
- az eltávolított és ezen belül a metasztatikus nyirokcsomók száma,
- a nem tumoros vékonybél nyálkahártya ép-e (különös tekintettel a coeliákiára).
c) Appendix
- gyulladás (akut, krónikus, follikuláris, granulomatózus),
- azonosított kórokozók,
- daganatok (grading, stádium, az eltávolítás teljes/részleges, rezekciós síkok).
Ha az appendixben gyulladás nincs, a szövettani lelet rövid. Ha az anyag mégis tartalmaz klinikai információt, azt a leletbe bele kell foglalni. Ilyenek lehetnek: Warthin-Finkeldey óriássejt (kanyaróra utal), lymphoid hyperplasia (mononucleosis infectiosa részjelensége lehet), endometriosis.
2.3.4. A vékonybélből származó kórszövettani anyag leletének klinikai konzekvenciái
Ha a szövettani vizsgálat coeliakia lehetőségét veti fel, a végső diagnózis a szérumban keringő specifikus antitestek meglététől, és/vagy a glutén megvonást követő klinikai választól függ. Aglutén megvonást követő második biopszia a szöveti válaszra ad felvilágosítást. Ha az ismételt szövettani mintákban a glutén megvonást követően sem látszik javulás, másodlagos felülfertőződést vagy enteropátiával összefüggő T-sejt limfómát kell keresni. A duodénumból származó szövetmintából a Crohn-betegség szövettani diagnózisa rendkívül nehéz, és soha ne állítsuk fel ezt anélkül, hogy konzultáltunk volna a klinikus és radiológus kollégákkal. A hibás szövettani diagnózis következménye még ismert Crohn-betegségben is súlyos lehet, mert a Crohn-eredetű duodenális fekélyt steroidokkal is kezelik, és ez perforációhoz vezethet, ha a fekély mégis peptikus eredetű. Az eltávolított appendixek felében az akut gyulladás szövettanilag igazolható, másik felében a féregnyúlvány szövettanilag ép. Legtöbb esetben az akut gyulladás oka nem meghatározható, kis százalékban ismert (féreg, yersiniosis, amoebiasis, actinomycosis). Crohn-betegség érintheti az appendixet, ugyanakkor a granulóma jelenléte nem szükségszerűen jelent Crohn-betegséget.Colitis ulcerosa szintén előfordulhat az appendixben még a proximális colon érintettsége nélkül is, azonban rendszerint az ilyen elváltozása már korábban felismert betegség részjelensége. A coecum vagy az appendix daganata is okozhat akut appendicitist a lumen obstrukciója révén. Ha az eltávolított féregnyúlvány serosája gyulladt de a nyálkahártya ép, appendixen kívüli okokat kell feltételezni. A serosa akut gyulladása gyakran fiatal asszonyoknál látható, mint acut salpingo-oophoritist követő másodlagos hashártyagyulladás. Krónikus follikuláris vagy granulomatózus gyulladás meglétekor kötőszövet betegségre, Crohn-betegségre, yersiniosisra, tuberkulózisra lehet gondolni.
2.4. Vastagbél és végbél
Az endoszkópiával összekötött célzott biopsziának mind a vastagbél idült gyulladásos, mind daganatos elváltozásaiban nem csak diagnosztikus, hanem esetenként terápiás jelentősége is van. Gyulladásos betegségek esetében elengedhetetlen a kórisme felállításában és a gyulladás kiújulásának felismerésében, az adenomák eltávolításának és a kiújulás folyamatos ellenőrzésének pedig kiemelkedő szerepe a vastagbélrák megelőzésében. A vastagbél idült gyulladásos megbetegedéseiből vett célzott biopszia, egyeztetve az endoszkópos lelettel, alátámasztja az ulcerativ colitis kórismét, vagy a specifikus granuloma jelenléte biztosítja a Crohn-betegség diagnózisát. Ezekben az idült colitis-formákban több helyről kell szövetmintát venni, így a coecumból, a colon ascendensből, a colon transversumból, a sigmabélből és a rectumból. A kísérőlevélben a patológussal közölni kell a betegség fennállásának időtartamát, a klinikai lefolyást, a nyálkahártya elváltozásainak minőségét, a fekélyek és polypoid elváltozások számát és makroszópos megjelenését, mert az endoszkópos lelet megkönnyíti a szövettani értékelést. Lényeges a gyulladás kiterjedésének ismerete is. Jobboldali colonfelet érintő folyamatnál tudni kell, hogy az ráterjedt-e a terminális ileumkacsra. Minden olyan colitis ulcerosában szenvedő beteg, akinek a betegsége több mint 10 éve fennáll és az egész vastagbélre kiterjed, fokozottan hajlamos colorectalis carcinomára. Tekintettel arra, hogy a vastagbélben igen gyakori a valódi adenoma és ennek malignus átalakulása, a protrudáló elváltozások egészben történő eltávolítása megkülönböztetett fontosságú. Gondoljunk arra, hogy a biopszia legfeljebb az adenoma tényét erősítheti meg de nem ad áttekintést az egész elváltozásról, pl. arról, hogy van-e infiltráció a nyélben vagy sem. Éppen ezért az adenoma bármelyik típusának diagnózisát polypektómiának kell követnie. Különösen herediter polyposis/rák-szindrómák esetén, lényegében negatív lelet mellett észlelt minimális endoszkópos eltérések észlelésekor is szükséges a biopszia vétele a flexura hepaticából, a flexura lienalisból, a colon descendensből és a rectumból, mert a kezdődő intramucosalis elváltozások csak így ismerhetők fel. Az adenomák vizsgálatával kapcsolatban a patológus tudomására kell hozni, ha halmozódásra utaló elváltozásokról van szó. Általában közölni kell a polypokszámát, megjelenési formáját és nagyságát. Carcinoma endoszkópos gyanúja esetén a kórszövettani vizsgálat szempontjából ugyancsak lényeges annak ismerete, hogy van-e a rák mellett adenoma vagy esetleg második carcinoma.
2.4.1. Az endoszkópos vastagbél biopszia vagy műtéti rezekátum anyagának előkészítése kórszövettani vizsgálatra és feldolgozásának általános elvei.
(Lásd: Általános irányelvek. A szövettani feldolgozás különös előkészítést nem igényel, ha mód van rá, a tumor szövetből és a szomszédos ép nyálkahártyából célszerű eltenni fixálatlan mélyfagyasztott szövetmintát további genetikai vizsgálatok céljára.)
2.4.2. A vastagbélből származó biopsziás vagy műtéti anyag kórszövettani diagnosztikájának általános elvei
Az ép vastagbél nyálkahártyában a mirigyek egymással párhuzamosan helyezkednek el, a kripta régió közvetlenül a muscularis mucosae fölött van. A kripták szerkezete és egymástól való távolsága csekély természetes variációt mutat, elágazódó kripták előfordulnak. A mirigyeket bélelő hám abszorptív sejtekből, kehelysejtekből és endokrin sejtekből áll, Paneth-sejtek normálisan csakacoecumban és a proximáliscolonbanfordulnakelő. A Paneth-sejtek megjelenése a disztális colonfélben krónikus gyulladás következménye. T-lymphocyták és elszórtan eozinofilek a mirigyek között a felszínes nyálkahártya régióban normálisan is megfigyelhetők. Apoptotikus sejtek jelenléte szintén normális lelet. Neutrofilek előfordulhatnak a lamina propriában és a kapillárisok lumenében, de jelenlétük a felszínen vagy a kriptákban kóros folyamatra utal. Krónikus gyulladás domináns sejtes elemei a plazmasejtek. A kripták bázisa és a muscularis mucosae között felszaporodott plazmasejtek és lymphociták erősen utalnak krónikus gyulladásos bélbetegségre (basalis plasmocytosis). Lymphoid aggregátumok és tüszők normálisan szintén jelen lehetnek a vastagbél nyálkahártyában. A tüszőket fedő hám különbözik a szokásos felszíni hámtól, mert a sejtek inkább köbösek mint hengeresek és nagyszámú intraepiteliális lymphocyta is megfigyelhető. Az említett jelenségeket nem szabad összekeverni kóros folyamatokkal. Megjegyzendő, hogy vastagbél biopsziák esetén is fontos a szövetminták helyes orientációja és a lokalizáció pontos feltüntetése.
A vastagbélrák rákmegelőző állapotai a következők: aberráns krypta gócok, adenoma dysplasiával, hyperplasticus polyp, juvenilis polyp, továbbá a colitis ulcerosa és a Crohn-betegség. A hyperplasticus polypokat és a hyperplasticus polyposis szindrómát (nem azonos a familiáris polyposissal) korábban nem tekintettük rákmegelőző állapotnak. Néhány soliter hyperplastikus polypban azonban dysplasia előfordul. A dysplasia néha a mirigyek fogazottságával jár együtt, az ilyen elváltozásokat fogazott ("serrated") adenomának nevezzük. Ez abban különbözik a hyperplastikus polyptól, hogy a tubulovillosus struktúra sokkal komplexebb,asejtekcytoplazmájánakeozionfiliája kifejezettebb és az endokrin sejtek hiányoznak, végül szemben a hyperplastikus polyppal, a BRAF gén E600V mutációja gyakori. A fogazott adenoma nem felel meg valódi adenomának, mert a proliferációs zóna nem terjed ki az egész elváltozásra, hanem csak a krypták alapján figyelhető meg. A többszörös hyperplastikus polypok és fogazott adenomák nagyobb rákkockázatot jelentenek.
Adenocarcinomát akkor lehet diagnosztizálni, amikor a daganatos mirigyek a muscularis mucosae-t áttörik. A diagnózis a jól orientált biopsziás anyagban rendszerint könnyű, kis biopsziás mintából azonban nehéz lehet eldönteni, hogy az anyag vajon adenomából származik-e, vagy a tumoros infiltráció már fennáll. Ilyenkor a sejt- és a mirigy strukturális rendellenességéneksúlyossága, valamint a környező stroma állapota segítheti a diagnózist. Stroma desmoplasia malignitás mellett szól.
A rezekciós specimen sikeres vizsgálatához azonnali és optimális fixálás szükséges, ami az autolysist meggátolja. A carcinoma diagnózisa ilyen esetekben nem jelent problémát, de nagyon fontos a daganat makroszkópos és mikroszkópos kiterjedtségének meghatározása. Erre a célra a legtöbb laboratóriumban az egyszerű és reprodukálható Dukes stádium beosztás, illetőleg ennek változatait, az Astler-Coller vagy az Australian Clinico-Pathological System (ACPS) rendszert használják. Rectum tumoroknál nagyon fontos a mélységi, valamint az alsó és felső rezekciós sík megítélése. Ha ezek valamelyikét a tumorszövet eléri, a kiújulás veszélye nagy, ezért a műtét palliatívnak tekintendő.
2.4.3. A vastagbélből származó biopsziás vagy rezekciós anyag szövettani lelete és az adható fontosabb kórszövettani diagnózisok
A gyulladásos vastagbélbetegségek korrekt diagnózisa komoly prognosztikai és terápiás következményekkel jár. Éppen ezért fontos tudni, hogy a különféle colitisek szövettani képe egymást átfedheti. Mind a felnőttek mind a gyermekek a colon vagy rectum biopsziáiban megfigyelt gyulladásos jelek elsősorban a colitis ulcerosa, a Crohn betegség vagy a fertőzéses eredetű colitis lehetőségét vetik fel. A differenciál-diagnosztikában felnőtteknél az ischemiás, az irradiációs, a mikroszkópikus (lymphocytás és collagen) colitis, gyermekeknél a tehéntej vagy egyéb allergiás colitisek fennállásának lehetőségét kell mérlegelni. Mindezen elváltozásoknak jellegzetes klinikai tünetei is vannak. Tekintve, hogy mikroszkópikus colitis gyakran társul coeliakiával, ez irányú további vizsgálatok indikálhatók. Avastagbélben a hyperplastikus polypokés ezt követően azadenomáka leggyakoribbak. A hamartomatózus polypok (Peutz-Jeghers polyp,juvenilis polyp) gyermekkorban és fiatal felnőttkorban fordulnakelő. Az úgynevezett jóindulatú lymphoid polypok egyesével, vagy a diffúz lymphoid polyposis részjelenségeként jelentkeznek. A soliter lymphoid polypok a rectumban találhatók és kifejezett nyiroktüszőkből épülnek fel. Lymphoid polyposis főleg gyermekkorban fordul elő és leginkább vírusinfekcióra adott választ jelent, de leírták familiáris formáját is.
Az adenomában kialakuló valódi dysplasiás és malignus elváltozások diagnózisát a sejtek atypiájára, szabálytalan elhelyezkedésére, a desmoplasiára, a kóros mirigystruktúrára és differenciáltságra kell alapozni. Azt a szövettanilag carcinomára emlékeztető elváltozást, amely nem infiltrál helyesebb súlyos dysplasiának tekinteni (in situ carcinoma diagnózis nem javasolt), mert ilyenkor áttét nem alakul ki. Ha az adenomában a tunica propria infiltrációja fokálisan megjelenik, de submucosa invázió nincs, intramucosalis adenocarcinoma diagnózis javasolt, melynek terápiája a súlyos dysplasiával egyező. Adenocarcinoma in polipo diagnózist a submucosát is infiltráló daganatra kell fenntartani. Ez esetben a terápiára vonatkozó javaslatok terén a vélemények megosztottak, a legújabb álláspont szerint rezekciós műtét ilyenkor is csak bizonyos esetekben szükséges (lásd 2.1.4. fejezet). Néhány nagyobb, főleg hosszabb ideje fennálló adenomában mirigyhám szigetek találhatók mélyen a muscularis mucosae alatt is. Ez a jelenség carcinomás infiltrációt utánozhat, valószínűleg a polyp nyelének többszörös magcsavarodása következtében alakul ki és un, pseudo-infiltrációnak tekinthető. Az ilyen mirigyeknél hiányoznak a malignitás szövettani kritériumai és a valódi daganatos növekedést kísérő desmoplasticus kötőszöveti reakció (a mirigyek körül többnyire tunica propria jellegű, laza, lymphoid stroma van!), továbbá gyakran tágult kapillárisok és haemosiderin pigmentáció figyelhető meg. A familiáris adenomatosus polyposis (FAP) jellegzetessége a sokszor igen nagyszámú polyposus vagy intramucosalis adenoma megjelenése a colonban és rectumban. Ezek mellett a vékonybélben adenomatosus polypok, intraabdominális desmoid tumorok, a retina pigment hámjánakcongenitális hyperplasiája,osteomákés csont cysták is kialakulhatnak. A Gardner és Turcot szindróma lényegében a FAP variánsainak tekinthető. Az adenomák megjelenése 10-20 éves kor között várható, számuk az életkor előrehaladtával nő. A FAP diagnosztikus kritériumai a következők:
(a) 100 vagy több colorectalis adenoma.
(b) Jellemző családi anamnézis és legalább az epidermoid cysta, osteoma vagy desmoid egyikének megléte.
(c) Az APC gén mutáció kimutatása egyedi DNS-teszt segítségével. Becslések szerint az összes vastagbélrák kevesebb mint 1%-a FAP eredetű.
A típusos Peutz-Jeghers polyp centrálisan simaizmot tartalmaz, a mirigyek villózusak vagy elágazódóak és lefűződhetnek a kötőszövetbe, ami valódi daganatos infiltrációval összekeverhető.
A familiáris juvenilis polyposis betegségben a hamartomatosus polypok elsősorban a vastagbélben és a végbélben jelennek meg de előfordulnak a gyomorban és a vékonybélben is. Az ilyen betegek fokozottan hajlamosak gastrointestinalis rákra. A hamartomatózus polypok mellett ritkábban valódi adenomák is megtalálhatók, illetve a juvenilis polypok mintegy felében enyhe dysplasia alakul ki, így az elváltozás gyakran hamartomatózus polyp -adenoma kevert fenotípusú. A polypokból kialakult carcinomák szövettanilag rosszul differenciáltak vagy nyáktermelőek. A kórképet a 18q21.1 kromoszóma régióban lévő tumor szupresszor SMAD4/DPC4 gén örökletes mutációja okozza.
A Cowden-betegség klinikai jellemzői a következők: a bőrben trichilemmomák, a vastagbélben hamartomatosus polypok jelennek meg, gyakori az uterus leiomyoma, a follikuláris vagy papilláris pajzsmirigyrák, az emlő fibrocystás betegsége és carcinomája. Ezek mellett macrocephalia, mentális retardáció és a kisagy gangliocytomája is előfordul. A betegséget a PTEN gén mutációja okozza. A mutáció kimutatása elegendő a Cowden-betegség diagnosztizálására, a mutáció hiánya azonban nem diagnosztikus értékű. A Bannayan-Ruvalcaba-Rilley-szindróma szintén a PTEN gén mutációjára vezethető vissza, fő tünetei a macrocephalia, a haemangiomatosis, a lipomatosis és a foltozott penis. A tünetek sokszor nagyon hasonlítanak a juvenilis polypózis és a Cowden-betegség tüneteire és ezért a Bannayan-Ruvalcaba-Rilley-kór lényegében része a PTEN-hamartoma-tumor szindrómának.
A vastagbélrákokat kétféleképpen osztályozhatjuk. A WHO osztályozás szerint vannak tubuláris, mucinózus, pecsétgyűrű-sejtes, adenosquamosus, medulláris vagy differenciálatlan carcinomák. A genetikai osztályozás megkülönböztet microsatellita stabil (MSS) és kromoszómálisan instabil, valamint mirosatellita instabil (MSI-H) és kromoszómálisan stabil, végül kevert fenotípusú (MSI-L) rákokat. Az MSS rákok adenomákból alakulnak ki az un. adenoma-carcinoma szekvencia során és az összes vastagbélrák mintegy 65%á-t teszik ki. Ezeka rosszabb prognózisú daganatok. Az MSI-L daganatok legnagyobb része sporadikus hyperplastikus polypból vagy a fogazott adenomából indul ki, előfordulási arányuk 15% és kórlefolyásuk alig valamivel kedvezőbb, mint az MSS típusú rákoké. Az MSI-H vastagbélrákok lehetnek sporadikusak vagy örökletesek. Familiáris előzmény nélkül inkább a jobb colonfélben, valamivel gyakrabban nőkben és átlagosan 70 éves kor fölött jelentkeznek. A tumorok soliterek vagy többszörösek, általában differenciált adenocarcinomák, gócos nyáktermeléssel és a daganatos mirigyek jellegzetes lymphocytás infiltrációjával. A p53 fehérje elszórtan csupán egy-egy daganatsejt magjában mutatható ki. Az MLH1 fehérje a nem-tumoros sejtmagokban immunhisztokémiával láthatóvá tehető, a daganatszövetben gócosan részlegesen vagy teljesen eltűnik. A herediter nem-polyposis colorectalis carcinoma (HNPCC, Lynch szindróma) szintén MSI-H fenotípust mutat. A betegségre hajlamos családtagok mintegy 85%-ában egymás után több generációban már fiatal korban és elsősorban a jobb colonfélben megjelenik a vastagbélrák. Az átlagos életkor 45 év, a tumor 70%-os gyakorisággal a flexura lienálistól proximálisan helyezkedik el. Egy időben több carcinoma is kialakulhat, mellettük néhány polyposus adenoma előfordulhat. Adenomák nem nagy számban, de valószínűleg gyakrabban fordulnakelő, mint a hasonló kor-összetételű kontrollokban. Míg egy szokványos polyp esetenként 8-10 év alatt alakul át carcinomává, a HNPCC polyp 2-3 év alatt malignizálódik. A HNPCC tumorok szövettani képe nagyon jellemző és már hematoxylin-eosin festésnél is utal a betegségre. A daganatok általában jól körülírtak és expanzív növekedési típust mutatnak. Szövettanilag rendszerint kevert szerkezetűek, egyes területeken differenciált mirigyes struktúrájúak, más részeken nyáktermelő vagy medulláris megjelenésűek, nem mirigyeket, inkább sejtkötegeket vagy sejtfészkeket képeznek. Jellemző a tumort infiltráló (intraepitelialis, CD3 pozitív) T-lymphocyták (TIL), jelenléte a nem-mucinosus területeken. A peritumorális B-lymphocyta aggregáció (SIL) szintén gyakran előfordul. A daganatsejtmagok relatíve egyformák, világosak (diploid DNS tartalmúak), nagy eosinofil nucleolust tartalmaznak. A betegséget leggyakrabban azMLHI vagy MSH2 gén mutációja okozza, ritkákaz egyéb "mismatch repair" gének (MSH6, PMS1, PMS2) mutációja. A felsorolt gének funkció-esztő mutációja és a heterozygozitás elvesztése (LOH) következtében a kódolt fehérje immunhisztokémiai festődése a súlyos dysplasiás mirigyekben és a ráksejtekben kiesik, az ép nyálkahártya mirigyekben, és a stromális sejtekben vagy lymphoid elemekben az egyik (apai vagy anyai) allél épsége miatt kimutatható. Vastagbélben a tiszta laphámsejtes, vagy kevert adenosquamosus carcinoma illetve az elsődleges lymphoma ritka. Neuroendocrin tumorok rendszerint kis nyálkahártya nodulusok formájában jelentkeznek, főleg a rectumban, de nagy, kifekélyesedő, rákra emlékeztető tumorok is előfordulnak.
Hirschsprung-betegségre jellemző a ganglionsejtek hiánya a submucosában, amelyet az idegek hyperplasiája és az idegrostok proliferációja kísér. Ezek a jellegzetességek nem jól látszanak a H&E metszetekben, ezért S-100 immunfestés is szükséges. A betegséget aszerint szokták osztályozni, hogy a ganglionsejt-hiányos bélszakaszok hova lokalizálódnak és milyen hosszúak. A rectum mindig érintett, ezért a biopsziát innen kell venni. A mintavétel helye legalább 2 cm-rel az anusgyűrű fölött legyen és a biopsziának a submucosát is tartalmaznia kell.
A vastagbél biopsziákés rezekciós specimenek szövettani leletében az elváltozás jellegétől függően az alábbiakra kell kitérni:
A) Vastagbél biopszia, gyulladásos bélbetegség gyanúja
- hámelváltozások:
- felszíni erózió, kifekélyesedés,
- a kripta strukturális elváltozásai,
- krypta abscessus, atrófia, óriássejtes reakció a krypták körül,
- a nyáktermelés csökkenése,
- Paneth-sejtes és/vagy pseudopylorikus metaplasia,
- epitheliális dysplasia
- a lamina propria állapota:
- a gyulladásos sejtpopuláció típusa, eloszlása,
- a granuloma jelenléte vagy hiánya,
- a submucosa érintettsége,
- stroma fibrosis, oedema, értágulat,
- intraepitheliális lymphocytaszám emelkedés (jellemző pl. lymphocytás colitisre)
- bazális membrán megvastagodás (jellemző kollagén colitisre),
- subepithelialis apoptosis (jellemző a gyógyszer indukált colitisekre),
- egyéb specifikus rendellenességek:
- kórokozók,
- besugárzás-okozta elváltozások,
- ischaemiás elváltozások.
B) Rezekciós specimen gyulladásos bélbetegségek esetén
- a betegség eloszlása és kiterjedése,
- kifekélyesedés megléte és típusa,
- a gyulladás kiterjedtsége, típusa,
- egyéb nyálkahártyaelváltozások,
- a submucosa, a muscularis propria és a serosa elváltozásai,
- nyirokcsomó státus (nem-specifikus hyperplasia, granulóma)
- előfordul-e dysplasia vagy malignus átalakulás, és ha igen, ezek súlyossága, kiterjedtsége.
C) Polypektómia. A leletben fel kell tüntetni a polyp típusát. Ez a következő lehet:
- hyperplastikus (metaplasztikus) polyp,
- hamartomatosus (Peutz-Jeghers polyp, juvenilis polyp),
- gyulladásos polyp,
- jóindulatú lymphoid polyp,
- adenoma
- tubuláris, tubulovillosus, villosus,
- méret,
- a dysplasia súlyossága,
- részleges vagy komplett excisio,
- pseudo-invázió vagy valódi invázió jelenléte.
D) Rosszindulatú daganatok műtéti preparátuma:
- a tumor típusa, a differenciáció foka,
- a tumor genetikai státusa, ha erre mód van (MSS, MSI-H, MSI-L),
- a KRAS 12. vagy 13. codonjánakés a BRAF 600. codonjának mutációja vagy annak hiánya
- a daganatos terjedés nagysága, az érbetörés jelenléte,
- a terjedés mintája (expanzív, diffúz),
- lymphocyta infiltráció hiánya vagy jellege a növekedési zónában,
- extramuralis, perineurális terjedés,
- tumorral összefüggő fibrosis,
- regressziós jelek
- az eltávolított és a metasztatikus nyirokcsomók száma,
- peritumorális nem-nyirokcsomó áttétek,
- a környező szervek érintettsége (uterus, vékonybél, húgyhólyag),
- a tumor távolsága a sebészi szélektől,
- a tumor melletti nyálkahártya állapota
- soliter vagy multiplex polypok, -gyulladásos bélbetegségek,
- divertikulózis,
- besugárzás-okozta nyálkahártyaelváltozások.
e) Különféle egyéb bélelváltozások miatt végzett műtétek preparátumai:
- diverticulosis:
- diverticulitis, tályogos beolvadás,
- lokális peritonitis,
- fistula, strictura, haemorrhagia,
-járulékos "chronic idiopathic inflammatory bowel disease", CIBD (diverticulosis betegség, ami ulcerativ colitist vagy Crohn-betegséget utánoz),
- ischemiás colitis, irradiatios colitis, arteritis:
- a nyálkahártya akut és krónikus ischaemiás elváltozásai
- submucosa vasculitis, irradiációs érelváltozások, atípusos fibroblasztok, fibrózis,
- a muscularis propria és serosa elváltozásai, mesenterialis érelváltozások,
- idiopathiás megacolon, idiopathiás constipatio, neuronalis dysplasia, Hirschsprung-betegség, progresszív szisztémás sclerosis,
- ki kell térni a nyálkahártya, a submucosa, a muscularis propria és a subserosa kóros elváltozásaira. 2.1.4. A vastagbélből származó kórszövettani anyag leletének klinikai konzekvenciái
Mind a colitis ulcerosa, mind a Crohn-betegség elsősorban endoszkópos diagnózis. A pozitív patológiai lelet megerősíti a klinikai diagnosztikus eljárás eredményét, a negatív lelet azonban nem zárja ki az említett betegségek meglétét. A rectum nyálkahártya soliter felületes acut fekélye előzetes colitises anamnézis nélkül az AIDS lehetőségét is felveti, ilyenkor szerológiai ellenőrzés javasolt.
Az adenoma (dysplasiával vagy anélkül) csakpolypektómiát igényel, ami nem csak a helyes diagnózist lehetővé tévő, de egyúttal terápiás beavatkozás is. Biopsziás anyagban a súlyos dysplasia és a differenciált carcinoma elkülönítése sokszor nehéz, nagy a felül- illetve alulértékelés veszélye, ezért radikális műtét előtt második vélemény kérése és ismételt biopszia végzése javasolt. A polypectomia az újabb szemlélet alapján elégséges beavatkozás intramucosalis carcinoma, illetve olyan, a submucosát is infiltráló daganat esetében is, amely legalább 1 mm-es ép szegéllyel lett eltávolítva, nem rosszul differenciált és nyirokérinvázió nem mutatható ki. Ekkora fennálló metastasis valószínűsége minimális. Az invazív carcinoma diagnózisa sebészi beavatkozást, a lymphoma diagnózisa elsősorban sugár- és/vagy kemoterápiás kezelést jelent. A MALT lymphoma mellett általában fennálló H. pylori fertőzést antibiotikus kezeléssel meg kell szüntetni.
Az örökletes rákszindrómák diagnózisának egyik legfontosabb kezdeti lépése a családi anamnézis összeállítása. Ezt a munkát a beteget először észlelő orvos végezheti el. A vizsgálatnak ki kell terjednie a családban előforduló összes ráktípusra, a daganat előfordulásának helyére, multiplicitására, az adott tumorral összefüggő rákmegelőző állapotok (pl. adenomák) előfordulási gyakoriságára, számára, az érintettek korára az elváltozás jelentkezésekor, végül a megelőző patológiai vizsgálatok eredményére is, ha az lehetséges. A diagnózis megerősítésére molekuláris genetikai teszt elvégzése szükséges, ezek után lehet a kezelés, a gondozás és a családtagok szűrésének legjobb módját meghatározni. A herediter nem-polyposis eredetű colorectalis carcinoma (HNPCC) esetén - függetlenül a carcinoma nagyságától - a TNM-re alapozott első és második stádiumban biztosan nem, de legtöbbször harmadik klinikai stádiumban sem igényel a betegség adjuváns kemoterápiát, hanem meg lehet elégedni a radikális műtéttel, mert a HNPCC kórlefolyása e nélkül is nagyon kedvező, az 5 éves túlélési arány 90% fölött van. Az esetleg alkalmazott DNS-t károsító kemoterápia ezekben a betegekben néha második primer rosszindulatú daganat kialakulásához vezet. Rákszindrómák műtéte után a visszamaradt vastagbélben néhány hónapon vagy éven belül újabb daganatok jelenhetek meg. A vastagbélrák mellett egyéb carcinomák előfordulási gyakorisága is jelentős, ezek a következők: endometrium, ovárium, vesemedence/uréter, vékonybél, gyomor, agy, máj- és epeutak, pancreas, bőr (faggyúmirigy adenoma és carcinoma, keratoacanthoma). Postoperativ betegkövetéskor a kontrollvizsgálatoknak ezekre a lokalizációkra is ajánlatos kitérni.
Ha a HNPCC kétségtelen klinikai, patológiai és genetikai bizonyítékai megvannak, az érintettek évenkénti colonoscopos kontrollja szükséges 20-25 éves kortól kezdődően, legalább 15 éven át. Más vélemények szerint az ellenőrzés 3 évenként is megfelelő, azonban a vastagbélrák felgyorsult kialakulása újabban bizonyítást nyert. A vastagbélen kívüli daganatos előfordulás vizsgálata, ezen belül az endometriumrák transvaginális uktrahangos szűrése és a petefészekrákCA-125 markerrel történő keresése 30 éves kor fölött szintén indokolt. Figyelembe kell azt is venni, hogy a petefészekrák kimutatásának ajánlott módszere nem elég érzékeny, illetve az említettektől eltérő lokalizációjú daganatok felismerése nehéz. Az összes ismert nehézség ellenére a HNPCC szűrése szükséges, mert a beteg meggyógyítható, a diagnózis és gyógykezelés együttes költsége pedig a daganat korai fázisában sokkal alacsonyabb, mint a betegség előrehaladott stádiumában.
A sporadikus MSI-H vastagbélrákok kórlefolyása is kedvezőbb, mint az azonos klinikai stádiumú MSS vastagbélrákoké. Az ebbe a kategóriába tartozó, de BRAF 600. codonjának V600E mutációját hordozó tumorok várható körlefolyása azonban rosszabb, minta hasonló, de BRAF negatív tumoroké.
Ellentétes biológiai viselkedés tapasztalható az MSS és MSI-H típusú rákoknál. Az előbbiek kórlefolyása rendszerint kedvezőtlen, ugyanakkor 5FU alapú adjuváns gyógyszeres kezelésre relatíve jól reagálnak. Ezzel szemben az MSI-H carcinomák kórlefolyása kedvezőbb, de nem jól reagálnak erre a terápiára. A klinikai gyakorlat számára tehát nagyon fontos megkülönböztetni ezt a kétféle daganatot.
A K-RAS gén mutáció kimutatásával kapcsolatban az ezen témával foglalkozó módszertani levél ajánlása javasolt.
Az Egészségügyi Minisztérium
módszertani levele
A hematológiai minták feldolgozásáról és patológiai diagnosztikájáról
Készítette: a Patológiai Szakmai Kollégium
Bevezetés
Az elmúlt években a hematológiai betegségek diagnosztikája robbanásszerű változáson ment keresztül, amely a patológiaokatésa patológiai diagnosztikát újkihívásokelé állította. A diagnosztika szerves részévé váltak a szövettani és immunhisztokémiai eljárásokon túlmenően az áramláscitometriai, citogenetikai, "in situ" hibridizációs és molekuláris patológiai eljárások. Ennek eredményeként a 2008-ban megjelent WHO osztályozás a hematológiai betegségeket morfológiai, fenotípus és genotípus alapokon osztályozza. További kihívásokat jelent, hogy a betegségek egy részénél a kezelés molekuláris clpontok ellen irányul illetve a kezelés indikációja és finanszírozása is genetikai illetve molekuláris eltérések alapján lehetséges. Ezeknek a változásoknak alapján a Patológiai Szakmai Kollégium indokoltnak látja szakmai levél megfogalmazását a hematológiai betegségek patológiai diagnosztikája tekintetében. A Patológiai Szakmai Kollégium a következő pontokba foglalva látja a haematológiai betegségek diagnosztikájának minimális követelményrendszerét:
1. A hematológiai betegségek diagnózisa hematopatológiai centrumban (továbbiakban centrum) történjen: A hematológiai betegségekdiagnosztikája költség és időigényes folyamat, így - a nemzetközi gyakorlattal összhangban - magyarországi viszonyok között sem finanszírozható, hogy minden patológiai diagnózist végző osztályon elérhető legyen a hematológiai diagnosztikához szükséges eszköztár. Ezen túl megfelelő évi vizsgálati szám szükséges a nagyobb betegségcsoportokban (myelodysplasia és acut leukaemiák, chronicus myeloproliferativ betegségek, lymphomák), egyenként, a megfelelő szakértelem szinten tartásához, továbbfejlesztéséhez és a vizsgálatok gazdaságosságának biztosításához. Az egyes fő betegségcsoportokban évi legalább 80 - 100 vizsgálati szám szükséges. Az ennek illetve az alábbiaknak eleget tevő diagnosztikai egység haematopatológiai centrum, melynek akkreditálása és regisztrálása 3-4 évekként a PSZK által kijelölt bizottsági vélemény alapján kívánatos.
1.1. A centrum infrastrukturális minimumfeltételei: A centrum működéséhez nélkülözhetetlen, hogy a diagnosztizálandó betegség (csoport) jelenlegi WHO klasszifikáció (l. alább) szerinti kritériumai vizsgálatához elengedhetetlen, alábbiakban felsorolt infrastrukturális feltételek közül szükségesek rendelkezésre álljanak. A centrum működésében nem kizáró ok, ha az adott diagnosztikus hely az általa nem végzett vizsgálatok eredményeit más laboratóriumoktól be tudja szerezni, továbbá azokat értelmezni tudja. Ajánlatos azonban, hogy az adott centrum a hozzá érkező mintákról minden részletre kiterjedő "komplex diagnózist alkosson".
a. Alap szövettani és festési eljárások (ha lehetséges automatizált)
b. Immunhisztokémiai eljárások (preferáltan automatizált)
c. Áramlási citometria (legalább 3 színű jelzés)
d. Metafázis citogenetika - molekuláris citogenetika
e. In situ hibridizáció - interfázis citogenetika
f. PCR és RT-PCR végzésére alkalmas rendszer
g. Valós idejű RT-PCR végzésére alkalmas rendszer
h. DNS szekvenáláshoz szükséges rendszer
1.2 A centrum személyi feltételei: A hematológiai diagnosztikát arra specializálódott, az előzőekben felsorolt technikákat ismerő személy kell, hogy végezze. A centrum működésének fontos része, hogy a centrumban több mint egy szakember dolgozzon, hogy biztosítva legyen a konzultáció lehetősége és a folyamatos működés.
1.3. A centrumok ellátási területe: A centrumok elsősorban a területébe tartozó klinikák és osztályok diagnosztikus tevékenységét látják el, azonban ez nem zárja ki annak a lehetőséget, hogy más intézetekből érkező mintákat is diagnosztizáljon az adott centrum.
2. A hematológiai minták feldolgozása: A hematológiai minták feldolgozása során törekedni kell arra, hogy a WHO ajánlásában foglalt minden vizsgálati eljárásra előkészítsük a mintát. Az adott minta patológiai diagnózisán túlmenően törekedni kell arra, hogy a betegség követhető legyen, illetve újabb terápiás célpontok megjelenésével az archivált mintából újabb vizsgálatok legyenek végezhetők.
2.2. Natív anyag feldolgozása: Optimális körülmények között natív, fixálatlan minta kerül a centrumba (szállítás: 6-12 órán belül, nedves gézben párásítva). Ezen esetben a mintát a következő formában ajánlatos előkészíteni:
a. Kimetszés formol-paraffinos beágyazásra
b. Lenyomati készítmény készítése (5-10 db)
c. Kimetszés -70 °C-os tárolásra
d. Kimetszés sejtszuszpenzió készítésére (flow citometria, molekuláris genetika, -180° tárolás)
2.2. Formalinban fixált anyag feldolgozása: A hematológiai minták egy része a klinikákról formalinban fixáltan érkezik. Ezen esetekben a minták feldolgozása nem tér el más szövettani minták patológiai feldolgozásától.
3. A hematológiai betegségek diagnózisa: A hematológiai betegségek diagnosztikája és besorolása a jelenlegi WHO osztályozásnak (WHO Classification -Tumours of Haematopoieticand Lymphoid Tissues, 2008) megfelelő kritériumok alapján kell történjen. A diagnosztikai procedurában képesnekkell lenni minden terápia releváns,a prediktiv patológia területébe eső kérdés megválaszolására is.
4. A hematológiai betegségek kezelésének alapjául szolgáló patológiai diagnózis: A malignus hematológiai betegségek kezelése jelentősen eltér egymástól, a patológiai diagnózistól függően. Az egyes, főként ritka kórképeket elkülönítő differenciáldiagnosztikai eljárások gyakran csak a teljes, komplex módszertant alkalmazni tudó centrumokban találhatók meg, ezért fontos, hogy az egyes oncohaematológiai betegségeket diagnosztizáló, a fenti minimum feltételeket teljesítő centrumok is éljenek - szükség szerint - a konzílium, "második vélemény" lehetőségével, illetve intézményével.
A módszertani levél érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
módszertani levele
Az aspirációs citológiai vizsgálatok gyakorlatáról
Készítette: a Patológiai Szakmai Kollégium
Bevezetés
A vékonytű aspirációs citológiai vizsgálat (angol nevén Fine Needle Aspiration Biopsy - FNAB, vagy Fine Needle Aspiration Citology - FNAC) felületes, vagy mélyen elhelyezkedő, tapintható, vagy képalkotókkal vizualizálható elváltozásokból vékonytű és szívóerő segítségével nyert sejtek mikroszkópos vizsgálatát jelenti diagnosztikus célból.
A vékonytűbiopszia indikációi:
Tapintható, vagy képalkotókkal pontosan lokalizálható térfoglaló elváltozások identifikálása, egyes diffúz gyulladásos elváltozások, pl. thyreoiditis, phlegmonosus gyulladások, tályogok mintavételezése, gyógyító célú kiürítése, tumoros betegek nyomon követése, staging és mintavétel már ismert daganatos elváltozásokból speciális vizsgálatok végzése céljából.
A citológiai vizsgálatok előnyei egyéb biopsziás eljárásokhoz képest, az hogy: gyors - a vizsgálat maga néhány percig tart, a festés és kiértékelés 5-10 percet vesz igénybe.
A sikeres vizsgálattal korrekt szövettani szintű diagnózishoz juthatunk.
A betegek jól tolerálják, jóval kevesebb fájdalommal és kellemetlenséggel jár, mint akár egy core biopsziás beavatkozás, minimális a szövődmény veszélye, tízezrelékben mérhető hasűri szerveknél is a komolyabb szövődmények előfordulása, cysták és tályogok esetében terápiás.
A szövődmények közül subcutan haematoma, felületes gyulladás, tüdő biopsziánál PTX, hasűri szerveknél parenchymás szervekben tok alatti vérzés, epehólyag sérüléseknél epés peritonitis a leggyakoribbak, a tumorsejtek terjedése virtuális, nem bizonyított veszély, a betegség prognózisát nem befolyásolja, alig tízezreléknyi valószínűséggel keletkezhet.
A vékonytű aspirációs citológiai mintavételezés két legfőbb módját ismerjük, a tapintásos módszert, amikor leggyakrabban patológusok, citopatológusok, kisebb számban klinikusok szabadkézi mintavételezést végeznek. Másik módszer a nem tapintható léziók vizsgálatánál használatos, radiológusok, vagy képalkotó vizsgálatokban jártas szakemberekáltal vagy jelenlétükben és segítségükkel vezérelten végzett mintavétel. Ennek hátránya, hogy citológus, vagy patológus gyakran nincs jelen a beavatkozásnál, ami a minta minőségét károsan befolyásolhatja. A vezérelt mintavételezésnek számos előnye van. Megadható a pontos lokalizáció és méret, a környező szervekhez való viszony.
Saját tapasztalatunk és irodalmi közlések alapján leghatékonyabbnak tekinthetjük azon módszert, mikor radiológus szakember és citopatológus közösen végzi a mintavételezést. A citológus jelenlétének előnyei: a mikroszkópos diagnózist felállító szakember sokrétű információt nyerhet az elváltozásokról, megtapinthatja, látja a monitoron, megismerkedhet a beteg egyéb képalkotó leleteivel, CT, MR, mammográfiás felvétellel. Nem kevésbé fontos, hogy a közvetlen betegvizsgálat révén személyesen gyűjthet adatokat, melyek a felállítandó diagnózis pontosságát szolgálják (pl. emlő esetében terhesség, vérzési rendellenesség, nyirokcsomó mellett észrevétlen maradt bőrelváltozás, stb.)
A vizsgálat kérése a beküldött anyag kérőlapja.
A beküldő lapnak tartalmaznia kell a következő adatokat:
- személyi adatok
- anamnézis
- vizsgálati eredmények
- pontos lokalizáció
- vizsgálat módja és körülményei, tűérzés, aspirátum milyensége
- fixálás módja
- jelölések, kenetek száma,
- klinikai diagnózis, vagy vélemény
- speciális kérés a citopatológus felé
A mintavételezés helyesen a következő módon történik:
A biopsziához 22-23 G vastag tűt használunk,ezek0,6-0,75 mm külső átmérővel rendelkező, közönséges injekciós tűk, melyekből több különböző hosszúságú kell, hogy rendelkezésre álljon. Vastagabb tűk használatánál növekszik a szövődmény, elsősorban a vérzés veszélye, illetve, hogy a minta véres lesz, és nem tartalmaz megfelelő számban értékelhető sejteket. Sűrű cysták, tályogok leszívásához vastagabb tűk használandóak. A vákuum létrehozásához 10 vagy 20 ml-es gumidugattyús fecskendőt használunk, a 20 ml-es nagyobb szívóerőt biztosít. A fecskendő befogó, elterjedt nevén Cameco pisztoly elengedhetetlen segédeszköz, szabaddá teszi ugyanis a vizsgáló egyik kezét. A tűt a fecskendővel összekötő gumi, vagy plasztik cső használata nem ajánlott, ugyanis az összekötőben levő levegő mennyisége és a cső falának mozgása a szívóerő jelentős részét használja el. Összekötőt használunkolyan esetekben azonban, ahol a nagyméretű fecskendő közelsége zavarja igen kisméretű elváltozások mintavételezését, pl. csecsemőknél szárnyas tűvel, összekötővel végezhetünk fej-nyakon biopsziát, felnőtteknél kényes helyeken, pl. a szem környékén, epibulbárisan.
Ha radiológus végzi a beavatkozást, legyen képzett és gyakorlott, ez évi minimum több száz beavatkozást jelent. Fontos az is, hogy a radiológus rendszeres közös mikroszkópos demonstráción vegyen részt, hogy megismerje az értékelést segítő minőségi mutatókfontosságát. (hasonlóan a radiológiában ismert klinikai "képvizit" gyakorlatához).
A mintavétel során a következő lépések kötelezőek:
- a beteg felvilágosítása
- a lézió tapintás útján, vagy képalkotókkal történt pontos lokalizálása
- a tű bevezetése az elváltozásba
- ezután a légköri nyomáshoz képest negatív nyomást hozunk létre a fecskendő segítségével (vákuum), a tűt enyhén mozgathatjuk az elváltozáson belül, ezáltal biztosítjuk, hogy a tű éle kis pengeként leválasszon környezetükről sejteket, szövetfragmentumokat, és ezeket a vákuum a tű lumenébe juttassa.
- ezt követően a gumidugattyút visszaengedve a negatív nyomást megszüntetjük, ezután húzzuk ki a tűt az elváltozásból. Így kerülhetjük el, a tű lumenének tartalma ne kerüljön a légköri nyomás hatására a nagyméretű fecskendőbe, illetve, hogy a tűútból visszafele sejtek kerüljenek a mintába.
Az aspirátumot kenetkészítéshez tárgylemezen szélesztjük.
A kenet készítése során nem fektetjük a kenő lemezt teljes felszínével a preparátum lemezre (mint a hematológiai vérkenet készítés gyakorlatában), hanem igyekszünk a tárgylemez egyetlen pontára elhelyezett aspirátumot nyomást nem vagy alig gyakorolva a kenőlemez élével és részben lapjával úgy széleszteni, hogy a kenet "V" alakú legyen. Egyik szélén minimálisan vastagabb - itt látjuk a szövetfragmentumokat - másik széle felé vékonyodik - itt az egyes sejtek lehetőleg sérülésmentes morfológiával válnak értékelhetővé.
Ezt követi a kenet fixálása, mely a vizsgáló laboratórium festési módszereitől függően más és más lehet. Papanicolaou és H.E. festés alkalmazásakor a kenetet nedvesen azonnal kell fixálni, optimális festődés csak így biztosítható. MGG festéshez a kenetet levegőn fixáljuk, ehhez segítségül hívhatunk akár hajszárítót is.
Gyakorlattól függően jobb eredmény érhető el, ha minden léziót kétszer mintavételezünk, így 15-20%-kal nagyobb valószínűséggel nyerünk értékelhető anyagot. A beavatkozást kötelező dokumentálni. Mindenképpen le kell írni a beavatkozást magát, annak körülményeit, és az esetleges szövődményeket is.
A vékonytű biopsziás vizsgálat főbb hibalehetőségei a következők:
Mintavételi hiba, mikor az elváltozás mellől veszünk anyagot.
Helytelen aspirációs technika és vastag tű használata fokozza az értékelhetetlen kenetek arányát, a keletkező vérzés, a kenetek véres kontamináltsága miatt.
A helytelen anyagkezelés, rossz szélesztés, fixálási hiba szintén nagymértékben megnehezíti a kiértékelést. Objektív okok közül a vizsgált elváltozás necroticus, cysticus, fibroticus volta a leggyakoribb hibalehetőség, ill. a jól differenciált tumorok esetében ál- negatív eredményeket alkothatunk. Az ál-negatív és ál-pozitív diagnózisok keletkezésének leggyakoribb oka azonban a gyakorlatlan vizsgáló: a mintavételezés egyszerűnek tűnik, a technikai hibák korrekciója azonban mikroszkóp alatt már lehetetlen. Ezen vizsgálatot ezért csak nagy gyakorlattal rendelkező professzionális szakemberek végezzék!
Amennyiben radiológus végzi a mintavételt, a következő elvárásoknak kell megfelelnie.
- Küldjön kifogástalanul kitöltött kérőlapot.
- Tanulja meg és gyakorolja a mintavételt és az anyag tökéletes kezelését, ehhez citologus, vagy patológus segítsége elengedhetetlen.
A szórványosan végezett mintavételezés "gazdaságilag" hozhat pozitív elszámolási eredményt, szakmailag azonban súlyos hiba! Egy gyakorlott mintavételező szakembertől több száz biopszia várható el évente.
Célszerű közös rendelést létrehozni, ahol radiológus és citopatológus együttműködve érhet el optimális eredményt.
A különböző állagú aspirátumok kezelése:
Legfőbb módszer a direkt kenet készítése szolid elváltozásokból nyert aspirátumból.
Elterjedőben van a folyadék alapú (liquid based, LB) citológiai vizsgálat is. Ilyenkor a nyert aspirátumot transzport közegbe, általában puffer vagy fixáló oldatba juttatjuk, és ezt dolgozzuk fel citocentrifuga vagy egyéb filter technikák segítségével. Készíthető sejtblokk az aspirátumból, erre speciális eszközök is rendelkezésre állnak, de nagyobb mennyiségű aspirátum esetében viszonylag egyszerűen elkészíthető a sejtblokk. Amennyiben sejtblokk és direkt kenet is készül egyazon elváltozásból, és a kétféle anyagot két szakember értékeli (patológusés citopatológus), fontos, hogy lássák mindkét anyagot mindketten, és legyenek tudatában annak, hogy ugyanazon elváltozásból nyert anyagot vizsgálnak különböző módszerekkel.
Speciális vizsgálatokra speciális eszközöket használhatunk, pl. FISH vizsgálatkor elektronikusan előkezelt tárgylemez, flow citometriás vizsgálatkor transzportfolyadék.
Legyen kéznél táptalaj bakteriológia számára, amennyiben gennyet szívunk le. A biopsziás módszer alkalmas arra, hogy a citológus, vagy radiológus molekuláris patológiai vizsgálatokra is anyagot biztosítson molekuláris patológiai laboratórium számára. Ez nem feltétlenül a helyi intézményben helyezkedik el, ezen anyagok szállítása könnyedén megoldható egy központi molekuláris laboratóriumba.
Amennyiben folyadékot aspirálunk, úgy azt különböző módszerekkel dolgozhatjuk fel.
Citocentrifuga a legegyszerűbb módszer, ennek hiányában ill. "érzékeny" sejtek vizsgálatára (liquor, vizelet) szűrés és ülepítés a választandó technika.
Nagy volumenű folyadékokat több lépcsőben célszerű feldolgozni, pl. vizeletcitologiánál először a nagyobb volumenű vizelet lecentrifugálása javasolt, majd az üledéket tartalmazó néhány ml folyadék dolgozandó fel citocentrifugával, vagy szűrőksegítségével. Fehérjében dús folyadékokból kicsapatással a sejtes elemek kinyerhetőek, ebből sejtblokk készülhet. Kicsapáshoz a folyadékkal megegyező volumenű 90%-os alkohol használható, de egyéb vegyszerek is alkalmazhatóak melyek denaturálják a fehérje természetű anyagokat.
Közvetlen kenet készítésekor az alábbiakra kell figyelni:
Használjunk mattírozott tárgylemezt, melyre grafit ceruzával írhatjuk fel a beteg azonosító adatait, nevét, stb. Fontos, hogy a kenetet biztonsággal el lehessen különíteni a többi kenettől: szerepeljen név, gyakori nevek esetén a születési év, amennyiben több lokalizációból veszünk mintát, úgy a lokalizáció is legyen megjelölve a kenetek mindegyikén. A kész kenetet fixálás után megfelelő törhetetlen szállító dobozba, edénybe helyezzük és vigyük, vagy küldjük a citológiai laboratóriumba.
A fixáláshoz alkohol, isopropil alkohol, metanol egyaránt alkalmazható, legpraktikusabb a sprayfixálás, melynek un. becsapódási műterméke keletkezhet ugyan, de ez az értékelést semmilyen szinten nem befolyásolja. Leggyakrabban használt festési eljárások a citológiai gyakorlatban a Papanicolaou, H.E. és MGG festés. Más és más iskolák más és más festési módokat preferálnak, korábban elterjedtebb volt a MMG festés, ezt használják gyakran mai napig nyirokcsomók, pajzsmirigy és nyálmirigyek vizsgálatához, gyakran használt módszer a Papanicolau festés, de sokan alkalmaznak H.E. festést is. Utóbbihoz ki kell pontosan kísérletezni az optimális festési eljárást, ugyanis a kenetek festése eltérhet metszeteknél alkalmazott festéstől. Legfontosabb, hogy a festéseinkstandardizáltak legyenek. A kész előhígított termékek megbízhatóak, de drágábbak. A hígított festékek minőségét naponta kell ellenőrizni, derítéskor az utolsó oldatnak színtelennek kell lennie, a fedőlemeznek 1.515 legyen a törésmutatója.
A citológiai lelet
A citológiai leletnek tartalmaznia kell a következőket:
- a beteg adatai
- anamnézis
- röntgen, labor, korábbi kezelések
- kenetszám, azonosítók, jelölések
- vizsgálat módja, a pontos lokalizáció, a vizsgálat körülményei
- klinikai vélemény
- le kell írni a kenet minőségét, fixáltságát, értékelhetőségét befolyásoló tényezőket - ha vannak,
- a részletes mikroszkópos leírás elengedhetetlen
- diagnózis vagy vélemény, melynél a szövettani nomenklatúrát használjuk,
- kerülendők különböző C, illetve P számozások kiegészítő vélemény nélkül
- a lelet ajánlást tehet további vizsgálatokra
A kenet minőségének értékelésekor a következőket kell figyelembe venni:
A nem értékelhető kenetek aránya kevesebb mint 15%, optimális esetben 5-10%. A sejtdússág fontos kritérium, legalább 10 sejtcsoport, melyek egyenként legalább 8-10 sejtet tartalmaznak fogadható el az értékelhetőség alsó határának. Egyes esetekben ugyanakkor a sejtmentesség is lehet diagnosztikus (pl. cystatartalom értékelésekor). A fixáltság minőségét, vér, egyéb zavaró anyag jelenlétét jelezni kell a leletben. A bizonytalan (u.n. szürke zóna) és diagnosztikus célból sebészi beavatkozást javasló kenetek aránya nem lehet magasabb 3-5%-nál.
Álnegatív és álpozitív eredmény okai citológiai vizsgálattal a következők:
Mintavételi hiba, a leggyakoribb ok helytelen aspiráció, helytelen anyagkezelés, necroticus, cysticus vagy fibroticus elváltozás, ill. jól differentiált tumor és gyakorlatlan vizsgáló szintén kudarcot okozhat.
Álpozitív leletek aránya nem lehet több 1%-nál, optimális esetben valódi álpozitiv citológiai vélemény extrém ritka esemény és minden esetben részletes ismételt vizsgálatot kell végezni az ok kiderítésére.
Álpozitív leletek oka lehet reactív degeneratív elváltozások túlértékelése, ill. a postirradiatios, vagy kemotherapiás elváltozások, és természetesen értelmetlen defenzió miatti tévedés.
Leggyakoribb ok, hogy diagnózist akarunk adni kevés sejtből, vagy elégtelen minőségű kenetből. Félrevezető klinikai információk szintén rossz irányba vihetik gondolkodásunkat.
Minőség-ellenőrzés a citológiai gyakorlatban:
1. Citológia és szövettan összevetése még az esetben is, ha a két vizsgálat különböző intézetekben történik.
2. Halottvizsálati adatokkal történő összevetés
3. Senzitivitás a dignitás kérdésében célszervektől függően 87-97% közé essen
4. Specificitás a célszervektől függően 92-98% közé essen
5. Értékelhetetlen minőségű kenetek aránya nem lehet több, mint 8%.
6. Bizonytalanság okán (tehát nem szövettani megerősítés, vagy pontosítás okán!) diagnosztikus célú biopsziát indikáló eredmény aránya nem haladhatja meg az 5%-ot.
7. Minden tévedést amennyiben bizonyítottá válik részletes vizsgálat kell, hogy kövessen, ami az okokat feltárja.
8. Ráépített citopatológus szakvizsga nélkül önállóan malignus diagnózis nem javasolt. Ilyen esetekben a keneteket második, szakvizsgával is rendelkező citopatológus is értékelje.
9. Minden leletben a fent felsoroltak megjelennek: beteg adatai, leletező orvos hiteles személyazonosítása, ki végezte a mintavételezést, annak körülményei, klinikai adatok, morfológiai leírás, diagnózis, ami a dignitásra vonatkozik, kiegészítő vélemény, ami szakorvosi összegző állásfoglalás az adott elváltozás tekintetében.
A korábbi citológiai vizsgálatokat össze kell vetni a később történt szövettani vizsgálatok eredményeivel.
Ritka, vagy különös esetek sorsának szoros követése, kinyomozása kívánatos. A tévedések okainak tisztázása elengedhetetlen, kliniko-citopatológiai megbeszélések ajánlottak ahol a vizsgálatot indikáló szakember, a mintavételezést és a mikroszkópos vizsgálatot segítő ill. végző szakember is jelen van.
A minták archiválása:
A leleteket nyomtatott és elektronikus formában is archiválni kell, az elektronikus adatokat naponta mentsük, havonta adathordozóra, DVD lemezre. A keneteket célszerű határozatlan időig, de minimum 10 évig megőrizni. Kenet "second opinion" vizsgálatát kezdeményezheti: az első vizsgálatot végző (szak)orvos, a "második vélemény" adására beteg által felhatalmazott szakorvos. Az ilyen vizsgálat csak a beteg ill. az első vizsgálatot végző szakorvos
beleegyezésével történhet. Az indokoltan másik intézményben elvégzett ismételt mintavételezés - amennyiben a szabályoknak megfelelt- nem konzíliumi vizsgálat! A másodikértékeléstvégző konzíliárus felel minden esetben azért, hogy a kenet(ek) (nem újra előállítható egyszeri mintáról van szó! ) az eredeti leletezőhöz visszakerüljenek. Amennyiben ez nem valósul meg, annak minden következményéért a második vizsgálatot kezdeményező (beteg vagy orvos) felel. Leghelyesebb a kenetek on site megtekintése, azaz az eredeti vizsgáló laboratóriumban elvégzett közös kenetértékelés. Amennyiben a kenetek transzportja ill. a közös vizsgálat sem megoldható, a második véleményre vonatkozó kérést nem szabad teljesíteni.
A második vélemény teljes, a kenetre és a betegre vonatkozó lelet, nem érinti az előző leletben foglaltak kritikáját akkor sem, ha attól alapjaiban eltér, kivéve, ha hatósági vagy szakmai szervek kérik a második vizsgálatot.
A módszertani levél érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai protokollja
A húgyhólyag, vesemedence és ureter daganatainak diagnosztikájáról, a biopsziás, illetve a műtéti anyagainak patológiai feldolgozásáról
Készítette: a Patológiai Szakmai Kollégium
I. Alapvető megfontolások Bevezetés
A protokoll segítséget szeretne adni a húgyhúgyhólyag- és húgyúti daganatok szövettani diagnosztikája során felmerülő problémák megoldására, megadja a klinikusok által megfogalmazott igényeket, vagyis azt, hogy a patológiai leletben mely paraméterek meghatározása ajánlott, illetve elengedhetetlen. A módszertani levél a húgyhólyagdaganatokszövettani vizsgálatára fókuszál, tekintettel azonban arra a tényre, hogy a vesemedencében, ill. az ureterben hasonló daganatok fordulnak elő, ill. e szervek műtéti anyagainak feldolgozása hasonló patológiai szempontokon alapul, a felsorolt szervek diagnosztikáját egy helyen tárgyaljuk.
A klinikusokelvárásait az Európai Urológus Társaság 2006-os útmutatása alapján fogalmaztuk meg. Jelen módszertani levél tartalmazza -legalább címszavak formájában- a daganat-diagnosztika legfontosabb lépéseit, kiemelve azokat, amelyek közvetve vagy közvetlenül a pathologus teendőit is meghatározzák.
A húgyhólyagdaganatok nevezéktana az elmúlt évtizedekben többször változott.
Különböző nézetek láttak napvilágot, melyek a papilloma fogalmát elismerték, vagy sem, a módszertani levélnek nem feladata minősíteni ezeket.
A klinikai szemlélet két alapvető csoportot különít el urothelialis daganatok esetén: felszínes (nem izom-invazív), és izominvazív daganatot. A húgyhólyagrák szövetileg jobbára urothelsejtes carcinoma (UCC), stádiumát illetően nem-invazív (pTa) és invazív (pT1-4) lehet.
Az 1998-as WHO/ISUP és a 2004-es WHO klasszifikáció a nem-invazív urothelsejtes tumorokat
- papilloma (exophyticus, ritkán invertált)
- papilláris urothelialis neoplasia, a rosszindulatúság kockázata csekély (papillary urothelial neoplasm of low malignant potential [PUNLMP])
- papilláris UCC, alacsony grádusú
- papilláris UCC, magas grádusú
- in situ UCC
típusokba sorolja. A nem-invaziv UCC-ka húgyhólyagrákok mintegy felét teszik ki.
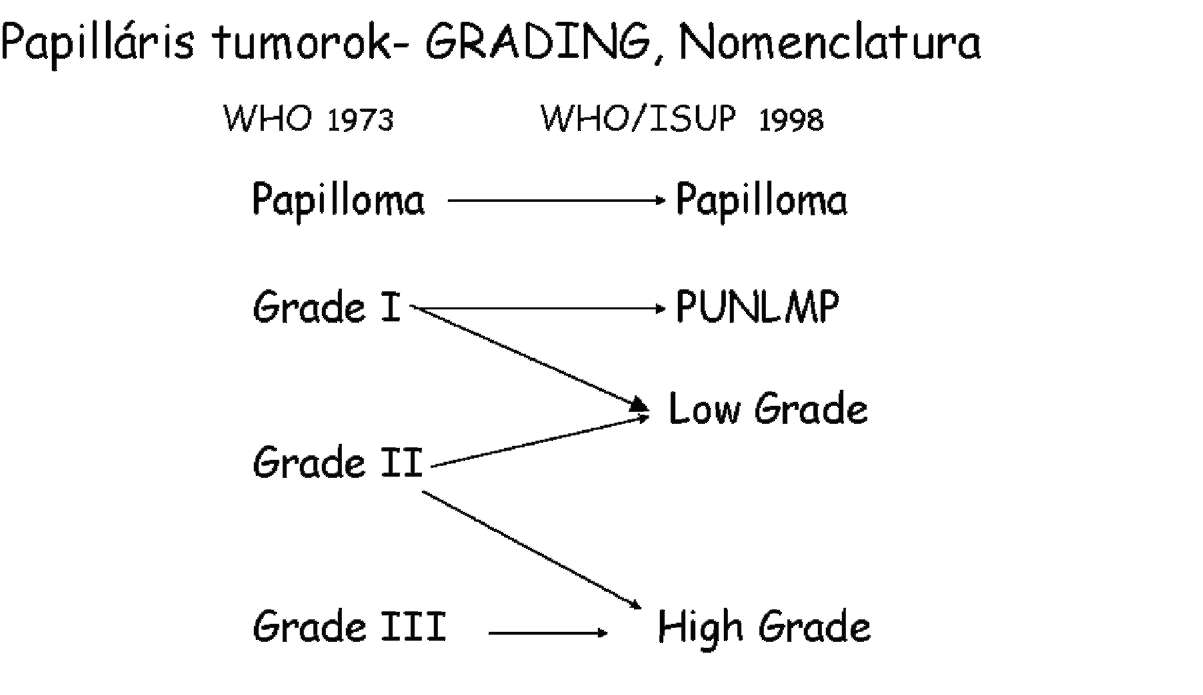
A táblázat a WHO 1973-as, illetve a WHO / ISUP 1998-as, urothelsejtes daganataira vonatkozó nevezéktanát hasonlítja össze.
Papilloma: papilláris laesio, mely centrális fibrovascularis tengellyel rendelkező, a normális urothel hámborításával egyező morfológiájú epithelialis réteggel borított növedék. A minta metsződése következtében "leszakadó papillák" mutatkoznak benne.
A korábban Grade I-nek véleményezett tumorok újnomenklatúra szerinti neve, a Papillaris Urothelialis Neoplasia with Low Malignant Potential (PUNLMP), azon filozófia alapján kapta "új nevét", mely szerint az elváltozás cytológiailag nem meríti ki a carcinoma kritériumait. Az elváltozás minimális cytológiai atypiát mutató, monoton megjelenésű urotheliális jellegű sejtekből épül fel, melyek papilláris konfigurációt mutatnak. A papillák vaskosabbak a papillomákban tapasztaltnál, azonban a papillákat borító sejtsorok számának nincs jelentősége. Osztódó formák ritkán, kizárólag a papillák basalis sejtsorában fordulnak elő. Az ilyen léziók minimális recidíva hajlamot mutatnak, ezért nem tekinthetőek teljesen ártalmatlan lézióknak.
A differenciáltság megállapításánál kizárólag a sejtek mérete, a polymorphia hiánya vagy megléte, valamint az osztódások száma és helye az, amire támaszkodni kell.
Az alacsony grádusú (low grade) urothelsejtes carcinoma kategóriába soroljuk azokat a tumorokat, melyek vaskos rétegekbe rendeződött, nem kifejezett, de azért egyértelmű cytológiai atypiát, ill. polymorphiát mutató daganatsejtekből épülnek fel. A sejtek polarizációja valamelyest megtartott, kisfokú rendezetlenség azonban szembetűnő. Osztódások előfordulnak, bár nem gyakoriak, és általában a papillák bázisán láthatóak, bár egy-egy felsőbb rétegben előforduló osztódás megengedett.
A magas grádusú (high grade) urothelsejtes carcinomákban a polymorphia kifejezett, az osztódó formák igen gyakoriak, bármely rétegben előfordulnak, és sokszor látható daganatos necrosis.
A magas grádusú kategóriába esik a korábbi Grade Il-es daganatok egy része, vagyis ez a csoport viszonylag sokféle szöveti képet foglal magába. Az eddigi vizsgálatok alapján úgy tűnik, nincs értelme további alkategóriákba sorolni e daganatokat, ugyanis egy mérsékelten polymorph, és egy kifejezetten polymorph szöveti képet mutató UCC-s beteg kezelése, ill. a betegség prognózisa azonos.
| Papilloma | PUNLMP | LG-UCC | HG-UCC | |
| Mintázat | ||||
| Papillák | Finom | Finom, elvétve összeolvadt | Összeolvadt, "ágas-bogas" | Összeolvadt, "ágas-bogas" |
| Sejtek elrendeződése | Normális urothellel egyező | Normális urothelhez hasonlóan rendezett, változó vastagságú, kohézió van | Döntően rendezett, kissé torlódó, minimálisan rendezetlen, kohézió megtartott | Polaritás elveszett, kohézió nincs |
| Cytologia | ||||
| Mag mérete | Normálissal egyező | Egyformán megnagyobbodott | Megnagyobbodott, polymorph | Megnagyobbodott, polymorph |
| Mag alakja | Normálissal egyező | Megnyúlt, kerekvagy ovális, uniform | Kerek vagy ovális, kisfokú alak/ méret-különbség | Kis, vagy nagyfokú polymorphizmus |
| Chromatin | Finoman egyenletese n elosztott | Finoman egyenletesen elosztott | Kisfokú eloszlási különbség | Hyperchrom, változatos eloszlású |
| Nucleolus | Nincs | Nem látható | Általában nem látszik | Prominens, többszörös |
| Mitózis | Nincs | Ritka, bazális | Ritka, bármely rétegben előfordulhat | Gyakori, bármely rétegben előfordulhat |
| Esernyősejtek | Jelen van | Jelen van | Általában jelen van | Hiányozhat |
A WHO / ISUP ajánlása papilláris daganatok mintázatának megítélésére - leletezési szempontok
Tekintettel arra, hogy egy-egy TUR mintában a differenciáció mértéke látóterenként változhat, a legkevésbé differenciált terület alapján kell a minta szöveti differenciáltságát megadni.
Nem papilláris szerkezetű daganat Carcinoma in situ (CIS)
Gyakran invazív folyamat prekurzora. Hyperchrom magvú polymorph sejtek láthatóak a hámban, - annak minden rétegben, vagy nagy részében. Sok az osztódó alak is a hám bármely rétegében előfordulhatnak. A sejtek orientációja megbomlott, rendezetlenség tűnik fel már kis nagyítással is. E kategóriába esnek a korábban "súlyos atypia", vagy "jelentős dysplasia" esetek is.
Egyéb, nem daganatos léziók:
Nem papilláris hyperplasia
Atypiát nem mutató szabályos, transitionalis sejtekből felépülő megvastagodott hám. A hámréteg sejtsorainakszámát nem érdemes vizsgálni, feltűnő hámvastagodás esetén diagnosztizálandó. Gyakran látni alacsony malignitású ("low grade") papilláris tumorok mellett. Önmagában semmi jelentősége, nem tekinthető premalignus eltérésnek.
Papilláris hyperplasia
Atypiát nem mutató szabályos, transitionalis sejtekből felépülő, megvastagodott hám, amely helyenként kissé kiemelkedik a környező felszínből. A kiemelkedés alapján előfordulhatnak dilatált capillarisok, azonban valódi kötőszövetes tengely nincs jelen.
Reaktív atypia
Prominens nucleolust tartalmazó, megnagyobbodott, magvú sejtekből felépülő hám sok (szabályos) mitózissal. (A háttérben heveny, és/vagy chronicus gyulladás látható). Amennyiben polymorphia, hyperchromasia, irreguláris chromatin nem látható, a folyamat nem nevezendő neoplasticusnak.
Atypia - bizonytalan klinikai jelentőségű
Ilyen esetekben az atypia, (esetleg kisfokú hyperchromasia, pleomorphismus is lehetséges) nem áll arányban, a háttérben látható gyulladással, de a folyamat neoplasticus jellege sem egyértelmű. Ezeket, a betegeket a gyulladás szanálása után újra kell vizsgálni, de ha ez nem is történik meg, fokozottan kell őket követni.
Dysplasia
A cytologiai, ill. strukturális eltérésekalapján a folyamat neoplasticus volta egyértelmű, de az elváltozások nem merítik ki a CIS kritériumait.
Igen fontos, hogy az adott szövettani leírásokat figyelembe véve a biopsiás mintákat valódi jelentőségük szerint osztályozzuk, vagyis próbáljuk meg elkerülni mind a felül-, mind az aluldiagnosztizálás hibáját. Ez a minta sorozatmetszeteken történő vizsgálatával, immunhisztokémiai reakciók elvégzésével (Ki67, P53, CK20 mintázat), ill. kétség esetén szakmai konzultációk igénybevételével lehetséges.
Az új nomenklatúra jobban tükrözi a különböző kategóriákba eső rizikócsoportokat.
Amíg a WHO 2004-es nevezéktan alapján meghatározott betegcsoportokat magukban foglaló tanulmányok eredményei véglegesen alátámasztják az új kategóriák létjogosultságát, a szövettani vizsgálat során célszerű a differenciáltsági fokot mindkét nomenklatúra szerint feltüntetni.
Az urothelialis tumorok megítélése - sok más patológiai elváltozás megítéléséhez hasonlóan - komoly szórást (interobserver variabilitást) mutathat a Ta/T1,stádium, a dysplasia/CIS, ill. a grade megítélésének a tekintetében.
A 2006-os irányelvek ajánlása szerint ideális, ha a metszeteket közös urológus/patológus találkozókon együtt is megvizsgálják. Az újnomenklatúra egyértelművé tételéhez, ill. biztos értelmezésének segítésére a http://www.pathology.jhu.edu/bladder internet oldal áll a patológusok rendelkezésére, melyen képekkel illusztrált magyarázatok olvashatóak. Kitűnő kézikönyv a Bostwick és Cheng által 2008-ban szerkesztett Urologic Surgical Pathology.
II. Diagnosztika
Tünetek: haematuria (Ta, T1 tumorok ritkán okoznak fájdalmat. Dysuria, frekvenciaváltozás, irritáció sem kíséri. Ilyen tünetek esetén CIS feltételezhető).
Előrehaladott daganat esetén: haematuria, fájdalom, dysuria, frekvenciafokozódás, kismedencei fájdalom jelentkezhet.
Fizikális vizsgálat: Ta, T1 daganatok esetén nem releváns.
Bimanuális vizsgálattal a lokálisan előrehaladott tumor gyakran kitapintható.
Képalkotók:
- Intravénás urográfia (IVU)
- Ultrahangvizsgálat
Előrehaladott tumor esetén: az előbbiek mellett
CT: a húgyhólyagon túlterjedő daganatok detektálására nem alkalmas, kb. 30%-os a T stádium alábecslése e módszerrel.
MRI: a CT vizsgálathoz hasonlóan korlátozott a diagnosztikus képessége a stádium meghatározásának tekintetében.
Cytologiai vizsgálat: alacsony malignitású ("low grade") tumorok esetén fals negatív eredményt adhat. A high grade tumorok esetén érzékenyebb módszer. A tumorsejtek jelenléte nem ad felvilágosítást a folyamat lokalizációjára.
Molekuláris biológiai tesztek: tumor antigének kimutatására alkalmas tesztek, fibrin degradációs protein kimutatási tesztek ma már forgalomban vannak. Ezek igen érzékenyek, de specificitásuk alacsony, így nagyszámú téves pozitív leletet eredményeznek, amelyek fölösleges további diagnosztikus vizsgálatot vonnak maguk után, vagyis rutinszerűen még nem alkalmazhatóak.
Cystoscopia
Transurethralis resectio (TUR) Ta, T1 tumorok esetén:
Amennyiben a daganat kicsi, és alappal együtt egyetlen mintába belefér, egy minta vétele is elegendő. Nagyobb daganatok esetén azonban a tumor alapjából külön kell mintát venni. Igen nagy kiterjedésű daganat jelenlétekor külön üvegben, külön jelzéssel ellátva a környező húgyhólyagfelszínből is szükséges a mintavétel, egyidejű CIS jelenlétének megállapítása vagy kizárása érdekében. A daganat alapjáról származó minta kell, hogy húgyhólyagfal izmot is tartalmazzon, enélkül a stádium megállapítása elégtelen (pTx). Kauterizáció kerülendő a szövet fragmentumok károsodásának elkerülése érdekében.
Előrehaladott tumorok esetén:
A tumor alapjából külön kell mintát venni az izominvázió megítélése céljából. Férfiaknál a pars prostatica, nőknél a húgyhólyagnyak biopsiája is szükséges. TUR végzése előtt és után is szükséges bimanuális vizsgálat végzése, annak megítélésére, hogy a daganat a kismedencéhez rögzül vagy sem.
Az N státusz megítélésére egyelőre az inguinális nyirokcsomók szövettani vizsgálatánál még nincs megbízhatóbb módszer.
Az M státusz megítélésére a mellkas RTG vizsgálata mellett a csont szcintigráfiára is szükség van. (A szérum alkalikus foszfatáz mérése önmagában nem elegendő csontáttétek megítélésére). Májáttétek keresésére elégséges a has UH vizsgálata, CT nem feltétlenül szükséges.
Második resectio (második ülés, "reTUR")
Az első TUR után 2-6 héttel végzik. Akkor van rá szükség, ha felmerül a gyanú, hogy az első resectio nem volt teljes, nagy, multiplex daganatról van szó, ha a patológiai vizsgálat nem talál izomréteget a mintában, vagy ha high grade tumort állapított meg. (HG UCC esetén, ha az első vizsgálat izominváziót nem állapított meg, 10 % az esélye annak, hogy a reTUR során az izominvázió mégis kimutatható. Ennek a beteg további kezelése szempontjából komoly jelentősége van - a kezelés módja lényegesen különbözik).
Térképbiopsziák
E kis "hideg" biopsiás minták vételére akkor van szükség, ha papilláris tumor jelenléte mellett (vagy anélkül) cystoscopiával vöröses, tumorgyanús területek is láthatók, és / vagy a cytológiai vizsgálat tumor jelenlétét/gyanúját állapítja meg. Ilyenkor a húgyhólyag különböző, "gyanús" és "nem gyanús" területeiről is érdemes biopsiát végezni. Trigonum elváltozás esetén a pars prostatica területéről is mintavétel indokolt.
Fluorescens cystoscopia
A húgyhólyagot kék fényben vizsgálva a hagyományos világítással nem látható léziók jobban láthatóvá válhatnak. Rutinszerű alkalmazása még nem terjedt el.
Recidíva arány és a progresszió megbecslése
A recidíva arány és a várható progresszió bekövetkeztének megbecslésére táblázat áll a klinikus kollégák rendelkezésére. Ennek alapján döntenek a lehetséges terápiás beavatkozásokról. A táblázatban szerepel a daganat nagysága, multifokalitása, T stádiuma, grade-je, "kísérő" CIS jelenléte, a recidíva megjelenésének ideje. E hat összetevőből többnek a megállapítása a patológiai vizsgálat feladata, ami igen komoly felelősséget tesz a leletező orvos vállára.
A szövettani diagnosztikus munkát ennek tudatában kell elvégezni.
TUR - szövettani vizsgálat - Leletben említendő transurethrális resecatum vizsgálatakor:
Releváns klinikai adatok ismertetése
Indítás: El kell kerülni a kazetták "túltömését". Nagy mennyiségű minta esetén csak akkor kell a resecatum egészét elindítani, ha azelső metszeteken a muscularis propria (MP) invázió nem mutatható ki. Ha ez jól látható, nem szükséges a resecatum egészének feldolgozása.
Makroszkópos leírás: mennyiség (célszerű cm3-ben, vagy grammban megadni), jellegzetességét - ha van -, leírni. Mikroszkópos
Hámfelszín - intakt, kifekélyesedett
Biopsia mélységének meghatározása (tartalmaz-e subepithelialis kötőszövetet, izmot?) Daganat szövettani differenciáltsága (UCC grading)
Paradox differenciáció - az invazív tumorsejtek jobban differenciáltnak tűnnek a non-invazív komponensnél Növekedési (infiltrálási) mintázat megítélése (sessilis, sessilis / papilláris) UCC stádium megállapítása
Lamina propria (LP; subepithelialis kötőszövet) invázió megítélése (a lamina propria elnevezés egy ideig nem volt használatos a muscularis mucosae (MM) csökevényes rostjainak egyenetlen megjelenése miatt, az utóbbi időben azonban újból teret hódított a húgyhólyagban a lamina propria megjelölése)
LP invázió gyanúját veti fel, ha a
- basalmembran nem egyenletes, a LP-ban az erek nem futnak a felszínnel párhuzamosan, stroma reakció látszik -fibroblastok, lobsejtek jelennek meg, - ez mikroinvázió mellett fordul elő.
- kicsi, szabálytalan sejtcsoportok mutatkoznak
Muscularis propria (MP; detrusor izom) invázió - nem keverendő össze a muscularis mucosae csökevényes rostjainak inváziójával. Amennyiben mikroszkóposan nem ítélhető meg biztonsággal, hogy a látható izom MM vagy a MP részlete, ezt külön megjegyzésként fel kell tüntetni a leleten (a simaizmot termikus károsodás esetén kötőszöveti rostoktól is nehéz lehet elkülöníteni, ilyenkor a h-caldesmon, desmin immunhisztokémiai reakció segíthet). Ha a resecatum nem tartalmaz detrusor izmot, a stádiumra nem lehet biztonsággal nyilatkozni, ezért ezek az esetek "pTx" jelölést kapnak.
Amennyiben a mintában egyértelműen láthatók vaskos izomkötegek, megbecsülhető, hogy a daganat mélységi terjedése alapján minimum T2a, vagy T2b kategóriába sorolható. Ha csak egyértelmű vaskos izomkötegek közötti infiltráció látható, a daganat megítélése "minimum" T2, megjegyzésben, véleményben érdemes leírni, hogy miért minimum T2, és nem T2a vagy T2b.)
Zsír jelenléte, - zsírt infiltráló tumor jelenléte- TUR mintában nem jelenti feltétlenül a perivesicalis szövetek tumoros infiltrációját, ugyanis zsírszövet előfordulhat a húgyhólyagfalban is.
A leletben a tumor stádium megadásakor érdemes a "minimum" szót megadni, (min. Ta, min. T1, stb.), ugyanis a minta alapján látható invázió mélysége nem biztos, hogy a daganat egész kiterjedését megmutatja.
Lymphaticus / Vaszkuláris invázió
Elkülönítendő a retrakciós műterméktől az infiltratív fészkek körül. (E jelenség érinvázió gyanúját keltheti, bizonytalanság esetén IH reakció végzendő az alul/túldiagnosztizálás elkerülésére).
Infiltráció típusa - köteges - trabeculáris,
- széles sejtcsoportok-nodularis,
- egysejtsoros, keskeny köteges - infiltratív
- kevert)
Tumorral szomszédos hámfelszín leírása Cystectomiás preparátum indításának szempontjai:
A húgyhólyag formalin-fixálását minél hamarabb el kell kezdeni. A húgyhólyagot az urethrán keresztül kell felvágni. Ezt kivételesen maga az urológus is elvégezheti.
A kivágást az általános szabályoknak megfelelően kell végezni. Felvágás előtt a resectios széleket tussal /alcián kékkel érdemes megfesteni. Ezután szárítás következik, hogy a festék ne kenődjön szét a nem resectiós felszíneken. Szükséges: több reprezentatív minta a tumorból, ép-kóros határ, legmélyebb penetráció helye, tumortól távol eső helyekről is minta, (CIS vizsgálata céljából) -oldalfalak, boltozat, trigonum. Resectios vonalak: ureterek, urethra, resectios vonala.
Tisztában kell lenni azzal a ténnyel, hogy megelőző TUR, ill. húgyhólyagba adott kemoterápiás kezelést követően előfordulhat, hogy a húgyhólyagban makroszkóposan feltűnő eltérés nincs.
A resectiós vonalak közül különösen kell ügyelni az urethra, az ureterek, prosztata felőli, ill. radiális resectiós szélekre. A nyirokcsomókat mind a lymphadenectomiás preparátumban, mind a cystectomiás preparátum perivesicalis zsírszövetében egyenként ki kell keresni. Amennyiben egy nyirokcsomó makroszkóposan érintett elegendő egy kimetszés, a többi nyirokcsomót egészben el kell indítani.
Amennyiben a cystectomiás preparatum környező szerveket is tartalmaz, (prostata, vesicula seminalis, vagina, uterus, rectum), ezekből a szervekből is kell indítani. Makroszkópos érintettség esetén a tumoros területről, ha a környező szerv makroszkóposan nem érintett, a szokásos reprezentatív helyekről, valamint a szerv-határok területéről kell mintátvenni. Húgyhólyagtumoros férfibetegeknél igen gyakran látni egyidejű prosztata carcinomát, ezért a prosztata különös gonddal vizsgálandó (reprezentatív minták valamennyi lebenyből, és a periurethrális területekről). Partialis cystectomiánál az eljárás hasonló: a resectios vonalak festése után keresztmetszetek készülnek a húgyhólyagfal-részletekből, valamint a resectios vonalak területéről.
Leletben említendő - Cystectomia
Makroszkópos Méret
Léziók helye, száma Infiltráció mélysége
Urethra, ureterek, prostata, vesicula seminalis, cervix Resectiós szélek (mucosa, lágyrészek)
Nyirokcsomók (eltávolított nyirokcsomók száma, mérete, tumorosan egyértelműen érintett nyirokcsomók száma) Mikroszkópos
A TUR-nál leírt szempontok mellett Resectiós szél hámja Resectiós szélek érintettsége
Urethra, ureterek, prostata, vesicula seminalis, vagy cervix érintettsége/érintetlensége Különleges szövettani típus megjelölése (ha van ilyen, ld. alább)
Nyirokcsomók
Érintett nyirokcsomók száma Tumor típus Tumor mennyisége Extranodális terjedés van-e
A stádium korrekt megállapítása
Néhány, nem-szokványos szövettani megjelenésű daganattípus különleges prognózissal járhat, ezért ezekre különös figyelmet kell fordítani:
kissejtes carcinoma
glanduláris, vagy laphám carcinoma területet is mutató TCC
orsósejtes carcinoma
TCC trophoblast proliferációval
lymphoepithelioma szerű carcinoma (LELC)
Míg az első négy említett daganatfajta a hagyományosnál rosszabb, addig az ötödik a hagyományosnál lényegesen jobb prognózissal jár. Cystectomia a kissejtes, ill. LELC-t hordozó betegeknél nem ajánlott, ugyanis a kissejtes daganatok esetében a várható túlélést nem befolyásolja a cystectomia, tiszta LELC esetében pedig a betegség chemo-radiotherápiával gyógyítható. A további szövettani altípusok (ld. lentebb) az UCC-nál rosszabb prognózisú betegséget jelölnek, itt azonban a terápia a tiszta TCC-val lényegében azonos elbírálás alá esik. A szövettani leletben meg kell említeni a daganat terjedési mintázatát (noduláris,trabeculáris vagy infiltratív), ugyanis az infiltratív terjedési mintázat rosszabb prognózissal jár.
Nyirokér- vagy vérérinvázió jelenlétét is jelölni kell a leleten, bár a nyirok-érinvázió legmegbízhatóbb mércéje a nyirokcsomók állapota (nyirokcsomó áttét jelenléte vagy hiánya).
Összefoglalva: a leletnek tartalmaznia kell a vizsgálati minta tipusát, a daganat helyét és a méretét, a daganat szöveti tipusát, differenciáltságát és növekedési mintázatát, a tumor melletti urothelben észlelt eltéréseket, a minta a stádiummeghatározásra adekvát volt-e, a stádiumot, valamint az egyéb észleleteket.
Kiegészítések:
A húgyhólyag, az ureter, a vesemedence tumorainak, szövettani típusai
(WHO 2004)
Urothelialis tumorok
Infiltráló urothelialis tumorok.
Invazív urothelialis carcinoma
Laphám differenciációval
Glanduláris differenciációval
Trophoblastos differenciációval
"Nested" (fészkes)
Microcysticus
Micropapilláris
Lymphoepithelioma szerű
Lymphoma szerű
Plasmocytoid
Sarcomatoid
Óriássejtes
Differenciálatlan
em Infiltráló urothelialis tumorok.
Carcinoma in situ
Papilláris carcinoma, High Grade
Papillaris carcinoma, Low Grade UNLMP
Urothelialis papilloma Invertált papilloma Laphám daganatok Laphám carcinoma Verrucosus carcinoma Laphám papilloma landuláris tumorok Adenocarcinoma Entericus Mucinosus Pecsétgyűrű sejtes Világos sejtes Villosus adenoma Neuroendocrin tumorok Kissejtes carcinoma Carcinoid Paraganglioma Melanocytás tumorok Malignus melanoma Naevusok
Mesenchymalis daganatok
Rhabdomyosarcoma
Leiomyosarcoma
Angiosarcoma
Osteosarcoma
"Malignus fibrosus histiocytoma" MFH (differenciálatlan high grade sarcoma)
Leiomyoma
Haemangioma
Egyéb
Haematopoieticus és lymphoid daganatok
Lymphoma
Plasmocytoma
Különféle eredetű, egyéb daganatok
Skene, Cowper, Littré mirigyekből kiinduló daganatok
Környező szervek daganatainak húgyhólyagra való terjedése
Metasztatikus daganatok Prognosztikai faktorok
Húgyhólyagban talált tumorgócok száma (egyszeres vagy multiplex) mérete: 5 cm Stádium Differenciáltság (grade)
Tumor mellett egyidejű dysplasia vagy CIS jelenléte Növekedési mintázat Vaszkuláris, / lymphaticus invázió Recidiva 3 hónapon belül
Moleculáris markerek kimutathatósága (P53, RB, Cadherinek, ploidia, Ki67)
Nyirokcsomó eltávolítás esetén nyirokcsomó áttét jelenléte / hiánya, pozitivitás esetén a pozitív nycs-k száma, mérete (oldaliság - egyoldali, kétoldali- kevésbé lényeges)
A húgyhólyagtumorokra vonatkozó 2002-es TNM klasszifikáció:
T Primer tumor:
T0Tumor jelenléte nem igazolható TX Primer tumor nem ítélhető meg Ta Nem invazív papilláris carcinoma Tis CIS "lapos" tumor T1 Tumor a subepitheliális kötőszövetben T2 Izom-invazív tumor
T2a Felszínes izomréteg infiltráció (belső fél)
T2b Mély
" (külső fél)
T3 Perivesicalis szövetek infiltrációja T3a Csak mikroszkóposan látható
T3b Makroszkóposan is látható (perivesicalis tumor massza) T4 Daganatos infiltráció az alábbi szövetekben: Prosztata, uterus, vagina, kismedence fala, hasfal T4a: prosztata, uterus, vagina T4b: kismedence fala, hasfal
Nyirokcsomók:
Nx.: Regionális nyirokcsomó áttét nem ítélhető meg. N0.: Regionális nyirokcsomó áttét nincs.
N1.: Egyetlen, 2 cm-es, vagy annál kisebb áttét regionális nycs-ban.
N2.: Metasztázis egy vagy több, 2 cm-nél nagyobb, de 5 cm-esnél kisebb nycs-ban.
N3.: Metasztázis 5 cm-nél nagyobb nycs-ban.
| Rövidítések: | |
| EORTC | European Organisation of Research and Treatment of Cancer |
| WHO | World Health Organisation |
| ISUP | International Society of Urological Pathology |
| TCC | Transitional Cell Carcinoma |
| PUNLMP | Papillary Urothelial Neoplasm of Low Malignant Potential |
| CIS | Carcinoma In Situ |
| LP | Lamina propria |
| BM | Basalmembran |
| MM | Muscularis mucosae |
| MP | Muscularis propria |
| Nycs | Nyirokcsomó |
| CC | Carcinoma |
| PIN | Prostata intraepithelialis neoplaia |
| IH | Immunhisztokémia |
| TCC | Transitionalis sejtes carcinoma |
| IVU | Intravénás urographia |
| MFH | Malignus fibrosus histiocytoma |
III. Irodalomjegyzék
1. Lopez-Beltran A, Bassi PF, Pavone-Macaluso M, Montironi R; European Society of Uropathology; Uropathology Working Group. Handling and pathology reporting of specimens with carcinoma of the urinary bladder, ureter, and renal pelvis. A joint proposal of the European Society of Uropathology and the Uropathology Working Group. Virchows Arch 2004;445:103-10.
2. Herr HW, Faulkner JR, Grossman HB, Crawford ED. Pathologic evaluation of radical cystectomy specimens: a cooperative group report. Cancer 2004;100:2470-5.
3. Eble JN, Sauter G, Epstein JI, Sesterhenn IA. Tumours of the urinary system and male genital organs. IARC Press, Lyon, 2004
4. Herr. HW. Pathologic evaluation of radical cystectomy specimens. Cancer 2002;95:668-9
5. Bostwick DG, Cheng L. Urologic surgical pathology. 2nd edition. Mosby Elsevier, 2008
A szakmai protokoll érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai irányelve
Szabványos negatív leletekről
Készítette: a Radiológiai Szakmai Kollégium
Bevezetés
Az ajánlásban foglaltak célja annak demonstrálása, hogy egy adott vizsgálati módszer alkalmazásakor mely tényezőkre kell a leletezőnek figyelnie, milyen információkat kell a leletben rögzítenie. Természetesen a konkrét leletformátum meghatározása minden intézmény saját joga és felelőssége, de mindenképpen törekedni kell a strukturált leletezés valamely formájának bevezetésére. Az ajánlásban foglaltak a jelenlegi szakmai ismereteinket tükrözik, a hazánkban általában elérhető vizsgálóberendezések figyelembevételével. Az ajánlást a technikai fejlődés, az új ismeretek, módszerek megjelenésével párhuzamosan folyamatosan frissíteni kell. Erre a beérkező észrevételek függvényében, de legkésőbb egy év múlva kerül sor.
A képalkotó diagnosztikai eljárás leletének tartalmaznia kell a CT-, MR-, UH-berendezés típusát, a vizsgálati metodikát (pl: régió, fázisok, szekvenciák), illetve az alkalmazott kontrasztanyag nevét és mennyiségét. Amennyiben van konkrét klinikai kérdés, a Véleményben erre is reagáljunk (pl.: "Vélemény: negatív lelet. Metastasis nem igazolható.").
A leletmintákban nem tértünk ki a klinikai jelentőséggel nem bíró alaki variációkra, ezeket természetesen meg kell említeni akkor is, ha nem tekinthetők kórosnak. Figyelni kell arra, hogy natív vizsgálat esetén a kontrasztanyag-adáshoz kötődő elemek (pl. kiválasztás, halmozás) ne szerepeljenek a leletben. CT:
Has és kismedence natív és több fázisú kontrasztanyagos CT-vizsgálat
A pleura-sinusokban folyadék nem látszik, az ábrázolódó tüdőterületeken kóros nem mutatható ki.
A máj nagysága, szerkezete, denzitása szabályos, benne körülírt gócos eltérés nem igazolható.
Az epeutak lefutása, tágassága szabályos. Az epehólyag normális nagyságú és falvastagságú, benne híg folyadék denzitás mérhető.
A pancreas alakja, nagysága, szerkezete szabályos, környezete reakciómentes, állományában térfoglaló folyamat vagy egyéb kóros nem látható.
A Wirsung-vezeték nem tágabb.
A lép normális nagyságú és szerkezetű.
A mellékvesék alakja, nagysága kóros eltérést nem mutat.
A vesék alakja, nagysága, helyzete, struktúrája, kontrasztanyag-halmozása és -kiválasztása szabályos, az üregrendszer szabályosan/részlegesen telődött, tágulat nem igazolható. A natív felvételeken kő, meszesedés nem mutatható ki. Ureter-tágulat nem ábrázolható.
Az uterus és az adnexumok / prostata alakja, nagysága, denzitása szabályos. A hólyag nagysága, falvastagsága normális. A kismedencei zsírszövet nem infiltrált.
A gastrointestinalis traktus megítélhető szakaszai kóros eltérést nem mutatnak. A hasi és kismedencei erek lefutása, átmérője szabályos.
A vizsgált régióban kóros folyadékgyülem, megnagyobbodott nyirokcsomó nem mutatható ki. Az ábrázolódó csontok alakja, szerkezete, denzitása szabályos.
Vélemény: negatív lelet.
Mellkas natív, kontrasztanyagos CT-vizsgálat
A mediastinum helyzete szabályos, területén megnagyobbodott nyirokcsomó, vagy egyéb térfoglaló folyamat nem látható. A mediastinalis zsírszövet nem infiltrált.
A szív normális nagyságú és konfigurációjú. Coronaria-, billentyű- és pericardium-meszesedés, pericardialis folyadék nem ábrázolódik.
A hilusokban nagyobb nyirokcsomó, egyéb térfoglaló folyamat nem mutatható ki.
A mediastinalis, hilusi és egyéb érképletek normális lefutásúakés tágasságúak, kontraszt-telődésük homogén.
A tüdők normális légtartalmúak, bennük körülírt vagy diffúz kóros eltérés nem látható.
Pleura-megvastagodás, pleuralis folyadékgyülem nem ábrázolódik.
A mellkasfali lágyrészekés csontos képletek szabályosak.
A felső hasi régió ábrázolódó területein kóros nem igazolható.
Vélemény: negatív lelet.
Nyaki lágyrész natív és kontrasztanyagos CT-vizsgálat
A pajzsmirigy alakja, nagysága, szerkezete szabályos.
A nyálmirigyek területén kóros eltérés nem látszik.
A gége és a trachea ábrázolódó szakasza normális falszerkezetű, szimmetrikus.
A hangszalagok vastagsága, a hangrés tágassága szabályos.
A naso-, meso- és hypopharynx normális tágasságú, szimmetrikus, környezetében kóros beszűrődés nem látszik. Az ábrázolódó erek lefutása, tágassága szabályos, a vascularis compartmentek szabadok. A izmok lefutása, átmérője szabályos.
A vizsgált régióban kórosan megnagyobbodott nyirokcsomó nem látszik. A látható csontos képletek területén eltérés nem igazolható.
Vélemény: negatív lelet.
Koponya CT: natív/kontrasztos
A kamrarendszer és a külső liquortér mind supra- mind infratentorialisan normális alakú, tágasságú. A középvonali képletek nem áttoltak.
A cerebralis cortex és a fehérállomány normális szerkezetű. A basalis ganglionok és a thalamusok szabályosak.
A cerebellum szürke- és fehérállomány aránya megtartott. A vermis és az agytörzs szabályos.
A corpus pineale és a hypophysis régiójában kóros nem látható. A craniocervicalis átmenet normális.
Az említett struktúrákban körülírt kóros képlet vagy diffúz eltérés nem mutatható ki. Vérzésre utaló hyperdenzitás nem észlelhető.
Az orbitákban és az orr-melléküregekben eltérés nem mutatkozik.
A koponyabázis és calvaria csontjai és az extracranialis lágyrészek épek.
Kontrasztanyag-adás után kóros halmozás nem látható.
A Willis-kör artériái és a venás sinusok szabályos képet mutatnak.
Vélemény: Negatív lelet.
Gerinc CT:
A nyaki/lumbalis lordosis/háti kyphosis megtartott. A csigolyák szabályos alakúak és szerkezetűek. A porckorongok normális denzitásúak, kóros előboltosulás nem látható.
A gerinccsatorna és a foramenek tágassága szabályos. Gyöki vagy durazsák-kompressziót okozó elváltozás nem mutatható ki.
Vélemény: Negatív lelet.
Sella natív és kontrasztanyagos CT-vizsgálat:
A sella alakja és tágassága normális.
A hypophysis normális nagyságú és denzitású. Állományában körülírt kóros képlet nem látható. Az adenohypophysis a kontrasztanyagot egyenletesen halmozza. A hypophysisnyél a középvonalban van, átmérője szabályos. Perisellárisan kóros eltérés nem mutatható ki.
Az agyállomány áttekinthető területein kóros képlet nem látható. Az ábrázolódó külső és belső liquorterek normális tágasságúak.
Vélemény: Negatív lelet.
Orbita natív és kontrasztanyagos CT-vizsgálat:
A bulbusok épek.
A külső szemmozgató izmok normális vastagságúak és denzitásúak. A nervus opticusok szabályosak.
Az intra- és extraconicus zsírszövet normális denzitású, homogén szerkezetű. Térfoglaló folyamatra utaló jel nem látszik.
Vélemény: Negatív lelet.
Agyi CT-angiographia és koponya CT-vizsgálat
Az ábrázolódó artériák/vénák lefutása, ármérője, kontrasztanyag-telődése normális. Elzáródás, kóros szűkület, körülírt tágulat, telődési hiány nem igazolható. Vascularis malformatio nem mutatható ki. Az erek falában meszesedés nem látható.
Az agyállományban kóros denzitású-halmozású terület nem látszik.
A kamrarendszer és a felszíni liquorterek normális tágasságúak, szimmetrikusak. A középvonal nem dislocált.
A craniospinalis átmenet területén nem látszik kóros.
Az ábrázolódó csontok és extracranialis képletek szabályosak.
Vélemény: Negatív lelet. Nyaki CT-angiographia
Az a. carotis communis és interna, illetve az a. vertebralis lefutása, átmérője, kontrasztanyag-telődése mindkét oldalon normális. Elzáródás, kóros szűkület, körülírt tágulat, telődési hiány nem igazolható. Az erek falában meszesedés nem látható.
A Willis-kör és ábrázolódó ágai területén kóros nem igazolható. A nyaki lágyrészek kóros eltérést nem mutatnak.
Vélemény: negatív lelet
A. pulmonalis CT-angiographia és mellkasi CT-vizsgálat
A truncus pulmonalis, a pulmonalis főtörzsek, illetve a lobaris, segmentalis ágak lefutása, átmérője, kontrasztanyag-telődése normális. Elzáródás, kóros szűkület, körülírt tágulat, telődési hiány nem igazolható. A mediastinalis képletek helyzete szabályos, területén megnagyobbodott nyirokcsomó, vagy egyéb térfoglaló folyamat nem látható. A mediastinalis zsírszövet nem infiltrált.
A szív normális nagyságú és konfigurációjú. Coronaria-, billentyű- és pericardium-meszesedés, pericardialis folyadék nem ábrázolódik.
A hilusokban nagyobb nyirokcsomó, egyéb térfoglaló folyamat nem mutatható ki.
A tüdők normális légtartalmúak, bennük körülírt vagy diffúz kóros folyamatra utaló eltérés nem látható.
Pleura-megvastagodás, pleuralis folyadékgyülem nem ábrázolódik.
A mellkasfali lágyrészekés csontos képletek szabályosak.
A felső hasi régió ábrázolódó területein kóros nem igazolható.
Vélemény: negatív lelet.
Hasi CT-angiographia
A hasi aorta és ágainak lefutása, átmérője, kontrasztanyag-telődése normális. Elzáródás, kóros szűkület, körülírt
tágulat, telődési hiány nem igazolható. Az erek falában meszesedés nem látható.
A pleura-sinusokban folyadék nem látszik, az ábrázolódó tüdőterületeken kóros nem mutatható ki.
A máj nagysága, szerkezete, denzitása szabályos, benne körülírt gócos eltérés nem igazolható.
Az epeutak lefutása, tágassága szabályos. Az epehólyag normális nagyságú és falvastagságú, bennéke híg folyadék denzitású.
A pancreas alakja, nagysága, szerkezete szabályos, környezete reakciómentes, állományában térfoglaló folyamat vagy egyéb kóros nem látható.
A Wirsung-vezeték nem tágabb.
A lép normális nagyságú és szerkezetű.
A mellékvesék alakja, nagysága kóros eltérést nem mutat.
A vesék alakja, nagysága, helyzete, struktúrája, kontrasztanyag-halmozása és -kiválasztása szabályos, az üregrendszer szabályosan/részlegesen telődött, tágulat nem igazolható.
A gastrointestinalis traktus megítélhető szakaszai kóros eltérést nem mutatnak.
A vizsgált régióban kóros folyadékgyülem, megnagyobbodott nyirokcsomó nem mutatható ki.
Az ábrázolódó csontok alakja, szerkezete, denzitása szabályos.
Vélemény: negatív lelet.
CT enteroklízis
A jejunum- és ileumkacsok lefutása, tágassága, falvastagsága szabályos, kóros kontrasztanyag-halmozás nem mutatható ki. A nyálkahártya ép, gyulladás, térfoglaló folyamat, egyéb kóros nem igazolható. A terminális ileum és a coecum ép.
A máj nagysága, szerkezete, denzitása szabályos, benne körülírt gócos eltérés nem igazolható.
Az epeutak lefutása, tágassága szabályos. Az epehólyag normális nagyságú és falvastagságú, bennéke híg folyadékdenzitású.
A pancreas alakja, nagysága, szerkezete szabályos, környezete reakciómentes, állományában térfoglaló folyamat vagy
egyéb kóros nem látható. A Wirsung-vezeték nem tágabb.
A lép normális nagyságú és szerkezetű.
A mellékvesék alakja, nagysága kóros eltérést nem mutat.
A vesék alakja, nagysága, helyzete, struktúrája, kontrasztanyag-halmozása és -kiválasztása szabályos, az üregrendszer szabályosan/részlegesen telődött, tágulat nem igazolható.
Az uterus és az adnexumok / prostata alakja, nagysága, denzitása szabályos. A hólyag nagysága, falvastagsága normális. A kismedencei zsírszövet nem infiltrált. Az erek lefutása, átmérője szabályos.
A vizsgált régióban kóros folyadékgyülem, megnagyobbodott nyirokcsomó nem mutatható ki. Az ábrázolódó csontok alakja, szerkezete, denzitása szabályos.
Vélemény: negatív lelet.
Virtuális colonoscopia
A vastagbél lefutása, tágassága, falvastagsága szabályos, kóros kontrasztanyag-halmozás nem mutatható ki. A nyálkahártya ép, térfoglaló folyamat illetve egyéb kóros nem igazolható. A terminális ileum ép.
A máj nagysága, szerkezete, denzitása szabályos, benne körülírt gócos eltérés nem igazolható.
Az epeutak lefutása, tágassága szabályos. Az epehólyag normális nagyságú és falvastagságú, bennéke híg folyadék denzitású.
A pancreas alakja, nagysága, szerkezete szabályos, környezete reakciómentes, állományában térfoglaló folyamat vagy egyéb kóros nem látható. A Wirsung-vezeték nem tágabb.
A lép normális nagyságú és szerkezetű.
A mellékvesék alakja, nagysága kóros eltérést nem mutat.
A vesék alakja, nagysága, helyzete, struktúrája, kontrasztanyag-halmozása és -kiválasztása szabályos, üregrendszeri tágulat nem igazolható.
Az uterus és az adnexumok / prostata alakja, nagysága, denzitása szabályos. A hólyag nagysága, falvastagsága normális. A kismedencei zsírszövet nem infiltrált. Az erek lefutása, átmérője szabályos.
A vizsgált régióban kóros folyadékgyülem, megnagyobbodott nyirokcsomó nem mutatható ki. Az ábrázolódó csontok alakja, szerkezete, denzitása szabályos.
Vélemény: negatív lelet.
MR:
Has és kismedence natív és több fázisú kontrasztanyagos MR-vizsgálat A pleura-sinusokban folyadék nem látszik.
A máj nagysága, szerkezete, denzitása szabályos, benne körülírt gócos eltérés nem igazolható.
Az epeutak lefutása, tágassága szabályos. Az epehólyag normális nagyságú és falvastagságú, híg folyadék-bennékű.
A pancreas alakja, nagysága, szerkezete szabályos, környezete reakciómentes, állományában térfoglaló folyamat vagy egyéb kóros nem látható. A Wirsung-vezeték nem tágabb.
A lép normális nagyságú és szerkezetű.
A mellékvesék alakja, nagysága kóros eltérést nem mutat.
A vesék alakja, nagysága, helyzete, struktúrája, kontrasztanyag-halmozása és -kiválasztása szabályos, üregrendszeri tágulat nem igazolható.
Az uterus és az adnexumok/ prostata alakja, nagysága, jelintenzitása szabályos. A hólyag nagysága, falvastagsága normális. A kismedencei zsírszövet nem infiltrált.
A gastrointestinalis traktus megítélhető szakaszai kóros eltérést nem mutatnak. Az erek lefutása, átmérője szabályos.
A vizsgált régióban kóros folyadékgyülem, megnagyobbodott nyirokcsomó nem mutatható ki. Az ábrázolódó csontok alakja, szerkezete, jelintenzitása szabályos.
Vélemény: negatív lelet.
Kismedence (nőgyógyászati) MR-vizsgálat
Az uterus és a cervix nagysága helyzete, zonális szerkezete szabályos, benne kóros jelintenzitás, kontrasztanyag-halmozás nem igazolható, külső kontúrja ép.
A parametrium nem infiltrált, a medencealapi és -fali izmok szerkezete szabályos.
A vagina normális képet mutat.
Az ováriumokjól ábrázolhatók, nagyságuk és szerkezetük, halmozásuk szabályos.
A húgyhólyag, rectum fala nem vastagabb, kóros jelintenzitás-változás, intraluminalis növedék nem igazolható. Ureter tágulat, kompresszió nem ábrázolható. A kismedencei zsírszövet nem infiltrált.
Megnagyobbodott nyirokcsomó, kóros folyadékgyülem nem látszik. A csontok alakja, szerkezete, jelintenzitása szabályos.
Vélemény: negatív lelet.
Mellkas natív, kontrasztanyagos MR-vizsgálat
A mediastinalis képletek helyzete szabályos, megnagyobbodott nyirokcsomó, vagy egyéb térfoglaló folyamat nem látható. A mediastinalis zsírszövet nem infiltrált.
A szív normális nagyságú és konfigurációjú. Pericardialis folyadék nem ábrázolódik.
A hilusokban nagyobb nyirokcsomó, egyéb térfoglaló folyamat nem mutatható ki.
A mediastinalis és hilusi érképletek normális lefutásúakés tágasságúak, kontraszt-telődésük homogén.
A tüdőkben körülírt vagy diffúz kóros folyamat nem látható.
Pleura-megvastagodás, pleuralis folyadékgyülem nem ábrázolódik.
A mellkasfali lágyrészekés csontos képletek szabályosak.
A felső hasi régió ábrázolódó területein kóros nem igazolható.
Vélemény: negatív lelet.
Nyaki lágyrész natív és kontrasztanyagos MR-vizsgálat
A pajzsmirigy alakja, nagysága, szerkezete szabályos. A nyálmirigyek területén kóros eltérés nem látszik
A gége és a trachea ábrázolódó szakasza normális falszerkezetű, szimmetrikus. A hangszalagok vastagsága, a hangrés tágassága szabályos.
A naso-, meso- és hypopharynx normális tágasságú, szimmetrikus, környezetében kóros beszűrődés nem látszik.
Az ábrázolódó erek lefutása, tágassága szabályos, a vascularis compartmentek szabadok.
A izmok lefutása, átmérője, szerkezete szabályos.
A vizsgált régióban kórosan megnagyobbodott nyirokcsomó nem látszik.
A látható csontos képletek területén eltérés nem igazolható.
Vélemény: negatív lelet.
Koponya MR: natív/kontrasztos
A külső és belső liquortér mind supra- mind infratentorialisan normális tágasságú. A középvonali képletek nem áttoltak. Az aquaeductus Sylvii nem szűkebb.
A meninxeken és az ependymán körülírt kóros képlet vagy diffúz eltérés nem látható. A cerebralis cortex és a fehérállomány normális szerkezetű. A basalis ganglionokés a thalamusokszabályosak.
A cerebellum szürke- és fehérállomány aránya megtartott. A vermis ép. Az agytörzs szabályos. Az említett struktúrákban diffúz eltérés vagy körülírt kóros képlet nem mutatható ki. A corpus pineale és a hypophysis régiójában kóros nem látható. A craniocervicalis átmenet normális.
Az orbitákban és az orr-melléküregekben eltérés nem mutatkozik. A koponyabázis és calvaria csontjai és az extracranialis lágyrészek épek. A Willis-kör artériái és a venás sinusok szabályos képet mutatnak. Kontrasztanyag-adás után kóros halmozás nem látható.
Vélemény: Negatív lelet.
Gerinc MR: natív/kontrasztos
A nyaki/lumbalis lordosis/háti kyphosis megtartott. A csigolyák szabályos alakúak és szerkezetűek.
A porckorongok normális jelintenzitásúak, kóros kiboltosulást nem mutatnak.
A gerinccsatorna és a foramenek tágassága a normális tartományban van. Gyöki vagy durazsák kompressziót okozó elváltozás nem mutatható ki.
A nyaki/háti gerincvelő/conus normális vastagságú és jelintenzitású. Kontrasztanyag-adás után kóros halmozás nem látható.
Vélemény: Negatív lelet.
Sella natív és dinamikus kontrasztanyagos MR-vizsgálat: A sella alakja és tágassága normális.
A hypophysis normális nagyságú és jelintenzitású. Állományában körülírt kóros képlet nem látható. Az adenohypophysis a kontrasztanyagot egyenletesen halmozza. A hypophysisnyél a középvonalban van, átmérője szabályos. Perisellárisan kóros eltérés nem mutatható ki.
Az ábrázolódott agyállományban kóros képlet nem látható. A külső és belső liqurterek normális tágasságúak. Vélemény: Negatív lelet. Orbita MR-vizsgálat: A bulbusok épek.
A külső szemmozgató izmok normális vastagságúak és jelintenzitásúak. A nervus opticusok szabályosak.
Az intra- és extraconikus zsírszövet normális jelintenzitású, homogén szerkezetű. Térfoglaló folyamatra utaló jel nem látszik.
Vélemény: Negatív lelet.
Belsőfül MR-vizsgálat
A kisagy-híd szögletekben és a belső hallójáratokban térfoglaló folyamat nem látható. A VII-VIII. agyidegek cysternalis és intrameatalis szakaszain kóros nem látható. A labirintusok és a cochleák szabályosak.
Az agyállományban kóros képlet nem látható. A külső és belső liqurterek normális tágasságúak
Vélemény: Negatív lelet.
Agyi MR-angiographia és koponya MR-vizsgálat
Az ábrázolódó artériák/vénák lefutása, ármérője, jelintenzitása normális. Elzáródás, kóros szűkület, körülírt tágulat,
telődési hiány nem igazolható. Vascularis malformatio nem mutatható ki.
Az agyállományban kóros jelintenzitású illetve kontrasztanyag-halmozás nem látszik.
A kamrarendszer és a felszíni liquorterek normális tágasságúak, szimmetrikusak. A középvonal nem dislocált.
A craniospinalis átmenet területén nem látszik kóros.
Az ábrázolódó csontok és extracranialis képletek szabályosak.
Vélemény: Negatív lelet.
Nyaki MR-angiographia
Az a. carotis communis és interna, illetve az a. vertebralis lefutása, átmérője, kontrasztanyag-telődése mindkét oldalon normális. Elzáródás, szignifikáns szűkület, körülírt tágulat, telődési hiány nem igazolható. A Willis-kör és ábrázolódó ágai területén kóros nem igazolható. A nyaki lágyrészek kóros eltérést nem mutatnak.
Vélemény: negatívlelet.
A. pulmonalis MR-angiographia és mellkas MR-vizsgálat
A truncus pulmonalis, a pulmonalis főtörzsek, illetve a lobaris és segmentalis ágak lefutása, átmérője,
kontrasztanyag-telődése normális. Elzáródás, kóros szűkület, körülírt tágulat, telődési hiány nem igazolható.
A mediastinalis képletek helyzete szabályos, területén megnagyobbodott nyirokcsomó, vagy egyéb térfoglaló
folyamat nem látható. A mediastinalis zsírszövet nem infiltrált.
A szív normális nagyságú és konfigurációjú. Pericardialis folyadék nem ábrázolódik.
A hilusokban kóros nyirokcsomó, egyéb térfoglaló folyamat nem mutatható ki.
A tüdőkben kóros eltérés nem látható.
Pleura-megvastagodás, pleuralis folyadékgyülem nem ábrázolódik.
A mellkasfali lágyrészekés csontos képletek szabályosak.
A felső hasi régió ábrázolódó területein kóros nem igazolható.
Vélemény: negatív lelet.
Hasi MR-angiographia és hasi MR-vizsgálat
A hasi aorta és ágainak lefutása, átmérője, kontrasztanyag-telődése normális. Elzáródás, kóros szűkület, körülírt tágulat, telődési hiány nem igazolható. Az erek falában meszesedés nem látható. A pleura-sinusokban folyadék nem látszik.
A máj nagysága, szerkezete, jelintenzitása szabályos, benne körülírt gócos eltérés nem igazolható.
Az epeutak lefutása, tágassága szabályos. Az epehólyag normális nagyságú és falvastagságú, bennéke híg folyadék denzitású.
A pancreas alakja, nagysága, szerkezete szabályos, környezete reakciómentes, állományában térfoglaló folyamat vagy egyéb kóros nem látható.
A Wirsung-vezeték nem tágabb.
A lép normális nagyságú és szerkezetű.
A mellékvesék alakja, nagysága kóros eltérést nem mutat.
A vesék alakja, nagysága, helyzete, struktúrája, kontrasztanyag-halmozása és -kiválasztása szabályos, üregrendszeri tágulat nem igazolható.
A gastrointestinalis traktus megítélhető szakaszai kóros eltérést nem mutatnak.
A vizsgált régióban kóros folyadékgyülem, megnagyobbodott nyirokcsomó nem mutatható ki.
Az ábrázolódó csontok alakja, szerkezete, jelintenzitása szabályos.
Vélemény: negatív lelet.
Csípő MR-vizsgálat (necrosis gyanúja)
Mindkét combfej alakja, kontúrja, jelintenzitása, szerkezete szabályos. Az acetabulumok épek.
Az ízfelszínek szabályosak, porcborításuk megtartott.
Velőűr-oedema, kóros intra- vagy periarticularis folyadékgyülem nem látszik.
A környező lágyrészek kóros eltérést nem mutatnak.
Vélemény: negatív lelet.
Térd MR-vizsgálat
A meniscusok, keresztszalagok és oldalszalagok épek.
A tibio-femoralis és femoro-patellaris ízfelszínek porcborítása megtartott. Az ízületi rés normális tágasságú. Az ízületi tokon belül kóros folyadékfelszaporodás nem látszik. Az ábrázolódó csontok területén kóros nem igazolható. A környező lágyrészek épek.
Vélemény: negatív lelet.
RTG:
Nyelőcső kontrasztanyagos röntgenvizsgálat
A nyelőcső lefutása, átmérője, kontúrja, redőzete szabályos. A kontrasztanyag a lumenben akadálytalanul végighalad, a peristaltica és az ürülés normális. Hiatus hernia, gastro-oesophagealis reflux fekvő helyzetben sem mutatható ki.
Vélemény: negatív lelet.
Gyomor röntgenvizsgálat
A nyelőcső lefutása, átmérője, kontúrja, redőzete szabályos. A kontrasztanyag a lumenben akadálytalanul végighalad, a peristaltica és az ürülés normális. Hiatus hernia, gastro-oesophagealis reflux fekvő helyzetben sem mutatható ki. A gyomor alakja, helyzete, tágassága, kontúrja, redőzete szabályos. A peristaltica normális, az ürülés akadálytalan, sebessége a normális tartományon belül. A duodenum lefutása, átmérője, kontúrja, redőzete szabályos. A proximalis jejunumkacsok területén nem látszik kóros.
Vélemény: negatív lelet.
Gyomor kettős kontrasztos röntgenvizsgálat
A gyomor alakja, helyzete, tágassága, kontúrja, redőzete szabályos. A duodenum lefutása, átmérője, kontúrja,
redőzete szabályos. A proximalis jejunumkacsok területén nem látszik kóros. Hiatus hernia, gastro-oesophagealis reflux fekvő helyzetben sem mutatható ki.
Vélemény: negatív lelet.
Felső passage vizsgálat
A nyelőcső lefutása, átmérője, kontúrja, redőzete szabályos. A kontrasztanyag a lumenben akadálytalanul végighalad, a peristaltica és az ürülés normális. Hiatus-hernia, gastro-oesophagealis reflux fekvő helyzetben sem mutatható ki. A gyomor alakja, helyzete, tágassága, kontúrja, redőzete szabályos. A peristaltica normális, az ürülés akadálytalan, sebessége a normális tartományon belül. A duodenum lefutása, átmérője, kontúrja, redőzete szabályos. A jejunum- és ileumkacsok szakaszosan telődnek, lefutásuk, tágasságuk, peristalticájuk szabályos, a passage normális tempójú.
Vélemény: negatív lelet.
Szelektív enterographia
A jejunum- és ileumkacsok szabályosan telődnek, lefutásuk, helyzetük, tágasságuk, redőzetük szabályos. A terminalis ileum és az ileo-coecalis átmenet területén nem látszik kóros.
Vélemény: negatív lelet.
Vastagbél kettős kontrasztos röntgenvizsgálat
A rectum normális helyzetű, tágasságú és kontúrú. A retrorectalis tér normális szélességű. A vastagbél lefutása, helyzete, tágassága, kontúrja, redőzete szabályos.
Vélemény: negatív lelet.
Mellkas röntgenvizsgálat
A rekesz éles kontúrú, normális helyzetű, a sinusok szabadok. A tüdőkben körülírt vagy diffúz transzparencia-eltérés nem ábrázolódik. A hilusi képletek szabályosak. A perifériás pulmonalis érképletek szabályosan ábrázolódnak. A szív alakja, helyzete, nagysága kóros eltérést nem mutat. Az egyéb mediastinalis képletek helyzete, kontúrjai normálisak.
Vélemény: negatív lelet.
Natív has röntgenvizsgálat
A rekesz éles kontúrú, normális helyzetű, a sinusok szabadok. A gastrointestinalis tractus valamennyi szakaszának gáztartalma szabályos, kóros gáz-folyadék nívó nem ábrázolódik. Kóros mésztartalmú képlet illetve gázgyülem nem látható. A parenchymás szervek vetületében kóros nem észlelhető.
Vélemény: negatív lelet.
Orr-melléküreg felvétel
Az orr-melléküregek alakja, légtartalma szabályos, bennük nyálkahártya-megvastagodás, folyadékretenció nem igazolható. A csont kontúrok szabályosak.
Vélemény: negatív lelet.
Csontfelvétel
Az ábrázolódó csontok alakja, struktúrája, mésztartalma szabályos, törésre, illetve egyéb kóros folyamatra utaló jel nem látható. A felvételen látható ízületi rések, normális tágasságúak, degeneratív, traumás illetve más eltérést nem mutatnak. Kóros kísérő lágyrészárnyék nem ábrázolódik.
Vélemény: negatív lelet.
Intravénás urographia
A natív felvételen a vesék helyzete, alakja, nagysága szabályos. A psoas-szélek differenciálhatók. A húgyutak vetületében kőre gyanús pozitív árnyék nem látható. Az iv. beadott kontrasztanyag mindkét oldalon szabályos időben, jó intenzitással kiválasztódik. Az üregrendszerek normális alakúak és tágasságúak. Az ureterek lefutása és tágassága szabályos, elfolyási akadály jele nem igazolható. A húgyhólyag homogénen, jól telődik. Vizelés után a húgyhólyagban residuum nem látható, az üregrendszerek ürülése jó.
Vélemény: Negatív lelet.
ERCP
A Vater-papilla kanülálását követően...
/...az epeutak szelektív töltése során a beadott kontrasztanyag az extra- és intrahepaticus epeutakat szabályos tágassággal, homogénen töltötte fel. Kő, szűkület nem mutatható ki. Az eszköz eltávolítása után a Vater papillán az ürülés akadálytalan, extravasatio nem mutatható ki.
/... a Wirsung-vezeték végig szabályos tágassággal, akadálytalanul, homogénen feltelődött. Szűkület vagy egyéb eltérés nem mutatható ki.
Vélemény: Negatívlelet.
UH:
Veseerek duplex UH-vizsgálata
A vesék helyzete, alakja, nagysága, echoszerkezete szabályos. A jobb vese nagysága ...x...x... cm, a bal vese nagysága .x.x. cm.
Üregrendszeri tágulat egyik oldalon sem látható. A vesék artériás és vénás keringése megtartott. A segmentalis ágakból és a hilusokból nyert áramlási görbék alakja szabályos. Az acceleratios idők normálisak, korai systolés csúcs megfigyelhető.
Az RI érték mindkét oldalon átlag ...%, a két oldal között significans különbség nem észlelhető. Vélemény: negatív lelet.
Teljes has és kismedence UH-vizsgálat
A máj normális nagyságú, homogén echoszerkezetű, benne körülírt kóros képlet nem látható. Az intra- és extrahepaticus epeutak nem tágabbak.
Az epehólyag normális nagyságú, híg folyadékkal telt, fala nem vastagabb, kő nem látható.
A pancreas jól ábrázolható, nem szélesebb, homogén echoszerkezetű. A Wirsung-vezeték nem tágabb.
A vesék szabályos alakúak, nagyságúak és helyzetűek. Üregrendszeri tágulat, kőreflexió egyik oldalon sem mutatható ki. A vese parenchyma mindkét oldalon szabályos vastagságú és echogenitású.
A lép normális nagyságú, szabályos, homogén echoszerkezetű.
Az ábrázolható régiókban kórosan megnagyobbodott nyirokcsomó nem látható. A megítélhető területeken megvastagodott falú bélkacs nem ábrázolódik. Szabad hasűri folyadék nem észlelhető. A hasi nagyerek lefutása, lumentágassága szabályos.
A hólyag jól telt, ép kontúrú, lumenében kóros eltérés nem látható. A prostata és vesicula seminalisok/ uterus és ovariumokábrázolódtak, echoszerkezetük szabályos.
Vélemény: negatív lelet.
Pajzsmirigy és nyaki lágyrész UH-vizsgálat
A pajzsmirigy mindkét lebenye normális nagyságú (a jobb lebeny mérete mm x mm x mm, a bal lebeny mérete mm x mm x mm), szabályos homogén echoszerkezetű. Az isthmus nem szélesebb. A nyakon kórosan megnagyobbodott nyirokcsomó nem látható.
Vélemény: negatív lelet.
Nyaki artériák UH-vizsgálata
A carotis rendszer extracranialis szakaszai normális tágasságúak és lefutásúak. Az intima ép, plaque nem látható. Az a. carotis communisban, valamint az a. carotis interna és externa megítélhető kezdeti szakaszában az áramlási görbék mindkét oldalon szabályosak, szűkületre utaló jelek nem észlelhetők. Az a. vertebralisok normális tágasságúak, bennük szabályos irányú áramlás detektálható.
Az a. subclaviák normális tágasságúak. A megítélhető szakaszokon az áramlási görbék szabályos, trifázisos jellegűek. Vélemény: negatív lelet. A vizsgált erekben áramlási eltérés, szignifikáns mértékű szűkület nem igazolható. Alsóvégtag artériákUH-vizsgálata
Az alsóvégtag artériáinak keringése a___-tól ...-ig szakaszon végig megtartott. Az áramlási görbék szabályos, trifázisos
jellegűek. Meszesedés, plaque képződés egyikérszakaszban sem észlelhető.
Vélemény: negatív lelet.
Férfi kismedence és here UH-vizsgálat
A hólyag közepesen telt, ép kontúrú. A prostata nem nagyobb, homogén echoszerkezetű. A vesicula seminalisok szabályosak.
A herék és mellékherék alakja, nagysága, echoszerkezete szabályos. Kóros folyadékgyülem, kórosan tágult véna nem látható.
Vélemény: negatív lelet.
Here UH- és color Doppler vizsgálat
A herék és mellékherék alakja, nagysága, echoszerkezete, vascularisatiója szabályos. Kóros folyadékgyülem, kórosan tágult véna nem látható. Kóros reflux provokációra sem mutatható ki.
Vélemény: negatív lelet.
Mindkét csípő UH-vizsgálat (csecsemőkori)
Jobb oldalon az alfa szög....., a béta szög.....fok. Bal oldalon az alfa szög..., béta szög... fok.
A porcos és a csontos vápa is normális meredekségű. A csontos vápasarok szögletes, hangárnyékot ad. A femurfejek centrális helyzetűek, a csontosodási mag mindkét oldalon megjelent, szimmetrikus A periarticularis lágyrészeket érintő kóros eltérés nem látható.
Vélemény: negatívlelet.
Hasi erek duplex/color Doppler UH-vizsgálata
A hasi aorta normális tágasságú. Meszesedés nem észlelhető. Az áramlás szabályos. A truncus coeliacus és az a. mesenterica superior eredése jól ábrázolható. Szűkületre utaló jelek sem ki, sem belégzésben nem észlelhetők. Az a. mesenterica superior szabályos ívvel ered az aortából, azzal hosszan, párhuzamosan fut. Aduodenum áthaladás szintjében a két ér közötti távolság ... mm.
Vélemény: negatív lelet. Szűkületre, leszorítási szindrómára utaló jelek sem az ereken, sem a duodenumon nem igazolhatók.
Alsó végtag mélyvénák duplex/color Doppler UH-vizsgálata
Az alsó végtag mélyvénás keringése végig megtartott. A látótérbe került vénák (felsorolás) területén thrombosisra, postthromboticus szindrómára utaló jelek nincsenek.
Vélemény: negatív lelet.
Nyálmirigy UH-vizsgálat
A submandibularis nyálmirigyek és parotisok normális nagyságúak, homogén echoszerkezetűek. Ductus tágulat vagy meszesedés nem észlelhető.
Vélemény: negatív lelet.
Arteria és vena ophtalmica UH-vizsgálat
Az arteria és vena centralis retinae, a. ophtalmica, v. ophtalmica superior áramlása megtartott.
Az artériás áramlási görbék szabályosak, a systolés emelkedés mértéke normális, a perifériás ellenállás nem magas. A két oldal között különbség nem észlelhető.
Vélemény: A vizsgált erekben áramlási eltérés nem igazolható.
a. radialis UH-vizsgálat
A(z) a. radialis a csukló magasságában _mm tágasságú. Az érlumen szabályos, számottevő meszesedés nem észlelhető. Az áramlási görbe normális.
Az a. ulnaris a csukló magasságában átlag _mm átmérőjű. Az áramlás itt is szabályos.
Aza. radialis compressio hatására aza.ulnaris átmérője számottevően nem változott, az áramlási sebesség jelentősen növekedett ( vs. cm/sec)
Vélemény: Az a. radialis bypass műtéthez graftnak alkalmas. Transplantált vese UH-vizsgálat
A graft ..mm hosszúságú, alakja, echoszerkezete szabályos. Perirenalisan kóros képlet, kóros folyadékgyülem nem látható. Üregrendszeri tágulat nem észlelhető.
Az artériás és vénás keringés megtartott. Az artériás áramlási görbék szabályosak, az RI érték nem magas, átl. _% Vélemény: negatív lelet. _ váll UH-vizsgálat
A bursákban folyadék nem látható. Az ábrázolódott csontok felszíne szabályos.
A rotator köpeny normális vastagságú, szabályos echoszerkezetű, szakadásra utaló jelek nem észlelhetők. A biceps ín szabályos lefutású, echoszerkezete normális.
Vélemény: negatív lelet.
Emlődiagnosztika
Negatív csak mammo
Fizikális vizsgálat: Az emlőkben és axillákban kóros nem tapintható.
Mammographia: normális szerkezetű, szimmetrikus mirigyállomány látható, amelyen belül kóros képlet, csoportos mikromeszesedés vagy szerkezeti torzulás nem mutatható ki. A bőr normális vastagságú.
Vélemény: Kóros eltérés nem mutatható ki.
Negatív mammo + UH
Fizikális vizsgálat: Az emlőkben és axillákban kóros nem tapintható.
Mammographia: normális szerkezetű, szimmetrikus mirigyállomány látható, amelyen belül kóros képlet, csoportos mikromeszesedés vagy szerkezeti torzulás nem mutatható ki. A bőr normális vastagságú.
Emlő ultrahang vizsgálat: Az emlők normális echoszerkezetűek. Kóros képlet vagy körülírt hangárnyék nem ábrázolódott. Az axillákban pathologiás nyirokcsomó nem észlelhető.
Vélemény: Kóros eltérés nem mutatható ki.
Negatív csak mammo (zsíremlő)
Fizikális vizsgálat: Az emlőkben és axillákban kóros nem tapintható.
Mammographia: teljes zsíros involutio látható. Kóros képlet, csoportos mikromeszesedés vagy szerkezeti torzulás nem mutatható ki. A bőr normális vastagságú.
Vélemény: Kóros eltérés nem mutatható ki. Negatív denz emlő
Fizikális vizsgálat: Az emlőkben és axillákban kóros nem tapintható.
Mammographia: szimmetrikus, denz mirigyállomány látható,amelyen belül kóros képlet,csoportos mikromeszesedés vagy szerkezeti torzulás nem mutatható ki. A bőr normális vastagságú.
Emlő ultrahang vizsgálat: Az emlők normális echoszerkezetűek. Kóros képlet vagy körülírt hangárnyék nem ábrázolódott. Az axillákban pathologiás nyirokcsomó nem észlelhető.
Vélemény: Kóros eltérés nem mutatható ki. Negatív csak UH (fiatal)
Fizikális vizsgálat: Az emlőkben és axillákban kóros nem tapintható. Mammographia a beteg fiatal kora miatt nem indokolt, ezért nem készítettük el.
Emlő ultrahang vizsgálat: Az emlők normális echoszerkezetűek. Kóros képlet vagy körülírt hangárnyék egyik oldalon sem ábrázolódik. Az axillákban pathologiás nyirokcsomó nem észlelhető.
Vélemény: Kóros eltérés nem mutatható ki.
A szakmai irányelv érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai protokollja
A traumás gerincvelősérültek orvosi rehabilitációjáról
(1. módosított változat)
Készítette: a Rehabilitációs Szakmai Kollégium
Konszenzus: A Traumatológiai- és az Idegsebészeti Szakmai Kollégiummal
Előzmények: Módszertani levél 1988. Felújítás: 1997. Ismételt felújítás 2006.
I. Alapvető megfontolások
A szakmai irányelv érvényességi területe: neurológiai deficitet okozó, sérülés következtében kialakult gerincvelő-károsodások mind gyermekek, mind felnőttek esetében.
Hangsúlyozzuk azonban azt, hogy egy konkrét betegség miatt kialakult gerincvelő károsodás esetén a betegség lefolyása, valamint az alapbetegség egyéb más szervi elváltozás és funkcionális zavar miatt jelentősen befolyásolhatja az orvosi rehabilitáció szükségletét, lehetőségeit, célját, eredményességét.
Általában: a gerincvelő-sérültek (trauma) korszerű, komplex ellátása a rehabilitáció mellett több, orvosi és nem orvosi szakma (oxyológia, neuro-traumatológia, idegsebészeti, intenzív terápia, urológia, plasztikai sebészet, kézsebészet, ortopédia, andrológia, orvostechnika, építészet, stb.) szoros szakmai együttműködését igényli, ezért a gerincvelő-sérültek ellátásának szakmai irányelveit a különböző érintett szakmák irányelvei tartalmazzák. Jelen esetben ezekről csak utalásszerűen teszünk említést.
A gerincvelősérültekellátásának folyamatában a különböző szakmák kompetenciája a sérült állapotának megfelelően alakul.
A betegség leírása
A gerincvelő-sérülés a központi idegrendszert (gerincvelő) érintő károsodás, amelyik a mai tudásunk szerint maradandó funkcionális és strukturális rendellenességet, az egyén számára hátrányos helyzetet okoz. Maga a károsodás az érintett gerincvelő szakasz beidegzésétől caudálisan lévő összes szerv működését érinti (érintheti), motoros, szenzoros, vegetatív zavar alakul, alakulhat ki. A gerincvelő-sérülés bármely életkorban, bármelyik nem esetén kialakulhat. Pontos magyarországi felmérések hiányában a külföldi adatokadaptációjával feltételezhető, hogy Magyarországon évente 350-550 friss, a balesetet túlélt gerincvelősérülés következik be, elsősorban közlekedési baleset következtében.
Definíciók
A gerincvelősérültek komplex ellátása, (tágabb értelemben véve a rehabilitáció) a baleset helyszínén megkezdődik, s tart az elsődleges ellátáson, az első rehabilitációs kezelésen keresztül a késői ellátáson át az élet végéig. A gerincvelősérültek komplex ellátása tehát magában foglalja az oxiológiai ellátást, valamint az akut (operatív és/vagy konzervatív) ellátást a megfelelő diagnosztikával.
Ha bármilyen trauma hatására a gerincvelőben károsodás következik be, akkor ennek következtében a gerincvelő szelvénynek megfelelő beidegzési területen és attól disztálisan motoros, szenzoros, vegetatív zavar alakul ki, vagy ezek kombinációja, és ekkor beszélünk traumás gerincvelő károsodásról.
A károsodás mértéke és típusa attól függ, hogy a gerincvelő mely keresztmetszeti struktúráit érintette a károsodás, illetve attól, hogy a gerincvelő mely szelvényei károsodtak, milyen magasságban van a károsodás. Attól függően, hogy a gerincvelő működése teljesen vagy részlegesen esik ki beszélünk teljes (plégia) vagy részleges (parézis) gerincvelő sérülésről.
Ha a gerincvelő nyaki szakasza sérül (karfonat kilépése), akkor tetraparézis,-plégia, ettől caudálisabb károsodás esetén paraplégia, -parézis alakul ki.
Súlyos trauma után a gerincvelő az úgynevezett gerincvelői shock állapotába kerül, ami a traumás, hemorrágiás shocktól eltérően a gerincvelő-sérülés szintje alatt petyhüdt plégiával, areflexiával és anesztéziával jár - így a teljes gerincvelő harántsérülés képét látjuk, még részleges sérülés esetében is. Ebben a stádiumban minden friss gerincvelő sérültet úgy kell tekintenünk, mintha a sérülés részleges lenne. A gerincvelői shock ideje 2-4 hét is lehet. A gerincvelői shock időtartamára esik bizonyosan a sérült szállítása, valamint az első kórházi ellátás.
II. Diagnózis
Traumatológia, idegsebészet, neurológia kompetenciája
III. Terápia
Traumatológia, idegsebészet, neurológia kompetenciája
IV. Rehabilitáció A rehabilitáció célja
A klasszikus rehabilitációs elvekkel ellentétben a gerincvelő sérülés mértéke a sérülés pillanatában csak részben dől el. A gerincvelő károsodása három komponensből tevődik össze:
1. primer mechanikus károsodás,
2. az első 6-8 óra alatt bekövetkező lokális keringési és anyagcsere-változások okozta károsodás,
3. perzisztáló kompresszió okozta károsodás a sérülést követő napok folyamán.
Az 1. a sérülés pillanatában kialakul, ez a balesetkor bekövetkező gerincvelő közvetlen károsodása. Az 2. és 3. ok megelőzésére (hatásának csökkentésére) hivatott az időben történő korszerű ellátás abból a célból, hogy ha lehetséges, akkor a strukturális/funkcionális károsodásból ne alakuljon ki a gerincvelősérült aktivitásának csökkenése (régebbi elnevezéssel fogyatékosság), illetve a károsodás miatt szükségképen kialakult aktivitás csökkenés mértéke a lehető legkisebb legyen, megelőzendő a gerincvelősérült hátrányos helyzetének nagyobb mértékű kialakulását (régebbi elnevezéssel rokkantság).
Az ellátás további célja az, hogy megelőzzüka sérülés (károsodás) következtében könnyen kialakuló szövődményeket. Gerincvelősérültek rehabilitációján az úgynevezett gerincvelősérült életmód megtanítását és begyakorlását értjük, lehetőség szerint a neurológiai és mozgásszervi funkciók javítása mellett. A rehabilitáció akkor is eredményes lehet, ha neurológiai tünetek maradnak vissza. Cél a sérült mindennapi önellátási képességeinek, a sérülés természetéből adódó maximális kifejlesztése, az életminőség javítása, figyelembe véve az egyén korát, nemét, előéletét, környezetét.
A rehabilitálhatóság feltételei
Helyszíni ellátás és szállítás
A gerincsérültek helyszíni ellátására és mentővel történő szállítására (primer és szekunder szállítás) vonatkozó részletes ajánlást a Mentés és Katasztrófaügyi Szakmai Kollégium egyetértésével az Országos Mentőszolgálat 1995-ben kiadott szakmai ajánlása, módszertani levele tartalmazza, illetve ennekfolyamatosan megújított változatai.
Ebből kiemelendő
A sérültet biztonságosan rögzített gerincoszloppal szabad mozgatni, szállítani, a rendelkezésre álló legkisebb szállítási traumát okozó járművel, ideális esetben helikopterrel.
A szállítás alatti ellátás
Súlyos gerinc és gerincvelő-sérülés gyanúja esetén a sérültet mozdítani, mozgatni csak úgy szabad, hogy a procedura során a sérült teljes gerince stabilizálva legyen (fordításhoz, átemeléshez több segítő összehangolt tevékenysége szükséges). Szállítás alatt a gerincet stabilan rögzíteni kell (pl. vákumágy).
Szállítás alatt, ha traumás shock, keringési-, légzészavar vagy társsérülés nincs, a gerincvelő sérült az un. megadózisú steroid adásán (amelynekegyértelmű jogosságát ma már megkérdőjelezik)kívül nem igényel különleges gyógyszeres ellátást, csak szoros megfigyelést a neurológiai státust, esetlegesen ennek változását illetően.
Hova történjen a szállítás?
A szállítás mindig direkt abba az intézménybe történjék, ahol minden egyéb szállítási szükséglet nélkül adottak időben és helyben a kellő személyi és tárgyi feltételek, valamint a mindenkori szakmai követelményeknek és feltételeknek megfelelően (diagnosztika, operatív és konzervatív ellátás, intenzív terápia, stb.) a folyamatos gyakorlat. Külön kiemelendő a 14 év alatti sérültek szállítási gyakorlatának megszervezése.
Primer akut intézeti ellátás helye
Gerincvelő sérült akut ellátásához csakott kezdjenek hozzá, ahol időben folyamatosan rendelkezésre állnaka személyi és tárgyi feltételek, valamint a gyakorlat. Ha a klinikai neurológiai kép és az egyéb vizsgálatok alapján primer műtéti ellátás nem szükséges, a gerinc stabil, mielőbbi rehabilitációs osztályon történő elhelyezés javasolt.
Primer akut intézeti ellátás célja
A primer ellátásnak 5 fontos célkitűzése van:
1. a károsodott idegrendszeri funkciók javítása
2. a megmaradt idegrendszeri funkciók konzerválása
3. a gerinc stabilitásának helyreállítása és megtartása
4. a sérült komfortjának helyreállítása
5. a korai rehabilitáció feltételeinek biztosítása
Primer akut intézeti ellátás követelménye
A primer konzervatív vagy operatív ellátás három követelménynek kell megfelelnie: az időbeni (a balesettől számított 2-6 órán belül)
1. repozició
2. dekompresszió (az önálló decompressiónak humán anyagon nincs kimutatható, statisztikailag értékelhető pozitív hatása)
3. stabilizáció
Mindhárom követelmény megvalósításának esetenként megvannak a konzervatív és/vagy operatív lehetőségei. Amennyiben ezen három követelmény az ellátás során nem valósítható meg, a sérült ellátása nem tekinthető teljesnek, korszerűnek, így rehabilitációja sem lehet teljes, korszerű.
Amennyiben a sérülés természete, a sérült általános állapota, kora, az egyéb sérülések milyensége és típusa miatt műtéti kezelés nem jön szóba, akkor a konzervatív terápia módszerei a követendők, esetlegesen kompromisszumokkal. (Az utóbbi években egyes centrumokban ismételten felmerült a konzervatív ellátás prioritása az operatív ellátással szemben . El Masry).
Primer rehabilitációs teendők az akut ellátó osztályon
Célszerű, ha már az akut ellátás során un. rehabilitációs team gondoskodik a gerincvelősérült hosszú távú orvosi ellátásának menedzseléséről. Már az akut ellátás során is érvényesülni kell a rehabilitációs szemléletnek, az akut ellátás olyan módon történjen, hogy az ne akadályozza, rontsa, illetve ne nehezítse a későbbi rehabilitációs lehetőségeket, az ellátás eredményességét.
Mindennemű beavatkozás, kezelés megtervezésekor figyelembe veendő az a tény, hogy a gerincvelősérült - nyaki sérült különösen un. deszimpatizált. állapotban van (élettani reakciói eltérhetnek a megszokottól).
Szövődmények, amelyek megelőzésére különös gondot kell fordítani:
- decubitus
- izületi kontractura
- hugyuti fertőzés (állandó katéter lehetőség szerint max. 48 órát, utána intermittáló katéterezés, vagy ha szükséges, akkor suprapubicus katéter
- légúti fertőzés
- széklet rendezése (paralitikus ileus)
- thromboembóliás szövődmények
- fel nem ismert tályog (pl. injectió csak érző területbe adható) Felvilágosítás
A sérült és/vagy a hozzátartozó felvilágosítása: mindenféle olyan felvilágosítás, ígéret, amely megvalósulásának nincsenek meg az objektív lehetőségei, illetve a jelen tudásunk, tapasztalatunk, mérvadó statisztikákszerint az állapot javulás bekövetkezésének kicsi a valószínűsége (bármennyire is szeretnénk azok megvalósulását) a rehabilitáció lehetőségét rontja, árt a sérült helyzetén.
Tájékoztatást csak a konkrét helyzetről kapjon a beteg, jóslásokba ne bocsátkozzunk. Az akut szakban ne történjen semmiféle olyan felvilágosítás sem a gerincvelősérült, sem a környezete számára, amely a gerincvelő-sérülés végkimenetelét célozza, tekintettel arra, hogy az akut szakban nem jósolható meg előre az, hogy a gerincvelő-sérülésből adódó bénulás és egyéb elváltozások kimenetele milyen lesz.
Kapcsolatfelvétel a gerincvelősérültek rehabilitációjára specializált osztállyal, az áthelyezés ideális időpontjának megválasztása érdekében.
Cél az, hogy a gerincvelősérült a lehető leghamarabb gerincvelősérültek komplex rehabilitációjára alkalmas rehabilitációs osztályra kerüljön.
Rehabilitációs osztályra történő átadás-átvétel feltételei
- A gerincvelősérült életkora, általános és mentális állapota, valamint kooperációs készsége alapján az eredményes mozgásszervi rehabilitáció reális cél.
- A sérült ne igényeljen olyan intenzív terápiás ellátást, amelyre a rehabilitációs osztály nincs felkészülve (pl. lélegeztetés)
- A gerincvelősérült általános állapota egyensúlyban legyen, légzési paraméterei, keringése
- Stabilak legyenek úgy, hogy a sérült mozgásszervi rehabilitációra (fizikai terhelés) alkalmasak legyen.
- A gerinc stabilitása biztosítva legyen operatív vagy konzervatív módon.
Hol történjen a gerincvelősérültek akut rehabilitációs ellátása?
A rehabilitációs osztály alkalmas legyen a gerincvelősérült rehabilitációja során esetlegesen fellépő komplikációk
- amelyek vagy a gerincvelő-sérülésből, vagy az egyén hátrányos helyzetéből (fogyatékosság), vagy az általános baleseti és egyéb megbetegedésekből adódhatnak - ellátására.
Ahol
- az ellátó intézmény felvállalja a gerincvelősérültek (paraplég és tetraplég esetek egyaránt) rehabilitációjának minden területen történő ellátását, folyamatosan
- a korszerű ellátásra megvannak a szakmai, tárgyi, környezeti, és anyagi feltételek (lásd minimum követelmények!), valamint a folyamatos, rutinszerű, napi gyakorlat
- az intézmény rendelkezik a gerincvelősérültek ellátásához szükséges összes szolgáltatás gyakorlatával (teljes vertikummal), rutinszerűen, folyamatosan, helyben (a hagyományos kórházi szolgáltatások mellett mozgásterápia, pszichoterápia, ergoterápia, neuro-urológia, sportterápia, szociális ellátás, testközeli és/vagy test távoli segédeszköz ellátás, valamint a sérültek ellátásához esetlegesen szükséges operatív beavatkozások folyamatos elvégzésének lehetősége)
- a társszakmákkal közösen megvannak a gerincvelősérültek akut problémáinak diagnosztikájára és ellátására a feltételek, illetve ezek ellátásának a zökkenőmentes folyamata.
- megvan a folyamatos lehetősége a gerincvelősérültek primer rehabilitáció utáni esetlegesen kialakuló kórós állapotok rendezésére (adottak a lehetőségek)
REHABILITÁCIÓ két szakasza:
1. Elsődleges rehabilitációs ellátás
Az úgynevezett gerincvelősérült életmód megtanítása a sérülést követő közvetlen időszak idején az akut ellátást végző centrumban, majd a specializált rehabilitációs osztályon.
2. Késői rehabilitációs ellátás
- A sérülés következtében az élet folyamán könnyen kialakuló szövődmények megelőzése, a testi és lelki kondíció megőrzése az élet végéig lehetőség szerint családi környezetben.
- Az élet folyamán a sérülés következtében kialakuló elváltozások, szövődmények ellátása járóbeteg, esetlegesen fekvőbeteg ellátás során.
- Az élet folyamán a gerincvelő-sérüléstől függetlenül is kialakuló elváltozások, betegségek, állapotok ellátása járóbeteg, esetlegesen fekvőbeteg ellátás során.
- Gondozás: A gerincvelő-sérüléssel együtt járó un kopási problémák enyhítésére, a gerincvelősérültek helyzetéből adódóan a rekreációs lehetőségek speciális ellátása.
Az állapot felmérése
A megszokott vizsgálatok mellett részletes neurológiai vizsgálat, amelynek ki kell térnie
- az izomerő legalább izomcsoportonkénti leírására
- érzés qualitások meghatározására és ezek határainak leírására
- vegetatív funkciók leírására (vizelet, széklet)
- izomtónus állapotára
- reflexkör leírására (felületes analis reflex, bulbocavernosus reflex) az állapot számszerűsítésére
- Frankel skála, esetlegesen ASIA scor
- izomstátus
- FIM
- egészségi állapot felmérés, FNO (szűkített)
- izomtónus állapotának felmérése (pl. Ashworth skála, reflex skála, stb.)
Elsődleges rehabilitációs ellátás:
Teendők a rehabilitációs osztályon az első felvétel során
Ez a tevékenység magába foglalja a mobilizálást, az önellátást, a tudatos vizelet- és székletürítést, a korai időszakban esetleg kialakult szövődmények kezelését (decubitus, kontraktura, infekciók, stb.), valamint az úgynevezett gerincvelő sérült életmód megtanulását.
Ezek során szükség lehet orvosi (sebész, ortopéd sebész, urológus, plasztikai sebész, rtg), gyógyszeres, fizioterápiás és segédeszköz ellátásra, valamint szociális gondozásra és a sérült (és környezete) helyes pszichés vezetésére. A gerincvelősérültek rehabilitációja tehát team feladat.
A gerincvelő sérültek rehabilitációjának fázisai ebben a szakaszban
A sérült fogadása, tájékozódás szociális, mentális és pszichés állapotáról, és ennek megfelelően mind a sérült, mind a család tájékoztatása és fokozatos felkészítése a rehabilitációs procedurára. Folyamatos kapcsolat kialakítása a családdal, hozzátartozókkal, esetlegesen tágabb környezetével.
- A sérült helyes fektetése, pozícionálása és forgatása. (ehhez megfelelő ágy biztosítása)
- Vizeletürítési zavar kezelése.
- Az előzetesen esetlegesen behelyezett állandó urethra katéter eltávolítása (ha a hólyagbénulás mellett ennek más indoka nincs)
- hólyag tréning nem szükséges
- Az intermittáló katéterezés előkészítése, megkezdése. Az intermittáló katéterezések számát a hólyag kapacitás, az elfogyasztott folyadék mennyisége, stb, elsősorban az urodynamikai paraméterek (compliance, detrusor nyomás, stb.) határozzák meg, akut esetben általában 4-6 alkalommal naponta. (II. szint.) Figyelemmel kell lenni arra, hogy egy katéterezéssel a vizelet mennyisége ne legyen több, mint 500 ml.
- Úgynevezett vizelési napló vezetése ajánlott. (III. szint)
- Időszakos UH vizsgálat kő, ectasia, stb. irányában.
- Az esetlegesen kialakult hólyag fertőzés kezelése
Bő folyadék fogyasztás, minimum napi 2-2,5 liter. (IV. szint)
Vizelet savanyítása (jelenleg ilyen gyári készítmény Magyarországon hivatalosan nincs forgalomban). Hólyag instillálása nem indikált (II. szint).
Vizelet fertőtlenítők adása (Maga a bacteruria még nem indikációja a vizelet fertőtlenítő és/vagy antibiotikum adásának.).
Antibiotikum adása csak szimptómás bacteruria esetén indokolt, akkor is célzottan.
Szimptómás bacteruria: a vizeletben a baktérium szám 100.000/ml és a leukocitaszám 100/mmt felett van együttesen.
- Urodinamikai vizsgálat az alapvető vizsgálat neurogén hólyag esetén (cystometria,
LPP, EMG, videourodinamika) (II.szint). Az urodinamikai vizsgálat alapján a megfelelő, biztonságos hólyag ürítési mechanizmus kialakítása.
Elsődleges cél: alacsony nyomású hólyag kialakítása a vesék védelmében.
Másodlagos cél: a sérülés típusa, a sérült általános állapota, valamint a sérült környezete alapján a biztonságos hólyag ürítési mechanizmus kialakítása, figyelembe véve a sérült tervezett életmódját, szociális helyzetét.
- A célok elérése érdekében szóba jövő lehetőségek (csak felsorolás)
- gyógyszerek detrusor aktivitás növelés, csökkentés adagolás módja: szisztémásan lokálisan pl. antimuscarin (I.a) hólyag kifolyás ellenállás növelés,-csökkentés
- segédeszközök (katéterek, urinálok, más megoldás híján nedvszívók, stb.)
- reflex mechanizmusok kialakítása (ingerlékeny hólyag esetében a "hólyag kopogtatása"), vagy az intravesicalis nyomás növelése a hasűri nyomás fokozásával (préselés) csak urodinamikai vizsgálattal folyamatosan kontrollált esetekben)
- fizikoterápia (elektroterápia neurostimuláció, -moduláció)
- anorectalis, intravesicalis, suprapubicus transcutan
- műtét (hólyag aktivitás növelése - ma már ritkábban alkalmazzák kifolyás ellenállás csökkentése hólyag kapacitás növelése hólyag aktivitás csökkentése kifolyás ellenállás növelése
- Székletürítés automatizmusának kialakítása.
- Lehetőségek
étkezési szokások kialakítása, diéta kúpok (elsősorban a kúp mechanikai hatása érvényesül) gyógyszerek: bélmozgatók, székletlazítók, igen enyhe hashajtók digitális ingerlés, manuális manipuláció
- Jól kialakított a gerincvelősérült széklet ürítése, ha az ürítési reflexek kialakítása után a széklet ürítés ideje akaratlagos, alkalmazkodik a sérült életmódjához. Nem jelent problémát az, ha a széklet ürítése két, esetlegesen három naponta történik.
- A mobilizálás előkészítése és időpontjának helyes megválasztása a sérülés és a sérült állapota alapján.
- Kinezoterápia
Ízületek passzív kimozgatása (a bénult területeken is)
Működő izmok erősítése, izomcsoportok funkcióinak tudatosítása
Kéz funkcióinak javítása. (parakoordináció)
Ülő, álló pozíció elérése.
Helyzetváltoztató gyakorlatok
Helyváltoztató gyakorlatok
Klinikai sport.
- Keringés stabilizálása.
Pozícionálás
Esetlegesen koffein (kávé), illetve rövid hatású vérnyomást emelő gyógyszer.
- Nyaki gerincvelő sérülés esetén a gyengült légzés ellenére a légcsere biztosítása.
Posturalis drainage
Asszisztált köhögtetés.
Bronchus váladék oldása (gyógyszer, inhalálás) Speciális légzőtorna, mellkas massage.
- Tracheostoma esetén ennek ellátása, ha a canül eltávolítása nem lehetséges, akkor trachea stent, beszélő canül.
- Magas nyaki gerincvelő-sérülés esetén a spontán légzés hiányában arteficiális lélegeztetés.(phrenicus pacemaker, home respirátor)
- Izomtónus fokozódás csökkentése, ha az izomspasmus a mindennapi élettevékenységet (önellátási képesség, ellátási nehézség) rontja. Fontos, hogy az izomspasmus bizonyos mértékű megléte előnyös is lehet (vénás keringés, stb.), valamint hatását ki lehet használni a függőleges testhelyzet elérése, megtartása érdekében.
Gyógytorna, speciális pozíciók megtartása Harántcsíkolt-izom lazító gyógyszerek Idegblokád, izomingerlési pont blokád Myotomia, myotenotomia Baclofen pumpa
- A várható végállapotnak megfelelő segédeszközök (testközeli, testtávoli) megtervezése, elkészíttetése, beszerzése, adaptálása, használatának megtanítása (esetenként bevonva a hozzátartozót), folyamatos ellenőrzése.
A rehabilitáció folyamata alatt olyan szükséges segédeszközök biztosítása, amelyek a rehabilitációs kezelés folyamatában szükségesek, de a későbbiekben a sérült számára már nem szükségesek.
- A kondíció megtartásához szükséges gyakorlatok megtanítása, begyakoroltatása, az egészségügyi intézményen kívüli életmód megtanítása, begyakoroltatása, esetenként a hozzátartozó bevonásával.
- A gerincvelősérült későbbi életében szükséges iratok, igazolások, engedélyek, stb. beszerzése, az otthoni élet előkészítése.
- Adaptációs szabadság az otthoni körülmények megtervezése, a gerincvelősérültnek az otthoni körülményekhez való alkalmazkodása, illetve a hozzátartozók gyakorlati felkészítése a fogyatékossal való együttélés céljából.
- A szűkebb és tágabb értelembe vett otthoni fizikai körülmények kialakítása, szükségszerű megtervezése, átalakítása, megfelelő adaptálása
- Mind a gerincvelősérült, mind hozzátartozóinak folyamatos felvilágosítása, pszichés vezetés.
- A gerincvelősérült felkészítése a számára alkalmas elfoglaltságra, foglalkozásra (ergoterápia). Az alábbi elváltozásokra különös tekintettel kell lenni:
Decubitus:
Rendszeres, két óránkénti forgatás, pozícióváltás; predilekciós helyek, nyomáspontok tehermentesítése, rendszeres ellenőrzése, szükség esetén sebészi kimetszés, a megfelelő plazmafehérje és hemoglobin szint biztosítása mellett. Speciális ágyak biztosítása.
Kontractura:
A bénult területeken is valamennyi izület rendszeres, naponkénti passzív, kíméletes átmozgatása, a nagyizületek változó helyzetben való pozícionálása.
Húgyútak:
Állandó katéter csak az intenzív ellátás idejére, lehetőség szerint limitált ideig (48 óra időtartamra). Ezután intermittáló katéterezés (az akut stádiumban 4-6 alkalommal naponta, később lehet 3-4 alkalommal. Lényeges, hogy egy alkalommal a lebocsátott vizelet mennyisége ne legyen több, mint 500 ml). Amennyiben bármilyen ok miatt állandó katéter szükséges, akkor szuprapubikusan bevezetett állandó katéter a javasolt. (II. szint). Ch 12 - Ch 14 méretű katéter javasolt (III. szint) ennél vastagabbnak nincs értelme.
Szükséges a bő folyadékfogyasztás, ha egyéb kontraindikáció nincs, akkor minimum napi 2-2,5 liter (IV. szint).
Gerincvelő-sérülés esetén szimptómás húgyúti infekcióról akkor beszélünk, ha a baktériumszám 100.000/ml és a leukocita szám 100/mmt felett van együttesen. Infekció profilaxis:
- az ürített vizelet mennyisége legalább 1,5 liter 24 óra alatt
- optimális pH 5,7 . 6,2 minden vizelés alkalmával. (Sajnos ma Magyarországon ilyen gyógyszer nincs forgalomban, pedig ezen gyári készítmények általában nem drágák.)
- vizelet fertőtlenítő adása jöhet szóba.
- profilaktikusan adott antibiotikum adása nem indokolt ebben a fázisban. Kivétel akkor, ha igen hosszú ideig kell állandó katétert használni valamilyen egyéb ok miatti gyógyítás céljából.
- Hólyag irrigáció, instilláció nem indokolt. (II. szint)
Nedvszívók alkalmazása indokolt
- a vizelet ürítési mechanizmus kialakításának, begyakorlásának idején, amelyben beleértendő a későbbiek folyamán bármilyen okból megváltozott vizeletürítési szokás kivizsgálása, ismételt vizeletürítési mechanizmus kialakítása,
- bármilyen vizeletürítési mechanizmus mellett a szociális biztonság érdekében,
- abban az esetben, ha a rendelkezésre álló más technikákkal dokumentálhatóan nem oldható meg az akaratlan vizeletvesztés (más megoldás híján).
Légutak: amennyiben az intercostalis izmok és/vagy a rekesz is érintett a légúti váladék eltávolítására asszisztált köhögtetés, poszturális drainage, a mellkas vibrációs masszázsa, inhalálás, a meglévő tracheostomán keresztül való direkt leszívás javasolt.
Paralitikus ileus (ami következmény) miatti passzázs zavar meteorizmust, a rekesz felnyomását és következményes légzészavart okozhat, ezért is fontos a passzázs mielőbbi megindítása (kúp, enyhe hashajtók, esetlegesen parasympatico-mimeticumok adásával is).
Tromboembóliás szövődmények megelőzésére, a vénás keringés javítására az ágyvég időszakos megemelése, a bénult végtagok passzív mozgatása, a bénult alsó végtagokra megfelelő méretű és minőségű un. kompressziós harisnya (1-es kompresszió) felhelyezése, pozícionálás, mint veszélyeztetett sérültek esetén gyógyszeres profilaxis. (Lásd az ebben a témában kiadott módszertani leveleket.)
Injekció
Bármiféle muszkuláris injekció csak olyan területen adható, amelyen a sérültnek nincsenek érzészavarai.
Késői rehabilitációs ellátás
(Az előzőekben említetteken kívül)
Cél: A sérülés következtében könnyen kialakuló szövődmények megelőzése, a testi és lelki kondíció megőrzése az élet végéig, lehetőség szerint családi környezetben.
Kiemelendő a gerincvelősérült élete folyamán könnyen kialakuló két legfontosabb probléma (felfekvés, valamint a vizelet inkontinencia okozta szövődmény) megelőzése.
- A vizelet rendszeres, a vizeletürítési mechanizmus időszakos ellenőrzése
- A veszélyeztetett (nyomásnak vagy egyéb fizikai károsodásnak kitett) bőrterületek rendszeres ellenőrzése.
- Rendezett, célorientált, aktív életmód
- Családon belüli munkavégzés esetlegesen családon belüli szerepcserével.
- Munkavégzés. Lehetőség szerint az eredeti foglalkozás, szükség esetén átképzés.
- Szabadidő hasznos eltöltése.
- Rendszeres testedzés a megtanult és begyakorolt gyakorlatok rendszeres végzése.(De a sérült teljes életét ne ez töltse ki, "nem azért élünk, hogy mozogjunk, hanem azért mozgunk, hogy éljünk".) (Adaptált fizikai aktivitás)
- Szabadidősport
- Rokkant sport
- A gerincvelősérült élet folyamán a sérülés következtében kialakuló elváltozások, szövődmények ellátása járóbeteg ellátás, esetlegesen fekvő beteg ellátás formájában (az egyéb, általános megbetegedések mellett).
- Decubitus.
Műtéti megoldásként az érnyeles bőr-izomlebeny átültetés a legmegbízhatóbb.
- Vizelet elvezető rendszer elváltozásai
Fertőzés (hólyag, vese).
Kőképződés (hólyag, uréter, vese).
Sipoly.
Veseelégtelenség.
- Vizelet ürítési zavar. (Utalunk az Urológiai Szakmai Kollégium által, az inkontinencia témában kiadott szakmai protokollra)
Konzervatív terápia (gyógyszer, fizikoterápia, megfelelő ingerlés, stb.) Operatív terápia (hólyag műtétek, speciális sphincter, pacemaker beültetés, stb.)
- Izomtónus fokozódása (Indikátora lehet bármiféle egyéb szervi elváltozásnak, betegségnek.) Az addigi terápia hatástalansága esetén
Gyógyszeres terápia felülvizsgálata Idegsebészeti, ortopédiai műtétek Ingerlő, gyógyszeres pumpa beültetése.
- Heterotop osszifikáció (Para-Articularis-Ossificatio)
Centrális idegkárosodás esetén, a bénult területeken, a nagy izületek körül (csípő, térd, könyök, váll) kialakuló pluszcsontosodás, amely ízületi mozgás-korlátozottságot, esetenként ankylosis okoz.
Kialakulását végtag duzzanat, izületi mozgáskorlátozottság jelzi, rtg felvételen mész.felhő., majd a folyamat előrehaladtával csont intenzitású képletet (corticalis, spongiosa) mutat a kérdéses ízület körül, valamint az esetek többségében az alkalikus phosphatase emelkedését. Megoldása
- konzervatív (az ízület passzív, nem forszírozott bemozgatása, esetlegesen salicylat, indometacin adása nem hatásos, rtg besugárzás (csak az igen kezdeti stádiumban), a megmerevedő izület funkcionális helyzetbe hozása), vagy
- operatív (az izület körül kialakult teljes csontos híd eltávolítása, arteficiális izület. kialakítása a csontos híd alatt vagy felett a funkció visszanyerése érdekében), de csak a kialakulás kezdetétől számított egy év után akkor, ha a csontosodás már biztosan befejeződött (labor lelet, az esetlegesen megemelkedett alkalikus phosphatase normalizálódása), abban az esetben, ha a már megmerevedett ízület helyzete az önellátásban, ellátásban problémát jelent.
- Tracheostoma ellátása
Amennyiben a stoma fenntartása szükséges, akkor ennek folyamatos ellátása, a hozzátartozó megtanítása. Amennyiben a stoma zárható (nincs leszívandó váladékozás, az esetlegesen felgyülemlett váladékot a gerincvelősérült képes kiköhögni (esetleg személyi segítséggel), a gerincvelősérült állapota stabil, várható az, hogy az eltávolítás után a légút biztosított, akkor szakorvosi megerősítés után eltávolítható a canul. Amennyiben bármilyen okból is szűkület alakulhat ki, trachea protézis (stent) beültetése jön szóba.
- Az addig nem észlelt neurológiai tünet megfelelő értékelése
- Posttraumássyringomyelia. Panaszokat okozó, életminőséget rontó esetben ellátása idegsebészeti beavatkozást igényel.
- Fájdalom
- Posttraumás gerinc és egyéb izületi deformitások
- Bénult kéz műtétek
- Kontrakturák konzervatív, operatív kezelése
- Szexuális és fertilitási zavarok teljes nyaki és a felső háti gerincvelősérültek 5 %-a képes a reflexes ejakulációra (masturbáció és/vagy coitus alkalmával) teljes cauda és conus sérültek 25 %-a képes pszichogén stimulus hatására coitusra részleges sérültek esetében mindegyik lehetőség, ezek kombinációja (egyéni és családterápia formájában)
- Szexuális vágy fokozása, növelése érdekében képzelőerő (fantázia) használata
a sérülés által nem érintett (érző) testrész, mint érintési terület használata mindkét partner "kedvezéseinek" felderítése próbálkozások más erotikus stimulusokkal
- Erekció érdekében per os gyógyszer
intracavernosus injectio (per os gyógyszerek háttérbe szorították) vákum erekciós eszköz és kompresszió megtartó gyűrű pénisz implantátum elülső sacralis gyök stimuláció
- Ejakuláció érdekében vibrátor
elektro ejakuláció
plexus hypogastricus stimuláció
- Spermiumok összegyűjtése érdekében reservoár beültetése sszegyűjtött spermiumok transcutan aspirációja (mellékheréből, ondóvezetékből)
- Mesterséges megtermékenyítés, fogamzás érdekében ondó mennyiségének növelése
mesterséges inseminatio mesterséges megtermékenyítés gaméták intrafallopian áthelyezése
- Autonóm dysreflexia ellensúlyozása érdekében 6 szegmentum feletti sérült
férfiak esetében ejakuláció ideje alatt nők esetében labour alatt sublinguinalis nifedipin vagy glicerinnitrat Ezen technikák egymásnak nem alternatívái.
Segédeszközök biztosítása
A megfelelő segédeszközök biztosítása a gerincvelősérültet ellátó (orvosi szempontból menedzselő) rehabilitációs szakember (team) feladata és kötelessége.
Az ellátásnak a jogszabályok betartása mellett folyamatosan figyelemmel kell lennie a gerincvelősérült
- általános és neurológiai állapotára
- testi adottságára
- korára
- aktivitására
- életvitelére
- társadalmi és fizikai környezetére, valamint
- a hazai segédeszközipar/kereskedelem mindenkori fejlettségére
- a hazai financiális lehetőségekre
Rendszeres kontroll Önkontroll
- a decubitus miatt különösen veszélyeztetett bőrterületek ellenőrzése
- a vizelet makroszkopos ellenőrzése
- az izomtónus változásának észrevétele
- a használt segédeszközök megfelelő (értelemszerű) ellenőrzése
Egészségügyi kontroll
- vizelet kéthavonta történő labor vizsgálata
- évente, később kétévente neuro-urológiai ellenőrzés
Az ellátás megfelelőségének indikátorai, a szakmai munka eredményességének mutatói
A gerincvelősérült életminőségét a károsodás testének, funkcióinak, életvitelének szinte minden területét érinti. Ismert az a tény, hogy az egyén életminőségéért az egészségügy csak max. 15-20 %-ban felelős, ugyan így az orvosi rehabilitáció a gerincvelősérültek életminőségének max. 15-20 %-át képes alapjaiban befolyásolni. Ebből következik, hogy a gerincvelősérültek esetében az orvosi rehabilitáció eredményessége a gerincvelősérültek tekintetében ezen kitétel figyelembevételével ítélendő meg.
Az indikátorok, mutatók mérésének eredményét igen nagymértékben befolyásolja magának a gerincvelősérült embernek a környezetéből, előéletéből, megváltozott státusából adódóan az aktivitása, motiváltsága, társadalmi helyzete. Az azonban állítható, hogy ha nem az egyes egyénre lebontva vizsgáljuk az ellátók tevékenységének eredményességét, akkor a mutatók alkalmasak lehetnek a gerincvelő-sérültet ellátó team munkájának eredményességének megítélésére.
Általános
- FIM felvétel. FIM távozás (FNO felvétel. FNO távozás ezen indikátor vizsgálata eredményes lenne, de használata komoly előkészítést igényel)
- Baleset (intenzív ellátás) és a felvétel között eltelt idő három héten belül felvettek aránya
egy hónapon belül felvettek aránya
felvett tertaplég sérültek - paraplég sérültek aránya
- Decubitus
kiírt decubitusos gerincvelősérültek száma/összes kiírt gerincvelősérült száma
az ellátó intézményben kialakult felfekvések száma/a kezelt gerincvelősérültek száma
- Vizeletürítés
kiírt állandó katétert viselők száma/kiírt gerincvelősérültek száma
- Mobilitás
teljes gerincvelősérültek sérülés magasságától függően elvárható helyváltoztató képessége (elvárható és a valós eredmény aránya) (felvételkori rehabilitációs terv, kontra végeredmény)
- Ápolás
Általános és speciális ápolási besorolás
V. Gondozás
"A gerincvelősérültek komplex ellátása, (tágabb értelemben véve a rehabilitáció) a baleset helyszínén megkezdődik, s tart az elsődleges ellátáson, az első rehabilitációs kezelésen keresztül a késői ellátáson át az élet végéig." (lásd definíciók), ami magában foglalja a fekvőbeteg ellátás keretei között nyújtott orvosi rehabilitációs szolgáltatások folytatásaként az járóbeteg ellátás formáit, valamint az alapellátásban történő ellátást, gondozást is. A gondozásnak ki kell terjednie
- a gerincvelő-károsodás következtében könnyen kialakuló szövődmények
- a gerincvelő-károsodás következtében az élet folyamán a szokásosnál hamarabb és/vagy súlyosabb formában kialakuló, a természetes elhasználódás miatt kialakult elváltozások
- a gerincvelő-károsodással szorosan nem összefüggő egyéb elváltozások, betegségek megelőzésére, észlelésére, vizsgálatára, ellátására, követésére, valamint
- a szükséges segédeszközökkel való folyamatos ellátásra, javításra.
Ennek keretében szükségessé válhat a gerincvelő-károsodottak ellátásában is jártas specialista igénybevételére, járó, esetenként fekvőbeteg szolgáltatás igénybevételére. Szerencsés az a helyzet, ha ezen típusú ellátás a gerincvelő-károsodott ember lakókörnyezetében történik.
Külön hangsúlyozzuk, hogy a tágabb értelembe vett komplex rehabilitáció részeként minden egészségügyi ok miatt hátrányos helyzetű emberszámára, így a gerincvelősérült emberek számára is, az orvosi rehabilitáció mellett szükség van a rehabilitáció többi területének (pedagógiai, foglalkozási és szociális) egyénre szabottan tervezett, időben és térben összehangolt, hatékony, folyamatos tevékenységére.
VI. Irodalomjegyzék
1. P. Abrams: Urodynamics, Springer 1997.
2. BanyóT. A neurogén hólyagdiszfunkciós betegek kezelési lehetőségei, Rehabilitáció, 11 (1): 2-4,2001
3. Bábel B.és mtsai: Az intrathecalis baclofen kezelés módszertana, Rehabilitáció, 13 (1): 18-21,2003.
4. H.Burgdörfer, H.Heidler, H.Madersbacher, H.Palmtag, D.Sauerwein, M.Stöher: Manual neuro-urology and spinal cord lesion 3. átdolgozott kiadás, Farco-Pharma Gmbh, Cologne, 2002.
5. I.M.Eltorai, J.K. Schmitt: Emergencies in chronic spinal cord injury patients Eastern Paralised Veterans Association, 3. kiadás
6. Erdei E. és mtsai: Az elektroejakuláció szerepe a gerincvelősérültek fertilitási zavarainak kezelésében, Rehabilitáció, 9 (2): 72-74. 1999
7. L. Guttmann: Spinal cord injuries, Blackwell Scientific Publications, 1973.
8. Inkontinencia, Diagnosztika-terápia-rehabilitáció Szerk:Katona Ferenc, Hamvas Antal, Klauber András, Medicina, 2006.
9. Jósvay J., Donáth A., Kertész Gy.: A tomportájéki decubitusok műtéti kezelése, Rehabilitáció, 9 (2):42-44,1999
10. Katona F.: A vizelettartás és .ürítés zavarai, Vizelet inkontinencia, Rehabilitáció, 12 (1): 27-32,2002
11. Kertész Gy.: Gerincvelő-károsodottak rehabilitációja, Orvosi Rehabilitáció113-126 o. szerk: Katona Ferenc, Siegler János Medicina, 1999.
12. Klauber A. és mtsai: Az első nervus phrenicus pacemaker beültetés Magyarországon, (esetismertetés) Clinical Neuroscience, 50(7-8): 262-266,1997.
13. Klauber A.: Neurogén hólyag rehabilitációja, Orvosi Rehabilitáció 127-137 o. szerk: Katona Ferenc, Siegler János Medicina, 1999.
14. Klauber A.: Gerincvelősérültek vizeletürítési zavarainak ellátása elektromos ingerléssel (irodalmi áttekintés), Rehabilitáció, 11 (1): 5-6,2001
15. Klauber A., Banyó T., Veszely J.: A neurogén hólyag diszfunkciójának konzervatív ellátási algoritmusa, Rehabilitáció, 12(4):17-20, 2002.
16. Klauber A., Havlikné G. I.: Gerincvelősérültek rehabilitációja, A rehabilitáció gyakorlata 239-280 o. Szerk: Katona Ferenc, Siegler János Medicina, 2004.
17. H. Madersbacher, J.J.Wyndale, Y. Igawa, E. Chartier-Kastler, M.Fall, A.Kovindha, I.Perkash, F.Pesce: Conservative management in neuropathic patient Incontinence 775-812 o. Health Publication Ltd, 1999.
18. Majoros A.: Katéterezés, önkatéterezés tanítása, A rehabilitáció gyakorlata 404-404 o. Szerk: Katona Ferenc, Siegler János Medicina, 2004.
19. K.F. Parsons, J.M. Fitzpatrick: Practical urology in spinal cord injury, Springer-Verlag London Ltd. 1991.
20. Tankó A.: Az alsó húgyutak funkcionális vizsgálata, Akadémia kiadó, Budapest, 1990.
21. Pharmacological Treatment of Urinary Incontinence, Inkontinencia, 3rd International Consultation on Incontinence Monaco, June 26-29, 2004 3rd Edition Szerk: P. Abrams, L. Cardozo, S. Khoury, Alan Wein, 2005
22. Vizelet inkontinencia, Urológiai Szakmai Irányelv Összeállította: Az Urológiai Szakmai Kollégium megbízásából Dr. Banyó Tamás
A szakmai protokoll érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai irányelve
A Stroke rehabilitációs ellátásról (felnőtt) (1. módosított változat)
Készítette: a Rehabilitációs Szakmai Kollégium
TARTALOM
Előszó
A. Hazai előzmények
B. A jelen irányelv megszületésének háttere
C. Az adaptált irányelv eredetijének megnevezése és elérhetősége
D. Az adaptált irányelv
E. Az irányelv érvényességi ideje
I. Bevezetés - az irányelv célja; kulcsfontosságú pontok; eredmény mérések
II. Rehabilitációs ellátás nyújtása
A. A post-acut stroke rehabilitációs ellátás szervezése
B. Standardizált felmérő eszközök használata
C. A terápia intenzitása/tartama
D. A páciens családja és gondozói
E. A páciens és a család/gondozó képzése
III. Rehabilitáció az akut szak során
A. Stroke betegek az akut szak során
B. A kórtörténet felvétele és a fizikális vizsgálat elvégzése
C. A stroke súlyosságának felmérése (NIHSS)
D. A stroke és egyéb arteriosclerotikus érbetegségek másodlagos megelőzésének bevezetése
IV. Poststroke rehabilitáció
A. A post-acut stroke betegek rehabilitációs szolgáltatások miatti felmérése
B. Kórtörténet és fizikális vizsgálat
C. A komplikációk kockázatának felmérése
D. A gondolkodás és a kommunikáció felmérése
E. Pszichoszociális felmérés
F. Funkció felmérés
G. Szüksége van-e a betegnek rehabilitációs intervencióra?
H. "Inpatient" (bentlakásos, kórházi) rehabilitáció indikált-e?
I. Független-e a beteg alapszintű és kiterjesztett önellátó képességét illetően?
J. A páciens korábbi otthonába/lakóhelyére bocsátása és orvosi követésének biztosítása az alapellátásban
K. A súlyos stroke által sújtott páciensekés/vagy maximális függőség és a funkcionális helyreállásra való kedvezőtlen
kórjóslat
L. A poststroke beteg "inpatient" (bentlakásos, kórházi) rehabilitációja M. Az ellátás optimális szintjének meghatározása
N. A páciens/család képzése, közös döntés elérése a rehabilitációs programról és a kezelési terv meghat.
O. Rehabilitációs programok és intervenciók bevezetése
P. Kész-e a páciens a lakóhelyi életre?
Q. A gyógykezeléshez kötöttség és a fejlődés akadályai
R. A páciens szükségletének felmérése a lakóközösségen alapuló rehabilitációs szolgáltatások iránt S. A lakóközösségen alapuló rehabilitációs szolgáltatások optimális környezetének meghatározása
V. Gondozás
VI. Irodalomjegyzék
VII. Függelék
Előszó
A. Hazai előzmények
Endres Mária dr. nevéhez fűződik a téma első módszertani levelének [1] összeállítása jó két évtizeddel ezelőtt. Ezután 9 évvel egy ajánlás [2] jelent meg hemiplégiásokat ill. strokebetegeket ellátó rehabilitációs osztályok működési kritériumairól, amely a Rehabilitációs Szakmai Kollégium által előzetesen megadott keretvázlat alapján az "inpatient" rehabilitáció sok kérdését érintette, a Kollégium által elfogadásra került, ezek által módszertani levél pótló szerepet tölött be. (Az azt megelőző évben pedig kísérlet történt geriátriai stroke betegek rehabilitációját végző egységek működési kritériumainak megfogalmazására [3].)
1995. december 12-én a stroke-betegek akut ellátásával foglalkozó hazai konszenzus konferencián a kerekasztalok egyikének témája a korai rehabilitáció volt [4], az 1996. május 11-ei, poststroke állapotokról szóló konszenzus konferencia fő területe a rehabilitáció volt. Ezen utóbbi előkészítése során egyebek között felhasználtuka "Post-Stroke Rehabilitation" című, részletes szakmai irányelvet magában foglaló könyvet [5], melynek második szerzője megegyezik a jelen irányelv alapjául szolgáló mű első szerzőjének személyével (Pamela W. Duncan). Ápolási irányelvet tartalmazó írás is született a témában [6].
A Magyar Stroke Társaság és a Neurológiai Szakmai Kollégium friss (2005.), hatályos szakmai irányelvei a cerebrovascularis betegségek megelőzéséről, diagnosztikájáról és ellátásáról [7] szólnak, a rehabilitációról nem. Ez a tény is egy önálló stroke rehabilitációs irányelv megjelentetésének szükségessége mellett szólt.
B. A jelen irányelv megszületésének háttere
Protokollok, működési standardok, ajánlások, módszertani levelek, irányelvek készítése mindig is szerepelt a Rehabilitációs Szakmai Kollégium feladatai között, munkaterveiben.
Már az előző összetételű Rehabilitációs Szakmai Kollégium elnöke is kiadta feladatként az elévült módszertani levelek átdolgozását vagy újraírását. Több témában el is készültek ezek, néhány terület, így a stroke rehabilitáció túlterhelt szakemberi azonban dacoltak kérésével. Időközben a nemzetközi gyakorlathoz való igazodás igénye fogalmazódott meg: módszertani levelek helyett inkább szakmai irányelvek írását inspirálta az ismét a szakmai kollégiumokgazdájává vált Egészségügyi Minisztérium (EüM), amely koordinálással, módszertani segítség nyújtásával (továbbképző konferencia 2005.október 12., nyomtatott kiadvány [8]) is igyekezett segíteni e munkát, ugyanakkor el is várja a művek beérkezését.
A készítés módszertanának megismerése során nyilvánvalóvá vált, hogy bizonyítékokon alapuló irányelv újonnan történő megalkotása a stroke rehabilitáció témakörében (is) olyan nagy számú szakember részvételét igényelné és olyan hosszú ideig tartana, hogy "célszerűbb ... más országok irányelvfejlesztő központjai által kidolgozott ajánlások adaptálása" [9].
Föl kellett tehát kutatni és át kellett tekinteni a meglévő, témába vágó irányelveket, szellemileg rákészülve arra is, hogy milyen szempontoknak kell megfelelnie az adaptálásra kiválasztandó munkának: legyen nyelvileg hozzáférhető, aktuális (naprakész), alapvetően bizonyítékokon alapuló (ahol még nem létezik bizonyíték ott konszenzuskonferencián alapuló), és lehetőleg legyen önállóan stroke rehabilitációs témájú (azaz ne egy stroke ellátással foglalkozó irányelv egy vagy néhány fejezetét kelljen kiragadni). Fentieknek a teljesség igényével felkutatott és áttekintett német, svéd, skót, új-zélandi, korábbi USA anyagok közül egyetlen irányelv felelt meg (ld.alább). E munkáról Szél István dr. beszámolt és jóváhagyást kapott a Rehabilitációs Szakmai Kollégium 2005. november 9-i ülésén.
C. Az adaptált irányelv eredetijének megnevezése és elérhetősége
Jelen irányelv az alábbi USA klinikai irányelv alapján készült: AHA/ASA-Endorsed Practice Guidelines Management of Adult Stroke Rehabilitation Care A Clinical Practice Guideline
Pamela W. Duncan, PhD, FAPTA, Co-Chair; Richard Zorowitz, MD, Co-Chair; Barbara Bates, MD; John Y. Choi, MD; Jonathan J. Glasberg, MA, PT; Glenn D. Graham, MD, PhD; Richard C. Katz, PhD; Kerri Lamberty, PhD Dean Reker, PhD
Szabadon letölthető a http://stroke.ahajournals.org/cgi/content/full/36/9/e100 adatbázisból.
Nyomtatásban csak ún. végrehajtási összegzés jelent meg: Stroke. 2005 Sep;36(9):2049-56. Ez utóbbi is szabadon
hozzáférhető az Interneten az alábbi helyen: http://stroke.ahajournals.org/cgi/content/full/36/9/2049
D. Az adaptált irányelv
A jelen irányelv a teljes anyag alapján készült: Annak ajánlásokra centráló tömörítését, fordítását és magyarra adaptálását a Rehabilitációs Szakmai Kollégium számára, annak megbízásából és tagjaként Szél István dr. készítette el (az adaptáció részleteit ld. a 4.sz.függelékben) és terjesztette be a Kollégium 2006. január 18-i ülésére. Nevezett személy az Országos Orvosi Rehabilitációs Intézet orvosa, semmilyen gyártó vagy forgalmazó cég felé sincs elkötelezettsége, ezen munkájához anyagi támogatásban nem részesül. A Rehabilitációs Szakmai Kollégium tagjai valamennyien hasonló helyzetben lévő, közalkalmazotti statusban dolgozó orvosok az ország egész területéről. 2006.január 18-i ülésén a Rehabilitációs Szakmai Kollégium egyhangúlag alkalmasnak találta a tervezetet a végleges változat alapjának és felkérte az előterjesztőt, hogy az ülésen javasoltaknak megfelelően fejlessze azt tovább és elektronikus levelezés útján mutassa be a változtatásokat a Kollégium tagjainak. A fentiek szerint módosított jelen anyagot még az alábbi két szakmai kollégiumnak látszik szükségesnek egyetértés elnyerése céljából megküldeni: Neurológiai Szakmai Kollégium, Háziorvostani Szakmai Kollégium. S bár az anyag kevés konkrétumot tartalmaz az ápolás, mozgásterápia, pszichológia, gyógypedagógia stb területéről, megfontolható ezen területek kollégiumainak, ennek hiányában szakmai szervezeteinek esetleg kamarájának egyetértését is kérni. Éppen a viszonylag kevés konkrétum valamint az anyag külföldi volta miattaz irodalomjegyzék tartalmazza a a magyarnyelven elérhető (néhány fordított cikk kivételével magyar szerzők által is írt) szakirodalom jegyzékét. (A rend kedvéért feltétlenül meg kell jegyezni, hogy a viszonylag kevés szakmai konkrétum nem kis részben a rövidítésnek tulajdonítható: terjedelmi okból a "szakmaiságot" adó magyarázatok, megbeszélések kihagyásra kerültek. Részben helyette szerepel a magyar nyelvű szakirodalomajánlása.) Az irodalomjegyzékben az irodalom töredékrésze már inkább csakorvostörténeti jelentőségű, döntő része részben a stroke rehabilitáció egészével vagy egyes aspektusaival, az ún. poststroke állapottal, a gondozással foglalkozik, ill. az irányelvben említett valamely témáról (pl. decubitus, érbetegségek másodlagos megelőzése) szóló recens közlemény.
Terjedelmileg a magyar szöveg az eredetinek csupán kis része, mivel ahol csak lehet, csak az ajánlásokat tartalmazza, megjelölve az ajánlás szintjét, az eredeti ajánlás- kategorizálás meghagyásával - ld. táblázat.
TÁBLÁZAT: Ajánlási fokozatok
| A | Erős ajánlás arra, hogy a beavatkozás mindig indikált és elfogadható |
| B | Ajánlás arra, hogy a beavatkozás hasznos/hatásos lehet |
| C | Ajánlás arra, hogy a beavatkozás megfontolható |
| D | Ajánlás arra, hogy egy eljárásmód haszon/hatás nélkülisége vagy ártalmas volta is megfontolandó |
| I | Elégtelen bizonyíték pro vagy kontra ajánlást tenni - a klinikus az ítélőképességére hagyatkozik |
Ezen ajánlási fokozatok elsősorban, de nem csak a szakirodalmi bizonyítéki szinten alapulnak. A táblázatból látható, hogy az'I'fokozatot pedig nem szabad ajánlásnak tekinteni, éppen az a lényege, hogy a szóban forgó kérdésben jelenleg nincs érdemlegesnek tekinthető (azaz magasszintű szakirodalmi adatokon vagy legalább konszenzus konferencián alapuló) ajánlás!! Kötelező érvényük pedig csak az 'A' szintű ajánlásoknak van, ezáltal esetleges jogi következmény is csak ezekből adódhat. Ezen erős ajánlások száma nem túl magas, s azok is meglehetősen általános megfogalmazásúak. Sajátos a helyzet a 'D' kategóriájú ajánlásokkal kapcsolatosan. Ezek -amennyiben a szakirodalmi megalapozottság és az ismeretekáltalános minősítése szerény - bizonytalanul szólnakaz eljárás ellen. Előfordul az anyagban olyan helyzet - a IV.O. pontnak a depresszió kezelésével kapcsolatos 10.alpontjában (profilaktikus antidepresszáns alkalmazás) -, hogy a jó evidencia minőség alapján szilárdan lehet állást foglalni a felvetés ellen, ill. az alkalmazás egyértelműen fölösleges volta mellett.
Az eredeti irányelv ajánlási osztályozásának átvétele egyúttal azt is jelenti, hogy a jelen munkában használt kategóriák nem egyeznek meg az EüM által kiadott "zöld füzet" [8] 2. anyagának 6. mellékletében (36.o.) leírt 4 fokozatú ('A'-tól 'D'-ig) ajánlási rangsorolásban használttal!!!
Meg kell még jegyezni, hogy az eredeti ajánlás sem mindenütt ad meg ajánlási kategóriát. Néhol pedig az eredeti anyagban a szövegtől elkülönített táblázatokban irodalmi hivatkozással együtt szereplő ajánlási kategóriák nem egyeztethetőek az eltérően strukturált szöveges ajánlással. Az irányelv tartalmára vonatkozóan két megjegyzést szükséges tenni:
1. A felmérésekről meglehetősen sok szó esik, ehhez képest a kezelések sajnos kissé háttérbe szorulnak.
2. A hozzátartozókkal való kommunikációt ugyan mi, hazai szakemberek is fontosnak tartjuk, annak mértékbe azonban nálunk az ajánlás által sugallt, az észak-amerikai kultúrában honos mértéket valószínűleg akkor sem érné el, ha a szakemberek száma ezt lehetővé tenné. Mindazonáltal az anyag bíztatást adhat e téren a hazai szakemberek számára is.
E. Az irányelv érvényességi ideje
Az eredeti irányelv - bármennyire kiérleltnek tűnő munka is - érvényességi időt meglepő módon nem határoz meg.
Irodalomjegyzék az előszóhoz
1. Az Országos Orvosi Rehabilitációs Intézet módszertani levele a hemiplégiás betegek rehabilitációjáról. Összeáll.: Endres Mária. Országos Orvosi Rehabilitációs Int., Budapest, 1985.
2. Szél I., Halmos B.: Hemiplegiásokat ill. strokebetegeket ellátó rehabilitációs osztályok működési kritériumai. Rehabilitáció, IV. (2) 280284 1994.
3. Szél I., Tróznai T.: Időskorú strokebetegek rehabilitációját végző osztályok ill. részlegek működési kritériumai. Rehabilitáció, III. (4), 178180,1993.
4. Konszenzus a cerebrovascularis betegségek ellátásában. Agyérbetegségek, 1996.évi 2.szám, 13.o.
5. Post-Stroke Rehabilitation. Clinical Practice Guideline, Number 16. U.S. Department of Health and Human Services, Rockville, Maryland, AHCPR Publication No. 95-0662, May 1995. ISBN: 0-16-045575-8
6/a. Egészségügyi Minisztérium (2002): Szakmai irányelv stroke betegek ápolásához. Eü.Közlöny 52 (11), 1344-59 6/b. Balogh Z (2003): A stroke-betegek ápolásának és rehabilitációjának egységes ápolási irányelvei. LAM 13 (1), 50-56
7. A Magyar Stroke Társaság és a Neurológiai Szakmai Kollégium szakmai irányelvei a cerebrovascularis betegségek megelőzéséről, diagnosztikájáról és ellátásáról. Tényekre támaszkodó ajánlások 2005. Promenade Publ.H., Bp., 2005. vagy in: Útmutató - klinikai irányelvek, Mediton, Bp., 2005.126-165
8. Minőségfejlesztési módszertani anyagok. Egészségügyi Minisztérium, Budapest, 2005. ("zöld füzet")
9. Vittay P (2004): Protokollok, módszertani levelek, irányelvek, ajánlások. Magyar Orvos XII (6):22-23.
I. Bevezetés
Az irányelv legfontosabb célja tudományos bizonyítékokat nyújtani agyi vérkeringési inzultuson (stroke) átesett felnőtt betegek rehabilitációja során az intervenciók és értékelések gyakorlatához. Amennyiben az ellátóhelyeken az ellátás folyamatai ennek megfelelőek, akkor remélhető leginkább az érintettek maximális funkcionális állapotának és függetlenségének elérése, javítva ezáltal a páciens és a család életminőségét.
A. Kulcsfontosságú pontok
- A rehabilitáció fő céljai: a komplikációk megelőzése, a károsodások minimalizálása és a funkciók maximalizálása.
- A stroke visszatérésének illetve koszorúér események, cardiovascularis eredetű halálozás megelőzése érdekében a szekunder prevenció alapvető fontosságú.
- A korai állapotfelmérés és intervenció döntő fontosságú a rehabilitáció optimalizálásához.
- Standardizált kiértékelések és valid állapotfelmérő módszerek nélkülözhetetlenek az átfogó kezelési terv kialakításához.
- A bizonyítékokon alapuló beavatkozásoknak funkcionális célokra kell épülniük.
- Optimális eredmény biztosításához szükséges, hogy minden beteg számára elérhető legyen egy tapasztalt multidiszciplináris rehabilitációs team.
- A páciens és családtagja és/vagy a páciens gondozója a rehabilitációs team nélkülözhetetlen tagja.
- A páciens és a család képzése növeli a tájékozott döntéshozatali képességet, a közösségbe való visszailleszkedést és a rehabilitáció révén visszanyertek fenntartását.
- A lakóhelyi visszailleszkedés érdekében a multidiszciplináris team törekedjéka lakóhelyi erőforrások kiaknázására.
- A túlélés biztosítása érdekében nélkülözhetetlen a kockázati tényezők és társult betegségek folyamatos orvosi kezelése.
B. Eredmény mérések (minőség indikátorok)
- Funkcionális állapot (beleértve a napi élettevékenységet - ADL (activity of daily living) - és a kiterjesztett napi élettevékenységet - IADL (instrumental activitiy of daily living) - mérését
- Rehospitalizációk száma
- Lakóhelyen maradási helyzet
- Halálozás
II. Rehabilitációs ellátás nyújtása
A. A post-acut stroke rehabilitációs ellátás szervezése Ajánlások
1. Jobb klinikai eredmény érhető el, amennyiben a rehabilitációra kijelölt post-acut stroke páciens összehangolt multidiszciplináris értékelésben és kezelésben részesül.
- Post-acut stroke ellátás olyan színhelyen nyújtassék, ahol a rehabilitációs ellátás hivatalosan szervezett és koordinált. Ajánlási fokozat:'A'. Magyarországon ezt a mimimumfeltételekés az ÁNTSz engedélyezése szavatolja.
- Post-acut stroke ellátás minden olyan szakellátásban nyújtható, amely tapasztalattal bír a poststroke ellátásban, biztosítva az ellentmondás-mentességet és csökkentve a komplikációk kockázatát.
- A multidiszciplináris team orvosból, nővérből, különböző (felsőfokú) végzettségű mozgásterapeutákból, foglalkoztató terapeutából, logopédusból, pszichológusból, esetleg egyéb szakemberekből valamint a páciensből és családtagjából/gondozójából állhat. Ajánlási fokozat:T(nincs ajánlás).
2. Amennyiben a szolgáltatóhelyen szervezett rehabilitációs team nem érhető el, a közepes vagy súlyos tüneteket mutató páciensek számára olyan szolgáltatóhelyre való áthelyezés kínálandó fel, ahol vagy van ilyen team, vagy legalábbis bevonható az ellátásba stroke ellátásban jártas orvos vagy rehabilitációs szakember. Ajánlási fokozat:'I'(nincs ajánlás).
3 A szervezett team szemléletmódnak a járóbeteg ill. lakóhelyi rehabilitációs ellátás összehangolásában is folytatódnia kell. Ajánlási fokozat:'I'(nincs ajánlás).
B. Standardizált felmérő eszközök használata Ajánlások
1. A stroke-ból való helyreállás felmérésére erősen ajánlott a NIH stroke skála (NIH: National Institute of Health, az USA Nemzeti Egészség Intézete) használata a beteg megjelenésekor/kórházi felvételekorvagy legalább a megjelenés utáni 24 órán belül. Ajánlási fokozat: 'A'.
2. Ajánlott az összes beteg szűrése depresszió, motoros, szenzoros, kognitív, kommunikációs és nyelési deficit irányában megfelelően képzett szakember által, standardizált és valid szűrőeszköz használatával. ('C' szintű ajánlás)
3. Ajánlott, hogy mindazon betegeken, akiknél a fentiek valamelyikének fennállása derül ki, az összehangolt rehabilitációs team megfelelő szakembere szabályszerű értékelést végezzen. ('C' szintű ajánlás)
4. Ajánlott, hogy a klinikus standardizált, valid felmérő eszközt használjon a páciens stroke által okozott károsodásánakés funkcionális állapotának kiértékeléséhez ('C' szintű ajánlás) és bátorítsa a páciens részvételét a közösségben és társas tevékenységeit.
5. Ajánlott a standardizált állapotfelmérés eredményeinek fölhasználása az eredményesség valószínűségének becslésében, az ellátás megfelelő szintjének meghatározásában és a terápiás eljárások kiválasztásában.
6. Ajánlott a felmérés megállapításainak megosztása és a várható kimenetel megvitatása a pácienssel és a családtagokkal/gondozókkal.
C. A terápia intenzitása/tartama Ajánlások
1. Erősen ajánlott, hogy a rehabilitációs terápia olyan korán induljon, ahogyan ez lehetséges, amint a beteg állapotának stabilitása ezt megengedi. Ajánlási fokozat: 'A'.
2. Ajánlott, hogy a beteg annyi kezelésben részesüljön, amennyi "szükséges", hogy adaptálódjon, felépüljön és/vagy helyreálljon funkcionális függetlenségének premorbid vagy optimális szintje. ('B' szintű ajánlás)
D. A páciens családja és gondozói Ajánlások
1. Ajánlott, hogy a stroke beteg családja/gondozója, ha elérhető, a lehető legkorábban legyen bevonva a döntéshozatalba és kezelés tervezésébe, s hasonlóképpen az egész rehabilitációs folyamat során végig.
2. Ajánlott, hogy az ellátók legyenek felkészülve arra a stresszre, amit a családban/gondozóban a beteg károsodásainak (pl. kognitív veszteség, vizelet-incontinentia, személyiség változás) felismerése válthat ki, és nyújtsanak támogatást, ha szükséges.
3. Ajánlott, hogy az akut ellátást végző kórház és a rehabilitációs ellátóhely rendelkezzen naprakész információval a lakóhelyi erőforrásokról, mind helyi, mind pedig országos szinten, hogy átadhassa ezt az információt a stroke betegeknek, családjuknak és gondozóiknak és hogy segítséget nyújthasson a szükséges szolgáltatások eléréséhez.
E. A páciens és a család/gondozó képzése Ajánlások
1. Ajánlott a páciens és a család/gondozó képzését interaktív és írásos formában nyújtani. ('B' szintű ajánlás)
2. Ajánlott, hogy a szakemberek fontolják meg egy meghatározott team tag kijelölését, aki felelős a páciensnek és a családnak/gondozónak a stroke természetéről, a stroke ellátással, rehabilitációval, eredményekkel kapcsolatos elvárásokról és ezeknek a rehabilitációs folyamatban játszott szerepéről történő tájékoztatásért. fC' szintű ajánlás)
3. Elismerendő, hogy a "család-értekezlet" az információ terjesztésének hasznos eszköze. ('C' szintű ajánlás)
4. Ajánlott, hogy a páciens és a család/gondozó képzése a kórlapban dokumentálva legyen, megelőzendő a fölösleges ismétléseket vagy a különböző szakterületekről származó, egymásnakellentmondó információkat. ('C' szintű ajánlás)
III. Rehabilitáció az akut szak során
A. Stroke betegek az akut szak során
A kórházi felvételt követő korai támogató ellátás céljai az alábbiak:
- Azon változások megfigyelése a páciens állapotában, amelyek különböző haladéktalan orvosi vagy sebészi beavatkozásokat tehetnek szükségessé.
- A kimenetel javítását megcélzó orvosi és sebészeti intézkedések elősegítése
- Intézkedések foganatosítása szubakut komplikációk megelőzésére
- Újabb stroke megelőzése érdekében szükséges kezelések tervezésének megkezdése.
- Rehabilitáció vagy egyéb technikák révén neurológiai funkciók helyreállásítására irányuló kísérlet megkezdése.
B. A kórtörténet felvétele és a fizikális vizsgálat elvégzése Ajánlások
1. Ajánlott a NIH stroke skála (ld.2.sz.függelék) használata a stroke súlyosságának felbecsülésére a kezdeti stádiumban, ami a halálozás és a hosszú távú kimenetel prediktora lehet.
2. Ajánlott, hogy a kezdeti értékelés foglalja magában a teljes kórtörténetet és fizikális vizsgálatot, különös hangsúllyal az alábbiakra:
- Újabb stroke előfordulására hajlamosító kockázati tényezők
- Kísérő betegségek
- Tudat vigilitásának szintje és kognitív állapot
- Nyelésre vonatkozó utalás
- A bőr folytonosságára vonatkozó utalás és felfekvésre hajlamosító tényezők számbavétele (ld. alább a B-1.alpontban)
- Végbél- és húgyhólyagfunkciók
- Mobilitás, figyelembe véve, hogy milyen mozgatási segítséget igényel a páciens
- Mélyvénás thrombosis kockázata (ld. alább a B-2.alpontban)
- Antiaggregánsok vagy véralvadásgátlók megelőző szedése (különösképpen a stroke létrejöttének idejében)
- Érzelmi támogatás a család és a gondozó részéről
B-1. Felfekvés kockázata Ajánlások
1. Ajánlott felvételkor a bőr folytonosságának tüzetes vizsgálata és azután legalább naponta történő követése. ('C'szintű ajánlás)
2. Ajánlott a megfelelő pozicionálás, forgatás és transzfer technikák használata; speciális matracok, védő pólyázás és párnázás használata a súrlódás vagy nagyon erős nyomás bőrkárosító hatásának elkerülésére. fC' szintű ajánlás)
B-2. Mélyvénás thrombosis kockázata
Ajánlások
1. Ajánlott a mobilizáció megkezdése, amilyen korán lehetséges. ('C' szintű ajánlás)
2. Ajánlott alacsony (megelőző) adagú subcutan heparin használata. Ajánlási fokozat:'A'.
Magyarországon az "A thromboemboliák megelőzése és kezelése" c. hatályos szakmai irányelv 3.5. alfejezetén belül a stroke népegésszégügyi jelentősége ellenére sem nyert önálló besorolást,a 3.5.6. alponton belül iscsakaz ischaemiás stroke szerepel, "nagy kockázati kategória" megjelöléssel, a prophylaxis időtartamára vonatkozó ajánlás nélkül. A Magyar Stroke Társaság szakmai irányelve [ld.az előszó 7.sz.hivatkozását] "Az akut stroke leggyakoribb szövődményei" c. fejezetben "a stroke miatt ágyhoz kötött, paretikus végtagú, tehát nagy kockázatú betegeknél" javasolja preventav adagú heparin adását, parenchymás vérzés esetén sem kizárva. A Rehabilitációs Szakmai Kollégium az utóbbi ajánlással egyetérve szükségesnek tartja iránymutatás adását a prophylaxis időtartamának meghatározásához. Abból
kiindulva, hogy heparin prophylaxis indítása akkor szükséges, ha a beteg ágyhoz kötött és/vagy alsó végtagi plegia (vagy plegia közeli paresis) áll fenn, figyelembe véve esetleges egyéb hajlamosító tényezőket (megelőző vénás thrombosis vagy tüdő-embolia, obesitas, malignoma), a preventio abbahagyható, ha a bénult alsó végtagi paresise közepesnél már nem súlyosabb, járóképességét visszanyerte, alsó végtagi vénás thrombosis gyanúja klinikailag nem merül fel. Megkönnyíti a döntést (fokozott kockázat esetén különösen) negatív D-dimer laboratóriumi teszt. Azokban a súlyos esetekben sem szükséges élethossziglani heparin-preventio, ha a helyreállási időszakban az alsó végtagi bénulás nem oldódik, ill. a beteg az erre irányuló erőfeszítések ellenére sem nyeri vissza járóképességét: Amennyiben alsó végtagi vénás thrombosis gyanúja klinikailag nem merül fel, s a D-dimer teszt negatív, a heparin adása abbahagyható. (Cardiogen agy-embolia -leggyakrabban pitvar-fibrillatio - esetén a betegség ezen szakaszában a bevagy visszaállított oralis antikoaguláns kezelés heparin adása nélkül is biztosítja a bénult megóvását a késői thromboemboliás szövődményektől.)
C. A stroke súlyosságának felmérése (NIHSS) Ajánlások
1. Erősen ajánlott a stroke súlyosságával kapcsolatosan a páciens felmérése a NIH stroke skála (ld.2.sz.függelék) használatával megjelenésekor/kórházi felvételekor vagy legalább a megjelenésétől számított 24 órán belül. Ajánlási fokozat: 'A'
2. Erősenajánlott, hogy valamennyi a stroke ellátásban részt vevő szakember ki legyen képezve és jogosítva legyen a NIH stroke skála használatára a stroke súlyosságának felméréséhez.
3. Ajánlott az akut ellátásból történő kibocsátáskor a páciens újrafelmérése a NIH stroke skála használatával.
4. Ajánlott, hogy amennyiben a rehabilitációra átkerült páciens hozott dokumentációjában nem szerepel a NIH stroke skála, akkor a rehabilitációs team végezzen el egy NIHSS felmérést.
D. A stroke és egyéb arteriosclerotikus érbetegségek másodlagos megelőzésének bevezetése Ajánlások
A stroke másodlagos megelőzésénekszükségessége élethossziglani és a rehabilitáció kritikus összetevője: Egyértelmű adatok szükségeseka hypertonia kezelésével, pitvar-fibrillatio esetén a kumarin alkalmazásával, agyi ischaemia esetén pedig az trombocita aggregáció gátló kezeléssel kapcsolatosan. Akár ischaemiás stroke, akár agyi állományvérzés esetén azonos ill. hasonló kockázati tényezők hajlamosítanak ischaemiás szívbetegségre is, melynek megelőzésére való törekvés szintén elengedhetetlen: antiaggregánsok, hypertonia uralása, ACE inhibitorok adásának megfontolása, lipid-csökkentő kezelés, mozgás, a dohányzás abbahagyása.
IV. Poststroke rehabilitáció
A. A post-acut stroke betegek rehabilitációs szolgáltatások miatti felmérése
Post-acut stroke: közvetlenül az akut ellátásból való kibocsátás utáni időszak. Ekkorra a beteg már stabil állapotot ért el, és az ellátás fókuszába a rehabilitáció kerül.
A rehabilitáció történhet rehabilitációs szakkórházban, általános kórház rehabilitációs osztályán (egységében), ápolási ellátóhelyen, a beteg otthonában és járóbeteg ellátásban.
A betegek egy része az akut ellátás ideje alatt oly mértékben felépül, hogy nem szorul rehabilitációs szolgáltatások igénybevételére.
B. Kórtörténet és fizikális vizsgálat ölelje fel az alábbi területeket:
- Komplikáció-kockázat (felfekvés, mélyvénás thrombosis kockázata, nyelési nehézség, végbél-és hólyag-dysfunctio, alultápláltság, esések, fájdalom)
- Károsodások meghatározása (nyelés, kognitív funkciók, kommunikáció; motoros, pszichés és a biztonsággal kapcsolatos tudatosság
- Pszichoszociális felmérés (család és gondozó, szociális támasz, financiális és kulturális megalapozottság)
- A megelőző és az aktuális funkcionális státusz felmérése
C. A komplikációk kockázatának felmérése
C-1. A nyelés felmérése (dysphagia) Ajánlások
1. Ajánlott, hogy folyadék vagy étel szájon át történő bevitelének megkezdése előtt minden beteg esetében egy egyszerű, valid, betegágynál elvégezhető nyelés-szűrés történjék. ('B' szintű ajánlás) A Rehabilitációs Szakmai Kollégium szükségesnek tartja ezt kiegészíteni azzal, hogy a dysarthria is felveti dysphagia gyanúját.
2. Ajánlott, hogy ez logopédus vagy ha logopédus nem elérhető, akkor más szakképzett és e feladatra kiképzett szakszemély (pl. ápoló vagy foglalkoztató terapeuta) által történjék. Ajánlási fokozat:T(nincs ajánlás).
3. Ha a szűrés szerint a nyelés nincs rendben, teljes betegágy melletti nyelésvizsgálat elvégzése ajánlott. Ezt ez irányban célzott képzésben részesített logopédus végezze. Ajánlási fokozat:'I'(nincs ajánlás).
4. Azon betegek körében, akiknél az aspiráció kockázata különösen nagy (pl. agytörzsi stroke), műszeres nyelésvizsgálat elvégzésének szükségessége mérlegelendő. ('B' szintű ajánlás)
5. Ajánlott a táplálék sűrűségét - állagát dietetikussal egyeztetni, ezzel biztosítva a standardizációt és élvezeti értéket.
C-2. Széklet- és vizelet-incontinentia kezelése Ajánlások
1. Szükség szerint ajánlott az akut stroke betegek hólyag funkciójának felmérése. A felmérés foglalja magába a következőket:
- Retentio mérés
- A vizelés gyakoriságának, mennyiségének mérése és kontrollálásának mértéke
- Dysuria esetleges fennállásának megállapítása
2. Ajánlatos a tartós transurethralis katéter eltávolításának megfontolása 48 órán belül. ('B' szintű ajánlás)
3. Amennyiben hólyag-katéter szükséges, ezüst ötvözettel bevont katéter alkalmazása ajánlott. (Az eredeti irányelvben 'B' szintű ajánlás, a Rehabilitációs Szakmai Kollégium Magyarországon jelenleg 'C' szintű ajánlást tart reálisnak. Részlegesen ld. 4.sz.függelék 5) pont.)
4. Nem áll rendelkezésre elegendő bizonyíték sem pro, sem kontra a hólyag funkció urodinamikával vagy egyéb módon történő felmérésével kapcsolatosan. Ajánlási fokozat:'I'(nincs ajánlás).
5. Vizelet-incontinens betegek esetében megfontolásra ajánlott egyénre szabott hólyag-tréning program kifejlesztése és megvalósítása. ('C' szintű ajánlás)
6. Vizelet-incontinens betegek esetében ajánlott ütemezett hólyagürítés alkalmazása. ('B' szintű ajánlás)
7. Tartós szorulás vagy széklet-incontinentia esetén széklet rendezési program alkalmazása ajánlott. Ajánlási fokozat:'I'(nincs ajánlás).
C-3. Alultápláltság
Ajánlások
1. Ajánlott, hogy a felvétel után a lehető leghamarabb történjék meg valamennyi beteg tápláltságánakés hidráltságának értékelése. A táplálék és folyadék bevitelt minden beteg esetében naponta követni kell, testsúlymérésre is rendszeresen sort kell keríteni. Ajánlási fokozat:'I'(nincs ajánlás).
2. Ajánlott, hogy több módszer legyen használatos a táplálék és a folyadék bevitel fenntartásában vagy növelésében. Ez megköveteli azon problémák kezelését, amelyek zavarják a bevitelt; segítség nyújtását az étkezésben, ha szükséges; folyadék konzekvens kínálását közvetlenül a dysphagiás beteg szájánál; és a beteg ízlésének figyelembe vételét az élelmezésben. Ajánlási fokozat:'I'(nincs ajánlás). Ha a bevitel szájon át nincs biztosítva, a táplálás gasztrosztómán keresztül válik szükségessé.
C-4. A fájdalom felmérése és kezelése Ajánlások
1. A fájdalom becslésére vizuális analóg skála (0-10) használata ajánlott. Ajánlási fokozata' (nincs ajánlás).
2. Ajánlott egy fájdalom menedzselési terv, amely a következők becslését tartalmazza: valószínűsíthető etiológia (úm. musculosceletalis, neuropathiás); a fájdalom lokalizációja; a fájdalom minősége, kiterjedése, tartama, intenzitása; és hogy mi súlyosbítja vagy csillapítja a fájdalmat.
3. A terápiát zavaró fájdalom uralandó.
4. A fájdalom miatt alkalmazott azon központi idegrendszerre ható szereket, amelyek zavartságot vagy a kognitív képességek romlását okozhatják, ajánlatos alacsonyabb adagban adni.
D. A gondolkodás és a kommunikáció felmérése Ajánlások
1. Ajánlott, hogy a gondolkodás, az éberség és a figyelem felmérése a következő területekre irányuljon: tanulás és emlékezés, vizuális neglect, figyelem, apraxia és probléma megoldás. (Tactilis neglect egyszerű vizsgálattal a betegágynál is könnyen szűrhető.)
2. Pro vagy kontra állásfoglalás nélkül tartalmaz a '3.' függelék standard szűrő és felmérő eszközöket.
3. Ajánlott, hogy a kommunikációs képességek felmérése a következő területekre irányuljon: beszédhallgatás, beszéd, olvasás, írás és a nyelvhasználat.
4. Pro vagy kontra állásfoglalás nélkül tartalmaz a '3.' függelék standard szűrő és felmérő eszközöket.
E. Pszichoszociális felmérés Ajánlások
1. Ajánlott, hogy valamennyi stroke beteg pszichoszociális felmérésben, intervencióban részesüljön. (B szintű ajánlás)
2. Ajánlott, hogy a családok, más fontos személyekés a gondozók tartozzanak bele a felmérésbe. (B szintű ajánlás)
3. Ajánlott valamennyi stroke beteg szociális munkáshoz irányítása átfogó pszichoszociális állapotfelmérésre és intervencióra. Ajánlási fokozat:'I'(nincs ajánlás).
4. Ajánlott, hogy a pszichoszociális állapotfelmérés foglalja magába a következő területeket:
- A stroke előtti történet (pl. demográfiai adatok, korábbi fizikai állapot és kezelésre adott válasz, anyagi javakkal való élés és visszaélés, pszichiátriai, érzelmi és szellemi állapot és történet, iskolázottság és foglalkozás; katonai, jogi és megküzdési stratégiák)
- Család/gondozó helyzete és kapcsolatai
- Erőforrások (pl. jövedelem, lakásviszony, társas kapcsolatok)
- Spirituális és kulturális tevékenységek
- Szabadidős tevékenységek, hobbik.
- A páciens/család/gondozó felfogása az állapotról, kezelésről és prognózisról, valamint reményeik és elvárásaik az ellátással kapcsolatosan
F. Funkció felmérés Ajánlások
1. Ajánlott, hogy standardizált állapotfelmérő eszközzel történjék a stroke beteg funkcionális állapotának felmérése. ('B' szintű ajánlás)
2. Ajánlott a FIM használatának megfontolása. (Ld.3.sz.függelék)
Megvitatás
A funkciófelmérés magában foglalhatja a következőket (nem feltétlenül korlátozódva azokra) abc sorrendben:
- Aerob kapacitás és teherbíró képesség
- Continentia
- Egyensúly
- Éberség, figyelem és gondolkodás
- Fájdalom
- Helyváltoztatás
- Izom teljesítmény (erő, energia, kitartás)
- Izületek épsége és mozgékonysága
- Járásmód
- Keringés (úm. cardiovascularis jelek/tünetek és pozíció-változásra adott válasz)
- Motoros funkció (úm. mozgásminták, koordináció, kézügyesség, mozgékonyság)
- Mozgástartomány
- Ortézisek, védő- és támasztó eszközök
- Önellátás (ADL, IADL)
- Reflex integritás
- Segítő és adaptív eszközök
- Szexuális aktivitás
- Testtartás
G. Szüksége van-e a betegnek rehabilitációs intervencióra? Ajánlások
1. Erősen ajánlott, hogy amint a beteg állapota stabil, az akut ellátást végző orvosa konzultáljon a rehabilitációs szolgáltatókkal (úm. fizioterápia, foglalkoztató terápia, logopédia, fizikális medicina), hogy mérjék fel a beteg rehabilitációs szükségleteit, és hogy ajánlják meg ezek kielégítésének legmegfelelőbb helyszínét. Ajánlott, hogy a standard eljárásmódot használó multidiszciplináris állapotfelmérés és annak dokumentálása minden beteg esetén történjen meg.
H. "Inpatient" (bentlakásos, kórházi) rehabilitáció indikált-e? Ajánlások
1. Erősen ajánlott, hogy a rehabilitációs szolgáltatások igénybevételére szoruló pácienseknek legyen hozzáférésük koordinált, szervezett stroke szolgáltatások nyújtásában jártas rehabilitációs teamhez. Az "inpatient" post-acut stroke ellátás összehangoltsága és szervezettsége javítja a kimenetelt. Ajánlási fokozat:'A'.
2. Nem tehető ajánlás egyik lehetséges rehabilitációs színhely típus mellett sem, meggyőző bizonyíték hiányában.
3. Ajánlott, hogy a páciens károsodásának súlyossága, a családi/társadalmi támogatás hozzáférhetősége és a páciens/család preferenciái határozzák meg az ellátás optimális környezetét. Ajánlási fokozatíI'(nincs ajánlás).
4. Ajánlott, hogy a páciensek addig maradjanak rehabilitációs ellátásuk "inpatient" keretében, ameddig szakképzett ápolás nyújtására, folyamatos orvosi ellátásra és sokrétű terápiás intervencióra van szükségük. Ajánlási fokozat:'I'(nincs ajánlás).
I. Független-e a beteg alapszintű és kiterjesztett önellátó képességét illetően? Ajánlások
1. Ajánlott, hogy valamennyi poststroke beteg elbocsátása előtt legyen újrafelmérve alapszintű (azaz személyes teendői terén való) önellátó képességét illetően. ('B' szintű ajánlás)
2. Ajánlatos, hogy valamennyi olyan páciens, aki terv szerint önálló életvitelt fog folytatni a lakóhelyén, elbocsátása előtt legyen felmérve kiterjesztett önellátó képességét illetően. ('B' szintű ajánlás)
3. Ajánlott, hogy legalább a következő képességek ill. lehetőségek legyenek meg, ha valaki otthonában egyedül tartózkodik: (1) egyszerű étel elkészítése vagy fölmelegítése, (2) biztonsági rendszabályok betartása, és józan ítélőképesség, (3) gyógyszerbevétel, (4) vészhelyzet esetén segítség igénybevételének lehetősége.
J. A páciens korábbi otthonába/lakóhelyére bocsátása és orvosi követésének biztosítása az alapellátásban Ajánlások
1. Ajánlott, hogy minden beteg részesüljön másodlagos megelőzési programban (ld. III-D)
2. Ajánlott a post-acut stroke betegek követése az alapellátásban (rizikófaktorok; kísérő betegségek kezelésének folytatása).
3. Ajánlott a páciensnek és a családnak a stroke rizikófakoraival kapcsolatos képzése.
J-1. Gyakorlás program Ajánlás
Ajánlott a páciens részvétele egy rendszeres erősítő, aerob gyakorló programban otthon vagy egy megfelelő közösségi programban, amely program a páciens kísérőbetegségeinek és funkcionális korlátainak figyelembe vételével épül fel. ('B' szintű ajánlás)
J-2. Adaptív eszközök, tartós orvosi eszközök, ortézisek és kerekes székek Ajánlások
1. Ajánlott, adaptív eszközök használata a biztonság és a funkció érdekében, ha a feladat véghezvitele más módon nem érhető el vagy nem tanulható meg vagy ha a páciens biztonsága aggályos. ('C' szintű ajánlás)
2. Ajánlott alsó végtag ortézis megfontolása, ha a boka vagy a térd stabilizálása szükséges jobb járásmód vagy esés megelőzése érdekében. ('C' szintű ajánlás)
3. Kezdetben előregyártott sín használata ajánlott. Méret-vétel alapján csak azoknak a pácienseknek készüljön ortézis, akiknek az esetében kiderül, hogy hosszú távon lesz szükségük az eszközre. ('C' szintű ajánlás)
4. Ajánlott, hogy kerekes szék felírása a páciens és a környezet (amelyben a kerekes széket használni fogja) gondos felmérésén alapuljon. ('C' szintű ajánlás)
5. Ajánlott a járási segédeszközök oly módon történő használata, hogy azok segítsék a helyváltoztatás hatékonyságát és biztonságát, ha szükséges.
J-3. Visszatérés a munkába Ajánlás
Ajánlott, hogy valamennyi olyan páciens-akinek az állapota lehetővé teszi - a munkába való visszatérésre vonatkozó képességének felmérésére bátorítást kapjon. ('C' szintű ajánlás)
J-4. Visszatérés a gépjárművezetéshez Ajánlások
1. Ajánlott, hogy minden beteg számára legyen adott fizikai, kognitív és viselkedési funkcióinak felmérése, hogy ezáltal eldönthető legyen, képes-e a gépjármű vezetéshez való visszatérésre. (Ajánlási fokozat: 'I' - nincs ajánlás.) Azokban az egyedi esetekben, amikor akár a családban, akár az ellátókban kétségek ébrednek, hatósági alkalmassági vizsga szükséges. Minden ellátóhelyen ismeretesnek kell lennie a stroke utáni autóvezetéssel kapcsolatos jogi szabályozásnak.
2. Ajánlott, hogy az ellátó szakemberekfontolják meg a reziduális deficittel küzdő páciens adaptív autóvezetési képzési programra irányítását a deficit minimalizálása, a biztonsággal kapcsolatos aggályok leküzdése érdekében és azért, hogy a hatósági alkalmassági vizsgán megfelelhessen. Ajánlási fokozat:'I' (nincs ajánlás).
J-5. Szexuális funkció Ajánlás
Ajánlott, hogy a szexualitással kapcsolatos kérdések a rehabilitáció során kerüljenek megbeszélésre, ha a poststroke páciens és partnere erre készséget mutat.
K. A súlyos stroke által sújtott páciensekés/vagy maximális függőség és a funkcionális helyreállásra való kedvezőtlen kórjóslat
Azoka páciensek, akiket súlyos stroke sújtott vagy a napi élettevékenység terén maximálisan függőekés a funkcionális helyreállásra vonatkozó kórjóslatuk kedvezőtlen, nem tekinthetőek rehabilitációs intervencióra jelölteknek. A családokat és a gondozókat a páciensek ellátásával kapcsolatos oktatásban kell részesíteni. Ennek a következőket kell magában foglalnia: újbóli stroke megelőzése, a lehetséges komplikációk és pszichés zavarok jelei és tünetei, gyógyszerbeadás, asszisztált napi élettevékenységgel kapcsolatos feladatok (pl. átültetés, fürdetés, pozicionálás, öltöztetés, etetés, ürítés, tisztántartás), nyelési technikák, táplálás és folyadékbevitel, tartós transurethralis katéterrel való foglalkozás, bőrvédelem, kontraktúrák, tápszonda használata, otthoni gyakorlás (mozgástartomány). A családoknak tanácsot kell kapniuk a hosszú távú ellátást biztosító ápolási otthonba helyezés előnyeiről.
L. A poststroke beteg "inpatient" (bentlakásos, kórházi) rehabilitációja
Az "inpatient" rehabilitáció definíciója: rehabilitációs szakkórházban vagy általános kórház rehabilitációs osztályán (egységében) véghezvitt bentlakásos rehabilitáció.
M. Az ellátás optimális szintjének meghatározása
Ajánlás
Erősen ajánlott, hogy a rehabilitációs szolgáltatások szervezett és koordinált post-acut stroke rehabilitációs környezetben nyújtassanak. Ajánlási fokozat: 'A'.
Magyarországon ilyennek tekinthetőek a rehabilitációs szakkórházak stroke-rehabilitációs, neurorehabilitációs vagy mozgásszervi rehabilitációs osztályai vagy részlegei, stroke centrum rehabilitációs osztálya, általános kórházak stroke-rehabilitációs, neurorehabilitációs és mozgásszervi rehabilitációs osztálya.
N. A páciens/család képzése, közös döntés elérése a rehabilitációs programról és a kezelési terv meghatározása Ajánlások
1. Ajánlott, hogy a klinikus team és a család/gondozó a rehabilitációs program felől közös döntésre jusson.
2. Ajánlott, hogy a rehabilitációs program különböző céljai a páciens, a család és a rehabilitációs team konszenzusa alapján fogalmazódjanak meg.
3. Ajánlott, hogy a páciens családja/gondozója vegyen részt egyes rehabilitációs munkafázisokban és szerezhessen gyakorlatot a páciens funkcionális tevékenységeinek segítésében, ha ez szükséges.
O. Rehabilitációs programok és intervenciók bevezetése
Nyelés: Dysphagia kezelés
Ajánlás
Azon stroke betegek számára, akik kellő táplálása és folyadékkal való ellátása szájon át nem biztosítható, mesterséges táplálás megfontolása ajánlott. ('B' szintű ajánlás)
Kommunikációs
1. Ajánlott, hogy a kommunikációs zavarral küzdő beteg korai kezelésben részesüljön, kommunikációs képességének változása pedig követve legyen azért, hogy kommunikációs készségének helyreállása a legkedvezőbben alakulhasson; hogy, ha szükséges, használható kompenzációs stratégiái alakulhassanak ki.
2. Ajánlott, hogy a logopédus képezze a rehabilitációs szakembereket és a családot/gondozót a kommunikációs zavarral küzdő pácienssel történő kommunikációt javító technikákban.
Motoros
Motoros működés-erősítés
AJÁNLÁS. Ajánlott, hogy az erősítés legyen belefoglalva a paretikus izomzatú stroke után lévő betegek akut rehabilitációjába. Ajánlási fokozat:'I'(nincs ajánlás).
Funkcionális elektromos stimuláció (FES)
Ajánlások
1. Károsodott izom-kontrakciót mutató páciensek FES kezelése ajánlott, különösen a boka/térd/csukló motoros károsodása esetén. ('B' szintű ajánlás)
2. Subluxált vállú páciensek FES kezelése ajánlott. ('B' szintű ajánlás)
Spaszticitás Ajánlások
1. Ajánlott, hogy a spaszticitás és a kontraktúrák antispasztikus pozicionálással, passzív mozgásgyakorlatokkal, nyújtással, sínezéssel, egyre fokozódó korrekciót biztosító sínezéssel vagy korrekciós műtéttel legyenek kezelve. ('C' szintű ajánlás)
2. Per os myorelaxansok adása mérlegelendő a spaszticitás miatt, ha az fájdalmat, a bőr nehezített tisztántarthatóságát vagy funkciócsökkenést okoz. ('B' szintű ajánlás)
3. Diazepam vagy egyéb benzodiazepin származék adása a stroke utáni helyreállási időszakban nem ajánlott. ('D' ajánlási kategória)
4. Botulin toxin vagy fenol/alkohol használata mérlegelendő válogatott esetekben, ha a spaszticitás extrém erős, fájdalmat, a bőr nehezített tisztántarthatóságát vagy funkciócsökkenést okoz. ('B' szintű ajánlás)
Biofeedback
AJÁNLÁS nem tehető, sem mellette, sem ellene.
Vállfájdalom
Ajánlások
1. Stroke után az érintett oldalon vállfájdalom megelőzésére az alábbi beavatkozások mérlegelése ajánlott:
- Elektromos stimuláció a váll kifelé rotációjának javítására
- Heveder
- A dolgozók oktatása a hemiplég váll traumatizálásának megelőzésére
2. A már kialakult vállfájdalom kezelésére az alábbi beavatkozások mérlegelése ajánlott:
- Localis (periarticularis) kortikoszteroid injekció
- Heveder
- A passzív mozgástartomány növelése olyan nyújtási és mobilizációs technikákkal, amelyek különösen a kifelé rotációra és az abdukcióra összpontosítanak, mint a befagyott váll és a váll-kéz-fájdalom szindróma megelőzési eszközére
- Kezelésmódok: jegelés, melegítés, lágyszövet masszázs
- FES
- Erősítés
Pszichés
Kognitív helyreigazítás
AJÁNLÁSOK
1. Ajánlott, hogy a páciens kognitív deficitek irányában legyen felmérve és részesüljön kognitív tréningezésben, amennyiben az alábbi körülmények valamelyike fennáll:
- Figyelem deficit ('A' szintű ajánlás)
- Vizuális neglect ('B' szintű ajánlás)
- Memória deficit
- Végrehajtó funkciók és probléma megoldás nehézségei ('C' szintű ajánlás)
2. Több területet érintő kognitív károsodás esetén hasznos lehet a kognitív tréningezés változatossága, amely több diszciplinát involválhat. ('C' szintű ajánlás)
3. Enyhe rövid távú memória deficit esetén kompenzációs stratégiákat kifejlesztő tréningezés alkalmazás ajánlott. ('B' szintű ajánlás)
Kedélyzavarok:
Depresszió és emocionális labilitás
Ajánlások
Vizsgálat
1. Egyik meghatározott diagnosztikus eszköz mellett sem történik ajánlás valamelyik másik rovására.
2. Meghatározott pszichiátriai tünetek felmérésére strukturált pszichometria alkalmazása ajánlott, valamint a tünetek időben való követése.
3. Ajánlatos a poststroke páciens vizsgálata egyéb pszichiátriai bajokat illetően is, beleértve a szorongást, a bipoláris betegséget és a patológiás indulatot.
KEZELÉS
4. Erős ajánlás diagnosztizált depresszió esetén, ha kontraindikáció nem áll fenn, antidepresszáns adásának megkísérlése.
5. Antidepresszáns csoporttal kapcsolatosan ajánlás nem történik, noha a mellékhatás-profil ismerete ebben a betegségcsoportban az SSRI-k (szelektív szerotonin újrafelvétel gátlók) előnyben részesítése mellett szólhat.
6. Súlyos, tartósan fennálló vagy zavaró sírás esetén antidepresszáns adásának megkísérlése ajánlott.
7. 6.pont esetén SSRI választása ajánlott.
8. Önmagában pszichoterápia alkalmazását illetően poststroke depresszió esetén nem áll rendelkezésre elegendő bizonyíték sem pro- sem kontra ajánláshoz.
9. Ajánlott a betegek informálása, tanács adása és lehetőség biztosítása arra, hogy beszélhessenek arról, milyen kihatással van betegségük az életükre.
10. Profilaktikus célzattal antidepresszánsok rutin alkalmazása poststroke betegek körében nem ajánlott. ('D' fokozatú (ellen)ajánlás, elsőszintű bizonyíték minőségmutatóval és jó átfogó minősítéssel)
11. Ajánlás, hogy a perzisztáló distresszt vagy a fogyatékosság rosszabbodását okozó kedélyzavarok kezelése tapasztalt klinikai szakpszichológus vagy pszichiáter által vagy tanácsai alapján történjék.
Vizuális és tér-neglect Ajánlások
1. Ajánlás, hogy a stroke betegek legyenek felmérve a vizuális és tér-neglect irányában. ('C' szintű ajánlás)
2. Ajánlása vizuális/tér-neglect jelenséggel küzdő betegek funkcionális adaptációra (pl. vizuális átpásztázás, a környezet adaptálása, a páciens/család oktatása) fókuszáló kezelése. ('B' szintű ajánlás)
Gyógyszeres
Gyógyszerhatóanyagok használata Ajánlások
1. A stroke utáni helyreállás időszakában neuroleptikumok, benzodiazepine^ fenobarbital,phenytoin adása ellenzendő. Ezeka hatóanyagokstroke betegek körében kellő körültekintéssel alkalmazhatóak, mérlegelve a vélelemezett előnyt a kimenetelre gyakorolt lehetséges kedvezőtlen hatásokkal szemben. ('B' szintű ajánlás)
2. Centrális hatású á2-adrenerg receptor agonista (clonidine és egyebek) és ál-receptor antagonista (prazosin és egyebek) adása antihypertensivumként stroke betegek körében ellenzendő a helyreállást károsító lehetséges hatásuk miatt. ('D' ajánlási kategória)
3. Központi idegrendszeri stimulánsok (pl. dextroamphetamine) optimális adagolásával és biztonságával kapcsolatosan nem áll rendelkezésre elegendő bizonyító erejű adat, ezért adásuk legfeljebb válogatott esetekben lenne fontolóra vehető. Magyarországon, ahol e gyógyszerhatóanyag korábban kivonásra került, ennek megvalósítása csak bizonyító erejű szakirodalmi adatok napvilágra kerülése után vetődhet érdemben fel.
P. Kész-e a páciens a lakóhelyi életre?
Ajánlások (valamennyi esetben az ajánlási fokozat'I', azaz nincs ajánlás)
1. Ajánlott, hogy a páciens, a család és a gondozók legyenek részletesen tájékoztatva, felkészítve és bevonva az egészség-fenntartási és biztonsági szükségletekkel kapcsolatosan.
2. Ajánlott, hogy a család és a gondozók minden a mozgatással kapcsolatos eszközt és tréningezést megkapjanak.
3. Ajánlott, hogy a páciensnek legyen megfelelő támogatási lehetősége a hivatásával és a jövedelmével kapcsolatosan. Azok a stroke betegek, akik a stroke előtt kereső foglalkozást űztek, kapjanak bátorítást a munkába való visszatérés képességének felmérésére, ha állapotuk ezt megengedi.
4. Ajánlott, hogy a páciens szabadidős tevékenységei legyenek ismeretesek és legyenek bátorítva és, hogy a páciensnek meg legyen engedve a részvétel valamely ilyen tevékenységben.
5. Ajánlott, hogy az akut ellátást végző kórház és a rehabilitációs ellátóhely tartson naprakész jegyzéket a lakóhelyi erőforrásokról, hogy átadhassa ezt az információt a stroke betegeknek, családjuknak és gondozóiknak és hogy segítséget nyújthasson a szükséges szolgáltatások eléréséhez.
Q. A gyógykezeléshez kötöttség és a fejlődés akadályai
Ha az egészségállapot nem stabil, akut ellátásba irányítás. Ha mentálhigiénés tényezőkről van szó, pszichiátriára irányítás.
A rehabilitációs folyamat során előfordulhat, hogy a páciensek váratlan akadályokkal kerülnek szembe, amelyek lehetetlenné teszik folyamatos fejlődésüket ill. a rehabilitációs terv megvalósulását. Ezek orvosi komplikációk vagy mentálhigiénés tényezők lehetnek, de a diagnózis, a prognózis a kezelés logikai megalapozottságának a hiánya vagy az ezzel kapcsolatos nem megfelelő információ szintén a fejlődés gátjává válhat.
Ez a vizsgálat és kezelés a legtöbb esetben az adott rehabilitációs keretben is megtörténhet és nem követeli e beteg máshová helyezését. Amint a korlátok sikeresen megfogalmazódtak, a kezelési célok felülvizsgálása jó szolgálatot tehet.
- Ha az az akadály, amellyel szembekerültünk, olyan testi betegség, amely a rehabilitációban való részvételt nehézzé teszi, a megfelelő ellátó helyre való áthelyezés tekinthető helyénvalónak.
- Ha a probléma mentálhigiénés tényezőkkel kapcsolatos, ezen faktorok pszichiáter/pszichológus által történő vizsgálata és kezelése szükséges.
R. A páciens szükségletének felmérése a lakóközösségen alapuló rehabilitációs szolgáltatások iránt.
A páciens rehabilitációját szolgáló optimális környezet meghatározása: járóbeteg ellátás vagy lakóközösségen alapuló
szolgáltatások.
Az ambuláns rehabilitáció meghatározása: vagy önálló vagy kórházhoz (akár általános, akár rehabilitációs) csatolt járóbeteg rendelőben véghezvitt rehabilitáció. A nappali kórházi ellátás az ambuláns rehabilitáció alesete, amikor a páciens a nappal nagyobb részét ezen ellátóhelyen tölti.
Az otthoni rehabilitáció meghatározása: A páciens lakhelyén nyújtott rehabilitációs program.
S. A lakóközösségen alapuló rehabilitációs szolgáltatások optimális környezetének meghatározása
Ajánlás
Erősen ajánlott, hogy a kórházon kívüli rehabilitációs szolgáltatásokabban a keretben folyjanak, amelyben a leginkább helyénvalóan és eredményesen kivitelezhetőek. Ez az egészség- és funkcionális állapoton, szociális helyzeten és az ellátás elérhetőségén alapul. Ajánlási fokozat:'A'.
V. Gondozás
VI. Irodalomjegyzék
A szabadon hozzáférhető teljes szöveg ("free full text") az alábbi Internet-helyről kiindulva érhető el, az azonos sorszámú hivatkozás hypertext-jére kattintva: http://stroke.ahajournals.org/cgi/content/full/36/9/2049
1. Gresham GE, Duncan PW, Stason WB, et al. Post-Stroke Rehabilitation. Clinical Practice Guideline, No. 16. Rockville, Md: US Department of Health and Human Services, Public Health Service, Agency for Health Care Policy and Research; May 1995. AHCPR Publication No. 95-0662.
2. Royal College of Physicians. National Clinical Guidelines for Stroke. 2nd ed. Prepared by the Intercollegiate Stroke Working Party. London: Royal College of Physicians; 2004. Available at: http://www.rcplondon.ac.uk/pubs/books/stroke/index.htm. Accessed July 20,2005.
3. Scottish Intercollegiate Guidelines Network (SIGN). Management of Patients with Stroke Part III: Identification and Management of Dysphagia, No. 20. Edinburgh, Scotland: Scottish Intercollegiate Guidelines Network; 1997. [Superseded by Management of Patients with Stroke: Identification and Management of Dysphagia, No. 78; 2004.]
4. United States Preventive Service Task Force (USPSTF). Guide to Clinical Preventive Services. 2nd ed. Baltimore, Md: Williamsand Wilkins; 1996.
5. American Heart Association. Heart and Stroke Statistical Update-2000. Dallas,Tex: American Heart Association; 1999.
6. Cifu DX, Stewart DG. Factors affecting functional outcome after stroke: a critical review of rehabilitation interventions. Arch Phys Med Rehabil. 1999; 80 (5 suppl 1): S35-S39
7. Stroke Unit Trialists' Collaboration. Organised inpatient (stroke unit) care for stroke. Cochrane Database Syst Rev. 2002
(1): CD000197.
8. Evans RL, Connis RT, Hendricks RD, Haselkorn JK. Multidisciplinary rehabilitation versus medical care: a meta-analysis. Soc Sci Med. 1995; 40:1699-1706
9. Duncan PW, Horner RD, Reker DM, Samsa GP, Hoenig H, Hamilton B, LaClair BJ, Dudley TK. Adherence to postacute rehabilitation guidelines is associated with functional recovery in stroke. Stroke. 2002; 33:167-177.[Abstract/Free Full Text]
10. Duncan PW, Lai SM, van Culin V, Huang L, Clausen D, Wallace D. Development of a comprehensive assessment toolbox for stroke. Clin Geriatr Med. 1999; 15:885-915
11. Barnett HJ, Taylor DW, Eliasziw M, Fox AJ, Ferguson GG, Haynes RB, Rankin RN, Clagett GP, Hachinski VC, Sackett DL, Thorpe KE, Meldrum HE, Spence JD. Benefit of carotid endarterectomy in patients with symptomatic moderate or severe stenosis. North American Symptomatic Carotid Endarterectomy Trial Collaborators. N Engl J Med. 1998; 339: 1415-1425.[Abstract/Free Full Text]
12. Albers GW, Amarenco P, Easton JD, Sacco RL, Teal P. Antithrombotic and thrombolytic therapy for ischemic stroke. Chest. 2001; 119 (1 suppl): 300S-320S.[Free Full Text]
13. Mohr JP, Thompson JL, Lazar RM, Levin B, Sacco RL, Furie KL, Kistler JP, Albers GW, Pettigrew LC, Adams HP Jr, Jackson CM, Pullicino P; Warfarin-Aspirin Recurrent Stroke Study Group. A comparison of warfarin and aspirin for the prevention of recurrent ischemic stroke. N Engl J Med. 2001; 345:1444-1451.[Abstract/Free Full Text]
14. Albers GW. Choice of endpoints in antiplatelet trials: which outcomes are most relevant to stroke patients? Neurology. 2000; 54:1022-1028.[Abstract/Free Full Text]
15. AlbersGW, Amarenco P, Easton JD, Sacco RL,Teal P. Antithrombotic and thrombolytic therapy for ischemic stroke: the Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy. Chest. 2004; 126 (suppl 3): 483S-512S.[Abstract/Free Full Text]
16. Geerts WH, Pineo GF, Heit JA, Bergqvist D, Lassen MR,Colwell CW, Ray JG. Prevention of venous thromboembolism: the Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy. Chest. 2004; 126 (suppl 3): 338S-400S.[Abstract/Free Full Text]
17. Prognosis of patients with symptomatic vertebral or basilar artery stenosis. The Warfarin-Aspirin Symptomatic Intracranial Disease (WASID) Study Group. Stroke. 1998; 29:1389-1392.[Abstract/Free Full Text]
18. European Stroke Prevention Study. ESPS Group. Stroke. 1990; 21:1122-1130.
19. Bellavance A. Efficacy of ticlopidine and aspirin for prevention of reversible cerebrovascular ischemic events. The Ticlopidine Aspirin Stroke Study. Stroke. 1993; 24:1452-1457.
20. Yusuf S, Sleight P, Pogue J, Bosch J, Davies R, Dagenais G. Effects of an angiotensin-converting-enzyme inhibitor, ramipril, on cardiovascular events in high-risk patients. The Heart Outcomes Prevention Evaluation Study Investigators. N Engl J Med. 2000; 342: 145-153.[Errata in N Engl J Med. 2000;342:1376; N Engl J Med.
2000;342:748.][Abstract/Free Full Text]
21. Yusuf S, Zhao F, Mehta SR, Chrolavicius S, Tognoni G, Fox KK; Clopidogrel in Unstable Angina to Prevent Recurrent Events Trial Investigators. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST-segment elevation. N Engl J Med. 2001; 345:494-502.[Errata in N Engl J Med. 2001;345:1716; N Engl J Med.
2001;345:1506.][Abstract/Free Full Text]
22. Dahlof B, Devereux RB, Kjeldsen SE, Julius S, Beevers G, de Faire U, Fyhrquist F, Ibsen H, Kristiansson K, Lederballe-Pedersen O, Lindholm LH, Nieminen MS, Omvik P, Oparil S, Wedel H; LIFE Study Group. Cardiovascular morbidity and mortality in the Losartan Intervention For Endpoint reduction in hypertension study (LIFE): a randomised trial against atenolol. Lancet. 2002; 359: 995-1003.
23. PROGRESS Collaborative Group. Randomised trial of a perindopril-based blood-pressure-lowering regimen among 6,105 individuals with previous stroke or transient ischaemic attack. Lancet. 2001; 358: 1033-1041.[Errata in: Lancet. 2001;358:1556; Lancet. 2002;359:2120.]
24. Randomised trial of cholesterol lowering in 4444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S). Lancet. 1994; 344:1383-1389.
25. Sacks FM, Pfeffer MA, Moye LA, Rouleau JL, Rutherford JD, Cole TG, Brown L, Warnica JW, Arnold JM, Wun CC, Davis BR, Braunwald E. The effect of pravastatin on coronary events after myocardial infarction in patients with average cholesterol levels. Cholesterol and Recurrent Events Trial investigators. N Engl J Med. 1996; 335: 1001-1009.[Abstract/Free Full Text]
26. Hunt D, Young P, Simes J, Hague W, Mann S, Owensby D, Lane G, Tonkin A. Benefits of pravastatin on cardiovascular events and mortality in older patients with coronary heart disease are equal to or exceed those seen in younger patients: results from the LIPID trial. Ann Intern Med. 2001; 134: 931-940.[Abstract/Free Full Text]
27. Schwartz GG, Olsson AG, Ezekowitz MD, Ganz P, Oliver MF, Waters D, Zeiher A, Chaitman BR, Leslie S, Stern T; Myocardial Ischemia Reduction with Aggressive Cholesterol Lowering (MIRACL) Study Investigators. Effects of atorvastatin on early recurrent ischemic events in acute coronary syndromes: the MIRACL study: a randomized controlled trial. JAMA. 2001; 285:1711-1718.[Abstract/Free Full Text]
28. Goldstein LB, Adams R, Becker K, Furberg CD,GorelickPB, Hademenos G, Hill M, Howard G, Howard VJ, Jacobs B, Levine SR, Mosca L, Sacco RL, Sherman DG, Wolf PA, del Zoppo GJ. Primary prevention of ischemic stroke: a statement for healthcare professionals from the Stroke Council of the American Heart Association. Circulation. 2001; 103: 163-182.[Free Full Text]
29. Wolf PA, Clagett GP, Easton JD, Goldstein LB, Gorelick PB, Kelly-Hayes M, Sacco RL, Whisnant JP. Preventing ischemic stroke in patients with prior stroke and transient ischemic attack: a statement for healthcare professionals from the Stroke Council of the American Heart Association. Stroke. 1999; 30:1991-1994.[Free Full Text]
30. Reding MJ, Potes E. Rehabilitation outcome following initial unilateral hemispheric stroke: life table analysis approach. Stroke. 1988; 19: 1354-1358.
31. The International Stroke Trial (IST): a randomised trial of aspirin, subcutaneous heparin, both, or neither among 19435 patients with acute ischaemic stroke. International Stroke Trial Collaborative Group. Lancet. 1997; 349:1569-1581.
32. Bath PM, Iddenden R, Bath FJ. Low-molecular-weight heparins and heparinoids in acute ischemic stroke: a meta-analysis of randomized controlled trials. Stroke. 2000; 31:1770-1778.[Abstract/Free Full Text]
33. Bath PM, Bath FJ, Smithard DG. Interventions for dysphagia in acute stroke. Cochrane Database Syst Rev. 2000; (2): CD000323.
34. Bijsterveld NR, Hettiarachchi R, Peters R, Prins MH, Levi M, Buller HR. Low-molecular weight heparins in venous and arterial thrombotic disease. Thromb Haemost. 1999; 82 suppl 1:139-147.
35. Kamran SI, Downey D, Ruff RL. Pneumatic sequential compression reduces the risk of deep vein thrombosis in stroke patients. Neurology. 1998; 50:1683-1688.
36. Warkentin TE. Heparin-induced thrombocytopenia: diagnosis and management. Circulation. 2004; 110: e454-e458.[Free Full Text]
37. Berlowitz DR, Brandeis GH, Anderson JJ, Ash AS, Kader B, Morris JN, Moskowitz MA. Evaluation of a risk-adjustment model for pressure ulcer development using the Minimum Data Set. J Am Geriatr Soc. 2001; 49: 872-876
38. Berlowitz DR, Brandeis GH, Morris JN, Ash AS, Anderson JJ, Kader B, Moskowitz MA. Deriving a risk-adjustment model for pressure ulcer development using the Minimum Data Set. J Am Geriatr Soc. 2001; 49: 866-871
39. Sussman C, Bates-Jensen BM, eds. Wound Care: A Collaborative Practice Manual for Physical Therapists and Nurses. Gaithersburg, Md: Aspen Publishers; 1998.
40. Nakayama H, Jorgensen HS, Pedersen PM, Raaschou HO, Olsen TS. Prevalence and risk factors of incontinence after stroke. The Copenhagen Stroke Study. Stroke. 1997; 28: 58-62.[Abstract/Free Full Text]
41. Venn MR, Taft L, Carpentier B, Applebaugh G. The influence of timing and suppository use on efficiency and effectiveness of bowel training after a stroke. Rehabil Nurs. 1992; 17:116-120
42. Evans A, Perez I, Harraf F, Melbourn A, Steadman J, Donaldson N, Kalra L. Can differences in management processes explain different outcomes between stroke unit and stroke-team care? Lancet. 2001; 358:1586-1592.
43. Langhorne P, Duncan P. Does the organization of postacute stroke care really matter? Stroke. 2001; 32: 268-274.[Abstract/Free Full Text]
44. Early Supported Discharge Trialists. Services for reducing duration of hospital care for acute stroek patients (Cochrane Review). The Cochrane Library. Issue 4. Oxford, UK: Update Software; 2001.
45. Rudd AG, Wolfe CD, Tilling K, Beech R. Randomised controlled trial to evaluate early discharge scheme for patients with stroke. BMJ. 1997; 315:1039-1044.[Erratum in: BMJ. 1998;316:435.][Abstract/Free Full Text]
46. Indredavik B, Slordahl SA, Bakke F, Rokseth R, Haheim LL. Stroke unit treatment. Long-term effects. Stroke. 1997; 28: 1861-1866.[Abstract/Free Full Text]
47. Indredavik B, Bakke F, Slordahl SA, Rokseth R, Haheim LL. Stroke unit treatment improves long-term quality of life: a randomized controlled trial. Stroke. 1998; 29:895-899.[Abstract/Free Full Text]
48. Indredavik B, Bakke F, Slordahl SA, Rokseth R, Haheim LL. Stroke unit treatment: 10-year follow-up. Stroke. 1999; 30: 1524-1527.[Abstract/Free Full Text]
49. Kalra L, Evans A, Perez I, Knapp M, Donaldson N, Swift CG. Alternative strategies for stroke care: a prospective randomised controlled trial. Lancet. 2000; 356: 894-899.
50. Langhorne P, Wagenaar R, Partridge C. Physiotherapy after stroke: more is better? Physiother Res Int. 1996; 1:75-88.
51. Kwakkel G, Wagenaar RC, Twisk JW, Lankhorst GJ, Koetsier JC. Intensity of leg and arm training after primary middle-cerebral-artery stroke: a randomised trial. Lancet. 1999; 354:191-196.
52. Finestone HM, Foley NC, Woodbury MG, Greene-Finestone L. Quantifying fluid intake in dysphagic stroke patients: a preliminary comparison of oral and nonoral strategies. Arch Phys Med Rehabil. 2001; 82:1744-1746.
53. Martin-Harris B, Logemann JA, McMahon S, Schleicher M, Sandidge J. Clinical utility of the modified barium swallow. Dysphagia. 2000; 15:136-141.
54. Rasley A, Logemann JA, Kahrilas PJ, Rademaker AW, Pauloski BR, Dodds WJ. Prevention of barium aspiration during videofluoroscopic swallowing studies: value of change in posture. AJR Am J Roentgenol. 1993; 160:1005-1009.
55. Robey RR. The efficacy of treatment for aphasic persons: a meta-analysis. Brain Lang. 1994; 47: 582-608.
56. Robey RR. A meta-analysis of clinical outcomes in the treatment of aphasia. J Speech Lang Hear Res. 1998; 41:172-187.
57. Whurr R, Lorch MP, Nye C. A meta-analysis of studies carried out between 1946 and 1988 concerned with the efficacy of speech and language therapy treatment for aphasic patients. Eur J Disord Commun. 1992; 27:1-17.
58. Whurr R, Lorch MP, Nye C. Efficacy of speech and language therapy for aphasia: a meta-analytic review. Neurol Rev Int. 1997; 1: 7-11.
59. Elman RJ, Bernstein-Ellis E. The efficacy of group communication treatment in adults with chronic aphasia. J Speech Lang Hear Res. 1999; 42:411-419.
60. Katz RC, Wertz RT. The efficacy of computer-provided reading treatment for chronic aphasic adults. J Speech Lang Hear Res. 1997; 40:493-507.
61. Wertz RT, Weiss DG,Aten JL,Brookshire RH,Garcia-Bunuel L, Holland AL, Kurtzke JF, LaPointe LL, Milianti FJ,Brannegan R, et al. Comparison of clinic, home, and deferred language treatment for aphasia: a Veterans Administration Cooperative Study. Arch Neurol. 1986; 43: 653-658.
62. Bohannon RW, Walsh S. Nature, reliability, and predictive value of muscle performance measures in patients with hemiparesis following stroke. Arch Phys Med Rehabil. 1992; 73: 721-725.
63. Andrews AW, Bohannon RW. Discharge function and length of stay for patients with stroke are predicted by lower extremity muscle force on admission to rehabilitation. Neurorehabil Neural Repair. 2001; 15: 93-97.
64. Visintin M, Barbeau H, Korner-Bitensky N, Mayo NE. A new approach to retrain gait in stroke patients through body weight support and treadmill stimulation. Stroke. 1998; 29:1122-1128.[Abstract/Free Full Text]
65. KosakMC, Reding MJ. Comparison of partial body weight-supported treadmill gait training versus aggressive bracing assisted walking post stroke. Neurorehabil Neural Repair. 2000; 14:13-19.
66. Dromerick AW, Edwards DF, Hahn M. Does the application of constraint-induced movement therapy during acute rehabilitation reduce arm impairment after ischemic stroke? Stroke. 2000; 31: 2984-2988.[Abstract/Free Full Text]
67. Glanz M, Klawansky S, Stason W, Berkey C, Chalmers TC. Functional electrostimulation in poststroke rehabilitation: a meta-analysis of the randomized controlled trials. Arch Phys Med Rehabil. 1996; 77: 549-553.
68. Price CI, Pandyan AD. Electrical stimulation for preventing and treating post-stroke shoulder pain: a systematic Cochrane review. Clin Rehabil. 2001; 15:5-19.Review.
69. BogatajU,Gros N, KljajicM, Acimovic R, MalezicM.The rehabilitation of gait in patients with hemiplegia: a comparison between conventional therapy and multichannel functional electrical stimulation therapy. Phys Ther. 1995; 75: 490-502.
70. Gelber DA, Good DC, Dromerick A, Sergay S, Richardson M. Open-label dose-titration safety and efficacy study of tizanidine hydrochloride in the treatment of spasticity associated with chronic stroke. Stroke. 2001; 32: 1841-1846.[Abstract/Free Full Text]
71. Ketel WB, Kolb ME. Long-term treatment with dantrolene sodium of stroke patients with spasticity limiting the return offunction.CurrMed ResOpin. 1984; 9:161-169.
72. Milanov IG. Mechanisms of baclofen action on spasticity. Acta Neurol Scand. 1992; 85: 305-310.
73. Katrak PH, Cole AM, Poulos CJ, McCauley JC. Objective assessment of spasticity, strength, and function with early exhibition of dantrolene sodium after cerebrovascular accident: a randomized double-blind study. Arch Phys Med Rehabil. 1992; 73:4-9.
74. Pedersen E, Arlien-Soborg P, Mai J. The mode of action of the gaba derivative baclofen in human spasticity. Acta Neurol Scand. 1974; 50: 665-680.
75. Goldstein LB. Common drugs influence motor recovery after stroke. The Sygen In Acute Stroke Study Investigators. Neurology. 1995; 45: 865-871.
76. Goldstein LB. Potential effects of common drugs on stroke recovery. Arch Neurol. 1998;55:454-456.[Abstract/Free Full Text]
77. Troisi E, Paolucci S, Silvestrini M, Matteis M, Vernieri F, Grasso MG, Caltagirone C. Prognostic factors in stroke rehabilitation: the possible role of pharmacological treatment. Acta Neurol Scand. 2002; 105:100-106.
78. Simpson DM, Alexander DN, O'Brien CF, Tagliati M, Aswad AS, Leon JM, Gibson J, Mordaunt JM, Monaghan EP. Botulinum toxin type A in the treatment of upper extremity spasticity: a randomized, double-blind, placebo-controlled trial. Neurology. 1996; 46:1306-1310.
79. Bakheit AM,Thilmann AF, Ward AB, Poewe W, Wissel J, Muller J, Benecke R, Collin C, Muller F, Ward CD, Neumann C. A randomized, double-blind, placebo-controlled, dose-ranging study to compare the efficacy and safety of three doses of botulinum toxin type A (Dysport) with placebo in upper limb spasticity after stroke. Stroke. 2000; 31: 2402-2406.[Abstract/Free Full Text]
80. Brashear A, Gordon MF, Elovic E, Kassicieh VD, Marciniak C, Do M, Lee CH, Jenkins S, Turkel C; Botox Post-Stroke Spasticity Study Group. Intramuscular injection of botulinum toxin for the treatment of wrist and finger spasticity after a stroke. N Engl J Med. 2002; 347: 395-400.[Abstract/Free Full Text]
81. Kirazli Y, On AY, Kismali B, Aksit R. Comparison of phenol block and botulinus toxin type A in the treatment of spastic foot after stroke: a randomized, double-blind trial. Am J Phys Med Rehabil. 1998; 77: 510-515.
82. Kong KH,Chua KS. Neurolysis of the musculocutaneous nerve with alcohol to treat poststroke elbow flexor spasticity. Arch Phys Med Rehabil. 1999; 80:1234-1236.
83. On AY, Kirazli Y, Kismali B, Aksit R. Mechanisms of action of phenol block and botulinus toxin Type A in relieving spasticity: electrophysiologic investigation and follow-up. Am J Phys Med Rehabil. 1999; 78: 344-349.
84. Meythaler JM,Guin-Renfroe S, Brunner RC, Hadley MN. Intrathecal baclofen for spastic hypertonia from stroke. Stroke. 2001; 32: 2099-2109.[Abstract/Free Full Text]
85. Van OuwenallerC, Laplace PM,Chantraine A. Painful shoulder in hemiplegia. Arch Phys Med Rehabil. 1986;67:23-26.
86. Cicerone KD, Dahlberg C, Kalmar K, Langenbahn DM, Malec JF, Bergquist TF, Felicetti T, Giacino JT, Harley JP, Harrington DE, Herzog J, Kneipp S, Laatsch L, Morse PA. Evidence-based cognitive rehabilitation: recommendations for clinical practice. Arch Phys Med Rehabil. 2000; 81:1596-1615.Review.
87. GrayJM, Robertson I, Pentland B,etal. Microcomputer-based attentional retraining after brain damage: a randomized group controlled trial. Neuropsychol Rehabil. 1992; 2: 97-115.
88. Niemann H, Ruff RM, Baser CA. Computer-assisted attention retraining in head-injured individuals: a controlled efficacy study of an outpatient program. J Consult Clin Psychol. 1990; 58:811-817.
89. Sohlberg MM, Mateer CA. Effectiveness of an attention-training program. J Clin Exp Neuropsychol. 1987; 9:117-130.
90. Sohlberg MM, Mateer CA. Training use of compensatory memory books: a three stage behavioral approach. J Clin Exp Neuropsychol. 1989; 11:871-891.
91. Strache W. Effectiveness of two modes of training to overcome deficits of concentration. Int J Rehabil Res. 1987; 10: 141-145.
92. Ryan TV, Ruff RM. The efficacy of structured memory retraining in a group comparison of head trauma patients. Arch Clin Neuropsychol. 1988; 3:165-179.
93. Antonucci G, Guariglia C, Judica A, Magnotti L, Paolucci S, Pizzamiglio L, Zoccolotti P. Effectiveness of neglect rehabilitation in a randomized group study. J Clin Exp Neuropsychol. 1995; 17: 383-389.
94. Beis JM, Andre JM, Baumgarten A, Challier B. Eye patching in unilateral spatial neglect: efficacy of two methods. Arch Phys Med Rehabil. 1999; 80: 71-76.
95. Fanthome Y, Lincoln NB, Drummond A, Walker MF. The treatment of visual neglect using feedback of eye movements: a pilot study. Disabil Rehabil. 1995; 17:413-417.
96. Paolucci S, Antonucci G, Guariglia C, Magnotti L, Pizzamiglio L, Zoccolotti P. Facilitatory effect of neglect rehabilitation on the recovery of left hemiplegic stroke patients: a cross-over study. J Neurol. 1996; 243: 308-314.
97. Rossetti Y, Rode G, Pisella L, Farne A, Li L, Boisson D, Perenin MT. Prism adaptation to a rightward optical deviation rehabilitates left hemispatial neglect. Nature. 1998; 395:166-169.
98. Wiart L, Come AB, Debelleix X, Petit H, Joseph PA, Mazaux JM, Barat M. Unilateral neglect syndrome rehabilitation by trunk rotation and scanning training. Arch Phys Med Rehabil. 1997; 78:424-429.
99. Robinson RG. The Clinical Neuropsychiatry of Stroke. New York: Cambridge University Press; 1998.
100. Tsouna-Hadjis E,Vemmos KN,Zakopoulos N,StamatelopoulosS. First-stroke recovery process: the role of family social support. Arch Phys Med Rehabil. 2000;81:881-887.
101. Andersen G. Treatment of uncontrolled crying after stroke. Drugs Aging. 1995; 6:105-111.Review.
102. Cole MG, Elie LM, McCusker J, Bellavance F, Mansour A. Feasibility and effectiveness of treatments for post-stroke depression in elderly inpatients: systematic review. J Geriatr Psychiatry Neurol. 2001; 14: 37-41.
103. Gill D, Hatcher S. Antidepressants for depression in medical illness. Cochrane Database Syst Rev. 2000 (4): CD001312.
104. Kimura M, Robinson RG, Kosier JT. Treatment of cognitive impairment after poststroke depression: a double-blind treatment trial. Stroke. 2000; 31:1482-1486.[Abstract/Free Full Text]
105. Reding JJ, Orto LA, Winters SW, Fortuna IM, DiPonte P, McDowell FH. Antidepressant therapy after stroke: a double-blind trial. Arch Neurol. 1986; 43: 763-765.
106. Robinson RG, Schultz SK, Castillo C, Kopel T, Kosier JT, Newman RM, Curdue K, Petracca G, Starkstein SE. Nortriptyline versus fluoxetine in the treatment of depression and in short-term recovery after stroke: a placebo-controlled, double-blind study. Am J Psychiatry. 2000; 157: 351-359.[Abstract/Free Full Text]
107. Wiart L, Petit H, Joseph PA, Mazaux JM, Barat M. Fluoxetine in early poststroke depression: a double-blind placebo-controlled study. Stroke. 2000; 31:1829-1832.[Abstract/Free Full Text]
108. Brown KW, Sloan RL, Pentland B. Fluoxetine as a treatment for post-stroke emotionalism. Acta Psychiatr Scand. 1998; 98: 455-458.
109. Burns A, Russell E, Stratton-Powell H,Tyrell P, O'Neill P, Baldwin R. Sertraline in stroke-associated lability of mood. Int J Geriatr Psychiatry. 1999; 14:681-685.
110. Gordon MT. Developing clinical guidelines for the management of patients with stroke. Scottish Intercollegiate Guidelines Network (SIGN). Int J Lang Commun Disord. 1998; 33 suppl: 152-157.
111. Robinson RG, Parikh RM, Lipsey JR, Starkstein SE, Price TR. Pathological laughing and crying following stroke: validation of a measurement scale and a double-blind treatment study. Am J Psychiatry. 1993; 150: 286-293.
112. Reding MJ, Borucki S. Effect of dextroamphetamine on motor recovery after stroke. Neurology. 1995; 45 (suppl 4): A222.Abstract.
113. Sonde L, Nordstrom M, Nilsson CG, Lokk J, Viitanen M. A double-blind placebo-controlled study of the effects of amphetamine and physiotherapy after stroke. Cerebrovasc Dis. 2001; 12: 253-257.
114. Gladstone DJ, DanellsCJ,Armesto A, Mcllroy WE, Staines R,GrahamSJ, Herrmann N,SzalaiJP,BlackSE; for the Subacute Therapy with Amphetamine and Rehabilitation for Stroke (STARS) Study Investigators. Physiotherapy coupled with dextroamphetamine for motor rehabilitation after hemiparetic stroke: a randomized controlled trial. In: Program Schedule and Abstracts of the 29th International Stroke Conference. Stroke. 2004; 35: 239.Abstract No. 23.
115. Grade C, Redford B, Chrostowski J, Toussaint L, Blackwell B. Methylphenidate in early poststroke recovery: a double-blind, placebo-controlled study. Arch Phys Med Rehabil. 1998; 79:1047-1050.
116. Scheidtmann K, Fries W, Muller F, Koenig E. Effect of levodopa in combination with physiotherapy on functional motor recovery after stroke: a prospective, randomised, double-blind study. Lancet. 2001; 358: 787-790.
117. Nishino K, Sasaki T, Takahashi K, Chiba M, Ito T. The norepinephrine precursor L-threo-3,4-dihydroxyphenylserine facilitates motor recovery in chronic stroke patients. J Clin Neurosci. 2001; 8: 547-550.
118. Dam M, Tonin P, De Boni A, Pizzolato G, Casson S, Ermani M, Freo U, Piron L, Battistin L. Effects of fluoxetine and maprotiline on functional recovery in poststroke hemiplegic patients undergoing rehabilitation therapy. Stroke. 1996; 27:1211-1214.[Abstract/Free Full Text]
119. Lazar RM, Fitzsimmons BF, Marshall RS, Mohr JP, Berman MF. Midazolam challenge reinduces neurological deficits after transient ischemic attack. Stroke. 2003; 34: 794-796.[Abstract/Free Full Text]
A szakmai irányelv érvényessége: 2010. szeptember 30.
VII. Függelék
1.sz.függelék
Magyar nyelvű szakirodalomjegyzék (abc rendben)
stroke rehabilitáció, másodlagos megelőzés, komplikációk, poststroke állapotok, gondozás témakörökben
1. Ádám Á, Bardócz M (2002): Alvászavarok - alvási apnoe - egy új rizikófaktor. Hippocrates 4 (3):164-7
2. Aradiné Csengődi Cs, Gardi Zs (1995): A gyógytorna-fizioterápia a stroke betegek rehabilitációjában. Rehabilitáció V (4):538-9
3. Arnold Cs, Tamás F: A szélütés/stroke megelőzése ellátása és gondozása. Melánia, Bp., 2004. ISBN: 963 9106 79 8
4. Balogh Z (2003): A stroke-betegek ápolásának és rehabilitációjának egységes ápolási irányelvei. LAM 13 (1):50-56
5. Bánhidi M (1986): A figyelemkoncentráció és rövididejű emlékezet javítása neuropszichológiai módszerrel. Balneológia, Rehabilitáció, Gyógyfürdőügy 2:121-126
6. Bereczki D (2004): Szekunder stroke-prevenció. Háziorvos Továbbképző Szemle IX (5), 420-425
7. Bereczki D (2004): A cerebrovascularis kórképek farmakoterápiája: 2004. MOTESZ Magazin (3-4), 31-34
8. Boros E, Ricsóy G (2003): A háziorvos szerepe a stroke rehabilitációban. Hippocrates V (4): 247-9
9. Boros E, Ricsóy G (2004): /Agyérbetegségek/ Rehabilitációs módszerek, monitorozás. Háziorvos Továbbképző Szemle IX (9), 692-6
10. Boros E, Ricsóy G: Gyógyszeres terápia a neurorehabilitációban. In: Hatóanyagok, készítmények, terápia - Fókuszban a neurológia és pszichiátria. Szerk: Bereczky D. és Bánki Cs. Melinda Kiadó és Reklámügynökség, 2006, 251-259.
11. Bors K, Boros E, Bodnár A, Lakatos P, Szűcs J, Horváth Cs (1999): Hemiparesises betegek csontvizsgálata densitometriával és ultrahanggal. Calcium és csont 14 (2), 2. különszám
12. Cseh Katalin, Hegyi Ágnes: Gyakorlatok az afázia kognitív nyelvi terápiájához. Nemz.Tankönyvk., Budapest, 1995. ISBN: 963 18 6812 5
13. Csornai M (1999): A gondozási munka post-stroke állapotban. Háziorvos Továbbképző Szemle IV (2):104-107
14. Csornai M (2002): A stroke-betegek gondozásának problémái. Ideggy.Szle 55 (3-4):138-141
15. Csornai M (2002): Neurológiai betegségekben jelentkező psychés zavarok. EGIS kiadvány, Budapest
16. Dénes Z (1996): Az immobilizációs szindróma. Orv.Hetil. 137 (32) 1739-43
17. Dénes Z (1997): A lábdeformitások műtéti kezelése a neurológiai károsodást szenvedett betegek mozgásszervi rehabilitációja során. M. traumatol. orthop. kézseb. plaszt. seb. 40 (5): 395-399
18. Dénes Z, KállayM (2003): A heterotopossificatio műtéti kezelésével szerzett tapasztalatainka neurorehabilitáció során. M. traumatol. orthop. kézseb. plaszt. seb. 46 (1):41-46
19. Dénes Z, Szél I (1995): Combnyaktáji törést szenvedett hemiplég betegeink rehabilitációs eredményei. Magyar Traumatológia 38 (3), 2436
20. Dénes Zoltán és mtsai (2002): Súlyos agykárosodást szenvedett betegek mesterséges táplálásával szerzett tapasztalatok a neurorehabilitáció során. Rehabilitáció 12 (4): 10-13
21. Dénes Zoltán és mtsai (2003): Tracheostomás betegek ellátásával szerzett tapasztalatok a neurorehabilitáció során. Rehabilitáció 13 (3-4): 18-20
22. Dénes Z, Lantos Ágnes, Laki M (2004): Az állandó hólyagkatéter eltávolításának problémája a neurorehabilitációs osztályon: új, nem invazív (ultrahangos), mobil hólyagtérfogat-mérő eszköz használata. Rehabilitáció 14 (2): 14-17
23. Egészségügyi Minisztérium (2002): Szakmai irányelv stroke betegek ápolásához. Eü.Közlöny 52 (11), 1344-59
24. Endres M (1980): A rehabilitáció szempontjai a cerebrovascularis betegek kezelésében. Ideggyógyászati Szemle, 33, 439-443
25. Endres M (1983): Elmélet és gyakorlat összefüggései a hemiplegiások rehabilitációjában. Orv Hetil. 124 (37): 2239-2244
26. Endres Mária (összeáll.): Az Országos Orvosi Rehabilitációs Intézet módszertani levele a hemiplégiás betegek rehabilitációjáról. Országos Orvosi Rehabilitációs Int., Budapest, 1985
27. Endres Mária és mtsai: Hemiplegiások rehabilitációja a lakóközösségben. OORI, Budapest, 1997. ISBN: 963 04 9172 9
28. Engl EM, Kotten A, Ohlendorf I, Poser E: Gyakorlatok az afázia terápiájához. Medicina, Budapest, 1990.
29. Erdős J, Erdős M (2003): Az antidepresszív gyógyszerek alkalmazása a rehabilitációban. Rehabilitáció 13 (1), 14-17
30. Fáy V (2003): A stroke betegek rehabilitációjának aktuális kérdései. Háziorvos Továbbképző Szemle 8 (1):29-30
31. Fazekas G (2004): Robotok alkalmazása féloldali bénultak felső végtagi gyógytornásztatásában. Orvosi Hetilap, 145 (25), 1327-31
32. Fehér M (1999): Neurológiai rehabilitáció. Orvosképzés 73 (6):372-3
33. Félegyházy Zs, Hatházi RáczV, Széplaki Z (2001): A poststroke depresszió neuroanatómiai összefüggései: restrospektív tanulmány. Neuropsychopharmacologia Hungarica. 3 (3): 131-6
34. Halmos B: Hemiplegiás érbetegek rehabilitációja és gondozása. In: Meskó É (szerk): Vascularis medicina. Therapia kiadó, sine loco, 2004,427-434
35. Halmos B (1998): Stroke-on átesett betegek lakókörnyezeti rehabilitációja. Háziorvos Továbbképző Szemle 3,371-3
36. Halmos B (2000): A rehabilitáció lehetőségei és korlátai stroke-ban. Kórház 7 (8):21-23
37. Halmos B (2000): A stroke következtében hemipareticus betegek rehabilitációja. Agyérbetegségek 6 (2):2-8
38. Halmos B (2002): A rehabilitációs program során fennálló betegségek és rizikófaktorok kezelése. Rehabilitáció XII (4):2-4
39. Halmos B, Kiss J (2002): A stroke-betegek rehabilitációját hátráltató tényezők. Rehabilitáció XII (4):14-16
40. Halmy L (2005): Az elhízás kezelésének irányelvei. Háziorvos Továbbképző Szemle 10 107-110
41. Harcos P (2002): A szélütést követő mentális zavarok és gyógyszeres kezelésük. Medicus Anonymus 10 (9): 29-33
42. Harvey RL (1999): Stroke-betegek személyre szabott rehabilitációja. Orvostovábbképző Szemle 6 (5), 24-35
43. Hegyi Ágnes: Afáziaterápiák. Javaslat az afázia kognitív nyelvi terápiájára. Nemzeti Tankönyvkiadó, Budapest, 1995. ISBN: 963 18 6811 7
44. Holczinger Zs és mtsai (2001): Stroke beteg otthon rehabilitációjának lehetőségei: a gyógytornász, logopédus és az Otthonápolási Szolgálat szemszögéből. Nővér 14 (1): 7-13
45. Horváth R (2004): Az obstruktív alvási apnoe (OSAS) klinikuma. IME 2 (10):36-40
46. Horváth S (2001): A krónikus agyi keringészavarok patológiai és klinikai következményei. Orv Hetil 142 (7):323-9
47. Kállay M (2002): Agyérbetegség maradványtünetei krónikus mozgásszervi betegséggel párosulva: megoldások. Praxis 11 (9): 39-43
48. Karádi I (2005): A kardiovaszkuláris terápiás konszenzus lipicsökkentő ajánlásai. Orvosok Lapja 2005 (3), 41-44
49. Kékes E (2004): Endothelvédelem hypertoniás betegeknél. LAM 14 (7), 467-474
50. Kellermann M, Gesztelyi R, Kovács A, Bereczki D (2001): Post-stroke depresszió: irodalmi áttekintés. Psychiatr.Hung. 16 (4):412-422
51. Kókai K, Ferenczy V, Veress M, Mittli G (1992): Sikeresen rehabilitált féloldali bénult betegek utánkövetéses vizsgálata otthoni környezetükben. Rehabilitáció 2 (3), 19-21
52. Kókai K (2003): A stroke utáni rehabilitáció szükséges és valóságos gyószerigénye. Rehabilitáció 13 (1), 9-13
53. Komoly S (2004): Az antidepresszánsok szerepe a fájdalom kezelésében. IME 2 (10):16-17
54. Kondákor I (2004): Neuronalis plaszticitás és gyógyszeres terápia poststroke aphasiában. Agyérbetegségek 10 (1), 11-15
55. Konszenzus a cerebrovascularis betegségek ellátásában. Agyérbetegségek, 1996.évi 2.szám, 13.o.
56. Kovács T (2005): A hypertonia kezelése stroke után. Praxis 14 (9):23-30
57. Kőrösfalvi M, Szél I, Deme É, Boros E (1992): Heterotop ossificatio előfordulása nem
58. traumás agykárosodás következtében féloldali bénulttá vált betegeinken. Rehabilitáció II. (3): 22-25
59. Köves P, Szakács Z (2005): Az obstruktív alvási apnoe és a kardiovaszkuláris rizikó, különös tekintettel a hipertóniára. Háziorvos Továbbképző Szemle X (2):137-142
60. Krasznárné Erdős Felícia és Feketéné Gacsó Mária (szerk): Tanulmányok az afázia témaköréből. Eötvös József Könyvkiadó, Budapest, 2005. ISBN 963 7338 09 8
61. Kullmann L (1992): Gondolatok az életminőség értelmezéséről. Orvosképzés 67, 387397
62. Kullmann L(1995): Rehabilitáció a lakóközösségben. Medicus Universalis 28 (2), 5760
63. Kullmann L (2002): A rehabilitáció korszerű szemlélete. Ideggy Szle 55 (1-2):30-37
64. Lakatos L (2001): A pitvarfibrillatio a stroke egyik oka, a rehabilitáció egyik gátja. Rehabilitáció 11 (3): 82-85
65. Lincoln, NB: Stroke: kórházban vagy az otthonukban kezeljüka betegeket? Csak a kórházak biztosíthatják a megfelelő ellátást. BMJ magyar kiadás, 478,1995.december.
66. Young, J: Stroke: kórházban vagy az otthonukban kezeljük a betegeket? Az otthoni ellátás nyújtja a legteljesebb javulást. BMJ magyar kiadás, 467, 1995.december.
67. Lyder, H (2003): A dekubituszok megelőzése és kezelése. JAMA-HU 5 (5), 329-332
68. A Magyar Stroke Társaság és a Neurológiai Szakmai Kollégium szakmai irányelvei a cerebrovascularis betegségek megelőzéséről, diagnosztikájáról és ellátásáról. Tényekre támaszkodó ajánlások 2005. Promenade Publ.H., Bp., 2005. vagy in: Útmutató - klinikai irányelvek, Mediton, Bp., 2005.126-165
69. Máhli Zs (2006): Alternatív módszer a felső végtag mozgásfejesztésére hemiparetikus betegeknél. Mozgásterápia. Megjelenés alatt.
70. Máté K, Birtalan Gy, Greguss S, Papy K, Sági B: Hemiplegiás betegek rehabilitációja. Főv.Tanács Tétényi úti Kórház évkönyve, 1961.
71. Mészáros K, Hacki T, Varga Zs (2005): Az oropharyngealis dysphagia komplex kezelése. LAM 15 (4), 289-293
72. Dr.Mogánné Tölgyesy Szilvia: A stroke betegek mindennapi élettevékenységét segítő megoldások az ergoterápia javaslata alapján. Országos Orvosi Rehabilitációs Intézet, Budapest /1998/
73. Molnár L (2001): Gyógypedagógiai rehabilitációs konzultációs munka a felnőtt afáziás betegek beszédrehabilitációjában. Gyógyped Szle 29 (2):124-133
74. Nagy Gy, Könyves L, Nyitrai G (2004): A diabetes kezelése stroke utáni állapot esetén. Praxis 13 (12):17-20
75. Nagy Z (2005): A vascularis neurológia, mint a klasszikus neurológia újiránya. LAM 15 (3), 187-190
76. Nikl J (2003): Post stroke rohamok, epilepsziák: jó az öreg a háznál... Praxis 12 (4):15-23
77. Osmanné Sági Judit (1991): Az afázia klasszifikációja és diagnosztikája I-II. Ideggy Szle 44 (8): 339-362
78. Pataky I, Kiss K (1999): A kognitív rehabilitáció alapjai. Háziorvos Továbbképző Szemle 4 (2): 100-103
79. Pataky I (2002): Neuropszichológiai rehabilitáció - neuropszichológiai tréning. Családorvosi Fórum 2002 (4):20-22
80. Péter Á: Neurológia. Neuropszichológia. 5.kiadás. Nemzeti Tankönyvkiadó, Bp., 1996.
81. Post-stroke állapotok: konszenzuskonferencia, Budapest, 1996. május 4. Agyérbetegségek 1996. (3):2-7
82. Ricsóy G, Boros E (2003): A rehabilitációs folyamat egyes elemei a stroke utáni rehabilitációban. Családorvosi fórum 2003 (7):19-23
83. Sikné Lányi Cecília és mtsai (2004): Interaktív rehabilitációs szoftver afáziás betegek részére. IME 3 (2):48-52
84. Simon Zs (2004): a) A vizeletincontinentia gyógyszeres kezelése. LAM 14 (7), 475-480 b) A vizeletincontinentia konzervatív kezelése. Rehabilitáció 14 (1) 12-17
85. Siró B, Bódor Cs: A családorvos szerepe az otthoni rehabilitációban. In: Huszár I, Kullmann L, Tringer L (szerk): A rehabilitáció gyakorlata. Medicina, Bp., 2000.201-215
86. Somlai Judit (szerk): Neuroophtalmologia. Literatura Medica, Budapest 1996. ISBN: 963 7715 07 X
87. Szapáry L (2004): A hypertonia jelentősége cerebrovascularis kórképekben. LAM 14 (4), 251-7
88. Szél I (1992): A strokerehabilitáció problémaorientált megközelítése. Rehabilitáció II. (3) 210
89. Szél I (1995): Az alsó végtagi vénás thrombosis megelőzésének szükségessége és lehetőségei "completed stroke"ot szenvedett betegek körében. Agyérbetegségek (1), 26
90. Szél I (1996): Strokebetegek. Med.Univ. XXIX (78), 2658
91. Szél I: Stroke betegek preventív szemléletű kórházi ellátása. In: Halmos T, Kautzky L, Mousios Georgiosné (szerk.): Uj utak az egészségmegőrzésben. Egészségmegőrző Kórházak Nemzeti Hálózata (Nemzeti Egészségvédelmi Intézet), Budapest, 1998., ISBN: 963 03 6237 6, (151168.oldal).
92. Szél I (1999): Mit jelent a stroke rehabilitáció? Háziorvos Továbbképző Szemle IV (2), 95-99
93. Szél I, Nagy Z: Funkcionálisan orientált akut stroke beteg ellátás. In: Nagy Z (szerk): Stroke kézikönyv, 2., bőv.kiadás. Springer, Bp., 1999. 287-296
94. Szél I: Az agyérbetegek rehabilitációja. In: Nagy Z (szerk): Stroke kézikönyv, 2., bőv.kiadás. Springer, Bp., 1999.303-305
95. Szél I: Rehabilitáció stroke után. In: Katona F, Siegler J (szerk): Orvosi rehabilitáció. Medicina, Budapest, 1999. (139146.oldal).
96. Szél I: Rehabilitáció krónikus neurológiai kórképekben és stroke után. In: Huszár I, Kullmann L, Tringer L (szerk): A rehabilitáció gyakorlata. Medicina, Bp., 2000.302-313
97. Szél I: Állapotfelmérés és tervkészítés a rehabilitáció folyamatában. In: Huszár I, Kullmann L, Tringer L (szerk): A rehabilitáció gyakorlata. Medicina, Bp., 2000.78-90
98. Szél I (2000): Segédeszközök alkalmazása hemiplegiások, ill. stroke-betegek ellátása során. Rehabilitáció X (2), 47-49
99. Szél I, Halmos B (1994): Hemiplegiásokat ill. strokebetegeket ellátó rehabilitációs osztályok működési kritériumai. Rehabilitáció, IV. (2) 280284
100. Szél I, TróznaiT (1993): Időskorú strokebetegek rehabilitációját végző osztályok ill. részlegek működési kritériumai. Rehabilitáció, III. (4), 178180
101. Szolnoki Z (2002): Fejfájás és más panaszok stroke után. Praxis 11 (3):57-59
102. Szűcs A és mtsai (2002): Alvási apnoe szindróma akut ischaemiás agyi inzultusban és agyvérzésben. A gyérbetegségek 8 (1):2-5
103. Szűcs T(1992): Szindrómaelemzés a neuropszichológiai gyakorlatban. Rehabilitáció 2 (3):11-18
104. Tariska P (2001): A XXI. század egyik nagy kihívása: a vascularis dementia. Agyérbetegségek 7 (1):2-9
105. Tenke P, Bálint P (2003): Az állandó katéterezéssel kapcsolatos teendők. Háziorvos Továbbképző Szemle VIII (8), 642-5
106. Tóthné Csordás Ágnes, Demeter Anikó (2000): A hemiplégiához társuló csípőtáji törést szenvedett betegek rehabilitációjának problémái. Rehabilitáció X (4):95-97
107. Török M és mtsai (2003): Másodlagos prevenciós gyakorlat ischaemiás stroke után: dokumentációs folyamataudit.
LAM 13 (2):139-145
108. Varga D (2002): A stroke neuropszichiátriai következményei. Ideggyógy. szle. 55 (3-4): 128-136
2. sz. függelék
NIH (Hational Institute of Health) Stroke pontozó Skála
| Pontszám | ||
| Tudati szint | Éber, élénk, reagál | 0 |
| Aluszékony, minimális stimulációval ébreszthető, együtt működő, válaszol, reagál | 1 | |
| Kellő számba ismétlődő stimulációra felfigyel, de letargiás vagy kábult; kellően erős fájdalomingerre nem sztereotíp mozgást végez | 2 | |
| Csak reflexes motoros vagy autonom effektusokkal, vagy egyáltalán nem válaszol, petyhüdt, nincsenek reflexek | 3 | |
| Kérdésekre adott válasz (dátumra és életkorra vonatkozó; csak az első válasz minősítendő) | Mind két válasz helyes | 0 |
| Egy válasz helyes | 1 | |
| Mind kettő helytelen | 3 | |
| Utasítások végre hajtása (a beteget felszólítjuk, hogy nyissa ki vagy csukja be a kezét és a szemét; csak az első válaszminősítendő; pont adható, ha egyértelmű kísérletet tesz, de az nem komplett( | Mind két utasítást végrehajtja | 0 |
| Egyik utasítást végrehajtja | 1 | |
| Egyik utasítást sem hajtja végre | 2 |
| Szemmozgások | Normál | 0 |
| Részleges tekintet bénulás; pont adható, ha a tekintet abnormális egy vagy mindkét szemen, de kifejezett deviatio vagy teljes tekintésbénulás nincs jelen | 1 | |
| A kifejezett deviatio vagyí a tekintésbénulás nem győzhető le oculochephalicus manőverrel | 2 | |
| Látótér | Nincs látótér kiesés | 0 |
| Parciális hemianopsia | 1 | |
| Teljes hemianopsia | 2 | |
| Facialis paresis | Normál | 0 |
| minor | 1 | |
| parcialis | 2 | |
| komplett | 3 | |
| Izomerő (felső végtag) | Végtagot 90 fokos pozícióban 10 mp .-ig megtartja | 0 |
| (csak gyengébb oldal) | Végtagot 90 fokos pozícióban megtartja, de 10 mp. -en belül sűllyed | 1 |
| Végtagot nem tudja megtartani 90 fokos pozícióban 10 mp. -ig, de van némi erőkifejtés gravítáció ellenébe | 2 | |
| Végtag leesik, nincs erőkifejtés gravitáció ellenébe | 3 | |
| Nincs mozgás | 4 | |
| Izomerő (alsóvégtag) | 30 fokos pozícióban 5 mp. -ig megtartja | 0 |
| (csak a gyengébb oldal) | 5 mp.-es periódus végére a végtag félmagasságra süllyed | 1 |
| Az 5 mp. -es periódus végére a lábat leejti az ágyba, de van némi erőkifejtés gravitációval szembe | 2 | |
| A végtagot azonnal leejti az ágyba, nincs erőkifejtés gravitációval szembe. | 3 | |
| Nincs mozgás | 4 | |
| Végtag ataxia | Nincs | 0 |
| Ataxia egy végtagon | 1 | |
| Ataxia két végtagon | 2 | |
| Érzőkör | Nincs érzészavar | 0 |
| (tűvel tesztelve) | Enyhétől a közepesig; a beteg a tűszúrást kevéssé élesnek, vagy tompának érzi, de tudatába van, hogy megszúrták | 1 |
| Kifejezettől a teljes érzésvesztésig; a beteg nincs tudatába a szúrásnak | 3 | |
| Neglect | Nincs neglect | 0 |
| Vizuális, taktilis vagy auditoros féloldali figyelmetlenség | 1 | |
| Kifejezett féloldali figyelmetlenség | 2 | |
| Dysarthria | Normál | 0 |
| Enyhétől a közepesig a beteg hibásan ejt ki legalább néhány szót, de azért kis nehézséggel megérthető | 1 | |
| A beteg beszéde érthetetlen | 2 | |
| Aphasia | Nincs | 0 |
| Enyhétől a közepesig; megnevezési hibák, szótalálási nehézség paraphasia, és/vagy a megértés kifejezett károsodása | 1 | |
| Súlyos Broca -vagy Wernicke (vagy variáns) aphasia | 2 | |
| Mutizmus vagy globális aphasia | 3 |
Maximális pontszám: 33 pont
Útmutató a NIH stroke skála szerinti pontozáshoz
i. Ugyanazt a beteget ugyanaz a személy pontozza a vizsgálat során mindvégig (ha ez nem lehetséges, az "átadásra" kell törekedni)
ii. Pontosan követni kell a pontozási szabályokat, még akkor is, ha a pontozás magától értetődőnek tűnik.
iii. Aszerint pontozzon, amit lát, ne pedig aszerint, hogy Ön szerint a beteg mire képes.
iv. Az elsőkért adott választ kell pontozni, nem szabad további utasításokkal segíteni, az eredményt azonnal fel kell jegyezni.
v. Csak megfelelő szakképesítéssel rendelkező klinikaív vizsgálóorvos végezheti el az értékelést és jegyezheti fel az eredményeket.
vi. Ha bizonytalan a pontozásban, akkor
a) Olvassa át a NI H pontozási szabályokat (lásd lentebb) b) Döntsön és pontozzon, semmi se maradjon üresen
c) Nejelölje be a "9"-es értéket csakazért, mert bizonytalan (a"9"-es értéké szigorúan a pontozási szabályokban leírtak szerint használja)
A stroke-skálán az itt leírt sorrendben haladjon végig. Az adott pont alatt leírt egyes vizsgálatok elvégzése után mindig írja fel a pontszámot. Ne menjen vissza, és ne változtasson a pontszámokon. Mindig kövesse az egyes vizsgálathoz adott technikai utasításokat. Az eredményeknek azt kell tükrözniük, amit a beteg csinál és nem azt, amire az orvos szerint a beteg képes lenne. Az orvos a vizsgálat közben jegyezze fel a választott pontszámokat, és dolgozzon gyorsan. Hacsak erre nincs külön utasítás, a betegnek nem szabad további útmutatást adni (vagyis nem szabad a beteget többször felszólítani, hogy próbálja újra)
Utasítások
| Pontszám és meghatározás | |
| la. Az öntudat szintje (LOC): A vizsgálónak még akkor is pontoznia kell, ha a teljes körű | 0 = Éber, élénken reagál |
| értékelés bizonyos akadályozó tényezők miatt nem lehetséges, mint például | 1 = Nem éber, de kisebb stimulációval rábírható, hogy teljesítse a feladatot, |
| endotracheális tubus, nyelvi gát, orotrachealis trauma/bandázs. | válaszoljon, illetve reagáljon |
| A "3"-as érték csak akkor választandó, ha a beteg (a reflexszerű helyzetvátoztatáson kívül) | 2 = Nem éber, figyelnie csak ismételt stimulációval kelthető fel vagy stupor áll fenn és |
| nem mozdul a noxius stimulusra. | erős vagy fájdalmas stimuláció kell ahhoz, hogy megmozduljon |
| A1611005 vizsgálati irányelvek: | 3 = (nem sztereotipizált). |
| - A vizsgáló határozza meg a pontszámot (az Ön benyomása számít) | Csak motoros reflex-választ ad vagy autonóm mozgások a reakció teljes hiányával, |
| - Ne adjon pótlólagos utasításokat | petyhüdtséggel, areflexiával |
| 1 b. LOC kérdések: A betegtől kérdezze meg, hogy milyen hónapot írunk, és hány éves. A | 0 = Mindkét kérdésre helyes választ ad |
| válasznak pontosnak kell lennie, nem v ehető figyelembe a "majdnem helyes" válasz. Afázia | 1 = Az egyik kérdésre ad helyes választ |
| és stupor esetén, ha a beteg nem érti meg a kérdést, 2 pontot kell adni. Ha a beteg | 2 = Egyik kérdésre sem ad helyes választ |
| endotracheális intubáció, orotrachealis trauma, bármilyen eredetű súlyos dysarthria, nyelvi | |
| gát vagy más, az afáziával össze nem függő ok miatt nem tud beszélni, 1 pontot kap. | |
| Fontos, hogy mindig az elsőkért adott választ kell pontozni, és hogy a vizsgáló sem verbális, | |
| sem nonverbális úton ne "segítsen" a betegnek. | |
| A 1611005 vizsgálati irányelvek: | |
| - Csak a helyes válasz számít | |
| - Az elsőként adott választ kell pontozni | |
| - Nem szabad segíteni | |
| - Afázia és stupor esetén: 2 pont | |
| - A beteg nem afáziás, de nem tud beszélni: 1 pont | |
| - Kómás betegek: 2 pont | |
| 1c. LOC utasítások: A beteget kérje meg, hogy a szemét nyissa ki és csukja be, majd a nem | 0 = Mindkét feladatot helyesen végrehajtja |
| paresises kezét szorítsa ökölbe és lazítsa el. Ha a kéz nem használható, adjon másit | 1 = Az egyik feladatot teljesíti helyesen |
| egylépéses utasítást. Ha a beteg egyértelmű kísérletet tesz, de a feladatot gyengeség miatt | 2 = Egy egyik feladatot sem teljesíti helyesen |
| nem tudja végrehajtani, 1 pontot kell adni. Ha a beteg nem reagál az utasításra, a feladatot | |
| meg kell mutatni (utánzás), és az eredményt értékelni kell (pl. nem teljesíti a feladatot, | |
| egyet teljesít, mindkettőt teljesíti). Trauma, ampúáció vagy más fizikai gátoltság esetén a | |
| betegnek megfelelő egy lépéses utasításokat kell adni. Csak az első próbálkozás | |
| pontozandó. | |
| A1611005 vizsgálati irányelvek: | |
| - Az egyértelmű próbálkozást is értékelni kell, az első próbálkozást kell pontozni | |
| - De: ha a beteg az utasításra nem reagál, mutassa meg a feladatot | |
| - Azoknak a betegeknek, akik az eredeti parancsot trauma vagy más gátoltság miatt nem | |
| tudják teljesíteni, adjon más, egylépéses parancsot |
| 2. Szemmozgások kordináltsága: Csak a horizontális szemmozgást vizsgáljuk. Az | 0 = Normál |
| akaratlagos vagy reflexszerű (oculocephalicus) szemmozgásokat pontozzuk, de kalorikus | 1 = Részleges tekintetbénulás. Akkor adandó 1 pont, ha a tekintet egyik vagy mindkét |
| ingerlést nem végzünk. Ha a beteg szeme conjugált eltérést mutat, ez azonban | szemben abnormális, de nem áll fenn kényszerű kitérés vagy teljes tekintetbénulás |
| akaratlagosan vagy reflexszerűen leküzdhető, 1 pontot kell adni Izolált perifériás | 2 = A kényszerű kitérés v agy a teljes tekintetbénulás oculocephalicus ingerrel sem |
| idegbénulás (III., IV. vagy VI. agyideg) esetén 1 pontot kell adni. A szemmozgások minden | küzdhető le |
| afáziás betegnél vizsgálhatók. Ocularis trauma, kelés, korábban 's fennálló vakság vagy | |
| más, látásélességgel és a látómezőkkel kapcsolatos egyéb rendellenesség esetén a beteget | |
| reflexszerű mozgásokkal és a vizsgáló által választott módszerrel kell vizsgálni. A részleges | |
| tekintetbénulás esetenként igazolható azzal, ha a beteggel szemkontaktust teremt, majd a | |
| beteg egyik oldaláról átmegy a másikra. | |
| A1611005 Vizsgálati irányelvek: | |
| - Csak a horizontális szemmozgást vizsgáljuk | |
| - Nem végzünk kalorikus ingerlést, de az oculocephalicus reflex kiváltása megengedett | |
| - Afáziás betegek: az ágy egyik oldaláról menjen át a másik oldalra | |
| - NEM kötelező az első reakciót pontozni, és szabad a beteget biztatni | |
| - Conjugált szemtengely deviáció, de nem fix eltérés: 1 pont | |
| - A III., IV.vagy VI. agyideg paresise: 1 pont | |
| 3. Látómezők: A látómezők (a felső és alsó kvadránsok) vizsgálatát látótérvizsgálattal kell | 0 = Nincs látótérkiesés |
| végezni, úgy, hogy a betegnek meg kell mondania, hogy az orvas hány ujját mutatja, vagy | 1 = Részleges hemianopia |
| vizuális stimulust kell alkalmazni. A beteget bátorítani kell, de ha helyesen a mozgó ujjak | 2 = Teljes hemianopia |
| oldalára néz, akkor ez normálisként pontozható. Féloldali vakság vagy enucleatio esetén a | 3 = Kétoldali hemianopia (vak, beleértve a corticalis vakságot is) |
| látómezőket a másik szemre kell pontozni. Csak akkor adandó 1 pont, ha egyértelmű az | |
| aszimmetria, ezen belül a quadrantanopia. Ha a beteg bármilyen okból vak, 3 pontot kell | |
| adni. Ezután kettős egyidejű stimulációt kell végezni. Extinctio esetén 1 pontot kell adni, és | |
| az eredményeket a 11. kérdés megválaszolásához is fel kell használni. | |
| A1611005 Vizsgálati irányelvek: | |
| - Csak az egyik szem vizsgálható? Akkor ezt a szemet kell vizsgálni | |
| - Egyértelmű aszimmetria, quadrantanopia? 1 pont | |
| - Extindio (egyidejű stimuláció) 1 pont | |
| 4. Faciális bénulás: Szóban vagy mutogatással kérje meg a beteget, hogy vicsorítson, vagy | 0 = Normál szimmetrikus mozgás |
| húzza fel a szemöldökét és csukja be a szemét. Ha a beteg reakciója gyenge vagy nem fogja | 1 = Enyhe paralysis (elsimult nasolabialis redő) |
| fel az utasítást, a noxius stimulusra adott grimasz szimmetriáját pontozza. Ha az arcot | 2 = Részleges paralysis (az arc alsó részének teljes vagy szinte teljes paralysi'se) |
| faciális's trauma/kötés, orotrachealis's tubus, szalag vagy másfizikai akadály fedi, ezeket | 3 = Egy-vagy kétoldali teljes paralysi's (arcmozgás hiánya az arc felső és alsó részében) |
| amennyire csak lehetséges, el kell távolítani. | |
| A1611005 Vizsgálati irányelvek: | |
| - Egyértelmű normálfunkció: 0 pont | |
| - Bizonytalan? Vagy az eredmények alapján nem lehet pontosan következtetni (pl., az arc | |
| felső része izolált) 1 pont | |
| - Egyértelmű felső motoros faciális bénulás: 2 pont | |
| - Nem reagáló betegeknél: a fájdalmas stimulusra adott grimasz szimmetriája értékelendő | |
| - Alsó motoros faciális bénulás 3 pont | |
| - Kómás bele 3 pont |
| 5., 6. Kar- és lábmozgás: A v égtagot először megfelelő helyzetbe kell helyezni: ki kell | 0 = Nincs süllyedés, a végtag a teljes 10 másodpercig 90 (illetve 45) fokban kinyújtva |
| nyújtani a karokat(a tenyérrel lefelé) 90 fokban (üléskor) illetve 45 fokban | marad |
| (hanyattfekvéskor), a lábakat pedig 30 fokban (ezt mindig hanyatt fekve kell vizsgálni). | 1 = Süllyedés, a végtag 90 (illetve 45) fokban megtartott, de a 10 másodperc lejárta |
| Süllyedést akkor kell pontozni, ha a kar 10 másodpercnél, illetve a láb 5 másodpercnél | előtt lesüllyed, azonban nem egészen az ágyig, ¡11. más támasztékig |
| hamarabb leesik. Afáziás betegeket a hang felemelésével és mutogatással kell bátorítani, | 2 = Némi erőfeszítés a gravitáció ellen, a végtag nem nyújtható ki, illetve megtartott 90 |
| de nem szabad fájdalmas stimulálást alkalmazni. A végtagokat egymás után kell vizsgálni a | (illetve 45) fokban, lesüllyed egészen az ágyig, ele a beteg némileg küzd a gravitáció |
| nem paresi'ses karral kezdve. Csak amputáció vagy a váll- illetve a csípőízületek | ellen |
| mozgásképtelensége esetén lehet a "9"-es értéket választani, és a vizsgálónak pontosan | 3 = Nem küzd a gravitáció ellen, a végtag leesik |
| meg kell jelölnie, hogy választását mi indokolja. | 4 = Nincs mozgás |
| A1611005 Vizsgálati irányelvek a karmozgás vizsgálatához: | 9 = Amputáció, ízületek mozgásképtelensége (kérjük részletezni): |
| - Az elsőként adott reakciót kell pontozni, azonban: | |
| - Kezdeti esés, de a kar nem süllyed le 0 port | 5a. Bal kar |
| - Bizonytalan a súlyos paresis? | 5b. Jobb kar |
| a) bármilyen mozgás? 3 pont | |
| b) egyáltalán nincs mozgás? 4 pont | |
| - A "9"-es érték csak amputált végtag esetén választható, és írásban indokolni kell | |
| - Afáziás beteg bátorítsa mutogatással és hangja felemelésével | |
| - A végtagokat sorban egymás után vizsgálja, a nem paresises végtaggal kezdve | |
| - Ne vizsgálja mindkét kart egyidejűleg | |
| A1611005 Vizsgálati irányelvek a lábmozgás vizsgálatához: | |
| - Mindig hanyattfekvésben vizsgálandó | 0 = Nincs süllyedés, a végtag a teljes 5 másodpercig 30 fokban kinyújtva marad |
| - A végtagokat sorban egymás után vizsgálja, a nem paresises végtaggal kezdve | 1 = Süllyedés, a végtag a 10 másodperc lejárta előtt lesüllyed, de nem egészen az |
| - Afáziás beteg: bátorítsa mutogatással és hangja felemelésével | ágyig |
| - A "9"-es érték csak amputált végtag esetén választható, és írásban indokolni kell | 2 = Némi erőfeszítés a gravitáció ellen, a végtag az 5 másodperc letelte előtt lesüllyed |
| az ágyig, de a beteg némileg küzd a gravitáció ellen | |
| 3 = Nem küzd a gravitáció ellen, a végtag azonnal visszaesik az ágyra | |
| 4 = Nincs mozgás | |
| 9 = Amputáció, ízületek mozgásképtelensége (kérjük kifejteni): | |
| 6a. Bal láb | |
| 6b. Jobb láb | |
| 7. Végtag ataxia: A cél az esetleges féloldali cerebellaris laesio fennállásának megállapítása. | 0 = Nincs ataxia |
| A vizsgálat közben a szem legyen nyitva. Látáshiba esetén a vizsgálatot az ép látómezőben | 1 = Ataxia az egyik végtagban |
| kell elvégezni. Az ujj-orr-ujj és a sarok-sípcsont tesztet mindkét oldalon el kell végezni, és az | 2 = Ataxia mindkét végtagban |
| ataxia csak akkor pontozható, ha a gyengeséggel aránytalan mértékben áll fenn Ataxia | Ha van, akkor ataxia a |
| nem áll fenn annál a betegnél, aki nem fogja fel a feladatd vagy paralysisben szenved. Csak | Jobb karban 1 = igen 2 = nem |
| amputáció vagy a váll-, illetve csípőízületek mozgásképtelensége esetén lehet a "9"-es | Bal karban 1 = igen 2 = nem |
| értéket választani, és a vizsgálónak pontosan meg kell jelölnie, hogy miért nem pontozott. | Jobb lábban 1 = igen 2 = nem |
| Vakság esetén a vizsgálat végrehajtásához a kart először ki kell nyújtani, és így kell | Bal lábban 1 = igen 2 = nem |
| megérinteni az orrot. | 9 = Amputáció vagy ízületek mozgásképtelensége (kérjük kifejteni): |
| A1611005 Vizsgálati irányelvek: | |
| - Ataxia csak akkor pontozandó, ha a gyengeséggel aránytalan mértékben áll fenn | |
| - Ha nem biztos az ataxia fennállásában, adjon 0 pontot | |
| - Ha a beteg nem fogja fel vagy nem tudja végrehajtani az ujj-orrhegy a | |
| sarok-sípcsontvizsgálathoz adott utasítást, 0 pontot kell adni | |
| - Az "1"-es és a "2"-es érték kizárólag egyértelmű ataxia esetére szolgál |
| 8. Érzésvizsgálat: A vizsgálatkor a tűszúrás által - illetve kába vagy afáziás beteg esetén a | 0 = Normális, nincs érzészavar |
| fájdalmas stimulus által - kiváltott érzés vagy grimasz. Kizárólag a stroke-nak betudható | 1 = Enyhe-közepes érzészavar, a beteg érzi a tűszúrást, de nem olyan élesen, vagy az |
| érzészavar pontozható rendellenesnek, és a vizsgálónak a test annyi területét [kar (nem | érintett oldalon tompán érez; vagy ha a tűszúrás nyomán nem érez felszíni fájdalmat, |
| kéz], láb, törzs, arc] kell megvizsgálnia, amennyi szükséges a féloldali érzéskiesés | de tudja, hogy megérintik. |
| kimutatásához. A "2"-es (súlyos vagy teljes) érték csak akkor adható, ha a súlyos vagy teljes | 2 = Súlyos-teljes érzéskiesés; a beteg nem érzékeli, hogy megérintették arcát, karját és |
| érzészavar egyértelműen kimutatható. Stupor vagy afázia esetén ezért a betegek | lábát. |
| valószínűleg 1 vagy 0 értéket kapnak. Agytörzsi stroke esetén az a beteg, akinél kétoldali | |
| érzészavar mutatható ki, 2 pontot kap. Ha a beteg nem reagál és quadriplegiás, 2 pontot | |
| kap. A kóma betegek (akiknél 1 a = 3) mindig 2 pontot kapnak. | |
| A1611005 Vizsgálati irányelvek: | |
| - Kizárólag a stroke-nak betudható érzéskiesés tekintendő rendellenesnek | |
| - A vizsgálatot ne a kézen és a lábfejen végezze (? szenzoros neuropathia) | |
| - Afázia/stupor esetén: 0 vagy 1 pont | |
| - 2 pont csak akkor adható, ha egyértelműen megállapítható | |
| - Agytörzsi stroke kétoldali érzéskiesés 1: 2 pont | |
| - Quadriplegiás beteg, nincs reakció: 2 pont | |
| - Kómás beteg: 2 pont | |
| 9. Beszédkészség: Az értetni képességről már a vizsgálat előző szakaszai során számos | 0 = Nincs afázia, normális |
| információ nyerhető. | 1 = Enyhe-közepes afázia; a beszédkészségben és a beszédfelfogásban némi zavar |
| A beteget kérje meg, hogy mondja el mi történik a neki mutatott képen, nevezze meg az | nyilvánvaló, de ez nem korlátozza súlyosan a gondolatok közlését és a kifejezésmód. A |
| átadott lapon lévő tárgyakat, és olvassa fel az átadott papíron álló mondatokat. | csökkent beszédkészség és/vagy felfogóképesség azonban megnehezíti vagy |
| Az értelmi képességet a fenti utasításokra és az előző neurológiai vizsgálatok során | lehetetlenné teszi az átadott anyagokról való beszélgetést. Az átadott anyagokról való |
| elhangzott utasításokra adott reakciókból lehet megítélni. Ha a vizsgálatok elvégzését | beszélgetés során például a vizsgáló a beteg válasza alapján azonosítani tudja a képet |
| látászavar hátráltatja, akkor a beteget meg kell kérni, hogy nevezze meg a kezébe adott | vagy a megnevezendő kártyát. |
| tárgyakat, ismételje meg az elhangzottakat, és beszéljen. Ha a beteg intubált, meg kell | 2 = Súlyos afázia; a kommunikáció során a beteg mindvégig csak szótöredékekben |
| kérni, hogy írjon. A kómában lévő betegek (akiknél 1 a = 3) 3 pontot kapnak. A vizsgálónak | képes kifejezni magát, nagy szükség van a hallgató általi közreműködésre, kérdezésre |
| kell eldönteni hogy milyen értéket kap a stuporos vagy korlátozottan együttműködő beteg | és találgatásra. Az átadható információk köre korlátozott; a hallgató előre a |
| de a "3"-as érték csak akkor választandó, ha a beteg néma és az egyik egy lépéses utasítást | beszélgetést. A vizsgáló a beteg válaszaiból nem tudja azonosítani az átadott |
| sem követi *AZ ÖSSZPONTSZÁM KISZÁMÍTÁSAKOR A "9"-ES ÉRTEKEKET NEM SZABAD | anyagokat. |
| FIGYELEMBEVENNI. | 3 = Néma, teljes afázia; nem képes érthető beszédre és a hallottakat nem fogja fel. |
| A1611005 Vizsgálati irányelvek: | |
| - Afáziás, de kommunkáló beteg 1 pont | |
| - A vizsgálónak kell vezetnie a beszélgetést 2 pont | |
| - Nem kooperáló betegek: a vizsgáló csak akkor válassza a "3"-as értéket, ha a beteg néma, | |
| és nem tudja követni az egy lépéses utasításokat | |
| - Kómás beteg: 3 pont | |
| - A megnevezésnél és a képeknél az ÖSSZES tárgyat végig kell venni | |
| - NEM kötelező az első reakciót pontozni | |
| - Látásproblémával küszködő beteg: kézbe adott tárgy felismerése | |
| - Intubált beteg: kérje meg, hogy írják le a választ | |
| 10. Dysarthria: Ha a beteg értelme elvben ép, meg kell vizsgálni beszédét. Ehhez meg kell | 0 = Normális |
| kérni, hogy olvassa fel vagy ismételje meg az átadott listán szereplő szavakat. Súlyosan | 1 = Enyhe-közepes; a beteg a szavak végét néha elnyeli, és a legrosszabb esetben némi |
| afáziás betegnél azt kell értékelni, hogy a spontán beszéd során mennyire artikulál tisztán. | nehézséget okoz beszédének megélése. |
| A "9"-es érték csak akkor választandó, ha a beteg intubált vagy más fizikai gát gátolja a | 2 = Súlyos; a beteg annyira rosszul ejti a szavakat, hogy beszéde érthetetlen, pedig |
| beszédben, és ilyenkor a vizsgálónak pontosan meg kell adnia, hogy miért nem pontoz. A | nem áll fenn dysphasia, vagy ha igen, akkor nincs arányban, és a beteg nem néma/nem |
| betegnek nem szabad elmondani, hogy a vizsgálatnak mi a célja. | anarthriás. |
| A1611005 Vizsgálati irányelvek: | 9 = Intubálás vagy más fizikai gát. Mégpedig: |
| - Afáziás betegeknél a spontán beszéd során kell értékelni az artikuláció tisztaságát | |
| érthető beszéd: 1 pont, nem érthető beszéd: 2 pont | |
| - Kómás/nem reagáló betegek: 2 pont |
| 11. Extinkció, érzékelési zavar: Az érzékelési zavar igazolásához elegendő információ | 0 = Nincs rendellenesség |
| nyerhető az előző vizsgálatokból. Ha a beteg látása súlyosan károsodott, így nem | 1 = Vizuális, tapintási hallási, térbeli vagy személyt illető érzékelési zavar vagy a |
| végezhető el a kettős egyidejű stimuláció, de a bőrstimulusra adott reakció normális, akkor | kétoldali egy idejű stimulálásnál jelentkező extintio az érzékelési módok egyikénél |
| az eredmény normális. Ha a beteg afáziás és a jelek szerint mindkét oldalra figyel az | 2 = Kifejezett féloldali érzékelési zavar vagy féloldali érzékelési zavar az érzékelési |
| eredmény akkor is normális. Ha vizuális térbeli érzékelési zavar vagy anosognosia áll fenn, | módok egyikénél. A beteg nem ismeri fel saját kezét vagy a térnek csak az egyik felére |
| az is a rendellenességre utalhat. Mivel a rendellenesség csak akkor pontozható, ha fennáll | figyel |
| nincs olyan eset, amikor ez a teszt nem végezhető el | |
| A1611005 Vizsgálati irányelvek: | |
| - Ha a beteg látása károsodott: a bőrstimulusra adott választ kell értékelni | |
| - Afáziás beteg, ha mindkét oldalra figyel: 0 port | |
| - Csak a tény legesen megállapított rendellenességet pontozza | |
| Kiegészítő vizsgálat; ami nem képezi a részét a NIH stroke skála pontozásnak. | 0 = Normális (5 másodperc elteltével sincs flexió) |
| A Distalis motoros funkció: A vizsgáló az alkarnál fogva felemeli a beteg kezét, és megkéri a | 1 = 5 másodperc után az ujjak valamennyire nyújtva vannak, de már nem teljesen. Ha |
| beteget, hogy nyújtsa ki ujjait, amennyire csak lehet. Ha a beteg nem tudja kinyújtani agy | az ujjak mozognak, de nem utasításra, az nem pontozandó. |
| nem nyújtja ki ujjait, a vizsgáló a beteg ujjait teljesen kinyújtja, és figyeli, hogy az ujjak 5 | 2 = 5 másodperc elteltével sincs akaratlagos nyújtás. Ha az ujjak máskor mozognak, az |
| másodperc elteltével nem görbültek-e vissza. Csak a beteg első próbálkozása pontozható. | nem pontozható. |
| Nem szabad az utasításokat és a vizsgálatot megismételni. | a. Bal kar |
| b. Jobb kar |
3. sz. függelék
A Stroke rehabilitációs ellátás c. klinikai irányelvhez: Felmérőeszközök (angolul)
(az eredeti US anyag 'D' appendixe)
Standard Instruments for Post-Stroke Assessment
| Pr Type | eferred Standard Instrumer Name and Source | ts for Patient Ass Approximate Time to Administer | essment in Stroke Strengths | Weaknesses |
| Level-of-consciousness scale | Glasgow Coma Scale] | 2 min | Simple, valid, reliable | None observed |
| Stroke deficit scales | NIH Stroke Scale | 2 min | Brief, reliable; Can be administered by non-neurologists | Low sensitivity |
| Canadian Neurological Scale | 5 min | Brief, valid, reliable | Some useful measures omitted | |
| Global disability scale | Rankin Scale | 5 min | Good for overall assessment of disability | Walking is the only explicit assessment criterion; Low sensitivity |
| Measures of disability/activities of daily living (ADLs) | Barthel Index | 5-10 min | Widely used for stroke; Excellent validity and reliability | Low sensitivity for high-level functioning |
| Functional Independence Measure (FIM™) [g] | 40 min | Widely used for stroke; Measures mobility, ADLs, cognition, functional communication | "Ceiling" and "floor" effects | |
| Mental status screening | Folstein Mini-Mental State Examination | 10 min | Widely used for screening | Several functions with summed score-May misclassify patients with aphasia |
| Neurobehavioral Cognition Status Exam (NCSE) | 10 min | Predicts gain in Barthel Index scores; Unrelated to age | Does not distinguish right from left hemisphere;No reliability studies in stroke; No studies of factorial structure; Correlates with education | |
| Assessment of motor function | Fugl-Meyer | 30-40 min | Extensively evaluated measure; Good validity and reliability for assessing sensorimotor function and balance | Considered too complex and time-consuming by many. |
| Motor Assessment Scale | 15 min | Good, brief assessment of movement and physical mobility | Reliability assessed only in stable patients; Sensitivity not tested | |
| Motricity Index | 5 min | Brief assessment of motor function of arm, le.g.,e.g.,e.g., and trunk | Sensitivity not tested | |
| Balance assessment | Berg Balance Assessment | 10 min | Simple, well established with stroke patients; sensitive to change | None observed |
| Mobility assessment | Rivermead Mobility Index | 5 min | Valid, brief, reliable test of physical mobility | Sensitivity not tested |
| Assessment of speech and language functions | Boston Diagnostic Aphasia Examination | 1-4 h | Widely used; Comprehensive, good standardization data; Sound theoretical rationale | Time to administer long; Half of patients cannot be classified |
| Porch Index of Communicative Ability (PICA) | 1/2-2 h | Widely used; Comprehensive, careful test development and standardization | Time to administer long; Special training required to administer; Inadequate sampling of language other than 1 word and single sentences | |
| Western Aphasia Battery | 1-4 h | Widely used. Comprehensive | Time to administer long; "Aphasia quotients" and "taxonomy" of aphasia not well validated | |
| Depression scales | Beck Depression Inventory (BDI) | 10 min | Widely used; Easily administered; Norms available; Good with somatic symptoms | Less useful in elderly and in patients with aphasia or neglect; High rate of false positives; Somatic items may not be due to depression |
| Center for Epidemiologic Studies Depression (CES-D) | < 15 min | Brief, easily administered, useful in elderly; Effective for screening in stroke population | Not appropriate for aphasic patients | |
| Geriatric Depression Scale (GDS) | 10 min | Brief, easy to use with elderly, cognitively impaired, and those with visual or physical problems or low motivation | High false-negative rates in minor depression | |
| Hamilton Depression Scale | < 30 min | Observer rated; Frequently used in stroke patients | Multiple differing versions compromise interobserver reliability | |
| Measures of instrumental ADLs | PGC Instrumental Activities of Daily Living | 5-10 min | Measures broad base of information necessary for independent living | Has not been tested in stroke patients |
| Frenchay Activities Index | 10-15 min | Developed specifically for stroke patients; Assesses broad array of activities | Sensitivity and interobserver reliability not tested; sensitivity probably limited | |
| Family assessment | Family Assessment Device (FAD) | 30 min | Widely used in stroke; Computer scoring available; Excellent validity and reliability; Available in multiple languages | Assessment subjective; sensitivity not tested; "ceiling" and "floor" effects |
| Health status/quality of life Medical Outcomes measures Study (MOS) 36-Item Short-Form Health Survey | 10-15 min | Generic health status scale SF36 is improved version of SF20; Brief, can be self-administered or administered by phone or interview; Widely used in the United States | Possible "floor" effect in seriously ill patients (especially for physical functioning), suggests it should be supplemented by an ADL scale in stroke patients |
| Sickness Impact Profile (SIP)* | 20-30 min | Comprehensive and well-evaluated; Broad range of items reduces "floor" or "ceiling" effects | Time to administer somewhat long; Evaluates behavior rather than subjective health; needs questions on well-being, happiness, and satisfaction |
ADLs indicates activities of daily living. lADLs, instrumental activities of daily living.
* Instrument is available from the Health Services Research and Development Center, The Johns Hopkins School of Hygiene and Public Health, 624 North Broadway, Baltimore, MD 21205.
Disability/ADL Assessment Katz Index of ADL40
Kenny Self-Care Evaluation41
LORS/LAD42
PECS43
Mental Status Assessment44
The Stroke Center at http://www.strokecenter.org/trials/scales/index.htm
Depression Assessment The Zung Scale45
IADL Assessment
OARS: Instrumental ADL46
Functional Health Status47
Stroke Impact Assessment48-50
The Stroke Impact Scale (SIS) - Web site: www2.kumc.edu/coa/Pepper/pepper.htm.
Assessment of Communication: Websites:
American Speech-Language-Hearing Association: http://www.asha.org National Aphasia Association: http://www.aphasia.org
Academy of Neurological Communication Disorders and Sciences: http://www.ancds.duq.edu/ University of Minnesota Duluth: http://www.d.umn.edu/~mmizuko/3411/may11.htm Neuropsychology Central: http://www.neuropsychologycentral.com/interface/content/resources/page_material/resources_general_materials _pages/resources_document_pages/aphasia_assessment.pdf
REFERENCES
1. Agency for Health Care Policy and Research (AHCPR), Gresham GE, Duncan PW, et al. Post-Stroke Rehabilitation (Clinical Practice Guideline, no. 16). Rockville, MD: U.S. Department of Health and Human Services, Public Health Service; 1995.
2. dale G, Murray G, Parker L, et al. Assessment of coma and impaired consciousness: a practical scale. Lancet. 1974;2:81-83.
3. dale G, Murray G, Parker L, et al. Adding up the Glasgow Coma Scale. Acta Neurochir. 1979;Suppl 28:13-16.
4. BrottT, Adams HP, Jr.,OlingerCP,et al. Measurements of acute cerebral infarction: a clinical examination scale. Stroke. Jul 1989;20(7):864-870.
5. Cote R, Hachinski VC, Shurvell BL, et al. The Canadian Neurological Scale: a preliminary study in acute stroke. Stroke. Jul-Aug 1986;17(4):731-737.
6. Rankin J. Cerebral vascular accidents in patients over the age of 60. II. Prognosis. Scott Med J. May 1957;2(5):200-215.
7. Bonita R, Beaglehole R. Recovery of motor function after stroke. Stroke. Dec 1988;19(12):1497-1500.
8. van Swieten JC, Koudstaal PJ, Visser MC, et al. Interobserver agreement for the assessment of handicap in stroke patients. Stroke. May 1988;19(5):604-607.
9. Mahoney FI, Barthel DW. Functional Evaluation: The Barthel Index. Md State Med J. Feb 1965;14:61-65.
10. Wade DT, Collin C. The Barthel ADL Index: a standard measure of physical disability? Int Disabil Stud. 1988;10(2):64-67.
11. Granger CV, Hamilton BB, Keith RA, et al. Advances in functional assessment for medical rehabilitation. Top Geriatr Rehabil. 1986;1(3):59-74.
12. Granger CV, Hamilton BB, Sherwin FS. Guide for the use of the uniform data set for medical rehabilitation. Buffalo, NY: Uniform Data System for Medical Rehabilitation Project Office, Buffalo General Hospital, NY; 1986.
13. Keith RA, Granger CV, Hamilton BB, et al. The functional [a] Teasindependence measure: a new tool for rehabilitation. In: Eisenberg MG, Grzesiak RC, eds. Advances in clinical rehabilitation. Vol 1. New York: Springer-Verlag; 1987:6-18.
14. Folstein MF, Folstein SE, McHugh PR. "Mini-mental state". A practical method for grading the cognitive state of patients for the clinician. J Psychiatr Res. Nov 1975;12(3):189-198.
15. Kiernan RJ, Mueller J, Langston JW, et al. The Neurobehavioral Cognitive Status Examination: a brief but quantitative approach to cognitive assessment. Ann Intern Med. Oct 1987;107(4):481-485.
16. Fugl-Meyer AR, Jaasko L, Leyman I, et al. The post-stroke hemiplegic patient. 1. a method for evaluation of physical performance. Scand J Rehabil Med. 1975;7(1):13-31.
17. Carr JH, Shepherd RB, Nordholm L, et al. Investigation of a new motor assessment scale for stroke patients. Phys Ther. Feb 1985;65(2):175-180.
18. Poole JL, Whitney SL. Motor assessment scale for stroke patients: concurrent validity and interrater reliability. Arch Phys Med Rehabil. Mar 1988;69(3 Pt 1):195-197.
19. Collin C, Wade D. Assessing motor impairment after stroke: a pilot reliability study. J Neurol Neurosurg Psychiatry. Jul 1990;53(7):576-579.
20. Demeurisse G, Demol O, Robaye E. Motor evaluation in vascular hemiplegia. Eur Neurol. 1980;19(6):382-389.
21. Berg KO, Maki BE, Williams JI, et al. Clinical and laboratory measures of postural balance in an elderly population. Arch Phys Med Rehabil. Nov 1992;73(11):1073-1080.
22. Berg K, Wood- Dauphinee S, Williams JI, et al. Measuring balance in the elderly: preliminary development of an instrument. Physiother Can. 1989:304-311.
23. Collen FM, Wade DT, Robb GF, et al. The Rivermead Mobility Index: a further development of the Rivermead Motor Assessment. Int Disabil Stud. Apr-Jun 1991;13(2):50-54.
24. Wade DT, Collen FM, Robb GF, et al. Physiotherapy intervention late after stroke and mobility. Bmj. Mar 7 1992;304(6827):609-613.
25. Goodglass H, Kaplan E. Test procedures and rationale. The assessment of aphasia and related disorders. Philadelphia: Lea and Febiger; 1972.
26. Goodglass H, Kaplan E. Manual for the Boston Diagnostic Aphasia Examination (BDAE). Philadelphia: Lea and Febiger; 1983.
27. Porch B. Porch Index of Communicative Ability (PICA). Palo Alto: Consulting Psychologists Press; 1981.
28. Kertesz A. Western Aphasia Battery. New York: Grune & Stratton; 1982.
29. Beck AT, Ward CH, Mendelson M, et al. An inventory for measuring depression. Arch Gen Psychiatry. Jun1961;4:561-571.
30. Beck AT, Steer RA. Beck Depression Inventory: manual (revised edition). New York: NY Psychological Corporation; 1987.
31. Radloff LS. The CES-D scale: a self-report depression scale for research in the general population. J Appl Psychol Meas. 1977;1:385-401.
32. Yesavage JA, Brink TL, Rose TL, et al. Development and validation of a geriatric depression screening scale: a preliminary report. J Psychiatr Res. 1982;17(1):37-49.
33. Hamilton M. A rating scale for depression. J Neurol Neurosurg Psychiatry. Feb 1960;23:56-62.
34. Hamilton M. Development of a rating scale for primary depressive illness. Br J SocClin Psychol. Dec 1967;6(4):278-296.
35. Lawton MP. Assessing the competence of older people. In: Kent D, Kastenbaum R, Sherwood S,eds. Research planning and action for the elderly. New York: Behavioral Publications; 1972.
36. Holbrook M, Skilbeck CE. An activities index for use with stroke patients. Age Ageing. May 1983;12(2):166-170.
37. Epstein NB, Baldwin LM, Bishop DS. The McMaster Family Assessment Device. J Marital and Fam Ther. 1983;9(2):171-180.
38. Ware JE, Jr., Sherbourne CD. The MOS 36-item short-form health survey (SF-36). I. Conceptual framework and item selection. Med Care. Jun 1992;30(6):473-483.
39. Bergner M, Bobbitt RA, Carter WB, et al.The Sickness Impact Profile: development and final revision of a health status measure. Med Care. Aug 1981;19(8):787-805.
40. Katz S, Ford AB, Moskowitz RW, et al. Studies Of Illness In The Aged. The Index Of Adl: A Standardized Measure Of Biological And Psychosocial Function. JAMA. Sep 21 1963;185:914-919.
41. Schoening HA, Iversen IA. Numerical scoring of self-care status: a study of the Kenny self-care evaluation. Arch Phys Med Rehabil.Apr 1968;49(4):221-229.
42. Carey RG, Posavac EJ. Program evaluation of a physical medicine and rehabilitation unit: a new approach. Arch Phys Med Rehabil. Jul 1978;59(7):330-337.
43. Harvey RF, Jellinek HM. Functional performance assessment: a program approach. Arch Phys Med Rehabil. Sep 1981;62(9):456-460.
44. Ben-Yishay Y, Diller L, Gerstman L,et al.The relationship between impersistence, intellectual function and outcome of rehabilitation in patients with left hemiplegia. Neurology. Sep 1968;18(9):852-861.
45. Zung WW. A Self-Rating Depression Scale. Arch Gen Psychiatry. Jan 1965;12:63-70.
46. Duke University Center for the Study of Aging and Human Development. Multidimensional functional assessment: the OARS methodology. Durham, NC: Duke University; 1978.
47. Rosow I, Breslau N. AGuttman health scale for the aged. J Gerontol. Oct 1966;21(4):556-559.
48. Duncan PW, Bode RK, Min Lai S, et al. Rasch analysis of a new stroke-specific outcome scale: the Stroke Impact Scale. Arch Phys Med Rehabil. Jul 2003;84(7):950-963.
49. Duncan PW, Lai SM, Tyler D, et al. Evaluation of proxy responses to the Stroke Impact Scale. Stroke. Nov 2002c;33(11):2593-2599.
50. Lai SM, Studenski S, Duncan PW, et al. Persisting consequences of stroke measured by the Stroke Impact Scale. Stroke. Jul 2002;33(7):1840-1844.
1. Czimbalmos Á és mtsai (1999): Páciens megelégedettségi vizsgálat SF-36 kérdőívvel, a magyarországi normálértékek meghatározása. Népegészségügy 80 (1):4-19
2. Kálmán János, Maglóczky Erzsébet, Janka Zoltán (1995):Óra rajzolási teszt: gyors és egyszerű demencia szűrőmódszer. Psychiatr Hung 10 (1):11-18
3. Osmanné Sági Judit (1991): Az afázia klasszifikációja és diagnosztikája I-II. Ideggy Szle 44 (8): 339-362
4. Szél I: Állapotfelmérés és tervkészítés a rehabilitáció folyamatában. In: Huszár I, Kullmann L, Tringer L (szerk): A rehabilitáció gyakorlata. Medicina, Bp., 2000.78-90
5. Molnár G, Molnár I (1999): A Beck- és Zung-féle depresszió önértékelő tesztek faktoranalízise. Pszichoterápia 8 (3):175-180
6. Tariska P, Paksy A (2003): Mini-Cog: a mentális hanyatlás "ultrarövid" és egyszerű szűrésének lehetősége. Orv Hetil 144 (17):803-9
7. Tariska P és mtsai (1990): A módosított Mini Mental State vizsgálat. Ideggy Szle 43 (10):443-9
FIM (functional independence measure, "funkcionális függetlenség mérés")
NÉV:........................................................
DÁTUM:_felvétel után távozás előtt kontroll
önellátás
A. ÉTKEZÉS
B. SZEMÉLYI HIGIÉNÉ
C. FÜRDÉS
D. ÖLTÖZKÖDÉS (felső testfél)
E. ÖLTÖZKÖDÉS (alsó testfél)
F. WC HASZNÁLAT
szfinkterirányítás
G. SZÉKLETTARTÁS
H. VIZELETTARTÁS_
mozgékonyság
I. ÁGYSZÉK, KEREKESSZÉK ÁTÜLÉSEK (transzferek, átszállások) J.WC TRANSZFER
K. KÁD vagy ZUHANY TRANSZFER_
helyváltoztatás L. JÁRÁS vagy KEREKESSZÉKHASZNÁLAT
M. LÉPCSŐ_
kommunikáció
N. MEGÉRTÉS
O. ÖNKIFEJEZÉS
szociális képességek
P. SZOCIÁLIS EGYÜTTMŰKÖDÉS
Q. PROBLÉMAMEGOLDÁS
R. EMLÉKEZÉS
Pontozás:
1. SEGITő SZEMÉLYRE NINCS SZÜKSÉG - Önellátó 7 =Teljes függetlenség (időben, biztonságosan) 6=Módosétott függetlenség (segédeszköz)
II. SZEMÉLYES SEGITSÉG SZÜKSÉGES
Részleges függőség 5=Felügyet
4=Minimális segétség (75%nál nagyobb önállóság) 3=Közepes segétség (50%nál nagyobb önállóság)
Teljes függőség
2=Maximális segétség (a vizsgált személy 2550%os részvételével) 1=Teljes segétség (a vizsgált személy 25% alatti részvételével) Ha egy tevékenység nem tesztelhető, a szint: 1
4. sz. függelék
A kiválasztott külföldi klinikai irányelv - Management of Adult Stroke Rehabilitation Care http://stroke.ahajournals.Org/cgi/content/full/36/9/e100 - adaptálása magyarországi viszonyokra: Változtatások fajtái az adaptálás során
1) tömörítés - ld. az irányelv előszavának'D' szakaszát
2) háttérismeretek ajánlása - magyar nyelvű szakirodalom (ld.l.sz.függelék)
3) kihagyások (ajánlásé vagy alszakaszé annak ajánlásával együtt)
AII/D pont 4. ajánlását kihagytam. Az eredeti anyagban e109. oldal: "Recommend that the patient and caregivers have their psychosocial and support needs reviewed on a regular basis, by a social workeror appropriate healthcare worker, to minimize caregiver distress.", a magyar szövegben a 7. oldalon lenne. Ajánlási kategóriája: nem volt megadva. A IV/C-1 pont 6. és 7. ajánlását kihagytam. Az eredeti anyagban e114. oldal: "There is insufficient evidence to recommend for or against fiberoptic endoscopic examination of swallowing with sensory testing (FEESST) for the assessment of dysphagia. Recommend that the diagnostic assessment, whether VFSS or another modality, include a definition of swallow physiology with identification of the physiological abnormality and treatment strategies to directly assess their effectiveness.", a magyar szövegben a 10. oldalon lenne.
AIV/G pont 2. ajánlását kihagytam. Az eredeti anyagban e119. oldal: "Recommend that a multidisciplinary assessment, using a standard procedure, be undertaken and documented for all patients. Patients with need of rehabilitation intervention should be referred to a specialist stroke rehabilitation team, as soon as possible.", a magyar szövegben a 13. oldalon lenne.
A IV/J-3 pont 2. és 3. ajánlását kihagytam. Az eredeti anyagban e122. oldal: "Recommend that all patients who were previously employed be referred to vocational counseling for assistance in returning to work. Recommend that all patients who are considering a return to work but who may have psychosocial barriers (eg, motivation,emotional,and psychological concerns) be referred for supportiveservices,such as vocational counseling or psychological services.",a magyar szövegben a 14. oldalon lenne.
A IV/N pont 4. és 5. ajánlását kihagytam. Az eredeti anyagban e124. oldal: "Recommend that patient and caregiver education be provided in an interactive and written format. Provide the patient and family with an information packet that may include printed material on subjects such as the resumption of driving, patient rights/responsibilities, support group information,and audiovisual programs on stroke. Recommend that the detailed treatment plan be documented in the patient's record to provide integrated rehabilitation care.", a magyar szövegben a 15. oldalon lenne. A IV/O pont "kommunikáció" szakaszból a "hosszú távú kommunikációs nehézségek" alszakaszt (e126. oldal) kihagytam. Nem valósítható meg Magyarországon. A magas QE szint számomra elfogadhatatlan és nem egyezik meg a Cochrane adatbázisban ugyanerről olvasottakkal.
A IV/O pont "motoros" szakaszból a futópad alszakaszt (e127. oldal) kihagytam. Ok: Újabb evidenciát ismerek (Moseley, AM; Stark, A; Cameron, ID; Pollock, A: Treadmill training and body weight support for walking after stroke. Cochrane Database of Systematic Reviews. 3,2005.), amely szerint csak a már járóképesek járását javítja valamelyest, az önálló járásra még képtelen bénultak esélyét nem növeli. Emiatt viszont nem érdemes jelentős vagyonért "futópadosítani" Magyarországot.
A IV/O pont "motoros" szakaszból a "kényszerítés által indulált mozgásterápia" alszakaszt (e127. oldal) kihagytam. Ok: Magyarországon még csak az eredeti (Taub-féle) verzió ismeretes, a módosított és valóban szélesebb körben használható verzióval meg kell ismertetni a honi környezetet, tapasztalatot kell szerezni. Az irányelv revíziója során lehet majd bevenni.
A IV/O pont "motoros" szakaszból az "NDT" alszakaszt (e128. oldal) kihagytam. Ok: Magyarországon nem honosodott meg, nem kell vele foglalkozni.
A IV/O pont "motoros" szakaszból a spaszticitás alszakasz 5. (intrathecalis baclofen) és 6. ajánlását kihagytam. Jelenleg azzal is elégedettnek kell lennünk, ha súlyos koponya-agy-sérülés (valamint természetesen gerincvelő sérülés) esetén van rá kapacitás Magyarországon. A legközelebbi revízió alkalmával érdemes lesz újra mérlegelni a hazai kapacitásokat.
A IV/O pont "motoros" szakaszból a vállfájdalom alszakasz 2. ajánlását kihagytam. Ok: Magyarországon szerencsére nem volt divat a bénult oldali váll mechanikus szerkezet általi rángatása.
A IV/P pont 5. ajánlását kihagytam. Az eredeti anyagban e135. oldal: "Recommend that case management be put in place for complex patient and family situations.", a magyar szövegben a 18. oldalon lenne.
4) ajánlások összevonása
A III/-2 pont 2. és 3. ajánlását összevontam. Az eredeti anyagban e112. oldal, a magyar szövegben 9. oldal. Ok: Mo.-on inkább LMWH-t használunk, mintsem nem-frackionált heparint.
5) ajánlási kategória megváltoztatása
AIV/C-2 pont 3. ajánlás esetében az ajánlási kategóriát 'B'-ről 'C'-re kívánatos módosítani, mivel Magyarországon, noha forgalomban van, de egyelőre szkepcticizmus övezi az ezüstötvözettel bevont állandó hólyag katéter használatát. (Eredeti anyagban e115. oldal: "Recommend the use of silver alloy-coated urinary catheters,if a catheter is required.", a magyar szövegben a 10. oldal alján lenne). Ezzel nem avatkozunk be durván a dolgokba (ráadásul olyan dolgokba, amelyek nagyobbrészt más diszciplinára tartoznak), mégis pozitívan hathatunk.
Irodalom az erdeti ajánlásban: Saint S, Elmore JG, Sullivan SD, Emerson SS, Koepsell TD. The efficacy of silver alloy-coated urinary catheters in preventing urinary tract infection: a meta-analysis. Am J Med. 1998; 105: 236-241. PURPOSE: Indwelling urinary catheters are implicated in most cases of nosocomial urinary tract infection. Silver-coating of catheters may reduce the risk of these infections; however, trials have provided mixed results. We performed a meta-analysis to estimate the effectiveness of silver-coated urinary catheters. SUBJECTS AND METHODS: Published or unpublished articles were sought using MEDLINE, reference review, and correspondence with original authors, catheter manufacturers, and experts. Trials using silver-coated urinary catheters in the treatment group and uncoated urinary catheters in the control group were included. Bacteriuria, as evaluated by urine culture, was the outcome variable used to indicate urinary tract infection. Summary odds ratios (OR) and 95% confidence intervals (CI) were calculated using Mantel-Haenszel methods with a fixed-effects model. RESULTS: Of 117 reports retrieved, eight trials with a total of 2,355 patients satisfied inclusion criteria. The summary OR for urinary tract infection was 0.59 (95% CI, 0.42 to 0.84) indicating a significant benefit in the patients receiving silver-coated catheters. A test of heterogeneity, however, indicated that the odds ratios varied significantly among studies. Silver alloy catheters (OR = 0.24; 95% CI, 0.11 to 0.52) were significantly more protective against bacteriuria than silver oxide catheters (OR = 0.79; 95% CI, 0.56 to 1.10). CONCLUSIONS: This meta-analysis clarifies discrepant results among trials of silver-coated urinary catheters by revealing that silver alloy catheters are significantly more effective in preventing urinary tract infections than are silver oxide catheters. Though silver alloy urinary catheters cost about $6 more than standard urinary catheters, they may be worth the extra cost since catheter-related infection is a common cause of nosocomial infection and bacteremia.
Általam talált újabb irodalmak: Plowman R, Graves N, Esquivel J, Roberts JA: An economic model to assess the cost and benefits of the routine use of silver alloy coated urinary catheters to reduce the risk of urinary tract infections in catheterized patients. J Hosp Infect. 2001 May;48(1):33-42. Prevalence studies generally find nosocomial urinary tract infections to be the most common type of nosocomial infection, accounting for between 21% and 45% of all HAIs.The main risk factor appears to be the presence of a urinary catheter, with an estimated 80% of these infections being associated with their use. This paper describes a model which quantifies the extent of the burden of these infections in terms of the number of patients affected and the costs incurred by the hospital sector; and identifies the potential benefits of the routine use of silver alloy coated catheters, as a means of reducing the incidence of this type of infection. An illustrative model of the annual costs and benefits associated with the routine use of this intervention in adult, non-day case patients admitted to the medical and surgical specialties of NHS hospitals throughout England is presented. The results suggest that a 14.6% reduction in the incidence of urinary tract infections in catheterized medical patients, and a 11.4% reduction in catheterized surgical patients, would cover the cost of the intervention. Any further reduction in incidence would result in net positive benefits. Copyright 2001 The Hospital Infection Society. Davenport K, Keeley FX: Evidence for the use of silver-alloy-coated urethral catheters. J Hosp Infect. 2005 Aug;60(4):298-303. Catheter-associated urinary tract infections (CAUTIs) are a common occurrence and are associated with increased patient morbidity and mortality. In addition, they delay patient discharge from hospital, substantially increase hospital costs and promote the emergence of resistant organisms. Any intervention resulting in a decrease in the incidence of CAUTIs would have a significant impact on patient quality of life and hospital costs. By reviewing the current literature, it can be seen that the use of silver-alloy-coated hydrogel catheters can reduce CAUTIs by up to 45%. Despite reducing CAUTIs in most hospital situations, the greatest reduction is seen in postoperative patients, intensive care unit patients and burns patients.
6) módosítás az ajánlás szövegében -kórház típus, szóhasználat,eltérő végzettség ("beszéd patológus" nálunk nincs)
7) tartalmi módosítás az ajánlás szövegében
e 130. oldal vállfájdalom-intraarticularis inj.szerepel az eredeti szövegben. Itthon periarticularisa használatos. Localis megnevezést használtam.
Az Egészségügyi Minisztérium
szakmai protokollja
A gyógyszeres fájdalomcsillapításról és gyulladásgátlásról a reumatológiai betegségekben
(1. módosított változat)
Készítette: a Reumatológiai és Fizioterápiás Szakmai Kollégium
I. Alapvető megfontolások
A reumatológiai megbetegedések vezető tünete a fájdalom. A betegek jelentős része az orvost első alkalommal a perzisztáló, vagy egyre erősödő fájdalom miatt keresi fel, amelynek hátterében leggyakrabban az ízületek vagy a gerinc degeneratív vagy gyulladásos megbetegedései állnak. Az oki kezelés mellett szinte mindig szükség van fájdalomcsillapításra. Amennyiben a beteg mozgásképtelen, cél, hogy az állapota oly mértékben javuljon, hogy önellátásra képes legyen, és lehetőleg ne szoruljon sem kórházi ellátásra, sem a családtagok folyamatos gondozására. Közismert, hogy a mozgásszervi megbetegedésekokozta fájdalom csillapítása komoly nehézséget okoz a kezelőorvos számára, amelynek fő oka az, hogy a mozgásszervi megbetegedések okozta fájdalom általában több komponensű.
1. A protokoll alkalmazási/érvényességi területe
1.1. A protokoll témájának pontos meghatározása
A reumatológiai betegségek okozta fájdalomban is biztonságosan alkalmazható a tumoros fájdalomcsillapításban már általánosan használt "WHO analgetikus létra" a fájdalomcsillapítás fokozatos és biztonságos felépítésére. Az esetek többségében elegendő az I. lépcsőszereinekalkalmazása. A terápiás ajánlást egyénre szabottan kell megadni. Heveny - és feltehetőleg rövid ideig tartó - fájdalom esetén akár maximális napi dózisú NSAID is alkalmazható. Az I. lépcső szereire nem reagáló esetekben vagy akkor, ha a fájdalom erőssége azt megkívánja: - pl. discus hernia, postlaminectomiás fájdalom egyértelmű klinikai képe esetén bátran lehet a II. csoport szereihez nyúlni. Amennyiben az analgetikus létra 2 fokán alkalmazandó gyenge opioid, az NSAID és a szükség esetén adagolandó adjuváns szerek kombinációja nem nyújt kielégítő analgetikus hatást, az erős opioidok alkalmazása ma már teljes mértékben elfogadott. Nem elfogadható, hogy a beteg gyenge opioid és/vagy középerős NSAID mellett szenvedjen! Az addikciótól való félelem az ellenőrzött, megfelelően vezetett kezelés mellett indokolatlan. (4,5)
Az erős hatású szerek alkalmazása a mozgásszervi megbetegedések csillapításában közel 15 éves múltra tekint vissza. Krónikus, nem daganatos megbetegedés okozta fájdalom esetében alacsonyabb adagokelegendők, azaz a szükséges gyógyszermennyiség stabil szinten tartható, szinte soha nincs szükség a dózis emelésére. A gyakorlat azt mutatja, hogy bizonyos elváltozások (pl. csípőprotesis beültetése) műtéti megoldása után az opioidra nincs többé szükség. A járóbeteg-szakellátásban különösen kedvező a transzdermális alkalmazás (a parenterális adás inkább a kórházi gyakorlat). (6,7,8,9,10,11,12,13)
Ezen erős hatású szerek nem tumoros, mozgásszervi indikációban történő alkalmazását állásfoglalásokban, szakmai ajánlásokban tették közé, melyek manapság általánosan elfogadottak a nemzetközi gyakorlatban. (I.a. bizonyíték)
A hagyományos fájdalomcsillapítók közül a paracetamol ajánlott első helyen. Az aminophenazon, metamizol és phenacetin toxicitása miatt tartós alkalmazásra nem ajánlott.
A tramadol centrálisan ható gyenge opioid, egyúttal gátolja a noradrenalin és szerotonin újrafelvételét.
1.2. A protokoll célja
Konkrét terápiás iránymutatás a reumatológiai eredetű fájdalmak kezelését végző szakorvosok (reumatológusok és társszakmák szakorvosai, ide értve a családorvosokat) számára
1.3. A protokoll célcsoportjai
Elsősorban a reumatológus szakorvosok, továbbá ortopéd-traumatológus, neurológus, idegsebész, pszichiáter, belgyógyász, gyermekgyógyász, onkológus szakorvosok, a reumatológiai eredetű fájdalommal szembesülő nem-orvos munkatársak, úgymint gyógytornász-fizioterapeuták, pszichológusok, szakdolgozókés azon civil segítők, akik tevékenységéhez a gyógyszeres fájdalomcsillapítás és gyulladáscsökkentés területén tájékozottság szükséges.
2. Definíciók, rövidítések
2.1.A reumatológiai eredetű fájdalom
A reumatológiai eredetű fájdalom patológiai típusait tekintve nociceptív, neuropathiás illetve e kettős mechanizmus együttese lehet.
A gyulladásos fájdalom elsősorban nociceptív, jól definiálható mediátorok és fájdalom-keltő mechanizmusok részvételével keletkezik. A neurogén és pszichoszociális tényezők elsősorban a krónikussá válásban játszanakszerepet (1,2).
A nem-gyulladásos okból keletkező regionális és diffúz mozgásszervi fájdalmak keletkezésében több a neuropathiás elem, azonban ezek megélésében, tartósságában igen nagy szerephez jut a pszichoszociális helyzet és környezet (származás, képzettség, fizikai megterhelés, ko-morbiditás) (3). A kiterjedt mozgásszervi fájdalom megélt súlyossága és gyakorisága Kelet-Európában különösen magas (4).
A gyógyszeres fájdalomcsillapítás és gyulladáscsökkentés legfőbb terápiás csoportjai:
1.) Hagyományos és kábító-fájdalomcsillapítók (csak fájdalomcsillapítás)
2.) Nem-szteroid gyulladáscsökkentők (NSAID) (fájdalom- és gyulladáscsökkentés)
3.) Glukokortikoidok (gyulladáscsökkentés)
4.) Neurológia-pszichiátriai határterület gyógyszerei (reumatológiai indikációjú regisztrációjukjelenleg nincs)
2.2.Hagyományos és kábító-fájdalomcsillapítók
A nem szteroid gyulladáscsökkentők klinikai alkalmazása jellemzően empirikusan indult meg. A hatásmechanizmus feltárása a következőket bizonyította.
A gyulladás exsudatív tüneteiért a prosztaglandinok (elsősorban PGE2) felelősek. A prosztaglandinok lipid-fragmentumok, melyek a termelő sejtben és annak mikrokörnyezetében hatnak. Élettani szerepük a célsejt aktiválásában van. A sejtmembránokhoz integrált enzim-kaszkád alakítja ki aktív szerkezetüket. Hatásukat az egyes célszervekben fejtik ki, annak függvényében, hogy az enzimrendszer ott jelen van-e. Kis mennyiségben állandóan termelődve a szervek homeosztázisát bizonyítják (gyomor-bélnyálkahártya, vérlemezke, vese, simaizomzat). A gyulladáscsökkentő szerep az ősi védekezés része.
A folyamat kulcs-enzime a ciklooxigenáz. Kitűnt, hogy szöveti sérülés esetén igen nagy mennyiségben keletkeznek prosztaglandinok. A PGE2 nemcsaka helyi gyulladásos érjelenségekben, hanem a fájdalomérzés perifériás és centrális szenzitizációjában is szerepet játszik.
A nagy mennyiségű PGE2 a ciklooxigenáz (COX) enzim megnövekedett mennyiségének eredménye. Kitűnt, hogy a COX enzimnek két formája van. A COX 1 konstitutív, a homeosztatikus PG termelést végzi, míg a COX-2 indukálható. A kötőszöveti és idegsejtekben szöveti sérülésre, citokinek jeladására expresszálódik. A COX 1 és a COX-enzimek térszerkezete fontos funkcionális helyeken eltér. Ezért ugyanazon molekula egészen más farmakokinetikai paraméterekkel gátolja a két enzimet.
A hagyományos NSAID-ok sorba rendezhetők biokémiai COX-1 és COX-2 specifitásuk alapján. Egyes hagyományos NSAID-okról kiderült, hogy viszonylag szelektív COX-2 gátlók. A gyógyszermolekula-tervezés lehetővé tette új, magasan specikus COX-2 gátlók kifejlesztését.
A klinikai biztonság oldaláról a NSAID-oknaka COX-mechanizmustól függő és COX független mellékhatásai lehetnek. Előbbire a gyomornyálkahártyasérülés, vérzés, hipertónia, ödéma, szív- érrendszeri obstruktív jelenségek utóbbira a hepatikus mellékhatások szolgálhatnak pédát.
A klinikai biztonság nem esik egybe COX-2 specifitással még a gyomor-bél mellékhatások esetében sem. Ezért a COX-gátlók biztonságosságát több mellékhatást illetően egyedileg kell súlyozni.
A "preferenciális", "szelektív", "specifikus" jelzőknek nincs különösebb jelentősége, azt fejezik ki, hogy egy vegyület a terápiás dózistartományban az egyikenzimet erősebben gátolja. A "coxib" elnevezés csupán molekulacsoportot jelöl.
A nem-szteroid gyulladáscsökkentők hatáserőssége eltérő ugyan, de dózisfüggő, így a klinikailag optimális dózistartományban gyulladáscsökkentő hatásuk lényegében azonosnak tekinthető. Ezért a nem-szteroid gyulladáscsökkentők reumatológiai szakmai értékének fő szempontja a biztonságosság, azaz az összességében kedvező mellékhatás-profil és kockázat/haszon (risk-benefit) arány. Ezt a reumatológiai betegségen belüli kockázati csoportok (gyulladásos betegség, tartós szedés, nagyobb adag igénye - akut fájdalmi szindrómák, rövid időtartamú kezelés, alacsonyabb adagok) illetve társuló kockázati tényezők (gyomor-bélrendszeri, véralvadási, szív-érrendszeri, stb.) által jellemzett csoportok szerint kell meghatározni és az egyedi terápiás döntéseket is ezek figyelembevételével kell meghozni.
A gyógyszercsoport legfőbb kockázata a gyomor-bélrendszeri fekély és vérzés kialakulása. Az egyéb, ritkább és kevésbé súlyos mellékhatások mellett (vízretenció, májlézió, stb.) új, következményeiben jelentős nem kívánatos hatásként jelent meg a cardiovascularis kockázat (thrombotikus események, köztük myocardialis infarktus).
Ezért újra kell értékelni valamennyi NSAID lehetséges toxikus hatásait és a risk/benefit viszonyokat. Úgy tűnik, hogy a dózisfüggő, magasan specifikus COX-2 enzimgátlás - mint mechanizmus - egyes cardiovascularis kockázati csoportokban növeli a thrombotikus események kockázatát. Ennek fényében az egyes nemzeti hatóságok figyelemmel kísérik a NSAID-ok alkalmazását és módosítják alkalmazási előirataikat. (15,16,17,18,19,20,21,22,23,24)
A nem-szteroid gyulladáscsökkentőket biztonság tekintetében az alábbi kategóriákba kell beosztani:
1. Gyomor-bélrendszeri tekintetben biztonságos, kardiológiai kockázat nem jelentős
2. Gyomor-bélrendszeri tekintetben biztonságos, kardiovaszkuláris kockázat lehetséges
3. Gyomor-bélrendszeri tekintetben kockázatos, egyébként átlagosan biztonságos
A fő kockázati betegcsoportokat az alábbiak szerint kell meghatározni:
1. Átlagos kockázat (nincs jelentős társult betegség vagy rizikó)
2. Magas gyomor-bélrendszeri kockázat (gyulladásos rendszerbetegség, ulcus vagy vérzés, vérzékenység, időskor, steroid szedés)
3. Magas szív-érrendszeri kockázat (infarktus, stroke, kezeletlen magas vérnyomás, hiperlipémia,diabetes,érbetegség, dohányzás)
4. Magas gyomor-bélrendszeri és szív-érrendszeri kockázat együttesen A javasolt NSAID alkalmazás ezért a következő:
1. Átlagos kockázat kockázat esetén hagyományos NSAID is adható, gyomorvédelem sem szükséges.
2. Magas gyomor-bélrendszeri kockázat esetén COX-2 szelektív szer vagy hagyományos NSAID és protonpumpa gátló gyomorvédő szer (PPI) adandó. A gyomorvédelem nem csökkenti az alsó gyomor-béltraktusban fellépő NSAID kockázatot.
3. Magas szív-érrendszeri kockázat esetén hagyományos NSAID és acetilszalicilsav (ASA) adandó. A protonpumpagátló adása csökkenti az ily módon keletkező gyomor-bélrendszeri kockázatot.
4. Magas gyomor-bélrendszeri és szív-érrendszeri kockázat esetén hagyományos NSAID+ASA+PPI adandó. A sima ASA kevésbé kockázatos az alsó gyomorbéltraktusra, mint a retard készítmény. COX-2+ASA+PPI kombináció is adható (különösen alsó gyomor-béltraktus-rizikó esetén).
Figyelembe kell venni, hogy a Helicobacter pylori infekció a NSAID-tól függetlenül növeli a fekélykeletkezés és -vérzés rizikóját, ezért eradikálni kell. A dyspepsiás panaszokat PPI-vel kell kezelni, tartós fennállás esetén endoscopia szükséges.
Idült ízületi gyulladásos betegségekben a nem szteroid gyulladáscsökkentő gyógyszerek alkalmazásának célja a fájdalom és duzzanat tüneti csökkentése. A progresszív anatómiai károsodás kivédésére nem alkalmasak.
A gyógyszer kiválasztásának legfőbb szempontjai:
1. a biztonság,
2. a hatásosság,
3. a hatás tartama,
4. a beteg életkora,
5. a beteg választása,
6. a szóba jövő hasonló gyógyszerekés az ára
2.3. Nem-szteroid gyulladáscsökkentők
A nem-szteroid gyulladáscsökkentők egyúttal fájdalomcsillapítóként is hatnak (l. a bizonyíték). A reumatológiai alkalmazás jelenlegi legelfogadottabb szabályait az Amerikai Reumatológiai Kollégium Fehér Könyve foglalja össze
(14).
A gyulladásgátlás és a gyulladásos fájdalom csillapításának leghatékonyabb eszközei a corticosteroidok, amelyek többféle mechanizmussal hatnak. RA-ban tartós alkalmazásuk mellékhatásaik és az újabb hatékony bázisterápiás szerek alkalmazása miatt visszaszorult annak ellenére, hogy több vizsgálat igazolta a szteroid kezelteken az ízületi destrukciók kialakulásának lelassulását (I.a. bizonyíték)
2.4.Glukokotikoidok
Idült ízületi gyulladásos betegségekben tartós alacsony adagú peros kezelés (5-7,5 mg prednisolon ekvivalens/nap alatt) alkalmazható. Célja a betegség aktivitásának minimalizálása, amíg a DMARD hatása megmutatkozik. Elfogadható célkitűzés a betegség aktivitásának csökkentése egy korlátozott időszakra (fellobbanás vagy speciális élethelyzet időtartamára is). Alkalmazható a nem szteroidok vagy DMARD-próbálkozások mellett is aktív betegség egyensúlyba hozására (pl. elfogadhatatlanul rossz betegségérzet vagy mozgásbeszűkülés esetén). Figyelembe kell venni, hogy az ízületi károsodás fokozódhat a tüneti javulás mellett. A kezdő és a fenntartó dózis megválasztása az egyénre szabottan történjék (általában magas kezdő és 4-6 mg metilprednisolon ekvivalens fenntartó adag). Az aktív synovitis okozta panaszok és tünetek csökkenése és a funkció javulása jelzi. A toxicitás monitorizálása céljából az ismert mellékhatások szerinti fizikális és laboratóriumi vizsgálatokat kell rendszeresen elvégezni. Különös figyelemmel kell követni a szteroid-indukálta oszteoporózis alakulását. Intézeti körülmények között 40-250 mg metilprednisolon tartalmú infúzió adható. Az ismételt 1000 mg metilprednisolon tartalmú pulzus infúzióka reumatológiai gyakorlatban csak kivételes esetekben, gondos megfigyelés mellett jöhetnek szóba.
A corticosteroidok lokális alkalmazása indokolt monarthritisben,ahol intra-articularisan adva, s néhány hónapon belül legfeljebb háromszor megismételve a gyulladásos folyamatot hatékonyan gátolják.
A lokális injekciók fő célja sokízületi gyulladásokban a legaktívabb ízület kezelése a betegség korai szakaszában. A betegség zajlása során egy vagy néhány ízület aktív gyulladásának kezelésére a gyulladás miatti mozgáskorlátozottság megszüntetésére alkalmazandók. A lokális kezelés a rendszerbetegségben csak időleges eredményt ad - a betegséget általánosan is kezelni kell. Nagyobb és tartós hatás elérésére tartós hatású készítményre van szükség. A mennyiség és koncentráció a kezelendő ízület méretéhez illő legyen. A hatásosság a synovitis mérséklődése, a mozgáskorlátozottság javulása útján mérhető le. A tartós hatású készítmény szövődménye a bőratrófia és porckárosodás lehet.
Az intraartikulárisan adható készítmények hazánkban a következők: betamethason, metilprednisolon, triamcinolon és hidrocortison .
Az alábbiakban a szakmai ajánlásokat ismertetjük egyes betegségek, illetve betegségcsoportok alapján.
Az Európai Reumatológiai Szövetség (EULAR) irányelvben foglalta össze a szisztémás glukokortikoid kezelés elfogadott szakmai szabályait (15). Az ajánlások és a legfontosabb monitorizálási területek a következők:
- A glukokortikoid kezelés megkezdése előtt mérlegelni kell a várható mellékhatásokat és ezeket a beteggel ismertetni kell, el kell látni betegkártyával
- A kezdő, fenntartó és tartós adagolást a reumatológiai alapbetegség, aktivitása, kockázata a circadián ritmusra gyakorolt hatás és a válaszkészség szabja meg
- A fennálló egyéb betegségeket ismerni és kezelni kell (hipertónia, diabetes, szürke- vagy zöldhályog, infekció, NSAID szedés)
- Törekedni kell az állapot indokolta legalacsonyabb adagra
- A beteg testsúlyát, vérnyomását, lipid, vér- és vizelet cukor értékeit, szemnyomását, ödéma készségét és szív-teljesítményét követni kell
- Három hónapnál hosszabb és napi 7.5 mg prednisolon-ekvivalensnél nagyobb adagok mellett kalcium, D-vitamin, rizikótényezőktől függően biszfoszfonát kezelés szükséges
- NSAID-dal együtt adva gasztroprotekció vagy COX-2 gátló NSAID választása szükséges
- Műtét esetén megfelelő hormonpótlás szükséges
- Terhesség alatt további kockázat nélkül adható
- Glukokortikoiddal kezelt gyermekek növekedését figyelni kell, szükség esetén növekedési hormon adása indokolt.
II. Diagnózis - III. Terápia
A leggyakoribb reumatológiai betegségeket a Betegségek Nemzetközi Osztályozása (BNO-10) szerint soroljuk fel, a diagnózis részleteit itt nem tárgyaljuk
1. Infektív kórképek
A kórokozókáltal kiváltott mozgásszervi kórképekben (M0010-M0130 bakteriális arthritisek, M0160-M0180 gomba és parazita okozta arthritisek, M4620- M4690 az infektív spondylitis, valamint az izmok, ínak és nyáktömlők fertőzéses betegségei. A betegség oki terápiája mellett különböző kiegészítő kezelések mellett alkalmazunkgyulladáscsökkentő, illetve fájdalomcsillapító hatású gyógyszereket is. E kórképek kezelésének - a Mycobacterium okozta kórképek kivételével - nemzetközileg is elfogadott terápiás ajánlása nincs, ezért a kiegészítő gyógyszeres kezelés a klinikai gyakorlati tapasztalatokon alapul. A fájdalomcsillapításra nem gyógyszeres módszerek, pl. nyugalomba helyezés, az ízületi folyadék leszívása, lokális hideg alkalmazása segítségével is sor kerülhet. Fájdalomcsillapítóként legfeljebb napi 4 gramm paracetamolt tartalmazó analgeticumot, ennek hatástalansága esetén tramadolt tartalmazó fájdalomcsillapítót adunk.
A vírus okozta kórképekben (M0140-M0150 vírusarthritisek) a Magyarországon előforduló kórképekben az oki terápia alkalmazására gyakran sor sem kerül, mivel az ízületi gyulladás az esetleges etiológiai diagnózis előtt spontán megszűnik. Ilyen esetekben a fájdalomcsillapítás és gyulladáscsökkentés nem gyógyszeres módszerei mellett tüneti kezelésként gyógyszeres kezelést (acetaminophen, nem szteroid gyulladásgátló) is alkalmazunk.
2. Gyulladásos ízületi és gerincbetegségek
Ide tartozó kórképeka M0200-M0290 reaktívarthritisek, M0500-M0690 rheumatoid arthritis (RA) és rokon betegségek, M0700-M0730 arthritis psoriatica (PsA), M0800-M0980 fiatalkori ízületi gyulladások, M45H0-M4620 spondylitis ankylopoetica). Krónikus lefolyásuk során - változó intenzitással - gyulladásos jelenségekkel és fájdalommal járnak.
A kristály-indukálta ízületi gyulladások - prototípusa a köszvény - főleg rohamokban jelentkező, fulmináns exsudatív gyulladásokban, ritkábban krónikus tárolási betegség formájában lépnek fel (M 1000-M 1190).
Az RA, szeronegatív arthritisek (PsA, SpA),és a fiatalkori ízületi gyulladások betegségmódosító és biológiai kezelésére hazai protokollokállnak rendelkezésre. A kezelés alapelve a nem gyógyszeres és gyógyszeres beavatkozások-a beteg állapotának megfelelően hierarchikusan rendezett - komplex alkalmazása. A gyógyszeres kezelésben a betegségmódosító és a biológiai választ módosító készítmények mellett kiegészítő kezelésként NSAID készítményeket alkalmazunk.
Hasonló a helyzet PsA-ban. A spondylitis ankylopoetica tüneti kezelésére nemzetközileg elfogadott ajánlások vannak, de hagyományos betegségmódosító készítménnyel nem rendelkezünk. A tüneti kezelés hatékony eszköze az NSAID-ek alkalmazása. Nem tisztázott, hogy a tartós NSAID kezelés vagy csak az akut periódusokra korlátozódó kezelés eredményessége között van-e különbség.
Az akut köszvényes roham kezelésére az Európai Reumatológiai Szövetség irányelvei a következőket ajánlják (26):
Perorális colchicin és vagy NSAID javasolt, az ízületi folyadékgyülem leszívása és az ízületbe adott glukokortikoid mellett (I.b. bizonyítékok).
3. Autoimmun betegségek
Ide sorolható betegségek (M3000-polyarteritis nodosa, Kawasaki-, Wegener-,Takayasu-kór, polymyalgia rheumatica, vasculitisek, systemás lupus erythematodes, dermatomyositis, polymyositis, progressiv systemás sclerosis, Sjögren-szindróma, Weber-Christian-kór, többszörös kötőszöveti betegség vagy MCTD = multiple connective tissue disease) több szervrendszert érintenek. A terápia célja az autoimmun gyulladás okozta tünetek megszüntetése kis dózisú, illetve nagy adagú vagy pulzus terápiában alkalmazott corticosteroid, citosztatikus és immunszuppressiv gyógyszerekkel. Amennyiben a betegség csak az ízületeket érinti, s más szervi manifesztáció nincs és a szerológiai aktivitás csekély, akkor van helye, tüneti kezelésként a NSAID készítményeknek. Az esetleges szervi szövődmények miatt a betegek fokozott ellenőrzést igényelnek.
4. Degeneratív ízületi és gerincbetegségek
Az ebbe a csoportba sorolt betegségek (M1500-M1990 arthrosis, M4710-M4890, ill. M5000-M5490 spondylosis) okozta fájdalom kezelésére első lépésben a nem gyógyszeres kezelés eszközeit (nyugalomba helyezés, fizioterápiás eljárások, segédeszköz használata, életmód változtatás) alkalmazzuk a 2 EULAR terápiás ajánlásai szerint (27,28,29). (I.a. bizonyítékok)
A gyógyszeres kezelés során a felületes ízületek esetén az elsőként választandó fájdalomcsillapító szer a capsaicin tartalmú lokálisan alkalmazható kenőcs, vagy NSAID tartalmú kenőcsök.
A lokális készítmények a bőrön át felszívódnak s nemcsak a bőr alatti kötőszövetben, hanem a térdízületben - a meniscusban és a porcban is - terápiásan hatékony koncentrációt érnekel, ugyanakkor a szérum koncentráció az orális adagolásnál elért szint legfeljebb 5 %-a. Ezáltal a mellékhatások gyakorisága az orális adagolásnál észlelt gyakoriság felére, a súlyos mellékhatásoké egyötödére csökkent. Kísérleti körülmények közt a ketoprofen és a diclofenac tartalmú készítmények felszívódása volt a leghatékonyabb.
A 4 illetve 12 hetes vizsgálatban a diclofenac gél a térdarthrosis okozta nyugalmi és terhelési fájdalmat, ízületi merevséget csökkentésében és a beteg fizikai teljesítőképességének javításában hatékonyabb volt, mint a placebo (30,31,32,33).
Amennyiben lokális kezeléssel a fájdalmat nem tudjuk csillapítani a következő választandó szer a paracetamol. A gyulladásos és nem gyulladásos ízületi fájdalom csillapítására használt paracetamolt a betegek 37%-a találta hatékonynak és megfelelőnek, a másodikként választandó nem szteroid gyulladáscsökkentőkkel összehasonlítva a betegek 38%-a hasonlónak vagy jobbnak ítélte a paracetamolt.
Az akut és krónikus derékfájás csillapításának nemzetközi ajánlások alapján javasolt gyógyszerei szintén a paracetamol, NSAID-ok, izomrelaxáns és szükség szerint opioid kiegészítéssel . A felsoroltak kombinálhatók (I.a. bizonyítékok) (34,35,36). A fájdalomcsillapítás alatt fokozott figyelemmel kell kísérni a neurológiai status alakulást!
5. Lágyrészbetegségek
A lágyrészek megbetegedéseiben (M6000-M6380 izombetegségek, M6500-M6880 ill. M 7600- M7790 ínbetegségek, M7000-M7550 a bursák betegségei) a fájdalom csillapítását a nem gyógyszeres eszközökkel kezdjük (nyugalomba helyezés, lokális fizioterápiás beavatkozások). Amennyiben hatástalanok, a betegnek fájdalomcsillapítót (acetaminophen vagy NSAID) adunk. A lágyrész-elváltozások okozta panaszok kezelésében az orálisan alkalmazott NSAID-ek hatékonyságát nem tudták igazolni, viszont a lokálisan alkalmazott NSAID a placebo kezelésnél hatékonyabb.
Speciális, reumatológiai-pszichiátriai határterületi kórkép a fibromyalgia, amely a fájdalomfeldolgozás zavara. Jellemzője a gyakori pszichiátriai illetve vegetatív ko-morbiditás (irritabilis colon, - hólyag, pánikbetegség, depressziós tünetek). Az EULAR irányelvei részletezik a nem-gyógyszeres terápia számos lehetőségét (multidiszciplináris megközelítés). A gyógyszeres kezelés fő pillérei: tramadol (Il.b. bizonyíték), egyszerű fájdalomcsillapítók, pl. paracetamol (IV. bizonyíték). Az antidepresszánsok (I.b. bizonyíték) és innovatív analgetikumok hazánkban jelenleg tiszta, szövődménymentes fibromyalgia indikációban nincsenek regisztrálva (37).
6. A protokoll bevezetésének feltételei
A tárgyi és személyi feltételek a reumatológiai ellátásban adottak. Az aneszteziológiai-intenzív terápiás szakterületen (fájdalom-klinikák) a tárgyi és személyi feltételek adottak, az invazív fájdalomcsillapítás vonatkozásában is. A fájdalmat okozó alapbetegség, a fő kiváltó ok feltárása és az invazív beavatkozások indikálásában a két szakma együttműködése, kölcsönös konzultáció formájában ajánlott és szükséges.
IV. Rehabilitáció
A gyógyszeres beavatkozás mellett a korai rehabilitáció és a fizikális gyógymódok alkalmazása elengedhetetlen.
V. Gondozás
A követés és gondozás alapvetően szükséges, elsősorban az akut fájdalom krónikussá válásának megelőzése céljából.
VI. Irodalomjegyzék
1. McDougall JJ: Neurogenic origin of joint pain. Arthritis Research&Therapy 8:220. 2006.
2. Backman CL: Psychosocial aspects in the management of arthritis pain. Arthritis Research&Therapy 8:221. 2006.
3. Macfarlane GJ, Norrie G, Atherton K et al: The influence of socio-economic status on the reporting of regional and widespread musculoskeletal pain: results from the 1958 British Birth Cohort Study. Ann Rheum Dis publ.online doi:10.1136/ard.2008.093088
4. Macfarlane GJ, Pye SR, Finn JD et al: Investigating the determinants of international differences in the prevalence of chronic widespread pain: evidence from the European Male Ageing Study (EMAS). Ann Rheum Dis publ.online doi:10.1136/ard.2008.089417
5. Dertwinkel R, Zenz M, Strumpf M, Donner B: Clinical Status of Opioid Tolerance in Long Term Therapy of Chronic Noncancer Pain In.:Progr Pain Res and Management, 14:129-141,1999
6. Katz WA: Use of nonopioid analgesics and adjunctive agents in the management of pain in rheumatic diseases. Curr Opin Rheumatol 14:63-71,2002
7. Libretto SE: Use of Transdermal Fentanyl in Patients with Continuous non-malignant pain. Clin Drug Invest 22, 473-483, 2002.
8. KatzW.A.: Pain management in rheumatic disease Curr Opin Rheumatol, 14:43-44,2002.
9. Roth S.H., Fleishmann R.M., Burch F.X., Dietz F., Bockow B., Rapaport R.J., Rutstein J., Lacouture P.G.:Around-the-Clock, controlled-release oxycodone therapy for osteoarthritis-related pain Arch Intern Med: 160:853-860,2000
10. Brevik H. : Opioids in cancer and chronic non-cancer pain therapy indications and controversies Acta Anaesthesiologica Scand. 45:1059-1066, 2001
11. Grilo R. M., Bertin P., Scottodi FazanoC.,Coyral D., Bonnet C., Vergne P. and Treves R.: Opioid rotation in the treatment of joint pain. A review of 67 cases. Joint Bone Spine 69: 495-497, 2002
12. Jage J.: Opioid tolerancie and dependencie- do they matter, Eur J of Pain 10.1016/j.ejpain.2004.11.009
13. Choquette D., McCarthy T., Rodrigues J., Kelly A., Hussein-Bhabba F.: Evaluation of Transdermal Fentanyl (TDF as a treatment option "for pain" in patients with osteoarthritis (OA)- Rheumatology Institute of Montreal J of Pain.5: Suppl.1.568, 2004.
14. Recommendations for use of selective and nonselective nonsteroidal antiinflammatory drugs: an American College of Rheumatology White Paper. Arthritis&Rheum 59:1058-1073. 2008.
15. Vane JR: Inhibition of prostaglandin biosynthesis as a mechanicsm of action of aspirin-like drugs. Nat New Biol 231: 232-235.1971.
16. van Tulder MW et al: Non steroidal anti-inflammatory drugs for low back pain. In: The Cochrane Library, Oxford, 2002, Issue 2
17. Garcia Rodriguez LA et al. Risk of hospitalization for upper gastrointestinal tract bleeding associated with ketorolac, other nonsteroidal anti-inflammatory drugs, calcium antagonists, and other antihypertensive drugs. Archives of Internal Medicine 158: 33-39. 1998.
18. Singh G, Ramey DR, Morfeld D et al: Gastrointestinal tract complications of nonsteroidal anti-inflammatory drug treatment in rheumatoid arthritis. A prospective observational cohort study. Arch Intern Med, 156:1530-1536.1996.
19. Griffin MR, Yared A, Ray WA: Nonsteroidal antiinflammatory drugs and acute renal failure in elderly persons. American Journal of Epidemiology 151: 488-496. 2000.
20. Heerdink ER et al: NSAIDs associated with increased risk of congestive heart failure in elderly patients taking diuretics. Arch Int Med 158:1108-1112.1998.
21. Blower AL, Brooks A, Fenn CG et al: Emergency admissions for upper gastrointestinal disease and their relation to NSAID use. Aliment Pharmacol Ther 11: 283-291.1997.
22. Porter J. : Addiction rare in patients treated with narcotics of NEJM 302:123,1988
23. Bolten WW: Problem of the atherothrombotic potential of non-steroidal anti-inflammatory drugs Ann Rheum Dis 65: 7-13 2006.
24. Boda A, Géher P: Infekciózus arthritisek in : Reumatológia szerk. Gömör B., Bálint G, Medicina, Budapest, 1989.
25. Hoes JN, Jacobs JWG, Boers M et al: EULAR evidence-based recommendations on the management of systemic glucocorticoid therapy in rheumatic diseases. Ann Rheum Dis 66:1560-1567.2007.
26. Zhang W, Doherty M, Bardin Tet al: EULAR evidence-based recommendations for gout. Part II: Management. Report of a task force of the EULAR Standing Committe For International Clinical Studies Including Therapeutics (ESCISIT). Ann Rheum Dis 65:1312-1324. 2006.
27. EULAR Recommendations 2003: an evidence based approach to the management of knee osteoarthritis: Report of a Task Force of the Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT). Ann Rheum Dis 62: 1145-1155. 2003.
28. Zhang W, Doherty M, Arden N et al: EULAR evidence based recommendations for the management of hip osteoarthritis: report of a task force of the EULAR Standing Committe for International Clinical Studies Including Therapeutics (ESCISIT). Ann Rheum Dis 64: 669-681. 2004.
29. Zhang W, Doherty M, Leeb BF et al: EULAR evidence-based recommendations for the management of hand osteoarthritis: Report of a task force of the EULAR Standing Committe For International Clinical Studies Including Therapeutics (ESCISIT). Ann Rheum Dis 66: 377-388. 2007.
30. Moore RA, Tramer MR, Carroll D et al: Quantitative systematic review of topically applied non-steroidal anti-inflammatory drugs. BMJ 316: 333-338.1998.
31. Tugwell PS et al: Equivalence study of a topical diclofenac solution (Pennsaid) compared with oral diclofenac in the symptomatic treatment of osteoarthritis of the knee: a randomized controlled study. Journal of Rheumatology 31: 2002-2012. 2004.
32. Roth SH, Shainhouse JZ: Efficacy and safety of a topical diclofenac solution (Pennsaid) in the treatment of primary osteoarthritis of the knee. Archives of Internal Medicine 164: 2017-2023. 2004.
33. Bookman AA et al. Effect of a topical diclofenac solution for relieving symptoms of primary osteoarthritis of the knee: a randomized controlled study. Canadian Medical Association Journal 171:333-338. 2004.
34. Koes BW, van TulderMW, Thomas S: Diagnosis and treatment of low back pain. BMJ 332:1430-1434. 2006.
35. Chou R, Huffman LH: Medications for acute and chronic low back pain: a review of the evidence for an American Pain Society/American College of Physicians Clinical Practice Guideline. Ann Intern Med 147:505-514. 2007.
36. Chou R, Qaseem A, Snow Vet al: Diagnosis and treatment of low back pain: a joint clinical practice guideline from the American College of Physicians and the American Pain Society. Ann Intern Med 147:478-491. 2007.
37. Carville SF, Arendt-Nielsen S, Bliddal H et al: EULAR evidence-based recommendations for the management of fibromyalgia syndrome
Kapcsolódó internetes oldalak
A szakmai protokoll érvényessége: 2012. június 30.
VII. Melléklet
1. A protokoll fejlesztés módszerei
1.1. Az irodalomkeresés módszerei
A releváns szakmai irodalomban az irányelvek és metaanalízisek keresése
1.2. Nemzetközi irányelvek adaptálásának módszerei
A Reumatológiai és Fizioterápiás Szakmai Kollégium nemzetközi irányelv fordítását, hazai adaptálását és közlését folyamatosan végzi. A jelen protokoll ezekből közöl, illetve hivatkozik.
1.3.Az érintett társszakmákkal való véleményezés
Az irányelvekés protokollok fejlesztéséről szóló jogszabály szerint.
1.4.A bizonyítékok szintjei
| Bizonyíték szint | Vizsgálat típusa |
| Ia | RCT metaanalízis vagy >1 azonos eredményű RCT |
| Ib | RCT |
| I Ia | Kontrollált, de nem randomizált vizsgálat |
| I Ib | Quasi-experimentalis vizsgálat |
| III | Nem experimentális, leíró, összehasonlító és esetkontrollos tanulmányok |
| IV | Tanácsadó testületi vélemények és/vagy hatósági vélemények |
2. Az ajánlás alkalmazását támogató segédanyagok, betegtájékoztatók
- A Magyar Reumatológia Haladásáért Alapítvány és a Spring Med Kiadó reumatológiai betegfelvilágosító kiadványsorozata.
- Szekanecz Zoltán: Reumatológiai gyógyszeres terápia Medicina Könyvkiadó Zrt. Budapest, 2009.
3. A protokollfejlesztést támogató szervezetek, szponzorok
- Reumatológiai és Fizioterápiás Szakmai Kollégium
- Magyar Reumatológusok Egyesülete
- Reumatológiai Egyetemi Tanszékek
- A Magyar Reumatológia Haladásáért Alapítvány
Az Egészségügyi Minisztérium
szakmai protokollja
A jó- és rosszindulatú strumák sebészi kezeléséről
(1. módosított változat)
Készítette: a Sebészeti Szakmai Kollégium
I. Alapvető megfontolások
1. Definíció
A struma a pajzsmirigy megnagyobbodása. A hormontermelést tekintve egy struma lehet euthyreotikus, hypofunctiós és hyperfunctiós (más néven toxikus). A mirigy rosszindulatú daganatainakösszefoglaló neve: malignus struma. A strumákat nagyságuk szerint fizikális vizsgálat alapján a WHO és az UNICEF az alábbiakban klasszifikálja:
0. okozat: nem tapintható, nem látható golyva.
1. fokozat: normál nyaki pozícióban, nyeléskor pajzsmirigy megnagyobbodás tapintható, de nem látható.
2. fokozat: ugyanebben a pozícióban a megnagyobbodott pajzsmirigy nyeléskor látható is, tapintható is.
2. Etiológia
2.1. Normofunkciós strumák Diffúz struma:
Megnövekedett pajzsmirigyhormon-igény pubertas korban és terhesség alatt, fiziológiás körülmények között is létrehozhat pajzsmirigy megnagyobbodást. Golyvaendémiás vidékeken a tartós jódhiány következményeként alakul ki nagy számban. (Magyarország négyötöde mérsékelten jódhiányos terület).
Kompenzatorikus pajzsmirigy hypertrophia jön létre, ha
- congenitális enzimdefektus akadályozza a normális thyroxinszintézist
- strumigen anyagok befolyásolják a hormonprodukciót (pl. thiokarbamid blokkolja a jódbeépülést, perchlorat és thiocyanat gátolja a jódkoncentrációt)
- autosomalis recessiv génkárosodás öröklődik (dyshormonogenetikus golyva) Multinodularis struma:
A jódhiány következtében jelentkező diffúz strúmák kb. 40 éves kortól göbösödésre hajlamosak, de a kor előrehaladtával jódhiánytól függetlenül is jellemző a göbképződés. A göbök egy része kolloidos degeneratio, cystosus,fibrotikus, esetleg kalcifikált részekkel, ezekalulműködőek. A jódhiány azonban, mint epigenetikus tényező a TSH receptor aktiváló mutációinakis kedvez, ezek során hyperfunctiós (izotóppal "meleg vagy forró") göbök alakulnak ki. Miután ezek autonóm működő follicularis adenomák, unifokális vagy multifokális autonómia a legpontosabb definíció, melléhelyezve a pajzsmirigyfunctió meghatározását (euthyreosis, latens vagy klinikai hyperthyreosis). A korábban használatos kifejezések (toxikus golyva vagy toxikus göb, kompenzált autonóm adenoma vagy dekompenzált autonóm adenoma kevésbé pontosak).
Uninodularis struma:
A göb lehet cystikus vagy szolid, hyperfunctiós vagy hypofunctiós. Jódhiányos területen a göbök malignitási aránya összességében (uni- és multinodularis golyvákban) 1 %. Normofunctiós vagy hyperfunctiós göb malignizálódása ritka. Uninodularis szolid, "hideg" göbök esetén azonban a malignitási arány 2-6 % is lehet.
Recidiv struma:
Kialakulásában szerepet játszhat az eredeti kórfolyamat progressziója vagy a pajzsmirigyműtétet követő relatív hormonhiányra visszavezethető fokozott TSH-produkció.
2.2. Hyperfunkciós (toxikus) strumák Graves-Basedow struma:
A pajzsmirigy megnagyobbodását a szervezet immunrendszerének megbetegedése idézi elő, amelyet genetikai predispositio, stressztényezők és környezeti hatások együttesen hoznak létre. Az autoimmun folyamatban a pajzsmirigy membránján található TSH-receptorokkal szemben képződnek olyan antitestek, amelyek permanensen fokozzák a TSH aktivitását. Ennek eredménye a fokozott pajzsmirigyhormon-elválasztás, amely mind a T3-ra, mind a T4-re vonatkozik.
Diffúz autonom struma:
Úgynevezett disszeminált autonómia. Viszonylag igen ritka. Ide tartozik az extrém ritka congenitalis hyperthyreosis, amelyet a TSH receptor örökletes aktiváló mutációja okoz.
Uninoduláris és multinoduláris toxikus golyva (a fenti meghatározás alapján helyesebben: unifokális és multifokális autonómia hyperthyreosissal).
A Graves-Basedow kórtól klinikailag az életkor (idősebb korban jellemzőbb), a multinodularis golyva és az endokrin ophthalmopathia hiánya különíti el. A cardialis ritmuszavarok viszont gyakoribbak, mint Graves-Basedow kórban. A pajzsmirigy izotóp vizsgálattal egy vagy több "forró" göb mutatható ki. A multifokális autonómia esetén "hideg" göbök is gyakoriak, míg az unifokális autonómiánál a környező ép pajzsmirigyszövet visszaszorított, az izotóp képen csak túlvezérléssel jeleníthető meg. Unifokális autonómia esetén a hormonproductió mértéke arányos az adenoma nagyságával, 3 cm felett a hyperthyreosis igen valószínű.
2.3. Speciális strumák
Pajzsmirigy-gyulladások. Különböző ethiológiájú, eltérő klinikai képet és kórlefolyást mutató megbetegedések tartoznak ide.
Akut gennyes thyreoiditis:
Ritkán előforduló, bakterialis infekciót követő, abscedáló folyamat. Leggyakoribb kórokozói a Streptococcus pyogenes vagy a Staphylococcus aureus, amelyek vagy haematogen úton, vagy a környezetből jutnak a pajzsmirigybe.
Subacut (de Quervain) thyreoiditis:
Feltételezetten vírus ethiológiájú (mumps, coxsackie) megbetegedés, elsősorban középkorú nőknél fordul elő. Hormonálisan kezdetben hyperfunctio jellemző, amelyet átmeneti hypofunctio követ, de gyógyulása után normális hormonstátusát visszanyeri a beteg. A pajzsmirigy megnagyobbodása mérsékelt, általában féloldali. Cytológiailag jellegzetes a sokmagvú óriássejtek jelenléte.
Chronicus lymphocytás (Hashimoto) thyreoiditis:
Ugyancsak középkorú nők jellegzetes megbetegedése, a nő-férfi arány 15:1 . Számuk Csernobyl óta növekvőben van. Autoimmun megbetegedés, magas titerben kimutatható a serumban a pajzsmirigy peroxidáz-enzim ellenes antitest. A mirigy lymphocytás infiltrációja korrelál az antitest-titer értékével, gyakran kifejezetten intenziv, lymphocyta-follikulusok képződnek. Mikroszkópban jellegzetesek a megnagyobbodott, eosinophyl Askenazy sejtek. A nagyfokú lymphocytás beszürődés következtében a pajzsmirigy megnagyobbodik, állománya tömör, radírgumi -tapintatú, amely később - a folyamat előrehaladtával - a következményes fibrosis miatt igen keménnyé válik és súlyos hypothyreosisba torkollik. Hashimoto thyreoiditis precursora lehet malignus lymphomának.
Chronicus fibrosus (Riedel) thyreoiditis:
Az előbbi ritka formája, ahol a fibrosis olyan mértékű, hogy a pajzsmirigy szinte "deszkakemény" és nemcsak magára a mirigyre terjed ki, hanem a környező nyaki szerveket (izmokat, tracheát, nyelőcsövet) is invasive komprimálja. Még műtét közben is összetéveszthető a pajzsmirigy karcinómájával.
2.4. Malignus strumák
A pajzsmirigy rosszindulatú daganatainak összefoglaló neve. A legtöbb európai országban a ritka tumorok közé tartoznak, éves incidenciájuk 0,002 - 0,003 %. Sokkal gyakoribbak a klinikailag latens, más néven okkult vagy mikrokarcinómák (0,5-3,5 %), amelyeket gyakran csak véletlenül találnak meg benignus strumamütétek sebészi preparatumaiban, vagy autopsiák során.
Többségükből nem is fejlődik ki manifest rák. Golyvaendémiás vidékeken prevalenciájuk magasabb, elsősorban a follikuláris szerkezetü karcinomáké. Rizikófaktoruk:
1. Tartós jódhiány, következményes TSH hatás.
2. Röntgen és ionizáló sugárzás (elősorban gyermekeknél 4 éves kor alatt).
3. Familiáris öröklődés medulláris rákokban (egyedül, vagy Multiplex Endokrin Neoplasia részeként).
Az Egészségügyi Világszervezet (WHO) klasszifikációja általánosan elfogadott beosztást adott a rosszindulatú pajzsmirigytumorokról, amely morfológiai elváltozásokon alapul és utal a várható prognózisra is.
Papilláris karcinóma
A legjobb prognózissal a papilláris szerkezetű pajzsmirigyrákok rendelkeznek, különösen a 40 évnél fiatalabb betegek esetén. Gyakori multicentrikus előfordulásuk és már korán adnak áttéteket a környéki nyaki nyirokcsomókba. Nem ritka, hogy egy-egy megnagyobbodott, áttétes nyirokcsomó a betegség megjelenésénekelső jele és a pajzsmirigyben még nem is tapintható a primer tumor. Gyermekeknél 90%-ban találunka tumorral együtt nyirokcsomó metasztázist, felnőtteknél 40-50 %-ban. Távoli áttéteket főleg a tüdőbe, ritkán a csontokba ad. Az 5 éves túlélés papilláris rákok esetén 90 %, a 10 éves 80 %.
Follikuláris karcinóma:
Többnyire 50 éves kor felett jelentkezik, frekventáltabban golyvaendémiás, jódhiányos területeken, ami valószinűsíti a TSH indukáló szerepét. Lehetnek enkapszuláltak (tokkal körülvett), vagy invazive növekvők, 20 %-ban oxyphil (Hürthle)-sejtesek. Az egyes follikuláris ráktipusok malignus potenciálja attól függ, milyen mértékben jelentkezik mikroszkóposan az ér- és tokbetörés. Nyirokcsomó metasztázisai ritkák, főleg haematogen úton ad áttéteket a csontokba. A follikuláris rákok 5 éves túlélése 80 %, a 10 éves 50 %. Az oncocytás (Hürthle)-sejtes típus biológiai viselkedése agresszívabb. Medulláris karcinóma:
A parafollikuláris, vagy C-sejtekből származnak, amelyek az APUD-systémához tartoznak és a calcitonint termelik. Etiológiájában a RET-protooncogen pontmutációi játszanak szerepet. Ha a tumor solitaer, ez sporadikus előfordulást jelent (80-90 %), mig multiplex formája familiáris megjelenést valószinűsít (10-20 %). Ilyen esetekben a medullaris (C-sejtes) rák autosomalis úton dominánsan öröklődik és már fiatal korban kifejlődik. A 10-es kromoszoma rendellenességét igazolni tudták, ez segithet a jövőben a családokban érintett egyént megtalálni. Familiáris medulláris karcinóma együttesen is előfordulhat a mellékvese pheochromocytomájával és a mellékpajzsmirigy hyperplasiájával, ezt nevezik II.A tipusu multiplex endokrin neoplasiának, más néven Sipple-syndromának. A II.B típusnál a mellékpajzsmirigy betegség helyett submucosus neurofibromatosisok szerepelnek marfanoid phenotípussal. A calcitonin, mint tumormarker mind a diagnózisban, mind az utánkövetésben segítségünkre van. A medulláris rák is előszeretettel ad nyaki nyirokcsomó metasztázisokat (60 %-ban), az 5 éves túlélés is 60 %, a tízéves 40%.
Anaplasztikus karcinóma:
Az emberi szervezet legagresszívabb tumora, expanzive növekszik, infiltrálja a nyaki szerveket és egyidejűleg ad regionális nyirokcsomó és távoli áttéteket is. Incidenciája ugyancsak endémiás golyvavidékeken magasabb. A betegek többsége ritkán éli túl az 1 évet. Előfordulása az idősebb korosztályban gyakoribb és az esetek egy részében korábbi differenciált pajzsmirigy carcinoma dedifferenciálódásából alakul ki.
Malignus lymphoma:
Ugyancsak gyorsan növekvő, ritka nyaki daganat, idősebb nőknél fordul elő elsősorban. Szövettanilag gyakran csak immunhisztokémiai módszerekkel lehet elkülöníteni az anaplasztikus (kissejtes) karcinómától.
3. Klinikai tünetek
Klinikai tünetek, vizsgálatok
Pajzsmirigy megbetegedéssel sebészhez forduló betegek panaszai két fő csoportra oszlanak: a mirigy megnagyobbodásából származó ill. a hormondysfunctióból eredő panaszokra.
Nyaki tünetek
A strumák többségükben lassan nőnek, a betegek általában csak akkor jelentkeznek orvosnál, ha már kozmetikai problémát okoznak. Gyors, fájdalmatlan növekedés karcinómára vagy bevérzésre utal. Nyelési nehezítettség (dysphagia) thyreoiditishez és anaplasztikus karcinómához társul. A dyspnoe, stridor a trachea deviációjának vagy kompressziójának következménye, amit a pajzsmirigy aszimmetrikus megnagyobbodása okoz. Rekedtség előzetes pajzsmirigy műtét nélkül csaknem biztosan malignus eredetű és az egyik nervus recurrens beszürtségét jelenti. Jelentkezhet még hypothyreotikus golyvánál is, ha a hangszalagok oedemásak.
A betegség természetéről sokszor mára beteg puszta megjelenése is árulkodik: az euthyreoid beteg konvencionálisan viselkedik. A hyperfunkciós gesztikulál, zajos, olykor nervosus. A hypothyreoid egykedvű, lassú mozgású, gyakran túlsúlyos.
A nyak megtekintése, a nyeletés, a fizikális vizsgálat kezdete. Feltünhetnek a tágult nyaki vénák (vena cava superior kompresszió, substernalis leterjedésnél), erythema (de Quervain vagy suppurativ thyreoiditis), pajzsporc deviációja (asszimmetrikus pajzsmirigy megnagyobbodás), "bőrbehúzottság" (lokálisan invazív rák).
A nyak fizikális vizsgálatánál a beteg háta mögött állunk, jobb kezünkkel a jobb, bal kezünkkel a bal nyaki régiót tapintjuk át a musculus sternocleidomastoideus lefutásának megfelelően. Tapintjuk a göböket, majd felszólítjuk a beteget nyelésre. (Esetleg egy pohár vizet adunkelőttea kezébe, a nyelés megkönnyítésére). Ilyenkor ítélhetjük meg a rögzítettséget, a substernalis leterjedést ("búvárgolyva" ). Végül a nyaki nyirokcsomók keresésével fejezzük be a vizsgálatot egészen az angulus mandibulae-ig.
A hypothyreosis jellegzetes tünetei:
száraz, pikkelyes bőr, vastagszálu, töredezett haj, macroglossia, renyhe reflexek.
A hyperthyreosis jellegzetes tünetei:
a Merseburgi Triász: 1/ struma, 2/ tachycardia, 3/ ophthalmopathia (ez utóbbi nem szükségszerűen társul hozzá). További tünetek: kézremegés (tremor), fokozott ingerlékenység, testsúlycsökkenés (megnövekedett étvágy ellenére), hasmenés, izomgyengeség, praetibialis oedema, vitiligo, hőhullámok, hyperreflexia, palpitációk.
II. Diagnózis
1. In vitro diagnosztika (a normális tartomány módszerfüggően eltérő lehet) Hormonkoncentrációk
TSH (pajzsmirigy stimuláló hormon). Normális tartomány: 0,4-4,0 mU/l
FT4 (szabad thyroxin). Normális tartomány: 8-25 pmol/l
FT3 (szabad trijódthyronin). Normális tartomány: 3-8 pmol/l
Calcitonin
Antitest vizsgálatok
TSH -receptor ellenes antitest
Pajzsmirigy peroxidáz enzim (TPO) ellenes antitest
Thyreoglobulin (Tg) ellenes antitest
Thyreoglobulin
RET-protoonkogén mutáció vizsgálata
2. Képalkotó vizsgálatok
a pajzsmirigy és környezetének ultrahang vizsgálata pajzsmirigy 131Iés 99mTc izotóp vizsgálata nyaki v.mellkasi CT, MR (ritkán indokolt) 18FDG-PET vizsgálat (csak kivételes esetekben) mellkas röntgen, trachea légsáv felvétel, nyelési próba finomtű aspirációs cytológia (FNAB) gégészeti vizsgálat (hangszalagfunctio?)
III. Terápia
1. Sebészi kezelés
1.1. Benignus struma műtéte: egy vagy kétoldali subtotalis resectio, near total vagy total thyreoidectomia
Normofunkciós golyvák műtéti indikációja:
abszolút: a/ malignitas lehetősége klinikai vagy cytológiai vizsgálat talapján
b/ nyaki szervek kompresszioja esetén
c/ retrosternalis v.intrathoracalis localisatio relativ: a/ kozmetikai és szocialis okok
Funkcionalis és technikai követelmények:
A subtotalis lebenyreszekciókat mindinkább felváltják a radikálisabb műtéti eljárások, a hemi- vagy totalis thyreoidectomiák. Adenomák esetében a választandó műtét a lobectomia. Subtotalis reszekciók után a recidivák aránya elérheti a 30 %-ot. (II-IV evidencia szint).
Incidentális pajzsmirigyrák 3-16 %-ban mutatható ki (IV evidencia szint), ami további sebészi beavatkozást igényel.
Prospektív, randomizált tanulmányokszerint a subtotalis és totalis thyreoidectomiák permanens szövődményi aránya nem különbözik, csupán az átmeneti hypocalcaemia aránya magasabb total thyreoidectomia után.
A pajzsmirigyműtétek két legfontosabb szövődménye a nervus laryngeus recurrens inferior sérülése és a hypoparathyreosis. Az előbbi aránya nem lehet magasabb, mint 1,4 % míg az utóbbi 2 % körüli lehet.
"C" fokozatú ajánlás szerint a total thyreoidectomia e szempontból is biztonságos és effektív, a kiújulási arány gyakorlatilag 0 %.
A nervus laryngeus recurrens sérülésének minimalizálására bevezették az intraoperatív idegmonitorizálást (IONM). Eddigi klinikai tanulmányok szerint ez az eljárás és a vizualis idegazonosítás között nincs szignifikáns különbség. Az endoszkópos thyreoidectomia (ET) ugyancsakelterjedőben lévő sebészi technika, amely speciális, endoszkópiában jártas sebészt igényel. Végezhető insufflatio-val vagy mechanikus retraktor-ral. Retrospektívtanulmányokszerintaz ET műtéti ideje hosszabb, mint a hagyományos pajzsmirigy műtéteké, a hangszalagbénulások aránya is magasabb, előnye viszont a jobb cosmesis. Jelenleg evidenciaszintű ajánlás még nincs .
A substernalis golyvák sebészi kezelésénél a III/IV szintű adatok szerint az alábbiakat kell tekintetbe venni:
1. A substernalis golyvában nem magasabb a rák incidencia, mint a nyaki strumákban.
2. Prospektív V szintű adatok szerint gyakorlott endokrin sebész kezében a substernalis golyva extracervicalis behatolásból is biztonságosan operálható, sternotomiára csak akkor kerül sor, ha a golyva tömege nagyobb, mint a mellkasi bemenet.
3. Magasabb e műtétek után a hypoparathyreosis és nervus recurrens sérülés, ha total thyreoidectomia történt substernalis golyva miatt ("C" fokozatú ajánlás).
4. Öt éven túl meglévő substernalis golyva rizikófaktortracheomaláciá-ra és tracheostomia-ra.("C" fokozatú ajánlás).
5. Prospektív V szintű adatok szerint a substernalis golyvaműtétek 5-10 %-át recidív vagy persistáló betegség miatt végzik subtotalis-, vagy hemithyreoidectomia után.
1.2. Hyperfunkciós golyvák műtéti indikációja:
abszolút: a/ multinodularis toxicus golyva b/ nagy Basedow struma
c/ uninodularis autonom adenoma, ha az átmérő nagyobb, mint 2 cm d/ malignitás gyanúja relativ: a/ gyermek- és fiatalkorban eredménytelen thyreostaticus kezelés b/terhesség első két trimeszterében
c/ uninodularis vagy multinodularis autonómia okozta hyperthyreosisban, ha a radiojód terapia sikertelen, vagy nincs compliance.
Funkcionalis és technikai követelmények
- Minél kevesebb pm.szövet maradjon még későbbi hypothyreosis árán is.
- A recidiv hyperthyreosist minden uton el kell kerülni!
- Sebészi vagy radiojód kezelés egyaránt javasolt a solitaer toxicus adenoma és multinodularis toxicus golyva esetén (IV szintű evidencia). Nincs evidencia a két terápiás módszer kimenetelére. A IV. evidenciaszint nagy kompressziós golyvák esetén a thyreoidectomiát támogatja a radiojóddal szemben.
- A III evidenciaszint ugyanezt javasolja Ethanol-lal végzett ablatioval szemben. Az V szintű adatok a sebészetet helyezik előtérbe, a cost-benefit vonatkozásában.
- A Mayo-klinikán 1356 multinodularis toxikus golyvás betegből 948-at (70 %) műtéttel kezeltek. (23)
- Nincs evidenciaszintű ajánlás arra, hogy a Graves-Basedow kór kezelésére melyik terápiás módszert válasszuk.
- A total thyreoidectomia szövődményi rátája azonos a kevéssé radikális reszekciókéval, magasabb viszont a gyógyulási arány, a kiújulás pedig elhanyagolható (I-IV szintű adatok "A" fokú ajánlással).
- A súlyos ophthalmopathiá-val együttjáró Basedow-golyva esetében műtét ajánlott, jóllehet a radiojóddal kombinált steroid kezelés is biztonságos (II-IV szintű adatok"B" ajánlással).
- A pajzsmirigyreszekció mértéke nem befolyásolja az ophthalmopathia kimenetelét (II szintű adatok, "B" ajánlás).
- A műtét gyermekkorban definitív kezelés (IV szintű adatok, "C" ajánlás).
- Gyermekeknél a radiojód kezelés fokozott rák-rizikóvaljár,ezisa műtét mellett szól (I szintű adatok"A" ajánlással).
- Műtét előtt a beteget euthyreoid állapotba kell hozni.
Az előkészítés lehetőségei:
- antithyreoidea gyógyszerek + Béta blokkoló (Propranolol)
- Lugol cseppek + Béta blokkoló (csak Graves-Basedow kór esetében)
- esetleg a három szer együttes kombinációja
1.3. Hypofunkciós golyvák műtéti indikációja
- ltalában nem javallt, kivéve, ha:
- nyaki kompresszió
- malignitás gyanuja áll fenn
1.4. Recidív golyvák műtéti indikációja
- malignitás gyanúja
- jelentős mechanikai komponens áll fenn
- kozmetikai indikáció (csak lobus pyramidalis recidiva esetén)
Lehetőleg intracapsularis subtotalis resectio vagy total thyreoidectomia a nervus recurrens és a parathyreoideák megkimélésével /sérülésük rizikója 6-szoros!/.
1.5. Malignus pajzsmirigytumorok sebészi kezelése
A rosszindulatú pajzsmirigydaganatok standard kezelésében a sebészeté a vezető szerep, célja az összes daganatszövet és a regionális nyaki nyirokcsomóáttétek komplett eltávolitása a mellékpajzsmirigyek, az externalis és recurrens laryngealis idegek megőrzésével. Ez általában teljes vagy "közel-teljes" (near-total) pajzsmirigykiirtás, a centális nyirokcsomók dissectiójával CND). A közel-teljes pajzsmirigykiirtás a tumoros oldalon lobectomia, az ellenoldalon a felső pólusnál körülbelül 1 grammnyi szövet visszahagyása. A carcinóma miatt végzett thyreoidectomia minden esetben magába foglalja a centralis, azaz a parathyreoidealis, a praelaryngealis és praetrachealis nyirokcsomók eltávolítását is.
A teljes pajzsmirigykiírtás előnyei
- alacsonyabb recidívaráta
- magasabb túlélési arány (tumor 1 cm)
- szenzitívebb a thyreoglobulin meghatározás
- teljes 131I-ablatio után a kiújulás detektálható
- alacsony morbiditási ráta (tapasztalt sebész)
- nincs anaplasticus tumortranszformáció
Tapintható, vagy ultrahangvizsgálattal gyanús lateralis nyaki nyirokcsomókesetén az azonos oldalon el kell végezni a szisztémás, lateralis nyirokcsomó-disszekciót - MRND-t - esetenként az ellenoldalon is. A profilaktikus nyaki nyirokcsomó-disszekció ma általánosan nem elfogadott.
Sporadikus medulláris rák esetén kötelezően elvégzendő az ipsilateralis, míg familiáris medulláris karcinóma esetén a kétoldali szisztémás nyaki nyirokcsomó disszekció. A mediastinalis nyirokcsomókdisszekciója az adott helyzettől függ. A funkcionális lymphadenectomia megkíméli a szomszédos képleteket, radikális nyaki block-disszekcióra csak tumoros infiltráció esetén kerül sor.
A tumor expanzív, extrathyreoidealis terjedése rossz prognózist jelent, a fentieknél radikálisabb műtét rutinszerű végzése nem ajánlott. Az elsődleges sebészi beavatkozás döntő a differenciált és a medulláris pajzsmirigyrákok multidiszciplináris kezelésében, ugyanis ezek közel 50 %-ában csak postoperative igazolódik a diagnosis. Az ilyen esetekben ismételt, ún. második műtét elvégzése szükséges. A komplettáló thyreoidectomiák fokozott morbiditással járnak, növekszika nervus recurrens sérülésekés a postoperativ hypoparathyreosisokszáma. A komplettáló műtétekre ezért célszerű a betegeket speciális endokrinsebészeti centrumokba küldeni. Tapasztalt sebészek műtétei után a végleges nervus recurrens paresisek aránya kevesebb, mint 1 %, a végleges hypoparathyreosisoké 2 %. Arra kell törekedni, hogy az elsődleges sebészi beavatkozás definitív terapia legyen. A differenciált és a medulláris pajzsmirigyrákokgyakran solitaer göbök formájában jelentkeznek (szcintigráfián "hideg"-göbök), amelyek malignitási rátája 2-6 %, jó jódellátottságú területen ennél magasabb. Tizennégy éves kor alatt és 60 év felett a solitaer göbök malignitási rátája elérheti az 50 %-ot! Ha a finomtű aspirációs cytológia (FNAB) gyanús, illetve bizonytalan, Hürthle-(oxyphil) sejtek vagy "follikuláris neoplasia" esetén, első lépésben lobectomia és isthmusreszekció a helyes sebészi eljárás, centrális nyirokcsomó disszekcióval. Ha az intraoperativ fagyasztott szövettani vizsgálat malignitást igazol, azonnal folytatható a műtét az ellenoldalon. Amennyiben ezzel sincs biztos diagnózis, meg kell várni a végleges hisztopatológiai eredményt. Az elsődlegesen elvégzett lobectomia tehát vagy végleges therapiának bizonyul, vagy a részletes szövettani vizsgálattal igazolt malignitás esetén komplettálni kell a műtétet, de már csak az ellenoldalon. Ezzel a stratégiával elkerülhető a postoperativ komplikációk számának növekedése, ami a komplettáló műtétek után többszörös lehet A papilláris pajzsmirigyrákok gyakran bilateralisak és multifokalisak, emiatt nem sorolhatók be "alacsony" vagy "magas" kockázatú csoportokba. A komplettáló thyreoidectomiát vagy az első műtétet követő harmadik-negyedik napon, vagy három hónap elteltével ajánlatos elvégezni.
A fagyasztott szövettani metszet rutinszerű vizsgálatát a solitaer pajzsmirigygöbök műtéteinél a finomtű aspirációs cytológia érájában sokan vitatják. Kétségtelen tény, hogy a "follikuláris neoplasiá"-k eseteiben kevéssé informativ azonban ha papilláris rák gyanúja merül fel, műtét közben a fagyasztott vizsgálat eldöntheti a kérdést.
Intraoperativ fagyasztott szövettani metszet - érvek mellette és ellene
- follicularis neoplasmák esetében nem informativ
- kiegészíti a bizonytalan FNAB leletet, különösen PTC gyanúja esetén
- totális thyreoidectomia során alkalmas az eltávolitott mellékpajzsmirigy identifikálására, gyanús nyirokcsomók dignitásának kimutatására
- csökkenti a reoperációk számát
- költséget takarit meg
- tapasztalt patológust igényel !
(FNAB: finomtű -aspirációs biopszia, PTC: papillaris thyreoidea carcinoma)
Az anaplasztikus pajzsmirigykarcinóma expanzive, rapidan növekvő, többnyire mindkét lebenyt érintő tumor, amely rövid idő alatt légúti obstrukcióhoz vezet, beszűri a rövid nyakizmokat, a musculus sternocleidomastoideust és a nyaki nagyereket. Számuk csökkenőben van, miután a differenciált rákok többnyire idejében műtétre kerülnek, de szerepe van ebben a rendszeres jódprofilaxisnak is. Prognózisa nagyon rossz, kurativ műtét végzésére alig kerülhet sor, csupán palliativ tumorcsökkentésre. A diagnózist a finomtű- vagy a hengerbiopszia biztosítja.
Külső, frakcionált sugárkezelés lassithatja a progressziv növekedést kombinálva doxorubicin adásával, ami sugárszenzitizáló is egyben. Súlyos fokú légúti obstrukció esetén elkerülhetetlen tracheostoma végzése.
Műtéti érzéstelenités: minden esetben intratrachealis narcosisban
1.6. A müűétek legnagyobb részénél a Kocher-féle gallérmetszés elégséges feltárást ad. Substernalis golyva, nagy malignus tumor esetén különösen, ha recidiváról van szó, szükség lehet a sternum szétválasztására - sternotomia-ra. Módositott radikális nyaki disszekció elvégzéséhez a standard Kocher-metszést egyik- vagy mindkét oldalon ki kell terjeszteni.
1.7. A pajzsmirigymütétek intra- és postoperativ szövődményei
Pajzsmirigysebészetben jártas szakember kezében a mütéti morbiditás alacsony, mortalitás 0-0,2 %. Néhány speciális szövődmény azonban életveszélyes állapotba sodorhatja a beteget, ezeket tehát megfelelő preparálási technikával, jó anatómiai ismerettel el lehet kerülni.
Intraoperativ szövődmények Vérzés:
Az arteria thyreoidea superior gyakran már magasan több ágra oszlik és egy-egy ága kicsúszhat a ligatúrából. Megelőzhető kettős lekötéssel. Substernalis golyva kiemelésekor elszakad egy kisebb véna, vagy arteria. Sternofissura-ból felkereshető, ellátható. Erőteljes parenchymás vérzés keletkezhet antithyreoidea szerekkel hosszasan kezelt golyvák mütétei közben. Ezeket nyolcas öltésekkel csillapithatjuk.
Légembólia:
Intubációs narkózisban végzett műtéteknél ezzel a szövődménnyel gyakorlatilag nem kell számolni. Ajánlatos azonban a tágult, nagy nyaki vénákat még átmetszésük előtt aláölteni.
Nervus laryngeus recurrens inferior sérülése. A leggyakrabban létrejövő sérülés, elkerülhető az idegek műűét alatti identifikálásával. Pajzsmirigy centrumokban a permanens nervus recurrens bénulásokaránya 1 % körüli. Mechanikus, de reverzibilis intraopertiv károsodás következtében az ún. transiens bénulások elérhetik a 2-4 %-ot, ezek 6 hónapon belül spontán megjavulnak. Egyoldali hangszalag bénulás rekedtséget, félrenyelést okoz, a kétoldali súlyos, többnyire sürgős tracheostomiát igénylő asphyxiát. Rosszindulatú daganatok, ill. recidivák műtéteinél különös gonddal (és műtéti jártassággal) kell ügyelni az idegek megváltozott anatómiai lefutására. Ugyanez vonatkozik a retrosternális nagy göbös golyvákra is. Nervus laryngeus superior sérülése:
Tünetei nem annyira feltűnőek, mint a recurrens sérülés esetén. A felső póluson belépő arteriák ligatúrájánál keletkezhet. A hang minősége változik meg csupán: a magas hangok képzése válik lehetetlenné, a beszéd fáradékony lesz.
Posztoperativ szövődmények Utóvérzés:
Ritkán fordul elő, a strumaműtétek egy százalékában. Tipusosan az első 24 óra szövődménye, egyaránt lehet arteriás vagy vénás eredetű. A hirtelen kialakuló, nagyfokú vérzés nyaki duzzanatot, következményes gége és subglottikus oedemát okoz, légúti obstructio miatt életveszélyes állapotba kerülhet a beteg. Azonnali intubáció szükséges, a haematoma evakuálása, a vérzésforrás megkeresése és sebészi ellátása. Ha súlyos légúti obstructio alakult ki, az intubációt a reoperáció után is fenntartjuk, esetleg tracheostomára is sor kerülhet. Egy francia retrospektív tanulmány során ismertté vált, hogy 15 év alatt végzett (6830) strumaműtét után 70 utóvérzést kellett sebészi feltárással ellátni, ezek 10 %-a a műtétet követően 24 órán túl jelentkezett. A tanulmány állásfoglalása: strumamütétek végzése egynapos-sebészet keretében nem ajánlott. Thyreotoxikus krízis:
A hyperthyreosis akut, műtét utáni fellángolása életveszélyes helyzetet teremt a mütött beteg számára. Ma szerencsére igen ritkán fordul elő, csak inadequat műtéti előkészítés után lép fel, amikor a beteg még toxikus állapotban kerül műtétre. A klinikai kép tipusos: magas láz, tachycardia (pitvarfibrillatio), nagyfokú nyugtalanság, delirium. Kezelése: nagydózisú thyreostaticum adása, Propranolol lassú infusióban EKG kontroll mellett. További supportiv therápia: intravénás folyadékbevitel, oxigen, corticosteroidok , 10 %-os MgSO4 , sedálás. Végső esetben plasmaferesis. Mindezek intenzív osztályon, betegmonitorizálás mellett. Hypoparathyreosis:
A mellékpajzsmirigyek excisiója vagy érellátásuk maradandó károsodása következtében hypocalcaemia alakul ki. A tünetek a műtét utáni első héten jelentkeznek: zsibbadásérzés a száj körül, tónusos görcsök a lábszár és a törzs izmaiban, őzfejtartás a kéz ujjaiban, nyelési nehezítettség, ritkábban laryngospasmus. Pajzsmirigyműtét után a serum-calcium szintet monitorizálni kell. A súlyos hypocalcaemia kezelése: 10 %-os Calcium-gluconat infusioban, szükség szerint 4-6 óránként megismételve, 2-3 g per os calcium hozzáadásával. Persistáló hypocalcaemia esetén ez utóbbit kell folyamatosan és tartósan adni alfa D3-vitaminnal vagy Rocaltrol-lal.
Követelmény nagyobb pajzsmirigyműtétek során mindkét oldalon egy-egy mellékpajzsmirigy vizualizálása és finom vérellátásuk megőrzése. Szövetkímélő technikával a postoperativ hypoparathyreosisokszáma nem több, mint 1-2%. Hypothyreosis és recidiv hyperthyreosis:
Hypothyreosis kialakulása thyreoidectomia után evidens. Hyperthyreosis miatt végzett pajzsmirigyműtét után visszahagyott parenchyma hormonprodukciója nemcsak annak méretétől, hanem az alapbetegség pathológiai természetétől is függ, továbbá a beteg korától, a műtét előtti pajzsmirigyellenes antitestek titerétől, a pajzsmirigyállomány lymphocytás infiltrációjának mértékétől.
Postoperativ hypothyreosis kisebb mértékben alakul ki toxikus nodularis golyvák műtétei után. Tapasztalt sebészi team műtétei után a recidiv hyperthyreosis rátának 5 % alatt kell maradnia.
IV. Rehabilitáció
V. Gondozás Utógondozás
Benignus struma műtéte után Recidiva megelőzés T4 -el Se -calcium
gégészet /nervus recurrens paresis/
sTSH
ultrahang
Malignus struma műtéte után
ablativ I131 kezelés, vagy percutan besugárzás
sTSH
Tg, Tg ellenes antitest (TgAb), calcitonin ultrahang
tg, csontscan, cytológia, I131 scan, CT, MRI, PET/CT/a lelettől függően/ Postoperativ gondozás
A pajzsmirigy műtét utáni funkciócsökkenés a TSH fokozott elválasztását és recidiv struma kialakulását vonhatja maga után. A postoperatív gondozás elsődleges célja ennek megakadályozása. A másik cél a szövődmények kezelése. A gondozási elvek az alapbetegség és a műtéti eljárások szerint változnak. Bármilyen alapbetegség miatt szükségessé vált kétoldali subtotalis resectio vagy thyreoidectomia után a beteget élete végéig rendszeresen ellenőrizni kell. Az utánkövetés interdiszciplináris feladat, sebész, nukleáris szakorvos és endokrinológus részvételével.
VI. Irodalomjegyzék
1. ACE/-AAES medical/surgical guidelines for clinical practice: management of thyroid carcinoma. American Assoc of Clinical Endocrinologists. American College of Endocrinology. Endocr Pract 2001; 7: 202-20.
2. Abzahrani AS, Mandil MA,Chaudhary A, Ahmed M, Mohammed GE. Frequency and predictive factors of malignancy in residual thyroid tissue and cervical lymph nodes after partial thyroidectomy for differentiated thyroid cancer. Surgery 2002; 131:443-9.
3. Agarwal G, V Agarwal. Is total thyreoidectomy the surgical procedure of choice for benign multinodular goiter ? An Evidence-Based Review. World J Surg 2008; 32:7,1313-24
4. Chirurgie der Schilddrüse. In: Chirurgie. Das offizieller Organ der Österreichischen Chirurgischen Vereinigungen. 3/2006.
5. ClarkO.H., Duh Q-Y., Kebebew E.: Updates of Endocrine Surgery. Surg Clin North Am 2004; Vol.84.
6. ClarkO.H., Duh Q-Y.: Endocrine Surgery. W.B.Saunders. Philadelphia, London,Toronto, Montreal, Sydney,Tokyo, 1997.
7. Deutsche Gesellschaft für Chirurgie: Leitlinien zur Therapie der benignen Struma. Grundlagen in der Chirurgie. 1998; Heft3.
8. Deutsche Gesellschaft für Chirurgie: Leitlinien der Therapie maligner Schilddrüsentumoren. Grundlagen der Chirurgie. 1996; Heft 3.
9. Dralle H, Sekulla C, Lorenz K, Brauckhoff M, Machens A, G IONM Study Group. Intraoperative monitoring of the recurrent laryngeal nerve in thyroid surgery. World J Surg 2008; 32:7,1358-66
10. ÉsikO.: Irányelvek a pajzsmirigyrákok kivizsgálása, kezelése és követése során. Orvosi Hetilap. 2001; Suppl. 142.
11. Gaál Cs.(szerk.): Sebészet. Medicina Könyvkiadó Rt. Budapest. 2007.
12. Jonas J, Blaich S, Nagel A, Bahr R. Hemithyroidectomy on principle in cases of nuclear fine-needle biopsy and frozen section findings. Zbl Chir 2001; 126: 964-68.
13. Kupferman ME, Mandel SJ, DiDonato L, Wolf P, Randal R. Safety of completion thyroidectomy following unilateral lobectomy for well-differentiated thyroid cancer. Laryngoscope 2002; 112:1209-12.
14. Leövey A.(szerk.): A klinikai endokrinológia és anyagcserebetegségek kézikönyve. Medicina Könyvkiadó Rt. Budapest. 2001.
15. Leteutre E, LeroyX, Patton F,WacrenievA,Carnaille B, ProyeC. Why do frozen section ave limited value in encapsulated or minimally invasive follicular carcinoma of the thyroid. Am J Clin Path 2001; 115:370-74.
16. Lukács GL, Szakáll Sz, Kozma I, Győry F, Balázs Gy. Veränderungen der epidemiologischen Parameter von SD-Erkrankungen in Ostungarn zehn Jahre nach Tschernobyl. Langenbecks Arch Chir Suppl II 1997; p.375-77.
17. Lukács G.: Benignus struma. In: Klinikai Irányelvek Kézikönyve. Medition Kiadó Kft. Budapest. 2002.
18. Lukács G. A jó és rosszindulatú strumák sebészi kezelése. In: Jakab F(szerk). Sebészeti Útmutató. Medition Kiadó Kft. Budapest 2005; 181-88.
19. Lukács G. A pajzsmirigyrákok korszerű komplex kezelése. LAM. 2008; 18:111-18
20. Machens A, Hinze R, Tomusch O, Dralle H. Pattern of nodal metastasis for primary and reoperative thyroid cancer. World JSurg 2002;26:22-28.
21. Miccoli P, Minuto MN, Ugolini C, Pisano R, Fosso A, Berti P. Minimally invasive video-assisted thyroidectomy for benign thyroid disease: An evidence-based review. World J Surg 2008; 32:7,1333-40
22. Mishra A, Mishra SK. Total thyroidectomy for differentiated thyroid cancer: primary compared with completion thyroidectomy. Eur J Surg 2002; 168: 283-7.
23. Moalem J,Suh I, Duh QY. Treatment and prevention of recurrence of multinodular goiter: an evidence-based review of the literature. World J Surg 2008; 32:7,1301-12
24 Morris P.J., Malt R.A.: Oxford Textbook of Surgery. Vol.1. Oxford University Press. New York, Oxford, Tokyo. 1994.
25. Palazzo FF, Savio GR, Reeve TS, Sidhu SB, Sywak MS, Robinson B, Delbridge LW. Lymphadenectomy for papillary thyroid cancer: Changes in practice over four decades. Eur J Surg Oncol 2006; 32: 340-44.
26. Péter F. A gyermekkori pajzsmirigybetegségek előfordulása hazánkban. Orvosi Hetilap 2002; 143: 2867-73.
27. Phitayakorn R. and McHenry Chr. R.. Follow-up after surgery for benign nodular thyroid disease: evidence-based approach. World J Surg 2008; 32:7,1374-84
28. Porterfield J R., Thompson G B., Farley D R., Grant C S.and Richards M L.. Evidence - based management of toxic multinodular goiter (Plummer's disease). World J Surg 2008; 32:7,1378-84
29. Reeve T, Thompson NW. Complications of thyroid surgery: how to avoid them, how to manage them, and observations on their possible effect on the whole patient. World J Surg 2000; 24,971-75
30. Schlumberger M., Pacini F.(szerk.): Thyroid Tumors. Éditions Nucléon. Paris. 1999.
31. Slotema E Th, Sebag F, Henry JF. What is the evidence for endoscopic thyroidectomy in the management of benign thyroid disease? World J Surg 2008; 32:7,1325-32
32. Solymosi T, Tóth GyL, Gál I, Sajgó C, Szabolcs I. Influence of iodine intake on the diagnostic power of fine-needle aspiration cytology of the thyroid gland. Thyroid 2002; 12:719-23
33. Stalberg P, Svensson A, Hessman O, Akerström G, Hellman P. Surgical treatment of Graves' disease: evidence-based approach. World J Surg 2008; 32:7,1269-77
34. Teurer M, Passler C, Denk DM, Schneider B, Mancusi G, Sickinger B, Niederle B, Bigenzahn W. Functional laryngeal results after thyroidectomy and extensive recurrent larangeal nerve dissection without neuromonitoring - an analysis of more than 1000 nerves at risk. Eur Surg 2003; 35: 262-7.
35. Sungler P, Niederle B. Surgical treatment of thyroid carcinoma. Eur Surg 2006; 38:41-4.
36. White ML, Doherty GM, Gauger PG. Evidence-based surgical management of substernal goiter. World J Surg 2008; 32:7, 1285-300
37. WHO/UNICEF/ICCIDD. Indicators for assessing iodine deficiency disorders and their control through salt iodization. Genova: World Health Organization, 1994.
A szakmai protokoll érvényessége: 2010. szeptember 30.
Egészségügyi Minisztérium
szakmai irányelve
Lágyéktáji és hasfali sérvek ellátásáról felnőttkorban
(1. módosított változat)
Készítette: a Sebészeti Szakmai Kollégium
Elfogadta: Háziorvostani Szakmai Kollégium Radiológiai Szakmai Kollégium
I. ALAPVETŐ MEGFONTOLÁSOK ELŐSZÓ
Az irányelvben megfogalmazott ajánlások az elérhető legmagasabb szintű tudományos eredmények, a klinikai tapasztalatok és a betegek szempontjai, valamint a magyar egészségügyi ellátórendszer sajátságainak együttes figyelembevételével készültek.
Az ajánlásokat az egészségügyi ellátásért felelős személyzet mindig az egyedi beteg állapotának, szükségleteinek, valamint az ellátás körülményeinek megfelelően alkalmazza. Az ajánlásoktól való eltérés indoklását dokumentálni kell.
AZ AJÁNLÁSOK BESOROLÁSA (27)
"A" szintű ajánlás: Az ajánlások legalább egy 1++fokozatú bizonyítéknak számító meta-analízisen,vagy rendszerezett irodalmi áttekintésen alapulnak, és a saját populációra jól adaptálhatók; vagy legalább 1+ szintű bizonyítéknak számító, a saját populációra jól adaptálható, és egyértelműen hasonló hatást mutató vizsgálatokon alapulnak. "B" szintű ajánlás: Az ajánlások legalább 2++ szintű bizonyítéknak számító, a saját populációra jól adaptálható, és egyértelműen hasonló hatást mutató vizsgálatokon alapulnak; vagy 1++ és 1 + szintű bizonyítékok extrapolálásán -"Extrapolálás" azt jelenti, hogy ugyan magas a bizonyíték háttér, mégis a hazai ellátórendszer jellemzői szerinti alkalmazása csak alacsonyabb szintű ajánlást tesz lehetővé.
"C" szintű ajánlás: Az ajánlások legalább 2+ szintű bizonyítéknak számító, a saját populációra jól adaptálható, és egyértelműen hasonló hatást mutató vizsgálatokon alapulnak; vagy 2++ szintű bizonyítékok extrapolálásán alapulnak.
"D" szintű ajánlás: Az ajánlások 3-4 szintű bizonyítékon; vagy 2+ szintű bizonyítékok extrapolálásán Az ajánlások bizonyíték hátterének besorolása a VI. fejezetben olvasható.
DEFINÍCIÓK
1. Sérvnek nevezzük bármely zsigernek a normál anatómiai helyzetéből (üregéből) valamely veleszületett vagy szerzett nyíláson való kitüremkedését, előesését.
2. Hasfali sérv (hernia parietis abdominis) a hasfal azon veleszületett vagy szerzett gyenge területén alakul ki, ahol az intraabdominalis nyomás szervet (szerveket) présel a hasfal elé.
3. A hasfali sérvek döntő többségét (82%) a lágyéktáji (inguinalis 80% és femoralis 2%) sérvek képezik. Erre, valamint a sajátos anatómiára és műtéti megoldásokra való tekintettel tárgyalásuk külön is indokolt és szokásos.
3.1. A lágyéksérv (hernia inguinalis) a canalis inguinalis területén alakul ki, ahol a funiculus spermaticus (nőkön a ligamentum rotundum) áthalad. Itt hiányzik a musculoaponeuroticus réteg, és csupán a fascia transversalis képez ellenállást az intraabdominális nyomással szemben. Anatómiai megjelenése szerint lehet: mediális (direkt, egyenes) laterális (indirekt, ferde), kombinált (pantalló), csuszamlásos (par glissement). Az esetek mintegy 25%-ában kétoldali. A herezacskóba leérő sérv a hernia scrotalis.
3.2. A combsérv (hernia femoralis) a Poupart-szalag mediális harmada alatt, a nagyerek (artéria és véna femoralis) mentén, a combcsatornán (canalis femoralis) lép ki a combhajlatba. Nőkön és idősebb embereken gyakoribb, különösen korábbi inguinális sérvműtét után. 40%-ban sürgősségi esetként kerül felismerésre kizáródás és/vagy stranguláció miatt. (20)
4. A hasfal lágyéktáji területén kívül megjelenő sérvei (18%): 8-10% posztoperatív (incizionális, parastomalis); 4-5% umbilicalis; a fennmaradó paraumbilicalis, epigastrialis, Spieghel-féle. Jelen irányelv a "hasfali sérv" meghatározás alatt ezt a csoportot érti.
4.1. Köldöksérv (hernia umbilicalis): a köldökgyűrű (anulus umbilicalis) a születés utáni első hetekben elzáródik, és helyét közvetlenül a bőr alatt hegszövet tölti ki. A záródás elmaradása esetén, vagy később, hasűri nyomásfokozódásra a gyengébb hegszövetben sérv képződhet (hernia umbilicalis congenita, illetve aquisita).
4.2. Posztoperatív hernia (cicatrica, incizionalis): a hegsérvek hasi műtét hegvonalában alakulnak ki. Keletkezésükért legtöbbször a seb suppuratioja, ritkábban hypoproteinaemiával, leromlással járó betegségek, a hasfali varrat korai terhelése, egy izomszelvényt ellátó ideg műtéti sérülése, esetleg hibás műtéti technika okolható.
4.3. Hernia parastomalis: a posztoperativ sérv speciális formája, amely azanus praenaturalis mellett alakul ki. A stoma elődomborodásával és a stomazsák használatának nehézségével jár.
4.4. Hernia epigastrica, paraumbilicalis: a linea albát a processus xyphoideus és a köldök között keskeny, erős kötőszövetes lemez képezi, mely a köldök felett szélesebb. A lemezt átfúró apró erek mentén hasűri nyomásemelkedéskor, az e helyeken preformált nyílások tágulnak, amelyeken át először a praeperitonealis zsírszövet, mint kis lipoma préselődik elő a bőralatti kötőszövetbe, majd később peritoneum csücsköt is húz maga után. A szűk kapuval rendelkező sérvtömlő legtöbbször üres, később csepleszrészlet nyomulhat belé. A kifejlődött epigastriális sérv a bőralatti zsírszövetben (esetenként gombaszerűen) szétterülő előboltosulás formájában tapintható. Ha közvetlenül a köldök felett vagy mellette valahol helyezkedik el, hernia paraumbilicalisnak nevezzük.
4.5. Spieghel-hernia: A hernia a linea semilunaris Spiegheli és a linea semicircularis Douglasi keresztezési pontján alakul ki a musculus rectus abdominis lateralis szélén a köldök alatt mintegy 5 cm-rel. A ritka hasfali sérvek sorában külön figyelmet érdemel. A nagy Spieghel-hernia hasfali tumor képét is utánozhatja. (30)
5. A sérvek megjelenési formái:
- Reponábilis sérvben a sérvtartalom a sérvkapun keresztül visszahelyezhető a hasüregbe.
- Accret sérvről akkor beszélünk, ha a sérvtartalom összenövések és hegesedések miatt nem, vagy csak részben helyezhető vissza, de életképessége nincs veszélyben.
- Incarcerált sérv esetén a hasfal elé préselt szerveket a szűk sérvkapun keresztül visszahelyezni nem lehet, a sérvtartalom az erek kompressziója, megtöretése következtében elhalhat. A sérvkizáródásnak két különleges formája ismert:
- A retrograd incarceratio úgy alakul ki, hogy a szoros sérvkapu nemcsak a sérvtömlőben, hanem a hasüregben lévő bélkacs/ok/ mesenterium gyökét is strangulálja. Ennek következtében a béliszkémia a hasüregben előbb okoz nekrózist, mint a sérvtömlőben(i). Ezen lehetőség ismerete a korrekt sebészi ellátáshoz szükséges.
- A Littré-féle sérv esetén csupán a bélfal egy kisebb területe képezi a sérvtartalmat. Littré eredetileg csak a Meckel-diverticulum sérvre vonatkoztatta a megjelölést. Ma minden kizáródott bélfalsérvet így nevezünk. Leírójáról helyesen Richter sérv.
- Csuszamlásos (par glissement) sérvekben a hashártyával csak ventrálisan fedett szervek (húgyhólyag, sigmabél, coecum) retroperitonealis része csúszik ki a sérvkapun, a tartószalagok meglazulása következtében.
6. A sérv alkotói
- A sérvkapu a hasfal musculoaponeuroticus rétegének veleszületett vagy szerzett nyílása.
- A sérvtömlő a fali hashártyának sérvkapun át kitüremkedő része.
- A sérvtartalom a sérvtömlőbe kipréselődött hasüregi szerv vagy szervek: leggyakrabban cseplesz és/vagy a hosszú mesenteriummal rendelkező (mobilis) bélkacsok.
RÖVIDÍTÉSEK
LH = laparoszkópos sérvműtét
IPOM = laparoszkópos műtét intraperitonealis onlay mesh módszerrel
TAPP = transabdominalis praeperitonealis laparoszkópos lágyéksérvműtét
TEP = totalis extraperitonealis laparoszkópos lágyéksérvműtét
LVHR = laparoszkópos hasfali sérvműtét a lágyéktáji műtétek kivételével
BEVEZETÉS
1. Az irányelv alkalmazási területe, ellátottak és ellátók köre
Az irányelv a felnőttkorú betegeken előforduló valamennyi típusú lágyéktáji és hasfali sérv általános jellemzőit, tüneteit, diagnosztikáját és sebészi kezelését írja le. Hangsúlyozottan foglalkozik a műtéti javallatokkal és műtéti megoldásokkal.
A gyermekkori sérvellátással külön irányelv foglalkozik (11) A irányelv ellátói célcsoportja
- Elsődlegesen az I-III. szinten, járóbeteg-, fekvőbeteg- és "egynapos" ellátás keretében működő sebészeti szakellátás orvosai.
- Együttműködő szakellátók, mint aneszteziológia és képalkotó diagnosztika
- Másodlagos felhasználóként tájékoztató jellegű információkat tartalmaz a beteg háziorvosa számára (diagnosztika, betegirányítás és utókezelés szempontjai)
2. Az irányelv célja
Az irányelv a felnőttkori lágyéktáji és hasfali sérvek ellátása során felmerülő döntéshelyzetekben, tudományos bizonyítékokon és a magyar ellátórendszer és betegpopuláció sajátosságain alapuló ajánlásokkal kívánja segíteni az egészségügyi szolgáltató és a beteg választását, az eredményes és biztonságos betegellátás érdekében.
Az irányelv olyan formában és tartalommal fogalmazza meg az ajánlásokat, hogy azokból az ellátás eredményességét, megfelelőségét, biztonságosságát és költséghatékonyságát felülvizsgáló szervek, ellenőrzési feladataikhoz, jó minőségű mutatókat képezhessenek.
Kiemelt célja:
- A beteg szükségleteit legjobban szolgáló műtéti típusok megnevezése.
- A kezelés elveinek egységesítse.
- Nemzetgazdasági szempontból a költséghatékonyabb műtétek megjelölése.
A irányelv olyan formában és tartalommal fogalmazza meg az ajánlásokat, hogy azokból az ellátás eredményességét, megfelelőségét, biztonságosságát és költséghatékonyságát felülvizsgáló szervek ellenőrzési feladataikhoz jó minőségű mutatókat képezhessenek.
3. Az irányelv kapcsolata hazai és nemzetközi szakmai ajánlásokkal
Jelen irányelv "A hasfali és lágyéktáji sérvek kezelése" (Egészségügyi Közlöny 2006. év 5. szám 2. kötet) szakmai irányelv frissítése.
Egyben visszavonásra kerül a "Minimálisan invazív sebészet" 2006-os szakmai irányelve. (http://www.eum.hu/ egeszsegpolitika/minosegfejlesztes/sebeszet), mert az egyes klinikai témák irányelveiben kerül részletes ismertetésre. Az "Ambuláns és egynapos sebészet" szakmai irányelvben a sérvsebészettel kapcsolatos fejezet ezzel az irányelvvel visszavonásra kerül.
E témához kapcsolódóan további részletek az alábbi érvényes magyar ajánlásokban olvashatóak: Egészségügyi Közlönyben megjelent ajánlások, az Egészségügyi Minisztérium honlapján elérhető, legfrissebb verziója (http://www.eum.hu/egeszsegpolitika/minosegfejlesztes/sebeszet)
- Műtéti területen véletlenül visszahagyott idegentestek kérdése
Az irányelvben megfogalmazott ajánlások az alábbi nemzetközi, bizonyítékokon alapuló irányelvek ajánlásainak hazai adaptációjával készültek:
A fejlesztőcsoport nem talált a témában olyan bizonyítékokon alapuló nemzetközi szakmai irányelvet, mely megfelelően adaptálható lenne.
Az ajánlások megfogalmazásában a sérvsebészetben nemzetközileg használt, 2001-es, összefoglaló Bendavid-kézikönyv (1) szolgált alapul. Mivel az ehhez felhasznált legfrissebb irodalom 1999-es megjelenésű, a irányelv szerzői a 2000 óta megjelent, összefoglaló tanulmányokkal egészítették ki a kézikönyv ajánlásait. Számos multicentrikus tanulmány zajlik jelenleg is, mások az első összefoglaló eredményeket közlik, mint pl. az "EU Hernia Trialists Collaboration", mely 60 együttműködő randomizált tanulmányból származó eredményeket számos tanulmányban jelentet meg (8)
SZAKMAI HATTER ES FELTETELEK
1.1 Az irányelv által érintett problémakör hazai helyzete, a témaválasztás indoklása Átfogó statisztikák szerint a hernia inguinalis a felnőtt lakosság 5%-ában fordul elő.
A lágyéksérvműtét az egyik leggyakrabban végzett (Magyarországon évente 18-20 ezer) általános sebészeti beavatkozás.
A műtéti megoldások sokfélesége (feszülő, feszülésmentes, laparoszkópos technikák) és egyes műtétek elfogadhatatlanul magas recidíva aránya indokolttá teszi a beteg érdekeit legjobban szolgáló megoldások meghatározását.
1.2 Az ellátás célja
Az ellátás célja a panaszok megszüntetése mellett a munkaképesség és a normális életvitel teljes helyreállítása.
1.3 A betegség/állapot jellemzői
3.1. Kórállapot általános jellemzői Jellemző életkor / nem:
A lágyéksérv inkább férfiak (4-5-ször gyakoribb), a combsérv inkább nőknek a betegsége. Minden életkorban előfordul.
Kockázati és kiváltó tényezők
- A veleszületett (congenitális) valamint fiatalkorban jelentkező sérvek csaknem kivétel nélkül fejlődési hibák: lágyéksérvben a here leszállását követően a hashártyatasak (processus vaginalis peritonei), köldöksérvben pedig a köldökgyűrű záródása elmarad. Felnőttkorban akkor jelentenek ellátási feladatot, ha gyermekkorban nem kerültek felismerésre, vagy műtéti ellátásra.
- A szerzett (aquirált) sérvek későbbi életkorban jelentkeznek: a hasfal musculoaponeuroticus rétege nem képes ellenállni az intraabdominalis nyomásnak. Keletkezésüket elősegítheti bármely hasűri nyomásfokozódással járó kóros állapot (makacs köhögés, vizeletürítési zavarok, székrekedés, hasi tumor, elhízás, ascites, stb.), illetve idős korban a hasfalgyengülés önmagában is. A szerzett hasfali sérvek nagy része ún. posztoperatív, incizionális hernia. Kialakulásukért a hasüregi műtétek (laparotomiák) zárási vonalában lévő csökkent értékű hegszövet okolható (hegsérv). A baleseti eredetű sérvek megállapítására sok körülmény alapos mérlegelése szükséges.
Prognosztikai jellemzők
- A jól megválasztott és korrekten végzett műtéttel általában teljes gyógyulás érhető el. A recidíva esélye fokozott kollagén anyagcserezavarokban dohányzókon, tartós hasűri nyomásemelkedéssel járó állapotokban stb. (3)
- Műtét nélkül a sérv növekedhet, a panaszok fokozódásához vezethet, kizáródhat, minek következtében életveszélyes állapot alakulhat ki, azonnali műtéti indikációt, képezve, mely műtét után a szövődmények incidenciája exponenciálisan növekszik.
3.2. Panaszok/Tünetek
Sérv keletkezésekor a sérvkapu tájékán a beteg húzó, égő, nyilalló, feszülő vagy nyomó fájdalmat jelez, majd ezzel egyidőben, de gyakran csak később, egy kisebb-nagyobb elődomborodó terime is megjelenik. Ennek nagysága mozgásra, emelésre vagy hasprésre változhat, lefekvéskor megkisebbedik vagy eltűnik.
Repozíciót követően tapintható a nyitott sérvkapu. A beteg panasza és a sérv nagysága nem mindig fedik egymást: sokszor nagy sérvek sem okoznak jelentős panaszt, máskor kicsiny praeperitonealis zsírcsomó kicsípődése is (pl. femoralis sérvekben) jelentős fájdalommal járhat.
A sérvkizáródást (incarceratio) heves hasfali és hasi fájdalom, görcsök, bélelzáródás, akut hasi katasztrófa képe kísérheti. Ha időben nem történik műtét, a kizáródott sérvtartalom elhalhat.
1.4 Az irányelv ajánlásainak megvalósításához szükséges feltételek
4.1. Ellátórendszer szintje:
A sérvellátás sebészeti szakellátási feladat, a laparoszkópos technika és recidív sérvek megoldásának kivételével I-III. ellátási szinten végezhető.
A laparoszkópos technika, valamint a recidív sérvek sebészete csak a II-III. ellátási szinten alkalmazható.
4.2. Tárgyi és személyi feltételek
A tárgyi és személyi feltételeknek a 60/2003. ESZCSM rendeletben a sebészet számára megfogalmazott, adott szolgáltató típus és szint számára meghatározott szempontok szerint kell érvényesülniük.
II. AZ ELLATASI FOLYAMATLEÍRÁSA
11.1 Az ellátási folyamat algoritmusa
Az algoritmus a lágyéktáji és hasfali sérv tipikus eseteinek ellátásához ad útmutatást. Az ajánlások részletezése,
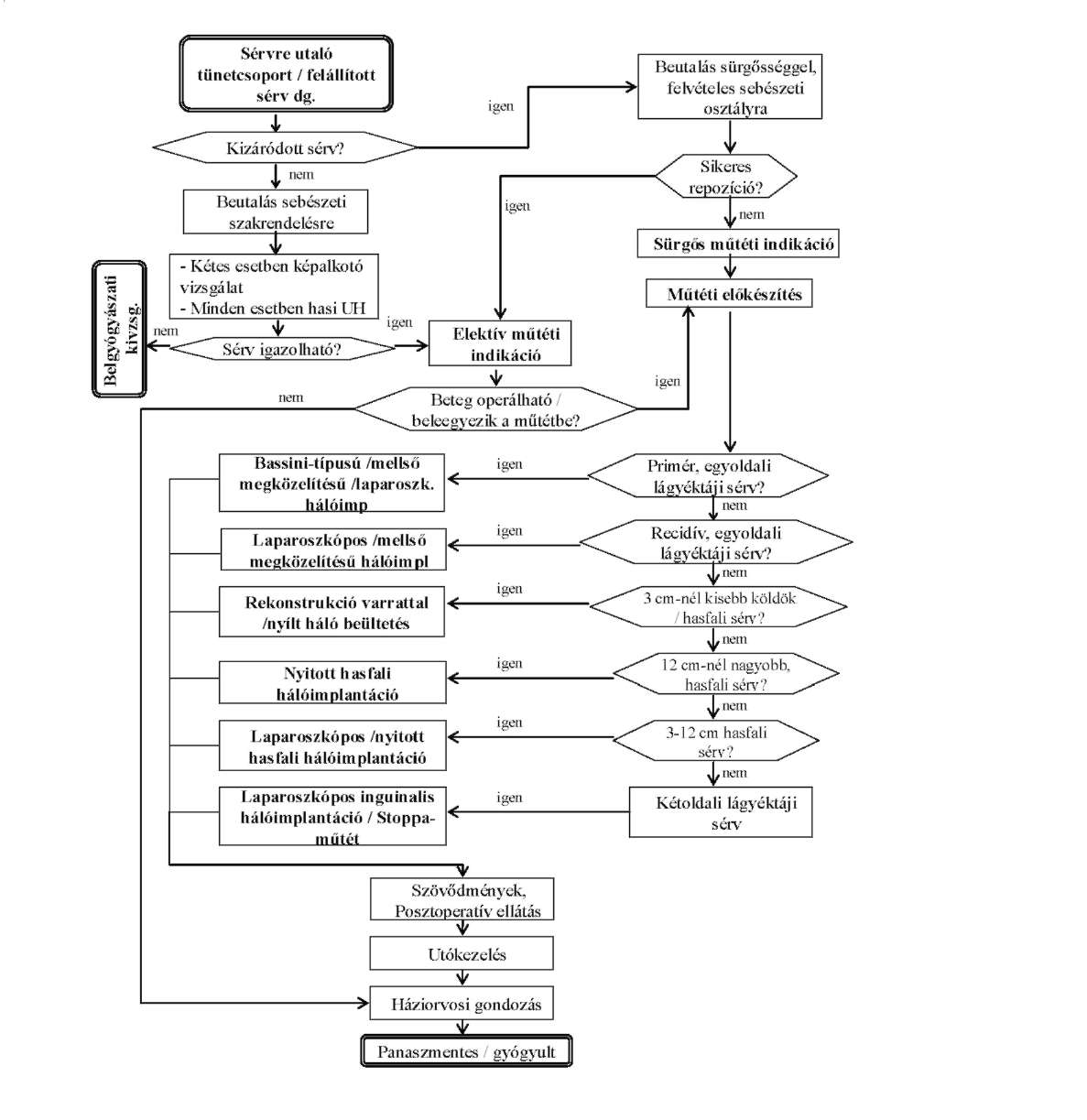
II.2 Az ellátási folyamat stratégiája
A lágyéktáji és hasfali sérv par excellence sebészi betegség, gyógyításának sine qua non-ja a hasfal rekonstrukciója. 2.1. Diagnózis felállítása, beutalás sebészeti szakellátásba
A legtöbb lágyéktáji és hasfali sérv egyszerű fizikai vizsgálattal diagnosztizálható, de esetenként szükség van képalkotó diagnosztika igénybevételére.
A diagnózis felállítása szakorvosi (háziorvos, belgyógyász, sürgősségi, sebész)feladat. A kizáródott sérv esetén meg kell kísérelni a repozíciót.
Az első észlelő szakorvos, felvetett diagnózis esetén előjegyzéssel, a sikeresen reponált vagy nem reponálható kizáródott sérv esetén pedig sürgősséggel, felvételes sebészeti osztályra utalja a beteget.
A beutalón fel kell tüntetni a-az egyébként is szükséges preoperatívinformációkon túl -a kórállapotjelentkezésének időpontját, kizáródás tényét és státuszát, lehetséges kiváltó tényezőket, célzott anamnézist.
III. Kezelés
2.2. Műtéti indikáció
- A felismert és szövődménymentes sérv műtéti javallatot képez.
- Kizáródott sérv sikeres repozícióját követően a beteg szoros obszervációja szükséges a visszahelyezett sérvtartalom nekrózisának, sérülésének, perforációjának lehetősége miatt, és mihamarabb javalljukaz elektív műtétet.
- Sürgős műtéti indikáció:
- nem reponálható kizáródott sérv és
- en block repozíció gyanúja (ha erőltetett visszahelyezési kísérlet következtében a sérvtartalom a leszakadt sérvkapuval - és így a továbbra is stranguláló gyűrűvel - együtt kerül a hasüregbe) esetén.
2.3. Műtéti előkészítés
- A sérvműtét speciális előkészítést nem igényel.
- Elektív műtétekesetében antibiotikus profilaxis csak magas sebfertőzési kockázatú betegeknél (mint pl. diabetes, immunhiányos állapot) jön szóba ("D" szintű ajánlás, 1++ szintű bizonyítékkal) (1,25)
- Ha a műtéti területen gyulladásos bőrjelenségek vagy gombás fertőzés észlelhető, akkor azok megfelelő kezelése után végezzük a beavatkozást (kivéve a sürgős műtéti indikációt).
2.4. A lágyéktáji sérvek kezelési stratégiája
2.4.1. Primer sérvek
- Primér sérvműtétek (kivéve a laparoszkópos műtéteket) az ellátás mindegyik szintjén, "egynapos" sebészi ellátás keretében is végezhetők.
- Csak primér sérvekben alkalmazhatók a feszülő varratokkal végzett rekonstrukciók (Bassini-típusú műtétek, Fabricius-műtét, Lotheissen-Reiche műtét, stb.).
- A mellső hálóimplantációs megoldások közül legelfogadottabb a Lichtenstein-műtét, mert a feszülésmentes (hálóimplantációs) technikának köszönhetően a recidíva alacsony (1% körüli), helyi infiltrációs érzéstelenítésben, és "egynapos" sebészeti ellátás keretében is végezhető.
- A laparoszkópos sérvműtét a korai teljes terhelhetőség igénye esetén, a laparoszkópos sérvműtét feltételeinek megléte mellett, a primér, egyoldali lágyéktáji sérvek elsőként választandó műtéti megoldása ("A" ajánlás, 1++ bizonyíték) (2;3,4,7,18). Laparoszkópos inguinalis sérvműtét után 7-10 nappal az operált teljesen terhelhető, eredeti munkáját folytathatja, fizikai munkát végezhet, sportolhat. Ez fontos szempont lehet sportolók, fizikai munkát végzők, utazók, sebészek, színészek, stb. primér sérvműtétjének megválasztásában.
- Hálóbeültetés utáni recidíva arány alacsonyabb, mint feszülő varratokkal végzett rekonstrukció után (29) (1++ bizonyíték)
2.4.2. Recidív sérvek
- Recidív sérvműtétek az ellátás magasabb szintjein, a II-III. szinten végezhetők.
- Recidív sérv csak hálóbeültetéssel műthető. Legjobb megoldás a laparoszkópos sérvműtét, mert ezen belső megközelítésű műtét során a belső hasfalon, érintetlen anatómiai környezetben, egy első műtét sikerének esélyével végezhető a rekonstrukció.
- Nyitott hálóimplantációk közül jó megoldás a Nyhus-, vagy Stoppa-féle hálóimplantáció.
- Feszülő varratokkal végzett műtét utáni recidívában újabb, ugyancsak feszülő varratokkal történő rekonstrukció nem végezhető a re-recidíva nagy esélye (30%) miatt.
- A mellső megközelítésű (hasfali feltárásból végzett), feszülésmentes hálóimplantációs műtétek közül a Lichtenstein-műtét, a musculoaponeuroticus rétegek kiszámíthatatlan összehegesedései miatt, nem ajánlható.
2.4.3. Bilateralis sérvek
Laparoszkópos hernioplastica TAPP módszere azért ajánlott, mert egyidőben mindkét oldalon, ugyanazon három trokáron keresztül, a betegre nézve érdemi többletterhelés nélkül végezhető a rekonstrukció.
2.4.4. Ellenoldali gyanított sérv esetén
Egyértelműen itt is a laparoszkópos sérvműtét ajánlható, mert lehetőséget kínál az ellenoldali rejtett sérv felismerésére, és egyidejű megoldására.
2.4.5. Ellátási szint:
- A laparoszkópos inguinalis sérvműtét ellátási szintje II-III.
- "Egynapos" sebészeti ellátás keretében kizárólag 20 órát meghaladó megfigyelési időszakkal végezhető ez az eljárás.
2.5. A hasfali sérvek kezelési stratégiája
2.5.1. Feszülő varratok
Feszülő varratokkal csak a kis (átmérő legfeljebb 3 cm) sérvek zárhatók. Ilyen választás lehet köldöksérvben a Spitzy vagy a Mayo műtét, illetve a kis paraumbilicalis, epigastrialis és posztoperativ sérvek suturája.
2.5.2. Nyílt vagy laparoszkópos hálóbeültetés
- A nagyobb, incizionális vagy recidív (6) hasfali sérvek biztonsággal csak háló implantációjával rekonstruálhatók. ("A" ajánlás, 1 + bizonyíték)
- A nyílt hálóbeültetéssel történő hasfali sérvrekonstrukció minden hasfali sérvnél ajánlható, de legfőképpen 12cm-nél nagyobb átmérőjű hasfali sérvek esetén. A hálóbehelyezési módszerek közül a háló sublay retromuscularis (peritoneum és az izom közé helyezett háló) pozícióba helyezése a legelőnyösebb eljárás. A beavatkozás csak II-III. szinten végezhető.
- A laparoszkópos hasfali rekonstrukció (laparoscopic ventral hernia repair=LVHR ) minden 12cm átmérőnél nem nagyobb hasfali sérvek esetén javasolt, de leginkább a 3 és 12cm közötti sérvnagyság esetén, szeparáló háló intraperitoneális beültetésével. Jó választás főleg az incizionális sérv esetén, amikor szatellit sérvesedés is fennáll.
2.5.3. Speciális esetek
- Kizárt hasfali sérvek esetén, ha nem áll fenn nekrózis, perforáció, gennyesedés, akkor a nyílt vagy laparoszkópos hálóimplantációnak nincsen akadálya. Ha fenti szövődmények közül bármelyikfennáll, hálóimplantáció csakakkor jön szóba, ha ez elkerülhetetlen. Laparoszkópos módszer azonban ezekben az esetekben nem ajánlott, csaka nyílt, kívülről kontrollálható (drainage, feltárás) eljárás.
- A parastomális sérvekesetén a fakultatív fertőzött környezet ellenére is a lokális anatómiához szabott (középen a bél körül öleléséhez ablakkal ellátott) háló implantáció jön szóba. A laparoszkópos eljárás előnye, hogy megkerülhető a stomával a fertőzött terület.
- Hasfali eventeráció megoldására a Rives-Stoppa eljárás (9,12,13) javasolt (a műtét II-III szinten végezhető).
2.5.4. Ellátási szint:
- A laparoszkópos hasfali sérvműtét ellátási szintje II-III.
- "Egynapos" sebészet keretében ezen eljárás nem végezhető.
2.6. Posztoperatív teendők
Posztoperatív hospitalizációs időtartamot (az operált emittálhatóságát) meghatározó szempontok:
- nincs bélműködési és vizeletürítési zavar,
- láztalan,
- relatív fájdalommentesség,
- zavartalan sebgyógyulás.
Teendők "egynapos" sebészeti ellátást követően:
- adequat fájdalomcsillapítás (pl. diclofenac)
- általános sebkezelés
- ágynyugalomra nincs szükség, az operált járkálhat, ezzel a tromboembóliás szövődmények is megelőzhetőek
2.7. Utókezelés Követés
- Gyulladás, váladékozás, sebszétválás, seroma/haematoma képződés, bélműködési zavar esetén, az esedékes kontrollon kívüli sebészi vizsgálat szükséges.
- Laparoszkópos műtétek után korai (7-10 nap) teljes terhelhetőség engedhető meg
- Hasfali feltárásból végzett műtétek után 6 hétig fizikai terhelés nem ajánlott Sebészeti ellenőrzés
- Műtét után egy hónappal sebészeti kontroll vizsgálat
- Záró sebészeti vizsgálat fél-1 év múlva
3. Diagnosztikai eljárások 3.1. Fizikális vizsgálatok
A legtöbb lágyéktáji és hasfali sérv egyszerű fizikális vizsgálattal diagnosztizálható.
3.2. Képalkotó vizsgálatok
Ha a sérv gyanúját felvető panaszok, tünetek és fizikális vizsgálat alapján a klinikai kép hátterében nem igazolható egyértelműen a lágyéktáji vagy hasfali sérv valamelyike, képalkotó diagnosztikára van szükség.
- Általános hasi UH vizsgálat: minden sérves betegen kötelező része a műtét előtti kivizsgálásnak, a rejtett társult betegségek (pl. cholelithiasis, gasztrointestinális tumorok) felderítése céljából, ami alapvetően módosíthatja a kezelési stratégiát
- Célzott hasfali UH vizsgálat
- Fizikális vizsgálattal egyértelműen nem tapintható sérvek (sérvgyanú) esetén pontosíthatja a dianózist. Segít elkülöníteni a kizáródott sérvet pathológiás nyirokcsomótól, hydrokelétől vagy egyéb tapintható terimétől.
- Inguinalis régió UH vizsgálata fekvő majd álló helyzetben, Valsalva manőver alkalmazásával 90%-os diagnosztikus szenzitivitással és specificitással rendelkezik a nem tapintható sérvek kiderítésére.
- A hasfali UH vizsgálat elsőként választandó képalkotó vizsgálati módszer a Spieghel -sérv kiderítésére. (30 - 3 bizonyíték)
- CT vizsgálat: Spieghel sérv gyanúja esetén, ha hasfali UH vizsgálattal nem egyértelmű a diagnózis (30 - 3 bizonyíték)
3.3. Diagnosztikus laparoszkópia
Sérvre jellemző makacs tünetek esetén, amikor a fizikális vizsgálattal és a képalkotó diagnosztikával sérv nem deríthető fel, diagnosztikus laparoszkópia végezhető, melynek pozitivitása esetén egyben laparoszkópos terápiás lehetőséget is kínál
3.4. Differenciáldiagnosztikai szempontok
- A hasfali lipoma, abscessus, tumor, cysta elkülönítése többnyire nem okoz nehézséget.
- Lágyéksérvekben a hydrokele testis, hydrokele funiculi spermatici és varicokele felismerése kíván némi tapasztalatot.
- Hasfali relaxatio a hasizmokat ellátó idegek sérülése (hasfalon végzett metszések) következtében alakulhat ki, és sérvesedéshez hasonló, hasprésre fokozódó, lapos elődomborodást okoz. Gondos vizsgálattal azonban megállapítható, hogy a hasfal kontinuitása nem sérült, sérvtartalom és sérvkapu nem tapintható.
- Rectus diastasis esetén a linea alba a felső median vonalban laminává szélesedik és elvékonyodik. Hasűri nyomásfokozódáskor a két egymástól eltávolodott musculus rectus abdominis között hosszanti, egyenletes elődomborodás mutatkozik. Ha funkcionális zavart okoz (hasűri nyomásfokozódással járó fizikai munkavégzés, sportolás) műtéti megoldással korrigálható.
4. Műtéti jellegű ellátás általános szempontjai
4.1. Műtéti érzéstelenítés
4.1.1. Inguinofemoralis sérvekben az érzéstelenítés függ a választott műtéti technikától.
- A Bassini-típusú, Lichtenstein- és háló-dugó műtétek helyi infiltrációs vagy gerincközeli (spinalis, epiduralis) érzéstelenítésben végezhetők, de a beteg kérésére vagy kellő kooperáció hiányában általános anesztézia mellett is dönthetünk.
- "Egynapos" sebészi ellátás esetén többnyire helyi érzéstelenítést alkalmazunk, mert gerincközeli érzéstelenítés után a vizeletürítési zavar és az éjjeli megfigyelés szükségessége gyakoribb. (31) ("A" ajánlás, 1+ bizonyíték)
- A laparoszkópos lágyéktáji sérvműtét és a Stoppa-műtét általános anesztéziát igényel.
4.1.2. Hasfali sérvekben
- Általában általános anesztéziát alkalmazunk
- Infiltrációs vagy gerincközeli érzéstelenítésben csak a kisebb sérvek varrattal vagy nyitott hálóbeültetéssel történő műtéteiben javasolható.
- Laparoszkópos technika alkalmazása esetén mindig általános anesztéziát alkalmazunk.
4.2. Általános műtéttechnikai szempontok
4.2.1. Sebészi anatómia
A vonatkozó információt a sebészeti műtéttani könyvekben találjuk meg. (9,12,13)
4.2.2. Valamennyi lágyéktáji és hasfali sérvben a rekonstrukció kétféleképpen történhet, a sérvkapu direkt zárásával (sutura), vagy a hiány pótlásával, melyhez autológ szövetet (fascia, irha, bőr, nyeles izomlebeny) vagy alloplasztikus anyagot (szövetbarát műanyagháló) használunk. A pótlás feszülésmentes (tension free) technikát jelent, szemben a többé-kevésbé feszülő varratokkal végzett műtétekkel. Elfogadott, varratokkal végzett rekonstrukció köldöksérvben, a Spitzy vagy Mayo műtét, illetve a kisebb paraumbilicalis, epigastriali és posztoperatív sérvek zárása
- Varrattal csak a kisebb, és így relatíve feszülésmentesen zárható sérvek rekonstruálhatók. A sérvsebészetben a feszülő varratok kerülése alapvető szabály, mert utánuk gyakori a recidíva (15-30%). (A feszülő varratok átvágnak -korai recidíva -, vagy a feszülő varratok mentén kialakult, csökkent értékű hegszövet nem képes ellenállni a hasüregi nyomásnak - késői recidíva -, a műtét után általában 2-5 évvel).
- Lágyéktáji egyoldali sérvekben primer műtétként elfogadható a Bassini-féle rekonstrukciók valamelyik formája, ezek közül leginkább a Sholudice-műtét javasolt.
- Inguinalis és femorális sérv együttes előfordulása esetén a laparoszkópos sérvműtét kontraindikációja esetén a Lotheissen-Reich féle műtét választandó.
4.2.3. A hálóbeültetés formái
- Onlay (ráfektető) technikában a protézis a musculoaponeuroticus rétegre kerül.
- Inlay módszerrel a hálófoltot a sérvkapu széleihez varrjuk.
- Sublay (retromuscularis) technikában a hálót a peritoneum és a musculoaponeuroticus réteg közé fektetjük. Amennyiben a peritoneum nem választható el a fasciától, az egyenes hasizom hüvelyét a mediális vonalban, hosszában meghasítjuk, az izmot felemelve mindkét oldalon felpreparáljuk az izom laterális széléig, és a hálót retromusculárisan az izomhas alá, az izom és a fascia közé helyezzük, egészen a lateralis izomhas széléig kiterítve. A háló szélét itt körkörösen rögzítjük, majd a hálóra az izmot ráfektetjük és az elülsö fasciát nem összehúzva, a szélét a hálóhoz egy ismételt öltéssorral rögzítjük/"double ring". Submusculárisan a háló és az izom közé, valamint subcutan elhelyezésben Redon zárt draint helyezünk
- IPOM technika a hálót intraabdominálisan a peritoneumra fektetjük.
Sublay és IPOM technika előnye, hogy a hálót, melynek helyzete praeperitonealis vagy intraabdominalis, a hasüregi nyomás is stabilizálja.
4.2.4. Intraabdominalis hálóimplantáció esetén ügyelni kell arra, hogy a háló belekkel vagy egyéb hasi szervvel közvetlen kontaktusba ne kerüljön, elkerülendő a háló irritatív hatása következtében kialakuló nem kívánatos reakciókat (adhaesio, penetratio, fistulaképződés, migratio, stb.). Mindez a háló és szervek közé illesztett peritoneum-vagy csepleszlebennyel megoldható. A speciálisan képzett (drága!) ún. szeparáló hálók (pl. titanium, proceed, parietex, expanded polytetrafluoroethylene, dual-mech, stb.) viscerális felszíne protektív réteggel van ellátva, mely nem, vagy alig irritáló hatású, és ezért a belekkel közvetlenül is érintkezhet.
4.2.5. A háló beültetés történhet laparoszkópos úton is (a laparoszkópos technika mindig hálóimplantációt jelent). A hasfali sérvek laparoszkópos rekonstrukciójában (laparoscopic ventral hernia repair = LVHR), és a laparoszkópos lágyéksérvműtét intraperitonealis onlay mesh (IPOM) módszerében a háló közvetlen kontaktusba kerül a belekkel, ezért ezen műtétek során csak a szeparáló hálók használhatók. A laparoszkópos lágyéksérvműtétek transabdominalis praeperitonealis (TAPP) és totalis extraperitonealis (TEP) formáiban, amikor a háló praeperitonealis, a belektől elzárt helyzetbe kerül, a mindkét felszínen "irritáló" hálók (polipropilen) is alkalmazhatók.
4.3. "Egynapos sebészet" szempontjai
- A helyi (infiltrációs) érzéstelenítésben végzett műtétek, mint a Lichtenstein vagy a Bassini-típusú műtétek az "egynapos ellátás" keretében mérlegelhetők.
- Az általános és gerincközeli érzéstelenítésben végzett műtétek "egynapos" ellátása csak 20 órát meghaladó megfigyelési időszakkal fogadható el. ("D" ajánlás, 4 bizonyíték)
- A laparoszkópos hasfali sérvműtét "egynapos" ellátás keretében történő végzése a magyar ellátórendszert támogató infrastruktúra mellett nem javasolt, mert ("D" ajánlás, 4 bizonyíték) a potenciális szövődmények lehetősége (vérzés, bél-, ill. hólyagperforáció) miatt tartósabb orvosi megfigyelés szükséges
- A laparoszkópos lágyéktáji sérvműtét "egynapos" ellátás keretében történő végzése kizárólag 20 órát meghaladó megfigyelési időszakkal fogadható el ("D" ajánlás, 4 bizonyíték)
5. Lágyéktáji (inguinofemoralis) sérvek műtéti ellátása
5.1. Hagyományos (varratokkal végzett) rekonstrukciók
5.1.1. Inguinális sérvek műtétei
- BASSINI műtét. (9,12,13) Lényege a sérvcsatorna hátsó falának erős, fel nem szívódó, csomós varratokkal való megerősítése. Nem ajánlott, magas recidiva aránya miatt. (2)
- SHOULDICE-műtét. A Bassini és a Bassini-típusú (Halstedt, Kirschner, Girard stb.) műtétektől eltérő, hosszútávú jó eredménye azzal magyarázható, hogy "átmenet" a feszülő és nem feszülő módszerek között. A tovafutó varratvonal feszülése egyenletesen megoszlik, eligazodika szövetekben; a felső - bőrhöz közelebb eső-varratsorokfesztelenítikaz alsóbbakat; többrétegűsége voltán pedig mintegy hálót imitálunk a sérvcsatorna hátsó falán (9,12,13).
A műtét előnyei:
- recidíva elfogadhatóan alacsony (1%)
- egyszerű a technikai kivitelezhetősége és csupán egy jó minőségű fonal (monofil, atraumatikus, nem felszívódó) szükséges hozzá,
- beavatkozás kis kockázatú,
- helyi érzéstelenítésben is végezhető.
A Bassini- és a Bassini-típusú műtétek (kivéve Shouldice műtétet) alapvető hátránya, hogy a m. obliquus abdominis internus feszülő varratokkal történő levarrásaa lig. inguinalehoz nem tekinthető fiziológiás beavatkozásnak, mert ez a két anatómiai struktúra élettani körülmények között egymáshoz képest szeparáltan létezik és finom elmozdulásokra képes. Másrészt az izomba helyezett feszülő varratok mentén fibrotikus degeneráció alakul ki, és a csökkent értékű hegszövet területén a műtét után évekkel (leggyakrabban 2-5 év múlva, de esetenként később) recidíva alakulhat ki. Átfogó statisztikák szerint a Bassini- műtétek után 10-15%-ban számolhatunk sérvkiújulással. Ez az arány még magasabb (a 30%-ot is elérheti) a recidivákban végzett hasonló típusú műtétek után. (2)
5.1.2. Femoralis sérvműtétek
A Fabricius-, Bassini-Kirschner-, Moschowitz- műtétek a femoralis sérvek megoldására szolgáló technikák, melyek a Bassini-típusú műtétek femoralis adaptációi. (9,12,13). Hátrányuk a magas recidíva, valamint, hogy az öltéssor a Poupart-szalag hátrafelé-lefelé húzásával kitágítja a külső lágyékgyűrűt, és kaput nyithat egy lágyéksérv keletkezéséhez. Preferálandó a laparoszkópos sérvműtét.
5.1.3. Inguinalis és femoralis sérvek együttes fennállása esetén
Nyitott műtétként alkalmazható a Lotheissen-Reich műtét, de itt is preferálandó a laparoszkópos sérvműtét.
5.2. Feszülésmentes technikával (hálóimplantációval) végzett lágyéktáji sérvműtétek
A hálóimplantációk-függetlenül attól, hogy a háló beültetése mellső (vagyis hasfali feltárásból végzett, nyitott) vagy hátsó (azaz laparoszkópos, zárt) megközelítésből történik - kiküszöbölik a feszülő varratokra visszavezethető nemkívánatos következményeket, mert a defektust nem zárjuk, hanem szövetbarát anyaggal pótoljuk. Ezenkívül a hálóimplantáció kivédi a sérvújdonképződés ún. metabolikus okait is: kísérletes munkákadatai szólnakamellett, hogy a kollagénképződés zavara - a legjobb sebészi technika és a legkiválóbb varróanyagok alkalmazása esetén is -recidívához vezethet. A feszülésmentes műtétek után a recidívák aránya csupán 1-2 %.
5.2.1. Nyitott műtétek
- LICHTENSTEIN műtét. A műtét lényege, hogy - elkerülendő a feszülő varratsort -, a canalis inguinalis hátsó falát szövetbarát anyagból készült háló implantációjával erősítjük meg (9,12,13). Egyszerűsége, és regionális, ill. helyi érzéstelenítésben történő alkalmazhatósága miatt "egynapos sebészi" beavatkozásként is elfogadott műtét.
- Nyhus-műtétben inguinalis feltárásból a hálót praeperitonealisan helyezzük el, közvetlenül a sérvcsatorna bemeneti kapujára fektetve.
- Stoppa- műtét. René Stoppa francia sebész a róla elnevezett műtétet az igen nagy, a recidívés a bilateralis sérvekre ajánlotta
- Háló-dugó ("plug") módszerek (Trabucco stb.): Az inguinalis és femoralis sérvek egyszerű és könnyen megtanulható műtéte. Lényege, hogy a sérvcsatornába megfelelő formában képzett háló-dugót tömeszelünk. A műtét szakirodalmi megítélése ambivalens: egyes szerzők kedvező morbiditási és recidíva adatokról számolnak be, mások a potenciális szövődmények miatt (a protézis kitapinthatóvá válik, minden irányban zsugorodva térfogatcsökkenés követeztében dugó-funkcióját elveszíti, elvándorol) alkalmazását nem javasolják.
5.2.2. Laparoszkópos inguinalis sérvműtét (LH)
A laparoszkópos sérvműtét a feszülésmentes technika minimálisan invazív módszerrel való alkalmazása: egyesíti magában a hálóbeültetés és a laparoszkópos technika valamennyi előnyét. A második leggyakoribb (cholecystectomia után) laparoszkópos műtét. Az alacsony recidivára (0.5%) és a korai teljes terhelhetőségre való utalással a laparoszkópos sebészek a lágyéksérvműtétek gold standardjának tekintik. Hazánkban jelenleg a laparoszkópiás lágyéksérvműtét társadalombiztosítási finanszírozása ugyanaz, mint a nyitott műtéteké. A gyakorlatban háromféle technika terjedt el, melyek a háló bevezetésének útja és elhelyezése tekintetében különböznek egymástól.
- Intraperitonealis onlay mesh (IPOM) technika. A legegyszerűbb laparoszkópos lágyéksérvműtét. Lényege, hogy transabdominalis úton a sérvtömlő bemeneti nyílására hálót borítunk, amit kapcsokkal rögzítünk a peritoneumhoz. Hátránya, hogy a háló a hasüregi szervekkel közvetlen kontaktusban marad, és ezért csak a viscerális felszínen protektív réteggel ellátott hálók használhatók, valamint hogy a laza peritoneumhoz kapcsolt háló könnyen elmozdulhat. Ennek következtében gyakoribb a recidíva. A másik két módszer kiszorította a gyakorlatból.
- Transabdominalis praeperitonealis (TAPP) technika. A leggyakrabban alkalmazott laparoszkópos sérvműtét. A műtét során a sérvtömlő bemeneti nyílása felett felhasított peritoneumot-éles és tompa preparálással - lelapozzuka lig. inguinale vonulata alá, miközben a sérvtömlőt a hasüregbe húzzuk. Függetlenül attól, hogy a betegnek milyen sérve van (külső vagy belső lágyéki, femoralis, vagy akár ezek kombinációja), a régió mindhárom sérvkapuját befedő, kb. 10x15 cm nagyságú hálót implantálunk. Ezáltal a potenciális sérvkapuk is zárásra kerülnek, és így megelőzhető egy későbbi sérvképződés ezen a területen. A hálót stabil anatómiai struktúrákhoz (fascia transversalis, lig.inguinale, lig.Cooper-i) kapcsoljuk, majd extra(prae)peritonizáljuk, azaz a hálót befedve rekonstruáljuk a peritoneumot. Szeparáló háló nem szükséges.
- Totális extraperitonealis (TEP) technika. A trokárokat nem vezetjük a hasüregbe, a preparálás végig a peritoneum és a fascia transversalis közötti praeperitonealis térben történik. Ennek képzéséhez felfújható ballon-katéter áll rendelkezésre. A háló nagysága és pozicionálása megegyezik a TAPP műtétével.
- A TAPP és TEP technika eredményességét összehasonlító randomizált kontrollált tanulmány alig nem áll rendelkezésre (32). A tapasztalatok szerint mindkét műtét teljesen hasonlóan jó eredményekkel jár, hiszen mindkét műtét lényege a praeperitoneális helyzetbe ültetett háló. A különbség csak a háló bevezetésének mikéntjében/útjában van: TAPP műtétben ez transabdominálisan, TEP műtétben pedig egy praeperitoneális tér kiképzését követően, végig extraperitoneális területen történik, a hasüregbe való behatolás nélkül. Hazánkban jelenleg a TAPP műtét terjedt el. A TAPP műtét előnyei a TEP műtéttel szemben ("D" ajánlás, 4 bizonyíték):
- Azáltal, hogy a hasüregben (és nem praeperitoneálisan) dolgozunk, az egész hasüreg áttekinthető, és okkult társuló betegségek felfedhetők, adott esetben endoszkóposan meg is oldhatók (adhaesiok, Meckel diverticulum, belső genitáliák, máj, epehólyag elváltozások stb.).
- Mivel a kamerával az egész hasüreget áttekintjük, az ellenoldali lágyéktájékon esetleg lévő, panaszmentes defektus nagyon jól láthatóvá válik. A kétoldal együlésben végzett rekonstrukciója megelőzi egy, egyébként 1-2 éven belül, akár sürgősséggel szükségessé váló, másik oldali sérvműtét beteg terheit és egészségügyi költségeit.
- A TAPP technika összenövésekkel gyógyuló nagy alhasi műtétek (prostatectomia, nőgyógyászati műtétek, stb.) után is végezhető, amikorTEP műtét biztosan nem, mert utóbbi esetében a praeperitoneális tér képzéséhez érintetlen hasfal szükséges.
A háló rögzítése történhet varrattal, kapcsokkal, legújabban fibrinragasztóval, vagy felszívódó kapcsokkal. A fibrinragasztó alkalmazása randomizált kontrollált tanulmányok eredménye szerint csökkenti a lábadozási időtartamot a fájdalom mérséklésével, a gépi kapocssorral szemben (a kapocssorral esetleg szorításba - "belövésre" került idegfonat neuralgiás fájdalmat okoz) (17;26) (1+;2+ bizonyíték). A műtétianyag költség kapocssor vagy fibrinragasztó alkalmazása esetén megegyezik, azonban a ragasztó alkalmazása hosszabb műtéti időt igényel.
A laparoszkópos lágyéksérvműtét előnyei. (18,22 bizonyíték)
- A posztoperatív jó komfortérzés alapja a minimális sebfájdalom. Ez annak köszönhető, hogy a hasfal belső felszínén, ahol a műtéti dissectio történik, érző idegvégződések alig találhatók.
- A korai teljes terhelhetőség a műtét leghatározottabb előnye: a beteg a beavatkozás után egy héttel eredeti munkáját folytathatja, akár fizikai munkát is végezhet, sportolhat.
- Bilateralis sérvekben (20-25%) ugyanazon három trokáron keresztül, szinkron operálható mindkét oldal, a beteg érdemi többletterhelése nélkül. TAPP technika alkalmazásakor az ellenoldali rejtett sérvek (10-12%) felismerhetők és egyidőben megoldhatók.
- Recidív sérvekben érintetlen anatómiai környezetben folyik a preparálás, és egy első műtét sikerének esélyével végezhető a rekonstrukció.
- A graduális és postgraduális képzésben jól demonstrálhatók a régió képletei, valamint egymás melletti viszonyukban a mediális és lateralis inguinalis, valamint femoralis sérvkapuk.
A laparoszkópos lágyéksérvműtét hátrányai.
- A laparoszkópos sérvműtét nem könnyű műtét, végzése csak egyéb laparoszkópos műtétekben szerzett kellő gyakorlattal rendelkező sebészi team kezében ajánlható.
- A sebészi anatómia is sokban különbözik a hagyományos műtétekben megszokottól.
- Elterjedésének további két gyakran hangoztatott akadálya az általános anesztézia igénye és a magas költségek. Ellenvetésként elmondható, hogy különbség van a műtét kórházi és szociális költségei között. Az utóbbiba ugyanis beleszámít a táppénzes napokszáma, és a munkából való kiesés "ára" is, de bele kell számolnunkegy esetleges recidíva újabb költségeit is. Így könnyen belátható, hogy nemzetgazdasági szempontból a laparoszkópos sérvműtét mégiscsak költségkímélőbb beavatkozás.
6. A hasfali sérvek műtéti ellátása
6.1. Hagyományos (varratokkal végzett) rekonstrukciók
6.1.1. SPITZY-műtét. A 3 cm-nél kisebb köldöksérvek műtéti megoldásaként javasolt technika (9,12,13)
6.1.2. MAYO-műtét. 3 cm körüli köldökés egyéb hasfali sérv esetén ajánlott, a hasfal tetőcserépszerű megkettőzésével járó eljárás (9,12,13)
6.2. Feszülésmentes technikával (hálóimplantációval) műtétek
6.2.1. Nyitott hálóimplantációk
A háló pozicionálásának lehetséges technikáit a II.4.2.4. pont írja le.
6.2.2. Laparoszkópos hasfali rekonstrukció (laparoscopic ventral hernia repair=LVHR) A laparoszkópos hasfali rekonstrukciók műtéti technikája:
Általános anesztéziában a pneumoperitoneum képzése után a sérv lokalizációjától függően laterálisan, a szemközti oldalon általában 3 trokárt alkalmazunk. A 10mm-es középső trokárba vezetjük az optikát. Az első az optikát vezető portnál fontos, hogy biztonsági trokárt használjunk a sérülések elkerülése végett. Ezt követően a szem ellenőrzése mellett tudjuk bevezetni a másik két trokárt, hogy a kamerától kellő távolságban (kb. 10cm) legyenek, a defektushoz viszonyítva tengelyük egymással közel merőleges szöget zárjon be. Ez a pozíció megkönnyíti az intraabdominalis manipulációt, az összenövések oldását, a sérvtartalom visszafejtését, az esetleges melléksérülések intraabdominalis laparoszkópos ellátását.
A laparoszkópos hasfali rekonstrukciónak elengedhetetlen feltétele a megfelelő minőségű, azaz intraabdominalisan jól pozícionáló és a legnagyobb trokáron behelyezhető, megfelelő nagyságú szeparáló háló. Fontos, hogy a háló a sérvkapu, illetve a sérvesedés széleinél minimum 3, de inkább 5cm-rel minden irányban túlérjen. A sérv illetve a sérvesedés területének méretét intraabdominalisan fonallal mérjük le. A kívülről való mérés fals eredményeket ad. A megfelelő méretű háló kiválasztása után, a háló széleibe általában 4-8-12 db. nullás prolene vagy PDS öltéseket előre behelyezünk, majd a háló pozícionálása után az előre behelyezett fonalakat fonal kihúzóval (endoclose) a hasüregből kihúzzuk, a bőr felöl 2mm-es bőrmetszésen át transfascialisan megcsomózzuk. Ezek kellő stabilitást, tartást biztosítanak, majd a háló széleit laparoszkópos kapocsrakóval a hasfalhoz klippeljük - egyrészt a tartást fokozva, másrészt, hogy a belek ne tudjanak a háló alá kicsúszni. A hálót a defektusok szélénél is klippekkel rögzíthetjük ("double ring"). Csomózásnál, klippelésnél az intraabdominalis nyomást 7-8 Hgmm-re leengedjük, a jobb rögzítés, valamint a klippelésnél szükséges ellentartás végett. A fonalkihúzó használata esetén ügyeljünk az arteria epigastrica inferior sérülésének elkerülésére. Kisebb sérvek és laza hasfal esetén a sérvkaput erős nem felszívódó intracorporalis öltésekkel is zárhatjuk a háló rögzítése előtt (Chelala módszer). Az eljárás azonban nem teljesen feszülésmentes. A sérvtömlő általában összehúzódik, tennivaló vele nem szükséges. Egyes esetekben a visszamaradó tömlőben seroma
képződhet, amit punkcióval tudunk kezelni. Nagyobb sérvtömlők esetén javasolható kis bőrmetszésből ennek eltávolítása a hasfal rekonstrukciója után. Drainálás nem szükséges.
A laparoszkópos hasfali hálóimplantáció előnyei (24,28,33) (3 bizonyíték):
- Hasfali dissectio nem történik, ezért mérsékeltebb a posztoperatív fájdalom, kevesebb a hasfali suppuratio, lerövidül a hospitalizáció és a rekonvaleszcencia ideje.
- A hasüregi összenövések felderítése és oldása laparoszkópos úton könnyebb és teljesebb.
- Alacsony a kiújulási ráta
- Alacsony az infekciós ráta
- Mind a funkcionális, mind az esztétikai eredmény jó
- Főleg incizionális sérvekben, a manifeszt, fizikális vizsgálattal is igazolt sérv mellett gyakran több, kisebb, occult sérvesedés is van (satellit sérvek), melyek csak laparoszkópos technikával deríthetők fel, és csak egy laparoszkóposan bemért nagyobb hálóval zárhatók biztonságosan.
- A háló a sérvcsatorna bemeneti nyílására kerül, minek okán - a nyitott sérvműtétek sublay helyzetű hálójához hasonlóan - az intraabdominalis nyomás is stabilizálja.
- Még kevés összefoglaló tanulmány hasonlítja össze a nyitott és laparoszkópos hasfali sérvműtét eredményességét, de az eddigiek szerint laparoszkópos technikával kevesebb a szövődmény, recidíva és a kórházi ápolás időtartama (23) bizonyíték)
A laparoszkópos hálóimplantáció hátrányai hasfali sérvműtéteknél (24,28,33) (3 bizonyíték):
A laparoszkópos hasfali plasztikához csak olyan háló használható, melynek viscerális felszíne protektív anyaggal védett, a belekkel érintkezve szövődményhez vezető reakciót (adhaesio, arrosio, penetracio, fistulaképződés) nem okoz. Ilyen hálók (parietex, proceed, dual mesh, titánium, composit, goretex, stb.) ma már nagy választékban állnak rendelkezésre, áruk rendkívül magas.
7. Műtéti dokumentáció szempontjai
A műtéti leírásban, a szokásos műtéti körülményeken túl az alábbi tények kiemelt jelentőségűek:
- Sérv jellemzői (oldaliság, nagyság, accret-jelleg, kizáródás ténye, sérvtartalom mibenléte és életképessége, hasfali sérv esetén satellit sérv jelenléte stb.)
- Hasüregi adhaesiok
- Háló jellemzői, a háló helyzete és rögzítésének módja
- Intraoperatív szövődmények és azok ellátása
- Műtét végén műtéti terület revíziója (mint mindig)
8. Műtéti és korai posztoperatív szövődmények
8.1. Érsérülések.
- A testicularis erek léziója a here sorvadásához vezethet.
- Bassini-, Schouldice- és Lichtenstein- műtétekben, a Poupart-szalag felöltésekor sérülhet az artéria vagy véna femoralis, Fabricius-műtétben a sérvkapu lateralis falát alkotó véna femoralis.
- Laparoszkópos inguinalis hernioplasticában ismerni és látni kell a "végzet háromszögét", ahol a ductus deferens és a testicularis erek által határoltan fut infraperitonealisan az artéria és véna iliaca externa, melyek sérülése konverziót igénylő erős vérzéssel járhat.
8.2. Bél-, és hólyagsérülések.
- A coecum, sigmabél és húgyhólyag sérülése par glissement sérvek preparálásakor, a vékonybeleké sérvtömlők megnyitásakor, ill. a tömlőbeli adhaesiók oldása során fordulhat elő.
- Laparoszkópos műtétekben diathermiás eszközzel (többnyire tanuló periódusban) nem áthatoló serosa sérülés okozható.
A bél- és hólyagsérülések ellátása a szokványos varrattechnikák valamelyikének alkalmazásával nem jelenthet nehézséget.
8.3. Tartós lágyéktáji fájdalom (inguinodynia).
Lágyék- és combsérvek után elhúzódó inguinalis fájdalmat okozhat az idegsérülésre visszavezethető neuralgia, az implantált háló zsugorodása, ostitis, periostitis, és ritkán, Lichtenstein-műtét után az interstitialis recidíva (sérvesedés a háló és hasfal között).
8.4. Idegsérülések.
- A műtét során okozott idegsérülések következménye a posztoperativ paraesthesia és neuralgia.
- Bassini-típusú műtétekés mellső megközelítésű hálóimplantációk végzésekor ügyelni kell arra, hogy a fascia és izomrostok között futó idegfonatokra varrat ne kerüljön, átvágásra, roncsolásra ne kerüljenek. E tekintetben a nervus iliohypogastricus és mellette laterálisan a nervus ilioinguinalis tekinthető veszélyeztetettnek.
- Laparoszkópos ingunalis hernioplasticában hálórögzítő kapocs kerülhet a ligamentum inguinale alatt közvetlenül haladó nervus cutaneus femoris lateralisra és a nervus genitofemoralis femoralis ágára. Ez utóbbi elkerülhető, ha a ligamentum. inguinalera és alá lateralisan, a "fájdalom háromszögébe" kapcsot egyáltalán nem helyezünk
A paraesthesia és neuralgia szerencsés esetben spontán vagy konzervativ kezelésre (B-vitaminok, fájdalomcsillapítás, helyi infiltrációs blokád) oldódik ill. elmúlik. Intenzív vagy perzisztáló fájdalom esetén műtéti megoldás (neurolysis, kapocskiemelés) indokolt.
8.5. Ostitis, periostitis.
Gyakrabban Bassini-típusú műtétek, ritkábban laparoszkópos inguinalis sérvműtét után, az os pubisba helyezett öltések vagy kapcsok által okozott szövődmény. Konzervatív kezelésre általában gyógyul.
8.6. Hydrokele testis et funiculi spermatici.
Kialakulásának oka az el nem látott vagy nem felszívódó serohaematoma, ill. a visszahagyott sérvtömlő. Megesik ugyanis, hogy az igen nagy, környezetéhez hegesedett sérvtömlő kipreparálása és rezekciója a rekonstrukció idején biztonsággal nem oldható meg, és azt a sebész egy későbbi időpontra halasztja.
Laparoszkópos ingunalis hernioplasticában elfogadott megoldás a nagy (srotalis) sérvtömlő műtét végére eső, külön kis metszésből való eltávolítása.
8.7. Másik sérv okozása.
Bassini-típusú műtétben a Poupart- szalag felfelé, Fabricius- műtétben hátrafelé-lefelé húzásával kitágulhat a szomszédos sérvkapu (a femoralis vagy a külső lágyékgyűrű), utat nyitva egy másik sérv keletkezéséhez. A Lotheissen-Reich-műtéttel, valamint hálóimplantációval egyszerre zárható mindkét sérvkapu.
8.8. Háló okozta szövődmények.
8.8.1. Hálóinfekció.
A műtéti terület fájdalmas infiltrációja, elhúzódó purulens váladékozás, sipolyképződés utal rá. Megoldás általában csak a háló műtéti eltávolításától várható, de nagy porozitású hálók esetén elégséges lehet a seb feltárása és lokális(antibiotikum,drenázs) kezelése. Újabb rekonstrukció csak a seb teljes feltisztulása után vállalható. Ha az implantátum pórus- és interstitium-mérete kisebb, mint 10 mikrométer (mindkét felszíni dimenziót tekintve, mint pl. fonott hálók, de fonott varróanyagok esetén is), akkor az átlagban 1 mikrométer méretű baktériumok elpusztítása lehetetlenné válik, mert a macrophagok és neutrophil granulocyták nem képesek a szűk pórusokon áthaladni. A phagocytákat és baktériumokat is egyaránt "beengedő", 10 mikrométernél nagyobb porozitású bioanyagok viszont akadályt képeznek a hálóinfekció kialakulásában és a mikroorganizmusok szaporodásában. Ezen túl, a nagyobb pórusméret gyorsabb fibroplasiát és angiogenesist is biztosít. Előfordul, hogy a megfelelő porozitású háló fertőződését, sipolyozását a rögzítésre használt polyphil varróanyag okozza.
8.8.2. Hálókilökődés.
A korszerű technikával és szövetbarát anyagokból készült műanyag háló kilökődése irodalmi ritkaság. Ha előfordul, az többnyire fertőzés következménye.
8.8.3. Üreges szerv eróziója, fistula képződése, a háló penetrációja, migrációja.
A hálóimplantáció súlyos szövődménye a protézis okozta erózió, a fistulaképződés, valamint a háló gyomor-béltraktusba, hólyagba, nagyerekbe történő penetrációja, migrációja. A szövődmény kialakulásával akkor kell számolni, ha a polypropylén háló peritoneum-, vagy cseplesz-fedettség nélkül érintkezik szervekkel, és kiemelten akkor, ha a háló körüli szövet állandó mozgásban van (mint pl. egy artéria pulzációja, vagy a gyomor, bél, ureter ill. hólyag peristalticája). A speciálisan képzett hálók (expanded polytetrafluoroaethylén,composix,titanium, dual mesh, proceed, parietex, stb.) visceralis felszíne védelmet jelent a hasüregi szövődmények kialakulásával szemben. Praeperitonealis hálóbeültetésekben fölösleges és ártalmas a retroperitonealis képletek (erek, ductus deferens) túlzott kipreparálása, mert ezáltal megfosztjuk azokat a védelmet jelentő zsír- és hártyarétegektől.
8.8.4. Béladhaesiók, posztoperatív ileus.
Az ideális háló legfontosabb jellemzője a makroporozitás és az érdes felszíni struktúra. Ezek a tulajdonságok együttesen segítik a hasfal kötőszövetes elemeinek prothesisbe történő penetrációját, a háló beépülését, azaz a rekonstrukció sikerét. De ha a háló irritativ hatása bélfalon érvényesül, ami a háló műtéti típushoz nem igazodó kiválasztása, vagy rossz pozícionálása következtében fordulhat elő, a nemkívánatos kitapadások, hegesedések, megtöretések passzázszavart, sőt ileust okozhatnak.
8.8.5. A háló zsugorodása.
Beültetés után a háló-folt 20%-nyit, a háló-dugó pedig méretének egynegyedére zsugorodhat, meghiúsítva ilyenformán a helyreállítás sikerét. A nagyfokban zsugorodó háló-dugó esetenként porchoz hasonló konzisztenciát vesz fel, kitapinthatóvá válik, elvándorol.
9. Gyógyászati segédeszköz
Sérvkötő alkalmazása akkor indokolt, ha a beteg műtétre alkalmatlan. Műtét helyett történő alkalmazása elvonja a beteg figyelmét a korszerű műtéti megoldásokról, veszélyezteti a beteg állapotát, ha kizáródás vagy stranguláció lép fel, mert a műtét nem történt meg megfelelő időben. (20)
A sérvkötő tartós használata egyébként is roppant teher a beteg számára: nemcsak kényelmetlen (nyom, elmozdul, bőrtüneteket, valamint esztétikai és higiénés gondokat okoz), hanem mozgás- és teljesítőképesség korlátozással is jár. A bőrt decubitálhatja, a sérvtömlőben és a sérvcsatornában hegesedések alakulhatnak ki, melyek a sérvtartalmat irreponábilissá teszik. Ilyenkor már értelmetlenné is válik a sérvkötő további alkalmazása, sőt megnehezíti egy későbbi műtét végzését. Minderre való tekintettel még idős és/vagy rossz általános állapotú betegeken is keresni kell a beteg szükségleteit jobban szolgáló műtéti megoldást. (20) Lágyéksérvműtétek után sérvkötő viselése nem indokolt. Hasfali sérveknél posztoperatív állapotokban javasolt. (2)
- A műtét után azonnal alkalmazva megelőzi a haematoma (mely egyébként infekcióforrás) kialakulását az első órákban.
- Posztoperatív 2 hónap során folyamatos használattal a hasizom működését támogatja recidíva veszély esetén, a háló beépülésének ideje alatt
- Magas recidíva hajlam esetén használata hosszútávon javasolt.
10. A beteg tájékoztatásának szempontjai 10.1. Választás az ellátási alternatívák közül
A tájékoztatás megfelelő tartalmú és formájú legyen ahhoz, hogy a beteg megalapozottan hozza meg döntéseit az ellátási folyamat azon pontjain, ahol megvan az alternatívák közötti választás lehetősége.
A tájékoztatást alapvetően a sebész szakorvos, aneszteziológiai kérdésekben az aneszteziológus végzi. A háziorvost be kell vonni a tájékoztatásba az ellátást elutasító betegek meggyőzéséhez.
10.1.1. Diagnosztizált, nem kizáródott sérv elektív műtéti indikációt jelent
A betegek egy része, különösen régóta fennálló, kevés panaszt okozó sérv esetén a műtétet elutasítja. Ilyenkor a kezelőorvos és a háziorvosa műtét elmaradásának negatív prognosztikai következményeire, veszélyhelyzetekre hívja fel a figyelmet. Hangsúlyozza, hogy a sérvkötő alkalmazása nem helyettesíti a műtétet, sőt lágyéksérvek esetén kockázatokkal jár.
10.1.2. "Egynapos" sebészeti ellátás lehetősége
Az "egynapos" sebészet keretében ellátható esetekben (primér, egyoldali inguinális sérv; 3 cm-nél kisebb, primér köldök és hasfali sérv) az "egynapos" ellátás általános és betegség specifikus szempontjairól kell tájékoztatni a betegeket:
- Műtét napján történő felvételből származó megszorítások (étel, ital, gyógyszerek)
- "Egynapos" ellátás keretében alkalmazható érzéstelenítés (lokális) hátrányai más lehetséges (gerincközeli, esetleg általános) érzéstelenítéssel szemben.
- Betegszállítási szükséglet és lehetőségek
- Korai posztoperatív teendők, ápolási szükséglet
10.1.3. Műtéti technika kiválasztása
Adott beteg kapcsán a kezelőorvos köteles tájékoztatni a beteget, milyen műtéttechnikai lehetőségek vannak az ő esetében, melyek közül az alábbi szempontok szerint kell választani (22)("A" ajánlás, 1++ bizonyíték)
- beteg állapota által megengedett érzéstelenítési módszer
- ellátásra kerülő sérv jellege (primér, recidív vagy kétoldali)
- adott sérv nyitott vagy laparoszkópos műtétre alkalmas
- a kezelőorvos jártassága a különböző módszerekben, különös tekintettel a laparoszkópos technikára
10.1.4. Korai terhelhetőség igénye esetén laparoszkópos műtéttechnika lehetősége egyoldali inguinális sérv esetén Amennyiben a korai (műtét után 7-10 nappal) terhelhetőség igénye (pl. sportoló) merül fel egyoldali inguinális sérv esetén, javasolható a laparoszkópos műtéttechnika, ha annak elvégzéséhez szükséges feltételek megvannak (tárgyi feltételekés megfelelő jártasság). A beteg választását befolyásolhatja, hogy ilyen műtéthez csak általános anesztézia alkalmazható. Ha helyben a feltételek nincsenek meg, a legközelebbi megfelelő ellátóhelyről kell tájékoztatni a beteget.
10.2. Adott ellátással kapcsolatos tájékoztatás
10.2.1. Általános műtéthez kapcsolódó tájékoztatás
- műtét előtti kivizsgálás lépései
- aneszteziológus tájékoztatása az érzéstelenítésről
- általános műtéti szövődmények lehetőségei
- közvetlen műtét utáni ellátások
- kórházi ápolás várható időtartama
- várható lábadozási időtartam
- otthoni ápolási szükséglet
- kontrollvizsgálatok gyakorisága, jellege
- "egynapos" sebészeti ellátás esetén ahhoz kapcsolódó általános tájékoztató
10.2.2. Kiemelt szempontok
Ld. IV. fejezetben a betegtájékoztató mintát.
IV. REHABILITÁCIÓ
V. AZ ELLÁTÁS MEGFELELŐSÉGÉNEK INDIKÁTORAI
1. Recidív sérvek ellátása
Mérés célja: külső értékelésre vagy önértékelés
STANDARD: Feszülő varratokkal végzett műtét utáni recidívában újabb, ugyancsak feszülő varratokkal történő rekonstrukció nem végezhető a re-recidíva nagy esélye (30%) miatt.
FELÜLVIZSGÁLATI SZEMPONT: adott beteg esetében varrattal végzett, ugyanolyan megjelenésű (inguinalis vagy hasi) és oldaliságú sérv recidívájának műtéte hálós technikával történik Adatgyűjtés: OEP finanszírozáshoz jelentett adatokból CÉLÉRTÉK: 100%
INDIKÁTOR:
Nevező: TAJ számmal azonosított, feszülő varrattal történt sérvműtéten (pl. inguinalis 55300/55320) átesett betegcsoport, akinél 5 éven belül ismét sérvműtét történik, ugyanazon az oldalon (55300/55310/55311/
55319/55320/55330/55331)
Számláló: nevezőben meghatározott csoportból azok száma, akinél a beavatkozás 55300/55320 volt
2. Feszülésmentes technika alkalmazásának aránya inguinális sérvműtét esetén Mérés célja: külső értékelésre vagyönértékelés
STANDARD: Hálóbeültetés utáni recidíva arány alacsonyabb, mint feszülő varratokkal végzett rekonstrukció után. FELÜLVIZSGÁLATI SZEMPONT: adott osztály adott ellátási időszakban végzett inguinális sérvműtétei közül hány %-ban végeztek hálóbeültetést Adatgyűjtés: OEP finanszírozáshoz jelentett adatokból
CÉLÉRTÉK: minimum 80%
INDIKÁTOR:
Nevező: vizsgált időszakban végzett sérvműtét esetei (55300/55310/55311/55319/55320/55330/55331)
Számláló: nevezőben meghatározott csoportból azok száma, akinél varrattal történt az ellátás (55310/55311/
55319/55330/55331)
3. Recidív vagy bilateralis inguinális sérvek hálóbeültetési technikája Mérés célja: önértékelés
STANDARD: Recidív vagy bilateralis inguinalis sérvek esetén a laparoszkópos technikával történő hálóbeültetés a "gold standard".
FELÜLVIZSGÁLATI SZEMPONT: laparoszkópos technika alkalmazására megfelelő feltételekkel rendelkező sebészeti
osztály, adott ellátási időszakban, recidív vagy bilateralis inguinalis sérv esetén végzett rekonstrukciója során hány
%-ban alkalmazta a laparoszkópos technikát
Adatgyűjtés: OEP finanszírozáshoz jelentett adatokból
CÉLÉRTÉK: minimum 40%
INDIKÁTOR:
Nevező: vizsgált időszakban, recidív (adatbázisban adott beavatkozást 2 évvel megelőző időszakban inguinalis sérvműtét szerepel) vagy bilateralis sérv (BNO oldaliság = U) esetén végzett műtét esetei (55310/55311/55319/
55330/55331)
Számláló: nevezőben meghatározott csoportból azokszáma, akinél laparoszkópos technikával történt a hálóbeültetés
(55311/55331)
4. Laparoszkópos technika alkalmazásának aránya 3-12 cm átmérőjű hasfali sérvek esetén Mérés célja: önértékelés
STANDARD: A laparoszkópos hasfali rekonstrukció minden 12cm átmérőnél nem nagyobb hasfali sérvek esetén javasolt, de leginkábba3és12cm közötti sérvnagyság esetén
FELÜLVIZSGÁLATI SZEMPONT: laparoszkópos technika alkalmazására megfelelő feltételekkel rendelkező sebészeti osztály, adott ellátási időszakban végzett, 3-12 cm átmérőjű, hasfali sérvműtétei közül hány %-ban végeztek laparoszkópos hálóbeültetést
Adatgyűjtés: ellátott esetek műtéti leírásából (méret meghatározása) adatlap alapján CÉLÉRTÉK: 40%
INDIKÁTOR:
Nevező: vizsgált időszakban, hálóbeültetéssel végzett, 3-12 cm átmérőjű sérv esetén végzett hasfali rekonstrukció esetei
Számláló: nevezőben meghatározott csoportból azokszáma, akiknél laparoszkóppal történt a hálóbeültetés
5. Nagyobb méretű illetve fokozott recidívahajlamú hasfali sérvek választott technikája Mérés célja: külső értékelésre vagyönértékelés
STANDARD: A nagyobb illetve fokozott recidívahajlamú hasfali sérvek biztonsággal csak háló implantációjával rekonstruálhatók.
FELÜLVIZSGÁLATI SZEMPONT: 3 cm átmérőjűnél nagyobb, illetve fokozott recidívahajlamú hasfali sérvek feszülésmentes technikával megoldott eseteinek aránya
Adatgyűjtés: ellátott esetek műtéti leírásából (méret és recidívahajlam meghatározása) adatlap alapján
CÉLÉRTÉK: minimum 90 %
INDIKÁTOR:
Nevező: vizsgált időszakban ellátott, 3 cm-nél nagyobb illetve fokozott hasfali sérvműtétek esetei
Számláló: nevezőben meghatározott csoportból azok száma, akiknél feszülésmentes technikával történt a műtéti
megoldás.
VI. IRODALOM
1. Irodalomjegyzék
1. Aufenacker, T.j.;Koelemay, M.J.W.;Gouma, D.J.; and Simons, M.P.: Systematic review and meta-analysis of the effectiveness of antibiotic prophylaxis in prevention of wound infection after mesh repair of abdominal wall hernia. British Journal of Surgery 2006; 93: 5-10
2. Bendavid R. Abdominal Wall Hernias. Springer-Verlag New York 2001.
3. Bendavid R :The Unified Theory of hernia formation. Hernia (2004) 8:171-176
4. Bittner R, Schwarz J, Kolb H. Hernioplastie d l'aine: cur coelioscopic TAPP. Le Jour de Coelio-chir 2006,59:5-10.
5. Chelala E, Elias B, Alle JL, Dessily M. Mesh outcomes and redo surgery after laparoscopic treatment of 620 ventral and incisional hernias. In: Bittner B. 18 Jahre. 1990-2007 Berlin Apfel Zet 2007;66-67.
6. den Hartog D, Dur AHM, Tuinebreijer WE, Kreis RW. Open surgical procedures for incisional hernias. Cochrane Database of Systematic Reviews 2008, Issue 3. Art. No.: CD006438. DOI: 10.1002/14651858.CD006438.pub2.
7. Estour E, Armand D, Begin GF, Berthou JC, Bruyns J,Cardin JLet al. La hernioplastie coelioscopiguegold standard de la reparation herniere, chirurgie d1élite? A propos de 43882 cas. Le Jour de Coelio-chir 2006;59:69-73.
8. EU Hernia Trialists Collaboration: Overview of randomized trials of inguinal hernia repair-a European Union Concerted Action. Surg Endosc(1999) 13:1030-1031
9. Gaál Cs.. Sebészet. 6. aktualizált és bővített kiadás. Medicina 2007.
10. Gál I., Bálint A, Szabó Z: Hasfali sérvek laparoscopos rekonstrukciójának eredményei - Eset kontrollált tanulmány.
Magy.Seb 2002; 55:290-4
11. Gyermeksebészeti Szakmai Kollégium: Az Egészségügyi Minisztérium szakmai protokollja a gyermekkori lágyéksérv kezeléséről. Egészségügyi Közlöny 2006. év 5. szám 2. kötet
12. Kiss J., Horváth Ő.P.: Sebészeti Műtéttan (Littmann sebészeti műtéttan nyomán) (2008 októberben még kiadás alatt)
13. Kiss János (szerk.): Gastroenterológiai sebészet. Medicina, Budapest
14. LeBlanc KA: Incisional hernia repair: laparoscopic techniques. World J Surg 2005; 29:1073-9
15. Licheri S, Erdas E, Pisano G, Garau A, Ghinami E, Pomata M. Chevrel technigue for midline incisional hernia: still an effective producere. Hernia 2008;12(2):121-126.
16. Lomato D, Iyer SG, Shabbir A, Cheaah WK. Laparoscopie versus open ventral herniamesh repair. A prospectiv study. Surg Endosc 2006;20:1030-1035.
17. Lovisetto F,Zonta S, Rota E, Mazzilli M, Bardone M, Bottero L, FaillaceG,Longoni M: Use of Human Fibrin Glue (Tissucol) Versus Staples for Mesh Fixation in Laparoscopic Transabdominal Preperitoneal Hernioplasty. Annals of Surgery Volume 245, Number 2, February 2007
18. McCormack K, Scott NW, Go PMNYH, Ross S, Grant AM, the EU Hernia Trialists Collaboration. Laparoscopic techniques versus open techniques for inguinal hernia repair. Cochrane Database of Systematic Reviews 2003, Issue 1. Art. No.: CD001785. DOI: 10.1002/14651858.CD001785
19. McCormack K, Wake B, Perez J, Fraser C, Cook J, McIntosh E, et al. Laparoscopic surgery for inguinal hernia repair: systematic review of effectiveness and economic evaluation. Health Technol Assess 2005;9(14)
20. McIntosh A, Hutchinson A, Roberts A, Withers H: Evidence-based management of groin hernia in primary care - a systematic review. Family Practice 2000; 17:442-447
21. Mouret PH. Coelio-hernioplastie: Gold Standard. Le Jour de Coelio-chir 2001;37:15-16.
22. National Institute for Clinical Excellence: Laparoscopic surgery for inguinal hernia repair. Technology Appraisal Guidance (www.nice.org.uk/TA083guidance). Issue date: September 2004 Review date: September 2007
23. Pierce RA, Spitler JA, Frisella MM, Matthews BD, Brunt LM: Pooled data analysis of laparoscopic vs. open ventral hernia repair:14 years of patient data accrual. Surg Endosc (2007) 21:378-386
24. Sanchez LJ, Bencini L, Moretti R: Recurrences after laparoscopic ventral hernia repair: result and critical review. Hernia 2004; 8: 138-43
25. Sanchez-Manuel FJ, Lozano-García J, Seco-Gil JL: Antibiotic prophylaxis for hernia repair. Cochrane Database Syst Rev. 2004;(4):CD003769.
26. Schwab R, Willms A, Kröger A, Becker HPLess chronic pain following mesh fixation using a fibrin sealant inTEP inguinal hernia repairHernia. 2006 Jun;10(3):272-7.
27. Az Egészségügyi, Szociális és Családügyi Minisztérium szakmai irányelve a bizonyítékokon alapuló szakmai irányelvek fejlesztéséhez. www.eum.hu; Egészségügyi Közlöny, 2004. január 22.
28. Sikorszki,L, Bezsilla J.,Botos1Á., Berecz J., ,Temesi R., Bende S.: Hasfali sérvek laparoscopos rekonstrukciója Magyar Sebészet, 2007(60)/4; 205-209
29. Scott N, Go PM, Graham P, McCormack K, Ross SJ, Grant A. Open Mesh versus non-Mesh for groin hernia repair. Cochrane Databaseof Systematic Reviews 2001/2008, Issue 3. Art. No.:CD002197. DOI: 10.1002/14651858.CD002197
30. VosDI,ScheltingaMR:Incidenceandoutcomeofsurgicalrepairofspigelianhernia:BrJSurg.2004May;91(5):640-4.
31. van Veen, R.N.; Mahabier, C.; Dawson, I.; Hop, W.C.; Kok, N.F.; Lange, J.F.; Jeekel, J.: Spinal or Local Anesthesia in Lichtenstein Hernia Repair: A Randomized Controlled Trial. Annals of Surgery. 2008. 247(3):428-433,
32. Wake BL, McCormack K, Fraser C, Vale L, Perez J, Grant A. Transabdominal pre-peritoneal (TAPP) vs totally extraperitoneal (TEP) laparoscopic techniques for inguinal hernia repair.. Cochrane Database of Systematic Reviews 2005, Issue 1. Art. No.: CD004703. DOI: 10.1002/14651858.CD004703.pub2.
33. Wéber Gy, Horváth ÖP: Hasfali sérvek műtéti kezelésének eredményei: varrattal, illetve háló beültetéssel (onlay vs.sublay) történő nyitott és laparoscopos hasfal rekonstrukció eredményeinek összehasonlítása (prospektív, randomizált, multicentrikus vizsgálat) MagySeb. 2002;55: 285-9
2. Kapcsolódó internetes oldalak http://www.mst.hu/Magyar Sebész Társaság honlapja http://www.eum.hu Egészségügyi Minisztérium honlapja, ahol az egészségpolitika / minőségfejlesztés menüpont alatt találhatóak meg a szakmai ajánlások, szakterületenként.
A szakmai irányelv érvényessége: 2010. szeptember 30.
VII. MELLÉKLET
1. Az irányelvfejlesztés módszerei
1.1. Az irodalomkeresés és kiválasztás módszerei
A szerzők elsődleges célja az volt, hogy bizonyítékokon alapuló szakmai irányelvet használjanak fel az ajánlások megfogalmazásához. Mivel ilyen tanulmány nem, vagy csak a témakör egy-egy kis elemére volt található, a jelenleg nemzetközileg elfogadott, 2001-es kiadású Bendavit-kézikönyvből indultak ki.
Második lépésben a 2000 óta megjelent, elektronikusan elérhető összefoglaló jellegű tanulmányok felkutatása történt meg. Itt alapvető szempont volt, hogy szisztematikusan készült összefoglalóról legyen szó (meta-analízis, szisztematikus összefoglaló), így elsődlegesen a Cochrane Kollaboráció összefoglalói kerültek értékelésre. Ha adott klinikai kérdésre nem volt elérhető szisztematikus összefoglaló, a kérdésre választ adó, legmagasabb szintű tanulmánytípus keresésére került sor (elsődlegesen randomizált kontrollált tanulmányok, randomizálás hiányában összehasonlító, multicentrikus vizsgálatok).
A keresés klinikai kérdéseken keresztül történt a PubMed és a Google keresők alkalmazásával. A tanulmányok eredményeinek felhasználása azok erősségének megfelelően, alapvetően a p-érték és a confidencia intervallum figyelembevételével történt, és nem a tanulmány következtetései alapján (számos esetben, még multicentrikus tanulmányok esetén is előfordult, hogy egyértelmű következtetést vont le a tanulmány nem szignifikáns különbségekből)
1.2. A tudományos eredmények adaptálásának módszerei
A tudományos bizonyítékok hazai alkalmazására megfogalmazott ajánlások esetében az alábbi szempontok kerültek figyelembevételre:
- Ellátórendszer szintjei, ehhez kapcsolódó sebészeti minimumfeltételek jogi szabályozása
- Jellemző betegirányítási szempontok.
- "Egynapos" sebészeti ellátás hazai körülmények (szolgáltató környezetében jellemző infrastruktúra fejlettsége, betegek jellemző elvárásai illetve egészségkultúrája; otthoni ápolási lehetőségek)
- Hazai sebészeti képzés szakképzés jelenlegi helyzete, különös tekintettel a minimál invazív sebészeti ellátásra.
1.3. A szakmával és érintett társszakmákkal való véleményezés és konszenzus
A szakmai ajánlás sebészeti szakterület részéről történő elfogadtatásának színtere elsődlegesen a Sebészeti Szakmai Kollégium és a Magyar Sebész Társaság. A szerkesztők a továbbiakban a Magyar Sebészet c. folyóiratban kívánják széleskörű szakmai vitára bocsátani.
Az érintett más szakterületekkel való véleményeztetést elektronikus konzultáció keretében végezték.
Az ajánlások egészségbiztosítási szempontból történő konzultációja folyamatos volt az Országos Egészségbiztosítási
Pénztár finanszírozási protokollok készítésével megbízott munkacsoportjával.
Az irányelv bevezetőjében feltüntetésre került, mely szakterületek egyetértését bírja a dokumentum.
Az irányelvet módszertanilag az Egészségügyi Minisztérium által megbízott szakértők konzultálták, a megállapításoknak megfelelően végezte el a módosításokat a szerkesztőbizottság.
1.4. A bizonyíték és ajánlás szintek meghatározása, magyarázata
A szakmai irányelv az Egészségügyi, Szociális és Családügyi Minisztérium szakmai irányelve a bizonyítékokon alapuló szakmai irányelvek fejlesztéséhez minisztériumi irányelv (27) szerinti bizonyíték és ajánlás besorolást alkalmazta. A felhasznált tanulmányok kritikus értékelése után az alábbi szempontok szerint történt meg a besorolása, ha pedig adott tanulmányban besorolt bizonyítékra hivatkoztak, akkor az adott besorolás adaptálása történt meg jelen besorolásra.
Az irányelv elején bemutatott ajánlás besorolás hátteréül az alábbi bizonyíték besorolás szolgál (27)
| 1++ | RCT-k jó minőségű meta-analízise vagy szisztematikus összefoglalója, vagy több, minimális szisztematikus hiba ("bias") valószínűségű RCT ugyanazzal az eredménnyel |
| 1 + | RCT-k elfogadható minőségű meta-analízise vagy szisztematikus összefoglalója, vagy több, kis szisztematikus hiba ("bias") valószínűségű RCT ugyanazzal az eredménnyel |
| bll- | RCT-k értékelhetetlen minőségű meta-analízise vagy szisztematikus összefoglalója, vagy magas szisztematikus hiba ("bias") valószínűségű RCT-k |
| 2++ | Eset-kontroll vagy kohorsz tanulmányok jó minőségű szisztematikus összefoglalója Jó minőségű eset-kontroll vagy kohorsz tanulmányok ugyanazzal az eredménnyel, melyekben minimális a hibalehetőség, és nagy az ok-okozati összefüggés valószínűsége |
| 2+ | Jó minőségű eset-kontroll vagy kohorsz t tanulmányok ugyanazzal az eredménnyel, melyekben kicsi a hibalehetőség, és mérsékelt az ok-okozati összefüggés valószínűsége |
| 2- | Elfogadható minőségű eset-kontroll vagy kohorsz tanulmányok ugyanazzal az eredménnyel, melyekben nagy a hibalehetőség, és kicsi az ok-okozati összefüggés valószínűsége |
| 3 | Az eredmények nem kísérleti tanulmányból származnak (esettanulmányok, esetsorozatok) |
| 4 | Az eredmények szakmai véleményen (szakmai kollégium, kutatócsoport, vagy a szakterületvezető egyéniségei) alapulnak. |
Megjegyzés:
++ Az adott tanulmány értékeléskor az alkalmazott kérdőív szinte valamennyi kritériumának megfelelt, vagy a nem megfelelő elemek nem befolyásolták lényegesen a tanulmány következtetéseit.
+ A kritikus értékelő kérdőív néhány kritériumának nem felelt meg a tanulmány, és a vizsgált kritériumnak nem megfelelő, hiányzó, vagy hiányosan kifejtett elemek nem valószínű, hogy befolyásolták a következtetéseket. - A tanulmány csak kevés, vagy egyetlen kritériumnak sem felelt meg, és a nem megfelelő, hiányzó, vagy hiányosan kifejtett elemek nagyvalószínűséggel befolyásolták a következtetéseket. A "-"jelzéssel rendelkező bizonyítékokat sohasem szabad ajánlás kialakítására felhasználni!
Az ajánlásokban a bizonyítékok hazai feltételrendszerben való alkalmazhatósága ugyanolyan erővel vesz részt, mint a támogató bizonyítékok besorolása, és előfordul, hogy a hazai ellátórendszer feltételei nem teszik lehetővé egy magas szintű bizonyíték gyakorlati alkalmazását, az ajánlások besorolása mellett a irányelv megadja annak bizonyíték hátterét is. (pl. "D" ajánlás 1+ bizonyítékkal).
Az irányelv Függelék fejezetében bizonyíték-tábla foglalja össze a felhasznált, jelentős tanulmányok eredményeit.
1.5. Az irányelv bevezetésének módszerei, feltételei
Az irányelv az Egészségügyi Közlönyben történő megjelenéssel hivatalossá válik. Az irányelv a sebészeti kötelező továbbképzés kötelező eleme. Az irányelv ajánlásaiból finanszírozási protokoll készül.
A sérvellátás minőségi önellenőrzésére az irányelvben javasolt indikátorok éves követése javasolt. A szakfelügyelet a sérvellátás szakmai hatósági ellenőrzése során jelen irányelvet veszi alapul.
1.6. Az irányelvfejlesztést támogató szervezetek, szponzorok
Az irányelv fejlesztését végző szakmai szakértők munkáját sem profit, sem non-profit orientált szervezet, semmilyen formában nem támogatta.
1.7. Az irányelv frissítésének módja
Az irányelv frissítéséért a Sebészeti Szakmai Kollégium a felelős.
Automatikus frissítés 3 évenként esedékes, a frissített dokumentum az Egészségügyi Közlönyben, minisztériumi honlapon, a Magyar Sebészet c. folyóiratban és a Magyar Sebész Társaság honlapján lesz elérhető. 3 éven belül akkor történik frissítés, ha valamely témakörben jelentős bizonyítékra derül fény, mely megváltoztatja valamely eljárás alkalmazhatóságát, vagy a magyar ellátórendszerben történik ilyen hatású változás.
AZ AJÁNLÁSOK ALKALMAZÁSÁT SEGÍTŐ SEGÉDANYAGOK, BETEGTÁJÉKOZTATÓK
Betegtájékoztató minta lágyéktáji és hasfali sérvműtétek esetén
A sérv az a kóros állapot, amelyben a hasfal valamelyik gyenge pontján hasi szervek türemkednek elő a hashártyát kiboltosítva. Elhelyezkedésük szerint megkülönböztetünk lágyéktáji (lágyék-, és comb-), valamint hasfali sérveket. A sérveknek úgynevezett kapuja van, amelyeken keresztül a hasűri nyomás különböző szerveket, leginkább bél vagy bélfodor, a sérvtömlőbe présel. Ez az úgynevezett sérvtartalom általában visszahelyezhető, ha ez nem lehetséges, akkor kizáródás áll fenn.
A sérvet csak műtéttel lehet gyógyítani. Kizáródás esetén sürgős műtétre van szükség, mely egyben életmentő is lehet, ha a kizáródott sérv tömlőjébe került bélszakaszt bélelhalás fenyegeti. Kizáródás nélkül - ha azt a beteg erőnléti állapota vagy az esetleges egyéb betegségei megengedik - egyeztetett időpontban javasoljuk a műtét elvégzését. Ilyenkor van idő a műtét előtti szükséges kivizsgálásra és előkészítésre.
A sérvműtét lényege: az előboltosuló sérvtömlő (hashártya) ellátása, és a hasi szervek visszahelyezése után a sérvkapu (hasfal tágult, gyenge pontja) zárása.
Mind a lágyéktáji, mind a hasfali sérveknél a sérvkapu zárása többféle módon történhet.
Lehetséges direkt varratokkal és lehet úgynevezett feszülésmentes technikával, hálóbeültetéssel.
A háló beültetéses sérvműtét kétféle eljárással oldható meg. Nyílt módszerrel, amikor a sérvkapu hálóval történő elzárását hasfali metszésen keresztül végezzük. A másik az úgynevezett laparoszkópos módszer, amikor a hasfalon nyílt, nagy sebzést nem ejtünk, hanem pici 0,5-1 cm-es bőrsebzéseken keresztül speciális eszközökkel végezzük a műtétet.
Műtéti érzéstelenítés: kisebb sérvek esetén - a legkisebb kockázattal járó - helyi érzéstelenítést is alkalmazhatjuk, nagyobb sérvek műtéte altatást vagy a gerinc közeli érzéstelenítő injekció használatát teszi szükségessé. Mint minden műtéti beavatkozásnak, a sérvműtétnek is van kockázata. Szövődmények léphetnek fel mind az érzéstelenítéssel, mind az operációval kapcsolatban.
Helyi szövődmények kialakulása esetén a sebben savó, vérömleny vagy akár genny is megjelenhet. Ezek a seb felnyitását tehetik szükségessé. Előfordulhat a szokásosnál nagyobb fájdalom (pl. idegvégződés izgalma a sebben), a seb duzzanata - lágyéksérv esetén - a here megnagyobbodása, érzékenysége. Általános szövődményként - egyéni hajlam alapjá - láz, visszérgyulladás, végtagi vénák vérrögösödése (ún. trombózis), hörgőgyulladás, tüdőgyulladás, tüdőembólia is felléphet. Nagy sérvek műtéte után bélösszenövés, ritkán bélelzáródás is előfordulhat. A szövődmények gyakoribbak ismételten operált betegeknél, szív tüdő, érrendszeri betegeknél, magas vérnyomásúaknál, anyagcsere betegeknél (p. cukorbetegség), időseknél, elhízottaknál, dohányosoknál, rendszeres alkohol és gyógyszerfogyasztóknál.
Késői szövődmények közül elsőnek a sérv kiújulását kell említeni. Bármilyen sikeres a műtét, ha a beteg idült légúti betegségben szenved, és állandó köhögéssel terheli a varratokat, ha nehezített vizelés, székelési erőlködés vagy hasvízkór folytán a hasüregi nyomás fokozódik, - a sérv kiújulási hajlama nő. Magas életkor, gyenge szövetek vagy a műtét utáni óvatlan mozdulat (erőlködés, elesés, stb.) is a kiújulást elősegíthetik.
Lágyéksérv műtétek után, későbbi szövődményként,férfiaknál ritkán heresorvadás is előfordulhat. Minél többször kell operálni egy sérvet, az eredmények - sajnos - egyre rosszabbak a kiújulás tekintetében.
A feszülésmentes technikák alkalmazása azonban a sérvek kiújulását minden esetben lényegesen csökkentik.
Természetesen a kockázat az orvos - beteg együttműködés javításával, az orvosi tanácsok betartásával is jelentősen csökkenthető.
Az előzőek tudomásulvételével, az operáló orvossal való egyeztetés alapján kérem, hogy rajtam *
a.) - nyílt sérvhelyreállító műtétet varratokkal,
b.) - nyílt feszülésmentes sérvhelyreállító műtétet hálóbeültetéssel,
c.) - laparoszkópos feszülésmentes sérvhelyreállító műtétet hálóbeültetéssel - végezzenek el. Dátum:
aláírás
Tanú
Megjegyzés: * A megfelelő rész aláhúzandó.
VIII. FÜGGELÉK
Bizonyíték tábla
| Beavatkozás | Megjelenés éve | Tanúim, típusa | Bizonyíték besorolás | Eredmény /Konklúzió | Tanulmány címe | Esetszám | Összehasonlítási alap |
| Inguinális sérvműtét technikája | 2001/20 08 | SR (Cochrane) | 1++ | Erős bizonyíték támogatja, hogy hálóbeültetés után 50-75 %-kal kevesebb a recidíva | 29. Scott N, Go PM, Graham P, McCormack K, Ross SJ, Grant A. Open Mesh versus non-Mesh for groin hernia repair. Cochrane Database of Systematic Reviews 2001/2008, Issue 3. Art. No.: CD002197. DOI: 10.1002/14651858.CD002197 | ?? | Feszülő varrat/ nyitott háló |
| Laparoszkópos inguinális sérvműtét | 2008 | SR (RCT) (Cochrane) | 1++ | ELŐNY: 1.Rövidebb lábadozási időszak 2. Enyhébb posztoperatív fájdalom HÁTRÁNY: 1. Műtéti időtartam kb. 15 perccel hosszabb. 2. Súlyos szövődmény gyakoribb (hólyag, érsérülés). NEM BEFOLYÁSOLJA 1. Recidíva arányt nem befolyásolja a laparoszkó-pos technika. | 18.McCormack K, Scott NW, Go PMNYH, Ross SJ, Grant AM, the EU Hernia Trialists Collaboration. Laparoscopic techniques versus open techniques for inguinal hernia repair. Cochrane Database of Systematic Reviews 2003, Issue 1. Art. No.: CD001785. DOI: 10.1002/14651858.CD001785 | 7161 | Nyitott hálóbeültetés |
| Laparoszkópos inguinális sérvműtét | 2007 | HTA (RCT) | 1++ | 1. Laparoszkópos műtét egyike az inguinális sérv műtéti megoldásának 2. A tájékozott beleegyezés érdekében meghatározott szempontok szerint kell a tájékoztatást nyújtani. 3. Laparoszkópos technikát csakjártas sebész véqezheti | 22. National Institute for Clinical Excellence: Laparoscopic surgery for inguinal hernia repair. Technology Appraisal Guidance (www.nice.org.uk/TA083guidance). Issue date: September 2004 Review date: September 2007 | nyitott háló/ laparoszkópos | |
| Laparoszkópos inguinális sérvműtét | 2005 | SR (Cochrane) | 1 + | 1. Egy RCT-t találtak, ez nem mutatott különbséget a TAPP /TEP között a műtéti időtartam, hematoma, kórházi ápolási idő, terhelhetőség időpontja és recidíva szempontjából 2. Nem randomizált tanulmányok szerint TAPP esetében több a port-hernia és szervsérülés, TEP esetében pedig több a konverzió | 32. Wake BL, McCormack K, Fräser C, Vale L, Perez J, Grant A. Transabdominal pre-peritoneal (TAPP) vs totally extraperitoneal (TEP) laparoscopic techniques for inguinal hernia repair.. Cochrane Database of Systematic Reviews 2005, Issue 1. Art. No.: CD004703. DOI: 10.1002/14651858.CD004703.pub2. | 1500 | TEP/TAPP |
| Laparoszkópos inguinális sérvműtét | 2005 | SR (RCT)/HTA | 1++ | 1 .Egyoldali inguinális sérvek esetében a nyitott hálóbeültetés olcsóbb, de alacsonyabb minőségi életévet (QALY) eredményez. 2. Kétoldali sérvek esetén a laparoszkópos technika költséghatékonyabb (csökkent műtéti időtartam és rövidebb lábadozási idő, magasabb QALY). 5. A laparoszkópos jártasság 50 beavatkozás elvégzése után alakul ki. | 19.McCormack K, Wake B, Perez J, Fräser C, Cook J, Mcintosh E, etal. Laparoscopic surgery for inguinal hernia repair: systematic review of effectiveness and economic evaluation. Health Technol Assess 2005;9(14). | 5560 | Nyitott hálóbeültetés |
| Beavatkozás | Megjelenés éve | Tanúim, típusa | Bizonyíték besorolás | Eredmény /Konklúzió | Tanulmány címe | Esetszám | Összehasonlítási alap |
| Háló rögzítési technika laparoszkópos inguinalis sérvműtétnél | 2007 | RCT | 1 + | Fibrinragasztó (Tissucol) alkalmazása TAPP során, gépi kapocssor helyett, csökkentette a műtét utáni fájdalmat (1,3 és 6 hónapban vizsgálva) (p<0,001), és csökkentette a lábadozási időszakot (p<0,001). | 17. Lovisetto F, Zonta S, Rota E, Mazzilli M, Bardone M, Bottero L, Faillace G, Longoni M: Use of Human Fibrin Glue (Tissucol) Versus Staples for Mesh Fixation in Laparoscopic Transabdominal Preperitoneal Hernioplasty. Annals of Surgery Volume 245, Number 2, February 2007 | 98/99 | gépi kapocssor /fibrinragasztó |
| Háló rögzítési technika laparoszkópos inguinalis sérvműtétnél | 2006 | eset-kontrol 1 | 2+ | A fibrinragasztóval történő rögzítés ugyanolyan eredményes volt, mint a kapocssorral való rögzítés. A fibrinragasztós csoportban alacsonyabb volt a krónikus fájdalom szindróma prevalenciája (p<0,002). | 26. Schwab R Schwab R, Willms A, Kroger A, Becker HPLess chronic pain following mesh fixation using a fibrin sealant in TEP inguinal hernia repairO;Hernia. 2006 Jun;10(3):272-7. | 86/87 | gépi kapocssor /fibrinragasztó |
| AB profilaxis inguinalis hálóbeültetés esetén | 2006 | MA (RCT) | 1 + | Inguinalis hernia műtét hálóbeültetéssel nem igényel AB profilaxist, különösen alacsony sebfertőzési rizikó mellett. | 1.Aufenacker,TJ; Koelemay,MJW; Gouma, DJ .and Simons,MP.: Systematic review and meta-analysis of the effectiveness of antibiotic prophylaxis in prevention of wound infection after mesh repair of abdominal wall hernia. British Journal of Surgery 2006; 93:5-10 | 990/993 | Placebo |
| AB profilaxis nyitott inguinalis sérvműtétekné 1 | 2004 | MA (RCT) | 1 + | Elektív inguinalis nyitott sérvműtétek esetén antbiotikus profilaxis nem javasolt, még magas sebfertőzési hajlam esetén sem. | 25. Sanchez-Manuel FJ, Lozano-Garcia J, Seco-Gil JL: Antibiotic prophylaxis for hernia repair. Cochrane Database Syst Rev. 2004;(4):CD003769. | 4128/25 77 | Ab nélkül |
| Anesztézia típusa Lichtenstein műtétben | 2008 | RCT(multic) | 1 + | 1 .Helyi érzéstelenítés esetén mérsékeltebb a műtét utáni fájdalom (p=0,021), rövidebb a műtéti idő (p< 0,001) 2. Spinál érzéstelenítés után gyakoribb a vizeletürítési zavar (p< 0,001), és az éjjeli megfigyelés szükségessége (p< 0,004) 3. A műtét utániaktivitásban nem volt különbség. | 31. van Veen, R.N.; Mahabier, C; Dawson, 1.; Hop, W.C.; Kok, N.F.; Lange, J.F.; Jeekel, J.: Spinal or Local Anesthesia in Lichtenstein Hernia Repair: A Randomized Controlled Trial. Annals of Surgery. 247(3):428-433 | 100 | Spinal / általános |
| Laparoszkópos hasi sérvműtét | 2007 | MA | 1++ | Laparoszkópos technikával kevesebb 1. a szövődmény (p< 0,0001), 2. a recidíva (p< 0,0001), 3. rövidebb ápolási idő (p< 0,0004), | 23..Pierce RA, Spitler JA, Frisella MM, Matthews BD, Brunt LM: Pooled data analysis of laparoscopic vs. open ventral hernia repair: 14 years of patient data accrual. Surg Endosc (2007)21:378-386 | 758/ 4582 | nyitott háló |
| Laparoszkópos hasi sérvműtét | 2007 | Retrosp. összehasonl ítás | 3 | Laparoscopos megoldás jelentősen csökkenti a szövődmények gyakoriságát, a kórházi ápolási időt, gyorsabb felépüléshez vezet, a nyílt műtétnél jóval alacsonyabb recidívaaránnyal jár, kozmetikailag kedvezőbb, lehetővé teszi incisionalis sérveknél a fel nem ismert kisebb sérvkapuk feltárását és fedését | 28. Sikorszki,L, Bezsilla J.,BotoslA., Berecz J., ,Temesi R., Bende S.: Hasfali sérvek laparoscopos rekonstrukciója Magyar Sebészet, 2007(60)74; 205-209 | 102/ 876 | Nyitott háló |
| Beavatkozás | Megjelenés éve | Tanúim, típusa | Bizonyíték besorolás | Eredmény /Konklúzió | Tanulmány címe | ||
| Incisionals hasfali sérv | 2008 | SR (Cochrane) | 1 + | 1 .Incisionals sérv megoldására sutura alkalmazása nem javasolt. 2. Nincs támogató bizonyíték arra vonatkozóan, hogy melyik hálóbeültetési (on-, sublay) módszert kell alkalmazni. | 6. den Hartog D, Dur AHM, Tuinebreijer WE, Kreis RW. Open surgical procedures for incisional hernias. Cochrane Database of Systematic Reviews 2008, Issue 3. Art. No.: CD006438. DOI: 10.1002/14651858.CD006438.pub2. | ||
| Spieghel sérv | 2004 | Retrosp. esetsorozat | 3 | Spigelian hernia is commonly encountered and requires surgical treatment because of the risk of strangulation. Operative treatment is simple and effective in the long term | 30. Vos DI, Scheltinga MR: Incidence and outcome of surgical repair of spigelian hernia : 0;Br J Surg. 2004 May;91(5):640-4. |
Az Egészségügyi Minisztérium
szakmai protokollja
A szemészeti szövődmények terápiájáról diabetes mellitusban
(1. módosított változat)
Készítette: a Szemészeti Szakmai Kollégium Összefoglalás
A diabetes mellitus szemészeti szövődményei a betegek közel egyharmadában lépnek fel, és minden tizedik cukorbeteg esetében súlyos látásromláshoz vezetnek. A kórképjelentőségét kiemeli, hogy hazánkban a diabeteszes retinopathia a második leggyakoribb vaksági ok. A multicentrikus vizsgálatok eredményei alapján a diabeteszes retinopathia és a vakság kivédésében döntő jelentőségű az optimális vércukor-, vérnyomás- és lipidbeállítás mellett a betegek korai szemészeti ellenőrzése és időben elvégzett szemészeti kezelése. A betegek szemészeti ellenőrzése a diabetes felismerésétől kezdve évente-félévente, majd praeproliferativ retinopathia esetén 2-4 havonta javasolt. Proliferativ retinopathia, valamint klinikailag szignifikáns macula-oedema esetén szemfenéki lézerkezelés sürgős elvégzése szükséges.
I. Alapvető megfontolások
1. Bevezetés
A diabetes szemészeti szövődményei gyakran vezetnek a legsúlyosabb szemészeti következményhez, a látás megromlásához, sőt elvesztéséhez is.1-4 Ausztráliában a statisztikai adatok szerint diabeteszes betegekben a retinopathia prevalenciája 21-36%, a látásromlással járó retinopathia prevalenciája pedig 6-13% közötti érték.5 A Wisconsin Epidemiologic Study of Diabetic Retinopathy szerint a diabetes mellitus 30 éves fennállása után csaknem minden betegben kialakul a retinopathia diabetica valamilyen formája, és a 65-74 év közötti diabeteszes betegek 14-20%-a vak.1,2 A retinopathia incidenciája az ausztrál diabeteszes betegekben 6-14% évente.5 Ehhez hasonló incidencia észlelhető hazánkban is (16%). Az 1996-2000. évekre vonatkozó, négy megyére kiterjedő vaksági statisztikai felmérés alapján Magyarországon évente kb. 1000 személy veszti el látását a cukorbetegség szemészeti szövődményei miatt, amely hazánkban a vakság második leggyakoribb oka54-56. A probléma súlyosságát jelzi, hogy a cukorbetegség eredetű vakság száma hazánkban növekvő tendenciát mutat54. A diabetes mellitus szemészeti jelentőségét tehát kiemeli, hogy ez a leggyakrabban vaksághoz vezető szisztémás betegség. A szemészeti tünetek többsége a microangiopathia következménye.
A diabetes mellitusnak számos más szemészeti tünete és szövődménye létezik, amelyeknek diagnosztikus és egyes esetekben a betegek életminőségét befolyásoló hatása is van. Ezeket a szövődményeket az 1. táblázat tartalmazza. A diabeteszes retinopathia szemészeti szűrésének, követésének, megelőzésének és kezelésének jól kidolgozottak az irányelvei, amelyek nagy multicentrikus vizsgálatok megalapozott eredményeire épülnek (2. táblázat). Az evidenciák alapján több országban szakmai irányelveket alkottak.5-8 Jelen irányelvben az említett vizsgálatok által megalapozott és a nemzetközi irányelvekben szereplő tényeket és ajánlásokat, a legfrissebb hazai vizsgálatok9-12 eredményeit és a Magyar Diabetes Társaság 2004. június 19-i konszenzus-értekezletén és a Szemészeti Szakmai Kollégium által 2005. június 3-án elfogadott ajánlásokat ismertetjük. A szerzők által javasolt legfrissebb aktualizálásokat a Szemészeti Szakmai Kollégium 2009. február 13-án fogadta el.
2. A retinopathia diabetica stádiumai és formái
A diabeteses retinopathia idővel változó mértékben valamennyi betegben kialakul. A retinopathia diabetica a következő stádiumokra osztható: 1. Praeretinopathia
A jól ismert szemfenéki elváltozások kialakulása előtt úgynevezett praeretinopathiás elváltozások lépnek fel a retinában, amelyek elsősorban a vérellátás hemodinamikájának megváltozását, illetve az érfal elváltozását jelentik, amely megbontja a vér-retina gát épségét.
2. Enyhe, illetve mérsékelten súlyos nonproliferativ vagy háttér-retinopathia
A második stádium alapjelenségei a retinalis microaneurismák, intraretinalis vérzések, lipoid (kemény) exsudátumok, puha exsudátumok (cotton-wool gócok, retinalis idegrost microinfarctus miatt) és oedema.
3. Praeproliferativ retinopathia (súlyos nonproliferativ retinopathia)
Az ischaemia fokozódásával a 2. stádiumban észlelt tünetek száma és szemfenéki kiterjedése nő, és átlépi azt a határt, amely fölött már súlyos nonproliferativ stádiumként definiáljuk (4:2:1-es szabály): 20-nál több intraretinális vérzés a négy kvadráns mindegyikében, vagy
- gyöngyfüzérszerű vénák kettő vagy több kvadránsban, vagy
- kifejezett IRMA (intraretinalis microvascularis abnormalitás) egy vagy több kvadránsban.
4. Proliferativ retinopathia
Ebben a stádiumban a papilla területéből kiinduló illetve a retina felszínén vagy annak síkjából kiemelkedve az
üvegtest irányába újonnan képződött erek nőnek, amelyek üvegtesti vérzés szövődményének lehetőségét hordozzák,
és trakciós látóhártya leválással fenyegetnek.
A proliferativ retinopathia alapjelenségei a következők:
Érújdonképződés
- NVD (neovascularization of the disc): Érújdonképződés a papillán, illetve papillától 1 papillányi sávban
- NVE (neovascularization of the retina elsewhere): Érújdonképződés a retinában, a papillától való távolság nagyobb, mint 1 papilla. A neovascularisatio kezdetben intraretinalis, majd áttörve a membrana limitans internát, a hátsó üvegtesti határfelszín és a membrana limitans interna között fejlődik tovább.
- NVI (nevascularization of the iris): érújdonképződés az irisen, a csarnokzugban vagy mindkettőn. Sub-ILM vérzés: A vérzés a membrana limitans internát választja le körülírtan a retina többi részéről. Subhyaloidealis (retrohyaloideális) vérzés: valódi preretinalis vérzés; vérzés az üvegtesti határmembrán és a membrana limitans interna között
Üvegtesti vérzés: Az üvegtesti gélben megjelenő vérzés. Retina leválás
- tractiós retina leválás
- kombinált, tractiós és rhegmatogen retina leválás
II. Diagnózis
1. Szűrővizsgálat
A cukorbetegek közül a retinopathiás esetek kiszűrése fontos népegészségügyi feladat. Tekintettel arra, hogy a cukorbetegekalapbetegségénekgondozása nem a szemészeknél történik, a retinopathia szűréséhez az alapbetegség kezelőorvosa (belgyógyász, diabetológus, endokrinológus, háziorvos) és a szemész szoros együttműködése szükséges. A diabetesz nagy volumenű szemészeti szűrésére az elmúlt évtizedben telemedicinális módszerek is alkalmazhatók.56
2. A cukorbetegek első szemészeti vizsgálata és ellenőrzése
Klinikailag és a szemészeti szövődmények megelőzéséhez nagyon fontos a cukorbetegek megfelelő időpontban történő szemészeti vizsgálata és a szükséges kezelések megfelelő időszakban való elvégzése. A fő irányelveket, és az ajánlások erősségét a 3. és 4. táblázat foglalja össze.
Az első szemészeti vizsgálatot-a hazai konszenzusnak megfelelően - a diabetes felfedezését követően közvetlenül el kell végezni. Ilyenkor részletes, tágított pupilla melletti, szemész általi vizsgálat szükséges.6 Az első szemészeti vizsgálat a következő elemekből áll:6
- legjobb korrigált látóélesség (A: I),
- szembelnyomás (A: III),
- gonioscopia (A: III),
- réslámpás elülső szegmens vizsgálat (A: III),
- a szemfenék hátsó pólusának térhatású vizsgálata, tágított pupilla mellett (A: I),
- a perifériás retina és az üvegtest vizsgálata (A: III).
3. Speciális kiegészítő vizsgálatok Fundusfotó
Hasznos eszköz az állapot rögzítésében, a progresszió megállapításában, a kezelésre adott válasz megítélésében. Fluoreszcein angiográfia
Nem rutinszerűen alkalmazandó eljárás, mivel réslámpa biomikroszkópos vizsgálattal a macula oedema, proliferatív elváltozások az esetek döntő többségében jól diagnosztizálhatóak. Elvégzése javasolt:
- A klinikailag szignifikáns mértékű macula oedema kezelésének tervezésekor
- Minden olyan esetben, amikor a látásromlás a szemfenéki kép alapján nem magyarázható (ischaemiás maculopathia feltárása)
- Kétes esetekben a neovascularisatio/ IRMA (intraretinális microvaculáris abnormalitás) elkülönítésében Ultrahang vizsgálat
Borús törőközegek, üvegtesti vérzés esetén elvégzése feltétlenül javasolt. Alkalmazása megfontolandó, ha indirekt szemtükrözés, réslámpa biomikroszkópiás vizsgálattal nem lehet pontosan kizárni a retina leválást. Optikai koherencia tomográfia
Ez a nem invazív módszer kitűnően alkalmazható a vitreoretinalis határfelszín, a retina, valamint a subretinalis tér állapotának vizsgálatában, egyes esetekben a vitreoretinalis műtétek indikációjának felállításában. Fontos kutatási eszköz a szemfenéki folyamat progressziójának, az alkalmazott beavatkozás hatékonyságának megítélésében.47,48
III. Terápia
A proliferativ retinopathia lézerbeavatkozással (fotokoaguláció), illetve bizonyos szövődmények esetén műtéttel kezelendő. A panretinalis lézerkezelés a perifériás retina destrukciója által csökkenti annak oxigénigényét és a vasoproliferativanyag(ok) felszabadulását. Hatására az újdonképzett erek regrediálnak, elhegesednek, csökkentve az üvegtesti vérzés veszélyét.13
A proliferativ diabeteszes retinopathia fokozott kockázatúnak (high risk) minősül a DRS (Diabetic Retinopathy Study Group) definiciója szerint, amennyiben megfigyelhető:
- egyharmad papillánál (papillányi területnél) nagyobb érújdonképződés a látóidegfőn vagy
- bármilyen méretű érújdonképződés a papillán, mely üvegtesti vagy praeretinalis vérzéssel társul vagy
- fél papilla területnél nagyobb érújdonképződés máshol (nem a papillán), amennyiben ez üvegtesti vagy praeretinalis vérzéssel társul.
Ilyenkor a látásromlás veszélye igen nagy, és sürgős panretinalis lézerkezelés szükséges, amelynek kedvező hatását nemzetközi vizsgálatok igazolták.1418 A fokozott kockázatú proliferativ retinophathia esetén a panretinalis lézerkezelés a jelentős látásromlás esélyét 45%-kal csökkenti négyéves nyomonkövetési idő alatt. A proliferativ retinopathia másik kezelési módja az üvegtest műtéti eltávolítása (vitrectomia), amelyet további szövődmények esetén végzünk, nevezetesen üvegtesti vérzés eltávolítása, illetve a látóhártyán tapadó fibrovascularis szövet eltávolítása céljából (membran-peeling), vagy kialakult látóhártya-leválás megszüntetésére. A vitrectomia során endolézerrel ezekben a szemekben is elvégzendő a panretinalis lézerkezelés.23-27 A vitrectomia nagy költség- és időigényű, bonyolult műtét, sok esetben szerény eredménnyel. Üvegtesti vérzés és iris rubeosis együttes fennállása ill a maculát fenyegető vagy érintő tractiós retina leválás esetén megfontolandó vitrectomia mielőbbi elvégzése, folyamat progressziójának megállítása, lassítása érdekében.
Mind a proliferatív retinopathia, mind a macula oedema kezelésével kapcsolatban vizsgálatok folynak az érújdonképződést gátló gyógyszerek (bevacizumab, ranimizumab) hatékonyságát illetően.
Macula oedema
A második stádiumtól kezdve bármelyik stádiumhoz kapcsolódhat diabeteszes maculopathia (macula-oedema vagy ischaemiás maculopathia) is. A diabeteszes macula-oedema a 2-es típusú diabetesben gyakoribb, és időseknél ez a látásromlás leggyakoribb oka. Külön kiemelendő a "klinikailag szignifikáns" macula-oedema fogalma, amelynek definíciója a következő:19
- a retina megvastagodása a fovea 500 mikronos körzetén belül, vagy
- kemény exsudátumok a fovea 500 mikronos körzetén belül, amennyiben retina megvastagodással járnak együtt, vagy
- legalább egy papillányi területű retinamegvastagodás, amelynek bármely része egy papilla átmérőnyire megközelíti a fovea centrumát.
Mivel a klinikailag szignifikáns macula-oedema esetén a további látásromlás veszélye jelentős, és (ugyanakkor) a kockázat lézerkezeléssel csökkenthető-amint azt nagy nemzetközi tanulmány (EarlyTreatment Diabetic Retinopathy Study- ETDRS) igazolta-a lézerkezelést minden betegnél, még jó látásélességű szemeknél is41 el kell végezni.19-21,42 Ez a kezelés lehet fokális, amely az aneurysmákat, szivárgó területeket látja el fluoreszcein angiográfia alapján, illetve lehet szabályos pontmintázatú, amely az oedemás terület pigmentepitheljére hat. Klinikailag szignifikáns macula-oedema esetén az enyhe látásromlás veszélyét 40%-kal csökkenti a macula lézerkezelése (hároméves nyomonkövetés tapasztalata).20,21
A diabeteszes maculopathia másik formája az ischaemiás maculopathia, amely az éleslátás területén a kapilláris keringés kiesését jelenti, és irreverzíbilis funkciókárosodással jár, amelyre nincs hatásos kezelés.21 A vitrectomia új indikációs területét képezik a macula-oedema azon esetei, amikor lézer fotokoagulációra rezisztens esetekben egyértelmű vitreomakuláris trakció mutatható ki.
Triamcinolon intravitreális injekciójánakalkalmazásával a macula oedema átmeneti, látványos javulását lehet elérni57, hosszú távon azonban ez nem bizonyult hatékonyabbnaka lézer kezelésnél59. Az új kezelési lehetőségek felderítésére és igazolására igen szerteágazó kutatások folynak, amelyeknek az irodalma is kiterjedt.49-50
IV. Rehabilitáció
Mint minden kétoldali súlyos látásromlás vagy teljes látásvesztés esetén nagyon fontos a rehabilitáció, amely visszaadhatja a beteg munkaképességét, visszaállítja az önálló életvitel lehetőségét, lehetővé teszi, hogy megszokott életmódjukat megváltozott élethelyzetükben is folytassák.58 Ez jelentheti látássegítő eszközök alkalmazását (optikai rehabilitáció: kézinagyító, távcsőszemüveg, olvasógép, elektronikus segédeszközök, stb), illetve ezekhez társulóan vagy függetlenül, a funkcionális látásvizsgálat és a beteg igényei szerinti látásrehabilitációt pld. kompenzációs technikák elsajátítása révén. Fontos a lelki segítségnyújtás, továbbá az is, hogy a látássérültek megismerjék szociális, egészségügyi, jogi, oktatási és művelődési lehetőségeiket.
V. Gondozás
Praeretinopathia esetén évente szükséges szemészeti ellenőrzés, háttér (enyhe, ill. mérsékelten súlyos nemproliferativ) retinophathia esetén pedig félévente, évente. Ilyenkor specifikus szemészeti kezelés még nem indokolt, nagyon fontos viszont az általános belgyógyászati, diabetológiai kezelés, és az optimális beállítás, amely vonatkozik mind a vércukor, mind a vérnyomás és a lipidstatus pontos kontrolljára.21,43-46
Praeproliferativ (súlyos, noproliferatív) retinopathia, illetve a "fokozott kockázatú" súlyosságot el nem érő proliferativ retinopathia esetén a fokozott kockázatú proliferativ retinopathia kialakulásának valószínűsége nagy, a 75%-ot is elérheti, ilyenkor 2-4 havonta szükséges az ellenőrző vizsgálat. Ezekben az állapotokban, amennyiben a beteg 2-4 havonkénti ellenőrzése nem biztosított, a panretinális lézerkezelés elvégzése indikált.6
Fokozott kockázatú proliferatív retinopathia és klinikailag szignifikáns macula-oedema esetén a megfelelő lézerkezelés haladéktalan elvégzése javasolt.6
Cukorbetegek terhessége esetén szemészeti vizsgálat szükséges a fogamzás előtt (A: I), az első trimesterben (A: I), majd a szemészeti állapot súlyosságától függően 1-12 hetente (A: III).6
A cukorbetegség szemészeti szövődményeinek kialakulásában és prognózisában döntő jelentőségük van a már korábban említett általános tényezőknek, az optimális vércukor-, vérnyomás- és lipidkontrollnak. Ezeket a tényeket multicentrikus vizsgálatokeredményei támasztják alá.2,21,22,30,31,36-40,43-46 Így a szoros vércukorkontroll 25%-kal csökkenti a microvascularis komplikációk számát. Fontos ismerni azonban azt a megfigyelést, hogy a szoros vércukor kontroll bevezetését követő első két évben a retinopathia progrediálhat.51
A HbA1c értékének 1%-kal való csökkentése 37%-kal csökkentette a szemfenéki lézerkezelés szükségességének számát. Ugyanakkor a vizsgálat azt is kimutatta, hogy az igen szoros vérnyomáskontroll 35%-kal csökkenti a fotokoaguláció szükségességét, és 10 Hgmm vérnyomáscsökkenés 11%-kal csökkenti a fotokoagulációra kerülő betegek számát. A diabeteszes retinopathia progresszióját befolyásoló további kockázati tényezőket az 5. táblázatban soroltuk fel.
Összefoglalva, retinopathia diabetica esetén az időben végzett, megfelelő lézerkezeléssel az esetek kb. 90%-ában megőrizhető a centrális látás.53 Jelenlegi tudásunk szerint, optimális vércukorbeállítás, vérnyomás- és lipidkontroll esetén, a jelenleg rendelkezésünkre álló és időben alkalmazott szemészeti kezeléssel a súlyos látásromlás 60%-ról 2% alá csökkenthető, továbbá a közepesen súlyos látásromlás több mint fele kivédhető.49 Ugyanakkor tudnunk kell, hogy a diabetes mellitus súlyos szemészeti szövődményeinek száma nem csökkent az optimálisan elérhető mértékben.53 Ennek oka kettős:
1. a vércukorszint, a vérnyomásérték, a lipidszintek eltérnek az optimálistól,
2. a betegek nem kerülnek időben szemészeti ellenőrzésre és kezelésre.
A panretinalis lézerkezelés perifériás látáskárosodást, látótérkiesést okoz, és éjszakai látászavarokkal is járhat, amely akár kizáró tényező lehet gépjárművezetésnél.18,53 Az evidenciákkal alátámasztott lézerkezelés célja a diabeteszes retinopathia folyamatának lassítása, a látásromlás csökkentése,. Ennek a tüneti kezelési módnak jellemzője, hogy javulás kevéssé várható, a microvascularis komplikációkat csak a normoglykaemia csökkenti. Ezért nagyon fontos az optimális diabetológiai beállítás és az, hogy a szemészeti kezelés időben megtörténjen. Sajnálatosan azonban a valóság ettől az ideális beállítástól eltér és az optimális időzítéstől elmarad. Angliában ismertté vált, hogy az első szemészeti vizsgálatkor a legtöbb betegnek már látásromlása volt.46,53 Így ma világszerte49 - és hazánkban is - a diabeteszes szemészeti szövődmények kivédésének legfőbb kihívása a cukorbetegek időben való azonosítása és azonnal szemészeti vizsgálatra való elküldése, szemészeti ellenőrzés alá vétele, szükség esetén pedig a lézerkezelés elvégzése, valamint az optimális diabetológiai beállítás megtalálása és fenntartása.
VI. Irodalomjegyzék
1. Klein, R, Klein, BE, Moss, SE: Visual impairment in diabetes. Ophthalmology 91:1-9,1984.
2. Klein, R, Klein, BE, Moss, SE, Cruickshanks, KJ: The Wisconsin Epidemiologic Study of Diabetic Retinopathy: XVII. The 14-year incidence and progression of diabetic retinopathy and associated risk factors in type 1 diabetes. Ophthalmology 105:1801-1815,1998.
3. Németh J, Süveges I: Vision 2020 - Világméretű program az elkerülhető vakság felszámolására. Szerkesztőségi közlemény a Látás napja alkalmából. Szemészet 138:115-117,2001.
4. PetőT, Jánó I, B.Tóth B, Dégi R, Kolozsvári L: A diabetes mellitus szerepe a vakság kialakulásában Csongrád megyében 1999-ben. Diabetol Hung 12: 51-55, 2004.
5. National Health and Medical Research Council: Management of Diabetic Retinopathy, Clinical Practice Guidelines. 1997. June
6. Preferred Practice Pattern, Diabetic Retinopathy, American Academy of Ophthalmology 2008. Elérhető: http://one.aao.org/CE/PracticeGuidelines/PPP.aspx
7. A retinopathia diabetica ellátása. (In: Hatvani I /szerk./: Az Országos Szemészeti Intézet módszertani útmutatója. OSZI, Budapest, 1999.) pp. 74-76.
8. Süveges I, Brooser G: A diabetes mellitus szemészeti szövődményei. (In: Halmos T, Jermendy Gy /szerk./: Diabetes mellitus. Elmélet és klinikum. Medicina Kiadó, Budapest, 2002.) pp. 424-449.
9. Bíró Zs, Kovács B: Diabeteszes maculaödéma "grid pattern" argon-laser kezelése. Szemészet 128: 73-75,1991.
10. Seres A, Papp A, Süveges I: A maculopathia diabetica lézerkezeléséről. Szemészet 137:163-171,2000.
11. Seres A: A diabétesz okozta vakság kezeléséről és megelőzéséről. Praxis 10: 56-58,2001.
12. Vámosi P, Berta A: Diabeteszes betegeken végzett panretinalis lézer-photocoagulatio hosszú távú követése, különös tekintettel a visus változására. Szemészet 136:257-261,1999.
13. Diabetic Retinopathy Study: Report number 6: design, methods, and baseline results. Report number 7: amodification of the Airlie House classification of diabetic retinopathy. Invest Ophthalmol Vis Sci 21:1-226,1981.
14. The Diabetic Retinopathy Study Research Group: Preliminary report on effects of photocoagulation therapy. Am J Ophthalmol 81: 383-396,1976.
15. The Diabetic Retinopathy Study Research Group: Photocoagulation treatment of proliferative diabetic retinopathy: the second report of Diabetic Retinopathy Study findings. Ophthalmology 85:82-106,1978.
16. The Diabetic Retinopathy Study Research Group: Four risk factors for severe visual loss in diabetic retinopathy. The third report from the Diabetic Retinopathy Study. Arch Ophthalmol 97:654-655,1979.
17. The Diabetic Retinopathy Study Research Group: Photocoagulation treatment of proliferative diabetic retinopathy: relationship of adverse treatment effects to retinopathy severity. Diabetic Retinopathy Study report N°. 5. Dev Ophthalmol 2: 248-261,1981.
18. The Diabetic Retinopathy Study Research Group: Photocoagulation treatment of proliferative diabetic retinopathy. Clinical application of Diabetic Retinopathy Study (DRS) findings, DRS report number 8.Ophthalmology 88: 583-600,
1981.
19. Early Treatment Diabetic Retinopathy Study Research Group: Photocoagulation for diabetic macular edema. Early Treatment Diabetic Retinopathy Study Report Number 1. Arch Ophthalmol 103:1796,1985.
20. Early Treatment Diabetic Retinopathy Study Research Group: Treatment techniques and clinical guidelines for photocoagulation of diabetic macular edema. Early Treatment Diabetic Retinopathy Study Report Number 2.Ophthalmology 94: 761-774,1987.
21. Early Treatment Diabetic Retinopathy Study Research Group: Focal photocoagulation treatment of diabetic macular edema. ETDRS Report Number 19. Arch Ophthalmol 113:1144-1155,1995.
22. Chew, EY, Klein, ML, Ferris, FL III, Remaley NA, Murphy RP, Chantry K, Hoogwerf BJ, Miller D, Early Treatment Diabetic Retinopathy Study Research Group: Association of elevated serum lipid levels with retinal hard exudate in diabetic retinopathy. ETDRS Report 22. Arch Ophthalmol 114:1079-1084,1996.
23. Diabetic Retinopathy Vitrectomy Study Research Group:Two-year course of visual acuity in severe proliferative diabetic retinopathy with conventional management.Diabetic Retinopathy Vitrectomy Study (DRVS) report 1.Ophthalmology 92: 492-502,1985.
24. Diabetic Retinopathy Vitrectomy Study Research Group: Early vitrectomy for severe vitreous hemorrhage in diabetic retinopathy. Two-year results of a randomized trial. Diabetic Retinopathy Vitrectomy Study report 2.Ophthalmology 103:1644-1652,1985.
25. Diabetic Retinopathy Vitrectomy Study Research Group: Early vitrectomy for severe proliferative diabetic retinopathy in eyes with useful vision. Results of a randomized trial. Diabetic Retinopathy Vitrectomy Study report 3. Ophthalmology 95:1307-1320,1988.
26. Diabetic Retinopathy Vitrectomy Study Research Group: Early vitrectomy for severe proliferative diabetic retinopathy in eyes with useful vision. Clinical application of results of a randomized trial. Diabetic Retinopathy Vitrectomy Study report 4. Ophthalmology 95:1321-1334,1988
27. Diabetic Retinopathy Vitrectomy Study Research Group:Early vitrectomy for severe vitreous hemorrhage in diabetic retinopathy. Four-year results of a randomized trial: Diabetic Retinopathy Vitrectomy Study report 5.Arch Ophthalmol 108: 958-964, 1990.
28. Diabetes Control and Complications Trial Research Group: The relationship of glycemic exposure (HbA1c) to he risk of development and progression of retinopathy in the Diabetes Control and Complications Trial. Diabetes 44: 968-983, 1995.
29. Diabetes Control and Complications Trial Research Group: Progression of retinopathy with intensive versus conventional treatment in the Diabetes Control and Complications Trial. Ophthalmology 102:647-661,1995.
30. Diabetes Control and Complications Trial Research Group: Lifetime benefits and costs of intensive therapy as practiced in the Diabetes Control and Complications Trial. JAMA 276:1409-1415,1996.
31. Diabetes Control and Complications Trial Research Group: The effect of intensive diabetes treatment on the progression of diabetic retinopathy in insulin-dependent diabetes mellitus. Arch Ophthalmol 113:36-51,1995.
32. Diabetes Control and ComplicationsTrial Research Group: The absence of a glycemic threshold for the development of long-term complications: the perspective of the Diabetes Control and Complications Trial. Diabetes 45: 1289-1298, 1996.
33. The Diabetes Control and Complications Trial/ Epidemiology of Diabetes Interventions and Complications Research Group: Retinopathy and nephropathy in platients with type 1 diabetes four years after a trial of intensive therapy. N Engl J Med 342: 381-389, 2000.
34. Epidemiology of Diabetes Interventions and Comlications (EDIC). Design, implementation, and preliminary results of a long-term follow-up of the Diabetes Control and Complications Trial Cohort. Diabetes Care 22:99-111,1999.
35. The Diabetes Control and Complications Trial/ Epidemiology of Diabetes Interventions and Complications Research Group: Retinopathy and nephropathy in patients with type 1 diabetes four years after a trial of intensive therapy. Am J Ophthalmol 129: 704-705, 2000.
36. UK Prospective Diabetes Study Group: Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38. BMJ 317:703-713,1998.
37. UK Prospective Diabetes Study Group: Intensive blood glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications inpatients with type 2 diabetes (UKPDS 33). Lancet 352:837-853, 1998.
38. UK Prospective Diabetes Study Group: Efficacy of atenolol and captopril in reducing risk of macrovasvular and microvascular complications in type 2 diabetes: UKPDS 39. BMJ 317: 713-720,1998.
39. Kohner, EM, Stratton, IM, Aldington, SJ, Holman, RR, Matthews, DR: Relationship between the severity of retinopathy and progression to photocoagulation in patients with type 2 diabetes mellitus in the UKPDS (UKPDS 52). Diabet Med 18: 178-184, 2001.
40. Kohner, EM, Aldington, SJ, Stratton, IM, Manley, SE, Holman, RR, Matthews, DR, Turner, RC: United Kingdom Prospective Diabetes Study, 30: diabetic retinopathy at diagnosis of non-insulin-dependent diabetes mellitus and associated risk factors. Arch Ophthalmol 116:297-303,1998.
41. Roldán-Pallarés, M, El Bromboly, TK, Vilar-Maseda, NF: Visual function after photocoagulation of diabetic macular edema with good visual acuity. Ann Ophthalmol 30: 361- 366,1998.
42. Akduman, L, Olk, J: Laser photocoagulation of diabetic macular edema. Ophthalmic Surgery and Lasers 28: 387- 408, 1997.
43. Klein, BE, Moss, SE, Klein, R,Surawicz,TS: The Wisconsin Epidemiologic Study of Diabetic Retinopathy. XIII. Relationship of serum cholesterol to retinopathy and hard exudate. Ophthalmology 98:1261-1265,1991.
44. Klein, R, Klein, BE, Moss, SE: Relation of glycemic control to diabetic microvascular complications in diabetes mellitus. Ann Intern Med 124: 90-96,1996.
45. Klein, R, Klein, BE, Moss, SE, Cruickshanks, KJ: Relationship of hyperglycemia to the long term incidence and progression of diabetic retinopathy. Arch Intern Med 154:2169-2178,1994.
46. Klein, R: Prevention of visual loss from diabetic retinopathy. Surv Ophthalmol 47 (Suppl): S246-S252,2002.
47. Hee MR, Puliafito CA, Duker JS: Topography of diabetic macular edema with optical coherence tomography. Ophthalmology 105:360-370,1998.
48. Nemes J, Somfai GM, Hargitai J: optikai koherencia tomográffal észlelt strukturális változásokdiabeteses maculopathia miatt végzett fotokoaguláció után Szemészet,141:41-44,2004.
49. Aiello, LM: Perspectives on Diabetic Retinopathy. Am J Ophthalmol 136:122-135,2003.
50. Fong, DS: Changing times for the management of diabetic retinopathy. Surv Ophthalmol 47 (Suppl): S238-S245,2002.
51. KROC Collaborative Study Group: Diabetic retinopathy after two years of intensified insulin treatment. JAMA 260:37, 1988.
52. Polak, BC, Dekker, JM, Moll, AC, Van Leiden, HA: Perspectives on diabetic retinopathy. Am J Ophthalmol 136:1193, 2003.
53. Kohner, E: Commentary: Treatment of diabetic retinopathy. BMJ 326:1024-1025,2003.
54. Németh J.,FrigyikA.,Vastag O.,Göcze P., PetőT., ElekI.: Vaksági okokMagyarországon. Szemészet 142:127-133,2005.
55. Németh J., Seres A.: A cukorbetegség szemészeti szövődményei. In: Winkler G. (főszerk.): Hatóanyagok, Készítmények, Terápia. Fókuszban a diabetológia. Melinda, Budapest, 125-131,2006.
56. Somfai G.M., Ferencz M., Fiedler O., Varga T., Somogyi A., Németh J.: Diabeteses retinopathia a XXI. Század elején: prevenció, diagnosztika és terápia. Magyar Belorvosi Archivum 62: 9-15,2007.
57. PappA., PregunT., Szabó A., Schneider M., Seres A., Vargha P., Hagyó K., Németh J.: Intravitreálistriamcinolon-acetonid a diffuz diabeteses macula-oedema kezelésében. Szemészet 144: 21-26,2007.
58. Németh J.: Tanácsadó Szolgálat a Látássérültekért Magyarországon. Szerkesztőségi közlemény. Szemészet 143: 137-138, 2006.
59. Diabetic Retinopathy Clinical Research Network. A randomized trial comparing intravitreal triamcinolone acetonide and focal/grid photocoagulation for diabetic macular edema. Ophthalmology, 2008 Sep;115(9):1445-6.
A szakmai protokoll érvényessége: 2010. szeptember 30.
VII. Melléklet
1. táblázat. A diabetes mellitus szemészeti szövődményei Extraocularis
- Szemhéj: blepharitis, xanthelasma
- Külső szemmozgató izmok: n. abducens (VI.) paresis, n. oculomotorius (III.) paresis
- Orbita: mucormycosis
- Conjunctiva: értágulatok Intraocularis
- Cornea: Csökkent cornea érzékenység, nehezen gyógyuló erosio, Descemet-membrán redők
- Elülső szemcsarnok: melanin-pigmentáció
- Glaucoma: Nyitott zugú glaucoma (diabeteses betegekben előfordulása gyakoribb), érújdonképződés következtében kialakuló másodlagos glaucoma.
- Rubeosis iridis (súlyos késői szövődmény, 0,25-10% az előfordulása)
- Sugártest: akkomodáció romlása
- Szemlencse: átmeneti myopia, senilis cataracta korai jelentkezése, diabeteszes hópehely cataracta
- Retinopathia diabetica
- Látóideg: Elülső ischaemiás opticus neuropathia, Akut papilla oedema
2. táblázat. A retinopathia diabetica lefolyását, megelőzését és kezelését vizsgáló multicentrikus tanulmányok 1980-1995 Wisconsin Epidemiologic Study of Diabetic Retinopathy (WESDR)1,2
1971-1975 Diabetic Retinopathy Study (DRS)13-18 1979-1990 Early Treatment Diabetic Retinopathy Study (ETDRS)19-22 1979-1990 Diabetic Retinopathy Vitrectomy Study (DRVS)23-27 1983-1993 Diabetes Control and Complications Study (DCCT)28-35 1977-1999 United Kingdom Prospective Diabetes Study (UKPDS)36-40
3. táblázat. Szemészeti ellenőrzések ajánlott időzítése diabeteszes betegekben6
1. Praeretinopathia: évente (retinopathia kialakulásának éves kockázata: 5-10%) (A: II)
2. Nonproliferativ retinopathia: 6-12 havonta (proliferatív retinopathia 4 éves kockázata: 16%) (A: III) Kivéve: Klinikailag szignifikáns macula-oedema: azonnali kezelés (A: I)
3. Praeproliferativ retinopathia: kontroll 2-4 havonként (A: I) vagy lézerkezelés (A: I) (proliferatív retinopathia éves kockázata: 75%)
4. Proliferativ retinopathia: azonnali kezelés (A: I)
4. táblázat. Szemészeti kezelések ajánlott időzítése diabeteszes betegekben6
1. Praeretinopathia: optimális beállítás (vércukor, vérnyomás, lipidek) (A: I). Lézerkezelés ebben a stádiumban nem indokolt (A: III)
2. Nonproliferativ retinopathia: optimális beállítás (vércukor, vérnyomás, lipidek) (A: I). Lézerkezelés ebben a stádiumban nem indokolt (A: III)
Kivéve: Klinikailag szignifikáns macula-oedema: azonnali lézerkezelés (A: I)
3. Praeproliferativ retinopathia: panretinalis lézerkezelés (A: I) Optimális beállítás (vércukor, vérnyomás, lipidek) (A: I)
4. Proliferativ retinopathia: panretinalis lézerkezelés (A: I), vitrectomia (A: III), Optimális beállítás (vércukor, vérnyomás, lipidek) (A: I)
5. táblázat. A retinopathia diabetica progresszióját befolyásoló kockázati tényezők4
- A kívánttól elmaradó glykaemiás kontroll
- Vesebetegség
- Magas vérnyomás
- Dyslipidaemia
- Anaemia
- Terhesség
- Étkezési rendellenességek
- Gastroparesis
- Elhízás52
Az Egészségügyi Minisztérium
szakmai irányelve
A felnőttkori szürkehályog diagnosztikájáról és kezeléséről
(1. módosított változat)
Készítette: a Szemészeti Szakmai kollégium
Tartalomjegyzék Rövidítések
VF14-Visualfunction
14 Bevezetés
1. Az irányelv általános meghatározása
1.1. Az irányelv fejlesztését indokoló tényezők
1.2. Az irányelv célja
1.3. Az irányelv célcsoportja
2. Az irányelvfejlesztés módszerei
2.1. Az irányelv készítői, érvényessége
2.2. Az irányelv fejlesztés módszerei
2.2.1. Bizonyítékok felkutatása
2.2.2. Bizonyítékok értékelése
2.2.3. Konszenzuson alapuló ajánlások
2.2.4. Konzultáció, konszenzuskialakítás társszakmákkal
2.2.5. Az irányelv hatásának értékelése
3. A főbb ajánlások összefoglalása
4. Klinikai háttér, epidemiológia
4.1. Rizikófaktorok
5. A katarakta preoperatív diagnosztikája
5.1. A katarakta felismerése és elsődleges diagnosztikája
5.1.1. Anamnezis
5.1.2. Látóélesség
5.1.3. Védőszervek vizsgálata
5.1.4. Szemmozgások
5.1.5. Szemnyomás mérés
5.1.6. Pupilla funkciók
5.1.7. Réslámpás vizsgálat
5.1.8. Szemfenék vizsgálat
5.1.9. Fakultatív vizsgálatok
5.2. űtéti indikáció
5.3. Az operáló orvos műtét előtti teendői
5.4. A beültetendő műlencse törőerejének megállapítása (Echobiometria)
5.4.1. Az echobiometria célja
5.4.2. Az echobiometria részei
5.4.3. Pontosság
5.4.4. Műszerezettség
5.4.5. Echobiometriai adatok
5.4.6. Az echobiometria elvégzése és az eredmény értékelése
5.4.7. Formulák
5.4.8. Ki végezze a biometriát?
5.4.9. Mikor kell a biometriát elvégezni?
5.4.10. Mi a teendő ha megbízható biometriai adatok nem nyerhetők?
5.5. Katarakta műtét előtti általános kivizsgálás
5.5.1. A család és/vagy a kezelőorvos által végzendő vizsgálatok
5.6. Általános érzéselenítés (altatás) esetén azanaesthesiológus feladata a katarakta műtét prae - intra és posztoperatív szakaszában
5.6.1. Betegvizsgálat
5.6.2. Anaesthesiológiai szempontok a különböző betegség csoportokban
5.6.3. Diagnosztikai vizsgálatok, általános premedicatio
5.6.4. Helyi érzéstelenítés
5.6.5. Általános érzéstelenítés
6. Műtéti technika
6.1. Intraocularis műlencsék
6.2. A műtéti gyakorlat megszerzése
6.3. Perioperativ infectio profilaxis
7. Intraoperatívés korai posztoperatív komplikációk
8. Késői posztoperatív komplikációk: A hátsó tok homályosodásának (PCO) kezelése
8.1. A Nd:YAG laser kezelés indikációja
8.2. A Nd:YAG laser kezelés komplikációi:
8.3. A Nd:YAG laser kezelés utáni követés:
9. Posztoperatív követés
9.1. Posztoperatív teendők
9.2. Posztoperatív ellenőrző vizsgálatok ideje
9.3. Az ellenőrző vizsgálatot végző személy
9.4. Az ellenőrző vizsgálat helye
9.5. Az ellenőrző vizsgálat elemei
10. A műtéti sikeresség (outcome)
10.1. A műtéti sikeresség kritériumai
10.1.1. A látási panaszok csökkenése
10.1.2. Látóélesség javulása
10.1.3. A tervezett refrakció elérése
10.1.4. Az életminőségjavulása (autóvezetés, munkaképesség)
10.1.5. Peri-és posztoperatív komplikációk
10.1.6. A lencse hátsó tokjának elszürkülése (PCO) Betegtájékoztató a szürkehályog (katarakta) műtétről
Műtéti beleegyező nyilatkozat szürkehályogos betegek részére A funkcionális károsodás mérésére szolgáló kérdőív (VF 14 alapján) Szakmai minimumfeltételrendszer Evidencia tábla Irodalom
Rövidítések
AAO - American Academy of Ophthalmology
ACL - Anterior Chamber Lens
ADVS - Activities of Daily Vision Scale
AMD - Age-related Macular Degeneration
ASCRS - American Society of Cataract and Refractive Surgeons
DM - Diabetes Mellitus
ECCE - Extra Capsular Cataract Extraction
EKG - Elektrokardiogram
HEMA - Hidroxy methyl metacrylate
Hb - Haemoglobin
Ht - Haematokrit
ICCE - Intra Capsular Cataract Extraction
IOL - Intraocular Llens
ISZB - Ischemias szívbetegség
ITN - Intratracheal narcosis
NCS - National Cataract Survey
ndYAG - Neodimium - Yttrium - Aluminium- Garnet
NEON - National Eyecare Outcomes Network
PCL - Posterior Chamber Lens
PCO - Posterior Capsule Opacification
PORT - Cataract Patient Outcomes Research Team
RPD - Retinopathia Diabetica
UV- Ultraviolet
VF14-Visual function 14
A szemlencse átlátszóságának vagy színének megváltozása optikai minőségváltozáshoz vezethet. A szürkehályog olyan lencseborússág, amely a látóélességet 0,6-re vagy ennél jelentősebb mértékben rontja (WHO definíció). A szürkehályogos beteg kezelésének elsődleges célja a látási funkció és az életminőségjavítása.
1. Az irányelv általános meghatározása
Az irányelv a felnőttkori (18 év feletti) szürkehályog diagnosztikájával és műtéti kezelésével foglalkozik. Az irányelv bizonyítékokon alapuló ajánlásokat tesz olyan szürkehályog műtéti megoldására, amely a beteg funkcionális állapotát kedvezően befolyásolja.
Az irányelv - a felnőttkori szürkehályog ellátására vonatkozó, - a kiadás időpontjában rendelkezésre álló tudományos és szakmai szempontok körültekintő mérlegelésén alapuló ajánlásokat tartalmaz. Az irányelv ajánlásai megfelelő helyi körülményekés feltételek (fizikai, személyi és szervezeti) esetén alkalmazhatók. Az irányelv ajánlásait az egészségügyi szolgáltató a beteg egyedi klinikai állapotának és az orvos egyéni preferenciájának ismeretében, önálló szakmai mérlegelés alapján használhatja.
1.1. Az irányelv fejlesztését indokoló tényezők
A szürkehályog műtét az egyik leggyakrabban végzett sebészeti beavatkozás. Az utóbbi néhány évben végbement változások (kis seb, varrat nélküli műtét, összehajtható, multifokális vagy tórikus lencsék alkalmazása) magyarországi elterjesztésének szükségessége indokolják az irányelvbevezetését.
1.2. Az irányelvcélja
Az irányelv általános célja a helyes klinikai gyakorlat valamint a betegellátás standardjainak meghatározása, és a műtét eredményességi kritériumainak megadása segítségével a modern szürkehályog sebészet kereteinek meghatározása.
Aszürkehályog műtét az ECOS (European Cataract Outcome Study) 2007 évi adatai adatai alapján az esetek több mint 83%-ban egynapos sebészet keretében történik. Az egynapos sebészet elterjedése Magyarországon is várható.
Az irányelv konkrét céljai:
- A szürkehályog felismerése és jellemzőinek meghatározása.
- Szempontok adása a szürkehályognak a beteg látására, funkcionális aktivitásra és életminőségére gyakorolt hatásának értékeléséhez.
- A beteg tájékoztatása a szürkehályog látásra gyakorolt hatásairól, a betegség természetes lefolyásáról, valamint a műtéti és nem műtéti beavatkozások hasznáról és kockázatairól, hogy a beteg megalapozott döntést hozhasson a kezeléséről.
- Ajánlások a szürkehályog műtéti előkészítésének és kezelésének módozataira
- Ajánlások a szürkehályogműtét aneszteziológiai vonatkozásairól.
- A kezelés sikerességét (outcome) meghatározó kritériumok megadása.
- Ajánlásoka posztoperatív kezelésre, rehabilitációra és a komplikációk ellátására.
1.3. Az irányelvcélcsoportja
Szemész szakorvosok, szemész rezidensek, szemészeti szakdolgozók, családorvosok és aneszteziológusok. 2. Az irányelvfejlesztés módszerei
2.1. Az irányelv készítői, érvényessége
Az irányelv a Szemészeti Szakmai Kollégium és az Országos Szemészeti Intézet ajánlása. Az irányelv fejlesztésében részt vett az Anaesthesiologiai és Intenzív Terápiás Szakmai Kollégium és az Országos Alapellátási Intézet. Az irányelv az Egészségügyi Minisztérium támogatásával készült. Az irányelvet az alábbi multidiszciplináris fejlesztő csoport állította össze.
A szakmai irányelv érvényessége: 2010. szeptember 30.
2.2. Az irányelv fejlesztés módszerei
Az irányelv nemzetközi, bizonyítékokon alapuló irányelvek ajánlásainak adaptációjával, és - ahol ez nem volt lehetséges - új bizonyítékok szisztematikus felkutatásával és értékelésével készült. Az irányelv készítésekor a bizonyítékokon alapuló irányelvfejlesztés szisztematikus módszertanát alkalmaztuk az Egészségügyi Minisztérium, valamint az országos TUDOR hálózat útmutatásai szerint. Az irányelvfejlesztés folyamata az alábbi lépésekből állt:
2.2.1. Bizonyítékok felkutatása
Szisztematikus irodalomkeresést végeztünk a fellelhető nemzetközi irányelv adatbázisokban. A keresés az elmúlt 5 évben (2002-2008) született irányelvekre irányult. Az irodalomkeresést a Medline és a Cochrane Library adatbázisokban végzett, a felnőttkori kataraktával kapcsolatos rendszerezett irodalmi áttekintésekre (systematic review), meta-analízisekre vagy randomizált vizsgálatokra vonatkozó keresés egészítette ki. Szisztematikus irodalomkereséssel 7 irányelvet, 10 rendszerezett irodalmi áttekintést és meta-analízist, továbbá 12 irodalmi összefoglalót találtunk. A fellelt szakirodalomból csak azokat az anyagokat választottuk ki, melyek teljesítették az alábbi kritériumokat:
Klinikai relevancia, azaz a felnőttkori katarakta sebészi kezelése (az egy-napos sebészeti kezelés kivételével) Magas rangú bizonyíték támasztja alá az ajánlásokat.
Explicit - lehetőség szerint bizonyítékokon alapuló - módszertan az ajánlások alátámasztására. Ezek alapján, a fellelt irányelvek közül két 1) a Brit Royal College of Ophthalmologists, és 2) az American Academy of Ophthalmology által 2001-ben kiadott, bizonyítékokon alapuló irányelv volt releváns, illetve felelt meg a módszertani és szakmai kritériumoknak. Az adaptáció megkönnyítése érdekében felkutattuk és felhasználtuk a felnőttkori szürkehályoggal foglalkozó hazai módszertani irányelvet és szakirodalmat.
2.2.2. Bizonyítékok értékelése
A kiválasztott irányelveket és szakirodalmat meghatározott szempontokat tartalmazó (TUDOR) kérdőív segítségével kritikus elemzésnek vetettük alá, és a bennük foglaltakat evidencia táblában összegeztük. Az egyes ajánlásokat alátámasztó bizonyítékokat rangsoroltuk, és az ajánlások erősségét a Scottish Intercollegiate Guidelines Network (SIGN) módszerei segítségével, az alábbi skálának megfelelően határoztuk meg:
| A bizonyítékok erőssége | Kategória | Ajánlási szint | Kategória |
| A bizonyítékok jól tervezett, randomizált, kontrollált klinikai tanulmányból származnak. Ide tartozik a randomizált tanulmányok meta-analízise is | I | Nagyon fontos ajánlás | A |
| Jól tervezett, kontrollált, de nem randomizált tanulmány Jól tervezett eset-kontroll tanulmány, lehetőleg több centrumból | II | Közepesen fontos ajánlás | B |
| Esettanulmányok Leíró tanulmányok Szakértői vélemények | III | Releváns, de nem fontos ajánlás | C |
| Konszenzuson alapuló | IV |
2.2.3. Konszenzuson alapuló ajánlások
Olyan esetekben, ahol nem találtunk az ajánlásokat alátámasztó bizonyítékokat, az irányelvfejlesztő csoport konszenzus véleményeit tüntettük fel. A megkülönböztető jel nélküli, egyszerű szöveges ajánlások konszenzuson alapulnak.
2.2.4. Konzultáció, konszenzuskialakítás társszakmákkal Aneszteziológiai és Intenzív Terápiás Szakmai Kollégium Háziorvostani Szakmai Kollégium
Országos Alapellátási Intézet Szemészeti Szakmai Kollégium
2.2.5. Az irányelv hatásának értékelése
Az irányelv hatásának vizsgálata helyi körülmények között, klinikai audit ciklusokban javasolt. Az irányelv használata során szerzett tapasztalatokat és észrevételeket az irányelv frissítésekor figyelembe vesszük. Ezért a szakmai észrevételeket kérjük a Szemészeti Szakmai Kollégiumnak hivatalosan megküldeni.
3. A főbb ajánlások összefoglalása
Ismeretes, hogy bizonyos rizikófaktorok megléte/tartós fennállása összefüggésbe hozható a szürkehályog kialakulásával. AII
A szürkehályog multifaktoriális megbetegedés, kialakulásában szerepet játszik a kor, a nem, táplálkozási szokások, szociális körülmények, alkohol fogyasztás, dohányzás, egyes betegségek, mint DM, hypertonia, UV sugárzás stb. A II Az operatőrnek tájékozódni kell a páciens általános állapotáról, esetleges allergiás epizódokról a család és/vagy kezelőorvos véleménye alapján is. Fontos a szemészeti anamnezis. AIII
Nincs speciális teszt arra vonatkozóan, hogy a praeoperativ látáséélességből következtetni lehessen a posztoperativ funkcionális eredményre. Ezért a látóélesség nem lehet alapja a műtéti indikációnak. AIII
Az AAO különböző speciális teszteket javasol a szubjektiv potenciális látóélesség (sztenopeikus lyuk, Maddox kereszt stb.), és az objektiv potenciális látóélesség felmérésére (elektroretinographia), de egyik sem szolgáltat jellemző adatokat a katarakta műtét eredményére vonatkozóan. AIII A páciens távoli, közeli látása, fényérzékelése lényeges az aktivitáshoz. AIII
A műtétre váró páciensnek jelezni kell, ha a praeoperativ vizsgálatok és a műtét között vizuális változás alakult ki. AIII Egyrészt a műtét elvégzésének esetleges anatómiai adottságok miatti nehezítettségét kell felmérni, másrészt az endophthalmitis rizikó faktoraira kell figyelmet fordítani (blepharitis, könnyszervek elváltozásai, könnyutak átjárhatósága stb.). AIII
Nystagmus, esetleges szemizom bénulások esetén az anaesthesia módját kell megtervezni. AIII
A biomikroszkópos vizsgálat
Pupilla tágítás előtt az elülső szegment állapotáról ill. esetleges kóros elváltozásairól ad felvilágosítást (cornea, csarnok, iris, pupilla, lencse helyzete, állapota). AIII
Pupilla tágítás után vizsgálandó a lencse, üvegtest, valamint előtét lencsével vagy direkt szemtükörrel a retina, különösen a macula állapota. AIII
A vizsgálatok elvégzése után minden esetben az operatőrnek kell felvilágosítást adni a tervezett műtét menetéről, az esetleges szövődményekről, a postoperativ kezelésről és életmódról valamint meg kell beszélni az érzéstelenítés lehetséges módjait. AIV
Phakoemulsifikació után a visus szignifikánsan jobb és stabilabb, kevesebb a komplikáció, kisebb a posztoperatív indukált astigmia, mint ECCE után./össszehasonlító randomizált tanulmány 1 éves követési idő./ AI - a lehető legkisebb, jól konstruált, kisfokú astigmiát indukáló seb készitése AI
A sebész a beteg szemészeti és általános betegségeit figyelembe véve választja meg a lencse típusát. AIII Szürkehályog műtét indokolt: AIII
a. ha a hályog a beteg vizuális funkcióit olyan mértékben rontja, hogy az a megszokott életvitelében zavarja.
b. Ha a hályog a szemfenék megítélését akadályozza vagy a feltételezett szemfenéki betegség gyógyítását gátolja.
c. ha a lencsehomályok a szemfenéki elváltozások pontos diagnózisát vagy kezelését akadályozzák. AIII Szürkehályog műtét kontraindikált: AIII
a. ha a beteg nem akarja
b. ha a beteg általános állapota nem teszi lehetővé a műtétet
A katarakta műtét előtt antibiotikum cseppnek nincs bizonyítottan profilaktikus hatása. CII
Kataracta műtét előtt adott fluoroquinolon tartalmu szemcseppek kombinálva povidon-iodine alkalmazásával signifikánsan csökkentik a conjunctiva zsák baktérium tartalmát A.I.
A szemhéj vagy a kötőhártyazsák leoltása csak bizonyos esetekben lehet indokolt műtét előtt. (pl. blepharitis, conjunctivitis). CII
Műtét előtt a szemöldökés a szemhéjakvalamint a szempillák 10 %-os Povidone iodine-nal való lemosása javasolt. A kötőhártya zsákot a műtét előtt 5 %-os Povidone iodine-nal kell átöblíteni két alkalommal. AII Ennél hígabb oldatban való alkalmazása csökkenti a baktérium colonizációt a posztoperatívperiodusban ha a műtét végén cseppentjük. Alkalmazása meggondolandó BII.
A műtét végén subconjunctiválisan adott antibiotikumnak nincs bizonyítottan profilaktikus hatása az esetleges endophthalmitis kivédésében. CII
Egy randomizált tanulmány adatai szerint phakoemulsificatio után az iris prolapsus előfordulása 0%, míg ECCE után 7.0 %. l éves követés után signifikánsan kevesebb komplikációt észleltek phakoemulsificatio után mint ECCE után. AI Azon lencséknél, melyeknek optikája un. vágott szélű, a PCO előfordulási aránya kisebb, viszont számolni kell nem kívánatos optikai jelenségek fellépésével (glare). AIII
A hátulsó tok homályosodásának effektív kezelése a YAG capsulotomia (lehetőleg minimum fél évvel a műtét után
kerüljön rá sor), melynek célja a látási funkció helyreállítása és a kontrasztérzékenység javítása. AIII
A katarakta műtétet végző orvosnak kötelessége tájékoztatni a beteget a lehetséges komplikációk tüneteiről, a szem
védelméről, a cseppentések módjáról, a kontrollok idejéről, és arról, hogy sürgős esetben hol látják el. AIII
Az endophtalmitis jeleiről (látóélesség csökkenés, növekvő fájdalom, fokozódó szemvörösség, szemkörüli duzzanat, váladékozás, újúszkáló homályok, fényérzékenység) fel kell világosítani a beteget, és ha ilyet észlel, azonnal forduljon szemészhez. AIII
Az orvos tájékoztassa a beteget a beteg felelősségéről, hogy kövesse az orvos tanácsait és utasításait a posztoperatív időszakban, és ha problémája van, azonnal értesítsen szemészt. AIII
Javasolt phacoemulsificatio után 4 hétig, extracapsularis katarakta extractio (ECCE) után 6 hétig 1%-os prednisolon acetetat használata csökkenő adagban. CIII
Varrat nélküli clear cornea sebek esetében a műtét napján, és azt követően quinolon tartalmu antibioticum csepp adása javasolt. Quinolon cseppek helyett Chloramphenicol/Bacitracin/neomycin /Polymixin is rendelhető (Profilaxis irányelvek:ESCRS study 2007)
A kontrollok idejét az operáló, illetve azt helyettesítő orvos határozza meg. AIII
Katarakta műtétet követően az első kontroll 24-48 órán belül, a második kontroll a 7-30. napon javasolt. CIII
Ha a műtét közben komplikáció lépett fel, akkor minden esetben egyedi elbírálás alapján történik a kontroll vizsgálatok idejének megállapítása. CIII
Minden posztoperatív kontroll tartalmazza a következőket: AIII
- Előző találkozás óta történt szemészeti események, a beteg panaszai
- Funkcionális látás megítélése (tesztek)
- Látási funkció mérése (nyers és korrigált látóélesség)
- Réslámpás vizsgálat
- Szemnyomás mérése
- Posztoperatív követési terv és gyógyszerelés megbeszélése.
A posztoperatív astigmatismus csökkenthető az esetleges varrat átvágásával, vagy eltávolításával a posztoperatív 4. héten. CIII
Soron kívüli vizsgálat akkor szükséges, ha szokatlan tünet, látásromlás, jelentkezik az esetleges késői szövődmények diagnosztizálására és kezelésére, vagy ha beteg bármit kérdezni akar. CIII
4. Klinikai háttér, epidemiológia
A szürkehályog olyan lencseborússág, amely a látóélességet 0,6-re vagy ennél jelentősebb mértékben rontja (WHO definíció, OSZI 1999).
A szürkehályog az életkor előrehaladtával egyre gyakoribb, általában kétszemes betegség.
A szürkehályog műtéti megoldása az egyik legeredményesebb sebészeti beavatkozás. Magyarországon a teljes populációra nézve nincsen értékelhető statisztikai adat a szürkehályog előfordulási gyakoriságát illetően. A rendelkezésre álló vaksági statisztikákban nincsenek külön feltüntetve a kataraktás betegekre vonatkozó adatok. Magyarországon az 1990-ben Beregi szerkesztésében jelent meg a "Centenariens in Hungary" című könyv, amelynek szemészeti fejezete Fürjes Éva munkája (Beregi, 1990). Egyetlen 100 éves betegnek sem volt teljesen tiszta a szemlencséje. Katarakta nuclearis fordult elő leggyakrabban 77/126 betegből. Nondummatur v. matur kataraktát találtak 41 beteg 50 szemén, ebből 9 betegnél teljes vakságot.).
Az AAO epidemiologiai adatai szerint az USA-ban az 55-64 év közötti nők 10%-nak, a férfiak 3,9 %-nak van kataraktája. A 65-74 év közötti nők 23,5%, a férfiak 14,3%-nak, mig a 75 év fölötti populációt tekintve a nők 45,9% és a férfiak 38,8%-nak volt kataraktája (Klein, 1992).
Salacz szürkehályog műtéttel kapcsolatos több évet felölelő statsztikai adatai szerint Magyarországon 1993-ban 22.398, 2001-ben 44.488, 2006-ban 64.207 hályogműtét volt (Salacz, 1994, 1997, 2000, 2002, 2007). Ezen adatok mögött nem feltétlenül a szürkehályog ilyen mértékű szaporodása áll, hanem a műtéti technika változásával a korábban, fiatalabb életkorban elvégzett műtétek állnak.
4.1. Rizikófaktorok
Ismeretes, hogy bizonyos rizikófaktorok megléte/tartós fennállása összefüggésbe hozható a szürkehályog kialakulásával. AII
A szürkehályog multifaktoriális megbetegedés, kialakulásában szerepet játszik a kor, a nem, táplálkozási szokások, szociális körülmények, alkohol fogyasztás, dohányzás, egyes betegségek, mint DM, hypertonia, UV sugárzás stb. (Facskó 1992,Christen 2001, Leske 1999, Delcourt 2000, Mchkarthy 1999, Hammond 2001,Taylor 1999, West 1989). AII Noha ezen rizikófaktorok szerepe ismert, hatásos prevencióval manapság még nem rendelkezünk. Jelenlegi tudásunk szerint nincs olyan gyógyszer, amely a szürkehályog kialakulását, biztosan megelőzné vagy a kezdeti stádiumban levő korhoz köthető szürkehályogot megszüntetné vagy a progressziót bizonyítottan megakadályozná. A szürkehályog gyógyítása műtéti. A mikrosebészeti technikák fejlődése, a műanyag szemlencsék széles skálája, a várható jó optikai rehabilitáció és nem utolsó sorban a betegek elvárása vitathatatlanul előbbre hozta a műtéti indikáció felállításának időpontját.
5. A katarakta preoperatív diagnosztikája
5.1. A katarakta felismerése és elsődleges diagnosztikája
A katarakta műtét olyan beavatkozás, mely az operatőrön kivűl szükségessé teszi a háziorvos véleményét a páciens általános állapotáról, gyógyszereléséről és intratracheális narkózis esetén az anaesthesiológus közreműködését is. Ezenkivül természetesen az operáló team tagjai a kellően képzett műtő személyzet és a prae-ill. posztoperatív szakban a fekvőbeteg részlegen dolgozó nővérek.
A katarakta műtét elvégzésének egyetlen indikációja a páciens életminőségének romlása. A jelenlegi megnövekedett vizuális ingerekkel és igénnyel teli környezetben nem lehet megvonni a határt a műtét indikációját jelentő látóélességben, annak ellenére, hogy a WHO definició szerint 0,6 látóélességet vagy ennél rosszabb értéket okozó lencseborusság esetén beszélünk szürkehályogról.
5.1.1. Anamnezis
Az operatőrnek tájékozódni kell a páciens általános állapotáról, esetleges allergiás epizódokról a család és/vagy kezelőorvos véleménye alapján is. Fontos a szemészeti anamnezis. AIII Milyen volt a két szem látása, korrekciója, amblyopiára utaló tünetek feltárása?
Bizonyos műlencsetípusok implantálása esetében tájékozódni kell, hogy melyik volt a beteg vezérszeme.
Mikor vette észre látásromlását?
Korábbi szembetegségek, kezelés, műtét?
Szemüveg, kontakt lencse, refraktív sebészeti beavatkozás?
5.1.2. Látóélesség
Nincs speciális teszt arra vonatkozóan, hogy a preoperativ látáséélességből következtetni lehessen a posztoperatív funkcionális eredményre. Ezért a látóélesség nem lehet alapja a műtéti indikációnak. AIII
Az AAO különböző speciális teszteket javasol a szubjektiv potenciális látóélesség (sztenopeikus lyuk, Maddox kereszt stb.), és az objektiv potenciális látóélesség felmérésére (elektroretinographia), de egyik sem szolgáltat jellemző adatokat a katarakta műtét eredményére vonatkozóan. AIII
A páciens távoli, közeli látása, fényérzékelése lényeges az aktivitáshoz. AIII A vizuális aktivitás felmérését a Visual Activities Questionnaire, AVD és VF14 tesztekkel végezhetők.
A műtétre váró páciensnek jelezni kell, ha a preoperativ vizsgálatok és a műtét között vizuális változás alakult ki. AIII
5.1.3. Védőszervek vizsgálata
Egyrészt a műtét elvégzésének esetleges anatómiai adottságok miatti nehezítettségét kell felmérni, másrészt az endophthalmitis rizikó faktoraira kell figyelmet fordítani (blepharitis, könnyszervek elváltozásai, könnyutak átjárhatósága stb.). AIII
5.1.4. Szemmozgások
Nystagmus, esetleges szemizom bénulások esetén az anaesthesia módját kell megtervezni, illetve a kettőslátás lehetőségéről a beteget tájékoztatni. AIII
5.1.5. Szemnyomás mérés
A fel nem fedezett glaucoma és az ismert, kezelt zöldhályog minden esetben rizikó faktort jelent a műtét eredményességének szempontjából.
5.1.6. Pupilla funkciók
A pupilla megfelelő tágassága alap feltétele a jól elvégezhető beavatkozásnak minden műtéti technikánál. Ezért ennek elvégezhetősége ill. akadályozásának tisztázása műtét előtt kell, hogy megtörténjen. AIII
5.1.7. Réslámpás vizsgálat
Pupilla tágítás előtt az elülső szegment állapotáról ill. esetleges kóros elváltozásairól ad felvilágosítást (cornea, csarnok, iris, pupilla, lencse helyzete, állapota). AIII
5.1.8. Szemfenék vizsgálat
Pupilla tágítás után vizsgálandó a lencse, üvegtest, valamint előtét lencsével vagy direkt szemtükörrel a retina, különösen a macula állapota. AIII
5.1.9. Fakultatív vizsgálatok
Spekular mikroszkóp, pachymetria csak cornea betegség esetén vagy idős korban végzendő. Cornea topographia irregularis asztigmia észlelésekor.
Fluorescein angiographia diabetes mellitus, macula betegségek, retinalis vagy subretinalis neovascularisatio előfordulásakor vagy feltételezésekor.
Ultrahang B-scan vizsgálat javasolt nagyfokú myopia, staphyloma illetve nem vizsgálható szemfenék esetén.
Látótér vizsgálat elvégzése glaucomás páciens esetében felvilágosítást adhat a várható eredményről is.
A vizsgálatok elvégzése után minden esetben az operatőrnek kell felvilágosítást adni a tervezett műtét menetéről, az esetleges szövődményekről, a posztoperatív kezelésről és életmódról valamint meg kell beszélni az érzéstelenítés lehetséges módjait. AIV
5.2. Műtéti indikáció A műtét indokolt:
- ha a szürkehályog a látóélességet 0,6-re vagy annál nagyobb mértékben rontja,
- ha a lencsehomályok a szemfenéki elváltozások pontos diagnózisát vagy kezelését akadályozzák, AIII
- ha a szürkehályog gyulladást vagy másodlagos glaucomát okoz,
- ha a beteg ragaszkodika mütéthez,a visusajobb0,6-nál de mindennapi megszokott tevékenységét, munkáját nem tudja ellátni (kontraszt érzékenység, glare test végzése),
- ha a mütét refraktív céllal történik (nagyfoku myopiás, nagyfoku hypermetropiás betegekben) (West 1999, Christen 1992, AREDS report No. 5 2001, Cuming 1997).
A műtét kontraindikált: /A:III/
- ha a beteg nem akarja,
- ha szemüveggel a látóélesség megfelelően korrigálható és ezzel a beteg elégedett,
- ha a beteg általános állapota nem teszi lehetővé a mütétet.
5.3. Az operáló orvos műtét előtti teendői
- Az operáló orvosnak meg kell vizsgálni a beteget.
- Meg kell bizonyosodnia a dokumentáció megfelelő voltáról és a műtéti indikáció helyességéről.
- Informálnia kell a beteget a mütét szükségességéről, annak előnyéről, a várható eredményről, az esetleges kockázatokról.
- Meg kell állapodniuk a beültetendő műlencse dioptriájáról, közelre vagy távolra szeretne-e szemüveg nélkül jól látni, esetleg multifokális/akkommodáló lencsét választ.
- A beteg -alkalmasság esetén- tájékoztatandó a multifokális, torikus műlencse beültetés lehetőségéről.
- Válaszolni kell a beteg minden kérdésére.
- A beleegyező nyilatkozatot a beteg megkapja az első vizit alkalmával, azt hazaviheti, otthon tanulmányozza, vagy aláírva hozza vissza vagy a felmerülő kérdésekre még választ kap a műtét előtt.
- Az orvos és a beteg megállapodik a posztoperatív vizitek és kezelés rendjében (AAO Policy statement 1998, Bass 1995,).
- A beteg általános állapotáról illetve műthetőségéről írásos véleményt kér (Lee 1999). AII
5.4. A beültetendő műlencse törőerejének megállapítása (Echobiometria)
5.4.1. Az echobiometria célja
- Az echobiometria elengedhetetlen lépés a szürkehályog műtét előtt
- Az echobiometria célja a beteg egyéni refrakciós igényének megfelelő beültetendő lencse kiválasztása
5.4.2. Az echobiometria részei A echobiometria alaplépései:
- A szem tengelyhossza (AL), melyet ultrahangos vagy optikai biometriával mérünk
- A központi szaruhártyagörbület értékei (K1 és K2)
A echobiometria eredményét a beteg kórlapjában kell tartani, és rajta fel kell pontosan tüntetni a beteg nevét és a megfelelő szemet.
5.4.3. Pontosság
A sebésznek biztosnak kell lennie abban, hogy a kapott adatok megbízhatóak, azokat nem befolyásolja a műszerek elégtelen működéséből vagy a rossz mérési technikából eredő pontatlanság. Az echobiometria pontosságát folyamatosan ellenőrizni kell, úgy, hogy a tervezett spherikus equivalenst és az elért spherikus equivalenst összehasonlítják.
5.4.4. Műszerezettség
A megfelelő műszerekkel végzett pontos echobiometria elengedhetetlen a katarakta műtét előtt. Megfelelő A-módú ultrahang berendezés (vagy lézer interferometer az optikai echobiometria elvégzéséhez) valamint keratométer szükségesek a vizsgálathoz. Minden osztály saját feladata a műszerek megfelelő szervízelése és kalibrálása.
5.4.5. Echobiometriai adatok
- A tengelyhossz eredmények 96%-a 21.0 és 25.5 mm közé esik, 60%-a pedig 22.5 és 24.5 mm közé.
- A K-eredmények 98%-a 40 és 48D közé esik, 68%-a pedig 42 és 45D közé.
- Hacsak nincs valamilyen patológiás eltérés, amely a szem méretét befolyásolja, (pl. egyoldali refrakciós hiba, coloboma, vagy staphyloma), a legtöbb emberben a két szem tengelyhossza közel azonos.
- A legtöbb cornea szabályos görbületű, és a két szem esetében hasonló nagyságú.
- Ha a két szem közötti tengelyhosszkülönbség nagyobb mint 0,3 mm, vagy a K értékek között egy dioptriát meghaladó eltérés van, akkor ezt ellenőrizni kell. Ezeket az eredményeket csak akkor szabad elfogadni, ha az ismételt mérések megerősítik az eredményeket.
- Ha túl nagy különbség van a Kértékek és/vagy a tengelyhossz értékek között, akkor gondolni kell az amblyopia vagy az olyan üvegtesti homályok, mint az asteroid hyalosis jelenlétére. Az ambyopiáról a beteg elfeledkezhet, és esetleg a szemüvegkorrekciója nem tartalmazza a kívánt diopriát.
5.4.6. Az echobiometria elvégzése és az eredmény értékelése Minden szem esetében el kell végezni a
- Tengelyhossz (3 mérés) és a
- K érték
meghatározását. Ha a mérések nem konzisztensek egy szemen belül vagy a két szem között, akkor az ok lehet műszerhiba, rossz mérési technika, vagy ocularis kórfolyamat.
Ha az echobiometria során bármilyen nehézség adódik, azt fel kell jegyezni a kórlapba, és a betegnek ezt el kell magyarázni.
5.4.7. Formulák
- Több mint 900 szem vizsgálata során összehasonlították az SRK I, SRK II, SRK/T, Holladay, Hoffer és Binkhorst II formulákat és az SRK/T és a Holladay formula adták a legjobb eredményeket.
- Másik tanulmányban 1993-ban 450 szem vizsgálata során a regressziót és a elméleti formulákat hasonlították össze, és azt találták, hogy az SRK I és az SRK II a legpontatlanabb. Ezért ezeket nem javasolt használni.
- Ugyanebben a tanulmányban nem volt statisztikai különbség az SRK/T, Hoffer Q és a Holladay formulák között. A meglévő bizonyítékok alapján a következő ajánlás adható:
| Tengelyhossz (mm) | Képlet |
| <22mm | HofferQ |
| 22-24.5mm | A Hoffer Q, Holladay és SRK/T képletek átlaga |
| 24.6-26mm | Holladay |
| >26mm | SRK/T |
Refraktív sebészeti beavatkozás után a műlencsetervezés megfelelő módosítása elengedhetetlen.
5.4.8. Ki végezze a biometriát?
A echobiometria nehéz feladat, melynek eredménye létfontosságú a műtét sikeréhez. A helyi előírásoknak megfelelően képzett szakemberek végezhetik a vizsgálatot.
A szakképzés alatt lévő szemészeknek meg kell tanulni a vizsgálatot elvégezni, azt jól ismerni, és alkalmazni. A betegeket tájékoztatni kell a echobiometriai vizsgálatok korlátairól.
5.4.9. Mikor kell a biometriát elvégezni?
Minden szürkehályog beavatkozás előtt szükséges a vizsgálatot elvégezni mindkét szemen. Fontos, hogy a műtétet végző orvos a műtét előtt annyi idővel lássa az adatokat, hogy a műtét jól tervezhető legyen, és ha szükséges a speciális IOL is megrendelhető legyen.
5.4.10. Mi a teendő ha megbízható biometriai adatok nem nyerhetők?
Bizonyos esetekben a szemészeti eltérés nem teszi lehetővé pontos echobiometria elvégzését. Ilyen esetben:
- Meg kell kérdezni, hogy volt-e korábbi refraktív beavatkozás.
- Teljes szemészeti vizsgálatot kell végezni, beleértve mindkét szem objektív és szubjektív refrakcióját is.
- Össze kell hasonlítani a két szem ultrahang és keratometriás eredményeit.
- Meg kell próbálni megszerezni a beteg korábbi refraktív adatait kezelőorvosától vagy optikusától.
Ha a vizsgálat nem végezhető el, vagy hiányos, akkor az elérhető adatok alapján kell választani. A másik szem adatai is segítségre lehetnek.
5.5. Katarakta műtét előtti általános kivizsgálás
A katarakta műtét érzéstelenítésének módját az operatőr dönti el a páciens vizsgálata ill. a vele történő konzultáció alapján. A helyi érzéstelenítés előtt az operatőr kéri a családorvos vagy kezelő orvos véleményét a beteg általános állapotáról. Általános érzéstlenítés esetén az anaesthesiológus véleményét is minden esetben ki kell kérni.
5.5.1. A család és/vagy a kezelőorvos által végzendő vizsgálatok
5.5.1.1. Anamnézis
- családi anamnézis, korábbi betegségek, műtétek műtéti terhelhetőség felmérése
- korábbi műtétek szövődményei
- krónikus betegségek: diabetes mellitus, asthma, bronchitis, hypertonia, szívritmus zavarok, antikoaguláns terápia allergia gyógyszerérzékenység rendszeresen szedett gyógyszerek
5.5.1.2. Általános rizikófaktorok alkohol, drog
5.5.1.3. Fizikális vizsgálat
5.5.1.4. Laboratóriumi vizsgálatok
Az Aneszteziológiai és Intenzív Terápiás Szakmai Kollégium ajánlásrendszere alapján: (2003-11)
| Kor- és betegségcsoportok | Feltétlenül szükséges vizsgálatok | Mérlegelendő kiegészítő vizsgálatok |
| Újszülött | Hb, ht, vizelet | Vérzési idő, PI, vércukor |
| Gyerek | Hb, ht, vizelet, EKG, ionok | |
| Férfi 40 évalatt | ||
| Nő 40 év alatt | Hb, ht, vizelet | |
| 40-60 év | Hb, ht, vizelet, EKG | |
| 60 év felett | Hb, ht, ionok, szérum kreatinin, vércukor, vizelet, EKG | (Mellkas rtg ) |
| Érbeteg, ISZB | Hb, ht, ionok, szérum kreatinin, vércukor, vizelet, mellkas rtg, EKG | |
| Tüdőbeteg/tartós dohányzás | Hb, ht, ionok, vizelet, mellkas rtg, EKG | |
| DM/anyagcsere | Hb, ht, ionok, szérum kreatinin, vércukor, szérum bilirubin, vizelet, EKG | Májenzimek |
| Idegrendszeri beteg | Hb, ht, ionok, vizelet, EKG | Mellkas rtg |
| Alkoholista, Drogfüggő | Hb, ht, ionok, szérum bilirubin, májenzimek, vizelet, mellkas rtg" EKG | |
| Fertőző beteg | Vérkép, ionok, szérum kreatinin, bilirubin, májenzimek, vizelet, mellkas rtg | EKG |
| Vesebeteg | Vérkép, ionok, szérum kreatinin, vizelet | |
| Májbeteg | Vérkép, ionok, májenzimek, szérum kreatinin, bilirubin, vizelet, prothrombin/INR | Coagulogram, mellkas rtg, EKG |
| Véralvadási zavar, Antikoagulált beteg | Vércsoport, vérkép, ionok, vizelet, vérzési-, alvadási idő, PTI, prothrombin/INR | Mellkas rtg, EKG, kvalitatív vérkép |
| Daganatos beteg | Vérkép, vizelet, mellkas rtg, EKG | Kvalitatív vérkép |
| Immundeprimált/ szteroid kezelt | Vércsoport, vérkép, ionok, vércukor, vizelet | Mellkas rtg, EKG, kvalitatív vérkép |
5.5.1.5. Vélemény a beteg műthetőségéről
A beteg műthetőségéről, a javasolt (elő)kezelésről és műtéti előkészítésről a háziorvos vagy kezelőorvos írásos nyilatkozata szükséges.
5.6. Általános érzéselenítés (altatás) esetén azanaesthesiológus feladata a katarakta műtét prae - intra és posztoperatív szakaszában
5.6.1. Betegvizsgálat Célja: kórisme felderítése
a beteg és kísérő betegségeinek jobb megismerése (sebészi és nem sebészi kísérőbetegségek) adatok nyerése a kockázat felismeréséhez (Benson, 1988-111)
Módszerei: anamnézis fizikális vizsgálat
laboratóriumi vizsgálatok elemzése
5.6.2. Anaesthesiologiai szempontoka különböző betegség csoportokban Idős beteg: hospitalizációs idő rövid legyen
helyi érzéstelenítés ajánlatos
szükség esetén csak enyhe szedációt alkalmazzunk
Diabeteses beteg:
hospitalizáció a műtét előtti napon történjen
a műtét lehetőleg a reggeli órákban legyen
a 2-es típusú cukorbeteg átállítása insulinra szükségtelen
altatás esetén az insulin-terápiában részesülő betegnek 150grammCH-t adjunk isotoniás glukóz oldatban, inzulinnal orális táplálást korán kell elkezdeni
hypertensio, coronaria-betegség: a beállított terápiát a műtét reggelén is adjuk
Krónikus légúti betegség: előzetes kezelést igényel a dohányzást 4 héttel előbb abba kell hagyni
Coagulopathia: a műtét narcosisban javallt a haematoma kialakulásának veszélye miatt Anticoagulans kezelésben részesülő beteg:
Thrombocyta-aggregatio ellenes szerek (Astrix, Ticlid, Plavix, Colfarit) szedését műtét előtt 7 nappal érdemes felfüggeszteni, mert gyakoribbak a műtét alatti és utáni vérzések. Ticlopidine hydrochloridot szedő betegen phacoemulsificatio végzendő kis sclerocorneális, vagy corneális seben keresztül (Saitoh, 1998-II). Syncumárt szedő betegnél a syncumár szedését műtét előtt 2 nappal javasolt abbahagyni. Fraxiparin mellett (2x0,3-0,6 ml sc.) INR 2 alatt (prothrombin 40-50%) a műtét elvégezhető súlyos vérzéses szövődmény nélkül. A műtét napján a Fraxiparin folytatása mellett a Syncumárt el kell kezdeni INR 2,5-3,5 eléréséig. Az irodalomban a Syncumár terápia megtartása mellett is végeztek katarakta műtéteket szövődmény nélkül (Hall, 1988-III) (Lebuisson, 1991-III) (Roberts, 1991-III) (Stone, 1985-IV). Az életet veszélyeztető szisztémás komplikációk elkerülése érdekében katarakta műtét előtt nem szabad mindig leállítani az anticoaguláns kezelést (Saitoh, 1998-II). Ismert viszont, hogy anticoaguláns kezelésben részesülő betegek katarakta műtétje során haemorrhagiás komplikációk sokkal gyakrabban fordulnak elő, mint anticoaguláns kezelésben nem részesülő betegekben (Saitoh, 1998-II). Helyi érzéstelenítés (retro-, parabulbáris) során rövidebb tű és egyszeri injekció alkalmazása biztonságosabbnak tűnik, míg a sub-Tenon és cseppérzéstelenítés még biztonságosabb (Konstantatos, 2001-II). A retrobulbáris vérzés gyakrabban fordul elő azokban a betegekeben, akik a katarakta műtét idejére nem hagyták abba az anticoaguláns szedését (Konstantatos, 2001-II). A modern mikrosebészeti módszerek (phacoemulsificatio) elterjedésével, az un. "clear cornea" seb alkalmazásával az anticoaguláns kezelést nem kell szüneteltetni a szürkehályog műtét idejére.
Összefoglalva konszenzusos javaslatunk:
A phacoemulsificatio elvégezthető kumarin kezelés mellett is cornealis seben keresztül, lehetőleg cseppérzéstelenítésben.
Ha az operatőr mégis corneoscleralis behatolást választ, akkor
- Nagy kockázatú betegségcsoportban (műbillentyűs betegek) a műtét előtt 2 nappal a kumarin kis molekulatömegű heparinra való átállítása javasolt a műtét napján való kumarin visszaállítással, az INR naponkénti ellenőrzése mellett.
- Kis kockázatú betegeknél (pitvarfibrilláció, mélyvénás thrombosis, pulmonalis embolia után, stb.) 2,0 és 2,5 közötti INR mellett a katarakta műtét elvégezhető.
Thrombocyta aggregatio ellenes szer adását a műtét előtt 7 nappal érdemes felfüggeszteni, műtét után visszaadni. 5.6.3. Diagnosztikai vizsgálatok, általános premedicatio
A premedicatio célja: anxiolysis, anélkül, hogy extrém somnolentiát idéznénk elő. (Barker, 1986) (Kumar, 1992-III) Az alábbi szerek használata javasolt helyi vagy általános érzéstelenítés előtt: Alprazolam (Xanax) - p.o. 0,25-0,5mg műtét előtt 1 órával
Midazolam (Dormicum) - p.o. 7,5mg -szemészetben helyi érzéstelenítésben nem ideális szer, a cooperatiot rontja Hydroxysine (Atarax) 100-200mg i.m. beavatkozás előtt 30-45 perccel Catapressan (Clonidin) 1-2tbl - a szemnyomást csökkenti!!
Diazepam (Seduxen) - p.o. 0,1-0,15mg/kg 2 órával a műtét előtt (felezési idő hosszú - elhúzódó hatás!)
5.6.4. Helyi érzéstelenítés
A katarakta műtétet elsődlegesen helyi érzéstelenítésben végezzük. Fajtái:
- retrobulbaris
- parabulbaris
- subtenon
- csepp
A helyi érzéstelenítés kontraindikációja Absolut:
gyermekek esetén, nem kooperáló, süket-néma beteg, pszichiátriai beteg (pánikbetegség, klausztrofóbia)
coagulopathia fennállása esetén (Campbell, 1993-II) (Heinze, 1992-II) (Tanniéres, 1992-111)
Relatív:
a beteg kéri az altatást verbális kommunikációs nehézségek Parkinson-kór - epilepszia osteoarticularis deformitas krónikus bronchitis, irritatív köhögés
Műtéti előkészítés -helyi érzéstelenítés előtt vérnyomás mérés
hemodinamikai és légzési reanimáció lehetőségét kell biztosítani
retrobulbaris érzéstelenítő beadása után a beteg tudatát verbális kontaktussal ellenőrizni kell. Műtét alatti teendők
monitorizálás - riasztóval ellátott pulsoxymeter, szükség esetén EKG CM5-ös elvezetés, vérnyomás mérés (FELTÉTLENÜL monitorizálni kell: mitralis stenosis, hipertrófiás obstruktív kardiomiopátiás betegeket) (Sulpicio, 1989-III)
oxigén biztosítása orrszondán vagymaszkon keresztül
műtét alatti szedálás kiegészítése - (Barker, 1986-111) (Debaillon-Vesque, 1989-111) (Nizzia, 1991-111) Dormicum - 1-5mg i.v. (idős betegeknek a legkisebb dózis) Fentanyl - 10-50 mg i.v. vagy Alfentanyl 3-4 mg/kg Propofol - 0,4-0,7mg/kg i.v.
A helyi érzéstelenítés szövődményei és elhárításuk
Oculocardiális -reflex: bradycardia, arrhythmia,vérnyomásesés, kollapszus
Terápia: Atropin 15 mg/kg i.v., volumenpótlás
Allergiás reakció - az amid-tipusú lokalanesztetikumok ritkán okoznak allergiát.
| Kezelés | |
| I. stádium: Bőrjelenségek és enyhe tünetek | |
| Erythema, urticaria, viszketés. Angioneurotikus ödéma, rhinitis, conjunctivitis. Égő érzés torokban, nyelven, tenyéren, talpon. Fejfájás, nyugtalanság, halálfélelem. | - A gyanúsított szer adásának, felszívódásának megszüntetése (adrenalin sc. Az injekció helyén, végtagleszorítás). - Vénabiztosítás (nagy lumen) - a korábban bevezetett kanült tilos eltávolítani! - Oxigénadás arcmaszkon keresztül (nagy áramlással: 6 l/perc). - Ca-Gluconicum (10 ml lassan) iv. - H1-blokkolók (clemastin 2mg, promethazin 25 mg) és H2-blokkolók (cimetidin 200 mg, ranitidin 50 mg, famotidin 20 mg) iv. - Folyamatos megfigyelés, monitorozás (” 24 óra). |
| II. stádium: Gastrointeestinalis és nem életveszélyes keringési, légzési tünetek | |
| Hányinger, hányás, hasi görcsök, hasmenés. Tachycardia, hipotonia. Kezdődő dyspnoe. | - Adrenalin 0,3-0,5 mg (1 mg/ml-es amp.: 0,3-0,5 ml) im., szükség esetén 5 percenkénti ismétlés. - Krisztalloid infúzió (sz.sz. 5Panaszok, Tünetek00-1000 ml) - Kortikoszteroid (metilprednizolon 200-500 mg) iv. - Bronchodilatator (aminofillin 1210-240 mg,teofillin 100-200 mg lassan) iv. |
| III. stádium: Éltveszélyes keringési, légzési, központi idegrendszeri tünetek | |
| Vasodilatativ sokk. Súlyos bronchospazmus, gégeödéma. Tudatzavar, görcsök, eszméletvesztés. | - Adrenalin 0,1-0,3 mg (0,1 mg/ml-es hígítás: 1-2 ml) iv. - sz.e. 5 percenként ismétlés vagy folyamatosan 4-8 mg/ttkg/perc gyógyszerpumpával. - Ha hatástalan: noradrenalin 0,05-2 mg/ttkg/perc, vagy dopamin 5-20 mg/ttkg/perc. - Endotracheal intubálás. - Erélyes volumenterápia (1000-2000 ml krisztalloid gyors infúzióban). - Kortikoszteroid (metilprednizolon 1000-2000 mg iv.). - b2-receptor-agonosta aeroszol (salbutamol, terbutalin, fenoterol). |
| IV. stádium: Légzés- és keringésleállás | |
| - Cardiopulmonaris reanimáció | |
Légzésleállás, tudatvesztés (keringésleállás lehet, vagy csak késve lép fel)
Oka: az érzéstelenítő liquorba kerülése miatt kialakult agytörzsi bénulás. Az érzéstelenítő beadása után 2-10 percen belül lép fel, és 30 perctől 8 óráig tarthat. (Ahn, 1987-IV) (Drysdale, 1984-II).
Terápia: apnoe észlelése esetén mesterséges lélegeztetést kell alkalmazni a spontán légzés visszatéréséig.
5.6.5. Általános érzéstelenítés
Kontraindikáció: Fokozott kockázat:
- cerebrális keringési zavar
- carotis stenosis - izolált carotis zörej nem képez kontraindikációt
- dekompenzált szívelégtelenség
A fenti állapotokban az általános érzéstelentés kérdésében megoszlanak a szakmai vélemények. Ilyen esetekben a beteg általános állapotát, egyéni preferenciáját, a helyi feltételeket is figyelembevevő aneszteziológiai és szemészeti konzílium dönt az általános érzéstelenítés alkalmazhatóságáról.
Relatív:
- idős kor
- hypertensio, coronaria betegség - megfelelő terápia mellett nincs aneszteziológiai kockázat
- krónikus légúti betegség - előzetes kezelést igényel
- jól előkészített betegnél előnyösebb a helyi érzéstelenítés
- irritatív köhögésben szenvedő betegnél a narcosis a választandó
- asthma: az intubatio, a mesterséges lélegeztetés a hisztaminfelszabadítást okozó szerek használata miatt a locál anaesthesia az ajánlatos
Alapkövetelmény, hogy a cataracta műtét narkózisa közben, az ébredési és a posztoperatív szakban a beteg ne köhögjön, a hasi vagy a mellkasi nyomást erőlködéssel ne növelje. Ugyancsak mindenképpen kerülendő a magas artériás vérnyomás megjelenése, mert intraocularis vérzés lehet a következménye.
Premedikációra leginkább a benzodiazepinek alkalmasak, az opioidoknál figyelembe kell venni az emetikus mellékhatásokveszélyét is. Intravénás premedikációs céllal a narkózis indukciója előtt 1-2 mg/ttkg fentanyl vagy ezzel ekvivalens mennyiségű egyéb opioid adható. A propofol vagy az etomidat ideális bevezető iv. anesztetikumok, mert csökkentik az intraocularis nyomást, a thiopental viszont átmeneti, mérsékelt nyomásemelkedést okoz, azonban ennek ellenére megfelelő alternatív szernek tekinthető.
Légút biztosítási eszközként egyaránt alkalmazható a speciálisan előhajlított vagy az acélszállal erősített endotrachealis tubus, hasonlóképpen megfelelő a megtöretés-mentes ("spirál") laryngeális maszk is. Az endotrachealis intubáció elvégzéséhez a succinyl-cholin és a nem depolarizáló izomrexánsok is alkalmazhatóak. Az előbbi a beadását követően 2 perccel növeli a szem belnyomását, de jelenség az 5. percre megszűnik. Emiatt a még zárt szemen a műtét megkezdése előtt a succlinyl-cholin veszélytelennek tekinthető. A nem depolarizáló izomrelaxánsok nem növelik az intraocularis nyomást. (Az endotrachealis intubálás előtt a gégefő lidocain-permetes érzéstelenítése (3-4 ml 4%-os lidocain) csökkenti a perioperatív köhögés kialakulásának esélyét.)
A narkózis fenntartáshoz az inhalációs anesztetikumok és az opioidok egyaránt előnyösek, mert csökkentik a szem belnyomását. A műtét alatta beteg lélegezhet spontán is, és végezhetünk intermittáló pozitív nyomású lélegeztetés is. Azonban a spontán légzés közben - a lélegeztetéshez képest - nagyobb a köhögés, a légzésvisszatartás, erőlködés megjelenésének valószínűsége. Ezért az intermittáló pozitív nyomású lélegeztetés a cataracta műtétek közben biztonságosabb narkózisfenntartást ad, mint a spontán légzés alkalmazása.
A posztoperatív időszakban gondoskodni kell a beteg fájdalommentességéről (elsősorban minor analgetikumokkal: diclofenac, paracetamol, ketoprofen), és hányinger esetén tanácsos azonnal antiemetikumot adni.
6. Műtéti technika
A szürkehályog eltávolítása többféle technikával történhet.
1. Zárt tokos, intracapsularis /ICCE/ lencse eltávolítás: ennek indikációja ma már nagyon leszűkült: a: az elülső csarnokba luxálódott lencse
b: subluxalodott lencse (üvegtestbe luxálódott)
2. Nyitott tokos hályogeltávolítás
- lehet: ECCE /extracapsuláris hályogműtét/, amikor 6-8 mm-es seben át távolítjuk el a magot és kézi vagy gépi szívóval a kérget, melyet műlencse (PMMA) beültetés követ;
- lehet: Phakoemulsificatio, amikor 1,8-3,2 mm-es seben át bevezetett kézivéggel, capsulorhexis végzése után, ultrahang energia segítségével daraboljuk, szívjuk ki a magot, majd egy erre alkalmas kézivéggel a kéregrészeket. Ezt követi (a lencsétől és implantáció módjától függően esetlegesen megnagyobbított seben át) az összehajtható műlencse lencsetokba történő beültetése.
- Az utóbbi években elfogadottá vált a biaxiális phacoemulsificatios műtéti technika, illetve várható a mini/mikro-coaxiális műtéti technika (MICS) elterjedése. Ez utóbbinál a műtéti seb1,5/1,7mm, 2.0-2.2 mm, illetve 2.0 mm alatt van. Az újabb, speciális műlencsék ezen sebméreten át beültethetőek.
A fenti műtéti megoldások közötti különbség
- a seb nagyságában
- a seb helyében
- a capsulotomia módjában
- a mageltávolítás módjában
- a műlencse típusában
- a posztoperatív gyógyulási időben
- a posztoperatív astigmia kialakulásában van.
Phakoemulsificatio után a visus szignifikánsan jobb és stabilabb, kevesebb a komplikáció, kisebb a posztoperatív indukált astigmia, mint ECCE után./össszehasonlító randomizált tanulmány 1 éves követési idő (Minassian 2001,Olson 1998, Steinert 1991, Kohnen 1995). AI
Magyarországon 1993-ban még csak4 intézetben végeztek phakoemulsificatiot.. Salacz statisztikája szerint 2001-ben minden másodikszürkehályogmütétvolt phakoemulsificatio,2006-raa phakoemulsificatio részesedése már88,6%-ra nőtt. A kívánatos tendencia a kisebb seben át végzett szürkehályog műtét. Egyes külföldi országokban a szürkehályog műtétek 95-98%-ában a phakoemulsificatios eljárást alkalmazzák (European Cataract Outcome Study 2007).
Ajánlás:
Az ideális mütéti technika a következő:
- A lehető legkisebb, jól konstruált, kisfokú astigmiát indukáló seb készítése. AI
- ECCE-nél is alkalmazhatunk az eddigi gyakorlatnál kisebb alagútsebet.
-A műtét az intraocularis szövetek megkímélésével történjék. Erre a célra viszkózus /viszkoelasztikusanyagogat (OVD) alkalmazunk, az irodalmi ajánlásoknak megfelelően (pl. soft shell, stb. technikák). Az Európában ("CE Certified" illetve USA-ban ("FDA Approved") OVD-k alkalmazása megengedett. A műtét végén az OVD kimosása ajánlott a posztoperatív szemnyomásemelkedés kivédése céljából.
- Őblítő folyadékként "BSS" vagy "BSS+" ajánlott.
- Összehajtható hátsó csarnok műlencsét alkalmazzunk a tokba helyezve.
- Amennyiben műtéti komplikáció miatt a műlencse nem helyezhető a tokba, azt a sulcus ciliarisba is ültethetjük. Kerülni kell a bag-sulcus fixatiót, mert az a műlencse decentrálódásához vezet.
- Ha a seb nem biztosan önzáró, akkor varrattal zárni kell.
6.1. Intraocularis műlencsék
Az intraocularis műlencse (IOL) alkalmazása az aphakiás állapot korrigálásának egyik -jelenleg legoptimálisabb -módja.
Az ideális műlencse biológiailag inert, a lencse cristallina funkcióját betölti, stabilan a helyén marad, optikailag tiszta, a hátulsó tok tisztaságát hosszú távon biztosítja (AII, Hollich, 1998, Kohnen 1996, Brown 1998, Mamalis 2000, Spalton 1999).
Jelenleg nincs olyan műanyag szemlencse, amely valamennyi fent felsorolt követelménynek megfelel. Ezért különböző anyagu, típusu, optikájú és haptikájú, felületű műlencse van forgalomban. Az elérhető műanyag szemlencsék két nagy csoportja imeretes: nem összehajtható és összehajtható. A nem összehajtható PMMA lencsékkel van a legrégibb tapasztalat (több mint 50 éves) ezek azonban csak nagy seben (5,5-7,0 mm) át implantálhatók.
Az összehajtható műanyag lencsék anyagukra nézve lehetnek: a: silicon, b: acryl c: collagén (HEMA collagén) alapanyagúak.
A sebész a beteg szemészeti és általános betegségeit figyelembe véve választja meg a lencse típusát. AIII Törekedni kell a két szembe azonos alapanyagú műlencse beültetésére.
Az utóbbi években megjelentek, és elfogadottaká váltak a bi/multifokális (un. pseudoakkommodáló) műlencsék, melyek diffrakció vagy refrakció elvén működnek. Ennek egyik speciális fajtája a "Mixand Match" műlencse beültetés (egyik szembe diffraktív, a másikba refraktív típusú IOL beültetése) alkalmazása.
A beteggel történt egyeztetés után alkalmazható az un. "monovision", melynél a vezér szem látásélességét távolra korrigáljuk, míg a másik szem közelre lesz korrigálva (myopiás törőerő).
Ugyancsak megjelentek az akkommodáló műlencsék, melyek eredményei különösen hosszú távon nem egyértelműen kedvezőek, az akkommodációs hatás csökkenése, és az átlagosnál magasabb arányban előforduló PCO képződés miatt.
Jelenleg 4 műlencse gyártó cég készít tórikus műlencséket.
Az európában engedélyezett ("CE certified"), illetve az USA-ban az FDA által engedélyezett műlencsék magyarországi felhasználását támogatjuk.
A két szem műtéte között ajánlott minimum 4-6 hetet várni, az első szem teljes gyógyulásáig, illetve a törőerő stabilizálódásáig.
Az elülső csarnok lencse (ACL) implantáció indokolt: a: ha a hátulsó tokon nagy centrális vagy a PCL implantációját lehetetlenné tevő perifériás szakadás van. b: ha a rhexis széle is sérült és lehetetlen a sulcusba helyezni a PCL-t.Csakaz un. modern, legújabb generációs ACL implantációja javasolt. Az elülső csarnok lencse implantációjánakjóaltenatívája lehet az iris-clip lencse implantálása.
Kontraindikált az ACL implantációja sekély csarnok, szűk csarnokzúg esetében, valamint ha a csarnokban üvegtest vagy lencse maradék van.
Sclera fixált, kivarrt lencse implantációja indokolt, ha egyáltalán nincsen a PCL hordozására alkalmas tok. A műlencsét bevarrhatjuk a primer beavatkozás során, vagy később is. Iris-clip lencse alkalmazása is szóba jön a hásó tok hiánya esetén.
Amennyiben a műlencsét (szövődmény miatt) a tok helyett a sulcusba ültetjük, figyelemmel kell lennünk a lencse megfelelő méretének illetve törőerejének a kiválasztására.
6.2. A műtéti gyakorlat megszerzése
Ma már vitathatatlan, hogy a műszerek, a bonyolult működésű gépek alapvető ismerete nélkül szemsebészeti műtét biztonsággal nem végezhető.
Ismerni kell az operációs mikroszkóp, a phakoemulsificatios készülék működését és működtetését.
A katarakta sebészetben végbemenő változások arra ösztönzik a szemészeket, hogy jobb eredményeket érjenek el,
lehetőleg gyorsabban, mint pl.10-20 évvel ezelőtt. Ez irányba hat a betegek nagyobb fokú tájékozottsága és elvárása, a
phakoemulsificatio egyre nagyobb térhódítása, a korábban elvégzett műtétek valamint a népesség életkorának
növekedése és ezáltal a katarakta előfordulásának növekedése.
A megfelelő gyakorlat megszerzése a komplikációk előfordulását csökkenti.
A gyakorlat megszerzése un. "Wet lab"-ben:
A modern katarakta sebészet nemcsak az operációs mikroszkóp alatti finom micromanipulációt jelenti, hanem a phakoemulsificatios készülék működésének ismeretét is feltételezi. A jól felszerelt laboratóriumban való gyakorlással a finom kéz és lábmozdulatok összehangolttá válnak. Jól felszerelt "wet lab" szükséges minden egyetemi klinikán.
A rendszeresen szervezett tréningeken a megfelelő oktató sebészek biztosítása elengedhetetlen.
Megfelelő gyakorlattal rendelkező türelmes sebész vezesse a kezdők első műtéteit. Műtét előtt a műtét lépéseinek átbeszélése, a kezdő sebész biztatása mindenképpen hasznos. Jó előre megállapodni, hogy milyen komplikiációk fellépése esetén mi a teendő, ill. mikor veszi át esetleg a műtétet a tapasztalt sebész.
6.3. Perioperativ infectio profilaxis
Noha a conjunctiva zsáksterillé tétele nem lehetséges, mindentel kell követni, hogy a fertőzés rizikóját csökkentsük. A preoperativ conjunctiva és szemhéjleoltás csak akkor indokolt, ha blepharitis vagy a nasolacrimalis rendszer gyulladása vagy elzáródása áll fenn.
Az 5%-os Povidone iodine alkalmazása a szemrésbe és az áthajlásokba a műtét előtt bizonyítottan csökkenti a baktérium kolonizációt a szemgolyó elülső felszínén és csökkenti a posztoperatív endophthalmitis kialakulásának lehetőségét (Speaker 1991). AII
- A szemhéjak és szempillák izolálása szükséges steril vízhatlan öntapadós fóliával
- Az intracameralisan alkalmazott antibiotikum (cefuroxime) bizonyítottan hatásos (ESCRS Endophhalmitis Study 2007.) A.I. Ne használjunk Vancomycint indokolatlanul a rezisztencia kialakulásának veszélye miatt. CII
Ajánlás:
1. A szemhéj vagy a kötőhártyazsák leoltása csak bizonyos esetekben lehet indokolt műtét előtt. (pl. blepharitis, conjunctivitis). CII
2. Műtét előtt a szemöldökés a szemhéjakvalamint a szempillák 10 %-os Povidone iodine-nal való lemosása javasolt. A kötőhártya zsákot a műtét előtt 5 %-os Povidone iodine-nal kell átöblíteni két alkalommal (behatási idő 3 perc). AII
3. A műtét végén subconjunctiválisan adott antibiotikumnak nincs bizonyítottan profilaktikus hatása az esetleges endophthalmitis kivédésében. CII
4. Ajánlott a műtét végén intracamerálisan cefuroxime adása (1 mg/0.1 ml), az ESCRS Endophthalmitis tanulmánya alapján.
5. Preoperative lokális antibiotikum adható. A műtét előtt alkalmazott fluoroquinolon tartalmú szemcseppel a posztoperatív endophthalmitis aránya tovább csökkenthető.
6. Posztoperativ lokális antibiotikum adása kötelező varrat nélküli clear cornea sebek esetében..
7. Intraoperativ és korai posztoperatív komplikációk
Intraoperatív komplikációk
Hibás sebkészítés
Endothel és Descemet sérülés
Elülső tok sérülés, inkomplett capsulorhexis
Iris sérülés
Hátsó tok ruptura
Mag- és/vagy kéreg részek, műlencse üvegtestbe süllyedése Üvegtest előesés a csarnokba vagy a sebbe Expulzív vérzés Zonula sérülés
Az intraoperatív komplikációk bizonyos eseteiben a sebész arra kényszerül, hogy a phacoemulsificatios technikáról áttérjen manuális módszerre. Ez elfogadott a további, súlyosabb komplikációk (pl. un. "dropped nucleus") megelőzésére.
Zonulasérülés esetén az un. "tokfeszítő gyűrű" alkalmazása ajánlott.
Amennyiben a műtét során a helyzet nem ideális műlencse beültetésre, akkor azt egy második lépésben (un. secundaer műlencse beültetés) kell elvégezni.
Korai posztoperatív szövődmények Filtráló seb Sekély csarnok Borús cornea
Szemnyomás emelkedés vagy hypotonia
Fixálva dilatált pupilla
Fibrines gyulladás
Akut postoperatív endophthalmitis
Dislocalt műlencse
Posztoperatív endophthalmitis gyakrabban fordul elő tokruptura, elülső vitrectomia, és elhúzódó műtét után, valamint diabetes mellitus, bőrelváltozások, szemhéjgyulladások, könnyútelzáródás esetén és immunsupprimált betegekben.
A maradandó látásvesztés katarakta műtét után ritka.
Az European Cataract Outcome Study (ECOS, 1995-2007) adatai szerint az átlagos intraoperativ komplikáció 2,2-4,5% volt, a hátsó tok ruptura 0,8-2,2%, az üvegtest veszteség 0,3-1,5 % volt. A study-ban 27 ország 91 szemészeti osztálya illetve klinikája vett részt és évi 4000-5000 beteg adatait dolgozták fel 1995-2007-es évekre vonatkozóan. Egy randomizált tanulmány adatai szerint phakoemulsificatio után az iris prolapsus előfordulása 0%, míg ECCE után 7.0 %. l éves követés után szignifikánsan kevesebb komplikációt észleltek phakoemulsificatio után mint ECCE után (Minassian 2001). AI
A National Cataract Surgery Survey adatai szerint, melyek 18472 betegre vonatkoznak: tokruptura és üvegtest veszteség 4,4%, inkomplett kéregeltávolítás 1%, iris trauma 0.7%, vér az elülső csarnokban 0,5%, sebzáródási probléma 0,25%, chorioidea vérzés 0,07%, üvegtestbe luxálódott IOL 0,16%.
Korai - 48 órán belüli komplikáció a betegek 23%-nál volt. A leggyakoribb a cornea oedema, 9,5%, emelkedett intraocularis nyomás 7.9%, uveitis 5,6%. Ezen tanulmány adatai szerint a komplikációk hasonló gyakorisággal fordultakelő phakoemulsificatio és ECCE után. A három hónapon belüli súlyos komplikáció viszonylag ritka.
| Endophthalmitis | 15 787 betegből | 0,1% (0,1-0,2) |
| Schein és mtsai adatai | 717 betegből | 0,14% |
| Retina leválás és szakadás | ||
| 15 787 beteegből | 0,1% (0,1-0,2) | |
| Schein és mtsai | 717 betegből | 0,14% |
IOL specifikus komplikáció ritka. Előfordul decentrálódás, nem megfelelő dioptriájú IOL implantációja, ritkán a műlencse opacifikációja. Azon lencséknél, melyeknek optikája un. vágott szélű, a PCO előfordulási aránya kisebb, viszont számolni kell nem kívánatos optikai jelenségek fellépésével (Farbowitz 2000, AIV Davison 2000, Masket 2000).
A III
Mind az intraoperatív szövődmények (pl. "dropped nucleus"), mind a posztoperatív szövődmények (pl. endophthalmitis, IOL luxatio) egy részénél előfordulhat az az állapot, hogy a komplikáció ellátásának nincsenek meg a személyi és tárgyi feltételei abban az intézetben, ahol a primer (cataracta) műtétet végezték. Ilyen esetben a beteget a komplikáció ellátására előzetes megbeszélés alapján kell a komplikációt ellátó fogadó intézetbe irányítani.
Nem várt posztoperatív refraktív eredmények
Ha a szürkehályog műtét után a refraktív eredmény nem várt értéket ad, akkor először ellenőrizni kell a preoperativ tervezést, a lencse típusát és az A konstanst.
Ha az implantátum dioptriája nem megfelelő, akkora következő lehetőségek vannak:
- Ha a beteg tudja viselni a refrakciót, a lencsét a helyén lehet hagyni.
- Kontakt lencse korrekció.
-A refrakció alapján intraocularis lencse cseréje (a szemésznektudatában kell lennie, hogy az eredeti IOL csomagolása is lehet hibás, amely ezt a lehetőséget megzavarhatja).
- Második korrekciós intraocularis lencse beültetése.
- Refraktiv sebészeti beavatkozás.
Ha a másik szemen is szükség van műtétre, akkor meg kell fontolni a második szembe ültetendő lencse dioptriáját, hogy a panaszt okozó aniseikonia elkerülhető legyen. Bármilyen további műtétet a beteggel meg kell beszélni.
8. Késői posztoperatív komplikációk: A hátsó tok homályosodásának (PCO) kezelése
A hátsó tok homályosodásának (PCO) megelőzésére alkalmazni kell az ismert műlencsével kapcsolatos kívánalmakat (éles szél, biokompatibilitás, maximális tok-műlencse kapcsolat /bioadhesio/, illetve az un. sebészi ("in-the bag" IOL beültetés, az optikát körbevevő capsulorhexis, hydrodissectio) faktorokat.
A hátulsó tok opálosodása a leggyakoribb késői posztoperatív komplikáció. A beültetett IOL típusától függően a betegek 25-50%-ánál fordul elő 5 éven belül (Rí). Az újabb típusú műlencsék mellett csökkenő tendenciáról számoltak be. (Hollich)
A hátulsó tok homályosodásának effektív kezelése a nd:YAG laser capsulotomia, melynek célja a látási funkció
helyreállítása és a kontrasztérzékenység javítása (Tan 1999). AIII
A Nd:YAG laser kezelés gyakorisága változó, 3 éven belül 3-53%.
A Cataract PORT Study szerint 19,2% 4 hónapon belül (Schein 1994). AIII
8.1. A Nd:YAG laser kezelés indikációja
1. ha a PCO olyan mértékben rontja a látóélességet, hogy az nem felel meg a beteg funkcionális szükségleteinek. AIII
2. Ha a tok homályosodása jelentősen rontja a hátulsó szegment vizsgálhatóságát.
3. Ha monoculáris diplopiát okoz.
A kezelést különös körültekintéssel indokolt tervezni:
1. intraoculáris gyulladás,
2. emelkedett szemnyomás, AIII
3. maculaoedema, (Seinert 1991) AIII
4. retina leválás kockázata esetén (pl. tengely myopia). (Koch 1989) AIII
A Nd:YAG laser kezelés elhatározásakor számba kell venni a beteg igényeit, a kezelés előnyeit és a kezelés rizikóját. AIII
Nd:YAG laser kezelést ne végezzünk profilaktikusan.
Ugyanazon a napon mindkét szemen ne végezzük el a kezelést.
A kezeléssel lehetőleg minimum fél évet várjunk a szürkehályog műtét után.
8.2. A Nd:YAG laser kezelés komplikációi:
1. átmeneti szemnyomás emelkedés (Slomovic 1985, Seon 2000, Rakofsky 1997) AII
2. a retina leválás - lehetősége növekszik, különösen tengely myopiában (Koch 1989)
3. cystoid macula oedema AIII
4. IOLsubluxatio (különösen "plate haptic" lencsék esetén, melyeknél 3 hónapon belül nem is javasolt a kezelés).
5. "lens pitting" (műlencse sérülése) - kevésbé fordul elő, ha a lehető legalacsonyabb energiát használjuk (Steinert 1991)
6. üvegtest előesés
7. lokális endophthalmitis exacerbatioja. (Tetz 1987)
8.3. A Nd:YAG laser kezelés utáni követés:
Lokális kezelés béta blokkoló cseppel közvetlenül a kezelés után. Legalább egy órás megfigyelés ajánlatos az eleve glaucomás és sulcus fixált PCL-es betegek esetében, melyeknél a tensio emelkedés szignifikánsan magasabb. A beteget fel kell világosítani, hogy látásromlás esetén azonnal jelentkezzen. Ajánlatos egy emlékeztetőt a beteg kezébe adni.
Ajánlás:
- a PCO a betegek 25-50 %-ánál fordulhat elő a katarakta műtét után 5 éven belül.
-Jelenleg a hátulsó tok homályosodásánaka Nd:YAGcapsulutomia a standard kezelése-bár létezik más alternatíva is.
A III
- A komplikációk ritkák.
- Beleegyező és emlékeztető nyilatkozat alkalmazása javasolt.
9. Posztoperatív követés
A posztoperativ vizsgálatok célja optimalizálni az operáció eredményességét, gyorsan felismerni és kezelni a szövődményeket. Ez a szövődmény gyors és pontos diagnózisát és kezelését, a szükséges optikai korrekció biztosítását, a beteg felvilágosítását és a posztoperatív teendők leírását igényli.
9.1. Posztoperatív teendők
Mielőtt a beteget elbocsájtják a kórházból, informálni kell a posztoperatív teendőkről szóban és írásban is.
- A katarakta műtétet végző orvosnak kötelessége tájékoztatni a beteget a lehetséges komplikációk tüneteiről, a szem védelméről, a cseppentések módjáról, a kontrollok idejéről, és arról, hogy sürgős esetben hol látják el. AIII
- Az endophtalmitis jeleiről (látóélesség csökkenés, növekvő fájdalom, fokozódó szemvörösség, szemkörüli duzzanat, váladékozás, újúszkáló homályok, fényérzékenység) fel kell világosítani a beteget, és ha ilyet észlel, azonnal forduljon szemészhez. AIII
- Az orvos tájékoztassa a beteget a beteg felelősségéről, hogy kövesse az orvos tanácsait és utasításait a posztoperatív időszakban, és ha problémája van, azonnal értesítsen szemészt. AIII
- Nincs bizonyíték a hypotensiv cseppek korai posztoperatív szakban való alkalmazásának előnyeiről, biztonságosságáról és hatékonyságáról minden betegre vonatkozóan.
- Nincs kontrollált tanulmány a megfelelő gyulladáscsökkentő helyi terápia alkalmazására sem. Jelenleg a döntés bármilyen antibiotikum, steroid, nonsteroid, szemnyomáscsökkentő szer egyedüli, vagy kombinációban való alkalmazása az operáló orvos feladata.
- Javasolt phacoemulsificatio után 4 hétig, extracapsularis katarakta extractio (ECCE) után 6 hétig 1%-os prednisolon acetetat használata csökkenő adagban. CIII
9.2. Posztoperatív ellenőrző vizsgálatok ideje
- A kontrollok idejét az operáló, illetve azt helyettesítő orvos határozza meg. AIII
- Katarakta műtétet követően első kontroll 24-48 órán belül, második kontroll a 7-30. napon. CIII
- Ha a műtét közben komplikáció lépett fel, akkor minden esetben egyedi elbírálás alapján történik a kontroll vizsgálatok idejének megállapítása. CIII
9.3. Az ellenőrző vizsgálatot végző személy
- a katarakta műtétet végző orvos, szemész szakorvos (területileg illetékes, vagy az operatőr által kijelölt szemész) CIII
9.4. Az ellenőrző vizsgálat helye
- az operációt végző intézmény ambulanciája, vagy szemészeti szakrendelő CIII
9.5. Az ellenőrző vizsgálat elemei
- Minden posztoperatív kontroll tartalmazza a következőket: AIII
- Előző találkozás óta történt szemészeti események, a beteg panaszai
- Funkcionális látás megítélése (tesztek)
- Látási funkció mérése (nyers és korrigált látóélesség)
- Réslámpás vizsgálat
- Szemnyomás mérése
- Posztoperatív követési terv és gyógyszerelés megbeszélése.
- Pupillatágítás akkor szükséges, ha a betegnek friss látási problémája van.
- A posztoperatív astigmatismus csökkenthető az esetleges varrat átvágásával, vagy eltávolításával a posztoperatív 4. héten. CIII
- Soron kívüli vizsgálat akkor szükséges, ha szokatlan tünet, látásromlás, jelentkezik az esetleges késői szövődmények diagnosztizálására és kezelésére, vagy ha beteg bármit kérdezni akar. CIII
- Szemüveget a korrekció stabilizálódása után, phacoemulsificatio esetében a 3-4. héten, ECCE esetén 6-8. héten érdemes felírni.
10. A műtéti sikeresség (outcome)
Minden beteg vonatkozásában egyedi, mert másoka betegekelvárásai, életmódjukés általános egészségi állapotuk.
10.1. A műtéti sikeresség kritériumai
1. A látási panaszok csökkenése
2. Látóélesség javulása
3. A tervezett refrakció elérése (indukált astigmatizmus<1D)
4. Az életminőség javulása (autóvezetés, munkaképesség)
5. Perioperatív komplikációkés posztoperatív komplikációk (tokruptura, üvegtest veszteség, magdarabka süllyedés) aránya
6. A lencse hátsó tokjának elhomályosodása (PCO)
Noha a katarakta műtét hatásossága magas, figyelembe kell venni néhány tényezőt, amely előre jelezheti, hogy mely betegek lesznek elégedettek a műtéti eredménnyel.
A Cataract PORT Study meghatározta az egymástól független, műtéti sikerességet befolyásoló tényezőket. Ezek az életkor, egyéb általános és szemészeti betegségek, cataract symptom score, preoperatív VF-14 érték (Schein, 1995-III), ADVS érték (Mangione, 1992-III).
10.1.1. A látási panaszok csökkenése
Funkcionális kérdőívek (cataract symptom score, preoperatív VF-14 pontszám, ADVS és PSC cataract) alapján mért gyengébb preoperatív látás, az AMD és diabetes hiánya esetén a javulás mértéke nagyobb (Bass, 1997-III, Mangione, 1995-II).
A 65 év alatti korosztály nagyobb javulást mutatott. A súlyosabb panaszokkal és dysfunctioval rendelkező betegek nagyobb javulást mutattak (Schein, 1995-III).
75 év feletti korban meglévő más szembetegségek (pl: AMD, glaucoma) esetén csekélyebb mértékű a javulás (Schein, 1995-III).
AMD-ben és diabetesben is mutatkozik azonban kisebb mértékű javulás. A fenti tanulmányok alapján az életminőség javulása a 75 év feletti életkorban is funkcionálisan és statisztikailag is szignifikáns. (Schein, 1995-III, Bass, 1997-III). National Swedish Cataract Register study: Catquest kérdőív: a betegek 91%-a javulásról számolt be a műtét után (Lundström, 1999-II).
ASCSR National Cataract Database alapján: az átlagos visual function score 3 hónap után 70,3% volt a preoperatív 55%-hoz képest (skála: 0-100-ig, 0= képtelen véghezvinni bármilyen aktivitást).
ADVS: Egyéb szemészeti és általános megbetegedések esetén a javulás 12 hó után: 80%-os (Mangione, 1994-I). NEON database szerint: a látás VF-14 teszt szerinti javulása 90% feletti. (Lum, 2000-II).
Ajánlás:
A látási panaszok katarakta műtét utáni csökkenését funkcionális kérdőívekkel lehet mérni. (Lásd: Függelék 3.)
10.1.2. Látóélesség javulása
A Snellen-féle látóélesség-vizsgálat a leggyakrabban alkalmazott módszere a műtéti sikeresség vizsgálatának, noha ez a beteg elégedettségének gyenge indikátora. (Lundström, 1998-II, Mangione, 1995-II)
A szakirodalom áttekintése azt mutatja, hogy ha nincs más szemészeti megbetegedés, a katarakta műtét a betegek több mint 92-95%-ban a látóélesség javulását eredményezi. Ha a betegnek egyéb szembetegsége is van, mint például macula degeneratio, glaucoma, RPD, amblyopia, a látóélesség javulása a betegek kevesebb, mint 80%-át érintheti (Powe, 1994-I, Lum, 2000-II, Lundström, 1998-II, Desai, 1999-I, Mangione, 1995-II).
10.1.3. A tervezett refrakció elérése
3 hónap után a betegek fénytörési hibája 74,6%-ban ± 1 D szférikus ekvivalensen belül volt és az átlagos indukált astigmatizmus: 0,59 D, 86%-ban az indukált astigmatizmus ±1 D-n belül volt (Lum, 2000-II).
Az ECOS 2007 évi tanulmánya alapján az indukált astigmia 0,34D volt és a szférikus eltérés a tervezettől átlagban 0,6 D volt.
10.1.4. Az életminőségjavulása (autóvezetés, munkaképesség)
Katarakta műtét után a VF-14 kérdőív szerint a betegek elégedettsége a látásjavulással 85%-os, a betegek beszámolói a látási nehézségekről a mindennapi életben 80%-os javulást mutatnak (Steinberg,1994-II).
Catquest tanulmány: A 85 év feletti más szembetegségben is szenvedők 30%-a, aki nem számolt be a műtét előtt mindennapos tevékenységekvéghezvitelének nehézségéről, 6 hónappal a műtét után nem észlelt javulást saját látási funkcióiban. Általánosságban a 85 év feletti életkorban a katarakta műtétnek jó eredményei vannak, az egyéb szembetegségben nem szenvedő betegek jobb látásról számolnak be (Lundström, 2000-II).
A látási funkció javulása korrelációt mutat a mentális állapot javulásával. Az ADVS alapján mért látásjavulás az egészségi állapottal összefüggő életminőség javulásához vezet, azt sugallván, hogy a látás javulásával csökkenthető a korral járó egészségromlás (Mangione, 1994-II, Jayamanne, 1999-III).
Katarakta műtét után idős személyekben több funkcionális agyi degeneratív folyamat lassulhat, vagy megállhat (Brenner, 1993-II).
10.1.5. Peri-és posztoperatív komplikációk
| NEON adatbázis | Cataract PORT | NCS | |
| (minden adat) | (N = 717) | ||
| (Powe,1994-I) | (Powe,1994-I) | (Desai,1999-I) | |
| Intraoperativ (%) | |||
| Hátsó tokszakadás vagy zonula szakadás | 1.8 | 1.95 | 4,4* |
| Iridodialysis/cyclodialysis/iris trauma | <1 | 0.84 | NA |
| Üvegtest veszteség, elülső vitrectomia | 1.2 | 1.39 | 4,4* |
| Lencse fragmentum elsüllyedése az üvegtesti térbe <1 | 0.28 | 0,3 | |
| Suprachorioidealis vérzés | <1 | 0.14 | 0,1 |
| Retrobulbáris vérzés | 0 | 0 | NA |
| Posztoperativ (az utolsó kontroll idején, vagy | |||
| 4 hónappal a műtét után) % | |||
| Sebszivárgás, sebszétválás | <1 | 0.84 | 1,2** |
| Műlencse dislocatio, eltávolítás, csere | <1 | 0.28 | NA |
| Endophthalmitis | <1 | 0.14 | 0,03** |
| Retina lyuk, szakadás, leválás | <1 | 0.14 | 0,1 |
| Cornea oedema | 1.4 | 1.95 | 9,5** |
| Szemnyomás emelkedés | NA | NA | 7,9** |
| Szignifikáns cystoid macula oedema | <1 | NA | NA |
| Cystoid macula oedema | NA | 3.21 | NA |
| Persistáló iritis | <1 | NA | 5,6** |
| Iris abnormalitások | NA | 2.51 | NA |
| NA = nincs adat. * = tokruptura és üvegtest veszteség együttesen ** = műtét után 48 órán belül |
| 10.1.6. A lencse hátsó tokjának elszürkülése (PCO) A lencse hátsó tokjánakelszürkülése 2 évvel a katarakta műtét és műlencse beültetés után akár az esetek 25-50%-ában is jelentkezhet (Spalton, 1999-II). Műtét után 1 évvel ECCE után szignifikánsan nagyobb arányban fordul elő a hátsó tok elszürkülése, mint phacoemulsificatio után (Minassian, 1994-I). |
| APPENDIX 1 |
| Betegtájékoztató a szürkehályog (katarakta) műtétről (A szöveg nagyobb, legalább 14 pt betűmérettel szedendő) |
| Ez a tájékoztató segít Önnekeldönteni, hogy vállalja-e a katarakta műtétet. Az operáció előtt alá kell írnia a beleegyező nyilatkozatot, ezért fontos, hogy értse, hogy mi történik önnel a műtét előtt, alatt és után. Ha bármilyen kérdése van, kérdezze meg kezelőorvosát. |
| A szürkehályog Az Ön szemész orvosa szürkehályog műtétet javasolt, mert a szemlencséje homályossá vált, megnehezítve mindennapos tevékenységének végzését. A szürkehályog műtét általában nem sürgős műtét. Ha nem operálják meg a kataraktáját, a látása ugyanolyan rossz marad, vagy tovább rosszabbodik, ennek üteme egyénenként változó. Ma már nem kell megvárni a szemlencse teljes elszürkülését. |
| Az operáció A műtét célja a homályos lencse eltávolítása, és műanyag lencse beültetése a szembe. A műtét általában helyi érzéstelenítésben, szükség esetén altatásban zajlik. Az érzéstelenítés módját az operáló orvos Önnel előzetesen megbeszéli. Közvetlenül az operáció előtt pupillatágító cseppeket fog kapni. Helyi érzéstelenítés esetén ezután érzéstelenítőt kap. Ez vagy egyszerű érzéstelenítő szemcsepp lesz, és/vagy helyi érzéstelenítő injekció a szem körüli szövetekbe adva. Az altatásban végzett műtét esetén a műtéti előkészítésről az altató orvos tájékoztatja Önt. A műtét alatt háton, nyugodtan kell feküdni. A műtét általában 15-30 percig tart, de akár 45 percig is eltarthat. A műtét során a szürkehályogot eltávolítjuk, és előzetesen kiválasztott műanyag szemlencsét ültetünk be. A műtéti sebet szükség esetén varrattal zárjuk. A műtét végén kötés kerülhet a szemre, a szemgolyó védelme céljából. |
| A műtét után Ha kellemetlen érzése lenne a műtét után, fájdalomcsillapítót bevehet. Ha panaszai nem enyhülnek, forduljon kezelő orvosához. A legtöbb esetben a sebgyógyulás 2-6 hetet vesz igénybe, ezután lehet felírni a szükséges újszemüveget. A műtét után szemcseppet fog kapni, melyet több hétig kell majd használni. A kórházban el fogják magyarázni, hogyan és milyen gyakran kell majd cseppenteni. A szemet nem szabad megdörzsölni! Egyes tünetek esetén azonnali kezelésre van szükség. Azonnal menjen a műtétet végző intézménybe, ha a következőket észleli: - Erős fájdalom - Látásromlás - A szem fokozódó vörössége |
| A látásjavulás valószínűsége A műtét után olvashat, TV-t nézhet. A gyógyuló szemnek időre van szüksége, hogy a végleges látóélesség kialakulhasson. A legtöbb szem látása javul a katarakta műtét után. Ne feledje, hogy ha más betegsége is van, mint pl. cukorbetegség, zöldhályog vagy időskori szemfenék elváltozás, akkor a látás egy sikeres műtét után is rossz maradhat. |
| A szürkehályog műtét előnye és kockázata A műtét legnagyobb előnye a látóélesség és a színlátás javulása. A megválasztott műlencse miatt a régebbi fénytörési hibát (rövidlátás, távollátás, astigmia) kompenzálni tudjuk. A műtét után távolra és/vagy közelre szüksége lehet szemüvegre. Tudnia kell, hogy nagyon kicsi a szövődmény valószínűsége mind a műtét alatt, mind a műtét után. |
| Néhány lehetséges szövődmény a műtét alatt - A lencse hátsó tokjának a szakadása, amely meghiusíthatja műlencse beültetését. Ebben az esetben a műlencsét később, újabb műtét során ültetjük be. - A lencsetok szakadásán keresztül lencsedarabok kerülhetnek a szem belsejébe, mely további műtétet tesz szükségessé. - A szem belsejébe történő vérzés. |
| Néhány lehetséges komplikáció a műtét után - A szem vagy szemhéjvéraláfutása. - Magas szembelnyomás. - Szaruhártya homályosság. - A műlencse elmozdulása. - Látóhártya vizenyő. - Látóhártya leválás, mely a látás elvesztésével is járhat. - Különböző mértékű szemgyulladás. - Allergia az alkalmazott szemcseppre. |
| Manapság a szövődmények igen ritkák és a legtöbb esetben eredményesen gyógyíthatók. Rendkívül ritka a jelentős látásromlás (ezer esetből egy = 0,1%) vagy látásvesztés (tízezer esetből kb. 3 = 0.03%). A leggyakoribb szövődmény a hátsó tok elhomályosodása. A műtét után hónapokkal, ill. évekkel alakul ki. Ebben az esetben a lencse hátsó tokja, mely a műtét közben a helyén maradt, és tartja a műlencsét, homályossá válik. Ez látásromlást okoz. Ez lézerkezeléssel ambulanter gyógyítható. Reméljük, hogy elég információhoz jutott ahhoz, hogy eldönthesse, szeretné-e a szürkehályog műtétet. A keretezett részbe beleírhatja a felmerült kérdéseit, melyeket az orvostól meg szeretne kérdezni. Ne féljen kérdezni, örömmel válaszolunk valamennyien a kérdéseire. APPENDIX 2 Műtéti beleegyező nyilatkozat szürkehályogos betegek részére Alulírott a szürkehályogos betegek részére írt "BETEGTÁJÉKOZTATÓT" elolvastam (részemre azt felolvasták), kezelőorvosom számomra részletes szóbeli tájékoztatást is adott. Az írásbeli és szóbeli tájékoztatás alapján betegségem lényegét és az elvégzendő műtét célját megértettem. Tudomásul veszem, hogy jogomban álla műtétet illetve a további kezeléseket visszautasítani, ennek várható következményeiről is felvilágosítottak. Felmerült kérdéseimre Dr.....................kezelőorvos érthető és kielégítő válaszokat adott. Tudomásul veszem, hogy szakszerű kezelés esetén is igen ritkán műtét alatti és műtét utáni szövődmények (komplikációk) léphetnekfel, melyekesetleg akára látás teljes elvesztését okozhatják. Bizonyos komplikációkfellépése esetén újabb műtétre lehet szükség. Általam ismert betegségeimről (például cukorbetegség, magas vérnyomás, vérzékenység), valamint gyógyszer-érzékenységről kezelőorvosomat tájékoztattam. A fentiek alapján minden kényszertől mentesen beleegyezem a szükséges vizsgálatokba és kezelésekbe, valamint szemem szürkehályog műtétjébe helyi érzéstelenítésben / altatásban*. | |
| Város, időpont: | |
| orvos | beteg |
| tanú (cím) | tanú (cím) |
2. Nehezére esik-e, akár szemüveggel is, újságot, vagy könyvet olvasni?
_Igen_Nem_Nem alkalmazható
Ha igen, jelenleg milyen fokú nehézséget okoz?
1. Kis mértékű
2. Közepes mértékű
3. Súlyos
4. Képtelen rá
3. Nehezére esik-e, akár szemüveggel is, nagy betűs könyveket, újságot elolvasni?
_Igen_Nem_Nem alkalmazható
Ha igen, jelenleg milyen fokú nehézséget okoz?
1. Kis mértékű
2. Közepes mértékű
3. Súlyos
4. Képtelen rá
4. Nehezére esik-e, akár szemüveggel is, felismerni az emberek arcát akkor is, ha közel vannak Önhöz?
_Igen_Nem_Nem alkalmazható
Ha igen, jelenleg milyen fokú nehézséget okoz?
1. Kis mértékű
2. Közepes mértékű
3. Súlyos
4. Képtelen rá
5. Nehezére esik-e, akár szemüveggel is, a lépcsők, járdaszegélyek észrevétele? _Igen_Nem_Nem alkalmazható
Ha igen, jelenleg milyen fokú nehézséget okoz?
1. Kis mértékű
2. Közepes mértékű
3. Súlyos
4. Képtelen rá
6. Nehezére esik-e, akár szemüveggel is, a közlekedési jelzések, utcatáblák, bolti feliratok felismerése, olvasása? _Igen_Nem_Nem alkalmazható
Ha igen, jelenleg milyen fokú nehézséget okoz?
1. Kis mértékű
2. Közepes mértékű
3. Súlyos
4. Képtelen rá
7. Nehezére esik-e, akár szemüveggel is, a finom kézimunka (például varrás, kötés, horgolás, faragás)? _Igen_Nem_Nem alkalmazható
Ha igen, jelenleg milyen fokú nehézséget okoz?
1. Kis mértékű
2. Közepes mértékű
3. Súlyos
4. Képtelen rá
8. Nehezére esik-e, akár szemüveggel is, a csekkek, nyomtatványok kitöltése? _Igen_Nem_Nem alkalmazható
Ha igen, jelenleg milyen fokú nehézséget okoz?
1. Kis mértékű
2. Közepes mértékű
3. Súlyos
4. Képtelen rá
9. Nehezére esik-e, akár szemüveggel is, a játék (például: bingo, kártya, domino, sakk)? _Igen_Nem_Nem alkalmazható
Ha igen, jelenleg milyen fokú nehézséget okoz?
1. Kis mértékű
2. Közepes mértékű
3. Súlyos
4. Képtelen rá
10. Nehezére esik-e, akár szemüveggel is, a sportolás (például: bowling, kézilabda, tenisz, golf)? _Igen_Nem_Nem alkalmazható
Ha igen, jelenleg milyen fokú nehézséget okoz?
1. Kis mértékű
2. Közepes mértékű
3. Súlyos
4. Képtelen rá
11. Nehezére esik-e, akár szemüveggel is, a főzés? _Igen_Nem_Nem alkalmazható
Ha igen, jelenleg milyen fokú nehézséget okoz?
1. Kis mértékű
2. Közepes mértékű
3. Súlyos
4. Képtelen rá
12. Nehezére esik-e, akár szemüveggel is, a TV nézés? _Igen_Nem_Nem alkalmazható
Ha igen, jelenleg milyen fokú nehézséget okoz?
1. Kis mértékű
2. Közepes mértékű
3. Súlyos
4. Képtelen rá
13. Vezet jelenleg autót?
_Igen (14. kérdéshez)_Nem (16. kérdéshez)
14. Milyen fokú nehézséget okoz a nappali vezetésben a látása?
1. Nem okoz nehézséget
2. Kisfokú nehézséget
3. Közepes mértékű nehézséget
4. Súlyos nehézséget
15. Milyen fokú nehézséget okoz az éjszakai vezetésben a látása?
1. Nem okoz nehézséget
2. Kisfokú nehézséget 3. Közepes mértékű nehézséget 4. Súlyos nehézséget
16. Vezetett valaha autót?
_Igen (17. kérdéshez)_Nem (Vége)
17. Mikor hagyta abba a vezetést? _kevesebb, mint 6 hónapja
_6-12 hónapja
_több, mint 12 hónapja
18. Miért hagyta abba a vezetést? _a látása miatt
_egyéb betegség miatt
_egyéb okból
Pontozás:
"Nem okoz nehézséget" = 4 pont "Kis mértékű" = 3 pont "Közepes mértékű" = 2 pont "Súlyos" = 1 pont "Képtelen rá" = 0 pont
A pontozásból ki kell hagyni azt a tevékenységet, amelyet a beteg nem végez (nem a látása miatt) A pontszámokat össze kell adni, és el kell osztani a megválaszolt kérdések számával. Az eredmény 0-4 közötti szám. Az átlagolt pontszámot 25-tel kell beszorozni. A végső pontszám 0-100 közötti (0 = a látása miatt képtelen a kérdezett tevékenységek végzésére, 100 = gond nélkül képes minden kérdezett tevékenység végzésére).
APPENDIX 4:
Szakmai minimumfeltételrendszer
Szemlencse műtétek: HBCS 0660; 0670; 0680; 069C
Ellátási szint: I.; II.; III.
Minimális tárgyi feltétel: Szemészeti műtőasztal Műtőlámpa
Operációs mikroszkóp (koaxiális megvilágítás) Operációs szék
Phakoemulsificator (elülső vitrectommal) Eszköztálcák
Műlencsék (megfelelő raktárkészlet) Viscoelasticus anyag Sz. e. altatógép
Minimális személyi feltétel: 1 fő szemész szakorvos 1 fő műtősnő 1 fő műtőssegéd
Az ellátás végzéséhez szükséges minimális műtéti szám évenként: 100 műtét Diagnosztikus háttér:
Labor, szemészeti A-scan UH, EKG, belgyógyászat
APPENDIX 5:
Evidencia tábla
| Forrás | Populáció (n) Ország | Főbb megállapítások (Összefoglaló megjegyzések a hazai adaptálhatóságra vonatkozóan) | Ajánlás fokozata |
| Műtéti sikeresség (outcome) | |||
| AAO | 426 USA | Funkcionális tesztek alapján mért gyengébb preoperatív látás, az AMD és diabetes hiánya esetén a látási panaszok javulásának mértéke nagyobb. | II, III |
| AAO | 552 USA | A látási panaszok csökkenése szempontjából a 65 év alatti korosztály nagyobb javulást mutat. A súlyosabb panaszokkal és dysfunctioval rendelkező betegek nagyobb javulást mutattak. | III |
| AAO | 552 USA | 75 év feletti korban meglévő más szembetegségek (pl: AMD, glaucoma) esetén csekélyebb mértékű a látási panaszok csökkenése. | III |
| AAO | 552 USA | Az életminőség javulása a 75 év feletti életkorban is funkcionálisan és statisztikailag is szignifikáns. | III |
| AAO | 1933 USA | A betegek 91%-a a látási panaszok javulásról számolt be a műtét után | |
| AAO | 464 USA | Egyéb szemészeti és általános megbetegedések esetén a javulás 12 hó után: 80%-os | |
| AAO | 7626 USA | a látás VF-14 teszt szerinti javulása 90% feletti. | II |
| Royal | 18000 Nagy-Britannia | A szakirodalom áttekintése azt mutatja, hogy ha nincs más szemészeti megbetegedés, a katarakta műtét a betegek több mint 95%-ában a látóélesség javulását eredményezi. Ha a betegnek más jellegű látási panaszai is vannak, mint például macula degeneratio esetén, a látóélesség javulása a betegek kevesebb, mint 80% -át érintheti. | |
| Skót | 2970 Svédország | A Snellen-féle látóélesség-vizsgálat a leggyakrabban alkalmazott módszere a műtéti sikeresség vizsgálatának, noha ez a beteg elégedettségének gyenge indikátora. | |
| AAO | 7626 USA | European Cataract Outcome Study 1999: Az átlagos indukált astigmatizmus: 0,59 D, 86%-ban az indukált astigmatizmus ±1 D-n belül volt. | |
| AAO | 766 USA | A VF-14 teszt szerinti látásjavulás 89%-os, a beteg elégedettsége a látásjavulással 85%-os, a betegek beszámolói a látási nehézségekről a mindennapi életben 80%-os javulást mutatnak | |
| skót | 464 USA | Az ADVS alapján mért látásjavulás az egészségi állapottal összefüggő életminőség javulásához vezet, azt sugallván, hogy a látás javulásával csökkenthető a korral járó egészségromlás. | |
| skót | 1025 USA | Katarakta műtét után idős személyekben több funkcionális degeneratív folyamat lassulhat, vagy megállhat. | |
| Forrás | Populáció (n) Ország | Főbb megállapítások (Összefoglaló megjegyzések a hazai adaptálhatóságra vonatkozóan) | Ajánlás fokozata |
| AAO | az USA-ban az 55-64 év közötti nők 10, a férfiak 3,9%-nak van cataractája. A 65 -74 év közötti nők 23,5, a férfiak 14,3%-nak, mig a 75 év fölötti populációt tekintve a nők 45,9 és a férfiak 38,8%-nak volt kataractája | II | |
| AAO | A szürkehályog multifaktoriális megbetegedés, kialakulásában szerepet játszik a kor,a nem, táplálkozási szokások, szociális körülmények, alkohol fogyasztás, dohányzás, egyes betegségek, mint DM, hypertonia, UV sugárzás stb. | II | |
| Műtéti indikáció | |||
| AAO | ha a szürkehályog a látóélességet 0,6-re vagy annál nagyobb mértékben rontja, ha a lencsehomályoka szemfenéki elváltozások pontos diagnózisát vagy kezelését akadályozzák | III | |
| AAO | ha a beteg ragaszkodik a mütéthez, a visusa jobb 0,6-nál de mindennapi megszokott tevékenységét, munkáját nem tudja ellátni /kontraszt érzékenység, glare test végzése. | IV | |
| ha a mütét refraktív céllal történik/nagyfokú myopiás, nagyfoku hypermetropiás betegekben/(Konsz.) | IV | ||
| AAO | Kontra-indikált | - ha a beteg nem akarja - ha szemüveggel a látóélesség megfelelően korrigálható és ezzel a beteg elégedett - ha a beteg általános állapota nem teszi lehetővé a mütétet | III |
| Műtéti technika | |||
| AAO | Phakoemulsifikació után a visus szignifikánsan jobb és stabilabb, kevesebb a komplikació, kisebb a posztoperatív indukált astigmia, mint ECCe után. /össszehasonlító randomizált tanulmány 1 éves követési idő/ | I | |
| AAO | a lehető legkisebb, jól konstruált, kisfokú astigmiát indukáló seb készítése javasolt | IV | |
| Intraocularis műlencsék | |||
| AAO | Az ideális műlencse biológiailag inert, olcsó, a lens cristallina funkcióját betölti, stabilan a helyén marad, optikailag tiszta, a hátulsó tok tisztaságát hosszú távon biztosítja. | II | |
| AAO | A sebész a beteg szemészeti és általános betegségeit figyelembe véve választja meg a lencse típusát. | III | |
| Törekedni kell PCL implantatiora. ACL csak kivételes esetben, megfelelő indikációval alkalmazható. | IV | ||
| Sclera fixált, kivarrt lencse implantációja indokolt, ha egyáltalán nincsen a PCL hordozására alkalmas tok. | IV | ||
| Perioperativ infectio profilaxis | |||
| AAO | Az 5 %-os Povidone iodine alkalmazása a szemrésbe és az áthajlásokba a műtét előtt bizonyítottan csökkenti a baktérium kolonizatiot a szemgolyó elülső felszínén és csökkenti a posztoperatív endophthalmitis kialakulásának lehetőségét | II | |
| Késői posztoperatív komplikációk | |||
| AAO | A hátulsó tok homályosodásának effektív kezelése a Nd-YAG capsulotomia, melynek célja a látási funkció helyreállítása. | III | |
| Nd-YAG laser kezelés indokolt | |||
| AAO | - Ha a PCO olyan mértékben rontja a látóélességet, amely nem felel meg a beteg funkcionális szükségleteinek. - Ha a tok megvastagodás jelentősen rontja a hátulsó szegment vizsgálhatóságát. - Ha monukuláris diplopiát okoz. A kezelést különös körültekintéssel indokolt tervezni: - intraoculáris gyulladás, - emelkedett szemnyomás, - macula oedema, -retina leválás kockázata esetén (pl. tengely myopia). | III |
APPENDIX 6:
Irodalom
1. Ahn J., Stanley J. A. - Subarachnoid injection as a complication for retrobulbar anaesthesia. Am. J. Ophthalmol., 1987, 103.225-230..
2. American Academy of Ophthalmology. Policy statement: An Ophthalmologist's Duties Concerning Postoperative Care. San Francisco: American Academy of Ophthalmology. 1998.
3. Apple DJ, Solomon KD, Tetz MR, et al. Posterior capsule opacification. Surv Ophthalmol 1992;237:73-116.
4. Apt L, Isenberg S, Yashimori R, Spierer A. Outpatient topical use of povidone iodine in preparing the eye for surgery. Ophtalmology. 1989;96:289-292.
5. Az Aneszteziológiai és Intenzív Terápiás Szakmai Kollégium ajánlásrendszere: Preoperatív aneszteziológiai vizsgálat. Aneszteziológia és Intenzív Terápia 32 (4): 53-71, 2002.
6. Badrinath S. K., Vazzery A., McCarthy R. J., Ivankovich A. D. - The effect of different methods of inducing anesthesia on intraocular pressure. Anesthesiology, 1986,65.431-435.
7. Barker L., Butchart D. G. M., Gibson J., Lawson J. I. M., MacKenzie N. - I. V. Sedation for conservative dentistry. A comparison of midazolam and diazepam. Br. J. Anaesth. 1986,58. 371-377.
8. Bass E.B., Steinberg E.T., Luthra R. et al. Do Ophthalmologists Anestesiologists and Internists agree about preoperativ testing in healthy patients undergoing cataract surgery? Arch Ophthalmol 1995;113:1248-56
9. Bass EB, Wills S, Scott IU, et al. Preference values for visual states in patients planning to undergo cataract surgery. Med Decis Making 1997; 17:324-30. (III)
10 Benson W. H., Farber M. E., Caplan R. D. - Increased morbidity rate after cataract surgery. A statistical analysis. Ophthalmology, 1988,95.1288-1292.
11. Beregi Edit (Edit.): Centenarians in Hungary. Sociomedical and Demographic Study. Interdiscipl. Top Gerontol. Ophthalmological examinations of Centenarians: Éva Fürjes. Basel, Kargel. Vol. 27. pp. 65-82. 1990.
12. Braun D.C., Grabov H.B., Martin RG. Et. al. Staar Collamer intraocular lens: Clóinical results from the phase 1 FDA core study. J Cataract Refract Surg. 1998;24:1032-8
13. Brenner MH, Curbow B, Jawitt JC, Legro MW, Sommer A. Vision change and quality of life in the elderly. Response to cataract surgery and treatment of other chronic ocular conditions. Arch Ophthalmol 1993;111:680-5. (II)
14. Campbell D. N.C., Lim M., Muir M. K., O"Sullivan G., Falcon M., Fison P., Woods R. - A prospective randomised study of local versus general anaesthesia for cataract surgery. Anaesthesia, 1993, 48. 422-428..
15. Channel MM, Beckman H. Intraocular pressure changes after Neodynium: YAG laser posterior capsulotomy. Arch Ophthalmol 1984;102:1024-26.
16. Christen WG,Ayani UA, Schaumberg DA, at al. Aspirin use and riskof cataract in postrial follow-up of Physicians Health Study I. Arch Ophthalmol 2001;119:405-12
17. Christen WG, Glynn RJ, Ayani UA, et al. Smoking cessation and risk of age-related catract in men. JAMA. 2000;284:713-16.
18. Dardenne MU, Gerten GJ, Kokkas K, Kermani O. Retrospective study of retinal detachment following Neodynium YAG laser posterior capsulotomy. J Cat Refract Surg 1989;15:676-680.
19. Davison JA. Positive and negative dysphotopsia in patients with acrylic intraocular lenses. J Cataract Refract Surg 2000,26:1346-55
20. Debaillon-Vesque P., Buffet J. P., Chaudon M. P., Poitrey H. F., Dhedin G. - Association de propofol á Tanesthésie régionale pour la chirurgie de la cataracte. Cahiers Anesthésiol. 1989, 37. 55-56.
21. Delcourt C, Carriere I, Ponton - Sanchez A, et al. Light exposure and the risk of cortical, nuclear and posterior subcapsular cataracts: The Patologies Oculaires Liees a l'Age (POLA) Study. Arch Ophthalmol. 2000;118:385-92.
22. Desai P, Reidy A, Minassian DC. Profile of patients presenting for cataract surgery: National data collection. Br J Ophthalmol 1999,83:893-896
23. Desai P, Minassian DC, Reidy A. National cataract survey 1997-98. A report of the results of the clinical outcomes. Br J Ophthalmol 1999;83:1336-6. (I)
24. Desai P, Minassian DC, Reidy A. The National Cataract Survey l997/98:A report of the results of clinical outcomes. Br J Ophthalmol 1999.83:1336-1340
25. Drysdale D. B. - Experimental subdural retrobulbar injection of anaesthetic. Ann. Ophthalmol. 1984,16. 716-718.
26. European Cataract Outcomes Study. Unpublished data.2000-2007.
27. Facskó Andrea, Süveges Ildikó: A katarakta műtétre került betegek életkorának változása klinikánk 10 éves beteganyagában: A környezeti hatások feltételezett szerepe a szürkehályog kialakulásában. Szemészet. 129:24-26. 1992.
28. Farbowitz MA, Zabriskie NA, Crandall AS, et al. Visual coplaints associated with the Acrysof acrylic intraocular lens /1/.J Cataract Refract Surg 2000,26:1339-45
29. Gills JP. Filters and Antibiotics in Irrigating Solution for Cataract Surgery. J Cat Refract Surg 1991;17:385.
30. Gordon YJ. Vancomycin profilaxis and emerging resistance: Are opthalmologists the villains? The heroes? Am J Ophthalmol 2001;131:371-76.
31. Hall D. L., Steen W. H., Drummond J. W., Byrd W. A. - Anticoagulants and cataract surgery. Ophthalmic Surg. 1988,19. 221-222.
32. Hammond CJ, Duncan DD, Snieder H, et al. The heritability of age-related cortical cataract: the twin eye study. Invest Ophthalmol Vis Sci. 2001;42:601-5.
33. Heinze J., Rohrbach M. - General anesthesia vs retrobulbar anesthesia in cataract surgery. A randomised comparison of patients at risk. Anaesthetist, 1992,41.481-488.
34. Hollick E.J., Spalton D.J., Ursel P.G., Pande M. V. Biocompatibility of polymethylmetacrylate, silicone and AcrySof intraocular lenses: Randomized comparison of the cellular reaction on the anterior lens surface. J Cataract Refract Surg. 1998;24:361-6
35. Javitt JC, Tielsch JM, Canner JK, Kolb MM, Sommer A, Steingberg EP. National outcomes of cataract extraction: increased risk of retinal complications associated with Nd: YAG laser capsulotomy. Ophthalmology 1992;99:1487-98.
36. Jayamanne DG, Allen ED,WoodCM,Currie S. Correlation between early, measurable improvement in quality of life and speed of visual rehabilitation after phacoemulsification. J Cataract Refract surg 1999;25:821-6. (III)
37. Klein BE, Klein R, Linton KL. Prevalence of age-related lens opacities in a population. The Beaver Dam Eye Study. Ophthalmology, 1992;99:546-52.
38. Koch DD, Liu JF, Gill EP, Parke DW. Axial myopia increases the risk of retinal comlications after neodynium: YAG posterior capsulotomy. Arch Ophthalmol 1989;107:986-990.
39. Kohnen S., Ferrer A., Braunweiler P. Visual function in pseudophakic eyes with polymethylmetacrylate, silicone and acrylic intraocular lenses. J Cataract Refract Surg 1996,22 (Suppl 2):1303-7
40. Konstantatos A: Anticoagulation and cataract surgery: a rewiewof the current literature (rewiew) 29 ref. Anaesthesia & Intensive Care. 29 (1): 11-8,2001.
41. Kumar A., Bose S., Bhattacharya A., Tandon O. P., Kundra P. - Oral clonidine premedication for elderly patients undergoing intraocular surgery. Acta Anaesthesiol. Scand.. 1992,36.159-164.
42. Lebuisson D. A., Waked N. - Peut-on opérer de la cataracte, en recourant á Tanesthésie locale, un patient sous anticoagulant oral? B. S.O. F. 1991,6-7.569-572.
43. Lee T. H., Marcantanio E.R., Mangione C.M. et al. Derivation and prospective validation of a simple index for prediction of cardiac risk of major non-cardiac surgery. Circulation. 1999:1010:1043-9.
44. Leske MC, Wu SY, Hennis A, et al. Diabetes, hypertension and central obesity as cataract risk factors in a black population. The Barbados Eye Study. Ophthalmology 1999; 106:35-41.
45. Liesegang TJ. Prophylactic antiniotics in cataract operations Mayo Clin Proc 1997;72:149-59
46. Lum F, Schein O, Schachat AP, et al. Initial two years of experience with the AAO National Eyecare Outcomes Network (NEON) cataract surgery database. Ophthalmology 2000; 107:691-7. (II)
47. Lundström M,Stenevi U,Thorburn W. Cataract surgery in the very elderly. J Cataract Refract Surg 2000; 26:408-14. (II)
48. Lundström M, Stenevi U,Thorburn W. Outcome of cataract surgery considering the preoperative situation: a study of possible predictors of the functional outcome. Br J Ophthalmol 1999;83:1272-6. (II)
49. Lundström M, Stenevi U,Thornburn W, Roos P. Catquest questionnaire for use in cataract surgery care: assessment of surgical outcomes. J Cataract Refract Surg 1998;24:968-74. (II)
50. Mangione CM, Orav EJ, Lawrence MG, et al. Prediction of visual function after cataract surgery. A prospectively validated model. Arch Ophthalmol 1995; 113:1305-11. (II)
51 Mangione CM, Phillips RS, Lawrence MG, et al. Improved visual function and attenuation of declines in health-related quality of life after cataract extraction. Arch Ophthalmol 1994; 112:1419-25. (II)
52. Mangione CM, Phillips RS, Seddon JM, et al. Development of the 'Activities of Daily Vision Scale'. A measure of visual functional status. Med Care 1992; 30:1111-26. (III)
53. Masket S. Truncated edge design, dysphotopsia, and inhibition of posterior capsule opatification. J Cataract Refract Surg 2000,26:145-7
54. McCharty CA, Mukesh BN, Fu CL, Taylor HR. The epidemiology of cataract in Australia. Am J Ophthalmol 1999;128:446-635.
55. Minassian D.C., Rosen P., Dart J.K. et. al. Extracapsular cataract extraction compared with small inscision surgery by phacoemulsification: A randomized trial. Br. J Ophthalmol 2001;85:822-9
56. Minassian DC, Rosen P, Dart JK, et al. Extracapsular cataract extraction compared with small incision surgery by phacoemulsification: a randomised trial. Br J Ophthalmol 2001;85:822-9. (I)
57. Minassian DC, Rosen P, Dart JK, et al. Extracapsular cataract extraction compared with small incision surgery by phakoemulsification: a randomised trial. Br J Ophthalmol 2001,85:822-9
58. Németh J.: Szemészeti ultrahangdiagnosztika és biometria. IX. Biometria. Budapest, Nyctalus, 119-145,1996.
59. Newland TJ, McDermott ML, Eliott D, et al. Experimental neodynium : YAG laser damage to acrylic, poly (methylmetacrylate) and silicone intraocular lens materials. J Cat Refract Surg. 1999;25:72-76.
60. Nizzia P., Lemedica A., Pescatori A., Cocco M. - Low-dose propofol in sedation for cataract surgery in loco-regional anesthesia. Minerva Anestesiol. 1991,57. 580.
61. Olson R.J., Krandall A. S. Prospective randomized comparison of phacoemulsification cataract surgery with a 3,2 mm vs a 5.5 mm sutureless incision. Am J Ophthalmol 1998;125:612-620
62. OSZI módszertani útmutatója. Szürkehályogműtét és műlencse. I. köt. 77-83.1999.
63. Powe NR, Schein OD, Gieser SC, et al. Synthesis of the literature on visual acuity and complications following cataract extraction with intraocular lens implantation. Cataract Patient Outcome Research Team. Arch Ophthalmol 1994; 112:239-52. (I)
64. Risk factors associated with age related nuclear and cortical cataract: A case control study in the Age Related Eye Disease Study. AREDS. Report No. 5. Ophthalmology 2001;108:1400-8.
65. Roberts C.W., Woods S. M.,Turner L. S.-Cataract surgery in anticoagulated patients. J. Cataract. Refract. Surg. 1991,17. 309-312.
66. Saitoh AK, Saitoh A, Tamiguchi H, Amemiya T.: Anticoagulation therapy and ocular surgery. Ophth Surg Lasers 29 (11):909-15, 1998.
67. Salacz György, Ferencz Mária, Papp Melitta: A hályogműtétek és a refraktív sebészet helyzete Magyarországon az ezredfordulón. Szemészet. 138:213-217. 2000.
68. Salacz György, Ferencz Mária: A hályogműtét technikájának változása Magyarországon az 1995-ös felmérés szerint. Szemészet. 134:135-138.1997.
69. Salacz György: A hályogműtét hazai állása 1993-ban. Szemészet. 132:193-195.1994
70. Salacz György: A katarakta és refraktív sebészet helyzete az évezred első évében Magyarországon. (2001-es felmérés adatai). SHIOL Kongresszus. 2002. Keszthely. Absztrakt.
71. Schein O.D., Katz J., Bass E.B. et. al. The value of rutine preoperative medical testing before cataract surgery. Study of Meical Testing for Cataract Surgery. N Engl. J Med. 2000;342:168-75
72. Schein OD, Steinberg EP, Cassard SD, et al. Predictors of outcome in patients who underwent cataract surgery. Ophthalmology 1995; 102:817-23. (III)
73. Schein OD, Steinberg EP, Cassard SD, Tielsch JM, Javitt JC, Sommer A. Predictors of outcome in patients who underwent cataract surgery. Ophthalmol 1995,102:817-823
74. Schein OD, Steinberg EP, Javitt JC, Cassard SD, Tielsch JM, Steinwasch DM. Variationin cataract surgery practice and clinical outcomes. Ophthalmol 1994,101:1142-1152
75. Schmitz S, Dick HB, Krummenauer F, Pfeiffer N. Endophtalmitis in cataract surgery: results of a German survey. Ophthalmology 1999;106:1869-77.
76. Schsein OD, Steinberg EP, Yavitt JCet al. Variation in cataract surgery practice and clinical outcomes. Ophthalmology 1994;101:1142-52.
77. Spalton DJ. Posterior capsular opacification after cataract surgery. Eye 1999; 13:489-92. (II)
78. Speaker MG, Manikoff JA. Prophylaxis of endophthalmitis with topical povidone iodine. Ophthalmology 1991;98:1769-1775.
79. Starr MB, Lally JM. Anti-microbiological prophylaxis for ophthalmic surgery. Surv. Ophthalmol 1995; 39:485-501.
80. Starr MB. Prophylatic antibiotics for ophthalmic surgery. Surv Ophthalmol 1983;27:353-73.
81. Steinberg EP, Tielsch JM, Schein OD, et al. National study of cataract surgery outcomes. Variation in 4-month postoperative outcomes as reflected in multiple outcome measures. Ophthalmology 1994; 101:1131-40; discussion 1140-1. (II)
82. Steinberg EP,Tielsch JM, Schein OD, et al. The VF-14. An index of functional impairment in patients with cataract. Arch Ophthalmol 1994; 112:630-8. (II)
83. Steinert RF, Puliafito CA, Kumar SR, et al. Cystoid macular oedema retinal detachment and glaucoma after Nd: YAG laser posterior capsulutomy. Am J Ophthalmol. 1991;112:373-380
84. Stone I. S., Kline O. R., Sklar S. - Intraocular lenses and anticoagulation and antiplatelet therapy. J. Am. Intra-ocul. Implant. Soc. 1985,11.165.
85. Sulpicio G. S., Rort S. I. - The use of pulse oxymetry to detect desaturation in patients receiving regional anesthesia with intravenous sedation. Reg. Anesth. 1989,14.2-9.
86. Tan JC, Spalton DJ, Arden GB.The effect of neodynium: YAG capsulotomy on contrast sensitivity and the evaluationof methods for its assesment. Ophthalmology 1999;106:703-709.
87. Tanniéres M. L., Coulbois B., Ghnassia M. D., Lebuisson D. A. - Critère de sélection des patiens pour l anesthésie locale ou générale en ophtalmologie. E. M. C. Ophtalmologie, I-1992,21780 B 10,4p.
88. Taylor HR. Epidemiology of age-related cataract. Eye. 1999;13:445-8.
89. Tetz MR, Apple DJ, Price FW Jr et al. A newly described complications of neodynium: YAG laser capsulotomy: egzacerbation o fan intraocular infection. Case report. Arch Ophthalmol 1987;105:1324-1325.
90. West S., Munos B, Emmet E.A., Taylor H.R.: Cigarette smoking and risk of nuclear cataracts. Arch. Ophthalmol 1989; 107:1166-9.
91. West S., Munos B., Emmet E.A., Taylor H.R.: Cigarette smoking and riskof nuclear cataracts Arch. Ophthalmol 1989; 107; 1166-9.
92. Yoshitake S., Matsumoto K., Matsumoto S., Uchiumi R., Taniguchi K., Honda N. - Effects of sevoflurane and isoflurane on intraocular pressure in adult patients. Masui, 1992,41.1730-1734.
93. Barry P, Seal DV, Gettinby G, Lees F, Peterson M, Revie CW; ESCRS Endophthalmitis Study Group. ESCRS study of prophylaxis of postoperative endophthalmitis after cataract surgery: Preliminary report of principal results from a European multicenter study. J Cataract Refract Surg. 2006 Mar;32(3):407-10. Erratum in: J Cataract Refract Surg. 2006 May;32(5):709.
94. Barry.P,Behrens-Baumann.W,Pleyer.U,Seal.D.,ESCRS Guidelines on prevention, investigation and management of postoperative endophthalmitis. 2007 .augustus .Supported by Santen
95. Kaspar.H.M,Kreutzer.T.C et al : A prospective randomized study to determined the efficacy of preoperative topical Levofloxacin in reducing conjunctival bacterial flora. Am J Ophthalmol 2008,145:136-142
96. Vasavada A,Gajjar.D,Raj.S,Vasavada .V,Comparison of 2 Moxifloxacin regimen for preoperative profilaxis:Prospective randomized triple -masked trial Part 1:Aqueous concentration of moxofloxacin. J Cat Refract Surg.2008,34:1379-1382
Az Egészségügyi Minisztérium
szakmai irányelve
A kontaktlencse rendelésről
Készítette: a Szemészeti Szakmai kollégium
I. Alapvető megfontolások Bevezetés
A kontaktlencse közvetlenül érintkezik a szemmel és ezért invazív orvostechnikai eszköznek számít. Ez azonban azt is jelenti, hogy a kontaktlencse nem megfelelő alkalmazása a szem elülső felszínének gyulladásos betegségét akár maradandó látáskárosodát is okozhatja. A szem elülső felszínének betegsége esetén, pedig annak lefolyását és kimenetelét súlyosbíthatja. A kontaktlencse viselés azonban kiváltója is lehet egyes szemészeti betegségeknek: pl. conjunctivitis allergica, keratoconjunctivitis sicca. Ezek mellett természetesen még a kontaktlencsét viselő páciens lencseviselési szabályokat be nem tartó magtartása is okozhat szemészeti szövődményeket.
A fentiek ismerete alapján nem engedhető meg, hogy a páciensek kontaktológiai ellátása egyszerű kereskedelmi forgalomban, hozzá nem értő személyek részvételével történjen (üzleti forgalmazás). A kontaktlencse biztonságos rendelését csak a megfelelő szemészeti-kontaktológiai ismeretekkel rendelkező szakemberek (szemész szakorvosok, optometristák) tudják biztosítani, ugyanis a szemészeti-kontaktológiai vizsgálatok alapján megrendelt lencsének a páciens általi átvételékor történő kipróbálása elengedhetetlen része a kontaktológiai tevékenységnek. A kontaktlencse rendelésére elsősorban a kontaktológiai ismeretekkel rendelkező szemész szakorvos jogosult, aki azonkívül, hogy a kontaktlencsét viselni szándékozó páciens kontaktológiai igényét az indikációs területeken teljeskörűen ki tudja elégíteni, szükség esetén a komplikációkat is rögtön kezelni tudja. Ez utóbbi nagyban hozzájárulhat a szövődménymentes gyógyuláshoz. Egyes indikációs területeken azonban megengedhető (l. indikációs területek), hogy a megfelelő szemészeti és kontaktológiai képzettséggel rendelkező optometrista is illeszthessen kontaktlencsét olyan páciensek számára, akiknél az illesztés előtt kötelezően végzendő szemészeti-kontaktológiai vizsgálatokkal kóros eltérés nem mutatható ki. Ha a szemészeti-kontaktológiai vizsgálatokkal kóros eltérés, vagy annak gyanúja észlelhető, az optometristának a pácienst kontaktológiai ismeretekkel rendelkező szemész szakorvoshoz kell irányítani. A kontaktlencsét viselő pácienseket mind a szemorvosnak, mind az optometristának rendszeres ellenőrizni kell meghatározott séma szerint (l. ellenőrzések), panasz esetén pedig soron kívül. Az ellenőrzések során az esetlegesen kialakuló szemészeti szövődmény észlelése esetén a kontaktlencse viselést azonnal abba kell hagyatni és a pácienst azonnal szemész szakorvosi ellátásba kell részesíteni, vagy oda irányítani. A rendelés során tájékoztatni kell a pácienst azokról a szemészeti ügyeleti helyekről is, ahová panasz esetén rendelési időn kívül is fordulhat.
A kontaktlencse fajtáji Lágylencsék
A lencsék fajtájának megválasztásakor a lágylencsék választása a keménylencsékkel szemben mind a páciensek és mind a lencsét illesztők számára kedveltebb. A páciensek elsősorban azért szeretika lágylencséket, mert hamar hozzá tudnak szokni a lencse viseléséhez és a lencseviselés első napjai sem okoznak igazán kényelmetlenséget. Az illesztők számára is kényelmesebb a lágylencsék illesztése, mivel a lágylencsék többségét egy lencseátmérő értékkel és egyre gyakrabban egy hátsó centrális görbületi sugárértékkel forgalmazzák, ami a nagyon jól kialakított lencsegeometriának és az újlencsealapanyagok nagyfokú flexibilitásának köszönhetően az esetek több mint 90 %-ában jó illeszkedést eredményez. Bár ez a páciens számára legmegfelelőbb lencse kiválasztását leegyszerűsíti, de nem jelentik a szemészeti-kontaktológiai vizsgálatok mellőzését. A lágylencsék rohamosabb terjedéséhez hozzájárul az is, hogy a lágylencsék nyújtotta kontaktológiai lehetőségek az utóbbi évtizedekben sokkal jobban fejlődtek, mint a keménylencséké: pl. eldobható, kiterjesztett viselésű, színezett és színes lágylencsék.
Azokat a lágylencse alapanyagokat, amelyek 4 %- nál több vizet tartalmaznak, lágy hidrogél kontaktlencséknek, 4 % alatti víztartalmúakat pedig lágy nem hidrogél lencséknek nevezik. Ha csak lágy kontaktlencséről beszélünk, a lágy hidrogél lencséket értjük rajta, mivel a 4 % víztartalom alatti lágy kontaktaktlencse alapanyag önmagában jelenleg nem kerül alkalmazásra: pl. a csak szilikon alapanyagot tartalmazó, víztartalommal nem rendelkező lágy kontaktlencséket kényelmetlen viselhetőségük miatt ma már nem alkalmazzák.
1986-ban az amerikai FDA (Food and Drog Administration) a lágy kontaktlencséket ionizáló- és
vízmegkötő-képességük alapján 4 csoportra osztotta (alacsony víztartalom <50 %, magas víztartalom >50%):
Nem ionizáló alapanyagok
alacsony víztartalommal: I. csoport
magas víztartalommal: II. csoport
Ionizáló alapanyagok
alacsony víztartalommal: III. csoport
magas víztartalommal: IV. csoport
Keménylencsék
Keménylencse illesztésére azonban továbbra is szükség van, mert bizonyos esetekben csak ettől a lencsetípustól várható a páciens számára megfelelő optikai hatás - pl. nagyfokú szabályos és szabálytalan szaruhártya asztigmia, keratoconus-, másrészről pedig a kezelhetősége könnyebb és alkalmazásukkor igen ritkák a fertőzéses komplikációk. A páciens lehető legjobb ellátása érdekében ezért feltétlen szükséges a keménylencsét is rendelni, ha ez a legmegfelelőbb a beteg optikai, szemészeti státuszának és életkörülményeinek.
Magyarországon - tekintettel a magyar kontaktológiai hagyományokra - a Györffy által a világon elsőként bevezetett üveget helyettesítő műanyag alapanyagból, a polietilén-metakrilátból (PMMA) készített oxigén áteresztésre nem képes keménylencsékegyre csökkenő mértékben még forgalomban vannak, de a fejlődés kívánalmainak megfelelően a korszerűbb kemény gázáteresztő-alapanyagokból készült lencsék fokozatosan átveszik a helyüket.
A kontaktlencse alapanyagok a mindennapi gyakorlatnak megfelelően
Ma már nehezen lehet naprakészen nyilvántartani a kontaktlencse alapanyagok nagy számát. A mindennapi gyakorlat szempontjából azonban célszerű a következő egyszerű felosztást ismerni, amely általában eleget tesz a lencse fajtájánakoptikai szempontból történő kiválasztásához és a megfelelő ápolószerek megválasztásához is útmutatót ad: Kemény kontaktlencsék
PMMA (polimetilén-metakrilát)
Kemény gázáteresztő Lágy kontaktlencsék
Alacsony víztartalmúak (kisebb mint 50%)
Magas víztartalmú (50%-nál nagyobb)
A kontaktlencse rendelés során a kontaktlencse fajtáján kívül (lágy vagy kemény) a lencse alkalmazásának megfelelően meg kell választani a lencse típusát is: pl. asztigmia lágylencsével való korrigálására tórikus felszínű lencse, presbyopia korrekciójára bifokális vagy multifokális lencse.
A lencseviselés formái
A lencséket lehet rendszeresen, vagy csakalkalomszerűen viselni. A lencsékviselésénekezenkívül két további formája is van: napi és kiterjesztett. A keménylencsék viselésére a rendszeres viselés és a napi viselési forma jellemző, lágylencséket lehet rendszeresen, vagy csak alkalomszerűen viselni és a napi viselési forma mellett - meghatározott lencsetípusoknál - a kiterjesztett viselési forma is alkalmazható.
A lencsék rendszeres viselése
Napi viselés
A legelterjedtebben használt lencseviselési forma, melynek lényege, hogy a lencsét a páciens csak a napi tevékenysége során viseli, éjszakára pedig a lencsét annakfelületi tisztítása után fertőtlenítő-tároló oldatba helyezi. Az újabban bevezetett multifunkcionális ápolóoldatok felületi tisztító és fertőtlenítő hatással egyaránt rendelkeznek. Jelenleg a napi viselési forma számít a legbiztonságosabb lencseviselési formánakis, mivel a lencsék a napi használat után rendszeresen tisztítva, fertőtlenítve vannak. Napi viselési formával hordják a napi eldobható lágylencséket is, amelyek a napi viselés után azonban kidobásra kerülnek. A lencsék napi viselési ideje:
a) Lágylencsék: általában 12 óra, maximum 16 óra.
b) Keménylencsék: általában 12 óra, de a magas gázáteresztő lencséknél sem tanácsos meghaladni a 16 óra viselési időt.
A napi viselés különleges formája a speciális lencsegeometriával és magas oxigénáteresztő-képességgel rendelkező keménylencsék csak éjszaki viselése: a folyamatos éjszakai viselés hatással van szaruhártya törőerejére a speciális lencsegeometria kialakításától függően és néhány hét után a szaruhártya törőereje napközben, a lencse viselése nélkül, aránylag stabil marad.
Kiterjesztett viselés
A kiterjesztett viselés azt jelenti, hogy a lencsét éjszakára nem kell levenni a szemről, hanem - a lencse típusától függően - több napig, vagy akár hetekig is lehet folyamatosan viselni. A kiterjesztett viselési mód a legtöbb esetben kényelmi szempont miatt terjedt el a lencse napi felhelyezése, levétele és ápolásával járó kényelmetlenségek megszüntetése céljából. A folyamatosan viselhető lencséket jelenleg, a típusuktól függően, 1 és 4 hét maximális időtartamig lehet viselni. Erre a viselési formára csak a nagyon jó oxigén-áteresztéssel rendelkező lágylencsék alkalmasak és lényeges az is, hogy a lencséknek ne legyen túl magas a víztartalmuk, mert az a fertőzési veszélyt növelheti. Az erre a viselési formára gyártott lágylencse típusok gyári dobozán fel van tüntetve, hogy a lencse maximum hány napos folyamatos viselésre használható. A lencse a levétele után - kivéve, ha ápolás céljából kerül levételre - nem használható újra. Erre a viselési módra csak azok a páciensek alkalmasak, akik szigorúan betartják a lencseviselés szabályait: beleértve azt is, ha bármilyen lencseviseléssel összefüggő panaszt észlelnek, rögtön abbahagyják a lencse viselését és visszamennek a kontaktlencse rendelésre, rendelési időn kívül pedig szemészeti szakrendelésre mennek.
A kiterjesztett viselési mód az optikai célból történő illesztésen kívül a kontaktológia más területén is eredményesen alkalmazható: pl. terápiás indikáció alapján történő lencseillesztés. Változó időtartamú viselés
A kiterjesztett viselés sajátos formája a változó időtartamú viselés. Ez a viselési mód azt jelenti, hogy a kiterjesztett viselésre alkalmas lágylencsét a páciens főként "napi viselés" szerint viseli, de alkalmanként - pl. utazás, éjszakába nyúló tanulás, éjszakai szórakozás -éjszakára, vagy az alvás idejére nem veszi le a szeméről, később azonban ismét visszatér a napi viselésre. Természetesen ennél a viselési módnál is, amikor a lencsék a napi viselés mód szerint vannak viselve, a lencséket rendszeresen ápolni kell.
A változó időtartamú viseléssel kapcsolatban ismerni kell a következőket is. A jelenleg forgalomban lévő kontaktlencsékfelszíni kiképzése olyan, hogy a mikroorganizmusok nem tudnakáthatolni rajta és nem tudnak a lencse állományába bejutni. Ha a lencse felületén apró sérülések keletkeznek, akkor a lencse anyagához könnyebben tudnak tapadni és állományába is bejutni. A lencsék mikrosérülésének veszélye felhelyezésük, levételük, valamint mechanikus tisztásuk alatt a legnagyobb. Ezért nem tanácsos a kiterjesztett viselésű lencsét előbb napi viseléssel viselni, majd napok múlva átállni a sok napos folyamatos viselésre, a kiterjesztett viselési módra.
A lencsék alkalmi viselése
Az utóbbi években, főként a napi eldobható lágylencsék (l. eldobható forma szerinti viselés) elterjedésének köszönhetően, a lágy kontaktlencsék alkalmi viselésének formája is megnövekedett. A kontaktlencse alkalmi viselésének főbb területei: sportolás, szórakozás. Ezekre az esetekre leggyakrabban a napi eldobható lencsék kerülnek alkalmazásra, amelyek gyakran csak néhány óráig vannak viselve. E napi eldobható lencsék viselésének előnye, hogy a páciensneka lencsék ápolásával nem kell foglalkoznia. A nem napi eldobható lencséket is lehet alkalomszerűen viselni (pl. festett színes lencsék), de ezeket a lencséket nem csak közvetlenül a szemről való levétel után kell ápolni, hanem ha hosszabb ideig viselés nélkül maradnak. Az ápolás gyakorisága a tároló folyadék összetételétől is függ: 4-5 naponként fertőtlenítő hatóanyagmentes tároló folyadék alkalmazása esetén (pl. elbomlott vagy közömbösített hidrogénperoxidos tároló folyadék),
5-6 hetenként fertőtlenítő hatóanyagot is tartalmazó tároló folyadék alkalmazása esetén (a legtöbb fertőtlenítő-tárolófolyadék).
A lencsék cseréje
A lencsék cseréjét alapanyaguk maximális viselhetősége is befolyásolja. A különböző alapanyagú lencsefajták
viselhetőségének javasolt maximális időtartama:
PMMA lencsék: több év
Kemény gázáteresztő lencsék (RGP): 1 -1,5 év
Lágylencsék: 1 nap-1év
A lencsék cseréjére alkalmazott formák: hagyományos, gyakori és az eldobható forma szerinti.
A kontaktlencsék hagyományos forma szerinti cseréje
Keménylencsék
A keménylencsék cseréje - a különlegesebb alkalmazásokra készülteket kivéve - a hagyományos forma szerint 1 - 1,5 éves (RGP), vagy több éves (PMMA) napi viselés után szükséges. A keménylencsék esetében ez az egyetlen cserélési mód és a lencseviselésnek - a lencseviselés szabályainak betartása esetén - nincs káros következménye ilyen hosszú viselési idő után sem.
Lágylencsék
A lágylencsék cseréje a hagyományos forma szerint minimum 6 hónap, maximum 1 éves napi viselés után esedékes. Lágy kontaktlencsék esetében, amelyeknél a hosszú viselési idő szövődmények száma megemelkedésével is járhat, ez a cserélési forma ma már csak akkor ajánlott, ha más lehetőség nincs.
A lágylencsék tömeggyártásának bevezetésével a lencsék forgalmazási árát és ezáltal a lencsék cseréjének idejét is drasztikusan sikerült lecsökkenteni. A legtöbb típusnál jelenleg maximum 1 hónapos viselési idő javasolt. Bizonyos esetekben azonban a pácienst tömeggyártású lágylencsével nem, csak egyénileg gyártott lencsével lehet megfelelően korrigálni. Ezeknek az egyedileg gyártott lágy kontaktlencséknek a cseréje - főként anyagi okok miatt -továbbra is a hagyományos forma szerint történik: pl. kézi festésű lencsék kozmetikai-esztétikai-szemorvosi indikáció alapján, egyedi gyártású tórikus lencsék. Ez nemcsak a Magyarországon forgalmazott egyedileg gyártott lágylencsékre vonatkozik, hanem a kontaktlencsét gyártó cégek az egész világon hasonló viselési időtartam megjelölésével forgalmazzák ezeket az egyedileg gyártott lencséket. Ez utóbbi esetekben a lencsék ápolása még nagyobb odafigyelést igényel. A gyártási technológia további fejlődése azonban biztos maga után fogja vonni az egyedileg gyártott lencsék előállítási költségének csökkenését és ezzel egyidejűleg a lencse gyakoribb cseréjét.
A kontaktlencsék gyakori cseréje
Az utóbbi kutatásokeredményeként az is bebizonyosodott, hogy főként a lágylencse viselésével kapcsolatba hozható allergo-toxicus reakciókért nem egyededül a kontaktlencse ápolószerei a felelősek, hanem a viselés során - rendszeres ápolás ellenére - a környezetből a kontaktlencse felszínén kicsapódó, és/vagy a lencse mikrosérülésein keresztül a lencse anyagába bejutó szennyeződés is. E nemkívánatos tünetek kialakulása megakadályozásának a legegyszerűbb módja a lencsék gyakoribb cseréje.
Jelenleg a legtöbb lágylencsénél a gyakori cserét alkalmazzák, amely azt jelenti, hogy a lencsék cserélési ideje két hét és hat hónap viselési idő között van. Ezek a lencsék napi, vagy kiterjesztett viselési forma szerint viselhetők, a kiterjesztett viselési idő azonban a lencse típustól is függően maximum 4 hét lehet. Jelenleg a legtöbb lágylencsét napi viseléssel hordják és havonta cserélik
A kontaktlencsék "eldobható" forma szerinti cseréje
Szintén a tömeggyártással előállított lágylencsék egyes típusai tartoznak ebbe a csoportba. A lencsék cserélési ideje a felhelyezés utáni percektől - ami a mindennapi gyakorlatban legalább néhány óra viselési időt jelent - maximum 2 hétig tartó viselés idő között van. A lencsék napi, vagy kiterjesztett viselési forma szerint viselhetők. Az amerikai FDA (Food and Drog Administration) eredeti meghatározása szerint az "eldobható" kifejezés azokra a lencsetípusokra vonatkozott, amelyeket maximum 1 hétig folyamatosan viseltek és a lencsék a szemről levéve már nem kerültek újraillesztésre. Az utóbbi időben azonban ez a kifejezés az összes, maximum két hétig viselhető lencsetípusra vonatkozik, függetlenül attól, hogy a lencsét napi, vagy kiterjesztett időtartamú viselési móddal hordják. A napi eldobható viselési forma a jelenlegi álláspont szerint a legkorszerűbb viselési forma, amelyet anyagi okok miatt csak lágy kontaktlencséknél alkalmaznak. Ez a viselési forma különösen jól alkalmazható érzékenyebb szeműek kontaktlencse viselésére. A napi eldobható kontaktlencsék árának további csökkenésével és választékuk bővülésével (pl. színes-, tórikus- bi- és multifokális kontaktlencsék) az alkalmi lencseviselők (pl. szórakozáshoz, sportoláshoz használók) számának jelentős emelkedése is várható. Mivel ezek a lencsék ápolást nem igényelnek, az alkalmi lencseviselőknek ápolószert sem kell vásárolniuk.
A kontaktlencse rendelés személyi feltételei
Szemorvos
2009. előtt szakvizsgázott és szakvizsgázó szemorvosok: kontaktológus vizsga is szükséges.
2009. után Magyarországon szakvizsgázó szemorvosok: kontaktológiai vizsga nem szükséges, mert a szakvizsgaképzés része.
Honosított szakvizsga esetén: kontaktológus vizsga is szükséges, kivéve ha a hazainak megfelelő kontaktológiai képzés dokumetummal is igazolható.
Optometrista
1987-1994 között tanfolyami képzésben végzett optometrista-látszerészeknek: kontaktológus vizsga szükséges 1995-től főiskolai diplomával végzett optometristák: kontaktológus vizsga nem szükséges
A lencseviselés indikációi és kontraindikációi
Szemorvos és az optometrista kontaktológiai tevékenységi köre az egyes lencseviselési indikációs csoportok alapján Optikai indikáció
Egyszerű optikai-kozmetikai indikáció Illesztheti: szemorvos, optometrista
Ebbe az indikációs területbe tartozik a kontaktlencsét viselők legnagyobb része, általában azok az esetek, amikor a páciens szemüveggel is jól lát, de a szemüvegét nem szereti viselni. Ebbe a csoportba sorolható a szem kisfokú ametropiájának kontaktlencsés korrekciói. Optikai-szemorvosi indikáció Illesztheti: szemorvos
Ebbe az indikációs csoportba azok az esetek tartoznak, amelyeknél a kétszemes látás szemüveggel nem, de kontaktlencsével megoldhatóvá válhat; valamint a látásélesség további javítása várható kontaktlencsével a szemüveggel szemben. Kétszemes látás helyreállítása
Szemüveggel a kétszemes látás nem hozható helyre az aniseiconia miatt:
a) féloldali aphakia
b) 3,0 D-nál nagyobb anisometropia
Szemészetileg szorosabb ellenőrzést igénylő nagyfokú ametropiákés szaruhártya deformitások
Ezekben az esetekben a látásélesség és/vagy látáskomfort további javulása is várható a szemüveggel szemben (a D
értékek a szemüveges korrekció értékeire vonatkoznak):
a) nagyfokú ametropiák esetei (progresszív myopia, glaucoma, keratoconus gyakoribb előfordulása miatt) 8,0 D feletti myopia
6,0 D feletti hypermetropia, (kétoldali aphakia is) 3,0 D feletti szabályos asztigmia
b) szabálytalan szaruhártya asztigmia, keratoconus Optikai-kozmetikai-szemorvosi indikáció Illesztheti: szemorvos
A szem szivárványhártyájának helyettesítése a kontaktlencsére festett szivárványhártya rajzolattal (szükség szerint ametropia korrekciót is alkalmazva). Ebbe a csoportba a szivárványhártya olyan veleszületett és más betegségei, műtét utáni állapotai tartoznak, amelyek a rossz látásélességgel összefüggésbe hozhatók: pl. aniridia, albinizmussal összefüggő átlátszóság, teljes coloboma, látást zavaró basalis iridectomia utáni állapot, a pupilla trauma és más betegség által okozott kitágulása.
Orvosi indikáció
A kontaktlencse viselésnek van olyan indikációs területe is, amelyben a lencseviselés indikációja valamilyen betegséggel áll összefüggésben. Orvosi-optikai indikáció Illesztheti: szemorvos
Ebbe a csoportba tartoznak a szemüveg viselhetetlenségének olyan esetei, melyek a szemüveg támaszkodásának megfelelő helyeken előforduló betegségekkel állnak összefüggésben: pl. bőrbetegségek, sérülések által keletkezett deformitások, fejlődési rendellenességek. Szemorvosi terápiás indikáció Illesztheti: szemorvos
A kontaktlencsék terápiás célból általában egyes szaruhártya betegségek gyógyításában kerülnek alkalmazásra. A terápiás lencsék alkalmazásának célja a legtöbb esetben a felső szemhéjmozgásnak a beteg szaruhártya felszínére gyakorolt irritáló hatásának megszüntetése, vagy a felsőszemhéj belső felszíni egyenetlensége által fellépő szaruhártya irritáció kiküszöbölése.
A terápiás kontaktlencse alkalmazása fő terápiaként
1. A szokványos terápiára rezisztens esetek:
a) A szaruhártya egyes krónikus betegségei, melyek a szokványosan alkalmazott konzervatív terápiára nem gyógyulnak: keratitis filiformis, erosio recidivans, egyéb felszíni hámosodási zavarok, kisebb steril fekélyek
b) Olyan kötőhártya betegségek, melyek a szaruhártya felszínét irritálják: conjunctivitis vernalis, superior limbic keratoconjunctivitis
c) Szaruhártya szövődménnyel járó keratoconjunctivitis sicca egyes esetei (csak átmeneti terápiaként)
2. Első terápiaként szaruhártya sérülések egyes eseteiben: lamellaris sérülés, perforáló kis átmérőjű sérülés, nagy hámhiányt okozó sérülés
3. Első terápiaként (a lehető legnagyobb lencseátmérőt választva) a kémiai sérülések után a symblepharon képződés megakadályozása. Ebbe a csoportba tartozik még a kontaktkagyló és a symblepharon gyűrű alkalmazása is.
A terápiás kontaktlencse alkalmazása kiegészítő terápiaként
1. Műtétek előtt, ha műtét elvégzése akadályba ütközik:
a) Szaruhártya műtétekelőtt: keratopathia bullosa, nagy átmérőjű ulcus és descemetocele, perforáció
b) Egyes szemhéjplasztikai műtétek előtt (pl. trichiasis)
2. Műtétek után a gyorsabb gyógyulási folyamat elősegítésére:
a) Szaruhártya műtétek után: lamellaris keratectomia (excimer lézerrel végzett műtéteket is beleértve), tartósan fennálló hámosodási zavar keratoplasztika után, több apró idegentest eltávolítása után, a szaruhártya felszínéről kiemelkedő képlet (pl. fonál) esetei
b) Panaszt okozó, a szemgolyó felé felszíni egyenetlenséggel járó kötőhártya és szemhéjplasztikai műtétek után Kozmetikai indikáció festett lencsék alkalmazásával
Ebbe a csoportba azokaz esetek tartoznak, amelyekben a páciens látásélességét a lencse festettsége nem befolyásolja és a páciens kozmetikai célból igényli, hogy a lencse festett legyen. A lencsék sokfélék, lehetnek színezettek (átlátszóak), vagy színesek (a pupilláris terület kivételével nem átlátszóak), amelyekkel a szivárványhártya színárnyalatát, vagy színét is meg lehet változtatni.
Egyszerű kozmetikai indikáció színezett vagy színes lencsék alkalmazásával (szemorvos, optometrista) Illesztheti: szemorvos, optometrista
Színezett, vagy színes lencsék alkalmazása a szivárványhártya színárnyalatának vagy színének megváltoztatása kozmetikai célból:
a) törőerővel ellátott lencsékkel (a szem ametropiájának korrekciójával)
b) törőerő nélküli lencsékkel Kozmetikai-esztétikai-szemorvosi indikáció Illesztheti: szemorvos
A színes lencsék lehet alkalmazni a látásfunkcióval nem rendelkező szemen, a szem felületén, vagy az elülső szegmentben kialakult feltűnő, torzító rendellenességek eltakarása céljából is. Ezekben az esetekben a festett szivárványhártyájú lencse pupillaris területe lehet átlátszó, vagy átlátszatlan fekete, amelyet az alapbetegségtől függően lehet megválasztani.
Foglalkozási indikáció
Illesztheti: szemorvos, optometrista
A lencseviselés olyan foglalkozási körökben is javasolt, amelyeknél a szemüveggel szemben a kontaktlencsés korrekció tudja jobban biztosítani a munkavégzéshez szükséges feltételeket: pl. előadóművészek, rendőrök, tűzoltók, szakácsok, sportolók (pl. előadóművészeknél a nagy fokú ametropia korrekció esetén kozmetikai célból javasolt a kontaktlencse, szakácsoknál a szemüveg párásódása miatt jobb a kontaktlencse, sportolóknál a szemüvegkeret veszélyes lehet és nagyfokú ametropia esetén a kontaktlencse jobb térlátást ad).
Indikációk lágy és kemény kontaktlencse viselésére
A lencse fajtájának megválasztását több tényező is befolyásolhatja. Vannak olyan indikációs területek is ahol mindkét lencsefajtát egyformát lehet alkalmazni: pl. kis fokú ametrópia korrekciója. A következőkben azok az irányelvek kerülnek leírásra amelyek segítséget nyújtanak a kontaktlencse fajtájának megválasztásában.
Indikációk lágy kontaktlencse viselésére:
- a viselés lehető leggyorsabb elkezdése,
- kényelmi szempontok,
- kozmetikai szempontok (színezett vagy színes lencsék alkalmazása),
- időszakos és alkalomszerű viselés,
- sporttevékenység,
- poros munkahelyi környezet (lehetőleg kerülni kell az illesztést),
- nystagmus,
- tágabb szemrés (pl. exophthalmus),
- csecsemők és kiskorú gyermekek kontaktlencsés korrekciója (szoros felügyelet mellett kiterjesztett viselési idejű lencsék alkalmazásával),
- terápiás célból való alkalmazás,
- nem szaruhártya-eredetű asztigmia,
- keménylencse viselhetetlensége esete.
Indikációk kemény kontaktlencse viselésére:
- ha a lehető legjobb optikai korrekció szükséges,
- nagy fokú szabályos szaruhártya asztigmia, általában 2,75 D feletti,
- szabálytalan szaruhártya asztigmia,
- a lencseviselés alvásközben, törőerő csökkentés céljából,
- idősebb páciensek aphakiája (egyszerűbb kezelhetőség, kisebb a szövődmény kialakulásának veszélye),
- monoculus és öregkori lencseviselés (egyszerűbb kezelhetőség, kisebb a szövődmény kialakulásának veszélye),
- a levegőben irritáló anyagok előfordulásának veszélye,
- tartós helyi szemészeti kezelés szükségessége (pl. glaucoma, de eldobható cserélési forma szerinti lágylencsék is alkalmazhatók),
- progrediáló myopia (a myopia progressziójának akadályozása céljából),
- limbus közeli naevus conjunctivae (a kis átmérő miatt a lencseszélnek nincs irritáló hatása).
Lágylencse és keménylencse viselésének egymással szembeni előnyei és hátrányai
Lágylencse viselésének előnyei és hátrányai keménylencsével szemben Előnyei:
- igen könnyű hozzászokás
- alkalomszerűen is viselhető,
- nehezebben veszíthető el,
- ritkán jut alá porszemcse. Hátrányai:
- a lágy alapanyagnak nincs annyira jó optikai tulajdonsága mint a keménylencsének,
- a lencsék cseréjének szükségessége gyakoribb mint a keménylencséké,
- ápolása nagy gondosságot igényel,
- a fertőzéses komplikációk súlyosabbak,
- utómegmunkálásra nincs lehetőség,
- száraz vagy vegyszergőzös levegőben viselése problémákat okozhat. Keménylencse viselésének előnyei és hátrányai lágylencsével szemben Előnyei:
- a kemény alapanyagnak nagyon jó az optikai leképezése,
- szaruhártya asztigmiája legalább 4,0 D-ig jól korrigálható egyszerű szférikus lencsével,
- a szaruhártya törőerejét tervezetten befolyásolhatja,
- élettartama 1-1,5 év, kemény PMMA lencséknél több év,
- ritkák a súlyosabb komplikációk,
- kezelése és tisztítása egyszerűbb,
- utómegmunkálásra is van lehetőség (újabb típusoknál korlátozottan),
- száraz levegő vagy vegyi gőzök esetén is viselhető.
Hátrányai:
- a viseléshez való hozzászokás időigényes,
- poros környezetben viselése problémát okozhat,
- könnyebben elveszíthető,
- esetenkénti viselésre nem alkalmas,
- törékeny,
- karcolódhat, ami nem minden típusnál javítható.
A kontaktlencse viselésének előnyei és hátrányai más korrekciós módszerekkel szemben
A lencseviselés előnyeit és hátrányait az ametropia más, gyakrabban alkalmazott korrekciós módszereivel szemben is össze lehet hasonlítani.
A lencseviselés előnyei és hátrányai a szemüvegviseléssel szemben Előnyei:
- Nagyfokú ametropia (myopia, hypermetropia, szabályos asztigmia) korrigálásakor is torzításmentes leképezést ad.
- Nagyfokú myopia korrigálása esetén az accomodatio-convergia helyes kapcsolata is helyreáll.
- 3,0 dioptriát meghaladó anisometropia esetén is helyreállítható a kétszemes látás (az aniseikonia megszüntethető).
- A szemüvegkeret látótérszűkítő hatása nem jelentkezik.
- A szaruhártya szabálytalan felszíni egyenetlenségének korrekciójakor (pl. szabálytalan asztigmia, keratoconus) is jó eredmény érhető el.
- Nagyfokú ametropiák korrigálása esetén a szemüvegviseléshez képest természetesebb megjelenés ad.
- Bizonyos foglalkozásoknál és sportolásnál használata előnyösebb.
- Kozmetikai célból a szem színét is meg lehet vele változtatni. Hátrányai:
- Nagyobb anyagi kiadásokkal jár.
- Rendszeres ápolást igényel (kivétel: napi eldobható lencsék, kiterjesztett viselésű lencsék).
- Alkalmazása kezdetben nehézkesebb, viseléséhez való hozzászokás időt igényel.
- Könnyebben elveszíthető.
- Több komplikációt okozhat.
- Keménylencse szemüveggel való felcserélése átmeneti látáspanaszt okozhat.
A lencseviselés előnyei és hátrányai refraktívsebészeti módszerekkel szemben Előnyei:
- Nagyfokú refrakciós hibák (ametropiák) is egyszerűen és jó eredménnyel korrigálhatók.
- A szem esetleges törőerő-változása is könnyen korrigálható másik törőerejű lencse illesztésével.
- A szaruhártya szabálytalan felszíni egyenetlensége (pl. szabálytalan asztigmia, keratoconus) esetén is jó eredmény érhető el.
- A kétszemes korrekció egyszerre való elkezdésének nincs kockázata.
- Nincs műtéti szövődménylehetősége.
- A lencseviselés rögtön elkezdhető a megfelelő kontaktológiai-szemészeti vizsgálatok és a páciens kontaktológiai betanítása után.
- Több kozmetikai lehetőség is adott (színezett és színes lencsék). Hátrányai:
- Jelenleg nagyobb anyagi kiadásokkal jár hosszabb távon.
- Rendszeres ápolást igényel (kivétel: pl. napi eldobható lencsék).
- Komplikációk a viselés közben előfordulhatnak (ha a páciens nem tartja be a viselés szabályait).
- Elveszíthető.
Kontraindikációk a lencseviselésre
A lencseviselés kontraindikációja többféle lehet. Az abszolút kontraindikáció megléte esetén a pácienst a lencseviselésről le kell beszélni; relatív és időleges kontarindikáció esetén egyénre szabva, a páciens körülményeinek ismeretében kell döntést meghozni a kontaktlencse viselhetőségéről, vagy újraviselhetőségéről.
Abszolút kontraindikáció
Az abszolút kontraindikációban felsorolásra kerülő tényezők bármelyike önmagában is kontraindikálja a lencseviselést.
Szemészeti betegségek:
a) a könnytermelés erős lecsökkenése vagy hiánya,
b) a szaruhártya érzéketlensége,
c) a lencsének a szaruhártyára való rossz felfekvése, centrálódásának hiánya,
d) a szemhéjzárás vagy nyitás kifejezett elégtelensége. Nem szemészeti betegségek:
a) öntudatlan állapot, vagy gyakori öntudatvesztéssel járó betegség,
b) neurotikus félelem a lencse illesztésétől és levételétől. Egyéb okok:
a tisztaság, intelligencia, megbízhatóság hiánya. Relatív kontraindikáció
Relatív kontraindikáció esetén az ok legtöbbször nem szüntethető meg. A lencseviselés során ezekben az esetekben a szövődmények megjelenésének veszélye fokozottabb (pl. csökkent könnytermelés), vagy szövődmény kialakulása esetén a következmény súlyosabb lehet (pl. félszemûség). Ilyen esetekben a lencseillesztést kerülni kell, csak olyan esetben lehet engedményt tenni az illesztő kontaktológus saját felelősségére, ha a páciens együttműködő, jól kontrollálható: rendszeresen eljár a sűrűbb ellenőrző vizsgálatokra és viselési probléma esetén abbahagyja a lencseviselést és rögtön jelentkezik a kontaktológiai rendelésre, vagy a szemészeti ügyeletre. Szemészeti betegségek:
a) csökkent könnytermelés,
b) félszeműség,
c) tartós lokális szemészeti kezelést igénylő szemészeti betegség (pl. glaucoma). Nem szemészeti betegségek:
a szervezet védekezőképességének tartós meggyengülésével járó betegségek (pl. autoimmun betegségek). Egyéb okok:
a lencseviselést befolyásoló, de nehezen megváltoztatható környezeti tényezők (pl. munkahelyi por, füst, vegyszergőzök).
Időleges kontraindikáció
Az időleges kontraindikáció a legtöbb esetben a fertőző betegségek akut időszakára vonatkozik, de idetartozik számos, a szemgolyó körüli helyreállító műtétet igénylő betegség is. A betegségek eredményes terápiája után lehet csak ismét a kontaktlencsét illeszteni. Szemészeti betegségek
a) szemhéjbetegségek: blepharitis, hordeolum, chalazeon, entropium, ektropium, ptosis, lagophthalmus
b) könnyszervek betegségei: dacryocystitis, dacryoadentitis
c) kötőhártya betegségek: conjunctivitis, pterygium egyes formái, postoperációs hegesedések egyes esetei
d) szaruhártya betegségek: keratitis, ulcus, erosio, idegentest
e) szivárványhártya betegségei: iritis, iridocyclitis
f) a szemben fennálló gyulladásos folyamatok
g) egyes szemcseppek időszakos alkalmazásának szükségessége: pl. antibiotikum, pupillatágító
h) a szemgolyó műtéti megoldást igénylő betegségei
Nem szemészeti betegségek
a) fertőző betegségek: pl. influenza
b) erős legyengüléssel járó betegségek
c) átmeneti öntudatlan állapottal járó betegségek
d) műtéti megoldást igénylő betegségeknél a műtétek időtartamára Egyéb okok
A környezeti vagy munkahelyi körülmények olyan átmeneti változása, mely a lencseviselés szövődményeinek kialakulását okozhatják: pl. poros, piszkos helyen való munkavégzés
II. Diagnózis
A kontaktlencse viselését szándékozó páciens vizsgálata Anamnézis felvétele
Az anamnézis felvétele, amely a kellő gyakorlattal rendelkező kontaktológus számára csak néhány percet vesz igénybe, igen fontos, mivel ennek segítségével már körvonalakban meg lehet ismerni a páciens motivációját, elvárásait a lencseviseléssel kapcsolatban. Ezenkívül az anamnézis felvétele során olyan adatok birtokába lehet jutni, amelyek segítik a kontaktológust a megfelelő lencsetípus és a viselési forma kiválasztásában, és egyes esetekben már ekkor felvetődhet a lencseviselés kontaindikációjának lehetősége is. Az anamnézis három fő részből áll: kontaktológiai, szemészeti-kontaktológiai és általános-kontaktológiai.
Kontaktológiai anamnézis
Fontos megismerni a páciens motivációját a kontaktlencse viselésre:
Miért szeretne lencsét viselni?
Honnan vannak ismeretei a lencseviselésről?
Ha a páciensnek van határozott elképzelése a lencseviselésről, az alábbiakra kell rákérdezni: Milyen célból szeretné a lencsét viselni? Milyen lencsét szeretne viselni?
Meg kell a pácienstől azt is kérdezni, hogy volt-e személyes tapasztalata a lencseviseléssel: Korábban viselt-e lencsét?
Ha viselt, milyen fajtájú és típusú lencsét (lencséket) viselt?
Ha viselt, milyen ápolószert (ápolószereket) alkalmazott?
Ha viselt, volt-e problémája a viseléssel és/vagy a lencseápolással?
Szemészeti-kontaktológia anamnézis
Különös tekintettel kell figyelembe venni a kontaktlencse viselés kontraindikációinak csoportjaiban felsorolt szemészeti betegségek fennállásának, vagy korábbi fennállásának lehetőségét. Ezen kívül fontosak lehetnek még általában a következő adatok is: hosszantartó szemészeti kezelés, visszatérő szemgyulladások, gyakori szemvörösödés, szárazságérzés, asthenopiás panaszok, lezajlott szembetegségek és operációk, heterophoria, kancsalság, amblyopia, a szemüveghordás kezdeténekés utolsó törőerő változtatásának időpontja stb.
Általános-kontaktológiai anamnézis
Szintén figyelembe kell venni a kontaktlencse viselés kontraindikációinakcsoportjaiban felsorolt általános betegségek fennállásának, vagy korábbi fennállásának lehetőségét. Gyakran előfordul az is, hogy a lencseviseléssel kapcsolatos panaszok hátterében szisztémás betegségek (pl. diabetes, allergiás betegségek), tartós nagydózisú gyógyszeres kezelés (pl. immunoszupresszív kezelés), vagy terhesség áll. Ezért ezek az adatoka későbbi viselési problémák okának tisztázásában segítséget nyújthatnak.
Szemészeti-kontaktológiai vizsgálatok
Az anamnézis felvétele utáni szemészeti-kontaktológiai vizsgálat célja a kontaktlencse viselésére való alkalmasság megállapítására és a próbalencse kiválasztásához szükséges adatok meghatározása.
A szemészeti-kontaktológiai vizsgálatok csoportjai
A lencseviselés alkalmasságának megállapítására alkalmazott vizsgálatok
A könnytermelés és a könnyfilm vizsgálata
A szemhéjak vizsgálata
A szem elülső szegmentjének vizsgálata
A szemfenék vizsgálata
Szükség esetén további vizsgálatok
A próbalencse kiválasztásához szükséges vizsgálatok A szemüveges korrekció értékének meghatározása
A vízszintesen látható legnagyobb szivárványhártya átmérő mérése (szaruhártya átmérő meghatározása) A szaruhártya elülső felszíne centrális görbületi sugarának mérése
A szemészeti-kontaktológiai vizsgálatok menete
A szemészeti-kontaktológiai vizsgálatokat az előző csoportosítástól függetlenül meghatározott sorrendben célszerű végezni:
A szemüveges korrekció értékének meghatározása
A vízszintesen látható legnagyobb szivárványhártya átmérő mérése
A könnytermelés vizsgálata
A szemhéjak vizsgálata
Réslámpás vizsgálatok
A szem elülső szegmentjének vizsgálata
Vizsgálatok a könnyfilm fluoreszceines festésével
A tarsalis kötőhártya vizsgálata
A szaruhártya elülső felszíne centrális görbületi sugarának mérése A szemfenék vizsgálata
Szükség esetén egyéb szemészeti-kontaktológiai vizsgálatok III. Kezelés
A lencse illesztésének általános szabályai
A próbalencse kiválasztása
1. A lencse fajtájának és típusának megválasztása
Az anamnézis és a szemészeti-kontaktológiai vizsgálati eredmények birtokában a kontaktológusnak el kell dönteni, hogy páciensének milyen fajtájú lencsét - lágyat vagy keményet - és ezen belül pedig, hogy milyen típus viselését javasolja : pl. egyszerű szférikus vagy tórikus. Döntésének okát meg kell, hogy beszélje a páciensével is és szükség esetén, ha a páciens más lencsére való kívánalmának nincs kontraindikációja, a lencse fajtájának és típusának megválasztásában módosítást is végezhet. Sajnos a választást nem egyszer az is befolyásolhatja, hogy a kontaktológus milyen próbalencse sorozatokkal rendelkezik. A páciensek különlegesebb igényű ellátásához igen sok próbasorozattal is kell rendelkezni a kontaktológusnak, ha erre nincs lehetőség, a különlegesebb igényű páciens inkább nagyobb, szélesebb választékkal rendelkező kontaktlencse laborba kell irányítani.
2. Az első próbalencse paramétereinek meghatározása
A próbalencse paraméterei meghatározása a legtöbb esetben a szemüveges korrekció értékéből (+- 3,75 D feletti törőerő értéknél átszámítás szükséges táblázat segítségével), a szaruhártya keratométeres vizsgálati eredményéből és a szivárványhártya vízszintes átmérőjének értékéből meghatározható. Egyszerűbb esetekben egyes lágylencse típusok illesztésénél a dioptria érték megadása is elegendő lehet a próbalencse kiválasztásához, ez azonban nem jelentheti a szemészeti-kontaktológiai vizsgálatok mellőzését.
Más esetekben, a szokványos vizsgálati eredményeken kívül, további méréseredményekre is szükség lehet a próbalencse kiválasztásához: pl. multifokális lencsék illesztése presbyopia korrigálására.
A próbalencse illesztésének menete
A próbalencsék illesztésének menete egyszerűbb esetekben hasonló lágy- és keménylencséknél. Az átlagostól eltérő lencsék illesztésénél a gyári útmutatókat kell pontosan követni: pl. tórikus lágylencsék, keratoconus keménylencsék.
1. Az próbalencse felhelyezése a páciens szemére
A lencsefelhelyezés menetéről való tájékoztatás után a kiválasztott próbalencsét a páciens szemére fel kell helyezni.
2. Az próbalencse illeszkedésének vizsgálata rögtön az illesztés után
Egyszerű réslámpás vizsgálat. Ilyenkora lencse illeszkedésének helyességéről még nem lehet pontosan nyilatkozni, de a durva illesztési hibák már ennél az első vizsgálatnál is észrevehetők. Durva illesztési hiba esetén a lencsét ki kell cserélni a lencse illesztési szabályainak megfelelően.
3. Tűrőképesség próba
Az illesztés menetének 2. és 4. pontja közötti időt, amely a lencse paramétereinek és mozgásának stabilizálódásához szükséges, egyben a lencseviselés tűrőképességének vizsgálatára használható. E lencseviselési idő alatt már támpontokat lehet kapni a páciens lencseviselési toleranciájával kapcsolatban. Míg a lágylencse viseléséhez való hozzászokás általában nem okoz problémát, keménylencsékhez való hozzászokás nehezebb, és sikertelen esetek is gyakrabban előfordulnak. Sokszor sikertelennek induló esetek is kis idő elteltével már jó irányú változást mutatnak, ezért a lencsefelhelyezés után rögtön nem tanácsos a páciensek feladni a lencseviselést. A tűrőképességi idő hosszúsága, a lencse paramétereinek és mozgásának stabilizálódásához szükséges időtartam, a lencsék fajtájától és típusától is függ, általában 30-40 perc.
4. A próbalencse illeszkedésének újbóli vizsgálata
A réslámpás vizsgálattal a finomabb illeszkedési sajátosságok is megfigyelhetővé válnak, nem megfelelő illeszkedés esetén a lencse cseréje szükséges az illesztési szabályok alapján.
A kontaktlencse illesztésekor a kontaktlencse a szaruhártya előtt elhelyezkedő könnyfilm tetejére kerül, majd a pislogás hatására a kontaktlencse felületén is könnyfilm képződik. A szaruhártyára illeszkedő kontaktlencse speciálisan kialakított hátsó felszíne geometriájának, valamint a szaruhártya és lencse között elhelyezkedő könnyfolyadék közötti összetett fizikai hatásoknak köszönhetően érhető el az, hogy ha a kontaktlencse a szemhéj, vagy szemmozgás hatására kimozdul centralizált nyugalmi helyzetéből, a kimozdító erő megszűnése után vissza tud jutni a nyugalmi helyzetébe: "centralizálódik". A kontaktlencsének a szemen való mozgására mindenképpen szükség van, hogy a lencse és a szaruhártya közötti könny cserélődjön.
A könny cserélődése a szaruhártya anyagcseréjének szempontjából igen fontos, mert így még több oxigén tud eljutni a szaruhártyához a könnyben oldott oxigén segítségével, másik jelentősége pedig az, hogy a könnybe kiválasztott szaruhártya anyagcseretermékek el tudnak távozni a szaruhártya felületéről.
A kontaktológusnak az a feladata, hogy ezt a mozgást bizonyos határok között tartsa, mivel ha a lencse a kelleténél jobban kimozdul (lapos illeszkedés), nehezen tér vissza a nyugalmi állapotába és könnyen leesik a szemről; ha nem mozdul ki nyugalmi helyzetéből (meredek illeszkedés) a könnyfilm cserélődési hiánya miatt a lencse és szaruhártya között felhalmozódó anyagcseretermékek toxikus hatást fejtenek ki. A mozgás mértéke keménylencsék esetében főként a lencse belső felszíne centrális görbületi sugarának, vagy a lencse átmérőjének változtatásával érzékenyen befolyásolható. A lágylencsék mozgásában, centralizációjában a lencse rugalmassága is nagy szerepet játszik, és az is, hogy a lágylencse nem csak a szaruhártyára egy részére, hanem a bulbáris kötőhártyára limbust körülvevő részére is illeszkedik,ami sokkal jobb tapadást és centralizációs hajlamot biztosít. A lágylencse rugalmassága miatta hátsófelszín centrális hátsó görbületi sugarának közepes értékével az esetek 90 % ában jó illeszkedést lehet elérni.
Az ideális illeszkedésnél a lencse hátsófelszíne és a szaruhártya felszíne közötti távolság a lencse egész területén azonos, amit párhuzamos illeszkedésnek neveznek. A lencse illeszkedése,a párhuzamos illeszkedésen kívül lehet még meredek vagy lapos, amelyeket az illesztési szabályoknak megfelelően új próbalencse felhelyezésével kell kiküszöbölni.
A kontaktlencse illeszkedésének fő formái a szaruhártyán
A szaruhártyára felhelyezett kontaktlencse - a speciális illeszkedési formákat kivéve - három fő illeszkedési formát mutathat mind kemény, mind lágy kontaktlencsék eseteiben: párhuzamos, meredek és lapos. A sokkal alaposabb vizsgálatot igénylő keménylencsék illeszkedését a könnyfilm fluresceines megfestésével a réslámpa kék megvilágító fényében is meg kell vizsgálni, ugyanis a lencse és a szaruhártya között elhelyezkedő megfestett könnyfilm színe igen érzékenyen változik a könnyfilm vastagságától függően és ezáltal jól megmutatja a lencse illeszkedését. Párhuzamos illeszkedés: A lencse és a szaruhártya között egyenlő vastagságú könnyfilm helyezkedik el. Párhuzamos vagy közel párhuzamos illeszkedés esetén a lencse a pislogásoknál és szemmozgásoknál kimozdul a szaruhártyán centralizált helyzetéből, de rögtön vissza is tér az eredeti helyzetébe.
Lapos illeszkedés: A kontaktlencse belső centrális görbületi sugara nagyobb, mint ami a párhuzamos illeszkedéshez szükséges lenne. A lencse és a szaruhártya között centrálisan vékonyabb, széli részek felé pedig vastagodó könnyfilm helyezkedik el. Lapos illeszkedés esetén a lencse a pislogásokkal és szemmozgásokkal a szaruhártyán centralizált helyzetéből nagy elmozdulásokat végez és a mozgás befejeztével nehezen tér vissza centralizált helyzetébe. A lencse nagy mozgékonysága irritációt okozhat mind a szaruhártya, mind a tarsalis kötőhártya felszínén. A laposan illesztett lencse viselésekora látása pislogás után nem éles, csak kis idő múlva-a lencse centrális helyzetbe való visszajutásának megfelelően - válik élessé. A pislogáskor és szemmozgáskor a lencse könnyen ki is eshet a szemrésből. Meredek illeszkedés: Ezekben az esetekben a kontaktlencse hátsó centrális görbületi sugara kisebb, mint amilyen a párhuzamos illeszkedéshez szükséges lenne. A lencse és a szaruhártya között centrálisan vastagabb, széli részek felé vékonyodó könnyfilm helyezkedik el. Meredek illeszkedés esetén a lencse a pislogásoknál és szemmozgásoknál alig vagy egyáltalán nem mozdul ki a szaruhártyán centralizált helyzetéből. A lencse "letapadása" az illesztés után hamarosan fájdalmas érzést okoz a páciensnek, egyrészt a lencse széleinek nyomó hatása által, másrészt a szaruhártya könnybejuttatott toxikus anyagcseretermékeinek a lencse alatti felhalmozódása miatt.
5. A legjobb látásélességet és legkomfortosabb látást biztosító törőerő meghatározása felülkorrigálással
Lágy próbalencsék esetében előbb a jól illeszkedő kontaktlencse látásélesség-korrigáló hatását meg kell vizsgálni, ezután pedig a kontaktlencse elé szemüvegkeretes előtétbe helyezett alacsony törőerejű (+- 0,25) szemüveglencsékkel kell kipróbálni - felülkorrigálni -, hogy valóban a felhelyezett kontaktlencsének van-e a lehető legjobb látásélességet és legkomfortosabb látást biztosító hatása, vagy pedig a páciensnek más törőerejű lencse lenne szükséges. Ha a próbalencse törőereje is megfelelő, a páciens a próbalencsét is viselheti majd, ha nem, akkora leendő lencséjének törőereje jól kiszámítható a jól illeszkedő próbalencse törőerejéből és a szükséges felülkorrigálás értékéből, újpróbalencsét már nem szükséges felhelyezni.
Kemény próbalencsékeseteiben, amelyek törőereje azonos értékű (leggyakrabban -3,0 D), a megrendelendő, legjobb látásélességet biztosító lencse törőerejét a jól illeszkedő próbalencse szemüveglencsés felülkorrigálásával kell meghatározni.
6. A vizsgálati eredmények kiadása, újabb időpont egyeztetés
A pontosan dokumentált szemészeti-kontaktológiai vizsgálatokról rövid összesítőt is célszerű készíteni, amit páciens ellenőrző könyvecskéjébe be kell írni. Ezután a pácienssel újabb időpontot kell egyeztetni, melynek során a megrendelt lencse kiadásra kerülhet. A pácienst ez újabb találkozás során célszerű megtanítani a lencseviselésre, lencseápolásra és tájékoztatni a lencseviselés sajátosságairól is. Ezt az időpontot is célszerű beírni a páciens ellenőrző könyvecskéjébe.
A próbalencse sikeres illesztése utáni teendők A kontaktlencse megrendelése Lágylencse megrendelésének sajátosságai
Lágy kontaktlencsék illesztése esetén, ha a kontaktológiai labor rendelkezik olyan nagy raktárkészlettel, hogy a gyakrabban kiadásra kerülő lencsékből akár több darab vagy doboz is van, nem kell minden újlencseillesztés után a lencséket megrendelni, hanem elég a forgalomtól függően bizonyos időnként pótolni a raktárkészletet. Ez a típusú rendelést a kontaktológiában "leltár" típusú rendelésnek nevezik, szemben a hagyományos "próbalencse" típusú rendeléssel, amelynél a próbalencse kipróbálása után, annak adatai és az estleges szemüveges felülkorrigálás értéke alapján rögtön történik a lencsék megrendelése.
Keménylencse megrendelésének sajátosságai
Keménylencsék esetében a "próbalencse" típusú rendelést lehet csak alkalmazni, mivel a "leltár" típusú rendeléshez a kontaktlencse labornak óriási raktárkészlettel kellene rendelkeznie.
A megrendelt lencsék ellenőrzése, kiadása
A megrendelt lencse szállításának tervezett időpontjától előfordulhatnak kisebb nagyobb eltérések, ezért a páciensek tanácsolni kell, hogy a megbeszélt vizsgálati időpont előtti napon telefonon tájékozódjon a lencse megérkezéséről, mert ha a lencsét még nem szállították le, újabb időpontot kell vele egyeztetni.
A lencsék kiadását célszerű összekötni a lencse felhelyezésénekés levételének megtanításával, valamint az ápolásával kapcsolatos tevékenységek elsajátításával. A kemény és lágy kontaktlencsék átadásakor ugyanazokat a tevékenységeket kell végezni, melyek meghatározott sorrendben történnek:
- A lencsét leszállításakor, de kiadása előtt is ellenőrizni kell, hogy a lencse tároló dobozán feltüntetett adatok megfelelnek-e a megrendelt értékeknek és nincs-e a tároló doboz megsérülve.
- A lencse tároló dobozának felbontása előtt, majd a felbontás után is ellenőrizni kell, hogy nem tapasztalható-e lencsével valamilyen rendellenesség: pl. beszakadás, anyaghiány.
-A lencséket ellenőrizni kell a szemre való felhelyezés után is: réslámpával meg kell vizsgálni a lencse illeszkedését és a lencsével korrigált látásélességet.
Ha a kapott vizsgálati eredmények megfelelnek a kívánalmaknak, akkor a lencse kiadható, ha nem, a lencsét vissza kell venni és ki kell deríteni az eltérés okát. Gyártási hiba esetén vissza kell a lencsét küldeni. A lencse kiadásával egyidőben a páciens számára lencsekártyát is szükséges kiadni a lencse adatainak feltüntetésével. A lencsekártyát minden lencseviselőnek ajánlott magával hordani, hogy esetlegesen előforduló öntudatlan állapotában (baleset vagy eszméletvesztés esetén) a lencse időben el legyen távolítva a szeméről.
Megtanítás a lencse felhelyezésére, levételére és ápolására
A lencse viselése csak akkor ajánlott, ha a páciens elsajátította a lencse felhelyezésének, levételének és ápolásának ismereteit és ezt önállóan is tudja végezni.
A páciens megtanítását a lencse felhelyezésére, levételére és ápolására kellő gyakorlattal rendelkező kontaktológiai asszisztens is végezheti, de ezekben az esetekben is a felelősség a kontaktológiai rendelést vezető kontaktológusé. A kontaktlencsegyártók számos képekkel is ellátott segédanyagot bocsájtottak ki erre a célra, amelyek nagyon jó oktatási segédeszközök, de nem pótolják a személyre szabott oktatást. Az oktatást addig kell végezni (addig nem javasolt a kontaktlencsét sem kiadni), amíg a páciens (esetleg hozzátartozója) ezeket a tevékenységeket önállóan is tudja végezni.
IV. Rehabilitáció
V. Gondozás
A lencseviseléssel kapcsolatos tudnivalók megbeszélése
A lencse felhelyezésére, levételére és ápolására való betanítás után a lencseviseléssel kapcsolatos további fontos információkról a páciens tájékoztatni kell. Egyes reklámanyagok erről adhatnak nagyon jó általános tájékoztatót, de a szóbeli megbeszélés nem hagyható el, mivel a reklámanyagok tartalma sohasem teljes, és nem biztos, hogy meg tud megfelelni a páciens egyéni elvárásainak. A tájékoztatást szintén végezheti a kellő gyakorlattal rendelkező kontaktológiai asszisztens, de nem egyértelmű, problémás esetekben ki kell kérni a kontaktológus véleményét is. A szemészeti és általános gyógyszerek kontaktlencsével való alkalmazhatóságát a páciensnek kontaktológus szemész szakorvossal kell megbeszélnie. A kontaktlencse viselésével kapcsolatban a pácienssel az alábbi témaköröket kell megbeszélni:
Kezdeti nehézségek a lencseviseléskor
A kontaktlencse viselésére való átállás rövidlátóknak kezdeti kényelmetlenséget okozhat általában olvasásnál vagy közeli munkavégzésnél, míg távollátóknál hasonló tevékenységek inkább könnyebbséget jelentenek. Nagyobb törőerejű kontaktlencsés korrekció alkalmazása esetén a megszokott szemüveges korrekcióhoz képest a képméretben, látótérben és térlátásban is változások tapasztalhatók, amely a lencseviselés kezdeti időszakában hibás távbecsléshez vezethetnek (pl. autóvezetés).
A lencseviseléshez való hozzászokás
A lencseviselés megszokásának legjobb ideje a munkából való hazatérés és a lefekvés közötti idő, mivel ekkor nyugodtan, általában sürgető körülmények nélkül gyakorolhatók a lencsével kapcsolatos procedúrák végzése. Hasznos tanácsok:
A viselési idő növelésével fellépő panaszok(szemvörösödés,égő érzés, szárazságérzés) esetén addig kell csökkenteni a viselési időt, amíg a lencsét újra panaszmentesen lehet viselni. A lencséket az ébredés után legalább 1 órával kell felhelyezni, mivel a szem alvás után még érzékenyebb.
A megszokási időszak alatt előforduló tünetek
A megszokási időszakban főként keménylencsék viselése esetén kellemetlen érzések léphetnek fel, amelyek lehetnek a megszokási idő természetes velejárói, de lehetnek szembetegség bevezető tünetei is. A leggyakoribb tünetek a következőkben kerülnek felsorolásra, ha azonban a páciens nem tudja biztosan eldönteni, hogy a lencseviseléssel kapcsolatos tünet a kóros, vagy nem kóros, mindenképpen szemész szakorvosi vizsgálat szükséges.
Kemény kontaktlencse viselésekor előforduló tünetek
- Kórosnak nem tekinthető tünetek: idegentest-érzés, zavaró fényreflexek, erősebb könnyezés, nagyobb érzékenység a környezeti ingerekre (pl. fényre, füstre, huzatra), a kontaktlencse hordásának érzése, a kontaktlencse mozgása által kiváltott irritáció.
- Kóros tünetek: a látásélesség csökkenése (a lencsékösszecserélésének lehetőségét ki kell zárni) a szem pirosodása, csökkenő viselési komfort a leggyakrabban előforduló tünetek; ezenkívül még előfordulhat égető-viszkető érzés, fájdalom, fénykerülés, ködös látás, vagy színes gyűrűk látása erősebb fényforrás körül.
Lágy kontaktlencse viselésekor előforduló tünetek
- Kórosnak nem tekinthető tünetek: Hasonlóak mint keménylencse viselésének esetében, azonban nem olyan kifejezetten jelentkeznek. Gyakran előfordul magasabb víztartalmú kontaktlencse viselésekor, hogy a lencseviselés kezdeti időszakában a nagy koncentrációt is igénylő nézéskor (pl. olvasás, képernyő előtt végzett munka, televízió nézés, autóvezetés) a lencse részlegesen kiszárad normál könnytermelés esetén is, ami kellemetlen idegentest érzéssel jár és a lencse a szemből könnyen ki is tud esni. Ez az átmeneti állapot az időnkénti tudatos pislogással könnyen megelőzhető.
- Kóros tünetek: A panaszok hasonlóak mint kemény kontaktlencse viselésekor, de enyhébben kezdődnek. Míg keménylencse viselése esetén a kóros tünetek jelentkezésével a páciens már nem tudja a lencséjét tovább viselni, lágylencse viselése esetén a lencse viselhetetlensége már csak akkor következik be, amikor a betegség már súlyosabb, szövődmények kialakulásával járó szakba került. Kóros, vagy nem eldönthető tünetek jelentkezése esetén a lencsét azonnal le kell venni a szemről és azonnal szemorvoshoz kell fordulni.
Kozmetikumok alkalmazása
Sminkelés előtt ajánlatos a lencséket felhelyezni, a sminket viszont csak a lencse eltávolítása után célszerű lemosni. Ezzel a módszerrel elkerülhető a lencse zsírral, vagy vegyszerrel való szennyeződése. A kozmetikumokat csak a szemhéj és a szempilla tövétől kintebb lévő helyekre célszerű felvinni, mert így a kozmetikumnak a lencséhez való tapadását elkerülhető. A hajlakkozását is csak zárt szemhéjak mellett szabad végezni.
Viselés időtartama
A lencsék lehetséges viselési időtartama napi viselés esetén általában a napi 12-14 óra, még teljes panaszmentesség esetén is kerülni kell a napi 16 órát meghaladó hordási időket. A napi viselésű lágylencséket lefekvés előtt, a kemény lencséket még a délutáni rövid alvás időtartamára is le kell venni a szemről a szaruhártya szövődményekelkerülésére.
Napi viselés esetén a szokásos hordási időt le kell rövidíteni:
- ha a páciens a lencséjét hosszabb ideig nem viselte,
- ha a páciens hosszabb időn át száraz, meleg, vagy poros helyen tartózkodik. A viselést abba kell hagyni:
- ha a páciensen fertőző betegség általános tünetei jelentkeznek. Csere szükségessége
A lencsék cseréjével kapcsolatban a forgalmazási előírások az irányadók, de bizonyos esetekben hamarabb is szükségessé válhat a lencsék cseréje:
Keménylencsék
- a lencse sérülése, vagy a lencse javíthatatlanná válik (egyes típusú lencsék korlátozott mértékben utánmunkálhatók),
- változik a páciens szemének törőereje
Lágylencsék
- a lencse sérülése,
- változik a páciens szemének törőereje.
Fel kell hívni a páciens figyelmét a lencseviselési szabályok betartásának jelentőségére a szövődmények elkerülése céljából
Elméletileg a lencseviseléssel kapcsolatos szövődmény nem fordulhat elő, ha a páciensek a lencseviselés szabályait pontosan betartják: a lencsékre vonatkozó viselési és cserélési időt pontosan betartják, megfelelő ápolószerekkel az előírásnak megfelelően ápolják, bármilyen lencseviseléssel összefüggő panasz esetén (ha ez nem a kezdeti viselési időszak múló panaszaira vonatkozik) a lencseviselést abbahagyják és kontaktológusukhoz fordulnak, ügyeleti időben pedig szemészeti szakrendelésre. Ennek ellenére, szerencsére egyre ritkábban, ma is fordulnak elő szemészeti szövődmények, amelyek kialakulásának hátterében mindig megtalálható a lencse viseléssel kapcsolatos szabályok be nem tartása. A szövődmények kialakulásának veszélye még tovább csökkenthető, ha a páciensek saját magukat is naponta ellenőrzik. A napi ellenőrzés 1-2 percet vesz igénybe, menete a következő:
1. Távoli tárgyra nézés külön-külön mindkét szemmel a látásélesség megállapítására: a látásélesség csökkenése betegségre utalhat.
2. A lencseviselés komfortérzésének vizsgálata mindkét szemre külön-külön koncentrálva: a komfortérzés csökkenése betegségre utalhat.
3. Tükör előtt a szemek vörösségének, váladékosságának kizárása: a szem vörössége és/vagy váladékozása betegségre utal.
Mindenek előtt figyelembe kell azt is venni, hogy lencseviseléskor is felléphetnek ugyanazok a gyulladásos betegségek a szem elülső felületén - pl. conjunctivitis -, amelyek a lencseviseléstől függetlenül is megjelenhetnek. Tudni kell azonban azt, hogy ezeknek a betegségek lefolyását a lencseviselés súlyosbíthatja, ezért a betegségre való gyanú esetén is a lencseviselést rögtön abba kell hagyni és szemorvoshoz kell a páciensnek fordulni. Minden lencseviselőnek ajánlatos, hogy legyen tartalékszemüvege, mert a lencseviselési problémák fellépése esetén a szemüveget nyugodtan viselheti.
Nyilatkozat aláíratása a pácienssel
A tájékoztató után az esetleges felmerülő kérdéseket meg kell a pácienssel beszélni, amelyben a páciens egyéni sajátosságaira (pl. sajátos munkakörülmény, sport, otthoni környezet) részletesebben ki kell térni. Ezek után a pácienssel alá kell íratni egy olyan nyilatkozatot is, amelyben a páciens elismeri, hogy a lencse felhelyezésére, levételére és ápolására vonatkozó betanítása megtörtént, részletes tájékoztatást kapott a kontaktlencse viseléséről és az ellenőrzővizsgálatokon való megjelenés fontosságáról, valamint arról, hogy panasz esetén rögtön abbahagyja a lencseviselést és ellenőrzővizsgálatra vagy ügyeleti időben szemész szakorvosi ügyeletre megy.
Az ellenőrzések időpontjai és menetük
A lencseviselés kapcsolatos tudnivalók ismertetése után a pácienssel meg kell beszélni az első ellenőrzés időpontját is, amelyet a pácienst ellenőrzési könyvecskéjébe is be kell jegyezni. Az ellenőrző vizsgálat rövid összefoglalóját és a következő ellenőrzés idejét is tanácsos bejegyezni a páciens ellenőrző könyvecskéjébe, amit a kontaktológusnak saját felhasználására is dokumentálni kell. Tanácsos a páciensnekszemüveget is hoznia magával az ellenőrző vizsgálatokra, ugyanis előfordulhat, hogy az ellenőrző vizsgálat során a kontaktológus javasolja a kontaktlencse viselés mellőzését. Az ellenőrzővizsgálatok után a pácienst utasításokkal, tanácsokkal kell ellátni, ha hiányosságok merülnének fel a lencseviselés szabályainak betartásával kapcsolatban. A lencse gondozásának szükségességét és a megfelelő higiénés körülmények biztosítását ismételten hangoztatni kell és a további ellenőrző vizsgálatok fontosságára sem árt ismételten felhívni a figyelmet.
Ellenőrzések időpontjai
A lencse átadását követő hetekben és hónapokban következik a szem valódi alkalmassági próbája. Ebben az időszakban mutatkozik meg igazán, hogy a lencseválasztás helyes volt-e, és hogy a páciens tudja-e lencséjét folyamatosan viselni. Az illesztett lencse alapanyagától, típusától és a páciens szemének individuális állapotától függően azonban bizonyos időközökben további ellenőrzések is szükségesek - panasz esetén azonnal -, hogy adott esetekben a lencse nem optimális illeszkedése, vagy kóros elváltozások kialakulása idejében felismerhető és kezelhető legyen. Előszokott azonban az is fordulni, hogy egyes hanyag páciensek nem az ajánlott ellenőrzéskor, hanem csak a már súlyos szövődmények kialakulása után jelentkeznek. Igaz, hogy a rendszeres ellenőrzésekről való hiányzás felelőssége a páciensre hárul, de ez csak abban az esetben bizonyítható, ha ezeknek az ellenőrzéseknek időpontjai jól dokumentálva vannak. A kontaktológusnak azonban meg kell próbálni arra is ügyelni, hogy hanyagabb páciensei is rendszeresen ellenőrizve legyenek. A páciensnek az ellenőrző vizsgálaton való megjelenésének fontosságára való figyelmeztetés korábbi módszerei azonban ma már nem igen hatékonyak:
- a kontaktlencse ápolószereinek vásárlásakor: számos esetben a páciens nem a lencserendelés helyén szerzi be az ápolószereit,
- levél elküldésével, amely a kontrolvizsgálatról való elmaradásról figyelmezteti: gyakran a páciens a számára kedvezőbb feltételekkel rendelkező kontaktlencse rendelésen szerzi be az újabb lencséit és sajnos nem egy esetben a lencseváltásra csak az anyagi szempontok motiválják.
A keménylencse és lágylencse viselése ellenőrzésének javasolt időpontjai és szempontjai kissé különböznek egymástól:
Kemény kontaktlencsét viselők ellenőrzése
Kötelező szabályok nem állíthatók fel az ellenőrzésekre, a páciensek egyéni hozzáállása és érzékenysége is szerepet játszik. Irányelvként a napi viselési idő fokozatos növelésére a következő sémát érdemes követni:
1. ellenőrzés: napi 4-5 óra viselési idő után, amelyet az első napi 1 óra viselési időből kiindulva, majd a napi viselési idő fokozatos növelésével, leghamarabb egy hét után célszerű elérni
2. ellenőrzés: napi 8-10 óra viselés után, amelyet 1 hónap alatt célszerű elérni
3. ellenőrzés: "egész napos" viselési idő elérése után (leggyakrabban 12-14 óra folyamatos viselés), amelyet 3 hónap alatt célszerű elérni
4. ellenőrzés: a lencse átadása után 1/2 évvel
5. további ellenőrzések: panaszmentesség esetén is 1/2-1 évente Panasz esetén azonnali ellenőrzés szükséges.
Lágy kontaktlencsét viselők ellenőrzése
A lágy kontaktlencsék viselése a keménylencsék viselésénél sokkal hamarabb megszokható, az "egész napos" viselés idő (leggyakrabban 12-14 óra), a viselési idő fokozatos növelésével igen hamar, akár egy hét alatt is elérhető. Általában már az első kontrolvizsgálatra az egész napos viselési idő elérésével jön a páciens vissza. Az ellenőrzések javasolt időpontja:
1. ellenőrzés: a lencse kiadása után egy héttel, már a napi 12-14 óra viselési idővel. Az első nap 2 óra viselési időből kiindulva a viselési időt fokozatosan, napi 2 órával javasolt továbbnövelni.
2. ellenőrzés: 1 hónappal az 1. kontrol után
3. ellenőrzés: 3 hónappal a 2. kontrol után
4. ellenőrzés: lencse átadása után 1/2 évvel
5. további ellenőrzések: panaszmentesség esetén is 1/2-1 évente Panasz esetén azonnali ellenőrzés szükséges.
Az ellenőrzések menete
Fontos előre kialakítani az ellenőrzések időrendjét is: pl. a pácienseket lehetőség szerint délután kell vizsgálni, amikor márórákóta viselika kontaktlencséjét, de a legalább 2 órával az ellenőrzővizsgálat előtt fel kell helyezni a lencsét, hogy az illeszkedés még jobban megítélhető legyen.
A páciens kikérdezése
A beszélgetés során feltétlenül rá kell kérdezni a lencseviseléssel kapcsolatos egyes fontos adatokra: napi viselés időtartamára; a lencse viselhetőségére; látásélesség milyenségére szemüveggel és kontaktlencsével, valamint nappal és este; az esetleges szubjektív panaszok megjelenésére a lencse viselése során (idegentest érzés, viszketési inger, égés, fénykerülés, szárazság érzés, stb.); a lencse spontán elcsúszási vagy kiesési hajlamára; a szem vörösödésére a hordási idő vége felé; a lencse viselésével való elégedettségre stb.
Vizsgálatok felhelyezett kontaktlencsével
- Látásélesség ellenőrzése kontaktlencsével és az esetleges szükséges kiegészítő törőerő megállapítása szemüveglencsével, felülkorrigálásos módszerrel.
- A lencseilleszkedés vizsgálata. Kemény lencseviselők esetében a könnyfilm fluoreszceines festése is szükséges a réslámpás vizsgálattal, lágy lencseviselők esetében egyszerű réslámpás vizsgálat elegendő.
Vizsgálatok a kontaktlencse levétele után
- A látásélesség ellenőrzése szemüveglencsével, ha a kontaktlencsés látásélesség vizsgálat jelentősen eltér a várttól.
- Réslámpás vizsgálattal ki kell zárni a kóros folyamatok lehetőségét a szemfelszínen és a szem elülső szegmentjében.
- A könnyfilm fluoreszcein festésével a könny minőségi változásának kimutatásán kívül, a szaruhártya és kötőhártya felszín finomabb patológiás eltérései is jól diagnosztizálhatók. A tarsalis kötőhártya vizsgálatát panaszmentesség esetén elég csak a kezdeti egy hónapos kontrolvizsgálatnál, későbbiekben pedig évenként megvizsgálni. A vizsgálat végén a fluorescein festékkel megfestett könnynek a szemrésből való elfolyását műkönny becseppentésével lehet siettetni, ami főként a magasabb víztartalmú lágylencse viselők esetében fontos, mivel a lencse a szemre visszahelyezve megfestődhet.
- A szaruhártya elülső felszíne centrális görbületi sugarának keratométeres ellenőrzése és a mérési eredmény összehasonlítása a korábbi mérési eredményekkel. A vizsgálat közben figyelni kell azt is, hogy a mérőjelek torzulásmentesen tükröződnek-e, mivel a mérőjelek tükörképének torzulása visszajelzése lehet a lencse nem megfelelő illeszkedésének.
- A könnytermeléscsökkenésére való gyanú esetén a könnytermelést is meg kell vizsgálni, nem egyértelmű vizsgálati eredmény esetén a pácienst vissza kell rendelni a lencseviselés nélküli állapotban és a könnytermelés mennyiségi és minőségi vizsgálatát újból el kell végezni.
A lencse tároló dobozának ellenőrzése
Különösen régebben volt nagyon szükséges, amikor a havonta vásárolt fertőtlenítő-tároló folyadékkal nem forgalmaztak tároló dobozt is, a tároló dobozt külön kellett megvásárolni, és a lencseviselők akár egy évig, vagy még tovább is használták. Számos esetben a tároló doboz rendszeres - legalább havonta egy alkalommal - tisztításáról gyakran megfeledkeztek és nemegyszer a tároló dobozok nem megfelelő higiéniája nagyban hozzájárult súlyos szemészeti szövődmények kialakulásához. Ma már az egy-másfél hónapig használatos fertőtlenítő-tároló folyadékokkal együtt szinte majdnem minden gyártó cég tároló dobozt is forgalmaz, ezért az utóbbi időben a tároló dobozok higiéniájával nem szokott probléma lenni.
Szemfenék vizsgálat
Az ellenőrzésekalkalmával, panaszmentesség esetén nem kell mindig elvégezni a szemtükörrel történő vizsgálatot is, de legalább egyszer egy évben ajánlott.
A kontaktológia tevékenység és feladatköreinek megoszthatósága
A kontaktológiai tevékenység lényege, hogy a páciens jó minőségű, igényeinek megfelelő kontaktlencsével és ápolószerrel folyamatosan el legyen látva. A páciens megfelelő anyagi hátterének hiánya nem mehet a minőség rovására, ebben az esetben jobb, ha egyáltalán nem visel lencsét. A lencsét viselni szándékozó páciensnek csak akkor ajánlható az önálló lencseviselés, ha a betanítás után önállóan, magabiztosan tudja a lencsét felhelyezni, levenni és ápolni, valamint tájékoztatatása is megtörtént a lencseviselés sajátosságairól és tudja, hogy panasz esetén mit tegyen és hova forduljon. Mindenképpen szükséges a lencseviselésre való megtanítás és a lencseviselésre való oktatás elismerését a pácienssel aláíratni, ami által a kontaktológus védheti magát a páciens hanyagságából bekövetkezett szövődmény jogi felelősségétől. A kontaktlencse rendelés zavartalan lebonyolításáért a kontaktológus a felelős, az esetleges hibákért is jogilag elsősorban a kontaktológus vonható felelősségre. Ez utóbbiak ismeretében jól képzett és már kellő gyakorlattal, tapasztalatokkal is rendelkező asszisztenssel - a rendelést irányító kontaktológus felelősségére -a kontaktológiai feladatok egy része megosztható:
A kontaktológus kizárólagos feladatkörei
- a páciens anamnézisének felvétele
- a kontaktológiai-szemészeti vizsgálatok végzése
- a próbalencse adatainak meghatározása
- a próbalencse illeszkedésének ellenőrzővizsgálata
- a vizsgálatok alapján a lencse paramétereinek meghatározása
- a lencsét viselő páciens ellenőrzése
- komplikáció esetén a páciens ellátása, vagy ha ez nem tartozik hatáskörébe (pl. optometristák esetében), a megfelelő helyre való irányítása
A kontaktológus asszisztens feladatkörei
- a páciens tájékoztatása a lencseviselés lehetőségeiről
- a vizsgálati időpontok bejegyzése, ellenőrző vizsgálatok egyeztetése
- a próbalencse illesztése (csak több éves szakmai gyakorlattal rendelkező kontaktológiai asszisztens végezheti)
- a lencse megrendelése a gyártó cégtől és a megrendelt lencse ellenőrzése
- a páciens betanítása a kontaktlencse felhelyezésére, levételére és gondozására (csak több éves szakmai gyakorlattal rendelkező kontaktológiai asszisztens végezheti)
- a páciens tájékoztatása a kontaktlencse viseléséről
- a kontaktlencse ápolószereinek és egyéb tartozékainak beszerzése, forgalmazása
- a próbasorozatok rendszeres ápolása, hiányainak pótlása
A kontaktlencse ápolása
A kontaktlencse ápolásának szükségessége
A kontaktlencse ápolása a kontaktlencse felületére tapadt szennyeződésektől való megtisztítását, a lencse fertőtlenítését és tárolását, valamint esetenként a viselés során a lencseviselési komfort és optikai minőség növelésére alkalmazott nedvesítő cseppek alkalmazását foglalja magába. Jelenleg a legelterjedtebb és a legbiztonságosabb viselési mód a napi viselés, amelynek alkalmazásakor a lencsék napi ápolást igényelnek, azonban kivételt képeznek ez alól a napi viselésű eldobható kontaktlencsék, mert ezeket a lencséket a viselés után közvetlenül ápolás nélkül kell kidobni.
Az ápolási procedúrákhoz hasonló mechanizmusoka szemfelszínen többnyire természetes úton is megtalálhatók (pl. a lencse felületének mechanikus tisztítása a pislogás segítségével, egyes könnyfehérjék antibakteriális hatása a lencsére, a lencse nedvesítése a könnyfilm vizes fázisával) és ezért engedhető meg bizonyos esetekben a kiterjesztett viselési idejű lencsék viselése napi ápolása nélkül. Ezekben az esetekben azonban sokkal szigorúban kell megvizsgálni a lencseviselésre való alkalmasság egyes tényezőit: pl. nemcsaképpen megfelelő, hanem jó könnytermelés szükséges; lényeges a páciens környezetének ismerete is higiéniás szempontból; igen fontos az együttműködő készsége is az ellenőrzéseken való megjelenéshez és esetleges viselési problémák megoldásához.
A kontaktlencse ápolása két fő részből áll - tisztításból és fertőtlenítés-tárolásból -, amelyek alkalmazása ma ma már egyidőben is történhet: pl. multifunkcionális oldatokkal történő ápolás. A lencséket nedvesen kell tárolni. A tároló dobozt óvatosan kell zárni, nehogy a lencse becsípődjön lágylencsék esetében. Folyamatos viselés mellett a tároló dobozt havonta, de legalább másfél havonta újra kell kicserélni. Ma már felesleges bajlódni a tároló doboz tisztítgatásával, mivel az egy-másfél hónapra elegendő multifunkcionális és más típusú fertőtlenítő-tároló folyadékok tartozéka a lencsetároló doboz.
A kontaktlencse ápolásának menete
Az ápolás menete lágy- és keménylencsék esetében azonos, az ápolófolyadékok összetétele azonban a legtöbb esetben eltér egymástól. A lencseápoló folyadék használata előtt meg kell arról győződni, hogy az valóban alkalmas-e a viselt lencsefajta és típus ápolására. A lágylencsék sokkal gondosabb ápolást igényelnek, a lencse viselhetetlenségéhez is vezető felrakódások is könnyebben létrejöhetnek rajtuk, emellett fertőzés forrásaként is gyakrabban szerepelhetnek a keménylencsékkel szemben, ápolási hiányosságok miatt.
A lencsék hagyományos forma szerinti ápolásának részei: mechanikus tisztítás, leöblítés, fertőtlenítés-tárolás, felhelyezés előtti leöblítés és kiegészítő ápolások. Az utóbbi időben a napi ápolási procedúrát igen leegyszerűsítette a multifunkcionális ápolóoldatok alkalmazása. Ezzel az ápolóoldattal a leggyakrabban hordott napi viselésű, gyakori cserélésű és napi viselésű, eldobható lágylencsék ápolása az esetek többségében további kiegészítő kezelés nélkül könnyen megoldhatók: a lencse levételkor belekerül a multifunkcionális oldattal frissen feltöltött tároló dobozba, majd reggel a kontaktlencse ebből az oldatból kerül felhelyezésre, ezután pedig a folyadéka tároló dobozból kiöntésre kerül.
A kontaktológusnak azonban mindenképpen ismerni kell a lencse hagyományos ápolásánakegyes részleteit is, mert ha szükséges a multifunkcionális ápolószerek alkalmazása mellett, főként a tisztítóhatás növelése céljából (pl. felületi mechanikus tisztítás, fehérjeoldás), vagy ápolószerre való érzékenység esetén (pl. a lencse felületének leöblítése a felhelyezés előtt), az egyes ápolási részeket különállóan is alkalmaztassa páciensével.
A kontaktlencse ápolásának hagyományos menete
Alkalmazása főként keménylencsék esetében és az egyre ritkább hagyományos viselési mód szerint hordott (viselési idő: 6 hó -1 év) lágy kontaktlencsék esetében még ma is szükséges.
Mechanikus tisztítás
Célja: A viselés során a kontaktlencse felületére tapadt szennyeződés, lerakódás eltávolítása. A szennyeződés a környezetből kerül a lencsére, a lerakódás pedig - főként lágylencsék viselésekor - a könnyfilmből. Kozmetikumok is rátapadhatnak a lencsére, ezért lencseviseléskor a szemkörül vízoldékony kozmetikumokat célszerű használni, mert ezek könnyen eltávolíthatók a lencséről.
Szükséges ápolófolyadék: Külön, erre a célra előállított felületaktív hatású tisztító folyadék (külön lágy- és külön keménylencsére) , amelynek a szembe kerülése veszélyes, ezért ezzel a folyadékokkal történt tisztítás után a kontaktlencsét nem szabad visszahelyezni a szemre, hanem tovább kell folyatatni a lencsék ápolásának menetét. Az alkalmazás menete: Alapos kézmosás után a kontaktlencsét a szemről le kell venni, majd a tenyérbe kell helyezni úgy, hogy a lencse konkáv felszíne legyen felfelé. Ezután néhány csepp tisztítófolyadékot kell a lencse belső felszínére csepegtetni, majd a másik kéz mutatóujjával legalább 10 másodpercig óvatosan kell dörzsölni a felszínt. Ugyanezt a műveletet el kell végezni a lencse kifordítása után is.
Leöblítés
A mechanikusan megtisztított lencse mindkét oldalát bőségesen, öblítő folyadékkal kell lemosni.
Célja: A mechanikus tisztítás által a kontaktlencse felületéről leválasztott szennyeződés, lerakódás és a szemre káros felületaktív tisztítóanyag maradékának lemosása.
Szükséges ápolófolyadék: Leggyakrabban az ápolás következő lépésében alkalmazásra kerülő fertőtlenítő-tároló folyadékalkalmazzákerre a célra. Azokat a fertőtlenítő-tároló folyadékokat, amelyeka szemfelszínre jutva maró-irritáló hatásúak (pl. hidrogénperoxid tartalmú ápolófolyadékok), ilyen célra nem kerülhetnek felhasználásra. Ez a szemre veszélyes hatás az ápolófolyadék használati utasításban jól fel van tüntetve, ezért ilyen fertőtlenítő-tároló folyadékok alkalmazása esetén leöblítésre a többféle kiszerelésben, kontaktológiai célra forgalomba hozott 0,9 %-os NaCl oldatot kell használni.
Az alkalmazás menete: A tenyérbe helyezett kontaktlencse mindkét felületének leöblítése. Fertőtlenítés és tárolás
A mechanikus tisztítás és öblítés után a lencsét fertőtlenítő-tároló folyadékkal feltöltött tároló dobozba kell helyezni. A tárolás és fertőtlenítés a mindennapi gyakorlatban együtt kerül alkalmazásra. A tároló dobozban a lencse a viselés mentes időszakban tárolódik, másrészt a tárolás során a hosszabb időt igénybevevő fertőtlenítő folyamat is végbemegy.
Célja: A kontaktlencse napi viselése során a kontaktlencse felületén megtapadt, vagy anyagába belekerült (lágy lencsék) mikroorganizmusok elpusztítása és a lencse tárolása. Jelenleg a kontaktlencsék fertőtlenítése a tároló oldatban oldott hatóanyagokkal, "kémiai módszerrel" történik. Ez a kémiai fertőtlenítés egyes fizikai fertőtlenítő módszerekkel helyettesíthető lenne - amire folyamatosan vannak próbálkozások -, azonban az eddig kipróbált módszerek alkalmazása igen nehézkes, ami miatt széles körben nem kerültek alkalmazásra: hődezinfekció (főzés), ultraibolya fény (260 nm), ultrahang (16-20 Hz), mikrohullám (600-700 W).
Szükséges ápoló folyadék: Fertőtlenítő-tároló folyadék külön lágy- és külön keménylencséhez (kivétel pl. hidrogénperoxid hatóanyagú ápolófolyadék)
Szükséges tároló doboz: A fertőtlenítő-tároló folyadékokat a lencse fertőtlenítésére-tárolására alkalmas tároló dobozokkal együtt forgalmazzák. Egyes tároló dobozok - meghatározott fertőtlenítő-tároló folyadékok alkalmazásával-a lencse tárolásán kívül más, önálló funkcióval is rendelkezneka lencse fertőtlenítési folyamatában: pl. a szemre maró hatású ápolóoldat közömbösítése, antibakteriális hatás. E tároló dobozok speciális hatásukat kizárólagosan, vagy a legjobban a velük együtt forgalmazott fertőtlenítő-tároló oldattal együtt alkalmazva tudják kifejteni. A fertőtlenítő-ápolófolyadékokat is a velük együtt forgalmazott tároló dobozzal együtt célszerű használni, vagy nagyon körültekintően lehet más gyártású tároló dobozra áttérni, mert a speciális hatás hiánya bizonyos esetekben szemészeti komplikációt okozhat: pl. hidrogénperoxid tartalmú fertőtlenítő-tároló oldat használatakor, a maró hatású folyadék semlegesítését végző katalizátor hiánya a tároló dobozban.
Az alkalmazás menete: A lencsék tároló dobozát az ápolófolyadék útmutatása alapján kell megtölteni a fertőtlenítő-tároló folyadékkal, ezután pedig a lencsét kell belehelyezni. A fertőtlenítő hatás kifejlődéséhez általában legalább 6 óra szükséges. Figyelmesen el kell olvasni az ápolófolyadék használati útmutatóját, mert egyes fertőtlenítő-tároló oldatok használata kissé eltérhet a megszokottól: pl. a hidrogénperoxid tartalmú fertőtlenítő oldatokat a fertőtlenítés végén - vagy a fertőtlenítés közben folyamatosan, a tároló dobozban lévő katalizátor segítségével - közömbösíteni kell, mivel hatóanyaga közömbösítés nélkül a szemre maró hatású. A fertőtlenítő-tároló folyadékot a lencsék szemre való felhelyezése után ki kell önteni a tároló dobozból és a tároló dobozt szárazon kell hagyni a következő használatáig.
Öblítés
Általában ez a lépés kihagyható, mivel a fertőtlenítő-tárolóoldatból (hidrogénperoxid hatóanyag alkalmazáskor az elbomlott, vagy közömbösített hatóanyagot tartalmazó ápolóoldatból) a lencse a szemre közvetlenül is visszahelyezhető. Érzékeny szeműeknél azonban tanácsos alkalmazni az öblítést.
Célja: A fertőtlenítő-tároló folyadékból kivett lencse felszínének lemosása a fertőtlenítő-tároló oldat maradványaitól, a lencse szemre való felhelyezése előtt.
Szükséges ápolófolyadék: Kontaktológiai célra különféle kiszerelésben forgalomba hozott 0,9%-os NaCl oldat.
Az alkalmazás menete: A tenyérbe helyezett kontaktlencse mindkét felületének leöblítése, vagy a kontaktlencsét tartalmazó tároló doboz feltöltése öblítő folyadékkal és a lencse belehelyezése 1-2 percig.
Kiegészítő ápolások
A kiegészítő ápolások alkalmazásának szükségességét, annak gyakoriságát több tényező befolyásolja: a lencse alapanyaga, a lencse hordási ideje, a páciens könnytermelésének mennyisége és könnyének összetétele, a páciens környezete. A kiegészítő kezelés szükségességét és annak gyakoriságát a kontaktológusnak kell eldönteni. Végzése a kiegészítő ápolószer mellékelt útmutatója alapján történik. Enzimes tisztítás
Az enzimes tisztítás elnevezést a kontaktológiában régebben a kontaktlencse felületén megtapadt fehérjeeltávolításra alkalmazták. Az enzimes fehérjeeltávolítás lényege az, hogy az enzim kontaktlencse felületén megtapadt, oldhatatlan (denaturált) fehérjét vízben oldható kisebb részekre - peptidekre - bontja szét.
A kontaktológiába újabban bevezetett enzinkombinációkkal már nemcsak a fehérje, hanem más szerves anyag - zsír, poliszacharid - eltávolítása is elvégezhető a kontaktlencse felületéről. A hatásmechanizmus ugyanaz ezekben az esetekben is: vízben oldható kisebb részekre való szétbontás.
Nedvesítés
A szemre felhelyezett kontaktlencse nedvesítésével a lencseviselési komfort és optikai minőség növelhető, ha a páciensnek a könnytermelése csökkentebb, vagy könny minősége nem megfelelő. Használatának szükségessége ezenkívül összefügghet még a lencseviselő környezetével, időjárási tényezőkkel (meleg, szeles idő), valamint a lencseviselő pislogásának gyakoriságával is.
A kontaktlencse ápolása multifunkcionális ápolófolyadékokkal
A multifunkcionális ápolófolyadékokat a jelenleg a legszélesebb körben viselt napi viselésű, maximum havi cserélésű lágylencsék ápolására vezették be, az egyre ritkább fél- egy éves hordásidejű lágylencsék ápolására azonban önmagában nem elegendő. Ez az ápolási forma az esetek többségében azért oldható meg a gyakori cserélésű és eldobható lágylencséknél, mivel az újabban bevezetett kontaktlencse alapanyagokra már nehezebben tapadnak rá a szennyeződésekés ezeket a sokkal igényesebb ápolást igénylő lágylencséket a viselők sokkal gyakrabban cserélik. Az utóbbi időben forgalmazásra kerültek a keménylencsék ápolására javasolt multifunkcionális ápolófolyadékok is. A hosszabb cserélési idejű keménylencsék ápolására a multifunkcionális ápolófolyadék a lencsetípustól függően azért lehet alkalmas, mivel a lencse felületére való lerakódási hajlam a lágylencsékhez képest jóval csekélyebb. A multifunkcionális oldatba helyezet lencse az ápolás legszükségesebb részein átesik: felületi tisztítás, fertőtlenítés. A multifunkcionális ápolóoldatok összetevőinek hatása hasonlóak a hagyományos ápolószerekben lévő hatóanyagokéhoz; fertőtlenítő hatásuk ugyanolyan, de a felületi tisztító és fehérjeoldó hatásukgyengébb, mert ezeket a hatóanyagokat csak olyan koncentrációban tartalmazzák, ami a szemre nem káros. Egyes esetekben, egyéni adottságtól függően - pl. könnyfilm fehérjedúsabb összetétele -, vagy egyes munkakörülményeknél - pl. poros környezet - a multifunkcionális ápolóoldat használatán kívül szükségessé válhatnak kiegészítő ápolások is a hagyományos ápolószerekkel (pl. felületi mechanikus tisztítás, fehérjeoldás), amelyről a kontaktológusnak kell dönteni.
Alkalmazásának célja: a lencse felületének tisztítása, fertőtlenítése és a lencse tárolása
Szükséges ápolófolyadék: multifunkcionális ápolófolyadék külön lágy- és külön keménylencséhez
Szükséges tároló doboz: a multifunkcionális ápolófolyadékot a lencse tárolására is alkalmas tároló dobozzal együtt forgalmazzák
Alkalmazásának menete: A lencse a szemről való levétele után közvetlenül belekerül a multifunkcionális oldattal frissen feltöltött tároló dobozba, majd reggel a kontaktlencse ebből az oldatból kerül a szemre vissza. Az ápolófolyadékban az éjszakai tárolás során az ápolás főbb szakaszai végbemennek: felületi tisztítás (a folyadék összetételétől függően enzimes tisztítás is lehetséges), fertőtlenítés.
A lencsék tárolása viselés nélkül, hosszabb ideig
A kontaktlencséket mindig nedvesen kell tárolni. Ha a lencse folyamatosan nincs használva, nem elbomló fertőtlenítőszert tartalmazó ápolófolyadékot célszerű alkalmaznia tárolásra és legalább 5-6 hetente célszerű kicserélni a tároló folyadékot a fertőtlenítő hatás fenntartása céljából. Hidrogénperoxidos fertőtlenítés esetén, amikor a lencsét tartalmazó ápoló folyadékban a hidrogénperoxid hatóanyag elbomlott vagy közömbösítődött, a lencsét 4-5 nap múlva újra kell fertőtleníteni, vagy áthelyezni nem elbomló fertőtlenítőszert tartalmazó tároló folyadékba.
A próbasorozat lencséinek ápolása
Napjainkban több fertőző betegségről tételezik fel, hogy esetleg a könny útján is átvihető, ezért igen fontos a próbalencsék fertőtlenítése (ápolása), valamint a rendelőben a higiéniás körülmények betartása.
Általános irányelvek a próbalencsék ápolására
A sokkal igényesebb lágy próbalencsék ápolási feladata az utóbbi időben jelentősen lecsökkent. Ez főként annak köszönhető, hogy a lágylencsékre kifejlesztett sorozatgyártás a lágylencse típusok többségének eladási árát jelentősen lecsökkentette és így a legtöbb kontaktlencsét forgalmazó cég ingyenes próbalencséket is tud biztosítania kontaktológus számára. Ha az ingyenes próbalencse a páciens számára nem megfelelő (rosszul illeszkedik, nem megfelelő a törőereje vagy a páciens mégsem akar lencsét viselni) a lencse kidobásra kerül. A legtöbb esetben azonban a páciensre felhelyezett próbalencse egyben a végleges lencse funkcióját is betöltheti, a kis eltéréssel nem megfelelő törőerejű próbalencse pedig a lencse felhelyezésének és levételének megtanításához alkalmazható.
1. A próbasorozat gyári csomagolásából felbontott és használt lágy- és keménylencséket hidrogénperoxidos kontaktlencse ápolófolyadékkal fertőtleníteni kell és ha 4-5 napon belül nem kerül újra felhasználásra a lencse, a szemre nem káros fertőtlenítő-tárolóoldatban kell tovább tárolni. A lencse tároló dobozán pontosan meg kell jelölni az utolsó fertőtlenítés időpontját is a lencse paramétereivel együtt.
2. A próbasorozat korábban már használt lágylencséit legalább 3 havonta egyszer újból hidrogénperoxidos kontaktlencse ápolófolyadékkal fertőtleníteni kell és ha 4-5 napon belül nem kerül újra felhasználásra a lencse, a szemre nem káros fertőtlenítő-tároló oldatban kell tovább tárolni. A nem használt kemény próbalencséknél a lágylencsékhez hasonló ápolást elegendő félévente újból elvégezni.
3. A kontaktlencséket még próbalencse céljára sem szabad felhasználni a gyártó által megjelölt viselhetőségi határidő lejárta után. Többször használt, majd hosszú ideig nem használt lágylencsék paramétereit ajánlatos ellenőrizni, mivel könnyen deformálódhatnak.
4. Nem lehet megfeledkezni a próbalencsék tároló dobozainak tisztításáról sem. A tároló dobozok vagy üvegből, vagy műanyagból készülnek. Az tároló dobozok könnyen tisztíthatók felületaktív mosogatószerekkel, ami után alaposan át is kell öblíteni azokat. A műanyag tároló dobozokat ajánlatos kifőzni is, míg az üvegből készülteket sterilizálni is. A műanyag tároló dobozokat azonban érdemes a próbalencsék fertőtlenítése alkalmával újra kicserélni.
VI. Irodalomjegyzék
1. Francceschetti Albert: Declaration of the European Contact Lens Society of Ophthalmologists. ECLSO, London, 2005
2. Key James E II: The CLAO pocket guide to contact lens fitting. Contact Lens Association of Ophthalmologists (second edition), New Orleans, 1998
3. Medical Device Directive 93/42/EEC, Annex IX
4. Roth Hans-Walter: Contact lens complication. Etiology, pathogenesis, prevention, therapy. Thieme, Stuttgart, 2003
5. Ruben Montague, Guillon Michel: Contact lens practice. Chapman & Hall Medical, London, 1994
6. Stein Harold A, Freeman Melvin I, Stein Raymond M, Maund Lynn D: CLAO residents contact lens curriculum manual. Kellner/Mc Caffery (second edition), New York, 1999
7. Süveges Ildikó: Szemészet. Medicina, Budapest, 2004
A szakmai protokoll érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai irányelve
A méhnyakrák szűrésének szempontjairól
Készítette: a Szülészeti és Nőgyógyászati Szakmai Kollégium
BEVEZETÉS
Meghatározás szerint a szűrés a tünetmentes népesség vizsgálata, valamilyen betegség elő- és/vagy korai állapotának felfedezése, a betegség kivédése, vagy eredményes gyógyítása, illetőleg a betegség okozta halálozás csökkentése végett. Ennek értelmében a nőgyógyászati rákszűrés csak a méhnyakrák szűrésre vonatkozik.A méhnyakrákszűrést a nőgyógyászati vizsgálat részeként végezzük. Ekként a méhnyakrák szűrésnél a szeméremtest, a hüvely, a méhtest, a függelékekés az emlők felől is tájékozódunk, ezek kezdeti, még eredményesen kezelhető, daganatos elváltozásainak némelyikét is felfedezhetjük. Ez azonban a szűrés fogalmába nem illeszthető, statisztikai álláspont szerint nem tekinthető rákszűrésnek. Miután a nőgyógyászati vizsgálathoz a hazai gyakrolatban a kolposzkópia is hozzátartozik, a nőgyógyászati rákszűrés Magyarországon a méhnyak sejtkenet (citológiai) és kolposzkópos vizsgálatát is magába foglalja.
Megjegyzés: A kolposzkópiának, mint rákszűrési módszernek a hatékonyságát előretekintő, véletlen beválasztásos vagy más népességi vizsgálatokkal nem tanulmányozták, ezért statisztikai értelemben vett - a tényekre alapozott orvoslás eszméje szerinti - értékét nem lehet megállapítani. Használhatóságáról inkább tapasztalat és résztanulmányokalapján alkothatunk véleményt. Megállapítható, hogy a kolposzkópia a CIN felismerésének érzékeny módszere, az elváltozást olyan esetekben is gyakorta jelez, amikor a sejtkenet negatív (1). A kolposzkópia hazai hagyománya közel egy évszázados, elhagyása a statisztikai tényszerűség hiánya ellenére sem lenne megalapozott. Ugyanis, amíg népességi (előretekintő, véletlen beválasztásos stb.) tanulmányok nem igazolják, hogy a kolposzkópiai alkalmazása a méhnyakrák szűrésében nem hatékony, elhagyása hiba lenne, s talán etikailag is megkérdőjelezhető. Amiért valamit részletesen nem tanulmányoztak, az még nem jelenti azt, hogy az a valami nem jó. A nemzetközi ajánlások méhnyakrák szűrésre a sejtkenet vizsgálatát (kolposzkópia nélkül) javasolják. Ezt a szűrési módszert támogatja a tényeken alapuló orvoslás, így alkalmazása elfogadott.
A szűrésen megjelent nőknél a "nem nőgyógyászati" rákszűrésen való részvételre (mammográfia, szájüregi rákok szűrése, vastagbélrák-szűrés, melanomaszűrés) a szűrést végző szakember felhívhatja a figyelmet.
A MÉHNYAKRÁKSZŰRÉS HAZAI IRÁNYELVEI
A méhnyakrák szűrésének ajánlott hazai alapirányelveit a folyamatábra összegezi.
SZOKÁSOS SZŰRÉS (KOLPOSZKÓPIAÉSASEJTKENETISNEGATÍV)
A nemi életet a lányok többsége tizenéves korban kezdi, következésképpen már a tizenévesek is fertőződ(het)nek HPV-vel. Ezért célszerű a nőgyógyászati rákszűrést két évvel a nemi élet megkezdése után, de legkésőbb a 21. életévtől elkezdeni. A fiatal nőknél évente javasolt nőgyógyászati rákszűrés, s amennyiben a méhnyaka kolposzkóppal is épnek látszik, és/vagy a sejtkenet nem utal kóros elváltozásra, a sejtkenetet elegendő kétévenként venni. Ha a sejtvizsgálat három egymás utáni alkalommal negatív súlyos elváltozás kialakulása három éven belül nem valószínű, ezért a háromévenkénti sejtkenetvizsgálat teljesen megfelelő. . A változókorúaknál, ha a kolposzkópia negatív, elegendő a háromévenkénti kenetvétel.
Magyarázat: A fiatalok HPV-fertőzöttsége nagyon gyakori, s a nagy kockázatú HPV-vel fertőzötteknél súlyos elváltozás viszonylag rövid idő alatt-akár két éven belül is - kialakulhat, a változókor után ez a veszély már elhanyagolható, ezért a szűrések közötti időtartam három évre biztonsággal kiterjeszthető.
Hatvanöt éves kor felett, ha nemi kapcsolat már nincs, és a korábbi szűrések eredményei negatívak voltak, további szűrés célszerűtlen, de egyedileg elvégezhető.
A POZITÍV LELET ÉRTÉKELÉSÉNEK SZEMPONTJAI ÉS A TEENDŐK Rövidítések:
| ASC | atypical squamous cells (kóros laphámsejtek) |
| ASC-US | atypical squamous cells of undetremined significance (bizonytalanul megítélhető kóros |
| laphámsejtek) | |
| ASC-H | atypical squamous cells, cannot rule out high-grade squamous intraepithelial lesion |
| (nem egyértelműen megítélhető, de a súlyos laphámelváltozás nem zárható ki) | |
| SIL | squamous intraepithelial lesions (laphámbeli elváltozások) |
| LSIL | low-grade squamous intraepithelial lesions, mild dyskaryosis (CINI-nek megfelelő sejteltérések) |
| HSIL | high-grade squamous intraepithelial lesions, sever atypia (CIN2/3-nak megfelelő sejteltérések) |
| AGC | atypical glandular cells (kóros mirigyhámsejtek) |
| AGC-NOS | atypical glandular cells, not otherweis specified (bizonytalanul megítélhető kóros |
| mirigyhámsejtek) | |
| AGC-FN | atypical glandular cells, favour neoplasia (nem egyértelműen megítélhető, de a mirigyrák |
| lehetőségét felvető sejteltérés) | |
| AIS | endocervical adenocarcinoma in situ (hámbeli mirigyrák) |
1. SEJTKENET NEGATÍV, KOLPOSZKÓPIA POZITÍV
Az ún. sejtnegatív, pozitív kolposzkópia olyan kolposzkóppal felismerhető kóros, rákelőző állapotokra jellemző hámeltérések (mozaikosság, pontozottság, ecetsavpozitívitás stb.) előfordulása, amelyeknél a sejtkenetekben kóros sejtek nem fedezhetők fel.
Az értékelés szempontjai:
Az ilyen esetek 30-50%-a nem CIN/GCIN (cervicalis intraepithelialis neoplasia, glandularis cervicalis intraepithelialis neoplasia), hanem jóindulatú hámeltérés, leginkább hámátalakulás (metaplasia) következménye. Hozzávetőlegesen 40%-a CIN1, CIN2/3 pedig legfeljebb 10%-ban fordul elő, s ezek zöme is visszafejlődik (1). Enyhe sejtkenetnegatív mozaikosság, pontozottság stb. jóindulatú, sőt élettani hám átalakulások mellett is hosszú évekig megmaradhat, különösen fiataloknál. Az effélék egyik különleges példája az ún. veleszületett átalakulási sáv (congenital transformation zone, CTZ).
TEENDŐK (folyamatábra):
Hat hónaponként kolposzkópia és sejtkenet javasolt. Ha a kolposzkóppal látott elváltozás megszűnik és a sejtkenet is negatív, visszatérhetünk a szokásos szűrésre. Amennyiben a kolposzkóppal észlelhető elváltozás súlyosbodik (durva mozaikosság, pontozottság, felszíni egyenetlenség stb.) vagy sejteltérés alakul ki, szövettani vizsgálat szükséges (ld. lejjebb).
2. ENYHE FOKÚ SEJTELVÁLTOZÁSOK (ASC-US, LSIL)
Az ASC-US- és az LSIL-kenetek klinikai megítélése hozzávetőlegesen egyforma (a súlyos CIN kialakulásának veszélye a nagy kockázatú HPV-pozitív ASC-US-keneteknél 28%, LSIL-keneteknél 27%); ez indokolja együttes tárgyalásukat (2-3).
Az értékelés szempontjai:
ASC-US-kenetek: Ezek a kenetek az összes sejtkenet ~5%-át teszik ki, vagyis meglehetősen gyakoriak, következésképpen jelentősen megterhelik a szűrési rendszert. A kóros sejteltérést mutató keneteknek pedig az50%-a az ASC-US.
Az ASC-US-kenetek 5-15%-ában fordul elő súlyos CIN, illetve a súlyos CIN kialakulásával a sejtvizsgálatot követő egy-két évben 5-15%-ban számolhatunk (4-5), a nagy kockázatú HPV-pozitív ASC-US keneteknél 26%-ban (2). A rák lehetősége elhanyagolható (6).A nagy kockázatú HPV-k az ASC-US csoportban átlagosan 40-50%-ban találhatók, a serdülőkorúaknál azonban akár az esetek 70-75%-ában is (7-9). A serdülőkorúak HPV-fertőzései csaknem mindig átmenetiek.
LSIL-kenetek: Az LSIL-sejtkenet gyakorisága hozzávetőlegesen 2%, de a HPV-vel erősen fertőzött népességben ennél több is lehet (10). A 15-19 éveseknél háromszor olyan gyakori (3,9%), mint a 30-39 éveseknél (1,3%) (11). Az Egyesült Államokban az LSIL-kenetek száma az utóbbi évtizedben megkétszereződött, feltételezhetően a folyadékalapú kenetvizsgálatok elterjedése miatt (12). Jone és munkatársainak (13) több mint tizenhatezer esetet felölelő vizsgálata szerint a CIN2 az LSIL-esetek 15%-ában, a CIN3 pedig 12%-ban fordul elő. A 2006-os Amerikai Útmutató ennél kisebb arányt ad meg: a súlyos CIN az LSIL-esetek 12-16%-ában alakul ki (14), a 20 évnél fiatalabbaknál azonban csak7%-ban (3). A LSIL hátterében minden életkorban a CIN1 a leggyakoribb (~70%), a fiataloknál különösen. A CIN1/2 elváltozások fele két éven belül gyógyul, tíz éven belül pedig közel 85-90%-uktűnikel, és csak töredékükből (0,1%) keletkezik rák 24 hónapon belül, de tíz év alatt is csak 0,4%-uk alakul méhnyakrákká (15). A változókor után az LSIL-kenetek hátterében álló CIN2/3 esetek előfordulása ritkább, mint a fogamzó korúaknál (16). Várandósok LSIL-keneteinek hátterében 90%-ban fordult elő CIN1, rák egyszer sem (8,17).A nagy kockázatú HPV az LSIL-kenetekben nagyjából 80-85%-ban mutatható ki a 35 évnél fiatalabbaknál és 40%-ban a 35 évfelettiekben (5,18-19). Fiataloknál az LSIL-kenetektöbb mint 90%-ban negatívvá válnak három éven belül (60%-ban egy év alatt); idősebbeknél az arány valamivel kisebb (70-75%) (20). A serdülőkorúaknál az LSIL - a HPV-fertőzéssel együtt - átlagosan nyolc hónap alatt lezajlik (21). A dohányzás a HPV-vel fertőzötteknél elősegíti az LSIL kialakulását. Megjegyzés: A nagy kockázatú HPV-negatív ASC-US/LSIL-kenetek rendre valamilyen jóindulatú hámelváltozás (hámátalakulás [metaplasia], szarusodási zavar [parakeratosis], függölyszerű [condyloma] szövetátalakulás), ritkán visszafejlődő CIN (leginkább CIN1), esetleg kenethiba következményei. A súlyos CIN-re vonatkoztatva a HPV-meghatározás érzékenysége ASC-US/LSIL-keneteknél 95%, de fajlagossága csak 30-60% (24-25), ami azt jelenti, hogy a nagy kockázatú HPV a súlyos CIN előfordulását ugyan 95%-os biztonsággal jelzi, de a pozitív esetek 40-70%-ában nincs súlyos CIN. Az ismételt sejtvizsgálat érzékenysége 92%, fajlagossága 45-55%: az álpozitív kenetek száma tehát még az ismétléskor is sok. teendők (folyamatábra):
a) Az estleges hüvelygyulladás vagy ösztrogénhiány kezelése Az ASC-US-kenetek hátterében gyakorta gyulladás, idősebbeknél ösztrogénhiány áll, amely szintén társulhat gyulladással. Mindkét esetben a kolposzkópiát és a kenetvételt is meg kell ismételni a gyulladás, illetve az ösztrogénhiány megszüntetése után 3-4 héttel.
b) HPV-meghatározás és ellenőrző vizsgálatokA HPV-meghatározás célja ezekben az esetekben is a súlyos CIN veszélyének felmérése, mely mindenekelőtt a későbbi teendők szempontjából fontos.
Ha a nagy kockázatú HPV nem mutatható ki (HPV-negatív vagy kis kockázatú HPV), a súlyos rákelőző elváltozás és a méhnyakrák kialakulásának esélye a vizsgálat idején és az elkövetkező 1-2 évben elhanyagolható (22-23). Ilyenkor nyugodtan várakozhatunk, de a kenetvizsgálatot és a kolposzkópiát hat hónap, a HPV-vizsgálatot egy év múlva célszerű megismételni. Két, hat havonta levett, negatív sejtkenet után, ha kolposzkóposeltérés sincs, visszatérhetünka szokásos szürésre.Ha az egy évre végzett ellenőrző vizsgálatnál sem mutatható ki nagy kockázatú HPV, a sejtvizsgálat már rendszerint negatívvá válik. Elviekben előfordulhat, hogy a sejtkenet egy év után is ASCUS/LSIL, ugyanakkor nagy kockázatú HPV nem mutatható ki és a kolposzkópia is negatív, Ilyenkor a legfontosabb a kenetek ellenőrzése, az eset megbeszélése a sejtkenetet kiértékelővel, esetleg másik sejttanász (citológus) bevonásával.
Ha a nagy kockázatú HPV kimutatható (a vizsgálatok 50-85%-a), a súlyos rákelőző elváltozás keletkezésének lehetősége fennáll, ám az esetek zömében nem következik be, s a HPV-fertőzés egy-két év alatt szokásosan lezajlik, kiváltképp a fiataloknál. Mégis, a súlyos elváltozás lehetősége miatt sejtkenetvételt és kolposzkópiát három, HPV-vizsgálatot hathavonta végezzünk. Ha két év múlva is fennáll az elváltozás, s a nagy kockázatú HPV is kimutatható, szövettani vizsgálat, elsősorban célzott kimetszés, célszerű. Ha a sejtkenet negatívvá válik, hat hónap múlva ismételjük meg. Hat hónap időkülönbséggel levett két negatív sejtkenet után, ha a kolposzkópia is negatív az érintetteket szokványosan szűrjük.
c) Az ASC-US/LSIL-kenetek mellett előforduló pozitív kolposzkópia (mozaikosság, pontozottság stb., az esetek 20-30%-a) nem befolyásolja a fenti ellátási elveket, jelentősége csupán az, hogy a CIN jelenlétének jóval nagyobb a valószínűsége, mint a kolposzkóposan negatív esetekben. A kolposzkópia tehát a sejtvizsgálat kiegészítője és ellenőre is. A negatív kolposzkópia értékelésénél alapvető, hogy látjuk-e az egész átmeneti sávot (transzformációs zóna). Ha igen, a CIN jelenléte valószínűtlen, de az AIS-sé is kétséges. Ha az átmeneti sáv nem hozható teljes egészében látótérbe, a nyakcsatornában esetleg kialakuló rákelőző állapotra a vizsgálatból nem következtethetünk.
d) Ha az ellenőrzés alatt HSIL-kenetre alakulnak ki, a szövettani vizsgálat elengedhetetlen. (Vö. HSIL-sejtkenet) Megjegyzés: a dohányosokat feltétlenül tájékoztassuk, hogy a dohányzás abbahagyása elősegíti a vírusok kiürülését, a sejteltérések visszafejlődését (26).
3. SÚLYOS ELVÁLTOZÁSOKRA UTALÓ KENETEK (HSIL, AIS, ASC-H, AGC)
A HSIL- és az AIS-sejtkenet egyértelműen súlyos hámelváltozásra utalnak. Az ASC-H-kenetek gyakorlati jelentőségét a szakembereka HSIL-lel megegyezőnek tartják, mondván, hogy a súlyos rákelőző állapot és a kezdődő rák ezeknél csak szövettani vizsgálattal zárható ki (3, 7). Hasonlóan, ha a kenetben kóros mirigysejtek láthatók, a súlyos rákelőző elváltozást (AIS) vagy a mirigyhámrákot biztonsággal csak szövettani vizsgálattal ismerhetjük fel, annakellenére, hogy a kóros sejtelváltozások mértéke a mirigyhámsejteknél is utal a betegség súlyosságára. A kóros mirigyhámsejteket tartalmazó sejtkeneteknél tehát szintén csak szövettani vizsgálattal tisztázhatjuk a méhnyak állapotát, ezért soroljuk ezeket is a HSIL-kenetekkel egy csoportba. Az értékelés szempontjai:
HSIL-kenetek: A HSIL-kenetekaránya a fejlett országokban kevesebb mint 1% (15-19 évesek: 0,7%; 20-29 évesek: 0,8%; 30-39 évesek: 0,7% ) (11). Ivarérett korú és idősebb nőknél a HSIL-kenetek hátterében célzott mintavétellel 70-80%-ban mutatható ki súlyos CIN, hurokkimetszéssel pedig 95%-ban (27), a 25 évnél fiatalabbaknál azonban csak az esetekfelében van CIN2/3. A 25-30 évnél idősebbek 2-5%-ában a HSIL mögött márrákáll.AserdülőkorúaknálaCIN2 jóval gyakoribb, mint a CIN3, rák pedig kivételesen fordul elő (a 20 év alatti korcsoportban 0-3 eset egy millió tizenévesre számolva) (28). HSIL-keneteknél a nagy kockázatú HPV-fertőzöttség a 90%-ot is meghaladja, csaknem mindegyik beteg HPV-pozitív. A HSIL-esetek alakulását nehéz megítélni: az érintetteket szokásosan kezeljük, és csak egy-egy kezelés nélküli esettanulmányt ismerünk. Hozzávetőlegesen azt állapíthatjuk meg, hogy az eseteknek legfeljebb egyharmada fejlődhet vissza, de a tizenéveseknél sokkal nagyobb arányban mérséklődik, válik negatívvá a HSIL-sejtkenet két év alatt (29).ASC-H-kenetek: Az ASC-US-kenetekkel ellentétben az ASC-H-kenetek hátterében gyulladás és/vagy ösztrogénhiány nem áll: ezek ugyanis a ráksejtre utaló sejteltéréseket nem idézik elő. A nemzetközi álláspont szerint az ASC-H kenetek az ún. előrehaladó HPV-fertőzés következményei. Súlyos CIN az esetek 40-50%-ában mutatható ki (30). ASC-H-kenetknél a nagy kockázatú HPV-fertőzésekaránya 80% (7).AGC-, AIS-kenetek: A kóros (atípusos) mirigysejteket tartalmazó keneteket a Bethesda-rendszer három fokozatra osztja: AGC-NOS (atypical glandular cells not otherwise specified; AGUS néven is előfordul), AGC-FN (atypical glandular cells favor neoplasia) és AIS (adenocarcinoma in situ). A kóros mirigysejteket együttesen AGC-nek (atypical glandular cells) nevezik. Mások az enyhe mirigyhámelváltozásokat AGC-nek, a súlyosakat AIS-nak mondják (31). A mirigyhám rák elő ző állapotainak szövettani fokozatai bizonytalanok, valódi rákelőző állapotnak csak az in situ mirigyrákot tartják (32). A méhnyak hámbeli mirigyrákja a harmincas éveikben járóknál a leggyakoribb, száma fokozatosan nő, és szokásosan az átmeneti sáv felső (nyakcsatornai) részében keletkezik és terjed azon túl a nyakcsatornában. Tehát túllép az átmeneti sávon.Az AGC-NOS-kenetek hátterében célzott kimetszéssel súlyos CIN-t (CIN2 és CIN3) 8-40%-ban, az AGC-FN-esetekben pedig 27-96%-ban fedeztek fel és rák is előfordult (33). Az utóbbi csoportban a méhtestráksem kivételes, sőt petefészek-vagy méhkürtrákot is kórisméztek. Az AGC-vel jelzett kenetek0-8%-ában AIS-t és 1-9%-ában rákot találtak (6). AIS-keneteknél az in situ mirigyrák 48-69%-ban, mirigyrák 38%-ban fordult elő, utalva arra, hogy a hámbeli és a már kialakult rákot a kóros mirigysejtek alapján nem nagyon lehet elkülöníteni (6, 34). A kóros mirigysejteket tartalmazó kenetek hátterében előforduló szöveti elváltozások tehát sokfélék (CIN, AIS, laphám-, mirigyrák), és előfordulásuk az irodalomban széles határok között változik. A egyöntetűség hiánya egyrészt arra vezethető vissza, hogy a sejttani jellemzők nem mindig ismerhetők fel egyértelműen - a sejtkenet értékelése így bizonytalan - másrészt, hogy a sejttanászok a keneteket különbözőképpen értékelik, véleményeik különbsége számottevő (interobserver variability). Ámbár az AGC-kenetek formái a mirigyrákok tekintetében súlyossági fokozatokat (AGC-NOS ® AGC-FN ® AIS) jelentenek, az in situ és mirigyrák mégis mindegyik csoportban előfordul, méghozzá nehezen felmérhető arányban. A súlyos CIN vonatkozásában nincs fokozati különbség: mindegyikben egyaránt megtalálható, és nem is ritkán. Ha a kóros mirigysejtek HSIL-kenetben láthatók, a laphámrákokgyakoribbak, mint a HSIL-keneteknél, a mirigyrákok azonban nem (33).A nagy kockázatú HPV az AIS-kenetek 70-90%-ában (80-85%-ban HPV16/18) mutatható ki (35).A kolposzkópia az esetek 20%-ában negatív, a felében pedig nem megfelelő, hiszen az elváltozás a szövetekben mélyen - a felszínt nem éri el - és a nyakcsatornában helyezkedik el, rendre az átmeneti sávon túlérve. Ha a mirigyhámbetegség laphám elváltozással társul (30-50%), a kolposzkóppal szokásosan a lap hám elváltozásokat látjuk. Jóllehet megfigyeltek kolposzkóppal felismerhető elváltozásokat -leginkább a kóros érrajzolat és valamelyest a felszíni egyenetlenség -, amelyek arra utalhatnak, hogy a folyamat az alaphártyát már áttörte, de ezek a jelek annyira nem megbízhatók, hogy ezek alapján a kezdődő rákot és a rákelőző állapotot biztonsággal elkülönítsük. Olyan kolposzkóppal látható elváltozás sincs, amely egyértelműen AIS-ra vagy mirigyrákra utalna. A negatív vagy nem megfelelő kolposzkópia miatt a ko poszkóppal vezérelt kimetszés sem lehetséges, illetve elégtelen.
TEENDŐK (folyamatábra):A súlyos hámelváltozásokra utaló (HSIL, AIS) vagy azok lehetőségét felvető (ASC-H, AGC-FN) kenetek eseteiben az alapszabály a szövettani vizsgálat elvégzése. A kúp- vagy hurokkimetszés az egyetlen megbízható módszer az AIS és a mirigyrák felismerésére, kiterjedésének megállapítására.
a) HSIL-, ASC-H-kenetek A HSIL- (ASC-H-) kenetnél a kúpkimetszés, hurokkimetszés a leghatékonyabb, Ilyenkor a HPV-meghatározásnak nincs gyakorlati jelentősége: a súlyos CIN-ek csaknem mindegyike és a laphámrák is nagy kockázatú HPV-pozitív. Elviekben HPV-meghatározással elkülöníthet nénk a "veszélyes" és az "ártalmatlan" ASC-H-eseteket - és ezt egyedi esetekben meg is tehetjük -, a nagy kockázatú HPV-fertőzések legalább 80%-os gyakorisága miatt a HPV-vizsgálatnak gyakorlati jelentősége vajmi kevés (7, 9). A 25 évnél fiatalabbaknál a HSIL (ASC-H) esteinek felében nincs súlyos CIN és a CIN2 is sokkal gyakoribb, mint a CIN3, a rák veszélye pedig elhanyagolható, ezért a kolposzkóppal vezérelt szöveti mintavétel elegendő. Ha ez CIN3-at vagy kezdeti rákot mutat, kúpkimetszést kell végezni.
c) AIS- és AGC-FN-kenetekAz AIS- és az AGC-FN-keneteknél is a kúp- vagy hurok kimetszés a leghelyesebb; a nyakcsatornából így lehet megfelelően szövettani vizsgálatra mintátvenni.. Az egyidejű méhkaparás elengedhetetlen a méhtestrák felismerése végett; a méhnyak- és méhtestrák együtt is előfordulhat. A kúp-hurok kimetszés előtt azonban célszerű a belső nemi szervek ultrahangvizsgálata - a méhnyálkahártya és a függelékek állapotának megítélésére-, a CA125-meghatározás és a HPV-vizsgálat.. Ha a méhtest-vagy függelékrák igazolódik, a kúpkimetszés szükségtelen. Ha a kenetben káros méhnyálkahártyasejtek láthatók, ultrahangvizsgálat és méhkaparás a legelső teendő.
d) AGC-NOS- (AGUS-) kenetekAGC-NOS-keneteknél az első a HPV-meghatározás. Ha nagy kockázatú HPV nincs, valamint a kolposzkópia és a medencei ultrahangvizsgálat is negatív, a szövettani vizsgálattól eltekinthetünk, a sejtvizsgálatot, a kolposzkópiát, a HPV-meghatározást és az ultrahangvizsgálatot hat hónaponként ismételjük meg. Két negatív eredményt (sejtkenet, kolposzkópia, ultrahang, HPV-meghatározás) követően visszatérhetünka szokásos szűrésre.Ha a nagy kockázatú HPV pozitív, szövettani vizsgálat végzendő.
e) A kolposzkópia lényegesen nem befolyásolja a megadott irányelveket, de a klinikust nagyon jól irányítja:
- kifejezett, egyenetlen mozaik és pontozottság stb. CIN3-ra utal, és fordítva, enyhe elváltozás CIN1/2-t valószínűsít;
- ha az egész átmeneti sáv látszik, a CIN megitélhető;
- irányítja a kúp-hurok kimetszést, de leginkább a célzott mintavételt;
- ha a kolposzkóppal nem látszik eltérés, nagyobb a valószinüsége annak, hogy a folyamat a nyakcsatornában fejlődött ki.
A szövettani vizsgálat utáni teendők
a) A CIN mindegyik formájánál a kúp-hurok kimetszés, ha az eltávolítást az épben végeztük, teljesen megfelelő kezelés. Ha nem az épben vágtuk ki az elváltozást, a legbiztonságosabb az ismételt kimetszés, szokásosan a sebgyógyulás után. Egyedi esetekben a betegek fokozott követése négy hónaponkénti HPV-, sejt- és kolposzkópos vizsgálattal is megengedett, különösen azoknál, akik még szülni szeretnének.
b) A 25 évnél fiatalabbaknál, akiknél csak célzott kimetszést végeztünk, ellenőrzés szükséges: hat hónaponkénti sejtvizsgálat és kolposzkópia ajánlott. Ha a HSIL (ASC-H) egy év után is fennáll, az elváltozás teljes eltávolítása tanácsos.
c) A hámbeli (in situ) mirigyrák gyakorta többgócú, ezért sokan az elváltozás megfelelő, ép szélekkel végzett kimetszését sem tartják elegendőnek, a méh eltávolítását javasolják. Ezt támasztja alá, hogy az AIS hajlamos kiújulásra, és mirigyrákká alakulhat (36). A szülni már nem akaró nőknél a méheltávolítás megfontolandó. A gyermeket akaróknál a várakozó álláspont is megengedett, egyedi megbeszélés, döntés szerint. Megfelelő ellenőrzés (4-6 hónaponkénti HPV-, sejtvizsgálat és kolposzkópia) mellett a méhnyakrák kockázata csekély, de a betegség kiújulása, az ismételt kúpkimetszés, a későbbi méheltávolítás és bizonyos mértékű várandóssági szövődmény (gyakoribb koraszülés, kissúlyú magzat stb.) lehetőségével számolni kell (37).Ha a sebészi szélek nem épek, vagy biztonsággal nem ítélhetők meg, a visszamaradt AIS lehetősége 50%, a ráké pedig 6% (38), következésképpen a kúp- vagy hurokkimetszés megismétlése javasolt, szokásosan három hónapon belül.
SZŰRÉSEK ÉS A HPV-VÉDŐOLTÁS
A HPV-védőoltás jelentőségének felméréséhez még hosszú évek kellenek: majd csak akkor becsülhetjük meg, hogy csökkentette-e a méhnyakrák előfordulását és milyen mértékben. Amíg elegendő tapasztalat nem gyűlik össze, a beoltottaknál is a rákszűrés fenti elveit alkalmazzuk.
KIEGÉSZÍTŐ MEGJEGYZÉSEK
A fentiekben megfogalmazott irányelveket a Szülészeti és Nőgyógyászati Szakmai Kollégium állította össze, és a kollégium hivatalos útmutatójának tekinthető. A kollégium ugyanis, a méhnyakrák keletkezésével kapcsolatos ismereteink robbanásszerű bővülése és az új megelőzési és vizsgálómódszerek miatt, szükségesnek tartotta a hazai nőgyógyászati rákszűrés elveinek módosítását, az új"szűrésútmutató" kiadását.Az irányelvek összeállításának alapvető szempontja a mindennapi orvosi gyakorlat és a már bevált (megfelelő irodalmi adattal alátámasztott) módszerekalkalmazásavolt. A méhnyakrákszűrésére javasolt ún. megtekintési, színelemzési módszerek,a polarprobe és a molekuláris jelzők (pl. p16 stb.) kísérleti szakaszban vannak, beépítésük a szűrési irányelvekbe még nem időszerű (39).A HPV-vizsgálat helye a szűrési útmutatókban még nem kristályosodott ki: többen vitatják jelentőségét a harminc évnél fiatalabb nőknél, mondván, hogy náluk a fertőzés és a rákelőző állapotok is nagyon gyakoriak, rák mégis csak elvétve alakul ki, következésképpen a vizsgálat nem "költséghatékony". A "költséghatékony" szót idézőjelbe tettük, egyrészt mivel elkoptatott divatszó, másrészt mert az egészségügyi ellátás nem kereskedelem, szakmai elveit alapvetően nem a költségek határozzák meg.Az egyes országokban (hazánkban is) elterjedt, ám visszaszorulóban lévő gyakorlat, a kolposzkóppal vezérelt célzott kimetszés, amelyet, ha az alaphártya áttörése, vagyis rák nem látható, az ún. szövetpusztító kezelés követ, nem javasolt. Az eljárás nagyon sok buktatót rejt magában: a tévedések aránya 30-40%, amit többszörös kimetszéssel igyekeznek csökkenteni (40).Szóba került az Isoprinosine (inosine pranobex) tabletta adása a nagy kockázatú HPV-vel fertőzötteknek, ám nincs tudományos bizonyíték arra, hogy hatásos lenne. A gyógyszer leírásban ez olvasható: az Isoprinosine adagolása nagy kockázatú HPV fertőzésekben megfontolandó. Ennek bizonyítására feltétlenül szükségesek a további vizsgálatok.Egyetlen szűrőmódszer sem 100%-os, jóllehet a társadalom ezt elvárná. A szűrés korlátairól a szűrendő lakosságot is tájékoztatni kell. A méhnyakrák szűrésével a méhnyakrákok messze nagy többsége kivédhető, de nem az összes. A szűrési módszer, a résztvevők stb. hibájából óhatatlanul előfordulhatnak fel nem ismert esetek. Aki a szűréseken részt vesz, az ezzel legyen tisztában. Az ilyen tájékoztatás a jogi következményeknek is elejét veheti.A megfogalmazott irányelvek nem előírások, csupán egyfajta útmutatásul szolgálnak, amelyet az egyedi igények, az adott beteg kívánalmainak megfelelően lehet módosítani. Minden orvosi kezelés egyedi, a beteg és a kezelő orvos(ok) közös döntése. Az eltérés az irányelvektől nem hiba, jogi következményei nem lehetnek.
IRODALOMJEGYZÉK
1. Pete I, Tóth V, Bősze P. The value of colposcopy in screening cervical carcinoma. Eur J Gynaecol Oncol 1998;19:118.
2. Cox JT, Schiffman M, Solomon, D, et al. Triage Study (ALTS) Group. Prospective follow-up suggests similar risk of subsequent cervical intraepithelial neoplasia grade 2 or 3 among women with cervical intraepithelial neoplasia grade 1 or negative colposcopy and directed biopsy. Am J Obstet Gynecol 2003;188:1406-12.
3. Moscicki AB. Management of adolescents who have abnormal cytology and histology. Obstet Gynecol Clin N Am 2008;35:633-43.
4. Melnikow J, Nuovo J, William AR, Chan BK, Howell LP. Natural history of cervical squamous intraepithelial lesions: a meta-analysis. Obstet Gynecol 1998;92:727-35.
5. Hughes SA, Sun D, Gibson C, Bellerose B, Rushing L, Chen H, et al. Managing atypical squamous cells of undetermined significance (ASCUS): human papillomavirus testing, ASCUS subtyping or follow-up cytology? Am J Obstet Gynecol 2002;186:396-403.
6. Wright TC, Cox JT, Massad LS, Twiggs LB, Wilkinson EJ. 2001 ASCCP-sponsored Consensus Workshop. Consensus guidelines for the management of women with cervical cytological abnormalities and cervical cancer precursors-part I: cytological abnormalities. JAMA 2002;287:2120-9.
7. ALTS, Duncan LD, Jacob SV, Atypical sqamous cell, cannot exclude a high-grade squamous intraepithelial lesion: the practice experience of a hospital-based reference laboratory with this new Bethesda system diagnostic category. Diagn Cytopathol 2005;32:243-6.
8. Boardman LA, StankoC, Weitzen S,etal. Atypical squamous cells of undetermined significance: human papillomavirus testing in adolescents. Obstet Gynecol 2005;105:741.
9. Evans MF, Anderson CS, Papillo JL, et al. Distribution of human papillomavirus types in ThinPrep Papanicolaou tests classified according to the Bethesda 2001 terminology and correlations with patient age and biopsy outcomes. Cancer 2006;106:1054-64.
10. Jone BA, Davey DD. Quality management in gynecologic cytology using interlaboratory comparison. Arch Pathol Lab Med 2000;124:672-81.
11. Mount SL, Papillo JL. A study of 10,296 pediatric and adolescent Papanicolaou smear diagnosis in Northen New England. Pediatrics 1999;103:539.
12. Davey DD, Neal MH, Wilbur CC,etal. Bethesda 2001 implementation and reporting rates: 2003 practices of participants in the College of American Pathologists Interlaboratory Comparison Program in Cervicovaginal Cytology. Arch Pathol Lab Med 2004;128:1224-9.
13. Jone BA, Novis DA. Follow-up of abnormal gynecologic cytology: a college of American Pathologists Q-probes study of 16132 cases from 306 laboratories. Arch Pathol Lab Med 2000;124:665-71.
14. Wright TC, Massad LS, Dunton CJ, et al. 2006 Consensus guidelines for the management of women with abnormal cervical cancer screening tests Am J Obstet Gynecol 2007;197:346-55.
15. Holowarty P, Miller AB, Rohan T,To T. Natural history of dysplasia of the uterine cervix. J Natl Cancer Inst 1999;91:252-8.
16. Eltoum IA, Chhieng DC, Roberson J,et al. Reflux human papillomavirus infection testing detects the same proportion of cervical intraepithelial neoplasia grade 2-3 in young versus elderly women. Cancer 2005;105:194-8.
17. Murta EF, de Andrade FC, Adad SJ, et al. Low-grade squamous intraepithelial lesion during pregnancy: conservative antepartum management. Eur J Gynecol Oncol 2004;25:600-2.
18. ASCUS-LSIL Triage Study (ALTS) Group. A randomized trial on the managament of low-grade squamous intraepithelial lesion cytology interpretations. Am J Obstet Gynecol 2003;188:1393-400.
19. Human papillomavirus testing for triage of women with cytologic evidence of low-grade squamous intraepithelial lesions: baseline data from a randomised trial. The Atypical Squamous Cells of Undetermined Significane/Low-Grade Squamous Intraepithelial Lesions Study (ALTS) Group. J Natl Cancer Inst 2000;92:397-402.
20. Moore K, Cofer A, Elliot L, et al. Adolescent cervical dysplasia: histological evaluation, treatment, and outcomes. Am J Obst Gynecol 2007;197:141,e1
21.Moscicki AB,etal. Regression of low-grade squamous intraepithelial lesions in young women. Lancet 2004;364:1678-83.
22. Castel PE, Cox JT, Jeronimo J, et al. An analysis of high-risk human papillomavirus DNA-negative cervical precancers int he ASC-US-LSIL Trial Study (ALTS) Obstet Gynecol 2008;111:847-56.
23. Safaeian M, Solomon D, Wacholder S, et al. Risk of precancer and follow-up management strategies for women with human papillomavirus-negative atypical squamous cells of undetermined significance. Obstet Gynecol 2007;109:1325-31.
24. Arbyn M, Buntinx F, Van Rast M, et al. Virologic versus cytologic triage of women with equivocal Pap smear: a meta-analysis of the accuracy to detect high-grade intraepithelial neoplasia. J Natl Cancer Inst 2004;96:280-93.
25. Arbyn M, Paraskevaidis E, Martin-Hirsch P, Prendeville W, Dillner J. Clinical utility of HPV-DNA detection: Triage of minor cervical lesions, follow-up of women treated for high-grade CIN: An update of pooled evidence. Gynecol Oncol 2005;99:S7-11.
26. Szarewski A, Jarvis MJ, Sasieni P, et al. Effect of smoking cessation on cervical lesion size. Lancet 1996;347:941-3.
27. Dunn TS, Burke M, Shwayder J. A'see and treat'management for high-grade sqamous intraepithelial lesion Pap smears. J Low Genit Tract Dis 2003; 7:104-6.
28. Chan PG, Sung HY, Sawaya GF. Changes in cervical cancer incidence after three decades of screening US women less than 30 years old. Obstet Gynecol 2003;102:765.
29. Case AS, Rocconi RP, Straughn JM Jr, et al. Cervical intraepithelial neoplasia in adolescent women: incidence and treatment outcomes. Obstet Gynecol 2006;108:1369.
30. Sherman ME, Castle PE, Solomon D, et al. Cervical cytology of atypical squamous cell cannot exclude high-grade intraepithelial lesions (ASC-H): characteristics and histologic outcomes. Cancer 2006;108:298-305.
31. Syrjanen KJ. Histology, Classification and Natural History of Cervical Intraepithelial Neoplasia (CIN). CME J Gyncol Oncol 2009;14: megjelenés alatt.
32. Lee KR, Flynn CE. Early invasive adenocarcinoma of the cervix. Cancer 2000;89:1048-55.
33. Westin MC, Derchain SF, Rabelo-Santos SH,et al. Atypical gűlandular cells and adenocarcinoma in situ according to the Bethesda 2001 classification: cytohistological correlation and clinical implications. Eur J Obstet Gynecol 2008;139:79-85.
34. Derchain SF, Rabelo-Santos SH, Sarian LO, et al. Human papillomavirus DNA detection and histological findings in women reffered for atypical glandular cells or adenocarcinoma in situ in their Pap smears. Gynecol Oncol 2004;95:618-23.
35. Castellsague X, Diaz M, de Sanjonse S, et al. Worldwide human papillomavirus etiology of cervical adenocarcinoma and its cofactors:implications for screening and prevention, J Natl Cancer Inst 2006;98:303-15.
36. Goldstein NS. An investigation of the mechanisms underlying the disparity between rate of residual endocervical adenocarcinoma in situ (AIS) in hysterectomy specimens and clinical failure following conservatively treated AIS. Am J Clin Pathol 2004;122:540-5.
37. Bull-Phelps SL, Granter EIO, Walsh ChS, Gehrig PA, Miller DS, Schorge JO,et al. Fertility spearing surgery in 101 women with adenocarcinoma in situ of the cervix. Gynecol Oncol 2007;107:316-9.
38. Denehy TR, Gregori CA, Breen JL, et al. Endocervical curettage, cone margins, and residual adenocarcinoma in situ of the cervix. Obstet Gynecol 1997;90:1-6.
39. Bősze P. A méhnyakrákszűrése és megelőzése: hagyomány és újirányzatok. Nőgyógy Onkol 2008;13:10-30.
40. Gage JC,Hanson VW, Abbey K, et al. Number of cervical biopsies and sensitivity of colposcopy. Obstet Gynecol 2006;108:264.
A szakmai irányelv érvényessége: 2010. szeptember 30.
MELLÉKLET
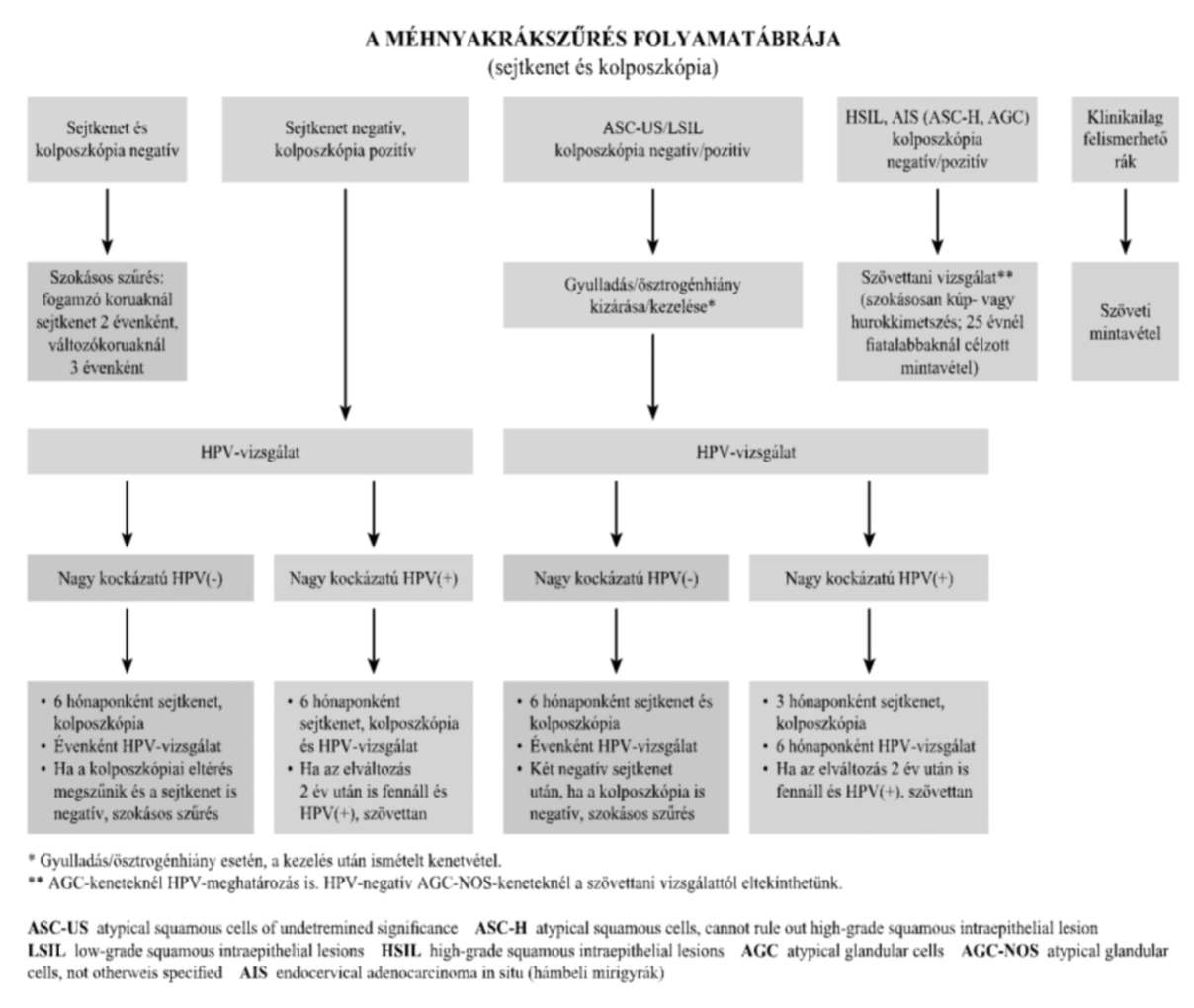
Az Egészségügyi Minisztérium
szakmai protokollja
Interstitialis tüdőbetegségekről
Készítette: a Tüdőgyógyászati Szakmai Kollégium
I. Alapvető megfontolások Bevezetés
A tüdő diffúz disszeminált gyulladásos megbetegedései heterogén csoportot alkotnak, több mint 200 kórkép sorolható ide. A betegségek kivizsgálása, kezelése és prognózisa különböző, mégis van néhány olyan közös tulajdonság (klinikai-radiológiai kép, az alveolitistől a tüdőfibrosisig vezető pathogenetikai út), amelyek alapján a közös csoportba sorolás indokolható. A betegségcsoport elnevezése nem egységes, a kórképek csoportosítása hasonlóképpen ellentmondásos. A fentiekből következik, hogy nincsenek általánosan elfogadott diagnosztikus és terápiás ajánlások sem.
Az elmúlt évtizedekben több olyan alap, és klinikai kutatási eredmény született, melynek egy része átkerült a klinikai gyakorlatba (képalkotó technikák, patológiai beosztás stb.).
A betegek eredményes kivizsgálása és kezelése csak a különböző szakterületek szoros együttműködése esetén valósulhat meg, a csapatmunkában a tüdőgyógyászoknak kitüntetett helye van. Az esetek többségében felfedezik, diagnosztizálják a betegséget, elvégzik a nem-sebészi mintavételi módszereket, és a részletes légzésfunkciós vizsgálatokat. A tüdőgyógyász szakma rendelkezik a legnagyobb tapasztalattal a diffúz parenchymás gyulladásos megbetegedések kivizsgálásában, kezelésében, követésében és gondozásában.
Definíció
A tüdő diffúz gyulladásos megbetegedéseihez egymástól igen eltérő kórképek tartoznak, melyek közös tulajdonsága, hogy azalveolusokés az interalveolarisszeptumok (kötőszöveti sejtek, kötőszöveti matrix,capillarisok) mellett érintik a perivascularis, perilymphaticus, és a peribronchialis szöveteket is. Az esetek egy részében a gyulladásos folyamatok tüdőfibrosishoz vezetnek. Az interstitialis tüdőbetegségek (továbbiakban ISTB) elnevezés nem fedi a kórkép valamennyi formáját, ennek ellenére a nemzetközi irodalomban ez az elnevezés terjedt el.
Epidemiológia
Pontos hazai és nemzetközi adatok nincsenek. Irodalmi adatok szerint férfiakban 31,5%000, nőkben pedig 26,1%000a prevalencia. E betegek a pulmonológiai praxis 5%-át jelentik.
1. táblázat
ISTB felosztása etiológiájuk alapján
ISTB pathologiája
| ISMERT ETIOLÓGIA | ISMERETLEN ETIOLÓGIA |
| Baktériumok, gombák, vírusok, protozoonok | Idiopathias tüdőfibrosis |
| Szervetlen anyagok (koniozisok) | Rendszerbetegséghez társuló ISTB |
| Silicosis | Granulomatosus kórképek |
| Asbestosis | Sarcoidosis |
| Berylliosis | Langerhans sejtes histiocytosis |
| Szerves vegyületek (hypersensitiv pneumonitis) | Vasculitisek |
| Gyógyszerek (bleomycin, amiodaron) | Wegener granulomatosis |
| Toxikus gőzök, gázok (ózon, klór) | Goodpasture szindróma |
| Sugárkezelés | Pulmonalis haemosiderosis |
| Szisztémás toxikus anyagok (paraquat) | Churg-Strauss szindróma |
| Más szervek betegségei | Kötőszöveti betegségek |
| Hepatitis, cirrhosis | Szisztémás sclerosis |
| Bal kamra elégtelenség | Rheumatoid arthritis |
| Krónikus uraemia | Polymyositis |
| Gyulladásos bélbetegségek | Dermatomyositis |
| Behcet szindróma | |
| Szisztémás lupus erythematosus | |
| Sjögren szindróma | |
| Spondylitis ankylopoetica | |
| Öröklődő megbetegedések | |
| Neurofibromatosis | |
| Sclerosis tuberosa | |
| Alveolaris proteinosis | |
| Microlithiasis alveolaris pulmonum | |
| Amyloidosis | |
| Lymphangioleiomyomatosis |
- Az interstitialis tüdőbetegségek egy (kisebb) részének jellegzetes szövettani képe van (silicosis/silicium kimutatásával, tuberculosis/a baktérium azonosításával, alveolaris proteinosis, lymphangioleiomyomatosis, amyloidosis, Langerhans sejtes histiocytosis).
- Egy másik csoport szövettani képe alátámasztja a klinikai diagnosist, de önmagában nem jellemző a kórképre. (granulomatosus elváltozások, vasculitisek).
- A fentiekhez nem sorolható ismeretlen eredetű interstitialis tüdőbetegségek beosztása a következő táblázaton látható. Az egyes szövettani típusok többféle klinikai kórképhez társulhatnak, egymással egyidőben keveredhetnek és egymásba átmehetnek. Az ATS/ERS beosztást javasoljuk a napi gyakorlatba átvenni.
2. táblázat
Ismeretlen eredetű interstitialis pneumoniák beosztása ATS/ERS 2002
| Szöveti kép | Klinikai - radiológiai -pathológiai diagnózisok |
| Usual Interstitial Pneumonia (UIP) | Idiopathias Pulmonary Fibrosis (IPF) Cryptogen Fibrosing Alveolitis (CFA) |
| Nonspecific Interstitialis Pneumonia (NSIP) | Nonspecific Interstitial Pneumonia (NSIP) |
| Organizing Pneumonia (OP) (BOOP) | Cryptogen Organizing Pneumonia (COP) (Idiopathias BOOP) |
| Diffúz alveolaris károsodás (DAD) | Acute Interstial Pneumonia (AIP) |
| Respiratory Bronchiolitis (RB) | Respiratory Bronchiolitis Interstitial Lung Disease (RBILD) |
| Desquamative Interstitial Pneumonia (DIP) | Desquamative Interstitial Pneumonia (DIP) |
| Lymphocytic Interstitial Pneumonia (LIP) | Lymphocytic Interstitial Pneumonia (LIP) |
Klinikai kép
Az ISTB felfedezése történhet tünetmentes állapotban mellkasröntgenen észlelt elváltozások miatt. A tünetek nem jellemzőek. Hosszú tünetmentes időszak után száraz köhögés, nehézlégzés alakulhat ki, kezdetben csak terheléskor, később nyugalomban is. A légszomjfokozatosan súlyosbodhat. Cyanosis, gyengeség, étvágytalanság, subfebrilitás, láz, légzési elégtelenség jelentkezhet. Légmell alakulhat ki, pleuritis jöhet létre. Később a légzési elégtelenség képe dominál. A rendszerbetegségekhez tartozó extrapulmonalis tünetegyüttesek sokféle formában jelentkezhetnek.
II. Diagnózis
Az ISTB diagnosztikája
A részletes kórtörténet felvételekor rögzíteni kell a dohányzási szokásokat, munkahelyi körülményeket, a hobby-szabadidő tevékenységet, a családban előforduló öröklődő megbetegedéseket. Ki kell térni a jelenleg és a korábban szedett gyógyszerekre, valamint az egyéb (korábbi) megbetegedésekre is.
A fizikális vizsgálat során rögzíteni kell a bőr, perifériás nyirokcsomók, máj-, lép állapotát. A tüdő hallgatózási lelete nem jellegzetes, kialakult fibrosis esetén belégzésben un. hóropogás-szerű hangok (fibroticus pattogás) hallhatók.
Képalkotó eljárások
Hazánkban az ernyőfényképszűrés előnyeit kihasználva megállapítható a tüdőelváltozás kezdetének hozzávetőleges időpontja, az esetleges spontán regresszió, illetve a progresszió gyorsasága stb. Az esetek jelentős részében a tüdőelváltozásokat hagyományos mellkasröntgen felvételeken fedezik fel. A leggyakoribb eltérések közé sorolható alveolaris infiltratumok, tejüvegszerű homályok, miliaris szórás, interstitialis elváltozások, nyirokcsomó eltérések, pleuralis folyadék, pneumothorax stb. egyike sem tekinthető kórkép-specifikusnak. Negatív mellkasröntgen felvétel ellenére felvetődő ISTB gyanú esetén a HRCT vizsgálat elvégzése indokolt.
A HRCT vékonyszeletes, szélkiemelő technikát használ, mely nagy térbeli felbontása révén alkalmas a tüdőszövet secunder lobulusok anatómiájának és patológiai folyamatainak megjelenítésére. A 16 szeletes CT-k felbontása 300ë körül van. A HRCT- felvételek natívan készülnek be- és kilégzésben (levegőcsapda/obstrukció kimutatására), háton/hason (funkcionális atelectasia/fibrosis bizonyítására). Egy síkban cine-mód felvételre is van lehetőség a légzés dinamikus értékeléséhez. A HRCT indikációja és feladata:
- negatív röntgenfelvétel és kóros légzésfunkciós teszt esetén korai diagnózis
- parenchyma eltérések morfológiai elemzése és osztályozása, differenciáldiagnózisa
- betegség aktivitásának megítélése (szteroid teszt DIP-ben),quantitatív mérések, prognózis meghatározása, terápia követése,
- biopszia típusának megválasztása, helyének kijelölése (transbronchialis, thoracotomias, VATS)
- biopsziák számának csökkentése - UIP és speciális morfológiájú diffúz tüdőbetegségek eseteiben Röntgen-morfológiai jellemzői:
- reticularis (vonalas) rajzolat (interface jel=hörgők, erek, pleurafelszínek mentén irregularis rajzolat a felszaporodott interstitium következtében)
- nodularis (gócos) rajzolat (1-10 mm gócok)
- tejüvegszerű homály (hörgőkés erek jól követhetők) GGO = ground-glass opacity
- beszűrődés (consolidatio) (erek nem követhetők, a légutak folyadékkal, proteinnel, sejtekkel stb. kitöltöttek, -levegőbronchogram)
- csökkent denzitású (cysticus) elváltozás
HRCT-vel jellegzetes képet mutató interstitialis tüdőbetegségek
- silicosis
- sarcoidosis
- lymphangitis carcinomatosa
- subacut hypersensitiv pneumonitis
- BOOP (COP = cryptogenic organizing pneumonia)
- idiopathiás tüdőfibrosis (UIP)
- lymphangioleiomyomatosis (LAM)
- Langerhans-sejtes histiocytosis
Egyéb képalkotó módszerek
Korábban a gallium scintigraphiánakdiagnosztikus és prognosztikai szerepet tulajdonítottak. Napjainkra igazolódott, hogy a módszer drága, időigényes, a kiértékelés sokszor pontatlan, a sorozatos vizsgálatok sugárterhelése pedig magas. Szerepe talán a biopszia számára nem elérhető extrapulmonalis sarcoidosis kimutatásában lehet. Egyéb scintigraphiás izotópos módszerek (99Tc-DTPA, indium-111 stb.), valamint a PET, az MRI és a CT napjainkban is a klinikai kutatások témái pl. a tüdőparenchyma elváltozások és a légzésfunkció kapcsolatában.
Laboratóriumi vizsgálatok
A betegség felfedezésekor általában elvégzett "rutin" laboratóriumi vizsgálatok magukban foglalják a kvantitatív és kvalitatív vérképet, vérsejt süllyedést, máj-, és vesefunkciót. Hypersensitiv pneumonitis esetén a feltételezett diagnosist megerősítheti a keringő ellenanyagok kimutatása, autoimmun kórképek esetén pedig anti-DNS ellenanyagok, RF (p, és vagy c) ANCA, vese/tüdő basalmembrán ellenes ellenanyag stb. vizsgálata indokolt. A serum angiotensin convertalo enzim (SACE) rutin vizsgálata sarcoidosis esetén nem ajánlott, mivel specificitása és sensitivitása alacsony. Ugyancsak alkalmatlan a SACE (a serum neopterinhez hasonlóan) a betegség lefolyásának követésére, vagy a terápia monitorozására. Hasznos és a terápiát befolyásoló parameter a serum Ca szint. Elsősorban differnciál-diagnosztikus jelentőséggel és terápiás következményei lehetneka tuberculin tesztnek, illetve a Quantiferon vizsgálat elvégzésének.
Légzésfunkciós vizsgálatok
Az ISTB-hez sorolt heterogén megbetegedések esetén különböző mértékű restrictív légzészavar mérhető. A tüdőtérfogatok csökkennek (a FEV1/FVC arány megtartott lehet) a CO diffúziós kapacitás, a tüdők rugalmassága csökken (kezdetben csak terheléskor, később nyugalomban is) és károsodik a gázcsere. Az előrehaladt esetek egy részében (sarcoidosis, Langerhans sejtes histiocytosis, ismeretlen eredetű tüdőfibrosis) légúti obstructio is regisztrálható. A légzésfunkciós vizsgálatoknak diagnosztikus értéke korlátozott.
A tüdőtérfogatok és a diffúziós kapacitás mérése jó közelítéssel felvilágosítást ad a megbetegedés kiterjedéséről. Nem igazolt egyértelműen, hogy terheléses vizsgálatokkal további (klinikailag relevans) információk nyerhetők. A fenti vizsgálatok egyike sem tud különbséget tenni az aktív gyulladásos folyamatok, illetve a fibrosis között. A megbetegedés lefolyásának, illetve a terápia eredményének monitorozásira a vitalkapacitás, diffúziós kapacitás, valamint a vérgázértékek megfelelő és egyszerű módszerek. Nem igazolt, hogy a terheléses vizsgálatok pontosabb adatokat szolgáltatnak. A légzésfunkciós vizsgálatok prediktív értéke alacsony.
Biopsziás módszerek
Annakellenére, hogy a korábbi ajánlásokjavasoltákaz ISTB diagnosisánakszövettani megerősítését, mind az USA-ban, mind pedig Angliában a betegek 8-33%-nál történt anyagvételi kísérlet. Napjainkban a biopsziás módszer kiválasztását a klinikai diagnosis valószínűsége, a szakmai/technikai adottságok, valamint a betegek általános állapota befolyásolja. A biopszia helyének kiválasztásában a képalkotó módszereknek jelentős szerepük van.
Bronchoalveolaris lavage (BAL)
A BAL több mint 20 éve alkalmazott klinikai vizsgálómódszer. Diagnosztikus szerepe lehet malignus tüdőfolyamatok (pl. lymphangiitis carcinomatosa), anorganikus porexpositio esetén, egyes gyógyszer-indukálta megbetegedéseknél és néhány ritka kórképnél (alveolaris proteinosis, Langerhans-sejtes histiocytosis esetén). Ugyancsak diagnosztikus értékű a vizsgálat obligat patogén kórokozók kimutatásánál (pl. Mycobacterium tuberculosis), vagy immunszupprimált betegek infekciója esetén (pl. HIV fertőzőtt betegek Pneumocystis jiroveci fertőzés esetén akár 90%-os diagnosztikus eredményesség is elérhető). Egyéb kórképekben a BAL-ban levő sejtek kisebb-nagyobb mértékben jellemzőek lehetnek az adott kórképre (illetve azok egyes gyulladásos szakaszaira). A 2008-ban Interstitialis tüdőbetegségek vonatkozásában kialakított guideline (British Thoracic Society, Thoracic Society of Australia and New Zealand, and Irish Thoracic Society) a BAL elvégzését a terápia megkezdése előtt javasolja, és a fentiekben is említett betegségeken túl, nem tartja szükségesnek azokban az esetekben, ahol a klinikai kép és HRCT idiopathiás pulmonalis fibrosisra típusos. Megemlíti viszont, hogy ha a klinikai kép és HRCT vizsgálat alapján a diagnosis bizonytalan, a BAL ismerete egyes kórképek diagnosztizálásában nagyobb magabiztosságot tesz lehetővé (hypersensitiv pneumonitis, sarcoidosis). Amikor a diagnosis kétes és a BAL megfontolandó, javasolják, hogy a beavatkozás olyan helyen történjen, ahol a mintavétel technikai és személyi feltételei, valamint a minta elemzéséhez szükséges szakértelem egyaránt adott. Mindenképpen ajánlják a BAL elvégzését azokban a betegekben, akiknél transzbronchialis biopsia is történik.
3. táblázat
BAL diagnosztikus értéke az interstitialis tüdőbetegségekben
| Neutrophil granulocyta | Lymphocyta | Eosinophil granulocyta | Egyéb | |
| Idiopathias interstitialis fibrosis | +++ | + | ++ | |
| Cryptogén organizálódó pneumonia | +++ CD4/CD8" | |||
| Sarcoidosis | +++ CD4/CD8 a | |||
| Asbestosis | ++ | Ferruginosus testek | ||
| Silicosis | Polarizált mikroszkóppal látható porszemcsék | |||
| Berylliosis | Pozitív lymphocyta transformációs teszt | |||
| Lipoid pneumonia | Macrophagokban zs rglobulusok (oil-red-O festés) Többmagvú óriássejtek | |||
| Rheumatoid arthritis | ++ | |||
| Hypersensitiv pneumonitis | +++ CD4/CD8" | + | ||
| Gyógyszer okozta ISTB | +++ | |||
| Diffúz alveolaris vérzés | Nagy számú erythrocyta, haemosiderin tartalmú macrophagok | |||
| Alveolaris proteinosis | PAS positiv granulumok | |||
| Malignitás (lymphangitis cc., BAC, lymphoma | Malignus sejtek |
Jelenleg nincs elegendő bizonyíték arra, hogy a BAL sejtek megoszlása értékelhető diagnosztikusus és/vagy prognosztikus jelentőséggel b rna.
Transbronchialis aspirációs tűbiopszia
A transbronchialis aspirációs tűbiopszia (TBNA) disszeminált kórképek esetén a megnagyobbodott nyirokcsomók vizsgálatára alkalmas. Leggyakrabban citológiai mintavétel történik, melynek eredménye (a malignus sejtek jelenlétét kivéve) csak a megbetegedés gyanúját veti fel.
Bronchoscopos tüdőbiopszia
A nem-sebészi mintavételek közül, a bronchoscopos tüdőbiopsziát (korábbi, ma is elterjedten használt elnevezése: transbronchialis tüdőbiopszia) alkalmazzuk leggyakrabban. Indikálásakor mérlegelni kell várható diagnosztikus eredményességet, az általános kockázatokat (a beteg általános állapota, kísérő betegségek stb.), valamint magának a beavatkozásnak a várható szövődményeit.
Morbiditása <3%, mortalitása <1%. Bronchoscopos tüdőbiopsia a választandó kezdeti eljárás minden olyan diffúz tüdőbetegségben, ahol a kis minták diagnosztikusak lehetnek, különösen ha a betegség bronchocentrikus lokalizációjúnak látszik. A HRCT a biopsia helyének kiválasztásában is segítséget nyújt. Diffúz pulmonalis betegségek esetén a bronchoscopos tüdőbiopsia diagnosztikus értékét a nemzetközi irodalomban eltérő módon adják meg (65-75%). Általában 4-6 feldolgozásra alkalmas tüdőminta vétele javasolt. Sarcoidosis gyanú esetén, az endobronchiális biopsiás mintán túl, bronchoscopos tüdőbiopsias minta vétele is ajánlott, mivel ez növeli a diagnosztikus eredményességét.
Nem javasolt a bronchoscopos tüdőbiopsia, mint kezdeti diagnosztikus eljárás interstitialis tüdőfibrozisra gyanús esetekben és ritka tüdőbetegség gyanúja esetén.
4. táblázat
Bronchoscopes tüdőbiopszia diagnosztikus értéke
| Diagnosztikus | Esetenként diagnosztikus | Ritkán diagnosztikus |
| Sarcoidosis | Langerhans sejtes histiocytosis | Ismeretlen eredetű tüdőfibrosis |
| Lymphangiitis carcinomatosa | Amyloidosis | Egyéb disszeminált kórképek |
| Alveolaris proteinosis | Wegener granulomatosis | |
| Bronchioloalveolaris carcinoma | Hypersensitiv pneumonitis | |
| Eosinophil pneumonia | Bronchiolitis obliterans organizing pneumonia (BOOP) | |
| Berylliosis |
Percutan tűbiopszia: Az ún. "vastagtű" (szövettani vizsgálatra alkalmas anyagvételt tesz lehetővé) alkalmazása interstitialis tüdőbetegségek esetén napjainkban teljesen kiszorult a klinikai gyakorlatból.
A sebészi mintavételt a kezelés megkezdése előtt javasolt elvégezni. Interstitialis pneumoniára gyanús esetekben, több, mint 1 biopsziás mintát kell venni, ami történhet egy lebeny több helyéről, de optimális a különböző lebenyekből vett minta. Többszörös, sok lebenyből történő tüdőbiopsia technikailag könnyebb VATS-al (Video Assisted Thoracoscopic Surgery), mint nyitott tüdőbiopsziával. Javasolt, hogy a mintavétel helyének megválasztása a HRCT-n látott elváltozások alapján történjen.
Irodalmi adatokkal egyezően a VATS vagy a thoracotomiás tüdőbiopszia mind a mai napig a legeredményesebb, legmegbízhatóbb biopsziás módszer ismeretlen eredetű interstitialis megbetegedés esetén, a diagnosis "gold standard"-ja. Szem ellenőrzése mellett, tetszőleges nagyságú anyag kivételét teszi lehetővé. Standard video-asszisztált thoracoscopiás tüdőbiopsia végzését fontolóra kell venni olyan ismeretlen okú interstitialis tüdőbetegségben szenvedő betegeken, akiknél a kórlefolyás subacut, tejüvegszerű opacitás látszik a HRCT-n, vagy idiopathiás pulmonalisfibrosisraatypusos a kép, tekintettel arra, hogy ezeka betegek reagálhatnaka terápiára. Kerülni kell a szükségtelen biopsiát, különösen ha az interstitialis pulmonalis fibrosis "klasszikus" radiológiai képe észlelhető. Egyéb szervek biopsziája (nyirokcsomó, bőr, máj, csont stb.) szisztémás és/vagy rosszindulatú megbetegedések esetén adhat definitív diagnosist.
1. ábra
Kivizsgálás algoritmusa
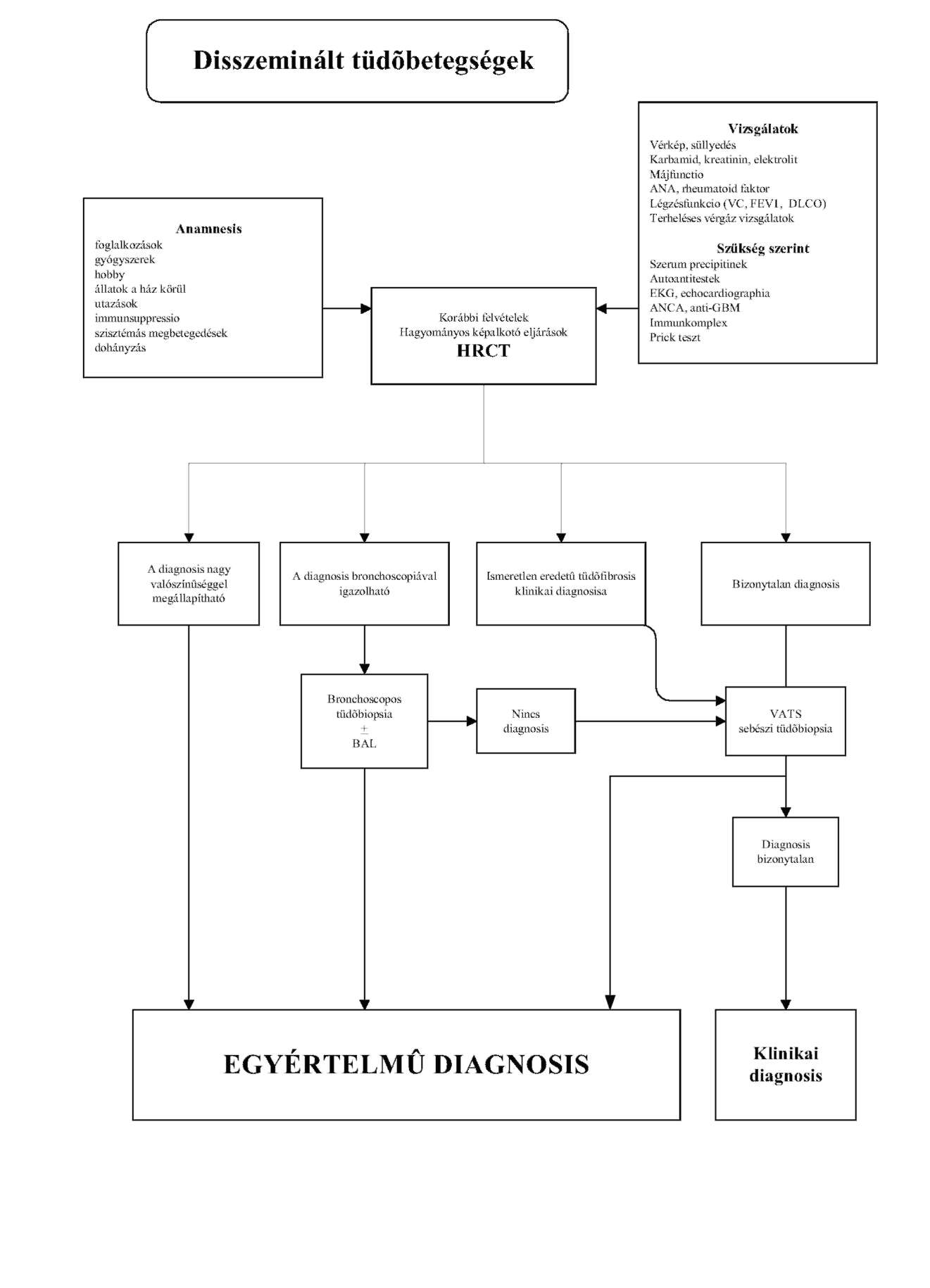
III. Kezelés
A sarcoidosis gyógyítása
A kórkép spontán gyógyulhat, esetleg stabilizálódhat. Kezelésének célja az alveolitis és a granulomaképződés megszüntetése, a tüdőfibrosis kialakulásának megelőzése. A panaszmentes I. stádiumú beteget egyáltalán nem szükséges kezelnünk. Löfgren szindromában nem szteroid gyulladásgátló, nagy ritkán 2-4 hetes szteroidadagolás javasolt. A II-III. stádium esetén a kezelést a panaszok intenzitása és a légzésfunkciós paraméterek romlása határozza meg. A panaszmentes és jó légzésfunkciójú beteget nem kell azonnal kezelni: 6-12 hónapos megfigyelés javasolt, amely alatt az esetek jelentős részében spontán regresszió várható.
Azonnali szteroid-adagolás szükséges progresszív, romló légzésfunkcióval, vagy panaszokkal járó parenchymainfiltráció, ill. extrapulmonalis, életfontosságú szervek érintettsége esetén (központi idegrendszer, szem, szív, vese, endokrin szervek). A kezelés 4 szakaszra bontható:
1. kezdő dózis (általában napi 0,6-0,8 mg/tskg prednizolon per os, 2.4-8 hét múlva ennek fokozatos csökkentése,
3. fenntartó kezelés (napi 10-15 mg prednizolon),
4. szteroidelvonás.
A klinikai tünetek javulása és a röntgenkép feltisztulása 4-8 héten belül várható, a szteroidra javuló esetekben a kúra időtartama 6-12 hónap.
Az optimális kezdő és fenntartó dózis, az adagolás időtartama prospektív, randomizált vizsgálatban máig nem tisztázott. Az inhalációs szteroid kezelés hatékonysága nem igazolt. A kezelés monitorozására együttesen a panaszok, a légzésfunkció és a mellkasröntgen ajánlható, az ún. aktivitási markerek (bronchoalveolaris lavage, SACE, gallium-scan stb.) megbízhatatlanok. A recidívák kezelése elveiben azonos az első kezeléssel. Az esetek 10-20 %-ában a panaszok még 2 év múlva is fennállnak, sokszor a légzésfunkció és a röntgenkép tovább romlanak. Az ilyen krónikus esetekben a szteroidelvonást relapsus követi, ezért minimális, napi 10-15 mg prednizolon dózisú fenntartó szteroidkezelés szükséges.
Methotrexat akut szteroid rezisztens kórformában monoterápiában, ill. szteroid dependens krónikus betegeknél a szteroid dózis csökkentése, a mellékhatások mérséklése céljából adható. Dózisa 10-15 mg hetente, a 6-8 hetenkénti fvs-szám csökkenés szükségessé teheti az dózis redukciót.
Krónikus refrakter tüdőbetegségben, ill. extrapulmonális sarcoidosisban szóbajön a maláriaellenes hydroxychloroquine(napi 2x200 mg), a TNF-release-t gátló pentoxyphyllin, vagy az anti-TNF antitest infliximab adása, bár ezek hatásosságát ellenőrzött vizsgálatokkal még kevéssé támasztották alá.
Az idiopathiás interstitiális pneumonitisek gyógyítása
Az ATS/ERS osztályozás elsősorban prognosztikus különbözőséget és eltérő gyógyíthatóságot jelent.
Az NSIP-ben szenvedő betegekegy részénél a szteroid monoterápia vagy a kombinált szteroid + immunosuppresszív
kezelés hatásos, más betegeknél viszont transzplantációra van szükség.
(Tüdőfibrózisban a hatásosság jelentheti a klinikai jellemzők javulását bizonyos idő elteltével, de jelentheti a túlélés növekedését is. Objektív javuláson azt értjük, ha 10 %-os FVC- (ill. TLC-), vagy 15 %-os diffúziós kapacitásemelkedést mérünk.)
A kombinált kezelés sémáját a 5. táblázat tartalmazza. A kezelést 12-18 hónapon keresztül kell folytatnunk, fél évnél korábban objektív javulás nem is várható. A gyógyszerek rossz tolerálhatósága, mellékhatások (leukopenia, infekciók, haemorrhagiás cystitis ) ezt nem mindig teszik lehetővé.
DIP-ben és RB/ILD-ben döntő a dohányzás abbahagyása, előbbiben azonban szteroidkezelés is szükséges. COP-ben 3-6 hónapos szteroidkezelés mellett a betegek l'-énél teljes radiológiai és légzésfunkciós regresszió várható; a perzisztáló, vagy recidíváló eseteknél viszont a szteroidot cyclophosphamiddal kell kiegészítenünk. Az AIP nagy dózisú szteroidot és gépi lélegeztetést igénylő forma.
A LIP (dysproteinaemia, vagy infekció nélküli) idiopathiás eseteiben egyértelmű a szteroidra való javulás.
A szövettanilag igazolt UIP/lPF-os betegek kórlefolyása szinte kivétel nélkül progresszív, gyógyszeres kezelésük hatástalan. A szteroidkezelés beidegzésszerű alkalmazása elfogadhatatlan, túlélési előnnyel nem jár, mellékhatásainak megjelenése dózis- és korfüggő. A szteroid-mellékhatások jelentősége a transzplantáció mérlegelésekor hatványozódik. A fibroproliferatio gátlása céljából adott interferon, colchicin, D penicillamin hatásossága kérdéses. Nagy dózisú szteroidot placebóval, vagy azathioprinnel kombinálva a két csoport között különbség nem volt, a cyclophosphamidról ugyanez mondható. Az N-acetylcysteint napi 3x600 mg dózisban szteroid + azathioprin kezelés mellé adva utóbbi szer nephrotoxicus hatása csökkent. A pirfenidon szintén antioxidáns, az akut (nem embolia, légmell, vagy infekció okozta) exacerbatiók kivédésében szerepe lehet.
UIP/IPF-ben a gyors progresszió miatt már a diagnózis pillanatában indokolt a tüdő transzplantáció felvetése, ill. a kivizsgálás megkezdése. A későbbieket illetően a 1/2, ill. egyéves légzésfunkciós trend döntő, mivel a stabil légzésfunkciójú, igen kisszámú beteg prognózisa a többiekétől élesen elválik. A dyspnoe fokozódása, a VC 10 %-os romlása, 40 % alatti diffúziós kapacitás a várólistára vétel mérlegelését indokolja. 65 évnél idősebb betegnél, társbetegségek, kifejezett szteroid mellékhatások, malignitás, nem megfelelő psychoszociális háttér, rossz vesefunkció esetén a műtét ellenjavallt.
5. táblázat
Kortikoszteroid (prednizolon vagy ekvivalens)
0,5 mg/tskg/die per os 4 héten át,
0,25 mg/tskg/die per os 8 héten át,
csökkentés 0,125 mg/tskg/die adagra plusz
azathioprin
2-3 mg/tskg/die,
a maximális orális dózis 150 mg/die,
az adagolást 25-50 mg/die dózissal kezdjük,
25 mg-onként emeljük 1-2 hetente
vagy cyclophosphamid
2 mg/tskg/die (minimum fél éven át), a maximális per os dózis 150 mg/die, az adagolást 25-50 mg/die-vel kezdjük, 1-2 hetente emeljük 25 mg-onként
IV. Rehabilitáció
Interstitialis tüdőbetegek rehabilitációja
A pulmonológiai rehabilitáció célja ebben a krónikus légzési betegcsoportban is a funkcióvesztés ütemének lassítása, a beteg mobilitásának, fizikai aktivitásának, önellátó képességének minél hosszabb időn át történő megtartása, az életminőség javítása. A rehabilitációs kezelések során mindvégig szem előtt kell tartani, hogy a beteg esetleg transzplantációs várólistára kerülhet, ezért a rehabilitációs programot úgy kell felépíteni, hogy az minden elemében a műtéti felkészítés céljait is szolgálja.
A rehabilitációs program legfőbb eleme a fizikai tréning. Az állapot-felmérést követően a munkát célszerű naponkénti két egyéni kezeléssel kezdeni, majd 4-5 nap után a beteg bevonható a csoportos foglalkozásba. A fizikai tréning különböző elemei (kerékpár, futószőnyeg, lépcsőjárás, felső végtagi edzés) legalább 45-60 perc időtartamot tegyenek ki naponta. Az ellenállással szemben végzett gyakorlatok hangsúlyozottan erősítő és kondicionáló hatásúak. A bemelegítés könnyű sétával, majd ütemes gyaloglással történhet. Ezt követi az alsóvégtagi tréning tornatermi kerékpáron a maximális terhelés 70-80 %-án. A felső végtagi és törzsizmok erősítése gumiszalaggal, könnyű (300-500 grammos) súlyzókkal és kézihajtókarral folyhat. A gyakorlatokismételt végzése növeli a betegek terheléstoleranciáját. A 6 perces járástávolság (6 MWD) jó információt adhat az elért eredményről, a beteg aktuális fizikai állapotáról. A fizikai tréning megkezdése előtt és a gyakorlás során is hasznos pulzusoximéterrel ellenőrizni a szaturációt. Amennyiben a beteg gyorsan deszaturálódik, vagy már a kezelés előtt is alacsonyabb (88-90%) értékeket mérünk, a terhelést célszerű oxigén adagolás mellett végezni.
A légzőgyakorlatokis fontos részét képezik a kezelésnek. Az alapvetően lassú, mély diafragmális légzést hangsúlyozó elemek a dyspnoe-érzékenység csökkenésének irányában hatnak. A légzőizom tréning minden esetben hasznos. A betegoktatás keretében a betegeket meg kell tanítani az inhalációs eszközök, nebulizer, személyi inhalátor előírás szerinti használatára. Ugyancsak fontos megtanítani az esetenként szükségessé váló non-invazív gépi légzéstámogatás (CPAP) technikáját is.
A rehabilitáció kiterjed az oxigénterápiával kapcsolatos kérdésekre, a beteg segédeszközökkel történő ellátására is. Ha a beteg állapota tartós oxigénterápiát indokol, különösen a fiatalabb, transzplantációra esélyes személyek esetében, folyékony oxigéntartály felírása célszerű, mivel ehhez az eszközhöz portábilis palack is tartozik, amelynek használatával a mobilitás, a fizikai aktivitás hosszabb ideig fenntartható.
A betegség jellegéből, lefolyásából, prognózisából adódóan gyakran lehet szükség pszichológus, pszichiáter segítségére. A pszichiátriai problémák (depresszió, reményvesztés stb.) egyik oka lehet, hogy az interstitialis tüdőbetegségben szenvedők rendszerint fiatalabbak, mint például a COPD-sek, és a betegség progressziójának a tempója is gyorsabb. A pszichológus segíthet a fentebb említett hordozható oxigéntartály által nyújtott előnyök elfogadásában, vagyis annak a helyzetnek a megfelelő feldolgozásában, hogy a vállon hordható oxigénpalack nem szégyellni való, ugyan olyan segédeszköz, mint a szemüveg, vagy a támbot, amivel fenntartások nélkül lehet bevásárolni, vagy moziba, színházba menni.
Jelentősebb testsúlyvesztés esetén dietetikus bevonására van szükség. A rehabilitációs programban részt vevő betegek fizikai teljesítményét naponta dokumentáljuk. A rehabilitációs team hetente értékeli a pacienssel kapcsolatos adatokat, és meghatározza a további tennivalókat.
V. Gondozás
VI. Irodalomjegyzék
1. American Thoracic Society/European Respiratory Society International Multidisciplinary Consensus Classifification of Idiopathic Interstitial Pneumonias. Am. J. Respir. Crit. Care Med. 165:277-304,2002.
2. Baughman, R.P., Lower, E.E: Novel Therapies for Sarcoidosis. Sem. Resp. Crit. C. Med.. 28:128-133,2007.
3. Diffuse Parenchymal Lung Disease. Eds. Costabel, U., du Bois, R.M., Egan. J.J. Karger, Basel, 2007.
4. Diagnostic Imaging. Chest. Gurney, J.W. et al. Amirsys Inc. Salt Lake City, Utah 2006.
5. Diffuse Lung Diseases Clinical Features, Pathology, HRCT. Eds. Maffessanti M. and Dalpiaz. G. Springer, Milan, Berlin, Heidelberg, New York, 2007.
6. Hunninghake, G.W., és mtsai. Utility of a lung biopsy for the diagnosis of idiopathic pulmonary fibrosis Am. J. Respir. Crit. Care Med. 164:193- 196, 2001.
7. Interstitial lung disease guideline: the British Thoracic Society in collaboration with the Thoracic Society of Australia and New Zealand and the Irish Thoracic Society. Thorax 63: (Supplement V.) v1-v58,2008.
8. Katzenstein, A.L. Idiopathic pulmonary fibrosis: to biopsy or not to biopsy. Editorials. Am. J. Respir. Crit. Care Med. 164:185-189, 2001.
9. King, T.E., Costabel, U., Cordier, J-F: Idiopathic pulmonary fibrosis: diagnosis and treatment. Am. J. Respir. Crit. Care Med. 161:646-664, 2000.
10. Martinez, F.J., Keane, M.P. Update in diffuse parenchymal lung diseases 2005. Am. J. Respir. Crit. Care Med. 173:1066-1071,2006.
11. Noth I., FJ.Martinez: Recent Advances in Idiopathic Pulmonary Fibrosis. Chest.. 132:637-650,2007.
12. Paramothayan S., T. Lasserson: Treatments for pulmonary sarcoidosis. Resp. Med. 102:1-9,2008.
13. Riley, D.J., Costanzo, E.J. Surgical biopsy: its appropriateness in diagnosing interstitial lung disease. Curr Opin Pulm Med 12:331-336, 2006.
14. Schwarz, M.I.,. KingT.E. Eds. Interstitial Lung Disease. B.C.Decker Inc., Hamilton, 2003.
15. The diagnosis, assessment and treatment of diffuse parenchymal lung disease in adults. British Thoracic Society Recommendation. Thorax: (Suppl. 1.) 54:1-30,1999.
16. Verbeken E.K. Classifying interstitial lung diseases in a fractal lung: a morphologist's view "anno Domini 2000". Eur. Respir. J.; (Suppl. 32) 18:107-113, 2001.
17. Walter, N., H.R.Collard,T.E. King Jr.: Current Perspectives on the Treatment of Idiopathic Pulmonary Fibrosis. Proc. Am. Thorac. Soc. 3:330-338, 2006.
18. Wells, A.U., Hogaboam, C.M. Update in diffuse parenchymal lung disease 2006. Am. J. Respir. Crit. Care Med. 175:655-660, 2007.
19. Woda, B.A. Hypersensitivity pneumonitis: an immunopathology review. Arch. Pathol. Lab Med 132:204 205,2008.
20. Zsiray M.: A mellkasi sarcoidosis kortikoszteroid kezelése. Med.Thorac. 54:172-177,2001.
21. Zsiray M.: Az ismeretlen eredetű tüdőfibrózis gyógyítása. Med.Thorac.. 58:136-140,2005.
A szakmai protokoll érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai irányelve
A krónikus obstruktiv légúti betegség
(chronic obstructive pulmonary disease - COPD) diagnosztikájáról és kezeléséről (1. módosított változat)
Készítette: a Tüdőgyógyászati Szakmai Kollégium
1. Bevezetés
1.1. A szakmai irányelv elkészitésének indoka, előzmények
A krónikus obstruktiv tüdőbetegség (a továbbiakban, a "chronic obstructive pulmonary disease" elnevezésből származtatott rövidés: COPD) a krónikus betegségek körében kiemelkedő jelentőségű: előfordulása tömeges, az általa okozott mortalitás magas az évtizedeken át folyó kezelés drága.
Az 1994-ben közölt Lung Health Study (6000 beteg, 5 éven át tartó megfigyelése) fordulópont a COPD szemléletében, amelynek következményeként a World Health Organisation (WHO) és a National Heart, Lung and Blood Institute (NHLBI-USA) szakértői 2001. áprilisában közzétettéka COPD diagnosztikájával és kezelésével kapcsolatos irányelveiket (Global Initiative for Chronic Obstructive Lung Diasease - GOLD)1.
A Tüdőgyógyászati Szakmai Kollégium hasonló irányelvei már 2000-ben megjelentek, és számos, lényeges ponton eltértek az előbbi, nemzetközi ajánlástól2. A GOLD új, 2003-ban közzétett szövege azonban már példaként szolgált a "nemzeti" COPD diagnosztikus és terápiás irányelvek szerkesztésénél 3 . A legutóbb, 2004-ben közölt magyar diagnosztikus és terápiás ajánlás a 2003. november 21-22.-én, Budapesten megrendezett COPD Konszenzus Konferencia megállapitásain alapult és a GOLD (2003) szövegének figyelembevételével jelent meg 4. A jelen irányelv is a GOLD (GOLD 2006) ajánlásai, valamint a hazai diagnosztikus és kezelési hagyományok alapján megújitott szöveg 5 .
Az alább következő diagnosztikus és terápiás ajánlások különböző erejű bizonyitékokon alapulnak, amelyeket - az állitás ill. javaslat végén, zárójelben - A, B, C, D betűkkel -jelölünk. A bizonyitékok forrásai a következők:
- A: magas esetszámú randomizált és ellenőrzött vizsgálatok
- B: az előbbinél kisebb betegszámon alapuló randomizált és ellenőrzött vizsgálatok (az adatok post hoc, alcsoport-elemzésen vagy meta-analizisen alapuló) eredményei
- C: nem-randomizált, nem-ellenőrzött klinikai vizsgálatokon/megfigyeléseken alapuló eredmények
- D: szakértő testület egyeztetett véleménye
1.2. A szakmai irányelv célja, érvényességi területe
A jelen irányelv a tüdőgyógyászati szakellátás, alapellátás és sürgősségi betegellátás számára szerkesztett részletes diagnosztikus és kezelési útmutatás.
2. A krónikus obstruktiv tüdőbetegség (chronic obstructive pulmonary disease-COPD) definiciója, epidemiológiája és kórtana
2.1. A krónikus obstruktiv tüdőbetegség (COPD) definiciója
A COPD megelőzhető és kezelhető betegség több extrapulmonális következménnyel, amelyek a tüdőbetegség súlyosságát és kimenetelét befolyásolják.
A COPD-t lassan és fokozatosan súlyosbodó funkciózavar (emelkedő bronchiális áramlási ellenállás) jellemzi, amely túlnyomóan irreverzibilis, de hörgtágitók vagy más kezelés hatására mérséklődhet az obstrukció. A légúti áramlási ellenállás-fokozódás a tüdő, szövetkárositó gázok és részecskék inhalációjának hatására kialakuló, kóros gyulladásos reakciójának a következménye5.
Világszerte a dohányzás legfontosabb kockázati tényező a betegség kialakulásában, de a fejlődő világ számos országában a fa (vagy más, a biomassza körébe tartozó anyagok) égetésének jelentősége felülmúlja a dohányzás hatását.
A krónikus obstruktiv bronchitisz vezető tünete a legalább két egymást követő évben, évente legkevesebb három hónapon át fennálló produktiv köhögés, amely nem sziv (pl. balkamra-elégtelenség) vagy más tüdőbetegség (tüdődaganat, hörgőtágulat stb.) következménye .
Hiperszekréció azaz éveken át fennálló produktiv köhögés légúti funkciózavar nélkül is előfordulhat (egyszerű krónikus bronchitis). A nyákmirigy hiperplázia ugyanis főként a centrális hörgők falában alakul ki, míg az obstrukció helye elsősorban a periférikus, un. kis légútak területe. Az egyszerű krónikus bronchitisz nem kezelendő ugyan, de a későbbi bronchiális obstrukció kialakulása szempontjából, a szakértőkegy része, magas kockázatú csoportnak tartja. Az emfizémát a terminális broncholustól disztálisan elhelyezkedő légterek túltágulása és faluk pusztulása (bullózus parenchyma-degeneráció) jellemzi és mindez nem tüdőfibrózis kisérő jelensége. A légúti obstrukció két összetevője tehát a perifériás ("kislégúti") hörgőszükület és a légutak támasztó környezetének pusztulása, az emfizémás szövet-destrukció. Ez utóbbi, jellegzetes un. asszimmetrikusobstrukciót okoz: az erőltetett kilégzési áramlási sebesség sokkal alacsonyabb a belégzési áramlásnál (2.1. ábra).
A krónikus obstruktiv bronchitisz és emfizéma kórfejlődése eltérő ugyan, de általában egymáshoz társulnak és egy adott betegben a bronchitiszes vagy emfizémás elem dominanciája megállapitható.
A COPD leggyakrabban évtizedeken át dohányzó, középkorú személyeket érint, igy ők más, a dohányzással és az öregedéssel összefüggő társbetegségek tüneteit is mutatják6. A COPD önmagában is számos extrapulmonális következménnyel jár: pl. testsúlycsökkenéssel, vázizom-diszfunkcióval, de a COPD-csoportban a myocardiális infarctus, angina, osteoporosis, csonttörések, mély légúti fertőzések, depressio, glaucoma, diabetes, anaemia kialakulása is gyakoribb.
2.1.1. A COPD súlyossági beosztása a spirometriás mérés alapján
Aspirometriás mérés meghatározójelentőségű a COPD okozta légúti funkciózavar súlyosságának meghatározásában. A 2.2. ábrán látható, hogy a légúti obstrukció fennállásának diagnózisa a FEV1/FVC <0,70 hányadoson, míg az obstrukció súlyossága a referencia-FEVi-értéktől való eltérésen alapul. A rögzitett FEVi/FVC-hányados alkalmazását több kritika érte (pl. idős korban igy hamisan kóros funkciócsökkenést, enyhe COPD-t diagnosztizálhatunk, míg fiatal csoportokban gyakoriak a "fals-negativ" eredmények, ezért a kóros és egészséges eredmény elkülönitését, több szakértő, a referencia érték alsó határvonalához hasonlitott FEVi-értékre alapozná). A ma elfogadott álláspont szerint, nagy csoportokon végzett mérésekalapján,a rögzitett, 0,70 alatti FEVi/FVC-hányados nagy biztonságal különiti el az obstruktiv beteget az egészségestől 7 .
A spirometriás mérést hörgtágitó inhalációja (leggyakrabban 400 μg salbutamol) után kell értékelni, hogy a légúti funkció variabilitása a legkisebb legyen, az irreverzibilis obstrukció fennállását biztonsággal megállapithassuk. A korábbi irányelvekkel ellentétben, a különböző hörgtágitókkal vagy kortikoszteroidokkal végzett reverzibilitási próbát nem javasolják sem a COPD-asztma bronchiale elkülönitésére, sem a tartós farmakoterápiás hatások becslésére.
Az a gyakran hangoztatott megállapitás, hogy a krónikusan dohányzók csupán 15-20%-ánál alakul ki progressziv tüdőfunkcióvesztést okozó COPD félrevezető8. A dohányfüst-expozició különböző szintjein jóval nagyobb arányban alakul ki kóros funkciócsökkenés, mint azt a Fletcher-Peto diagram alapján feltételeznénk. A tüdőfunkció-vesztés "egyéni útjai" igen eltérőek és végül, a betegek többsége kardiovaszkuláris betegségek, hörgőrák, a súlyos COPD eseteiben légzési elégtelenség következtében hal meg 9.
I. súlyossági csoport: enyhe COPD- (FEVi/FVC < 0,70 : FEVi > a referencia-érték80%-a) krónikus köhögés és köpetürités kisérheti, de nem mindig
II. súlyossági csoport: közepesen súlyos COPD-(FEVi/FVC < 0,70 : 50%< FEVi < 80%)
a fizikai terhelés közben fellépő légszomj jellemző tünet, míg köhögés és köpetürités nem mindig jelentkezik ebben a súlyossági csoportban (általában az "effort-dyspnoe" vagy az első exacerbáció miatt keresi a beteg az orvos segitségét)
III. súlyossági csoport: súlyos COPD - (FEV1/FVC < 0,70 : 30% < FEV1 < 50%)
a fizikai terhelhetőség további csökkenése, ismétlődő exacerbációk, romló életminőség
IV. súlyossági csoport: nagyon súlyos COPD - (FEV1/FVC < 0,70 : FEV1 < 30% vagy a FEV1 < 50% ugyan, de a beteg krónikus légzési elégtelenség, cor pulmonale tüneteit mutatja)
A krónikus légzési elégtelenség tehát minősiti a COPD súlyosságát, a légúti funkciócsökkenéstől függetlenül is. A légzési elégtelenség definiciója: PaO2 < 8,0 kPa (60 Hgmm) +/- PaCO2 > 6,7 kPa (50 Hgmm).
2.1.2. COPD és asztma bronchiale
Az asztma bronchiale - definiciójának megfelelően - reverzibilis légúti obstrukciót jelent és az asztmás gyulladás jellege is más, mint a bronchiális inflammáció COPD-ben (2.3. ábra).
Olyan betegek esetében, akiknél a légúti funkciózavar megszüntethető, elvethető a COPD-diagnózis. Ugyanakkor, a krónikus asztmás betegek egy részénél a légúti funkciózavar reverzibilitása - a COPD-hez hasonlóan - csupán részleges, ezért a COPD-asztma elkülönitése nehéz (főként időskori intrinsic asztmában).
Az obstruktiv bronchitis-emfizéma (COPD) tünetegyüttes időszakosan asztmás jellemzőket mutathat (vagy a COPD asztma bronchialéhoz társulhat).
2.2. A COPD prevalenciája, mortalitása, a betegség társadalmi költségei
A COPD prevalenciájára vonatkozó adatok, a betegség diagnosztikus kritériumainak, a légúti funkciómérés módszereinek eltérései miatt nagy eltéréseket mutatnak.
Az eddig közölt, igényes módszerekkel nyert, adatok alapján megállapitható, hogy a COPD a felnőtt lakosság 4 - 7 %-át érinti a fejlett, ipari országokban.
A PLATINO-vizsgálat azonban (the Latin American Project for the Investigation of Obstructive Lung Disease), az ATS iránymutatását követő spirográfiás mérések alapján, Dél-Amerika 5 nagyvárosában, a 60 évnél idősebb lakosság körében 18,4-32,1% között találta a betegség előfordulását11.
Magyarországon pontos epidemiológiai adatok nincsenek, de a becsült betegszám 400 - 500 000 lehet (a tüdőgondozókban 2007-ben nyilvántartott 109 999 betegszám 4-5 szöröse). A hazai nyilvántartás főként a súlyos, rendszeresen kórházi kezelést igénylő eseteket tartalmazza, míg az enyhébb, a megelőző ill. hörgtágitó terápia szempontjából igéretesebb többség ismeretlen azaz nem kezelt és gondozott beteg 12.
A COPD a halálokok rangsorában jelenleg világszerte a 4.-6. helyen áll (az USA-ban a 45 évnél idősebbek csoportjában
a 4. vezető halálok) 2020-ra, várhatóan, a COPD a 3. leggyakoribb halálokká válik a világon13.
A leggyakrabban halált okozó betegségek közül a COPD mortalitása nő az Egyesült Államokban, miközben például a
kardiovaszkuláris betegségek okozta halálozás csökken (ugyanitt 1970 és 2000 között a nők, COPD következtében
regisztrált, halálozása folyamatosan nőtt) 14. Európában a COPD mortalitása több országban csökken (egy 2000 -ben
közzétett WHO statisztika szerint a 35-74 éves férfiak COPD miatti halálozási statisztikájában 78%ooo-kel
Magyarország az első, a nők csoportjában a 8-10-ik helyen áll, a tavalyi KSH nyilvántartása szerint a COPD mortalitása
Magyarországon 45 %ooo, amely az Európai Közösség mortalitás-adataival összehasonlitható érték)12,15,16.
A COPD kezelése drága: kb. az asztma bronchiale terápiájának 2,5-szerese, ugyanakkor a jelenlegi farmakoterápiás lehetőségek hatásfoka gyenge, igy ebben a betegcsoportban a megelőzés különösen kiemelkedő fontosságú.
A fejlett országokban a COPD exacerbációinak kezelése jelenti a legnagyobb költséget. Az Európai Unióban a légzőszervi betegségek közvetlen költségei az egészségügyi össz-kiadás 6%-át emésztik fel, ezen belül a források
56%-a a COPD ellátásával kapcsolatos, túlnyomóan kórházi költség. Ennek csökkentését, számos országban, úgy próbálják elérni, hogy az ápolást, oxigén-kezelést, légzésrehabilitációt és még a gépi légzéstámogatást is, a beteg otthonában szervezik meg 17.
2.3. A COPD kórtana
2.3.1. Kockázati tényezők
A COPD poligenetikus betegség, de a genetikus prediszpozició részleteit alig ismerjük. A súlyos, örökletes a1-antitrypsin hiánnyal járó betegség kivétel. Az enzimhiány recessziven öröklődik, korai, panlobuláris emfizémát okoz, dohányzó/nem-dohányzó, főként észak-európai eredetű betegekben. A tüdőfunkció-csökkenés, betegenként azonos mértékű enzimhiány esetén is, igen eltérő lehet, amely a környezeti tényezők jelentőségére utal 18. A COPD kialakulásának öröklődő kockázatát dohányzó ikerpárok vizsgálatával is bizonyitották. Újabb asszociációs vizsgálatokkal (TGF-R1, TNF-a stb.) a COPD kialakulásában jelentős gén-variánst egyelőre nem sikerült azonositani19. A dohányfüst messze a legfontosabb kockázati tényező a COPD kialakulásában: a tartósan dohányzók légúti tünetei, funkcionális eltérései (az évi FEV1-vesztés sebessége) egyértelműen súlyosabbak, mint a nem-dohányzó kontroll-csoporté 20. A dohányzás kezdete (életkor), a dohányzás intenzitása (cigaretta csomag-év) prognosztikus jelentőségűek a kialakuló COPD súlyosságának szempontjából (meghatározzák a mortalitást is)21. Foglalkozási inhalációs kárositó anyagok játszanak szerepet a COPD eseteinek 10-20%-ában. A világon kb. 3 milliárd ember főz/fűt fa és szén (vagya biomassza más változatainak) égetésével. Ázsiában, Afrikában és a Közel-Keleten. Az előbbi, lakótéren belüli inhalációs ártalom fontos tényező a COPD kialakulásában (Kelet-Ázsiában a dohányzás is rendkivül intenziv) 22,23.
A fejlett, ipari országokban a COPD prevalenciája, megközelitően, azonos a nemek között24.
Az alacsony szociális/gazdasági státusz a COPD kialakulásának magas kockázatát jelenti. Egyelőre nem tudjuk, hogy ez a lakótéren kivüli/belüli inhalációs szennyezés, esetleg a légúti infekciók gyakoriságában vagy a táplálkozás minőségében jelentkező különbségekből adódik25.
2.3.2. Pathogenesis
A dohányfüst és más belégzett kárositó anyagok a légútak és tüdőszövet gyulladásos reakcióját okozzák. A COPD esetében a gyulladásos válasz fokozott, amely a tüdőparenchyma pusztulását (emfizéma) és a normális helyreállitó (gyógyulási) funkció gátlásával, kislégúti fibrózist, következményes bronchiális szűkületet okoz. Mindennek következménye progressziv légúti obstrukció, dinamikus hiperinfláció ("air trapping"), kezdetben csak fizikai terhelés alatt, később nyugalomban is fellépő dyspnoe.
A 2.4. ábrán a jellegzetes gyulladásos változások láthatók a légzőrendszer különböző területein. A gyulladásos mediátorokszéles köre toboroz különböző gyulladásos sejteket a keringésből, amelyek proinflammatorikuscitokinek forrásai. Az egyre fokozódó gyulladás következménye végül, növekedési faktorok közreműködésével, szerkezeti átépülés a hörgőfalban és a tüdőparenchymában (remodeling). A gyulladásos és szerkezeti eltérések annál kifejezettebbek, minél előrehaladott a betegség. A progrediáló gyulladást és szöveti destrukciót, hosszabb dohányfüst-expozició után (ezt > 15 csomag/évre becsülik), a dohányzás megszakitása sem mérsékeli. A COPD-t tehát a normális gyulladásos válasz kóros fokozódása jellemzi. A kórosan reagáló személyeket nevezte 1977-ben C. Fletcher és R. Peto "dohányfüstre érzékenyeknek" (susceptible to smoke) 25. A fokozott gyulladásos reakció okát ma sem ismerjük. Feltételezhetően genetikus prediszpozició különiti el, a krónikus dohányzók csoportján belül, a súlyos COPD jelöltjeit (15-20%). Nem-dohányzók körében is kialakulhat COPD (a betegek " 5-10%-a), ennek okát sem ismerjük 26.
A kórosan fokozott gyulladásos reakciót tovább súlyosbitja az oxidativ stressz és a proteáz-antiproteáz egyensúly zavara COPD-ben.
Az oxidativ stressz biomarkerei (hydrogenperoxid, isoprostan) kórosan magas koncentrációban mutathatók ki a kilégzett levegőben, az indukált köpetben és perifériás vérben is COPD-ben (szintjük tovább emelkedik a betegség akut exacerbációiban). A cigarettafüst aktivált makrofágokból, neutrofil sejtekből oxidánsok kiválasztását indukálja27. Az oxidativ stressz következményei a tüdőben: gyulladásos gének, aktivációja, antiproteázok inaktiválása, a plazma-exsudatio és a bronchiális nyákelválasztás fokozása. Az oxidativ stressz eredményezi a histon deacetiláz-aktivitás csökkenését a COPD-s betegek tüdőszövetében (és dohányzó asztmásokében is ) és ez magyarázhatja a kortikoszteroidok mérsékelt gyulladáscsökkentő hatását az előbbi betegcsoportokban 28. Bizonyitott, hogy a kötőszövetet lebontó proteázok és az ezt gátló antiproteázok közötti egyensúly megbomlott COPD-ben. Számos, inflammációs és epitheliális sejtből származó, proteáz szintje emelkedett (2.5. ábra). Az elasztin a kötőszövet fontos szerkezeti eleme, amelynek, proteáz-mediálta, destrukciója eredményezi az irreverzibilis emfizémás parenchyma-degenerációt29.
Az asztma bronchiale és COPD a légútak krónikus gyulladásos betegségei, de a gyulladásos sejtek, mediátorok, valamint a tünetek és a terápiás lehetőségek tekintetében jelentősen különböznek. A súlyos, részben irreverzibilis légúti obstrukciót mutató asztmás és a COPD-s légúti gyulladás hasonló30 (2.6. ábra).
A COPD súlyos formáiban gázcserezavar alakul ki: a domináló emfizémát progrediáló PaO2-csökkenés ("parciális légzési elégtelenség"), míg a kislégúti obstrukció és emfizéma kevert klinikai formáit a diffuziós felület csökkenése, ventillációs/perfuziós (Va/Q) egyensúlyzavar, légzőizom-kifáradás okozta hypoxaemia és hypercapnia ("globális légzési elégtelenség") jellemzi.
A COPD kórfejlődésének végstádiumában alakul ki enyhe, mérsékelten súlyos pulmonális hipertenzió, amelynek háttere a kis arteriolák, hypoxaemia okozta, konstrikciója, vaszkuláris remodeling (intima hyperplasia, később simaizom hypertrophia/hyperplasia) és a pulmonális érkeresztmetszet csökkenése (főként emfizémában)3i. A COPD akut exacerbációjakor a gyulladás intenzitásának fokozódik: a köpetben és hörgőfalban nő az neutrofil (ritkábban az eozinofil) sejtek száma, emelkedik a TNF-a, LTB4, IL-8, valamint az oxidativ stressz biomarkereinek koncentrációja32. Mindennek következménye a légúti obstrukció, a dinamikus hiperinfláció, a hypoxaemia és a következményes dyspnoe súlyosbodása.
Irodalom
1. Anthonisen NR, Connett JE, Kiley JP és mtsai.: Effects of smoking intervention and the use of an inhaled anticholinergic bronchodilatoron the rate of decline of FEVi. The Lung Health Study. JAMA: 1994: 272:1497-1505.
2. A krónikus obstruktiv légúti betegség (chronic obstructive pulmonary disease - COPD) diagnosztikája és kezelése. A Tüdőgyógyászati Szakmai Kollégium ajánlása. Medicina Thoracalis: 2000:53:1-11.
3. Global Initiative for Chronic Obstructive Lung Disease. Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease, updated 2003. National Institutes of Health, National Heart, Lung, and Blood Institute: 2003. (www.goldcopd.com)
4. COPD Konszenzus Konferencia. Program és előadások. Hotel Sofitel Atrium Hotel, Budapest 2003. november 21-22. Kézirat: 2003.
5. Global Initiative for Chronic Obstructive Lung Disease. Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease - 2006. MCR Vision Inc.
6. Soriano JB, Visick GT, Muellerova H és mtsai: Patterns of comorbidities in newly diagnosed COPD and asthma in primary care. Chest 2005:128(4): 2099-107.
7. Johannessen A, Lehmann S, Omenaas ER és mtsai: Post-bronchodilator spirometry reference values in adults and implications for disease management. Am J Respir Crit Care Med 2006: 173(12): 1316-25.
8. Rennard S,Vestbo J: COPD: the dangerous underestimate of 15%. Lancet 2006:367:1216-9.
9. Mannino DM, Doherty DE, Buist SA: Global Initiativeon Obstructive Lung Disease (GOLD) classification of lung disease and mortality: findings from the Atherosclerosis Risk in Communities (ARIC) study. Respir Med 2006:100(1): 115-22.
10. Thomson NC, Chaudhuri R, Livingston E: Asthma and cigarette smoking. Eur Respir J 2004: 24(5): 822-33.
11. Menezes AM, Perez-Padilla R,Jardim JR és mtsai: Chronic obstructive pulmonary disease in five Latin American cities (the PLATINO study): a prevalence study. Lancet 2005: 366(9500): 1875-81.
12. A pulmonológiai intézmények 2007. évi epidemiológiai és működési adatai. Az Országos Korányi Tbc és Pulmonológiai Intézet kiadása, 2008.
13. Murray CJL, Lopez AD: Evidence-based health policy - lessons from the Global Burden of Disease Study. Scince 1996: 274: 730-733.
14. Jemal A, Ward E, Hao Y és mtsai: Trend sin the leading causes of death in the United States, 1970-2002. JAMA 2005: 294(10): 1255-9.
15. Chapman KR, Mannino DM, Soriano JB és mtsai: Epidemiology and costs of chronic obstructive pulmonary disease. Eur Respir J 2006: 27(1): 188-207.
16. World Health Organization. World Healt Report, Geneve, 2000.
17. FaurouxB, Howard P, MuirJF: Home treatment forchronic respiratory insufficiency: the situation in Europein 1992. Eur Respir J 1994: 7: 1721-6.
18. StollerJK,Aboussan LS: Alpha1-antitrypsin deficiency. Lancet 2005: 365(9478): 2225-36.
19. Wu L,Chau J, Young RPes mtsai: Transforming growth factor-betal genotype and susceptibility to chronic obstrctive pulmonary disease. Thorax 2004:59(2): 126-9.
20. US Surgeon General. The health consequences of smoking: chronic obstructive pulmonary disease. Washington,D.C.: US Department of Health and Human Services: 1984.
21. Smith CA, Harrison DJ: Association between polymorhysm in gene for microsomal epoxide hydrolase and suspectibility to emphysema. Lancet 1997:350(9078): 630-3.
22. Ezzati M: Indoor air pollution and health in developing countries. Lancet 2005:366(9480): 104-6.
23. Boman C, Forsberg B, Sandström T: Shedding new light on wood smoke: a riskfactor for respiratory health. Eur Respir J 2006: 27(3): 446-457.
24. National Heart, Lung and Blood Institute. Morbidity and mortality chartbook on cardiovascular, lung and blood diseases. Bethesda, Maryland: US Department of Health and Human Services, Public Health Service, National Institutes of Health, 2004. http://www.nhlbi.nih.gov/resources/docs/cht-book.htm.
25. Fletcher C, Peto R:The natural history of chronic airflow obstruction. BMJ 1977:1:1645-1648.
26. Birring SS,Brightling CE,Bradding P esmtsai: Clinical,radiologic,and induced sputum features ofchronicobstructive pulmonarydisease in nonsmokers: a descriptive study. Am J Respir Crit Care Med 2002: 166(8): 1078-83.
27. MacNee W: Oxidative stress and lung inflammation in airways disease. Eur J Pharmacol 2001:429(1-3): 195-207.
28. Ito K, Ito M, Elliot WM es mtsai: Decreased histone deacetylase activity in chronic obstructive pulmonary disease. N Engl J Med 2005: 352(19): 1967-76.
29. Barnes PJ: Mediators ofchronic obstructive pulmonarydisease. Pharmacol Rev 2004: 56(4): 515-48.
30. Thompson NC, Chaudhuri R, Livingston E: Asthma and cigarette smoking. Eur Respir J 2004: 24(5): 822-33.
31. Barbera JA, Peinado VI, Santos S: Pulmonary hypertension in chronic obstructive pulmonary disease. Eur Respir J 2003: 21(5): 892-905.
32. DrostEM,Skwarski KM,Sauleda Jesmtsai: Oxidativestressand airwayinflammation in severe exacerbations of COPD. Thorax 2005: 60(4): 420-8.
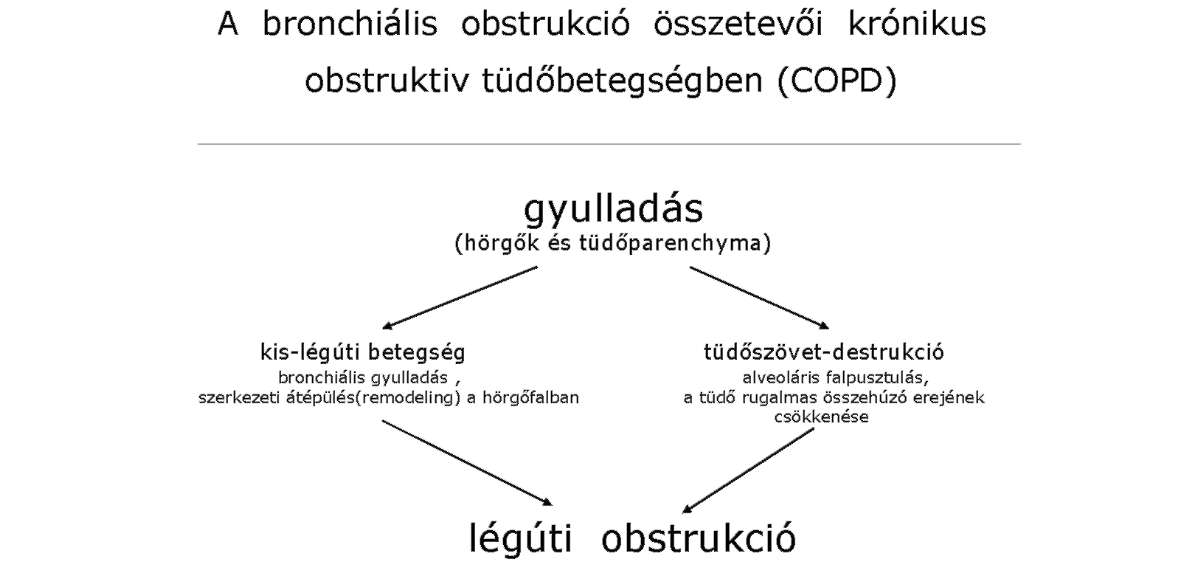
2.1. ábra
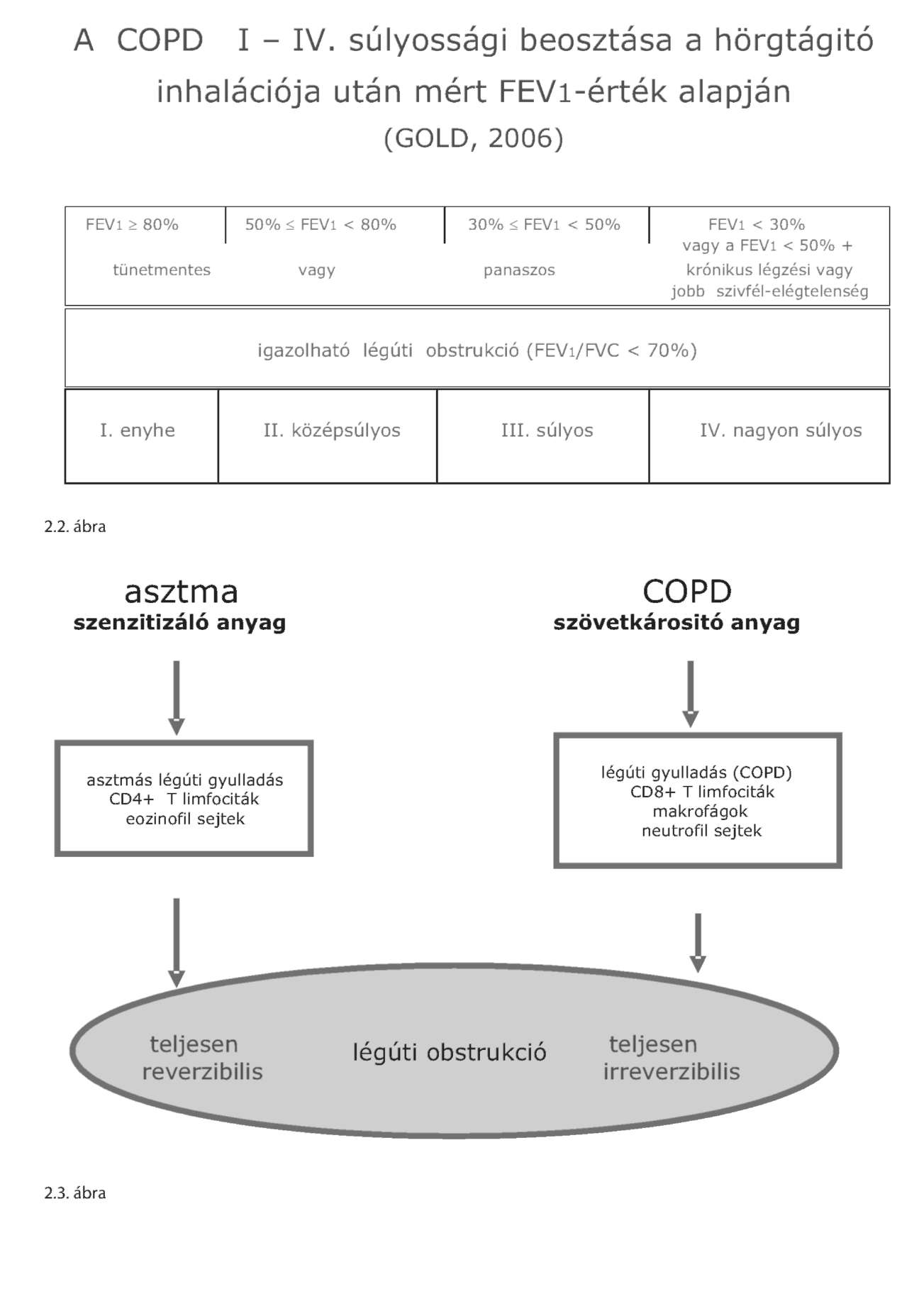

asztma bronchiale és krónikus obstruktivtüdőbetegség (COPD): hasonlóságok és különbségek
| COPD | asztma bronchiale | súlvos asztma | ||||
| sejtek | neutrofilek ++, makrofágok +++, | eozinofilek ++, makrofágok + , | neutrofilek +, makrofágok+ + . | |||
| CD8+ sejtek | CD4 sejtek (Th2) | CD4+ sejtek (Th2), CD8+ sejtek | ||||
| fő mediátorok | IL-S, TNFa, IL-ip, IL-6 NO + | eotaxin IL-4, IL-5, IL-13, NO +++ | IL-8, IL-5, IL-13, NO + + | |||
| a gyulladás helye | perifériás légutak, parenchyma. | főleg a nagy légutak | főként a perifériás légutak | |||
| tüdőé rek | ||||||
| következmények | hámsejtes metaplázia, nyákpangás. | "törékeny" epitélium, a bazális | részlegesen reverzibilis légúti | |||
| kislégúti fibrózis, parenchyma- | membrán megvastagodása | obstrukció, a bazális membrán | ||||
| pusztulás, vaszkuláris remodeling | megvastagodása | |||||
| terápiás válasz | kis funkcionális javulás hörgtágitó | kifejezett hörgtágitó és | csökkent hörgtá | gitó és | ||
| hatására, gyenge steroid-hatás | ko rti koszté ro id -h a tá s | korti koszté roid hatás | ||||
2.6. ábra
3. Tünettan, diagnosztika
A COPD diagnózisa minden olyan esetben fel kell merüljön, amikor a betegnek légszomja van, krónikusan köhög (ez produktivvagynem-produktivköhögésegyarántlehet) és/vagydohányfüstexpozició,munkahelyi inhalációsártalom szerepel a kórelőzményben. A gyanú spirometriás méréssel bizonyitható: a hörgtágitó aeroszol inhalációja után mért FEVi/FVC < 0,70 és a FEVi-nek a referencia-érték 80%-ánál alacsonyabb nagysága "nem teljesen reverzibilis" légúti obstrukciót jelent ( 3.i. ábra ).
3.i. Kórelőzmény
A dohányzás kezdete, mértéke (az esetleges leszokási kisérletek), a környezeti, munkahelyi kockázati tényezők, a köhögés gyakorisága, jellege, "sipoló" vagy ziháló légzési hang, az akut légúti betegségek gyakorisága, természete, a nehézlégzés súlyossága mind fontos adatok. A COPD tünetei a felnőtt korban jelentkeznek, a betegek többsége elmondja, hogy az őszi/téli meghűlések alkalmával a köhögés, kinzó fulladás fokozódik. A panaszok akut súlyosbodása, a lassan progrediáló COPD első komoly, gyakran kórházi kezelést igénylő, exacerbációja vagy a mérsékelt fizikai terhelés közben fellépő légszomj miatt fordulnak a betegek először orvoshoz. Az "effort-dyspnoe" jelentkezése már a légzési tartalék (FEVi) 40-50%-ának elvesztését jelenti. Főként a COPD dominálóan emfizémás tipusaiban alakulhat ki jelentős légúti funkciózavar anélkül, hogy a képet krónikus köhögés és köpetürités kisérné.
3.2.Tünetek
A betegség két jellegzetes fenotipusa,a dominálóan emfizémás és a bronchitiszes forma jól elkülönithető tipusok(3.2. ábra). Kétségtelen, hogy a konkrét klinikai esetek többsége "kevert forma", nem sorolhatók egyértelműen az emfizémás (pirosan szuszogó - "pink puffer") vagy bronchitiszes (kéken fulladó - "blue bloater") csoportokba h 2. Mégis, az előbbi megkülönböztetés segit a kivizsgálási irányok és terápiás célok meghatározásában. A mellkas megtekintése a tüdő hiperinflációjának számos jelét mutathatja: a súlyos emfizémát a mellkas túltágulása (hordómellkas), alacsony rekeszállás, halk légzési- és szivhangok, az inspiratórikus segédizmok aktivitása, belégzés közben az alsó bordaközök behúzódása, az ajkak szükitő hatású csücsöritése exspiriumban ("ajakfékes légzés", auto-PEEP hatás) jellemzi 3. A nyugalmi légzési frekvencia gyakran > 20/perc.
Hallgatózással gyakran gyengült légzési hang hallható, de ennek diagnosztikus értéke csekély. A légúti obstrukció viszont valószinüsithető, amikor hallgatózással sipoló légzési hangot észlelünk vagy az erőltetett kilégzés hossza > 6 s. A dyspnoe, a légszomj vagy a légzési diszkomfort nehezen meghatározható tünetek, mivel számos kórtani, pszichológiai, szociális és környezeti tényező hatására alakul ki betegenként igen eltérő formában. A COPD-s beteg kezdetben csak a szokatlan nagy erőfeszitést észleli pl. lépcsőnjáráskor, majd, a betegség súlyosbodásakor tapasztalja, hogy lassabban mozog, mint hasonló életkorú társai, végül már az öltözködést, mosakodást, evést is akadályozza a fulladás. A dyspnoe súlyosságát egyszerű kérdőivekkel lehet értékelni (ezek általában a British Medical Research Council kérdőivének4 változatai, lásd a 7. fejezetet)
Krónikus obstruktiv tüdőbetegségben a légszomj oka összetett: egyszerre jelentkezik a légzőizomzat fokozott terhelése és gyengesége, gázcserezavar (hypoxia és hypercapnia), valamint dinamikus légúti kompresszió. Míg a hiperinfláció mértéke szorosan, a FEV1-csökkenés igen gyengén korrelál a dyspnoe intenzitásával COPD-ben 5,6.
3.3.Laboratóriumi vizsgálatok
a./Mellkas-röntgen: a röntgeneltéréseka betegség késői tünetei, csak súlyos emfizéma esetén diagnosztikus értékűek ill. a peribronchiális infiltrátumok, a tág pulmonális érrajzolat utalhatnak idült obstruktiv bronchitiszre. Nélkülözhetetlen azonban a mellkasröntgen-felvétel más, krónikus, produktiv köhögést okozó sziv- és tüdőbetegség kizárása szempontjából.
Az emfizémás szövetpusztulás diagnosztikájában a mellkasi computer tomográfia (CT) érzékeny módszer (ez nem rutin-vizsgálat, de térfogatredukciós műtétek előtt, az emfizémás szövetdestrukció pontos lokalizálása céljából a HRCT-vizsgálat elengedhetetlen).
b./ Spirometria (hörgtágitó inhalációja előtt és után): nélkülözhetetlen a légúti obstrukció fennállása, súlyossága, a reverzibilitása mértékének megállapitása céljából. A légúti obstrukció korai felfedezésére korábban ajánlott "kis légúti funkcionális jellemzők" (dinamikus compliance, záródó térfogat stb.) mérése körülményes vagy az eredmények nagy variabilitása teszi lehetetlenné az értékelést. Kétségtelen azonban, hogy az erőltett kilégzési áramlási sebesség/térfogat hurokregisztrátumon olyan, a FEV1, FEV1/FVC-értékekben nem tükröződő, ugyanakkor kislégúti obstrukcióra utaló deformációk jelenhetnek meg, amelyet szakértő tüdőgyógyász értékelni tud. Aspirométerekhitelesitését,a mérési manőver lebonyolitását és az eredményekértékelését számos irányelv részletezi 7,8,9 . A jó technikai feltételek mellett, gyakorlott vizsgáló által mért FEV1 intraindividuális variabilitása 4-5% (igy a legalább 3 éven át megfigyelt FEV1-csökkenés alapján a veszélyeztett, a progressziv tüdőfunkcióvesztést mutató betegcsoport elkülönithető: a normális 25-30 ml/év helyett ilyenkor az évi térfogatvesztés meghaladja az 50 ml-t, akár 80-100 ml lehet az évi FEV1-csökkenés). Az előbbi módszer igazolhatja egy terápiás eljárás hatását ellenőrzött klinikai vizsgálatokban, de a funkcióvesztés változatainak sokfélesége miatt, egyéni prognózis becslésére kevésbé alkalmas. Jóllehet a hordozható spirométerek mérési pontossága sokat javult, kezelhetősége egyszerűsödött, ára csökkent az utóbbi évtizedekben, az alapellátás orvosainak töredéke képes jó minőségű spirográfiás vizsgálatot végezni10,11.A spirográfia nem hasonlitható az EKG-vizsgálathoz vagy vérnyomásméréshez: a beteg együttműködése, a vizsgáló szakértelme és türelme mellett, a pontos eredmény nélkülözhetlen feltétele 12. Érthető, hogy az újabb ajánlások világszerte a "minőségi spirometriás szolgáltatás" igénybevételét ajánljáka háziorvosoknak,amelyre Magyarországon a tüdőgyógyászati szakrendelések képesek13,14.
A csúcsáramlás érzékenysége a COPD diagnosztikájában, a szakértők többsége szerint, gyengébb, mint a FEV1-é. A National Health and Nutrition Examination Survey (USA) adatai alapján viszont a csúcsáramlás mérésével, a spirometriával azonositott obstruktiv betegek 90%-át diagnosztizálták15.
A lakosságnak vagy magas kockázatú csoportoknak (pl. dohányzó, 40 évnél idősebb személyek) spirometriás szűrését támogató érvek ellentmondásosak. Kétségtelen, hogy a FEV1 és FVC aktuális értéke meghatározza a dohányzástól független össz-mortalitást, valamint a légúti funkciócsökkenés alapján elkülönithető egy pl. hörgőrák vagy stroke által veszélyeztetett csoport is16.
A COPD meghatározta életkilátások pontosabban prognosztizálhatók összetett, több klinikai jellemzőt tartalmazó mutatókkal, mint egyedül a FEV1-el: a BODE-index, a FEV1 mérése mellett, a testtömeg index-el (body mass index-BMI), a dyspnoe mértékével és a fizikai terhelhetőséggel számol17,18.
A légúti obstrukció reverzibilitásának vizsgálata á2-receptor agonista és antikolinerg aeroszolokkal, valamint orális kortikoszteroiddal, a korábbi várakozásokkal ellentétben, nem nyújt segitséget a COPD prognózisának vagy az alkalmazott terápia várható, későbbi hatásának megítélésében 19. Bizonytalan diagnózis esetén (pl. asztmára utaló éjszakai fulladásos rosszullétek, köhögési rohamok) elvégezhető a vizsgálat (3.3. ábra).
c./ reziduális térfogat (RV) és CO-diffuziós kapacitás (DlCO): a diffúziós kapacitás mérése az emfizéma korai diagnosztikájában fontos módszere, de az RVés DlCO meghatározása csak különleges körülményekfennállása esetén javasolt (pl. tervezett bullectomia, térfogat-redukciós műtét előtt vagy ha a légúti obstrukció mértékével nincs összhangban a nehézlégzés intenzitása) 20.
d./vérgázanalizis: enyhe formákban elvégzése szükségtelen, de ha a FEV1 <50%vagy légzési elégtelenség klinika jeleit észleljük indokolt a vizsgálat (a tartós oxigénterápia kezdeményezése csak a PaO2 és PaCO2 ismeretén alapulhat)21.
e./ "i-antitripszin-hiány mutatható ki a COPD-esetek kevesebb, mint 1%-ában. A vizsgálat indokolt, ha COPD, panlobuláris emfizéma, terápiarezisztens "asztma" vagy egyéb okkal nem magyarázható májcirrhozis tünetei alakulnak ki 50 évesnél fiatalabb, nem-dohányzó betegben. A normális a-1-antitripszin szérum-koncentrációjánál 15-20%-al alacsonyabb érték felveti homozygota a1-antitripszin-hiánygyanúját 22.
3.4. Elkülönitő diagnosztika:
3.4. táblázat
3.5. A betegség kórfejlődésének, a szövődmények és társbetegségek kialakulásának ellenőrzése
Klinikai remisszióban lévő COPD esetén, a tüdőfunkció-romlás megitélésére legfeljebb évente egyszer érdemes spirometriát végezni. A vizsgálat, elsősorban, az állapot súlyosbodásakor indokolt.
Más tüdőfunkciós vizsgálatok, mint a DlCO, belégzési kapacitás (IC), intratorakális gáztérfogat (ITGV), légúti áramlási ellenállás (Raw), nem tartoznak a klinikai rutin körébe, a finomabb diagnosztikus részletek megállapitásához szükségesek.
A pulzus-oximetra alkalmazható a vérgázanalizis helyetesitésére, de 90 %-nál alacsonyabb SaO2 esetén, végezzünk vérgázelemzést.
Amennyiben a jobb szivfél-elégtelenség közepesen súlyos légúti obstrukció és enyhe SaO2-csökkenés mellett alakul ki gondoljunk arra, hogy alvási apnoe szindróma, következtében O2-deszaturáció okozza az arteria pulmonális nyomásemelkedését. Ilyenkor kezdeményezzünk éjszakai poligráfiás vizsgálatot.
Irodalom
1. Georgopoulos D, Anthonisen NR: Symptoms and signs of COPD. In: CherniackNSszerk. Chronic obstructive pulmonary disease. Toronto: WB Saunders 1991. p. 357-363.
2. Burrows B, Niden AH, Barclay WR és mtsai: Chronic obstructive lung disease II. Relationships of clinical and physiological findings to the severity of airway obstruction. Am Rev Respir Dis 1965: 91:665-678.
3. Bianchi R, Gigliotti, Romagnoli I, Lanini B és mtsai: Chest wall kinematics and breathlessness during pursed-lip breathing in patients with COPD. Chest 2004:125(2): 459-65.
4. BestallJC, Paul EA,Garrod Rés mtsai: Usefulness of the Medical Research Council (MRC) dyspnoea scale as a measure of disability in patients with chronic obstructive pulmonary disease. Thorax 1999: 54(7): 581-6.
5. Manning HL, Schwartzstein RM: Pathophysiology of dyspnea. New Engl J Med 1995: 33:1547-52.
6. Mahler DA, Jones PW, Guyatt GH: Clinical measurement of dyspnea. In: Mahler DA szerk. Dyspnea. Marcel Dekker (New York) 1998: pp. 149-98.
7. Ferguson GT, Enright PL, Buist AS és mtsai: Office spirometry for lung health assessment in adults: A consensus statement from the National Health Educational Program. Chest 2000:117(4): 1146-61.
8. Pellegrino R, Viegi G, Brusasco V és mtsai: Interpretative strategies for lung function tests. Eur Respir J 2005: 26(5): 948-68.
9. Miller MR, Hankinson J, Brusasco V és mtsai: Standadization of spirometry. Eur Respir J 2005: 26(2): 319-38.
10. Enright PL, StudnickaM,Zielinski J: Spirometry to detect and manage COPDand asthma. Eur Respir Mon 2005:31:1-14.
11. Walters J, Hansen E, Mudge P és mtsai: Barriers to the use of spirometry in general practice. Aust Fam Physician 2005: 34: 201-203.
12. Lusuardi M, De Benedetto F, Paggiaro P és mtsai: A randomized controlled trial on office spirometry in asthma and COPD in standard general practice. Chest 2006:129:844-852.
13. Obbágy V: COPD-tüdogondozós szemmel. Medicina Thoracalis 2005:58:56-61.
14. BednarekM, Maciejewski J, WozniakM és mtsai: Prevalence, severity and underdiagnosis of COPD in the primary care setting. Thorax 2008: 63: 402-407.
15. Jackson H, Hubbard R: Detecting chronic obstructive pulmonary disease using peak flow rate: cross sectional survey BMJ 2003: 327(7416): 653-4.
16. Lofdahl CG, Postma DS, Laitinen LA és mtsai: The European Respiratory Society study on chronic obstructive pulmonary disease (EUROSCOP): recruitmen methods and strategies. Respir Med 1998: 92(3): 467-72.
17. Wilt TJ, Niewoehner D, Kim C és mtsai: Use of spirometry for case finding, diagnosis, and management of chronic obstructive pulmonary disease (COPD). Evid Rep Technol Assess (Summ) 2005:121:1-7.
18. Celli BR, Cote CG, Marin JM és mtsai: The body-mass index, airflow obstruction, dyspnea, and exercise capacity index in chronic obstructive pulmonary disease. N Engl J Med 2004:350(10): 1005-12.
19. Calverley PM, Burge PS, Spencer S és mtsai: Bronchodilator reversibility testing in chronic obstrctive pulmonary disease. Thorax 2003: 58(8): 659-64.
20. McLean A, Warren PM, Gillooly M és mtsai: Microscopic and macroscopic measurements of emphysema: relation to carbon monoxide gas transfer. Thorax 1992:47:144-149.
21. Rodriguez-Roisin R,MacNee W: Pathophysiology of chronic obstructive pulmonary disease. In: Postma DS, Siafakas NM szerk. Management of chronic obstructive pulmonary disease. European Respiratory Monograph 1998: 3:107-126.
22. McElvaney NG, Crystal RG : Inherited susceptibility of the lung to proteolytic injury. In: Crystal RG, West JB, Weibel ER, Barnes PJ szerk. The Lung: scientific foundations. Lippincott-Raven, Philadephia 1997: p. 2537-2553.

3.1. ábra
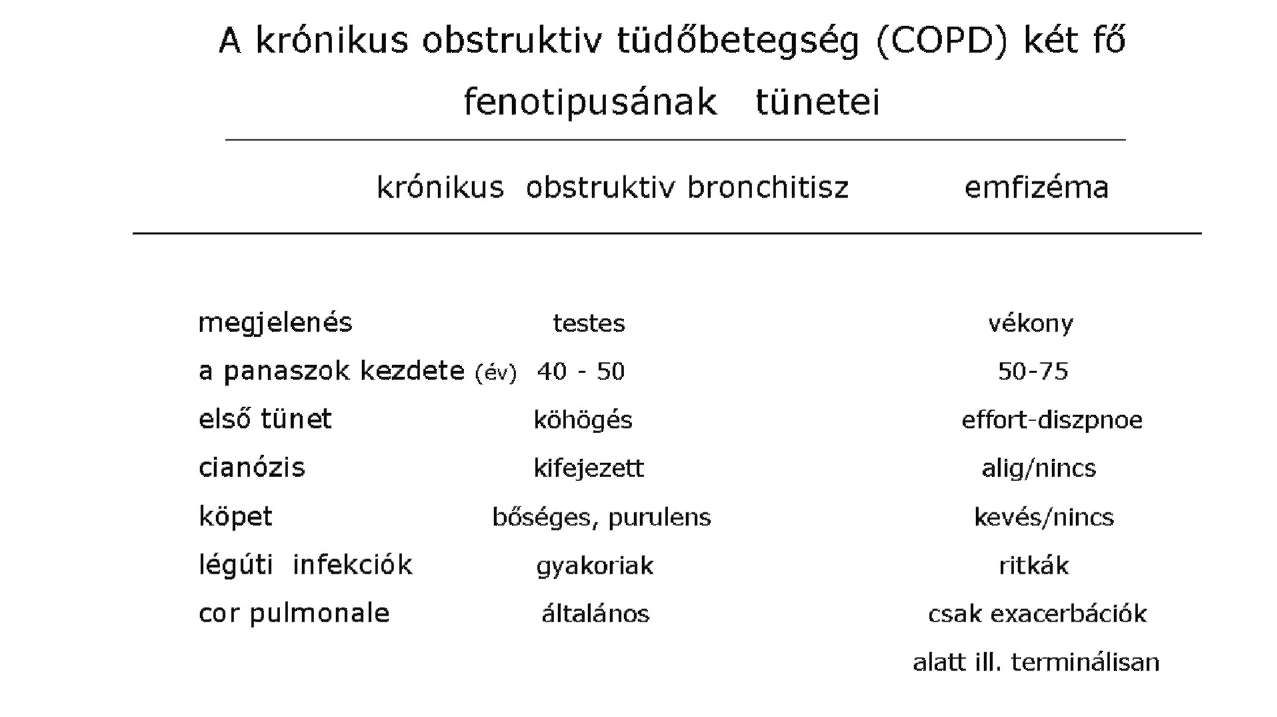
3.2. ábra

3.3 ábra

4. Megelőzés
4.1. A dohányzásról való leszokás
A COPD etiológiája multifaktoriális: a genetikus prediszpozició mellett környezeti hatások következtében alakul ki a betegség. Az utóbbi kockázati tényezők közül legfontosabb a dohányzás. A COPD-ben szenvedő betegek 80%-a dohányzik, vagy dohányzott. A dohányosok relatív kockázata, a betegség kialakulása tekintetében, 12-szeres1. Már az in utero dohányfüst-expozició csökkenti a csecsemű születési súlyát és a légúti betegségek halmozódását okozza kisgyermek-korban. Ugyanigy, a kisgyermek-korban elszenvedett passziv dohányfüst-hatás következménye: gyakori mély légúti infekciókés később krónikus tüdőbetegségek kialakulása lehet2,3.
A dohányzás abbahagyása fékezni képes a bronchiális áramlási ellenállás progressziv fokozódását COPD-ben (A bizonyiték)1. A dohányzás abbahagyása a légúti funkciócsökkenés sebességét a felére csökkenti, igy az összes dohányzó betegnél meg kell kisérelni a dohányzás felfüggesztését.
A dohányzó légzőszervi betegek kezelésében a dohányzásról való leszoktatás kulcsfontosságú, a farmakoterápiával egyenrangú intervenció1,3. A kezelőorvos feladata, hogy tájékozódjon a beteg dohányzási szokásairól és dokumentálja is azt. Ez már önmagában emeli a dohányzásról való leszokási arányt (A bizonyiték)5.
A leszokás legeredményesebb módja a három hónapos támogatott programszerű leszokás. Enyhe fokú nikotin-függőség esetében ez lehetséges gyógyszermentes módszerekkel: tanácsadás segitségével, egyéni, vagy csoportos magatartásorvoslási terápiával
(B bizonyiték)5. Közepes, vagy erős függőség esetén ajánlott a jól megválasztott farmakoterápia, amely csökkenti az átmenetileg kialakuló megvonási tüneteket és növeli a leszokás arányát. Ezek lehetnek vény nélkül kapható nikotinpótló készítmények (rágógumi, tapasz, szopogató tabletta), vagy orvosi rendelvényre felírható gyógyszerek: bupropion (jelenleg hazánkban nincs a leszokás támogatás indikációjában törzskönyvezve) 6 vagy a vareniklin (A bizonyiték)7.
Magyarországon a tüdőgondozókban működnek dohányzásról való leszokást segítő rendelések.
4.2. Foglalkozási por- és füstártalmak
Az Egyesült Államokban a munkahelyi por- és füstártalom COPD-t okozó vagy súlyosbitó hatását a dohányzó csoportban az esetek 19 %-ában, a nem-dohányzók körében 31 %-ban valószinűsitik8. E hatás, feltételezhetően, még súlyosabb ott, ahol munkavédelmi előirások nincsenek vagy lazák.
Irodalom
1. Anthonisen NR,Connett JE, KileyJPés mtsai: Effects of smoking intervention and the use of an inhaled anticholinergic bronchodilatatoron the rate of decline of FEV1. The Lung Health Study. JAMA 1994; 272(19) :1497-1505
2. Yu-Fen L, Gilland FD, Berhane Kés mtsai: Effects of in utero and environmental tobacco smoke on lung function in boys and girls with or without asthma. Am J Respir Crit Care Med 2000:162: 2097-104.
3. The Health Consequences in Involuntary Exposure to Tobacco Smoke: A Report of the Surgeon General, Department of Health and Human Services. Washington, DC, US: 2006.
4. Tonnesen P., Carozzi L, Fagerstrom KO és mtsai: Smoking cessation in patients with respiratory diseases. Eur Resp J 2007: 29(2): 390-417
5. The tobacco use and dependence clinical practice guideline panel, staff, and consortium representatives. A clinical practice guideline for treating tobacco use and dependence. JAMA 2000: 28:3244-54.
6. Jorenby DE, LeischowSJ, Nides MA és mtsai: A controlled trial of sustained-release bupropion, a nicotin patch, or both for smoking cessation. N Engl J Med 1999: 340(9): 685-91.
7. Tonstad S, Tonnesen P, Hajek P és mtasi: Effect of maintenance therapy with varenicline on smoking cessation: a randomized controlled trial JAMA, 2006; 96(1): 64-71
8. Celli BR, Halbert RJ, Nordyke RJ és mtsai: Airway obstruction in never smokers: results from the Third National Health and Nutrition Examination Survey. Am J Med 2005:118:1364-72.
5. A COPD kezelése klinikai remisszióban ("stable COPD")
A Tüdőgyógyászati Szakmai Kollégium 2003-ban elfogadott COPD kezelési ajánlásainak döntő többsége ma is érvényes 1. A klinikai remisszióban lévő, stabil COPD terápiás ajánlásainakjelen változata elsősorban a korábbi hazai ajánlásokra, az azóta megjelent új klinikai vizsgálati eredményekre, valamint a GOLD 2006-ban megújitott kiadására támaszkodik 2.
Az újabb terápiás eredmények ismeretében a, nemzetközi irányelvekben hangsúlyozott állitás, hogy a "COPD megelőzhető és kezelhető betegség", elfogadható3.
A klinikai remisszióban lévő COPD kezelésének célja: a tünetek csökkentése, a betegség progressziójának megakadályozása/fékezése, a fizikai terhelési tolerancia javítása, a szövődményekés az exacerbatiók megelőzése, az általános egészségi állapot, életminőség javitása, valamint a mortalitás csökkentése kell, hogy legyen. Ezeket a célokat a komorbiditások figyelembe vételével a kezelés okozta minimális mellékhatások mellett kell elérni2,3. Az asthma lépcsőzetes kezelési elveivel ellentétben a COPD tartós (fenntartó) terápiájával, ha a tüneti kontrollt sikerül elérni, a kezelés redukciója (a terápia lépcsőn való lefelé lépés) nem jön szóba23. A terápia egyénre szabott kell, hogy legyen, melyhez a légúti obstrukció súlyossági fokozatai ( 5.1. ábra ) csak általános útmutatásul szolgálnak. A COPD konkrét klinikai eseteiben ugyanis a betegség súlyosságát számos más, nem "funkcionális" tényező is jelentősen befolyásolja, így a panaszok intenzitása, az exacerbatiók gyakorisága és súlyossága, a szövődmények (pl.a vérgáz-eltérések nagysága), a társbetegségek száma, jellege, az általános testi állapot és a betegség hatásos befolyásolásához szükséges gyógyszerek száma (gyógyszerrezisztencia, mellékhatások)2,3.
A COPD, mint krónikus - így folyamatos terápiára szoruló betegség - kezelésének integráns része a betegoktatás, beleértve a dohányzás leszoktatás elősegítését segítő tevékenység is. A beteg tájékoztatása a betegségét előidéző, súlyosbitó tényezőkről, dohányzók esetében a dohányzásról való leszoktatás jelentőségéről, a betegség természetéről, az inhalációs eszközök használatáról, az exacerbatiók felismeréséről, a nehézlégzés minimalizálásának módszereiről, a terheléses tréning, otthon is folytatható, formáiról, mind fontos elemei a betegoktatásnak. Igen súlyos COPD-ben a beteg és a hozzátartozó tájékoztatását ki kell terjeszteni a várható szövődményekre, a folyamatos oxigén terápiával és a betegség végstádiumával kapcsolatos ismeretekre, teendőkre2. A beteg dönthet arról is, hogy állapota, intenziv légzésterápiát igénylő, súlyosbodásakor, kivánja-e ezt?
5.1. Farmakoterápia
Az eddig közölt eredményekalapján megállapítható, hogy a farmakoterápia egyik formája sem képes a légúti funkció progresszív hanyatlását megállítani COPD-ben (A bizonyiték)4,5,6. Meg kell jegyezni azonban, hogy több, jelenleg még nem lezárt, 3-4 éve folyó klinikai vizsgálat ismert részeredményei igéretesek.
A gyógyszeres kezelés tüneti hatása jelentős: a panaszokat enyhíti és a szövődmények kialakulásának valószínűségét csökkenti.
A COPD farmakoterápiájának általános irányelvei:
- a klinikai tünetek súlyosságához illeszkedő lépcsőzetesen bővülő kezelés (5.1. ábra)
- rendszeres, folyamatosan azonos gyógyszerhatást biztosító terápia mindaddig, amíg a mellékhatások vagy a betegség súlyosbodása a "fenntartó" kezelés megváltoztatását nem teszik szükségessé
- a "terápiás válasz" és a mellékhatások előfordulása betegenként igen eltérő lehet: ennek gondos észlelése, a gyógyszeradagok szükség szerinti módosítása szükséges2.
A COPD-ben alkalmazott gyógyszereket és kiszerelési formáikat az 5.2.ábra sorolja fel. 5.1.1. Hörgtágítók
A hörgő simaizom-tónust befolyásolva tágítják a légutakat, csökkentik a tüdő dinamikus hiperinflációját nyugalomban és terhelés alatt, javítják a terhelhetőséget.
A hörgtágító kezelés központi szerepet játszik a COPD tüneti rosszabbodásának kezelésében, mind szükség szerint adva, mind pedig tartósan alkalmazva a panaszok csökkentésére (A bizonyiték)2. Inhalációs alkalmazásukat előnybe kell részesíteni a szisztémás adással szemben a mellékhatásokelőfordulásának kisebb esélye miatt (A bizonyiték) 7,8.A bronchodilatátorok mindegyik csoportjában a FEVremelkedésre vonatkoztatott dózis-hatás görbe lapos COPD-ben. Mindegyik hörgtágító csoportra érvényes, hogy javítják COPD-ben a terhelési kapacitást a FEV1 szignifikáns javulása nélkül is (A bizonyiték) 9,10. Elhúzódó hatástartamú bronchodilatátorokkal történő rendszeres (fenntartó) kezelés hatásosabb és kényelmesebb, mint a rövid hatástartamúakkal történő terápia (A bizonyiték)11,12,13,14,15,16. A hörgtágítók kombinációban való adása javíthatja a hatást, és az egymagában adott bronchodilatátor dózisának emelésével való összehasonlításban csökkenti a mellékhatások kockázatát (A bizonyiték)17,18.
5.1.1.1. Antikolinerg és R2 -receptor agonista hörgtágítók
Inhalált hörgtágítók jelentik a COPD farmakoterápiájának alapját. A "2-szimpatikomimetikumok és antikolinerg hörgtágítók - különböző, ill. egymást kiegészítő hatásmódjuk, valamint farmakokinetikájuk eredményeként -kombinációban hatásosabbak, mint külön-külön és a tachyphylaxia kialakulása is ritkább17,18. A rövid hatású Ik-receptor agonistáka COPD bármely súlyossági lépcsőjében használhatók szükség szerint a tünetek enyhítésére. Hörgtágító hatásuk kezdete lassúbb COPD-ben, mint asztmások esetében. Maximális broncholízis 15-30 perc alatt alakul ki, amely átlagosan 4-6 órán át tart (A bizonyiték)9.
Rövid hatástartamú antikolinerg hörgtágítók, a I2-szimpatikomimetikumokhoz hasonlóan, a COPD bármely súlyossági fokozatában alkalmazhatók szükség szerint. Hatásuk hosszabb, mint a rövid hatású I2-agonistáké: átlagosan 6-8 óra ( A bizonyiték )14.
Elhúzódó hatástartamú ^-receptor agonista vagy antikolinerg hörgtágító kúraszerű alkalmazása ajánlott, ha a FEV1 nem éri el a referencia-érték80%-át akkor is, ha a beteg panaszmentes. Ilyen mértékű légúti funkciócsökkenés ugyanis általában légzészavart okoz, de a betegekegy része fokozatosan alkalmazkodik az obstrukcióhoz: panaszt nem okozó terhelési módokat választ vagy természetesnek veszi a légszomjat a fizikai erőfeszítés adott szintjén. A hörgtágító kúra elindítását tehát ne a beteg panasza, hanem az obstrukció objektív súlyossága vezesse.
Ugyanakkor a gyógyszerhatás lemérése nem alapulhat kizárólag a FEV1 vagy FVC változásának megfigyelésén. Az erőltetett kilégzési manőver ugyanis hörgőkollapszust, a bronchiális áramlási ellenállás igen kifejezett emelkedését okozza, amely elfedi a nyugalmi légzés mellett megnyilvánuló farmakoterápiás hatásokat. Ezért az inspiratórikus kapacitás (IC) vagy vitálkapacitás (IVC) érzékenyebben jelzi a légúti funkciójavulást a FEV1-nél COPD-ben (az IC, IVC egyszerű spirométerekkel is vizsgálható)9,10,16.
Fontos légzésmechanikai változás még e betegcsoportban a tüdő hiperinflációja. A hiperinfláció statikus eleme főként a tüdőparenchyma rugalmasságcsökkenésének kompenzációjaként alakul ki (kevésbé az aktív bronchospasmus következtében), a dinamikus komponens viszont fizikai terhelés hatására, a tachypnoe, a rövid kilégzési idő eredményeként jön létre (légcsapdák, a ventillációból kizáródó, "trapping" térfogatok alakulnak ki). A hörgtágítók tüneti hatásai szorosan összefüggnek a hiperinfláció változásával, így az IC és IVC alakulása a tüdők túltágulásának mértékéről is tájékoztat 16. Ugyanígy a beteg panaszainak csökkenése, a fizikai terhelhetőség fokozódása általában fontosabb adat COPD-ben, mint a spirometria eredménye. Az utóbbi változások különböző, Magyarországon ritkán használt, módszerekkel "objektivizálhatók": betegnaplók, életminőség kérdőívek, 6 perces séta 716. COPD-ben a légúti obstrukció reverzibilis komponense főként a fokozott kolinerg simaizom-tónussal kapcsolatos, amelyet az antikolinergikumok az acetilkolin kompetetiv gátlásával csökkentenek. A I-szimpatikomimetikumok broncholitikus hatásukat a I-adrenerg receptorok stimulálásával ill. az intracelluláris cAMP-szint emelésével érik el.
Az ipratropium és a rövid hatású LVagonista aeroszolok a szokásos adagban COPD-ben egyenértékű hörgtágítók (A bizonyiték) 16. Egyes vizsgálatok szerint az ipratropium csúcshatása és hatástartama meghaladja a rövid hatású b-szimpatikomimetikumokét COPD-ben (B bizonyiték)7.
A COPD II. súlyossági lépcsőjétől kezdve fenntartó kezelésre az elhúzódó hatástartamú inhalációs hörgtágítók (LVagonisták/antikolinerg szer) ajánlottak, de akut tünetek megszüntetésére, a légszomj gyors csillapitására rövid hatástartamú b2-receptor agonista aeroszolt rendeljünk ( 5.1. ábra ).
Az elhúzódó hatású quaterner antikolinerg hörgtágitó tiotropium több mint 24 órán át mérsékeli a tüneteket és -placeboval, valamint ipratropiummal összehasonlítva - szignifikánsan javítja a FEVi és FVC értékét, a fizikai terhelhetőséget, mérsékeli a hiperinflációt és a panaszokat, valamint ritkítja az akut bronchitiszes exacerbatiók gyakoriságát (A bizonyiték)10,12,16.
5.1.1.2. Xantin származékok
Ateofillin közepes hörgtágitó hatása mellett javítja a mucociliárisclearance-t, csökkenti a légúti gyulladást, bronchiális hypereaktivitást és nehézlégzést, javítja a légzőizmok kontraktilitását, a jobb és bal kamrai ejekciós frakcióját, a fizikai terhelhetőséget, valamint csökkenti a pulmonális arteriális nyomást is (B bizonyiték) 21, 22. A xantin származékok analeptikus hatása miatt a PaO2 általában emelkedik, és a PaCO2 csökken, de gyakran alvászavarok és gyomorpanaszok jelentkezhetnek.
A terápiás ablak szűk, és a kedvező hatások gyakran közel toxikus dózisok mellett jelentkeznek (A bizonyiték) 21, 23.A metilxantinok nem-specifikus foszfodieszteráz enzim-gátlók, ez magyarázza a mellékhatások széles körét. A többi bronchodilatátorral szemben a túladagolás veszélye fokozott, mely enyhébb esetben fejfájást, hányingert, súlyos esetben pitvari és kamrai arrhythmiákat "grand mal" konvulsiót okozhat. Ezek a mellékhatások azonban már akár a terápiás tartományban is megjelenhetnek.
5.1.2. Glükokortikoszteroidok
A szisztémás hatású orális glükokortikoszteroidokat 8-12 napos kúrában régóta és sikerrel alkalmazzák a COPD akut exacerbatióiban (ld. később). Tartós adásuk - ismert súlyos mellékhatásaik miatt - COPD-ben nem ajánlott (A bizonyiték) 24.
Az inhalációs glükokortikoszteroidok (ICS) rendszeres adása olyan panaszos COPD-s betegeknél indokolt, akiknek a FEV1 értéke a referenciaérték <50%-a (III. és IV. súlyossági csoport) és ismétlődő exacerbatióik vannak, pl. legalább 3 exacerbatió az utóbbi 3 évben (A bizonyiték) 25,26. A rendszeresen adott ICS terápia csökkenti az exacerbatiók számát, és ezáltal javítja az egészségi állapotot (A bizonyiték) 26,27. Az ICS kezelés visszavonása a betegek egy részénél exacerbatiót eredményezhet. Több hosszantartó klinikai vizsgálat adatainak összesített eredménye alapján az ICS kezelés csökkenti a COPD-s beteg, összes okra vonatkoztatott mortalitását.
Az ICS elhúzódó hatású [u-receptor agonistával való kombinációban COPD-ben sokkal hatásosabb az akut exacerbációk gyakoriságának csökkentésében, a tüdőfunkció és életminőség javitásában, mint az egyedi komponensek ( A bizonyiték ) 28,31.
Az ICS-el való tartós kezelés - a kedvező hatások ellenére - nem módosítja a COPD-s betegek hosszú távú FEV1-csökkenésének ütemét 27, 31.
5.1.3. Mukolitikumok
Afokozott légúti váladéktermelés a COPD egyik vezetőtünete, ezért számos vegyület hatását vizsgálták acélból,hogy a köpetüritést megkönnyitsékés igy a légúti vezetőképességet javitsák:
- a dohányzás abbahagyása a hiperszekréció csökkentésének leghatékonyabb módszere
- az antikolinerg hatású és L2-agonista hörgtágitók, valamint a xantin-készitmények is jelentősen javitják a tüdő öntisztulását
- az N-acetilcisztein, karbocisztein, bromhexol, ambroxol in vitro csökkenti a nyák viszkozitását, de klinikai hatásukat nem támogatják egyértelmű bizonyitékok 32,33. Ugyanakkor az N-acetilcisztein erős antioxidánsként ritkitja a COPD akut exacerbációinak jelentkezését és a lefolyás súlyosságát is mérsékeli (B bizonyiték)34.
5.1.4. Pneumococcus vakcináció: a nemzetközi ajánlások többsége javasolja a vakcinációt COPD-ben, ha a beteg 65 évesnél idősebb, 5-6 évenként . Bizonyitott az is, hogy a közösségben szerzett pneumonia előfordulás csökken 65 évesnél fiatalabb, kis légzési tartalékkal rendelkező (a FEV1 alacsonyabb, mint a referencia-érték 40%-a) betegek csoportjában is (B bizonyiték ) 35.
5.1.5. Influenza vakcináció: a súlyos COPD exacerbációinak szövődményeit hatásosan védi ki, az exacerbáció kialakulásának valószinűsége 50%-al csökken a vakcinációban részesült csoportban, összehasonlitva a kontrollal (A bizonyiték) 36,37.
5.1.6. Immunstimulánsok: az OM85-BV (Broncho-Vaxom) a leggyakoribb légúti kórokozók liofilizált kivonatának keveréke, amely immunmodulátor hatású (a makrofágok működését aktiválja). A COPD exacerbációinakgyakoriságát ritkitja, súlyosságát enyhiti38.
5.1.7. Köhögéscsillapitó: a köhögés, jóllehet gyakran a COPD kinzó tünete, protektiv hatású. Ezért a köhögés csillapitóknak nincs helye a COPD terápiájában.
5.2. Nem-farmakológiai kezelés
5. 2.1. Oxigén-terápia
Az oxigén-kezelés az elsődleges nem farmakológiai terápia a IV. stádium (igen súlyos) COPD-okozta hypoxaemia esetén 39, 40, 41. Adásának három módja van: 1) folyamatos (tartós) O2 kezelés, 2) terhelés alatti O2-kezelés, 3) az akut dyspnoe mérséklése céljából adott O2-kezelés. Az oxigén kezelés elsődleges célja a PaO2 legalább 8,0 kPa-ra (60 Hgmm) és/vagy az SaO2 legalább 90%-ra való megemelése, mely elegendő O2-t biztosít a vitális szervek funkciójának megőrzésére.
A tartós otthoni oxigén-kezelés (mely naponta >15 órán át tartó oxigénpótlást jelent) előrehaladott COPD-okozta hypoxia esetén átlagosan 6-7 évvel megnyújtja az élettartamot (A bizonyiték)40, 41. Az oxigénpótlás javítja a haemodinamikát, a tüdő mechanikát, a beteg mentális állapotát, gátolja a pulmonális hypertensio súlyosbodását, mérsékeli a másodlagos polycythaemiát és összességében a beteg életminősége válikjobbá42,43. A tartós otthoni oxigén-kezelést, intézeti megfigyelést követően, akkor javasolhatják, ha a beteg klinikai szempontból kiegyensúlyozott állapotában, optimális farmakoterápia mellett, a dohányzás abbahagyása után ezt a PaO2 és a SaO2 értéke szükségessé teszi. Tartós otthoni oxigénkezelés indokolt, ha a PaO2 7,3 kPa-nál (55 Hgmm-nél) vagy a SaO2 nyugalomban 88%-nál alacsonyabb. Az otthoni oxigén-kezelés javallatát nem elég egy mérés eredményére alapozni, hanem legalább két, 3 hét időkülönbséggel végzett vizsgálat eredményét kell tekintetbe venni. Jóllehet a pulzus-oximetria alkalmas arra, hogy a hipoxémia fennállását kizárjuk, a tartós oxigénterápia csak a nyugalmi PaO2 mérésén alapulhat, miután 30 percen át, nyugalomban szobalevegőt légzett a beteg. A pulzus-oximetria később az oxigén-adagolás korrekciójában segíthet. Az olyan betegek akár felénél, akiknél az oxigénpótlást hibásan, dekompenzált állapotukban kezdeményeztük, az otthoni oxigénterápia néhány hét után feleslegessé válhat. A dohányzás folytatása magas biztonsági kockázatot jelent otthoni oxigénkezelés esetén, emellett a terápia előnyei általában sem érvényesülnek, ha a beteg folytatja a dohányzást és a carboxyhemoglobin-szint emelkedett marad. Amennyiben a PaO2 magasabb ugyan (7,3 - 8,0 kPa vagy 55 Hgmm - 60 Hgmm között van), ennek ellenére dekompenzált pulmonális hipertenzió tüneteit észleljük, tartós otthoni oxigénkezelés mérlegelendő44. Ilyenkora kép hátterében a COPD-ben gyakori alvási légzészavar, köztük az átlagpopulációénál nem gyakoribb, obstruktív alvási apnoe-okozta éjszakai deszaturációk, gyanúja is fel kell merüljön45. Az éjszakai pulzusoximetriás mérés általában elegendő, hogy az alvás alatti artériás oxigén-deszaturációs epizódokat kimutassuk, bizonytalan esetben poliszomnográfiás vizsgálat is szükségessé válhat46.
Az általában orrszondán keresztül adagolt oxigénpótlást (palackból percenként kb. 1-3 L, oxigénkoncentrátorból 2-4 L) naponta legalább 15 órán át kell folytatni, hogy a klinikai tünetekre, túlélésre kifejtett előnyös hatások érvényesüljenek (A bizonyiték)40,41. Oxigénpótlás mellett a vérgáznyomásokat gondosan ellenőrizni kell: a rotamétert úgy kell beállítani, hogy a PaO2 8 kPa (60-65 Hgmm), a SaO2 90% fölé emelkedjen anélkül, hogy a PaCO2 növekedése meghaladná a 2,0 kPa-t (15 Hgmm-t).
Javasolt, hogy a tartós otthoni oxigénkezelés hatását fél évente a terápiát kezdeményező orvos ambuláns vizsgálattal ellenőrizze.
Az oxigénkoncentrátor a legalacsonyabb fajlagos költségű oxigénforrás (Magyarországon a koncentrátorok energiaköltségét a betegbiztositó nem támogatja, míg a palackos oxigénterápia támogatása jelentős). Az új koncentrátor kihelyezését az Országos Korányi Tbc és Pulmonológiai Intézetben, a beteg adatlapja (vérgázértékei) alapján, hagyjákjóvá (a használat meghosszabbítását a regionális szakfőorvos is engedélyezheti.). Az oxigénpalackok bérlete olcsó ugyan, és a gyors palackcsere Budapesten és a nagyobb vidéki városokban megoldott, de a nagyméretű (3 m3-es) palack is, napi 15 órán át tartó oxigénadagolás mellett, 2-3 nap alatt kiürül, így a koncentrátornál sokkal drágább.
A regionális szakfőorvos engedélyével hozzáférhető cseppfolyós oxigénellátó rendszerek lehetővé teszik a beteg lakáson kívüli mozgását és rehabilitációját.
A fizikai terhelés alatti oxigénadás alkalmas arra is, hogy fizikai tréning alatt mérsékeljük a dinamikus hiperinflációt, a légzésszámot és ezzel a dyspnoe-t, ezzel a rehabilitáció során növelhessük a tréningintenzitást, amely a beteg mozgásképességének, életminőségének jelentős javulását eredményezi 42. A terhelés alatt adott oxigén növeli a terhelhetőséget, egy adott terhelési szint tolerálhatóságának idejét (az állóképességet) és/vagy csökkenti a terhelés utáni nehézlégzés intenzitását (A bizonyiték)47,48.
A súlyos dyspnoe (mint pl. a lépcsőzés után fellépő dyspnoe) kivédése céljából terhelés előtt vagy után rövid ideig adott (short burst) oxigénnek nincs kedvező hatása nem hypoxaemiás COPD-s betegeken (B bizonyiték)49.
Oxigén használat légi utazásnál
Jóllehet általában biztonságos a légi utazás, a krónikus légzési elégtelenségben szenvedő, folyamatosan O2-kezelésben részesülők számára mégis ajánlatos, hogy a repülés ideje alatt 1-2 L/perccel megemeljék az O2 adagját. Azon COPD-sekesetében, akiknél nyugalomban, tengerszinten a PaO2 9,3 kPa (70 Hgmm) általában nem szükséges O2 adás. Súlyosabb esetben a beteget ajánlatos légi utazásnál hordozható O2 tartállyal is felszerelni 50.
5.2.2. Rehabilitáció
A rehabilitáció lényege, hogy csökkentse a tüneteket, panaszokat, fokozza a fizikai és emocionális részvételt a mindennapi aktivitásban, és összességében javítsa a beteg életminőségét 2,3. A rehabilitáció a COPD-s betegek II-IV. súlyossági fokozatában a nem gyógyszeres terápia integráns része. A főként fizikai terhelés hatására fulladó COPD-s beteg terhelhetősége, így mozgásképessége csökken, kerülni fogja a megterhelő mozgást, mely dekondicionálódáshoz, szociális izolációhoz, szorongáshoz, depresszióhoz vezet. Mind a dekondicionálás, mind a depresszió fokozza a dyspnoe-percepciót. A légzésmechanika alig romlik ugyan, de egyre kisebb terhelés okoz nehézlégzést51. E circulus viciosust segít megszakítani a rehabilitáció 1 3351,52. A rehabilitációs kúra elsősorban olyan légzéskárosodott - elsősorban COPD-ben szenvedő - betegek esetében indokolt, akik az optimális gyógyszeres kezelés ellenére fulladnak, fizikai terhelhetőségük erősen korlátozott.
A pulmonális rehabilitáció komplex folyamatában (állapotfelmérés, farmakoterápia, légzőtorna, expektorációs és inhalációs technikák, mellkasi fizioterápia, terhelési tréning, diétás tanácsadás, pszichoszociális támogatás, betegoktatás) a rendszeres dinamikus tréning csak az egyik fontos elem, de hatásosságát illetően a bizonyítékok egyértelműek (A bizonyiték) 51.
A terheléses tréningnek két formáját alkalmazzák: az állóképességet (endurance) fejlesztő és az erőfejlesztő edzést. Az előbbi során nagyobb izomcsoportok közepes intenzitású, hosszabb ideig tartó, míg az utóbbi formánál kisebb izomtömeg nagyobb, intenzív, rövid ideig tartó terhelését végzik. Mindkét módszer enyhíti a panaszokat, javítja a fizikai terhelhetőséget és az életminőséget. Az edzési program megtervezésének és a kardiális kockázat pontos becslésének előfeltétele az, hogy először kardiopulmonális terheléses vizsgálat történjen. Ezután a kondicionáló tréning, ellenőrzött feltételek mellett, akár egy tüdőgyógyászati járóbeteg-rendelésen is folyhat. Már 6-8 hetes, hetente 3-5 alkalommal végzett, 30-45 perces kerékpár-ergométeres vagy járószalag tréning jelentősen javíthatja a fizikai terhelhetőséget anélkül, hogy a nyugalmi légzésfunkciós értékek változnának (A bizonyiték)53. Számos vizsgálat eredményének összegzése alapján ma már egyértelmű, hogy COPD-ben a pulmonális rehabilitáció javítja a terhelési kapacitást, csökkenti a nehézlégzés érzetet, javítja az egészséggel kapcsolatos életminőséget, csökkenti a hospitalizációkszámát és a kórházban töltött napok számát, csökkenti a COPD-vel kapcsolatos anxietast és depressziót (A bizonyiték) 53,54.
A felső végtagi erőfejlesztő és "állóképességi" tréning javítja a kar funkcióját (B bizonyiték) 54. A pulmonális rehabilitáció kedvező hatása a tréning befejezését messze meghaladja, és növeli a túlélés esélyét (B bizonyiték)54.
A légzőizmok tréningjének hatása különösen akkor kedvező, ha általános terhelési tréning is társul hozzá. A pszichoszociális intervenció is kedvező hatású (Cbizonyiték) 54.
A COPD a légzőrendszer krónikus, progressziv funkcióvesztéssel járó betegsége és, az esetek 20-50% -ában, kóros mértékű testsúlycsökkenéssel jár. Az alultápláltság korrekciója a COPD fenntartó kezelésének fontos eleme: bizonyitottan javitja a betegek életminőségét és túlélését. A megfelelő diéta mellett alkalmazott terheléses tréning fokozza a táplálásterápia hatását. A COPD akut exacerbációiban nagy energiatartamú tápszerekalkalmazása indokolt. A COPD-re a malnutritio kevert formája jellemző, amely az izom és zsigeri fehérjék mennyiségének csökkenésével, a zsirraktárak eltűnésével, az immunvédekezés gyengülésével, végül anergiával jellemezhető. A súlycsökkenés főként a vázizomzat atrófiájának a következménye (a maradék izomzat dysfunkciója is jellemző). Az izomatrófia hátterét nem ismerjük.
Az alultáplálátság súlyosságának megitélésére a testtömeg indexet (body mass index - BMI) vagy, újabban a zsirmentes testtömeg (fat free mas - FFM) becslését használjuk.
Az alultápláltság aránya a COPD súlyosságával párhuzamosan nő. 20 kg/m2 - nél alacsonyabb testtömeg indexet mutat a közepesen súlyos COPD-s betegek 20-25, a súlyos betegek 25-35 és a légzési elégtelenség tüneteit mutató betegek 35-50%-a. A testsúly-csökkenés főként a, dominálóan, emfizémás csoportban kifejezett. A tesstömeg-index csökkenése a COPD-mortalitás független kockázati tényezője (A bizonyiték) 55, 56. Ennek oka, feltételezhetően az, hogy a tápláltsági állapot javitása fokozza a légzőizomzat erejét, növeli a légzési tartalékot, javitja a betegség prognózisát.
30- nál magasabb BMI esetén a testsúly csökkentése ajánlott, míg 21-nél alacsonyabb BMI táplálás-terápiát indokol: az orális táplálékfelvétel emelése mellett nagy energiatartalmú tápszerekkel kell a diétát kiegésziteni. A táplálás-terápia bevezetése gyakran a COPD akut exacerbációja idején válik elkerülhetetlenné (ilyenkor a tápszerek nélkülözhetetlenek).
Tekintettel arra, hogy a súlyos COPD-t a gázcsere zavara jellemzi, ezért a CO2-képződést azaz a szénhidrát-bevitelt korlátozni kell. A COPD táplálás-terápiájánál a következő összetételű diéta javasolt: 50-60% szénhidrát, 20-30% zsir, 20% fehérje
- a testsúlyhiány korrekciója idején naponta 1,6 - 2,5 g/tsgk fehérje- és a nyugalmi energiafelhasználás (resting energy expenditure- REE) 1,5-szeresénak megfelelő kalóriabevitel javasolt
- a fenntartó étrendben naponta 1,2-1,9 g/tskg fehérje- és a nyugalmi energiafelhasználás 1,0 - 1,2-szeresének megfelelő kalóriabevitel ajánlott
A legújabb bizonyitékokarra utalnak, hogy a táplálásterápiát célszerű egy komplex rehabilitációs stratégia keretébe illeszteni. A kalóriabevitel kombinálása terheléses tréninggel bizonyitottan felülmúlja a táplálásterápiás hatást (nem-specifikus anabolikus effektus) 57.
5.2.3. Sebészi kezelés
Bullectomia
Gondosan válogatott esetekben a bullectomia javítja a tüdőfunkciót, és csökkenti a légzési panaszokat (C bizonyiték) 58. Leginkább olyan nagy bullák esetében javasolt bullectomia, amikora diffúziós kapacitás normális vagy legfeljebb enyhén csökkent, nincs jelentős hypoxaemia és a megmaradó tüdő perfúziója jó. A pulmonális hypertenzió, hypercapnia és a súlyos emfizéma sem jelent abszolút kontraindikációt58.
Tüdő volumen-redukciós műtét
A túltágult emfizémás tüdő egy részének sebészi eltávolítása a maradék tüdő rugalmasság-tartalékának felszabaditását és az emfizémás tüdőterületek, nem szellőző légtereivel kapcsolatos "kompressziós" légzési munka csökkentését jelenti, mindez a dyspnoet jelentősen mérsékelheti59.
A National Emphysema Treatment Trial igazolta, hogy a felsőlebeny dominanciájú, alacsony terhelési kapacitású emfizémás betegeken optimális farmakoterápia és légzésrehabilitáció mellett a volumen-redukciós műtét jelentősen javítja a fizikai terhelhetőséget, és az egészséggel kapcsolatos életminőséget és a túlélést60. A palliativ műtét elvégzése -a komplikációkveszélye miatt - csak gondos mérlegelés után, válogatott esetekben ajánlott61.
Tüdőtranszplantáció
Megfelelően szelektáltvégstádiumban lévő,dominálóan emfizémás,COPD-s betegcsoportban a tüdőtranszplantáció (egyoldali is) javította az életminőséget, és a funkcionális kapacitást, de a túlélést befolyásoló hatás bizonytalan 62,63.
Irodalom
1. A krónikus obstruktiv légúti betegség (chronic obstructive pulmonary disease - COPD) diagnosztikája és kezelése. A 2003. november 21-22.-én rendezett Konszenzus Konferencián elfogadott irányelvek alapján szerkesztett ajánlás. Budapest 2003, kézirat
2. Global Initiative for Chronic Obstructive Lung Disease. Global strategy for the diagnosis management and prevention of chronic obstructive pulmonary disease 2006. www.goldcopd.org
3. Standards for the diagnosis and treatment of patients with COPD: a summary of the ATS/ERS position paper. Szerk.: Celli BR és MacNee W. Eur Respir J 2004.: 23: 932-946.
4. Anthonisen NR, Connel JE, Kiley JP és mtsai: Effect of smoking intervention and the use of inhaled anticholinergic bronchodilatatoron the rate of decline of FEVi. The Lung Health Study. JAMA 1994: 272:1497-1505.
5. Pauwels RA, Löfdahl CG, Laitinen LA és mtsai: Long-term treatment with inhaled budesonide in persons with mild chronic obstructive pulmonary disease who continue smoking. European Respiratory Society Study on Chronic Obstructive Pulmonary Disease. N Engl J Med 1999:340:1948-1953.
6. Burge PS, Calverley PM, Jones PW. és mtsai: Randomised, double blind, placebo controlled study of fluticason propionate in patients with moderate to severe chronic obstructive pulmonary disease: the ISOLDE trial. BMJ 2000:
320: 1297-1303.
7. Gross NJ, Petty TL, Friedman M .és mtsai: Dose response to ipratropium as a nebulised solution in patients with chronic obstructive pulmonary disease. A three-center study. Am Rev Respir Dis 1989:139(5): 1188-1191.
8. Higgins BG, Powell RM, Cooper S és mtsai: Effect of salbutamol and ipratropium bromide on airway calibre and bronchial reactivity in asthma and chronic bronchitis. Eur Respir J 1991:4(4): 415-420.
9. Man WD, Mustfa N, Nikoleton D. és mtsai: Effect of salmeterol on respiratory muscle activity during exercise in poorly reversible COPD. Thorax 2004:59:471-476.
10. O'Donnel DE, FlugeT,Gerken F.és mtsai: Effects of tiotropium on lung hyperinflation,dyspnea and exercise tolerance in COPD. Eur Respir J 2004:23: 832-840.
11. Dahl R, Greefhorst LA, Novak D. és mtsai: Inhaled formoterol dry powder versus ipratropium bromide in chronic obstructive pulmonary disease. Am J Resp Crit Care Med 2001.164:778-784.
12. OstenbrinkJB, Rutten-van Molken MP, Ai MJ és mtsai.: One-year cost effectiveness of tiotropium versus ipratropium to treat chronic obstrcutive pulmonary disease. Eur Respir J 2004: 23: 241-249.
13. Sutherland ER, Chermiack RM.: Management of chronic obstructive pulmonary disease. N Engl J Med 2004: 350: 2689-2697.
14. Belman MJ,BotnickWC, Shin JW.: Inhaled bronchodilatators reduce dynamic hyperinflation during exercise in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1996: 153:967-975.
15. Mahler DA, Donohue JF, Barbee RA és mtsai: Efficacy of salmeterol xinafoate in the treatment of COPD. Chest 1999: 115(4): 957-965.
16. Celli B, ZuWallackR, Wang S. és mtsai: Improvement in resting inspiratory capacity and hyperinflation with tiotropium in COPD patients with increased static lung volume. Chest 2003.124:1743-1748.
17. The COMBIVENT Inhalation Solution Study Group. Routine nebulized ipratropium and albuterol together are better than either alone in COPD. Chest 1997:112(6): 1514-1521.
18. Gross N, Tashkin D, Miller R és mtsai: Inhalation by nebulization of albuterol-ipratropium combination (Dey combination) is superior to either agent alone in the treatment of chronic pulmonary disease. Dey Combination Solution Study Group. Respiration 1998: 65(5): 354-362.
19. Shim CS, Williams MH Jr: Bronchodilator response to oral aminophylline and terbutaline versus aerosol albuterol in patients with chronic obstructive pulmonary disease. Am J Med 1983: 75(4): 697-701.
20. van SchayckCP, Folgering H, Harbers H és mtsai: Effects of allergy and age on responses to salbutamol and ipratropium bromide in moderate asthma and chronic bronchitis. Thorax 1991:46(5): 35-359.
21. Murciano D, Auclair MH, Pariente R. és mtsai: A randomized controlled trial of theophylline in patients with severe chronic obstructive pulmonary disease. N Engl J Med 1989: 320:1521-1525.
22. Barnes PJ.: Theophylline: new perspectives for an old drug. Am J RespirCrit Care Med 2003:167: 813-818.
23. McKay SE, Howie CA, Thomson AH es mtsai: Value of theophylline treatment in patients handicapped by chronic obstructive lung disease. Thorax 1993:48(3): 227-232.
24. Thompson WH, Nielson CP, Carvalho P es mtsai: Controlled trial of oral prednisone in outpatients with acute COPD exacerbation. Am J Respir Crit Care Med 1996:154: 407-412.
25. Mahler DA, Wire P, Horstman D. es mtsai: Effectiveness of fluticasone propionate and salmeterol combination delivered via the discus device in the treatment of chronic obstructive pulmonary disease. AmJ Respir Crit Care Med 2002: 166: 1084-1091.
26. Jones PW, Willits LR, Burge PS.es mtsai: Disease severity and the effect of fluticasone propionate on chronic obstructive pulmonary disease exacerbations. Eur Resp J 2003: 21:68-73.
27. Sin DD, Wu L, Anderson JA. es mtsai: Inhaled corticosteroids and mortality in chronic obstructive pulmonary disease. Thorax 2005: 60: 992-997.
28. Szafranski W, Cukier A, Ramirez A. es mtsai: Efficacy and safety of budesonide/formoterol in the management of chronic obstructive pulmonary disease. Eur Respir J 2003.21:74-81.
29. Calverley P, Pauwels R, Vestbo J. es mtsai: Combined salmeterol and fluticasone in the treatment of chronic obstructive pulmonary disease: a randomized controlled trial. Lancet 2003.361:449-456.
30. Calverley PM, Boonsawat W, Cseke Z. es mtsai: Maintenance therapy with budesonide and formoterol in chronic obstructive pulmonary disease. Eur Resp J 2003: 22: 912-919.
31. Calverley PM, Anderson JA, Celli B es mtsai: TORCH investigators. Salmeterol and fluticasone propionate and survival in chronic obstructive pulmonary disease. N Engl J Med 2007: 356(8): 775-89.
32. British Thoracic Society Research Commitee: Oral N-acethylcysteine may improve general well-beeing in patients with chronic bronchitis and severe airways obstruction. Thorax 1985:40:832-835.
33. Rasmussen JB, Glonnow C.: Reduction in days of illness after long-term treatment with N-acetylcysteine controlled-release tablets in patients with chronic bronchitis. Eur Resp J 1988. 1: 351-355.
34. Decramer M, Rutten-van Molken M, Dekhuijzen PN. es mtsai: Effects of N-acetylcysteine on outcomes in chronic obstructive pulmonary disease (Bronchitis Randomized on NAC Cost-Utility Study, BRONCUS): a randomized placebo-controlled trial. Lancet 2005: 365: 1552-1560.
35. Alfageme I, Vazquez R, Reyes N es mtsai: Clinical efficacy of anti-pneumococcal vaccination in patients with COPD. Thorax 2006: 61: 189-95.
36. Nichol KL, Margolis KL, Wuorenma J es mtsai: The efficacy and cost effectiveness of vaccination against influenza among elderly persons living in the community. N Engl J Med 1994: 331(12) : 778-84.
37. Wongsurakiat P, Lertakyamenee J, Maranetra KN es mtsai: Economic evaluation of influenza vaccination in Thai chronic obstructive pulmonary disease patients. J Med Assoc Thai 2003:86(6): 497-508.
38. Anthonisen NR:OM-8BV for COPD. Am J Respir Crit Care Med 1997: 156(6): 1713-4.
39. Siafakas NM, Vermeire P, Pride NB. es mtsai: Optimal assesment and management of chronic obstructiv pulmonary disease (COPD). The European Respiratory Society Task Force. Eur Respir J 1995.8:1398-1420.
40. Medical Research Council Working Party. Long term domiciliary oxygen therapy in chronic hypoxic cor pulmonale complicating chronic bronchitis and emphysema. Lancet 1981: 1: 681-686.
41. Nocturnal Oxygen Therapy Trial Group. Continuous or nocturnal oxygen therapy in hypoxaemia chronic obstructive lung disease: a clinical trial. Ann Intern Med 1980: 93: 391-398.
42. Torpy SP, Celli BR.: Long-term oxigen therapy in COPD. Chest 1995: 113(333): 710-714.
43. Zielinsky J,Tobiasz M, Hawrilkiewitz I, es mtsai.: Effects of long term oxygen therapy on pulmonary hemodynamics in COPD patients: a 6-year prospective study. Chest 1998: 113: 65-70.
44. Oba Y, Salzman GA, Willsie SK.: Reevaluation of continuous oxygen therapy after initial prescription in patients with chronic obstructive pulmonary disease. Respir Care 2000.45:401-406.
45. McNicolas WT: Sleep in chronic obstructive pulmonary disease. In: Postma DS, Siafakas NM: Management of chronic obstructive pulmonary disease. Eur Respir Mon 2006: 38:325-336.
46. Weitzenblum E, Choonat A.: Sleep and chronic obstructive pulmonarydisease. Sleep Med Rev 2004: 4: 281-291.
47. Emtner M,PorszaszJ,BurnsM esmtsai: Benefits ofsupplemental oxygen in exercisetraining in nonhypoxemicchronic obstructive pulmonary disease patients. Am J Respir Crit Care Med 2003:168(9): 1034-1042.
48. Stevenson NJ, Calverley PM.: Effect of oxygen on recovery from maximal exercise in patients with chronic obstructive pulmonarydisease. Thorax 2004: 59: 668-672.
49. Lewis CA, Eaton TE, Young P. és mtsai : Short-burst oxygen immediately before and after exercise is ineffective in nonhypoxemicCOPD patients. Eur Respir J 2003: 22:584-588.
50. Christiensen CC, Ryg M, Refvem OK. és mtsai.: Development of severe hypoxaemia in chronic obstructive pulmonary disease patients at 2,438 m (8.000 Ft) altitude. Eur Respir J 2000: 15: 635-639.
51. Nici L, Donner C, Wanters E. és mtsai: American Thoracic Society/European Respiratory Society statement on pulmonary rehabilitation. Am J Respir Crit Care Med 2006: 173:1390-1413.
52. Somfay A.:Pulmonológiai rehabilitáció. Medicina Thoracalis 2002: LV:1-9.
53. Griffits TL, Burr ML, Campbell A. és mtsai: Results at 1 yearof outpatient multidisciplinary pulmonary rehabilitation: a randomised controlled trial. Lancet 2000: 355 : 362-368.
54. Ries AL, Bauldoff GS, Carlin BW és mtsai: Pulmonary rehabilitation. Joint ACCP/AACVRP Evidence Based Clinical
Practice Guidelines. Chest 2007:131(S5): 4S-42S.
55. Chailleux E, Laban JP, Veale D: Prognostic value of nutritional depletion in patients with COPD treated by long-term oxygen therapy. Chest 2003: 123: 1460-66.
56. Schols AM, Wouters EF: Nutritional abnormalities and supplementation in chronic obstructive pulmonary disease. Clin Chest Med 2000: 21(4): 753-762.
57. Steiner MC, Barton RL, Singh SJ és mtsai: Nutritional enhancement of exercise performance in chronic obstructive pulmonary disease: a randomised controlled trial. Thorax 2003: 58(9): 745-51.
58. MehranRJ, Deslauriers J.: Indications for surgery and patient work-up for bullectomy. Chest Surg Clin N Am 1995: 5: 717-734.
59. Hughes JA, McArthur AM, Hutchinson DC. és mtsai.: Long term changes in lung function after surgical treatment of bullous emphysema in smokers and ex-smokers. Thorax 1984: 39:140-142.
60. Fessler HE, Permutt S.: Lung volume reduction surgery and airflow limitation. Am J Respir Crit Care Med. 1998: 157: 715-722.
61. Naunheim KS, Wood DE, Mohsenifar Z. és mtsai: Longterm follow-up of patients receiving lung-volume-reduction surgery versus medical therapy for severe emphysema by National Emphysema Treatment Trial Research Group. Ann Thorac Surg 2006: 82: 431-443.
62. Arcasor SM, Kotloff RM.: Lung transplantation N EnglJMed 1999: 340: 1081-1091.
63. Hosenpud JD, Bennet LE, Keck BM. és mtsai: The Registry of the International Socety for Heart and Lung Transplantation:fifteenth official report- 1998. J Heart Lung Transplant 1998:17:656-668.
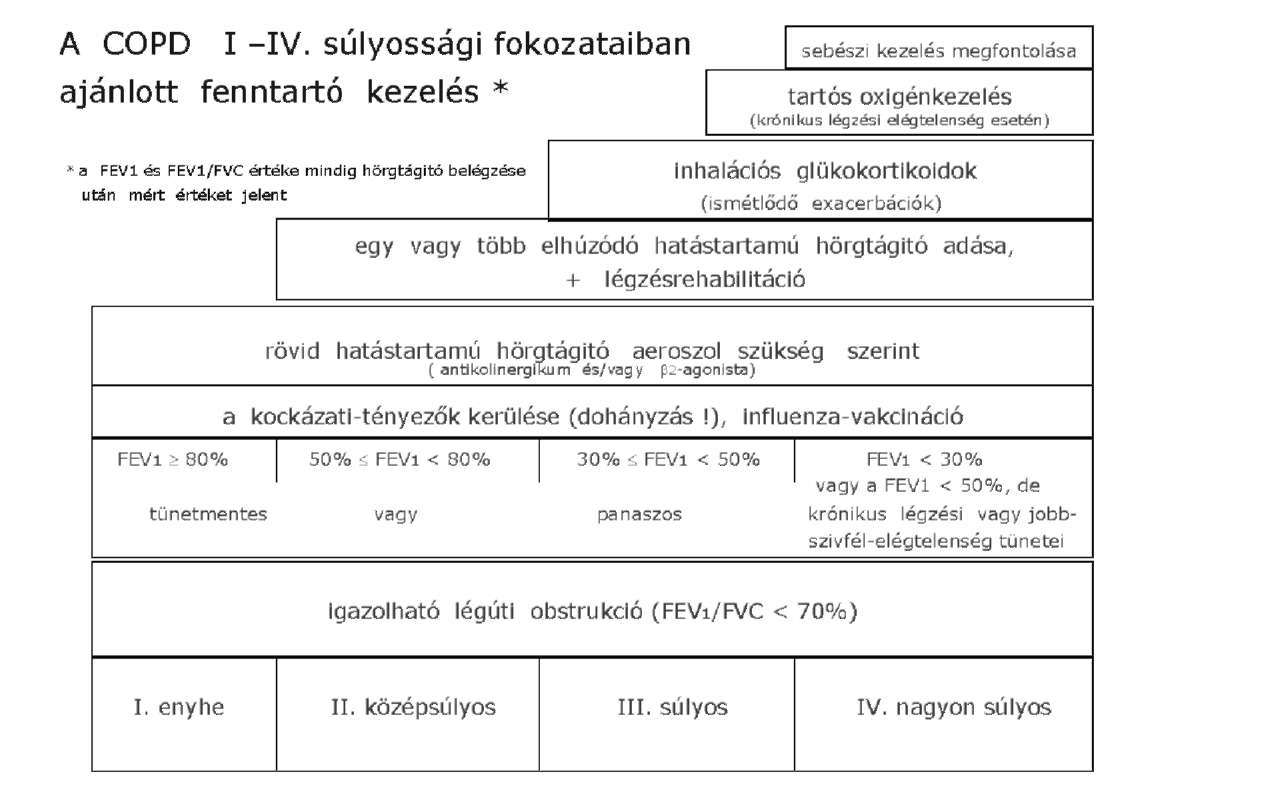
5.1. ábra
A krónikus obstruktiv tüdó'betegségben (COPD) alkalmazott hörgtágító és gyulladáscsökkentő gyógyszerek formái és adagjai
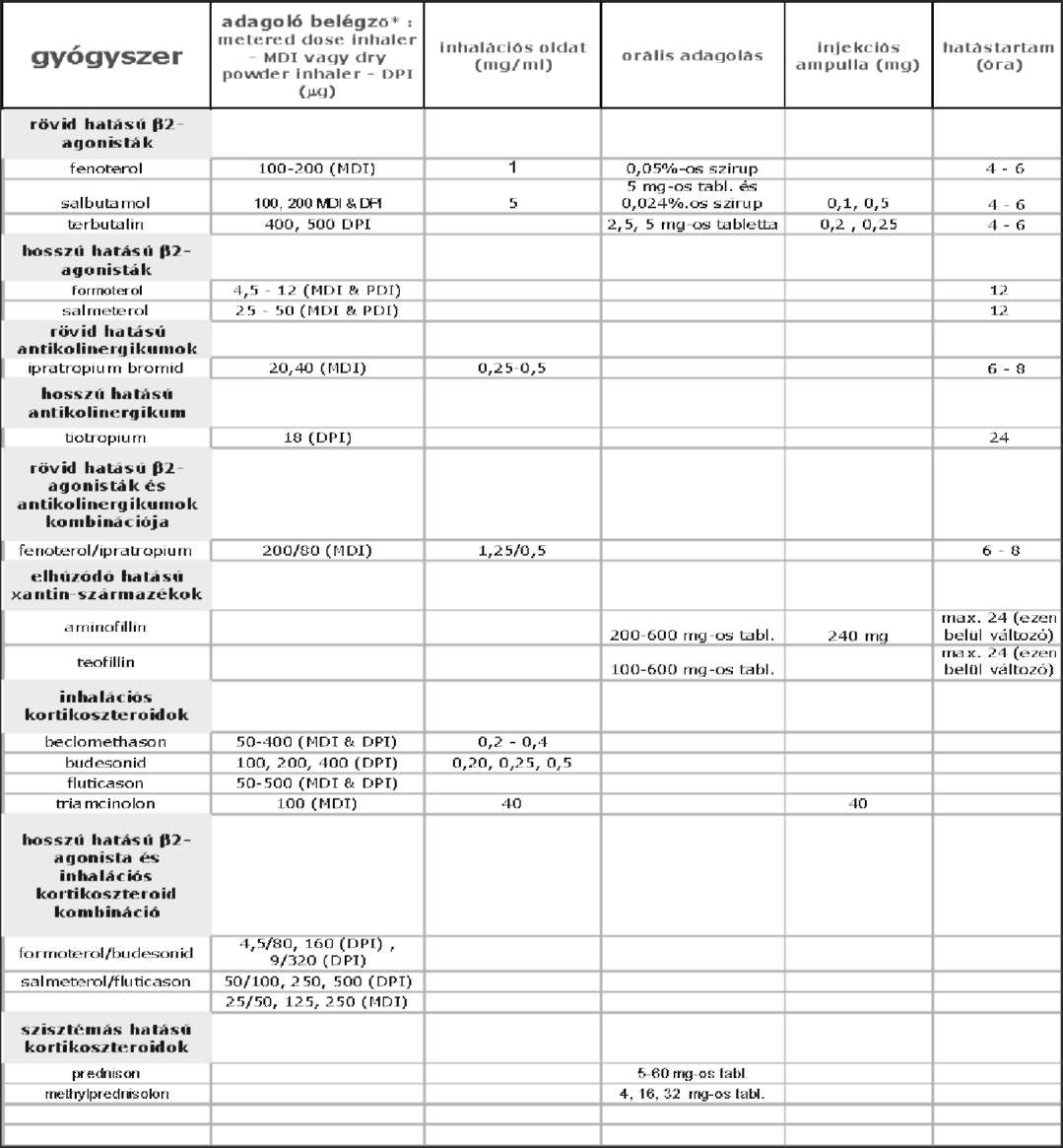
*MDI:metered dose inhaler (meghatározott dózist adagoló inhalátor), DPI: dry powder inhaler (száraz poradagoló inhalátor)
5.2. ábra
5. A COPD akut exacerbációinak kezelése 5.1. Definició, súlyossági besorolás
ACOPDakutexacerbációjaa beteg állapotánakelhúzódó (legalább két napon át) tartó rosszabbodása, amely hirtelen kezdődik, meghaladja a panaszok (dyspnoe, köhögés és/vagy köpetürítés) napi ingadozását és az alapbetegség fenntartó kezelésének megváltoztatását teszi szükségessé12.
A krónikus bronchitis akut exacerbációinak oka összetett: vírusinfekció vagy a légszennyezés fokozódása súlyosbíthatja a krónikus légúti gyulladást és így megkönnyíti másodlagos bakteriális infekciók kialakulását, súlyosbodását (amelyek forrása legtöbbször a felső és alsó légúti bakteriális kolonizáció). Bizonyos esetekben új bakteriális törzsek megjelenése okozza az exacerbációt3.
Ma, a források többsége, az akut exacerbációk kb. 50% -át tartja bakteriális infekció következményének. Fontos hangsúlyozni, hogy az esetek legalább 20 - 25%-a nem purulens, hanem un. mucoid exacerbáció, amelyeket nem bakteriális infekció okoz 4,5.
Újabb közlések, főként a virusdiagnosztika fejlődésének eredményeként, az infekciós eredetet magasabb százalékban adják meg: virális/bakteriális infekció az akut exacerbációk 78 %-ában (virális 48 %, bacteriális 58 %) igazolható 6. A légúti neutrofilia az összes infekciós eredetű akut exacerbációban megjelenik az indukált köpetmintában, míg az eosinophilia elsősorban a virusinfekció okozta exacerbációkat jellemzi . A virus- vagy a virális/bakteriális infekciókokozta exacerbációk klinikai lefolyása súlyosabb, mint a csak bakteriálisakfertőzéseké. Az akut exacerbáció tüneteit a következő betegségek utánozhatják: pneumonia, pneumothorax, balkamra-elégtelenség,tüdőembolia,felső légúti obstrukció, progrediáló bronchusrák, altatószer mérgezés, diabetes, éhezés, agyvérzés stb. Ezek kizárása legtöbbször csak kórházi/klinikai osztályon lehetséges.
Az exacerbáció súlyosságának megítélése : itt figyelembe kell venni a COPD súlyosságát, a kísérő betegségeket és a megelőző exacerbációk kórlefolyását. A fizikális vizsgálatkor a kóros haemodinamika és a légzőrendszer tüneteit regisztráljuk. A diagnosztikus lépések a vizsgálat helyétől függően változnak . A pontos súlyossági besoroláson a beteg élete múlhat ( 6.1. ábra ).
Az exacerbációk I., II. és III. súlyossági fokozatba sorolhatók: I .fokozat: otthon kezelhető a beteg,
II. fokozat: a beteg kórházi elhelyezést igényel,
III. fokozat: légzési elégtelenség áll fenn - intenzívosztályos elhelyezés mérlegelendő 7.
6.1. ábra A COPD akut exacerbációinak súlyossági fokozatai
| I. fokozat | II.fokozat | III.fokozat | |
| Anamnézis | |||
| kísérő betegség# | + | +++ | +++ |
| exacerbációk gyakorisága | + | +++ | +++ |
| a COPD súlyossága | enyhe/mérsékelt | mérsékelt/súlyos | súlyos |
| (I,II) | (II,III) | (IV) | |
| Fizikális lelet | |||
| haemodinamikai értékelés | stabil | stabil | stabil/instabil |
| légzési segédizmok használata, | nincs | ++ | +++ |
| tachypnoe | nincs | ++ | +++ |
| kezdeti terápia után perzisztáló tünetek | nincsenek | ++ | +++ |
| Diagnosztikus eljárások | |||
| oxigén-szaturáció | igen* | igen | igen |
| artériás vérgáz | nem | igen | igen |
| mellkas röntgen | nem | igen | igen |
| kémiai laborl | nem | igen | igen |
| gyógyszer vérszint+ | ha lehet | ha lehet | ha lehet |
| köpet Gram festés és tenyésztés | nem§ | igen | igen |
| EKG | nem | igen | igen |
Magyarázat:
+ nem valószínű, ++ valószínű, +++ nagyon valószínű
#a COPD akut exacerbációjának rossz prognózisát jelentő kisérő betegségek: szívelégtelenség, koszorúsér-betegség, diabetes mellitus, vese- és máj elégtelenség
*tüdőgondozó segitségének igénybevétele (ha a háziorvos nem rendelkezik pulzus oxyméterrel) 1 laboratóriumi vizsgálatok: vérkép, szérum-elektrolytek, vese és májfunkciók +akkor, ha a beteg theophyllint, digoxint, carbamazepint vagy acenokumarolt szed § ajánlott, ha a beteg a közelmúltban szedett antibiotikumot
5.2. Antibiotikumok
A COPD akut exacerbációi idején a mély légúti váladékmintákból kitenyészthető kórokozók a gyakoriság sorrendjében: Haemophilus influenzae, Haemophilus parainfluenzae, Streptococcus pneumoniae és Moraxella catarrhalis 4,9, de kórokozó lehet, a szokványos módszerekkel nem tenyészthető, Chlamydia pneumoniae és Mycoplasma pneumoniae is.
Változatlanul érvényesek az ún. Winnipeg kritériumok (fokozott dyspnoe, a köpet gennytartalmának, illetve mennyiségének fokozódása), amelyek alapján az exacerbáció három típusa különíthető el. Eszerint az I-es és II-es típusú exacerbáció, ahol az előbbi tünetek közül mindhárom vagy kettő fennáll, feltételezhetően bakteriális infekció következménye és az antibiotikum terápia várhatóan hatásos, míg a III-as típusú, a három exacerbációs tünet közül csupán egyet mutató formában a spontán gyógyhajlam jó, az antibiotikum kúra hatása a placeboéval azonos volt 5. Exacerbáció során purulens köpet jelenléte azonban önmagában is elegendő indikációja az antibiotikum-kúra elkezdésének (C bizonyiték) 10.
Az antibiotikum-választást az exacerbáció klinikai súlyossága határozza meg ( 6.2. ábra ). A klinikai súlyossághoz hozzárendelhetők a kórokozóként szóba jövő mikrobák. Ezek alapján a 6.3. ábrán felsorolt antibiotikumok választhatók 11.
Az akut exacerbáció kimenetelét rontó tényezők: elsősorban az alapbetegség (COPD) súlyossága kísérőbetegségek jelenléte, évente háromnál több exacerbáció, három hónapon belül történt antibiotikum kezelés.
A P. aeruginosa-infekció kockázatát fokozó körülmények: kórházi ápolás a közelmúltban, gyakori antibiotikum adása (az előző év során legalább 4 kúra), a tünetek alapján súlyos exacerbáció és egy korábbi, stabil állapotban kolonizáló
P. aeruginosa izolálása.
A COPD súlyos, kórházi kezelést igénylő exacerbációiban a megfelelő antibiotikum kiválasztása életmentő lehet ( B bizonyiték)12,13,14.
Magyarországon a S. pneumoniae törzsek amoxicillin-rezisztencia gyakorisága kb. 14 % (ez elsősorban a harmadik generációs orális cephalosporinok hatásvesztésével párosul), a makrolid rezisztenciáé kb. 40 %. Ez utóbbi körülményt a COPD akut exacerbációinak enyhébb formáiban is ajánlott mérlegelni 15,16.
| csoport | definició | leggyakoribb kórokozók |
| A-csoport | enyhe exacerbáció, a kimenetelt rontó tényező nélkül | S. pneumoniae, H. influenzae, M. catarrhalis, Chlamydia pneumoniae, vírusok |
| B-csoport | mérsékelten súlyos exacerbáció, a kimenetelt rontó valamely tényező jelenlétével | A-csoport + penicillin rezisztens S. pneumoniae, Enterobacteriaceae (K. pneumoniae, E. coli, Proteus) |
| C-csoport | súlyos exacerbáció, P. aeruginosa veszélye mellett | B-csoport + P. aeruginosa |
6. 2. ábra A COPD akut execerbációinak leggyakoribb kórokozói
| csoport | orális kezelés | további orális terápiás lehetőségek | parenterális kezelés |
| A-csoport | béta-laktámok (béta-laktamáz aktivitású baktérium esetén nem megfelelő), tetracyclin, trimethoprim-sulfamethoxazol | béta-laktamáz inhibitor + béta-laktámantibiotikum, makrolidek, II.,III. generációs cefalosporinok | |
| B csoport | béta-laktamáz inhibitor + béta laktamáz | respirációs fluorokinolonok | béta-laktamáz inhibitor + béta laktám antibiotikum, generációs cefalosporinok, respirációs fluorokinolonok |
| C csoport | fluorokinolonok (ciprofloxacin, levofloxacin ) | anti-pseudomonas béta laktám, fluorokinolonok (levofloxacin, cipro-floxacin) |
6.3. ábra Az exacerbáció súlyossága alapján valószinűsitett kórokozók és az ezekre ható antibiotikumok
5.3. Hörgtágítók
A fenntartó kezelés módosítása szükséges, ha az obstrukció fokozódik. A COPD exacerbációinak otthoni ellátásakor emelni kell a rövid hatású, elsősorban inhalált L2-receptor agonista hörgtágitó dózisát és/vagy adagolásának gyakoriságát (A bizonyiték ).
A legmagasabb ajánlható adag rövid hatású LVreceptor agonista adagoló aeroszolból 3-400 mg 1-2 óránként, amíg a panaszok nem enyhülnek17,18. A mellékhatások (tremor, tachycardia, szívritmuszavarok) fokozódnak az adag emelésével (ilyenkor rövid hatástartamú antikolinerg hörgőtágitó ipratropiummal kombinálhatjuk a a2-agonista aeroszolt). A L-sympathicomimeticum adagjának óvatos titrálása javasolt, ha a beteg coronariabetegségben, balkamra-elégtelenségben szenved vagy tudomásunk van korábbi sziv-ritmuszavarokról.
Az ipratorpium bromid hatása megközeltően azonos a rövid hatástartamú L2-sympathicomimeticumokéhoz, a két hörgtágitó kombinációja ajánlott a COPD akut exacerbációiban (A bizonyiték). Ipratropium bromid monoterápia csak akkor ajánlható, ha a [^-receptor agonista aeroszol effektivitása gyenge vagy a beteg nem tolerál nagy adagokat az utóbbi gyógyszerből ( B bizonyiték)17,18.
Széles körű elterjedtségük ellenére a methylxanthinok alkalmazása COPD exacerbációban ellentmondásos. Ma a methylxanthinokat (theophyllin vagy aminophyllin) másodvonalbeli i.v. terápiaként fogadják el, amennyiben a rövid hatású hörgőtágítók hatása elégtelen (B bizonyiték)19. Hörgőtágitó hatásuk csekély és nem konzisztens, ugyanakkora mellékhatások gyakran súlyosak , ezért akut exacerbációban mellőzésük javasolt.
5.4. Glükokortikoszteroidok
A szisztémás hatású glükokortikoszteroidok meggyorsitják a gyógyulást és a légúti funkció visszatérését a kiindulási értékre a COPD akut exacerbációiban (A bizonyiték) 20,21,22. Az emelt dózisú hörgőtágító kezelés kortikoszteroiddal való kiegészítése különösen fontos akkor, ha a mért FEV1 alacsonyabb a referenciaérték 50%-nál. Az ajánlott napi szteroidmennyiség 40 mg metilprednisolon 10 napon át (C bizonyiték )23.
A COPD súlyos esetei kórházban kezelendők. A kórházi beutalás kritériumai a következők: a beteg zavart, aluszékony, nyugalmi légszomja van, a légzésszám >25/perc, a pulzusszám >120/perc, mélyülő cyanosis, az inspiratorikus segédizmok használata. A tudatzavar önmagában, míg a többi tünetből kettő megléte indokol kórházi beutalást. Ugyanígy kórházi kezelés ajánlott akkor, ha a COPD exacerbációjának súlyossága az előbbinél enyhébb ugyan, de a beteg súlyos COPD-ben szenved, jelentős kísérő betegségei vannak, új keletű ritmuszavar észlehető, vagy otthoni ápolása, felügyelete megoldhatatlan 24. Néhány beteg, a súlyos légzési elégtelenség okozta együttműködési képtelenség, kóma miatt, közvetlenül intenzívosztályos felvételt igényel.
5.5. Kontrollált oxigén terápia
Az oxigénpótlás az akut COPD-exacerbáció kórházi kezelésének a sarokköve. A cél: megfelelő oxigén-szint elérése (PaO2 >60 Hgmm vagy SaO2 >90%), anélkül, hogy veszélyes PaCO2-emelkedést okoznánk. Az oxigén kezelés megkezdését követően 30-60 perc múlva artériás vérgáz-vizsgálat szükséges annak megítélésére, hogy nem alakult-e ki szignifikáns CO2 retenció ill. acidózis?
Az oxigénpótlás súlyos esetekben gyakran , orrszonda helyett, csak maszkkal lehetséges.
5.6. Nem-invazívgépi lélegeztetés (NIV)
Az intermittáló NIV csökkenti a respiratórikus acidózist (csökkenti a PaCO2-t emeli a pH-t), mérsékeli a légzésszámot, a dyspnoe súlyosságát és megrövidíti a kórházi tartózkodás idejét (A bizonyiték). Alkalmazásakor csökken az intubáció,a kontrollált gépi légzéstámogatás igénye25. A NIV kudarca esetén, az intubációt követően kontrollált gépi lélegeztetés vezetésére alkalmas osztály elérhető közelségben legyen !
Irodalom
1. Rodriguez-Roisin R: Toward a consensus definition for COPD exacerbations. Chest 2000:117(Suppl 2): 398S-401S
2. Bürge S, Wedzicha JA: COPD exacerbations:definitions and classifications. Eur. Respir. J. 2003: 41(Suppl): 46S-53S
3. Sethi S, Evans N, Grant BJ és mtsai: New strains of bacteria and exacerbations of chronic obstructive pulmonary disease. N.Engl. J. Med. 2002:347: 465-471.
4. Sethi S: Infectious origin of acute exacerbation of chronic bronchitis. Chest 2000:117:380S-385S
5. Anthonisen NR, Manfreda J, Warren CPW és mtsai: Antibiotic therapy in exacerbations of chronic obstructive pulmonary disease. Ann. Intern. Med. 1987:106:196-204.
6. Papi A, Bellettato CM, Braccioni F és mtsai: Infections and airway inflammation in chronic obstructive pulmonary disease severe exacerbations. Am J Respir Crit Care Med 2006: 173: 1114-1121.
7. ConnorsAF,Jr,Dawsnon NV,ThomasCésmtsai: Outcomes following acuteexacerbation ofseverechronicobstructive lung disease. The SUPPORT Investigators (Study to Understand Prognosis and Preferences for Outcomes and Risks of Treatments). Am J Respir Crit Care Med 1996:154(4 Pt 1):959-967.
8. Celli BR, MacNee W és a bizottsági tagok: Standards for the diagnosis and treatment of patients with COPD: a summary of the ATS/ERS position paper. Eur. Respir. J. 2004: 23:932-946.
9. Sethi S, Wrona C, Grant BJ és mtsai. Strain-specific immune response to Haemophilus influenzae in chronic obstructive pulmonary disease. Am. J. Respir. Crit. Care Med. 2004: 169:448-453.
10. Stockley RA, O'Brien C, Pye A és mtsai: Relationship of sputum colour to nature and outpatient management of acute exacerbations of COPD. Chest 2000: 117:1638-1645.
11. Global Initiative for Chronic Obstructive Lung Disease MCR Vision Inc 2006. www.goldcopd.com
12. Empfehlungen einer Expertkommission der Paul-Ehrlic-Gesellschaft für Chemotherapie: Rationaler Einsatz oraler Antibiotika bei Erwachsenen. Chemother. J. 2002: 11: 47-58.
13. Sethi S, Fogarty C, Fulambarker A: A randomized, double-blind study comparing 5 days oral gemifloxacin with 7 days levofloxacin in patients with acute eacerbation of chronic bronchitis. Respir. Med. 2004: 98:697-707.
14. Wilson R: Bacteria, antibiotics and COPD. Eur. RepsirJ. 2001:17: 995-1007,2001).
15. Konkoly Thege M, Ludwig E és a Mikrobiológiai Munkacsoport: a nosocomiális Gram-negatív patogének, a Streptococcus pneumoniae és a Bacteroides fragilis meropenem és komparatorai iránti érzékenysége Magyarországon - prospektiv, multicentrikus tanulmány. Mikrobiológiai vonatkozások. LAM 2002: 12. különszám, S2-8.
16. Országos Epidemiológiai Központ: a 2006. évi antibiotikum rezisztencia adatai www.oek.hu
17. McCrory DC, Brown C, Gelfand SE és mtsai: Management of exacerbations of COPD: a summary and appraisal of the published evidence. Chest 2001: 119: 1190-1209.
18. Snow V, Lascher S, Mottur-Pilson C: Evidence base for management of acute exacerbations of chronic pulmonary disease. Ann. Intern. Med. 2001: 134: 595-599.
19. Duffy N, Walker P, Diamante Fés mtsai. Intravenous aminophylline in patients admitted to hospital with non-acidotic exacerbations of chronic obstructive pulmonary disease:a prospective randomised controlled trial. Thorax 2005:60: 713-717.
20. Thompson WH, Nielson CP, Carvalho P és mtsai: Controlled trial of oral prednisone in outpatients with acute COPD exacerbation. Am.J.Respir.Crit.Care Med. 1996:154:407-412,1996.
21. Davies L, Angus RM, Calverley PM: Oral corticosteroids in patients admitted to hospital with exacerbations of chronic obstructive pulmonary disease.: a prospective randomised controlled trial. Lancet 1999: 354:456-460.
22. Maltais F, Ostinelli J, Bourbeau J és mtsai: Comparison of nebulized budesonideand oral prednisolone with placebo in the treatment of acute exacerbations of chronic obstructive pulmonary disease: a randomised controlled trial. Am.J.Respir.Crit.Care Med. 2002:165: 698-703.
23. Niewoehner DE, Erbland MR, Deupree RH és mtsai: Effect of systemic glucocorticoids on exacerbations of chronic obstructive pulmonary disease. Department of Veterans Affairs Cooperative Study Group. N.Eng.J.Med. 1999: 340: 1941-1947.
24. Emerman CL, Connors AF, Lukens és mtsai: Relationship between arterial blood gases and spirometry in acute exacerbations of chronic obstructive pulmonary disease. Ann. Emerg. Med. 1989:18: 523-527.
25. Lightowler JV, Wedzicha JA, Elliott MW és mtsai: Non-invasive positive pressure ventilation to treat respiratoryfailure resulting from exacerbations of chronic obstructive pulmonary disease: Cochrane systemic review and meta-analysis. BMJ 2003: 326 (7382) : 185.
7. COPD a háziorvosi gyakorlatban
- A COPD hazánkban is jelentős mértékben aluldiagnosztizált betegség, kezelése is elmarad a szakmai irányelvekben javasolttól. A korai kórisme és az eredményes kezelés érdekében az ismeretek hatékonyabb terjesztése szükséges.
- A 40 év feletti dohányosok közül kerül ki a betegek 85-90%-a, ezért a háziorvos - tüdőgyógyász együttműködés lehet csak eredményes a korai felderítésben és a prevencióban 1,3,5.
- A betegség diagnózisában és kezelésében, gondozásában a spirometria alapvető fontosságú, ezért el kell érni, hogy minden érintettnél megtörténjen ez a könnyen elérhető, egyszerű és olcsó vizsgálat.
- A COPD főleg az idősebb kor betegsége, melyet többször csak későn ismernek fel az ismertebb társbetegségek (pl. hypertonia, ISZB) árnyékában. Ezért a háziorvos-belgyógyász-kardiológus kooperációba be kell vonni a pulmonológusokat is.
A COPD napjainkban növekvő jelentősége két alapvető tényezővel hozható összefüggésbe. A meghatározóbb a betegség fő rizikófaktorának, a dohányzásnak az elterjedtsége, ami hazánkban kb 3,5 millió aktív dohányost jelent. A másik az életkor növekedése és az idősebb korosztály számarányának bővülése, mivel a COPD főleg a 40 év felettiek között fordul elő. A dohányosok 15-20 %-ában alakul ki a progresszív légúti funkcióvesztéssel jellemzett betegség, ami hazánkban közel fél millió embert érint. Nemzetközi statisztikai mutatók is a felnőtt lakosság 5%-a körüli értékeket jeleznek, így a 4-500 ezres hazai betegszám reális lehet. Ezzel szemben a tüdőgondozókban nyilvántartott esetszám 2007-ben 110 ezer volt, vagyis a tényleges esetek 25%-át ismerjük2.
7.1. Diagnosztika
A korai diagnózis az eredményes kezelés alapfeltétele, mivel a progresszív tüdőfunkció - romlás ekkor még hatékonyabban fékezhető. A figyelem felkeltése, a magas kockázatú betegek kiemelése és időszakos követése javasolt.
7.1.1. Légúti tünetek
A betegség leggyakoribb tünete a terhelésre fellépő nehézlégzés és a köhögés. A köhögést a beteg a dohányzás természetes következményének tartja és ezért nem fordul orvoshoz. Fontos a rendszeresen köhögők alaposabb kikérdezése és vizsgálata. A 15-20 csomagév (1 doboz cigaretta elszívása 15-20 éven át) dohányzás bármely mellkasi panasz esetén fel kell hogy keltse COPD gyanúját is.
Az effort dyspnoe csak akkor tudatosul a betegben, amikor a funkcióromlás előrehaladott és a légzési tartalékok közel fele (FEV1 kb. 50 %) már elveszett. A terhelésre fellépő légszomjat sokan az évek múlásával magyarázzák. A napi gyakorlatban használható a brit Medical ReseachCouncil (MRC) dyspnoe skálája, ami nemcsaka kórisme felállításában, hanem a betegség gondozásában is könnyen használható ( 7.1. ábra).
7.1. A dyspnoe súlyossági fokozatai
| fokozat | a dyspnoe mértéke |
| 0 | csak erős terhelésre fullad |
| 1 | sietéskor vagy lejtőn felfele dyspnoe |
| 2 | sík talajon csak lassabban tud menni kortársainál, vagy saját ritmusában sem tud tartósan sétálni |
| 3 | 100 m megtétele után fullad |
| 4 | nem tud otthonról elmenni fulladás miatt |
| 5 | nyugalomban is fullad |
7.1.2. Spirometria
A COPD diagnózisához elengedhetetlen vizsgálat. Az erőltetett kilégzési másodperctérfogat (FEV1) és az erőltetett kilégzési vitálkapacitás (FVC) aránya alapján lehet a légúti obstrukciót véleményezni. Mivel asztmában reverzibilis a hörgők szűkülete, ezért a hörgőtágító (2-400 ég salbutamol) adását követően megismételt vizsgálat a kórjelző. Minél kisebb a bronchodilátorra adott válasz és minél nagyobb a reziduális áramláskorlátozottság, annál nagyobb a COPD fennállásának a valószinűsége. Ha a FEV1/FVC hörgtágitó belégzése után 0,7 felett marad, akkor a COPD fennállása nem valószinű.
Ezt követően a FEV1 értékei alapján történik a súlyossági fokozat megállapítása is (enyhe, mérsékelten súlyos, súlyos, nagyon súlyos). Így a spirometria a gyógyszeres kezelés beállításához és az állapot nyomonkövetéséhez is nélkülözhetetlen.
A spirometria egyszerű, olcsó, a háziorvosi praxisban is művelhető vizsgálat, de csak megfelelő minőségű műszerrel és alkalmazására kiképzett személyzettel ad megbízható eredményt. Bármely feltétel hiánya esetén nemcsak az alul-, hanem a túldiagnosztizálás torzításával is számolni kell. Jelenleg a spirometria rutinszerű művelése nem általános a hazai praxisokban, ezért a tüdőgyógyászati szakrendelések, tüdőgondozók konzíliumát kell igénybe venni, ahol az korlátozás nélkül hozzárférhető.
A kilégzési csúcsáramlás (PEF) mérése durva tájékozódásra alkalmas lehet, de nem helyettesítheti a spirometriát.
7.2. Társbetegségek
A 40 év feletti, főleg dohányos egyénekben a COPD mellett több betegség is fennálhat. Leggyakrabban a hypertonia, ISZB és tüdőrák társulásával kell számolni. Ezekre a dohányzás önmagában is nagyobb esélyt teremt, de COPD esetén a tüdőrák és a szívbetegség rizikója tovább emelkedik. Ezért fontos, hogy a háziorvosi gyakorlatban a szív-érrendszeri betegségekhez hasonló hangsúlyt kapjanak a dohányzással szorosan összefüggő tüdőbetegségek, mint a COPD és a tüdőrák. Nem ritkán találkozunk olyan esetekkel, amikor a mellkasi panaszok hátterében nem a kardiovaszkuláris kórkép, hanem a COPD a meghatározó, de érdemi diagnosztikára (légzésfunkció, vérgáz) csak későn kerül sor. A szívelégtelenség nemcsak a hypertonia, ISZB, hanem a COPD progressziója során kialakuló pulmonális hypertonia következménye (cor pulmonale) is lehet.
A COPD patológiájában a krónikus gyulladás a meghatározó, ami a domináló légzőrendszeri elváltozások mellett szisztémás manifesztációt (pl. vázizom-diszfunkció, izomvesztés, osteoporosis, szív-érrendszeri komplikációk) is eredményezhet. A szisztémás gyulladás egyik markere, a C-reaktív protein, ami COPD-s betegekegy részében tartósan is magas lehet, az atherosclerosis kialakulását is elősegíti.
7.3. Gyógyszeres terápia
A bronchodilatátorok rendszeres alkalmazása a COPD-s tünetek enyítésének legfontosabb módszere. Leghatásosabb az inhalációs bevitel, de a technikát rendszeresen ellenőrizni kell. Hajtógázas adagoló aeroszolok esetén előtét alkalmazása növeli a kislégúti depozíciót. Ha a rövid hatású antikolinerg és/vagy béta-2 agonista szerekkel a tüneti kontroll nem megfelelő, tartós hatású antikolinerg és/vagy béta-2 agonista inhalációs készítmények alkalmazandók, melyek csökkentik az akut exacerbációk gyakoriságát és javítják az életminőséget. Ezek napi egy vagy kétszeri alkalmazásával jobb compliance tartható fenn. Az orális teofillin készítmények additív hörgőtágítást eredményezhetnek, de a gyakori mellékhatás és a szűk terápiás spektrum miatt csak az előző terápia nem kielégítő hatása esetén javasolt. A porlasztóval (kompresszoros vagy ultrahangos) történő otthoni hörgőtágító kezelés drága, csak a súlyos COPD-sek kis hányadánál javasolt, főleg exacerbációk időszakában.
A kortikoszteroidoka COPD-s légúti gyulladást-szemben az asztmás gyulladással - nem kellő hatékonysággal képesek csak fékezni. Inhalációban alkalmazzuk magas dózisban. Súlyos (GOLD III-IV. stádium) esetekben indokolt adásuk, ha évente legalább 2-3 akut exacerbáció fordul elő. Ezen betegcsoportban - főleg tartós hatású R2-receptor agonistával kombinációban alkalmazva - hatékonyan csökkentik a heveny fellángolások számát, így hozzájárulnak a kórlefolyás mérséklődéséhez.
Köptetők közül a carbocistein és acetylcistein készítmények - antioxidáns hatásuk miatt - produktív köhögés esetén megfontolandók.
A tartós gyógyszeres kezelés eredményességének, indikációjának elbírálásra félévenként szakorvosi ellenőrzés javasolt.
7.4. Otthoni oxigénkezelés
Akkor indokolt, ha az egyensúlyi állapotban lévő, súlyos COPD-s betegben tartós hypoxaemia áll fenn (az artériás vér oxigén parciális nyomása kisebb mint 55 Hgmm vagy pulzoximetriával mért szaturáció 88% alatt van, illetve a PaO2 55-60 Hgmm közötti értéke mellett a jobszívfél elégtelenség tüneteit észleljük). Fontos a kórházban kititrált dózírozás (általában 1-2 l/min, legalább napi 16 órán át), mert csak a folyamatos használat mellett javul a túlélés, csökken a policitémia és nem progrediál a pulmonális hypertonia. A tudati állapot romlása esetén gépi légzéstámogatás igénye merülhet fel, ezért azonnal kórházba kell juttatni a beteget.
Dohányzás rontja az oxigénkezelés hatékonyságát, veszélyes is lehet, ezért a leszokás támogatásában feltétlenül eredményt kell elérni.
Az indikáció tartós fennállását félévenként vérgáz vizsgálattal kell igazolni.
7.5. Akut exacerbáció
Jelentős epizód a COPD-s betegek életében, főleg a súlyos esetekben és téli időszakban gyakoribb. A tünetek tartós, több napon át észlelt rosszabodása, ami a gyógyszerelés átmeneti megváltoztatását teszi szükségessé. Fokozódó dyspnoe, fokozódó mennyiségű és purulenciájú köpet hívja fel a figyelmet.
Akut exacerbációban a gyors hatású bronchodilatátorok adagjának növelése mellett 10-14 napig orális szteroidot adunk napi 40 mg metilprednizolon formájában.
Antibiotikumot infekcióra utaló jelek társulása (pl. fokozódó mennyiségű és purulenciájú köpet, láz) esetén alkalmazunk a feltételezett kórokozó és a helyi rezisztencia-adatok alapján empirikusan. A széles spektrumú antibiotikumokat (légúti fluorokinolonok) az elsődleges antibakteriális kezelésre nem reagáló vagy a kis tartalékokkal (FEVi < 50%) rendelkező, súlyos COPD-sekre célszerű tartalékolni, esetenként törekedni kell bakteriológia és rezisztencia alapján történő célzott kezelésre.
Az exacerbáció kórházi kezelése szükséges, ha a beteg állapota tovább romlik, vagy az alábbiakat észleljük: romló tudati állapot, aluszékonyság, fokozódó dyspnoe, cyanosis, perifériás oedema, súlyos társbetegségek, rossz szociális helyzet.
Az exacerbáció megelőzésére évente influenza oltás javasolt. Bár kevesebb bizonyíték támogatja hatékonyságát COPD-ben, de súlyos esetekben 5-6 évente Pneumococcus elleni védőoltás is javasolt.
7.6. Rehabilitáció
Mivel a légúti obstrukció COPD-ben nem teljesen reverzibilis, gyógyszeres kezelés önmagában nem elegendő a panaszmentes életvitelhez. A légszőszervi rehabilitációval igazoltan
- csökken a dyspnoe
- jobb funkcionális állapot érhető el nyugalomban és terheléskor
- javul az egészségi állapottal összefüggő életminőség
Azoknak a COPD-seknek kell elérhetővé tenni, akik a betegségük miatt korlátozottnak érzik magukat napi tevékenységükben. Sarokköve az egyénileg előírt terheléses tréning, kiegészítve légzőgyakorlatokkal, étrendi javaslatokkal, gyógyszerelési és életvezetési tanácsokkal. Már az akut exacerbáció miatti hospitalizáció időszakában elkezdhető és tüdőgondozókban folytatható az optimálisan 8 hetes program. Az aktivitás megőrzése azt követően is fontos, ennekellenőrzésében a háziorvos támogatása segíthet. Otthoni oxigénkezelésben részesülőknél is indokolt, a szükséges mobilitás folyékony oxigénnel biztosítható.
7.7. Megelőzés
A dohányzásról leszokás támogatásában a szükséges pszichés vezetés mellett a farmakoterápiás lehetőségek (nikotin tartalmú szerek, bupropion, vareniclin) is rendelkezésre állnak, melyekkel a nikotin elvonás tünetei hatékonyan mérsékelhetők. Mivel legfeljebb 3 hónapig szedhetők és ezalatt a dohányzást teljesen el kell hagyni, jelentős anyagi többletkiadást nem kell viselni a betegnek.
A leszokást segítheti, ha a beteg szembesül csökkent spirometriás-értékeivel már a betegség korai stádiumában, mielőtt a lényeges panaszok megjelennének. Tudomására kell hozni az a fenyegető tényt, hogy ennek gyors ütemű romlása várható, ha nem hagy fel a dohányzással. Ezért fontos, hogy valamennyi 40 év feletti köhögő dohányosban időszakos spirometriás vizsgálat is történjen. Tüdőgyógyászati szakrendelésen ezzel egy időben mellkas rtg is készülhet, ami a tüdőrák korai felismerését is segítheti. Ezen gyakorlat támogatása a háziorvosok szerepvállalása nélkül nem lehet sikeres, mert ezt a veszélyeztetett csoportot ők tudják hatékonyan elérni és a megfelelő segítséghez hozzájuttatni. Hazai spirometriás szűrés is igazolta, hogy célzott vizsgálattal hatékonyan -10% feletti találati aránnyal -lehet a COPD-t diagnosztizálni 4.
Irodalom
1. Global Initiative for Chronic Obstuctive Lung Disease. Global strategy for the diagnosis, management, and prevention of chronic obstrucitve pulmonary disease, 2006. www.goldcopd.com
2. A pulmonológiai intézmények 2007. évi epidemiológiai és működési adatai. Országos Korányi TBC és Pulmonológiai Intézet, 2006, Budapest
3. Bellamy D, Brooker R: COPD az alapellátásban. Springmed, Budapest, 2006
4. Somfay A, Jeney E: Spirometriás szűrés COPD-ben országos reprezentatív minta alapján. Medicina Thoracalis 2006; 59:2-6.
5. Háziorvostani Szakmai Kollégium: A felnőttkori krónikus obstruktiv légzőszervi betegségek (COPD) háziorvosi ellátása. Háziorvos Továbbképző Szemle 2007:12: 633-638.
A szakmai irányelv érvényessége: 2010. szeptember 30.
Az Egészségügyi Minisztérium
szakmai protokollja
Az egészséges csecsemő (0-12 hónap) táplálásáról
Készítette: a Védőnői Szakmai Kollégium
I. Alapvető megfontolások
Az egészséges csecsemő optimális táplálási módja a 6 hónapos korig tartó - a csecsemő igénye szerinti - kizárólagos szoptatása, amely - kiegészítő táplálás mellett - egyéves korig a domináns táplálási mód.
A védőnői ellátás célja a táplálással kapcsolatos ismeretek biztosítása az anya számára, döntéseinek elősegítése a különböző táplálási elvekkel, módszerekkel kapcsolatban.
1. Alkalmazási/érvényességi területe
A védőnő a jogszabályok (ld. a IV. sz. fejezetben) és a szakma szabályai alapján [A védőnő preventív alapfeladatai, kötelezettsége és felelőssége a megelőző ellátásban OTH 2004.; "A védőnői ellátás folyamata" I.3. A Magyar Egészségügyi Ellátási Standardok Kézikönyve MEES], komplex csecsemőgondozást végez az alapellátás keretében a családokotthonában és a védőnői tanácsadóban, valamint közösségi -egészségfejlesztésre alkalmas -helyszíneken.
1.1. Protokoll témájának megválasztása, témaválasztás indoklása
A csecsemő táplálása egész további életére meghatározó, amelyet az Egészségügyi Világszervezet és a szakmai tudományos publikációk is alátámasztanak. Az egészséges csecsemő korszerű táplálása, a szülők egységes szakmai irányelvek alapján történő tájékoztatása és támogatása mellett valósulhat meg.
1.2. A protokoll célja
Az egészséges csecsemő szoptatásához és hozzátáplálásához szükséges alapelvek és tevékenységek összefoglalása.
1.3. A protokoll célcsoportjai
Az alap- és szakellátásban dolgozó védőnők.
2. Definíciók, rövidítések
A szoptatással és a csecsemőtáplálással kapcsolatos fogalmak: Az egészséges csecsemő fogalma:
Jelen protokoll tekintetében a betöltött 37. gesztációs hétre, legalább 2500 gramm születési súllyal született újszülött, akikre az alábbiak jellemzők a megszületés után:
- születési súlya legfeljebb 7-10 %-kal csökken
- 14. életnapra visszanyeri a születési súlyát
- életnapig legalább három székletet ürít, amelynek színe életkorának megfelel (az első széklet általában az első 24 órában ürül)
- a 4. naptól kezdve naponta legalább 6-szor kellően nedves a pelenkája, vizelete víztiszta vagy halványsárga (az első vizelet általában az első 8 órában ürül)
- időkorlátozás nélkül szopik, naponta átlagosan legalább 8 szor (általában 8-16-szor)
- súlya korának megfelelő ütemben gyarapodik
A WHO a csecsemőtáplálás módját - a szoptatás /anyatejes táplálás szempontjából - a következő módon határozza meg:
Kizárólagos szoptatás
A csecsemő anyatejet - beleértve a saját anya lefejt tejét és az idegen női tejet - kap. Ez a definíció megengedi a vitaminok, ásványi anyagok, és gyógyszerek csepp és szirup formában történő adását és az ORS-t (orális rehidráló folyadék), de ezen kívül semmi mást.
Szoptatás folyadék-kiegészítéssel / Túlnyomó szoptatás/
A kizárólagos szoptatás definíciójától abban különbözik, hogy az ott megfogalmazottakon túl, folyadék (víz, víz-alapú italok, gyümölcslé) adását is megengedi, de ezen kívül semmi egyebet (nem érthetők bele a humán tej, tápszer, egyéb étel alapú folyadékok).
Szoptatás kiegészítő táplálással - Kevert táplálás /Hozzátáplálás/
Az anyatej mellett minden egyéb adása. Szolidok (az anyatejen és tápszeren kívüli ételek) vagy nem-humán tej és tápszer adása. Ez a definíció nem tesz különbséget olyan táplálási módok között, amikor az anyatejen kívül csak tápszert, csak nem-humán tejet, csak szilárd és pépes ételeket vagy ezeket különböző kombinációban vagy arányban alkalmazzák.
Ugyancsak nem veszi figyelembe, hogy a 24 órás táplálékban milyen az anyatej aránya. Mesterséges táplálás /a szoptatás/ anyatej hiánya/
Bármelyétel vagy folyadék - beleértve a nem-humán tejet és tápszert - anyatej ill. idegen női tejnélküli táplálás. A csecsemő igénye szerinti szoptatás:
A csecsemő minden alkalommal mellre kerül, amikor jelzi szopás iránti igényét. A szoptatások gyakorisága és időtartama nem korlátozott, játszó-, nyugtató cumit nem használ.
Komfortszopás:
A szopás nemcsak a táplálkozásra fordított időre korlátozódik, hanem ettől függetlenül további igény jelentkezik a szopásra, amely az anyától és a csecsemőtől függően tetszőleges ideig eltarthat. Ezt az igényt a csecsemő ideális esetben az anyamellen elégíti ki.
Elválasztódás
A csecsemő maga határozza meg, hogy nem fogadja el a szopást, mint táplálási módot ("kinövi") és a szopást magától (külső segítség nélkül), fokozatosan abbahagyja. A szopás hirtelen abbahagyása nem elválasztódás, hanem szopási sztrájk, amin át kell segíteni a csecsemőt.
Elválasztás
A szopás nem a csecsemő döntése alapján szűnik meg. Az elválasztás hátterében az anya döntése, valamint egészségügyi- és szociális változások állhatnak.
Tandem-szoptatás
Az anya folytatja a szoptatást a következő várandósság alatt, majd egyszerre szoptatja a két különböző várandósságból született gyermekét.
3. Az állapot leírása
3.1 Kiváltó tényezők:
A születést követően a tejelválasztás hormonális és reflexesen szabályozott élettani folyamat.
3.2 Genetikai háttér: Nem bizonyított.
3.3 Incidencia /Prevalencia/ Népmozgalmi adatok:
Az anyák 97%-a képes szoptatni gyermekét, ha helyes információkhoz jut, és támogatást kap a családjától, a közösségtől és az egészségügyi szakemberektől. Hazánkban a hazabocsátott újszülöttek 61,3 %-a 3 hónapos koráig kizárólag szoptatott volt, hathónapos korban a csecsemők 43,9%-a volt kizárólag szoptatott. Hat hónapos kor után is anyatejet kapott csecsemők aránya 55,1 %, egy éves kort követően is kapott anyatejet a kisdedek 32.1 %-a. (2007. év KSH-OTH adat)
3.4 Jellemző életkor és nem:
- csecsemő hat hónapos koráig kizárólagosan szoptatott
- csecsemő hat hónapos koráig kiegészítő táplálásban részesült
- csecsemő hat hónapos koráig mesterségesen táplált
- csecsemő hat hónapos korát követően is kizárólagosan szoptatott
- csecsemő hat hónapos korát követően kiegészítő táplálásban részesült
- csecsemő hat hónapos korát követően is mesterségesen táplált
3.5 Panaszok /Tünetek/ Általános jellemzők:
A kizárólagos, igény szerinti szoptatás nem teljesül a csecsemő 6 hónapos koráig. A szoptatás nem folytatódik 6 hónapos koron túl, szemben azzal a nemzetközi ajánlással, hogy a szoptatás a megfelelő kiegészítő táplálás mellett folytatódhat akár két éves korig, vagy azon túl.
3.6 Érintett szervrendszerek
- anyai mell mirigyállománya
- az anya hormonális rendszere
- az anya idegrendszere, lelki állapota
- a csecsemő hormonális rendszere
- a csecsemő emésztőrendszere
- a csecsemő idegrendszere
- a csecsemő izomrendszere
- a csecsemő immunrendszere
- a csecsemő érzékszervei
- a csecsemő kiválasztása
3.7 Gyakori társbetegségek
A helytelen - nem a csecsemő élettani szükségleteinek megfelelő - csecsemőtáplálás következtében az egészségi állapotot rövid-, illetve hosszútávon meghatározó állapotok, betegségek alakulhatnak ki.
4. Az ellátási folyamat leírása, ellátási algoritmus A védőnő feladata, hogy
- folyamatos megfigyelésen alapuló
- tanácsadással és egészségneveléssel
- támogassa (és menedzselje) a csecsemőkor zavartalan, harmonikus folyamatát (testi, lelki, szellemi és szociális jól-léte érdekében), az egészséges életkezdet kialakítását,
- segítséget nyújtson az édesanyának és családjának gyermeke egészségkárosodásának elkerülése érdekében,
- figyeljen a család életében bekövetkező kedvező vagy kedvezőtlen változásokra. /A csecsemőtáplálás támogatásának folyamatábrája 1.sz. melléklet./
II. Gondozási szükséglet feltárás (diagnosztikai eljárások)
1. Anamnézis felvétele
Célja: Az egészséges életkezdet esélyének táplálkozás oldaláról történő biztosítása érdekében információ gyűjtés, a csecsemő igénye, valamint szükséglete szerinti táplálásának megtervezése érdekében, a megvalósulásánaksegítése. Helye: A csecsemő tartózkodási helye (kórház, a csecsemő otthona, tanácsadó, közösségi helyszínek). Ideje: Az első találkozást követően folyamatosan.
1.1 Általános anamnézis (első alkalommal)
A család szociokulturális helyzetét tárja fel.
1.2 Célzott anamnézis (első alkalommal)
- az anya / apa gyermek fejlődését befolyásoló betegségei
- szülészeti előzmények
- perinatális történések
- az anya korábbi szoptatási eredményessége
- jelenleg szoptatott testvérek (ikertestvér, idősebb testvér) száma
- az első védőnői találkozást megelőző időszak táplálási adatai
1.3 Életvitel anamnézis (időszakonként)
- a család szerzett és tanult ismeretei, kulturális és tradicionális értékrendje és gyakorlata a szoptatással, csecsemőtáplálással kapcsolatban
- anya táplálkozási szokásai (ideértve az alkalmazott konyhatechnikkat)
- az anyai szenvedélybetegségek feltérképezése (dohányzás, alkohol, kábítószer, gyógyszer, stb.)
- fizikai megterhelés, sport, munkavégzés
- átlagostól eltérő napirend
2. Fizikális vizsgálatok
Célja: A helytelen csecsemőtápláláshoz vezető gyakorlat következtében kialakult elváltozások lehető legkorábbi észlelése és az észlelést követő helyreállítása.
Helye: A csecsemő tartózkodási helye (kórház, a csecsemő otthona, tanácsadó, közösségi helyszínek). Ideje: Az első találkozáskor, ezt követően minden további alkalommal. 2.1 Fizikális állapot felmérése
- testtömeg mérés
- hosszmérés
- fejkörfogat mérés
- mellkörfogat mérés
- bőrredővastagság (szükség szerint)
- icterus megítélése
(Lásd még: Az Egészségügyi Minisztérium szakmai protokollja A védőnő feladatai újszülött és gyermekágyas anya otthoni első látogatásakor I.sz. és II. sz. melléklet)
Az általános anamnézis és a fizikális állapot felmérés ismeretében értékeljük a csecsemő fejlődését úgy, hogy az aktuális mérési adatokat az előző mérésekadataival összevetjük és a percentil-táblázatban rögzítjük. Ezen túlmenően figyelni kell a csecsemő szopási magatartásának változását, valamint mentális és mozgás fejlődésének alakulását.
3. Kötelező (minimálisan elvégzendő) szükséglet-feltáró (diagnosztikai) vizsgálatok és azok gyakorisága
3.1 A védőnő által végzett, szükségletet feltáró (diagnosztikai) vizsgálatok 3.1.1. Megtekintés:
- az anyai mellek (anatómia)
- a csecsemő általános megtekintése a szopások ideje alatt
- a szopási, táplálkozási testhelyzet
- a hatékony mellre-tapadás jelei, eltérések
- a tej átjutás jelei az anyánál és a csecsemőnél
- higiénés és környezeti körülmények /A szoptatás módja 2.sz. melléklet./
/A megfelelő testhelyzet és mellre helyezés, a hatékony és nem hatékony szoptatás jelei 3.sz melléklet/
3.2 Állapot felmérés kikérdezéssel:
- az anya általános és aktuális egészségi állapota
- anyai étrend
- az anya pszichés állapota (Az Egészségügyi Minisztérium szakmai protokollja: A szülést követő időszak pszichés változásai. Védőnők szerepe, lehetősége, kompetenciája a szülés körüli hangulatzavarok felismerésében)
- a csecsemő két táplálás közötti magatartása
- a csecsemő táplálkozás iránti igényének jelei
- a sírás, alvás-ébrenlét, magatartás és a táplálás összefüggései
- a csecsemő széklete, vizelete
- hányás, bukás
- táplálási ritmus, gyakoriság, időtartam
- táplálással összefüggő eszközök használata (bimbóvédő, cumi, cumisüveg, kanál, pohár, speciális segédeszközök)
3.3 Segítő tevékenységek
- a csecsemő helyes mellre helyezésének és mellre tapadásának segítése
- információ átadás az egészséges fejlődés folyamatáról és az élettani váltózásokról az adott életkor függvényében. /pl. növekedési ugrás, székletürítés változásai, stb./
- a mell állapotának vizsgálata, ha szükséges
- kézi és eszközös fejés megmutatása, segítése
- szoptatási segédeszközök használatának megmutatása
- anyatejtárolása és a tárolt anyatejfelhasználása, ha ez szükséges. /Az emlő fejése és a lefejt anyatejtárolása 4.sz. melléklet /
3.4 Szükséglet szerinti (diagnosztikai) algoritmusok
A védőnő sekunder prevenció körébe tartozó feladata, hogy figyelje, és felhívja a figyelmét az anyának a gondozást végző orvos által előírt tanácsok, terápiás eljárások, valamint a kontroll és egyéb (szűrő) vizsgálatok elvégzésére, és hogy azok időben történjenek meg. A védőnő feladata segíteni az információadást és a csecsemő korénak és állapotának, illetve ha szükséges, a terápiás javaslatoknak megfelelő táplálást.
4. Ellátástervezés/Gondozás 4.1 Gondozási terv
Célja: A gondozási diagnózis ismeretében a védőnő a szülőkkel közösen meghatározza a csecsemő táplálási szükségleteinek kielégítésére irányuló célokat és azok eléréséhez szükséges feladatokat. Helye: Védőnői tanácsadó, vagy a család otthona, a közösségi programok helyszínei. Felülvizsgálat: rendszeresen, havonta, ill. szükség szerint.
A gondozási terv kiterjed az alábbiakra:
- a csecsemő táplálási módja és ideje
- a táplálás és táplálkozás alatt jelentkező testi-lelki változások
- a táplálással és táplálkozással összefüggő elvégzendő vizsgálatok (ha szükséges)
- fiziológiás és kóros tünetek megfigyelése
A terv magában foglalja: az egészséges és természetes táplálkozás megteremtésének feltételeit, a tanácsadások és a családlátogatások rendszerét, szoptatásra felkészítő tanfolyamok, valamint a szoptatástámogatás lehetőségeit, gyakoriságát, függetlenül attól, hogy az anya szoptatja a csecsemőt, vagy egyéb módon táplálja.
4.2 Tanácsadás
- önálló védőnői tanácsadás
- orvos-védőnő közös tanácsadás, helyi eljárási rend szerint
4.3 Családlátogatás
Az első életév ideje alatt - a gondozási tervben rögzítettek szerint-, lehetőleg havonta, (ebből az első látogatás a gondozásba vételtől számított 72 órán belül, 0-6 hetes korban minimum 6 alkalommal), fokozott gondozást igénylők esetén szükség szerint.
4.4 Szülésre, szülőszerepre felkészítő, valamint szoptatást támogató csoportok vagy tanfolyam helyi eljárásrend szerint
4.5 Fogadóóra
III. Gondozás (segítségnyújtás az állapotromlás megelőzésében) rehabilitáció
1. Védőnői tevékenység, beavatkozások, műveletek a szoptatás és táplálás során 1.1. Az egészséges csecsemőtáplálás megvalósulásának feltétele
Ideális esetben a felkészítés már a várandósság időszakában megtörténik. (anya és családja)
Tájékoztatni kell a várandóst a megszületést követő azonnali bőr-bőr kontaktus, a korai mellre helyezés, a rooming-in elhelyezés és az igény szerinti szoptatás jelentőségéről. Tájékoztatni kell az anyát a természetes, gyógyszermentes szülési fájdalomcsillapítás lehetőségeiről és módszereiről és arról, hogy az anyai fájdalomcsillapítók gátolhatják az újszülöttet az emlő spontán keresésében és az eredményes szopási magatartásban. [ESPGHAN2008] Amennyiben a várandósság alatt a felkészítés elmarad, akkor is megvalósítható az egészséges csecsemőtáplálás, azonban ez fokozottabb gondozást, ismeretátadást, differenciált kommunikációt igényel. 1.2 Tíz lépés a sikeres szoptatáshoz irányelvek ismertetése (5sz. melléklet) /A WHO Kódex Ismertetése 6 sz. melléklet/
2. Gondozási műveletek (Fizikai aktivitás)
2.1 A szoptatás támogatása 0-6 hónapos korban
Az anyateja csecsemő optimális gyarapodásához szükséges összes folyadékot és tápanyagot tartalmazza. Az érett és a várandósság idejének megfelelő súlyú újszülöttnek nincs szüksége víz, tea, glukóz oldat, tápszer, stb. kiegészítésre, csak akkor, ha az orvosi szempontból indokolt.
Minden anyának ismernie kell a szoptatás és az anyatejes táplálás természetes folyamatát. Erről szóban és írásban körültekintő módon, érthetően kell tájékoztatni és annak megértéséről meggyőződni.
Az anyát tájékoztatni kell:
- az anyatej-tejtermelődés mennyiségének szabályozásáról, miszerint azt a csecsemő képes befolyásolni, mert minél többet szopik, annál több tej termelődik,
- az emlő túltelítődésének megelőzéséről - korai, gyakori, helyes szoptatással és fejéssel,
- az emlőbimbó fájdalom és sérülésének megelőzéséről, - az anya és a csecsemő helyes testtartásával és a csecsemő megfelelő mellre helyezésével
- arról, hogy hogyan tudja a tejtermelést fenntartani abban az esetben, ha a kisbaba elkülönítése szükséges, vagy valamilyen oknál fogva nem tud mellből szopni.
Az anyának a szülés után 24 órán belül meg kell mutatni, miről ismerheti fel szopási készséget, és hogyan válaszoljon újszülöttjének táplálkozás iránti igényének korai jeleire.
Az újszülött táplálkozás iránti igényének korai jelei:
- éberebb, aktívabb, nyugtalanabb,
- gyors szemmozgások láthatók a szemhéjalatt
- szemkontaktus az anyával
- szopó és kereső mozgások
- kezének nyalogatása, szopó- és cuppogó hangok,
- finom hangadás, gőgicsélés, sóhajtozás.
Minden anyának tudnia kell, hogy a szoptatást akkora legkönnyebb megkezdeni, ha csecsemője nyugodt éber vagy aktív éber állapotban van. Ismernie kell, hogy az aluszékony csecsemőt hogyan lehet felébreszteni.
Ébresztési "technikák"
- a csecsemő ruháinak levétele a pelenka kivételével
- pelenka csere
- bőrkontaktus az anyával, csecsemő az anya mellkasán
- a csecsemő különböző testrészeit finoman masszírozzuk
- a csecsemő szoptatási helyzetének megváltoztatása
- csecsemő ringatása, függőleges ("ülő") és fekvő testhelyzetet váltogatva ill. gyengéden előre-hátra, míg ki nem nyitja a szemét
- a csecsemőhöz való beszéd és szemkontaktust létesítése
- a szoba megvilágításának megváltoztatása
Szoptatás közbeni ébresztése technikák
- a csecsemő szoptatási helyzetének megváltoztatása
- a csecsemőhöz való beszéd és szemkontaktus létesítése
- tej szájba való fejése
- a szoptatás serkentése a mell ritmikus összenyomásával vagy simogatásával
- "büfiztetés"
- a pelenka kicserélése a mellváltás közben
Az anyákat tájékoztatni kell arról is, hogy naponta (24 órán belül) megközelítőleg nyolc vagy annál több szopás szükséges ahhoz, hogy a szopás elegendő mennyiségű legyen. Vannak csecsemők, akik elegendő mennyiséghez jutnak egy mellből és vannak, akik minden alkalommal mindkét mellből szopnak. Az első mellen addig kell a csecsemőt hagyni, amíg spontán elengedi a mellet, és csak ezt követően ajánlja fel az anya a másik mellett. Jól megy a szoptatás ha:
- a csecsemő időkorlátozás nélkül szopik, naponta átlagosan legalább 8-szor.
- a csecsemő súlyvesztése kisebb, mint 7%.
- az első 24 órát követő 3. napon csecsemőnek naponta legalább 3 széklete van, az 5. naptól széklete ún. anyatejes, élénksárga.
- a 4. naptól a csecsemőnek 24 óra alatt legalább 6 vizelete van, színe víztiszta vagy halványsárga.
- a csecsemő súlygyarapodása az 5. naptól megindul, a 10-14. napra visszanyeri születési súlyát.
- az emlőkön az 5. napra a feszesség jellemző, valamint súlyuk és méretük megnövekedett.
- az emlőbimbón nem látszik sérülés, (a szoptatás első néhány percében átmeneti érzékenység elfogadható).
- az emlőben érzett teltség a szoptatás alatt csökken.
Szoptatási probléma jelentkezése esetén fel kell tárni, mi áll a háttérben és ennek megfelelően kell támogatni azanyát. A jól fejlődő csecsemő gyakori sírása esetén szükséges az anyát megnyugtatni, megfelelő információt adni, valamint fokozott támogatásban részesíteni. A hirtelen jelentkező fokozott szopásigény normális, ezzel szabályozza a csecsemő a számára szükséges mennyiségű és minőségű anyatejtermelését. Ezekaz időszakokgyakran esnekegybe a csecsemő "növekedési ugrásaival", ezért ezekben a helyzetekben általában a megnyugtatáson és fokozott támogatáson kívül másra nincs szükség.
Fokozott támogatást igénylő helyzetek - a csecsemő kockázati tényezői
- megengedettnél nagyobb súlyesés, nem megfelelő súlyfejlődés
- gyenge szopás
- hyperbilirubinaemia,
- állandó aluszékonyság vagy ingerlékenység
- hosszú időközök az egyes táplálások közt
- anatómiai eltérések (pl.: rövid nyelvfék)
- többes szülés
Fokozott támogatást igénylő helyzetek - az anya kockázati tényezői
- nehézségek az előző szoptatáskor
- a csecsemő elkülönítése
- sérült, berepedt vagy vérző emlőbimbó
- a tej anya által vélt elégtelen mennyisége
- akut vagy krónikus betegség
- gyógyszerszedés
- emlő vagy emlőbimbó anatómiai elváltozásai
- korábbi emlőműtét vagy-sérülés
- hormonbetegség, pl. polycystás petefészek szindróma
Avédőnőismételten tájékoztassaazanyát,hogyaszoptatási problémák-minta fájdalmas,sebesemlőbimbó,azemlő túltelődése (mastitis előjelei is lehetnek) - megfelelő testhelyzettel, a testhelyzetek, pozíciók váltogatásával, korrekt mellre helyezéssel és a csecsemő igénye szerinti szoptatással megelőzhetők. A felsorolt módszerekkel elkerülhető a szoptatás idő előtti abbahagyása.
Az egészséges csecsemőtáplálás eredményességének egyik nélkülözhetetlen eleme, hogy a védőnő rendszeresen konzultáljon és egyeztessen a csecsemő gondozását végző orvossal annak érdekében, hogy minden lehetséges módszert felhasználjanak, hogy az anyatejes táplálás és szoptatás minél tovább folytatódjon
A szoptató anya étrendje
Az anyáknaka kiegyensúlyozott, szélsőségektől mentes táplálkozást kell javasolni. Nincs szükség semmilyen étel és ital tiltására addig, amíg a csecsemő tünet- és panaszmentes kivéve a túlzott alkohol- és a koffein fogyasztása. Azoknál a szoptató anyáknál, akik nem fogyasztanak állati eredetű fehérjéket, jelentős a kockázata annak, hogy csecsemőjük vitaminhiányos lesz, amely hiánybetegségeket okozhat. Ezért ezeknek az anyáknak ásványi anyag és vitaminpótlásra van szükségük, csecsemőjüknek, pedig fokozott gondozásra, gyermekorvosi felügyeletre. Amennyiben az anya nem hajlandó táplálékát az említett vitaminokkal és ásványi anyagokkal kiegészíteni, úgy gondoskodni kell arról, hogy a csecsemő kapjon megfelelő vitamin-és ásványi anyag kiegészítést. Amennyiben az anyánál bizonyított vashiány nem áll fenn, úgy az ő táplálékának kiegészítése vassal felesleges és káros.
2.2 Szoptatás kiegészítő táplálással 0-6 hónapos korban
A csecsemő igényeit az első hat élethónapban (26 hét) a kizárólagos szoptatás /anyatej/optimálisan kielégíti. Ebben az életszakaszban bármilyen pótlás megkezdésének eldöntése orvosi kompetencia: az anyatej-helyettesítő tápszer elkezdése orvosi indikáció alapján történik. Ha az anya a szoptatást folytatni kívánja, fontos hogy a pótlás olyan módon történjen, hogy a szoptatást kövesse a kiegészítő táplálék.
A pótlás irányelvei:
- elsősorban az édesanya saját tejének adásával,
- másodsorban pasztörizált női tej adásával,
- harmadsorban anyatej-helyettesítő tápszerrel történjen.
Meg kell erősíteni az anyát abban, hogy saját teje a csecsemőjének bármilyen kis mennyiségben is értékes. A szoptatás fenntartása jelentős hatással van az anya-gyermek kapcsolatra, a kötődésre.
A védőnő feladata
az anyatej-helyettesítő tápszer elkészítésének bemutatása, az ajánlott mennyiség adásának ellenőrzése /A mesterséges táplálás biztonságának növelése 7. sz. melléklet/
2.3 A mesterséges táplálás 0-6 hónapos korban
A mesterséges táplálás bevezetése tápszerrel és egyéb szolidokkal, vagy arra való áttérés 6 hónapos korig orvosi indikáció és kompetencia körébe tartozik. /Az Eü. Min. Protokollja. Az egészséges csecsemő táplálásáról/. A védőnő feladata, hogy a korszerű, életkornak megfelelő hozzátáplálás irányelveit - figyelembe véve az orvosi javaslatot -ismertesse a szülőkkel, és segítse a fokozatos, hozzátáplálást.
2.4 A 6 hónapon túli csecsemő táplálása, hozzátáplálás
A csecsemő kiegészítő-táplálását hat hónapos korban el kell kezdeni. Hat és nyolc hónapos kor között naponta 1-2 szer, kilenc hónapos kor után napi 3-4-szer, 12 hónapos kor után napi 4-5-ször. adható kiegészítést Bármely életkorban kezdi is el az egyéb étkek fogyasztását a csecsemő, fokozatosan kell emelni az étkezések számát. Elfogadva, hogy az anya dönt arról, hogy mennyi ideig szoptatja gyermekét, támogatni kell az anyát abban, hogy folytathassa a szoptatást akár a csecsemőt két éves koráig és azt követően is. / WHO ajánlás /
2.4.1 A kiegészítő táplálás megkezdésének feltételei:
- hónapos kort követően
- a nyelv-kilökőreflex megszűnik
- gyakori szopási igény saját korábbi szopási gyakoriságához képest
- tartósan stagnáló, vagy csökkenő súlygörbe
2.4.2 Az új táplálék bevezetésének szempontjai:
- a szopás után történik az új étel kínálása,
- egyszerre csak egy új étel kerüljön bevezetésre,
- figyelni kell az étel hatását, hogy nem vált-e ki allergiás tüneteket,
- az adagok fokozatos emelése: az első nap 1-2 kanál, majd fokozatosan emelhető a teljes adagig,
- kezdő ételnek ajánlott a gyümölcs-, majd a zöldségpüré bevezetése (hat hónapos kor után a sorrendnek nincs nagy jelentősége),
- folytatólag kiegészül a zöldség hússal, olajjal, a gyümölcs és zöldség gabonával,
- legutoljára 1 éves kor körül a tejtermékek és a tojás kerülnek bevezetésre
Jól szopó csecsemőnek a második félévben sincs szüksége ún. "követő" tápszerekre és tejpépekre. Utóbbi különösen káros lehet, mivel nagy mennyiségben tartalmaz módosítás nélküli, teljes tehéntejet.
/8.sz. melléklet Az életkornak és a fejlettségi szintnek megfelelő ételek fogyasztásának képességére/ /9 sz. mellékelt Az egészséges csecsemő táplálása 6 hónap és 1 év között /
3. Fizikai aktivitás
Az egészséges csecsemőtáplálást támogató színterek és gondozási módszerek
3.1.
- a család otthona
- tanácsadó
- közösségi programok
3.2 színterei:
- szoptatást támogató anyacsoport
- baba-barát területek
- anyatejgyűjtő program
- baba-mama klub
- csecsemő masszázs klub
- játszóház stb.
- a szoptatás és anyatej világnapja programok
- rendszeres és időszakos kampányok
- lakossági ismeretterjesztő kiadványok
- média (írott, elektronikus)
4. Sürgősségi ellátás
- telefonos szoptatási tanácsadás
- tanácsadói ügyelet
5. Állapotromlás, szövődményes állapot gondozása
Speciális szoptatási tanácsadási lehetőségekről tájékoztatás, IBCLC szoptatási szaktanácsadóhoz vagy szakorvoshoz küldés.
6. Célcsoport oktatása, ismeretterjesztés, tájékoztatás
A védőnőkés az anyák legújabb információkhoz juttatásának speciális formája, mely felhasználja a csoport speciális erőforrásait.
7. Kiegészítő/alternatívgondozás
8. Prognózis
Az eredményes szoptatás biztosítja az egészséges testi-, lelki- és szociális fejlődést az egyén és családja számára. A lehetséges szövődmények megelőzése, segítség az állapotromlás megakadályozásában.
9. Ellenőrzés
15/2005. (V.2.) EüM. rendelet az egészségügyi szolgáltatók szakmai felügyeletéről
10. A gondozás várható időtartama: 1 év.
IV. Az ellátás megfelelőségének indikátorai 1. Szakmai munka eredményességének mutatói
1.1. A szakmai protokoll szerinti ellátás ellenőrzésére szolgáló folyamat indikátorok:
- A gondozásba vétel időpontjához viszonyítva a látogatások száma és ütemezése megfelelő
- Gondozási terv követi a csecsemő állapotában estelegesen bekövetkező változásokat és a gondozási terv szerinti ellátás megvalósult
- A dokumentáció vezetés megvalósult
1.2. Az ellátás eredményességének mutatói eredmény indikátorok alapján /10 sz. melléklet/
1.3. Gondozott elégedettsége az ellátási ciklus befejeztével
V. A protokoll bevezetésének feltételei Tárgyi feltételek
60/2003. (X. 20.) EszCsM rendelet az egészségügyi szolgáltatások nyújtásához szükséges szakmai minimumfeltételekről
Személyi feltételek
49/2004.(V.21.) EszCsM rendelet- a területi védőnői ellátásról Szakmai/képzési feltételek
36/1996. (III. 5.) Korm. rendelet az egészségügyi felsőoktatás alapképzési szakjainak képesítési követelményeiről (mód: 166/2003 (X.21.) Korm. r.)
27/1998. (VI. 17.) NM rendelet az egészségügyi szakképesítést szerzett személyek alapnyilvántartásáról, valamint az egészségügyi szakdolgozók működési nyilvántartásának szabályairól
28/1998. (VI. 17.) NM rendelet az egészségügyi szakdolgozók továbbképzésének szabályairól
47/1997. (XII. 17.) NM rendelet a kötelező egészségbiztosítás keretében járó anyatejellátás feltételeiről
VI. Irodalomjegyzék Irodalom
1. Egészséges újszülöttek ellátása szülőszobán és a gyermekágy ideje alatt (Egészségügyi Minisztérium Szakmai Protokollja), készítette a Csecsemő és Gyermekgyógyászati Szakmai Kollégium
2. A védőnő preventív alapfeladatai, kötelezettsége és felelőssége a megelőző ellátásban (OTH 2004.)
3. Védőnői Ellátási Standardok (VES. - Eü. Közlöny 2005./12.)
4. A "Védőnői Ellátás Folyamata" I./3. Magyar Egészségügyi Ellátási Standardok kézikönyvéről (MEES) 1.0 változat - Eü. Közlöny, 2007.év 4.szám. (727-740.)
5. Védőnői Szakmai Kollégium Módszertani útmutatói I-II-III. 2007. A védőnői ellátás céljai, általános feladatai, módszerei .A területi védőnő feladatai a komplex családgondozásban .A kórházi/klinikai védőnő feladatai az intézményi ellátásban
6. Agostini C, Decsi T, Fewtrell M etal.Complementary Feeding: Medical Position Paper,ACommentary bythe ESPGHAN Committee on Nutrition Journal of Pediatric Gastroenterology and Nutrition, 2008;46:99-110
7. Védőnői Módszertan (jegyzet),szerk. Székely -Szél -Szeles - Kispéterné Semmelweis Egyetem Egészségügyi Főiskolai Kar Budapest 2002.
8. A pszichomotoros fejlődés zavarainak felismerése és ellátása az alapellátás gyakorlatában 2.sz. módszertani levél OGYEI-MAVE.2005.
9. Egészségügyi Minisztérium - Egészségügyi Szakképző és Továbbképző Intézet (2005. november) "Közös kincsünk a gyermek" Nemzeti Csecsemő és Gyermekegészségügyi Program
10. A szülést követő időszak pszichés változásai. Védőnők szerepe, lehetősége, kompetenciája a szülés körüli hangulatzavarok felismerésében. (Az Egészségügyi Minisztérium szakmai protokollja - Eü. Közlöny 2006. március 31.)
11. Maródi László Gyermekgyógyászat Medicina Kiadó 2003.
12. Szülészet -Nőgyógyászat Protokoll szerk. Dr. Papp Zoltán Golden Book kiadó 2002.
13. Szoptatás támogatása a szülés körüli időszakban egészséges anya és érett újszülött esetén - Academy of Breastfeeding Medicine 5. sz. protokollja (ABM Clinical Protocoll/5: Peripartum breastfeeding management for healthy mother and infant at term -, Academy of Breastfeeding Medicine Protocoll Committee 2002 november 16.) Elérhető: http://www.szoptatasportal.hu/
14. A kizárólagos szoptatás elérésének irányelvei ILCA Kiadó: ETI 2005. június
15. Tomsits E. A csecsemőtáplálás elvei és gyakorlati szempontjai. (2003). Praxis, 12.
16. WHO. Indicators forassessing breast-feeding practices (1991). WHO, Genf.
17. WHO/UNICEF. Global Strategy for Infant and Young Child feeding. (2003)WHO Geneva.
18. Work Group on Breastfeeding. Breastfeeding and the Useof Human Milk. (1997). Pediatrics, 100., 3., 1035-1037.
19. Magyar Táplálékallergia és Táplálékintolerancia Adatbank szerk: Barna Mária (2000)
20. Nagy szoptatóskönyv szerk: Hannah Lothrop (2005)
21. Szoptatás szerk: Gumberger, Márta Guóth - Hormann, Elizabeth (2003
22. A szoptatás védelme, támogatása és elősegítése Európában: Indítvány
Jogszabályok
1. 1990. évi LXV. törvény a helyi önkormányzatokról
2. 1992. XXII tv Munka törvénykönyve
3. 1997. évi CLIV. törvény az egészségügyről
4. 51/1997. (XII. 18.) NM r. a kötelező egészségbiztosítás keretében igénybe vehető betegségek megelőzését és korai felismerését szolgálóe gészségügyi szolgáltatásokról ésa szűrővizsgálatok igazolásáról (módosította: 67/2005.(XII. 27.) Eü.M.rendelet)
5. 49/2004. (V.21.) ESzCsM rendelet a védőnői területi ellátásról
6. Egészség Évtizedének Johan Béla Nemzeti Programjáról 46/2003. (IV. 16.) OGY határozat,
7. Nemzeti Csecsemő és Gyermek Egészségügyi Program (2005. Eü. M.)
8. "Legyen jobb a gyermekeknek" Nemzeti Stratégiáról 47/2007.(V.31.) OGY határozat
9. 1997. évi XXXI. Tv. A gyermekek védelméről és gyámügyi igazgatásról
10. 2002. évi LVIII. Tvegyes az egészségügyet és társadalombiztosítást érintő törvények módosításáról
Kapcsolódó internetes oldalak Magyar honlapok
Országos Gyermekegészségügyi Intézet (http://www.ogyei.hu/)
Szoptatás Portál (http://www.szoptatasportal.hu/)
La Leche Liga Magyarország (http://www.lll.hu/)
Kismama Magazin (http://www.kismama.hu/)
Szoptatás Támogató Nemzeti Bizottság (http://www.sztnb.hu/)
Szoptatásért Magyar Egyesület (http://www.szoptatasert.hu/)
Nemzetközi honlapok
Breastfeeding (http://www.breastfeeding.com/) ILCA (http://www.ilca.org/) World Health Organization (http://www.who.int/) IBFAN (http://www.ibfan.org/)
A szakmai protokoll érvényessége: 2010. szeptember 30. VII. Mellékletek
1. sz. melléklet: A csecsemőtáplálás támogatásának folyamatábrája
2. sz. melléklet: A szoptatás módja
3. sz. melléklet: Ajánlás a hatékony szoptatás megítéléséhez 4 .sz. melléklet: Az emlő fejése és a lefejt anyatejtárolása
5. sz. melléklet: Tíz lépés a sikeres szoptatáshoz
6. sz. melléklet: A WHO Kódex: tíz pontos összefoglaló
7. sz. melléklet: Óvintézkedések a mesterséges táplálás biztonságosságának növelésére
8. sz. melléklet: A példák az életkornak és a fejlettségi szintnek megfelelő ételek fogyasztásának képességére
9. sz. melléklet: Az egészséges csecsemő táplálásának irányelv
10.sz. melléklet: Az egészséges újszülött és csecsemő táplálásának megfelelősségének indikátorai
1. sz. melléklet - A csecsemőtáplálás támogatásának folyamatábrája
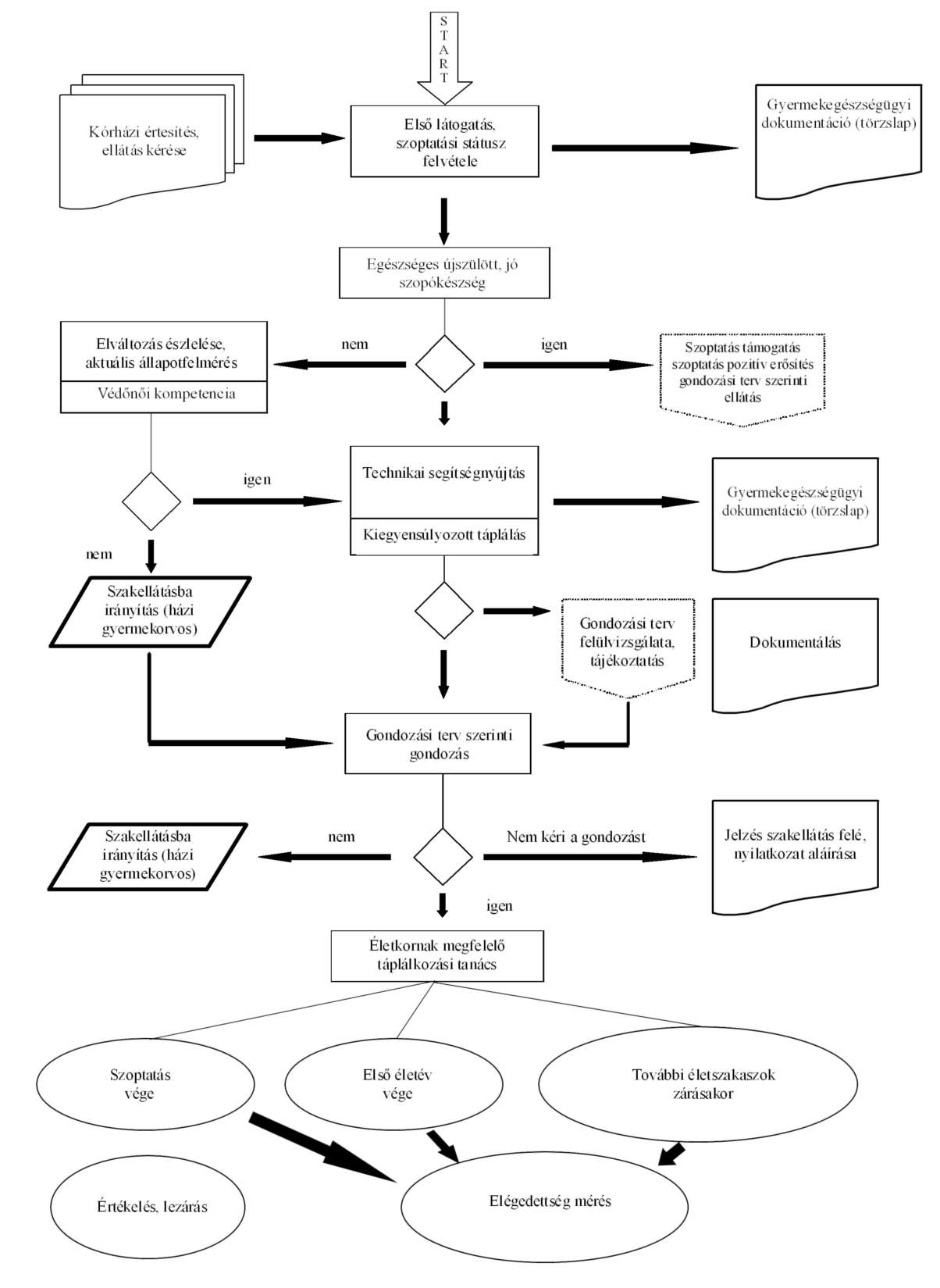
2. sz. melléklet A szoptatás módja
Alapvető fontosságú, hogy a szoptatások nyugalomban teljenek és kellemes élményt nyújtsanak az anya és a gyermeke számára. Az anyát meg kell tanítani a helyes szoptatási technikára, hogy szorongásmentesen, kellő önbizalommal tudjon szoptatni.
1. Az anya és csecsemő elhelyezkedése a szoptatáshoz
Az anya és csecsemő ruházata legyen kényelmes, nem korlátozó.
Szoptatni legkényelmesebb ülve vagy fekve. Ülő helyzetben többféle módon tehetjük mellre a csecsemőt; bölcső-, kereszt-, hónalj-tartásban, nagyobb csecsemőket lovagló-tartásban. Az anyának legyen támasztéka, ne dőljön hátra vagy ne hajoljon előre.
Az anya fordítsa maga felé a csecsemőt és támassza meg a nyaka és a válla (ne a feje) mögött, a csecsemő füle, válla, csípője legyen egyvonalban, tartsa testközelben (az anya és csecsemő mellkasa érjen egymáshoz) és mell magasságban úgy, hogy a csecsemő szája legyen egy magasságban a mellbimbóval és legyen lehetőség a szemkontaktusra.
2. Helyes mellrehelyezés
A helyes mellrehelyezés elengedhetetlen ahhoz, hogy a csecsemő hatékonyan szopjon és hogy a bimbósérüléseket megelőzzük. A mell megtámasztásánál ügyelni kell arra, hogy az "C" alakban történjen (hüvelykujj a bimbóudvar felett, a többi ujj az emlő alatt) és nem a nálunk hagyományos "olló" tartásban. Így biztosítható a megfelelő mellre tapadás.
Megérintve a gyermekajkát a mellbimbóval, meg kell várni, míg az nagyra nyitja a száját (mintha ásítana), majd az anya határozott mozdulattal húzza magához a csecsemőt, az alsó ajkat a bimbóudvar alsó széle felé irányítva.
3. Helyes mellretapadás jelei
- a bimbó körüli területből legalább 2,5 cm-t a szájába vesz, a bimbóudvarból több
- látszik a felső ajak felett
- száját szélesre tátja (a szájzug 100°-nál nagyobb szöget zár be)
- ajkai kifelé fordulnak,
- nyelve a mell alatt van és félkörben simul a mellhez,
- fejét enyhén hátrahajtja, állával nekitámaszkodik a mellnek, orrhegye érinti az emlőt,
- az orrnyílások szabadok.
4. A hatékony szopás jelei A csecsemőnél
- ritmikusan szopik (présel, szív, nyel), az állkapocs izmainak mozgása kiterjed a fülekig, olykor a fülcimpa is mozog
- a ritmikus szopás legalább 5-10 percig tart
- az orcák kitöltöttek; nem horpadnak be
- hallhatóan/láthatóan nyel, nem nehezített a légzése
- nem szorítja ökölbe a kezét, ellazult testtartást vesz fel,
- nedves a szája (tejcsöppek)
- a csecsemő magától engedi el a mellet, szoptatás után elégedett Az anyánál
- az oxytocin reflex jelei észlelhetőek, szomjúságérzet, ellazult érzés, álmosság,
- méhösszehúzódások az első 3-5 napban bőséges lochia ürül a szopás közben és után
- tejcsepegés a másik mellből
- az anya kényelmesen érzi magát, nem érez fájdalmat a mellében
- ellazult érzés, álmosság
- csökken a mell telítettségérzete
- szoptatás után a mellbimbó kicsit megnyúlik, de nem deformált, nem sebes
A helyes szoptatási technikával nagyrészt kivédhetőek a szoptatás során fellépő szövődmények (emlőbimbó kisebesedés, tejvezeték elzáródás, mastitis stb).
3. sz. A megfelelő testhelyzet és mellre helyezés, a hatékony és a nem hatékony szoptatás jelei
| Jelek, melyek esetén a szoptatás valószínűleg eredményes | Jelek, melyek esetén a szoptatás során nehézségek, problémák léphetnek fel |
| AZ ANYA ÉS A CSECSEMŐ TESTHELYZETE | |
| Az anya elengedett, kényelmes testhelyzetben van A csecsemő az anya testéhez közel van A csecsemő feje és teste egyvonalban van és az emlő felé tekint A csecsemő álla érinti az emlőt A csecsemő egész teste alá van támasztva A csecsemő orra érinti az emlőt Az anya és a csecsemő között van szemkontaktus | Az anya vállai feszesek, a csecsemő fölé hajlanak A csecsemő az anya a testétől távol van A csecsemő feje és nyaka elfordul a szopáskor A csecsemő álla nem érinti az emlőt Csak a csecsemő feje és nyaka van alátámasztva A csecsemő alsó ajka/álla érinti az emlőt Az anya és a csecsemő között nincs szemkontaktus |
| A SZOPÁS | |
| A csecsemő száját nagyra tátja A csecsemő alsó és felső ajka kifelé fordul A csecsemő nyelve ráharapáskor látható, az félkörívben öleli az emlőbimbót és a bimbóudvart az alsó ajak felett A csecsemő orcája a szopáskor gömbölyű A csecsemő felső ajkánál a bimbóudvarból nagyobb felület látható A szopás lassú, mély, szünetek tapasztalhatók A szívás/nyelés/légvétel ciklus látható vagy hallható | A csecsemő száját kicsire tátja A csecsemő ajkai befelé fordulnak, csücsörít A csecsemő nyelve ráharapáskor nem látható A csecsemő orcája a szopáskor behúzódik A csecsemő alsó ajkánál a bimbóudvarból nagyobb felület látható A szopás gyors, kapkodó, felületes Cuppanó, csattogó hang hallható |
| AZ EREDMÉNYES TEJ-ÁTÁRAMLÁS JELEI | |
| A csecsemő szája körül nedvesség látható A csecsemő keze és a karja fokozatosan ellazul A szopás során az emlő fokozatosan puhává válik Az ellenkező oldalon csepeg a teja mellből Az oxytocin reflex jelei, tapasztalhatók a szopás alatt (szomjúság, megnyugvás vagy álmosság, fokozott méhösszehúzódás, lochia távozása) A csecsemő maga ereszti el az emlőt a szopás végén | A csecsemő nyűgős, nyugtalan ki-be kapja az emlőt Az anya mellében, illetve a bimbó körül fájdalmat vagy kellemetlen érzést tapasztal Az emlők vörösek, duzzadtak, fájdalmasak Az oxytocin reflex jelei nem tapasztalhatók Az anya veszi el a mellet |
4. sz. melléklet: Az emlő fejése és a lefejt anyatejtárolása Az emlő fejése és a lefejt anyatejtárolása
Ha az anya igény szerint szoptat, fejésre csak bizonyos esetekben lehet szüksége, amelyek a következők:
1. Anyatejgyűjtése
- ha a csecsemő beteg vagy koraszülött
- ha nincs együtt az anya és a csecsemő
- ha az anya visszatér a munkahelyére
- tárolás céljából
- donor anyatej leadása céljából
2. A szoptatás kezdetén, hogymeginduljon a tejáramlása
3. A mell teltségének csökkentésére túltelítődés, tejcsatorna elzáródás és mastitis esetén
4. A tejképződés fokozása céljából, ha a csecsemőnek szopási nehézsége van
5. A tej eltávolítása céljából, ha specifikus gyógyszer szedése miatt a csecsemő nem szoptatható
Kézi fejés
A kézi fejés módját minden szoptató anyának meg kell tanulnia. ( A sikeres szoptatáshoz vezető Bababarát Kórház Kezdeményezés 5.lépése).
A fejés előtt a mell masszírozása, meleg alkalmazása elősegíti a tejleadó reflexet.
Fejés módja: Az anya hajoljon előre, támassza meg a mellét a kezével, hüvelykujját helyezze a bimbóudvaron a mellbimbó fölé, mutató és középső ujját pedig a bimbó alá., attól kb. 2.5-3 cm-re. Közelítse a szembenálló ujjakat, a nyomást a mellkasfal felé
(kb 1-2 cm) irányítva és az összenyomást-felengedést többször ismételje meg. Rotálja az ujjakat körbe, hogy a mell minden szegmenséből el tudja távolítani a tejet.
Mellszívók
A kézi mellszívók és elemmel működtetett vagy elektromos fejőgépek széles választéka kapható, azonban legtöbbjüknek vannak hátrányai az ideális mellszívóval támasztott elvárások tükrében. Az ideális mellszívó képes a mellet kiüríteni és a tejtermelést stimulálni, tiszta, nem kontaminált, könnyű a használata, nem drága és atraumatikus.
A mellszívókat és fejőgépeket használat előtt fertőtleníteni kell.
A tej biztonságos fejése és előkészítése, tárolásra:
Kézmosás fejés ill. a női tej kezelése előtt feltétlenül szükséges
- Törekedjünk arra, hogy amikor csak lehet, friss lefejt tejet adjunk
- Tároljuk a lefejt tejet tiszta, szorosan záró csavaros edényben (üveg vagy kemény plasztik ajánlott) és cimkézzük a tárolóedényt, rögzítve a fejés időpontját
- Az előreláthatólag két napon belül nem felhasznált tejet mélyhűtsük
- Ne használjuk fel a már használt cumisüvegben maradt tejet egy következő táplálásra
- Az egy tárolóedénybe szánt mennyiség eléréséig a már lehűtött tejhez 24 órán belül a továbbiakban lefejt és lehűtött tejhozzáönthető
- Ne adjunk frissen lefejt tejet a tárolóedényben már lefagyasztott tejhez
- Mindég a legrégebben lefagyasztott tejet használjuk fel először
A fagyasztott tej biztonságos kiolvasztása
- A rendelkezésre álló időtől függően vagy tegyük át a tejet a mélyhűtőből a hűtőszekrénybe vagy tegyük az üveget meleg vízbe és rázogassuk vagy tegyük melegvízsugár alá (a melegvíz ne érje az üveg száját)
- Ne használjunk mikrohullámú sütőt a felmelegítésre (egyenetlen hőmérséklet- a csecsemő megégetheti a száját, tápanyagok minőségromlása)
- A felolvasztott tej24 óráig tartható a hűtőszekrényben Az egyszer már lefagyasztott tejet újra fagyasztani tilos.
Frissen lefejt anyatejtárolása az egészséges érett csecsemő számára (otthoni körülmények között)
| Tárolás helye | Hőmérséklet | A felhasználhatóság tartama | Megjegyzés |
| Szobahőmérsékleten | Max 25 C° | 6-8 óra | A tárolóedényt le kell fedni és a lehető legalacsonyabb hőmérsékleten tartani (pl. betekerni hidegvizes törölközővel) |
| Hűtőtáska | 4-15C° | 24 óra | A hűtőelemet tartsuk közvetlenül a tejmellett és kerüljük a táska nyitását |
| Hűtőszekrény | 4C° | 5 nap | Tároljuk a tejet a hűtőszekrény hátsó részén |
| Fagyasztó tér a hűtőszekrényen belül | -15 C° | 2 hét | Tároljuk a tejet a fagyasztó hátsó részén, ahol a legstabilabb a hőmérséklet. Az így tárolt tej biztonságos, de egyes lipidek degradálódnak és gyengébb minőségűek |
| Fagyasztó tér a hűtőszekrényen belül külön ajtóval | -18 C° | 3-6 hónap* | |
| Mélyhűtőláda vagy különálló mélyhűtő szekrény (manuális leolvasztású) | -20 C° | 6-12 hónap |
*3 hónap automatikusan leolvasztó mélyhűtő esetén
A fenti ajánlások nem vonatkoznak a koraszülött, beteg csecsemők számára vagy donor anyatej céljára gyüjtött tej kezelésére és tárolására.
Donor női tej
Magyarországon a donor anyatejgyűjtését és elosztását Anyatejgyűjtő Állomások végzik. Amennyiben a szoptatás és lefejt anyatej adása nem lehetséges, meghatározott feltételek teljesülése esetén a jelenleg érvényben levő 47/1997. (XII. 17.) NM rendelet térítésmentes anyatej ellátásra ad lehetőséget.
(1.§ a koraszülött, kis súlyú újszülött továbbá az érett újszülött és csecsemő, ha súlyos táplálkozási allergiában, felszívódási zavarban, hasműtéttel járó fejlődési rendellenességben szenved, és az anya saját tejével táplálni nem tudja., 2.§ ha az anya fizikailag alkalmatlan az anyatejjel történő táplálásra, olyan fertőző betegségben vagy mérgezésben szenved, amely a csecsemő egészségét veszélyezteti, olyan gyógyszert szed, amely szedése a szoptatás időszakában ellenjavallt, súlyos, gyakori tudatvesztéssel járó állapotban van, pszichés állapota a szoptatást lehetetlenné teszi)
5. sz. melléklet: Tíz lépés a sikeres szoptatáshoz
A sikeres szoptatáshoz vezető 10 lépés (WHO/UNICEF)
A WHO és az UNICEF 1991-ben indította el a Bababarát Kórház Kezdeményezést. Az erre a címre pályázó szülészeti ellátást biztosító egészségügyi intézményeknek tíz pontnak kell eleget tenniük, továbbá be kell tartaniuk a Nemzetközi Kódex előírásait.
A 2005-ben megjelent hazai Nemzeti Csecsemő-és Gyermekegészségügyi Program I./9 céljaként a Bababarát Kórház kezdeményezés szerepel.
1. lépés. A kórház rendelkezzen írásos szoptatási irányelvekkel, amelyeket rendszeresen ismertessenek az egészségügyi dolgozókkal.
2. lépés. Minden egészségügyi dolgozó kapjon megfelelő felkészítést az irányelvek alkalmazásához.
3. lépés. Tájékoztassanak valamennyi várandós nőt a szoptatás előnyeiről és gyakorlatáról.
4. lépés. Segítsék az anyákat, hogy az újszülöttet már a születést követő első félórában a mellükre tehessék. Ez úgy értendő, hogy közvetlenül a megszületése után helyezzék az újszülöttet bőrkontaktusba az anyjával, tartsák ott legalább egy óra hosszat és bátorítsák az anyát, hogy felismerje, mikor áll készen az újszülött a szopásra és ajánljanak fel segítséget, ha szükséges.
5. lépés. Mutassák meg az anyáknak, hogyan kell szoptatni és a tejelválasztást fenntartani, még akkor is, ha valamilyen okból el vannak különítve az újszülöttjüktől.
6. lépés. A csecsemő ne kapjon az anyatejen kívül más ételt vagy italt, amennyiben az orvosi szempontból nem indokolt.
7. lépés. Legyen általános gyakorlat az anya és az újszülött együttes elhelyezése (rooming-in) a nap 24 órájában.
8. lépés. Ösztönözzék az igény szerinti szoptatást.
9. lépés. A szoptatott csecsemőnek ne adjanak cumit.
10 lépés. Támogassák a szoptatást segítő anyacsoportok létrehozását és az egészségügyi intézményekből távozó anyákat irányítsák ezekhez.
6. sz. melléklet: A WHO Kódex: tíz pontos összefoglaló
Az Anyatejet Helyettesítő Készítmények Marketingjének Nemzetközi Kódexe és az Egészségügyi Világszervezet
(WHO) azt követő határozatai
| 1. Cél: | A Kódex célja az, hogy a szoptatás védelmével és támogatásával hozzájáruljon a csecsemők biztonságos és megfelelő táplálásához. |
| 2. Tárgykör: | A Kódex az anyatejet helyettesítő termékekre vonatkozik, ha a marketing vagy egyéb tevékenység azt állítja, hogy a termék módosítással vagy anélkül alkalmas az anyatej teljes vagy részleges pótlására. Az anyatejet helyettesítő termékek közé tartoznak: - a kezdő tápszerek - a követő tápszerek - egyéb tehéntej-alapú termékek - babateák és-gyümölcslevek - tejpépek és zöldségpürék A Kódex tárgykörébe tartoznak a cumisüvegek és cumik is.° Mivel az első 6 hónapban a csecsemő legjobb táplálási módja a szoptatás, minden kiegészítő élelmiszer, amiről bármiféle módon azt állítják, hogy alkalmas a 6 hónaposnál kisebb csecsemő táplálására, anyatejet helyettesítő terméknek minősül. |
| 3. Reklám: | A fenti termékek reklámozása tilos. |
| 4. Termékminták: | A fenti termékekből az édesanyák, családjuk és az egészségügyi dolgozók nem kaphatnak ingyenes mintát. |
| 5. Egészségügyi intézmények: | Tilos a fenti termékek népszerűsítése: nem szabad őket kiállítani, nem szabad posztereket, naptárakat kiakasztani, nem szabad propaganda-anyagot osztogatni. |
| 6. Egészségügyi dolgozók: | Tilos ajándékot vagy ingyenes termékmintát adni egészségügyi dolgozónak. A termékinformáció szigorúan tudományos és tényszerű legyen. |
| 7. Adományok: | Az egészségügyi ellátó rendszeren belül egyetlen intézmény/személy sem kaphat ingyenes vagy erősen árengedményes adományt anyatejet helyettesítő termékből. |
| 8. Tájékoztatás: | A tájékoztató és oktató anyagoknak tartalmazniuk kell, mennyire előnyös a szoptatás, és azt is, milyen veszélyekkel jár a cumisüveges táplálás és a kezdő tápszerek alkalmazása. |
| 9. Termékcímkék: | A termékcímkén szerepeljen, hogy a csecsemő legjobb tápláléka az anyatej, hogy a készítmény csak orvosi javallatra alkalmazható, valamint az is, milyen veszélyekkel jár a termék alkalmazása. Nem lehet a címkén csecsemő képe vagy más olyan illusztráció, szöveg, amely a tápszerhasználatot idealizálja. |
| 10. Minőség: | A nem megfelelő termékeket - mint pl. az édesített sűrített tejet - tilos csecsemőtáplálás céljára reklámozni. Minden termék legyen kiváló minőségű (feleljen meg a Codex Alimentarius követelményeinek), és vegye figyelembe a felhasználó ország éghajlatát és tárolási lehetőségeit. |
7. sz. melléklet Óvintézkedések a mesterséges táplálás biztonságosságának növelésére
Mesterséges táplálásra van szükség, ha az anya a szoptatással kapcsolatos tájékoztatás ellenére tápszerrel kívánja táplálni csecsemőjét, vagy ha átmenetileg nem szoptathat, vagy ha dolgozik és a kizárólagos szoptatás/anyatejjel való táplálás nem valósítható meg, vagy ha a szoptatás kontraindikált.
A megfelelő és biztonságos táplálás érdekében fentiekben leírt helyzetben levő anyákat teljes körűen és személyre szólóan kell tájékoztatni az alábbiakról.
- A por alakú tápszer nem steril termék. Bizonyított, hogy intrinsic módon tartalmazhat kórokozó baktériumokat. A kezeléssel, a tárolással és az elkészítéssel pedig extrinsic módon is fertőződhet. A fertőzés veszélyének csökkentése érdekében szigorú higiénés szabályokat kell alkalmazni.
- A kereskedelemben kapható egyszer használatos üvegben vagy tetra-pack kartonban árusított kész folyadék alapú tápszerek steril termékek. Ezek a felnyitás után a környezetből szennyeződhetnek kórokozó baktériumokkal. Ezért ezeknél a termékeknél is szükséges a fertőzés megelőzése érdekében a szigorú higiénés eljárások betartása.
- por alakú tápszernél fontos a használati utasítás pontos betartása. Ne legyen sem túl koncentrált sem túl higított, mert mindkét eset veszélyes lehet a csecsemőre.
- higítatlan tehéntej (vagy más állat teje), a sűrített tej, csökkentett zsírtartalmú tehéntej, illetve az otthon végzett hígításokkal készített tej egyike sem alkalmas a csecsemőtáplálásra, ezért egy éves kor alatt nem adhatók.
- kisded táplálásában egy éves kor felett a teljes zsírtartalmú tehéntej adható. A zsírszegény tehéntejek használatát két éves korig kerülni kell.
A tápszerekotthoni biztonságos elkészítése, tárolása és odaadása érdekében az alábbi eljárás betartására van szükség: A fertőzés megelőzése (pl.: kézmosás, eszközök, edények, a konyha tisztán tartása)
- Minden egyes etetés előtt, frissen kell készíteni a tápszert.
- Sterilizált edények használata - alapos elmosogatás után sterilizálás:
- 10 percig tartó forralással,
- mikrohullámú sterilizátorral.
A fertőzés megelőzéséhez a tápszert forró vízzel (>70 °C) vagy felforralt és 70 °C-ra lehűtött vízzel kell készíteni. Az elkészített tápszert gyorsan kell lehűteni (nem tarthat 30 percnél tovább) és azonnal fel kell használni. Az etetés előtt meg kell győződni arról, hogy megfelelő hőmérsékletű-e, nehogy megégesse a csecsemő száját. A megmaradó tápszert többször nem lehet felhasználni.
8. sz. melléklet:Azéletkornak és a fejlettségi szintnek megfelelő ételek fogyasztásának képességére
| Életkor (hó) | Reflexek/képességek | Étel jellege, melyet képes elfogyasztani | Példák ételekre |
| 0-6 | Szopás/szívás és nyelés | Folyadékok | Csak anyatej |
| 4-7 | Korai "csámcsogás'Vrágás megjelenése; a szopás erősségének növekedése; az öklendező reflex elmozdulása nyelv középső harmadától a hátsó harmadig | Pépes ételek - akkor, amikor szükségessé válik a kiegészítő táplálás | Anyatej és főtt, pépes hús; zöldségpüré (pl. répa) vagy gyümölcspüré (pl. alma), krumplipüré; glutén-mentes cereáliák (pl. rizs) |
| 7-12 | A kanálról az ételt ajkaival lehúzza; harap és rág; a nyelv oldalirányú mozgatása és az étel mozgatása a fogakhoz. Finom mozgások megjelennek, melyek segítik az önálló evésben | Újés a család által fogyasztott változatos, különféle pépes és a feldarabolt ételek. Háromszori fő étkezés és közöttük kétszer kisebb étkezés (tízórai, uzsonna) | Anyatej és főtt, darált hús; krumplipüré, főtt és nyers apróra vágott zöldség, gyümölcs (pl. paradicsom, dinnye); cereáliák* (búza, zab) és kenyér |
| 12-24 | körmozgásos rágás; álkapocs stabilitás, | Család étrendje | Anyatejés bármi, amit a család is fogyaszt, feltéve, ha az egészséges mennyiségben és összetételben egyaránt. |
9. sz. melléklet - Az egészséges csecsemő táplálása 6 hónap és 1 év között
Az első szolidok lehetnek gyümölcsök, gluténmentes (pl. rizs, kukorica) vagy glutén-tartalmú (búza, árpa, rozs, zab) cereáliák és főzelékfélék. Gluten tartalmú szolidokat, 7 hó előtt mindenképpen fokozatosan be kell vezetni, lehetőség szerint, amíg a csecsemő szopik (csökkenti a coeliakia, a diabetes mellitus és a búzaallergia kockázatát). A hozzátáplálás gyümölccsel való kezdés esetén: alma, őszibarack után óvatosan idénygyümölcsként: a sárgadinnye, a meggy, a cseresznye, a jó minőségű, hámozott szilva, majd a toleranciának és érzékenységnek megfelelően körte..... következzen. A citrus félék adása 1 év alatt nem ajánlott.
Csecsemőnél kerüljük az apró magvas, nehezen tisztítható, hisztamin felszabadulást kiváltó (eper, málna) gyümölcsöket.
Friss hiányában mélyhűtött gyümölcs is adható.
A főzelékfélék bevezetését burgonyával kezdjük, és a csecsemőkor idején leginkább ezzel történjen a sűrítés is. Ezen kívül a rántás helyett használhatunk rizs, illetve kukoricapelyhet is.
A csecsemő kora és a zöldség fajtája szerint passzírozás vagy turmixolás mellett (zöldborsó héját csak passzírozással lehet eltávolítani) adjuk a főzelékeket.
A burgonya után a sárgarépa, a cékla, a saláta, a sütőtök, a szelőtök, a gesztenye, a brokkoli, a kelbimbó, a spenót, a zöldborsó, a zöldbab és a spárga következzék. Magas, nehezebben emészthető rosttartalmuk miatt a kelkáposztát, karalábét, karfiolt csak 8 hónapos kor után javasolt a bevezetése
Főzelékekhez bio-termesztésű zöldség lenne az ideális, de ennek hiányában mindenképpen törekedjünk arra, hogy ellenőrzött beszerzési helyről (élelmezés-egészségügyi várakozási idő betartása) vásárolt alapanyagot használjanak fel.
Spenótot, sóskát magas oxalát tartalma miatt csak hetente egy alkalommal adjunk. A száraz hüvelyesek felhasználása csecsemőkorban leginkább a vegetáriánus módon étkezőknél bír jelentőséggel.
Fagyasztott alapanyagot használhatunk, de a csecsemő ne kapjon tartósítószert, festékanyagot, mesterséges édesítőt tartalmazó élelmiszert.
A főzelék komplettálás és a vashiány megelőzése céljából 6-7 hónapos kortól adjunk húst is. (Fiatal állattól, zsírtalanított, elsősorban baromfi és sertés.) Húskészítményt, felvágottat ne használjunk. A hal (szálkamentes édesvízi) adása táplálkozás-élettani szempontból hasznos lenne, de fokozott figyelmet igényel a túlérzékenység gyakorisága szempontjából. (A csirkemáj adása előnyei mellett méregtelenítő-szerv szerepe miatt meggondolandó és legfeljebb hetente egyszer fiatal állaté adható.) Állati fehérje komplettálásra a tojás is hasznos, de allergizáló tulajdonsága miatt csak 8 hónapos kortól ajánlott a főtt tojásnak a szétválasztott sárgája, majd 1 év felett a fehérje.
Tehéntejet 12 hónapos kor alatt ne, de tejterméket (sajt, túró, joghurt) már (a családi anamnézistől függően), kis mennyiségben a főzelék komplettálására adhatunk legkorábban 7-9 hónapos kortól..
A főzelékbe 6-7 hónapos kortól növényi olaj adása is ajánlott (1 dl-hez 1 kávéskanál). Az ételt lehetőleg ne sózzunk és cukrozzunk. Nagyobb csecsemőnél alkalmazhatunk enyhe fűszerezést (só pótló) pl. zöldpetrezselyem, kapor, fehérrépa, paradicsom stb.
Az egyéb szolidok közül kiemelendő az, hogy 1 éves kor alatt a méz és a gyógyteák esetleges pollentartalmuk miatt nem javasolhatók. Az olajos magvak sem adhatók az allergizálódás veszélye miatt.
Alternatív táplálkozás (vegetáriánus irányzatok) esetén vas, B12-vitamin, D-vitamin bevitelére fokozott figyelmet kel fordítani.
10. sz. melléklet Az egészséges újszülött és csecsemő táplálásának megfelelőségének indikátorai
| Indikátor megnevezése | Az indikátorszámítás metodikája | Egysége | Cél | Körzeten belül előző évekkel | Intézeten belül védőnői körzetek között | Azonos szintű intézetek között | Régiók között | Országos | Minőséget befolyásoló okok | |||
| számláló | nevező | szorzószám | ||||||||||
| összehasonlítás | ||||||||||||
| 4 hónapos korig kizárólag szoptatott/anyatejjel táplált csecsemők | 4. hónapot betöltött csecsemők közül kizárólag anyatejjel tápláltak száma | Összes gondozásba vett csecsemő száma | 100 | % | 4 hónapos korig kizárólag szoptatott/anyatejjel táplált csecsemők számának meghatározása | A védőnő gondozási tevékenységét jellemzi. Befolyásolja: kórházból való hazabocsátás módja A gondozott populáció összetétele, a populáció szociális megoszlása. A védőnő családban való elfogadottsága, család gondozása, szakmai felkészültsége. | ||||||
| 4 hónapos korig főleg anyatejjel táplált csecsemők | 4. hónapot betöltött csecsemők közül főleg anyatejjel tápláltak száma | Összes csecsemő száma | 100 | % | 4 hónapos korig főleg szoptatott/anyatejjel táplált csecsemők számának meghatározása | A védőnő gondozási tevékenységét jellemzi. Befolyásolja: az anya munkavégzése, és egészségi állapota. A gondozott populáció összetétele, a populáció szociális megoszlása. A védőnő családban való elfogadottsága, család gondozása, szakmai felkészültséqe. | ||||||
| 6 hónapos korig kizárólag szoptatott/anyatejjel táplált csecsemők | 6. hónapot betöltött csecsemők közül kizárólag anyatejjel tápláltak száma | Összes csecsemő száma | 100 | % | 6 hónapos korig kizárólag szoptatott/anyatejjel táplált csecsemők számának meghatározása | A védőnő gondozási tevékenységét jellemzi. Befolyásolja: az anya elkötelezettsége, a csecsemő egészségi állapota. Csecsemő gondozását végző team (anya/család, gondozó orvos, védőnő) megfelelő együttműködése, az anya együttműködési készsége, egészségi állapota. A gondozott populáció összetétele, a populáció szociális megoszlása. A védőnő családban való elfogadottsága, család gondozása, szakmai felkészültsége. | ||||||
| Indikátor megnevezése | Az indikátorszámítás metodikája | Egysége | Cél | Körzeten belül előző évekkel | Intézeten belül védőnői körzetek között | Azonos szintű intézetek között | Régiók között | Országos | Minőséget befolyásoló okok | |||
| számláló | nevező | szorzószám | ||||||||||
| összehasonlítás | ||||||||||||
| 6 hónapos korig főleg anyatejjel táplált csecsemők | 6. hónapot betöltött csecsemők közül főleg anyatejjel tápláltak száma | Összes csecsemő száma | 100 | % | 6 hónapos korig főleg szoptatott/anyatejjel táplált csecsemők számának meghatározása | A védőnő gondozási tevékenységét jellemzi. Befolyásolja: az anya elkötelezettsége, a csecsemő egészségi állapota. Csecsemő gondozását végző team (anya/család, gondozó orvos, védőnő) megfelelő együttműködése, az anya együttműködési készsége, egészségi állapota. A gondozott populáció összetétele, a populáció szociális megoszlása. A védőnő családban való elfogadottsága, család gondozása, szakmai felkészültsége. | ||||||
| 12 hónapos korig az anyatejes táplálás fennmarad | 12. hónapot betöltött csecsemők közül az anyatej még jelen van a táplálásban | Összes csecsemő száma | 100 | % | Befolyásolja: az anya elkötelezettsége, a csecsemő egészségi állapota. Csecsemő gondozását végző team (anya/család, gondozó orvos, védőnő) megfelelő együttműködése, az anya együttműködési készsége, egészségi állapota. A gondozott populáció összetétele, a populáció szociális megoszlása. A védőnő családban való elfogadottsága, család gondozása, szakmai felkészültsége | |||||||
| Indikátor megnevezése | Az indikátorszámítás metodikája | Egysége | Cél | Körzeten belül előző évekkel | Intézeten belül védőnői körzetek között | Azonos szintű intézetek között | Régiók között | Országos | Minőséget befolyásoló okok | |||
| számláló | nevező | szorzószám | ||||||||||
| összehasonlítás | ||||||||||||
| 24 hónapos korig az anyatejes táplálás fennmarad | 24. hónapot betöltött csecsemők közül az anyatej még jelen van a táplálásban | Összes csecsemő száma | 100 | % | Befolyásolja: az anya elkötelezettsége, a csecsemő egészségi állapota. Csecsemő gondozását végző team (anya/család, gondozó orvos, védőnő) megfelelő együttműködése, az anya együttműködési készsége, egészségi állapota. A gondozott populáció összetétele, a populáció szociális megoszlása. A védőnő családban való elfogadottsága, család gondozása, szakmai felkészültsége | |||||||
| Mesterségesen tápláltak | első életnaptól mesterségesen táplált csecsemők száma | Összes csecsemő száma | 100 | % | Befolyásolja: a születés időpontja (kora) a gondozott feltárt egészségügyi állapota, családi anamnézis, a populáció összetétele, a populáció szociális megoszlása. | |||||||
| A megfelelően kitöltött csecsemőgondozási lapok közül hány tartalmaz a szükségletek szerinti tevékenységet, tanácsokat | Szükségletek szerint adott tanácsokat, tevékenységet tartalmazó, megfelelően kitöltött csecsemőgondozási lapok száma | Összes megfelelően kitöltött csecsemőgondo zási lapok száma | 100 | % | A szükségletek szerint adott tanácsokat tartalmazó csecsemő gondozási lapok számának meghatározása | A védőnő gondozási tevékenységének tartalmát, a tanácsadást, és ezek minőségét jellemzi. Befolyásolja: a kórháztól kapott dokumentáció, a családi anamnézis, a populáció összetétele, a populáció szociális megoszlása, a védőnő családban való elfogadottsága, csecsemő gondozása, a védőnő szakmai felkészültsége. | ||||||
| Indikátor megnevezése | Az indikátorszámítás metodikája | Egysége | Cél | Körzeten belül előző évekkel | Intézeten belül védőnői körzetek között | Azonos szintű intézetek között | Régiók között | Országos | Minőséget befolyásoló okok | |||
| számláló | nevező | szorzószám | ||||||||||
| összehasonlítás | ||||||||||||
| Helytelen táplálkozás okozta elváltozás csecsemőkor végén | 12. hónapot betöltött csecsemők közül helytelen táplálkozás miatt fellépő elváltozás | Összes csecsemő száma | 100 | % | A szövődménymentesen lezajlott terhességek számának meghatározása | A védőnő gondozási tevékenységét jellemzi. Befolyásolja: csecsemő gondozási team (anya/család, gondozó orvos, védőnő) megfelelő együttműködése, az anya/család együttműködési készsége, családi és csecsemői anamnaesise. A gondozott populáció összetétele, a populáció szociális megoszlása. A védőnő családban való elfogadottsága, család gondozása, szakmai felkészültsége. | ||||||
A cél: az egészséges csecsemőtáplálás támogatásának minőségét mérni.
Fontos, hogy a körülményektől független védőnői teljesítményt mérjük. A minőséget befolyásoló okokból látható, hogy ez nehéz feladat.
A vonatkozó törvények, a MEES, a módszertani útmutatók előírása alapján a csecsemőtáplálás megfelelőségét/minőségét az időbeliség, a kockázatfelmérés, (szociális, szomatikus, pszichés) a gondozás (a kockázatfelmérés alapján történt tevékenység, tanácsadás) és az előírt dokumentáció megléte, határozzák meg. A fenti indikátorok ezeknek a tevékenységeknek számszerűsíthető, egyszerű mutatói.
I. Kívánatos lenne a csecsemők 6 hónapos korig tartó kizárólagos szoptatása
II. Az anyatejes táplálás 12 hónapos korig fennmaradjon.
III. A megfelelően kitöltött csecsemőgondozási lap a kockázatfelmérés mibenlétét és a dokumentációt jellemzi. Ha megtörténtek a családlátogatások és ezek dokumentációja és kikérdezés alapján a kockázatfelmérés, akkor azt lehetősége van a védőnőnek megfelelően dokumentálni.
IV. Csak a megfelelően kitöltött, (jó kockázat felmérési adatokat tartalmazó) csecsmő gondozási lapok esetében van értelme, mert azt méri, hogy a gondozás/tanácsadás a szükségletek szerint történt-e. Ha ugyanis nincs megfelelően kitöltve a gondozási lap kockázatfelmérés rovata, a védőnő tevékenysége, tanácsadása feltehetően nem tud a szükségletek szerinti lenni, (legalábbis dokumentáltan nem az)
V. Az egészségben lezajlott csecsemőkor alapvetően a Családgondozási team (anya/család, gondozó orvos, védőnő), és a család együttműködését jellemzi. Természetesen jellemzi a védőnő munkáját is, de alapvetően nem a körülményektől "független" védőnői teljesítményt méri.
Az indikátorokkal mért adatok durva adatok, de ha valamelyik esetben elfogadhatatlan %-ban hiányosságotjeleznek,akkora minőséget befolyásoló okokból lehet magyarázó változókat képezni és feltárni a gondozási hiányosság mögöttes tényezőit. Esetleg lehet az adatokat súlyozni, indexet képezni. Ugyanakkor fontos a monitorozó személye. Feltehetően nem szerencsés, ha védőnőt jól ismerő, közvetlen felettes végzi azt.
Az lenne a legszerencsésebb, ha egy független szakértő ellenőrizne. így az értékelés mentesebb lehet a szubjektívelemektől, mert csak az adott dokumentációra korlátozódik.
Lábjegyzetek:
[1] A Hivatalos Értesítő 2009. évi 46. számában közzétett dokumentum módosítással egységes szerkezetbefoglalt szövege.


